Группа изобретений относится к технологии приготовления металлорганических полимеров, а именно, к металлорганическому полимеру на основе ионов алюминия, координированных лигандами тримезиновой кислоты, который синтезируется сольвотермальным методом и может найти применение для аккумулирования газов, в частности в системах хранения и транспортировки природного газа, метана.
Металлорганические полимеры или, как их еще называют металлорганические структуры, представляют класс пористых адсорбентов, состоящих из ионов или кластеров металлов, координированных полиорганическими лигандами (линкерами). Широкий выбор органических лигандов в сочетании с различными катионами металлов приводит к огромному разнообразию потенциальных пористых материалов с обширным спектром свойств пористой поверхности и химически регулируемыми структурами, которые за это время не раз критически оценивались с точки зрения вариантов применения, включая хранение и разделение газа. В патенте (US №7202385, МПК С07С 41/03; С07С 43/11; C08G 18/28; C08G 65/26; C08G 65/28) приведено большинство структур, описанных в литературе, что иллюстрирует многообразие уже существующих в настоящее время металлорганических полимеров.
Металлорганические полимеры характеризуются уникальными структурно-энергетическими характеристиками, в т.ч. регулярной кристаллической структурой, высокой удельной поверхностью (до 10000 м2/г) и большим объемом микропор, зачастую превышающих аналогичные характеристики цеолитов и активированных углей, и используются как высокоэффективные адсорбенты, например, для хранения и разделения газа [Т.А. Makal, J.R. Li, W. Lu, H.-C.Zhou Methane storage in advanced porous materials // Chem. Soc. Rev. 2012. V. 41. P. 7761-7779].
Для создания высокоэффективных металлорганических полимеров, способных применяться в системах хранения и транспортировки газов, они должны обладать не только соответствующими адсорбционными характеристиками, но и температурной стабильностью.
Наиболее известным и распространенным металлорганическим полимером, обладающим потенциалом для хранения и разделения газов, в том числе, метана [Цивадзе А.Ю., Аксютин О.Е., Ишков А.Г., Фомкин А.А., Меньшиков И.Е., Прибылов А.А., Исаева В.И., Кустов Л.М., Школин А.В., Стриженов Е.М. Адсорбция метана на металлорганической каркасной структуре MOF-199 при высоких давлениях в области сверхкритических температур, Физикохимия поверхности и защита материалов. 2016. Т. 52. №1. С. 24-29.] [Baichuan Sun, Sibnath Kayal, Anutosh Chakraborty, Study of HKUST (Copperbenzene-l,3,5-tricarboxylate, Cu-BTCMOF)-1 metalorganic frameworks for CH4 adsorption: An experimental Investigation with GCMC (grandcanonical Monte-carlo) simulation, Energy (2014), 1-9] является MOF-199, относящийся к семейству HKUST-1, например, патент (US 9925516, МПК B01D 53/02; B01J 20/22; B01J 20/28). Однако, структура MOF-199 обладает недостаточной термической устойчивостью, определяющейся прочностью связей металл-лиганд, так как в случае MOF-199 используется двухвалентный катион меди Cu(II). Решить данную проблему возможно при помощи замены двухвалентного катиона меди на другой катион с более высокими значениями валентности.
Наиболее предпочтительным для поставленной задачи является использование трехвалентного катиона алюминия Al(III), так как металлорганические полимеры на основе алюминия обладают высокой температурной стабильностью и механической прочностью, развитым объемом микропор для аккумулирования газов, а также относительно невысокой стоимостью производства, например, по сравнению со схожими по механическим свойствам металлорганическими полимерами на основе циркония Zr(IV) или титана Ti(IV).
Среди способов синтеза металлорганических полимеров встречаются, как правило, модификации двух наиболее известных методов: сольвотермальный, например, [RU 2457213 С1, МПК C07F 11/00, опубл. 27.07.2012] и под воздействием СВЧ, например, патент [RU 2578599 С1, МПК C08F 293/00, B01J 32/00].
Сольвотермальный способ, частично описанный в РФ 2457213, включает смешение исходных компонентов, в частности, нитрата хрома(III) и терефталевой кислоты в водном растворе при нагревании. Нагревание производят в закрытом объеме со скоростью 11,5°/мин до 220°С, с последующей выдержкой.
Способ получения координационного полимера под воздействием СВЧ, например, в RU 2578599, заключается в смешении соли алюминия состава AlCl3×6H2O и органической 2-амино-1,4-бензолдикарбоновой кислоты в присутствии смеси воды и полярного органического растворителя, взятых при массовом соотношении 1:1÷5, соответственно. Затем полученную реакционную смесь нагревают при атмосферном давлении и температуре 120-130°С под воздействием СВЧ-излучения мощностью до 200 Вт. В качестве полярного органического растворителя используют растворитель с температурой кипения выше 130°С, способный эффективно нагреваться в условиях СВЧ-излучения, например диметилсульфоксид, N,N'-диметилформамид или N,N'-диэтилформамид.
Недостатком описанных подходов является то, что они позволяют получить неактивированные металлорганические полимеры, для которых требуется трудоемкий подбор режимов активации для удаления остатков растворителя при сохранении структуры материала с целью использования их в качестве сорбентов газа.
Наиболее близким по сути и достигаемому результату является способ [US 9878906 В2, МПК С01В 3/00, B01D 53/02, опубл. 30.01.2018], включающий взаимодействие при перемешивании и давлении не более 2 бар (абсолютное), по меньшей мере одного соединения металла с по меньшей мере одним, по меньшей мере, бидентатным органическим соединением, которое может координироваться с металлом в присутствии неводного органического растворителя, выбранного из DMF, DEF и NMP, с образованием пористой металлорганической структуры, где металл представляет собой Mg, Са, Be, Sr, Ga или Al, и органическое соединение, которое имеет, по меньшей мере, два атома, выбранных из кислорода, серы или азота, через которые органическое соединение может координироваться с металлом, где, по меньшей мере, одно бидентатное органическое соединение представляет собой ди-, три- или тетракарбоновую кислоту. Реакцию проводят без дополнительного основания, при этом сформированный металлорганический каркас дополнительно прокаливают при температуре выше 250°С. Пример 13 данного изобретения наиболее близок к достигаемому нами результату. В нем осуществляют синтез металлорганического каркасного полимера с растворителем N,N'-диметилформамидом, заключающийся в том, что 7,8 г тримезиновой кислоты (ВТС) и 22,9 г Al(NO3)3*9H2O растворяют в 520,5 г N,N'-диметилформамида при 130°С и выдерживают в течение 4-х дней с перемешиванием полученной суспензии, которую фильтруют промывкой N,N'-диметилформамидом два раза объемом по 100 мл и метанолом четыре раза объемом по 100 мл. Затем фильтр с осажденным на нем веществом просушивают путем термовакуумной сушки при температуре 200°С в течение 16-ти часов. Образованный порошок металлорганического каркаса прокаливают с целью активации при 330°С в муфельной печи с продувкой воздухом с расходом 100 л/час в течение 3-х суток. При этом скорость нагрева печи составляет 75 град/час. Полученный металлорганический каркасный полимер на основе алюминия имеет удельную поверхность, определенную по методу Лэнгмюра, 1791 м2/г.
Задачей настоящей группы изобретений являлась разработка способа синтеза металлорганического координационного полимера со структурой металлорганического геля, на основе ионов алюминия, координированных лигандами тримезиновой кислоты, обладающего развитой поверхностью нанопор и повышенной термической стабильностью, обеспечивающей возможность использования полученного металлорганического геля в качестве адсорбента в системах транспортировки и хранения газов, в частности, природного газа, метана.
Техническим результатом, на достижение которого направлена группа изобретений, является:
- создание и сохранение структуры геля у синтезируемого металлорганического координационного полимера;
- повышение его термической стабильности;
- сокращение материальных и энергетических затрат на производство за счет снижения времени синтеза и использования одного растворителя на стадии синтеза и промывки.
Технический результат достигается за счет того, что в способе получения металлоорганического координационного полимера для аккумулирования природного газа, метана, включающем стадию синтеза, состоящую из взаимодействия эквимолярных количеств кристаллогидрата нитрата алюминия и тримезиновой кислоты, растворенных в апротонном полярном органическом растворителе с температурой кипения выше 80°С, взятом в эквимолярном или избыточном к реагентам количестве, при этом раствор кристаллогидрата нитрата алюминия нагревают до 110°С, раствор тримезиновой кислоты нагревают до температуры 80-110°С, нагретый раствор тримезиновой кислоты по каплям при интенсивном перемешивании добавляют к нагретому раствору нитрата алюминия со скоростью 5-15% об. в минуту, смесь растворов нагревают до 140°С со скоростью 10-15°С в час, выдерживают до образования золя, который помещают в автоклав и выдерживают в нем при температуре 100-150°С в течении 2-3 суток до образования металлорганического координационного полимера со структурой геля, и стадию активации, состоящую из промывки синтезированного металлорганического координационного полимера со структурой геля нагретым до 40-60°С апротонным полярным органическим растворителем, используемым на стадии синтеза, с помощью вакуумсоздающей фильтрующей системы при перепаде давления не менее 90 кПа, сушки при комнатной температуре, сушки в сушильном шкафу при 100-150°С, инсталляции в термовакуумной камере при 120-300°С и остаточном давлении до 0,26 кПа, стадию активации завершают при стабилизации массы металлорганического координационного полимера со структурой геля.
Металлоорганический координационный полимер со структурой геля для аккумулирования природного газа, метана, обладающий термической стабильностью при температурах не менее 500°С, содержащий поры с эффективным внутренним диаметром 0,75-0,80 нм, удельной поверхностью от 1300 до 1700 м2/г, объемом микропор 0,5-0,6 см3/г, суммарным объемом пор 1,0-1,8 см3/г.
Группа изобретений поясняется таблицами и иллюстрациями:
Таблица 1 - Химический состав поверхности синтезированного металлорганического геля, где: Wt - весовые проценты, At - атомные проценты;
Таблица 2 - Параметры пористой структуры синтезированных образцов металлорганического геля, где: V0 - удельный объем микропор, см3/г; Е0 - характеристическая энергия адсорбции азота, кДж/моль; D - эффективный внутренний диаметр микропор, нм; Е - характеристическая энергия адсорбции бензола, кДж/моль; SБЭТ - площадь удельной поверхности по методу БЭТ, м2/г; Vs - суммарный объем пор, см3/г; Sme - площадь мезопор, м2/г; Vme - объем мезопор, см3/г.
Фиг. 1 - Фотография электронной сканирующей микроскопии полученного образца металлорганического координационного полимера со структурой геля;
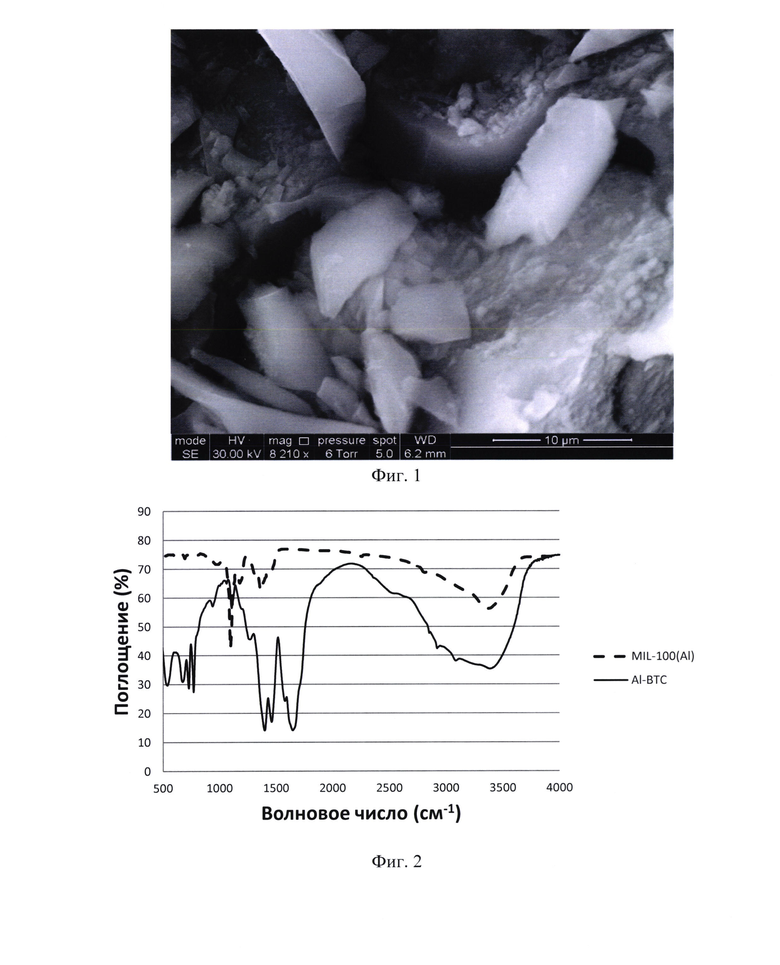
Фиг. 2 - ИК-спектры синтезированного металлорганического координационного полимера со структурой геля - сплошная линия, металлорганический полимер на основе алюминия (прототип) - пунктирная линия.
Фиг. 3 - Дифрактограммы синтезированного металлорганического координационного полимера со структурой геля - линия сверху, металлорганический полимер на основе алюминия (прототип) - линия снизу.
Фиг. 4 - Термогравиметрические кривые: сплошная линия -синтезированный образец металлорганического координационного полимера со структурой геля; пунктирная линия - металлорганический полимер на основе алюминия (прототип).
Фиг. 5 - Изотерма адсорбции-десорбции азота при 77 К на образце (1). Светлые символы - адсорбция. Темные символы - десорбция.
Фиг. 6 - Каркасная модель фрагмента синтезированного металлоорганического координационного полимера, где D - эффективный внутренний диаметр микропоры.
Предлагаемая группа изобретений реализуется следующим образом.
Пример 1
Тримезиновую кислоту (1,3,5-бензолтрикарбоновую кислоту (Н3ВТС)) и кристаллогидрат нитрата алюминия Al(NO3)3⋅9H2O растворяли в органическом растворителе N,N'-диметилформамиде в мольном соотношении 1:1 (1 моль кислоты на 1 моль растворителя, и 1 моль соли на 1 моль растворителя). Полученные растворы подогревали, раствор соли алюминия до 110°С, раствор тримезиновой кислоты до 80°С. Затем разогретый раствор тримезиновой кислоты по каплям, со скоростью 5-15% об./мин, приливали к раствору соли алюминия, при интенсивном перемешивании магнитной мешалкой, постепенно повышая температуру реакционной смеси до 140°С, и выдерживали до образования золя (загустевания раствора). Полученный золь помещали в аналитический автоклав с плотной завинчивающейся крышкой и фторопластовым вкладышем, после чего отправляли в печь, где вели синтез при температуре 100°С с постепенным нагревом до 140°С, и выдерживали еще двое суток. Активацию проводили следующим образом: образующийся осадок металлоорганического геля (МОГ) отделяли от маточного раствора методом термовакуумного фильтрования (десорбции молекул растворителя), а именно, многократно в условиях вакуума, при перепаде давления не менее 90 кПа промывали растворителем - N,N'-диметилформамидом, объемом 150 мл, нагретым до температуры 60°С. Далее осадок сушили сначала в стандартных условиях, затем в сушильном шкафу при температуре 100°С, с подъемом в течение 20 ч до 140°С, и выдерживали при 140°С еще 4 ч. При таком режиме сушки сначала удаляется поверхностная вода (при 100°С), затем внутренняя не связанная (100-140°С), что позволяет стабилизировать каркас синтезированного МОГ. Полученный образец МОГ активировали для максимального удаления внутренней связанной (кристаллогидратной) воды и растворителя в термовакуумной камере при температуре 200°С, остаточном давлении до 0,26 кПа (2 мм рт.ст.) до постоянной массы (около 6 часов).
Полученный образец представляет собой металлорганический координационный полимер (МОКП) на основе ионов алюминия, координированных лигандами тримезиновой кислоты, имеет структуру геля и химический состав поверхности, указанный в таблице 1. Его физико-химические свойства подтверждаются данными результатов анализа, приведенными на: Фиг. 2 - характеристика поглощения материалом ИК-спектра, Фиг. 3 - дифрактограмма, Фиг. 4 - термогравиметрическая кривая, Фиг. 5 - изотермы адсорбции. Фотография электронной сканирующей микроскопии полученного образца МОКП со структурой геля (Фиг. 1), показывает наличие кристаллов различных размеров и небольшое количество аморфной фазы между ними, что свидетельствует о неоднородности молекулярно-массового распределения полученного полимера за счет сокращения, по сравнению с прототипом, времени его синтеза. Выбор специальных условий активации для максимального удаления как свободной, так и связанной жидкой фазы способствует сохранению структуры пор, обеспечивает приемлемую прочность и термическую стабильность МОКП (Фиг. 4). В условиях высокой аэродинамической нагрузки, которой подвергается в ходе эксплуатации аккумулятор природного газа, такие характеристики предпочтительны, что объясняет преимущества полученной структуры полимерного геля для обозначенного целевого использования, перед структурами МОКП с высокой степенью кристалличности, твердыми, но хрупкими.
Полосы поглощения ИК-спектра синтезированного МОКП, Фиг. 2, наблюдаемые в интервале 663-766 см-1, соответствуют колебаниям связей в бензольном кольце и вне плоскости ароматического кольца. Полосы, возникающие между 827-1153 см-1, относятся к симметричным и асимметричным деформационным колебаниям O-С=O. Интенсивные пики поглощения при 1368, 1445 и 1640 см-1 связаны с деформационными колебаниями связей С-О, асимметричным и симметричным типами С=O соответственно в группе -СООН (в тримезиновой кислоте). Такие характеристики также свидетельствуют об образовании МОКП заявленного химического состава.
Результаты анализа термической стабильности синтезированного МОКП со структурой геля, представленные на Фиг. 4, позволили установить, что его термическое разложение наступает при температурах выше 500°С. Это свидетельствует о повышенной термической стабильности полученного полимера в сравнении с известными металлорганическими координационными полимерами на основе катионов алюминия, координированных лигандами тримезиновой кислоты.
Анализ параметров пористой структуры синтезированного образца (1) (см. таблицу 2) металлорганического геля по изотерме стандартного пара азота при температуре минус 196,15°С (77 K), Фиг. 5, проводили методом БЭТ и теории объемного заполнения микропор. Изотерма адсорбции имеет вид, характерный для микро-мезопористых адсорбентов. На Фиг. 6 приведена каркасная модель фрагмента металлоорганического геля (МОГ), схематически иллюстрирующая его геометрию и поровые характеристики.
Пример 2.
Отличается от примера 1 тем, что раствор тримезиновой кислоты подогревали до 110°С, затем приливали к раствору кристаллогидрата нитрата алюминия при перемешивании со скоростью 1 мл/мин. Стадию синтеза проводили при повышении температуры от 100 до 120°С и далее выдерживали при температуре 120°С еще 60 ч. Стадию сушки в сушильном шкафу проводили при температуре 100°С с постепенным нагревом до 120°С. Выдерживали в термовакуумной камере при 120°С. Результаты анализа пористой структуры полученного образца металлорганического геля (2) представлены в таблице 2.
Пример 3.
Отличается от примера 1 тем, что тримезиновую кислоту и кристаллогидрат нитрата алюминия растворяли в органическом растворителе диэтилсульфоксиде в мольном соотношении 1:2 (1 моль кислоты на 2 моль растворителя, и 1 моль соли на 2 моль растворителя). Стадию синтеза проводили при повышении температуры от 100 до 150°С и далее выдерживали при температуре 150°С еще 48 ч. Стадию сушки в сушильном шкафу проводили при температуре 100°С и постепенным нагревом до 130°С. Выдерживали в термовакуумной камере при 250°С. Результаты анализа пористой структуры полученного образца металлорганического геля (3) представлены в Таблице 2.
Пример 4.
Отличается от примера 1 тем, что в качестве растворителя использовали диэтилформамид, стадию синтеза проводили при температуре 120°С в течении 60 ч. Стадию сушки в сушильном шкафу проводили при температуре 100°С с постепенным нагревом до 120°С. Выдерживали в термовакуумной камере при 300°С. Результаты анализа пористой структуры полученного образца металлорганического геля (4) представлены в Таблице 2.
Пример 5.
Отличается от примера 1 тем, что стадию синтеза проводили при температуре 130°С при повышении температуры до 140°С и далее выдерживали при температуре 140°С еще 48 ч, а стадию активации - методом фильтрования растворителем диметилсульфоксидом, подогретым до температуры 40°С, сушку в сушильном шкафу проводили при 100°С с нагревом до 140°С, выдерживали в термовакуумной камере при 160°С. Результаты анализа пористой структуры полученного образца металлорганического геля (5) представлены в Таблице 2.
Предлагаемая группа изобретений позволяет получить металлоорганический координационный полимер со структурой геля, с развитой внутренней поверхностью, состоящей из микро- и мезопор, обладающий, по сравнению с аналогичными материалами, более высокой термической стабильностью, а параметры сушки и активации способствуют максимальному сохранению полученных на стадии синтеза поровых характеристик, что в целом свидетельствует о достижении заявленного технического результата.


| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения термоактивированного металлоорганического координационного полимера и способ получения композитного нанопористого адсорбента на его основе | 2020 |
|
RU2782026C2 |
| Блочный композитный материал для аккумулирования газов и способ его получения | 2021 |
|
RU2782932C1 |
| Металлорганическая каркасная структура бензолтрикарбоксилата лантана (III) La-BTC и способ его получения | 2022 |
|
RU2796682C1 |
| Металлорганическая каркасная структура бензолтрикарбоксилата иттрия (III) Y-BTC для аккумулирования водорода и способ её получения | 2022 |
|
RU2796292C1 |
| Металлорганическая каркасная структура бензолтрикарбоксилата церия (III) Ce-BTC и способ её получения | 2022 |
|
RU2800447C1 |
| СПОСОБ ПОЛУЧЕНИЯ МЕТАЛЛОРГАНИЧЕСКИХ КОМПЛЕКСОВ НА ОСНОВЕ 8-ОКСИХИНОЛИНА В ОБЪЕМЕ ВЫСОКОПОРИСТЫХ АЭРОГЕЛЕЙ | 2022 |
|
RU2805740C1 |
| Люминофорный материал на основе металлорганических комплексов однородно распределенных в объеме аэрогеля и способ его получения | 2020 |
|
RU2757593C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОРИСТОГО КООРДИНАЦИОННОГО ПОЛИМЕРА NH-MIL-101(Al) И ПОРИСТЫЙ КООРДИНАЦИОННЫЙ ПОЛИМЕР NH-MIL-101(Al), ПОЛУЧЕННЫЙ ЭТИМ СПОСОБОМ | 2015 |
|
RU2578599C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОРИСТОГО КООРДИНАЦИОННОГО ПОЛИМЕРА MOF-177 | 2016 |
|
RU2629361C1 |
| Протонно-обменная мембрана на основе металлорганической каркасной структуры HKUST-1 | 2022 |
|
RU2787343C1 |


Изобретение относится к способу получения металлоорганического координационного полимера для аккумулирования природного газа, метана. Способ включает в себя стадию синтеза, состоящую из взаимодействия эквимолярных количеств кристаллогидрата нитрата алюминия и тримезиновой кислоты, растворенных в апротонном полярном органическом растворителе с температурой кипения выше 80°С, взятом в эквимолярном или избыточном к реагентам количестве, при этом раствор кристаллогидрата нитрата алюминия нагревают до температуры 110°С, раствор тримезиновой кислоты нагревают до температуры 80-110°С, нагретый раствор тримезиновой кислоты по каплям при интенсивном перемешивании добавляют к нагретому раствору нитрата алюминия со скоростью 5-15% об. в минуту, смесь растворов подогревают до температуры 140°С, выдерживают до образования золя, который полимеризуют при температуре 100-150°С в течение 2-3 суток до образования металлоорганического координационного полимера со структурой геля, и стадию активации, состоящую из многократной промывки синтезированного металлоорганического координационного полимера со структурой геля в условиях вакуума при перепаде давления не менее 90 кПа нагретым до температуры 40-60°С апротонным полярным органическим растворителем, используемым на стадии синтеза, сушки до 24 часов сначала в стандартных условиях, затем при температуре 100-150°С, термовакуумирования до 6 часов при температуре 120-300°С и остаточном давлении до 0,26 кПа. При этом стадию активации завершают при стабилизации массы металлоорганического координационного полимера со структурой геля. Также предложен металлоорганический координационный полимер для аккумулирования природного газа, метана. Предложенный способ позволяет снизить материалоемкость процесса за счет использования одного растворителя на стадии синтеза и активации, сократить время получения полимерного геля, который характеризуется наличием активных мезо- и микропор, что позволит применять его в качестве основы в различных адсорбционных процессах, в том числе в системах хранения природного газа. 2 н.п. ф-лы, 6 ил., 2 табл., 5 пр.
1. Способ получения металлоорганического координационного полимера для аккумулирования природного газа, метана, включающий в себя стадию синтеза, состоящую из взаимодействия эквимолярных количеств кристаллогидрата нитрата алюминия и тримезиновой кислоты, растворенных в апротонном полярном органическом растворителе с температурой кипения выше 80°С, взятом в эквимолярном или избыточном к реагентам количестве, при этом раствор кристаллогидрата нитрата алюминия нагревают до температуры 110°С, раствор тримезиновой кислоты нагревают до температуры 80-110°С, нагретый раствор тримезиновой кислоты по каплям при интенсивном перемешивании добавляют к нагретому раствору нитрата алюминия со скоростью 5-15% об. в минуту, смесь растворов подогревают до температуры 140°С, выдерживают до образования золя, который полимеризуют при температуре 100-150°С в течение 2-3 суток до образования металлоорганического координационного полимера со структурой геля, и стадию активации, состоящую из многократной промывки синтезированного металлоорганического координационного полимера со структурой геля в условиях вакуума при перепаде давления не менее 90 кПа нагретым до температуры 40-60°С апротонным полярным органическим растворителем, используемым на стадии синтеза, сушки до 24 часов сначала в стандартных условиях, затем при температуре 100-150°С, термовакуумирования до 6 часов при температуре 120-300°С и остаточном давлении до 0,26 кПа, при этом стадию активации завершают при стабилизации массы металлоорганического координационного полимера со структурой геля.
2. Металлоорганический координационный полимер для аккумулирования природного газа, метана, полученный способом по п. 1, имеющий структуру геля и обладающий термической стабильностью при температуре не менее 500°С, содержащий поры с эффективным внутренним диаметром 0,75-0,80 нм, удельной поверхностью от 1300 до 1700 м2/г, объемом микропор 0,5-0,6 см3/г, суммарным объемом пор 1,0-1,8 см3/г.
| US 9878906 В2, 30.01.2018 | |||
| БАТРАКОВА М.К | |||
| и др., Синтез и структурно-энергетические характеристики металлорганической каркасной структуры MOF AL-BTC, Физикохимия поверхности и защита материалов, 2017, т | |||
| Веникодробильный станок | 1921 |
|
SU53A1 |
| РАДИОПРИЕМНИК - ВОЛНОМЕР | 1923 |
|
SU563A1 |
| SAHA D | |||
| et al, Synthesis, characterization and hydrogen adsorption on metal-organic frameworks Al, Cr, Fe and Ga-BTB, | |||
Авторы
Даты
2022-10-31—Публикация
2021-11-15—Подача