Изобретение относится к области медицины, а именно к способам получения склерозирующих лекарственных пен (склеропен), используемых, в том числе, в терапии вен.
Одним из эффективных методов лечения варикозной болезни вен нижних конечностей является флебосклерозирование. Этот метод малотравматичен, имеет низкую себестоимость и обладает высоким косметическим эффектом. Применяемыми в настоящее время обычными склерозирующими жидкостями являются многоатомные спирты, например в России часто используется лауромакрогол 400 (1-3%). В целях уменьшения количества вводимого препарата он используется во вспененной форме. Практика показывает, что особенности структуры склерозирующей лекарственной пены оказывают существенное влияния на эффективность процесса склерозирования [1].
Материалы с иерархической структурой уже зарекомендовали себя в различных областях науки и техники, включая биоинженерию, биомедицину, нанотехнологию, в частности было показано, что с их использованием возможно получение материалов структурно близких к пенам, обладающих комплексом уникальных адсорбционных, газочувствительных, фотокаталитических и других свойств [2, 3].
Известно изобретение, описывающее образование терапевтического вспененного материала с микропузырьками газа [4]. Получение вспененного материала, пригодного для использования в склерозирующей спектроскопии, включает пропускание смеси физиологически приемлемого, диспергируемого в крови газа и водной склерозирующей жидкости через один или более каналов, имеющих, по меньшей мере, один размер поперечного сечения, составляющий от 0.1 до 30 мкм. При этом соотношение между газом и жидкостью регулируют таким образом, что получают вспененный материал с микропузырьками газа, имеющий плотность от 0.07 до 0.19 г/мл и период полупревращения не мене 2 минут. Устройство для получения вспененного материала содержит корпус, в котором расположена камера, выполненная с возможностью повышения давления в ней и содержащая водную склерозирующую жидкость, проходной канал с одним или более выходными отверстиями для прохода жидкости из камеры, выполненной с возможностью повышения давления или закрытия проходного канала от камеры до наружного пространства. В том случае, когда давление в контейнере повышено и проходной канал открыт, текучая среда, находящаяся в камере, будет вытеснять вдоль проходного канала через одно или более выходных отверстий. Вспененный материал с микропузырьками газа имеет плотность от 0.07 до 0.19 г/мл и способен проходить через иглу калибра 21 так, что 50% или более количества его пузырьков с диаметром, по меньшей мере, 25 мкм сохраняют диаметр 150 мкм или менее и, по меньшей мере, 95% этих пузырьков сохраняют диаметр 280 мкм или менее. Недостатком такого способа является большая дисперсия микропузырьков по размеру, которая обуславливает невозможность контроля структуры склерозирующей лекарственной пены, в том числе, получения пены с иерархической структурой.
Описано устройство для вспенивания и введения лекарственного препарата [5]. Устройство представлено цилиндром, открытый конец которого закрыт крышкой с упором для пальцев и фиксаторами, совмещающимися с выемками на наружной стенке цилиндра. При этом на закрытом конце цилиндра находится конический выступ со сквозным отверстием, имеющим расширение, которое открывается в полость цилиндра. Расширение содержит рассекатель в виде крестообразной пластинки с открывающимися под ним капиллярами, которые сообщаются с воздушным каналом, проходящим в утолщении стенки цилиндра, имеющим у открытого конца цилиндра расширение с закругленными выпуклыми концами, конгруэнтными с закругленными торцами цилиндрического затвора с рычагом. Он, в сою очередь, под прямым углом жестко закреплен на стенке затвора и выходит наружу через продольную щель в стенках цилиндра и крышки. Кроме того, расширение сообщается с полостью цилиндра и наружу через отверстие, проходящее в дне крышки. Использование технического решения оптимизирует процесс образования пены склерозирующего препарата путем упрощения конструкции устройства. Недостатком технического решения является невозможность получения склерозирующих лекарственных пен с микропузырьками заданного размера, а том числе с иерархической структурой.
Также описаны композиции и устройства для склеротерапии с применением светоотверждаемых клеев [6]. Композиция для склеротерапии содержит фармацевтически приемлемый тканевой клей и склерозирующее лекарственное средство. При этом указанный фармацевтически приемлемый тканевой клей представляет собой инъекционный, светоотверждаемый или светоактивируемый, биологически разлагаемый и/или биологически совместимый клей. Клей представляет собой акрилат и указанный акрилат имеет период полувыведения в ткани, составляющий менее 2 лет. Также обеспечивается катетерное устройство для инъекций для введения указанной композиции, содержащее источник света, где клей и газ загружают в катетер и применяют при последующем болюсном введении. Существенным недостатком такого способа является недостаточная эффективность процесса денатурирования эндотелия вены при использовании светоотверждаемых клеев в сравнении с использованием склерозирующих лекарственных пен, в том числе с иерархической структурой.
Известно изобретение, описывающее устройства и способы получения инъекционных склеропен для сосудов с помощью матрицы-носителя и их применение [7]. Склерозирующая лекарственная пена содержит матрицу, по меньшей мере одну жидкость, по меньше мере один склерозирующий препарат, медицинский газ, подходящий для внутривенного введения, при этом указанная матрица имеет вязкость, сопоставимую с вязкостью денатурированной крови. Указанная денатурированная кровь была получена из образца свежей человеческой венозной цельной крови объемом 1 мл, который нагревают в цилиндрическом полиэтиленовом контейнере с внутренним диаметром 3 мм и наружным диаметром 3,4 мм в течение от 0,5 мин до 10 мин при температуре от 70°С до 100°С. Также описан способ получения склерозирующей лекарственной пены, устройство для ее получения, набор для лечения венозной недостаточности и способ лечения с применением склерозирующей лекарственной пены. Склерозирующая лекарственная пена по изобретению характеризуется повышенными вязкостью и периодом полураспада. Недостатком такого способа получения инъекционных склеропен является значительная сложность подготовки, обусловленная необходимостью использовать матрицу, предпочтительно содержащую денатурированную кровь, предпочтительно полученную из образца аутологичной крови. Также недостатком способа является невозможность управления структурой формируемой пены, в том числе получение пены с иерархической структурой.
Наиболее близким по технической сущности к предлагаемому решению является способ получения склерозирующей лекарственной пены путем смешивания жидкого склерозанта с медицинским газом, таким как О2 или СО2, или комнатным воздухом, известный как метод Тессари (Tessari) [8]. Сущность данного способа заключается в том, что жидкий склерозант смешивают с медицинским газом путем от 10 до 20-кратного инъецирования «туда-обратно» из одного шприца в другой через запорный кран или наконечник шприца, путем встряхивания шприца, с помощью одновременной аспирации жидкости и газа или механическим способом с применением насосов, устройств положительного или отрицательного давления, перфорированных отверстий или клапанов или с помощью вертушек или вращающихся щеток.
Техническим результатом настоящего изобретения является склерозирующая лекарственная пена с иерархической структурой, обладающая повышенной эффективностью в отношении процесса некроза стенок вен.
Это достигается тем, что в известном способе склерозирующую лекарственную пену получают смешиванием жидкого склерозанта с медицинским газом, таким как О2 или СО2, или комнатным воздухом путем от 10 до 20-кратного инъецирования «туда-обратно» из одного шприца в другой через запорный кран или наконечник шприца. При этом в соответствии с предлагаемым изобретением жидкий склерозант перед вспениванием охлаждают до температуры 0°С, в результате чего формируется пена с иерархическим распределением пузырьков по размеру, состоящая из крупных (более 100 мкм) и мелких (менее 50 мкм) микропузырьков, причем поверхность крупных заполняется мелкими.
Пример выполнения способа. Способ получения склерозирующей лекарственной пены с иерархической структурой на основе лауромакрогола 400.
1. В качестве жидкого склерозанта использовался 1%-ный раствор этоксисклерола (активное вещество лауромакрогола 400) с тремя различными температурами: 1) комнатной температуры 22°С; 2) охлажденный до 0°С; 3) нагретый до 36,5°С.
2. По методу Тессари 1 мл 1%-ого раствора этоксисклерола смешивали с 1 мл комнатного воздуха путем 20-кратного инъецирования «туда-обратно» из одного шприца в другой через запорный кран, в результате чего образовывалась склерозирующая лекарственная пена.
На фиг. 1 представлено оптическое микроскопическое изображение структуры склерозирующей лекарственной пены, полученной на основе 1%-ого раствора этоксисклерола. Анализ представленных изображений показывает, что при температуре 22°С (фиг. 1, а) и 36.5°С (фиг. 1, в) образуются монодисперсные пузырьки крупного и мелкого размера соответственно. При температуре 0°С (фиг. 1, б) формируются микропузырьки, для которых характерно иерархическое распределение по размерам, причем поверхность больших микропузырьков заполнена мелкими, что позволяет говорить о получении склерозирующей лекарственной пены с иерархической структурой.
3. Склерозирующую лекарственную пену, формируемую на основе жидкого склерозанта с температурами 22°С, 0°С и 36,5°С, наносили на участки препаратов нативных вен, полученных после проведенной плановой флебоэктомии. После 2 секунд взаимодействия пену смывали физиологическим раствором. Один из участков нативной вены использовался для контроля результатов.
4. Препараты вен готовились по стандартной методике гистологических исследований. В качестве окраски использовался гематоксилин-эозин.
Одной из основных задач при терапии вен с помощью склерозирующих лекарственных пен является максимальное воздействие на разрушение клетки внутренней поверхности вены при минимальном количестве вещества (для снижения общетоксического действия препарата). Известно, что воздействие этого вещества на внутреннюю поверхность вены приводит к разрушению клеток последней с дальнейшим закрытием сосуда. При этом одним из главных параметров, определяющих эффективность данного процесса, является эффективная площадь взаимодействия активного вещества (например, лауромакрогол 400) с внутренней поверхностью сосуда. При этом существуют два полярных варианта формирования пен: пена с мелкими пузырьками (менее 50 мкм) и пена с крупными пузырьками (более 100 мкм). Использование пены с мелкими пузырьками показывает большую эффективность процесса разрушения структур вены. Это связано с высокой удельной площадью поверхности вспененного таким образом вещества. Однако эффективно взаимодействует с эндотелием только та часть пузырьков, которая находится на поверхности крупного агломерата, что приводит к неэффективному использованию препарата, который удален от интерфейса «пузырек-эндотелий». В случае использования препарата с большим размером пузырьков для формирования пены заданного объема имеет место быть меньший расход вещества, но за счет малой площади поверхности крупного пузыря эффективность разрушения эндотелия снижается. Решением данной проблемы является использование склерозирующей лекарственной пены с иерархическим распределением микропузырьков по размерам. При этом крупные микропузырьки, поверхность которых заполнена мелкими микропузырьками, выступают в качестве носителя препарата по внутренней поверхности вены, а мелкие микропузырьки взаимодействуют с эндотелием, разрушая его за счет процесса денатурирования.
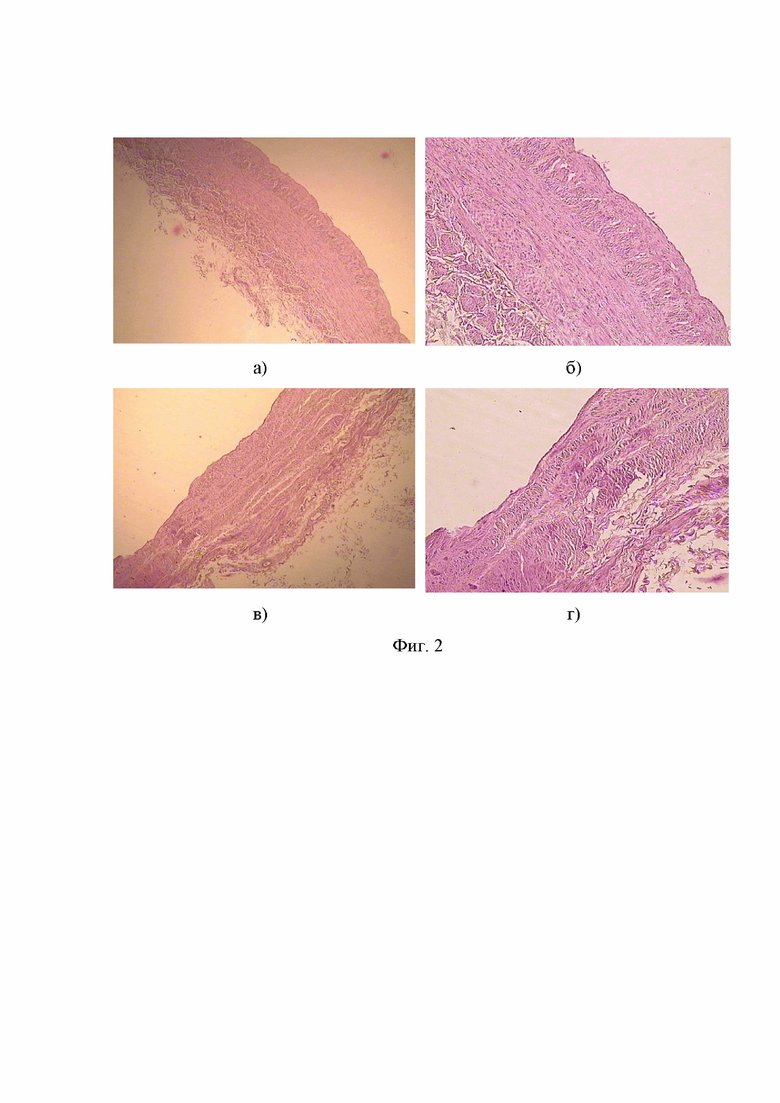
На фиг. 2 и 3. представлено оптическое микроскопическое изображение препаратов вен до (увеличение 40Х фиг. 2, а, увеличение 100Х фиг. 2, б) и после 2 секундного воздействия склерозирующей лекарственной пены, полученной при температуре:
1) 22°С (увеличение 40Х фиг. 2, в, увеличение 100Х фиг. 2, г),
2) 0°С (увеличение 40Х фиг. 3, а, увеличение 100Х фиг. 3, б)
3) 36,5°С (увеличение 40Х фиг. 3, в, увеличение 100Х фиг. 3, г).
Анализ изображения нативного (фиг. 2, а, б) препарата вены (до воздействия склерозирующей лекарственной пены) показывает, что стенка вены не повреждена и включает (изнутри-наружу): эндотелий, подэндотелиальный слой, мышечную оболочку (продольный, поперечный и опять продольный слои), адвентициальную оболочку. При воздействии склерозирующей лекарственной пены, полученной при температуре 22°С и 36,5°С наблюдается повреждение сосудистой стенки глубиной до циркулярного слоя мышечных волокон (фиг. 2, в, г) и до мышечной оболочки соответственно (фиг. 3, в, г). Воздействие склерозирующей лекарственной пены с иерархической структурой (фиг. 1, б) приводит к некрозу сосудистой стенки глубиной до наружного продольного мышечного слоя (фиг. 3 а, б), что подтверждает ее повышенную эффективность.
Предлагаемый способ получения склерозирующей лекарственной пены с иерархической структурой может найти широкое применение в медицине и терапии, например в терапии вен, обеспечивая полную денатурацию эндотелия стенок вен при использовании минимального количества лекарственного препарата.
Источники информации
1. Bottaro, E., Paterson, J.A.J., Quercia, L. et al. In vitro and ex vivo evaluation of the biological performance of sclerosing foams // Scientific Reports. 2019. V. 9. P. 9880.
2. Chen C., Singh M.K., Wunderlich K. et al. Polymer cyclization for the emergence of hierarchical nanostructures // Nature Communication. 2021. V. 12, P. 3959.
3. Пронин И.А., Якушова Н.Д., Карманов А.А., Аверин И.А., Мошников В.А. Модель сборки нанокомпозитных и иерархических наноструктур в золь-гель-процессах // Нано- и микросистемная техника. 2016. Т. 18. № 8. С. 472-478.
4. Патент РФ № 2261700, А61К 9/12, А61М 5/31, B65D 83/16, А61Р 9/14 Образование тераевтического вспененного материала с микропузырьками газа // Бюл. № 28 от 10.10.2005.
5. Патент РФ № 2017111397 А61М 5/178 Устройство для вспенивания и введения лекарственного препарата // Бюл. № 19 от 03.07.2018.
6. Патент РФ № 2738739 A61L 24/00 Композиции и устройства для склеротерапии с применением светоотверждаемых клеев // Бюл. № 35 от 16.12.2020.
7. Патент РФ № 2683033 А61К 9/12, А61К 47/42, А61К 31/045, А61К 31/08, А61К 31/185, А61К 49/22, А61М 5/00, А61М 25/01, А61Р 9/14 Устройства и способы получения инъекционных склеропен для сосудов с помощью матрицы-носителя и их применение // Бюл. № 9 от 26.03.2019.
8. Cavezzi A., Frullini A., Ricci S., Tessari L. Treatment of Varicose Veins by Foam Scleroterapy: Two Clinical Series / Phlebology. 2002. V. 17. P. 13-18.
| название | год | авторы | номер документа |
|---|---|---|---|
| УСТРОЙСТВА И СПОСОБЫ ПОЛУЧЕНИЯ ИНЪЕКЦИОННЫХ СКЛЕРОПЕН ДЛЯ СОСУДОВ С ПОМОЩЬЮ МАТРИЦЫ-НОСИТЕЛЯ И ИХ ПРИМЕНЕНИЕ | 2015 |
|
RU2683033C2 |
| КОМПОЗИЦИИ И УСТРОЙСТВА ДЛЯ СКЛЕРОТЕРАПИИ С ПРИМЕНЕНИЕМ СВЕТООТВЕРЖДАЕМЫХ КЛЕЕВ | 2015 |
|
RU2738739C2 |
| СПОСОБ ЛЕЧЕНИЯ ЭКСТРАКРАНИАЛЬНЫХ АРТЕРИОВЕНОЗНЫХ МАЛЬФОРМАЦИЙ ГОЛОВЫ И ШЕИ | 2023 |
|
RU2841253C2 |
| ОБРАЗОВАНИЕ ТЕРАПЕВТИЧЕСКОГО ВСПЕНЕННОГО МАТЕРИАЛА С МИКРОПУЗЫРЬКАМИ ГАЗА | 2000 |
|
RU2261700C2 |
| СПОСОБ ФЛЕБЭКТОМИИ | 2005 |
|
RU2301026C2 |
| СПОСОБ КОМБИНИРОВАННОЙ СКЛЕРОТЕРАПИИ ВАРИКОЗНО ИЗМЕНЕННЫХ ПОДКОЖНЫХ ВЕН | 2017 |
|
RU2669728C1 |
| Пенная композиция для склерозирующей терапии венозных мальформаций головы и шеи у детей и способ проведения терапии с ее применением | 2021 |
|
RU2777202C1 |
| Способ склеротерапии микропенной артерио-венозных мальформаций челюстно-лицевой области пациента под ультразвуковым контролем | 2018 |
|
RU2693344C1 |
| ГИАЛУРОНОВАЯ КИСЛОТА И ЕЕ ПРИМЕНЕНИЕ В ЛЕЧЕНИИ ВЕНОЗНОЙ НЕДОСТАТОЧНОСТИ И ВАРИКОЗНОГО РАСШИРЕНИЯ ВЕН | 2012 |
|
RU2674478C2 |
| СПОСОБ ЭНДОСКОПИЧЕСКОГО СКЛЕРОЗИРОВАНИЯ ВАРИКОЗНО-РАСШИРЕННЫХ ВЕН ПИЩЕВОДА И ЖЕЛУДКА | 2015 |
|
RU2601861C1 |


Изобретение относится к области медицины, а именно к способам получения склерозирующих лекарственных пен. Способ получения склерозирующей лекарственной пены с иерархической структурой заключается в том, что жидкий склерозант смешивают с медицинским газом, таким как О2 или СО2, или комнатным воздухом, путем от 10- до 20-кратного инъецирования «туда-обратно» из одного шприца в другой через запорный кран или наконечник шприца. При этом жидкий склерозант перед вспениванием охлаждают до температуры 0°С, в результате чего при смешивании формируется пена с иерархическим распределением пузырьков по размеру, состоящая из крупных и мелких микропузырьков, причем поверхность крупных микропузырьков заполняется мелкими. Использование изобретения позволяет повысить эффективность склерозирующей лекарственной пены с иерархической структурой в отношении процесса некроза стенок вен, а также обеспечивает полную денатурацию эндотелия стенок вен при использовании минимального количества лекарственного препарата. 3 ил.
Способ получения склерозирующей лекарственной пены с иерархической структурой, заключающийся в том, что жидкий склерозант смешивают с медицинским газом, таким как О2 или СО2, или комнатным воздухом путем от 10- до 20-кратного инъецирования «туда-обратно» из одного шприца в другой через запорный кран или наконечник шприца, отличающийся тем, что жидкий склерозант перед вспениванием охлаждают до температуры 0°С, в результате чего при смешивании формируется пена с иерархическим распределением пузырьков по размеру, состоящая из крупных и мелких микропузырьков, причем поверхность крупных микропузырьков заполняется мелкими.
| УСТРОЙСТВА И СПОСОБЫ ПОЛУЧЕНИЯ ИНЪЕКЦИОННЫХ СКЛЕРОПЕН ДЛЯ СОСУДОВ С ПОМОЩЬЮ МАТРИЦЫ-НОСИТЕЛЯ И ИХ ПРИМЕНЕНИЕ | 2015 |
|
RU2683033C2 |
| ОБРАЗОВАНИЕ ТЕРАПЕВТИЧЕСКОГО ВСПЕНЕННОГО МАТЕРИАЛА С МИКРОПУЗЫРЬКАМИ ГАЗА | 2000 |
|
RU2261700C2 |
| Способ кропения хромировочными красителями | 1926 |
|
SU9362A1 |
| WO 2007045897 A1, 26.04.2007 | |||
| WO 2017085209 A1, 26.05.2017 | |||
| VALENZUELA GC et al | |||
| Foam sclerosants are more stable at lower temperatures | |||
| Eur J Vasc Endovasc Surg., 2013, 46(5):593-9. | |||
Авторы
Даты
2022-11-30—Публикация
2022-03-17—Подача