Область применения
Изобретение относится к биотехнологии и может быть использовано для сохранения in vitro растительного материала, необходимого для научных исследований или для коммерческого растениеводства.
Уровень техники
Долговременное сохранение in vitro коллекций ценных клонов вегетативно размножаемых растений, в настоящее время, необходимо использовать для обеспечения эффективности научных исследований и коммерческого растениеводства. Асептическое хранение растительного материала в ингибирующих рост условиях позволяет минимизировать количество процедур по замене питательных сред и, следовательно, сокращает затраты на содержание коллекций растений in vitro.
Опубликованы разработанные ранее способы сохранения в асептических условиях растений, принадлежащих к различным систематическим группам:
• сохранение in vitro растений земляники (Самсонова О.Н., Трушечкин В.Г. Способ сохранения in vitro жизнеспособности растений: А.С. №1630708 //Бюлл. изобр. 1991. №8. С. 16; Reed В.М. Cold storage of strawberries in vitro: A comparison of three storage systems//Fruit Varieties Journal. 1992. 46. P. 98-102; Lisek A., Orlikowska T. Factors influencing long-term storage of strawberry shoots in vitro//Acta Horticulturae. 2001. V. 560. P. 189-192; Высоцкая O.H. Способ сохранения in vitro растений земляники (Fragaria L.)//Патент России №2564565. Бюлл. изобр. 2015. №28.);
• сохранение in vitro растений рябины (Kjavina D., Ievinsha G. Growth of tissue culture and changes in oxidative enzyme activity of Sorbus and tayberry cultivars during cold storage // Acta Universitatis Latviensis. Biology. 2008. V. 745. P. 179-186; Бъядовский И. А. Влияние жасмоновой кислоты и пониженной температуры на способность к хранению рябины (Sorbus L.) в культуре in vitro // Плодоводство и ягодоводство России. 2017. 51. С. 52-55);
• сохранение in vitro микро-растений картофеля (Sarkar, D., Naik, P.S. Factors affecting minimal growth conservation of potato micro-plants in vitro //Euphytica. 1998. 102. P. 275-280. https://doi.org/10.1023/A:1018309300121; Sarkar D., Sub K.C., Chakrabarti S.K., Naik P.S. Growing of potato micro-plants in the presence of alginate-silver-thiosulfate capsules reduces ethylene-induced culture abnormalities during minimal growth conservation in vitro//Plant Cell, Tissue and Organ Culture. 2002. 68. P. 79-89; Sarkar D., Pandey S.K., Chanemougasoundharam A., Sud K.C. The role of calcium nutrition in potato (Solanum tuberosum) microplants in relation to minimal growth over prolonged storage in vitro//Plant Cell, Tissue and Organ Culture. 2005. V. 81. P. 221-227; Chappell A.L., Koym J.W., Scheuring D.C., Miller Jr J.C., Vales M.I. The Incorporation of Mannitol in Tissue Culture Media for Long-Term Storage of Potatoes at Moderately Low Temperature and Effect on Subsequent Micropropagation. American Journal of Potato Research. 2020. 1-8. https://doi.org/10.1007/s12230-020-09780-6);
• Высоцкая O.H. Длительное сохранение коллекции растений картофеля in vitro // Биофизика живой клетки. 2006. Т. 8. С. 255-260.
В каждом из упомянутых выше методов присутствует одно или несколько технических решений, которые способствовали поддержанию жизнеспособности изолированных от внешней среды in vitro образцов растительного материала без смены и пополнения питательных сред. Такой эффект, как правило, связан с использованием различных способов ингибирования роста растений (Rajasekharan Р.Е., Sahijram L. In Vitro Conservation of Plant Germplasm //Plant Biology and Biotechnology. Eds.: Bahadur В., Venkat Rajam M., Sahijram L., Krishnamurthy K. Springer, New Delhi. 2015. P. 417-443. https://doi.org/10.1007/978-81 -322-2283-5 22; Chauhan R., Singh V., Quraishi A. In Vitro Conservation Through Slow-Growth Storage / Synthetic Seeds. Eds.: Faisal M., Alatar A. Springer, Cham. 2019 P. 397-416. https://doi.org/10.1007/978-3-030-24631-0_19).
Однако мы не обнаружили опубликованных протоколов, которые предлагали бы комплексный подход к долговременному поддержанию in vitro жизнеспособности растительного материала из различных систематических групп без обновления питательной среды и замены сосудов хранения.
Наиболее близким к заявляемому нами техническому решению является способ, который без обновления питательной среды обеспечивает сохранение клонов растительного материала земляники более 2 лет (Высоцкая О.Н. Способ сохранения in vitro растений земляники (Fragaria L.)//Патент России №2564565 Бюлл. изобр. 2015. №28). Протокол данного способа предусматривает размещение побегов земляники, размноженных in vitro, на модифицированной питательной среде, дополненной 6% сахарозы, 10-12 г/л агар-агара, 0,2 мг/л 6-бензиламинопурина и 0,1-0,5 мг/л паклобутразола в пробирках, закрытых с использованием пищевой полиэтиленовой пленки, которые помещают в ингибирующие рост условия (температура от 1 до 10°С, 6 часовой день и освещенность 0,5-0,8 клк). Данный способ отличается тем, что в питательную среду вместо минеральных солей кальция вводят 6 мМ глюконата кальция, а на ее поверхность помещают тиосульфат серебра в альгинате кальция.
Недостатком этого способа является то, что условия хранения образцов растительного материала узко адаптированы для коллекций земляники in vitro. В связи с этим, новый, заявляемый способ хранения растений in vitro был скорректирован для долговременного поддержания жизнеспособности in vitro других растений с иными жизненными формами, онтогенезом и стратегией выживания.
Задача изобретения
Задачей, на решение которой направлено настоящее изобретение, является создание комплексного способа, использование которого позволит длительно сохранять in vitro различный растительный материал в состоянии "минимального роста" без обновления питательной среды.
Решение задачи
Поставленная задача решается тем, что представленный способ сохранения растительного материала in vitro, где используют модификации разработанных ранее протоколов, заключается в асептическом сохранении тканей, органов и целых растений на специальных питательных средах в условиях ингибирования роста и состоит из последовательно выполняемых этапов: культивирование in vitro растительного материала в оптимальных для роста условиях, сохранение образцов растительного материала на модифицированных питательных средах, дополненных 6-9 мМ глюконата кальция - С12Н22СаО14 или нитрата кальция, 6-10% сахарозой, 4-6 г/л маннита, 0,2-0,5 мг/л 6-бензиламинопурина, 0,01-0.05 мг/л индолилмасляной кислоты, 0,2-1 мг/л паклобутразола [1-(4-хлорофенил)-4, 4-диметил-2(1,2,4-триазол-1-ил) пентан-3-ол] и 10-12 г/л агар-агара при +1-20°С в темноте или при 4-16 часовом дне, освещенности 0,5-1 клк в присутствии инкапсулированного альгинатом кальция тиосульфата серебра.
Перечень иллюстративных материалов
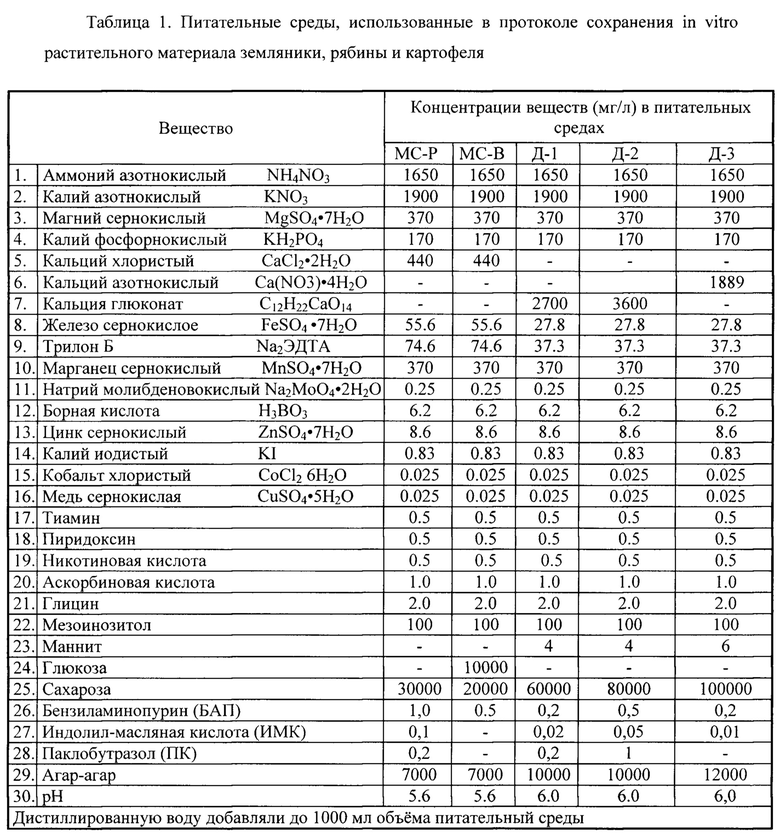
Табл. 1. Питательные среды, использованные в протоколе сохранения in vitro растительного материала земляники, рябины и картофеля
Табл. 2. Сорта земляники, клоны которых сохраняли in vitro (питательная среда Д-1, таблица 1), в соответствии с протоколом из заявленного способа (пример №1)
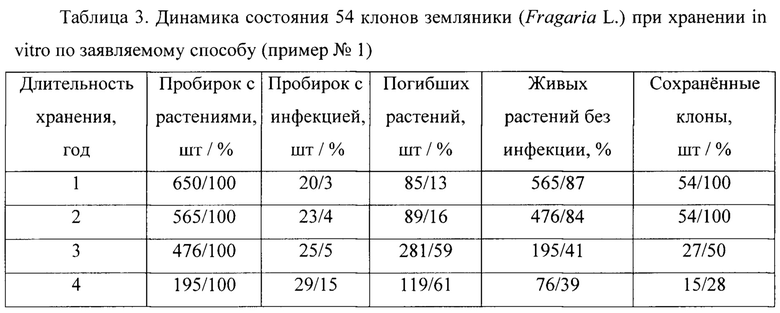
Табл. 3. Динамика состояния клонов земляники (Fragaria L.) при хранении in vitro по заявляемому способу (пример №1)
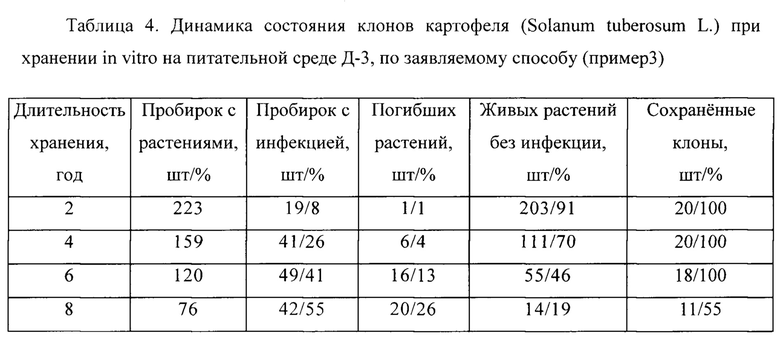
Табл. 4. Динамика состояния клонов картофеля (Solanum tuberosum L.) при хранении in vitro по заявляемому способу (пример №3)
Фиг. 1. Растения земляники садовой (Fragaria L.) после длительного хранения in vitro (3,5-4,4 года) на среде Д-1 с использованием заявляемого способа (пример №1). Фотографии сделаны 18.12.2020. На фотографиях указаны дата посадки и сорт побега.
Фиг. 2. Растения рябины (Sorbus L.) сортов Десертная Мичурина, Титан и Невежинская, которые сохраняли более 4,5 лет на питательной среде Д-2 по заявляемому способу (пример №2) с 20.12.2016 по 24.08.2021 (1708 дней).
Фиг. 3. Клонированный растительный материал картофеля (Solanum tuberosum L., cv. Desire), который сохраняли на среде Д-3 более 4 лет (1598 дней, с 30.10.2004) и более 8 месяцев (269 дней с 20.06.2008) при использовании заявляемого способа (пример №3). Фотография сделана 16.03.2012.
Новизна изобретения
Новизной заявляемого изобретения является комплекс модификаций разработанных ранее способов сохранения in vitro растений из разных систематических групп, где для ингибирования активного роста растительного материала используют: питательные среды, дополненные 6-9 мМ глюконата кальция - С12Н22СаО14 или 6-9 мМ нитрата кальция; 6-10% сахарозы; 4-6 г/л маннита; 0,2-0,5 мг/л 6-бензиламинопурина; 0,01-0.05 мг/л индолилмасляной кислоты; 0,2-1 мг/л паклобутразола [1-(4-хлорофенил)-4, 4-диметил-2(1,2,4-триазол-1-ил) пентан-3-ол] и 10-12 г/л агар-агара, причем сосуды с образцами изолируют от внешней среды с использованием пищевой полиэтиленовой пленки и хранят их при +1-20°С в темноте или на свету в присутствии инкапсулированного альгинатом кальция тиосульфата серебра.
Сущность изобретения
Сущность настоящего изобретения состоит в том, что предлагаемый способ представляет собой комплекс модификаций разработанных ранее способов долговременного сохранения растительного материала, где культивируемые in vitro ткани, органы и целые растения помещают на специализированные питательные среды, содержащие глюконат кальция или нитрат кальция, 6-10% сахарозы, маннит и/или паклобутразол, в изолированные от внешней среды полиэтиленовой пищевой пленкой сосуды вместе с тиосульфатом серебра в альгинате кальция.
Технический результат изобретения
Техническим результатом настоящего изобретения является то, что разработанные ранее способы хранения растений в состоянии "минимального роста" были модифицированы, адаптированы и усовершенствованы для сохранения in vitro ценного растительного материала из разных систематических групп (фиг. 1, 2, 3).
Настоящее изобретение подтверждается следующими примерами.
Пример 1.
Побеги земляники 54 сортов (табл. 2) после размножения in vitro (среда МС-Р) помещают на модифицированную питательную среду Д-1, дополненную 6 мМ (2700 мг/л) глюконата кальция, 6% сахарозы, 4 г/л маннита, 0,2 мг/л 6-бензиламинопурина, 0,02 мг/л индолилмасляной кислоты, 0,5 мг/л паклобутразола и 10 г/л агар-агара (табл. 1) в пробирки вместе с капсулами альгината кальция, содержащими 3% тиосульфата серебра. Затем, пробирки закрывают стеклянным колпачком, который закрепляют пищевой полиэтиленовой пленкой, и сохраняют в холодной камере (1-6°С, 6 часовой день при освещенности 0,5-0,8 клк). После 24 месяцев хранения 65% растений земляники 54 сортов оставались в жизнеспособном состоянии (табл. 3). Следует отметить, что при хранении в данных условиях у многих растений земляники отсутствовали признаки этиолирования и не вытягивались черенки листьев (фиг. 1).
После хранения, живые побеги земляники извлекают из пробирок и изолируют из них меристематические верхушки, которые на агаризованной питательной среде МС-В восстанавливают свой рост. Экспериментально показано, что данный протокол заявляемого способа эффективно использован для долговременного сохранения in vitro коллекции земляники в Институте физиологии растений имени К.А.Тимирязева Российской академии наук (Высоцкая О.Н. Способ сохранения in vitro растений земляники (Fragaria L.)//Патент России №2564565 Бюлл. изобр. 2015. №28; Высоцкая О.Н., Спринчану Е.К., Высоцкий В.А. Испытания технологий долговременного сохранения in vitro коллекций земляники // Плодоводство и ягодоводство России. 2016. 45. Р. 50-53).
Пример 2
Побеги рябины (Sorbus L.) 3 сортов (Десертная Мичурина, Титан и Невежинская) после размножения in vitro (среда МС-Р) помещают на 15 мл модифицированной питательной среды Д-2, дополненной 8 мМ (3600 мг/л) глюконата кальция, 8% сахарозы, 0,5 мг/л 6-бензиламинопурина, 0,05 мг/л индолилмасляной кислоты, 1,0 мг/л паклобутразола и 12 г/л агар-агара (табл. 1), в биологические пробирки вместе с 3% тиосульфатом серебра в капсулах альгината кальция. Затем, пробирки закрывают несколькими слоями пищевой полиэтиленовой пленки и сохраняют в холодной камере (1-6°С, 6 часовой день при освещенности 0,5-1,0 клк). Все пробирки после 4,5 лет хранения содержат жизнеспособные образцы рябины всех 3 сортов (фиг. 2) без визуальных признаков грибной или бактериальной инфекции. Наблюдение за пробирками с растительным материалом рябины (фиг. 2) продолжают для определения максимальной продолжительности сохранения жизнеспособности данного материала в условиях, определенных предлагаемым способом.
Пример 3
В первом эксперименте, побеги картофеля (Solarium tuberosum L.), полученные из меристем этиолированных побегов клубней 20 клонов, сохраняют in vitro на модифицированной питательной среде (Д-3) при 2-6°С без света. Для этого облиственные побеги картофеля длиной 5-7 см помещают на 15 мл среды Д-3 в биологические пробирки, закрытые несколькими слоями пищевой пленки. Один раз в два года проводят визуальный учет состояния образцов растительного материала и регистрируют количество пробирок с погибшими растениями, количество пробирок с инфекцией и количество пробирок с живыми растениями без визуальных признаков инфекции (табл. 4). В ходе хранения экспланты картофеля формируют этиолированные побеги с микроклубнями и корнями. Растения картофеля в 70% пробирок оставались живыми после 4 лет хранения и не были инфицированы (табл. 4). Через 8 лет хранения некоторые образцы выглядели жизнеспособными и после пересадки на свежую питательную среду и формируют зеленые облиственные побеги (Высоцкая О.Н. Длительное сохранение коллекции растений картофеля in vitro // Биофизика живой клетки. 2006. Т. 8. С. 255-260).
В заключительном эксперименте побеги картофеля (cv. Desire) помещают вместе с 3% тиосульфатом серебра в капсулах альгината кальция на 10 мл питательной среды D-2 (табл. 1) в химические пробирки, которые закрывают несколькими слоями пищевой полиэтиленовой пленки. После 4 лет хранения без смены питательной среды в климатической камере (температура 20°С, 16 часовой день, освещенность: 0,5-1,0 клк) образцы оставались живыми без признаков инфицирования (фиг. 3).
Таким образом, экспериментально показана возможность сохранения in vitro коллекций клонированного растительного материала картофеля более 4 лет (на свету и в темноте) без смены питательной среды.
Результаты изобретения
Заявленный способ предназначен для сохранения культивированного in vitro растительного материала в состоянии "минимального роста" и отличается от известных способов тем, что ткани, органы и целые растения из разных систематических групп сохраняют на модифицированных питательных средах, дополненных глюконатом кальция или нитратом кальция, паклобутразолом и/или маннитом в сосудах, изолированных от внешней среды пищевой полиэтиленовой пленкой, на свету или в темноте при 1-20°С в присутствии или в отсутствии альгинатных капсул с тиосульфатом серебра.
Заявляемый способ позволяет сохранять in vitro 100% клонов земляники садовой в течение двух лет, 100% клонов рябины в течение 4,5 лет и 100%) клонов картофеля в течение 4 лет.
Использование комплексного метода сохранения in vitro растительного материала, позволяет существенно сократить расходы на содержание растущих коллекций разнообразных растений и оперативно возобновлять ценные образцы для использования в научных исследованиях, производстве и процессе подготовки специалистов для сельского хозяйства и биотехнологии, а также в сферах экологии и защиты окружающей среды.

| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ СОХРАНЕНИЯ in vitro РАСТЕНИЙ ЗЕМЛЯНИКИ (Fragaria L.) | 2014 |
|
RU2564565C1 |
| СПОСОБ ХРАНЕНИЯ РАСТЕНИЙ РОДА RUBUS В УСЛОВИЯХ IN VITRO | 2018 |
|
RU2731061C2 |
| СПОСОБ КРИОСОХРАНЕНИЯ IN VITRO МЕРИСТЕМ, ИЗОЛИРОВАННЫХ ИЗ РАСТЕНИЙ ЗЕМЛЯНИКИ САДОВОЙ (FRAGARIA L.) | 2006 |
|
RU2302107C1 |
| СПОСОБ КРИОСОХРАНЕНИЯ МЕРИСТЕМ, ИЗОЛИРОВАННЫХ ИЗ РАСТЕНИЙ МАЛИНЫ КРАСНОЙ (RUBUS IDAEUS L.), IN VITRO | 2003 |
|
RU2248121C1 |
| СПОСОБ ДЛИТЕЛЬНОГО ХРАНЕНИЯ IN VITRO МИКРОРАСТЕНИЙ БЕРЕЗЫ | 2016 |
|
RU2634409C1 |
| Универсальная модифицированная питательная среда M-S для клонирования микрорастений земляники сорта Ирма, Елизавета в условиях in vitro | 2020 |
|
RU2747781C1 |
| СПОСОБ РАЗМНОЖЕНИЯ IN VITRO ШТАМБОВЫХ СОРТОВ МАЛИНЫ | 2019 |
|
RU2751250C2 |
| ПИТАТЕЛЬНАЯ СРЕДА ДЛЯ УКОРЕНЕНИЯ ПОБЕГОВ ВИНОГРАДА В КУЛЬТУРЕ IN VITRO | 2017 |
|
RU2676127C2 |
| ПИТАТЕЛЬНАЯ СРЕДА ДЛЯ УКОРЕНЕНИЯ РАСТЕНИЙ IN VITRO | 1996 |
|
RU2111653C1 |
| СПОСОБ РЕГЕНЕРАЦИИ МИКРОПОБЕГОВ HYSSOPUS OFFICINALIS L. В УСЛОВИЯХ IN VITRO | 2014 |
|
RU2529837C1 |



Изобретение относится к области биотехнологии. Изобретение представляет собой способ сохранения растительного материала in vitro, где используют модификации разработанных ранее протоколов, заключающийся в асептическом культивировании растений при оптимальных условиях, в изолировании эксплантов для хранения и их переносе на специальные питательные среды в сосуды для хранения, в сохранении сосудов с образцами растительного материала в условиях ингибирования роста и состоящий из последовательно выполняемых этапов: культивирование in vitro растительного материала в оптимальных для роста условиях, сохранение образцов растительного материала на модифицированных питательных средах, дополненных 3-9 мМ глюконата кальция - С12H22СаО14 или нитрата кальция, 6-10% сахарозой, 4-6 г/л маннита, 0,2-0,5 мг/л 6-бензиламинопурина, 0,01-0,05 мг/л индолилмасляной кислоты, 0,2-1 мг/л паклобутразола [1-(4-хлорофенил)-4,4-диметил-2(1,2,4-триазол-1-ил)пентан-3-ол] и 10-12 г/л агар-агара при +1-20°С на свету (4-16 часовой день при освещенности 0,5-1,0 клк) или в темноте в присутствии или в отсутствие тиосульфата серебра в капсулах альгината кальция. Производят восстановление роста растительного материала in vitro на агаризованных питательных средах, дополненных 3% сахаров (1% глюкозы и 2% сахарозы), 0,5 мг/л 6-бензиламинопурина, и размножение восстановленных образцов на специализированных питательных средах для активного роста. Заявляемый способ позволяет сохранять in vitro побеги картофеля до 8 лет. 3 ил., 4 табл., 3 пр.
Способ сохранения in vitro растений рябины и картофеля, заключающийся в асептическом сохранении растительного материала на специальных питательных средах в условиях ингибирования роста, состоящий из последовательно выполняемых этапов: культивирование растительного материала в оптимальных для роста условиях, сохранение образцов растительного материала в условиях ингибирования роста на модифицированных питательных средах, дополненных 9 мМ глюконата кальция - C12H22CaO14, 8% сахарозой, 4 г/л маннита, 0,5 мг/л 6-бензиламинопурина, 0.05 мг/л индолилмасляной кислоты, 1 мг/л паклобутразола [1-(4-хлорофенил)-4,4-диметил-2(1,2,4-триазол-1-ил)пентан-3-ол] и 10 г/л агар-агара при +1-20°С, 6-16 часовом дне и освещенности 0,5-1 клк в присутствии инкапсулированного альгинатом кальция тиосульфата серебра.
| СПОСОБ СОХРАНЕНИЯ in vitro РАСТЕНИЙ ЗЕМЛЯНИКИ (Fragaria L.) | 2014 |
|
RU2564565C1 |
| КНЯЗЕВА И.В | |||
| и др | |||
| Элементы оптимизации технологии сохранения смородины черной in vitro, Вестник КрасГАУ, 2020, N 6, с | |||
| Приспособление для автоматической односторонней разгрузки железнодорожных платформ | 1921 |
|
SU48A1 |
| БЛЮДНЕВА Е.А | |||
| и др | |||
| Сохранение видов и сортов растений в коллекции in vitro ботанического сада Саратовского госуниверситета, Известия Саратовского | |||
Авторы
Даты
2022-12-12—Публикация
2021-09-02—Подача