Область техники
[0001]
Настоящее изобретение относится к гетероциклическому соединению, в частности гетероциклическому соединению, обладающему активностью, способствующей созреванию кардиомиоцитов, и способу получения зрелых кардиомиоцитов.
[0002]
(Предшествующий уровень техники)
Заболевания сердца являются основной причиной смерти в мире. Пересадка сердца, которая в настоящее время является единственным вариантом лечения пациентов с тяжелой сердечной недостаточностью, страдает от нехватки доноров. Потенциальным возможным методом лечения в качестве альтернативы пересадки сердца является трансплантация кардиомиоцитов, полученных из плюрипотентных стволовых клеток (например, iPS-клеток (индуцированные плюрипотентные стволовые (iPS) клетки), ES-клеток (эмбриональные стволовые клетки), и т.п.). Альтернативный вариант желательно было разработать в кратчайшие сроки. Более того, кардиомиоциты, полученные из плюрипотентных стволовых клеток (например, iPS-клетки, ES-клетки и т.п.), также необходимы в качестве клеток, используемых для тестов на токсичность лекарственного средства и исследований на моделях заболеваний сердца.
Повышение эффективности и безопасности имеет важное значение для применения зрелых кардиомиоцитов, полученных из iPS-клеток, в регенеративной медицине. Что касается эффективности, то существует проблема низкой экономической эффективности, поскольку количество кардиомиоцитов, способных индуцировать созревание, невелико, а белки, такие как факторы роста в культуральной среде, являются очень дорогими. Что касается безопасности, то существует проблема, что кардиомиоциты имеют низкую чистоту, и пролиферативные клетки, отличные от кардиомиоцитов, могут быть загрязнены, так что существует риск развития раковой опухоли.
Более того, для испытаний на токсичность лекарственного средства и исследований на моделях заболеваний сердца с использованием кардиомиоцитов необходимо собрать большое количество зрелых кардиомиоцитов, которые в достаточной степени имитируют кардиомиоциты в живом организме. Кардиомиоциты теряют свой потенциал деления одновременно с рождением, и регенерация этих клеток очень затруднена. Благодаря таким свойствам был проведен ряд исследований по индукции дифференцировки плюрипотентных стволовых клеток в кардиомиоциты с целью получения большого количества кардиомиоцитов (патентный документ 1, патентный документ 2, непатентный документ 1, непатентный документ 2 и непатентный документ 3).
Однако в целом считается, что кардиомиоциты, полученные из плюрипотентных стволовых клеток человека, находятся в незрелой стадии, аналогичной эмбриональным кардиомиоцитам, и что их функция ионных каналов недостаточна по сравнению со взрослыми кардиомиоцитами. Таким образом, для скрининга лекарственной токсичности и терапевтических средств в отношении ионных каналов необходимо использовать зрелые кардиомиоциты.
Поэтому зрелые кардиомиоциты и способ их получения необходимы в качестве клеток, используемых для трансплантации кардиомиоцитов и для скрининга лекарственной токсичности и терапевтического лекарственного средства.
[0003]
В патентном документе 3 сообщается о соединении, представленном следующей формулой
[0004]
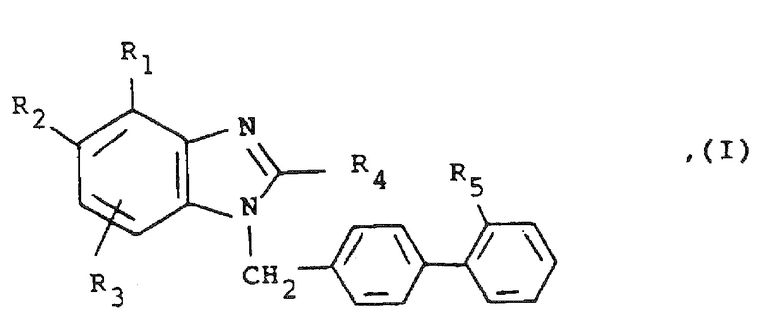
[0005]
где каждый символ имеет значения, указанные выше,
в качестве производного бензимидазола, полезного для лечения заболевания сердца, заболевания легких или расстройства центральной нервной системы (например, болезни Альцгеймера, ишемической болезни).
[0006]
Получить зрелые кардиомиоциты можно путем культивирования незрелых кардиомиоцитов в течение длительного периода (например, 1 год и более). Однако как коммерческий способ получения зрелых кардиомиоцитов, такой способ занимает слишком много времени и требует дорогостоящей среды и добавок к среде.
Следовательно, все еще желательна разработка низкомолекулярных соединений, обладающих активностью, способствующей созреванию кардиомиоцитов, которые могут эффективно получать зрелые кардиомиоциты высокой чистоты за короткий период при низких затратах.
Список цитируемых документов
Патентный документ
[0007]
Патентный документ 1: WO 2007/002136
Патентный документ 2: WO 2009/118928
Патентный документ 3: DE 4212748
Непатентный документ
[0008]
Непатентный документ 1: Yan P, et al, Biochem Biophys Res Commun. 379:115-20 (2009)
Непатентный документ 2: Laflamme MA, et al., Nat Biotechnol, 25:1015-1024 (2007)
Непатентный документ 3: Yang L et al., Nature, 453:524-528 (2008)
Сущность изобретения
Задачи, решаемые с помощью изобретения
[0009]
Настоящее изобретение направлено на обеспечение низкомолекулярных соединений, обладающих активностью, способствующей созреванию кардиомиоцитов, которые позволяют эффективно получать зрелые кардиомиоциты с высокой чистотой за короткий период при низкой стоимости.
Средства решения задач
[0010]
Авторы настоящего изобретения обнаружили, что соединение, представленное следующей формулой (I), или его соль (в настоящем описании, иногда называемое соединением (I)) обладает активностью, способствующей созреванию кардиомиоцитов. В результате дальнейших исследований, они завершили настоящее изобретение.
[0011]
Соответственно, настоящее изобретение заключается в следующем.
[1] Соединение, представленное формулой (I):
[0012]
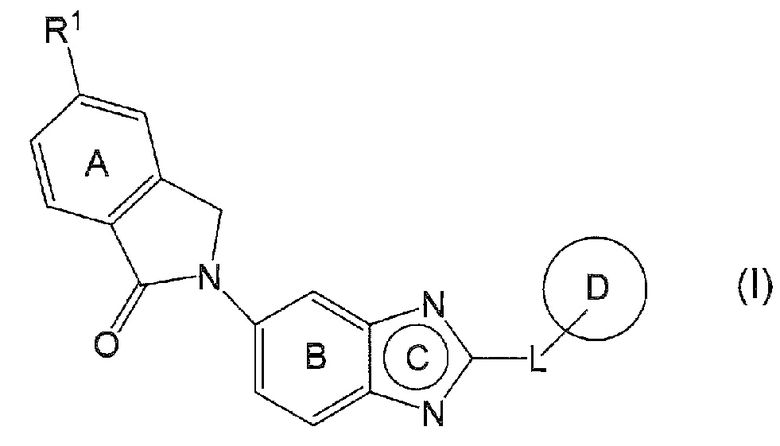
[0013]
где
кольцо A и кольцо B, каждое независимо, представляют собой необязательно дополнительно замещенное бензольное кольцо,
кольцо C представляет собой имидазольное кольцо, необязательно дополнительно замещенное C1-6 алкильной группой(ами), необязательно замещенной 1-3 заместителями, выбранными из
(1) атома галогена,
(2) нитрогруппы,
(3) цианогруппы,
(4) аминогруппы,
(5) гидроксигруппы, и
(6) необязательно галогенированной C1-6 алкоксигруппы,
L представляет собой связь или необязательно замещенную метиленовую группу,
R1 представляет собой атом водорода или заместитель, и
Кольцо D представляет собой необязательно дополнительно замещенное кольцо,
или его соль (далее в настоящем документе именуемое соединением (I)).
[0014]
[2] Соединение или его соль согласно вышеуказанному [1], где в формуле (I),
Кольцо A представляет собой бензольное кольцо;
Кольцо В представляет собой бензольное кольцо;
Кольцо C представляет собой имидазольное кольцо, необязательно дополнительно замещенное C1-6 алкильной группой(ами);
L представляет собой связь или метиленовую группу;
R1 представляет собой
(1) атом водорода,
(2) атом галогена,
(3) моно- или ди-C1-6 алкиламиногруппу,
(4) 5-14-членную ароматическую гетероциклическую группу, или
(5) 3-14-членную неароматическую гетероциклическую группу, необязательно замещенную 1-3 C1-6 алкильными группами; и
Кольцо D представляет собой
(1) бензольное кольцо, необязательно дополнительно замещенное 1-3 заместителями, выбранными из
(a) атома галогена,
(b) гидроксигруппы,
(c) C1-6 алкильной группы, необязательно замещенной 1-3 C1-6 алкоксигруппами,
(d) C1-6 алкоксигруппы, необязательно замещенной 1-3 заместителями, выбранными из
(i) карбоксигруппы,
(ii) C1-6 алкоксикарбонильной группы,
(iii) C7-16 аралкилоксикарбонильной группы,
(iv) карбамоильной группы, необязательно моно- или дизамещенной заместителем(ями), выбранным из
(I) C1-6 алкильной группы, необязательно замещенной 1-3 заместителями, выбранными из
(A) C3-10 циклоалкильной группы,
(B) C6-14 арильной группы,
(C) C6-14 ариламиногруппы, необязательно замещенной 1-3 атомами галогена,
(D) 5-14-членной ароматической гетероциклической группы,
(E) 3-14-членной неароматической гетероциклической группы, и
(F) карбамоильной группы, необязательно моно- или дизамещенной заместителем(ями), выбранным из C1-6 алкильной группы и C7-16 аралкильной группы,
(II) C2-6 алкенильной группы, необязательно замещенной 1-3 C6-14 арильными группами,
(III) C3-10 циклоалкильной группы, необязательно замещенной 1-3 C1-6 алкильными группами,
(IV) C6-14 арильной группы, необязательно замещенной 1-3 заместителями, выбранными из
(A) атома галогена, и
(B) C1-6 алкильной группы,
(V) C7-16 аралкильной группы,
(VI) 5-14-членной ароматической гетероциклической группы, и
(VII) 3-14-членной неароматической гетероциклической группы, и
(v) 3-14-членной неароматической гетероциклилкарбонильной группы, необязательно замещенной 1-3 заместителями, выбранными из
(I) гидроксигруппы, и
(II) C1-6 алкильной группы, и
(e) C7-16 аралкилоксигруппы,
(2) циклогексановое кольцо,
(3) пиридиновое кольцо,
(4) изоксазольное кольцо,
(5) тиофеновое кольцо,
(6) пиперидиновое кольцо, необязательно дополнительно замещенное 1-3 C1-6 алкоксикарбонильными группами, или
(7) тетрагидропирановое кольцо.
[0015]
[3] N-(1,1-Диоксидо-2,3-дигидро-1-бензотиофен-5-ил)-2-(4-(5-(1-оксо-5-(пиперидин-1-ил)-1,3-дигидро-2H-изоиндол-2-ил)-1H-бензимидазол-2-ил)фенокси)ацетамид, или его соль.
[4] 2-(2-(4-Бромфенил)-1H-бензимидазол-5-ил)-5-(морфолин-4-ил)изоиндолин-1-он или его соль.
[5] 5-(Пиперидин-1-ил)-2-(2-(пиридин-3-ил)-1H-бензимидазол-5-ил)изоиндолин-1-он или его соль.
[6] 5-(Пиперидин-1-ил)-2-(2-(пиридин-4-ил)-1H-бензимидазол-5-ил)изоиндолин-1-он или его соль.
[7] 2-(2-(4-Гидроксифенил)-1H-бензимидазол-5-ил)-5-(пиперидин-1-ил)изоиндолин-1-он или его соль.
[0016]
[8] Промотор созревания кардиомиоцитов, содержащий соединение или соль согласно вышеуказанному [1].
[9] Способ получения зрелых кардиомиоцитов, который включает стадию культивирования незрелых кардиомиоцитов в присутствии соединения или соли согласно вышеуказанному [1].
[10] Зрелый кардиомиоцит, полученный способом согласно вышеуказанному [9].
Эффект изобретения
[0017]
Поскольку вышеупомянутое соединение (I) оказывает действие на созревание кардиомиоцитов, его можно использовать в качестве промотора созревания кардиомиоцитов. Способ стимулирования созревания кардиомиоцитов с использованием вышеупомянутого соединения позволяет созревать незрелым кардиомиоцитам за короткий период при низкой стоимости по сравнению со способом культивирования незрелых кардиомиоцитов в течение длительного периода.
Краткое описание фигур
[0018]
[Фигура 1]
На фиг. 1 показаны результаты анализа экспрессии mCherry (контроль (без добавления)) с помощью проточной цитометрии в экспериментальном примере 2.
[Фигура 2]
На фиг. 2 показаны результаты анализа экспрессии mCherry (контроль (добавление DMSO)) с помощью проточной цитометрии в экспериментальном примере 2.
[Фигура 3]
На фиг. 3 показаны результаты анализа экспрессии mCherry (добавление соединения примера 8) с помощью проточной цитометрии в экспериментальном примере 2.
[Фигура 4]
На фиг. 4 показаны результаты анализа экспрессии mCherry (добавление соединения примера 46) с помощью проточной цитометрии в экспериментальном примере 2.
[Фигура 5]
На фиг. 5 показаны результаты анализа экспрессии mCherry (добавление соединения примера 45) с помощью проточной цитометрии в экспериментальном примере 2.
[Фигура 6]
На фиг. 6 показаны результаты анализа экспрессии mCherry (добавление соединения примера 4) с помощью проточной цитометрии в экспериментальном примере 2.
[Фигура 7]
На фиг. 7 показаны результаты анализа экспрессии mCherry (добавление соединения примера 17) с помощью проточной цитометрии в экспериментальном примере 2.
[Фигура 8]
На фиг. 8 показаны результаты анализа экспрессии mCherry с помощью проточной цитометрии в экспериментальном примере 3. На фигурах показаны результаты в случаях контроля (без добавления), контроля (добавление DMSO), добавления соединения примера 8 и соединения A (пример 8: 8-9 дней, соединение: 10-15 дней), и добавления соединения примера 8 и соединения A (пример 8: 8-15 дней, соединение A: 10-15 дней), в порядке с начала.
[0019]
(Подробное описание изобретения)
Определение каждого заместителя, используемого в настоящем описании, подробно описано ниже. Если не указано иное, каждый заместитель имеет следующее значение.
В настоящем описании примеры «атома галогена» включают фтор, хлор, бром и йод.
В настоящем описании примеры «C1-6 алкильной группы» включают метил, этил, пропил, изопропил, бутил, изобутил, втор-бутил, трет-бутил, пентил, изопентил, неопентил, 1-этилпропил, гексил, изогексил, 1,1-диметилбутил, 2,2-диметилбутил, 3,3-диметилбутил и 2-этилбутил.
В настоящем описании примеры «необязательно галогенированной C1-6 алкильной группы» включают C1-6 алкильную группу, необязательно имеющую от 1 до 7, предпочтительно, от 1 до 5, атомов галогена. Конкретные примеры включают метил, хлорметил, дифторметил, трихлорметил, трифторметил, этил, 2-бромэтил, 2,2,2-трифторэтил, тетрафторэтил, пентафторэтил, пропил, 2,2-дифторпропил, 3,3,3-трифторпропил, изопропил, бутил, 4,4,4-трифторбутил, изобутил, втор-бутил, трет-бутил, пентил, изопентил, неопентил, 5,5,5-трифторпентил, гексил и 6,6,6-трифторгексил.
В настоящем описании примеры «C2-6 алкенильной группы» включают этенил, 1-пропенил, 2-пропенил, 2-метил-1-пропенил, 1-бутенил, 2-бутенил, 3-бутенил, 3-метил-2-бутенил, 1-пентенил, 2-пентенил, 3-пентенил, 4-пентенил, 4-метил-3-пентенил, 1-гексенил, 3-гексенил и 5-гексенил.
В настоящем описании примеры «C2-6 алкинильной группы» включают этинил, 1-пропинил, 2-пропинил, 1-бутинил, 2-бутинил, 3-бутинил, 1-пентинил, 2-пентинил, 3-пентинил, 4-пентинил, 1-гексинил, 2-гексинил, 3-гексинил, 4-гексинил, 5-гексинил и 4-метил-2-пентинил.
В настоящем описании примеры «C3-10 циклоалкильной группы» включают циклопропил, циклобутил, циклопентил, циклогексил, циклогептил, циклооктил, бицикло[2.2.1]гептил, бицикло[2.2.2]октил, бицикло[3.2.1]октил и адамантил.
В настоящем описании примеры «необязательно галогенированной C3-10 циклоалкильной группы» включают C3-10 циклоалкильную группу, необязательно имеющую от 1 до 7, предпочтительно, от 1 до 5, атомов галогена. Конкретные примеры включают циклопропил, 2,2-дифторциклопропил, 2,3-дифторциклопропил, циклобутил, дифторциклобутил, циклопентил, циклогексил, циклогептил и циклооктил.
В настоящем описании примеры «C3-10 циклоалкенильной группы» включают циклопропенил, циклобутенил, циклопентенил, циклогексенил, циклогептенил и циклооктенил.
В настоящем описании примеры «C6-14 арильной группы» включают фенил, 1-нафтил, 2-нафтил, 1-антрил, 2-антрил и 9-антрил.
В настоящем описании примеры «C7-16 аралкильной группы» включают бензил, фенетил, нафтилметил и фенилпропил.
[0020]
В настоящем описании примеры «C1-6 алкоксигруппы» включают метокси, этокси, пропокси, изопропокси, бутокси, изобутокси, втор-бутокси, трет-бутокси, пентилокси и гексилокси.
В настоящем описании примеры «необязательно галогенированной C1-6 алкоксигруппы» включают C1-6 алкоксигруппу, необязательно имеющую от 1 до 7, предпочтительно, от 1 до 5, атомов галогена. Конкретные примеры включают метокси, дифторметокси, трифторметокси, этокси, 2,2,2-трифторэтокси, пропокси, изопропокси, бутокси, 4,4,4-трифторбутокси, изобутокси, втор-бутокси, пентилокси и гексилокси.
В настоящем описании примеры «C3-10 циклоалкилоксигруппы» включают циклопропилокси, циклобутилокси, циклопентилокси, циклогексилокси, циклогептилокси и циклооктилокси.
В настоящем описании примеры «C1-6 алкилтиогруппы» включают метилтио, этилтио, пропилтио, изопропилтио, бутилтио, втор-бутилтио, трет-бутилтио, пентилтио и гексилтио.
В настоящем описании примеры «необязательно галогенированной C1-6 алкилтиогруппы» включают C1-6 алкилтиогруппу, необязательно имеющую от 1 до 7, предпочтительно от 1 до 5 атомов галогена. Конкретные примеры включают метилтио, дифторметилтио, трифторметилтио, этилтио, пропилтио, изопропилтио, бутилтио, 4,4,4-трифторбутилтио, пентилтио и гексилтио.
В настоящем описании примеры «C1-6 алкилкарбонильной группы» включают ацетил, пропаноил, бутаноил, 2-метилпропаноил, пентаноил, 3-метилбутаноил, 2-метилбутаноил, 2,2-диметилпропаноил, гексаноил и гептаноил.
В настоящем описании примеры «необязательно галогенированной C1-6 алкилкарбонильной группы» включают C1-6 алкилкарбонильную группу, необязательно имеющую от 1 до 7, предпочтительно от 1 до 5 атомов галогена. Конкретные примеры включают ацетил, хлорацетил, трифторацетил, трихлорацетил, пропаноил, бутаноил, пентаноил и гексаноил.
В настоящем описании примеры «C1-6 алкоксикарбонильной группы» включают метоксикарбонил, этоксикарбонил, пропоксикарбонил, изопропоксикарбонил, бутоксикарбонил, изобутоксикарбонил, втор-бутоксикарбонил, трет-бутоксикарбонил, пентилоксикарбонил и гексилоксикарбонил.
В настоящем описании примеры «C6-14 арилкарбонильной группы» включают бензоил, 1-нафтоил и 2-нафтоил.
В настоящем описании примеры «C7-16 аралкилкарбонильной группы» включают фенилацетил и фенилпропионил.
В настоящем описании примеры «5-14-членной ароматической гетероциклилкарбонильной группы» включают никотиноил, изоникотиноил, теноил и фуроил.
В настоящем описании примеры «3-14-членной неароматической гетероциклилкарбонильной группы» включают морфолинилкарбонил, пиперидинилкарбонил и пирролидинилкарбонил.
[0021]
В настоящем описании примеры «моно- или ди-C1-6 алкилкарбамоильной группы» включают метилкарбамоил, этилкарбамоил, диметилкарбамоил, диэтилкарбамоил и N-этил-N-метилкарбамоил.
В настоящем описании примеры «моно- или ди-C7-16 аралкилкарбамоильной группы» включают бензилкарбамоил и фенетилкарбамоил.
В настоящем описании примеры «C1-6 алкилсульфонильной группы» включают метилсульфонил, этилсульфонил, пропилсульфонил, изопропилсульфонил, бутилсульфонил, втор-бутилсульфонил и трет-бутилсульфонил.
В настоящем описании примеры «необязательно галогенированной C1-6 алкилсульфонильной группы» включают C1-6 алкилсульфонильную группу, необязательно имеющую от 1 до 7, предпочтительно, от 1 до 5, атомов галогена. Конкретные примеры включают метилсульфонил, дифторметилсульфонил, трифторметилсульфонил, этилсульфонил, пропилсульфонил, изопропилсульфонил, бутилсульфонил, 4,4,4-трифторбутилсульфонил, пентилсульфонил и гексилсульфонил.
В настоящем описании примеры «C6-14 арилсульфонильной группы» включают фенилсульфонил, 1-нафтилсульфонил и 2-нафтилсульфонил.
[0022]
В настоящем описании примеры «заместителя» включают атом галогена, цианогруппу, нитрогруппу, необязательно замещенную углеводородную группу, необязательно замещенную гетероциклическую группу, ацильную группу, необязательно замещенную аминогруппу, необязательно замещенную карбамоильную группу, необязательно замещенную тиокарбамоильную группу, необязательно замещенную сульфамоильную группу, необязательно замещенную гидроксигруппу, необязательно замещенную сульфанильную (SH) группу и необязательно замещенную силильную группу.
В настоящем описании примеры «углеводородной группы» (включая «углеводородную группу» в составе «необязательно замещенной углеводородной группы») включают C1-6 алкильную группу, C2-6 алкенильную группу, C2-6 алкинильную группу, C3-10 циклоалкильную группу, C3-10 циклоалкенильную группу, C6-14 арильную группу и C7-16 аралкильную группу.
[0023]
В настоящем описании примеры «необязательно замещенной углеводородной группы» включают углеводородную группу, необязательно имеющую заместитель(и), выбранный из следующей группы заместителей A.
[Группа заместителей A]
(1) атом галогена,
(2) нитрогруппа,
(3) цианогруппа,
(4) оксо группа,
(5) гидроксигруппа,
(6) необязательно галогенированная C1-6 алкоксигруппа,
(7) C6-14 арилокси группа (например, фенокси, нафтокси),
(8) C7-16 аралкилоксигруппа (например, бензилокси),
(9) 5-14-членная ароматическая гетероциклилокси группа (например, пиридилокси),
(10) 3-14-членная неароматическая гетероциклилокси группа (например, морфолинилокси, пиперидинилокси),
(11) C1-6 алкилкарбонилокси группа (например, ацетокси, пропаноилокси),
(12) C6-14 арилкарбонилокси группа (например, бензоилокси, 1-нафтоилокси, 2-нафтоилокси),
(13) C1-6 алкоксикарбонилокси группа (например, метоксикарбонилокси, этоксикарбонилокси, пропоксикарбонилокси, бутоксикарбонилокси),
(14) моно- или ди-C1-6 алкилкарбамоилокси группа (например, метилкарбамоилокси, этилкарбамоилокси, диметилкарбамоилокси, диэтилкарбамоилокси),
(15) C6-14 арилкарбамоилокси группа (например, фенилкарбамоилокси, нафтилкарбамоилокси),
(16) 5-14-членная ароматическая гетероциклилкарбонилокси группа (например, никотиноилокси),
(17) 3-14-членная неароматическая гетероциклилкарбонилокси группа (например, морфолинилкарбонилокси, пиперидинилкарбонилокси),
(18) необязательно галогенированная C1-6 алкилсульфонилокси группа (например, метилсульфонилокси, трифторметилсульфонилокси),
(19) C6-14 арилсульфонилокси группа, необязательно замещенная C1-6 алкильной группой (например, фенилсульфонилокси, толуолсульфонилокси),
(20) необязательно галогенированная C1-6 алкилтиогруппа,
(21) 5-14-членная ароматическая гетероциклическая группа,
(22) 3-14-членная неароматическая гетероциклическая группа,
(23) формильная группа,
(24) карбоксигруппа,
(25) необязательно галогенированная C1-6 алкилкарбонильная группа,
(26) C6-14 арилкарбонильная группа,
(27) 5-14-членная ароматическая гетероциклилкарбонильная группа,
(28) 3-14-членная неароматическая гетероциклилкарбонильная группа,
(29) C1-6 алкоксикарбонильной группы,
(30) C6-14 арилоксикарбонильная группа (например, фенилоксикарбонил, 1-нафтилоксикарбонил, 2-нафтилоксикарбонил),
(31) C7-16 аралкилоксикарбонильная группа (например, бензилоксикарбонил, фенетилоксикарбонил),
(32) карбамоильная группа,
(33) тиокарбамоильная группа,
(34) моно- или ди-C1-6 алкилкарбамоильная группа,
(35) C6-14 арилкарбамоильная группа (например, фенилкарбамоил),
(36) 5-14-членная ароматическая гетероциклилкарбамоильная группа (например, пиридилкарбамоил, тиенилкарбамоил),
(37) 3-14-членная неароматическая гетероциклилкарбамоильная группа (например, морфолинилкарбамоил, пиперидинилкарбамоил),
(38) необязательно галогенированная C1-6 алкилсульфонильная группа,
(39) C6-14 арилсульфонильная группа,
(40) 5-14-членная ароматическая гетероциклилсульфонильная группа (например, пиридилсульфонил, тиенилсульфонил),
(41) необязательно галогенированная C1-6 алкилсульфинильная группа,
(42) C6-14 арилсульфинильная группа (например, фенилсульфинил, 1-нафтилсульфинил, 2-нафтилсульфинил),
(43) 5-14-членная ароматическая гетероциклилсульфинильная группа (например, пиридилсульфинил, тиенилсульфинил),
(44) аминогруппа,
(45) моно- или ди-C1-6 алкиламиногруппа (например, метиламино, этиламино, пропиламино, изопропиламино, бутиламино, диметиламино, диэтиламино, дипропиламино, дибутиламино, N-этил-N-метиламино),
(46) моно- или ди-C6-14 ариламиногруппа (например, фениламино),
(47) 5-14-членная ароматическая гетероциклиламиногруппа (например, пиридиламино),
(48) C7-16 аралкиламиногруппа (например, бензиламино),
(49) формиламиногруппа,
(50) C1-6 алкилкарбониламиногруппа (например, ацетиламино, пропаноиламино, бутаноиламино),
(51) (C1-6 алкил)(C1-6 алкилкарбонил)аминогруппа (например, N-ацетил-N-метиламино),
(52) C6-14 арилкарбониламиногруппа (например, фенилкарбониламино, нафтилкарбониламино),
(53) C1-6 алкоксикарбониламиногруппа (например, метоксикарбониламино, этоксикарбониламино, пропоксикарбониламино, бутоксикарбониламино, трет-бутоксикарбониламино),
(54) C7-16 аралкилоксикарбониламиногруппа (например, бензилоксикарбониламино),
(55) C1-6 алкилсульфониламиногруппа (например, метилсульфониламино, этилсульфониламино),
(56) C6-14 арилсульфониламиногруппа, необязательно замещенная C1-6 алкильной группой (например, фенилсульфониламино, толуолсульфониламино),
(57) необязательно галогенированная C1-6 алкильная группа,
(58) C2-6 алкенильная группа,
(59) C2-6 алкинильная группа,
(60) C3-10 циклоалкильная группа,
(61) C3-10 циклоалкенильная группа, и
(62) C6-14 арильная группа.
[0024]
Число вышеуказанных заместителей в «необязательно замещенной углеводородной группе» составляет, например, от 1 до 5, предпочтительно, от 1 до 3. Когда число заместителей составляет два или более, соответствующие заместители могут быть одинаковыми или различными.
В настоящем описании примеры «гетероциклической группы» (включая «гетероциклическую группу» в составе «необязательно замещенной гетероциклической группы») включают (i) ароматическую гетероциклическую группу, (ii) неароматическую гетероциклическую группу и (iii) 7-10-членную мостиковую гетероциклическую группу, каждая из которых содержит, в качестве составляющих кольцо атомов, помимо атома углерода, от 1 до 4 гетероатомов, выбранных из атома азота, атома серы и атома кислорода.
[0025]
В настоящем описании примеры «ароматической гетероциклической группы» (включая «5-14-членную ароматическую гетероциклическую группу») включают 5-14-членную (предпочтительно 5-10-членную) ароматическую гетероциклическую группу, содержащую в качестве составляющих кольцо атомов, помимо атома углерода, от 1 до 4 гетероатомов, выбранных из атома азота, атома серы и атома кислорода.
Предпочтительные примеры «ароматической гетероциклической группы» включают 5- или 6-членные моноциклические ароматические гетероциклические группы, такие как тиенил, фурил, пирролил, имидазолил, пиразолил, тиазолил, изотиазолил, оксазолил, изоксазолил, пиридил, пиразинил, пиримидинил, пиридазинил, 1,2,4-оксадиазолил, 1,3,4-оксадиазолил, 1,2,4-тиадиазолил, 1,3,4-тиадиазолил, триазолил, тетразолил, триазинил и тому подобное; и
8-14-членные конденсированные полициклические (предпочтительно, би- или три-циклические) ароматические гетероциклические группы, такие как бензотиофенил, бензофуранил, бензимидазолил, бензоксазолил, бензизоксазолил, бензотиазолил, бензизотиазолил, бензотриазолил, имидазопиридинил, тиенопиридинил, фуропиридинил, пирролопиридинил, пиразолопиридинил, оксазолопиридинил, тиазолопиридинил, имидазопиразинил, имидазопиримидинил, тиенопиримидинил, фуропиримидинил, пирролопиримидинил, пиразолопиримидинил, оксазолопиримидинил, тиазолопиримидинил, пиразолотриазинил, нафто[2,3-b]тиенил, феноксатиинил, индолил, изоиндолил, 1H-индазолил, пуринил, изохинолил, хинолил, фталазинил, нафтиридинил, хиноксалинил, хиназолинил, циннолинил, карбазолил, β-карболинил, фенантридинил, акридинил, феназинил, фенотиазинил, феноксазинил и тому подобное.
[0026]
В настоящем описании примеры «неароматической гетероциклической группы» (включая «3-14-членную неароматическую гетероциклическую группу») включают 3-14-членную (предпочтительно, 4-10-членную) неароматическую гетероциклическую группу, содержащую в качестве составляющих кольцо атомов, помимо атома углерода, от 1 до 4 гетероатомов, выбранных из атома азота, атома серы и атома кислорода.
Предпочтительные примеры «неароматической гетероциклической группы» включают 3-8-членные моноциклические неароматические гетероциклические группы, такие как азиридинил, оксиранил, трииранил, азетидинил, оксетанил, тиетанил, тетрагидротиенил, тетрагидрофуранил, пирролинил, пирролидинил, имидазолинил, имидазолидинил, оксазолинил, оксазолидинил, пиразолинил, пиразолидинил, тиазолинил, тиазолидинил, тетрагидроизотиазолил, тетрагидрооксазолил, тетрагидроизооксазолил, пиперидинил, пиперазинил, тетрагидропиридинил, дигидропиридинил, дигидротиопиранил, тетрагидропиримидинил, тетрагидропиридазинил, дигидропиранил, тетрагидропиранил, тетрагидротиопиранил, морфолинил, тиоморфолинил, азепанил, диазепанил, азепинил, оксепанил, азоканил, диазоканил и тому подобное; и
9-14-членные конденсированные полициклические (предпочтительно, би- или трициклические) неароматические гетероциклические группы, такие как дигидробензофуранил, дигидробензимидазолил, дигидробензоксазолил, дигидробензотиазолил, дигидробензизотиазолил, дигидронафто[2,3-b]тиенил, тетрагидроизохинолил, тетрагидрохинолил, 4H-хинолизинил, индолинил, изоиндолинил, тетрагидротиено[2,3-c]пиридинил, тетрагидробензазепинил, тетрагидрохиноксалинил, тетрагидрофенантридинил, гексагидрофенотиазинил, гексагидрофеноксазинил, тетрагидрофталазинил, тетрагидронафтиридинил, тетрагидрохиназолинил, тетрагидроциннолинил, тетрагидрокарбазолил, тетрагидро-β-карболинил, тетрагидроакридинил, тетрагидрофеназинил, тетрагидротиоксантенил, октагидроизохинолил и тому подобное.
[0027]
В настоящем описании предпочтительные примеры «7-10-членной мостиковой гетероциклической группы» включают хинуклидинил и 7-азабицикло[2.2.1]гептанил.
В настоящем описании примеры «азотсодержащей гетероциклической группы» включают «гетероциклическую группу», содержащую в качестве образующего кольцо атома, по меньшей мере, один атом азота.
В настоящем описании примеры «необязательно замещенной гетероциклической группы» включают гетероциклическую группу, необязательно имеющую заместитель(и), выбранный(ые) из вышеуказанной группы заместителей A.
Число заместителей в «необязательно замещенной гетероциклической группе» составляет, например, от 1 до 3. Когда число заместителей составляет два или более, соответствующие заместители могут быть одинаковыми или различными.
[0028]
В настоящем описании примеры «ацильной группы» включают формильную группу, карбоксигруппу, карбамоильную группу, тиокарбамоильную группу, сульфиногруппу, сульфогруппу, сульфамоильную группу и фосфоногруппу, каждая из которых необязательно содержит «1 или 2 заместителя, выбранные из C1-6 алкильной группы, C2-6 алкенильной группы, C3-10 циклоалкильной группаы, C3-10 циклоалкенильной группы, C6-14 арильной группы, C7-16 аралкильной группы, 5-14-членной ароматической гетероциклической группы и 3-14-членной неароматической гетероциклической группы, каждая из которых необязательно имеет от 1 до 3 заместителей, выбранных из атома галогена, необязательно галогенированной C1-6 алкоксигруппы, гидроксигруппы, нитрогруппы, цианогруппы, аминогруппы и карбамоильной группы».
Примеры «ацильной группы» включают также углеводородную-сульфонильную группу, гетероциклилсульфонильную группу, углеводородную-сульфинильную группу и гетероциклилсульфинильную группу.
В настоящем документе углеводородная-сульфонильная группа означает связанную с углеводородной группой сульфонильную группу, гетероциклилсульфонильная группа означает связанную с гетероциклической группой сульфонильную группу, углеводородная-сульфинильная группа означает связанную с углеводородной группой сульфинильную группу, и гетероциклилсульфинильная группа означает связанную с гетероциклической группой сульфинильную группу.
Предпочтительные примеры «ацильной группы» включают формильную группу, карбоксигруппу, C1-6 алкилкарбонильную группу, C2-6 алкенилкарбонильную группу (например, кротоноил), C3-10 циклоалкилкарбонильную группу (например, циклобутанкарбонил, циклопентанкарбонил, циклогексанкарбонил, циклогептанкарбонил), C3-10 циклоалкенилкарбонильную группу (например, 2-циклогексанкарбонил), C6-14 арилкарбонильную группу, C7-16 аралкилкарбонильную группу, 5-14-членную ароматическую гетероциклилкарбонильную группу, 3-14-членную неароматическую гетероциклилкарбонильную группу, C1-6 алкоксикарбонильную группу, C6-14 арилоксикарбонильная группа (например, фенилоксикарбонил, нафтилоксикарбонил), C7-16 аралкилоксикарбонильную группу (например, бензилоксикарбонил, фенетилоксикарбонил), карбамоильную группу, моно- или ди-C1-6 алкилкарбамоильную группу, моно- или ди-C2-6 алкенилкарбамоильную группу (например, диаллилкарбамоил), моно- или ди-C3-10 циклоалкилкарбамоильную группу (например, циклопропилкарбамоил), моно- или ди-C6-14 арилкарбамоильную группу (например, фенилкарбамоил), моно- или ди-C7-16 аралкилкарбамоильную группу, 5-14-членную ароматическую гетероциклилкарбамоильная группа (например, пиридилкарбамоил), тиокарбамоильную группу, моно- или ди-C1-6 алкилтиокарбамоильную группу (например, метилтиокарбамоил, N-этил-N-метилтиокарбамоил), моно- или ди-C2-6 алкенилтиокарбамоильную группу (например, диаллилтиокарбамоил), моно- или ди-C3-10 циклоалкилтиокарбамоильную группу (например, циклопропилтиокарбамоил, циклогексилтиокарбамоил), моно- или ди-C6-14 арилтиокарбамоильную группу (например, фенилтиокарбамоил), моно- или ди-C7-16 аралкилтиокарбамоильную группу (например, бензилтиокарбамоил, фенетилтиокарбамоил), 5-14-членную ароматическую гетероциклилтиокарбамоильную группу (например, пиридилтиокарбамоил), сульфино группу, C1-6 алкилсульфинильную группу (например, метилсульфинил, этилсульфинил), сульфо группу, C1-6 алкилсульфонильную группу, C6-14 арилсульфонильную группу, фосфоногруппу и моно- или ди-C1-6 алкилфосфоногруппу (например, диметилфосфоно, диэтилфосфоно, диизопропилфосфоно, дибутилфосфоно).
[0029]
В настоящем описании примеры «необязательно замещенной аминогруппы» включают аминогруппу, необязательно имеющую «1 или 2 заместителя, выбранных из C1-6 алкильной группы, C2-6 алкенильной группы, C3-10 циклоалкильной группы, C6-14 арильной группы, C7-16 аралкильной группы, C1-6 алкилкарбонильной группы, C6-14 арилкарбонильной группы, C7-16 аралкилкарбонильной группы, 5-14-членной ароматической гетероциклилкарбонильной группы, 3-14-членной неароматической гетероциклилкарбонильной группы, C1-6 алкоксикарбонильной группы, 5-14-членной ароматической гетероциклической группы, карбамоильной группы, моно- или ди-C1-6 алкилкарбамоильной группы, моно- или ди-C7-16 аралкилкарбамоильной группы, C1-6 алкилсульфонильной группы и C6-14 арилсульфонильной группы, каждая из которых необязательно имеет от 1 до 3 заместителей, выбранных из группы заместителей A».
Предпочтительные примеры необязательно замещенной аминогруппы включают аминогруппу, моно- или ди-(необязательно галогенированный C1-6 алкил)аминогруппу (например, метиламино, трифторметиламино, диметиламино, этиламино, диэтиламино, пропиламино, дибутиламино), моно- или ди-C2-6 алкениламиногруппу (например, диаллиламино), моно- или ди-C3-10 циклоалкиламиногруппу (например, циклопропиламино, циклогексиламино), моно- или ди-C6-14 ариламиногруппу (например, фениламино), моно- или ди-C7-16 аралкиламиногруппу (например, бензиламино, дибензиламино), моно- или ди-(необязательно галогенированный C1-6 алкил)-карбониламиногруппу (например, ацетиламино, пропиониламино), моно- или ди-C6-14 арилкарбониламиногруппу (например, бензоиламино), моно- или ди-C7-16 аралкилкарбониламиногруппу (например, бензилкарбониламино), моно- или ди-5-14-членную ароматическую гетероциклилкарбониламиногруппу (например, никотиноиламино, изоникотиноиламино), моно- или ди-3-14-членную неароматическую гетероциклилкарбониламиногруппу (например, пиперидинилкарбониламино), моно- или ди-C1-6 алкоксикарбониламиногруппу (например, трет-бутоксикарбониламино), 5-14-членную ароматическую гетероциклиламиногруппу (например, пиридиламино), карбамоиламиногруппу, (моно- или ди- C1-6 алкилкарбамоил)аминогруппу (например, метилкарбамоиламино), (моно- или ди-C7-16 аралкилкарбамоил)аминогруппу (например, бензилкарбамоиламино), C1-6 алкилсульфониламиногруппу (например, метилсульфониламино, этилсульфониламино), C6-14 арилсульфониламиногруппу (например, фенилсульфониламино), (C1-6 алкил)(C1-6 алкилкарбонил)аминогруппу (например, N-ацетил-N-метиламино) и (C1-6 алкил)(C6-14 арилкарбонил)аминогруппу (например, N-бензоил-N-метиламино).
[0030]
В настоящем описании примеры «необязательно замещенной карбамоильной группы» включают карбамоильную группу, необязательно имеющую «1 или 2 заместителя, выбранных из C1-6 алкильной группы, C2-6 алкенильной группы, C3-10 циклоалкильной группы, C6-14 арильной группы, C7-16 аралкильной группы, C1-6 алкилкарбонильной группы, C6-14 арилкарбонильной группы, C7-16 аралкилкарбонильной группы, 5-14-членной ароматической гетероциклилкарбонильной группы, 3-14-членной неароматической гетероциклилкарбонильной группы, C1-6 алкоксикарбонильной группы, 5-14-членной ароматической гетероциклической группы, карбамоильной группы, моно- или ди-C1-6 алкилкарбамоильной группы и моно- или ди-C7-16 аралкилкарбамоильной группы, каждая из которых необязательно имеет от 1 до 3 заместителей, выбранных из группы заместителей A».
Предпочтительные примеры необязательно замещенной карбамоильной группы включают карбамоильную группу, моно- или ди-C1-6 алкилкарбамоильную группу, моно- или ди-C2-6 алкенилкарбамоильную группу (например, диаллилкарбамоил), моно- или ди-C3-10 циклоалкилкарбамоильную группу (например, циклопропилкарбамоил, циклогексилкарбамоил), моно- или ди-C6-14 арилкарбамоильную группу (например, фенилкарбамоил), моно- или ди-C7-16 аралкилкарбамоильную группу, моно- или ди-C1-6 алкилкарбонилкарбамоильную группу (например, ацетилкарбамоил, пропионилкарбамоил), моно- или ди-C6-14 арилкарбонилкарбамоильную группу (например, бензоилкарбамоил) и 5-14-членную ароматическую гетероциклилкарбамоильную группу (например, пиридилкарбамоил).
[0031]
В настоящем описании примеры «необязательно замещенной тиокарбамоильной группы» включают тиокарбамоильную группу, необязательно имеющую «1 или 2 заместителя, выбранных из C1-6 алкильной группы, C2-6 алкенильной группы, C3-10 циклоалкильной группы, C6-14 арильной группы, C7-16 аралкильной группы, C1-6 алкилкарбонильной группы, C6-14 арилкарбонильной группы, C7-16 аралкилкарбонильной группы, 5-14-членной ароматической гетероциклилкарбонильной группы, 3-14-членной неароматической гетероциклилкарбонильной группы, C1-6 алкоксикарбонильной группы, 5-14-членной ароматической гетероциклической группы, карбамоильной группы, моно- или ди-C1-6 алкилкарбамоильной группы и моно- или ди-C7-16 аралкилкарбамоильной группы, каждая из которых необязательно имеет от 1 до 3 заместителей, выбранных из группы заместителей A».
Предпочтительные примеры необязательно замещенной тиокарбамоильной группы включают тиокарбамоильную группу, моно- или ди-C1-6 алкилтиокарбамоильную группу (например, метилтиокарбамоил, этилтиокарбамоил, диметилтиокарбамоил, диэтилтиокарбамоил, N-этил-N-метилтиокарбамоил), моно- или ди-C2-6 алкенилтиокарбамоильную группу (например, диаллилтиокарбамоил), моно- или ди-C3-10 циклоалкилтиокарбамоильную группу (например, циклопропилтиокарбамоил, циклогексилтиокарбамоил), моно- или ди-C6-14 арилтиокарбамоильную группу (например, фенилтиокарбамоил), моно- или ди-C7-16 аралкилтиокарбамоильную группу (например, бензилтиокарбамоил, фенетилтиокарбамоил), моно- или ди-C1-6 алкилкарбонилтиокарбамоильную группу (например, ацетилтиокарбамоил, пропионилтиокарбамоил), моно- или ди-C6-14 арилкарбонил-тиокарбамоильную группу (например, бензоилтиокарбамоил) и 5-14-членную ароматическую гетероциклилтиокарбамоильную группу (например, пиридилтиокарбамоил).
[0032]
В настоящем описании примеры «необязательно замещенной сульфамоильной группы» включают сульфамоильную группу, необязательно имеющую «1 или 2 заместителя, выбранных из C1-6 алкильной группы, C2-6 алкенильной группы, C3-10 циклоалкильной группы, C6-14 арильной группы, C7-16 аралкильной группы, C1-6 алкилкарбонильной группы, C6-14 арилкарбонильной группы, C7-16 аралкилкарбонильной группы, 5-14-членной ароматической гетероциклилкарбонильной группы, 3-14-членной неароматической гетероциклилкарбонильной группы, C1-6 алкоксикарбонильной группы, 5-14-членной ароматической гетероциклической группы, карбамоильной группы, моно- или ди-C1-6 алкилкарбамоильной группы и моно- или ди-C7-16 аралкилкарбамоильной группы, каждая из которых необязательно имеет от 1 до 3 заместителей, выбранных из группы заместителей A».
Предпочтительные примеры необязательно замещенной сульфамоильной группы включают сульфамоильную группу, моно- или ди-C1-6 алкилсульфамоильную группу (например, метилсульфамоил, этилсульфамоил, диметилсульфамоил, диэтилсульфамоил, N-этил-N-метилсульфамоил), моно- или ди-C2-6 алкенилсульфамоильную группу (например, диаллилсульфамоил), моно- или ди-C3-10 циклоалкилсульфамоильную группу (например, циклопропилсульфамоил, циклогексилсульфамоил), моно- или ди-C6-14 арил-сульфамоильную группу (например, фенилсульфамоил), моно- или ди-C7-16 аралкилсульфамоильную группу (например, бензилсульфамоил, фенетилсульфамоил), моно- или ди-C1-6 алкилкарбонилсульфамоильную группу (например, ацетилсульфамоил, пропионилсульфамоил), моно- или ди-C6-14 арилкарбонилсульфамоильную группу (например, бензоилсульфамоил) и 5-14-членную ароматическую гетероциклилсульфамоильную группу (например, пиридилсульфамоил).
[0033]
В настоящем описании примеры «необязательно замещенной гидроксигруппы» включают гидроксильную группу, необязательно имеющую «заместитель, выбранный из C1-6 алкильной группы, C2-6 алкенильной группы, C3-10 циклоалкильной группы, C6-14 арильной группы, C7-16 аралкильной группы, C1-6 алкилкарбонильной группы, C6-14 арилкарбонильной группы, C7-16 аралкилкарбонильной группы, 5-14-членной ароматической гетероциклилкарбонильной группы, 3-14-членной неароматической гетероциклилкарбонильной группы, C1-6 алкоксикарбонильной группы, 5-14-членной ароматической гетероциклической группы, карбамоильной группы, моно- или ди-C1-6 алкилкарбамоильной группы, моно- или ди-C7-16 аралкилкарбамоильной группы, C1-6 алкилсульфонильной группы и C6-14 арилсульфонильной группы, каждая из которых необязательно имеет от 1 до 3 заместителей, выбранных из группы заместителей A».
Предпочтительные примеры необязательно замещенной гидроксигруппы включают гидроксигруппу, C1-6 алкоксигруппу, C2-6 алкенилоксигруппу (например, аллилокси, 2-бутенилокси, 2-пентенилокси, 3-гексенилокси), C3-10 циклоалкилоксигруппу (например, циклогексилокси), C6-14 арилоксигруппу (например, фенокси, нафтилокси), C7-16 аралкилоксигруппу (например, бензилокси, фенетилокси), C1-6 алкилкарбонилокси группу (например, ацетилокси, пропионилокси, бутирилокси, изобутирилокси, пивалоилокси), C6-14 арилкарбонилокси группу (например, бензоилокси), C7-16 аралкилкарбонилокси группу (например, бензилкарбонилокси), 5-14-членную ароматическую гетероциклилкарбонилоксигруппу (например, никотиноилокси), 3-14-членную неароматическую гетероциклилкарбонилоксигруппу (например, пиперидинилкарбонилокси), C1-6 алкоксикарбонилоксигруппу (например, трет-бутоксикарбонилокси), 5-14-членную ароматическую гетероциклилоксигруппу (например, пиридилокси), карбамоилокси группу, C1-6 алкилкарбамоилокси группу (например, метилкарбамоилокси), C7-16 аралкилкарбамоилоксигруппу (например, бензилкарбамоилокси), C1-6 алкилсульфонилоксигруппу (например, метилсульфонилокси, этилсульфонилокси) и C6-14 арилсульфонилоксигруппу (например, фенилсульфонилокси).
[0034]
В настоящем описании примеры «необязательно замещенной сульфанильной группы» включают сульфанильную группу, необязательно имеющую «заместитель, выбранный из C1-6 алкильной группы, C2-6 алкенильной группы, C3-10 циклоалкильной группы, C6-14 арильной группы, C7-16 аралкильной группы, C1-6 алкилкарбонильной группы, C6-14 арилкарбонильной группы и 5-14-членной ароматической гетероциклической группы, каждая из которых необязательно имеет от 1 до 3 заместителей, выбранных из группы заместителей A» и галогенированной сульфанильной группы.
Предпочтительные примеры необязательно замещенной сульфанильной группы включают сульфанильную (-SH) группу, C1-6 алкилтио группу, C2-6 алкенилтиогруппу (например, аллилтио, 2-бутенилтио, 2-пентенилтио, 3-гексенилтио), C3-10 циклоалкилтиогруппу (например, циклогексилтио), C6-14 арилтиогруппу (например, фенилтио, нафтилтио), C7-16 аралкилтиогруппу (например, бензилтио, фенетилтио), C1-6 алкилкарбонилтиогруппу (например, ацетилтио, пропионилтио, бутирилтио, изобутирилтио, пивалоилтио), C6-14 арилкарбонилтиогруппу (например, бензоилтио), 5-14-членную ароматическую гетероциклилтио группу (например, пиридилтио) и галогенированную тиогруппу (например, пентафтортио).
[0035]
В настоящем описании примеры «необязательно замещенной силильной группы» включают силильную группу, необязательно имеющую «от 1 до 3 заместителей, выбранных из C1-6 алкильной группы, C2-6 алкенильной группы, C3-10 циклоалкильной группы, C6-14 арильной группы и C7-16 аралкильной группы, каждая из которых необязательно имеет от 1 до 3 заместителей, выбранных из группы заместителей A».
Предпочтительные примеры необязательно замещенной силильной группы включают три-C1-6 алкилсилильную группу (например, триметилсилил, трет-бутил(диметил)силил).
[0036]
В настоящем описании примеры «углеводородного кольца» включают C6-14 ароматическое углеводородное кольцо, C3-10 циклоалкан и C3-10 циклоалкен.
В настоящем описании примеры «C6-14 ароматического углеводородного кольца» включают бензол и нафталин.
В настоящем описании примеры «C3-10 циклоалкана» включают циклопропан, циклобутан, циклопентан, циклогексан, циклогептан и циклооктан.
В настоящем описании примеры «C3-10 циклоалкена» включают циклопропен, циклобутен, циклопентен, циклогексен, циклогептен и циклооктен.
В настоящем описании примеры «гетероцикла» включают ароматический гетероцикл и неароматический гетероцикл, каждый содержащий в качестве составляющих кольцо атомов, помимо атома углерода, от 1 до 4 гетероатомов, выбранных из атома азота, атома серы и атома кислорода.
[0037]
В настоящем описании примеры «ароматического гетероцикла» включают 5-14-членный (предпочтительно, 5-10-членный) ароматический гетероцикл, содержащий в качестве составляющих кольцо атомов, помимо атома углерода, от 1 до 4 гетероатомов, выбранных из атома азота, атома серы и атома кислорода. Предпочтительные примеры «ароматического гетероцикла» включают 5- или 6-членные моноциклические ароматические гетероциклы, такие как тиофен, фуран, пиррол, имидазол, пиразол, тиазол, изотиазол, оксазол, изоксазол, пиридин, пиразин, пиримидин, пиридазин, 1,2,4-оксадиазол, 1,3,4-оксадиазол, 1,2,4-тиадиазол, 1,3,4-тиадиазол, триазол, тетразол, триазин и тому подобное; и
8-14-членные конденсированные полициклические (предпочтительно, би- или трициклические) ароматические гетероциклы, такие как бензотиофен, бензофуран, бензимидазол, бензоксазол, бензизоксазол, бензотиазол, бензизотиазол, бензотриазол, имидазопиридин, тиенопиридин, фуропиридин, пирролопиридин, пиразолопиридин, оксазолопиридин, тиазолопиридин, имидазопиразин, имидазопиримидин, тиенопиримидин, фуропиримидин, пирролопиримидин, пиразолопиримидин, оксазолопиримидин, тиазолопиримидин, пиразолопиримидин, пиразолотриазин, нафто[2,3-b]тиофен, феноксатиин, индол, изоиндол, 1H-индазол, пурин, изохинолин, хинолин, фталазин, нафтиридин, хиноксалин, хиназолин, циннолин, карбазол, β-карболин, фенантридин, акридин, феназин, фенотиазин, феноксазин и тому подобное.
[0038]
В настоящем описании примеры «неароматического гетероцикла» включают 3-14-членный (предпочтительно, 4-10-членный) неароматический гетероцикл, содержащий в качестве составляющих кольцо атомов, помимо атома углерода, от 1 до 4 гетероатомов, выбранных из атома азота, атома серы и атома кислорода. Предпочтительные примеры «неароматического гетероцикла» включают 3-8-членные моноциклические неароматические гетероциклы, такие как азиридин, оксиран, тииран, азетидин, оксетан, тиетан, тетрагидротиофен, тетрагидрофуран, пирролин, пирролидин, имидазолин, имидазолидин, оксазолин, оксазолидин, пиразолин, пиразолидин, тиазолин, тиазолидин, тетрагидроизотиазол, тетрагидрооксазол, тетрагидроизоксазол, пиперидин, пиперазин, тетрагидропиридин, дигидропиридин, дигидротиопиран, тетрагидропиримидин, тетрагидропиридазин, дигидропиран, тетрагидропиран, тетрагидротиопиран, морфолин, тиоморфолин, азепанин, диазепан, азепин, азокан, диазокан, оксепан и тому подобное; и
9-14-членные конденсированные полициклические (предпочтительно, би- или трициклические) неароматические гетероциклы, такие как дигидробензофуран, дигидробензимидазол, дигидробензоксазол, дигидробензотиазол, дигидробензизотиазол, дигидронафто[2,3-b]тиофен, тетрагидроизохинолин, тетрагидрохинолин, 4H-хинолизин, индолин, изоиндолин, тетрагидротиено[2,3-c]пиридин, тетрагидробензазепин, тетрагидрохиноксалин, тетрагидрофенантридин, гексагидрофенотиазин, гексагидрофеноксазин, тетрагидрофталазин, тетрагидронафтиридин, тетрагидрохиназолин, тетрагидроциннолин, тетрагидрокарбазол, тетрагидро-β-карболин, тетрагидроакридин, тетрагидрофеназин, тетрагидротиоксантен, октагидроизохинолин и тому подобное.
В настоящем описании примеры «азотсодержащего гетероцикла» включают гетероцикл, содержащий, по меньшей мере, один атом азота в качестве образующего кольцо атома, среди «гетероцикла».
[0039]
В настоящем описании примеры «кольца» включают «углеводородное кольцо» и «гетероцикл».
В настоящем описании примеры «5-6-членной моноциклической ароматической циклической аминогруппы» включают 5-6-членную моноциклическую ароматическую гетероциклическую группу, содержащую, по крайней мере, один атом азота в качестве составляющего атома кольца и имеющую связь с атомом азота, среди «5-6-членной моноциклической ароматической гетероциклической группы». Конкретные примеры включают 1-пирролил, 1-имидазолил, 1-пиразолил, 1-триазолил, 1-тетразолил и тому подобное.
В настоящем описании примеры «3-8-членной моноциклической неароматической циклической аминогруппы» включают 3-8-членную моноциклическую неароматическую гетероциклическую группу, содержащую, по меньшей мере, один атом азота в качестве составляющего атома кольца и имеющую связь на атоме азота, среди «3-8-членной моноциклической неароматической гетероциклической группы». Конкретные примеры включают 1-азиридинил, 1-азетидинил, 1-пирролинил, 1-имидазолидинил, 1-пиразолидинил, 3-оксазолидинил, 3-тиазолидинил, 3-тетрагидроизоксазолил, 3-тетрагидроизотиазолил, 1-пиперидил, 1-пиперазинил, 4-морфолинил, 4-тиоморфолинил и тому подобное.
[0040]
Определение каждого символа в формуле (I) подробно описано ниже.
Кольцо A и кольцо B, каждое независимо, представляют собой необязательно дополнительно замещенное бензольное кольцо.
[0041]
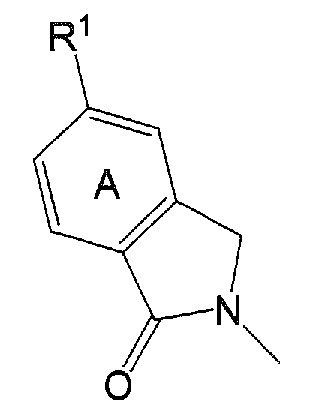
«Необязательно дополнительно замещенное бензольное кольцо», представленное кольцом A, необязательно дополнительно имеет заместитель(ли) в дополнение к R1 в формуле (I). Примеры заместителя включают заместитель(b), выбранный из вышеупомянутой группы заместителей A. Число заместителей составляет от 1 до 3, предпочтительно 1 или 2. Когда число заместителей составляет 2 или более, соответствующие заместители могут быть одинаковыми или различными.
[0042]
Кольцо A предпочтительно представляет собой бензольное кольцо.
[0043]
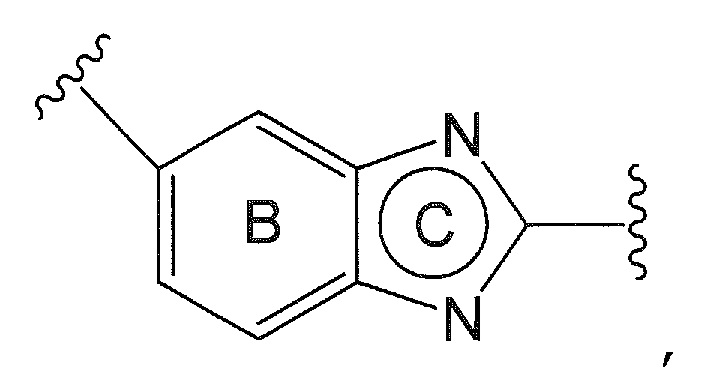
«Необязательно дополнительно замещенное бензольное кольцо», представленное кольцом В, необязательно дополнительно имеет заместитель(ли), в дополнение к
[0044]
[0045]
в формуле (I). Примеры заместителя включают заместитель(и), выбранный из вышеупомянутой группы заместителей A. Число заместителей составляет от 1 до 3, предпочтительно 1 или 2. Когда число заместителей составляет 2 или более, соответствующие заместители могут быть одинаковыми или различными.
[0046]
Кольцо В предпочтительно представляет собой бензольное кольцо.
[0047]
Кольцо C представляет собой имидазольное кольцо, необязательно дополнительно замещенное C1-6 алкильной группой(ами), необязательно замещенной 1-3 заместителями, выбранными из
(1) атома галогена,
(2) нитрогруппы,
(3) цианогруппы,
(4) аминогруппы,
(5) гидроксигруппы, и
(6) необязательно галогенированной C1-6 алкоксигруппы,
в дополнение к -L-кольцу D в формуле (I).
[0048]
Кольцо C предпочтительно представляет собой имидазольное кольцо, необязательно дополнительно замещенное C1-6 алкильной группой(ами) (например, метил).
Кольцо C представляет собой более предпочтительно имидазольное кольцо.
[0049]
Частичная структура, представленная формулой:
[0050]
[0051]
в формуле (I), является частичной структурой, представленной формулой:
[0052]
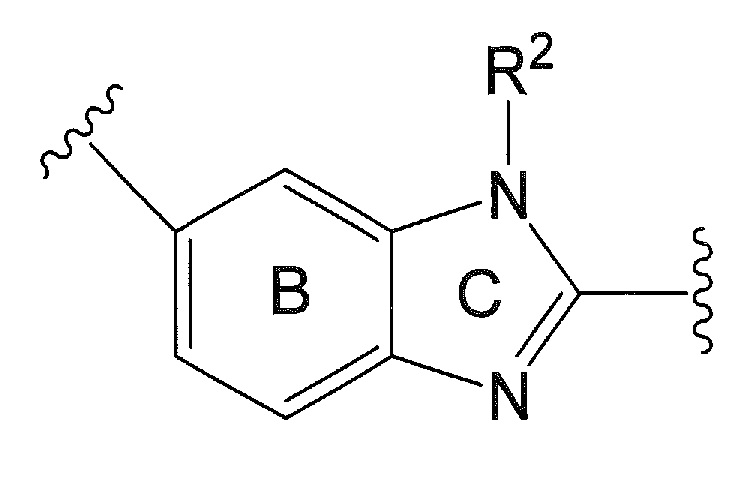 или
или 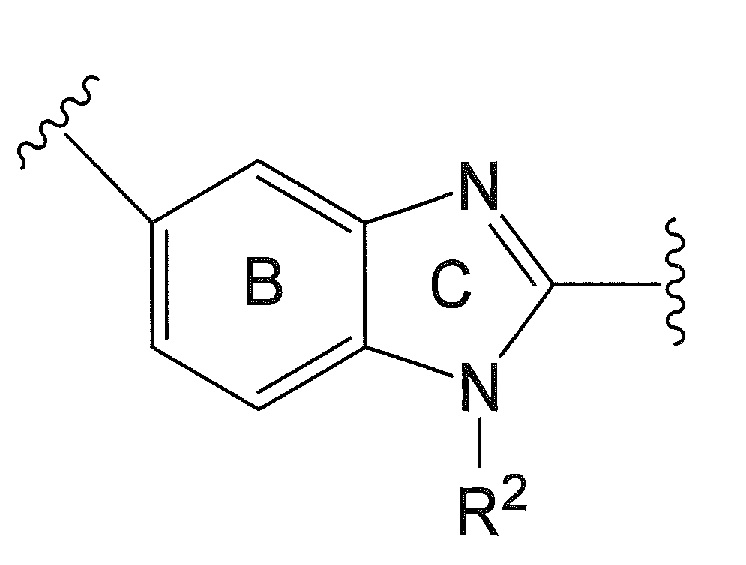 ,
,
[0053]
где R2 представляет собой
(1) атом водорода, или
(2) C1-6 алкильную группу, необязательно замещенную 1-3 заместителями, выбранными из
(a) атома галогена,
(b) нитрогруппы,
(c) цианогруппы,
(d) аминогруппы,
(e) гидроксигруппы, и
(f) необязательно галогенированной C1-6 алкоксигруппы.
[0054]
L представляет собой связь или необязательно замещенную метиленовую группу.
Примеры заместителя в «необязательно замещенной метиленовой группе», представленной L, включают заместитель(и), выбранный из вышеупомянутой группы заместителей A. Число заместителей составляет 1 или 2, предпочтительно 1. Когда число заместителей составляет 2, соответствующие заместители могут быть одинаковыми или различными.
[0055]
L предпочтительно представляет собой связь или метиленовую группу.
L более предпочтительно представляет собой связь.
[0056]
R1 представляет собой атом водорода или заместитель.
R1 предпочтительно представляет собой
(1) атом водорода,
(2) атом галогена (например, атом брома),
(3) необязательно замещенную аминогруппу (предпочтительно моно- или ди-C1-6 алкиламиногруппу (например, диметиламино, диэтиламино)),
(4) необязательно замещенную 5-14-членную ароматическую гетероциклическую группу (предпочтительно 5-6-членную моноциклическую ароматическую гетероциклическую группу, более предпочтительно 5-6-членную моноциклическую ароматическую циклическую аминогруппу (например, 1-пирролил)), или
(5) необязательно замещенную 3-14-членную неароматическую гетероциклическую группу (предпочтительно 3-8-членную моноциклическую неароматическую гетероциклическую группу, более предпочтительно 3-8-членную моноциклическую неароматическую циклическую аминогруппу (например, 1-пиперидил, 1-пиперазинил, 4-морфолинил)).
[0057]
Примеры заместителя вышеупомянутой «необязательно замещенной 5-14-членной ароматической гетероциклической группы» и «необязательно замещенной 3-14-членной неароматической гетероциклической группы» включают заместитель(и), выбранный из вышеупомянутой группы заместителей A. Число заместителей составляет предпочтительно 1-3. Когда число заместителей составляет 2 или более, соответствующие заместители могут быть одинаковыми или различными.
[0058]
R1 представляет собой более предпочтительно
(1) атом водорода,
(2) атом галогена (например, атом брома),
(3) моно- или ди-C1-6 алкиламиногруппу (например, диметиламино, диэтиламино),
(4) 5-14-членную ароматическую гетероциклическую группу (предпочтительно 5-6-членную моноциклическую ароматическую гетероциклическую группу, более предпочтительно 5-6-членную моноциклическую ароматическую циклическую аминогруппу (например, 1-пирролил)), или
(5) 3-14-членную неароматическую гетероциклическую группу (предпочтительно 3-8-членная (предпочтительно 5-6-членная) моноциклическая неароматическая гетероциклическая группа, более предпочтительно 3-8-членная (предпочтительно 5-6-членная) моноциклическая неароматическая циклическая аминогруппа (например, 1-пиперидил, 1-пиперазинил, 4-морфолинил)), необязательно замещенную 1-3 C1-6 алкильными группами (например, метил).
[0059]
R1 кроме того более предпочтительно представляет собой 3-8-членную (предпочтительно 5-6-членную) моноциклическую неароматическую гетероциклическую группу (предпочтительно 3-8-членную (предпочтительно 5-6-членную) моноциклическую неароматическую циклическую аминогруппа (например, 1-пиперидил, 4-морфолинил)).
[0060]
R1 еще более предпочтительно представляет собой 3-8-членную (предпочтительно 5-6-членную) моноциклическую неароматическую циклическую аминогруппу (например, 1-пиперидил, 4-морфолинил).
[0061]
R1 особенно предпочтительно представляет собой 6-членную моноциклическую неароматическую циклическую аминогруппу (например, 1-пиперидил, 4-морфолинил).
[0062]
Кольцо D представляет собой необязательно дополнительно замещенное кольцо.
«Кольцо» «необязательно дополнительно замещенного кольца», представленного кольцом D, предпочтительно представляет собой C6-14 ароматическое углеводородное кольцо (например, бензол), C3-10 циклоалкан (предпочтительно C3-8 циклоалкан (например, циклогексан)), 5-14-членный ароматический гетероцикл (предпочтительно 5-6-членный моноциклический ароматический гетероцикл (например, пиридин, изоксазол, тиофен)) или 3-14-членный неароматический гетероцикл (предпочтительно 3-8-членный моноциклический неароматический гетероцикл (например, пиперидин, тетрагидропиран)), более предпочтительно бензольное кольцо, циклогексановое кольцо, пиридиновое кольцо, изоксазольное кольцо, тиофеновое кольцо, пиперидиновое кольцо или тетрагидропирановое кольцо, особенно предпочтительно бензольное кольцо.
[0063]
Кольцо D предпочтительно представляет собой
(1) необязательно дополнительно замещенное C6-14 ароматическое углеводородное кольцо (например, бензол),
(2) необязательно дополнительно замещенный C3-10 циклоалкан (предпочтительно C3-8 циклоалкан (например, циклогексан)),
(3) необязательно дополнительно замещенный 5-14-членный ароматический гетероцикл (предпочтительно 5-6-членный моноциклический ароматический гетероцикл (например, пиридин, изоксазол, тиофен)), или
(4) необязательно дополнительно замещенный 3-14-членный неароматический гетероцикл (предпочтительно 3-8-членный моноциклический неароматический гетероцикл (например, пиперидин, тетрагидропиран)).
[0064]
Вышеупомянутые «необязательно дополнительно замещенное C6-14 ароматическое углеводородное кольцо», «необязательно дополнительно замещенный C3-10 циклоалкан», «необязательно дополнительно замещенный 5-14-членный ароматический гетероцикл» и «необязательно дополнительно замещенный 3-14-членный неароматический гетероцикл», каждый необязательно дополнительно имеет заместитель(ли) в дополнение к -L-кольцу C/кольцу B в формуле (I). Примеры заместителя включают вышеупомянутый «заместитель». Число заместителей составляет предпочтительно 1-3. Когда число заместителей составляет 2 или более, соответствующие заместители могут быть одинаковыми или различными.
[0065]
Кольцо D представляет собой более предпочтительно
(1) C6-14 ароматическое углеводородное кольцо (например, бензол), необязательно дополнительно замещенное 1-3 заместителями, выбранными из
(a) атом галогена (например, атом фтора, атом хлора, атом брома),
(b) гидроксигруппы,
(c) C1-6 алкильной группы (например, метил), необязательно замещенной 1-3 C1-6 алкоксигруппами (например, метокси),
(d) C1-6 алкоксигруппы (например, метокси, этокси, пропокси, изопропокси, гексилокси), необязательно замещенной 1-3 заместителями, выбранными из
(i) карбоксигруппы,
(ii) C1-6 алкоксикарбонильной группы (например, метоксикарбонил),
(iii) C7-16 аралкилоксикарбонильной группы (например, бензилоксикарбонил),
(iv) карбамоильной группы, необязательно моно- или дизамещенной заместителем(ями), выбранным из
(I) C1-6 алкильной группы (например, метил, этил, пропил, изопропил, изобутил), необязательно замещенной 1-3 заместителями, выбранными из
(A) C3-10 циклоалкильной группы (например, циклопропил),
(B) C6-14 арильной группы (например, фенил),
(C) C6-14 ариламиногруппы (например, фениламино), необязательно замещенной 1-3 атомами галогена (например, атом фтора),
(D) 5-14-членной ароматической гетероциклической группы (предпочтительно 5-6-членная моноциклическая ароматическая гетероциклическая группа (например, пиридил)),
(E) 3-14-членной неароматической гетероциклической группы (предпочтительно 3-8-членная моноциклическая неароматическая гетероциклическая группа (например, тетрагидропиранил)), и
(F) карбамоильной группы, необязательно моно- или дизамещенной заместителем(ями), выбранным из C1-6 алкильной группы (например, метил) и C7-16 аралкильной группы (например, 2-фенилэтил),
(II) C2-6 алкенильной группы (например, пент-2-ил), необязательно замещенной 1-3 C6-14 арильными группами (например, фенил),
(III) C3-10 циклоалкильной группы (например, циклопропил), необязательно замещенной 1-3 C1-6 алкильными группами (например, метил),
(IV) C6-14 арильной группы (например, фенил), необязательно замещенной 1-3 заместителями, выбранными из
(A) атома галогена (например, атом фтора, атом хлора), и
(B) C1-6 алкильной группы (например, метил),
(V) C7-16 аралкильной группы (например, бензил),
(VI) 5-14-членной ароматической гетероциклической группы (предпочтительно 5-6-членная моноциклическая ароматическая гетероциклическая группа (например, пиридил)), и
(VII) 3-14-членной неароматической гетероциклической группы (предпочтительно 3-8-членная моноциклическая неароматическая гетероциклическая группа (например, тетрагидропиранил), 9-14-членная конденсированная полициклическая (предпочтительно би- или трициклическая) неароматическая гетероциклическая группа (например, 1,1-диоксидодигидробензотиенил)), и
(v) 3-14-членной неароматической гетероциклилкарбонильной группы (предпочтительно 3-8-членная моноциклическая неароматическая гетероциклилкарбонильная группа (например, пирролидинилкарбонил, пиперидилкарбонил, морфолинилкарбонил, 1,1-диоксидотиазолидинилкарбонил)), необязательно замещенной 1-3 заместителями, выбранными из
(I) гидроксигруппы, и
(II) C1-6 алкильной группы (например, метил), и
(e) C7-16 аралкилоксигруппы (например, бензилокси),
(2) C3-10 циклоалкан (предпочтительно C3-8 циклоалкан (например, циклогексан)),
(3) 5-14-членный ароматический гетероцикл (предпочтительно 5-6-членный моноциклический ароматический гетероцикл (например, пиридин, изоксазол, тиофен)), или
(4) 3-14-членный неароматический гетероцикл (предпочтительно 3-8-членный моноциклический неароматический гетероцикл (например, пиперидин, тетрагидропиран)), необязательно дополнительно замещенный 1-3 C1-6 алкоксикарбонильными группами (например, трет-бутоксикарбонил).
[0066]
Кольцо D, кроме того, более предпочтительно представляет собой
(1) бензольное кольцо, необязательно дополнительно замещенное 1-3 заместителями, выбранными из
(a) атома галогена (например, атом фтора, атом хлора, атом брома),
(b) гидроксигруппы,
(c) C1-6 алкильной группы (например, метил), необязательно замещенной 1-3 C1-6 алкоксигруппами (например, метокси),
(d) C1-6 алкоксигруппы (например, метокси, этокси, пропокси, изопропокси, гексилокси), необязательно замещенной 1-3 заместителями, выбранными из
(i) карбоксигруппы,
(ii) C1-6 алкоксикарбонильной группы (например, метоксикарбонил),
(iii) C7-16 аралкилоксикарбонильной группы (например, бензилоксикарбонил),
(iv) карбамоильной группы, необязательно моно- или дизамещенной заместителем(ями), выбранным из
(I) C1-6 алкильной группы (например, метил, этил, пропил, изопропил, изобутил), необязательно замещенной 1-3 заместителями, выбранными из
(A) C3-10 циклоалкильной группы (например, циклопропил),
(B) C6-14 арильной группы (например, фенил),
(C) C6-14 ариламиногруппы (например, фениламино), необязательно замещенной 1-3 атомами галогена (например, атом фтора),
(D) 5-14-членной ароматической гетероциклической группы (предпочтительно 5-6-членная моноциклическая ароматическая гетероциклическая группа (например, пиридил)),
(E) 3-14-членной неароматической гетероциклической группы (предпочтительно 3-8-членная моноциклическая неароматическая гетероциклическая группа (например, тетрагидропиранил)), и
(F) карбамоильной группы, необязательно моно- или дизамещенной заместителем(ями), выбранным из C1-6 алкильной группы (например, метил) и C7-16 аралкильной группы (например, 2-фенилэтил),
(II) C2-6 алкенильной группы (например, пент-2-ил), необязательно замещенной 1-3 C6-14 арильными группами (например, фенил),
(III) C3-10 циклоалкильной группы (например, циклопропил), необязательно замещенной 1-3 C1-6 алкильными группами (например, метил),
(IV) C6-14 арильной группы (например, фенил), необязательно замещенной 1-3 заместителями, выбранными из
(A) атома галогена (например, атом фтора, атом хлора), и
(B) C1-6 алкильной группы (например, метил),
(V) C7-16 аралкильной группы (например, бензил),
(VI) 5-14-членной ароматической гетероциклической группы (предпочтительно 5-6-членная моноциклическая ароматическая гетероциклическая группа (например, пиридил)), и
(VII) 3-14-членной неароматической гетероциклической группы (предпочтительно 3-8-членная моноциклическая неароматическая гетероциклическая группа (например, тетрагидропиранил), 9-14-членная конденсированная полициклическая (предпочтительно би- или трициклическая) неароматическая гетероциклическая группа (например, 1,1-диоксидодигидробензотиенил)), и
(v) 3-14-членной неароматической гетероциклилкарбонильной группы (предпочтительно 3-8-членная моноциклическая неароматическая гетероциклилкарбонильная группа (например, пирролидинилкарбонил, пиперидилкарбонил, морфолинилкарбонил, 1,1-диоксидотиазолидинилкарбонил)), необязательно замещенной 1-3 заместителями, выбранными из
(I) гидроксигруппы, и
(II) C1-6 алкильной группы (например, метил), и
(e) C7-16 аралкилоксигруппы (например, бензилокси),
(2) циклогексановое кольцо,
(3) пиридиновое кольцо,
(4) изоксазольное кольцо,
(5) тиофеновое кольцо,
(6) пиперидиновое кольцо, необязательно дополнительно замещенное 1-3 C1-6 алкоксикарбонильными группами (например, трет-бутоксикарбонил), или
(7) тетрагидропирановое кольцо.
[0067]
Кольцо D еще более предпочтительно представляет собой бензольное кольцо, необязательно дополнительно замещенное 1-3 заместителями, выбранными из
(a) атома галогена (например, атом брома), и
(b) C1-6 алкоксигруппы (например, метокси), необязательно замещенной 1-3 заместителями, выбранными из
(i) карбамоильной группы, необязательно моно- или дизамещенной заместителем(ями), выбранным из
(I) C1-6 алкильной группы (например, метил, изобутил), необязательно замещенной 1-3 C3-6 циклоалкильными группами (например, циклопропил), и
(II) 3-8-членной моноциклической неароматической гетероциклической группы (например, тетрагидропиранил), и
(ii) 3-8-членной моноциклической неароматической гетероциклилкарбонильной группы (например, пиперидилкарбонил), необязательно замещенной 1-3 заместителями, выбранными из
(I) гидроксигруппы, и
(II) C1-6 алкильной группы (например, метил).
[0068]
В другом варианте осуществления кольцо D еще более предпочтительно представляет собой
(1) бензольное кольцо, необязательно дополнительно замещенное 1-3 заместителями, выбранными из
(a) атома галогена (например, атом брома),
(b) гидроксигруппы, и
(c) C1-6 алкоксигруппы (например, метокси), необязательно замещенной карбамоильной группой(ами), необязательно моно- или дизамещенной 9-14-членной конденсированной полициклической (предпочтительно би- или трициклической) неароматической гетероциклической группой(ами) (например, 1,1-диоксидодигидробензотиенил), или
(2) пиридиновое кольцо.
[0069]
В варианте осуществления кольцо D особенно предпочтительно представляет собой бензольное кольцо, дополнительно замещенное одним заместителем, выбранным из
(a) атома галогена (например, атом брома), и
(b) C1-6 алкоксигруппы (например, метокси), замещенной карбамоильной группой(ами), монозамещенной 9-14-членной конденсированной полициклической (предпочтительно би- или трициклической) неароматической гетероциклической группой (например, 1,1-диоксидодигидробензотиенил).
[0070]
Предпочтительные примеры соединения (I) включают следующие соединения.
[0071]
[Соединение A]
Соединение (I), где
Кольцо A представляет собой необязательно дополнительно замещенное бензольное кольцо;
Кольцо B представляет собой необязательно дополнительно замещенное бензольное кольцо;
Кольцо C представляет собой имидазольное кольцо, необязательно дополнительно замещенное C1-6 алкильной группой(ами), необязательно замещенной 1-3 заместителями, выбранными из
(1) атома галогена,
(2) нитрогруппы,
(3) цианогруппы,
(4) аминогруппы,
(5) гидроксигруппы, и
(6) необязательно галогенированной C1-6 алкоксигруппы;
L представляет собой связь или необязательно замещенную метиленовую группу;
R1 представляет собой
(1) атом водорода,
(2) атом галогена (например, атом брома),
(3) необязательно замещенную аминогруппу (предпочтительно моно- или ди-C1-6 алкиламиногруппу (например, диметиламино, диэтиламино)),
(4) необязательно замещенную 5-14-членную ароматическую гетероциклическую группу (предпочтительно 5-6-членную моноциклическую ароматическую гетероциклическую группу, более предпочтительно 5-6-членную моноциклическую ароматическую циклическую аминогруппу (например, 1-пирролил)), или
(5) необязательно замещенную 3-14-членную неароматическую гетероциклическую группу (предпочтительно 3-8-членную моноциклическую неароматическую гетероциклическую группу, более предпочтительно 3-8-членную моноциклическую неароматическую циклическую аминогруппу (например, 1-пиперидил, 1-пиперазинил, 4-морфолинил)); и
Кольцо D представляет собой
(1) необязательно дополнительно замещенное C6-14 ароматическое углеводородное кольцо (например, бензол),
(2) необязательно дополнительно замещенный C3-10 циклоалкан (предпочтительно C3-8 циклоалкан (например, циклогексан)),
(3) необязательно дополнительно замещенный 5-14-членный ароматический гетероцикл (предпочтительно 5-6-членный моноциклический ароматический гетероцикл (например, пиридин, изоксазол, тиофен)), или
(4) необязательно дополнительно замещенный 3-14-членный неароматический гетероцикл (предпочтительно 3-8-членный моноциклический неароматический гетероцикл (например, пиперидин, тетрагидропиран)).
[0072]
[Соединение B]
Соединение (I), где
Кольцо A представляет собой бензольное кольцо;
Кольцо В представляет собой бензольное кольцо;
Кольцо C представляет собой имидазольное кольцо, необязательно дополнительно замещенное C1-6 алкильной группой(ами) (например, метил);
L представляет собой связь или метиленовую группу;
R1 представляет собой
(1) атом водорода,
(2) атом галогена (например, атом брома),
(3) моно- или ди-C1-6 алкиламиногруппу (например, диметиламино, диэтиламино),
(4) 5-14-членную ароматическую гетероциклическую группу (предпочтительно 5-6-членную моноциклическую ароматическую гетероциклическую группу, более предпочтительно 5-6-членную моноциклическую ароматическую циклическую аминогруппу (например, 1-пирролил)), или
(5) 3-14-членную неароматическую гетероциклическую группу (предпочтительно 3-8-членная (предпочтительно 5-6-членная) моноциклическая неароматическая гетероциклическая группа, более предпочтительно 3-8-членная (предпочтительно 5-6-членная) моноциклическая неароматическая циклическая аминогруппа (например, 1-пиперидил, 1-пиперазинил, 4-морфолинил)), необязательно замещенную 1-3 C1-6 алкильными группами (например, метил); и
Кольцо D представляет собой
(1) C6-14 ароматическое углеводородное кольцо (например, бензол), необязательно дополнительно замещенное 1-3 заместителями, выбранными из
(a) атома галогена (например, атом фтора, атом хлора, атом брома),
(b) гидроксигруппы,
(c) C1-6 алкильной группы (например, метил), необязательно замещенной 1-3 C1-6 алкоксигруппами (например, метокси),
(d) C1-6 алкоксигруппы (например, метокси, этокси, пропокси, изопропокси, гексилокси), необязательно замещенной 1-3 заместителями, выбранными из
(i) карбоксигруппы,
(ii) C1-6 алкоксикарбонильной группы (например, метоксикарбонил),
(iii) C7-16 аралкилоксикарбонильной группы (например, бензилоксикарбонил),
(iv) карбамоильной группы, необязательно моно- или дизамещенной заместителем(ями), выбранным из
(I) C1-6 алкильной группы (например, метил, этил, пропил, изопропил, изобутил), необязательно замещенной 1-3 заместителями, выбранными из
(A) C3-10 циклоалкильной группы (например, циклопропил),
(B) C6-14 арильной группы (например, фенил),
(C) C6-14 ариламиногруппы (например, фениламино), необязательно замещенной 1-3 атомами галогена (например, атом фтора),
(D) 5-14-членной ароматической гетероциклической группы (предпочтительно 5-6-членная моноциклическая ароматическая гетероциклическая группа (например, пиридил)),
(E) 3-14-членной неароматической гетероциклической группы (предпочтительно 3-8-членная моноциклическая неароматическая гетероциклическая группа (например, тетрагидропиранил)), и
(F) карбамоильной группы, необязательно моно- или дизамещенной заместителем(ями), выбранным из C1-6 алкильной группы (например, метил) и C7-16 аралкильной группы (например, 2-фенилэтил),
(II) C2-6 алкенильной группы (например, пент-2-ил), необязательно замещенной 1-3 C6-14 арильными группами (например, фенил),
(III) C3-10 циклоалкильной группы (например, циклопропил), необязательно замещенной 1-3 C1-6 алкильными группами (например, метил),
(IV) C6-14 арильной группы (например, фенил), необязательно замещенной 1-3 заместителями, выбранными из
(A) атома галогена (например, атом фтора, атом хлора), и
(B) C1-6 алкильной группы (например, метил),
(V) C7-16 аралкильной группы (например, бензил),
(VI) 5-14-членной ароматической гетероциклической группы (предпочтительно 5-6-членная моноциклическая ароматическая гетероциклическая группа (например, пиридил)), и
(VII) 3-14-членной неароматической гетероциклической группы (предпочтительно 3-8-членная моноциклическая неароматическая гетероциклическая группа (например, тетрагидропиранил), 9-14-членная конденсированная полициклическая (предпочтительно би- или трициклическая) неароматическая гетероциклическая группа (например, 1,1-диоксидодигидробензотиенил)), и
(v) 3-14-членной неароматической гетероциклилкарбонильной группы (предпочтительно 3-8-членная моноциклическая неароматическая гетероциклилкарбонильная группа (например, пирролидинилкарбонил, пиперидилкарбонил, морфолинилкарбонил, 1,1-диоксидотиазолидинилкарбонил)), необязательно замещенной 1-3 заместителями, выбранными из
(I) гидроксигруппы, и
(II) C1-6 алкильной группы (например, метил), и
(e) C7-16 аралкилоксигруппы (например, бензилокси),
(2) C3-10 циклоалкан (предпочтительно C3-8 циклоалкан (например, циклогексан)),
(3) 5-14-членный ароматический гетероцикл (предпочтительно 5-6-членный моноциклический ароматический гетероцикл (например, пиридин, изоксазол, тиофен)), или
(4) 3-14-членный неароматический гетероцикл (предпочтительно 3-8-членный моноциклический неароматический гетероцикл (например, пиперидин, тетрагидропиран)), необязательно дополнительно замещенный 1-3 C1-6 алкоксикарбонильными группами (например, трет-бутоксикарбонил).
[0073]
[Соединение C]
Соединение (I), где
Кольцо A представляет собой бензольное кольцо;
Кольцо В представляет собой бензольное кольцо;
Кольцо C представляет собой имидазольное кольцо, необязательно дополнительно замещенное C1-6 алкильной группой(ами) (например, метил);
L представляет собой связь или метиленовую группу;
R1 представляет собой
(1) атом водорода,
(2) атом галогена (например, атом брома),
(3) моно- или ди-C1-6 алкиламиногруппу (например, диметиламино, диэтиламино),
(4) 5-14-членную ароматическую гетероциклическую группу (предпочтительно 5-6-членную моноциклическую ароматическую гетероциклическую группу, более предпочтительно 5-6-членную моноциклическую ароматическую циклическую аминогруппу (например, 1-пирролил)), или
(5) 3-14-членную неароматическую гетероциклическую группу (предпочтительно 3-8-членная (предпочтительно 5-6-членная) моноциклическая неароматическая гетероциклическая группа, более предпочтительно 3-8-членная (предпочтительно 5-6-членная) моноциклическая неароматическая циклическая аминогруппа (например, 1-пиперидил, 1-пиперазинил, 4-морфолинил)), необязательно замещенную 1-3 C1-6 алкильными группами (например, метил); и
Кольцо D представляет собой
(1) бензольное кольцо, необязательно дополнительно замещенное 1-3 заместителями, выбранными из
(a) атома галогена (например, атом фтора, атом хлора, атом брома),
(b) гидроксигруппы,
(c) C1-6 алкильной группы (например, метил), необязательно замещенной 1-3 C1-6 алкоксигруппами (например, метокси),
(d) C1-6 алкоксигруппы (например, метокси, этокси, пропокси, изопропокси, гексилокси), необязательно замещенной 1-3 заместителями, выбранными из
(i) карбоксигруппы,
(ii) C1-6 алкоксикарбонильной группы (например, метоксикарбонил),
(iii) C7-16 аралкилоксикарбонильной группы (например, бензилоксикарбонил),
(iv) карбамоильной группы, необязательно моно- или дизамещенной заместителем(ями), выбранным из
(I) C1-6 алкильной группы (например, метил, этил, пропил, изопропил, изобутил), необязательно замещенной 1-3 заместителями, выбранными из
(A) C3-10 циклоалкильной группы (например, циклопропил),
(B) C6-14 арильной группы (например, фенил),
(C) C6-14 ариламиногруппы (например, фениламино), необязательно замещенной 1-3 атомами галогена (например, атом фтора),
(D) 5-14-членной ароматической гетероциклической группы (предпочтительно 5-6-членная моноциклическая ароматическая гетероциклическая группа (например, пиридил)),
(E) 3-14-членной неароматической гетероциклической группы (предпочтительно 3-8-членная моноциклическая неароматическая гетероциклическая группа (например, тетрагидропиранил)), и
(F) карбамоильной группы, необязательно моно- или дизамещенной заместителем(ями), выбранным из C1-6 алкильной группы (например, метил) и C7-16 аралкильной группы (например, 2-фенилэтил),
(II) C2-6 алкенильной группы (например, пент-2-ил), необязательно замещенной 1-3 C6-14 арильными группами (например, фенил),
(III) C3-10 циклоалкильной группы (например, циклопропил), необязательно замещенной 1-3 C1-6 алкильными группами (например, метил),
(IV) C6-14 арильной группы (например, фенил), необязательно замещенной 1-3 заместителями, выбранными из
(A) атома галогена (например, атом фтора, атом хлора), и
(B) C1-6 алкильной группы (например, метил),
(V) C7-16 аралкильной группы (например, бензил),
(VI) 5-14-членнй ароматической гетероциклической группы (предпочтительно 5-6-членная моноциклическая ароматическая гетероциклическая группа (например, пиридил)), и
(VII) 3-14-членной неароматической гетероциклической группы (предпочтительно 3-8-членная моноциклическая неароматическая гетероциклическая группа (например, тетрагидропиранил), 9-14-членная конденсированная полициклическая (предпочтительно би- или трициклическая) неароматическая гетероциклическая группа (например, 1,1-диоксидодигидробензотиенил)), и
(v) 3-14-членной неароматической гетероциклилкарбонильной группы (предпочтительно 3-8-членная моноциклическая неароматическая гетероциклилкарбонильная группа (например, пирролидинилкарбонил, пиперидилкарбонил, морфолинилкарбонил, 1,1-диоксидотиазолидинилкарбонил)), необязательно замещенной 1-3 заместителями, выбранными из
(I) гидроксигруппы, и
(II) C1-6 алкильной группы (например, метил), и
(e) C7-16 аралкилоксигруппы (например, бензилокси),
(2) циклогексановое кольцо,
(3) пиридиновое кольцо,
(4) изоксазольное кольцо,
(5) тиофеновое кольцо,
(6) пиперидиновое кольцо, необязательно дополнительно замещенное 1-3 C1-6 алкоксикарбонильными группами (например, трет-бутоксикарбонил), или
(7) тетрагидропирановое кольцо.
[0074]
[Соединение D]
Соединение (I), где
Кольцо A представляет собой бензольное кольцо;
Кольцо В представляет собой бензольное кольцо;
Кольцо C представляет собой имидазольное кольцо;
L представляет собой связь;
R1 представляет собой 3-8-членную (предпочтительно 5-6-членную) моноциклическую неароматическую гетероциклическую группу (предпочтительно 3-8-членную (предпочтительно 5-6-членную) моноциклическую неароматическую циклическую аминогруппу (например, 1-пиперидил, 4-морфолинил)); и
Кольцо D представляет собой бензольное кольцо, необязательно дополнительно замещенное 1-3 заместителями, выбранными из
(a) атома галогена (например, атом брома), и
(b) C1-6 алкоксигруппы (например, метокси), необязательно замещенной 1-3 заместителями, выбранными из
(i) карбамоильной группы, необязательно моно- или дизамещенной заместителем(ями), выбранным из
(I) C1-6 алкильной группы (например, метил, изобутил), необязательно замещенной 1-3 C3-6 циклоалкильными группами (например, циклопропил), и
(II) 3-8-членной моноциклической неароматической гетероциклической группы (например, тетрагидропиранил), и
(ii) 3-8-членной моноциклической неароматической гетероциклилкарбонильной группы (например, пиперидилкарбонил), необязательно замещенной 1-3 заместителями, выбранными из
(I) гидроксигруппы, и
(II) C1-6 алкильной группы (например, метил).
[0075]
[Соединение E]
Соединение (I), где
Кольцо A представляет собой бензольное кольцо;
Кольцо В представляет собой бензольное кольцо;
Кольцо C представляет собой имидазольное кольцо;
L представляет собой связь;
R1 представляет собой 3-8-членную (предпочтительно 5-6-членную) моноциклическую неароматическую гетероциклическую группу (предпочтительно 3-8-членную (предпочтительно 5-6-членную) моноциклическую неароматическую циклическую аминогруппу (например, 1-пиперидил, 4-морфолинил)); и
Кольцо D представляет собой
(1) бензольное кольцо, необязательно дополнительно замещенное 1-3 заместителями, выбранными из
(a) атома галогена (например, атом брома),
(b) гидроксигруппы, и
(c) C1-6 алкоксигруппы (например, метокси), необязательно замещенной карбамоильной группой(ами), необязательно моно- или дизамещенной 9-14-членной конденсированной полициклической (предпочтительно би- или трициклической) неароматической гетероциклической группой(ами) (например, 1,1-диоксидодигидробензотиенил), или
(2) пиридиновое кольцо.
[0076]
[Соединение F]
Соединение (I), где
Кольцо A представляет собой бензольное кольцо;
Кольцо В представляет собой бензольное кольцо;
Кольцо C представляет собой имидазольное кольцо;
L представляет собой связь;
R1 представляет собой 3-8-членную (предпочтительно 5-6-членную) моноциклическую неароматическую циклическую аминогруппу (например, 1-пиперидил, 4-морфолинил); и
Кольцо D представляет собой бензольное кольцо, дополнительно замещенное одним заместителем, выбранным из
(a) атома галогена (например, атом брома), и
(b) C1-6 алкоксигруппы (например, метокси), замещенной карбамоильной группой(ами), монозамещенной 9-14-членной конденсированной полициклической (предпочтительно би- или трициклической) неароматической гетероциклической группой (например, 1,1-диоксидодигидробензотиенил).
[0077]
[Соединение G]
N-(1,1-диоксидо-2,3-дигидро-1-бензотиофен-5-ил)-2-(4-(5-(1-оксо-5-(пиперидин-1-ил)-1,3-дигидро-2H-изоиндол-2-ил)-1H-бензимидазол-2-ил)фенокси)ацетамид или его соль (Пример 17).
2-(2-(4-бромфенил)-1H-бензимидазол-5-ил)-5-(морфолин-4-ил)изоиндолин-1-он или его соль (Пример 8).
5-(пиперидин-1-ил)-2-(2-(пиридин-3-ил)-1H-бензимидазол-5-ил)изоиндолин-1-он или его соль (Пример 46).
5-(пиперидин-1-ил)-2-(2-(пиридин-4-ил)-1H-бензимидазол-5-ил)изоиндолин-1-он или его соль (Пример 45).
2-(2-(4-гидроксифенил)-1H-бензимидазол-5-ил)-5-(пиперидин-1-ил)изоиндолин-1-он или его соль (Пример 4).
[0078]
Конкретные примеры соединения (I) включают соединения нижеприведенных примеров 1-73.
[0079]
В качестве соли соединения, представленного формулой (I), фармакологически приемлемая соль является предпочтительной, и примеры такой соли включают соль с неорганическим основанием, соль с органическим основанием, соль с неорганической кислотой, соль с органической кислотой, соль с основной или кислотной аминокислотой и тому подобное.
Предпочтительные примеры соли с неорганическим основанием включают соли щелочного металла, такие как натриевая соль, калиевая соль и тому подобное; соли щелочноземельного металла, такие как кальциевая соль, магниевая соль и тому подобное; алюминиевая соль; аммониевая соль и тому подобное.
Предпочтительные примеры соли с органическим основанием включают соли с триметиламином, триэтиламином, пиридином, пиколином, этаноламином, диэтаноламином, триэтаноламином, трометамин[трис(гидроксиметил)метиламин], трет-бутиламином, циклогексиламином, бензиламином, дициклогексиламином, N, N-дибензилэтилендиамином и тому подобное.
Предпочтительные примеры соли с неорганической кислотой включают соли с хлористоводородной кислотой, бромистоводородной кислотой, азотной кислотой, серной кислотой, фосфорной кислотой и тому подобное.
Предпочтительные примеры соли с органической кислотой включают соли с муравьиной кислотой, уксусной кислотой, трифторуксусной кислотой, фталевой кислотой, фумаровой кислотой, щавелевой кислотой, виноградной кислотой, малеиновой кислотой, лимонной кислотой, янтарной кислотой, яблочной кислотой, метансульфоновой кислотой, бензолсульфоновой кислотой, п-толуолсульфоновой кислотой и тому подобное.
Предпочтительные примеры соли с основной аминокислотой включают соли с аргинином, лизином, орнитином и тому подобное.
Предпочтительные примеры соли с кислотной аминокислотой включают соли с аспарагиновой кислотой, глутаминовой кислотой и тому подобное.
[0080]
Способ получения соединения (I) описаны ниже.
[0081]
Используемое исходное соединение и реагент, а также соединение, полученное на каждой стадии в следующем способе получения, могут быть каждое в форме соли, и примеры таких солей включают соли, подобные солям соединения, представленного формулой (I), и тому подобное.
[0082]
Когда соединение, полученное на каждой стадии, находится в свободной форме, его можно преобразовать в целевую соль хорошо известным способом. Когда соединение, полученное на каждой стадии, представляет собой соль, оно может быть преобразовано в целевую свободную форму или другую соль хорошо известным способом.
[0083]
В качестве альтернативы соединение, получаемое на каждой стадии, может быть выделено и очищено из реакционной смеси хорошо известным способом, например, способами разделения, такими как концентрирование, кристаллизация, перекристаллизация, дистилляция, экстракция растворителем, фракционная перегонка, колоночная хроматография и тому подобное.
[0084]
Когда соединения исходных веществ или реагент, используемые на каждой стадии, коммерчески доступны, являются коммерчески доступными, такие коммерчески доступные продукты могут быть использованы напрямую.
[0085]
При осуществлении реакции на каждой стадии, хотя время реакции варьируется в зависимости от типа используемого реагента и растворителя, обычно оно составляет от 1 мин до 48 часов, предпочтительно от 10 минут до 8 часов, если не указано иное.
[0086]
При осуществлении реакции на каждой стадии, хотя температура реакции варьируется в зависимости от типа используемого реагента и растворителя, обычно она составляет от -78°C до 300°C, предпочтительно от -78°C до 150°C, если не указано иное.
[0087]
При осуществлении реакции на каждой стадии, хотя давление варьируется в зависимости от типа используемого реагента и растворителя, оно обычно составляет от 1 атм до 20 атм, предпочтительно от 1 атм до 3 атм, если не указано иное.
[0088]
Микроволновый синтезатор, такой как Initiator производства Biotage и тому подобное, может использоваться при осуществлении реакции на каждой стадии. Хотя температура реакции варьируется в зависимости от типа используемого реагента и растворителя, обычно она составляет от комнатной температуры до 300°C, предпочтительно от 50°C до 250°C, если не указано иное. Хотя время реакции варьируется в зависимости от типа используемого реагента и растворителя, обычно оно составляет от 1 мин до 48 часов, предпочтительно от 1 мин до 8 часов, если не указано иное.
[0089]
При осуществлении реакции на каждой стадии реагент используют в количестве от 0,5 эквивалентов до 20 эквивалентов, предпочтительно от 0,8 эквивалентов до 5 эквивалентов, по отношению к субстрату, если не указано иное. Когда реагент используют в качестве катализатора, реагент используются в количестве от 0,001 эквивалента до 1 эквивалента, предпочтительно от 0,01 эквивалента до 0,2 эквивалента по отношению к субстрату. Когда реагент используют в качестве реакционного растворителя, реагент используют в количестве растворителя.
[0090]
Если не указано иное, реакцию на каждой стадии осуществляют без растворителя или путем растворения или суспендирования соединения исходного материала в соответствующем растворителе. Примеры растворителя включают растворители, описанные в примерах, и следующие растворители.
спирты: метанол, этанол, трет-бутиловый спирт, 2-метоксиэтанол и тому подобное;
простые эфиры: диэтиловый эфир, дифениловый эфир, тетрагидрофуран, 1,2-диметоксиэтан и тому подобное;
ароматические углеводороды: хлорбензол, толуол, ксилол и тому подобное;
насыщенные углеводороды: циклогексан, гексан и тому подобное;
амиды: N, N-диметилформамид, N-метилпирролидон и тому подобное;
галогенированные углеводороды: дихлорметан, терахлорид углерода и тому подобное;
нитрилы: ацетонитрил и тому подобное;
сульфоксиды: диметилсульфоксид и тому подобное;
ароматические органические основания: пиридин и тому подобное;
ангидриды кислот: уксусный ангидрид и тому подобное;
органические кислоты: муравьиная кислота, уксусная кислота, трифторуксусная кислота и тому подобное;
неорганические кислоты: хлористоводородная кислота, серная кислота и тому подобное;
сложные эфиры: этилацетат и тому подобное;
кетоны: ацетон, метилэтилкетон и тому подобное;
вода.
Вышеуказанные растворители могут быть использованы в виде смеси двух или более растворителей в подходящем соотношении.
[0091]
Когда для реакции на каждой стадии используется основание, его примеры включают основания, описанные в примерах, и следующие основания.
неорганические основания: гидроксид натрия, гидроксид магния, карбонат натрия, карбонат кальция, гидрокарбонат натрия и тому подобное;
органические основания: триэтиламин, диэтиламин, пиридин, 4-диметиламинопиридин, N, N-диметиланилин, 1,4-диазабицикло[2.2.2]октан, 1,8-диазабицикло[5.4.0]-7-ундецен, имидазол, пиперидин и тому подобное;
алкоксиды металлов: этоксид натрия, трет-бутоксид калия и тому подобное;
гидриды щелочных металлов: гидрид натрия и тому подобное;
амиды металлов: амид натрия, диизопропиламид лития, гексаметилдисилазид лития и тому подобное;
литийорганические соединения: н-бутиллитий и тому подобное.
[0092]
Когда при осуществлении реакции на каждой стадии используют кислоту или кислотный катализатор, то используют любые из указанных далее кислот или кислотных катализаторов или, например, из кислот или кислотных катализаторов, описанных в примерах.
неорганические кислоты: хлористоводородная кислота, серная кислота, азотная кислота, бромистоводородная кислота, фосфорная кислота и тому подобное;
органические кислоты: уксусная кислота, трифторуксусная кислота, лимонная кислота, п-толуолсульфоновая кислота, 10-камфорсульфокислота и тому подобное;
кислоты Льюиса: комплекс трифторид бора-диэтиловый эфир, йодид цинка, безводный хлорид алюминия, безводный хлорид цинка, безводный хлорид железа и тому подобное.
[0093]
Если не указано иное, реакцию на каждой стадии осуществляют в соответствии с известным способом, например, способом, описанным в Jikken Kagaku Kouza, 5th Edition, vol.13-19 (the Chemical Society of Japan ed.); Shin Jikken Kagaku Kouza, vol.14-15 (the Chemical Society of Japan ed.); Fine Organic Chemistry, Revised 2nd Edition (L.F. Tietze, Th. Eicher, Nankodo); Organic Name Reactions, the Reaction Mechanism and Essence, Revised Edition (Hideo Togo, Kodansha); ORGANIC SYNTHESES Collective Volume I-VII (John Wiley & Sons Inc.); Modern Organic Synthesis in the Laboratory A Collection of Standard Experimental Procedures (Jie Jack Li, OXFORD UNIVERSITY); Comprehensive Heterocyclic Chemistry III, Vol .1 - Vol. 14 (Elsevier Japan); Strategic Applications of Named Reactions in Organic Synthesis (translated by Kiyoshi Tomioka, Kagakudojin); Comprehensive Organic Transformations (VCH Publishers Inc.), 1989, или тому подобное, или способом, описанным в примерах.
[0094]
Реакцию введения или удаления защитной функциональной группы на каждой стадии осуществляют в соответствии с известным способом, например, способом, описанным в “Protective Groups in Organic Synthesis, 4th Ed”, Wiley-Interscience, Inc., 2007 (Theodora W. Greene, Peter G. M. Wuts); “Protecting Groups 3rd Ed.” Thieme, 2004 (P.J. Kocienski), или тому подобное, или способом, описанным в примерах.
Примеры защитной группы для гидроксильной группы спирта и тому подобное или фенольной гидроксильной группы включают защитные группы простого эфира, такие как метоксиметиловый эфир, бензиловый эфир, трет-бутилдиметилсилиловый эфир, тетрагидропираниловый эфир и тому подобное; защитные группы типа сложного эфира карбоксилата, такие как сложный эфир уксусной кислоты и тому подобное; защитные группы типа сложных эфиров сульфоновой кислоты, такие как сложный эфир метансульфоновой кислоты и тому подобное; защитные группы типа сложных эфиров угольной кислоты, такие как трет-бутилкарбонат и тому подобное; и так далее.
Примеры защитных групп для карбонильной группы в альдегиде включают защитные группы типа ацеталя, такие как диметилацеталь и тому подобное; защитные группы типа циклического ацеталя, такие как 1,3-диоксан и тому подобное, и тому подобное.
Примеры защитных групп для карбонильной группы кетона включают защитные группы типа кеталя, такие как диметилкеталь и тому подобное; защитные группы типа циклического кеталя, такие как 1,3-диоксан и тому подобное; защитные группы типа оксима, такие как O-метилоксим и тому подобное; защитные группы типа гидразона, такие как N, N-диметилгидразон и тому подобное, и тому подобное.
Примеры защитных групп для карбоксильной группы включают защитные группы типа сложного эфира, такие как метиловый сложный эфир и тому подобное; защитные группы типа амида, такие как N, N-диметиламид и тому подобное, и тому подобное.
Примеры защитных групп для тиола включают защитные группы типа простого эфира, такие как простой бензилтио эфир и тому подобное; защитные группы типа сложного эфира, такие как сложный эфир тиоуксусной кислоты, тиокарбонат, тиокарбамат и тому подобное, и тому подобное.
Примеры защитных групп для аминогруппы или ароматического гетероцикла, такого как имидазол, пиррол, индол или тому подобное, включают защитные группы карбаматного вида, такие как бензил карбамат и тому подобное; защитные группы амидного вида, такие как ацетамид и тому подобное; защитные группы алкиламинового вида, такие как N-трифенилметиламин и тому подобное; защитные группы сульфонамидного вида, такие как метансульфонамид и тому подобное, и тому подобное.
Защитные группы могут быть удалены известным способом, например, способом с использованием кислоты, основания, ультрафиолетового света, гидразина, фенилгидразина, натрий N-метилдитиокарбамата, фторида тетрабутиламмония, ацетата палладия, триалкилсилил галогенида (например, триметилсилил йодид, триметилсилил бромид), и тому подобное, способом восстановления или тому подобное.
[0095]
В случае осуществления реакции восстановления, на каждой стадии примеры используемого восстанавливающего агента включают гидриды металлов, такие как литийалюминийгидрид, триацетоксиборгидрид натрия, цианоборгидрид натрия, диизобутилалюминийгидрид (DIBAL-H), боргидрид натрия, триацетоксиборгидрид тетраметиламмония и тому подобное; бораны, такие как комплекс боран-тетрагидрофуран и тому подобное; никель Ренея; кобальт Ренея; водород; муравьиная кислота; триэтилсилан и так далее. В способе восстановления углерод-углерод двойной связи или тройной связи может быть использован катализатор, такой как палладий-углерод, катализатор Линдлара или тому подобное.
[0096]
В случае осуществления реакции окисления, на каждой стадии, примеры используемого окислительного агента включают перкислоты, такие как м-хлорпербензойная кислота (mCPBA), пероксид водорода, трет-бутилгидропероксид и тому подобное; перхлораты, такие как тетрабутиламмония перхлорат и тому подобное; хлораты, такие как хлорат натрия и тому подобное; хлориты, такие как хлорит натрия и тому подобное; перйодаты, такие как перйодат натрия и тому подобное; реагенты йода высокой валентности, такие как йодосилбензол и тому подобное; реагенты, содержащие марганец, такие как диоксид марганца, перманганат калия и тому подобное; соединения свинца, такие как тетраацетат свинца и тому подобное; хромсодержащие реагенты, такие как пиридиния хлорхромат (PCC), пиридиния дихромат (PDC), реагенты Джонса и тому подобное; соединения галогенов, такие как N-бромсукцинимид (NBS) и тому подобное; кислород; озон; комплекс триоксид серы-пиридин; тетраоксид осмия; диоксид селена; 2,3-дихлор-5,6-дициано-1,4-бензохинон (DDQ); и тому подобное.
[0097]
В случае осуществления реакции радикальной циклизации, на каждой стадии примеры используемого радикального инициатора включают азо соединения, такие как азобисизобутиронитрил (AIBN) и тому подобное; водорастворимые радикальные инициаторы, такие как 4-4'-азобис-4-цианопентановая кислота (ACPA) и тому подобное; триэтилборон в присутствии воздуха или кислорода; бензоилпероксид; и тому подобное. Примеры используемого радикального реагента включают трибутилстаннан, тристриметилсилилсилан, 1,1,2,2-тетрафенилдисилан, дифенилсилан, йодид самария и тому подобное.
[0098]
В случае осуществления реакции Виттига, на каждой стадии примеры используемого реагента Виттига включают алкилиденфосфораны. Алкилиденфосфораны могут быть получены известным способом, например, взаимодействием соли фосфония с сильным основанием.
[0099]
В случае осуществления реакции Хорнера-Эммонса, на каждой стадии примеры используемых реагентов включают сложные эфиры фосфоноуксусной кислоты, такие как метилдиметилфосфоноацетат, этилдиэтилфосфоноацетат и тому подобное; и основания, такие как гидриды щелочных металлов, литийорганические соединения и тому подобное.
[0100]
В случае осуществления реакции Фриделя-Крафтса, на каждой стадии примеры используемых реагентов включают комбинацию кислоты Льюиса и хлорангидрида кислоты или комбинацию кислоты Льюиса и алкилирующего агента (например, алкил галогенид, спирт, олефин и т.п.). Альтернативно, вместо кислоты Льюиса могут быть использованы органическая кислота или неорганическая кислота, и вместо хлорангидрида кислоты может быть использован ангидрид, такой как уксусный ангидрид или тому подобное.
[0101]
В случае реакции ароматического нуклеофильного замещения, на каждой стадии в качестве реагентов используют нуклеофил (например, амины, имидазол и т.п.) и основание (например, органическое основание и т.п.).
[0102]
В случае осуществления реакции карбанион-опосредованного нуклеофильного присоединения, карбанион-опосредованной нуклеофильной реакции 1,4-присоединения (реакция присоединения по Микаэлю) или карбанион-опосредованного нуклеофильного замещения, на каждой стадии примеры используемого основания для образования карбаниона включают литийорганические соединения, алкоксиды металлов, неорганические основания, органические основания и тому подобное.
[0103]
В случае осуществления реакции Гриньяра, на каждой стадии примеры используемого реактива Гриньяра включают арилмагнийгалогениды, такие как фенилмагнийбромид и тому подобное; и алкил магний галогениды, такие как метилмагнийбромид и тому подобное. Реактив Гриньяра может быть получен известным способом, например, путем взаимодействия алкилгалогенида или арилгалогенида с металлическим магнием в присутствии простого эфира или тетрагидрофурана в качестве растворителя.
[0104]
В случае осуществления реакции конденсации Кневенагеля, на каждой стадии в качестве реагентов используются соединения с активными метиленовыми группами, связывающими две электроноакцепторные группы (например, малоновая кислота, диэтилмалонат, малононитрил и т.п.) и основания (например, органическое основание, алкоксид металла, неорганическое основание).
[0105]
В случае осуществления реакции Вильсмайера-Хаака, на каждой стадии в качестве реагентов используются хлорокись фосфора и производное амида (например, N, N-диметилформамид и т.п.).
[0106]
В случае осуществления реакции азидирования спиртов, алкилгалогенида или сульфоната, на каждой стадии примеры используемого азидирующего агента включают дифенилфосфорилазид (DPPA), триметилсилилазид, азид натрия и тому подобное. Для реакции азидирования спиртов используют, например, способ с использованием дифенилфосфорилазида и 1,8-диазабицикло[5.4.0]ундец-7-ена (DBU), способ с использованием триметилсилилазида и кислоты Льюиса и тому подобное.
[0107]
В случае осуществления реакции восстановительного аминирования, на каждой стадии примеры используемого восстанавливающего агента включают триацетоксиборгидрид натрия, цианоборгидрид натрия, водород, муравьиную кислоту и тому подобное. Когда субстрат представляет собой соединение амина, примеры используемого карбонильного соединения включают параформальдегид, альдегиды, такие как ацетальдегид и тому подобное, и кетоны, такие как циклогексанон и тому подобное. Когда субстрат представляет собой карбонильное соединение, примеры используемых аминов включают аммиак, первичные амины, такие как метиламин и тому подобное; вторичные амины, такие как диметиламин и тому подобное; и тому подобное.
[0108]
В случае осуществления реакции Мицунобу, на каждой стадии в качестве реагентов используются азодикарбоксилат (например, диэтилазодикарбоксилат (DEAD), диизопропил азодикарбоксилат (DIAD) и т.п.) и фосфин (например, трифенилфосфин, трибутлфосфин).
[0109]
В случае осуществления реакции этерификации, реакции амидирования или реакции образования мочевины, на каждой стадии примеры используемых реагентов включают ацилгалогениды, такие как хлорангидрид кислоты, бромиды кислот и тому подобное; активированные карбоновые кислоты, такие как ангидриды кислот, активированные сложные эфиры, сульфаты и тому подобное. Примеры активирующего агента карбоновых кислот включают карбодиимидные конденсирующие агенты, такие как гидрохлорид 1-этил-3-(3-диметиламинопропил)карбодиимида (WSCD) и тому подобное; триазиновые конденсирующие агенты, такие как 4-(4,6-диметокси-1,3,5-триазин-2-ил)-4-метилморфолиния хлорид n-гидрат (DMT-MM) и тому подобное; конденсирующие агенты на основе карбоната, такие как 1,1-карбонилдиимидазол (CDI) и тому подобное; дифенилфосфорилазид (DPPA); соль бензотриазол-1-илокси-трисдиметиламинофосфония (реагент BOP); 2-хлор-1-метил-пиридиния йодид (реагент Мукаяма); тионилхлорид; низшие алкилгалогенформиаты, такие как этилхлорформиат и тому подобное; O-(7-азабензотриазол-1-ил)-N, N,N',N'-тетраметилурония гексафторфосфат (HATU); серная кислота; их сочетания; и так далее. В случае использования карбодиимидного конденсирующего агента в реакционную смесь могут быть, кроме того, добавлены добавки, такие как 1-гидроксибензотриазол (HOBt), N-гидроксисукцинимид (HOSu), диметиламинопиридин (DMAP) или тому подобное.
[0110]
В случае осуществления реакции конденсации, на каждой стадии примеры используемого металлического катализатора включают соединения палладия, такие как ацетат палладия(II), тетракис(трифенилфосфин)палладий(0), дихлорбис(трифенилфосфин)палладий(II), дихлорбис(триэтилфосфин)палладий(II), трис(дибензилиденацетон)дипалладий(0), хлорид 1,1'-бис(дифенилфосфино)ферроцен палладия(II) и тому подобное; соединения никеля, такие как тетракис(трифенилфосфина)никель(0) и тому подобное; соединения родия, такие как трис(трифенилфосфин)родий(III) хлорид и тому подобное; соединения кобальта; соединения меди, такие как оксид меди, йодид меди(I) и тому подобное; соединения платины и тому подобное. В реакционную смесь может, кроме того, быть добавлено основание и примеры такого основания включают неорганические основания и тому подобное.
[0111]
В случае осуществления реакции тиокарбонилирования, на каждой стадии в качестве агента тиокарбонилирования обычно используется пентасульфид дифосфора. Помимо пентасульфида дифосфора может быть использован реагент, имеющий структуру 1,3,2,4-дитиадифосфетан-2,4-дисульфида, такой как 2,4-бис(4-метоксифенил-1,3,2,4-дитиадифосфетан-2,4-дисульфид (реагент Лавессона) или тому подобное.
[0112]
В случае осуществления реакции Воля-Циглера, на каждой стадии примеры используемого галогенирующего агента включают N-йодсукцинимид, N-бромсукцинимид (NBS), N-хлорсукцинимид (NCS), бром, сульфурилхлорид и тому подобное. На реакционную смесь, чтобы тем самым ускорить реакцию, может быть добавлено воздействие радикального инициатора, такого как нагревание, свет, пероксид бензоила, азобисизобутиронитрил или тому подобное.
[0113]
В случае осуществления реакции галогенирования гидроксигруппы, на каждой стадии примеры используемого галогенирующего агента для хлорирования включают галогенводородную кислоту и галогенангидриды неорганических кислот, в частности, хлористоводородную кислоту, тионил хлорид, оксихлорид фосфора или тому подобное, и для бромирования 48%-ную бромистоводородную кислоту или тому подобное. Также может быть использован способ получения алкилгалогенида реакцией спирта с трифенилфосфином и терахлоридом углерода или тетрабромидом углерода и т.п. В качестве альтернативы также может быть использован способ получения алкилгалогенида посредством двух стадий, включающих преобразование спирта в соответствующий сульфонат и затем взаимодействие сульфоната с бромидом лития, хлоридом лития или иодидом натрия.
[0114]
В случае осуществления реакции Арбузова, на каждой стадии примеры используемых реагентов включают алкилгалогениды, такие как этилбромацетат и тому подобное; и фосфиты, такие как триэтилфосфит, три(изопропил)фосфит и тому подобное.
[0115]
В случае осуществления реакции сульфоновой этерификации, на каждой стадии примеры используемого сульфонирующего агента включают метансульфонилхлорид, п-толуолсульфонилхлорид, ангидрид метансульфоновой кислоты, ангидрид п-толуолсульфоновой кислоты и тому подобное.
[0116]
В случае осуществления реакции гидролиза, на каждой стадии в качестве реагента используются кислота или основание. В реакционную смесь при осуществлении кислотного гидролиза трет-бутилового сложного эфира для восстановительного улавливания побочных продуктов трет-бутилового катиона могут быть добавлены муравьиная кислота, триэтилсилан или тому подобное.
[0117]
В случае осуществления реакции дегидратации, на каждой стадии примеры используемого дегидратирующего агента включают серную кислоту, дифосфор пентаоксид, оксихлорид фосфора, N, N'-дициклогексилкарбодиимид, оксид алюминия, полифосфорную кислоту и тому подобное.
[0118]
Соединение (I) можно получить из соединения (II) способом, указанным далее.
[0119]
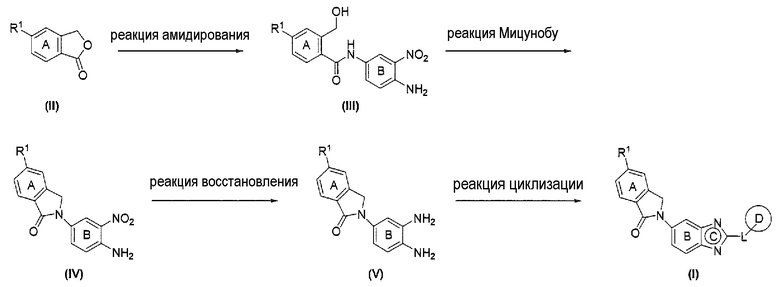
[0120]
где каждый символ определен выше.
[0121]
Соединение (II) может быть получено известным способом или аналогичным ему способом.
[0122]
Соединение (III) может быть получено реакцией амидирования соединения (II).
[0123]
Соединение (IV) может быть получено реакцией Мицунобу соединения (III).
[0124]
Соединение (V) может быть получено реакцией восстановления соединения (IV).
[0125]
Соединение (I) может быть получено реакцией циклизации соединения (V). Примеры реагента включают альдегид, хлорангидрид и т.п., которые соответствуют -L-кольцу D. Натрия гидросульфит, триэтиламин и тому подобное могут быть добавлены в реакционную систему.
[0126]
В полученном таким образом соединении (I) внутримолекулярная функциональная группа также может быть преобразована в целевую функциональную группу посредством комбинации химических реакций, хорошо известных. Примеры химической реакции включают реакцию окисления, реакцию восстановления, реакцию алкилирования, реакцию ацилирования, реакцию образования мочевины, реакцию гидролиза, реакцию аминирования, реакцию этерификации, реакцию сочетания арила, реакцию снятия защиты и тому подобное.
[0127]
В вышеупомянутом способе получения, когда исходное соединение имеет аминогруппу, карбоксильную группу, гидроксигруппу, карбонильную группу или меркаптогруппу в качестве заместителя, в них может быть введена защитная группа, обычно используемая в химии пептидов, и целевое соединение может быть получено путем удаления защитной группы, если необходимо, после реакции.
[0128]
Соединение (I), полученное вышеупомянутым способом получения, может быть выделено и очищено известными способами, такими как экстракция растворителем, преобразование жидкости, фазовый перенос, кристаллизация, перекристаллизация, хроматография и тому подобное.
Когда соединение (I) содержит оптический изомер, стереоизомер, регио-изомер и ротамер, эти соединения также включены в соединение (I), и каждое из них может быть получено в виде отдельного продукта с помощью способа синтеза или способа разделения, хорошо известного. Например, когда оптический изомер существует в соединении (I), оптический изомер, выделенный из соединения, также включается в соединение (I).
В настоящем документе оптический изомер может быть получен известным способом.
Соединение (I) может быть кристаллом.
Кристалл соединения (I) (в дальнейшем иногда сокращенно обозначаемый как кристалл настоящего изобретения) может быть получен путем кристаллизации соединения (I), применяя способ кристаллизации, хорошо известный.
[0129]
В настоящем описании, температура плавления означает температуры плавления, измеренную, например, с помощью микро прибора для измерения температуры плавления (Yanako, MP-500D или Buchi, B-545), прибора DSC (дифференциальная сканирующая калориметрия) (SEIKO, EXSTAR6000) и тому подобное.
Как правило, температура плавления иногда меняется в зависимости от измерительного устройства, условий измерения и т.п. Кристалл в настоящем описании может быть кристаллом, температура плавления которого отличается от значений, описанных в настоящем описании, при условии, что разница находится в пределах общего диапазона ошибок.
[0130]
Вышеуказанное соединение может быть гидратом, негидратом, сольватом или несольватом.
Кроме того, вышеуказанное соединение может быть мечено изотопом или замещено изотопом (например, 2H, 3H, 11C, 14C, 18F, 35S, 125I и т.п.) и тому подобное.
Вышеупомянутое соединение также охватывает преобразованную дейтерированную форму, где 1H преобразован в 2H(D).
Вышеупомянутое соединение также охватывает таутомеры.
Вышеупомянутое соединение может быть фармацевтически приемлемым сокристаллом или сокристаллической солью. Сокристалл или сокристаллическая соль означает кристаллическое вещество, состоящее из двух или более отдельных веществ, которые являются твердыми при комнатной температуре, каждый из которых имеет различные физические свойства (например, структура, температура плавления, теплота плавления, гигроскопичность, растворимость, стабильность и т.д.). Сокристалл и сокристаллическая соль могут быть получены известным способом сокристаллизации.
[0131]
Промотор созревания кардиомиоцитов по настоящему изобретению можно использовать как таковой или путем смешивания с фармакологически приемлемым носителем и составления смеси в соответствии с хорошо известным способом.
[0132]
Поскольку соединение (I) обладает превосходной активностью, способствующей созреванию кардиомиоцитов, его можно использовать в качестве промотора созревания кардиомиоцитов. Следовательно, при культивировании незрелых кардиомиоцитов в присутствии соединения (I) или его соли зрелые кардиомиоциты могут быть получены за более короткий период, чем при культивировании только в компонентах среды.
[0133]
Используемый в настоящем описании термин «плюрипотентность» означает способность дифференцироваться в различные ткани или клетки, имеющие разную морфологию и/или функции, и дифференцироваться в любую серию клеток из трех зародышевых листков. «Плюрипотентность» не может дифференцироваться в бластодиск. Таким образом, «плюрипотентность» отличается от термина «тотипотентность», который может дифференцироваться в каждую ткань живого организма, включая бластодиск, тем, что он не имеет способности к формированию целого организма.
[0134]
Используемый в настоящем документе термин «мультипотентность» означает способность дифференцироваться в несколько ограниченных количеств серий клеток. Например, мезенхимальные стволовые клетки, гемопоэтические стволовые клетки и нейральные стволовые клетки являются мультипотентными, но не плюрипотентными.
[0135]
Как используется в настоящем документе, примеры «стволовых клеток» включают плюрипотентные стволовые клетки.
[0136]
"Кардиомиоциты", к которым применяют соединение (I), конкретно не ограничены, и они предпочтительно получены от млекопитающего (например, мыши, крысы, хомяка, кролика, кошки, собаки, коровы, овцы, свиньи, обезьяны, человека), более предпочтительно получены от человека.
[0137]
Кардиомиоциты, созревание которых может быть стимулировано соединением (I), особо не ограничены, если только можно определить, что они находятся в незрелой стадии на основе указанных ниже уровней экспрессии маркеров, морфологий и структур (например, саркомера, митохондрий), свойств (например, пульсативность, электрофизиологическое созревание) и т.п.
Кардиомиоциты, созреванию которых может способствовать соединение (I), также могут быть клетками, полученными с помощью индукции дифференциации из плюрипотентных стволовых клеток, или незрелыми кардиомиоцитами, выделенными из живого организма (например, кардиомиоцитами, полученными из плода мыши или крысы или новорожденного).
[0138]
Примеры плюрипотентных стволовых клеток включают, но не ограничиваются ими, эмбриональные стволовые (ES) клетки, стволовые клетки зародышевой линии («GS-клетки»), эмбриональные половые клетки («EG-клетки»), индуцированные плюрипотентные стволовые (iPS) клетки, эмбриональные стволовые клетки, полученные из клонированного эмбриона, полученного путем перенесения ядра (клетки ntES), и т.п. Плюрипотентные стволовые клетки предпочтительно представляют собой ES-клетки, iPS-клетки или ntES-клетки.
[0139]
(A) Эмбриональные стволовые клетки
ES-клетки представляют собой стволовые клетки, созданные из внутренней клеточной массы раннего эмбриона (например, бластоцисты) млекопитающего, такого как человек, мышь и т.п., которые обладают плюрипотентностью и способностью к росту за счет самообновления.
ES-клетки представляют собой стволовые клетки, полученные из эмбриона, происходящие из внутренней клеточной массы бластоцисты, которая представляет собой эмбрион, образовавшийся после стадии 8 клеток и стадии морулы оплодотворенной яйцеклетки. ES-клетки обладают способностью дифференцироваться в любые клетки, составляющие взрослого человека, то есть так называемую плюрипотентность дифференцировки и способность к росту за счет самообновления. ES-клетки были обнаружены у мышей в 1981 г. (M. J. Evans and M. H. Kaufman (1981), Nature 292: 154-156), и после чего были созданы линии ES-клеток приматов, таких как человек, обезьяна и тому подобное (J. A. Thomson et al. (1998), Science 282: 1145-1147; J. A. Thomson et al. (1995), Proc. Natl. Acad. Sci. USA, 92: 7844-7848; J. A. Thomson et al. (1996), Biol. Reprod., 55: 254-259; J. A. Thomson and V. S. Marshall (1998), Curr. Top. Dev. Biol., 38: 133-165).
ES-клетки могут быть созданы путем удаления внутренней клеточной массы из бластоцисты оплодотворенной яйцеклетки субъекта-животного с последующим культивированием внутренней клеточной массы на питающих фибробластах. Клетки можно поддерживать путем субкультивирования с использованием культуральной среды, дополненной веществом (веществами), таким как лейкоз-ингибирующий фактор (LIF), основной фактор роста фибробластов (bFGF) и тому подобное. Способы создания и поддержания ES-клеток человека и обезьяны описаны, например, в US 5843780 B; Thomson JA, et al. (1995), Proc Natl. Acad. Sci. USA. 92: 7844-7848; Thomson JA, et al. (1998), Science. 282: 1145-1147; H. Suemori et al. (2006), Biochem. Biophys. Res. Commun., 345: 926-932; M. Ueno et al. (2006), Proc. Natl. Acad. Sci. USA, 103: 9554-9559; H. Suemori et al. (2001), Dev. Dyn., 222: 273-279; H. Kawasaki et al. (2002), Proc. Natl. Acad. Sci. USA, 99: 1580-1585; и Klimanskaya I, et al. (2006), Nature. 444: 481-485.
Что касается культуральной среды для получения ES-клеток, человеческие ES-клетки можно поддерживать, например, с использованием культуральной среды DMEM/F-12, дополненной 0,1 мМ 2-меркаптоэтанола, 0,1 мМ заменимых аминокислот, 2 мМ L-глутаминовой кислоты, 20% KSR и 4 нг/мл bFGF при 37°C во влажной атмосфере 2% CO2/98% воздуха (O. Fumitaka et al. (2008), Nat. Biotechnol., 26:215-224). ES-клетки необходимо субкультивировать каждые 3-4 дня, и субкультивирование можно проводить с использованием, например, 0,25% трипсина и 0,1 мг/мл коллагеназы IV в PBS, содержащем 1 мМ CaCl2 и 20% KSR.
Отбор ES-клеток обычно можно проводить методом ПЦР в реальном времени с использованием в качестве индекса экспрессию маркерного гена, такого как щелочная фосфатаза, Oct-3/4, Nanog и т.п. В частности, для отбора человеческих ES-клеток экспрессия маркерного гена, такого как OCT-3/4, NANOG, ECAD и т.п., может быть использована в качестве индекса (E. Kroon et al. (2008), Nat. Biotechnol., 26: 443-452).
Что касается ES-клеток, таких как ES-клетки мыши, доступны различные линии ES-клеток мыши, созданные inGenious targeting laboratory, Riken (Institute of Physical and Chemical Research) и т.п., и в качестве ES-клеток человека доступны различные линии ES-клеток человека, созданные NIH, Riken, Kyoto University, Cellartis и т.п. Например, примеры линий ES-клеток человека включают линию CHB-1 - CHB-12, линию RUES1, линию RUES2, линию HUES1 - HUES28 и т.п., от NIH, линию H1 и линию H9 от WisCell Research, и линию KhES-1, линию KhES-2, линию KhES-3, линию KhES-4, линию KhES-5, линию SSES1, линию SSES2, линию SSES3 и т.п., от Riken. В качестве альтернативы могут использоваться клеточные линии клинического применения, исследовательские или клинические клеточные линии, полученные из этих клеточных линий и т.п.
[0140]
(B) Стволовые клетки зародышевой линии
Стволовые клетки зародышевой линии представляют собой плюрипотентные стволовые клетки, полученные из семенников, и играют роль источника сперматогенеза. Подобно ES-клеткам, эти клетки могут быть индуцированы к дифференцировке в различные серии клеток, и, например, они обладают свойством обеспечивать получение химерной мыши путем трансплантации клеток в бластоцисту мыши (M. Kanatsu-Shinohara et al. (2003) Biol. Reprod., 69: 612-616 ; K. Shinohara et al. (2004), Cell, 119: 1001-1012). Стволовые клетки зародышевой линии способны к самообновлению в культуральной среде, содержащей нейротрофический фактор глиальной клеточной линии (GDNF), и, повторяя их субкультивирование в тех же условиях культивирования, что и для ES-клеток, можно получить стволовые клетки зародышевой линии (Masanori Takehashi et al. (2008), Experimental Medicine, 26(5) (extra edition): 41-46, Yodosha (Tokyo, Japan)).
[0141]
(C) Эмбриональные половые клетки
Эмбриональные половые клетки образуются из эмбриональных примордиальных клеток и обладают плюрипотентностью, как и ES-клетки. Они могут быть созданы путем культивирования примордиальных клеток в присутствии таких веществ, как LIF, bFGF, фактора роста стволовых клеток и т.п. (Y. Matsui et al. (1992), Cell, 70: 841-847; J. L. Resnick et al. (1992), Nature, 359: 550-551).
[0142]
(D) Индуцированные плюрипотентные стволовые клетки
“Индуцированные плюрипотентные стволовые (iPS) клетки (iPSC)” относятся к клетке, полученной путем введения определенного фактора (фактор ядерного репрограммирования) в соматическую клетку млекопитающего или недифференцированную стволовую клетку для осуществления репрограммирования. В настоящее время существуют различные «индуцированные плюрипотентные стволовые клетки», и те, которые также могут быть использованы, являются следующими: iPSC, созданные Yamanaka, et al., путем введения четырех факторов, Oct3/4, Sox2, Klf4 и c-Myc в фибробласт мыши (Takahashi K, Yamanaka S., Cell, (2006) 126: 663-676); а также iPSC, полученные из клетки человека, созданной путем введения тех же четырех факторов в фибробласт человека (Takahashi K, Yamanaka S., et al. Cell, (2007) 131: 861-872.); клетка Nanog-iPS, созданная путем введения четырех факторов, описанных выше, и последующего проведения скрининга с экспрессией Nanog в качестве индекса (Okita, K., Ichisaka, T., and Yamanaka, S. (2007). Nature 448, 313-317.); iPS-клетка, полученная способом, в котором c-Myc не включен (Nakagawa M, Yamanaka S., et al. Nature Biotechnology, (2008) 26, 101-106); и iPS-клетка, созданная введением шести факторов свободным от вируса методом (Okita K et al. Nat. Methods 2011 May;8(5):409-12 , Okita K et al. Stem Cells. 31(3):458-66). Кроме того, индуцированная плюрипотентная стволовая клетка, полученная Thomson, et al., которая создана путем введения четырех факторов, OCT3/4, SOX2, NANOG and LIN28 (Yu J., Thomson JA. et al., Science (2007) 318: 1917-1920.), индуцированная плюрипотентная стволовая клетка, полученная Daley, et al. (Park IH, Daley GQ. et al., Nature (2007) 451: 141-146), и индуцированные плюрипотентные стволовые клетки, полученные Sakurada, et al. (выложенная заявка на патент Японии No. 2008-307007), также могут быть использованы.
Кроме того, любые индуцированные плюрипотентные стволовые клетки, известные в данной области, описаны во всех опубликованных статьях (например, Shi Y., Ding S., et al., Cell Stem Cell, (2008) Vol 3, Issue 5, 568-574; Kim JB., Scholer HR., et al., Nature, (2008) 454, 646-650; Huangfu D., Melton, DA., et al., Nature Biotechnology, (2008) 26, No 7, 795-797), или патентах (например, выложенная заявка на патент Японии No. 2008-307007, выложенная заявка на патент Японии No. 2008-283972, US 2008-2336610, US 2009-047263, WO 2007-069666, WO 2008-118220, WO 2008-124133, WO 2008-151058, WO 2009-006930, WO 2009-006997, WO 2009-007852) также могут быть использованы.
В качестве линий индуцированных плюрипотентных клеток доступны различные линии iPSC, созданные NIH, Riken, Kyoto University, и др. Например, примеры линий iPSC человека включают линию HiPS-RIKEN-1A, линию HiPS-RIKEN-2A, линию HiPS-RIKEN-12A и линию Nips-B2 от Riken, линию 253G1, линию 201B7, линию 409B2, линию 454E2, линию 606A1, линию 610B1 и линию 648A1 от Kyoto University, и подобное. В качестве альтернативы могут использоваться клеточные линии клинического уровня, предоставленные Kyoto University, Cellular Dynamics International etc., исследовательские или клинические клеточные линии, полученные из этих клеточных линий, и т.п.
[0143]
Термин «соматические клетки», используемый в настоящем документе, означает любые клетки животных (предпочтительно клетки млекопитающих, включая человека), за исключением клеток зародышевой линии и тотипотентных клеток, таких как яйца, ооциты, клетки ES и т.п. Примеры соматических клеток включают, но не ограничиваются этим, любые эмбриональные соматические клетки, неонатальные соматические клетки и зрелые, здоровые или больные соматические клетки, а также любые из первично культивируемых клеток, субкультивированных клеток и устойчивых клеточных линий. Конкретные примеры соматических клеток включают (1) тканевые стволовые клетки (соматические стволовые клетки), такие как нейральные стволовые клетки, гемопоэтические стволовые клетки, мезенхимальные стволовые клетки, стволовые клетки пульпы зуба и тому подобное; (2) тканевые клетки-предшественники; (3) дифференцированные клетки, такие как лимфоциты, эпителиальные клетки, эндотелиальные клетки, мышечные клетки, фибробласты (клетки кожи и т.п.), волосковые клетки, клетки печени, клетки слизистой оболочки желудка, энтероциты, клетки селезенки, клетки поджелудочной железы (экзокринные клетки поджелудочной железы и т.д.), клетки головного мозга, клетки легкого, клетки почек, адипоциты и тому подобное, и тому подобное.
В настоящем изобретении млекопитающее-индивидуум, от которого собирают соматические клетки, не ограничивается, и предпочтительно человек. В случаях, когда полученные клетки iPS должны использоваться для регенеративной медицины человека, особенно предпочтительно собирать соматические клетки у самого пациента или другого человека, имеющего тот же самый или по существу тот же самый тип человеческого лейкоцитарного антигена (HLA), с точки зрения предотвращения реакции отторжения. В настоящем документе «по существу тот же самый» тип HLA означает, что тип HLA соответствует в той степени, которая позволяет выживать трансплантированным клеткам за счет использования иммунодепрессанта(ов) и/или того подобного, когда клетки, полученные путем индукции дифференцировки из iPS-клеток, полученных из соматических клеток, трансплантируют пациенту. Например, это означает, что человек имеет те же самые основные HLA (например, в трех локусах гена HLA-A, HLA-B и HLA-DR), что и пациент (то же самое применяется и далее). С другой стороны, в случаях, когда клетки не вводят (трансплантируют) человеку, например, в способе тестирования токсичности лекарственного препарата-кандидата для кардиомиоцитов, происхождение соматических клеток, которые будут использоваться в качестве источника клеток iPS, не ограничено. В случаях, когда iPS-клетки используют в качестве источника клеток для скрининга для оценки чувствительности к лекарственному средству или побочных эффектов пациента, предпочтительно собирать соматические клетки от самого пациента или другого человека, имеющего такой же генетический полиморфизм(ы), связанный с чувствительностью к лекарственному средству или побочными эффектами.
[0144]
(E) Клетки ES, полученные из клонированного эмбриона, полученного путем ядерной передачи
Клетки ntES представляют собой ES-клетки, полученные из клонированного эмбриона, полученного методом ядерной передачи, и имеют почти те же свойства, что и ES-клетки, полученные из оплодотворенных яйцеклеток (T. Wakayama et al. (2001), Science, 292: 740-743 ; S. Wakayama et al. (2005), Biol. Reprod., 72: 932-936 ; J. Byrne et al. (2007), Nature, 450: 497-502). То есть клетка ntES (ядерная передача ES) представляет собой ES-клетку, полученную из внутренней клеточной массы бластоцисты, полученной из клонированного эмбриона, полученного путем замены ядра неоплодотворенной яйцеклетки ядром соматической клетки. Для получения клеток ntES используют комбинацию метода ядерной передачи (J.B. Cibelli et al. (1998), Nature Biotechnol., 16: 642-646) и метода получения клетки ES (описанного выше) (Sayaka Wakayama et al. (2008), Experimental Medicine 26(5) (extra edition), pp. 47-52). При ядерной передачи перепрограммирование может быть достигнуто путем инъекции ядра соматической клетки в безъядерную неоплодотворенную яйцеклетку млекопитающего и культивирования полученного в течение нескольких часов.
[0145]
Используемый в настоящем документе термин «кардиомиоцит» означает клетку, экспрессирующую по меньшей мере один маркерный ген, выбранный из группы, состоящей из сердечного тропонина (cTNT), αMHC (тяжелая цепь α миозина, MYH6) и βMHC (MYH7). Примеры cTNT включают NCBI accession number NM_000364 в случае человека и NM_001130176 в случае мыши. Примеры αMHC включают NCBI accession number NM_002471 в случае человека, и NM_001164171 в случае мыши. Примеры βMHC включают NCBI accession number NM_000257 в случае человека, и NM_080728 в случае мыши.
Известно, что происходит переключение изоформы, при котором экспрессия тропонина I1 (TNNI1) снижается, а экспрессия тропонина I3 (TNNI3) увеличивается по мере созревания кардиомиоцитов (Fikru B. Bedada, (2014) 3(4): 594-605.). Используемый в настоящем документе термин «кардиомиоциты созрели (зрелые)» означает, что по меньшей мере экспрессия TNNI3 увеличена.
[0146]
Что касается методов индукции дифференцировки плюрипотентных стволовых клеток в незрелые кардиомиоциты, кардиомиоциты можно получить из плюрипотентных стволовых клеток, например, способом, описанным Laflamme MA et al. (Laflamme MA & Murry CE, Nature 2011, Review).
Другие примеры способа включают, но не ограничиваются ими, способ, в котором кардиомиоциты получают путем образования клеточной массы (эмбриоидные тельца) суспензионной культурой индуцированных плюрипотентных стволовых клеток, способ, в котором кардиомиоциты получают в присутствии вещества, которое подавляет передачу сигналов костного морфогенетического белка (BMP) (WO 2005/033298), способ, в котором кардиомиоциты получают путем добавления активина A и BMP в этом порядке (WO 2007/002136), способ, в котором кардиомиоциты получают в присутствие вещества, которое способствует активации канонического пути передачи сигнала Wnt (WO 2007/126077), способ, в котором Flk/KDR-положительные клетки выделяют из индуцированных плюрипотентных стволовых клеток с последующим получением кардиомиоцитов в присутствии циклоспорина A (WO 2009/118928) и тому подобное.
Кроме того, также предлагаются способ индукции дифференцировки кардиомиоцитов с использованием цитокинов путем образования эмбриоидных телец (Yang L, et al., Human cardiovascular progenitor cells develop from a KDR+ embryonic-stem-cell-derived population., Nature., 2008 May 22;453(7194):524-8), способ индукции дифференцировки кардиомиоцитов с помощью адгезивной культуры в условиях отсутствия цитокинов (Lian X, et al., Robust cardiomyocyte differentiation from human pluripotent stem cells via temporal modulation of canonical Wnt signaling., Proc Natl Acad Sci USA. 2012 July 3;109(27):E1848-57), метод индукции дифференцировки кардиомиоцитов путем комбинированного использования адгезивной культуры и суспензионной культуры в условиях отсутствия цитокинов (Minami I, et al., A small molecule that promotes cardiac differentiation of human pluripotent stem cells under defined, cytokine- and xeno-free conditions., Cell Rep., 2012 Nov 29;2(5):1448-60) и тому подобное.
[0147]
Среда для получения незрелых кардиомиоцитов из плюрипотентных стволовых клеток особо не ограничивается, и можно использовать среды, хорошо известные. Их примеры включают среду IMDM, среду Medium 199, среду минимальная эссенциальная среда Игла (EMEM), среду αMEM, среду среда Игла в модификации Дульбекко (DMEM), среду F12 Хэма, среду RPMI 1640, среду Фишера, нейробазальную среду (Life Technologies), StemPro34 (Invitrogen), среду после удаления раствора C из StemFit AK02 (AJINOMOTO AK02, 400 мл раствора A и 100 мл раствора B, всего 500 мл), среду Essential 6 (Thermo Fischer Scientific) и и их смешанные среды, и тому подобное.
В эти среды могут быть добавлены хорошо известные добавки, в зависимости от клеток и условий культивирования. Например, среда может содержать сыворотку или может быть бессывороточной. При необходимости среда может содержать один или несколько заменителей сыворотки, таких как альбумин, трансферрин, заменитель сыворотки Knockout (KSR) (заменитель сыворотки для FBS во время культивирования ES-клеток), добавка N2 (Invitrogen), добавка B27 (Invitrogen), жирные кислоты, инсулин, предшественники коллагена, микроэлементы, 2-меркаптоэтанол, 1-тиолглицерин и т.п., а также могут содержать одно или несколько веществ, таких как липиды, аминокислоты, L-глутамин, глутамакс (Invitrogen), заменимые аминокислоты, витамины, факторы роста, низкомолекулярные соединения, антибиотики, антиоксиданты, пировиноградная кислота, буферы, неорганические соли и тому подобное. Среди них предпочтительной средой является StemPro34 или среда после удаления раствора C из StemFit AK02, каждая из которых содержит трансферрин, 1-тиолглицерин, L-глутамин и аскорбиновую кислоту, или RPMI1640, содержащую добавку B27.
[0148]
Комбинация активина A, BMP4 и bFGF или CHIR99021 используется в качестве начальной добавки для индукции дифференцировки кардиомиоцитов с использованием вышеупомянутой среды.
В случае комбинации активина A, BMP4 и bFGF используемые концентрации этих добавок предпочтительно составляют от 1 нг/мл до 100 нг/мл для активина A, 1 нг/мл до 100 нг/мл для BMP4, и 1 нг/мл до 100 нг/мл для bFGF, более предпочтительно 6 нг/мл для активина A, 10 нг/мл для BMP4, и 5 нг/мл для bFGF.
В случае CHIR99021 используемая концентрация предпочтительно составляет от 100 нМ до 100 мкМ, более предпочтительно 4-6 мкМ.
[0149]
После добавления вышеупомянутой добавки, путем добавления в среду фактора роста эндотелия сосудов (VEGF) и ингибитора Wnt, плюрипотентные стволовые клетки могут быть дифференцированы в кардиомиоциты.
Концентрация используемого VEGF предпочтительно составляет от 1 до 100 нг/мл, более предпочтительно 10 нг/мл.
Примеры ингибитора Wnt включают белок DKK1 (например, NCBI accession number:NM_012242 в случае человека), склеростин (например, NCBI accession number:NM_025237 в случае человека), IWR-1 (Merck Millipore), IWP-2 (Sigma-Aldrich), IWP-3 (Sigma-Aldrich), IWP-4 (Sigma-Aldrich), PNU-74654 (Sigma-Aldrich), XAV939 (Sigma-Aldrich) и их производные, и т.п. Среди них предпочтительно использовать IWP-3, IWP-4 и IWR-1.
Концентрация используемого ингибитора Wnt особо не ограничивается, пока он ингибирует Wnt, и предпочтительно составляет от 1 нМ до 50 мкМ, особенно предпочтительно от 1 до 2 мкМ.
[0150]
Период культивирования для получения незрелых кардиомиоцитов из плюрипотентных стволовых клеток составляет, например, от 5 до 365 дней, предпочтительно от 5 до 100 дней, более предпочтительно от 5 до 60 дней, еще более предпочтительно от 5 до 40 дней, еще наиболее предпочтительно от 5 до 30 дней.
[0151]
Количество соединения, которое должно использоваться в качестве промотора созревания кардиомиоцитов по настоящему изобретению, особо не ограничено, и оно составляет, например, от 0,01 до 100 мкМ, предпочтительно от 0,1 до 30 мкМ, более предпочтительно от 1 до 10 мкМ, на 1×104-1×107 клеток незрелых кардиомиоцитов.
[0152]
Промотор созревания кардиомиоцитов по настоящему изобретению может содержать конкретное соединение, описанное в настоящем документе, отдельно или в комбинации одного или более. В качестве альтернативы промотор созревания кардиомиоцитов по настоящему изобретению может содержать комбинацию одного или нескольких конкретных соединений, описанных в настоящем документе, и одного или нескольких соединений, обладающих активностью, способствующей созреванию кардиомиоцитов, отличной от описанных в настоящем документе (например, соединения, которые, как можно подтвердить, обладают активностью, способствующей созреванию кардиомиоцитов в соответствии со способами, описанными в экспериментальных примерах в настоящем документе, например, 2-метокси-5-((Z)-2-(3,4,5-триметоксифенил)винил)фенол, (1-этил-1H-бензотриазол-5-ил)метил (2-(2-метокси-4-метилфенил)-4-метил-1,3-тиазол-5-ил)карбамат, (2'бета)-22-оксовинкалейкобластин, 2-(2-(4-хлорфенил)этил)-6-(2-фурил)-3H-имидазо[4,5-b]пиридин, 4,5-ангидро-1,2-дидезокси-4-метил-2-((N-(морфолин-4-илацетил)-L-аланил-O-метил-L-тирозил)амино)-1-фенил-L-трео-пент-3-улоза, 3-(3-метоксифенил)-N7,N7-диметилизохинолин-1,7-диамин, метил 4-(2-бензилбензоил)-2,5-диметил-1H-пиррол-3-карбоксилат, 2'-(4-аминофенил)-1H,1'H-2,5'-бибензимидазол-5-амин и их соли).
[0153]
В качестве показателя зрелости кардиомиоцитов можно использовать уровень экспрессии маркера созревания кардиомиоцитов, морфологию и структуру (например, саркомер, митохондрии), свойства (например, пульсативность, электрофизиологическое созревание) и т.п. Эти показатели могут быть подтверждены хорошо известным способом.
Например, уровень экспрессии маркера созревания кардиомиоцитов может быть проанализирован путем измерения уровня экспрессии маркерного гена с помощью ПЦР; проанализирован по уровню экспрессии маркерного белка с помощью вестерн-блоттинга и т.п.; или проанализирован с помощью флуоресцентной метки с использованием микроскопа или проточной цитометрии. Показатель электрофизиологического созревания может быть проанализирован по степени мембранного потенциала покоя с использованием метода patch clamping и т.п. Показатель микроструктуры саркомера или митохондрий можно наблюдать с помощью электронного микроскопа; анализировать с помощью флуоресцентной метки с использованием микроскопа или проточной цитометрии; или функционального анализа с помощью анализатора внеклеточного потока и т.п.
[0154]
В одном варианте осуществления зрелые кардиомиоциты, полученные с использованием соединения (I) по настоящему изобретению, можно использовать в регенеративной медицине сердца. Например, композицию, содержащую клеточную массу кардиомиоцитов, полученную способом по настоящему изобретению, можно вводить в сердце пациента, страдающего сердечным заболеванием. В частности, кардиомиоциты, полученные способом по настоящему изобретению, могут быть непосредственно трансплантированы в сердце пациента, страдающего сердечным заболеванием, в виде клеточной суспензии или в форме слоя кардиомиоцитов (однослойного или многослойного). Например, WO 2012/133945, WO 2013/137491, WO 2014/192909 и WO 2016/076368 относятся к способу получения слоев кардиомиоцитов.
В другом варианте осуществления кардиомиоциты, полученные с использованием соединения (I) по настоящему изобретению, также можно использовать для скрининга лекарственного средства или оценки кардиотоксичности лекарственного средства для лечения сердечного заболевания, поскольку кардиомиоциты являются равномерно зрелыми. Например, путем введения тестируемого лекарственного средства в кардиомиоциты, полученные способом по настоящему изобретению, и затем измерив ответ кардиомиоцитов, можно оценить эффект и токсичность тестируемого лекарственного средства.
В другом варианте осуществления кардиомиоциты с пониженной автоматией, полученные с использованием соединения (I) по настоящему изобретению, можно использовать в регенеративной медицине сердца.
Примеры
[0155]
Настоящее изобретение подробно объясняется ниже со ссылкой на примеры и экспериментальные примеры. Однако примеры не ограничивают настоящее изобретение, и примеры могут быть модифицированы в пределах объема настоящего изобретения.
«Комнатная температура» в следующих примерах указывает, что диапазон обычно составляет от примерно 10°С до примерно 35°С. Отношение для смешанного растворителя, если не указано иное, представляет собой объемное соотношение смешивания и % означает мас. %, если не указано иное.
Элюирование с помощью колоночной хроматографии в примерах проводили под наблюдением с помощью TLC (тонкослойной хроматографии), если не указано иное. При наблюдении с помощью TLC 60 F254 производства Merck использовали в качестве пластины для TLC, растворитель, используемый в качестве элюирующего растворителя в колоночной хроматографии, использовали в качестве элюента, а УФ-детектор использовали для обнаружения. В колоночной хроматографии на силикагеле указание NH означает, что используется аминопропилсилан-связанный силикагель, а указание Diol означает использование 3-(2,3-дигидроксипропокси)пропилсилан-связанный силикагель. В препаративной ВЭЖХ (высокоэффективной жидкостной хроматографии) указание C18 означает использование октадецил-связанного силикагеля. Соотношение для растворителя для элюирования, если не указано иное, является объемным соотношением компонентов смеси.
1H ЯМР осуществляли путем ЯМР с фурье-преобразованием. Для анализа 1H ЯМР использовали программное обеспечение ACD/SpecManager (торговое название) или тому подобное. Ничего не указывается об очень слабовыраженных пиках протонов гидроксильной группы, аминогруппы и так далее.
МС измеряли методом LC/MS. В качестве метода ионизации использовали метод ESI или метод APCI. Данные показывали фактическое измеренное значение (найдено). Хотя обычно наблюдался пик молекулярного иона, иногда наблюдался фрагментный ион. В случае соли, как правило, наблюдается пик молекулярного иона или пик фрагментного иона свободной формы.
Единица концентрации образца (c) для оптического вращения ([α]D) составляла г/100 мл.
Значение элементного анализа (Анал.) описывается как вычисленное значение (вычисл.) и фактическое измеренное значение (найдено).
[0156]
Пики порошковой рентгеновской дифракции в примерах означают пики, измеренные при комнатной температуре с использованием Ultima IV (Rigaku Corporation, Japan) с излучением Cu Kα в качестве источника излучения. Условия измерения следующие.
Электрическое напряжение/Сила тока: 40 кВ/50 мА
Скорость сканирования: 6 град/мин
Диапазон сканирования 2 тета: 2-35 град
Кристалличность по порошковой рентгеновской дифракции в примерах рассчитывали по методу Германса.
В следующих примерах используются следующие сокращения.
Темп. плавл.: температура плавления
MS: масс-спектр
M: мольная концентрация
н: нормальность
CDCl3: дейтерированный хлороформ
DMSO-d6: дейтеродиметилсульфоксид
1H ЯМР: протонный ядерный магнитный резонанс
LC/MS: жидкостная хроматография с масс-спектрометрией
ESI: электрораспылительная ионизация
APCI: химическая ионизация при атмосферном давлении
THF: тетрагидрофуран
MeOH: метанол
EtOH: этанол
TEA: триэтиламин
DEAD: диэтил (E)-диазен-1,2-дикарбоксилат.
[0157]
Пример 1
2-(2-фенил-1H-бензимидазол-5-ил)-5-(пиперидин-1-ил)изоиндолин-1-он
[0158]
A) 5-(пиперидин-1-ил)-2-бензофуран-1(3H)-он
К смеси 5-бром-2-бензофуран-1(3H)-она (25.0 г), пиперидина (13,92 мл) и толуола (250 мл) добавляли ацетат палладия (2,63 г), 2,2’-бис(дифенилфосфино)-1,1'-бинафтил (10,96 г) и карбонат цезия (26,78 г) при комнатной температуре. Смесь перемешивали при 100°C в течение 12 ч. К смеси добавляли дихлорметан, примеси удаляли фильтрованием через целит и фильтрат концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/петролейный эфир) с получением указанного в заголовке соединения (13,0 г).
MS: [M+H]+218.
[0159]
B) N-(4-амино-3-нитрофенил)-2-(гидроксиметил)-4-(пиперидин-1-ил)бензамид
К смеси 2-нитробензол-1,4-диамина (9,17 г) и THF (200 мл) по каплям добавляли 2М раствор триметилалюминий в толуоле (65,89 мл) при 0°C, и смесь перемешивали при комнатной температуре в течение 1 ч. К реакционной смеси добавляли смесь 5-(пиперидин-1-ил)-2-бензофуран-1(3H)-она (13,0 г) и THF (100 мл) при комнатной температуре, и реакционную смесь перемешивали при комнатной температуре в течение 48 ч. К смеси добавляли насыщенный водный раствор гидрокарбоната натрия при 0°C, примеси удаляли фильтрованием через целит, и фильтрат экстрагировали этилацетатом. Органический слой отделяли, промывали насыщенным солевым раствором, сушили над безводным сульфатом натрия, и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (MeOH/дихлорметан) с получением указанного в заголовке соединения (3,35 г).
MS[M+H]+371.
[0160]
C) 2-(4-амино-3-нитрофенил)-5-(пиперидин-1-ил)изоиндолин-1-он
К смеси N-(4-амино-3-нитрофенил)-2-(гидроксиметил)-4-(пиперидин-1-ил)бензамида (3,35 г), трибутилфосфина (2,9 мл) и THF (130 мл) добавляли DEAD (5,12 мл) при комнатной температуре. Смесь перемешивали при комнатной температуре в течение 16 ч, и реакционный раствор концентрировали. К полученному остатку добавляли воду и этилацетат, и полученное твердое вещество собирали путем фильтрации, промывали этилацетатом и сушили с получением указанного в заголовке соединения (1,68 г).
MS[M+H]+353.
[0161]
D) 2-(3,4-диаминофенил)-5-(пиперидин-1-ил)изоиндолин-1-он
К смеси 2-(4-амино-3-нитрофенил)-5-(пиперидин-1-ил)изоиндолин-1-она (1,68 г) и EtOH (80 мл) добавляли 10% палладий на углероде (1,68 г) при комнатной температуре. Смесь перемешивали в атмосфере водорода при 3,4 атм, при комнатной температуре в течение 12 ч. Катализатор удаляли путем фильтрации, и фильтрат концентрировали при пониженном давлении с получением указанного в заголовке соединения (1,0 г).
MS[M+H]+323.
[0162]
E) 2-(2-фенил-1H-бензимидазол-5-ил)-5-(пиперидин-1-ил)изоиндолин-1-он
К смеси 2-(3,4-диаминофенил)-5-(пиперидин-1-ил)изоиндолин-1-она (0,075 г) и THF (2 мл) добавляли TEA (0,035 мл) и смесь бензоилхлорида (0,027 мл) и THF (1 мл) при 0°C. Смесь перемешивали при 0°C в течение 30 мин, и затем перемешивали при комнатной температуре в течение 1 ч, и реакционный раствор концентрировали. Полученный остаток разделяли между этилацетатом-THF-водой, и органический слой промывали насыщенным водным раствором гидрокарбоната натрия и насыщенным солевым раствором, сушили над безводным сульфатом натрия, и концентрировали при пониженном давлении. К полученному остатку добавляли MeOH (5 мл) и конц. хлористоводродной кислотой (0,3 мл), и смесь кипятили с обратным холодильником в течение 12 ч, и реакционный раствор концентрировали. К полученному остатку добавляли насыщенный водный раствор гидрокарбоната натрия, и полученное твердое вещество собирали путем фильтрации, промывали этилацетатом, и сушили с получением указанного в заголовке соединения (0,037 г).
[0163]
Пример 2
2-(2-бензил-1H-бензимидазол-5-ил)-5-(пиперидин-1-ил)изоиндолин-1-он
К смеси фенилацетальдегида (0,046 г) и EtOH (2 мл) добавляли натрия гидросульфит (0,181 г) и 2-(3,4-диаминофенил)-5-(пиперидин-1-ил)изоиндолин-1-он (0,125 г) при 0°C. Смесь перемешивали при комнатной температуре в течение 16 ч, и реакционный раствор концентрировали. К полученному остатку добавляли воду, и полученное твердое вещество собирали путем фильтрации, и промывали водой. Остаток очищали с помощью ВЭЖХ (L-колонка 2 ODS, подвижная фаза: вода/ацетонитрил (содержащая 0,1% муравьиной кислоты)) с получением указанного в заголовке соединения (0,024 г).
[0164]
Пример 3
2-(2-(4-(бензилокси)фенил)-1H-бензимидазол-5-ил)-5-(пиперидин-1-ил)изоиндолин-1-он
К смеси 4-(бензилокси)бензальдегида (0,082 г) и EtOH (2 мл) добавляли натрия гидросульфит (0,181 г) и 2-(3,4-диаминофенил)-5-(пиперидин-1-ил)изоиндолин-1-он (0,125 г) при 0°C. Смесь перемешивали при комнатной температуре в течение 18 ч, и реакционный раствор концентрировали. К остатку добавляли воду, и полученное твердое вещество собирали путем фильтрации, промывали водой, и сушили. Остаток очищали с помощью ВЭЖХ (L-колонка 2 ODS, подвижная фаза: вода/ацетонитрил (содержащая 10 мМ ацетат аммония)) с получением указанного в заголовке соединения (0,030 г).
[0165]
Пример 4
2-(2-(4-гидроксифенил)-1H-бензимидазол-5-ил)-5-(пиперидин-1-ил)изоиндолин-1-он
К смеси 2-(2-(4-(бензилокси)фенил)-1H-бензимидазол-5-ил)-5-(пиперидин-1-ил)изоиндолин-1-она (0,150 г), MeOH (6 мл) и THF (3 мл) добавляли 10% палладий на углероде (0,1 г) при комнатной температуре. Смесь перемешивали при нормальном давлении атмосферы водорода, при комнатной температуре в течение 16 ч. Катализатор удаляли путем фильтрации, и фильтрат концентрировали при пониженном давлении. Остаток промывали диэтиловым эфиром и MeOH, и сушили с получением указанного в заголовке соединения (0,070 г).
[0166]
Пример 5
метил (4-(5-(1-оксо-5-(пиперидин-1-ил)-1,3-дигидро-2H-изоиндол-2-ил)-1H-бензимидазол-2-ил)фенокси)ацетат
К смеси метил (4-формилфенокси)ацетата (0,120 г) и EtOH (3 мл) добавляли натрия гидросульфит (0,290 г) и 2-(3,4-диаминофенил)-5-(пиперидин-1-ил)изоиндолин-1-он (0,2 г) при 0°C. Смесь перемешивали при комнатной температуре в течение 16 ч, и реакционный раствор концентрировали. К полученному остатку добавляли воду, и полученное твердое вещество собирали путем фильтрации, промывали водой, и сушили. Полученное твердое вещество очищали с помощью колоночной хроматографии на силикагеле (MeOH/дихлорметан) с получением указанного в заголовке соединения (0,120 г).
[0167]
Пример 6
(4-(5-(1-оксо-5-(пиперидин-1-ил)-1,3-дигидро-2H-изоиндол-2-ил)-1H-бензимидазол-2-ил)фенокси)уксусная кислота
К смеси метил (4-(5-(1-оксо-5-(пиперидин-1-ил)-1,3-дигидро-2H-изоиндол-2-ил)-1H-бензимидазол-2-ил)фенокси)ацетата (1,3 г), THF (13 мл) и воды (13 мл) добавляли гидроксид лития (0,330 г) при комнатной температуре. Смесь перемешивали при комнатной температуре в течение 16 ч, и к реакционному раствору добавляли воду. Смесь разделяли между этилацетатом-водой, и водный слой подкисляли 1 н. хлористоводродной кислотой (pH<4). Полученное твердое вещество собирали путем фильтрации, промывали водой и MeOH, и сушили с получением указанного в заголовке соединения (0,710 г).
[0168]
Пример 8
2-(2-(4-бромфенил)-1H-бензимидазол-5-ил)-5-(морфолин-4-ил)изоиндолин-1-он
[0169]
A) 5-(4-морфолинил)-2-бензофуран-1(3H)-он
Смесь ацетата палладия (0,948 г), 2,2’-бис(дифенилфосфино)-1,1’-бинафтила (3,95 г), карбоната цезия (9,64 г) и толуола (70 мл) перемешивали в атмосфере азота в течение 5 мин. К этой смеси добавляли 5-бром-2-бензофуран-1(3H)-он (9,0 г) и морфолин (4,4 мл), и смесь перемешивали в атмосфере азота при 100°C в течение 4 ч. Смесь охлаждали, и концентрировали при пониженном давлении. К остатку добавляли хлороформ, и нерастворимое вещество удаляли путем фильтрования через целит, и фильтрат концентрировали при пониженном давлении. К остатку добавляли этилацет, и полученное твердое вещество собирали путем фильтрации с получением сырого вещества. Сырое вещество кристаллизовали из THF и этилацетата с получением указанного в заголовке соединения (6,39 г).
1H ЯМР (200 МГц, CDCl3) δ3,31-3,36 (4H, м), 3,85-3,90 (4H, м), 5,22 (2H, с), 6,82 (1H, д, J=1,6 Гц), 7,00 (1H, дд, J=8,8, 2,2 Гц), 7,77 (1H, д, J=8,8 Гц).
[0170]
B) 2-(4-бромфенил)-5-нитро-1H-бензимидазол
К смеси 4-нитробензол-1,2-диамина (5,0 г), триэтиламина (5,0 мл) и THF (80 мл) по каплям добавляли смесь 4-бромбензоилхлорид (7,17 г) и THF (20 мл) при 0°C, и смесь перемешивали в течение 30 мин, и затем при комнатной температуре в течение 1 ч. Смесь концентрировали при пониженном давлении, добавляли насыщенный водный раствор гидрокарбоната натрия, и полученное твердое вещество собирали путем фильтрации, промывали водой с получением сырого вещества. К смеси этого сырого вещества и метанола (100 мл) добавляли конц. хлористоводродную кислоту (10 мл), и смесь перемешивали при 80°C в течение 22 ч, и концентрировали при пониженном давлении. К остатку добавляли насыщенный водный раствор гидрокарбоната натрия, и полученное твердое вещество собирали путем фильтрации, и промывали последовательно водой и этилацетом с получением указанного в заголовке соединения (8,84 г).
1H ЯМР (200 МГц, DMSO-d6) δ7,71 (2H, д, J=8,8 Гц), 7,81 (1H, дд, J=9,0, 0,6 Гц), 8,17 (1H, дд, J=8,9, 2,3 Гц), 8,28 (2H, д, J=8,8 Гц), 8,50 (1H, д, J=2,0 Гц).
[0171]
C) 2-(4-бромфенил)-1H-бензимидазол-5-амин
Смесь 2-(4-бромфенил)-5-нитро-1H-бензимидазола (7,68 г), олова(II) хлорид дигидрата (27,2 г) и этанола (300 мл) перемешивали при 65°C в течение 3 часов. Смесь охлаждали до комнатной температуры, доводили до pH=8 с помощью насыщенного водного раствора гидрокарбоната натрия, и концентрировали при пониженном давлении. К остатку добавляли этилацета и воду, нерастворимое вещество удаляли фильтрованием через целит, и водный слой отделяли, и экстрагировали этилацетатом. Органические слои объединяли, промывали насыщенным водным раствором гидрокарбоната натрия и насыщенным солевым раствором, сушили над безводным сульфатом натрия, и концентрировали при пониженном давлении. Остаток промывали этилацетом с получением указанного в заголовке соединения (5,61 г).
1H ЯМР (200 МГц, DMSO-d6) δ4,96 (2H, шир), 6,54 (1H, дд, J=8,7, 2,1 Гц), 6,67 (1H, с), 7,29 (1H, д, J=8,4 Гц), 7,70 (2H, д, J=8,6 Гц), 8,00 (2H, д, J=8,4 Гц), 12,18 (1H, шир.с).
[0172]
D) N-(2-(4-бромфенил)-1H-бензимидазол-5-ил)-2-(гидроксиметил)-4-(4-морфолинил)бензамид
К смеси 2-(4-бромфенил)-1H-бензимидазол-5-амина (1,0 г) и THF (100 мл) по каплям добавляли 1M гексановый раствор (13,9 мл) диметилалюминий хлорида, и смесь перемешивали в течение 5 мин. Добавляли к смеси 5-(4-морфолинил)-2-бензофуран-1(3H)-он (760,9 мг), и смесь перемешивали в течение 4 дней. Добавляли 0,005 н. хлористоводродную кислоту небольшими порциями, и полученное твердое вещество собирали путем фильтрации, последовательно промывали 0,005 н. хлористоводродной кислотой, водой, насыщенным водным раствором гидрокарбоната натрия и водой с получением сырого вещества. Продукт кристаллизовали из THF-метанола с получением указанного в заголовке соединения (1,033 г).
1H ЯМР (300 МГц, DMSO-d6) δ 3,22 (4H, м), 3,77 (4H, м), 4,69 (2H, д, J=4,3 Гц), 5,43 (1H, т, J=4,8 Гц), 6,93 (1H, дд, J=8,7, 2,5 Гц), 7,16 (1H, д, J=2,4 Гц), 7,44 (1H, с), 7,57 (2H, д, J=8,5 Гц), 7,77 (2H, м), 8,09 (2H, д, J=8,5 Гц), 8,20 (1H, с), 10,33 (1H, с), 12,92 (1H, с).
[0173]
E) 2-(2-(4-бромфенил)-1H-бензимидазол-5-ил)-5-(морфолин-4-ил)изоиндолин-1-он
К смеси N-(2-(4-бромфенил)-1H-бензимидазол-5-ил)-2-(гидроксиметил)-4-(4-морфолинил)бензамида (0,95 г) и N, N-диметилформамида (10 мл) добавляли трибутилфосфин (1,75 мл), и затем DEAD (1,36 мл) по каплям добавляли. Смесь перемешивали в течение 1 ч, и реакционный раствор концентрировали. К полученному остатку добавляли этилацет и небольшое количество воды, и смесь кипятили с обратным холодильником в течение 3 мин. Смесь охлаждали, и полученное твердое вещество собирали путем фильтрации, промывали этилацетом, и сушили с получением указанного в заголовке соединения (807 мг).
1H ЯМР (300 МГц, DMSO-d6) δ 3,29 (4H, т, J=4,7 Гц), 3,77 (4H, т, J=4,3 Гц), 4,99 (2H, с), 7,11 (2H, м), 7,72 (5H, м), 8,14 (3H, м), 13,00 (1H, с).
[0174]
Пример 17
N-(1,1-диоксидо-2,3-дигидро-1-бензотиофен-5-ил)-2-(4-(5-(1-оксо-5-(пиперидин-1-ил)-1,3-дигидро-2H-изоиндол-2-ил)-1H-бензимидазол-2-ил)фенокси)ацетамид
К смеси (4-(5-(1-оксо-5-(пиперидин-1-ил)-1,3-дигидро-2H-изоиндол-2-ил)-1H-бензимидазол-2-ил)фенокси)уксусной кислоты (15 мг), N, N-диизопропилэтиламина (0,027 мл) и N, N-диметилацетамида (1 мл) добавляли хлор-N, N,N',N'-бис(тетраметилен)формамидиния гексафторфосфат (16 мг) при комнатной температуре, и смесь перемешивали при комнатной температуре в течение 0,5 ч. К смеси добавляли 5-амино-2,3-дигидробензо[b]тиофен 1,1-диоксид (11,4 мг) при комнатной температуре, и смесь перемешивали в течение 3 дней. Смесь фильтровали, и остаток очищали с помощью ВЭЖХ (YMCTriartC18, подвижная фаза: вода/ацетонитрил (содержащая 10 мМ бикарбонат аммония)) с получением указанного в заголовке соединения (8,7 мг).
1H ЯМР (300 МГц, DMSO-d6) δ 1,57-1,67 (6H, м), 3,36-3,39 (6H, м), 3,53-3,61 (2H, м), 4,87 (2H, с), 4,95 (2H, с), 7,01-7,13 (2H, м), 7,14-7,22 (2H, м), 7,49-7,79 (5H, м), 7,91 (1H, с), 7,98-8,28 (3H, м), 10,57 (1H, шир.с), 12,78 (1H, шир.с).
[0175]
Пример 9-16 и 18-28
К смеси (4-(5-(1-оксо-5-(пиперидин-1-ил)-1,3-дигидро-2H-изоиндол-2-ил)-1H-бензимидазол-2-ил)фенокси)уксусной кислоты (0,029 г, 0,06 ммоль), хлор-N, N,N',N'-бис(тетраметилен)формамидиния гексафторфосфата (0,030 г) и N, N-диметилацетамида (1 мл) по каплям добавляли N, N-диизопропилэтиламин (0,052 мл) при комнатной температуре, и смесь перемешивали при комнатной температуре в течение 0,5 ч. К смеси добавляли соответствующий амин (0,12 ммоль) при комнатной температуре, и смесь перемешивали в течение 2 ч. К смеси добавляли воду (0,5 мл), и смесь концентрировали при 60°C. Остаток очищали с помощью ВЭЖХ (YMCTriartC18, подвижная фаза: вода/ацетонитрил (содержащая 10 мМ бикарбонат аммония)) с получением соединений примеров 9-16 и 18-28.
[0176]
Пример 29-38
Смесь соответствующего амина (0,16 ммоль), 2-(4-(5-(5-морфолино-1-оксо-1,3-дигидро-2H-изоиндолин-2-ил)-1H-бензимидазол-2-ил)фенокси)уксусной кислоты (0,039 г, 0,08 ммоль) (синтезировали в соответствии со способами примера 1 стадий A-C и примеров 5-6, за исключением использования морфолина вместо пиперидина), O-(7-азабензотриазол-1-ил)-N, N,N',N'-тетраметилуроний гексафторфосфата (0,037 г), N, N-диизопропилэтиламина (0,056 ммоль) и N, N-диметилформамида (1 мл) перемешивали при комнатной температуре в течение 16 ч, и смесь концентрировали при 60°C. Остаток очищали с помощью ВЭЖХ (YMCTriartC18, подвижная фаза: вода/ацетонитрил (содержащая 10 мМ бикарбонат аммония)) с получением соединений примера 29-38.
[0177]
Пример 45
5-(пиперидин-1-ил)-2-(2-(пиридин-4-ил)-1H-бензимидазол-5-ил)изоиндолин-1-он
К смеси 2-(3,4-диаминофенил)-5-(пиперидин-1-ил)изоиндолин-1-она (0,125 г) и THF (3 мл) добавляли TEA (0,119 мл) и смесь изоникотиноилхлорида гидрохлорида (0,069 г) и THF (2 мл) при 0°C. Смесь перемешивали при 0°C в течение 30 мин, и затем при комнатной температуре в течение 16 ч, и реакционный раствор концентрировали. Полученный остаток разделяли между этилацетатом-THF-водой, и органический слой промывали насыщенным водным раствором гидрокарбоната натрия и насыщенным солевым раствором, сушили над безводным сульфатом натрия, и концентрировали при пониженном давлении. К полученному остатку добавляли MeOH (10 мл) и конц. хлористоводродную кислоту (0,6 мл), и смесь кипятили с обратным холодильником при 70°C в течение 16 ч, и реакционный раствор концентрировали. К полученному остатку добавляли насыщенный водный раствор гидрокарбоната натрия, и полученное твердое вещество собирали путем фильтрации с получением сырого вещества. Это сырое вещество очищали с помощью ВЭЖХ (L-колонка 2 ODS, подвижная фаза: вода/ацетонитрил (содержащая 10 мМ бикарбоната аммония)) с получением указанного в заголовке соединения (32 мг).
1H ЯМР (500 МГц, DMSO-d6) δ 1,62 (6H, шир.с), 3,37 (4H, шир.с), 4,96 (2H, с), 7,07-7,10 (2H, м), 7,57 (1H, д, J=8,2 Гц), 7,69 (2H, кв, J=8,7 Гц), 8,09 (2H, д, J=4,6 Гц), 8,19 (1H, с), 8,74 (2H, д, J=4,9 Гц).
[0178]
Пример 46
5-(пиперидин-1-ил)-2-(2-(пиридин-3-ил)-1H-бензимидазол-5-ил)изоиндолин-1-он
К смеси никотинальдегида и EtOH добавляли натрия гидросульфит (0,290 г) и 2-(3,4-диаминофенил)-5-(пиперидин-1-ил)изоиндолин-1-он (0,200 г) при 0°C. Смесь перемешивали при комнатной температуре в течение 16 ч, и реакционный раствор концентрировали. К полученному остатку добавляли воду, и полученное твердое вещество собирали путем фильтрации, промывали водой, и сушили с получением сырого вещества. Это сырое вещество очищали с помощью ВЭЖХ (L-колонка 2 ODS, подвижная фаза: вода/ацетонитрил (содержащая 10 мМ бикарбонат аммония)) с получением указанного в заголовке соединения (48 мг).
1H ЯМР (500 МГц, DMSO-d6) δ 1,62 (6H, шир.с), 3,37 (4H, шир.с), 4,96 (2H, д, J=7,0 Гц), 7,07-7,10 (2H, м), 7,56-7,60 (3H, м), 7,72 (0,6H, д, J=8,5 Гц), 7,88 (0,4H, д, J=8,5 Гц), 8,09 (0,4H, шир.с), 8,29 (0,6H, шир.с), 8,47-8,51 (1H, м), 8,67-8,68 (1H, м), 9,34-9,36 (1H, м), 13,10 (1H, шир.с).
[0179]
Соединения примеров показаны в следующих таблицах. MS в таблицах означает фактическое измеренное значение. Соединения примеров 7, 39-44 и 47-73 в следующих таблицах были синтезированы способами, показанными в вышеупомянутых примерах, или аналогичным им способом.
[0180]
[Таблица 1-1]
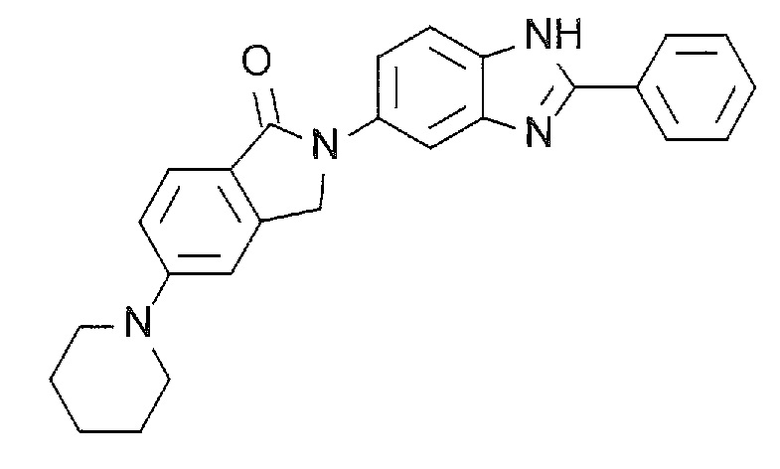
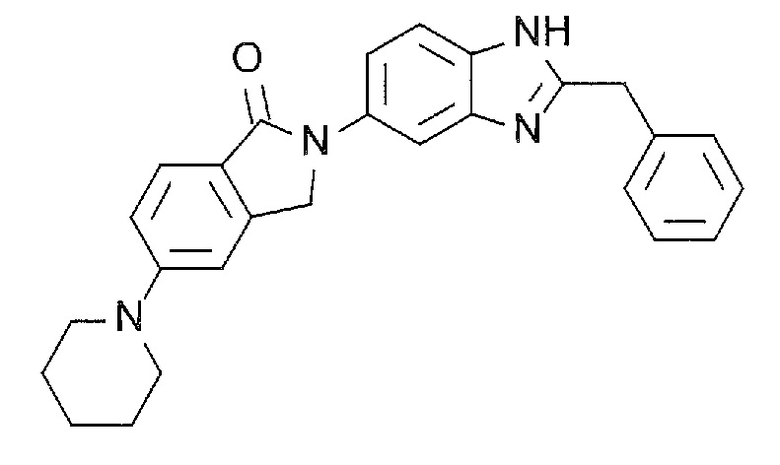
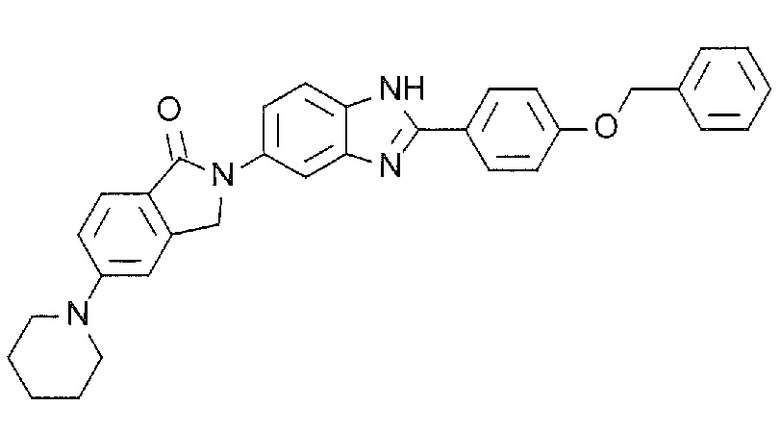
[0181]
[Таблица 1-2]
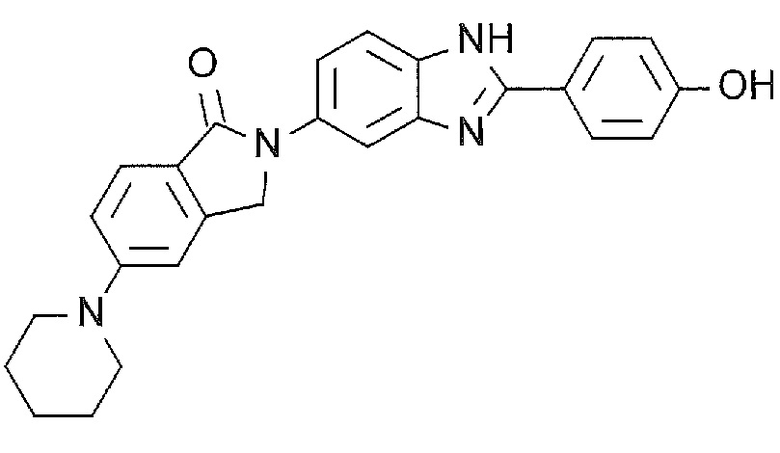
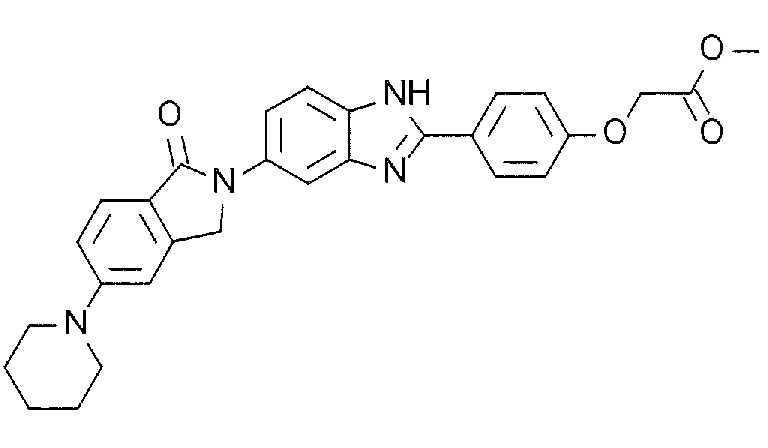
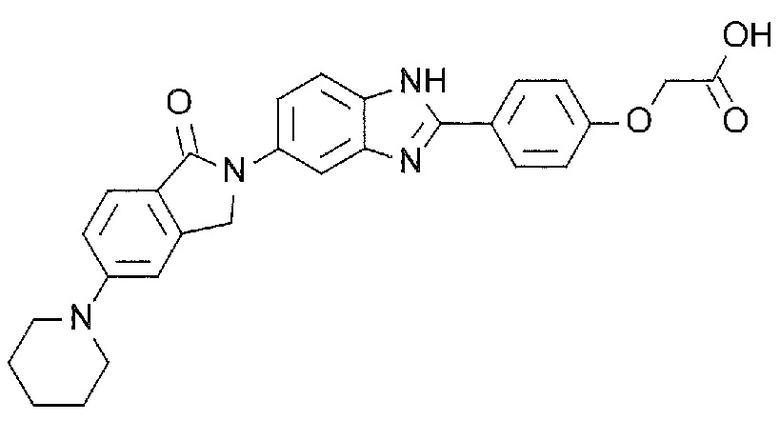
[0182]
[Таблица 1-3]
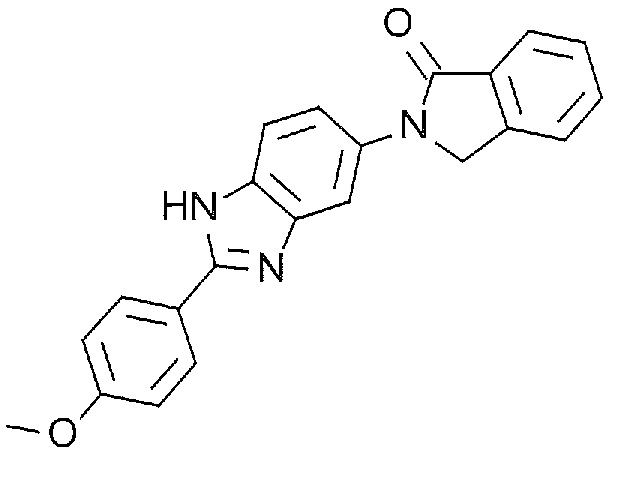
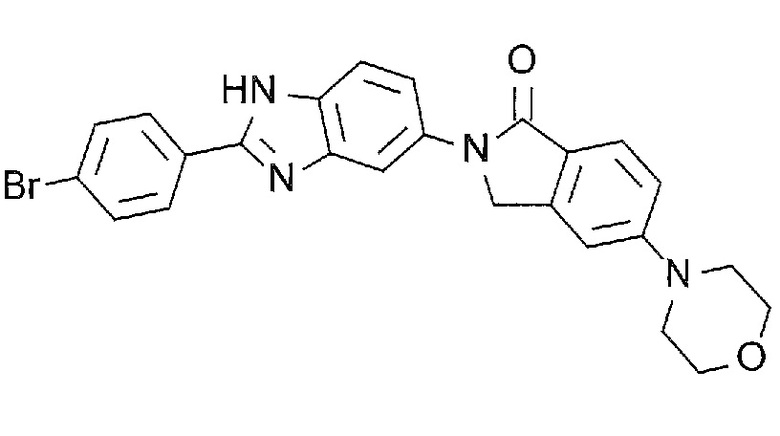
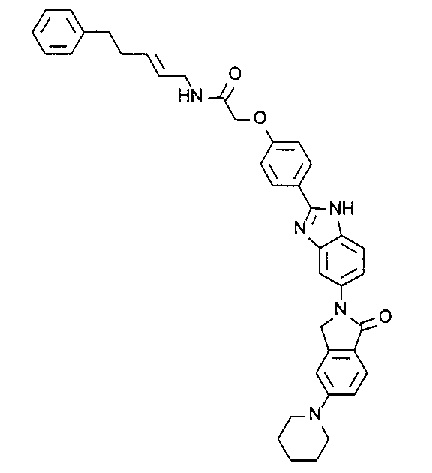
[0183]
[Таблица 1-4]
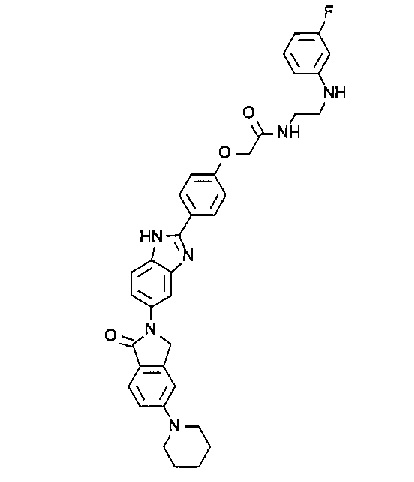
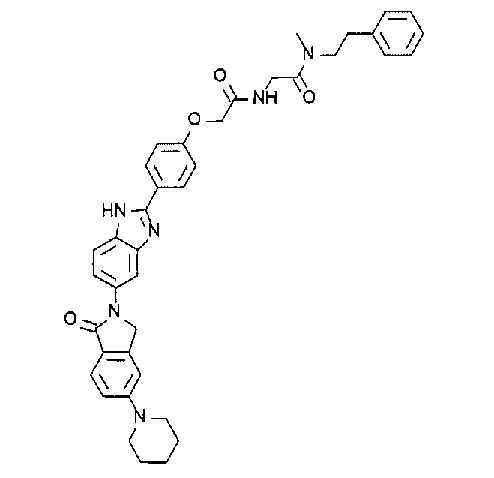
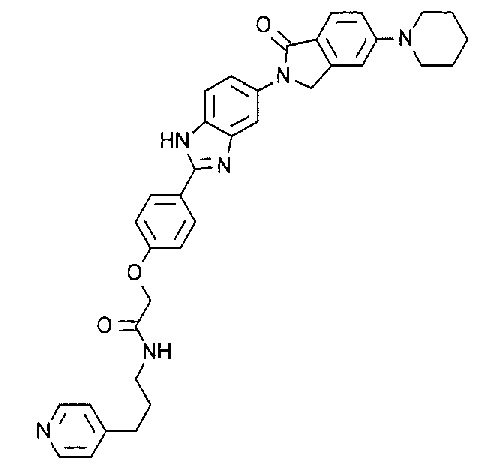
[0184]
[Таблица 1-5]
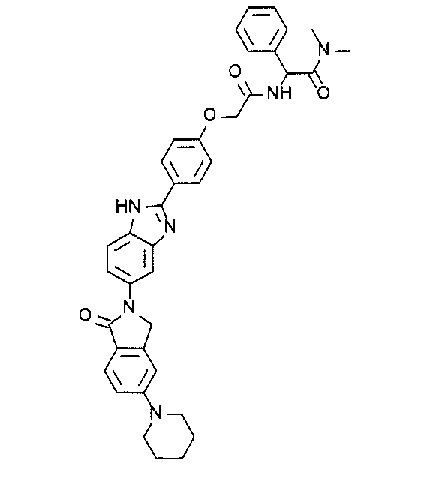
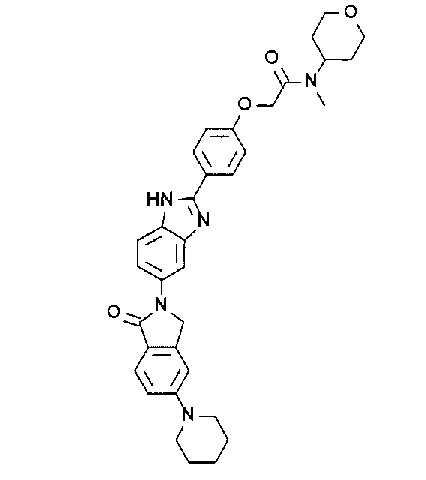
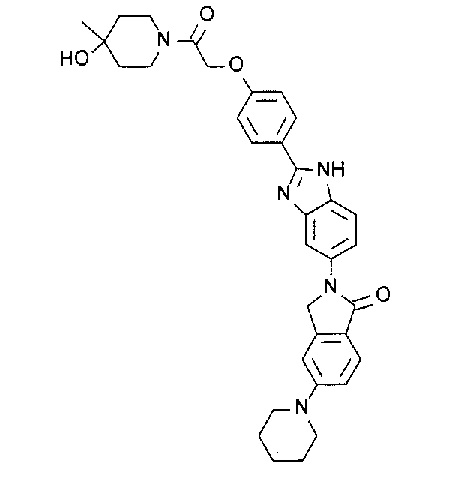
[0185]
[Таблица 1-6]
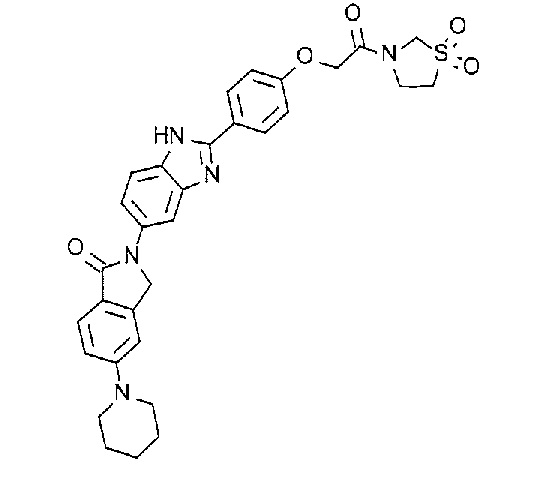
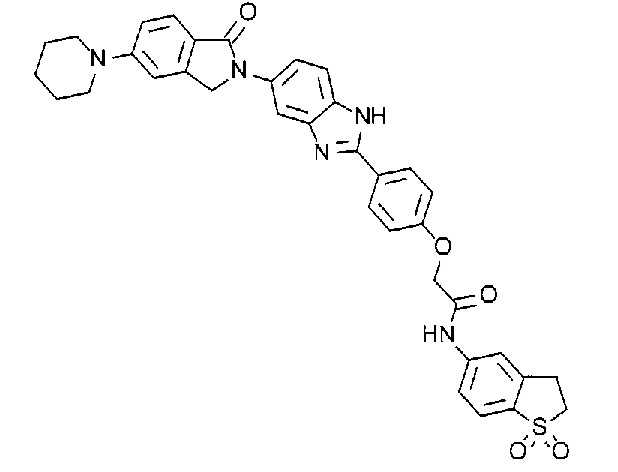
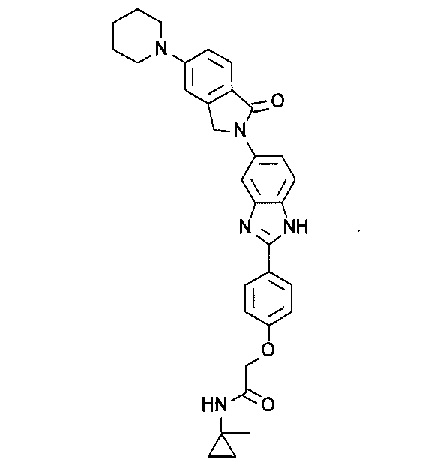
[0186]
[Таблица 1-7]
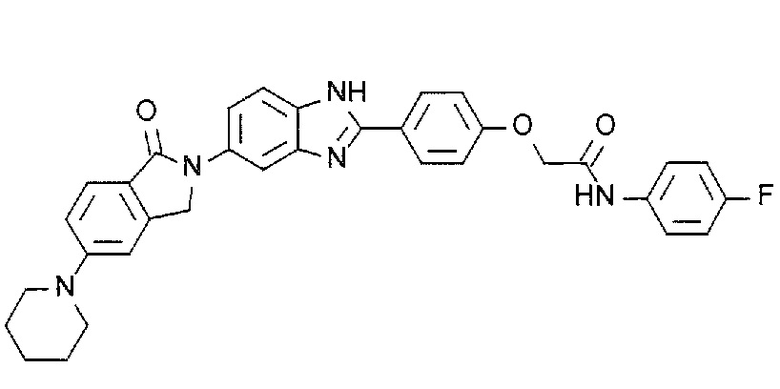
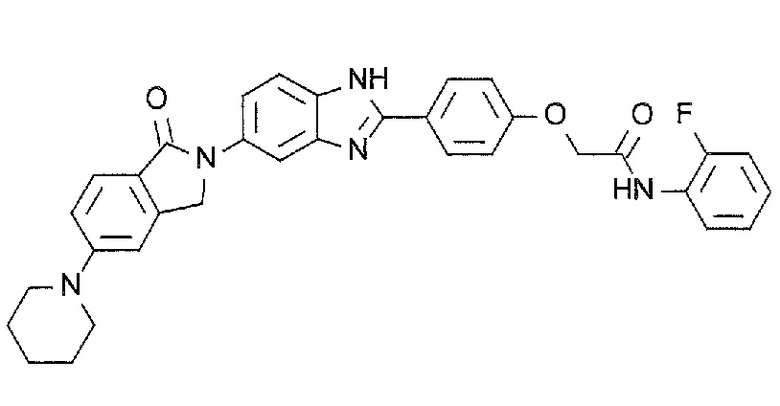
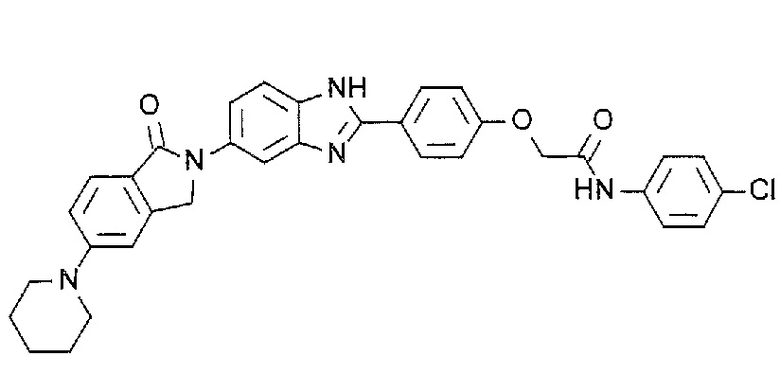
[0187]
[Таблица 1-8]
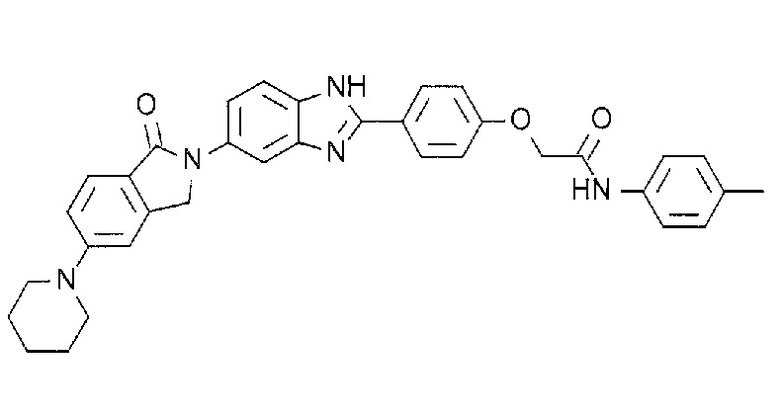
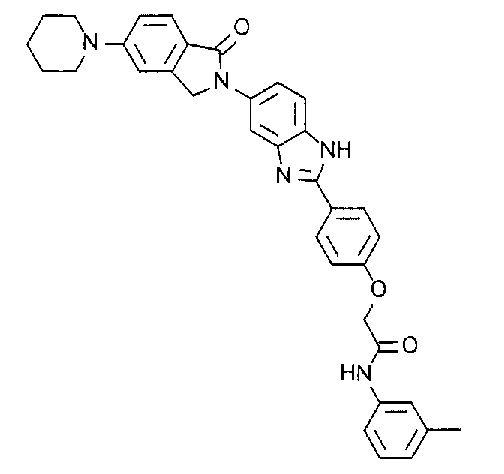
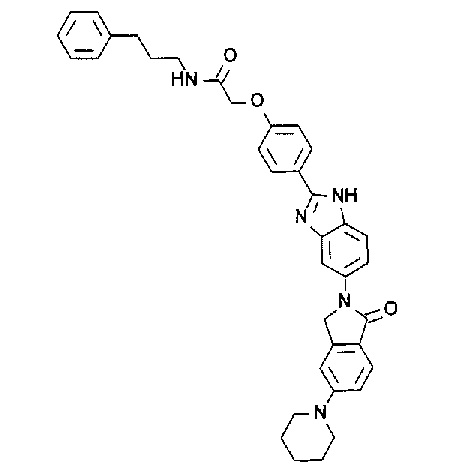
[0188]
[Таблица 1-9]
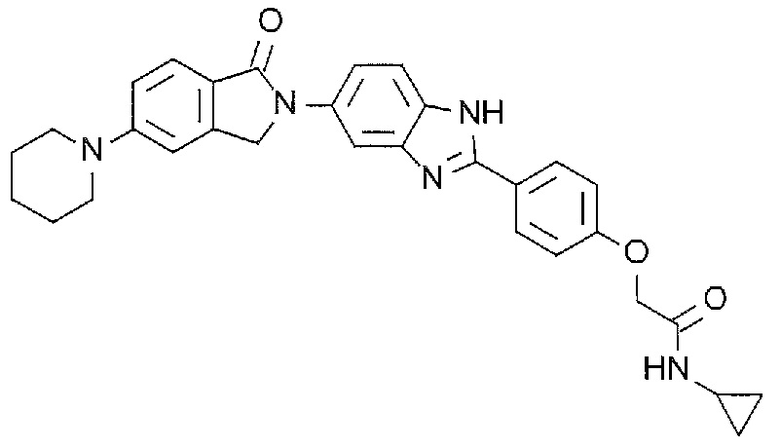
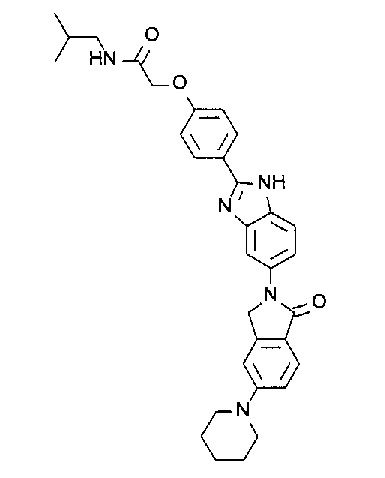
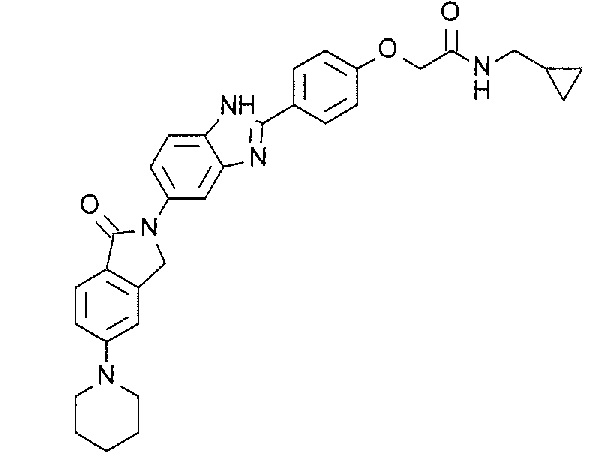
[0189]
[Таблица 1-10]
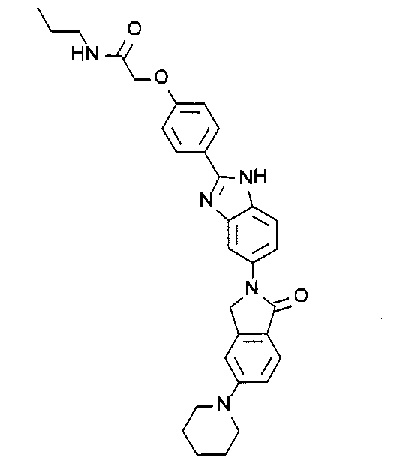
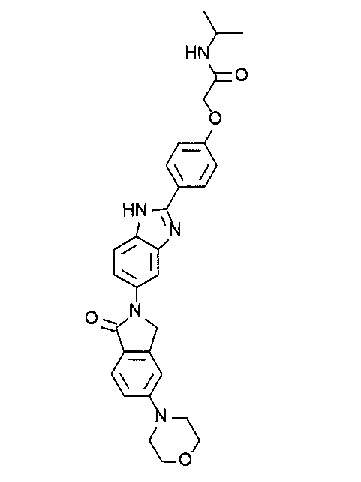
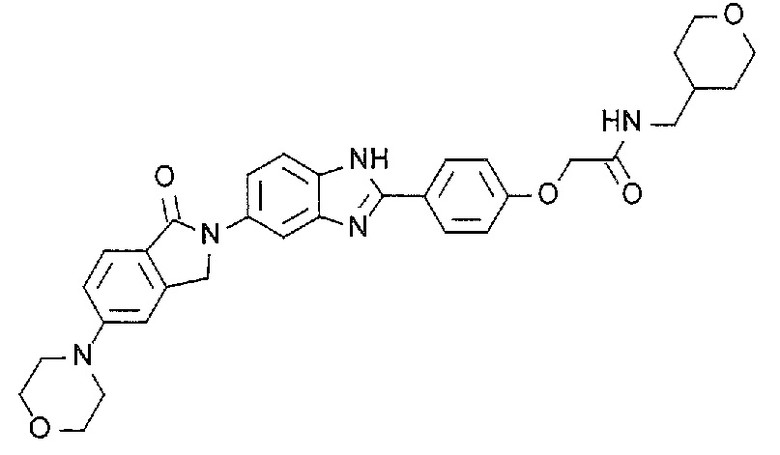
[0190]
[Таблица 1-11]
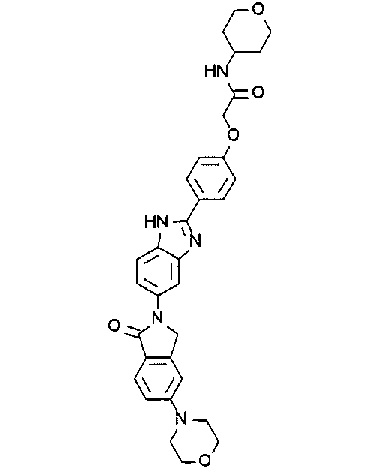
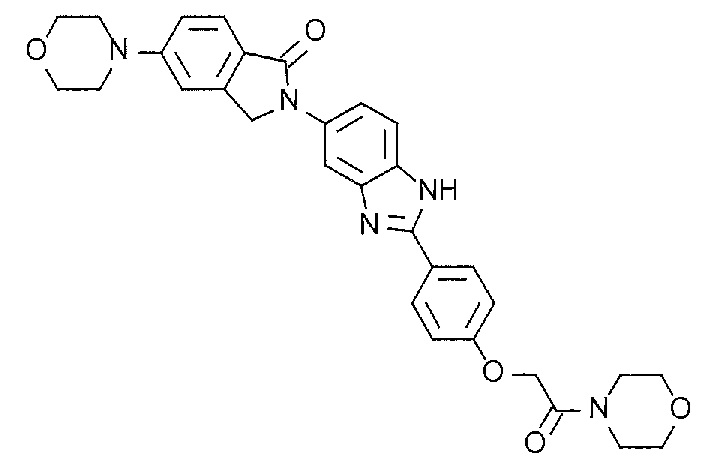
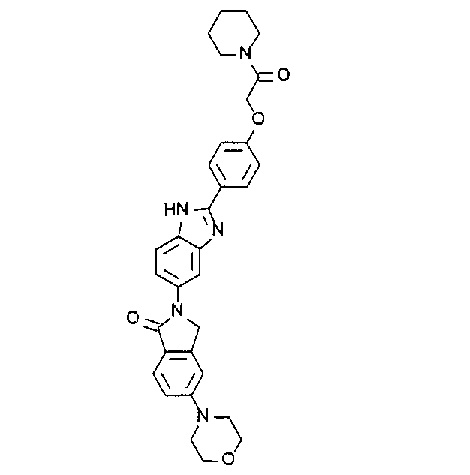
[0191]
[Таблица 1-12]
[0192]
[Таблица 1-13]
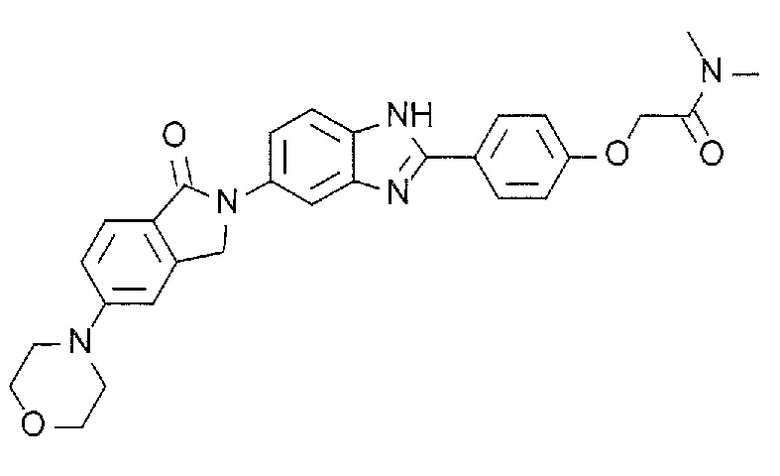
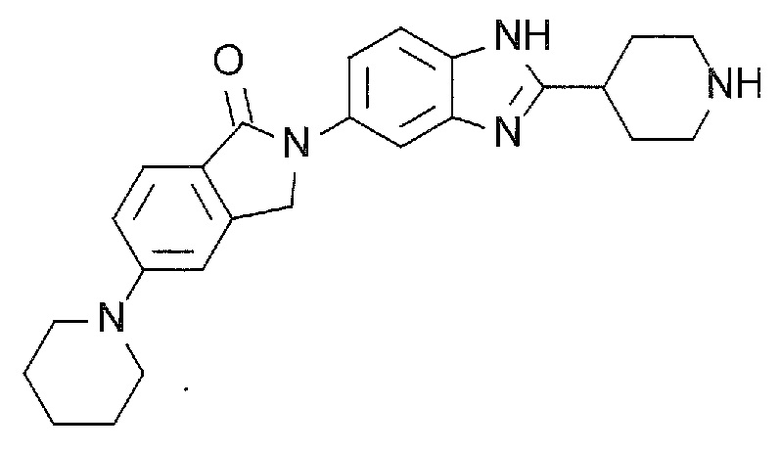
[0193]
[Таблица 1-14]
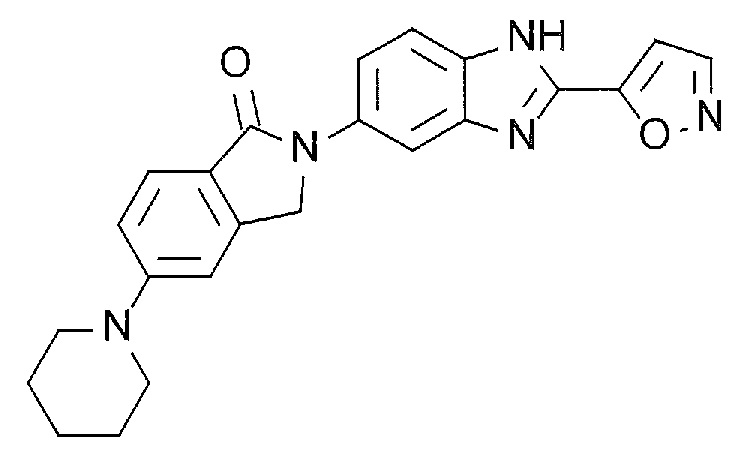
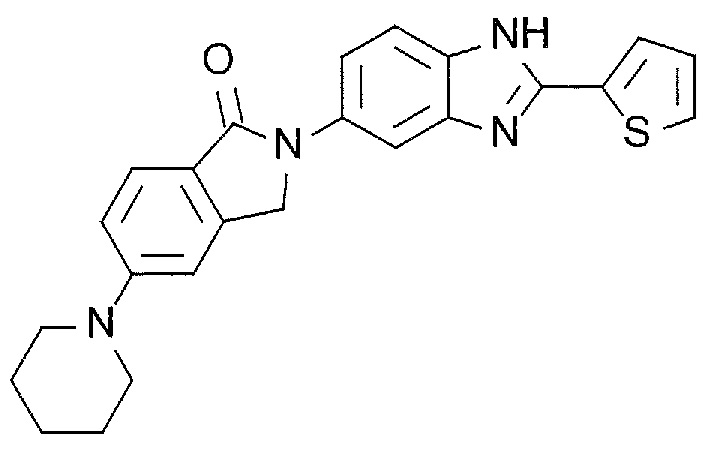
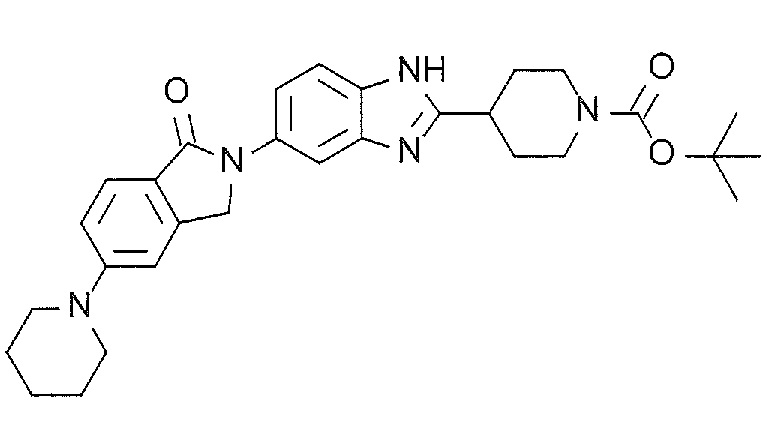
[0194]
[Таблица 1-15]
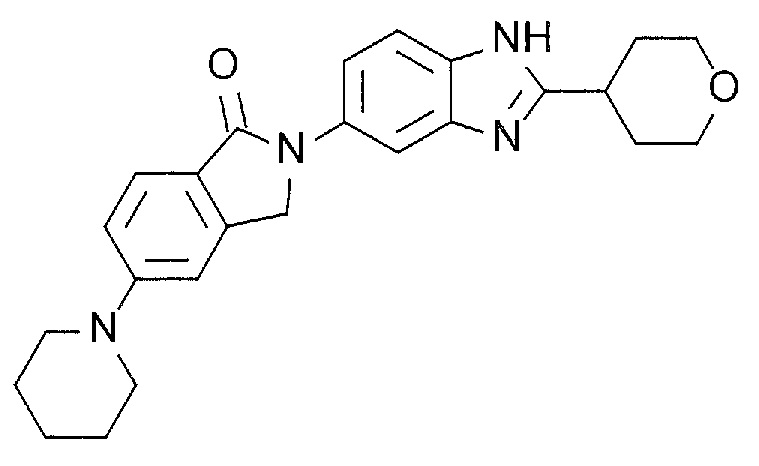
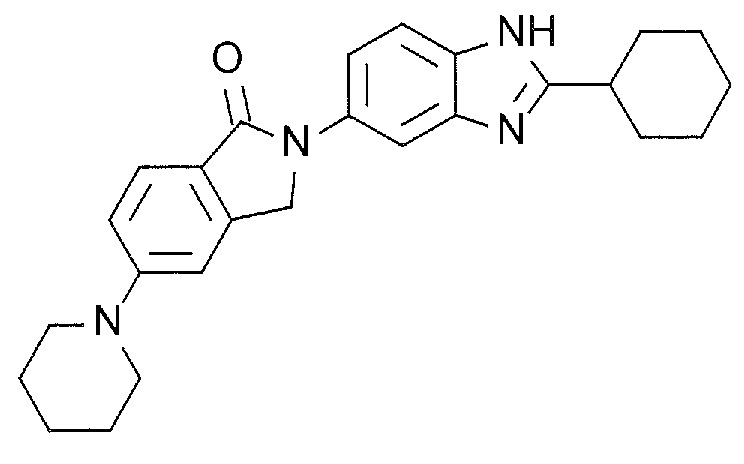
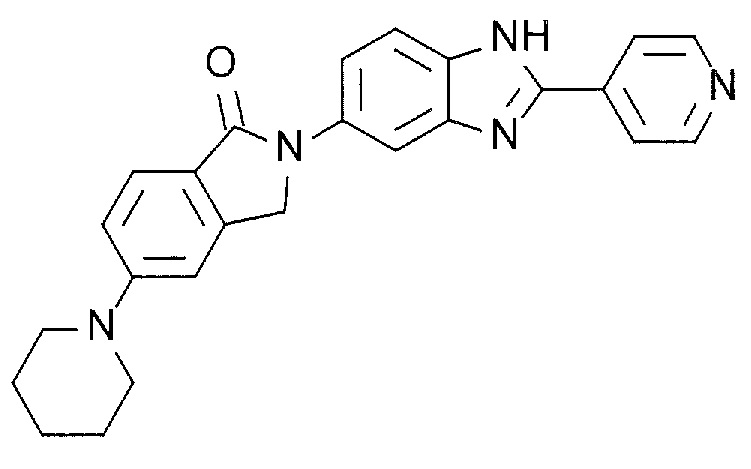
[0195]
[Таблица 1-16]
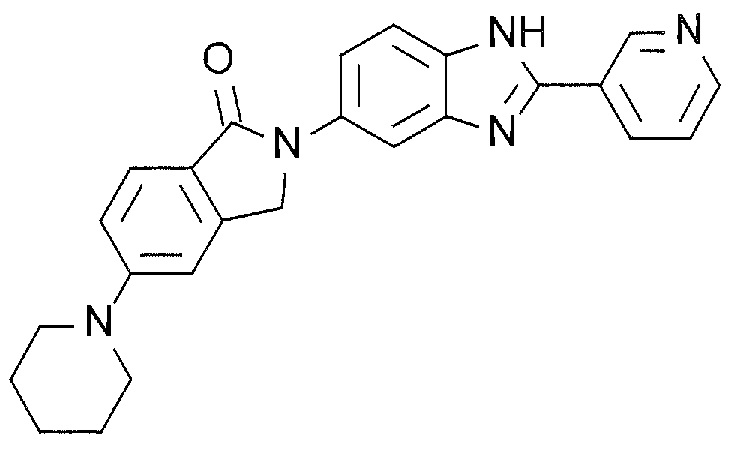
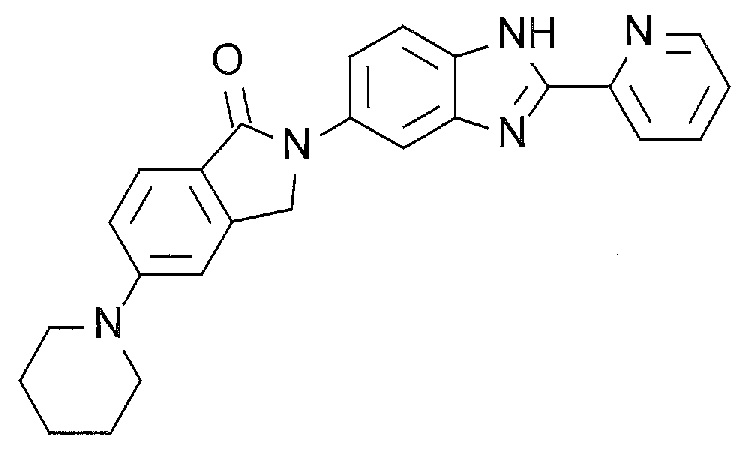
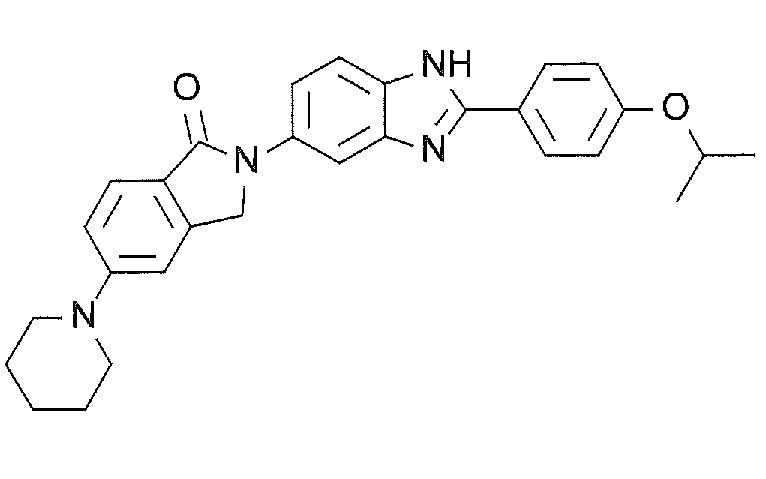
[0196]
[Таблица 1-17]
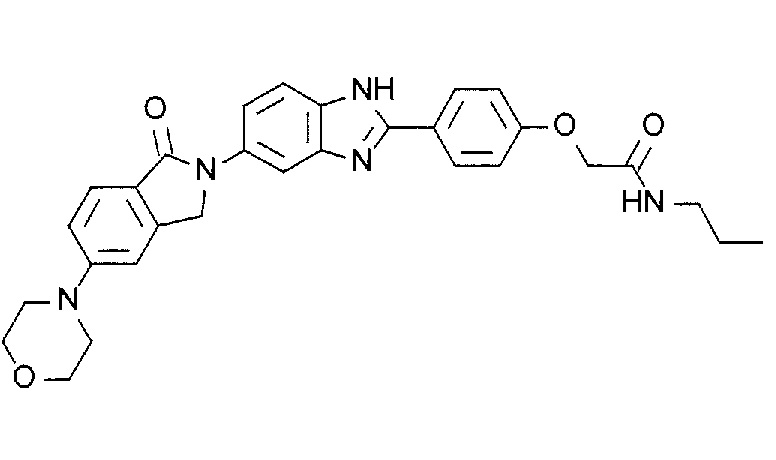
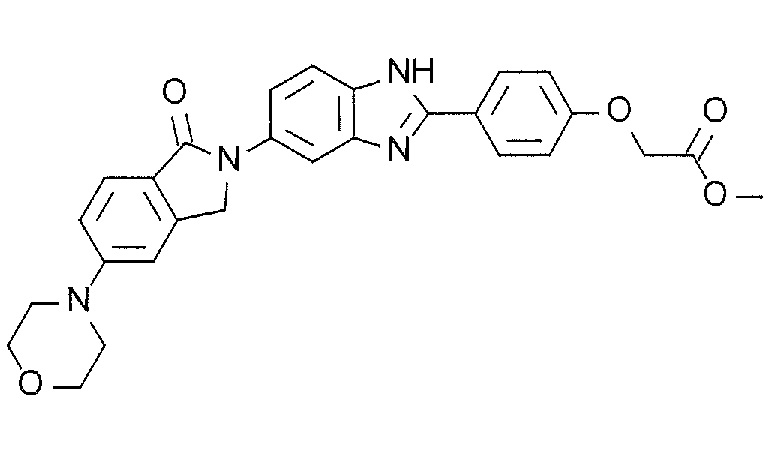
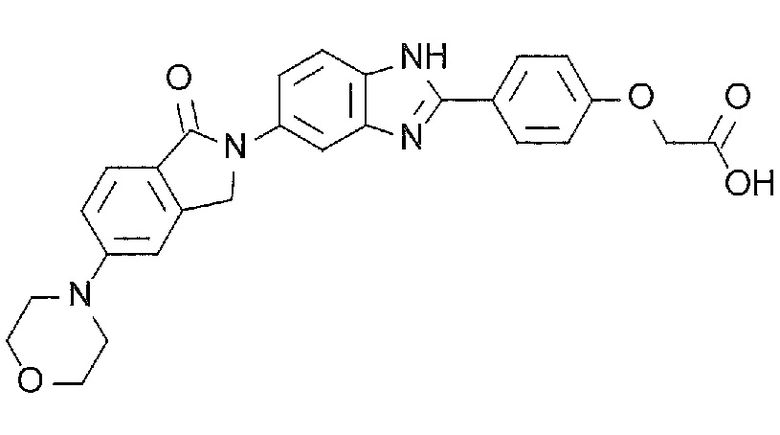
[0197]
[Таблица 1-18]
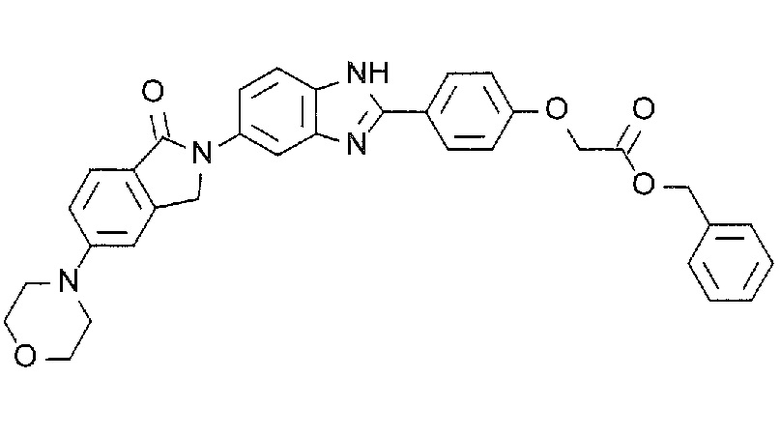
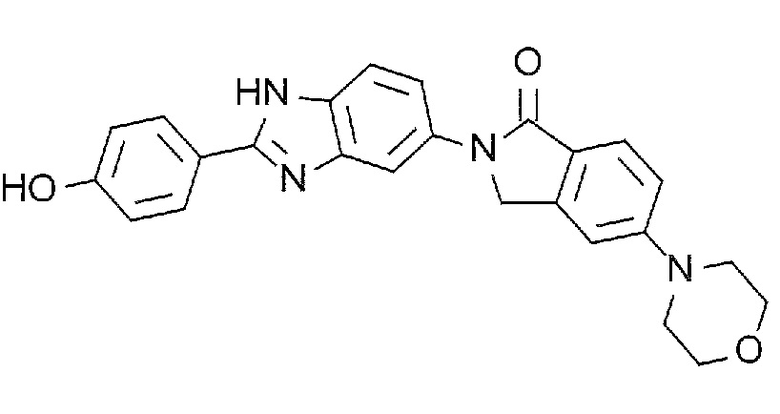
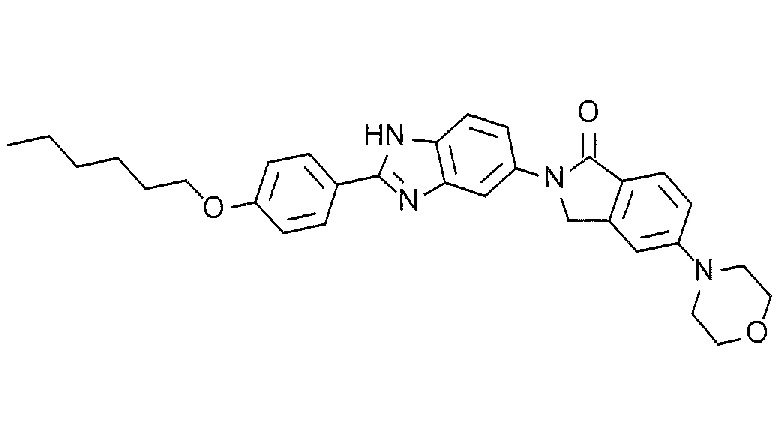
[0198]
[Таблица 1-19]
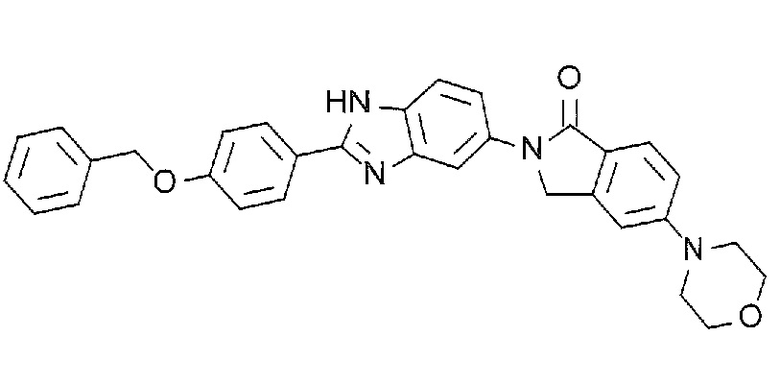
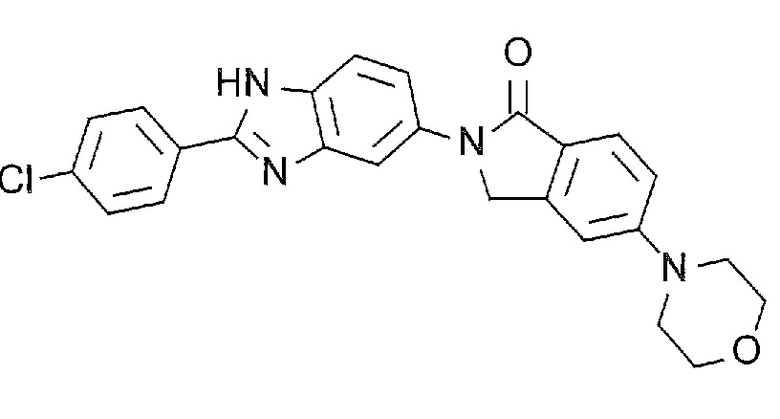
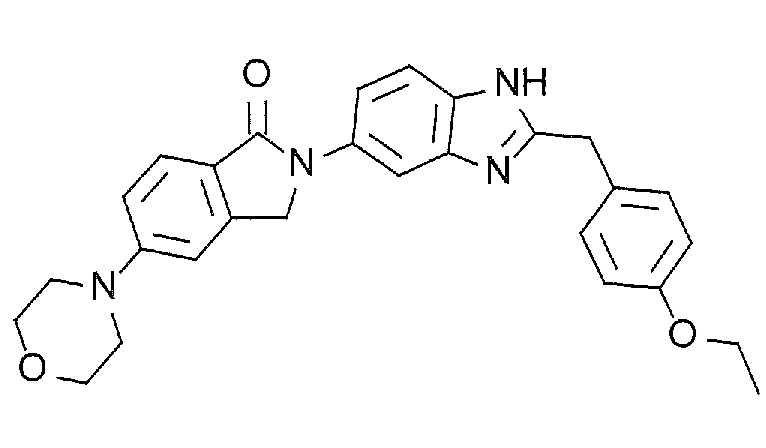
[0199]
[Таблица 1-20]
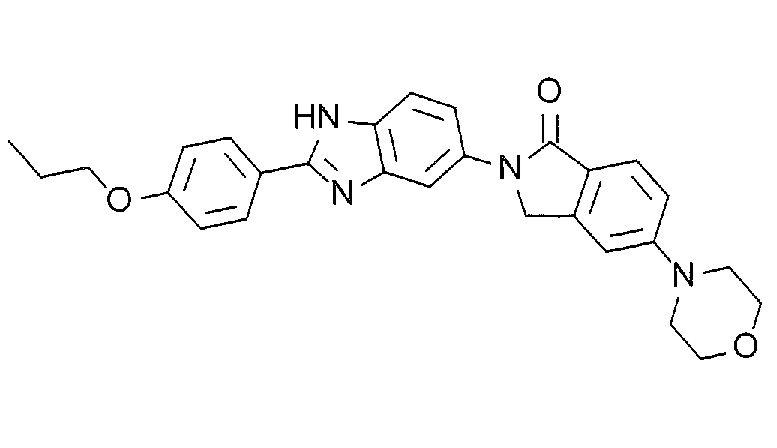
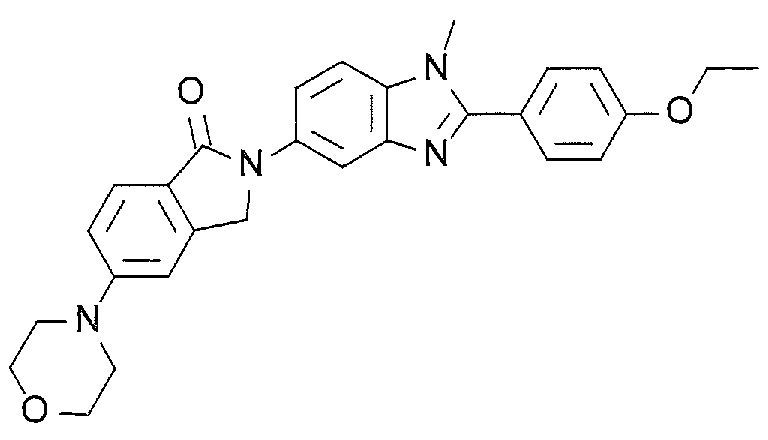
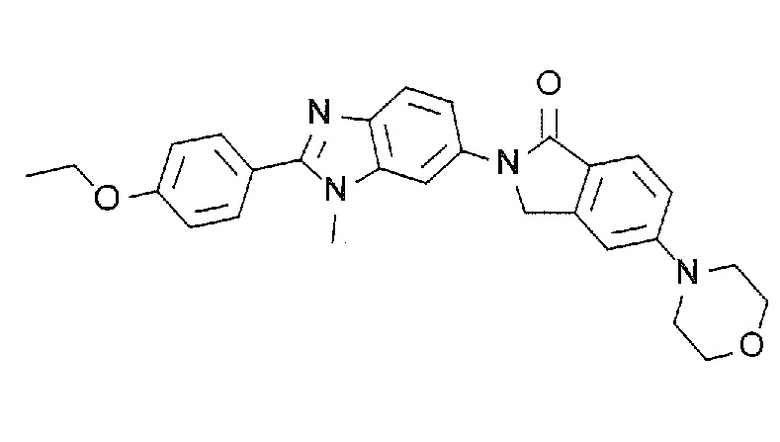
[0200]
[Таблица 1-21]
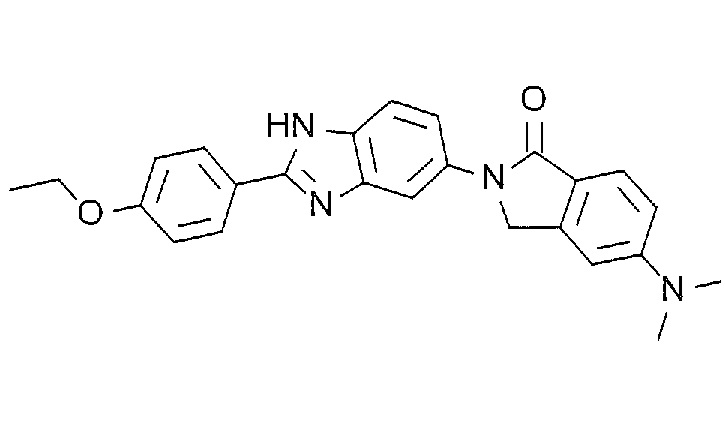
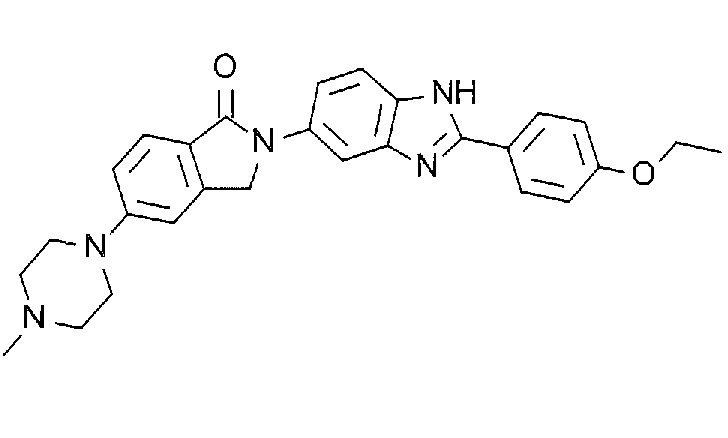
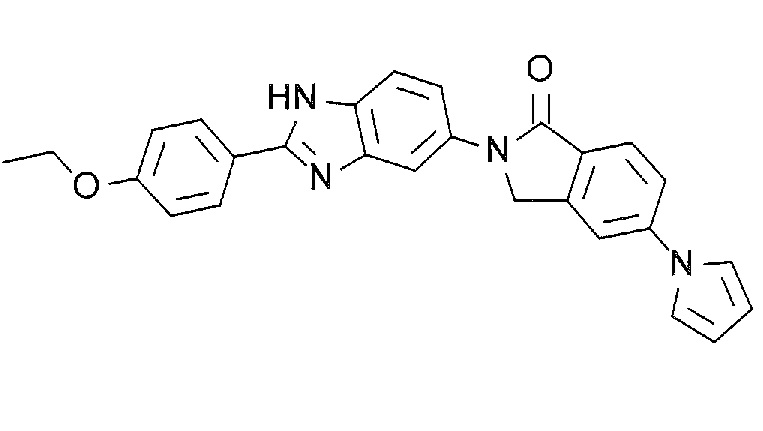
[0201]
[Таблица 1-22]
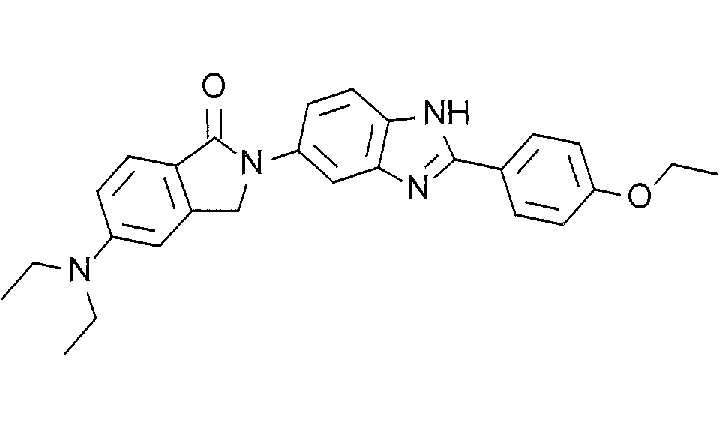
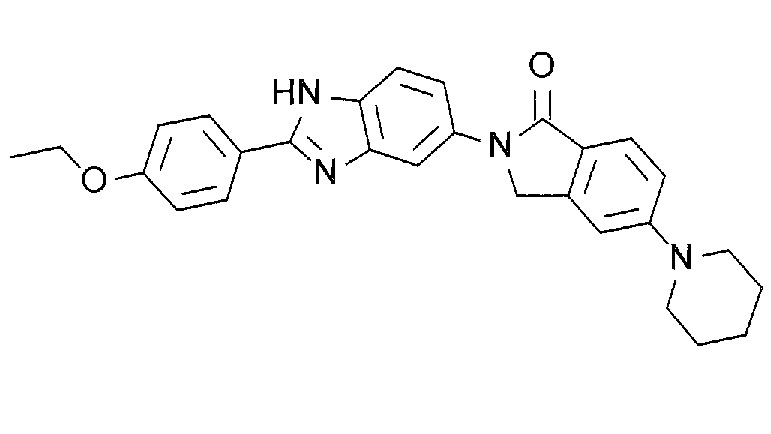
[0202]
[Таблица 1-23]
[0203]
[Таблица 1-24]
[0204]
[Таблица 1-25]
[0205]
Экспериментальный пример 1
Для обнаружения созревания кардиомиоцитов были получены линии клеток iPS человека с двойным нокаутом, в которых последовательности репортерного белка EmGFP (номер последовательности 1) и mCherry (номер последовательности 2) были вставлены в генные локусы для TNNI1 и TNNI3, соответственно (iPS-клетки человека получали из эписомного вектора (нагруженный ген; OCT3/4, KLF4, SOX2, L-MYC, LIN28, p53DD мыши) с использованием PBMC (LP_167, Sample ID:20130318) приобретенных из CTL (справочная литература; Okita K, et al. Stem Cells. 2012 Nov 29. doi: 10.1002/stem.1293)).
Поддержание культуры вышеупомянутых репортерных линий iPS-клеток осуществляли обычным способом (Okita K, et al. Stem Cells. 2012 Nov 29. doi: 10.1002/stem.1293).
[0206]
Для индукции дифференцировки в кардиомиоциты репортерные линии iPS-клеток обрабатывали 0,5×TrypLE select (Life Technologies, разбавленный 1/2 с 0,5 мМ EDTA/PBS) в течение 4-5 минут, и клетки снимали, используя скребок для клеток (IWAKI), и затем диссоциировали на отдельные клетки с помощью пипетирования. Среду удаляли центрифугированием (1000 об/мин, 5 мин), и полученные клетки высевали в биореактор (ABLE) из расчета 1×107 клеток на 30 мл биореактора, и затем культивировали в среде, полученной путем добавления 1% L-глутамина, трансферрина 150 мкг/мл, аскорбиновой кислоты 50 мкг/мл (Sigma), монотиоглицерина 4×10-4 M, 10 мкМ ингибитора Rock (Y-27632), 2 нг/мл BMP4 (R&D) и 0,5% Матригеля (со сниженным фактором роста) в среду после удаления раствора C из StemFit AK02 (AJINOMOTO AK02, 400 мл раствора A и 100 мл раствора B, всего 500 мл), при 37°C, в условиях 5% кислорода (55 об/мин, способ культивирования с перемешиванием суспензии) для образования эмбриоидных телец (0 день).
На следующий день (1-й день) 9 мкл (конечная концентрация 3 нг/мл) 10 мкг/мл активина A, 15 мкл (конечная концентрация 5 нг/мл) 10 мкг/мл bFGF и 24 мкл (конечная концентрация 10 нг/мл) 10 мкг/мл BMP4 добавляли в биореактор, и клетки культивировали при 37°C в течение дополнительных 2 дней, в условиях 5% кислорода.
Затем (3-й день), полученные эмбриоидные тельца собирали в центрифужную пробирку на 50 мл, и затем подвергали центрифугированию (200 g, 1 мин). Среду удаляли, и эмбриоидные тельца культивировали в среде, полученной путем добавления 1% L-глутамина, трансферрина 150 мкг/мл, аскорбиновой кислоты 50 мкг/мл (Sigma), монотиоглицерина 4×10-4 M, 10 нг/мл VEGF, 1 мкМ IWP-3, 0,6 мкМ дорсоморфина и 5,4 мкМ SB431542 в среду после удаления раствора C из StemFit AK02 (AJINOMOTO AK02, 400 мл раствора A и 100 мл раствора B, всего 500 мл), при 37°C, в течение 3 дней, в условиях 5% кислорода (55 об/мин, способ культивирования с перемешиванием суспензии).
Затем (6-й день) биореактор оставляли стоять для осаждения эмбриоидных телец и удаляли от 80 до 90% среды. Среду, полученную путем добавления 1% L-глутамина, трансферрина 150 мкг/мл, аскорбиновой кислоты 50 мкг/мл (Sigma), монотиоглицерина 4×10-4 M и 5 нг/мл VEGF в среду после удаления раствора C из StemFit AK02 (AJINOMOTO AK02, 400 мл раствора A и 100 мл раствора B, всего 500 мл), добавляли в биореактор так, чтобы общий объем стал 30 мл, эмбриоидные тельца культивировали в течение 8 дней при 37°C, в условиях 5% кислорода (55 об/мин, способ культивирования с перемешиванием суспензии). Во время культивирования среду заменяли средой в тех же условиях каждые 2-3 дня.
[0207]
На 14-й день после начала индукции дифференцировки эмбриоидные тельца обрабатывали 2 мг/мл коллагеназы типа I (Sigma) в течение 2 часов, а затем 0,25% трипсин/EDTA (Invitrogen) в течение 10 минут. Добавляли к смеси 50% FBS/IMDM (Thermo Fisher Science), и эмбриоидные тельца диссоциировали на отдельные клетки с помощью пипетирования, и затем подвергали центрифугированию (1000 об/мин, 5 минут). После центрифугирования супернатант удаляли, и клетки ресуспендировали в 100 мл среды AK02 на основе среды StemFit AK02 для дифференцировки кардиомиоцитов (полученной добавлением аскорбиновой кислоты 50 мкг/мл, L-глутамина 2 мМ, трансферрина 150 мг/мл, монотиоглицерина 4×10-4 M и VEGF 5 нг/мл в AJINOMOTO AK02 (400 мл раствора A и 100 мл раствора B, всего 500 мл)). Ресуспендированные клетки высевали на микропланшет CellCarrier-384 Ultra (Perkin Elmer/6057300), предварительно покрытый iMatrix-511 (приобретенный у Nippi, Inc.), в количестве 1,0×104 клеток/лунку и культивировали в среде AK02 на основе среды StemFit AK02 для дифференцировки кардиомиоцитов (полученной добавлением аскорбиновой кислоты 50 мкг/мл, L-глутамина 2 мМ, трансферрина 150 мг/мл и монотиоглицерина 4×10-4 M в AJINOMOTO AK02 (400 мл раствора A и 100 мл раствора B, всего 500 мл) по 70 мкл/лунку).
Тестируемое соединение (1 или 30 мкМ, одно соединение на лунку) добавляли в лунки по 50 мкл/лунку на 3-й и 6-й дни культивирования. На 8-й день культивирования клетки фиксировали параформальдегидом (Wako Pure Chemical Corporation, 163-20145), и подвергали иммуноокрашиванию с использованием крысиного анти-mCherry антитела (Invitrogen, M11217) в качестве первичного антитела и козьего анти-IgG крысы Alexa 647 (Invitrogen, A-21247) в качестве вторичного антитела. Уровень экспрессии Alexa 647 измеряли с помощью системы HCS (одновременный многопараметрический анализ) (Perkin Elmer/OperaPhenix High Contents Imaging System) (режим съемки; неконфокальная линза объектива; 10×air NA0.3).
Средняя интенсивность флуоресценции (среднее n=60) контрольной лунки (без добавления тестируемого соединения) составляла 797, рассчитанная из измеренных интенсивностей флуоресценции. Результаты показаны в таблице 2 (среднее n=3 (примеры 1-7, 9-59, 61-71) или n=6 (примеры 8, 60, 72 и 73)). Символ «-» в таблице 2 означает, что среднюю интенсивность флуоресценции не может быть оценена из-за уменьшения количества клеток.
[0208]
Таблица 2-1
[0209]
Таблица 2-2
[0210]
Таблица 2-3
[0211]
Экспериментальный пример 2
Для обнаружения созревания кардиомиоцитов были получены линии клеток iPS человека с двойным нокаутом, в которых последовательности репортерного белка EmGFP (номер последовательности 1) и mCherry (номер последовательности 2) были вставлены в генные локусы для TNNI1 и TNNI3, соответственно (iPS-клетки человека получали из эписомного вектора (нагруженный ген; OCT3/4, KLF4, SOX2, L-MYC, LIN28, p53DD мыши) с использованием PBMC (LP_167, Sample ID:20130318) приобретенных из CTL (справочная литература; Okita K, et al. Stem Cells. 2012 Nov 29. doi: 10.1002/stem.1293)).
Поддержание культуры вышеупомянутых репортерных линий iPS-клеток осуществляли обычным способом (Okita K, et al. Stem Cells. 2012 Nov 29. doi: 10.1002/stem.1293).
[0212]
Для индукции дифференцировки в кардиомиоциты репортерные линии iPS-клеток обрабатывали 0,5×TrypLE select (Life Technologies, разбавленный 1/2 с 0,5 мМ EDTA/PBS) в течение 4-5 минут, и клетки снимали, используя скребок для клеток (IWAKI), и затем диссоциировали на отдельные клетки с помощью пипетирования. Среду удаляли центрифугированием (1000 об/мин, 5 мин), и полученные клетки суспендировали в среде, полученной путем добавления 1% L-глутамина, трансферрина 150 мкг/мл, аскорбиновой кислоты 50 мкг/мл (Sigma), монотиоглицерина 4×10-4 M, 10 мкМ ингибитора Rock (Y-27632), 2 нг/мл BMP4 (R&D) и 0,5% Матригеля (со сниженным фактором роста) к StemPro-34 SFM (ThermoFisher) в 6-луночном планшете по 2×106 клеток/1,5 мл/лунку, и затем подвергали статическому культивированию при 37°C, в условиях 5% кислорода для образования эмбриоидных телец (0 день).
На следующий день (1-й день) среду, полученную путем добавления 1% L-глутамина, трансферрина 150 мкг/мл, аскорбиновой кислоты 50 мкг/мл (Sigma), монотиоглицерина 4×10-4 M, 1,8 мкл (концентрация 12 нг/мл) 10 мкг/мл активина A, 15 мкл (концентрация 10 нг/мл) 10 мкг/мл bFGF и 2,7 мкл (концентрация 18 нг/мл) 10 мкг/мл BMP4 к 1,5 мл StemPro-34 SFM (ThermoFisher), добавляли в каждую лунку 6-луночного планшета, содержащего эмбриоидные тельца, для доведения объема в сочетании со средой 0 дня до конечных 3 мл (активин A: 6 нг/мл, bFGF: 5 нг/мл, BMP4: 10 нг/мл), и эмбриоидные тельца культивировали при 37°C в течение дополнительных 2 дней, в условиях 5% кислорода.
Затем (3-й день), 6-луночный планшет, содержащий эмбриоидные тельца, наклоняли, и затем оставляли на 1-2 минуты до тех пор, пока эмбриоидные тельца не осаждались по краям лунок, и супернатант аспирировали, чтобы не засосать эмбриоидные тельца. Затем в каждую лунку добавляли среду IMDM (ThermoFisher), и, как указано выше, планшет наклоняли, а затем оставляли на 1-2 минуты, и супернатант аспирировали, чтобы не засосать эмбриоидные тельца. Среду, полученную путем добавления 1% L-глутамина, трансферрина 150 мкг/мл, аскорбиновой кислоты 50 мкг/мл (Sigma), монотиоглицерина 4×10-4 M, 10 нг/мл VEGF, 1 мкМ IWP-3, 0,6 мкМ дорсоморфина и 5,4 мкМ SB431542 к 3 мл StemPro-34 SFM (ThermoFisher), добавляли в каждую лунку 6-луночного планшета, и затем эмбриоидные тельца культивировали при 37°C в течение 3 дней, в условиях 5% кислорода.
Затем (6-й день), 6-луночный планшет, содержащий эмбриоидные тельца, наклоняли, и затем оставляли на 1-2 минуты до тех пор, пока эмбриоидные тельца не осаждались по краям лунок, и супернатант аспирировали, чтобы не засосать эмбриоидные тельца. Среду, полученную путем добавления 1% L-глутамина, трансферрина 150 мкг/мл, аскорбиновой кислоты 50 мкг/мл (Sigma), монотиоглицерина 4×10-4 M и 5 нг/мл VEGF к 2 мл StemPro-34 SFM (ThermoFisher), добавляли в каждую лунку 6-луночного планшета, и затем эмбриоидные тельца культивировали при 37°C в течение 2 дней, в условиях 5% кислорода.
Затем (8-й день), 6-луночный планшет, содержащий эмбриоидные тельца, наклоняли, и затем оставляли на 1-2 минуты до тех пор, пока эмбриоидные тельца не осаждались по краям лунок, и супернатант аспирировали, чтобы не засосать эмбриоидные тельца. Среду, полученную путем добавления (1) 1% L-глутамина, трансферрина 150 мкг/мл, аскорбиновой кислоты 50 мкг/мл (Sigma), монотиоглицерина 4×10-4 M и 5 нг/мл VEGF, и (2) тестируемого соединения (каждое 3 мкМ), показанного в таблице 3, или DMSO (0,1% добавление относительно объема среды) к 2 мл StemPro-34 SFM (ThermoFisher), добавляли в каждую лунку 6-луночного планшета, и затем эмбриоидные тельца культивировали при 37°C в течение 2 дней, в условиях 5% кислорода.
Затем (10-й день), 6-луночный планшет, содержащий эмбриоидные тельца, наклоняли, и затем оставляли на 1-2 минуты до тех пор, пока эмбриоидные тельца не осаждались по краям лунок, и супернатант аспирировали, чтобы не засосать эмбриоидные тельца. Среду, полученную путем добавления (1) 1% L-глутамина, трансферрина 150 мкг/мл, аскорбиновой кислоты 50 мкг/мл (Sigma), монотиоглицерина 4×10-4 M и 5 нг/мл VEGF, и (2) тестируемого соединения (каждое 3 мкМ), показанного в таблице 3, или DMSO (0,1% добавление относительно объема среды) к 3 мл StemPro-34 SFM (ThermoFisher), добавляли в каждую лунку 6-луночного планшета, и затем эмбриоидные тельца культивировали при 37°C в течение 6 дней, в условиях обычного кислорода. На 13-й день среду заменяли средой при тех же условиях.
[0213]
На 16-й день после того, как эмбриоидные тельца при каждом условии были сфотографированы с помощью флуоресцентного микроскопа, 6-луночный планшет, содержащий эмбриоидные тельца, наклоняли, и затем оставляли на 1-2 минуты до тех пор, пока эмбриоидные тельца не осаждались по краям лунок, и супернатант аспирировали, чтобы не засосать эмбриоидные тельца. Затем в каждую лунку добавляли 2 мл PBS, и, как указано выше, планшет наклоняли, и затем оставляли на 1-2 минуты, и PBS аспирировали, чтобы не засосать эмбриоидные тельца. В каждую лунку добавляли раствор, полученный путем добавления ДНКазы 10 мкг/мл и либеразы 100 мкг/мл к 3 мл IMDM, и планшет оставляли стоять при 37°C в течение 1 часа, в условиях обычного кислорода. Через 1 час планшет наклоняли, и затем оставляли на 1-2 минуты до тех пор, пока эмбриоидные тельца не осаждались по краям лунок, и супернатант аспирировали, чтобы не засосать эмбриоидные тельца. Затем в каждую лунку добавляли 2 мл PBS, и, как указано выше, планшет наклоняли, и затем оставляли на 1-2 минуты, и PBS аспирировали, чтобы не засосать эмбриоидные тельца. Раствор, полученный путем добавления ДНКазы 10 мкг/мл к 2 мл TrypLE select, добавляли в каждую лунку, и планшет оставляли стоять при 37°C в течение 10 минут, в условиях обычного кислорода. Затем среду, полученную путем добавления 1% L-глутамина, трансферрина 150 мкг/мл, аскорбиновой кислоты 50 мкг/мл (Sigma), монотиоглицерина 4×10-4 M, 5 нг/мл VEGF и ДНКазы 10 мкг/мл к 2 мл StemPro-34 SFM (ThermoFisher), добавляли в каждую лунку, и эмбриоидные тельца диссоциировали на отдельные клетки с помощью пипетирования, и затем подвергали центрифугированию (1000 об/мин, 5 минут). После центрифугирования супернатант удаляли, клетки суспендировали в 1-2 мл 2% FBS/PBS, и экспрессию mCherry в клетках TNNI1+ анализировали с помощью проточной цитометрии (BD FACSAria Fusion, клеточный сортер). Результаты представлены в таблице 3 и на фиг. 1-7.
[0214]
Таблица 3

[0215]
Экспериментальный пример 3
Для обнаружения созревания кардиомиоцитов были получены линии клеток iPS человека с двойным нокаутом, в которых последовательности репортерного белка EmGFP (номер последовательности 1) и mCherry (номер последовательности 2) были вставлены в генные локусы для TNNI1 и TNNI3, соответственно (iPS-клетки человека получали из эписомного вектора (нагруженный ген; OCT3/4, KLF4, SOX2, L-MYC, LIN28, p53DD мыши) с использованием PBMC (LP_167, Sample ID:20130318), приобретенных из CTL (справочная литература; Okita K, et al. Stem Cells. 2012 Nov 29. doi: 10.1002/stem.1293)).
Поддержание культуры вышеупомянутых репортерных линий iPS-клеток осуществляли обычным способом (Okita K, et al. Stem Cells. 2012 Nov 29. doi: 10.1002/stem.1293).
[0216]
Для индукции дифференцировки в кардиомиоциты репортерные линии iPS-клеток обрабатывали 0,5×TrypLE select (Life Technologies, разбавленный 1/2 с 0,5 мМ EDTA/PBS) в течение 4-5 минут, и клетки снимали, используя скребок для клеток (IWAKI), и затем диссоциировали на отдельные клетки с помощью пипетирования. Среду удаляли центрифугированием (1000 об/мин, 5 мин), и полученные клетки суспендировали в среде, полученной путем добавления 1% L-глутамина, трансферрина 150 мкг/мл, аскорбиновой кислоты 50 мкг/мл (Sigma), монотиоглицерина 4×10-4 M, 10 мкМ ингибитора Rock (Y-27632), 2 нг/мл BMP4 (R&D) и 0,5% Матригеля (со сниженным фактором роста) в StemPro-34 SFM (ThermoFisher) в 6-луночном планшете по 2×106 клеток/1,5 мл/лунку, и затем подвергали статическому культивированию при 37°C, в условиях 5% кислорода для образования эмбриоидных телец (0 день).
На следующий день (1-й день) среду, полученную путем добавления 1% L-глутамина, трансферрина 150 мкг/мл, аскорбиновой кислоты 50 мкг/мл (Sigma), монотиоглицерина 4×10-4 M, 1,8 мкл (концентрация 12 нг/мл) 10 мкг/мл активина A, 15 мкл (концентрация 10 нг/мл) 10 мкг/мл bFGF и 2,7 мкл (концентрация 18 нг/мл) 10 мкг/мл BMP4 к 1,5 мл StemPro-34 SFM (ThermoFisher), добавляли в каждую лунку 6-луночного планшета, содержащего эмбриоидные тельца, для доведения объема в сочетании со средой 0 дня до конечных 3 мл (активин A: 6 нг/мл, bFGF: 5 нг/мл, BMP4: 10 нг/мл), и эмбриоидные тельца культивировали при 37°C в течение дополнительных 2 дней, в условиях 5% кислорода.
Затем (3-й день), 6-луночный планшет, содержащий эмбриоидные тельца, наклоняли, и затем оставляли на 1-2 минуты до тех пор, пока эмбриоидные тельца не осаждались по краям лунок, и супернатант аспирировали, чтобы не засосать эмбриоидные тельца. Затем в каждую лунку добавляли среду IMDM (ThermoFisher), и, как указано выше, планшет наклоняли, а затем оставляли на 1-2 минуты, и супернатант аспирировали, чтобы не засосать эмбриоидные тельца. Среду, полученную путем добавления 1% L-глутамина, трансферрина 150 мкг/мл, аскорбиновой кислоты 50 мкг/мл (Sigma), монотиоглицерина 4×10-4 M, 10 нг/мл VEGF, 1 мкМ IWP-3, 0,6 мкМ дорсоморфина и 5,4 мкМ SB431542 к 3 мл StemPro-34 SFM (ThermoFisher), добавляли в каждую лунку 6-луночного планшета, и затем эмбриоидные тельца культивировали при 37°C в течение 3 дней, в условиях 5% кислорода.
Затем (6-й день), 6-луночный планшет, содержащий эмбриоидные тельца, наклоняли, и затем оставляли на 1-2 минуты до тех пор, пока эмбриоидные тельца не осаждались по краям лунок, и супернатант аспирировали, чтобы не засосать эмбриоидные тельца. Среду, полученную путем добавления 1% L-глутамина, трансферрина 150 мкг/мл, аскорбиновой кислоты 50 мкг/мл (Sigma), монотиоглицерина 4×10-4 M и 5 нг/мл VEGF к 2 мл StemPro-34 SFM (ThermoFisher), добавляли в каждую лунку 6-луночного планшета, и затем эмбриоидные тельца культивировали при 37°C в течение 2 дней, в условиях 5% кислорода.
Затем (8-й день), 6-луночный планшет, содержащий эмбриоидные тельца, наклоняли, и затем оставляли на 1-2 минуты до тех пор, пока эмбриоидные тельца не осаждались по краям лунок, и супернатант аспирировали, чтобы не засосать эмбриоидные тельца. Среду, полученную путем добавления (1) 1% L-глутамина, трансферрина 150 мкг/мл, аскорбиновой кислоты 50 мкг/мл (Sigma), монотиоглицерина 4×10-4 M и 5 нг/мл VEGF, и (2) соединения Примера 8 (3 мкМ) или DMSO (0,1% добавление относительно объема среды) к 2 мл StemPro-34 SFM (ThermoFisher), добавляли в каждую лунку 6-луночного планшета, и затем эмбриоидные тельца культивировали при 37°C в течение 2 дней, в условиях 5% кислорода.
На 10-й день среду заменяли средой, полученной путем добавления (1) 1% L-глутамина, трансферрина 150 мкг/мл, аскорбиновой кислоты 50 мкг/мл (Sigma), монотиоглицерина 4×10-4 M и 5 нг/мл VEGF, и (2) соединения A (40 нМ, структура показана ниже), или смеси соединения Примера 8 (3 мкМ) и соединения A (40 нМ), или DMSO (0,1% добавление относительно объема среды) к 2 мл StemPro-34 SFM (ThermoFisher), и затем эмбриоидные тельца культивировали при 37°C в течение 6 дней, в условиях обычного кислорода. На 13-й день среду заменяли средой при тех же условиях.
[0217]
На 16-й день после того, как эмбриоидные тельца при каждом условии были сфотографированы с помощью флуоресцентного микроскопа, 6-луночный планшет, содержащий эмбриоидные тельца, наклоняли, и затем оставляли на 1-2 минуты до тех пор, пока эмбриоидные тельца не осаждались по краям лунок, и супернатант аспирировали, чтобы не засосать эмбриоидные тельца. Затем в каждую лунку добавляли 2 мл PBS, и, как указано выше, планшет наклоняли, и затем оставляли на 1-2 минуты, и PBS аспирировали, чтобы не засосать эмбриоидные тельца. В каждую лунку добавляли раствор, полученный путем добавления ДНКазы 10 мкг/мл и либеразы 100 мкг/мл к 3 мл IMDM, и планшет оставляли стоять при 37°C в течение 1 часа, в условиях обычного кислорода. Через 1 час планшет наклоняли, и затем оставляли на 1-2 минуты до тех пор, пока эмбриоидные тельца не осаждались по краям лунок, и супернатант аспирировали, чтобы не засосать эмбриоидные тельца. Затем в каждую лунку добавляли 2 мл PBS, и, как указано выше, планшет наклоняли, и затем оставляли на 1-2 минуты, и PBS аспирировали, чтобы не засосать эмбриоидные тельца. Раствор, полученный путем добавления ДНКазы 10 мкг/мл к 2 мл TrypLE select, добавляли в каждую лунку, и планшет оставляли стоять при 37°C в течение 10 минут, в условиях обычного кислорода. Затем, среду, полученную путем добавления 1% L-глутамина, трансферрина 150 мкг/мл, аскорбиновой кислоты 50 мкг/мл (Sigma), монотиоглицерина 4×10-4 M, 5 нг/мл VEGF и ДНКазы 10 мкг/мл к 2 мл StemPro-34 SFM (ThermoFisher), добавляли в каждую лунку, и эмбриоидные тельца диссоциировали на отдельные клетки с помощью пипетирования, и затем подвергали центрифугированию (1000 об/мин, 5 минут). После центрифугирования супернатант удаляли, клетки суспендировали в 1-2 мл 2% FBS/PBS, и экспрессию mCherry в клетках TNNI1+ анализировали с помощью проточной цитометрии (BD FACSAria Fusion, клеточный сортер). Результаты представлены в таблице 4 и на фиг. 8.
[0218]
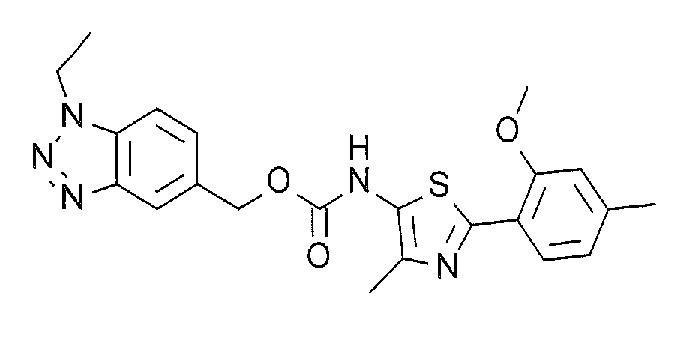
[0219]
Таблица 4

[0220]
Экспериментальный пример 4
Для анализа электрофизиологической функции кардиомиоцитов использовали клеточные линии iPS 409B2 (полученные из эписомного вектора (pCXLE-hOCT3/4-shp53-F, pCXLE-hSK, pCXLE-hUL) с использованием HDF1388, приобретенного у Cell Applications, Inc (справочная литература; Okita et al., Nat Methods. 8(5):409-12.(2011))).
Поддержание культуры вышеупомянутых клеточных линий iPS осуществляли обычным способом (Takahashi K, et al. Cell. 131: 861-72, 2007 and Nakagawa M, et al. Nat Biotechnol. 26: 101-6, 2008).
[0221]
Для индукции дифференцировки в кардиомиоциты клеточные линии iPS обрабатывали раствором CTK (ReproCELL) в течение 2 минут, раствор удаляли, и затем клеточные линии iPS обрабатывали Accumax (инновационные клеточные технологии) в течение 5 минут, и клетки диссоциировали на отдельные клетки с помощью пипетирования. Клетки собирали центрифугированием (1000 об/мин, 5 мин), и высевали на 96-луночный планшет с низким прикреплением (Corning) 5000 клеток/70 мкл/лунку, и культивировали в среде, полученной путем добавления 1% L-глутамина, трансферрина 150 мкг/мл, аскорбиновой кислоты 50 мкг/мл (Sigma), монотиоглицерина 4×10-4 M, 10 мкМ ингибитора Rock (Y-27632), 2 нг/мл BMP4 (R&D) и 0,5% Матригеля (со сниженным фактором роста) в StemPro-34 SFM (ThermoFisher), при 37°C, в условиях 5% кислорода для образования эмбриоидных телец (0 день).
На следующий день (1-й день) среду (70 мкл), полученную путем добавления 1% L-глутамина, трансферрина 150 мкг/мл, аскорбиновой кислоты 50 мкг/мл (Sigma), монотиоглицерина 4×10-4 M, 12 нг/мл активин A, 10 нг/мл bFGF и 18 нг/мл BMP4 к StemPro-34 SFM (ThermoFisher), добавляли в каждую лунку 96-луночного планшета, содержащего эмбриоидные тельца, для доведения объема в сочетании со средой 0 дня до конечных 140 мкл, и эмбриоидные тельца культивировали при 37°C в течение дополнительных 2 дней, в условиях 5% кислорода.
Затем (3-й день) полученные эмбриоидные тельца собирали, среду удаляли центрифугированием (1000 об/мин, 3 мин), и добавляли Accumax (инновационные клеточные технологии). Через 5 минут, эмбриоидные тельца диссоциировали на отдельные клетки с помощью пипетирования, добавляли IMDM (5 мл, invitrogen), и среду удаляли центрифугированием (1000 об/мин, 5 мин). Клетки высевали на 96-луночный планшет с низким прикреплением (Corning) по 10000 клеток/100 мкл/лунку, и культивировали в среде, полученной путем добавления 1% L-глутамина, трансферрина 150 мкг/мл, аскорбиновой кислоты 50 мкг/мл (Sigma), монотиоглицерина 4×10-4 M, 10 нг/мл VEGF и 1 мкМ IWP-3 в StemPro-34 SFM (ThermoFisher), при 37°C, в течение 3 дней, в условиях 5% кислорода.
Затем (6-й день), полученные эмбриоидные тельца собирали, и помещали в 6-луночный планшет с низким прикреплением, чтобы не превышать 60 EB на лунку. 6-луночный планшет, содержащий эмбриоидные тельца, наклоняли, и затем оставляли на 1-2 минуты до тех пор, пока эмбриоидные тельца не осаждались по краям лунок, и супернатант аспирировали, чтобы не засосать эмбриоидные тельца. Среду, полученную путем добавления 1% L-глутамина, трансферрина 150 мкг/мл, аскорбиновой кислоты 50 мкг/мл (Sigma), монотиоглицерина 4×10-4 M и 5 нг/мл VEGF к 2 мл StemPro-34 SFM (ThermoFisher), добавляли в каждую лунку 6-луночного планшета, и затем эмбриоидные тельца культивировали при 37°C в течение 4 дней, в условиях 5% кислорода. На 8-й день среду заменяли средой при тех же условиях.
Затем (10-й день), 6-луночный планшет, содержащий эмбриоидные тельца, наклоняли, и затем оставляли на 1-2 минуты до тех пор, пока эмбриоидные тельца не осаждались по краям лунок, и супернатант аспирировали, чтобы не засосать эмбриоидные тельца. Среду, полученную путем добавления 1% L-глутамина, трансферрина 150 мкг/мл, аскорбиновой кислоты 50 мкг/мл (Sigma), монотиоглицерина 4×10-4 M и 5 нг/мл VEGF к 2 мл StemPro-34 SFM (ThermoFisher), добавляли в каждую лунку 6-луночного планшета, и затем эмбриоидные тельца культивировали при 37°C в течение 10 дней, в условиях обычного кислорода. Во время культивирования среду заменяли средой в тех же условиях каждые 2-3 дня.
Затем (20-й день), 6-луночный планшет, содержащий эмбриоидные тельца, наклоняли, и затем оставляли на 1-2 минуты до тех пор, пока эмбриоидные тельца не осаждались по краям лунок, и супернатант аспирировали, чтобы не засосать эмбриоидные тельца. Затем в каждую лунку добавляли 2 мл PBS, и, как указано выше, планшет наклоняли, и затем оставляли на 1-2 минуты, и PBS аспирировали, чтобы не засосать эмбриоидные тельца. В каждую лунку добавляли раствор, полученный путем добавления ДНКазы 10 мкг/мл и либеразы 100 мкг/мл к 3 мл IMDM, и затем эмбриоидные тельца оставляли стоять при 37°C в течение 1 часа, в условиях обычного кислорода. Через 1 час планшет наклоняли, и затем оставляли на 1-2 минуты до тех пор, пока эмбриоидные тельца не осаждались по краям лунок, и супернатант аспирировали, чтобы не засосать эмбриоидные тельца. Затем в каждую лунку добавляли 2 мл PBS, и, как указано выше, планшет наклоняли, и затем оставляли на 1-2 минуты, и PBS аспирировали, чтобы не засосать эмбриоидные тельца. Раствор, полученный путем добавления ДНКазы 10 мкг/мл к 2 мл TrypLE select, добавляли в каждую лунку, и затем эмбриоидные тельца оставляли стоять при 37°C в течение 10 минут, в условиях обычного кислорода. Затем, среду, полученную путем добавления 1% L-глутамина, трансферрина 150 мкг/мл, аскорбиновой кислоты 50 мкг/мл (Sigma), монотиоглицерина 4×10-4 M, 5 нг/мл VEGF и ДНКазы 10 мкг/мл к 2 мл StemPro-34 SFM (ThermoFisher), добавляли в каждую лунку, и эмбриоидные тельца диссоциировали на отдельные клетки с помощью пипетирования. Клетки подвергали центрифугированию (1000 об/мин, 5 мин). После центрифугирования супернатант удаляли, и клетки суспендировали в 1-2 мл 2% FBS/PBS, и окрашивали SIRPa и Lineage (CD31, CD49a, CD90, CD140b) антителом, и группу SIRPa+Lin-клеток собирали проточной цитометрией (клеточный сортер BD FACSAria Fusion) (см., Dubois NC, et al. Nat Biotechnol. 29: 1011-8, 2011). Собранные клетки подвергали центрифугированию (1000 об/мин, 5 мин), суспендировали в среде, полученной путем добавления 1% L-глутамина, трансферрина 150 мкг/мл, аскорбиновой кислоты 50 мкг/мл (Sigma), монотиоглицерина 4×10-4 M и 5 нг/мл VEGF в StemPro-34 SFM (ThermoFisher), и высевали в чашку со стеклянным дном, предварительно покрытую фибронектином, в количестве 5×104 клеток/5 мкл, и чашку оставляли на 2-3 ч при 37°C, в условиях обычного кислорода. Затем, среду, полученную путем добавления 1% L-глутамина, трансферрина 150 мкг/мл, аскорбиновой кислоты 50 мкг/мл (Sigma), монотиоглицерина 4×10-4 M и 5 нг/мл VEGF к 2 мл StemPro-34 SFM (ThermoFisher), добавляли в чашку и клетки культивировали при 37°C в течение 5 дней, в условиях обычного кислорода. Во время культивирования среду заменяли средой в тех же условиях каждые 2-3 дня.
[0222]
На 25-й день среду удаляли из чашки и заменяли средой, содержащей тестируемое соединение I (соединение Примера 8, 30 мкМ), тестируемое соединение II (смесь соединения Примера 8 (30 мкМ) и соединения A (40 нМ)) или DMSO (конечная концентрация 0,1%) в качестве контроля (среду получали добавлением 1% L-глутамина, трансферрина 150 мкг/мл, аскорбиновой кислоты 50 мкг/мл (Sigma), монотиоглицерина 4×10-4 M и 5 нг/мл VEGF в StemPro-34 SFM (ThermoFisher)). Клетки культивировали при 37°C в течение 4 дней, в условиях обычного кислорода, и на 28 день клетки подвергали анализу мембранного потенциала.
Среду удаляли из чашки, содержащей клетки, на 28-й день, и раствор, полученный путем добавления 0,2 мкл красителя мембранного потенциала FluoVoltTM (Invitrogen, F10488) к 200 мкл светлого сбалансированного солевого раствора (Sigma), добавляли по каплям в стеклянную часть чашки, и клетки инкубировали при 37°C в течение 15 мин, в условиях обычного кислорода. После инкубации раствор, содержащий краситель мембранного потенциала, удаляли, в чашку добавляли 1 мл светлого сбалансированного солевого раствора, и клетки инкубировали в инкубаторе на предметном столике микроскопа (37°C, общий кислород) в течение 1 часа. После инкубации клетки подвергали флуоресцентной реакции в течение 30 секунд каждые 5,9 миллисекунды с возбуждающим светом 490 нм с использованием AquaCosmos 2.6 (Hamamatsu Photonics K.K). Диапазон измерения (ROI) устанавливали на 512×64 пикселей, и три ROI были измерены на чашку. Результаты представлены в таблице 5.
[0223]
Таблица 5
ударов в минуту (каждая группа n=3, среднее ± стандартное отклонение)
Промышленная применимость
[0224]
Поскольку соединение (I) обладает активностью, способствующей созреванию кардиомиоцитов, оно полезно в качестве промотора созревания кардиомиоцитов.
[0225]
Настоящая заявка основана на заявке на патент No. 2018-69872, поданной 30 марта 2018 г. в Японии, содержание которой полностью включено в настоящий документ.
--->
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> Kyoto University
Takeda Pharmaceutical Company Limited
<120> ГЕТЕРОЦИКЛИЧЕСКОЕ СОЕДИНЕНИЕ
<130> 092884
<150> JP2018-069872
<151> 2018-3-30
<160> 2
<170> PatentIn version 3.5
<210> 1
<211> 720
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Изумрудно-зеленый флуоресцентный белок (EmGFP)
<400> 1
atggtgagca agggcgagga gctgttcacc ggggtggtgc ccatcctggt cgagctggac 60
ggcgacgtaa acggccacaa gttcagcgtg tccggcgagg gcgagggcga tgccacctac 120
ggcaagctga ccctgaagtt catctgcacc accggcaagc tgcccgtgcc ctggcccacc 180
ctcgtgacca ccttcaccta cggcgtgcag tgcttcgccc gctaccccga ccacatgaag 240
cagcacgact tcttcaagtc cgccatgccc gaaggctacg tccaggagcg caccatcttc 300
ttcaaggacg acggcaacta caagacccgc gccgaggtga agttcgaggg cgacaccctg 360
gtgaaccgca tcgagctgaa gggcatcgac ttcaaggagg acggcaacat cctggggcac 420
aagctggagt acaactacaa cagccacaag gtctatatca ccgccgacaa gcagaagaac 480
ggcatcaagg tgaacttcaa gacccgccac aacatcgagg acggcagcgt gcagctcgcc 540
gaccactacc agcagaacac ccccatcggc gacggccccg tgctgctgcc cgacaaccac 600
tacctgagca cccagtccgc cctgagcaaa gaccccaacg agaagcgcga tcacatggtc 660
ctgctggagt tcgtgaccgc cgccgggatc actctcggca tggacgagct gtacaagtaa 720
<210> 2
<211> 711
<212> ДНК
<213> Искусственная последовательность
<220>
<223> mCherry
<400> 2
atggtgagca agggcgagga ggataacatg gccatcatca aggagttcat gcgcttcaag 60
gtgcacatgg agggctccgt gaacggccac gagttcgaga tcgagggcga gggcgagggc 120
cgcccctacg agggcaccca gaccgccaag ctgaaggtga ccaagggtgg ccccctgccc 180
ttcgcctggg acatcctgtc ccctcagttc atgtacggct ccaaggccta cgtgaagcac 240
cccgccgaca tccccgacta cttgaagctg tccttccccg agggcttcaa gtgggagcgc 300
gtgatgaact tcgaggacgg cggcgtggtg accgtgaccc aggactcctc cctgcaggac 360
ggcgagttca tctacaaggt gaagctgcgc ggcaccaact tcccctccga cggccccgta 420
atgcagaaga agaccatggg ctgggaggcc tcctccgagc ggatgtaccc cgaggacggc 480
gccctgaagg gcgagatcaa gcagaggctg aagctgaagg acggcggcca ctacgacgct 540
gaggtcaaga ccacctacaa ggccaagaag cccgtgcagc tgcccggcgc ctacaacgtc 600
aacatcaagt tggacatcac ctcccacaac gaggactaca ccatcgtgga acagtacgaa 660
cgcgccgagg gccgccactc caccggcggc atggacgagc tgtacaagta g 711
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| ГЕТЕРОЦИКЛИЧЕСКОЕ СОЕДИНЕНИЕ | 2019 |
|
RU2806347C2 |
| ГЕТЕРОЦИКЛИЧЕСКОЕ СОЕДИНЕНИЕ | 2018 |
|
RU2791533C2 |
| СРЕДСТВО ДЛЯ ПРОФИЛАКТИКИ ИЛИ ЛЕЧЕНИЯ НЕВРОПАТИИ | 2003 |
|
RU2337682C2 |
| АНАЛОГИ НОЦИЦЕПТИНА | 2002 |
|
RU2426730C2 |
| ПРОИЗВОДНЫЕ БЕНЗИМИДАЗОЛА И ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ НА ИХ ОСНОВЕ | 2002 |
|
RU2265018C2 |
| 2,5-ЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ ОКСАЗОЛОПИРИМИДИНА | 2011 |
|
RU2554874C2 |
| (ГЕТЕРО)АРИЛЦИКЛОПРОПИЛАМИНЫ В КАЧЕСТВЕ ИНГИБИТОРОВ LSD1 | 2012 |
|
RU2681211C2 |
| ГЕТЕРОЦИКЛИЧЕСКОЕ СОЕДИНЕНИЕ | 2018 |
|
RU2768473C2 |
| ГЕТЕРОЦИКЛИЧЕСКОЕ СОЕДИНЕНИЕ | 2018 |
|
RU2773441C2 |
| ИНГИБИТОР РОСТА | 2019 |
|
RU2825665C2 |
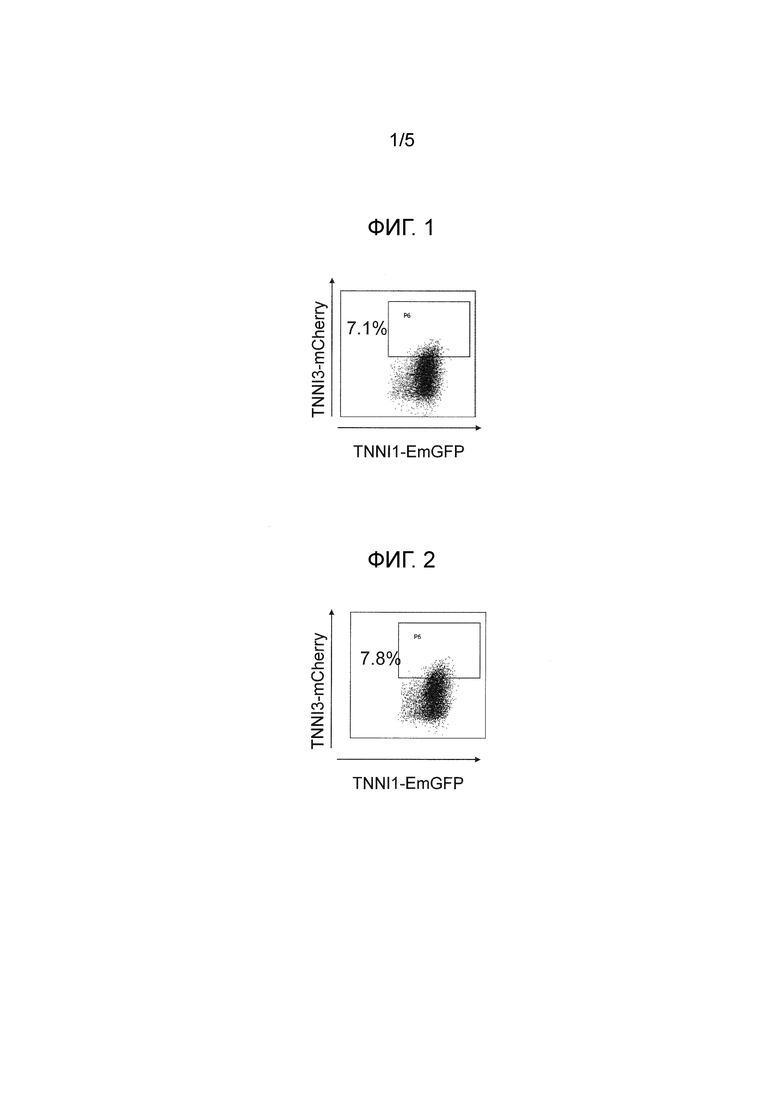
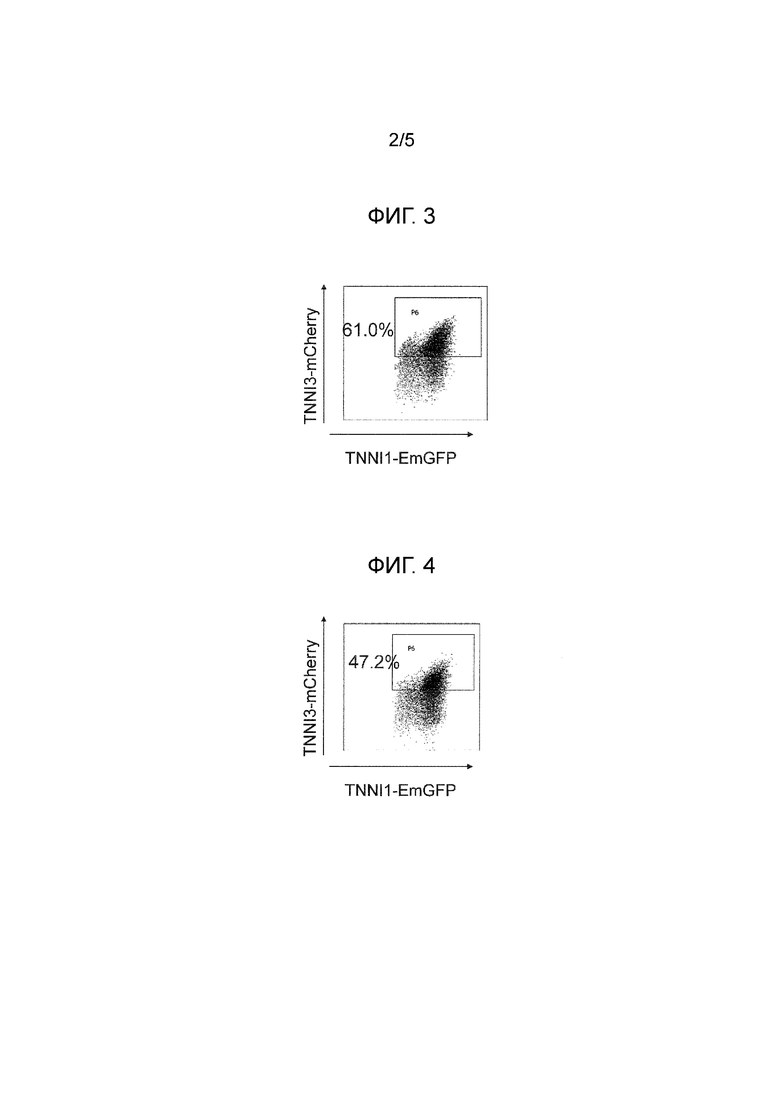
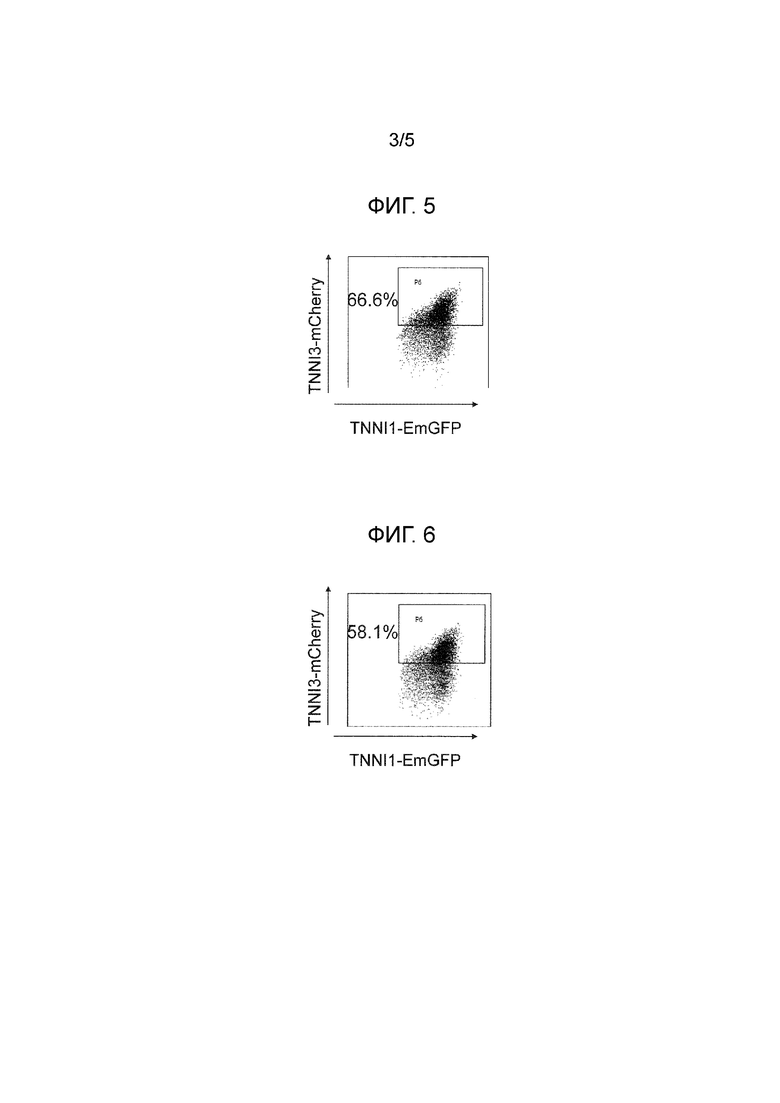
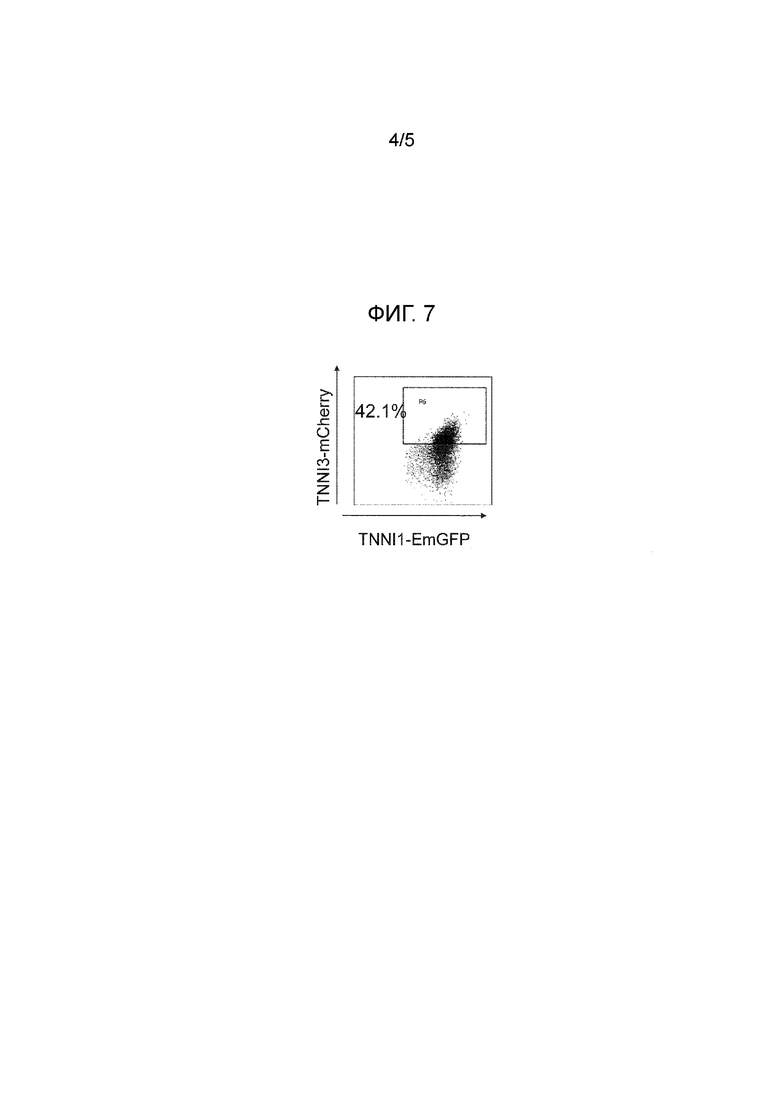
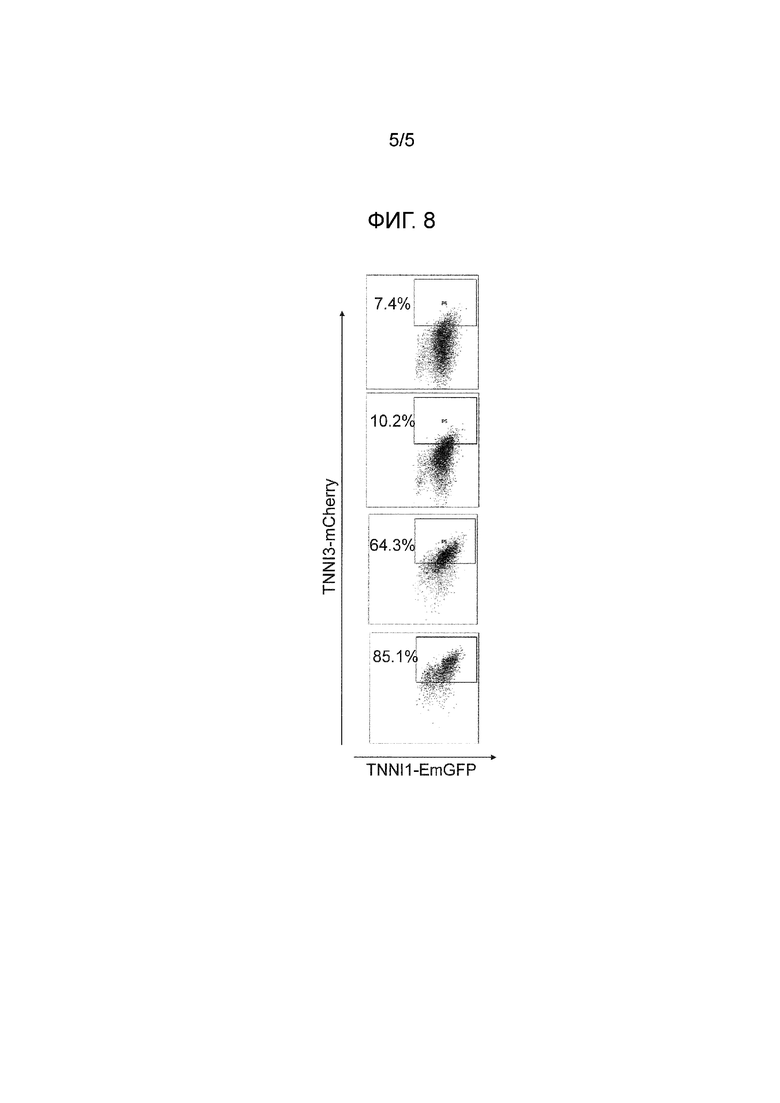
Изобретение относится к соединению формулы (I) или его фармакологически приемлемой соли, где кольцо A представляет собой бензольное кольцо; кольцо В представляет собой бензольное кольцо; кольцо C представляет собой имидазольное кольцо, необязательно дополнительно замещенное C1-6 алкильной группой; L представляет собой связь или метиленовую группу; R1 представляет собой (1) атом водорода, (2) атом галогена, (3) ди-C1-6 алкиламиногруппу, (4) пирролил, или (5) пиперидил, пиперазинил, необязательно замещенный одной C1-6 алкильной группой, или морфолинил; и кольцо D представляет собой (1) бензольное кольцо, необязательно дополнительно замещенное 1-3 заместителями, выбранными из (a) атома галогена, (b) гидроксигруппы, (c) C1-6 алкильной группы, необязательно замещенной 1 C1-6 алкоксигруппой, (d) C1-6 алкоксигруппы, необязательно замещенной 1 заместителем, выбранным из (i) карбоксигруппы, (ii) C1-6 алкоксикарбонильной группы, (iii) бензилоксикарбонильной группы, (iv) карбамоильной группы, необязательно моно- или дизамещенной заместителем(ями), выбранным из (I) C1-6 алкильной группы, необязательно замещенной 1-3 заместителями, выбранными из (A) циклопропила, (B) фенила, (C) фениламино, необязательно замещенного 1-3 атомами галогена, (D) пиридила, (E) тетрагидропиранила, и (F) карбамоильной группы, необязательно моно- или дизамещенной заместителем(ями), выбранным из C1-6 алкильной группы и 2-фенилэтила, (II) C2-6 алкенильной группы, необязательно замещенной одним фенилом, (III) C3-10 циклоалкильной группы, необязательно замещенной 1 C1-6 алкильной группой, (IV) фенильной группы, необязательно замещенной 1 заместителем, выбранным из (A) атома галогена, и (B) C1-6 алкильной группы, (V) бензила, (VI) пиридила, и (VII) тетрагидропиранила или 1,1-диоксидигидробензотиенила, и (v) пирролидинилкарбонила, морфолинилкарбонила, 1,1-диоксидотиазолидинилкарбонила или пиперидилкарбонила, необязательно замещенного 1 или 2 заместителями, выбранными из (I) гидроксигруппы и (II) C1-6 алкильной группы, и (е) бензилокси, (2) циклогексановое кольцо, (3) пиридиновое кольцо, (4) изоксазольное кольцо, (5) тиофеновое кольцо, (6) пиперидиновое кольцо, необязательно дополнительно замещенное 1-3 C1-6 алкоксикарбонильными группами, или (7) тетрагидропирановое кольцо. Технический результат – получены новые соединения, которые могут найти применение в качестве промотора созревания кардиомиоцитов. 8 н. и 2 з.п. ф-лы, 8 ил., 5 табл., 73 пр.
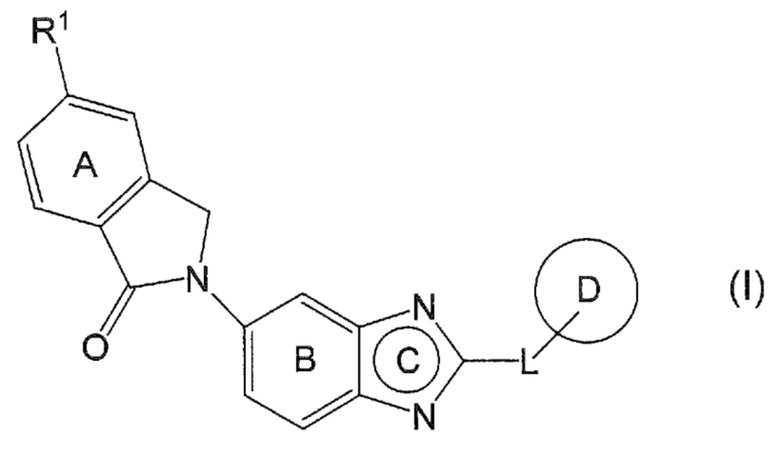
1. Соединение, представленное формулой (I):
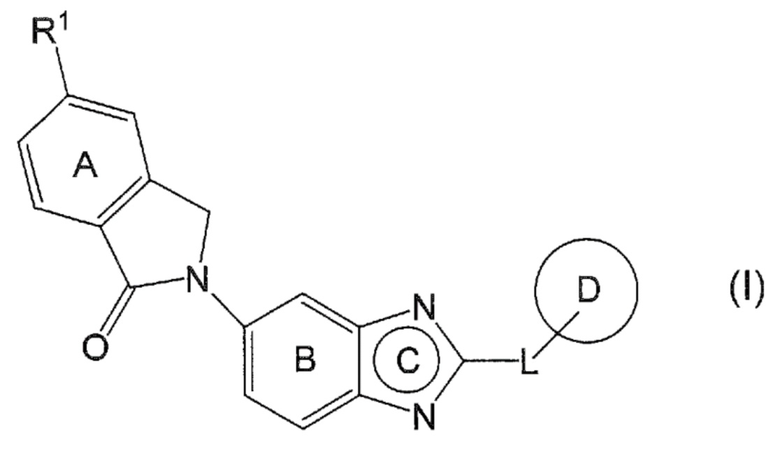
где
Кольцо A представляет собой бензольное кольцо;
Кольцо В представляет собой бензольное кольцо;
Кольцо C представляет собой имидазольное кольцо, необязательно дополнительно замещенное C1-6 алкильной группой; L представляет собой связь или метиленовую группу;
R1 представляет собой
(1) атом водород,
(2) атом галогена,
(3) ди-C1-6 алкиламиногруппу,
(4) пирролил, или
(5) пиперидил, пиперазинил, необязательно замещенный одной C1-6 алкильной группой, или морфолинил; и
Кольцо D представляет собой
(1) бензольное кольцо, необязательно дополнительно замещенное 1-3 заместителями, выбранными из
(a) атома галогена,
(b) гидроксигруппы,
(c) C1-6 алкильной группы, необязательно замещенной 1 C1-6 алкоксигруппой,
(d) C1-6 алкоксигруппы, необязательно замещенной 1 заместителем, выбранным из
(i) карбоксигруппы,
(ii) C1-6 алкоксикарбонильной группы,
(iii) бензилоксикарбонильной группы,
(iv) карбамоильной группы, необязательно моно- или дизамещенной заместителем(ями), выбранным из
(I) C1-6 алкильной группы, необязательно замещенной 1-3 заместителями, выбранными из
(A) циклопропила,
(B) фенила,
(C) фениламино, необязательно замещенного 1-3 атомами галогена,
(D) пиридила,
(E) тетрагидропиранила, и
(F) карбамоильной группы, необязательно моно- или дизамещенной заместителем(ями), выбранным из C1-6 алкильной группы и 2-фенилэтила,
(II) C2-6 алкенильной группы, необязательно замещенной одним фенилом,
(III) C3-10 циклоалкильной группы, необязательно замещенной 1 C1-6 алкильной группой,
(IV) фенильной группы, необязательно замещенной 1 заместителем, выбранным из
(A) атома галогена, и
(B) C1-6 алкильной группы,
(V) бензила,
(VI) пиридила, и
(VII) тетрагидропиранила или 1,1-диоксидигидробензотиенила, и
(v) пирролидинилкарбонила, морфолинилкарбонила, 1,1-диоксидотиазолидинилкарбонила или пиперидилкарбонила, необязательно замещенного 1 или 2 заместителями, выбранными из (I) гидроксигруппы и (II) C1-6 алкильной группы, и
(е) бензилокси,
(2) циклогексановое кольцо,
(3) пиридиновое кольцо,
(4) изоксазольное кольцо,
(5) тиофеновое кольцо,
(6) пиперидиновое кольцо, необязательно дополнительно замещенное 1-3 C1-6 алкоксикарбонильными группами, или
(7) тетрагидропирановое кольцо,
или его фармакологически приемлемая соль.
2. Соединение или соль по п. 1, где
Кольцо A представляет собой бензольное кольцо;
Кольцо В представляет собой бензольное кольцо;
Кольцо C представляет собой имидазольное кольцо;
L представляет собой связь;
R1 представляет собой пиперидил или морфолинил; и
Кольцо D представляет собой
(1) бензольное кольцо, необязательно дополнительно замещенное 1 заместителем, выбранным из
(a) атома галогена,
(b) гидроксигруппы,
(c) C1-6 алкоксигруппы, необязательно замещенной 1 карбамоильной группой, необязательно монозамещенной 1,1-диоксидигидробензотиенилом, или
(2) пиридиновое кольцо.
3. Соединение или соль по п.1, где
Кольцо А представляет собой бензольное кольцо;
Кольцо B представляет собой бензольное кольцо;
Кольцо С представляет собой имидазольное кольцо;
L представляет собой связь;
R1 представляет собой пиперидил или морфолинил; и
Кольцо D представляет собой бензольное кольцо, дополнительно замещенное одним заместителем, выбранным из
(а) атома галогена, и
(b) C1-6 алкоксигруппы, замещенной одной карбамоильной группой, монозамещенной 1,1-диоксидигидробензотиенилом.
4. N-(1,1-Диоксидо-2,3-дигидро-1-бензотиофен-5-ил)-2-(4-(5-(1-оксо-5-(пиперидин-1-ил)-1,3-дигидро-2H-изоиндол-2-ил)-1H-бензимидазол-2-ил)фенокси)ацетамид или его фармакологически приемлемая соль.
5. 2-(2-(4-Бромфенил)-1H-бензимидазол-5-ил)-5-(морфолин-4-ил)изоиндолин-1-он или его фармакологически приемлемая соль.
6. 5-(Пиперидин-1-ил)-2-(2-(пиридин-3-ил)-1H-бензимидазол-5-ил)изоиндолин-1-он или его фармакологически приемлемая соль.
7. 5-(Пиперидин-1-ил)-2-(2-(пиридин-4-ил)-1H-бензимидазол-5-ил)изоиндолин-1-он или его фармакологически приемлемая соль.
8. 2-(2-(4-Гидроксифенил)-1H-бензимидазол-5-ил)-5-(пиперидин-1-ил)изоиндолин-1-он или его фармакологически приемлемая соль.
9. Промотор созревания кардиомиоцитов, содержащий соединение или соль по любому из пп.1-8.
10. Способ получения зрелых кардиомиоцитов, который включает стадию культивирования незрелых кардиомиоцитов в присутствии соединения или соли по любому из пп. 1-8.
| WO 2014200339 A1, 18.12.2014 | |||
| WO 2014200339 A1, 18.12.2014 | |||
| WO 2015182765 A1, 03.12.2015 | |||
| WO 2012026491 A1, 01.03.2012 | |||
| WO 2009118928 A1, 01.10.2009 | |||
| ПРОИЗВОДНЫЕ БЕНЗИМИДАЗОЛА, ИХ СОЛИ ИЛИ ГИДРАТЫ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ С АНТАГОНИСТИЧЕСКОЙ В ОТНОШЕНИИ АНГИОТЕНЗИНА II АКТИВНОСТЬЮ НА ИХ ОСНОВЕ | 1993 |
|
RU2124007C1 |
Авторы
Даты
2022-12-22—Публикация
2019-03-28—Подача