Изобретение относится к медицине, в частности к онкологии, и может применяться для комбинированного лечения местнораспространенных злокачественных новообразований шейного отдела пищевода и гортаноглотки.
Лечение местнораспространенных злокачественных новообразований шейного отдела пищевода и гортаноглотки осуществляется с использованием комбинированного подхода, включающего выполнение дистанционной лучевой терапии в сочетании с системной лекарственной противоопухолевой терапией и последующим хирургическим лечением.
Хирургическое лечение при местнораспространенных злокачественных новообразованиях шейного отдела пищевода и гортаноглотки требует удаления опухоли в пределах здоровых тканей, для достижения отрицательного края резекции, подтвержденного патоморфологическими методами исследования. Объем хирургического лечения включает в себя удаление гортани, гортаноглотки и пищевода (ларингофарингоэзофагэтомия), а также реконструктивный этап, заключающийся в восстановлении целостности верхних отделов желудочно-кишечного тракта.
Методы реконструкции включают в себя использования свободных трансплантатов подвздошной кишки, подвздошно-ободочного угла, толстой кишки, а также биоинженерного трансплантата в виде желудочного стебля (операция по типу gastric pull-up).
(1. Marion, Y., et al. "Gastric pull-up reconstruction after treatment for advanced hypopharyngeal and cervical esophageal cancer." European annals of otorhinolaryngology, head and neck diseases 133.6 (2016): 397-400.
(2. Sreehariprasad A.V., Krishnappa R., Chikaraddi B.S., & Veerendrakumar K. (2012). Gastric pull up reconstruction after pharyngo laryngo esophagectomy for advanced hypopharyngeal cancer. Indian journal of surgical oncology, 3(1), 4-7. https://doi.org/10.1007/sl3193-012-0135-5
(3. Cahow CE, Sasaki CT. Gastric Pull-up Reconstruction for Pharyngo-laryngo-esophagectomy. Arch Surg. 1994;129(4):425-430. doi:10.1001/archsurg.1994.01420280103013.
К недостаткам вышеперечисленных способов реконструкции относятся несостоятельность анастомоза и гибель трансплантата, возникающие в 10-47% случаев, приводящих к развитию пневмонии и медиастинита, основной причиной которого является недостаточное кровоснабжение тканей трансплантата и тканей зоны формирования анастомоза после проведенной дистанционной лучевой терапии в сочетании с системной лекарственной противоопухолевой терапией. Основной проблемой несостоятельности глоточно-желудочного анастомоза при использовании узкого трансплантата из большой кривизны желудка является ишемия дистального фрагмента последнего из-за анатомически обусловленного отсутствия прямой коммуникации между правой и левой желудочно-сальниковыми артериями у 23,5% больных [Tomioka К., Murakami М., Saito A. et al. Anatomical and surgical evaluation of gastroepiploic artery // Okajimas Folia Anat. Jpn., 92 (3-4): 49-52, February, 2016.].
Техническим результатом изобретения является снижение количества осложнений, связанных с несостоятельности анастомоза, и гибели трансплантата при реконструкции с использованием желудочного стебля за счет развития сети внутриорганного кровоснабжения трансплантата.
Указанный технический результат достигается в способе комбинированного лечения местнораспространенных злокачественных опухолей шейного отдела пищевода и гортаноглотки, включающем удаление опухоли, формирование желудочного трансплантата для закрытия дефекта, проведение лучевой и химиотерапии, в котором на первом этапе осуществляют лапароскопическое формирование желудочного трансплантата с клипированием левой желудочной артерии - с целью развития сети внутриорганного кровоснабжения трансплантата, и трубчатой гастростомии из малой кривизны желудка с последующим проведением дистанционной лучевой терапии в сочетании с химиотерапией и последующим радикальным хирургическим лечением с реконструкцией дефекта желудочным трансплантатом в виде узкого желудочного стебля.
Способ иллюстрируется фиг. 1-3, где:
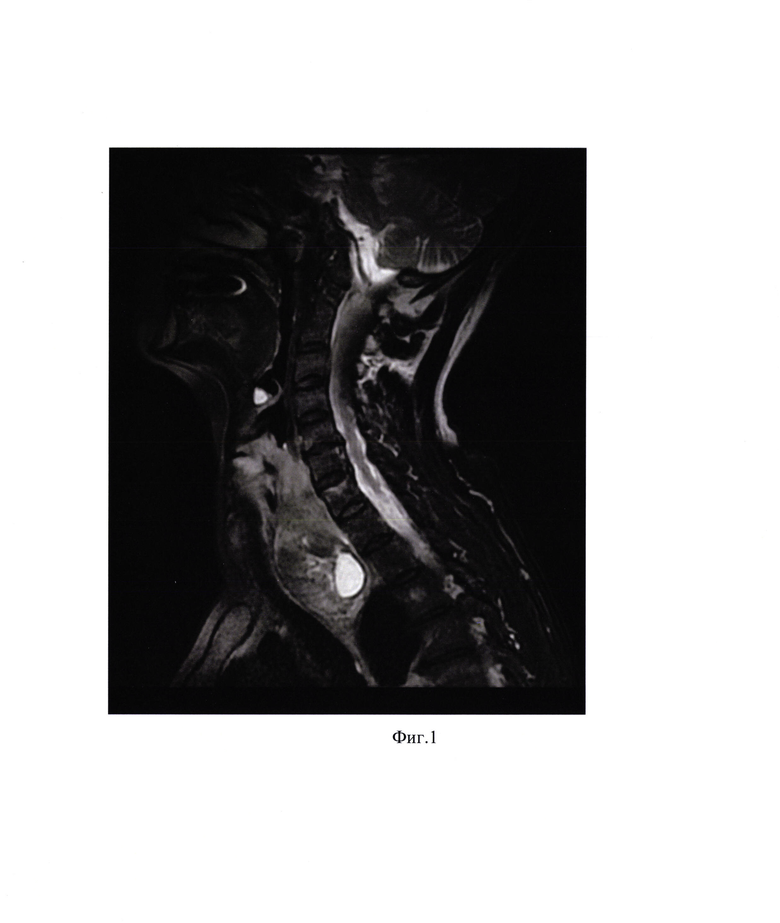
На фиг. 1 - магнитно-резонансная томография (МРТ) мягких тканей шеи с внутривенным контрастированием до лечения: рак шейного отдела пищевода с врастанием в гортаноглотку;
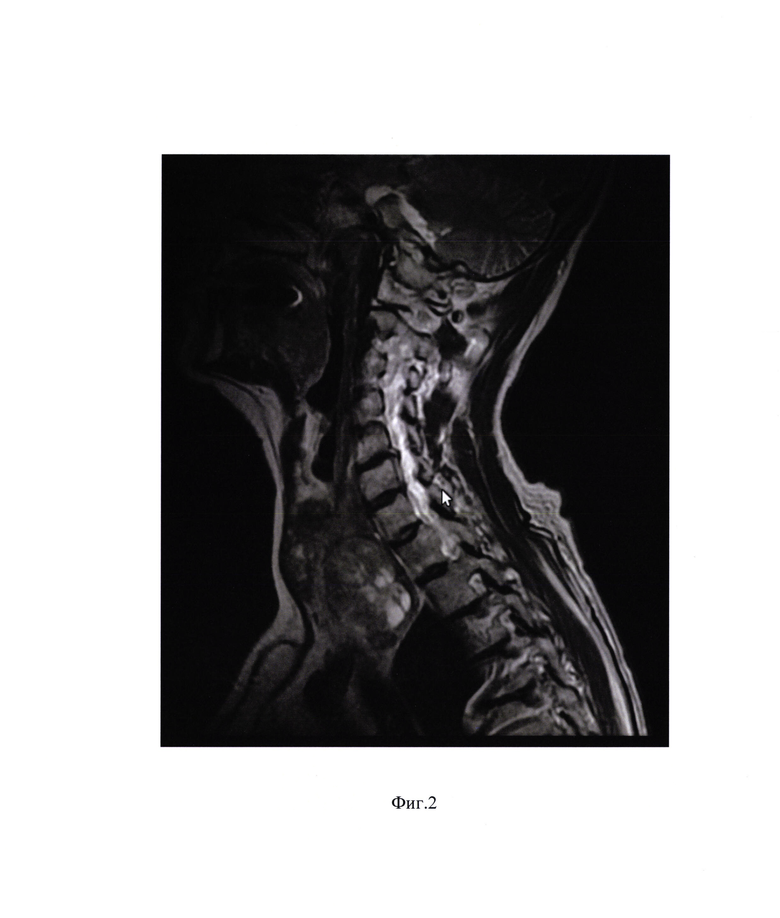
На фиг. 2 - МРТ мягких тканей шеи с внутривенным контрастированием после 2-х циклов полихимиотерапии: частичный регресс опухоли;
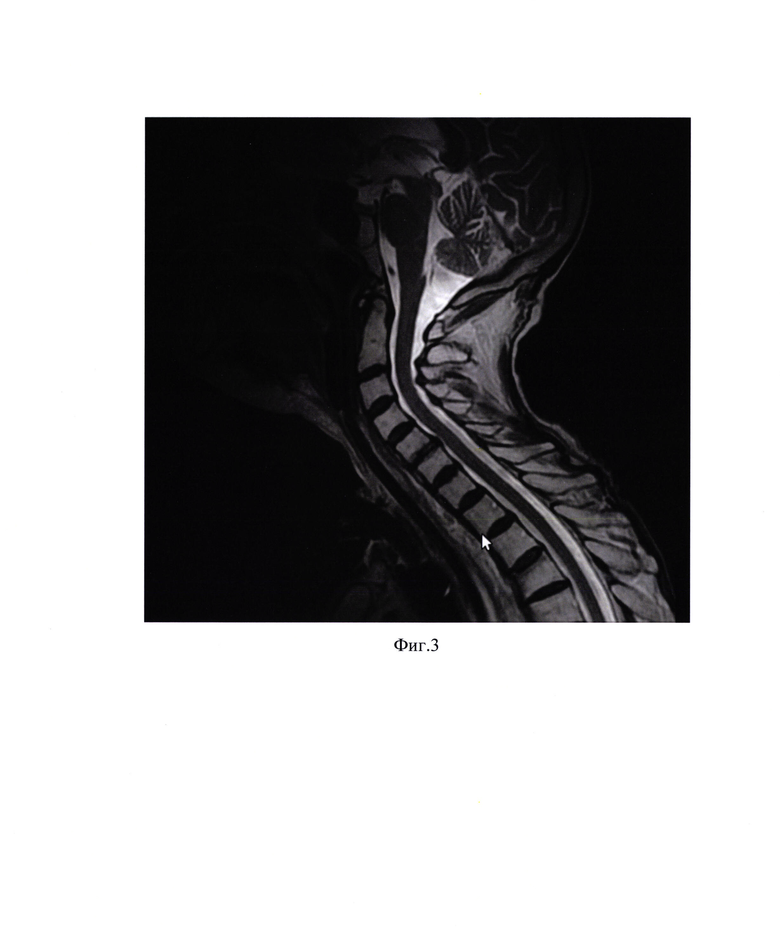
На фиг. 3 - МРТ мягких тканей шеи с внутривенным контрастированием после лечения: данных за рецидив нет.
Способ осуществляют, например, следующим образом.
На первом этапе пациенту выполняют лапароскопическое начальное формирование узкого желудочного стебля из антральной части и тела желудка с перевязкой левой желудочной артерии и трубчатой гастростомией из малой кривизны желудка. Хирургическая операция проводиться в условиях операционной под общей комбинированной анестезией, положение пациента на операционном столе - на спине. Накладываются три лапароскопических порта: один по средней линии ниже пупка на 1 сантиметр, второй - в мезогастральной области справа от первого порта на средине условного отрезка соединения первого порта с точкой пересечения передней подмышечной линии с реберной дугой. Третий порт устанавливается на 4 см ниже реберной дуги по среднеключичной линии. После ревизии органов брюшной полости при помощи ультразвукового скальпеля пересекается левая желудочная вена, выделяется и клипируется левая желудочная артерия с последующим формированием узкого трубчатого стебля из большой кривизны желудка путем наложения аппаратного степлерного шва на 5 см выше привратника по малой кривизне на протяжении 15-16 сантиметров (3 шва линейного эндоскопического аппарата 6/0) таким образом что вторая часть тела желудка по малой кривизне мобилизуется для трубчатой гастростомы. Сформированная таким образом гастростомическая трубка выводится через имеющийся боковой порт в области левого подреберья, вскрывается ее верхушка и фиксируется через все слои к коже при помощи отдельных узловых швов. В ее просвет вводится катетер Пельцера. Отдельные швы на раны от двух других портов.
Вторым этапом после формирования желудочного трансплантата пациенту проводят курс дистанционной конформной лучевой терапии в суммарной дозе 66-70 Гр и разовой дозе 2 Гр с проведением сеансов лучевой терапии по схеме 5 сеансов в неделю с одновременным проведением двух циклов полихимиотерапии продолжительностью 5 суток и интервалом между курсами 21 сутки с использованием платиносодержащих препаратов (цисплатин в дозе 75 мг/м2 или карбоплатин AUC5) и 5-фторурацила в дозе 750 мг/м2 с последующей оценкой эффекта лечения через 21 день с помощью магнитно-резонансной томографии мягких тканей шеи с внутривенным контрастированием.
Третьим этапом после проведения химиолучевой терапии выполняется торакоскопия с мобилизацией грудного отдела пищевода, релапароскопия, завершающее формирование трансплантата из большой кривизны желудка путем продолжения степлерного шва, наложенного на первом этапе, радикальное хирургическое удаление опухоли шейного отдела с тотальным удалением пищевода и желудка с пластикой дефекта сформированным узким желудочным стеблем проведенным ретростернально с пищеводно-желудочным анастомозом слева от шейного отдела трахеи.
Операция выполняется в условиях операционной под общей комбинированной анестезией, положение больного на животе. Накладываются 3 торакоскопических порта в 7-м по задней подмышечной линии, в 6-м и 9-м межреберьях по средней подмышечной. Под видеоторакоскопическим контролем выполняется выделение пищевода с обязательным удалением клетчатки и всех региональных лимфатических узлов. Подготовительный торакальный этап завершается пересечением пищевода на уровне средней трети при помощи линейного степлерного аппарата 6/0. Далее пациент перемещается в положение лежа на спине. Накладываются пять лапароскопических портов: один по средней линии живота ниже пупка на 1 сантиметр, два - у подреберий справа и слева по передним подмышечным линиям, следующие два - на середине условных отрезков, соединяющих крайние порты с центральным. Выполняется релапаросокопия, ревизия органов брюшной полости, разъединение спаек. Гастростомическая желудочная трубка отсекается от передней брюшной стенки при помощи линейного степлерного аппарата, производится мобилизация желудка по малой и большой кривизне с сохранением правой желудочно-сальниковой артерии. Пересекаются желудочно-селезеночная и желудочно-диафрагмальные связки. Формируется узкий желудочный стебель из большой кривизны желудка путем продолжения линейного степлерного шва, наложенного во время формирования гастростомы, с полным отсечением узкого стебля на уровне кардиального отдела желудка. В области пищеводного отверстия диафрагмы мобилизируется абдоминальный отдел пищевода, дистальная (отсеченная в грудной клетке) часть пищевода низводится в брюшную полость, пищеводное отверстие диафрагмы ушивается. В переднем средостении лапаросокпически формируется тоннель для проведения трансплантата на шею.
Окаймляющими гастростомическое отверстие разрезами производится полнослойное иссечение внутристеночной части гастростомы. Через сформированную таким образом минилапаротомию извлекается препарат (дистальная часть пищевода в моноблоке с оставшейся частью желудка) и оральный конец сформированного трансплантата, на который накладывается несколько швов в качестве держалок.
Выполняется шейный доступ к пищеводу по переднему краю кивательной мышцы слева, выделяется шейный отдел пищевода, препарат вывихивается в рану вместе с проксимальной частью пищевода, отсекается выше опухоли. После удаления препарата оральный конец пищевода прошивается кисетным швом с введением в просвет последнего головки циркулярного сшивающего аппарата. Через сформированный ретростернальный тоннель при помощи наложенных держалок узкий желудочный стебель выводится на шею. В дистальной части, параллельно степлерному шву, вскрывается просвет стебля, через который вводится циркулярный сшивающий аппарат с формированием пищеводножелудочного анастомоза конец-в-бок. Дистальная часть желудочного трансплантата после извлечения циркулярного аппарата отсекается при помощи линейного степлерного шва.
В подшитом трансплантате под микроскопом выделяют короткие брыжеечные сосуды и накладывают микрососудистый анастомоз между ними и поперечной артерии шеи и внутренней яремной веной. Рана послойно ушивается, дренируется двумя вакуум-дренажами.
Способ подтверждается клиническим примером.
Пациент, женщина, 58 лет. 21.07.2015 г. установлен диагноз: рак шейного отдела пищевода с врастанием в гортаноглотку T4N0M0, IIIС стадия (фиг. 1). Морфологическая верификация опухолевого процесса: плоскоклеточный умереннодифференцированный рак.
С 08.09.2015 по 19.10.2015 Первым этапом проведено 2 цикла полихимиотерапии по схеме цисплатин (100 мг/м2, день 1) и 5-фторурацил (1000 мг/м2, непрерывная внутривенная инфузия в течение 96 часов) с интервалом 21 день.
22.10.2015 - магнитно-резонансная томография мягких тканей шеи с внутривенным контрастированием: частичный регресс опухоли (фиг. 2). 27.10.2015 г. - лапароскопическое начальное формирование узкого желудочного стебля из антральной части и тела желудка с перевязкой левой желудочной артерии и трубчатой гастростомией из малой кривизны желудка. 19.11.2015 г. - 23.12.2015 г. - пациенту проведен курс конформной дистанционной лучевой терапией в суммарной дозе 66 Гр, (разовая доза облучения составляла 2 Грея, режим облучения - 5 дней в неделю) с одновременным проведением 2 циклов полихимиотерпии по схеме PF (цисплатин 75 мг/м2 + 5-фторурацил 750 мг/м2) с интервалами между циклами 21 день.
23.01.2016 г. - магнитно-резонансная томография шеи с внутривенным контрастированием: частичный регресс изменений. 12.03.2016 г. - ларингофарингоэзофагэктомия с пластикой узким желудочным стеблем.
Гистологическое исследование: умеренно-дифференцированный ороговевающий плоскоклеточный рак пищевода с инвазией в гортань с выходом на слизистую оболочку, мышцы гортани, правую и левую доли щитовидной железы. Лечебный патоморфоз опухоли по Mandard 4, по Becker 3. Края резекции пищевода, края резекции желудка, перешеек щитовидной железы вне опухоли. pT4bN0.
04.2016 г. - 06.2016 г. - пациенту проведено 2 цикла полихимиотерапии по схеме PF (цисплатин 100 мг/м2 + 5-фторурацил 1000 мг/м2) в адъювантном режиме. По данным магнитно-резонансной томографии от 25.07.2016 года - данных за рецидив нет (фиг. 3).
В период с 01.09.2013 года по 01.07.2019 года по заявляемому способу было пролечено 10 пациентов, показатель общей 3-летней выживаемости составил 51%, показатель безрецидивной 3-летней выживаемости - 44,3%.
Заявляемый способ позволяет снизить количество несостоятельности анастомоза и гибели трансплантата при реконструкции с использованием желудочного стебля за счет развития сети внутриорганного кровоснабжения трансплантата.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ФАРИНГОПЛАСТИКИ В УСЛОВИЯХ ДЕФИЦИТА ПЛАСТИЧЕСКОГО МАТЕРИАЛА | 2010 |
|
RU2427339C1 |
| Способ формирования гастростомы из малой кривизны желудка с прекондиционированием желудка | 2022 |
|
RU2790118C1 |
| СПОСОБ МИКРОХИРУРГИЧЕСКОЙ РЕКОНСТРУКЦИИ ГЛОТКИ И ШЕЙНОГО ОТДЕЛА ПИЩЕВОДА ТОЛСТОКИШЕЧНО-САЛЬНИКОВЫМ АУТОТРАНСПЛАНТАТОМ У ОНКОЛОГИЧЕСКОГО БОЛЬНОГО | 2014 |
|
RU2565836C1 |
| СПОСОБ ФОРМИРОВАНИЯ ПИЩЕВОДНО-ЖЕЛУДОЧНОГО АНАСТОМОЗА НА ШЕЕ | 2020 |
|
RU2737585C2 |
| СПОСОБ ПЛАСТИКИ ПИЩЕВОДА ПРИ РАКЕ ВЕРХНЕГРУДНОГО И ШЕЙНОГО ОТДЕЛОВ | 2012 |
|
RU2480162C1 |
| СПОСОБ ПРОФИЛАКТИКИ ПЛЕВРО-МЕДИАСТИНАЛЬНЫХ ОСЛОЖНЕНИЙ ПОСЛЕ ЭЗОФАГЭКТОМИИ С ПЛАСТИКОЙ ЖЕЛУДОЧНЫМ СТЕБЛЕМ И АНАСТОМОЗОМ НА ШЕЕ | 2023 |
|
RU2832970C1 |
| СПОСОБ РЕКОНСТРУКЦИИ ВЕРХНИХ ОТДЕЛОВ АЭРОДИГЕСТИВНОГО ТРАКТА | 2014 |
|
RU2565830C1 |
| Способ реконструктивно-пластической операции у пациентов с местно-распространенным раком гортаноглотки T4A, с распространением опухоли на шейный отдел пищевода | 2022 |
|
RU2779370C2 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ РАКА ГЛОТКИ | 2007 |
|
RU2343853C1 |
| СПОСОБ ЛЕЧЕНИЯ БОЛЬНЫХ НЕРЕЗЕКТАБЕЛЬНЫМ РАКОМ ПИЩЕВОДА | 2001 |
|
RU2196521C1 |
Изобретение относится к медицине, а именно к онкологии, гастроэнтерологии. Выполняют лапароскопическое формирование желудочного трансплантата с клипированием левой желудочной артерии и трубчатой гастростомии из малой кривизны желудка. Проводят дистанционную лучевую терапию в сочетании с химиотерапией. После чего выполняют радикальное хирургическое лечение с реконструкцией дефекта желудочным стеблем. Способ позволяет снизить количество осложнений, связанных с несостоятельностью анастомоза, за счет развития сети внутриорганного кровоснабжения трансплантата, повысить показатели общей выживаемости и качества жизни, а также снизить показатели 30-дневной смертности. 3 ил., 1 пр.
Способ комбинированного лечения местнораспространенных злокачественных опухолей шейного отдела пищевода и гортаноглотки, включающий удаление опухоли, формирование желудочного трансплантата для закрытия дефекта, проведение лучевой и химиотерапии, отличающийся тем, что на первом этапе осуществляют лапароскопическое формирование желудочного трансплантата в виде желудочного стебля с клипированием левой желудочной артерии и трубчатой гастростомии из малой кривизны желудка с последующим проведением дистанционной лучевой терапии в сочетании с химиотерапией и последующим радикальным хирургическим лечением с реконструкцией дефекта сформированным желудочным трансплантатом в виде желудочного стебля.
| РАДЖАБОВА З.А | |||
| и др., Анализ результатов комбинированного лечения пациентов с верифицированным раком шейного отдела пищевода и гортаноглотки с применением хирургического лечения с одномоментной пластикой дефекта, Опухоли головы и шеи, 2016 | |||
| т | |||
| Приспособление для точного наложения листов бумаги при снятии оттисков | 1922 |
|
SU6A1 |
| Насос | 1917 |
|
SU13A1 |
| Способ улучшения кровоснабжения проксимального отдела желудочного трансплантата при эзофагопластике | 2016 |
|
RU2614213C1 |
| CN 214910775 U, 30.11.2021 | |||
| MINGOL-NAVARRO F | |||
| Et al | |||
| Ischaemic | |||
Авторы
Даты
2022-12-26—Публикация
2022-03-09—Подача