Изобретение относится к ранозаживляющим средствам на основе биологически активных веществ из базидиальных грибов и может быть использовано в медицине и биотехнологической промышленности. Одной из перспективных групп продуцентов, чей химический состав биологически активных веществ и свойства этих веществ в настоящее время изучены достаточно полно, являются высшие базидиальные грибы.
Исследованием лечебных свойств высших базидиальных грибов и практическим их применением в области медицины занимаются ученые ряда стран на протяжении последних 50-ти лет. Результаты этих исследований особо широко используются в Китае, Японии, Корее, США, Канаде, России и в последнее время в Норвегии.
Среди метаболитов высших базидиальных грибов выделены и идентифицированы вещества, которые являются иммуномодуляторами и проявляют противоопухолевые, кардиоваскулярные, противовирусные, антибактериальные, противопаразитарные, гепатозащитные и противодиабетические свойства (Материалы IV Международной конференции «Наука и практика грибоводства»/М., Международная Ассоциация Грибоводов. 1997 г. - 92 с; Перспективы использования в медицине веществ, образуемых базидиальными грибами. Обзор /International Journal of Medicinal Mushrooms. Vol. 3, 31-62, 1999).
Показано, что высшие базидиомицеты, способны синтезировать широкий комплекс биологически активных веществ, таких как полисахариды, гликопротеины, терпены, стеролы, пигменты и др. [5-9], которые могут проявлять антибактериальные [5, 10], антивирусные [5, 11-14], противоопухолевые, антипаразитарные и иммуномодулирующие свойства [5-8, 15]. При этом указанные комплексы из базидиомицетов, как правило, не являются токсичными для человека или животных [5-11].
Поэтому высшие базидиальные грибы и вещества, выделенные из них, например, из гриба чаги Inonotus obliquus [5-7, 13-14, 16], гриба вешенки обыкновенной Pleurotus ostreatus [5, 15], могут быть использованы в качестве перспективного сырья для фармацевтической промышленности, в частности, для разработки на их основе мазей для местного (медикаментозного) лечения ран.
Полисахариды - наиболее хорошо изученные сильнодействующие вещества, извлеченные из грибов, обладающих противоопухолевыми и иммуномодулирующими свойствами. В частности, показано, что полисахаридные фракции, выделенные из клеточных стенок плодовых тел вешенки Pleurotus ostreatus, ингибируют рост саркомы-180 у мышей, а также активны в отношении вируса иммунодефицита человека и вируса гриппа (Теплякова Т.В., Косогова Т.А. Высшие грибы Западной Сибири -перспективные объекты для биотехнологии лекарственных препаратов. Новосибирск, 2014. - 298 с).
Известен препарат, влияющий на тканевой обмен, и применение штамма гриба Pleurotus ostreatus 1137 для его получения (патент РФ №2192873, МПК А61К 35/70, опубл. 2001 г.), используемый в медицинской и биотехнологической промышленности для производства физиологически активных препаратов и пищевых добавок на основе грибных продуцентов биологически активных веществ, применяемых в медицине для снижения токсических проявлений противоопухолевых препаратов. Меланины - природные пигменты, участвуют в работе живых систем различного уровня организации. Меланины содержатся в микроорганизмах, грибах и растениях, в тканях животных и человека (придают окраску волосам, ресницам, коже), в ряде пищевых продуктов (чай, кофе, грибы, гречиха и др.). Меланины - высокомолекулярные соединения, образуются в результате полимеризации тирозина, диоксифенилаланина или катехоламинов на белковой матрице, обладают широким спектром биомедицинских и технических свойств. Известны сообщения о практическом применении синтетических, полусинтетических и выделенных из биологических источников меланинов в медицине, косметологии, пищевой и лакокрасочной отраслях промышленности, технике и электронике.
По данным доклинического фармакологического исследования водорастворимые меланины не токсичны. После однократного внутрижелудочного или внутрибрюшинного введения в дозах от 100 до 3000 мг/кг не отмечено гибели мышей. При введении в течение 15 суток не зафиксировано смертельных исходов, нарушения общего состояния, патологических изменений внутренних органов, не выявлено канцерогенного действия. В то же время опубликованные данные указывают на наличие у меланинов разнообразных фармакологических свойств.
В экспериментах на грызунах показано, что меланин обладает антистрессорным, противосудорожным и антимутагенным действием, повышает физическую работоспособность, усиливает иммунную защиту организма, вызывает продукцию цитокинов, таких как интерлейкины - 6 и 8, туморнекротического фактора, ростового фактора эндотелия, ускоряет рост массы тела и нормализует гематологический статус.
Сообщается об успешном применении меланина в схеме комплексной терапии онкологических заболеваний и при сахарном диабете.
Известно противовирусное средство на основе меланина (патент РФ №2480227, МПК А61К 36/06, опубл. 27.04.2013 г.). В качестве меланина оно содержит водорастворимый меланин в концентрации от 0,002 мг/мл до 25 мг/мл, полученный экстракцией из базидиального гриба Inonotus obliquus и обладающий противовирусной активностью в отношении вирусов гриппа, простого герпеса 2-го типа, иммунодефицита (ВИЧ-1) и осповакцины.
Известно применение экстракта базидального гриба Inonotus obliquus, полученного водной экстракцией при температуре 50-95°С в течение от 1,0 до 72 часов, для ингибирования репликации коронавируса SARS-CoV-2, который при концентрации в диапазоне 0,75-11,6 мкг/мл проявляет 50%-ную противовирусную дозазависимую активность против SARS-CoV-2 в тестах на клеточных культурах Vero Е6 и Vero. (патент РФ №2741714, МПК А61К 36/06, опубл. 28.01.2021 г.).
Мазь, изготовленная с использованием меланина (мазь: туба 15 г, регистрационные номера №11/947 и №12/947, от 06.12.2011 г.) рекомендована в качестве фотопротектора для наружного применения.
Водорастворимый меланиновый экстракт (http://melanin.com.ua/voda-s-melaninom/38-melaninovyy-ekstrakt.html) рекламируется в качестве средства для лечения инсульта, диабета, язвенной болезни желудка и 12-перстной кишки, антирадиационного, иммуномодулирующего и противовирусного средства при СПИДе.
Однако выше приведенные аналоги не исследованы в качестве ранозаживляющих средств.
Наиболее близким техническим решением (прототипом) является публикация об экспериментальной оценке специфической ранозаживляющей активности мази на основе меланина из природного сырья чаги Inonotus obliquus и мази на основе меланина, полученного на основе глубинной культуры штамма чаги Inonotus obliquus F-1244. Меланинсодержащие экспериментальные мази включали из расчета на 25 г мази 50 мг меланина, растворенный в 12 мл изотонического раствора. Основу мази составляли: 7 г вазелинового масла, 3,0 г эмульгатора Т-2 и 3,0 г Твин-60 (Пугач О.А., Цветкова В.А., Барашкин B.C., Ставский Е.А., Лебедев Л.Р., Теплякова Т.В./ «ОЦЕНКА СВОЙСТВ МЕЛАНИНА ИЗ ЧАГИ IN VIVO»//МАТЕРИАЛЫ 5-ГО МЕЖДУНАРОДНОГО СЪЕЗДА ФИТОТЕРАПЕВТОВ И ТРАВНИКОВ, посвященного 100-летию патриарха отечественной фитотерапии Карпа Абрамовича Трескунова, опубл. 11.02.2019 г.
(https://www.secret-dolgolet.rn/pugach-o-a-tsvetkova-v-a-barashkin-v-s-stavskiy e-a-lebedev-l-r-teplyakova-t-v-otsenka-svoystv-melanina-iz-chagi-in-vivo/).
Однако опубликованные ранозаживляющие средства на основе меланина в мазевой форме из природного сырья чаги Inonotus obliquus и мази на основе меланина, полученного на основе глубинной культуры штамма чаги Inonotus obliquus F-1244 по своей ранозаживляющей активности не превышают широко используемой в практической медицине для лечения ран различного происхождения мази сравнения Левомикону.
Техническим результатом заявляемого изобретения является повышение ранозаживляющей активности мазевого средства на основе биологически активных веществ из базидиальных грибов Inonotus obliquus и/или Pleurotus ostreatus.
Указанный технический результат достигается тем, что ранозаживляющая мазь для наружного применения, содержащая биологически активные вещества из базидиальных грибов и мазевую основу, согласно изобретения, в качестве биологически активных веществ из базидиальных грибов она содержит меланин из природного сырья гриба чаги или глубинной культуры гриба чаги Inonotus obliquus, или суммарный полисахарид из вешенки обыкновенной Pleurotus ostreatus, или смесь вышеуказанных меланина и суммарного полисахарида в соотношении от 1:1 до 1:2, а количественное содержание компонентов из расчета 25 г мази составляет:
биологически активные вещества из базидиальных грибов 0,25-0,75 г;
мазевая основа - остальное до 25 г.
В первом варианте выполнения мазь содержит в качестве биологически активных веществ из базидиальных грибов меланин из природного сырья гриба чаги Inonotus obliquus, в качестве мазевой основы - изотонический раствор, вазелин и эмульгатор ланолин, а количественное содержание компонентов из расчета 25 г мази составляет:
Во втором варианте выполнения мазь содержит в качестве биологически активных веществ из базидиальных грибов меланин из глубинной культуры гриба чаги Inonotus obliquus, в качестве мазевой основы - изотонический раствор, вазелин и эмульгатор ланолин, а количественное содержание компонентов из расчета 25 г мази составляет:
В третьем варианте выполнения мазь содержит в качестве биологически активных веществ из базидиальных грибов суммарный полисахарид из природного сырья гриба вешенки обыкновенной Pleurotus ostreatus, в качестве мазевой основы - изотонический раствор, вазелин и эмульгатор ланолин, а количественное содержание компонентов из расчета 25 г мази составляет:
В четвертом варианте выполнения мазь содержит в качестве биологически активных веществ из базидиальных грибов суммарный полисахарид из природного сырья гриба вешенки обыкновенной Pleurotus ostreatus, в качестве мазевой основы - изотонический раствор, вазелин и эмульгатор ланолин, а количественное содержание компонентов из расчета 25 г мази составляет:
В пятом варианте выполнения мазь содержит в качестве биологически активных веществ из базидиальных грибов смесь меланина из глубинной культуры гриба чаги Inonotus obliquus и суммарного полисахарида из природного сырья гриба вешенки обыкновенной Pleurotus ostreatus в соотношении 1:1, в качестве мазевой основы - изотонический раствор, вазелин и эмульгатор ланолин, а количественное содержание компонентов из расчета 25 г мази составляет:
В шестом варианте выполнения мазь содержит в качестве биологически активных веществ из базидиальных грибов смесь меланина из природного сырья гриба чаги Inonotus obliquus и суммарного полисахарида из природного сырья гриба вешенки обыкновенной Pleurotus ostreatus в соотношении 1:2, в качестве мазевой основы - изотонический раствор, вазелин и эмульгатор ланолин, а количественное содержание компонентов из расчета 25 г мази составляет:
Ниже приведен пример 1 составов образцов 1-7 ранозаживляющей мази.
Пример 1. Представлено количественное содержание компонентов ранозаживляющего средства в мазевой форме из расчета 25 г мази составляет:
Состав образца 1.
Состав образца 2.
Состав образца 3.
Состав образца 4.
Состав образца 5.
Состав образца 6.
Состав образца 7.
Пример 2.
Получение опытных образцов мазей, содержащих биологически активные вещества из высших базидиомицетов, в частности, образцов 1-3 из гриба чаги Inonotus obliquus и определение in vivo их ранозаживляющей активности. При этом образцы 1 и 2 получали на основе меланина из природного сырья березового гриба (чаги), а образец 3 на основе меланина из глубинной культуры Inonotus obliquus F-1244. Меланины из природного сырья березового гриба (чаги) и из глубинной культуры Inonotus obliquus F-1244 получали методами согласно патентам [13, 14].
Для приготовления образца 1 использовали 50 мг меланина, в образце 2-250 мг меланина, в образце 3 - 400 мг меланина. Меланин в образцах 1, 2 и 3 растворяли в 12 мл изотонического раствора.
Для получения 25,0 г мази образцов 1-3 применяли следующую пропись. Меланин 50 мг (образец №1), меланин 250 мг (образец №2) из природного сырья гриба чаги и меланин 400 мг (образец 3) из глубинной культуры гриба Inonotus obliquus F-1244 растирали до мельчайшего порошка в фарфоровой ступке, затем растворяли в 2,5 мл физиологического раствора, добавляли в качестве эмульгатора 2,5 г ланолина, затем вазелина -остальное до 25 г. продолжая при этом растирание смеси в ступке при 50-60°С до получения гомогенной мази, а затем расфасовывали.
Ранозаживляющую активность образцов 1-3 мазей оценивали на модели кожной плоской резаной раны у здоровых неинбредных мышей с массой тела 17-19 г. колонии ICR обоего пола питомника ФБУН ГНЦ ВБ «Вектор» Роспотребнадзора. Животных распределяли по следующим группам (по 20 мышей в каждой):
- группа №1 - контрольная, мыши ничем не леченные;
- группа №2 - контрольная, леченная мазью сравнения (мазь Левомикон-ТФФ);
- группа №3 - опытная, животные, леченные мазью, содержащая 50 мг меланина из природного сырья чаги Inonotus obliquus (образец 1);
- группа №4 - опытная, животные, леченные мазью, содержащая 250 мг меланина из природного сырья гриба чаги Inonotus obliquus (образец 2);
- группа №5 - опытная, леченная мазью, содержащая 400 мг меланина, полученного на основе глубинной культуры штамма гриба чаги Inonotus obliquus F-1244 (образец 3).
Действующим началом мази сравнения (мазь Левомикон-ТФФ) является метилурацил 4,00 г и хлорамфеникол - 0,75 г. Вспомогательные компоненты: Макрогол-1500 - 19,05 г, макрогол-400 - 76,20 г. Мазь оказывает антимикробное действие, прежде всего за счет антибиотика широкого спектра действия хлорамфеникола. Метилурацил обладает анаболической активностью. Оказывает противовоспалительное, иммуностимулирующее, гемопоэтическое, лейкопоэтическое действие. Нормализуя нуклеиновый обмен, ускоряет процессы регенерации в ранах, ускоряя рост и грануляционное созревание ткани и эпителизацию (электронное издание справочника Видаль 2011 г. дата обновления: 2019.07.31).
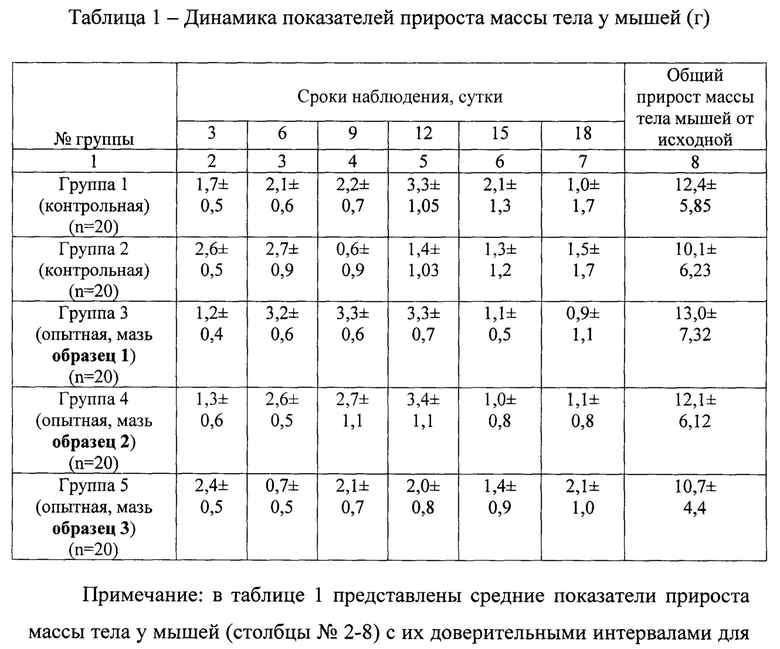
вероятности 95% 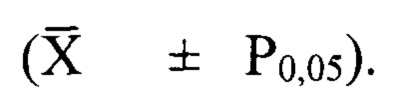
 - среднее арифметическое; P0,05 - доверительный интервал для вероятности 95%; n - число мышей в группе.
- среднее арифметическое; P0,05 - доверительный интервал для вероятности 95%; n - число мышей в группе.
После премедикации белых мышей хлороформом животным на спине наносили нестерильными ножницами без соблюдения правил асептики плоскую резаную рану. Экспериментальных животных групп №№2-4 лечили ежедневно путем нанесения на раны шпателем 0,2 г мази Левомикона (группа №2) и 0,2 г мази с меланином (образец №1), с содержанием в ней 0,4 мг меланина (группа №3); для группы №4 (образец №2) - 0,2 г мази содержало 2,0 мг меланина, а для группы №5 (образец №3) - 0,2 г мази содержало 3,2 мг меланина. Лечение мышей продолжали до момента заживления у них резаных ран. Ежедневно у мышей во всех группах оценивали площади ран по методу Л.Н. Поповой [17], двигательную активность, аппетит, динамику и характер заживления ран, а также через каждые трое суток оценивали изменение у них массы тела (см. табл. 1-2). Далее в примерах 3, 4 и 5 получение модели кожной раны и алгоритм лечения и наблюдения за ее заживлением были аналогичны примеру 2.
Из данных, представленных в табл.1, следует, что динамика показателей прироста массы тела у мышей, как в экспериментальных группах, так и в контрольных группах животных была положительной. При этом значения этих показателей были очень близкими и не различались с достоверностью 95% между группами.
В ходе эксперимента подопытные животные в группах №№1-2 в течение первых пяти дней выглядели менее активными, по сравнению с мышами №№3-5 групп. Последние охотнее поедали свой корм, более того, после нанесения мази мыши частично съедали меланиновую мазь с ран друг у друга. На 18 сутки наблюдения прирост массы тела по группам у мышей достиг сопоставимых величин, не различавшихся между группами с достоверностью 95%. Полученные данные, таким образом, свидетельствовали об отсутствии негативного (токсического) влияния меланиновых мазей разных прописей на организм мышей.
Динамика заживления ран в опытных группах животных (табл. 2) по сравнению с контрольными группами различалась. Визуально у мышей опытных групп №4 и №5, леченных мазью с пятикратно и более увеличенной концентрацией меланина по сравнению с группой №3, корочки на ранах уже на 12 сутки отпали, раны зарубцевались, на поверхности рубцов покрытых по периферии отрастающей шерстью остались только следы от корочек размерами 0,01-0,02 см2. В то же время у мышей контрольных групп №1 и №2, а также группы №3 аналогичный результат заживления ран у животных был получен только на 21 сутки. Однако следует отметить, что в группе мышей №3 была выявлена тенденция более быстрого заживления ран (начиная с 15 суток наблюдения) по сравнению с животными групп №1-2, включая контрольную группу №2, леченных контрольной мазью сравнения Левомиконом - ТФФ.
Представленные в табл. 1-2 данные показали, что образцы мазей 1-3, содержащие меланин в диапазоне 2,0-3,2 мг в одноразовой дозе (0,2 г) мази, наносимой ежедневно на рану мышам, не обладают токсичностью, обладают ранозаживляющей активностью сопоставимой с контрольной мазью Левомикон-ТФФ. При этом образцы №2 и №3 мази, содержащий пятикратно и более увеличенную концентрацию меланина, существенно превосходит по своей эффективности Левомикон-ТФФ. Меланины как из природного сырья чаги Inonotus obliquus, так и меланины из глубинной культуры Inonotus obliquus F-1244 обладают ранозаживляющей активностью. Мазевая основа прописи 2,5 г ланолина и 20,0 г вазелина не обладает токсичностью для животных и может быть использована в составе меланинсодержащих мазей. При этом экспериментальные меланиновые мази продемонстрировали, как противовоспалительные, так и регенеративные свойства меланина (особенно в прописи мази с пятикратным содержанием меланина) не уступающие, по крайней мере, таковым у хлорамфеникола и метилурацила контрольной мази сравнения Левомикон-ТФФ.
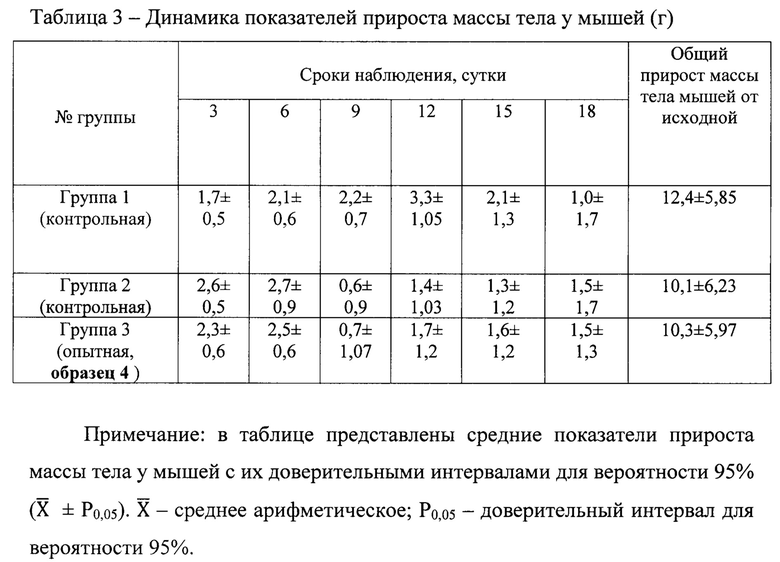
Пример 3. Получение образцов мазей, содержащих биологически активные вещества из высших базидиомицетов, в частности, образца №4 в виде суммарных полисахаридов из природного сырья гриба вешенки Pleurotus ostreatus и определение in vivo его ранозаживляющей активности (данные представлены в табл. 3-4).
Для выделения суммарных полисахаридов тщательно отмытые и осушенные плодовые тела гриба вешенки измельчали гомогенизатором (соотношение биомасса: дистиллированная вода 1:5), грибной гомогенат прогревали на кипящей водяной бане в течение 12 часов. Далее осаждали полисахариды из водного экстракта 96%-ным этиловым спиртом (соотношение водный экстракт: этиловый спирт 1:1), выдерживали в течение 18 часов при температуре (6±2)°С, центрифугировали в течение 20 мин при 10000 об/мин, полученный осадок полисахаридов высушивали при температуре не более 40°С. Повторно центрифугированием отделяли от ресуспендированных в дистиллированной воде полисахаридов нерастворимую фракцию, полученную надосадочную жидкость с суммарными полисахаридами высушивали. Для получения 25,0 г мази 0,5 г полисахарида растирали до мельчайшего порошка в фарфоровой ступке, затем последовательно добавляли 2,5 мл физиологического раствора, 2,5 г ланолина (эмульгатор) и вазелина - остальное до 25 г. продолжая при этом растирание смеси в ступке при 50-60°С до получения гомогенной мази, а затем расфасовывали.
Ранозаживляющую активность мази образца 4 оценивали на модели кожной резаной раны аналогично алгоритму примера 2 на животных, распределенных по следующим группам (по 20 мышей в каждой):
группа №1 - контрольная, мыши ничем не леченные;
группа №2 - контрольная, леченная мазью Левомикон-ТФФ;
группа №3 - опытная, леченная мазью с полисахаридным комплексом из гриба вешенки Pleurotus ostreatus (образец 4).
Из данных, представленных в табл.3, следует, что динамика показателей прироста массы тела у мышей, во всех группах животных была положительной. При этом значения этих показателей были очень близкими и практически не различались. Подопытные животные в группах №№1-2 в течение первых пяти дней выглядели менее активными, по сравнению с мышами группы №3.
На 18 сутки наблюдения прирост массы тела по группам у мышей достиг сопоставимых величин, что свидетельствовало об отсутствии негативного влияния, как со стороны компонентов мазевой основы, так и лечебных составляющих мази - суммарного полисахаридного комплекса на организм мышей.
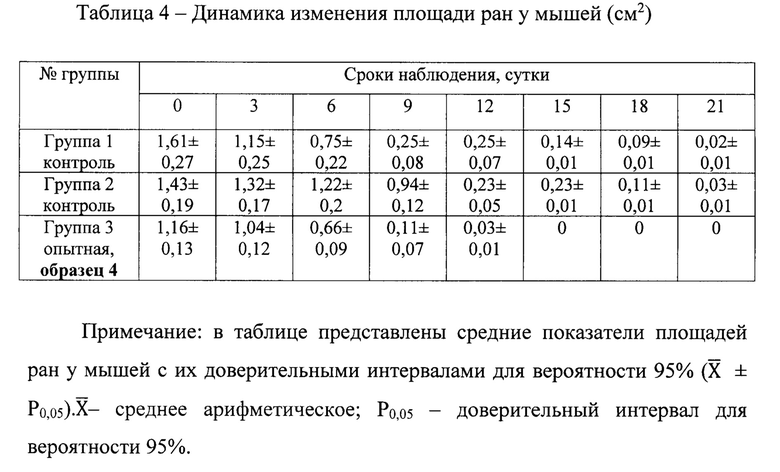
Динамика заживления ран между опытной группой животных (таблица 4) и контрольными группами различалась. Визуально у мышей опытной группы №3 (образец №4), леченных полисахаридсодержащей мазью из вешенки, содержащей в одной дозе 0,2 г мази 4 мг полисахарида корочки на ранах уже на 12 сутки отпали, раны зарубцевались, на поверхности рубцов покрытых отрастающей шерстью остались только следы от корочек размерами 0,01-0,03 см2. В то же время у мышей контрольных групп №1 и №2 аналогичный результат заживления ран у животных был получен только на 21 сутки.
Мазевая основа прописи, содержащая 2,5 г ланолина и 20,0 г вазелина, не обладает токсичностью для животных. При этом экспериментальная полисахаридсодержащая мазь продемонстрировала, как противовоспалительные, так и регенеративные свойства суммарного полисахаридного комплекса не уступающие, по крайней мере, таковым у хлорамфеникола и метилурацила контрольной мази сравнения Левомикон -ТФФ.
Пример 4. Получение образцов мазей, содержащих биологически активные вещества из высших базидиомицетов, в частности, образца №5 на основе суммарных полисахаридов из гриба вешенки Pleurotus ostreatus и образца №6 на основе комплекса (смеси 1:1) меланина из глубинной культуры гриба чаги Inonotus obliquus и суммарных полисахаридов из гриба вешенки Pleurotus ostreatus, а также и определение in vivo их ранозаживляющей активности (данные представлены в таблицах 5-6).
Выделение суммарных полисахаридов из гриба вешенки Pleurotus ostreatus проводили аналогично методики, приведенной в примере 3, а меланина - аналогично в примере 1.
Для получения 25,0 г мази (образец №5) 0,6 г полисахарида растирали до мельчайшего порошка в фарфоровой ступке, затем последовательно добавляли 2,5 мл физиологического раствора, 2,5 г ланолина (эмульгатор) и вазелина - остальное до 25 г., продолжая при этом растирание смеси в ступке при 50-60°С до получения гомогенной мази, а затем расфасовывали.
Для получения 25,0 г мази в виде смеси меланина и полисахарида в соотношении 1:1 (образец №6) 0,35 г меланина и 0,35 г суммарного полисахарида растирали до мельчайшего порошка в фарфоровой ступке, затем последовательно добавляли 2,5 мл изотонического раствора, 2,5 г ланолина (эмульгатор) и вазелина - остальное до 25 г., продолжая при этом растирание смеси в ступке при 50-60°С до получения гомогенной мази, а затем расфасовывали.
Ранозаживляющую активность мази образцов №5 и №6 оценивали на модели кожной резаной раны аналогично алгоритму примеров 2, 3 и 4 на животных, распределенных по следующим группам (по 20 мышей в каждой):
группа №1 - контрольная, мыши ничем не леченные;
группа №2 - контрольная, леченная мазью Левомикон-ТФФ;
группа №3 - опытная, леченная полисахаридной мазью (образец №5);
группа №4 - опытная, леченная меланинполисахаридной мазью (образец №6).
Экспериментальных животных групп №№2-4 лечили ежедневно путем нанесения на раны шпателем 0,2 г мази Левомикона (группа №2); 4,8 мг полисахаридного комплекса в 0,2 г мази (группа №3, образец мази №5) и 2,8 мг меланина и 2,8 мг полисахаридного комплекса в 0,2 г мази (группа №4, образец мази №6). Данные по оценке лечебных свойств и токсичности указанных выше опытных мазей представлены в табл. 5-6.
Из данных, представленных в таблице 5, следует, что динамика показателей прироста массы тела у мышей, во всех группах животных была положительной. При этом значения этих показателей были очень близкими и практически не различались.
Подопытные животные в группах №№1-2 в течение первых пяти дней выглядели менее активными, по сравнению с мышами группы №3 и №4 (образцы №5 и №6). На 18 сутки наблюдения прирост массы тела по группам у мышей достиг сопоставимых величин, что свидетельствовало об отсутствии негативного влияния, как со стороны компонентов мазевой основы, так и лечебных составляющих мази образцов №5 на основе полисахарида и №6 - меланинполисахаридного комплекса на организм мышей.
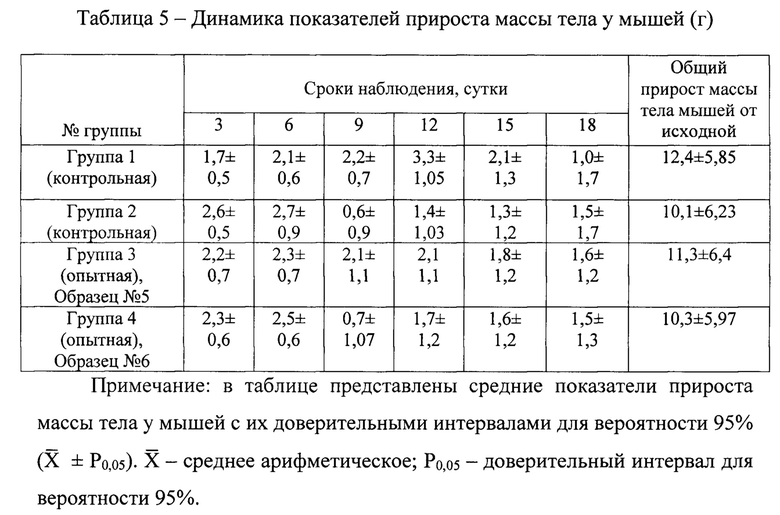
Динамика заживления ран между опытными группами животных и контрольными группами различалась (табл.6). Визуально у мышей опытных групп №3 и №4, леченных полисахаридсодержащей мазью (образец №5) и меланинполисахаридсодержащей мазью (образец №6), корочки на ранах уже на 12 сутки отпали, раны зарубцевались, на поверхности рубцов покрытых отрастающей шерстью остались только следы от корочек размерами 0,01-0,03 см2. В то же время у мышей контрольных групп №1 и №2 аналогичный результат заживления ран у животных был получен только на 21 сутки.
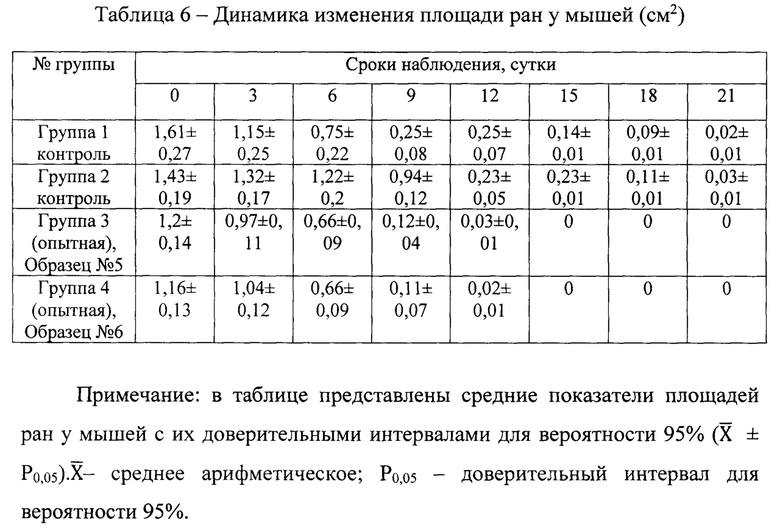
Мазевая основа прописи ланолин (эмульгатор) с вазелином не обладает токсичностью для животных. При этом экспериментальная меланинполисахаридная и полисахаридная мази продемонстрировали, как противовоспалительные, так и регенеративные свойства не уступающие, по крайней мере, таковым у хлорамфеникола и метилурацила контрольной мази сравнения Левомикон-ТФФ.
Пример 5. Получение образцов мазей, содержащих биологически активные вещества из высших базидиомицетов, в частности, образца №7 на основе комплекса меланина из природного сырья чаги Inonotus obliquus и суммарных полисахаридов из гриба вешенки Pleurotus ostreatus в соотношении 1:2 и определение in vivo их ранозаживляющей активности (данные представлены в таблицах 7-8).
Для получения 25,0 г меланинполисахаридсодержащей мази 0,25 г меланина и 0,5 г полисахарида растирали до мельчайшего порошка в фарфоровой ступке, затем последовательно добавляли 2,5 мл изотонического раствора, 2,5 г ланолина (эмульгатор) и вазелина -остальное до 25 г. продолжая при этом растирание смеси в ступке при 50-60°С до получения гомогенной мази, а затем расфасовывали. Ранозаживляющую активность мази образца №7 оценивали на модели кожной резаной раны аналогично алгоритму примеров 2 и 3 на животных, распределенных по следующим группам (по 20 мышей в каждой):
группа №1 - контрольная, мыши ничем не леченные;
группа №2 - контрольная, леченная мазью Левомикон-ТФФ;
группа №3 - опытная, леченная меланинполисахаридной мазью (образец №7).
Экспериментальных животных групп №№2-3 лечили ежедневно путем нанесения на раны шпателем 0,2 г мази Левомикона (группа №2) и 6,0 мг меланинполисахаридного комплекса (меланина - 2 мг и полисахарида - 4 мг) в 0,2 г мази (группа №3). Данные по оценке лечебных свойств и токсичности указанных выше опытных мазей представлены в табл.7-8.
Из данных, представленных в таблице 7, следует, что динамика показателей прироста массы тела у мышей, во всех группах животных была положительной. При этом значения этих показателей были очень близкими и практически не различались.
Подопытные животные в группах №№1-2 в течение первых пяти дней выглядели менее активными, по сравнению с мышами группы №3. На 18 сутки наблюдения прирост массы тела по группам у мышей достиг сопоставимых величин, что свидетельствовало об отсутствии негативного влияния, как со стороны компонентов мазевой основы, так и лечебных составляющих мази образца 7 - меланинполисахаридного комплекса на организм мышей.
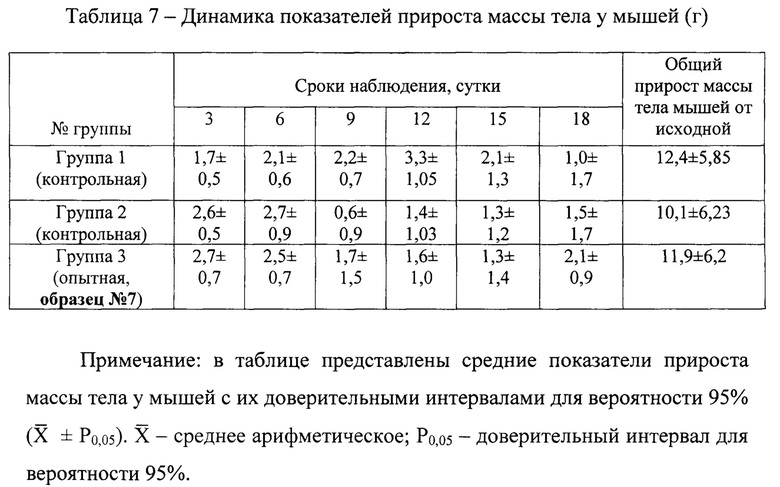
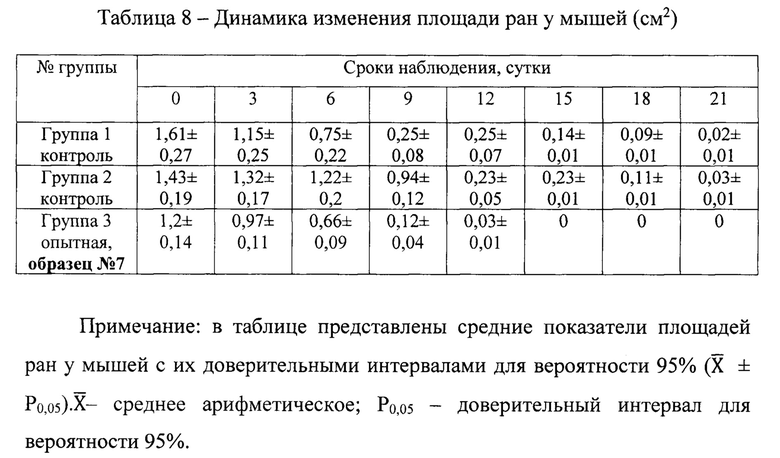
Динамика заживления ран между опытной группой животных (табл.8) и контрольными группами различалась. Визуально у мышей опытной группы №3, леченных меланинполисахаридсодержащей мазью (образец №7), корочки на ранах уже на 12 сутки отпали, раны зарубцевались, на поверхности рубцов покрытых отрастающей шерстью остались только следы от корочек размерами 0,01-0,03 см2. В то же время у мышей контрольных групп №1 и №2 аналогичный результат заживления ран у животных был получен только на 21 сутки.
Мазевая основа прописи ланолин (эмульгатор) с вазелином не обладает токсичностью для животных. При этом экспериментальная меланинполисахаридная мазь продемонстрировала, как противовоспалительные, так и регенеративные свойства меланинполисахаридного комплекса не уступающие, по крайней мере, таковым у хлорамфеникола и метилурацила контрольной мази сравнения Левомикон - ТФФ.
Таким образом, данные приведенные в примерах 2-5, подтверждают заявляемый технический результат, заключающийся в повышении ранозаживляющей активности мазевого средства на основе биологически активных веществ из базидиальных грибов Inonotus obliquus и/или Pleurotus ostreatus по сравнению с ближайшими аналогами и прототипом. Причем экспериментальные данные показывают, что дальнейшее увеличение концентрации меланина и/или полисахаридов в мазевой форме существенно не повышают ранозаживляющую способность заявляемой мазевой формы. Источники научно-технической и патентной информации
1. Гончар A.M., Коган А.С, Салганик Р.И. Раневой процесс и иммобилизованные протеолитические ферменты. Новосибирск, 1986, - 115 с.
2. Радаева И.Ф., Костина Г.А. Гиалуроновая кислота: очистка, свойства, применение // Биотехнология. - 1996. - №5. - С. 44-47.
3. Сандахчиев Л.С., Ставский Е.А., Зиновьев В.В. и др. Оценка воздействия мази, содержащей коллагеназу камчатского краба, на инфицированную рану в эксперименте // Бюллетень экспериментальной биологии и медицины. 1997, Том 124, N 10, с. 421-424.
4. Сандахчиев Л.С., Ставский Е.А., Зиновьев В.В. и др. Экспериментальное изучение лечебных свойств и токсичности мази, содержащей коллагеназу камчатского краба // Вестник РАМН, 1998, N 4, с. 50-55.
5. Теплякова Т.В., Косогова Т.А. Высшие грибы Западной Сибири -перспективные объекты для биотехнологии лекарственных препаратов. Новосибирск, 2014. - 298 с.
6. Сакович В.В. Базидиомицеты как источники биологически активных веществ/В.В. Сакович, Д. Д. Жерносеков//Вестник Полесского государственного университета. - 2018. - №1. - с. 3-13.
7. Саерова К.В., Мухтарова А.Р. Извлечение биологически активных компонентов из водного экстракта чаги / Саерова К.В., Мухтарова А.Р.//Молодежь и наука: шаг к успеху. - 2018. - с. 254-257.
8. Сушинская Н.В., Курченко В.П., Горовой Л.Ф., Сенюк О.Ф. Получение и использование в медицине меланинов из трутовых грибов // Успехи медицинской микологии. - 2005. - Т. 6. - С. 255-259.
9. Teplyakova T.V., Ilyicheva T.N., Andreeva I., Solovyanova N. The activity of components of true tinder mushroom, chaga Inonotus obliquus (Fr.) Pil. against viruses, bacteria and fungi // Abstract of the 10th International Medicinal Mushroom Conference (September 19-22, 2019, Nantong, China). P. 11.
10. Цветкова B.A., Пугач O.A., Андреева И.С., Ставский Е.А., Теплякова Т.В.Определение антибиотической активности грибов из коллекции ФБУН ГНЦ ВБ «Вектор» Роспотребнадзора/ Современные проблемы фитотерапии и травничества: Материалы 5-го международного съезда фитотерапевтов и травников (Москва, 19-20 января 2019 г. ) / под научной редакцией д.м.н., акад. РАЕН, проф. Корсуна В.Ф. - М.: Русские, 2019. - с. 390-394.
11. Ильичева Т.Н., Ананько Г.Г., Косогова Т.А., Олькин С.Е., Омигов В.В., Таранов О.С., Теплякова Т.В. Противовирусная активность меланина из чаги {Inonotus obliquus), полученного на основе культивирования штамма F-1244, выделенного в чистую культуру // Химия растительного сырья. 2020. №2. С. 283-289.
12. Teplyakova T.V., Ilyicheva T.N., Kosogova Т.A. Higher Fungi Against Influenza Viruses. International Journal of Medicinal Mushrooms-2021.-23 (2).-P. 1-11
13. Пат. 2480227 Российская Федерация, МПК А61К 36/06, А61К 31/785, А61Р 31/22, А61Р 31/12, А61Р 31/16, А61Р 31/18. Противовирусное средство на основе меланина / Т.В. Теплякова [и др.]; заявитель и патентообладатель Федеральное бюджетное учреждение науки «Государственный научный центр вирусологии и биотехнологии «Вектор». - №2011127305/15; заявл. 01.07.2011; опубл. 27.04.2013, Бюл. №12. - 11 с.
14. Пат. 2741714 Российская Федерация, МПК А61К 36/06, BOID 11/02, А61Р 31/14. Ингибитор репликации коронавируса SARS-CoV-2 на основе водного экстракта гриба Inonotus obliquus / Т.В. Теплякова [и др.]; заявитель и патентообладатель Федеральное бюджетное учреждение науки «Государственный научный центр вирусологии и биотехнологии «Вектор». -№2020127270; 13.08.2020; опубл. 28.01.2021, Бюл. №4. - 12 с.
15. Bindhi, J. Antimicrobial, antioxidant and anticancer activity of the ethanol extract of Pleurotus ostreatus/J.Bindhi [at al]//Jornal of nature remains. - 2020. - Vol. 20. - №2. - P. 110-115.
16. Вязовая E.A., Ананько Г.Г., Теплякова T.B., Оценка солнцезащитного потенциала грибного меланина, полученного из чаги (Inonotus obliquus) II Успехи медицинской микологии. - Т. 19. - М.: нац. акад. микол., 2018. - С. 265-272.
17. Савченко Ю.П., Федосова СР. Методы определения раневой поверхности. Вестник хирургии. 2007. - Т. - 166. - №1. - е. 102-105.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения средства на основе экстрактов из базидиальных грибов, обладающего противовирусным действием | 2023 |
|
RU2830096C1 |
| Способ получения биологически активных веществ из грибов | 2017 |
|
RU2657431C1 |
| Сухой оздоровительный напиток | 2016 |
|
RU2673042C2 |
| Штамм базидиального гриба Inonotus obliquus - продуцент пигмента меланина, обладающего противовирусной и противоопухолевой активностью | 2019 |
|
RU2716590C1 |
| Водорастворимый пигмент меланин из базидиального гриба Inonotus obliquus, обладающий противовирусной активностью | 2022 |
|
RU2800446C1 |
| ИНГИБИТОР РЕПРОДУКЦИИ ВИРУСА ИММУНОДЕФИЦИТА ЧЕЛОВЕКА ПЕРВОГО ТИПА | 2008 |
|
RU2375073C1 |
| ПРОТИВОВИРУСНОЕ СРЕДСТВО НА ОСНОВЕ МЕЛАНИНА | 2011 |
|
RU2480227C2 |
| ПРОТИВОЛУЧЕВАЯ КОМПОЗИЦИЯ НА ОСНОВЕ ХИТИНО-ГЛЮКАНОВОГО КОМПЛЕКСА ГРИБА ВЕШЕНКИ ОБЫКНОВЕННОЙ | 2022 |
|
RU2804298C1 |
| Ингибитор репликации коронавируса SARS-CoV-2 на основе меланина из гриба Inonotus obliquus | 2020 |
|
RU2747018C1 |
| Ингибитор репликации коронавируса SARS-CoV-2 на основе водного экстракта гриба Inonotus obliquus | 2020 |
|
RU2741714C1 |
Изобретение относится к фармацевтической промышленности, а именно к ранозаживляющему средству на основе биологически активных веществ из базидиальных грибов. Ранозаживляющая мазь для наружного применения, содержащая биологически активные вещества из базидиальных грибов и мазевую основу, включающую изотонический раствор, вазелин, которая в качестве биологически активных веществ из базидиальных грибов содержит меланин из природного сырья гриба чаги или глубинной культуры гриба чаги Inonotus obliquus, или суммарный полисахарид из вешенки обыкновенной Pleurotus ostreatus, или смесь вышеуказанных меланина и суммарного полисахарида в соотношении от 1:1 до 1:2, в качестве мазевой основы содержит также эмульгатор ланолин, количественное содержание компонентов из расчета 25 г мази составляет: биологически активные вещества из базидиальных грибов 0,25-0,75 г; изотонический раствор 2,5 мл; эмульгатор ланолин 2,5 г; вазелин остальное до 25 г; причем суммарный полисахарид вешенки обыкновенной получен путем измельчения вешенки обыкновенной гомогенизатором при соотношении биомасса : дистиллированная вода 1:5, прогревания грибного гомогената, осаждения полисахаридов из водного экстракта 96%-ным этиловым спиртом в соотношении водный экстракт : этиловый спирт 1:1, выдерживания в течение 18 часов при температуре 6±2°С, центрифугирования в течение 20 минут при 10000 об/мин, высушивания полученной надосадочной жидкости с суммарными полисахаридами. Вышеописанная мазь обладает повышенной ранозаживляющей активностью. 3 з.п. ф-лы, 8 табл., 5 пр.
1. Ранозаживляющая мазь для наружного применения, содержащая биологически активные вещества из базидиальных грибов и мазевую основу, включающую изотонический раствор, вазелин, отличающаяся тем, что в качестве биологически активных веществ из базидиальных грибов она содержит меланин из природного сырья гриба чаги или глубинной культуры гриба чаги Inonotus obliquus, или суммарный полисахарид из вешенки обыкновенной Pleurotus ostreatus, или смесь вышеуказанных меланина и суммарного полисахарида в соотношении от 1:1 до 1:2, в качестве мазевой основы содержит также эмульгатор ланолин, количественное содержание компонентов из расчета 25 г мази составляет:
причем суммарный полисахарид вешенки обыкновенной получен путем измельчения вешенки обыкновенной гомогенизатором при соотношении биомасса : дистиллированная вода 1:5, прогревания грибного гомогената, осаждения полисахаридов из водного экстракта 96%-ным этиловым спиртом в соотношении водный экстракт : этиловый спирт 1:1, выдерживания в течение 18 часов при температуре 6±2°С, центрифугирования в течение 20 минут при 10000 об/мин, высушивания полученной надосадочной жидкости с суммарными полисахаридами.
2. Мазь по п. 1, отличающаяся тем, что она содержит в качестве биологически активных веществ из базидиальных грибов меланин из природного сырья или глубинной культуры гриба чаги Inonotus obliquus, в качестве мазевой основы - изотонический раствор, вазелин и эмульгатор ланолин, а количественное содержание компонентов из расчета 25 г мази составляет:
3. Мазь по п. 1, отличающаяся тем, что она содержит в качестве биологически активных веществ из базидиальных грибов суммарный полисахарид из вешенки обыкновенной Pleurotus ostreatus, в качестве мазевой основы - изотонический раствор, вазелин и эмульгатор ланолин, а количественное содержание компонентов из расчета 25 г мази составляет:
4. Мазь по п. 1, отличающаяся тем, что она содержит в качестве биологически активных веществ из базидиальных грибов смесь меланина из природного сырья или глубинной культуры гриба чаги Inonotus obliquus и суммарного полисахарида из природного сырья гриба вешенки обыкновенной Pleurotus ostreatus в соотношении от 1:1 до 1:2, в качестве мазевой основы - изотонический раствор, вазелин и эмульгатор ланолин, а количественное содержание компонентов из расчета 25 г мази составляет:
| ПУГАЧ О.А | |||
| и др | |||
| Кипятильник для воды | 1921 |
|
SU5A1 |
Авторы
Даты
2022-12-30—Публикация
2022-02-04—Подача