Изобретение относится к новому штамму базидиального гриба Inonotus obliquus - продуцента меланина, обладающего противовирусным и противоопухолевым действием, и может быть использовано в биотехнологии, фармацевтической промышленности для получения медицинских препаратов, в косметической промышленности для изготовления кремов, лосьонов, тоников, в пищевой промышленности для полученияи биологически активных добавок.
Получение меланиновых пигментов из биомассы мицелия и культуральной жидкости (КЖ) чаги на основе эффективных штаммов-продуцентов является очень актуальным направлением медицинской биотехнологии.
Известен целый ряд культур микроорганизмов, синтезирующих меланиновый пигмент в небольших количествах, - Microsporum ganis, Trichophyton rubrum (Малама А.А. и Касперович T.B. Изучение пигментов грибов Microsporum ganis и Trichophyton rubrum // Микология и фитопатология. - Т. 10. - Ленинград, 1976. - С. 422).
Для промышленного производства эти культуры интереса не представляют.
Известен меланинообразующий штамм гриба Cladosporium cladosporidies-396 (А.с. СССР 1063834А, МПК C12N 15/00; C02F 3/34; C12R 1/645, опубл. 1983), предложенный авторами для связывания тяжелых металлов при очистке сточных вод. Гриб является аэробом, оптимум роста и спороношения при 25°С, оптимальное значение активности воды равно 0,98, оптимальная кислотность среды рН 4-5, высокоустойчив к тотальным дозам УФ и γ-излучения, искусственному солнечному свету высокой интенсивности. Гриб усваивает нитратные формы азота, в качестве источника углерода использует глюкозу, сахарозу, крахмал, пектин, целлюлозу, лимонную, щавелевую, уксусную кислоты, обладает целлюлозолитической и тиразиназной активностью. Образующуюся при росте гриба биомассу отделяют фильтрованием от культуральной жидкости и высушивают при 60°С. Выход биомассы гриба составляет 15-20 г/л. Меланиновый пигмент выделяется из биомассы гриба по модифицированному методу путем гидролиза ее немеланиновых компонентов при кипячении в смеси уксусной и соляной кислот.
Однако, штамм не находит практического применения, так как имеет невысокую меланинообразующую способность и, являясь аэробом, требует значительных затрат для промышленного культивирования.
Известно использование гриба Inonotus obliquus для профилактики и лечения желудочно-кишечных заболеваний [Патент RU 2076728, МПК A61K 35/78, опубл. 10.04.1997.].
Известно биостимулирующее средство, одним из компонентов которого является березовый гриб чага (Inonotus obliquus) [Патент RU 2125460, МПК A61K 35/78, опубл. 27.01.1999 г. ].
Известен состав, обладающий противоопухолевым, гепатопротекторным и иммуностимулирующим действием, в котором чага используется в качестве добавки к листовому или гранулированному чаю [Патент RU 2125460, МПК A61K 35/78, опубл. 20.01.2004 г.].
Известно противовирусное средство на основе меланина из природной чаги Inonotus obliquus (Патент RU №2480227, МПК C12N 1/14; A61K 36/06, опубл. 27.04.2013 г.), в котором 2,5%-ный водный раствор меланинов из склероция чаги проявлял противовирусный эффект в отношении вируса простого герпеса 2 типа (ВПГ-2), вируса иммунодефицита человека (ВИЧ-1), вируса гриппа (ВГ) и вируса осповакцины (ВОВ).
Однако во всех выше приведенных изобретениях используется природное сырье из склероциев (бесплодных тел чаги), произрастающих на деревьях, а не чистая культура штамма чаги, выращенная в стерильных глубинных условиях.
Известен штамм гриба Aspergillus niger БМП-97/2 (КПМКБ-Г-1-9) для производства меланина (патент Республики Беларусь №5057, МПК C12N 1/14, опубл. 30.03.2003 г.). Штамм получен путем многоступенчатой селекции культуры, выделенной из плесневого налета на стенах бытовых помещений. Штамм депонирован в коллекции промышленных микроорганизмов концерна "Белбиофарм", регистрационный номер Г-1-9 от 1.09.1999. Гриб является факультативным анаэробом, растет в интервале температур от 18 до 40°С. Оптимальная температура для роста культуры - 28°С, биосинтеза меланина - 37°С. Оптимальный рН - 6,5±0,5. Синтезирует меланин внутри клеток и внеклеточно. В качестве источника углерода гриб использует большинство сахаров (глюкоза, сахароза, мальтоза, арабиноза), не усваивает этиловый спирт. Коагулирует и пептонизирует молоко, разжижает желатин. Обладает протеазной и оксидазной активностью. Гриб выращивают на косяках (сусло-агар) 14 сут., суспензию спор получают 14 сут. Ферментацию культуры ведут в анаэробных условиях при температуре 37±1°С в течение 20 сут. Получают 12 г меланина технического, после растворения которого в 40% растворе едкого натра, нейтрализации и сушки получают 8 г субстанции меланина. Культура используется в производстве лекарственных форм на основе меланина в АО "Белмедпрепараты".
Однако штамм имеет ряд недостатков: длительный процесс получения посевного спорового материала гриба (два пересева по 14 сут.) - всего 28 сут.; длительная ферментация культуры гриба (20 сут.); анаэробные условия культивирования, что усложняет технологичность процесса выращивания культуры; синтез меланина при высокой температуре - 37±1°С; использование спорообразующей культуры, что загрязняет окружающую среду и может вызвать аллергию у работающих.
Известен штамм I. obliquus БИМ F-350 Д БИМ F-350 Д - продуцент меланина, обладающий антимутагенными свойствами (Патент Республики Беларусь №10670, МПК C12N 1/14, С12Р 19/00, опубл. 30.06.2008 г.). Штамм I. obliquus БИМ F-350 Д является аэробом, способен расти в интервале температур 18-30°С, оптимальная температура для роста 24-25°С, оптимальные значения рН 6,0-7,0. Характеризуется синтезом экзо- и эндомеланинов. Исследования антимутагенной активности меланинсодержащей субстанции на самцах мышей линии "Af" показало, что внутрибрюшинное введение ее в дозе 50 мг/кг веса животного снижает уровень радио индуцированных транслокаций в сперматоцитах в 2 раза, что свидетельствует о высоких антиоксидантных и генопротекторных свойствах меланин-содержащей субстанции гриба I. obliquus БИМ F-350 Д.
Однако при культивировании на агаризованной среде (сусло-агар) в чашках Петри при температуре 24-25°С полное зарастание чашки наблюдается только к 20-23 суткам, скорость роста колоний составляет 2-2,3 мм/сут., длительное время для наработки посевного материала на жидкой среде (7 суток), жидкая питательная среда содержит относительно дорогостоящие компоненты, которые мало применяются в промышленном микробиологическом производстве (пивное сусло, тиамин, тирозин). Применяется относительно высокое количество посевного материала, 15%. Отмечается также невысокий выход меланинсодержащей биомассы - 12 г/л. Из культуральной жидкости наблюдается низкий выход меланина - 1,3 г/л.
Кроме того, меланин из штамма гриба-прототипа не исследовался на противовирусную активность.
Заявляемый новый штамм имеет преимущества по сравнению с выше указанным штаммом-аналогом по количеству накапливаемой в среде ГТС биомассы, содержащей меланин, и по количеству выделяемого меланина из культуральной жидкости. В таблице 1 приведены сравнительные характеристики заявляемого штамма Inonotus obliquus TV-18, штамма-аналога Inonotus obliquus БИМ F-350.
Наиболее близким аналогом (прототипом), является штамм Inonotus obliquus F-1244, выделенным нами из склероция чаги, привезенного из Тувы (Косогова Т.А. Штаммы базидиальных грибов юга Западной Сибири - перспективные продуценты биологически активных препаратов: автореф. Диссертации канд. биол. наук, 03.01.06., Кольцово, 2013. - с. 26).
Однако штамм-прототип имеет недостаточное количество накапливаемой в среде ГТС биомассы, содержащей меланин и количество выделяемого меланина. Кроме того, нет данных о противоопухолевой активности штамма-прототипа.
Техническим результатом заявляемого изобретения является получение штамма базидиального гриба Inonotus obliquus - продуцента меланиновых пигментов, имеющего более высокую продуктивность при наработке биомассы гриба, содержащей меланин и более высокий выход меланиновых пигментов из культуральной жидкости, обладающих как противовирусным, так и противоопухолевым действием.
Указанный технический результат достигается получением нового штамма базидиального гриба Inonotus obliquus - продуцента меланиновых пигментов, обладающих противовирусной и противоопухолевой активностью, депонированного в коллекции бактерий, бактериофагов и грибов ФБУН ГНЦ ВБ Вектор (р.п. Кольцово, Новосибирская обл.) под номером F-1375 (справка прилагается).
Заявляемый штамм имеет следующие характеристики.
Штамм Inonotus obliquus TV-18 (авторское наименование) выделен в 2018 году из природного склероция чаги, найденного на березе вблизи р.п. Кольцово Новосибирской области. Штамм Inonotus obliquus TV-18 имеет следующие культурально-морфологические и физиолого-биохимические признаки.
Колонии на агаризованной среде на основе овсяного отвара ватообразные, белого цвета, переходящего в желто-соломенный, песочный и коричневый цвета. Гифы септированные, тонкостенные, без пряжек, гиалиновые до желтоватых, ветвящиеся, 2-4 мкм в диаметре, переходящие в толстостенные, ржаво-бурые, параллельно расположенные гифы 3,5-7 мкм в диаметре. На агаризованных питательных средах часто формирует плодовые тела от светло-коричневого до темно-коричневого цвета с неровной поверхностью.
Выращивают (культивируют) штамм на агаризованных и жидких питательных средах при температуре 24-27°С.Скорость роста колонии - чашка Петри зарастает за 8-9 суток.
Состав жидкой среды. Глюкозо-триптонная среда (ГТС), г/л: глюкоза - 30; триптон - 10,0; дрожжевой экстракт - 5,0; КН2РО4 - 1,1; K2HPO4 - 4,4; MgSO4 х 7 H2O- 0,25 г/л; вода - 1 л, значение рН 7-8. При культивировании на глюкозо-триптонной среде к 9-м суткам питательная среда приобретает темно-коричневый цвет за счет выделения в нее меланина.
Состав агаризованной среды. Жидкая среда ГТС, 20 г агар-агара из расчета на 1 л раствора.
Изобретение поясняется следующими графическими материалами.
На фиг. 1 приведены результаты исследований чувствительности популяции клеток эпидермоидной карциномы человека А431 к действию меланина. На фиг. 2 представлены данные по оценке противоопухолевой активности меланина из глубинной культуры чаги Inonotus obliquus TV-18 на опухолевой модели ксенографтов эпидермоидной карциномы кожи человека А-431 при многократном введении. На фиг. 3 представлены колонии штамма чаги I. obliquus F-1375 (TV-18), а на фиг. 4 - плодовое тело штамма чаги I. obliquus F-1375 (TV-18) на среде ГТС.
Пример 1. Выращивание биомассы мицелия на основе штамма Inonotus obliquus TV-18 в глубинных условиях на качалке.
Выращивание чаги осуществляли в глюкозо-триптонной среде (ГТС) в глубинных условиях на круговой качалке (скорость вращения 180-200 об./мин, 25±2°С). Засев колб осуществляли культурой с этой же среды, только агаризованной, включающей 20 г агар-агара на 1 л. Из колоний в чашках Петри стерильным пробочным сверлом диаметром 10 мм вырезали блоки и вносили по 10 шт в колбы (500 мл) с жидкой средой объемом 100 мл. После 3-х суток культивирования жидкую культуру использовали для засева новых колб в дозе 10% (10 мл на 100 мл жидкой среды). Начиная с 8-9 суток роста на качалке, питательная среда приобретала темно-коричневый цвет за счет выделяющегося в нее меланина.
В этот период в культуре наблюдались многочисленные фрагменты гиф коричневатого цвета.
Для получения меланина ферментацию на качалке заканчивали на 10 сутки. В таблице 1 представлены данные по накоплению биомассы и меланина в глубинной культуре чаги штаммом-аналогом Inonotus. obliquus БИМ F-350 Д, штаммом-прототипом Inonotus. obliquus F-1244 и новым штаммом I. obliquus TV-18.
Выход биомассы штамма чаги I. obliquus TV-18 по сухим веществам составляет в среднем 18,2 г/л. В сравнении со штаммом-прототипом Inonotus obliquus F-1244 это больше на 1 г/л (таблица 1).

Общий выход меланина заявляемого штамма I. obliquus TV-18 составляет 7,5 г/л, а у прототипа I. obliquus F-1244 выход меланин 6,0 г/л.
Таким образом, заявляемый штамм имеет преимущества по времени культивирования, по количеству накапливаемой в среде ГТС биомассы, содержащей меланин и по количеству выделяемого меланина из культуральной жидкости.
Пример 2. Выделение меланина из культуральной жидкости
После культивирования гриба на качалке мицелий отделяли от темно-коричневой культуральной жидкости фильтрованием через капроновый фильтр. Культуральную жидкость после отделения бимассы гриба доводили HCl до рН=2,0 и центрифугировали. Осадок, содержащий меланин, доводили 0,01 н. NaOH до рН=7,0 (до растворения меланина) и подвергали очистке. Очистка меланина включала последовательное 3-х кратное переосаждение с последующей 3-х кратной промывкой осадка меланинов в 0,1 н растворе соляной кислоты. Полученный, после 3-х кратного переосаждения, осадок меланина промывали подкисленной водой. Очищенные меланины ресуспендировали в дистиллированной воде, переносили в мерный стакан, доводили рН до значения 7-8 единиц с помощью 40% раствора NaOH. Выход меланина из культуральной жидкости составляет 2,5-3,0 г/л. Из общей массы, содержащей меланин, выход сухих меланинов составляет 7,0-7,5 г/л. Высушенный меланин представляет собой блестящие кристаллы, а после помола - коричневатый матовый порошок.
Пример 3. Проведение контроля качественных и количественных показателей меланина
Для проверки принадлежности выделенных пигментов к меланинам проводили три качественных теста на присутствие в их молекуле хиноидных и фенольных структур. Для проведения качественных реакций готовили 0,1% раствор пигмента (15 мг пигмента растворяли в 15 мл 0,1 Н раствора NaOH). Затем проводили следующие процедуры:
- 5 мл раствора пигмента переливали в пробирку вместимостью 10 мл и приливали 0,5 мл 10% перекиси водорода. Положительная реакция - обесцвечивание раствора.
- 5 мл раствора пигмента переливали в пробирку вместимостью 10 мл и приливали 0,1 мл 0,1 М раствора KMnO4. Положительная реакция - раствор зеленеет.
- 5 мл раствора пигмента переливали в пробирку вместимостью 10 мл и приливали 0,1 мл 5% раствора FeCl3. Положительная реакция - образуются крупные коричневые хлопья, в растворе с избытком хлорида железа осадок растворяется.
Готовили 0,001% раствор меланина: для этого 10 мг порошка меланина растворяли в 100 мл 0,1 Н раствора NaOH. Затем с помощью спектрофотометра измеряли оптическую плотность раствора при длине волны 465 нм (ОФС.1.2.1.0003.15), используя в качестве контроля 0,1 Н раствор NaOH. Оптическая плотность 0,001%) раствора меланина была не менее 0,040 единицы.
Пример 4. Определение токсичности и противовирусной активности меланина, выделенного из жидкой культуры штамма чаги Inonotus obliquus TV-18
Работу с вирусами гриппа проводили на культуре клеток MDCK, используя вирус A/California/07/09 (H1N1 pdm09) из коллекции ФБУН ГНЦ ВБ Вектор. Для работы с вирусом иммунодефицита человека использовали линию клеток человека МТ-4 и штамм ВИЧ-1 - MTZN, субтип А.
Определение токсичности и противовирусной активности меланина в отношении вируса простого герпеса 2 типа проводили в культуре клеток Vero. В работе был использован штамм MS вируса простого герпеса 2 типа (получен из Американской коллекции типовых культур).
Исследования проведены в вирусологических лабораториях в соответствии с правилами и методиками работ с культурами клеток и вирусами (Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ / Под общей редакцией члена-корреспондента РАМН, профессора Р.У. Хабриева. - 2-изд., перераб. и доп.- М.: ОАО «Издательство «Медицина», 2005. - 832 с.). Данные по токсичности и противовирусной активности меланина из глубинной культуры Inonotus obliquus TV=18 в отношении вируса гриппа, штамма A/California/07/09 (H1N1 pdm09), ВИЧ-1, вируса простого герпеса 2 типа приведены в таблице 2.
Как видно из таблицы 2, образец нового штамма Inonotus obliquus TV-18 на всех вирусах в независимых исследованиях проявил себя наилучшим образом.
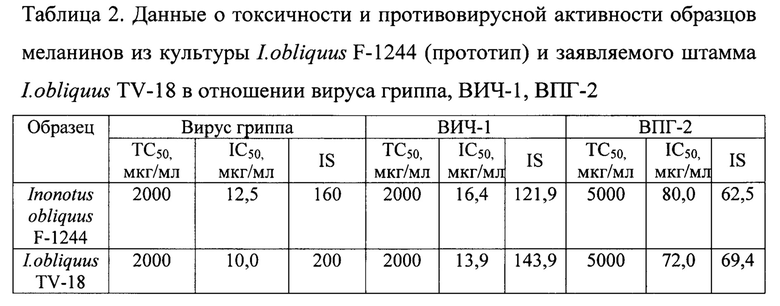
Примечания: ТС50 - 50% токсическая концентрация меланина, доза меланина, подавляющая рост клеток на 50%; IC50 - 50% ингибирующая концентрация меланина, доза меланина, ингибирующая размножение вируса на 50%; IS - индекс селективности, или терапевтический индекс: равен отношению 50%-ной токсической дозы препарата к 50%-ной ингибирующей дозе (TC50/IC50).
При низкой токсичности меланин из глубинной культуры чаги Inonotus obliquus TV-18 показал противовирусный эффект в отношении вируса гриппа A/California/07/09 (H1N1 pdm09), IC50=10,0 мкг/мл, IS=200, вируса иммунодефицита человека (ВИЧ-1, субтип A, MTZN), IC50=13,9 мкг/мл, IS=143,9), герпеса (ВПГ-2, штамм MS), IC50=72 мкг/мл, IS=69,4).
Полученные данные свидетельствуют о перспективности получения меланина из культуральной жидкости и биомассы штамма чаги Inonotus obliquus TV-18, обладающего противовирусной активностью.
Пример 5. Оценка цитотоксического действия препарата меланина на культуре клеток эпидермоидной карциномы человека А 431.
Анализ цитотоксического действия препарата меланина в отношении клеток эпидермоидной карциномы человека А431 проводили с помощью МТТ-теста, который позволяет оценивать уровень жизнеспособности клеток по их способности к восстановлению 3-(4,5-диметилтиазолил-2)-2,5 - дифенилбромидтетразолиевого (МТТ) [Mosmann Т. Rapid colorimetric assay for cellular growth and survival: application to proliferation and cytotoxicity assays. J Immunol Methods. 1983 Dec 16; 65(l-2):55-63].
Клетки карциномы помещали по 104/лунку в 96-луночные микропланшеты (ТРР, Швейцария) в полной среде DMEM (Биолот) с 10% эмбриональной телячьей сывороткой (HyClone, США) и 0,04 мг/мл гентамицина. Через сутки от начала культивирования в лунки вносили водный раствор меланина в убывающих концентрациях (от 95,7 до 0,37 мкг/мл), каждое разведение исследовали в 6 повторах, в контрольные лунки вносили физиологический раствор. Клетки инкубировали в СО2-инкубаторе (SHEL-LAB, США) при температуре 37°С в течение 72 часов, затем измеряли оптическую плотность восстановленного МТТ-реагента (Sigma - Aldrich) на ридере Multiskan EX (Thermo, Финляндия) при длине волны 540 нм. По соотношению оптической плотности опытных и контрольных лунок рассчитывали процент живых клеток для каждого разведения исследуемого препарата (индекс МТТ, %=ОПопыт/ОПконтроль ×100). Экспериментальные данные обрабатывали методами вариационной статистики с помощью пакета программ "Statgraphics, Vers.5.0". Для оценки значимости межгрупповых различий использовали U-критерий Манна-Уитни, критический уровень значимости при проверке статистических гипотез (р) принимали равным 0,05.
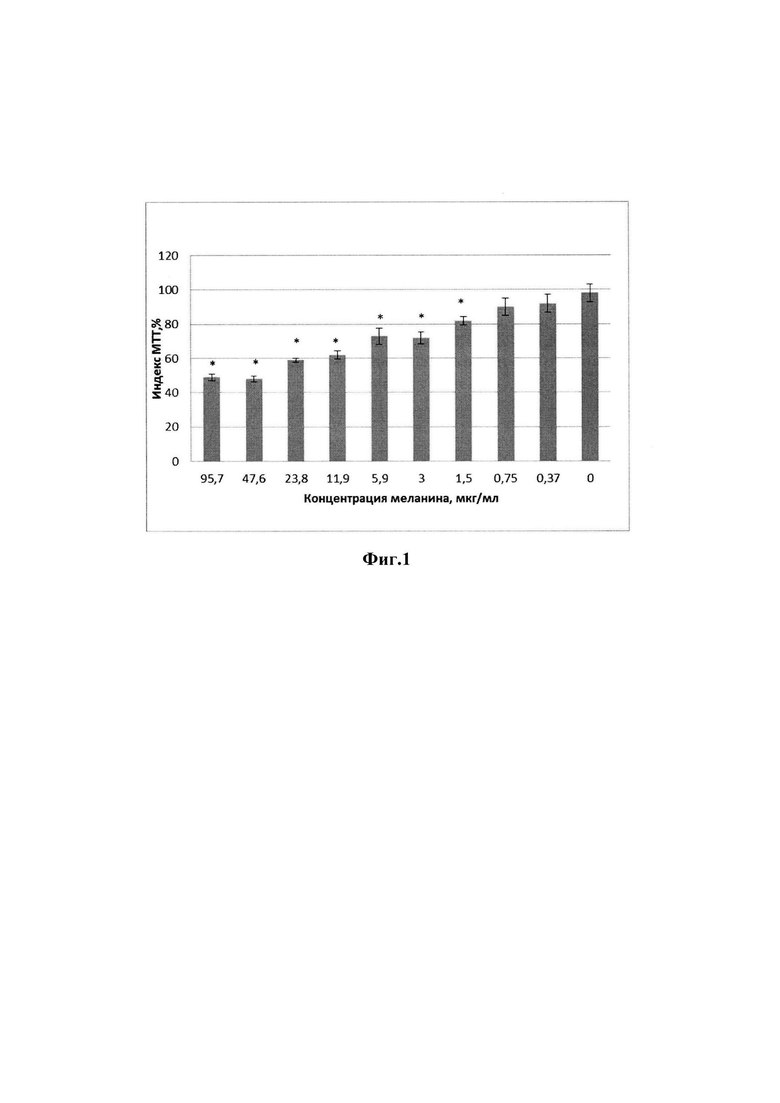
На фиг. 1 представлен процент живых клеток эпидермоидной карциномы А431 после инкубации с препаратом меланина в течение 72 часов. * - достоверное отличие от контроля, р≤0,05.
Исследование показало, что до 50% популяции клеток карциномы А431 оказались чувствительными к действию меланина (Фиг. 1).
Цитотоксический эффект препарата носил дозозависимый характер. Достоверные различия индекса МТТ опухолевых клеток, инкубированных с меланином, и клеток контрольных лунок наблюдались в интервале концентраций от 95,7 до 1,5 мкг/мл; наиболее выраженные изменения были отмечены при инкубации с препаратом в максимальной использованной дозе. Полученные данные подтверждают наличие у препарата меланина прямого противоопухолевого действия.
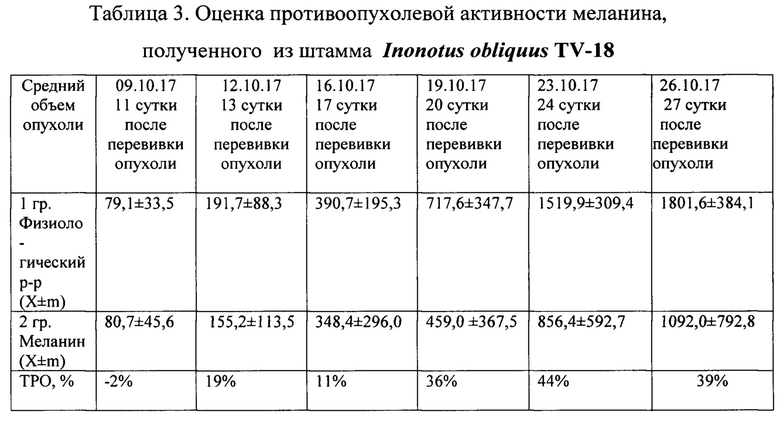
Пример 6. Оценка противоопухолевой активности меланина из глубинной культуры чаги Inonotus obliquus TV-18 на опухолевой модели ксенографтов эпидермоидной карциномы человека А-431 при многократном введении.
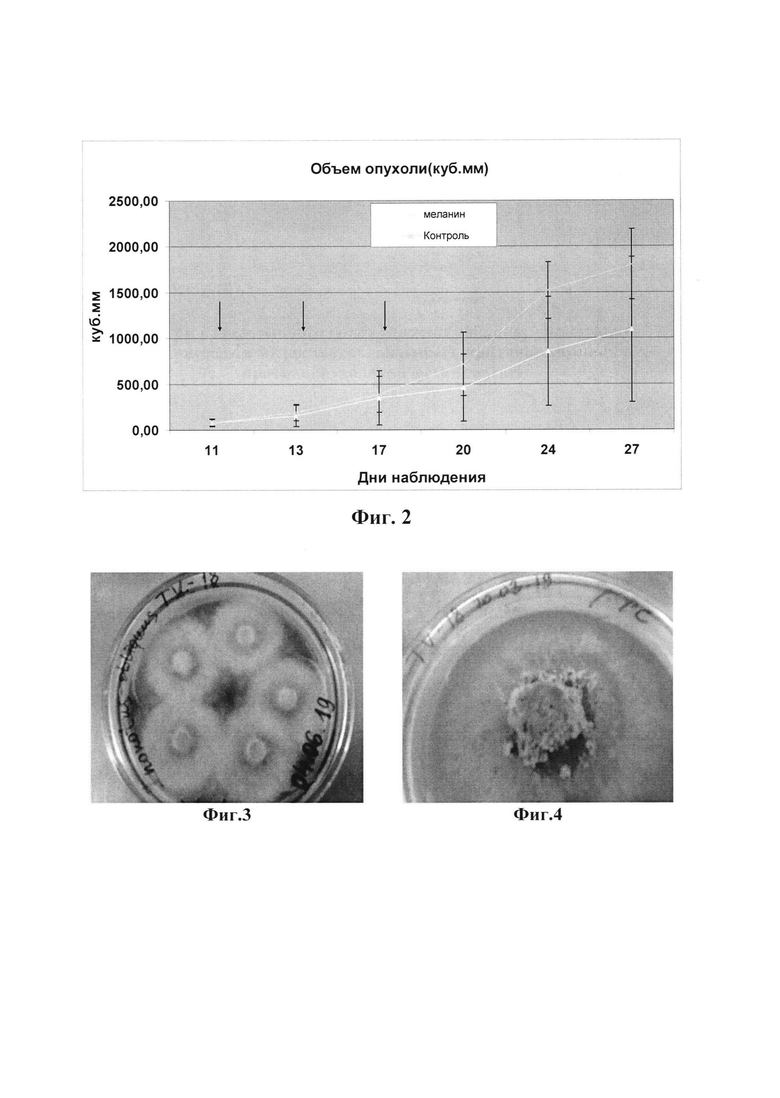
В работе использовали самок мышей линии nude в возрасте 6-8 нед, весом 18-20 г. Для формирования опухолей мышам вводили суспензию клеток эпидермоидной карциномы человека А-431 подкожно в дозе 5,5*106 клеток/мышь в объеме 0,1 мл физиологического раствора (0,9% NaCl) в левый бочок мыши ближе к бедру. Время формирования опухолей (ксенографтов) составляло 8 дней, после которых в эксперимент было отобрано 18 мышей с опухолями объемом 60-100 мм3. Мышей разделили на две группы: опытную и контрольную (n=8 и n=10). Мышам опытной группы 3 раза с интервалом 2-4 дня (на 11, 13, 17 сутки после перевивки опухоли) в район опухоли вводили препарат меланина из глубинной культуры чаги Inonotus obliquus TV-18 в дозе 0,4-0,2 мг на мышь в объеме 0,1 мл. Мышам контрольной группы аналогично вводили 100 мкл 0,9%-го NaCl. Общий период наблюдения составил 27 дней. Каждые 2-3 дня перед инъекцией препарата и далее до конца эксперимента проводили замер линейных размеров опухоли в двух взаимно перпендикулярных направлениях. Противоопухолевый эффект препарата оценивали по изменению объема опухолевого узла и проценту торможения роста опухоли. Объем опухоли вычисляли по формуле: V (мм)=0,5*а*b*b, где a, b - длина, ширина, мм, соответственно. Процент торможения роста опухоли вычисляли по формуле: ТРО (%)=(Vк-Vо)/Vк⋅100, где Vк -средний показатель объема опухоли в контрольной группе; Vо - средний показатель объема опухоли опытной группы. Результаты эксперимента показали (фиг. 2), что в контрольной группе животных наблюдался постоянный рост опухоли, которая к 27 дню достигла размеров (1801,6±384,1) мм3. Четверо из восьми животных погибли в разные сроки наблюдения. В опытной группе животных погибло трое животных из 10 в первые дни эксперимента, средняя величина опухоли к 27 дню составила (1092,0±792,8) мм3. Эффект торможения был отмечен через 2 суток после первой инъекции препарата и сохранялся до конца эксперимента (7 суток после окончания введения), достигая максимума ТРО 44% через 7 суток после последнего введения препарата. Через 10 суток после последнего введения препарата эффект ТРО снизился и составил 39%. Показано, что трехкратное, с интервалом в 2-4 суток, интратуморальное введение меланина в дозе 0,2-0,4 мг/мышь на опухолевой модели ксенографтов эпидермоидной карциномы кожи человека А-431 оказывало ингибирующий эффект на развитие опухоли. Величина торможения роста опухоли при введении препарата составила 44%, эффект ингибирования сохранялся в течение 10 суток после введения (таблица 3).
Приведенные примеры 1-6 подтверждают достижение заявляемого технического результата, который заключается в получении штамма базидиального гриба Inonotus obliquus TV-18 (депонирован под номером F-1375) - продуцента меланиновых пигментов, имеющего по сравнению с прототипом (штамм Inonotus obliquus F-1244) более высокую продуктивность при наработке в среде ГТС биомассы гриба, содержащей меланин и более высокий выход меланиновых пигментов из культуральной жидкости, обладающих как противовирусным, так и противоопухолевым действием.
| название | год | авторы | номер документа |
|---|---|---|---|
| Водорастворимый пигмент меланин из базидиального гриба Inonotus obliquus, обладающий противовирусной активностью | 2022 |
|
RU2800446C1 |
| ПРОТИВОВИРУСНОЕ СРЕДСТВО НА ОСНОВЕ МЕЛАНИНА | 2011 |
|
RU2480227C2 |
| Способ получения средства на основе экстрактов из базидиальных грибов, обладающего противовирусным действием | 2023 |
|
RU2830096C1 |
| Ингибитор репликации коронавируса SARS-CoV-2 на основе меланина из гриба Inonotus obliquus | 2020 |
|
RU2747018C1 |
| Ранозаживляющая мазь для наружного применения | 2022 |
|
RU2787233C1 |
| Питательная среда для культивирования базидиального гриба Inonotus obliquus | 2021 |
|
RU2808749C2 |
| ИНГИБИТОР РЕПРОДУКЦИИ ВИРУСА ИММУНОДЕФИЦИТА ЧЕЛОВЕКА ПЕРВОГО ТИПА | 2008 |
|
RU2375073C1 |
| Ингибитор репликации коронавируса SARS-CoV-2 на основе водного экстракта гриба Inonotus obliquus | 2020 |
|
RU2741714C1 |
| Штамм базидиального гриба Daedaleopsis confragosa, содержащий белки, проявляющие противоопухолевую и противовирусную активность | 2017 |
|
RU2663111C1 |
| ИНГИБИТОР РЕПРОДУКЦИИ ВИРУСА ГРИППА А НА ОСНОВЕ ЭКСТРАКТА БАЗИДИАЛЬНОГО ГРИБА Phallus impudicus | 2011 |
|
RU2475529C2 |
Изобретение относится к биотехнологии. Штамм базидиального гриба Inonotus obliquus TV-18, обладающий противовирусной и противоопухолевой активностями, депонирован в коллекции бактерий, бактериофагов и грибов ФБУН ГНЦ ВБ Вектор под регистрационным номером F-1375. Штамм базидиального гриба Inonotus obliquus может быть использован для получения медицинских препаратов, кремов, лосьонов, тоников и биологически активных добавок. Изобретение позволяет повысить выход меланина. 4 ил., 3 табл., 6 пр.
Штамм базидиального гриба Inonotus obliquus - продуцент пигмента меланина, обладающего противовирусной и противоопухолевой активностью, депонированный в коллекции бактерий, бактериофагов и грибов ФБУН ГНЦ ВБ Вектор Роспотребнадзора под номером F-1375.
| Прибор для определения уровня жидкости в сосуде | 1928 |
|
SU10670A1 |
| Ручная косилка | 1925 |
|
SU5057A1 |
| АНАНЬКО Г.Г., ТЕПЛЯКОВА Т.В | |||
| и др | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| XIV, с | |||
Авторы
Даты
2020-03-12—Публикация
2019-09-30—Подача