Настоящая заявка испрашивает приоритет на основании заявок на патент Китая №№2019102824189, 2019102824225, 2019102824174, 201910282416Х и 2019102819867, поданных в Национальное управление по интеллектуальной собственности Китая 9 апреля 2019 года, каждая из которых включена в данный документ в полном объеме посредством ссылки.
ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится к технической области биомедицинских материалов и в частности к биомиметическому материалу, подавляющему рост льда, и криоконсервирующему раствору, содержащему этот материал.
УРОВЕНЬ ТЕХНИКИ
Криоконсервация представляет собой сохранение биологического материала при сверхнизких температурах, замедляющих или останавливающих метаболизм и деление клеток, с возможностью продолжения их развития после восстановления нормальных физиологических температур. С момента ее создания данная технология стала одной из самых незаменимых исследовательских методик в области естественных наук и была широко принята повсеместно. В последнее время, ввиду нарастающего напряжения современной жизни, год от года наблюдается тенденция к снижению репродуктивной способности у людей, и, соответственно, сохранение репродуктивной способности становится все более и более насущным. Важным средством сохранения репродуктивной способности становится криоконсервация половых клеток человека (сперматозоидов и ооцитов), гонадных тканей и т.п. Кроме того, поскольку мировая человеческая популяция становится все более возрастной, быстро растет потребность в криоконсервации донорских человеческих клеток, тканей или органов, которые могут быть использованы для регенеративной медицины и трансплантации органов. Следовательно, вопрос эффективной криоконсервации ресурсов ценных клеток, тканей и органов на случай непредвиденных ситуаций становится научно-технической проблемой, требующей неотложного решения.
В настоящее время наиболее распространенным способом криоконсервации является витрификация. Технология витрификации предполагает применение проникающего или непроникающего криопротектора. И хотя жидкость внутри и снаружи клетки может быть витрифицирована непосредственно в ходе процесса быстрой заморозки, что позволяет избегать повреждений, связанных с формированием кристаллов льда в процессе замораживания, криоконсервирующие реагенты, известные из современного уровня техники, не обеспечивают эффективного сдерживания роста кристаллов льда в ходе процесса размораживания, что приводит к повреждениям клеток. Поскольку механизмы подавления роста льда у антифризных белков и биомиметических материалов, подавляющих рост льда, на молекулярном уровне все еще неоднозначны и вызывают споры, научно-исследовательские работы в области биомиметических материалов, подавляющих рост льда, базируются на методе «проб и ошибок», т.е. эффект подавления роста льда проверяют у конкретного материала, испытываемого в качестве ингибитора роста льда, что связано с высокой трудоемкостью процесса исследований и низкой вероятностью успеха. Криоконсервирующие реагенты, обычно используемые в настоящее время, характеризуются проблемами, связанными с их неспособностью эффективно сдерживать рост кристаллов льда в ходе процесса размораживания, а также с их высокой токсичностью.
РАСКРЫТИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
Для преодоления недостатков существующего уровня техники в настоящем изобретении предложен способ молекулярного проектирования биомиметических материалов, подавляющих рост льда, и способ скрининга материалов, подавляющих рост льда, руководствуясь которыми исследователи могут целенаправленно синтезировать и отбирать биомиметический материал, подавляющий рост льда. В настоящем изобретении также предложен биомиметический материал, подавляющий рост льда, полученный согласно указанному способу, и криоконсервирующий реагент, содержащий указанный материал.
В настоящем изобретении предложены следующие технические решения:
Согласно первому аспекту настоящего изобретения предложен способ молекулярного проектирования материалов, подавляющих рост льда, включающий следующие стадии:
(1) создание библиотеки структур молекул соединений, в которой указанные молекулы соединений содержат гидрофильную группу и группу, имеющую сродство ко льду;
(2) моделирование и оценивание способности каждой из молекул соединений распределяться по межфазной границе «лед-вода» путем применения моделирования методом молекулярной динамики (MD); и
(3) скрининг (отбор) молекул соединений, подавляющих рост льда, с желаемой степенью сродства ко льду и воде согласно стадии (2).
Согласно настоящему изобретению основная цепь молекулы, подавляющей рост льда, представляет собой углеродную цепь или пептидную цепь.
Согласно настоящему изобретению указанная гидрофильная группа представляет собой функциональную группу, способную к образованию нековалентного взаимодействия с молекулой воды, например, путем образования водородной связи, ван-дер-ваальсового взаимодействия, электростатического взаимодействия, гидрофобного взаимодействия или π-π взаимодействия с водой; в качестве иллюстрации гидрофильная группа может быть выбрана из по меньшей мере одной из таких групп, как гидроксильная группа (-ОН), аминогруппа (-NH2), карбоксильная группа (-СООН), амидогруппа (-CONH2) и т.п. или, например, из молекул соединений, таких как гидрофильные аминокислоты, например, пролин (L-Pro), аргинин (L-Arg) и лизин (L-Lys), глюконодельталактон (GDL) и сахарид, или их молекулярных фрагментов.
Согласно настоящему изобретению указанная группа, имеющая сродство ко льду, представляет собой функциональную группу, способную к образованию нековалентного взаимодействия со льдом, например, путем образования водородной связи, ван-дер-ваальсового взаимодействия, электростатического взаимодействия, гидрофобного взаимодействия или π-π взаимодействия со льдом; в качестве иллюстрации группа, имеющая сродство ко льду, может быть выбрана из гидроксила (-ОН), аминогруппы (-NH2), фенила (-С6Н5) и пирролидинила (-C4H8N) или, например, из молекул соединений, таких как аминокислоты, имеющие сродство ко льду, такие как глутамин (L-Gln), треонин (L-Thr) и аспарагиновая кислота (L-Asn), бензольное кольцо (С6H6) и пирролидин (C4H9N), и их молекулярных фрагментов.
Согласно настоящему изобретению материал, подавляющий рост льда, может быть образован путем связывания гидрофильной группы и группы, имеющей сродство ко льду, посредством ковалентной связи.
Согласно настоящему изобретению материал, подавляющий рост льда, может быть образован из гидрофильной группы и группы, имеющей сродство ко льду, посредством нековалентной связи, например, за счет ионного взаимодействия.
Согласно настоящему изобретению указанный способ дополнительно включает стадию (4): стадию синтеза молекул соединения, подавляющего рост льда (материала, подавляющего рост льда), например, посредством известных способов химического синтеза, таких как реакция полимеризации, реакция конденсации, или способа биологической ферментации с использованием бактерий, полученных методами генной инженерии.
В настоящем изобретении также предложен подавляющий рост льда материал, полученный способом молекулярного проектирования согласно первому аспекту данного изобретения.
Согласно второму аспекту настоящего изобретения предложен способ скрининга материалов, подавляющих рост льда, включающий следующие стадии: (а) определение сродства материала, подавляющего рост льда, к воде и (b) определение способности материала, подавляющего рост льда, распределяться по межфазной поверхности «лед-вода».
В качестве варианта воплощения настоящего изобретения стадию (а) можно реализовать такими способами, как определение растворимости, константы гидратации, степени диспергирования и коэффициента диффузии материала, подавляющего рост льда, в воде и/или расчет количества межмолекулярных водородных связей, образующихся между молекулами материала, подавляющего рост льда, и молекулами воды; в частности, количество межмолекулярных водородных связей, образующихся между молекулами материала, подавляющего рост льда, и молекулами воды, определяют с помощью MD моделирования, а степень диспергирования материала, подавляющего рост льда, в водном растворе определяют с помощью метода динамического светорассеяния.
В качестве варианта воплощения настоящего изобретения стадию (b) можно реализовать путем определения количества материала, подавляющего рост льда, адсорбированного на поверхности льда на межфазной границе «лед-вода», и/или сродство материала, подавляющего рост льда, ко льду можно определять путем расчета количества межмолекулярных водородных связей, образующихся между молекулами материала, подавляющего рост льда, и молекулами воды в структуре льда; в частности, количество межмолекулярных водородных связей, образующихся между молекулами материала, подавляющего рост льда, и молекулами воды в структуре льда, определяют с помощью, например, MD моделирования, или количество молекул материала, подавляющего рост льда, адсорбированных на поверхности льда определяют на межфазной границе «лед-вода» в ходе эксперимента по адсорбции материала льдом.
Согласно настоящему изобретению эксперимент по адсорбции материала льдом включает определение количества материала, подавляющего рост льда, адсорбированного на поверхности льда.
Согласно настоящему изобретению количество материала, подавляющего рост льда, адсорбированного на поверхности льда, = (масса материала, подавляющего рост льда, адсорбированного на поверхности льда (m1)) / (общая масса материала, подавляющего рост льда, содержащаяся в исходном растворе, содержащем материал, подавляющий рост льда (m2)) × 100%.
В одном из вариантов воплощения настоящего изобретения эксперимент по адсорбции материала льдом включает следующие стадии:
S1: взятие навески материала, подавляющего рост льда, массой m2 с приготовлением водного раствора материала, подавляющего рост льда, и охлаждение до температуры переохлаждения;
S2: внесение в водный раствор предварительно охлажденного стержня регулирования температуры, так чтобы вызывать рост слоя льда на поверхности стержня регулирования температуры, при этом водный раствор постоянно перемешивают, давая возможность материалу, подавляющему рост льда, равномерно адсорбироваться на поверхности слоя льда, а температуру водного раствора и стержня регулирования температуры поддерживают на уровне температуры переохлаждения раствора; и
S3: определение количества m1 материала, подавляющего рост льда, адсорбированного на поверхности льда.
Согласно варианту воплощения настоящего изобретения стержень регулирования температуры представляет собой изделие в форме стержня, выполненное из теплопроводящего материала. Изделие в форме стержня может быть сплошным или полым внутри. Если стержень регулирования температуры внутри полый, то в его полой внутренней полости обеспечивается протекание охлаждающей жидкости, а температуру стержня регулирования температуры можно контролировать путем регулирования температуры охлаждающей жидкости, и таким образом контролируется скорость роста блока льда.
Согласно варианту воплощения настоящего изобретения стержень регулирования температуры может быть предварительно охлажден одним из таких способов, как замораживание жидким азотом, сухим льдом, с помощью охлаждающего устройства со сверхнизкими температурами и т.п.
Согласно варианту воплощения настоящего изобретения степень переохлаждения и время адсорбции на протяжении эксперимента по адсорбции материала льдом поддерживают неизменными, так чтобы площадь поверхности льда, сформировавшегося на поверхности стержня регулирования температуры, оставалась неизменной в пределах допустимой погрешности.
Согласно варианту воплощения настоящего изобретения водный раствор материала, подавляющего рост льда, с различными концентрациями для проведения эксперимента по адсорбции материала льдом готовят таким образом, чтобы можно было оценить применимые диапазоны концентраций того же материала, подавляющего рост льда, в конкретных областях применения.
Согласно варианту воплощения настоящего изобретения материал, подавляющий рост льда, на стадии S1, может быть мечен флуоресцентной меткой, например, флуоресцеином, и указанный флуоресцеин может быть выбран из по меньшей мере одного из следующих соединений: флуоресцеина изотиоцианата (FITC), тетраэтилродамина (RB200), тетраметилродамина изотиоцианата (TRITC), пропидий иодида (PI) и т.п. Специалистам в данной области техники понятно, что флуоресцентная метка служит для определения количества материала, подавляющего рост льда, и таким образом, если количество адсорбированного материала, подавляющего рост льда, может быть точно измерено другими средствами или сам материал способен поглощать в ультрафиолетовом или флуоресцентном спектре, применение флуоресцентной метки не требуется.
Согласно варианту воплощения настоящего изобретения стадия S3 включает следующее:
S3а: извлечение блока льда после адсорбции, промывка поверхности льда очищенной водой и плавление блока льда с получением адсорбционного раствора материала, подавляющего рост льда; и
S3b: определение объема V полученного плавлением адсорбционного раствора материала, подавляющего рост льда, определение массово-объемной концентрации (с) материала, подавляющего рост льда, в адсорбционном растворе и расчет массы (m1) материала, подавляющего рост льда, адсорбированного на поверхности льда, посредством формулы m1=cV.
Согласно варианту воплощения настоящего изобретения на стадии S3b концентрацию с можно определять способами, известными из уровня техники, такими как спектроскопия в ультрафиолетовой и видимой области спектра и флуоресцентная спектроскопия.
Согласно настоящему изобретению указанный способ применяют для скрининга материала для подавления роста кристаллов льда, такого как ПВС, полиаминокислоты, антифризные белки и полипептиды.
Согласно настоящему изобретению после стадии (а) и/или стадии (b) способ дополнительно включает стадию (с): оценку сродства материала к воде и характеристик способности материала распределяться по межфазной поверхности «лед-вода», причем материал с высокой способностью к такому распределению имеет и хорошие показатели по подавлению роста льда.
В качестве специальной схемы оценки на стадии (с) настоящего изобретения предложено следующее: чем меньшее количество материала, подавляющего рост кристаллов льда, требуется для покрытия определенной площади поверхности льда, тем лучше показатели распределения этого материала, т.е. удовлетворительным является коэффициент распределения S>0, где S=γI-W - (γIRIA-I+γIria-W), где γI-W является константой, т.е. межфазная энергия на границе раздела «лед-вода» γI-W выше суммы межфазных энергий на границах раздела «материал-лед» и «материал-вода» γIRIA-I+γIRIA-W (где γIRIA-I - межфазная энергия на границе раздела «материал-лед»; γIRIA-W - межфазная энергия на границе раздела «материал-вода»).
В настоящем изобретении термин «температура переохлаждения» относится к температуре, которая ниже температуры замерзания воды, но при которой вода еще не заморожена и не закристаллизована. При комнатной температуре 25°С температура переохлаждения обычно находится в диапазоне от -0,01 до -0,5°С, например, равна -0,1°С. В настоящем изобретении также предложено устройство для проведения экспериментов по адсорбции материалов льдом, включающее многослойную полость для размещения жидкости, стержень регулирования температуры и температурный регулятор, где многослойная полость для размещения жидкости последовательно включает (перечисляя изнутри наружу) полость для адсорбции материала льдом, полость бани и полость для размещения охлаждающей жидкости; при этом стержень регулирования температуры установлен в полости для адсорбции материала льдом, и температуру стержня регулирования температуры и полости для размещения жидкости регулируют посредством температурного регулятора.
В устройстве для проведения экспериментов по адсорбции материалов льдом согласно настоящему изобретению стержень регулирования температуры имеет полую структуру и выполнен из теплопроводящего материала, а полая структура стержня регулирования температуры имеет входное отверстие для жидкости и выходное отверстие для жидкости; температурный регулятор представляет собой жидкостной регулятор температуры и снабжен концевым отверстием для выпуска и концевым отверстием для возврата охлаждающей жидкости; при этом два конца полости для размещения охлаждающей жидкости имеют входное отверстие для жидкости и выходное отверстие для жидкости; причем концевое отверстие для выпуска охлаждающей жидкости температурного регулятора, входное отверстие для жидкости стержня регулирования температуры, выходное отверстие стержня регулирования температуры, входное отверстие резервуара для размещения охлаждающей жидкости, выходное отверстие резервуара для размещения охлаждающей жидкости и концевое отверстие для возврата охлаждающей жидкости температурного регулятора последовательно соединены трубками, по которым протекает охлаждающая жидкость.
В устройстве для проведения экспериментов по адсорбции материалов льдом многослойная полость для размещения жидкости снабжена крышкой.
При применении устройства полость для адсорбции материала льдом предполагается наполнять водным раствором материала, подавляющего рост льда, и полость бани в среднем слое предполагается заполнять средой для бани, имеющей заданную температуру, например, это может быть водяная баня, ледяная баня или масляная баня; после достижения заданной температуры охлаждающей жидкости охлаждающая жидкость подается из температурного регулятора и поступает в полую структуру стержня регулирования температуры, чтобы регулировать температуру стержня регулирования температуры, затем выходит из выходного отверстия для жидкости стержня регулирования температуры и поступает в полость для размещения охлаждающей жидкости в наружном слое, обеспечивая заданный уровень температуры для среды, используемой в бане, и затем проходит через выходное отверстие резервуара для размещения охлаждающей жидкости и концевое отверстие для возврата охлаждающей жидкости температурного регулятора и поступает в температурный регулятор для циркуляции.
Способ молекулярного проектирования и способ скрининга материалов, подавляющих рост льда, согласно настоящему изобретению могут быть реализованы как по отдельности, так и в комбинации. В одном из вариантов воплощения настоящего изобретения предложен комплексный способ проектирования и скрининга материалов, подавляющих рост льда, включающий последовательно: стадии проектирования молекул согласно первому аспекту изобретения и стадии скрининга материалов, подавляющих рост льда, согласно второму аспекту настоящего изобретения.
В частности указанный способ включает следующие стадии:
(1) создание библиотеки структур молекул соединений, в которой указанные молекулы соединений содержат гидрофильную группу и группу, имеющую сродство ко льду;
(2) моделирование и оценка способности каждой молекулы соединения распределяться по межфазной поверхности «лед-вода» путем применения моделирования методом молекулярной динамики (MD); и
(3) скрининг молекул соединений, подавляющих рост льда, с желаемой степенью сродства ко льду и воде согласно стадии (2);
(4) синтезирование отобранных в ходе скрининга молекул соединений, подавляющих рост льда (материала, подавляющего рост льда), имеющих желаемое сродство ко льду и воде;
(5) определение сродства материала, подавляющего рост льда, к воде; и
(7) определение показателей способности материала, подавляющего рост льда, распределяться по межфазной поверхности «лед-вода».
Согласно техническим решениям, предложенным в настоящем изобретении, за стадией (7) следует стадия (с) по дальнейшей оценке показателей способности материала, подавляющего рост льда, распределяться по межфазной поверхности «лед-вода», причем материал с высокой способностью к такому распределению имеет хорошие показатели по подавлению роста льда.
В качестве специальной схемы оценки на стадии (с) настоящего изобретения предложено следующее: чем меньшее количество материала, подавляющего рост льда, требуется для покрытия определенной площади поверхности льда, тем лучше показатели распределения этого материала, т.е. удовлетворительным является коэффициент распределения S>0, где S=γI-W - (γIRIA-I+γIRIA-W), γI-W является константой, т.е. межфазная энергия на границе раздела «лед-вода» γI-W выше суммы межфазных энергий на границах раздела «материал-лед» и «материал-вода» γIRIA-I+γIRIA-W (где γIRIA-I - межфазная энергия на границе раздела «материал-лед»; γIRIA-W - межфазная энергия на границе раздела «материал-вода»).
Согласно упомянутым выше способам молекулярного проектирования и скрининга авторы настоящего изобретения обнаружили, что тактичность гидроксильных групп также влияет на способность поливинилового спирта (ПВС) контролировать рост кристаллов льда, и кроме того, было обнаружено, что ПВС со специфической диадной синдиотактичностью обладает превосходной способностью контролировать рост кристаллов льда, при этом ПВС должен иметь диадную синдиотактичность (r) в пределах 45%-60% и молекулярную массу в пределах 10-500 кДа, и в более предпочтительном варианте ПВС должен иметь диадную синдиотактичность (r) в пределах 50%-55% и молекулярную массу в пределах 10-30 кДа.
Согласно настоящему изобретению также проектировали и синтезировали различные пептидные соединения, такие как дипептидные, трипептидные, пептоидные и гликопептидные соединения, которые также показали отличную способность в контролировании роста ледяных кристаллов.
Пептидные соединения получают путем реакции аминокислот, имеющих сродство ко льду, таких как треонин (L-Thr), глутамин (L-Gln), аспарагиновая кислота (L-Asn) и т.п., с другими гидрофильными аминокислотами, которые могут быть выбраны из аргинина, пролина, аланина и т.п., или с глюконодельталактоном (GDL) или сахаридами. Пептидные соединения состоят из аминокислот, содержащих группу, имеющую сродство ко льду, и аминокислот, содержащих гидрофильную группу. В одном варианте воплощения аминокислоты, входящие в состав пептидных соединений, представляют собой аминокислоты двух или более типов или аминокислоты одного или более типов и GDL или сахариды.
Согласно настоящему изобретению также было установлено, что некоторые специфические аминокислоты или полиаминокислоты обладают отличной способностью в контролировании роста ледяных кристаллов.
Указанные аминокислоты представляют собой аминокислоты, содержащие группу, имеющую сродство ко льду, и гидрофильную группу, а указанные полиаминокислоты представляют собой гомополимеры аминокислот, например, полиаминокислота представляет собой гомополимер аминокислоты, выбранной из аргинина, треонина, пролина, лизина, гистидина, глутаминовой кислоты, аспарагиновой кислоты, глицина и т.п.; степень полимеризации равна предпочтительно 2-40, более предпочтительно 2-20, например, 6, 8, 15 или 20; например, полиаминокислота представляет собой одну из таких полиаминокислот, как поли-L-пролин, поли-L-аргинин, или комбинацию из двух или более таких полиаминокислот.
В качестве иллюстрации аминокислоту выбирают из одной или двух таких аминокислот, как аргинин, треонин, пролин, лизин, гистидин, глутаминовая кислота, аспарагиновая кислота, глицин и т.п., например, это может быть комбинация аргинина и треонина.
Согласно третьему аспекту настоящего изобретения предложен криоконсервирующий раствор, содержащий материал, подавляющий рост льда, спроектированный способом согласно первому аспекту настоящего изобретения, или материал, подавляющий рост льда, отобранный способом скрининга согласно второму аспекту настоящего изобретения. В одном из вариантов воплощения данного изобретения материал, подавляющий рост льда, представляет собой одно или комбинацию одного или более из таких соединений, как ПВС, аминокислота или полиаминокислота и/или пептидное соединение; указанный криоконсервирующий раствор также содержит полиол, водорастворимый сахарид (или его производное, например, водорастворимую целлюлозу) и буфер.
В одном из вариантов воплощения данного изобретения криоконсервирующий раствор содержит пептидное соединение и в частности содержит на 100 мл 0,1-50 г пептидного соединения, 0-6,0 г ПВС, 0-9,0 г полиаминокислоты, 0-15 мл ДМСО, 5-45 мл полиола, водорастворимый сахарид в концентрации 0,1-1,0 моль/л, 0-30 мл сыворотки, при этом остальное количество составляет буфер.
В одном из вариантов воплощения данного изобретения криоконсервирующий раствор содержит ПВС и в частности содержит на 100 мл 0,01-6,0 г ПВС, 0-50 г пептидного соединения, 0-9,0 г полиаминокислоты, 0-15 мл ДМСО, 5-45 мл полиола, водорастворимый сахарид в концентрации 0,1-1,0 моль/л, 0-30 мл сыворотки, при этом остальное количество составляет буфер.
В одном из вариантов воплощения данного изобретения криоконсервирующий раствор содержит аминокислоту или полиаминокислоту и в частности содержит на 100 мл 0,1-50 г аминокислоты или полиаминокислоты, 0-6,0 г ПВС, 0-15 мл ДМСО, 5-45 мл полиола, водорастворимый сахарид в концентрации 0,1-1,0 моль/л, 0-30 мл сыворотки, при этом остальное количество составляет буфер. Согласно настоящему изобретению содержание аминокислоты и/или полиаминокислоты в криоконсервирующем растворе может быть в пределах 0,5-50 г, предпочтительно в пределах 1,0-35 г на 100 мл. Например, содержание аминокислоты может составлять 5,0-35 г, предпочтительно 15-25 г в присутствии аминокислоты; содержание полиаминокислоты может составлять 0,5-9,0 г, предпочтительно 1,0-5,0 г в присутствии полиаминокислоты.
Согласно настоящему изобретению полиол может представлять собой полиол, имеющий 2-5 атомов углерода, предпочтительно диол, имеющий 2-3 атома углерода, и/или триол, например, любой из таких полиолов, как этиленгликоль, пропиленгликоль и глицерин; предпочтительным вариантом является этиленгликоль.
Согласно настоящему изобретению водорастворимый сахарид может представлять собой по меньшей мере один из таких вариантов, как невосстанавливающий дисахарид, водорастворимый полисахарид, водорастворимая целлюлоза и гликозид, и, например, может быть выбран из сахарозы, трегалозы, гидроксипропилметилцеллюлозы и полисахарозы; предпочтительным вариантом является сахароза. Водорастворимый сахарид может защищать клеточные мембраны и препятствовать седиментации клеток.
Согласно настоящему изобретению буфер может быть выбран из по меньшей мере одного из DPBS, HEPES-буферизованного HTF или другого буфера для культивирования клеток.
Согласно настоящему изобретению сыворотка может содержать человеческий сывороточный альбумин или его заместитель, такой как додецилсульфат натрия, для криоконсервации материала человеческого происхождения, и может содержать фетальную бычью сыворотку или бычий сывороточный альбумин для криоконсервации материала не человеческого происхождения.
Согласно настоящему изобретению содержание ДМСО в криоконсервирующем растворе составляет 0-10 мл, предпочтительно 1,0-7,5 мл, например, 1,5-5 мл, на 100 мл. В другом варианте воплощения данного изобретения содержание ДМСО в криоконсервирующем растворе составляет 0 в 100 мл.
Согласно настоящему изобретению содержание сыворотки в криоконсервирующем растворе составляет 0,1-30 мл, например, 5,0-20 мл и 10-15 мл на 100 мл. В другом варианте воплощения данного изобретения содержание сыворотки в криоконсервирующем растворе составляет 0 в 100 мл.
Согласно настоящему изобретению содержание водорастворимого сахарида в криоконсервирующем растворе составляет 0,1-1,0 моль/л, например, 0,1-0,8 моль/л и 0,2-0,6 моль/л в 100 мл, в частности, например, 0,25 моль/л, 0,5 моль/л или 1,0 моль/л.
Согласно настоящему изобретению содержание полиола в криоконсервирующем растворе составляет 5,0-40 мл, например, 6,0-20 мл и 9-15 мл в 100 мл.
Согласно настоящему изобретению рН криоконсервирующего раствора составляет 6,5-7,6, например, 6,9-7,2. Согласно настоящему изобретению пептидные соединения или аминокислоты и полиаминокислоты имеют вышеуказанные значения.
Согласно настоящему изобретению ПВС выбирают из одного или комбинации из двух или более ПВС, таких как изотактический ПВС, синдиотактический ПВС и атактический ПВС. Например, ПВС имеет диадную синдиотактичность в пределах 15%-65%, в частности, например, в пределах 40%-60% или 53%-55%. Предпочтителен атактический ПВС, например, ПВС с диадной синдиотактичностью в пределах 45%-65%.
Согласно настоящему изобретению ПВС может быть выбран из ПВС с молекулярной массой 10-500 кДа или более, например, 10-30 кДа, 30-50 кДа, 80-90 кДа или 200-500 кДа.
Согласно настоящему изобретению ПВС может быть выбран из ПВС, имеющих степень гидролиза более 80%, например, 80%-99%, 82%-87%, 87%-89%, 89%-99% или 98%-99%.
В одном из вариантов воплощения настоящего изобретения криоконсервирующий раствор содержит следующие компоненты в расчете на 100 мл: 0,5-50 г аминокислоты, 5,0-45 мл полиола, 0-10 мл ДМСО, 0,1-30 мл сыворотки, водорастворимый сахарид в концентрации 0,1-1,0 моль/л, при этом остальное количество составляет буфер. Предпочтительно криоконсервирующий раствор содержит следующие компоненты в расчете на 100 мл: 2,0-20 г L-Arg, 1,0-10 г L-Thr, 5,0-15 мл этиленгликоля, 5,0-10 мл ДМСО, 5,0-20 мл сыворотки, сахарозу в концентрации 0,1-1,0 моль/л, при этом остальное количество составляет буфер DPBS.
В одном из вариантов воплощения настоящего изобретения криоконсервирующий раствор содержит следующие компоненты в расчете на 100 мл: 0,5-9,0 г полиаминокислоты, 5,0-45 мл полиола, 0-10 мл ДМСО, 5,0-20 мл сыворотки, водорастворимый сахарид в концентрации 0,1-1,0 моль/л, при этом остальное количество составляет буфер. Предпочтительно криоконсервирующий раствор содержит следующие компоненты в расчете на объем 100 мл: 1,0-8,0 г поли-L-пролина или поли-L-аргинина, 5-45 мл этиленгликоля, 0,1-10 мл ДМСО, 5,0-20 мл сыворотки, сахарозу в концентрации 0,1-1,0 моль/л, при этом остальное количество составляет буфер DPBS.
В одном из вариантов воплощения настоящего изобретения криоконсервирующий раствор содержит следующие компоненты в расчете на объем 100 мл: 0,01-6,0 г ПВС, 5,0-45 мл полиола, 0,1-30 мл сыворотки, водорастворимый сахарид в концентрации 0,1-1,0 моль/л, при этом остальное количество составляет буфер.
Предпочтительно криоконсервирующий раствор содержит следующие компоненты в расчете на 100 мл: 0,01-6,0 г ПВС, 5,0-30 мл этиленгликоля, 10-20 мл сыворотки, сахарозу в концентрации 0,1-0,6 моль/л, при этом остальное количество составляет буфер DPBS.
В одном из вариантов воплощения настоящего изобретения криоконсервирующий раствор содержит следующие компоненты в расчете на 100 мл: 1,0-5,0 г ПВС, 5,0-20 мл полиола, 0,1-10 мл ДМСО, 0,1-20 мл сыворотки, водорастворимый сахарид в концентрации 0,2-0,8 моль/л, при этом остальное количество составляет буфер. Предпочтительно криоконсервирующий раствор содержит следующие компоненты в расчете на 100 мл: 1,0-4,0 г ПВС, 5,0-15 мл этиленгликоля, 4-10 мл ДМСО, 10-20 мл сыворотки, сахарозу в концентрации 0,2-0,6 моль/л, при этом остальное количество составляет буфер DPBS.
В одном из вариантов воплощения настоящего изобретения криоконсервирующий раствор содержит следующие компоненты в объеме 100 мл: 0,1-6,0 г ПВС, 10-45 мл полиола, водорастворимый сахарид в концентрации 0,2-1,0 моль/л, при этом остальное количество составляет буфер. Предпочтительно криоконсервирующий раствор содержит следующие компоненты в объеме 100 мл: 1,0-5,0 г ПВС, 5,0-20 мл этиленгликоля, сахарозу в концентрации 0,2-0,6 моль/л, при этом остальное количество составляет буфер DPBS.
В одном из вариантов воплощения настоящего изобретения криоконсервирующий раствор содержит следующие компоненты в объеме 100 мл: 0,5-9,0 г полиаминокислоты, 5,0-45 мл полиола, 0,1-6 г ПВС, 0-20 мл сыворотки, водорастворимый сахарид в концентрации 0,1-1,0 моль/л, при этом остальное количество составляет буфер. Предпочтительно криоконсервирующий раствор содержит следующие компоненты в объеме 100 мл: 1,0-8,0 г поли-L-пролина или поли-L-аргинина, 5-45 мл этиленгликоля, 0,1-6 г ПВС, 5,0-20 мл сыворотки, сахарозу в концентрации 0,1-1,0 моль/л, при этом остальное количество составляет буфер DPBS.
В настоящем изобретении дополнительно представлен способ приготовления криоконсервирующего раствора, включающий следующие стадии:
(1) взятие навески одной или нескольких аминокислот или полиаминокислоты, ПВС и пептидного соединения, растворение по отдельности в порции буфера и доведение рН с получением раствора;
(2) растворение водорастворимого сахарида в другой порции буфера, и после полного растворения водорастворимого сахарида добавление других компонентов, за исключением сыворотки, с получением раствора; и
(3) охлаждение растворов, полученных на стадии (1) и стадии (2), до комнатной температуры, после чего их смешивают, регулируют рН и доводят до заданного объема буфером с получением криоконсервирующего раствора.
Согласно способу приготовления криоконсервирующего раствора, предложенного в настоящем изобретении, если криоконсервирующий раствор содержит сыворотку, то эту сыворотку добавляют при применении криоконсервирующего раствора.
Согласно способу приготовления, раскрытого в данном документе, ПВС растворяют путем нагревания на теплой бане и перемешивания, и, например, нагревание производят на водяной бане или на масляной бане; например, температура водяной бани составляет 65-85°С или 70-80°С; перемешивание представляет собой механическое перемешивание, например, с помощью магнитной мешалки.
Согласно способу приготовления, раскрытого в данном документе, растворение водорастворимого сахарида представляет собой растворение с помощью ультразвука.
Криоконсервирующий раствор, раскрытый в данном документе, можно применять в комбинации с замораживающим уравновешивающим раствором. В одном из вариантов воплощения настоящего изобретения предложен замораживающим уравновешивающий раствор, содержащий в расчете на 100 мл 5,0-45 мл полиола и буфер (остающийся объем до 100 мл).
Замораживающий уравновешивающий раствор, раскрытый в данном документе, дополнительно и необязательно содержит 0-15 мл ДМСО, 0-30 мл сыворотки и/или 0-5,0 г ПВС.
В замораживающем уравновешивающем растворе, раскрытом в данном документе, содержание полиола составляет 6,0-28 мл, например, 7,0-20 мл или 10-15 мл.
В замораживающем уравновешивающем растворе, раскрытом в данном документе, содержание ДМСО составляет 0,1-15 мл, например, 1,0-10 мл или 5,0-7,5 мл. В одном из вариантов воплощения настоящего изобретения содержание ДМСО равно 0.
В замораживающем уравновешивающем растворе, раскрытом в данном документе, содержание сыворотки составляет 0,1-30 мл, например, 5,0-20 мл или 10-15 мл. В одном из вариантов воплощения настоящего изобретения содержание сыворотки равно 0.
В замораживающем уравновешивающем растворе, раскрытом в данном документе, содержание ПВС составляет 0,1-5,0 г, например, 0,1 г, 0,5 г, 1,0 г или 2,0 г. В одном из вариантов воплощения настоящего изобретения содержание ПВС равно 0.
В замораживающем уравновешивающем растворе, раскрытом в данном документе, полиол, сыворотку и буфер можно выбирать из таких же вариантов, какие используются и в криоконсервирующем растворе. В одном из вариантов воплощения настоящего изобретения, если криоконсервирующий раствор не содержит сыворотку, то в замораживающий уравновешивающий раствор добавляют ПВС.
В одном из вариантов воплощения настоящего изобретения замораживающий уравновешивающий раствор в расчете на 100 мл содержит 5,0-7,5 мл полиола, 5,0-7,5 мл ДМСО, 10-20 мл сыворотки и буфер (остающийся объем до 100 мл).
В одном из вариантов воплощения настоящего изобретения замораживающий уравновешивающий раствор в расчете на 100 мл содержит 7,5-15 мл полиола, 10-20 мл сыворотки и буфер (остающийся объем до 100 мл).
В одном из вариантов воплощения настоящего изобретения замораживающий уравновешивающий раствор в расчете на 100 мл содержит 1,0-5,0 г ПВС, 7,5-15 мл полиола и буфер (остающийся объем до 100 мл).
В настоящем изобретении дополнительно представлен способ приготовления замораживающего уравновешивающего раствора, включающий растворение каждого компонента в буфере, хранение сыворотки отдельно и добавление сыворотки к замораживающему уравновешивающему раствору при его применении.
Криоконсервирующий реагент содержит упомянутый выше замораживающий уравновешивающий раствор и упомянутый выше криоконсервирующий раствор, причем указанный замораживающий уравновешивающий раствор и указанный криоконсервирующий раствор представлены независимо.
В криоконсервирующем реагенте, раскрытом в данном документе, если криоконсервирующий раствор не содержит сыворотку, то в замораживающий уравновешивающий раствор добавляют ПВС.
В частности, если содержание ДМСО в криоконсервирующем растворе равно 0, то замораживающий уравновешивающий раствор в расчете на 100 мл содержит 0-5,0 г ПВС, 7,5-15 мл полиола, 10-20 мл сыворотки и буфер (остающийся объем до 100 мл). Если содержания ДМСО и сыворотки в криоконсервирующем растворе одновременно равны 0, то замораживающий уравновешивающий раствор в расчете на 100 мл содержит 1,0-5,0 г ПВС, 7,5-15 мл полиола и буфер (остающийся объем до 100 мл).
Криоконсервирующий раствор или замораживающий уравновешивающий раствор, раскрытые в данном документе, можно применять для криоконсервации различных клеток, тканей и органов. Различные типы клеток включают, но не ограничиваются ими, половые клетки, такие как ооциты и сперматозоиды, и различные стволовые клетки, такие как пуповинные мезенхимальные стволовые клетки; различные типы тканей включают, но не ограничиваются ими, овариальные ткани, эмбриональные ткани и оплодотворенные яйцеклетки; различные типы органов включают, но не ограничиваются ими, яичники или другие органы млекопитающих.
Кроме того, в настоящем изобретении предложено применение упомянутых выше криоконсервирующего раствора или замораживающего уравновешивающего раствора, или комбинации этих растворов для криоконсервации клеток, тканей и органов. В одном из вариантов воплощения настоящего изобретения упомянутые выше криоконсервирующий раствор или замораживающий уравновешивающий раствор, или комбинацию этих растворов применяют для криоконсервации ооцитов; в одном из вариантов воплощения настоящего изобретения упомянутые выше криоконсервирующий раствор или замораживающий уравновешивающий раствор, или комбинацию этих растворов применяют для криоконсервации эмбрионов; в одном из вариантов воплощения настоящего изобретения упомянутые выше криоконсервирующий раствор или криоконсервирующий уравновешивающий раствор, или комбинацию этих растворов применяют для криоконсервации овариальных тканей или овариальных органов; в одном из вариантов воплощения настоящего изобретения упомянутые выше криоконсервирующий раствор или замораживающий уравновешивающий раствор, или комбинацию этих растворов применяют для криоконсервации стволовых клеток.
В настоящем изобретении также предложен способ замораживания и размораживания клеток или эмбрионов, включающий следующее:
(1) помещение клеток или эмбрионов в криоконсервирующий раствор, раскрытый в данном документе, с получением суспензии клеток, и замораживание ее; и
(2) помещение клеток или эмбрионов в размораживающий раствор для размораживания.
Согласно раскрытому в данном документе способу замораживания и размораживания клетки или эмбрионы сначала помещают в уравновешивающий раствор для достижения равновесия, после чего их помещают в криоконсервирующий раствор.
В настоящем изобретении дополнительно предложен способ криоконсервации стволовых клеток, в котором применяют микрокапельный метод. Например, способ криоконсервации стволовых клеток включает следующие стадии: добавление к стволовым клеткам криоконсервирующего раствора, пипетирование смеси для диспергирования стволовых клеток с получением суспензии стволовых клеток, и помещение суспензии стволовых клеток на предметное стекло для замораживания и криоконсервация в жидком азоте (при -196°С).
Согласно варианту воплощения настоящего изобретения размораживание криоконсервированных стволовых клеток включает помещение предметного стекла с замороженными стволовыми клетками в среду а-МЕМ и размораживание клеток при температуре 37°С.
Согласно варианту воплощения настоящего изобретения упомянутые стволовые клетки представляют собой различные стволовые клетки, которые известны в данной области техники и способны к дифференциации, такие как тотипотентные, плюрипотентные или унипотентные стволовые клетки, включая, но не ограничиваясь ими, эмбриональные стволовые клетки, мезенхимальные стволовые клетки различных типов (например, мезенхимальные стволовые клетки пуповины, мезенхимальные стволовые клетки жировой ткани и мезенхимальные стволовые клетки костного мозга), гемопоэтические стволовые клетки и т.п.
В настоящем изобретении дополнительно предложен способ криоконсервации органов и/или тканей, включающий помещение органов и/или тканей в замораживающий уравновешивающий раствор для достижения равновесия, затем помещение органов и/или тканей в криоконсервирующий раствор, далее помещение органов и/или тканей на предметное стекло для замораживания и криоконсервацию в жидком азоте.
В одном из вариантов воплощения настоящего изобретения орган и/или ткань представляют собой овариальную ткань или овариальный орган, которые могут представлять собой срез овариальной ткани или цельную овариальную ткань.
В настоящей заявке на изобретение термины «криоконсервация» и «криогенная консервация» имеют одно и то же значение и используются взаимозаменяемо для обозначения консервации вещества, или клетки, ткани или органа при низких температурах с сохранением их исходной физико-химической и/или биологической активности, а также их физиологических и биохимических функций.
В настоящей заявке на изобретение термины «молекула, подавляющая рост льда» и «материал, подавляющий рост льда» имеют одно и то же значение и относятся к соединению, способному подавлять рост кристаллов льда в водном растворе. В одном из вариантов воплощения настоящего изобретения молекула, подавляющая рост льда, имеет хорошие показатели распределения по межфазной поверхности границы раздела «лед-вода» и способна снизить размер зерен ледяных кристаллов, или молекула, подавляющая рост льда, не имеет теплового гистерезиса или имеет достаточно малый тепловой гистерезис, чтобы значительно сократить формирование ледяных кристаллов в водном растворе.
Преимущества
1. В настоящем изобретении впервые установлен механизм контролирования роста кристаллов льда в смешанной фазе «лед-вода» молекулами, подавляющими рост льда. От материала, подавляющего рост льда, требуется хорошее сродство как ко льду, так и к воде. Сродство молекул, подавляющих рост льда, ко льду может обеспечить хорошую адсорбцию молекул, подавляющих рост льда, на поверхности льда; сродство этих молекул к воде может обеспечить улучшенное распределение этих молекул по границе раздела «лед-вода», позволяющее покрывать максимальную площадь поверхности льда как можно меньшим количеством материала. Исходя из установленного механизма подавления роста льда, предложена идея проектирования молекул, подавляющих рост льда, со сродством как ко льду, так и к воде, что обеспечивает новый способ синтеза материалов, подавляющих рост льда.
2. В настоящем изобретении в процесс проектирования молекулярной структуры материала, подавляющего рост льда, впервые включено MD моделирование, посредством которого проводят оценку сродства молекул, подавляющих рост льда, ко льду и воде, прогнозируют показатели ингибирования процесса роста льда для проектируемого материала, подавляющего рост льда, и таким образом получают возможность добиться оптимизации его структуры.
3. В настоящем изобретении сочетание предложенного механизма подавления роста льда с MD моделированием позволяет хорошо преодолевать ограничение, связанное с тем, что в процессе исследований и разработки материала, подавляющего рост льда, материалы, известные в данной области техники, можно подвергать анализу на показатели пригодности и скринингу только с применением экспериментального подхода - метод «проб и ошибок», обеспечивает новую идеологию в проектировании молекулярных структур и способно значительно ускорить разработку и применение материалов, контролирующих рост льда.
4. Криоконсервирующий раствор, предложенный в настоящем изобретении, имеет своим преимуществом широкую доступность, хорошую биологическую совместимость, низкую токсичность, высокую безопасность и значительное сокращение количества используемого ДМСО, и при его применении даже без добавления ДМСО может обеспечить равные или даже более высокие показатели выживаемости клеток, чем у промышленного криоконсервирующего раствора, содержащего ДМСО в количествах не менее 15% и обычно применяемого в современной клинической практике. Раскрытый в данном описании криоконсервирующий раствор также имеет своим преимуществом простоту состава, легкодоступные исходные материалы и низкую стоимость, и может широко применяться для криоконсервации различных клеток и тканей, таких как ооциты, эмбрионы, стволовые клетки, овариальные ткани и овариальные органы, с сохранением их хорошей биологической активности.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
ФИГ. 1: Схема молекулярной структуры материала, подавляющего рост льда;
ФИГ. 2: Агрегационные состояния атактического ПВС (а-ПВС) и изотактического ПВС (i-ПВС) на межфазной границе «лед-вода», полученные методом MD моделирования;
ФИГ. 3: Спектр протонного ядерного магнитного резонанса (ЯМР) для а-ПВС, синтезированного в Примере 1;
ФИГ. 4: Спектры протонного ЯМР для PBVE и i-ПВС, синтезированных в Примере 1, где спектр А относится к PBVE, а спектр В относится к i-ПВС;
ФИГ. 5: Кривые гель-проникающей хроматографии (ГПХ) для PBVE, синтезированного в Примере 1;
ФИГ. 6: Распределения по размерам частиц дисперсий а-ПВС (А) и i-ПВС (В) в воде при различных концентрациях, определенные в эксперименте по динамическому светорассеянию (DLS);
ФИГ. 7: Микрофотографии роста ледяных кристаллов в растворах двух типов ПВС, где снимок А относится к а-ПВС, а снимок В относится к i-ПВС; С показывает зависимость между средним размером крупнейших зерен льда (MLGS), выраженным в % относительно величины этого показателя в буфере PBS, и концентрацией для этих двух типов ПВС;
ФИГ. 8: Топография ледяных кристаллов, модифицированных а-ПВС (снимки А и В) и i-ПВС (снимки С и D), в очищенной воде;
ФИГ. 9: Модели молекулярных структур двух типов ПВС, полученные методом MD моделирования;
ФИГ. 10: Площади контактируемой поверхности для молекул двух типов ПВС с молекулами воды в жидкой воде и молекулами воды в структуре льда на межфазной границе «лед-вода» при 240 K, полученные методом MD моделирования, где верхняя часть фигуры показывает 3 результата для молекул а-ПВС, а нижняя часть фигуры показывает 3 результата для молекул i-ПВС;
ФИГ. 11: Вероятности агрегации для двух типов ПВС в водном растворе, полученные методом MD моделирования и вычислений;
ФИГ. 12: Количество межмолекулярных водородных связей, образующихся между молекулами двух типов ПВС и молекулами воды при 240 K в водном растворе, и количество межмолекулярных водородных связей, образующихся между молекулами двух типов ПВС и молекулами воды в жидкой фазе и в структуре льде при 240 K на межфазной границе «лед-вода» (данные получены методом MD моделирования и вычислений);
ФИГ. 13: Оптические микрофотографии, показывающие подавление процесса роста кристаллов льда при использовании GDL-L-Thr (соединения формулы (6)), и статистическая диаграмма гранулометрического состава зерен льда;
ФИГ. 14: Топография ледяного кристалла, модифицированного GDL-L-Thr, в очищенной воде;
ФИГ. 15: Оптические микрофотографии, показывающие подавление процесса роста кристаллов льда при использовании GDL-L-Ser (соединения формулы (7)), и статистическая диаграмма гранулометрического состава зерен льда;
ФИГ. 16: Оптические микрофотографии, показывающие подавление процесса роста кристаллов льда при использовании GDL-L-Val (соединения формулы (8)), и статистическая диаграмма гранулометрического состава зерен льда;
ФИГ. 17: Оптические микрофотографии, показывающие подавление процесса роста кристаллов льда при использовании короткоцепочечного пептида TR, приготовленного в Примере 3, и статистическая диаграмма гранулометрического состава зерен льда;
ФИГ. 18: Топография ледяного кристалла, модифицированного короткоцепочечным пептидом TR, приготовленным в Примере 3, в очищенной воде;
ФИГ. 19: Результаты подавления процесса роста ледяных кристаллов при использовании пептоидов R-COOH, R-СН3 и R-CH2CH3, приготовленных в Примере 8;
ФИГ. 20: Топографии ледяных кристаллов, модифицированных пептоидами R-COOH (A), R-СН3 (В) и R-CH2CH3 (С), приготовленными в Примере 8, в очищенной воде;
ФИГ. 21: Схема эксперимента по адсорбции материалов льдом и устройства для его проведения;
ФИГ. 22: Графики зависимости количества адсорбированного льдом материала от концентрации двух типов ПВС, полученных в Примере 9;
ФИГ. 23: Микрофотографии роста ледяных кристаллов в растворах DPBS при использовании двух типов ПВС, где снимок А относится к а-ПВС, а снимок В относится к i-ПВС;
ФИГ. 24: Снимок окрашенного среза свежего (незамороженного) овариального органа новорожденной мыши 3-дневного возраста;
ФИГ. 25: Снимок окрашенного среза криоконсервированного овариального органа, полученный в Сравнительном варианте реализации 8 после размораживания;
ФИГ. 26: Снимок окрашенного среза криоконсервированного овариального органа, полученный в Варианте применения 13 после размораживания;
ФИГ. 27: Снимок окрашенного среза криоконсервированного овариального органа, полученный в Варианте применения 14 после размораживания;
ФИГ. 28: Снимок окрашенного среза криоконсервированного овариального органа, полученный в Варианте применения 15 после размораживания;
ФИГ. 29: Снимок окрашенного среза свежей (незамороженной) овариальной ткани половозрелой мыши;
ФИГ. 30: Снимок окрашенного среза криоконсервированной овариальной ткани, полученный в Сравнительном варианте воплощения 9 после размораживания;
ФИГ. 31: Снимок окрашенного среза криоконсервированной овариальной ткани, полученный в Варианте применения 16 после размораживания;
ФИГ. 32: Снимок окрашенного среза криоконсервированной овариальной ткани, полученный в Варианте применения 17 после размораживания;
ФИГ. 33: Снимок окрашенного среза криоконсервированной овариальной ткани, полученный в Варианте применения 18 после размораживания;
ФИГ. 34: Снимок окрашенного среза криоконсервированной овариальной ткани, полученный в Варианте применения 26 после размораживания;
ФИГ. 35: Снимок окрашенного среза криоконсервированной овариальной ткани, полученный в Варианте применения 27 после размораживания;
ФИГ. 36: Снимок окрашенного среза криоконсервированной овариальной ткани, полученный в Варианте применения 28 после размораживания;
ФИГ. 37: Снимок окрашенного среза криоконсервированной овариальной ткани, полученный в Варианте применения 29 после размораживания;
ФИГ. 38: Снимок окрашенного среза криоконсервированной овариальной ткани, полученный в Варианте применения 30 после размораживания;
ФИГ. 39: Снимок окрашенного среза криоконсервированной овариальной ткани, полученный в Варианте применения 31 после размораживания;
ФИГ. 40: Снимок окрашенного среза криоконсервированной овариальной ткани, полученный в Варианте применения 37 после размораживания; и
ФИГ. 41: Снимок окрашенного среза криоконсервированной овариальной ткани, полученный в Варианте применения 38 после размораживания.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Способ приготовления согласно настоящему изобретению будет более подробно проиллюстрирован на представленных далее частных примерах. Следует понимать, что представленные далее примеры являются лишь показательными иллюстрациями и пояснениями к настоящему изобретению, и их не следует интерпретировать как исчерпывающие описания, определяющие объем правовой охраны настоящего изобретения. Все методики, разрабатываемые на основании вышеупомянутого содержания настоящего изобретения, подпадают под общий объем правовой охраны настоящего изобретения.
Если иное не оговорено особо, экспериментальные методы, используемые в последующих примерах, представляют собой обычные традиционные методы. Если иное не оговорено особо, реактивы, материалы и т.п., используемые в последующих примерах, относятся к серийно выпускаемым товарам, представленным на рынке.
А. Молекулярное проектирование материала, подавляющего рост льда
Центральную молекулу материала, подавляющего рост льда, можно спроектировать в сочетании с различными группами, имеющими сродство с водой, и с группами, имеющими сродство со льдом, соединенными посредством ковалентных связей или нековалентных связей, таких как ионные связи.
Раскрытый в данном описании способ молекулярного проектирования материала, подавляющего рост льда, включает следующие стадии:
(1) создание библиотеки структур молекул соединений, в которой молекулы соединений содержат гидрофильную группу и группу, имеющую сродство ко льду;
(2) моделирование и оценивание способности указанных молекул соединений распределяться по межфазной границе «лед-вода» путем применения метода молекулярной динамики (MD); и
(3) скрининг молекул, подавляющих рост льда, с желаемой степенью сродства ко льду и воде.
Согласно настоящему изобретению основная цепь молекулы, подавляющей рост кристаллов льда, представляет собой углеродную цепь или пептидную цепь.
Согласно настоящему изобретению MD моделирование на стадии (2) можно проводить с использованием программных пакетов GROMACS, AMBER, CHARMM, NAMD или LAMMPS.
Согласно настоящему изобретению, при проведении MD моделирования на стадии (2) модель молекулы воды можно выбрать из таких моделей, как ТIР3Р, ТIР4Р, TIP4P/2005, SPC, ТIР3Р, ТIР5Р и SPC/E, при этом для моделирования молекулы воды предпочтительно брать модель ТIР4Р/2005.
Согласно настоящему изобретению, при проведении MD моделирования на стадии (2) параметры силового поля берут, используя одно из таких силовых полей, как GROMOS, ESFF, силовое поле MM, AMBER, CHARMM, COMPASS, UFF, CVFF и другие силовые поля.
Согласно настоящему изобретению, при проведении MD моделирования на стадии (2) моделирование и расчет выполняют по взаимодействиям между молекулами материала, подавляющего рост льда, по взаимодействиям между молекулами материала, подавляющего рост льда, и молекулами воды в жидкой фазе и по взаимодействиям между молекулами материала, подавляющего рост льда, и молекулами воды в структуре льда. Взаимодействия включают образование водородной связи, ван-дер-ваальсовое взаимодействие, электростатическое взаимодействие, гидрофобное взаимодействие, π-π взаимодействие и т.п.
Согласно настоящему изобретению, при проведении MD моделирования на стадии (2), когда смоделированные и рассчитанные молекулы взаимодействуют, производят соответствующую корректировку температуры и давления. В одном из вариантов воплощения настоящего изобретения для регулирования температуры и давления используют регулятор температуры V-rescale (модифицированный Berendsen) и регулятор давления.
Согласно настоящему изобретению, при проведении MD моделирования на стадии (2) молекулярную конфигурацию молекулы соединения поддерживают путем выбора параметра потенциальной энергии. Предпочтительно выбирать такой параметр потенциальной энергии, чтобы молекулярная конфигурация молекулы соединения сохранялась и при повышенных температурах.
Согласно настоящему изобретению, на стадии (2) задают периодические граничные условия для направления х, направления у и направления z, если моделируется система водного раствора; в случае моделировании смешанной системы «лед-вода» периодические граничные условия задают для направления х и направления у.
Согласно настоящему изобретению, при проведении MD моделирования на стадии (2) выбирают кубический или октаэдрический блок воды, и предпочтительным является кубический блок воды с размерами 3,9 × 3,6 × 1,0 нм3.
В конкретном варианте воплощения настоящего изобретения в процессе молекулярно-динамических расчетов при MD моделировании температуру и давление регулируют с помощью регулятора температуры V-rescale (модифицированного Berendsen) и регулятора давления.
При MD моделировании и расчетах главным условием для определения существования водородной связи являются энергетические критерии или геометрические критерии, предпочтительно геометрические критерии; если расстояние (шаг) между атомами кислорода меньше 0,35 нм, а угол НО…Н меньше 30 градусов, то образуется водородная связь между двумя гидроксильными группами или между гидроксильной группой и молекулой воды.
В конкретном варианте воплощения настоящего изобретения материал, подавляющий рост льда, может представлять собой соединение, имеющее в качестве основной цепи углеродную цепь с заместителями в виде группы, имеющей сродство ко льду, и гидрофильной группы; материал, подавляющий рост льда, может содержать группу, которая является одновременно гидрофильной и имеющей сродство ко льду, такую как гидроксильная группа и аминогруппа, и может дополнительно содержать группу, имеющую сродство ко льду, и гидрофильную группу по отдельности. Например, молекулярная структура материала, подавляющего рост льда, спроектирована так, чтобы в ней имелось повторяющееся звено -[СH2-СНОН]-.
В одном из вариантов воплощения настоящего изобретения молекула материала, подавляющего рост льда, представляет собой ПВС (поливиниловый спирт). ПВС выбирают из одного или комбинации двух или более из таких вариантов, как изотактический ПВС, синдиотактический ПВС и атактический ПВС. Например, ПВС имеет диадную синдиотактичность 15%-65%, в частности, например, 40%-60% или 53%-55%. Предпочтителен атактический ПВС, например, ПВС с диадной синдиотактичностью 45%-65%. ПВС может быть выбран из ПВС, имеющего молекулярную массу 10-500 кДа или более, например 10-30 кДа, 30-50 кДа, 80-90 кДа или 200-500 кДа. ПВС может быть выбран из ПВС, имеющего степень гидролиза более 80%, например, 80%-99%, 82%-87%, 87%-89%, 89%-99% или 98%-99%.
В одном из вариантов воплощения настоящего изобретения молекула материала, подавляющего рост льда, представляет собой пептидное соединение. Пептидные соединения получают реакцией аминокислот, имеющих сродство ко льду, таких как треонин (L-Thr), глутамин (L-Gln) и аспарагиновая кислота (L-Asn), с другими гидрофильными аминокислотами, которые могут быть выбраны из аргинина, пролина, аланина и т.п. или GDL, или сахаридов.
Пептидное соединение состоит из не менее чем двух аминокислотных звеньев, например, 2-8 аминокислотных звеньев, в частности 2-5, например, 2, 3, 4, 5 или 6 аминокислотных звеньев, при этом все аминокислотные звенья разные. В указанном пептидном соединении мольное соотношение аминокислот, имеющих сродство ко льду, таких как треонин, и других гидрофильных аминокислот составляет (0,1-3): 1, предпочтительно (0,5-2): 1. Расположение аминокислот, имеющих сродство ко льду, и других гидрофильных аминокислот в структуре пептидного соединения особенно не ограничивается, и они могут быть присоединены посредством аминокислотных связующих групп или химических связей, известных из уровня техники. Например, аминокислоты, имеющие сродство ко льду, и гидрофильные аминокислоты могут располагаться поочередно, или несколько аминокислот, имеющих сродство ко льду, или гидрофильных аминокислот могут быть соединены между собой, образуя фрагмент из аминокислот, имеющих сродство ко льду, или фрагмент из гидрофильных аминокислот, который затем связывают с гидрофильной аминокислотой (или фрагментом из гидрофильных аминокислот) или с аминокислотой, имеющей сродство ко льду (или фрагментом из аминокислот, имеющих сродство ко льду), соответственно.
В одном из вариантов воплощения настоящего изобретения пептидное соединение представляет собой по меньшей мере одно из таких соединений, как L-Thr-L-Arg (TR), L-Thr-L-Pro (TP), L-Arg-L-Thr (RT), L-Pro-L-Thr (PT), L-Thr-L-Arg-L-Thr (TRT), L-Thr-L-Pro-L-Thr (TPT), L-Ala-L-Ala-L-Thr (AAT) или L-Thr-L-Cys-L-Thr (TCT).
В другом варианте воплощения пептидное соединение представляет собой GDL-L-аминокислоту, например, GDL-L-Thr, GDL-L-Ser или GDL-L-Val.
В еще одном варианте воплощения пептидное соединение имеет одну из структур, представленных формулами (1)-(8):
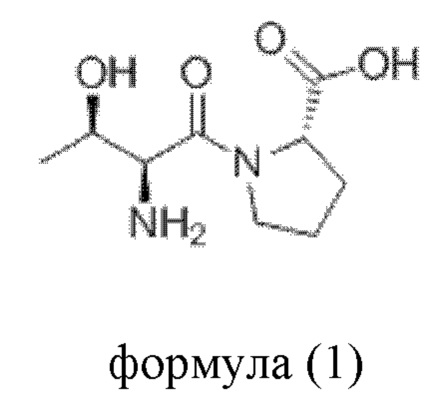
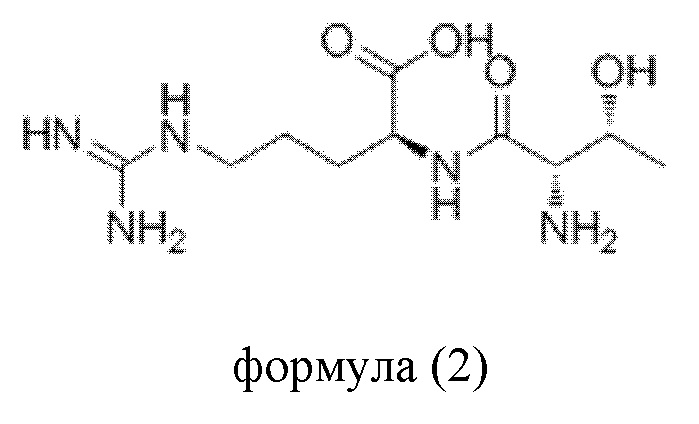
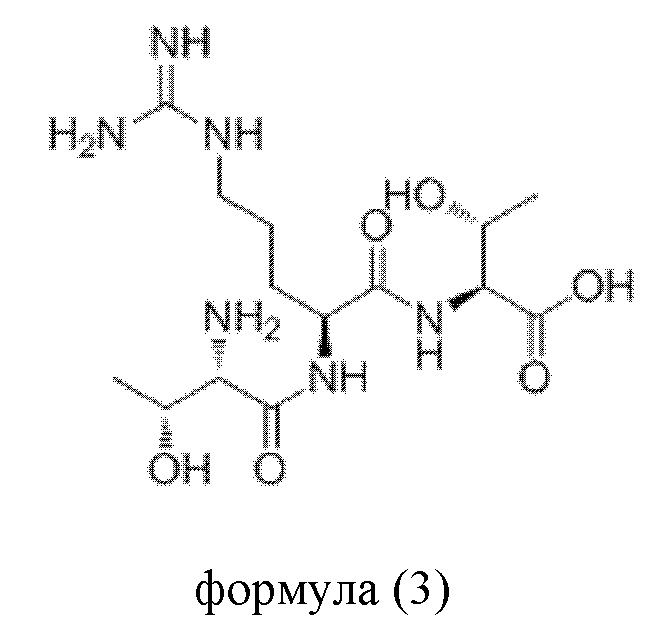
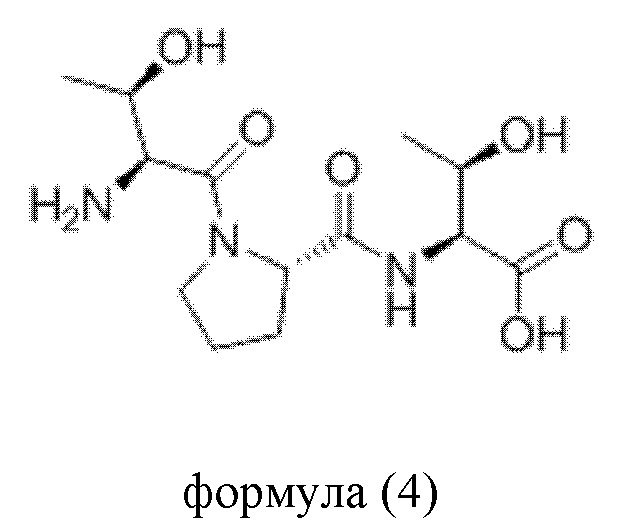
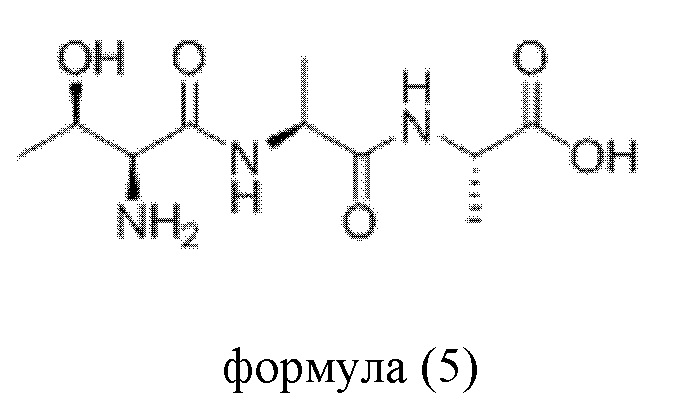
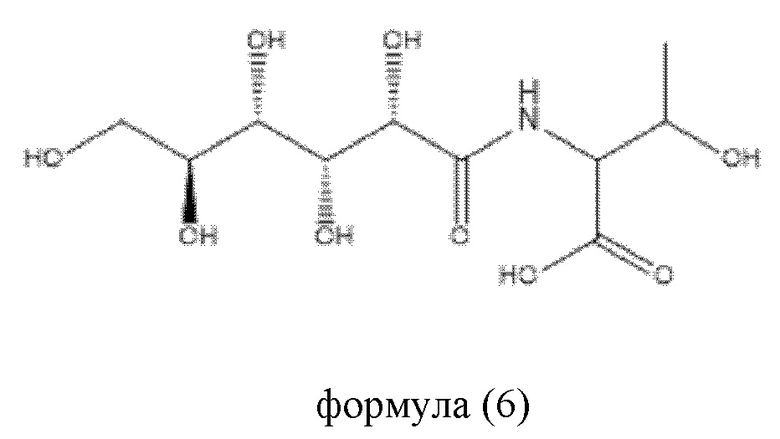
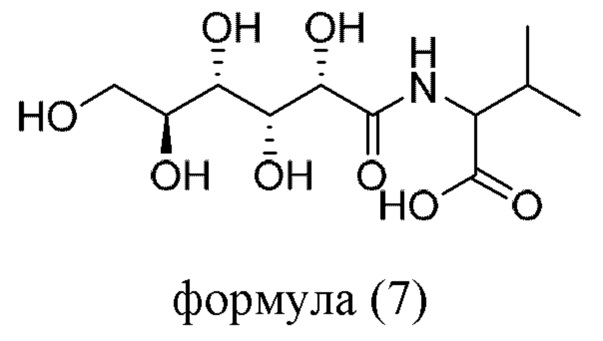
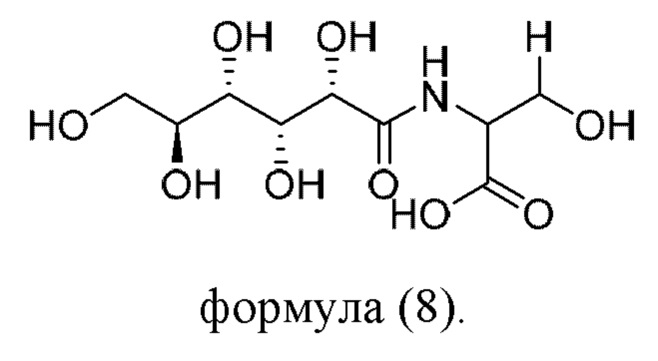
Приведенные выше пептидные соединения можно синтезировать посредством способа синтеза полипептидов, известного в данной области техники, такого как способ твердофазного синтеза.
Раскрытый в данном документе способ приготовления включает следующие стадии: набухание смолы, ковалентное связывание набухшей смолы с аминокислотой, аминогруппа которой защищена, снятие защиты, добавление другой аминокислоты, аминогруппа которой защищена, для реакции конденсации, снятие защиты, отщепление и очистка.
Производное гликопептида можно приготовить посредством известного способа, используя реакцию аминокислоты с сахаридом. Например, производное гликопептида можно приготовить реакцией глюконодельталактона или других сахаридов с аминокислотой в органическом растворителе или путем применения способа твердофазного синтеза. Глюконодельталактон (GDL) растворяют в органическом растворителе, аминокислоту и щелочной катализатор смешивают с органическим растворителем и полученную смесь добавляют к раствору GDL для реагирования при 55-60°С после полного растворения аминокислоты и щелочного катализатора, и после завершения реакции белый осадок отфильтровывают, и фильтрат выпаривают досуха, получая сырой продукт.
Согласно способу приготовления, раскрытому в данном документе, органический растворитель можно выбирать из метанола, этанола и т.п.
В одном из вариантов реализации производное гликопептида получают, используя способ твердофазного синтеза, включающий: набухание смолы, ковалентное связывание набухшей смолы с аминокислотой, аминогруппа которой защищена, снятие защиты, добавление сахарида (такого как GDL с раскрытым циклом) для проведения реакции конденсации, отщепление и очистка. GDL-L-Val и GDL-L-Ser синтезировали, руководствуясь способом, использовавшимся для синтеза GDL-L-Thr.
В настоящем изобретении дополнительно предложено пептидное соединение формулы (9):
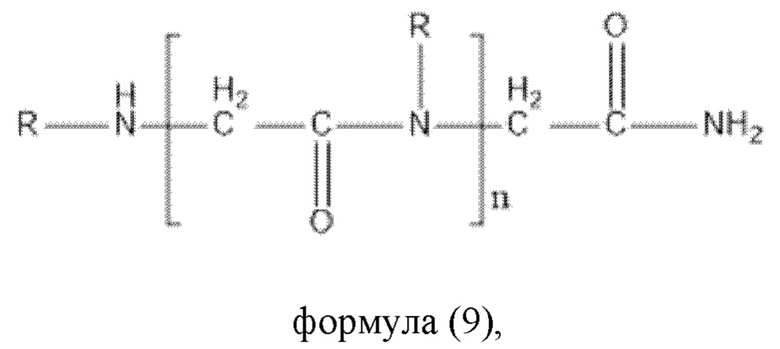
где R выбирают из замещенного или незамещенного алкила, а заместитель можно выбирать из -ОН, -NH2, -СООН, -CONH2 и т.п. Например, R представляет собой замещенный или незамещенный C1-6 алкил, и предпочтительно R представляет собой -СН3, -СН2СН3, -СН2СН2СООН; n представляет собой целое число, равное не менее 1 и не более 1000, и, например, может представлять собой целое число в диапазоне от 1 до 100. В некоторых вариантах реализации настоящего изобретения n представляет собой целое число, такое как 2, 3, 4, 5, 6, 7, 8, 9 или 10.
В одном из вариантов реализации настоящего изобретения соединение формулы (9) имеет структуру одного из следующих типов:
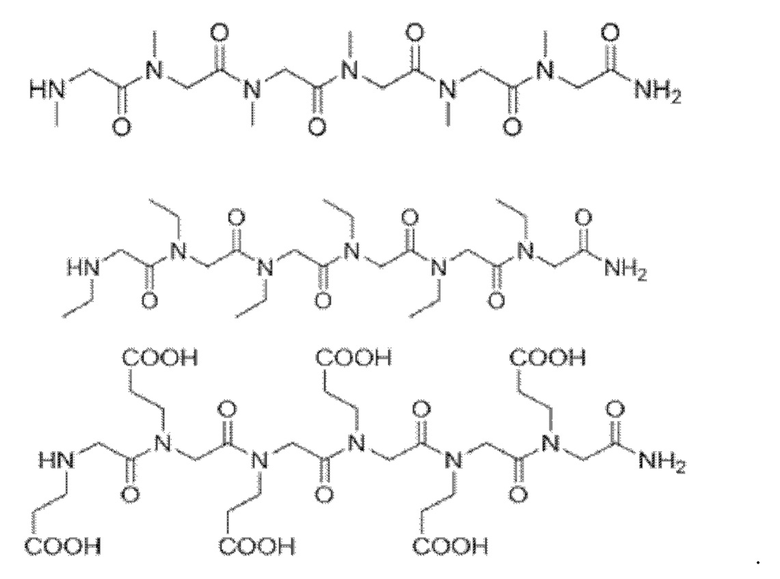
Согласно настоящему изобретению соединение формулы (9) получают, используя следующий путь синтеза:
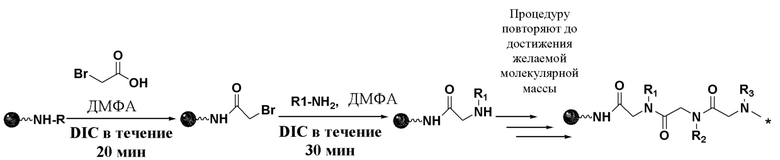
В одном из вариантов реализации настоящего изобретения молекула материала, подавляющего рост льда, представляет собой аминокислоту или полиаминокислоту. В настоящем изобретение дополнительно предложено применение упомянутой выше молекулы материала, подавляющего рост льда, такой как ПВС, пептидное соединение, аминокислота и полиаминокислота, для контроля роста кристаллов льда в водном растворе и применение пептидного соединения при приготовлении криоконсервирующего раствора для клеток или тканей.
Материалы, подавляющие рост льда, спроектированные и полученные согласно настоящему изобретению, такие как ПВС, пептидное соединение, аминокислота и полиаминокислота, применяют при приготовлении криоконсервирующего раствора для криоконсервации клеток, тканей, органов и т.п.
[Пример 1]
(1) Проектирование молекулярной структуры соединения:
Проектировали молекулы соединения, имеющие повторяющееся звено -[СН2-СНОН]-, для получения библиотеки молекулярных структур, которая включает молекулярные модели атактического и изотактического ПВС.
(2) Эксперимент по MD моделированию:
Разность в сродстве атактического ПВС и изотактического ПВС ко льду и воде прогнозировали в экспериментах по MD моделированию.
a. MD моделирование проводили с использованием GROMACS 5.1, а в качестве модели воды использовали модель ТГР4Р/2005, имеющую температуру плавления около 252,5K. Параметры взаимодействия молекул ПВС получали с использованием силового поля GROMOS54A7, и использовали скачкообразный алгоритм интегрирования с величиной шага интегрирования в 2 фс. Электростатическое взаимодействие рассчитывали по методу РМЕ, а радиусы отсечения для кулоновского потенциала и потенциала L-J составляли 1,0 нм в обоих случаях. Для регулирования температуры и давления использовали регулятор температуры V-rescale (модифицированный Berendsen) и регулятор давления. Временную константу установили на значение 0,1 пс.
b. Моделировали и выбирали для исследований соединения с молекулярными цепочками, имеющими 7 повторяющихся звеньев. Файлы топологии молекул ПВС генерировали посредством АТВ, и чтобы поддерживать тактичности двух типов молекул ПВС, требовалось соответствующим образом отрегулировать функции потенциала двухгранного угла углеродной цепи в этих молекулах.
c. Периодические граничные условия задавали для направления х, направления у и направления z, если моделировали системы водных растворов этих ПВС; в случае моделировании смешанных систем «лед-вода» периодические граничные условия задавали для направления х и направления у. Все системы моделировали до 120 нc, а для анализа использовали данные за последние 60 нc.
Сначала использовали системы водных растворов рассматриваемых молекул. В системе, имеющей только одну цепочку ПВС, использовали в целом 1491 молекулу воды, давление составило 1 атм, а температуры составили 240K, 250K, 260K, 270K, 300K и 330K.
В системах, взятых для исследования взаимодействий молекул ПВС со льдом, 6 молекулярных цепочек ПВС помещали в блок воды размерами 3,9 × 3,6 × 1,0 нм3; блок льда, включающий 1100 молекул воды, уравновешивали при 240К в течение 10 нc, после чего блок льда помещали под блоком воды вдоль оси z. Размер смешанной системы в направлении z увеличивали до 10 нм, и смешанную систему «лед-вода» помещали в центр блока воды.
Файлы топологии молекул ПВС генерировали посредством АТВ, и затем эти файлы топологии использовали непосредственно. Чтобы поддерживать тактичности двух типов молекул ПВС, параметры потенциальной энергии устанавливали на значение 50 ккал/моль, так чтобы молекулярные конфигурации этих двух типов молекул ПВС могли сохраняться и при повышенных температурах.
Модели молекулярных структур для двух типов ПВС, полученные MD моделированием, показаны на ФИГ. 9.
(3) Оценка моделирования
Молекула а-ПВС способна эффективно генерировать водородное связывание с поверхностью льда и таким образом адсорбироваться на поверхности льда, поскольку трехкратная величина расстояния между соседними группами ОН в ней соответствует размеру кристаллической решетки льда. В молекуле i-ПВС изменяется только направление гидроксильных групп, но не изменяется расстояние между соседними группами ОН, так что и i-ПВС, и а-ПВС имеют аналогичную способность адсорбироваться льдом. Тем не менее, согласно результатам MD моделирования, количество межмолекулярных водородных связей, образующихся между молекулой а-ПВС и молекулами воды, больше количества межмолекулярных водородных связей, образующихся между молекулой i-ПВС и молекулами воды, что указывает на более сильное сродство к воде у а-ПВС, чем у i-ПВС. Кроме того, состояния 6 молекулярных цепочек ПВС у межфазной границы «лед-вода», полученные в ходе MD моделирования, показывают, что молекулы а-ПВС имеют тенденцию больше распределяться вдоль межфазной границы «лед-вода» ввиду их хорошего сродства как ко льду, так и к воде, тогда как молекулы i-ПВС имеют тенденцию больше агрегироваться у межфазной границы «лед-вода» ввиду их более слабого сродства к воде (см. ФИГ. 2).
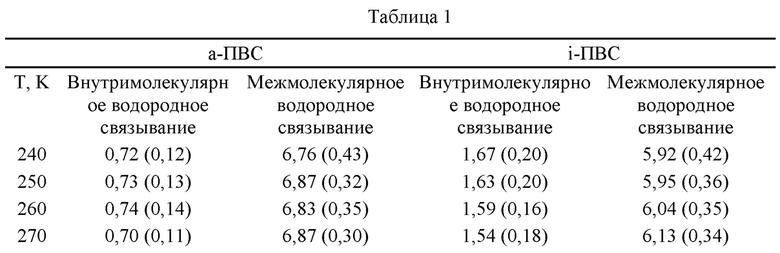
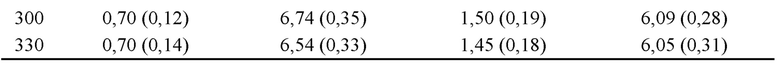
MD моделирование показывает величины контактируемой площади для двух типов молекул ПВС с молекулами воды у межфазной границы «лед-вода» при 240К, из которых видно, что контактируемая площадь а-ПВС больше контактируемой площади i-ПВС, еще раз подтверждая, что показатели распределения вдоль межфазной границы «лед-вода» у а-ПВС лучше, чем у i-ПВС (см. ФИГ. 10). Вероятность агрегации в водном растворе, рассчитанная при MD моделировании, у i-ПВС очевидно выше, чем у а-ПВС (ФИГ. 11). При 240К количество водородных связей, образующихся между этими двумя типами молекул ПВС и молекулами воды в структуре льда вдоль межфазной границы «лед-вода», аналогично, однако, количество водородных связей, образующихся между молекулой а-ПВС и молекулами воды вдоль межфазной границы «лед-вода» и в свободном водном растворе, очевидно больше, чем у i-ПВС. Следовательно, а-ПВС может лучше распределяться вдоль межфазной границы «лед-вода», тогда как i-ПВС больше агрегируется (см. ФИГ. 12).
Таким образом, многочисленные результаты MD моделирования показывают, что а-ПВС имеет более высокие показатели распределения вдоль межфазной границы «лед-вода» ввиду более сильного сродства его молекулярной структуры к молекулам воды, и поэтому оказывает более сильный эффект в подавлении роста льда, чем i-ПВС.
(4) Синтез спроектированных молекул ПВС
(4.1) Приготовление атактического поливинилового спирта а-ПВС с молекулярной массой, равной приблизительно 13-23 кДа, и диадной синдиотактичностью r, равной приблизительно 55%
Винилацетат (VAc, Sigma-Aldrich), из которого удален ингибитор, растворяли в 100 мл растворителя (метанола) в круглодонной колбе объемом 250 мл в атмосфере аргона, так чтобы получить 25-45% раствор VAc. После охлаждения полученного раствора до -5°С к нему осторожно по каплям добавляли 80 мМ 2,2'-азобис(2-метилпропионитрила) (Sigma-Aldrich). Затем раствору давали нагреться до комнатной температуры, после чего его перемешивали в течение 15 часов, разбавляли 1 л ацетона и по каплям добавляли к метанолу, получая белый осадок. Указанный осадок промывали метанолом, фильтровали и сушили в сушильном шкафу при 60°С под вакуумом в течение 6,0 часов, в результате чего получали твердое вещество белого цвета. Это твердое белое вещество растворяли в метаноле с получением раствора концентрацией (10 масс. %), и затем через этот раствор пропускали аргон для удаления из него кислорода. Затем к указанному раствору по каплям добавляли 25%-ный метанольный раствор гидроксида калия, и реакционную смесь перемешивали в течение 4 часов. После перемешивания реакционную смесь разбавляли 2М раствором хлористоводородной кислоты и добавляли к 2,0М метанольному раствору аммиака для осаждения, в результате чего получали атактический поливиниловый спирт (а-ПВС). Спектр протонного ЯМР (ФИГ. 3) показывает, что полученное соединение представляет собой полностью гидролизованный а-ПВС.
(4.2) Приготовление изотактического поливинилового спирта i-ПВС с молекулярной массой примерно 14-26 кДа и изотактичностью m, равной примерно 84%:
a. Приготовление поли-трет-бутилвинилового эфира (PBVE). Третбутилвиниловый эфир (t-BVE, Sigma-Aldrich) растворяли в 100 мл сухого толуола в круглодонной колбе объемом 250 мл в атмосфере аргона, в результате чего получали 2,5%-ный толуольный раствор t-BVE. После охлаждения полученного раствора до -78°С к нему осторожно по каплям добавляли 0,2 мМ диэтилэфирата трехфтористого бора (BF3⋅OEt2, Sigma-Aldrich), и через 2,0 часа дополнительно добавляли еще 0,2 мМ BF3⋅OEt2. Затем полученный раствор перемешивали при -78°С в течение 3,0 часов, после чего реакцию останавливали путем добавления небольшого количества метанола. Реакционный раствор по каплям добавляли в 2,0 л метанола при быстром перемешивании, в результате чего получали осадок светло-желтого цвета. Этот осадок промывали метанолом, фильтровали и сушили в сушильном шкафу при 60°С под вакуумом в течение 6,0 часов, в результате чего получали порошок твердого вещества светло-желтого цвета, которое, как показал спектр протонного ЯМР (ФИГ. 4А), представляло собой PBVE. Молекулярную массу синтезированного PBVE регулировали путем варьирования концентраций диэтилэфирата трехфтористого бора и третбутилвинилового эфира. Были успешно синтезированы разные образцы PBVE с различными молекулярными массами, что подтверждали хроматограммами гель-проникающей хроматографии (ГПХ), полученными с использованием тетрагидрофурановой (ТГФ) системы со скоростью потока 1 мл/мин (см. ФИГ. 5).
b. Приготовление сухого газообразного бромистого водорода (НВr). К 10 мл 48% водного раствора бромистого водорода (НВr, Alfa Aesar) в двугорлой колбе объемом 100 мл по каплям добавляли 5,0-30 мл трехбромистого фосфора (РВr3, Aladdin). Выделяющийся газ последовательно пропускали через тетрахлорметан (ССl4), красный фосфор (Р, Alfa Aesar) и хлористый кальций (СаСl2), в результате чего получали сухой газообразный НВr.
c. Приготовление изотактического поливинилового спирта (изотактический-ПВС, i-ПВС). Навеску 0,5 г PBVE растворяли в 15 мл сухого толуола в атмосфере аргона, после чего сухой аргон непрерывно пропускали через полученный раствор для удаления из него кислорода. Затем через вышеуказанный не содержащий кислорода раствор PBVE при 0°С пропускали сухой газообразный НВr, приготовленный на стадии (b). Примерно через 5,0 минут начинал выпадать светло-желтый осадок, и пропускание сухого газообразного НВr через раствор продолжали вплоть до прекращения выпадения осадка. Вышеуказанный реакционный раствор вливали в 200 мл метанольного раствора аммиака (2,0М). Полученный осадок промывали метанолом, фильтровали и сушили в вакуумном сушильном шкафу при 60°С в течение 6,0 часов, в результате чего получали порошок твердого вещества светло-желтого цвета. Как показывает спектр протонного ЯМР (ФИГ. 4А), гидролиз PBVE прошел полностью, в результате чего получили твердый i-ПВС.
(5) Верификация эффекта подавления роста льда у синтезированного ПВС (5.1) Эксперимент по динамическому светорассеянию (DLS) Распределение по размерам частиц дисперсий двух типов ПВС (а-ПВС с молекулярной массой примерно 13-23 кДа и диадной синдиотактичностью r, равной примерно 55% (Sigma-Aldrich); i-ПВС с молекулярной массой примерно 14-26 кДа и изотактичностью m, равной примерно 84%) в водном растворе при 25°С определяли в DLS эксперименте, и эксперимент проводили на приборе Nano ZS (Malvern Instruments) с термостатируемой камерой и лазером He-Ne 4 мВт (λ=632,8 нм), при этом угол рассеяния составлял 173°. Сначала готовили водные растворы а-ПВС и i-ПВС с концентрациями 1,0 мг/мл, 4,0 мг/мл, 10 мг/мл и 20 мг/мл, затем примерно по 1,0 мл каждого раствора ПВС добавляли в одноразовые полистироловые кюветы толщиной 12 мм для измерений.
Результаты DLS эксперимента показывают, что при одинаковых концентрациях растворов а-ПВС имеет гораздо меньший размер частиц, диспергированных в водном растворе, чем i-ПВС (см. ФИГ. 6). Это означает, что по сравнению с а-ПВС i-ПВС в водном растворе имеет тенденцию находиться в агрегированном состоянии. Это согласуется с результатами MD моделирования, показывающими, что количество внутримолекулярных водородных связей у а-ПВС меньше, чем у i-ПВС, а количество межмолекулярных водородных связей, образующихся между молекулами а-ПВС и молекулами воды, больше количества таких же связей, образующихся между молекулами i-ПВС и молекулами воды.
(5.2) Количественный анализ на активность по подавлению перекристаллизации льда (IRI)
Активность по IRI оценивали с применением способа «замораживания брызг», в котором образец растворяют и диспергируют в растворе буфера DPBS, после чего 10-30 мкл полученного раствора капают на поверхность чистого кремниевого диска, предварительно охлажденного до -60°С с высоты не менее 1,0 м; замороженные образцы раствора медленно нагревали до -6°С со скоростью 10°С в минуту на предметном столике с системой нагрева-охлаждения и «отжигали» при этой же температуре в течение 30 минут; размеры ледяных кристаллов наблюдали и регистрировали с помощью поляризационного микроскопа и высокоскоростной фотокамеры. Образцы на предметном столике с системой нагрева-охлаждения герметизировали, чтобы обеспечивать поддержание их внутренней влажности на уровне примерно 50%. Процедуру повторяли не менее трех раз для каждого образца, а размеры ледяных кристаллов измеряли с помощью нано-измерителя Nano Measurer 1.2 с погрешностью результата, равной стандартному отклонению.
(5.3) Наблюдение топологии льда (DIS) и измерение теплового гистерезиса (ТН)
Наблюдения DIS и измерения ТН проводили с использованием нанолитрового осмометра. Сначала нагревали стеклянную трубку на пламени спиртовки до начала плавления с одновременным ее оттягиванием, так чтобы получился очень тонкий капилляр с микроскопическим просветом, который затем соединяли с микрошприцем. Иммерсионное масло с повышенной вязкостью наносили на диск с микронными лунками, и водный раствор, в котором растворен исследуемый материал, выдавливали в микролунки с помощью микрошприца. Капельки раствора быстро замораживали путем регулирования температуры и затем медленно нагревали, добиваясь формирования монокристалла льда. Затем монокристалл льда медленно охлаждали с точностью 0,01°С и проводили наблюдения DIS и измерения ТН с помощью микроскопа, снабженного высокоскоростной фотокамерой.
Способность а-ПВС (Mw 13-23 кДа) подавлять рост ледяных кристаллов гораздо лучше, чем у i-ПВС (Mw 14-26 кДа) с аналогичной молекулярной массой (см. ФИГ. 7). Как можно видеть на ФИГ. 7А, размер частиц в растворе а-ПВС гораздо меньше, чем в растворе i-ПВС при одинаковых концентрациях растворов. Как можно видеть на ФИГ. 7В, показатель среднего размера крупнейших кристаллов (MLGS) при образовании льда в присутствии а-ПВС относительно этого показателя в буфере DPBS после 2,0 мг/мл достигает минимума, составляющего 20% (относительно MLGS ледяных кристаллов в буфере DPBS). Величина MLGS для i-ПВС с различными молекулярными массами относительно MLGS в буфере DPBS возрастает с ростом концентрации и при 10 мг/мл достигает минимума, который составляет всего лишь приблизительно 50% (относительно MLGS ледяных кристаллов в буфере DPBS). При этом MLGS не убывает с ростом концентрации, а слегка повышается, и продолжает повышаться до 20 мг/мл. i-ПВС (Mw 14-26 кДа) со степенью полимеризации более 333 с большим трудом растворяется при концентрациях более 30 мг/мл. Соответственно, ввиду ограничения в растворимости i-ПВС, IRI-активность i-ПВС оптимально составляет 50% относительно MLGS в DPBS при концентрации 10 мг/мл, тогда как IRI-активность а-ПВС оптимально составляет 20% относительно MLGS в DPBS при концентрации 2,0 мг/мл. Это согласуется с полученными при MD моделировании выводами о том, что а-ПВС более легко распределяется вдоль межфазной границы «лед-вода», чем i-ПВС, за счет чего а-ПВС способен лучше подавлять рост кристаллов льда даже при более низких дозировках, чем i-ПВС.
Можно видеть, что результаты MD моделирования и результаты реальных подтверждающих экспериментов хорошо согласуются между собой. Показатели подавления роста кристаллов льда для материала, подавляющего рост льда, могут быть точно предсказаны с помощью MD моделирования, и соответственно молекулярное проектирование материалов, подавляющих рост льда, можно применять с достаточно высокой эффективностью.
Соединения с формулами (1)-(9) были спроектированы таким же способом молекулярного проектирования, синтезированы и исследованы на эффекты по подавлению роста льда.
[Пример 2] Синтез соединения формулы (1)
(1) 2-хлортритилхлоридную смолу помещали в реакционную пробирку и добавляли ДХМ (20 мл/г). Полученную смесь встряхивали в течение 30 минут. Затем растворитель удаляли с помощью воронки Шотта путем отсасывания вакуумом. К полученному остатку добавляли трехкратный мольный избыток Fmoc-L-Pro-OH и восьмикратный мольный избыток DIEA, после чего добавляли ДМФА для растворения. Полученную смесь встряхивали в течение 30 минут. Для блокировки концевых групп применяли обработку метанолом в течение 30 минут.
(2) Удаляли растворитель (ДМФА). Затем добавляли 20% раствор пиперидина в ДМФА (10 мл/г) и через 5 минут растворитель удаляли. Затем снова добавляли 20% раствор пиперидина в ДМФА (10 мл/г), и через 15 минут раствор пиперидина удаляли. Отбирали небольшое количество смолы и промывали ее этанолом три раза, затем добавляли реактив нингидрина и нагревали при 105-110°С в течение 5 минут. Появлялась темно-синяя окраска, что свидетельствовало о положительной реакции.
(3) После того, как продукт, полученный в результате вышеприведенной реакции, последовательно промывали ДМФА (15 мл/г, дважды), метанолом (15 мл/г, дважды) и ДМФА (15 мл/г, дважды), в реакционную пробирку добавляли двукратный избыток Fmoc-L-Thr(tBu)-ОН, растворенный в как можно меньшем количестве ДМФА, и двукратный избыток HBTU. Сразу после этого добавляли восьмикратный избыток DIEA, и смесь оставляли реагировать в течение 30 минут.
(4) После удаления раствора отсасыванием отбирали небольшое количество смолы и промывали ее этанолом три раза, затем добавляли реактив нингидрина и нагревали при 105-110°С в течение 5 минут. Отсутствие окраски смеси свидетельствовало об отрицательной реакции, т.е. о том, что реакция завершена.
(5) После того, как продукт, полученный в результате вышеприведенной реакции, последовательно промывали ДМФА (15 мл/г, дважды), метанолом (15 мл/г, дважды) и ДМФА (15 мл/г, дважды), растворитель удаляли. Затем добавляли 20% раствор пиперидина в ДМФА (10 мл/г) и через 5 минут растворитель удаляли. Затем снова добавляли 20% раствор пиперидина в ДМФА (10 мл/г), и через 15 минут раствор пиперидина удаляли. Отбирали небольшое количество смолы и промывали ее этанолом, добавляли реактив нингидрина и нагревали при 105-110°С в течение 5 минут. Появлялась темно-синяя окраска, что свидетельствовало о положительной реакции.
(6) После того, как продукт, полученный в результате вышеприведенной реакции, последовательно промывали ДМФА (15 мл/г, дважды), метанолом (15 мл/г, дважды) и ДХМ (15 мл/г, дважды), смолу высушивали путем отсасывания растворителя вакуумом.
(7) Полученный продукт отщепляли от смолы с помощью отщепляющей жидкости (15 мл/г, TFA:вода:EDT:Tis=95:1:2:2, об/об) в течение 90 мин. Отщепляющую жидкость выпаривали насухо продувкой азотом, остаток лиофилизировали, и в итоге получали сырой продукт полипептида.
(8) Полипептид очищали и подвергали солевой трансформации или обессоливанию методом ВЭЖХ. Условия хроматографирования: tR=6,1 мин, колонка для очистки: модель Kromasil 100-5С18, 4,6 мм*250 мм, градиент подвижной фазы: ацетонитрил с 0,1% TFA и водный раствор с 0,1% TFA, 0 мин. - 1:99, 20 мин - 1:9. Очищенный раствор лиофилизировали и получали очищенный продукт L-Thr-L-Pro (обозначаемый как TP). Выход составлял примерно 80%.. Масс-спектр показал [М+Н]+ при 217,3.
[Пример 3] Синтез соединения формулы (2)
(1) 2-хлортритилхлоридную смолу помещали в реакционную пробирку и добавляли ДХМ (20 мл/г). Полученную смесь встряхивали в течение 30 минут. Затем растворитель удаляли с помощью воронки Шотта путем отсасывания вакуумом. К полученному остатку добавляли трехкратный мольный избыток Fmoc-L-Thr(tBu)-OH и восьмикратный мольный избыток DIEA, после чего добавляли ДМФА для растворения. Полученную смесь встряхивали в течение 30 минут. Для блокировки концевых групп применяли обработку метанолом в течение 30 минут.
(2) Удаляли растворитель (ДМФА). Затем добавляли 20% раствор пиперидина в ДМФА (10 мл/г), и через 5 минут растворитель удаляли. Затем снова добавляли 20% раствор пиперидина в ДМФА (10 мл/г), и через 15 минут раствор пиперидина удаляли. Отбирали небольшое количество смолы и промывали ее этанолом три раза, затем добавляли реактив нингидрина и нагревали при 105-110°С в течение 5 минут. Появлялась темно-синяя окраска, что свидетельствовало о положительной реакции.
(3) После того, как продукт, полученный в результате вышеприведенной реакции, последовательно промывали ДМФА (15 мл/г, дважды), метанолом (15 мл/г, дважды) и ДМФА (15 мл/г, дважды), в реакционную пробирку добавляли двукратный избыток Fmoc-L-Arg(Pbf)-ОН, растворенный в как можно меньшем количестве ДМФА, и двукратный избыток HBTU. Сразу после этого добавляли восьмикратный избыток DIEA, и смесь оставляли реагировать в течение 30 минут.
(4) После удаления раствора отсасыванием отбирали небольшое количество смолы и промывали ее этанолом три раза, затем добавляли реактив нингидрина и нагревали при 105-110°С в течение 5 минут. Отсутствие окраски смеси свидетельствовало об отрицательной реакции, т.е. о том, что реакция завершена.
(5) После того, как продукт, полученный в результате вышеприведенной реакции, последовательно промывали ДМФА (15 мл/г, дважды), метанолом (15 мл/г, дважды) и ДМФА (15 мл/г, дважды), растворитель удаляли. Затем добавляли 20% раствор пиперидина в ДМФА (10 мл/г), и через 5 минут растворитель удаляли. Затем снова добавляли 20% раствор пиперидина в ДМФА (10 мл/г), и через 15 минут раствор пиперидина удаляли. Отбирали небольшое количество смолы и промывали ее этанолом, добавляли реактив нингидрина и нагревали при 105-110°С в течение 5 минут. Появлялась темно-синяя окраска, что свидетельствовало о положительной реакции.
(6) После того, как продукт, полученный в результате вышеприведенной реакции, последовательно промывали ДМФА (15 мл/г, дважды), метанолом (15 мл/г, дважды) и ДХМ (15 мл/г, дважды), смолу высушивали путем отсасывания растворителя вакуумом.
(7) Полученный продукт отщепляли от смолы с помощью отщепляющей жидкости (15 мл/г, TFA:вода:EDT:Tis=95:1:2:2, об/об) в течение 90 мин. Затем отщепляющую жидкость выпаривали насухо продувкой азотом, остаток лиофилизировали, и в итоге получали сырой продукт полипептида.
(8) Полипептид очищали и подвергали солевой трансформации или обессоливанию методом ВЭЖХ. Условия хроматографирования: tR=4,8 мин, колонка для очистки: модель Kromasil 100-5С18, 4,6 мм*250 мм, градиент подвижной фазы: ацетонитрил с 0,1% TFA и водный раствор с 0,1% TFA, 0 мин. - 1:99, 20 мин - 1:4. Очищенный раствор лиофилизировали и получали очищенный продукт L-Thr-L-Arg (или TR). Выход составлял примерно 80%. Масс-спектр показал [М+Н]+ при 276,2.
[Пример 4] Синтез соединения формулы (3)
(1) 2-хлортритилхлоридную смолу помещали в реакционную пробирку и добавляли ДХМ (20 мл/г). Полученную смесь встряхивали в течение 30 минут. Затем растворитель удаляли с помощью воронки Шотта путем отсасывания вакуумом. К полученному остатку добавляли трехкратный мольный избыток Fmoc-L-Thr(tBu)-OH и восьмикратный мольный избыток DIEA, после чего добавляли ДМФА для растворения. Полученную смесь встряхивали в течение 30 минут. Для блокировки концевых групп применяли обработку метанолом в течение 30 минут.
(2) Удаляли растворитель (ДМФА). Затем добавляли 20% раствор пиперидина в ДМФА (10 мл/г), и через 5 минут растворитель удаляли. Затем снова добавляли 20% раствор пиперидина в ДМФА (10 мл/г), и через 15 минут раствор пиперидина удаляли. Отбирали небольшое количество смолы и промывали ее этанолом три раза, затем добавляли реактив нингидрина и нагревали при 105-110°С в течение 5 минут. Появлялась темно-синяя окраска, что свидетельствовало о положительной реакции.
(3) После того, как продукт, полученный в результате вышеприведенной реакции, последовательно промывали ДМФА (15 мл/г, дважды), метанолом (15 мл/г, дважды) и ДМФА (15 мл/г, дважды), в реакционную пробирку добавляли двукратный избыток Fmoc-Arg(Pbf)-ОН, растворенный в как можно меньшем количестве ДМФА, и двукратный избыток HBTU. Сразу после этого добавляли восьмикратный избыток DIEA, и смесь оставляли реагировать в течение 30 минут.
(4) После удаления раствора отсасыванием отбирали небольшое количество смолы и промывали ее этанолом три раза, затем добавляли реактив нингидрина и нагревали при 105-110°С в течение 5 минут. Отсутствие окраски смеси свидетельствовало об отрицательной реакции, т.е. о том, что реакция завершена.
(5) После того, как продукт, полученный в результате вышеприведенной реакции, последовательно промывали ДМФА (15 мл/г, дважды), метанолом (15 мл/г, дважды) и ДМФА (15 мл/г, дважды), растворитель удаляли. Затем добавляли 20% раствор пиперидина в ДМФА (10 мл/г), и через 5 минут растворитель удаляли. Затем снова добавляли 20% раствор пиперидина в ДМФА (10 мл/г), и через 15 минут раствор пиперидина удаляли. Отбирали небольшое количество смолы и промывали ее этанолом, добавляли реактив нингидрина и нагревали при 105-110°С в течение 5 минут. Появлялась темно-синяя окраска, что свидетельствовало о положительной реакции.
(6) После того, как продукт, полученный в результате вышеприведенной реакции, последовательно промывали ДМФА (15 мл/г, дважды), метанолом (15 мл/г, дважды) и ДМФА (15 мл/г, дважды), смолу высушивали путем отсасывания растворителя вакуумом.
(7) Стадии (3)-(5) повторяли для связывания аминокислоты Fmoc-L-Thr(tBu)-OH. После того, как продукт, полученный в результате данной реакции, последовательно промывали ДМФА (15 мл/г, дважды), метанолом (15 мл/г, дважды) и ДХМ (15 мл/г, дважды), смолу высушивали путем отсасывания растворителя вакуумом.
(8) Полученный продукт отщепляли от смолы с помощью отщепляющей жидкости (15 мл/г, TFA:вода:EDT:Tis=95:1:2:2, об/об) в течение 90 мин. Затем отщепляющую жидкость выпаривали насухо продувкой азотом, остаток лиофилизировали, и в итоге получали сырой продукт полипептида.
(9) Полипептид очищали и подвергали солевой трансформации или обессоливанию методом ВЭЖХ. Условия хроматографирования: tR=3,9 мин, колонка для очистки: модель Kromasil 100-5С18, 4,6 мм*250 мм, градиент подвижной фазы: ацетонитрил с 0,1% TFA и водный раствор с 0,1% TFA, 0 мин. - 1:99, 20 мин - 1:4. Очищенный раствор лиофилизировали и получали очищенный продукт L-Thr-L-Arg-L-Thr (или TRT). Выход составлял примерно 75%. Масс-спектр показал [М+Н]+ при 377,4.
[Пример 5] Синтез соединения формулы (4)
(1) 2-хлортритилхлоридную смолу помещали в реакционную пробирку и добавляли ДХМ (20 мл/г). Полученную смесь встряхивали в течение 30 минут. Затем растворитель удаляли с помощью воронки Шотта путем отсасывания вакуумом. К полученному остатку добавляли трехкратный мольный избыток Fmoc-L-Thr(tBu)-OH и восьмикратный мольный избыток DIEA, после чего добавляли ДМФА для растворения. Полученную смесь встряхивали в течение 30 минут. Для блокировки концевых групп применяли обработку метанолом в течение 30 минут.
(2) Удаляли растворитель (ДМФА). Затем добавляли 20% раствор пиперидина в ДМФА (10 мл/г), и через 5 минут растворитель удаляли. Затем снова добавляли 20% раствор пиперидина в ДМФА (10 мл/г), и через 15 минут раствор пиперидина удаляли. Отбирали небольшое количество смолы и промывали ее этанолом три раза, затем добавляли реактив нингидрина и нагревали при 105-110°С в течение 5 минут. Появлялась темно-синяя окраска, что свидетельствовало о положительной реакции.
(3) После того, как продукт, полученный в результате вышеприведенной реакции, последовательно промывали ДМФА (15 мл/г, дважды), метанолом (15 мл/г, дважды) и ДМФА (15 мл/г, дважды), в реакционную пробирку добавляли двукратный избыток Fmoc-L-Pro-OH, растворенный в как можно меньшем количестве ДМФА, и двукратный избыток HBTU. Сразу после этого добавляли восьмикратный избыток DIEA, и смесь оставляли реагировать в течение 30 минут.
(4) После удаления раствора отсасыванием отбирали небольшое количество смолы и промывали ее этанолом три раза, затем добавляли реактив нингидрина и нагревали при 105-110°С в течение 5 минут. Отсутствие окраски смеси свидетельствовало об отрицательной реакции, т.е. о том, что реакция завершена.
(5) После того, как продукт, полученный в результате вышеприведенной реакции, последовательно промывали ДМФА (15 мл/г, дважды), метанолом (15 мл/г, дважды) и ДМФА (15 мл/г, дважды), растворитель удаляли. Затем добавляли 20% раствор пиперидина в ДМФА (10 мл/г), и через 5 минут растворитель удаляли. Затем снова добавляли 20% раствор пиперидина в ДМФА (10 мл/г), и через 15 минут раствор пиперидина удаляли. Отбирали небольшое количество смолы и промывали ее этанолом, добавляли реактив нингидрина и нагревали при 105-110°С в течение 5 минут. Появлялась темно-синяя окраска, что свидетельствовало о положительной реакции.
(6) После того, как продукт, полученный в результате вышеприведенной реакции, последовательно промывали ДМФА (15 мл/г, дважды), метанолом (15 мл/г, дважды) и ДМФА (15 мл/г, дважды), смолу высушивали путем отсасывания растворителя вакуумом.
(7) Стадии (3)-(5) повторяли для связывания аминокислоты Fmoc-L-Thr(tBu)-OH. После того, как продукт, полученный в результате данной реакции, последовательно промывали ДМФА (15 мл/г, дважды), метанолом (15 мл/г, дважды) и ДХМ (15 мл/г, дважды), смолу высушивали путем отсасывания растворителя вакуумом.
(8) Полученный продукт отщепляли от смолы с помощью отщепляющей жидкости (15 мл/г, TFA:вода:EDT:Tis=95:1:2:2, об/об) в течение 90 мин. Затем отщепляющую жидкость выпаривали насухо продувкой азотом, остаток лиофилизировали, и в итоге получали сырой продукт полипептида.
(9) Полипептид очищали и подвергали солевой трансформации или обессоливанию методом ВЭЖХ. Условия хроматографирования: tR=7,6 мин, колонка для очистки: модель Kromasil 100-5С18, 4,6 мм*250 мм, градиент подвижной фазы: ацетонитрил с 0,1% TFA и водный раствор с 0,1% TFA, 0 мин. - 1:99, 20 мин - 2:8. Очищенный раствор лиофилизировали и получали очищенный продукт L-Thr-L-Pro-L-Thr (или ТРТ). Выход составлял примерно 70%. Масс-спектр показал [М+Н]+ при 318,3.
[Пример 6] Синтез соединения формулы (5)
(1) 2-хлортритилхлоридную смолу помещали в реакционную пробирку и добавляли ДХМ (20 мл/г). Полученную смесь встряхивали в течение 30 минут. Затем растворитель удаляли с помощью воронки Шотта путем отсасывания вакуумом. К полученному остатку добавляли трехкратный мольный избыток Fmoc-L-Thr(tBu)-OH и восьмикратный мольный избыток DIEA, после чего добавляли ДМФА для растворения. Полученную смесь встряхивали в течение 30 минут. Для блокировки концевых групп применяли обработку метанолом в течение 30 минут.
(2) Удаляли растворитель (ДМФА). Затем добавляли 20% раствор пиперидина в ДМФА (10 мл/г), и через 5 минут растворитель удаляли. Затем снова добавляли 20% раствор пиперидина в ДМФА (10 мл/г), и через 15 минут раствор пиперидина удаляли. Отбирали небольшое количество смолы и промывали ее этанолом три раза, затем добавляли реактив нингидрина и нагревали при 105-110°С в течение 5 минут. Появлялась темно-синяя окраска, что свидетельствовало о положительной реакции.
(3) После того, как продукт, полученный в результате вышеприведенной реакции, последовательно промывали ДМФА (15 мл/г, дважды), метанолом (15 мл/г, дважды) и ДМФА (15 мл/г, дважды), в реакционную пробирку добавляли двукратный избыток Fmoc-L-Ala-OH, растворенный в как можно меньшем количестве ДМФА, и двукратный избыток HBTU. Сразу после этого добавляли восьмикратный избыток DIEA, и смесь оставляли реагировать в течение 30 минут.
(4) После удаления раствора отсасыванием отбирали небольшое количество смолы и промывали ее этанолом три раза, затем добавляли реактив нингидрина и нагревали при 105-110°С в течение 5 минут. Отсутствие окраски смеси свидетельствовало об отрицательной реакции, т.е. о том, что реакция завершена.
(5) После того, как продукт, полученный в результате вышеприведенной реакции, последовательно промывали ДМФА (15 мл/г, дважды), метанолом (15 мл/г, дважды) и ДМФА (15 мл/г, дважды), растворитель удаляли. Затем добавляли раствор 20% пиперидина в ДМФА (10 мл/г), и через 5 минут растворитель удаляли. Затем снова добавляли раствор 20% пиперидина в ДМФА (10 мл/г), и через 15 минут раствор пиперидина удаляли. Отбирали небольшое количество смолы и промывали ее этанолом, добавляли реактив нингидрина и нагревали при 105-110°С в течение 5 минут. Появлялась темно-синяя окраска, что свидетельствовало о положительной реакции.
(6) После того, как продукт, полученный в результате вышеприведенной реакции, последовательно промывали ДМФА (15 мл/г, дважды), метанолом (15 мл/г, дважды) и ДМФА (15 мл/г, дважды), смолу высушивали путем отсасывания растворителя вакуумом.
(7) Стадии (3)-(5) повторяли для связывания аминокислоты Fmoc-L-Ala-OH. После того, как продукт, полученный в результате данной реакции, последовательно промывали ДМФА (15 мл/г, дважды), метанолом (15 мл/г, дважды) и ДХМ (15 мл/г, дважды), смолу высушивали путем отсасывания растворителя вакуумом.
(8) Полученный продукт отщепляли от смолы с помощью отщепляющей жидкости (15 мл/г, TFA:вода:EDT:Tis=95:1:2:2, об/об) в течение 90 мин. Затем отщепляющую жидкость выпаривали насухо продувкой азотом, остаток лиофилизировали, и в итоге получали сырой продукт полипептида.
(9) Полипептид очищали и подвергали солевой трансформации или обессоливанию методом ВЭЖХ. Условия хроматографирования: tR=7,9 мин, колонка для очистки: модель Kromasil 100-5С18, 4,6 мм*250 мм, градиент подвижной фазы: ацетонитрил с 0,1% TFA и водный раствор с 0,1% TFA, 0 мин. - 1:99, 20 мин - 1:9. Очищенный раствор лиофилизировали и получали очищенный продукт L-Thr-L-Pro-L-Thr (или ТРТ). Выход составлял примерно 70%. Масс-спектр показал [М-8Н]+ при 260,1.
[Пример 7] Синтез соединений формулы (6), формулы (7) и формулы (8) Приготовление соединения формулы (6):
(1) GDL-L-Thr приготавливали с применением способа твердофазного синтеза.
(2) Очистка методом ВЭЖХ. Условия хроматографирования: tR=3,4 мин, колонка для очистки: тип SHIMADZU Intertsil ODS-SP (4,6 мм*250 мм*5 мкм), градиент подвижной фазы: ацетонитрил с 0,1% TFA и водный раствор с 0,1% TFA, 0,01-20 минут - 1:99, 20-30 минут -21:79, 30-40 минут - 100:0, 40-50 минут - 1:99. Выход составлял около 50%. Масс-спектр показал [М-Н]+ при 296,099.
Соединение GDL-L-Thr, приготовленное с применением способа твердофазного синтеза, имеет более высокую чистоту, и его легче выделять. Экспериментальные результаты показывают, что GDL-L-Thr, приготовленное с применением способа твердофазного синтеза, обладает повышенной чистотой и имеет хорошую способность в подавлении роста ледяных кристаллов (см. ФИГ. 13).
Оба соединения с формулами (7) и (8) можно получать способом твердофазного синтеза. [Пример 8] Синтез соединения формулы (9)
(1) В пробирку для синтеза полипептида вливали раствор дихлордиметилсилана в ДХМ, и после выдержки в течение 30 минут пробирку высушивали на воздухе перед дальнейшим использованием.
(2) В пробирку для синтеза помещали 100 мг смолы, добавляли 2 мл ДМФА и пропускали ток азота. Смола набухала в течение 10 минут, после чего ее фильтровали путем отсасывания под вакуумом.
(3) Для снятия защиты добавляли 1 мл раствора 4-метилпиперидина в ДМФА, который удаляли через 5 минут. Затем снова добавляли 1 мл раствора 4-метилпиперидина в ДМФА, который удаляли через 15 минут. Смесь барботировали азотом и фильтровали с отсасыванием под вакуумом.
(4) Полученную смесь промывали ДМФА 5 раз, барботировали азотом и фильтровали с отсасыванием под вакуумом.
(5) К смеси последовательно добавляли 0,5 мл 2М раствора бромуксусной кислоты в ДМФА и раствор N,N-диизопропилкарбодиимида в ДМФА, барботировали в течение 20 минут, фильтровали с отсасыванием под вакуумом и промывали ДМФА 3 раза.
(6) Затем к смеси добавляли 1 мл 1М раствора первичного амина в ДМФА, барботировали в течение 30 минут, промывали ДМФА и промывали дихлорметаном (3 раза).
(7) Стадии (5) и (6) повторяли до тех пор, пока не была достигнута желаемая молекулярная масса.
(8) Затем к смеси добавляли 4 мл отщепляющей жидкости, перемешивали до однородности и продували азотом досуха. В заключение продукт лиофилизировали и затем очищали с получением очищенного продукта.
В полученном пептоиде R представляет собой -СН3, -СН2СН3 или -СН2СН2СООН. Масс-спектр показывает [М+Н]+ при 444,6, если R=-СН3, [М+Н]+ при 528,8, если R=-СН2СН3, и
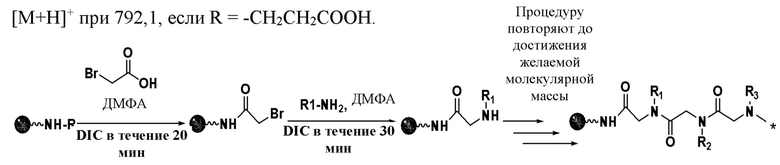
[Эксперимент по оценке подавления перекристаллизации льда (TRI)]
Активность по IRI оценивали с применением способа «замораживания брызг», в котором образец растворяют и диспергируют в растворе буфера DPBS, после чего 10-30 мкл полученного раствора капают на поверхность чистого кремниевого диска, предварительно охлажденного до -60°С с высоты не менее 1,0 м. Замороженные образцы раствора медленно нагревали до -6°С со скоростью 10°С в минуту на предметном столике с системой нагрева-охлаждения и «отжигали» при этой температуре в течение 30 минут. Размеры ледяных кристаллов наблюдали и регистрировали с помощью поляризационного микроскопа и высокоскоростной фотокамеры. Образцы на предметном столике с системой нагрева-охлаждения герметизировали, чтобы обеспечить поддержание их внутренней влажности на уровне примерно 50%. Процедуру повторяли не менее трех раз для каждого образца, а размеры ледяных кристаллов измеряли с помощью нано-измерителя Nano Measurer 1.2 с погрешностью результата, равной стандартному отклонению.
Наблюдения топологии льда (DIS) и измерения теплового гистерезиса (ТН) проводили с использованием нанолитрового осмометра. Сначала нагревали стеклянную трубку на пламени спиртовки до начала плавления с одновременным ее оттягиванием, так чтобы получился очень тонкий капилляр с микроскопическим просветом, который затем соединяли с микрошприцем. Иммерсионное масло с повышенной вязкостью наносили на диск с микронными лунками, после чего водный раствор, в котором растворен исследуемый материал, выдавливали в микролунки с помощью микрошприца. Капельки раствора быстро замораживали путем регулирования температуры и затем медленно нагревали, добиваясь формирования монокристалла льда. Затем монокристалл льда медленно охлаждали с точностью 0,01°С и проводили наблюдения DIS и измерения ТН с помощью микроскопа, снабженного высокоскоростной фотокамерой.
Испытания на IRI-активность проводили способом «замораживания брызг» на 20 мкл DPBS раствора соединения TR, приготовленного в Примере 3. Величины MLGS (как % относительно их значений в буфере DPBS) показаны на ФИГ. 17. Величины MLGS в случае соединения TR, связанного химическими связями, очевидно меньше, чем в случае DPBS растворов аргинина и треонина при тех же концентрациях.
Деионизированные водные растворы соединения TR, приготовленного в Примере 3, брали для наблюдений DIS с использованием нанолитрового осмометра. Было установлено, что соединение TR оказывает слабый модифицирующий эффект на топографию ледяных кристаллов (при степени переохлаждения -0,1°С, от -0,4°С до 0,01°С), как это показано на ФИГ. 18. Никакого теплового гистерезиса (ТН) не наблюдали.
Испытания на IRI-активность проводили способом «замораживания брызг» на 20 мкл DPBS растворов соединений GDL-L-Thr, GDL-L-Ser и GDL-L-Val, приготовленных в Примере 7. Величины MLGS (как % относительно их значений в буфере DPBS) показаны на ФИГ. 13 и ФИГ. 15-16. Величины MLGS в случае соединений GDL-L-Thr, GDL-L-Ser и GDL-L-Val, связанных химическими связями, очевидно меньше, чем в случае DPBS растворов GDL и аминокислот при тех же концентрациях, и меньше, чем в случае DPBS растворов смесей GDL с аминокислотами при тех же концентрациях.
Деионизированные водные растворы соединения GDL-L-Thr, приготовленного в Примере 7, брали для наблюдений DIS с использованием нанолитрового осмометра. Было установлено, что соединение GDL-L-Thr оказывает слабый модифицирующий эффект на топографию ледяных кристаллов (при степени переохлаждения -0,1°С, от -0,4°С до 0,01°С), как это показано на ФИГ. 14. Никакого теплового гистерезиса (ТН) не наблюдали.
Испытания на IRI-активность проводили способом «замораживания брызг» на 20 мкл DPBS растворов соединений, приготовленных в Примере 8. Величины MLGS (как % относительно их значений в буфере DPBS) показаны на ФИГ. 19.
Деионизированные водные растворы трех пептоидов, приготовленных в Примере 8, брали для наблюдений DIS с использованием нанолитрового осмометра. Было установлено, что пептоиды, в которых R=-СН3 и -СН2СН3, имели довольно очевидные модифицирующие эффекты на топографию ледяных кристаллов, а пептоиды, в которых R=-СН2СН2СООН, не оказывали никакого модифицирующего эффекта на топографию ледяных кристаллов (при степени переохлаждения -0,1°С, от -0,4°С до 0,01°С). Полученная топография показана на ФИГ. 20. Никакого теплового гистерезиса (ТН) в случае всех трех пептоидов не обнаруживали.
Приведенные выше результаты показывают, что полученные пептидные соединения обладают активностью в подавлении роста ледяных кристаллов и оказывают модифицирующее воздействие на топографию ледяных кристаллов. В частности, соединение формулы (9), в котором R=-СН3 или -СН2СН3, обладает отличным модифицирующим эффектом на топографию ледяных кристаллов при отсутствии ТН и может проявлять эффект контролирования роста ледяных кристаллов. Соответственно, указанное соединение можно использовать в составе криоконсервирующего раствора.
В. Оценка показателей подавления роста льда и скрининг материалов, подавляющих рост льда
Количество материала, подавляющего рост льда, адсорбированного на поверхности льда, выражается как (масса материала, подавляющего рост льда, адсорбированного на поверхности льда (m1)) / (общая масса материала, подавляющего рост льда, содержащаяся в исходном растворе, содержащем материал, подавляющий рост льда (m2)) × 100%.
В одном из вариантов воплощения настоящего изобретения эксперимент по адсорбции материала льдом включает следующие стадии:
S1: взятие навески материала, подавляющего рост льда, массой m2 с приготовлением водного раствора материала, подавляющего рост льда, после чего его охлаждают до температуры переохлаждения (ниже температуры кристаллизации);
S2: размещение в водном растворе предварительно охлажденного стержня регулирования температуры, так чтобы вызывать рост слоя льда на поверхности стержня регулирования температуры, при этом водный раствор постоянно перемешивают, давая возможность материалу, подавляющему рост льда, равномерно адсорбироваться по поверхности ледяного слоя, а температуру водного раствора и температуру стержня регулирования температуры постоянно поддерживают на уровне температуры переохлаждения; и
S3: определение количества материала, подавляющего рост льда, адсорбированного на поверхности льда.
Для проведения эксперимента по адсорбции материалов льдом использовали устройство, показанное на ФИГ. 21. Указанное устройство включает многослойную полость для размещения жидкости, стержень регулирования температуры и температурный регулятор, где многослойная полость для размещения жидкости последовательно включает (перечисляя изнутри наружу) полость для адсорбции материала льдом, полость бани и полость для размещения охлаждающей жидкости. Стержень регулирования температуры установлен в полости для адсорбции материала льдом. Температуру стержня регулирования температуры и полости для размещения жидкости задают посредством температурного регулятора. Стержень регулирования температуры имеет полую структуру и выполнен из теплопроводящего материала, и полая структура стержня регулирования температуры имеет входное отверстие для жидкости и выходное отверстие для жидкости. Температурный регулятор представляет собой регулятор температуры жидкостей и снабжен концевым отверстием для выпуска охлаждающей жидкости и концевым отверстием для возврата охлаждающей жидкости. Два конца полости для размещения жидкости также имеют входное отверстие для жидкости и выходное отверстие для жидкости, концевое отверстие для выпуска охлаждающей жидкости температурного регулятора, входное отверстие для жидкости стержня регулирования температуры, выходное отверстие для жидкости стержня регулирования температуры, входное отверстие резервуара для размещения охлаждающей жидкости, выходное отверстие резервуара для размещения охлаждающей жидкости и концевое отверстие для возврата охлаждающей жидкости температурного регулятора последовательно соединены трубками, по которым протекает охлаждающая жидкость. Многослойная полость для размещения жидкости снабжена крышкой. При использовании полость для адсорбции материала льдом предполагается наполнять водным раствором материала, подавляющего рост льда, и полость бани в среднем слое предполагается заполнять средой для бани, имеющей заданную температуру, например, это может быть водяная баня, ледяная баня или масляная баня. После достижения заданной температуры охлаждающей жидкости, охлаждающая жидкость вытекает из температурного регулятора и подается в полую структуру стержня регулирования температуры, чтобы обеспечить регулирование температуры стержня регулирования температуры, затем выходит из выходного отверстия для жидкости стержня регулирования температуры и поступает в полость для размещения охлаждающей жидкости в наружном слое, обеспечивая заданный уровень температуры для среды, используемой в бане. Затем охлаждающая жидкость протекает через выходное отверстие для жидкости резервуара для размещения охлаждающей жидкости и концевое отверстие для возврата охлаждающей жидкости температурного регулятора и поступает в температурный регулятор для циркуляции.
[Пример 9]
а-ПВС: молекулярная масса, равная примерно 13-23 кДа, диадная синдиотактичность r, равная примерно 55% (Sigma-Aldrich);
i-ПВС: молекулярная масса, равная примерно 14-26 кДа, изотактичность m, равная примерно 84%.
(1) Измерение показателей распределения двух типов ПВС вдоль межфазной границы «лед-вода»
Количества двух типов ПВС, адсорбированных на поверхности льда, определяли путем проведения эксперимента по адсорбции материалов льдом. Устройство для проведения эксперимента показана на ФИГ. 21.
a. Образцы а-ПВС и i-ПВС маркировали флуоресцентной меткой FITC Изомер I.
b. Меченные FITC водные растворы (по 40 мл) двух типов ПВС с различными концентрациями разливали в лабораторные стаканы, которые затем помещали в рециркуляционную охлаждающую баню, и температуру растворов и стержня регулирования температуры доводили до -0,1°С.
c. Стержень регулирования температуры перед погружением в предварительно охлажденные меченные FITC водные растворы ПВС сначала погружали в жидкий азот на 1 минуту для предварительного охлаждения. Затем стержень регулирования температуры быстро опускали в предварительно охлажденные меченные FITC водные растворы ПВС, так чтобы инициировать образование предельно тонкого слоя льда на поверхности стержня регулирования температуры, с тем чтобы инициировать дальнейшее нарастание льда.
d. Меченные FITC водные растворы ПВС непрерывно перемешивали магнитной мешалкой при температуре переохлаждения -0,1°С в течение 1,0 часа, чтобы обеспечить равномерную и постепенную адсорбцию ПВС на поверхности льда. Степень переохлаждения и время адсорбции поддерживали неизменными на протяжении всего адсорбционного эксперимента, так чтобы площадь поверхности образующегося льда сохранялась практически неизменной в пределах допустимой погрешности.
e. Сформировавшийся блок льда извлекали из раствора, и поверхность льда споласкивали очищенной водой для удаления с его поверхности раствора. Затем блок льда размораживали.
f. Количество ПВС, адсорбированного на поверхности льда, получали из отношения массы растворенного ПВС в ледяном блоке, и массы растворенного ПВС в исходном растворе. Концентрацию раствора ПВС определяли методом спектрофотометрии в ультрафиолетовой и видимой области, а объем раствора определяли пипеткой и мерным цилиндром.
В экспериментах по адсорбции льдом количества а-ПВС и i-ПВС, адсорбированные при каждой концентрации, показаны на ФИГ. 22. Можно видеть, что количество а-ПВС, адсорбированное на поверхности льда, увеличивается с 16,3% при концентрации 0,2 мг/мл до 28,7% при концентрации 1,0 мг/мл, а при концентрациях свыше 1,0 мг/мл количество а-ПВС, адсорбированное на поверхности льда, достигает насыщения на уровне приблизительно 36,5%. Количество i-ПВС, адсорбированное на поверхности льда, при концентрациях до 1,0 мг/мл составляет от 0% до 19,3% и меньше, чем количество а-ПВС, адсорбированное на поверхности льда, при тех же концентрациях. При низких концентрациях количества обоих типов ПВС, адсорбированных на поверхности льда, далеки от насыщения, и площадь поверхности льда, покрытая i-ПВС, меньше площади поверхности льда, покрытой а-ПВС.
Количество i-ПВС, адсорбированное на поверхности льда, превышает количество а-ПВС, адсорбированное на поверхности льда, когда концентрация i-ПВС равна 1,2 мг/мл и более. При этом количество i-ПВС, адсорбированное на поверхности льда, достигает насыщения при концентрации 2,0 мг/мл и составляет примерно 56,5%. Кроме того, установлено, что количество i-ПВС, требуемое для насыщения, гораздо больше количества а-ПВС, требуемого для насыщения, при адсорбции на поверхности льда одинакового размера. Таким образом, а-ПВС может покрывать поверхность льда более эффективно.
(2) Количественный анализ активности в подавлении перекристаллизации льда (ГОЛ)
Активность в подавлении перекристаллизации льда (ГОЛ) оценивали с применением способа «замораживания брызг», в котором два типа ПВС по отдельности растворяли и диспергировали в растворах буфера DPBS. Затем по 10-30 мкл полученного раствора капали на поверхность чистого кремниевого диска, предварительно охлажденного до -60°С с высоты не менее 1,0 м. Замороженные образцы раствора медленно нагревали до -6°С со скоростью 10°С в минуту на предметном столике с системой нагрева-охлаждения и «отжигали» при этой температуре в течение 30 минут. Размеры ледяных кристаллов наблюдали и регистрировали с помощью поляризационного микроскопа и высокоскоростной фотокамеры. Образцы на предметном столике с системой нагрева-охлаждения герметизировали, чтобы гарантировать сохранение их внутренней влажности на уровне примерно 50%. Процедуру повторяли не менее трех раз для каждого образца, а размеры ледяных кристаллов измеряли с помощью нано-измерителя Nano Measurer 1.2 с погрешностью результата, равной стандартному отклонению.
Результат показан на ФИГ. 23, из которого видно, что размеры частиц а-ПВС значительно меньше, чем у i-ПВС, при одних и тех же концентрациях. Это говорит о том, что способность подавлять рост ледяных кристаллов у а-ПВС гораздо выше, чем у i-ПВС.
Согласно результатам, полученным в Примере 9, i-ПВС обладает более слабым сродством к воде, чем а-ПВС. Следовательно, i-ПВС имеет тенденцию находиться в более агрегированном состоянии, как в водном растворе, так и на поверхности раздела фаз «лед-вода», тогда как а-ПВС может хорошо распределяться в водном растворе и на поверхности раздела «лед-вода». Количество i-ПВС, требуемое для достижения насыщения в процессе адсорбции на поверхности льда, гораздо больше, чем количество а-ПВС, требуемое для достижения насыщения при адсорбции на поверхности льда такого же размера. Следовательно, по сравнению с i-ПВС, а-ПВС является лучшим материалом, подавляющим рост льда, и лучше выполняет функцию по ингибированию роста ледяных кристаллов при более низких концентрациях.
С. Составление рецептуры криоконсервирующего раствора, его приготовление и варианты применения
[Пример 10] Приготовление криоконсервирующего раствора, содержащего ПВС в качестве материала, подавляющего рост льда
1. Приготовление криоконсервирующих растворов: криоконсервирующие растворы готовили согласно приведенным ниже рецептурам.
Криоконсервирующий раствор А содержит следующие компоненты на 100 мл:
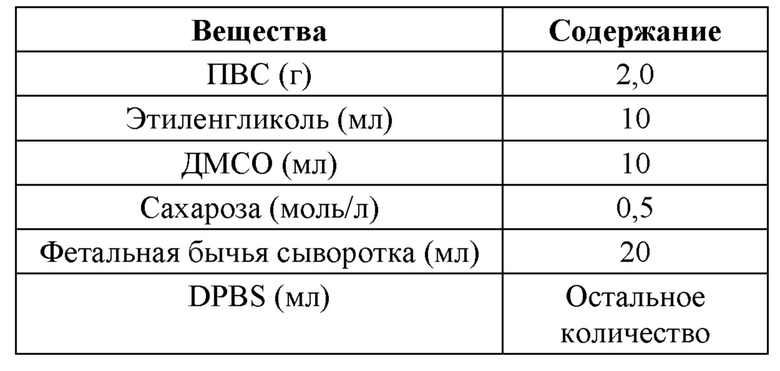
Процедура приготовления раствора: Навеску 2,0 г ПВС растворяли в 25 мл буфера DPBS на водяной бане при 80°С с магнитной мешалкой с нагревом. После полного растворения ПВС и охлаждения раствора до комнатной температуры доводили рН до 7,0, в результате чего получали Раствор 1. Навеску сахарозы 17 г (0,05 моль) (конечная концентрация сахарозы в криоконсервирующем растворе составляла 0,5 моль/л) растворяли с помощью ультразвука в 25 мл буфера DPBS, и после полного растворения сахарозы к полученному раствору добавляли 10 мл этиленгликоля и 10 мл ДМСО, в результате чего получали Раствор 2. После достижения комнатной температуры Раствор 1 и Раствор 2 смешивали до однородности, рН полученного раствора корректировали, и его объем доводили до 80 мл буфером. Сыворотку в объеме 20 мл хранили отдельно и добавляли в криоконсервирующий раствор при его применении.
Криоконсервирующий раствор В содержит следующие компоненты на 100 мл:

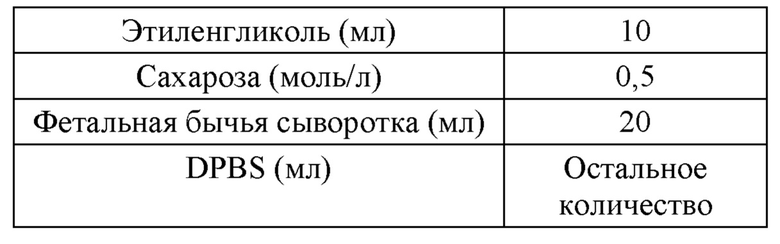
Процедура приготовления раствора: Навеску 2,0 г ПВС растворяли в 20 мл буфера DPBS на водяной бане при 80°С с магнитной мешалкой с нагревом, и рН полученного раствора доводили до 7,1, в результате чего получали Раствор 1. Навески 8,0 г L-Arg и 4,0 г L-Thr растворяли в 20 мл буфера DPBS, и рН полученного раствора доводили до 7,1, в результате чего получали Раствор 2. Навеску сахарозы 17 г (0,05 моль) (конечная концентрация сахарозы в криоконсервирующем растворе составляла 0,5 моль/л) растворяли с помощью ультразвука в 20 мл буфера DPBS, и после полного растворения сахарозы к полученному раствору добавляли 10 мл этиленгликоля, в результате чего получали Раствор 3. После достижения комнатной температуры Раствор 1, Раствор 2 и Раствор 3 смешивали до однородности, рН полученного раствора корректировали, и его объем доводили до 80 мл буфером. Сыворотку в объеме 20 мл хранили отдельно и добавляли в криоконсервирующий раствор при его применении.
Криоконсервирующий раствор С содержит следующие компоненты на 100 мл:
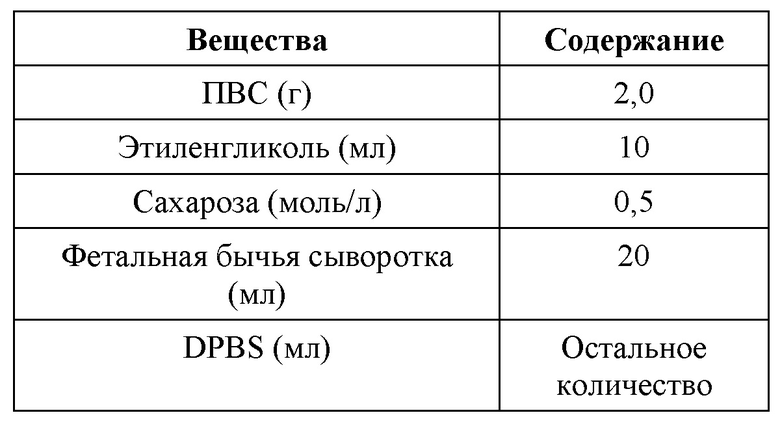
Процедура приготовления раствора: Навеску 2,0 г ПВС растворяли в 25 мл буфера DPBS на водяной бане при 80°С с магнитной мешалкой с нагревом, и рН полученного раствора доводили до 6,9, в результате чего получали Раствор 1. Навеску сахарозы 17 г (0,05 моль) (конечная концентрация сахарозы в криоконсервирующем растворе составляла 0,5 моль/л) растворяли с помощью ультразвука в 25 мл буфера DPBS, и после полного растворения сахарозы к полученному раствору добавляли 10 мл этиленгликоля, в результате чего получали Раствор 2. После достижения комнатной температуры Раствор 1 и Раствор 2 смешивали до однородности, рН полученного раствора корректировали, и его объем доводили до 80 мл буфером. Сыворотку в объеме 20 мл хранили отдельно и добавляли в криоконсервирующий раствор при его применении.
Криоконсервирующий раствор С1 содержит следующие компоненты на 100 мл:
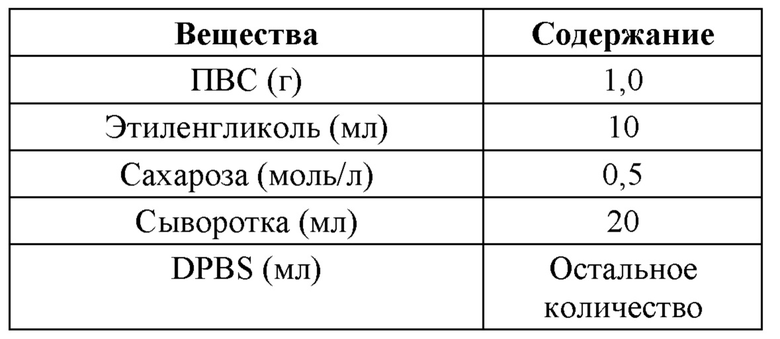
Процедура приготовления раствора такая же, как и для криоконсервирующего раствора С. Криоконсервирующий раствор D содержит следующие компоненты на 100 мл:

Процедура приготовления раствора: Навеску 2,0 г ПВС растворяли в 30 мл буфера DPBS на водяной бане при 80°С с магнитной мешалкой с нагревом, и рН полученного раствора доводили до 7,0, в результате чего получали Раствор 1. Навеску сахарозы 17 г (0,05 моль) (конечная концентрация сахарозы в криоконсервирующем растворе составляла 0,5 моль/л) растворяли с помощью ультразвука в 25 мл буфера DPBS, и после полного растворения сахарозы к полученному раствору добавляли 10 мл этиленгликоля, в результате чего получали Раствор 2. После достижения комнатной температуры Раствор 1 и Раствор 2 смешивали до однородности, рН полученного раствора корректировали, и его объем доводили до 100 мл буфером для дальнейшего применения.
Криоконсервирующий раствор Е содержит следующие компоненты на 100 мл:
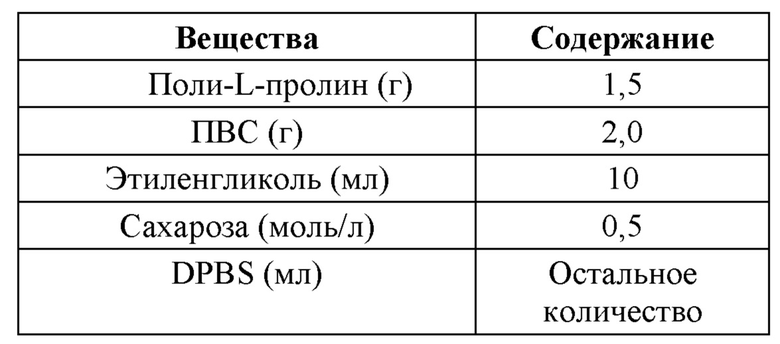
Процедура приготовления раствора: Навеску 2,0 г ПВС растворяли в 25 мл буфера DPBS на водяной бане при 80°С с магнитной мешалкой с нагревом, и рН полученного раствора доводили до 7,0, в результате чего получали Раствор 1. Навеску 1,5 г поли-L-пролина (со степенью полимеризации, равной 15) растворяли с помощью ультразвука в дополнительных 20 мл буфера DPBS, и рН полученного раствора доводили до 7,0, в результате чего получали Раствор 2. Навеску сахарозы 17 г (0,05 моль) (конечная концентрация сахарозы в криоконсервирующем растворе составляла 0,5 моль/л) растворяли с помощью ультразвука в 25 мл буфера DPBS, и после полного растворения сахарозы к полученному раствору добавляли 10 мл этиленгликоля, в результате чего получали Раствор 3. После достижения комнатной температуры Раствор 1, Раствор 2 и Раствор 3 смешивали до однородности, рН полученного раствора корректировали, и его объем доводили до 100 мл буфером для дальнейшего применения.
Криоконсервирующий раствор F содержит следующие компоненты на 100 мл:
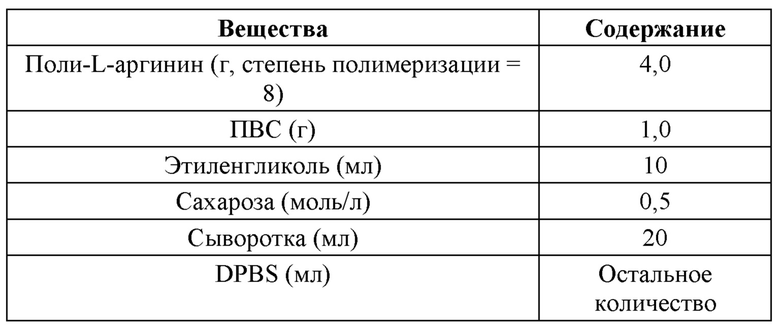
Процедура приготовления такая же, как и для криоконсервирующего раствора Е, а сыворотку добавляют в криоконсервирующий раствор при его применении.
2. Приготовление замораживающих уравновешивающих растворов: замораживающие уравновешивающие растворы готовили согласно приведенным ниже рецептурам.
Замораживающий уравновешивающий раствор а: 7,5 мл этиленгликоля и 7,5 мл ДМСО добавляли к 65 мл буфера DPBS и перемешивали до однородности, а 20 мл сыворотки добавляли в замораживающий уравновешивающий раствор при его применении.
Замораживающий уравновешивающий раствор b: 7,5 мл этиленгликоля растворяли в 72,5 мл буфера DPBS и перемешивали до однородности, а 20 мл сыворотки добавляли в замораживающий уравновешивающий раствор при его применении.
Замораживающий уравновешивающий раствор с: 2,0 г ПВС растворяли в 50 мл буфера DPBS на водяной бане при 80°С с магнитной мешалкой с нагревом, и после полного растворения ПВС рН полученного раствора доводили до 7,0. Затем к раствору добавляли 7,5 мл этиленгликоля, перемешивали до однородности, корректировали рН, а объем доводили до 100 мл для дальнейшего применения.
Сравнительный пример:
Замораживающий уравновешивающий раствор а содержит, в расчете на 1 мл, 7,5% (об/об) ДМСО, 7,5% (об/об) этиленгликоля, 20% (об/об) фетальной бычьей сыворотки и остальной объем - буфер DPBS;
Криоконсервирующий раствор №1 содержит, в расчете на 1 мл, 15% (об/об) ДМСО, 15% (об/об) этиленгликоля, 20% (об/об) фетальной бычьей сыворотки, 0,5М сахарозы и остальной объем - буфер DPBS;
Замораживающий уравновешивающий раствор №2 содержит, в расчете на 1 мл, 7,5% (об/об) этиленгликоля, 20% (об/об) фетальной бычьей сыворотки и остальной объем - буфер DPBS;
Криоконсервирующий раствор №2 содержит, в расчете на 1 мл, 10% (об/об) этиленгликоля, 20% (об/об) фетальной бычьей сыворотки, 0,5М сахарозы и остальной объем - буфер DPBS;
Криоконсервирующий раствор №3 содержит, в расчете на 1 мл, 10% (об/об) ДМСО, 15% (об/об) фетальной бычьей сыворотки и остальной объем - среда а-МЕМ (USA, Invitrogen, С12571500 ВТ).
Размораживающие растворы, использовавшиеся в Примере 10 и сравнительных примерах, имели три следующих рецептуры:
Размораживающий раствор №1 содержит размораживающий раствор I (содержащий сахарозу в концентрации 1,0 моль/л, 20% сыворотки и остальной объем - буфер DPBS), размораживающий раствор II (содержащий сахарозу в концентрации 0,5 моль/л, 20% сыворотки и остальной объем - буфер DPBS), размораживающий раствор III (содержащий сахарозу в концентрации 0,25 моль/л, 20% сыворотки и остальной объем - буфер DPBS) и размораживающий раствор IV (содержащий 20% сыворотки и остальной объем - буфер DPBS).
Размораживающий раствор №2 содержит размораживающий раствор I (содержащий сахарозу в концентрации 1,0 моль/л, ПВС в концентрации 20 мг/мл и остальной объем - буфер DPBS), размораживающий раствор II (содержащий сахарозу в концентрации 0,5 моль/л, ПВС в концентрации 20 мг/мл и остальной объем - буфер DPBS), размораживающий раствор III (содержащий сахарозу в концентрации 0,25 моль/л, ПВС в концентрации 20 мг/мл и остальной объем - буфер DPBS) и размораживающий раствор IV (содержащий ПВС в концентрации 20 мг/мл и остальной объем - буфер DPBS).
Размораживающий раствор №3 содержит размораживающий раствор I (содержащий сахарозу в концентрации 1,0 моль/л, ПВС в концентрации 20 мг/мл, полипролин в концентрации 10 мг/мл и остальной объем - буфер DPBS), размораживающий раствор II (содержащий сахарозу в концентрации 0,5 моль/л, ПВС в концентрации 20 мг/мл, полипролин в концентрации 5,0 мг/мл и остальной объем - буфер DPBS), размораживающий раствор III (содержащий сахарозу в концентрации 0,25 моль/л, ПВС в концентрации 20 мг/мл, полипролин в концентрации 2,5 мг/мл и остальной объем - буфер DPBS) и размораживающий раствор IV (содержащий ПВС в концентрации 20 мг/мл и остальной объем - буфер DPBS).
[Пример применения 1] Ооциты и эмбрионы подвергали криоконсервации с применением замораживающих уравновешивающих растворов и криоконсервирующих растворов из представленных выше примеров и сравнительных примеров согласно схемам, приведенным в Таблице 1 и Таблице 2, соответственно. Показатели выживаемости в различных вариантах воплощения настоящего изобретения определяли как среднее из показателей выживаемости в 3-12 повторных экспериментах.
1. Криоконсервация ооцитов
Мышиные ооциты сначала уравновешивали в замораживающем уравновешивающем растворе в течение 5 минут, затем помещали в приготовленный криоконсервирующий раствор на 1 минуту. Уравновешенные ооциты в криоконсервирующем растворе помещали в криоконсервационную соломинку, затем быстро опускали в жидкий азот (-196°С) и постоянно сохраняли их в нем после герметизации несущего стержня. При необходимости размораживания замороженные ооциты уравновешивали в размораживающем растворе I при 37°С в течение 5 минут, и затем последовательно уравновешивали в размораживающих растворах II-IV по 3 минуты в каждом. Затем размороженные ооциты культивировали в течение 2 часов, подсчитывали количество выживших клеток и рассчитывали показатели выживаемости (см. Таблицу 1).
2. Криоконсервация эмбрионов
Мышиные эмбрионы сначала уравновешивали в замораживающем уравновешивающем растворе в течение 5 минут, затем помещали в криоконсервирующий раствор, приготовленный в соответствии с рецептурами, указанными в приведенных выше примерах и сравнительных примерах, на 50 секунд. Уравновешенные эмбрионы в криоконсервирующем растворе вводили в криоконсервационную соломинку, затем быстро опускали в жидкий азот (-196°С) и постоянно сохраняли в нем после герметизации несущего стержня. При необходимости размораживания замороженные эмбрионы уравновешивали в размораживающем растворе I при 37°С в течение 3 минут, и затем последовательно уравновешивали в размораживающих растворах II-IV по 3 минуты в каждом. Затем размороженные эмбрионы культивировали в течение 2 часов, подсчитывали количество выживших эмбрионов и рассчитывали показатели выживаемости (см. Таблицу 2).
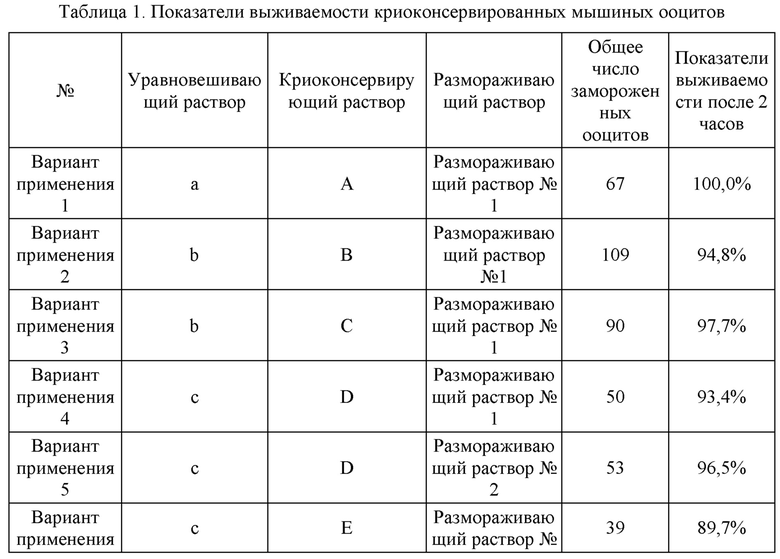
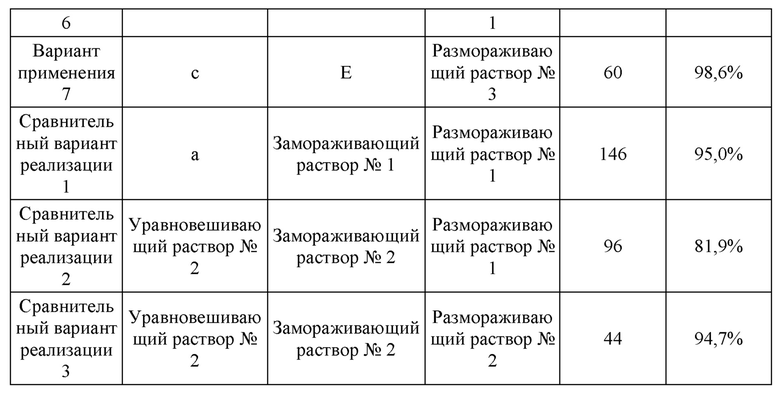
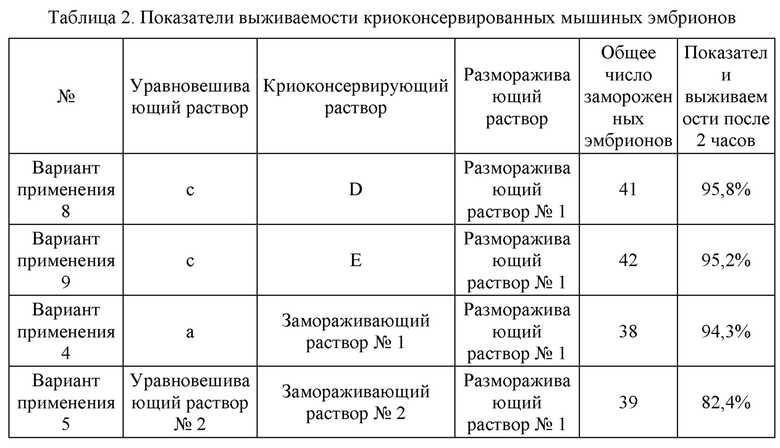
Приведенные выше данные говорят о том, что при применении предложенного криоконсервирующего раствора показатель выживаемости может быть не меньше 90% и даже составлять 100%, и скорость размораживания при криоконсервации может достигать или быть значительно выше, чем у промышленного серийного криоконсервирующего раствора, содержащего 15% ДМСО, который сейчас обычно применяется в клинической практике. Как можно видеть из сравнения варианта применения 1 (с включением 10% ДМСО), Сравнительного варианта реализации 2 (с включением 7,5% ДМСО) и Сравнительного варианта реализации 1 (с использованием промышленного серийного раствора для криоконсервации ооцитов, содержащего 15% ДМСО), показатель выживаемости ооцитов значительно повышается по мере добавления ПВС. Варианты применения 2-3 также показывают, что криоконсервирующий раствор может демонстрировать более высокие показатели выживаемости ооцитов или эмбрионов при добавлении небольших количеств ДМСО или вообще без добавления ДМСО, что позволяет решить одну из проблем промышленного криоконсервирующего раствора, обычно применяемого в клинической практике, связанную с высокой концентрацией ДМСО, приводящей к значительным повреждениям клеток. Кроме того, варианты применения 5 и 7-9 показывают, что повышенных показателей выживаемости ооцитов или эмбрионов можно добиваться и без добавления ДМСО и сыворотки в замораживающие растворы, уравновешивающие растворы и размораживающие растворы. Криоконсервирующий раствор, не содержащий ДМСО или не содержащий сыворотки, решает проблему короткого срока годности, опасности введения паразитарных биологических загрязнителей и т.п., связанной с сывороткой, содержащейся в промышленных серийных криоконсервирующих растворах, обычно применяемых в клинической практике в настоящее время.
[Пример применения 2] Криоконсервация человеческих пуповинных мезенхимальных стволовых клеток
Человеческие пуповинные мезенхимальные стволовые клетки подвергали криоконсервации с применением криоконсервирующих растворов, предложенных в приведенных выше примерах и сравнительных примерах, и согласно схеме, представленной в Таблице 3.
Криоконсервацию человеческих пуповинных мезенхимальных стволовых клеток проводили микрокапельным способом по следующей процедуре: расщепление человеческих пуповинных мезенхимальных стволовых клеток в чашке Петри с использованием 25% раствора панкреатина в течение 2 минут, помещение человеческих пуповинных мезенхимальных стволовых клеток после расщепления в культуральный раствор (10% FBS+культуральная среда а-МЕМ) того же объема, мягкое пипетирование до полного выпадения стволовых клеток, перенос клеток в центрифужную пробирку объемом 1,5 мл для центрифугирования в течение 5 минут при 1000 об/мин, отбрасывание надосадочной жидкости (отделение клеток от культуральной среды), добавление 10 мкл замораживающего раствора в нижнюю часть центрифужной пробирки, мягкое пипетирование для диспергирования кластеров стволовых клетко, помещение 10 мкл замораживающего раствора со стволовыми клетками на предметное стекло для замораживания и криоконсервация раствора в жидком азоте (-196°С). При необходимости размораживания соломинку с клетками и замораживающим раствором помещают непосредственно в культуральную среду при 37°С для оттаивания. После размораживания клетки подкрашивают трипановым синим для определения показателей выживаемости, и количество клеток подсчитывают с использованием прибора JIMBIO-FIL. Показатель выживаемости представляет собой отношение числа живых клеток к общему числу имеющихся клеток (см. Таблицу 3).
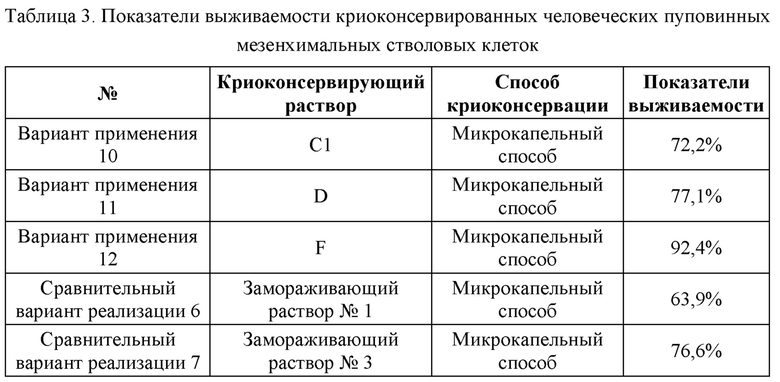
Когда раскрытый в данном документе криоконсервирующий раствор применяют для криоконсервации человеческих пуповинных мезенхимальных стволовых клеток, показатели выживаемости стволовых клеток могут достигать значений 92,4% и 72,2% (в вариантах применения 12 и 10, соответственно) даже без добавлений ДМСО. Кроме того, показатель выживаемости может составлять 77,1% даже без добавлений ДМСО и сыворотки, достигая уровня выживаемости уже известного замораживающего реагента. Это означает, что предлагаемый замораживающий реагент может при замораживании стволовых клеток обладать такой же эффективностью, что и традиционный замораживающий раствор, а скорость размораживания предложенного реагента при криоконсервации может достигать или даже быть значительно выше, чем у обычно применяемого сегодня криоконсервирующего раствора, содержащего 10% ДМСО (см. Сравнительный вариант реализации 7). Криоконсервирующий эффект при применении замораживающего раствора на основе ПВС значительно превосходит криоконсервирующий эффект, наблюдающийся без использования ПВС, как это можно видеть из Сравнительного варианта реализации 6.
[Пример применения 3] Криоконсервация овариальных органов и овариальных тканей Овариальные органы новорожденных мышей возрастом до 3 дней и срезы овариальных тканей половозрелых мышей подвергали криоконсервации посредством замораживающих уравновешивающих растворов и криоконсервирующих растворов, предложенных в приведенных выше примерах и сравнительных примерах, и согласно схемам, представленным в Таблице 4 и Таблице 5.
Цельные овариальные органы или срезы овариальных тканей сначала уравновешивали в уравновешивающем растворе при комнатной температуре в течение 25 минут, после чего помещали в приготовленный криоконсервирующий раствор на 15 минут. Затем цельные овариальные органы или срезы овариальных тканей помещали в криоконсервационную соломинку и погружали в жидкий азот для консервации. После размораживания цельные овариальные органы или срезы овариальных тканей помещали в культуральный раствор (10% FBS+а-МЕМ) в инкубаторе при 37°С в присутствии 5% СО2 на 2 часа для дальнейшего размораживания. Затем цельные овариальные органы или срезы овариальных тканей фиксировали в 4%-ном растворе параформальдегида, заливали в парафин и подвергали окрашиванию НЕ (гематоксилином и эозином), после чего анализировали их морфологию. Результаты показаны на ФИГ. 24-33, где ФИГ. 24 представляет собой снимок среза свежего, незамороженного овариального органа, а ФИГ. 29 представляет собой снимок среза свежей, незамороженной овариальной ткани.
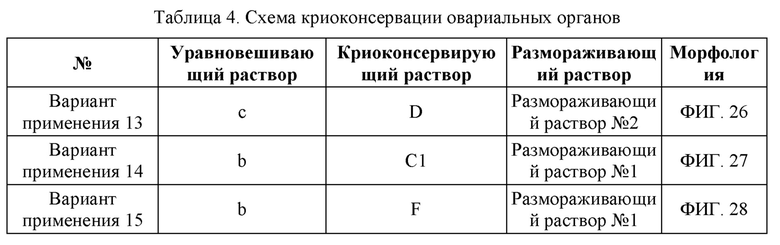

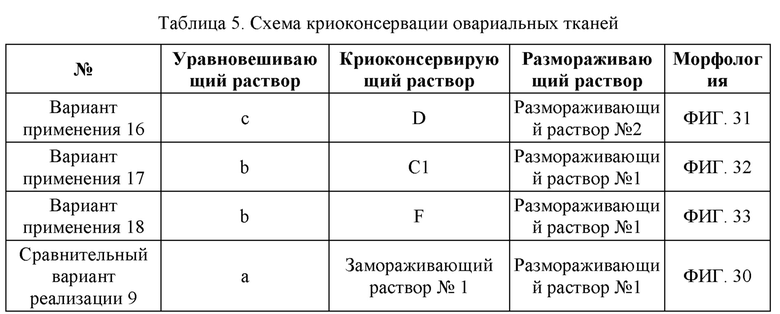
Как можно видеть из ФИГ. 24-28, по отношению к Сравнительному варианту реализации 8, где не применяли поливиниловый спирт, и свежим, незамороженным овариальным органам, схемы, предложенные в вариантах применения 13-15, отличаются следующим: исходная структура фолликул остается относительно нетронутой, интерстициальная структура остается относительно нетронутой, цитоплазма клеток относительно однородна и слегка окрашена в относительно небольшом количестве, а сокращения ядер и глубокое окрашивание относительно умеренны, кровеносные сосуды имеют нетронутую структуру стенок и минимальное сужение просвета, цитоплазма клеток эндотелия относительно однородна и слегка окрашена в относительно небольшом количестве, а сокращения ядер и глубокое окрашивание относительно умеренны. Как можно видеть, варианты применения 13-15 показывают лучшие эффекты при криоконсервации овариальных органов.
Как можно видеть из ФИГ. 29-33, по отношению к Сравнительному варианту реализации 9 и свежим, незамороженным овариальным тканям, схемы, предложенные в вариантах применения 16-18, отличаются следующим: структура антральных фолликул остается относительно нетронутой, интерстициальная структура остается относительно нетронутой, цитоплазма клеток относительно однородна и слегка окрашена в относительно небольшом количестве, а сокращения ядер и глубокое окрашивание относительно умеренны. Можно видеть, что раскрытый в данном описании криоконсервирующий раствор показывает лучший эффект при криоконсервации овариальных тканей, чем криоконсервирующий раствор, традиционно принятый из уровня техники.
Можно видеть, что раскрытый в данном описании криоконсервирующий раствор, приготовленный с применением биомиметического материала, подавляющего рост льда, на основе ПВС, в качестве основного компонента, оказывает хороший ингибирующий эффект на рост кристаллов льда, может быть приготовлен с уменьшенным содержанием ДМСО в системе консервации и даже без содержания ДМСО, поддерживает хорошую биологическую совместимость и может одновременно применяться для криоконсервации ооцитов, эмбрионов, стволовых клеток, репродуктивных органов и тканей, позволяя достигать высоких показателей выживаемости клеток и хорошей биологической активности.
[Пример 11] Приготовление криоконсервирующего раствора, содержащего аминокислоты в качестве материала, подавляющего рост льда
Криоконсервирующий раствор G содержит следующие компоненты в расчете на 100 мл раствора:
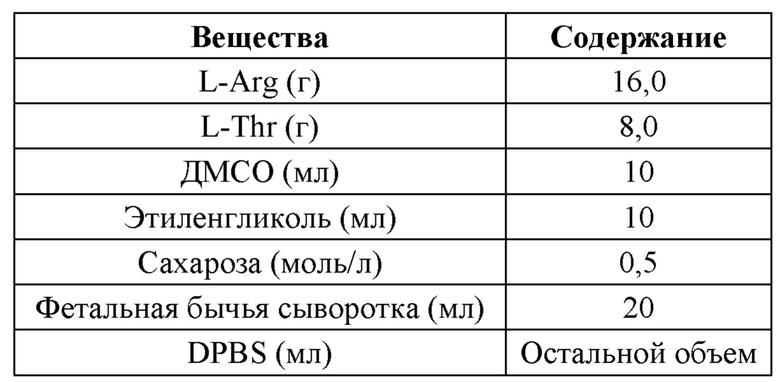
Процедура приготовления раствора (общий объем: 100 мл): Навески 16 г L-Arg и 8 г L-Thr растворяли в 25 мл буфера DPBS, и рН полученного раствора доводили до 6,9, в результате чего получали Раствор 1. Навеску сахарозы 17 г (0,05 моль) (конечная концентрация сахарозы в итоговом криоконсервирующем растворе составляла 0,5 моль/л) растворяли с помощью ультразвука в 25 мл буфера DPBS, и после полного растворения сахарозы к полученному раствору последовательно добавляли 10 мл этиленгликоля и 10 мл ДМСО, в результате чего получали Раствор 2. После достижения комнатной температуры Раствор 1 и Раствор 2 смешивали до однородности, рН полученного раствора корректировали до уровня 6,9, и его объем доводили до 80 мл буфером DPBS. Фетальную бычью сыворотку в объеме 20 мл хранили отдельно и добавляли в криоконсервирующий раствор перед его применением.
Криоконсервирующий раствор Н содержит следующие компоненты в расчете на 100 мл раствора:

Процедура приготовления раствора: Навеску 1,5 г поли-L-пролина (со степенью полимеризации равной 15) растворяли с помощью ультразвука в 25 мл буфера DPBS, и рН полученного раствора доводили до 6,8, в результате чего получали Раствор 1. Навеску сахарозы 17 г (0,05 моль) растворяли с помощью ультразвука в 25 мл буфера DPBS, и после полного растворения сахарозы к полученному раствору последовательно добавляли 10 мл этиленгликоля и 10 мл ДМСО, в результате чего получали Раствор 2. После достижения комнатной температуры Раствор 1 и Раствор 2 смешивали до однородности, рН полученного раствора корректировали до уровня 7,0, и его объем доводили до 80 мл буфером DPBS. Сыворотку в объеме 20 мл хранили отдельно и добавляли в криоконсервирующий раствор перед его применением.
Криоконсервирующий раствор I содержит следующие компоненты в расчете на 100 мл раствора:

Процедура приготовления раствора (в расчете на 100 мл раствора): Навеску 1,5 г поли-L-аргинина (со степенью полимеризации равной 8) растворяли с помощью ультразвука в 25 мл буфера DPBS, и рН полученного раствора доводили до 7,0, в результате чего получали Раствор 1. Навеску сахарозы 17 г (0,05 моль) растворяли с помощью ультразвука в 20 мл буфера DPBS, и после полного растворения сахарозы к полученному раствору последовательно добавляли 10 мл этиленгликоля и 10 мл ДМСО, в результате чего получали Раствор 2. После достижения комнатной температуры Раствор 1 и Раствор 2 смешивали до однородности, рН полученного раствора корректировали до уровня 7,0, и его объем доводили до 80 мл буфером DPBS. Сыворотку в объеме 20 мл хранили отдельно и добавляли в криоконсервирующий раствор перед его применением.
Криоконсервирующий раствор J содержит следующие компоненты в расчете на 100 мл раствора:

Процедура приготовления такая же, как и для криоконсервирующего раствора I.
Криоконсервирующий раствор K содержит следующие компоненты в расчете на 100 мл раствора:


Процедура приготовления такая же, как и для криоконсервирующего раствора I.
Криоконсервирующий раствор L содержит следующие компоненты в расчете на 100 мл раствора:
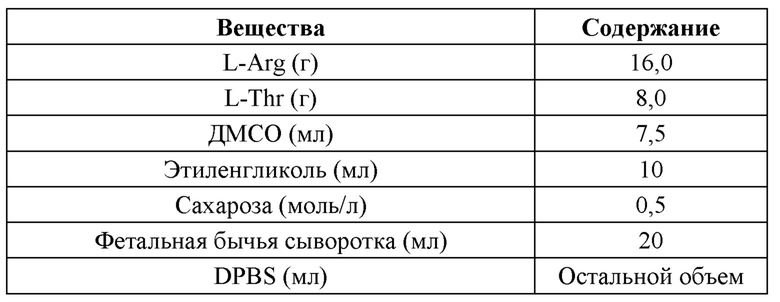
Процедура приготовления такая же, как и для криоконсервирующего раствора G.
Приготовление замораживающих уравновешивающих растворов: замораживающие уравновешивающие растворы готовили согласно приведенным ниже рецептурам.
Замораживающий уравновешивающий раствор а: 7,5 мл этиленгликоля и 7,5 мл ДМСО добавляли к 65 мл буфера DPBS и перемешивали до однородности, а 20 мл сыворотки добавляли в замораживающий уравновешивающий раствор перед его применением.
Замораживающий уравновешивающий раствор b: 7,5 мл этиленгликоля растворяли в 72,5 мл буфера DPBS и перемешивали до однородности, а 20 мл сыворотки добавляли в замораживающий уравновешивающий раствор перед его применением.
Сравнительный пример 2:
Замораживающий уравновешивающий раствор а содержит, в расчете на 1 мл, 7,5% (об/об) ДМСО, 7,5% (об/об) этиленгликоля, 20% (об/об) фетальной бычьей сыворотки и остальной объем - буфер DPBS;
Криоконсервирующий раствор №1 содержит, в расчете на 1 мл, 15% (об/об) ДМСО, 15% (об/об) этиленгликоля, 20% (об/об) фетальной бычьей сыворотки, 0,5М сахарозы и остальной объем - буфер DPBS.
Криоконсервирующий раствор №3 содержит, в расчете на 1 мл, 10% (об/об) ДМСО, 15% (об/об) фетальной бычьей сыворотки и остальной объем - культуральная среда а-МЕМ (USA, Invitrogen, С12571500 ВТ).
Размораживающие растворы, использовавшиеся в Примере 11 и Сравнительном примере 2, имели следующую рецептуру:
Размораживающий раствор №1 содержит размораживающий раствор I (содержащий сахарозу в концентрации 1,0 моль/л, 20% сыворотки и остальной объем - буфер DPBS), размораживающий раствор II (содержащий сахарозу в концентрации 0,5 моль/л, 20% сыворотки и остальной объем - буфер DPBS), размораживающий раствор III (содержащий сахарозу в концентрации 0,25 моль/л, 20% сыворотки и остальной объем - буфер DPBS) и размораживающий раствор IV (содержащий 20% сыворотки и остальной объем - буфер DPBS). [Пример применения 4] Криоконсервация ооцитов и эмбрионов
Ооциты и эмбрионы подвергали криоконсервации с применением замораживающих уравновешивающих растворов и криоконсервирующих растворов, предложенных в Примере 11 и Сравнительном примере 2, согласно схемам, представленным в Таблице 6 и Таблице 7. Способы замораживания и размораживания были те же, что и в примере применения 1.
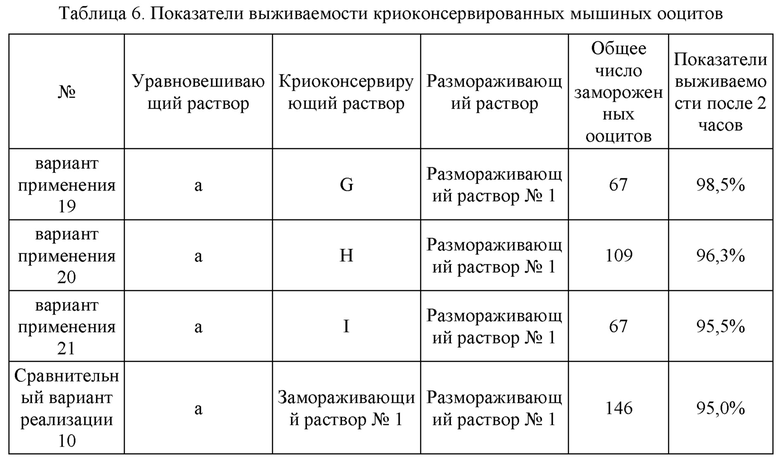
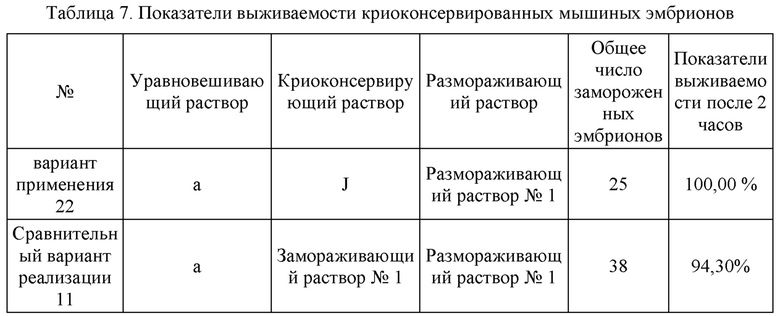
Как можно видеть из данных, представленных в Таблицах 6 и 7, при применении раскрытого в данном описании криоконсервирующего раствора для криоконсервации ооцитов и эмбрионов, после снижения содержания ДМСО и EG (этиленгликоля) показатель выживаемости ооцитов может достигать не менее 95%, а показатель выживаемости эмбрионов может достигать 100%. Скорость размораживания после криоконсервации для раскрытого в данном описании криоконсервирующего раствора может достигать или быть значительно выше, чем у промышленного серийного криоконсервирующего раствора, содержащего 15% ДМСО, который сейчас широко применяется в клинической практике (см. Сравнительные варианты реализации 10-11). Криоконсервирующий эффект при добавлении биомиметического аминокислотного материала, подавляющего рост льда, значительно превосходит криоконсервирующий эффект, наблюдающийся без добавления биомиметического аминокислотного материала, подавляющего рост льда.
[Пример применения 5] Криоконсервация человеческих пуповинных мезенхимальных стволовых клеток
Человеческие пуповинные мезенхимальные стволовые клетки подвергали криоконсервации с применением криоконсервирующих растворов, предложенных в Примере 11 и Сравнительном примере 2, согласно схеме, представленной в Таблице 8. Способы замораживания и размораживания были те же, что и в примере применения 2.
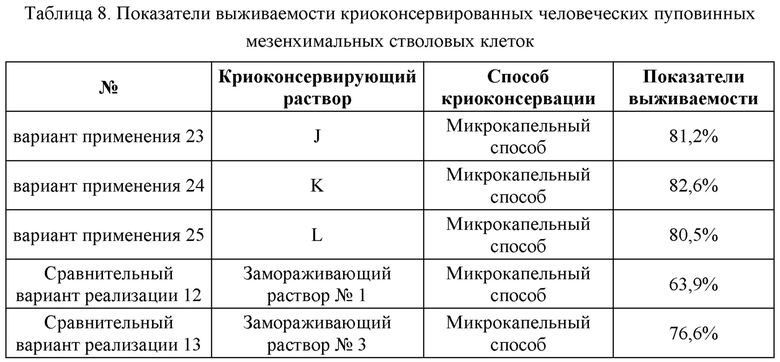
Когда раскрытый в данном документе криоконсервирующий раствор применяют для криоконсервации человеческих пуповинных мезенхимальных стволовых клеток, показатели выживаемости стволовых клеток могут достигать значений не менее 80% при добавлении лишь небольших количеств ДМСО (7,5%) или даже без добавления ДМСО (например, как в вариантах применения 23-25). Это означает, что предлагаемый замораживающий реагент при замораживании стволовых клеток может не только обладать такой же эффективностью, что и традиционный замораживающий раствор, но и показывать скорость размораживания при криоконсервации значительно более высокую, чем у обычно применяемого сегодня криоконсервирующего раствора, содержащего 10% ДМСО (см. Сравнительный вариант реализации 13). Криоконсервирующий эффект при добавлении биомиметического аминокислотного материала, подавляющего рост льда, значительно превосходит криоконсервирующий эффект, наблюдающийся без добавления биомиметического аминокислотного материала, подавляющего рост льда (см. Сравнительные варианты реализации 14 и 15).
[Пример применения 6] Криоконсервация овариальных органов и овариальных тканей
Овариальные органы новорожденных мышей возрастом до 3 дней и срезы овариальных тканей половозрелых мышей подвергали криоконсервации с применением замораживающих уравновешивающих растворов и криоконсервирующих растворов, предложенных в Примере 11 и Сравнительном примере 2, согласно схемам, представленным в Таблице 9 и Таблице 10. Способы замораживания и размораживания овариальных органов и овариальных тканей половозрелых мышей представлены в примере применения 3.
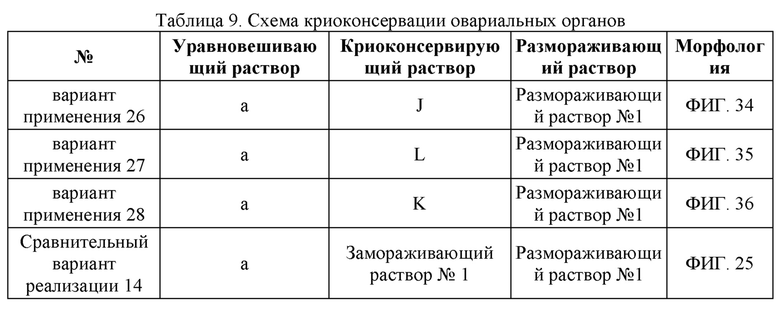
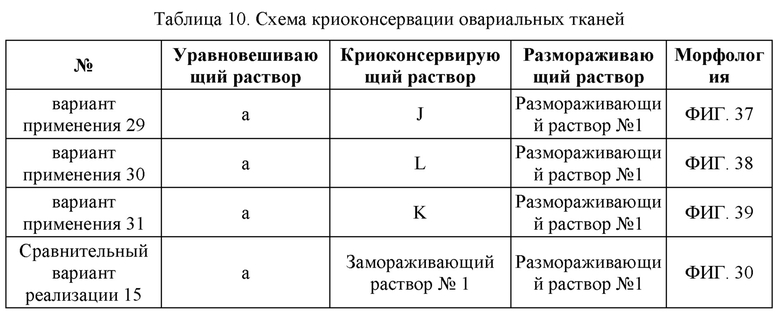
[Пример 11] Приготовление криоконсервирующего раствора, содержащего пептидное соединение в качестве материала, подавляющего рост льда Криоконсервирующий раствор М содержит следующие компоненты в расчете на 100 мл раствора:
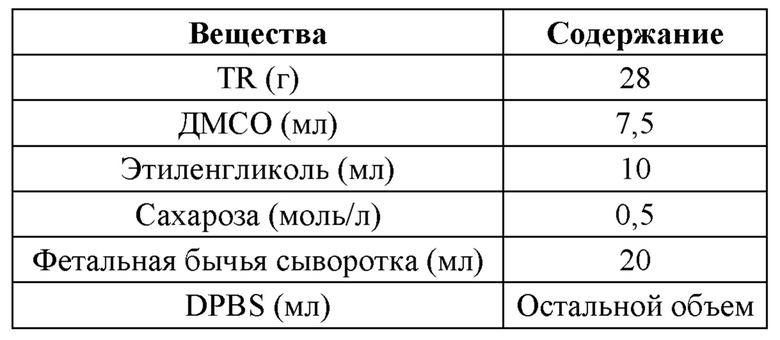
Процедура приготовления раствора (в расчете на 100 мл раствора): Навеску 28 г TR растворяли с помощью ультразвука в 25 мл буфера DPBS, и рН полученного раствора доводили до 7,0, в результате чего получали Раствор 1. Навеску сахарозы 0,05 моль растворяли с помощью ультразвука в 25 мл буфера DPBS, и после полного растворения сахарозы к полученному раствору последовательно добавляли 10 мл этиленгликоля и 7,5 мл ДМСО, в результате чего получали Раствор 2. После достижения комнатной температуры Раствор 1 и Раствор 2 смешивали до однородности, корректировали рН полученного раствора, и его объем доводили до 80 мл буфером DPBS. Сыворотку в объеме 20 мл добавляли в криоконсервирующий раствор перед его применением.
Криоконсервирующий раствор N содержит следующие компоненты в расчете на 100 мл раствора:
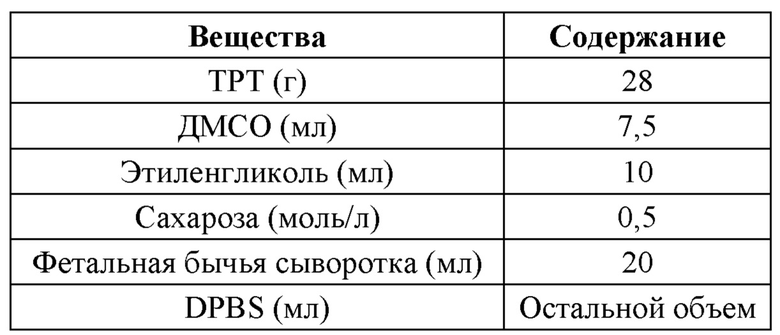
Процедура приготовления раствора (в расчете на 100 мл раствора): Навеску 28 г ТРТ растворяли с помощью ультразвука в 25 мл буфера DPBS, и рН полученного раствора доводили до 7,0, в результате чего получали Раствор 1. Навеску сахарозы 0,05 моль растворяли с помощью ультразвука в 25 мл буфера DPBS, и после полного растворения сахарозы к полученному раствору последовательно добавляли 10 мл этиленгликоля и 7,5 мл ДМСО, в результате чего получали Раствор 2. После достижения комнатной температуры Раствор 1 и Раствор 2 смешивали до однородности, корректировали рН полученного раствора, и его объем доводили до 80 мл буфером DPBS. Сыворотку в объеме 20 мл добавляли в криоконсервирующий раствор перед его применением.
Криоконсервирующий раствор О содержит следующие компоненты в расчете на 100 мл раствора:
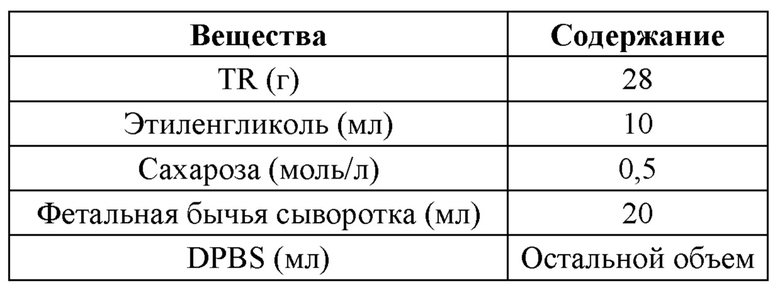
Процедура приготовления раствора (в расчете на 100 мл раствора): Навеску 28 г TR растворяли с помощью ультразвука в 25 мл буфера DPBS, и рН полученного раствора доводили до 7,0, в результате чего получали Раствор 1. Навеску сахарозы 0,05 моль растворяли с помощью ультразвука в 25 мл буфера DPBS, и после полного растворения сахарозы к полученному раствору последовательно добавляли 10 мл этиленгликоля, в результате чего получали Раствор 2. После достижения комнатной температуры Раствор 1 и Раствор 2 смешивали до однородности, корректировали рН полученного раствора, и его объем доводили до 80 мл буфером DPBS. Сыворотку в объеме 20 мл хранили добавляли в криоконсервирующий раствор перед его применением.
Приготовление замораживающих уравновешивающих растворов: замораживающие уравновешивающие растворы готовили согласно приведенным ниже рецептурам.
Замораживающий уравновешивающий раствор а: 7,5 мл этиленгликоля и 7,5 мл ДМСО добавляли к 65 мл буфера DPBS и перемешивали до однородности, а 20 мл сыворотки добавляли в замораживающий уравновешивающий раствор перед его применением.
Сравнительный пример 3:
Замораживающий уравновешивающий раствор а содержит, в расчете на 1 мл, 7,5% (об/об) ДМСО, 7,5% (об/об) этиленгликоля, 20% (об/об) фетальной бычьей сыворотки и остальной объем - буфер DPBS;
Криоконсервирующий раствор №1 содержит, в расчете на 1 мл, 15% (об/об) ДМСО, 15% (об/об) этиленгликоля, 20% (об/об) фетальной бычьей сыворотки, 0,5М сахарозы и остальной объем - буфер DPBS.
Криоконсервирующий раствор №3 содержит, в расчете на 1 мл, 10% (об/об) ДМСО, 15% (об/об) фетальной бычьей сыворотки и остальной объем - культуральная среда а-МЕМ (USA, Invitrogen, С12571500 ВТ).
Размораживающие растворы, применявшиеся в Примере 12 и Сравнительном примере 3, имели следующую рецептуру:
Размораживающий раствор №1 содержит размораживающий раствор I (содержащий сахарозу в концентрации 1,0 моль/л, 20% сыворотки и остальной объем - буфер DPBS), размораживающий раствор II (содержащий сахарозу в концентрации 0,5 моль/л, 20% сыворотки и остальной объем - буфер DPBS), размораживающий раствор III (содержащий сахарозу в концентрации 0,25 моль/л, 20% сыворотки и остальной объем - буфер DPBS) и размораживающий раствор IV (содержащий 20% сыворотки и остальной объем - буфер DPBS).
[Пример применения 7] Криоконсервация ооцитов и эмбрионов
Ооциты и эмбрионы подвергали криоконсервации с применением замораживающих уравновешивающих растворов и криоконсервирующих растворов, предложенных в Примере 13 и Сравнительном примере 3, согласно схемам, представленным в Таблице 11 и Таблице 12. Способы замораживания и размораживания были те же, что и в примере применения 1.
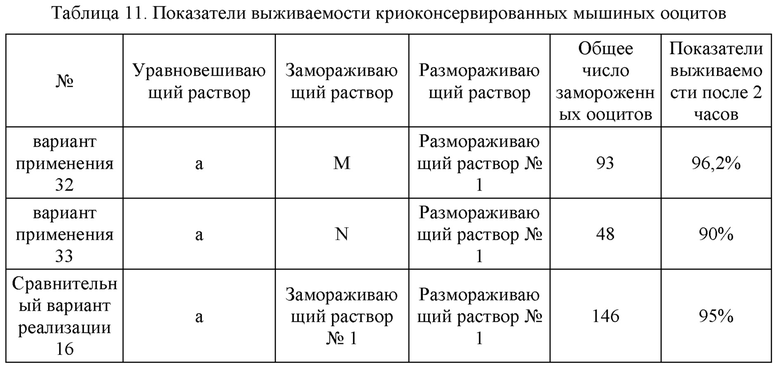
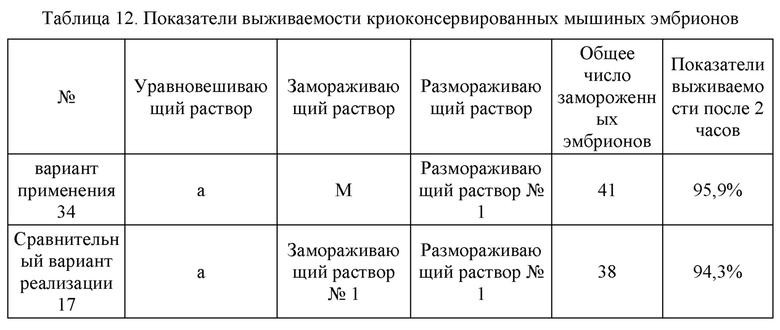
Как можно видеть из данных, представленных в Таблицах 11 и 12, раскрытые в данном описании полипептиды можно применять для криоконсервации ооцитов и эмбрионов, и при этом показатели выживаемости ооцитов и эмбрионов могут достигать уровней, характерных для промышленного серийного криоконсервирующего раствора (содержащего 15% ДМСО), путем добавления гораздо меньшего количества ДМСО (7,5%). Данные, полученные в вариантах применения 32 и 34, показывают, что полипептиды TR оказывают более выраженный криоконсервирующий эффект на ооциты и эмбрионы.
[Пример применения 8] Криоконсервация человеческих пуповинных мезенхимальных стволовых клеток
Человеческие пуповинные мезенхимальные стволовые клетки подвергали криоконсервации с применением криоконсервирующих растворов, предложенных в Примере 12 и Сравнительном примере 3, согласно схеме, представленной в Таблице 13. Способы замораживания и размораживания были те же, что и в примере применения 2.
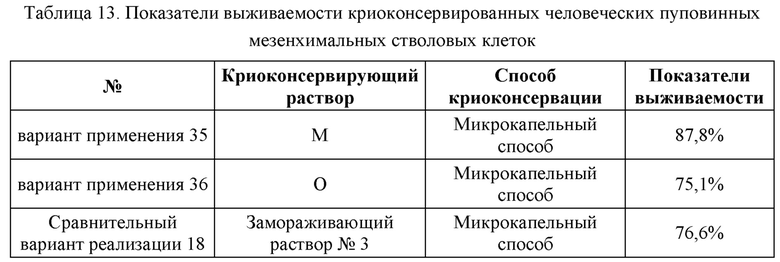
Как можно видеть из результатов, представленных в Таблице 13, раскрытый в данном документе криоконсервирующий раствор, не содержащий ДМСО или содержащий лишь небольшое количество ДМСО (7,5%), может иметь показатели выживаемости клеток, сравнимые с показателями, характерными для промышленного серийного криоконсервирующего раствора (содержащего 10% ДМСО), известного из уровня техники. Таким образом, значительно уменьшается количество ДМСО, т.е. снижается вероятность повреждения и токсического поражения клеток этим реагентом, а устойчивость к замораживанию-размораживанию и активность стволовых клеток после криоконсервации может быть значительно повышена.
[Пример применения 9] Криоконсервация овариальных органов и овариальных тканей
Овариальные органы новорожденных мышей возрастом до 3 дней и срезы овариальных тканей половозрелых мышей подвергали криоконсервации с применением замораживающих уравновешивающих растворов и криоконсервирующих растворов, предложенных в Примере 12 и Сравнительном примере 3, согласно схемам, представленным в Таблице 14 и Таблице 15. Способы замораживания-размораживания овариальных органов и овариальных тканей половозрелых мышей представлены в примере применения 3.
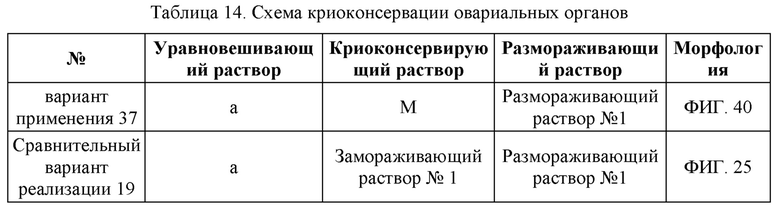
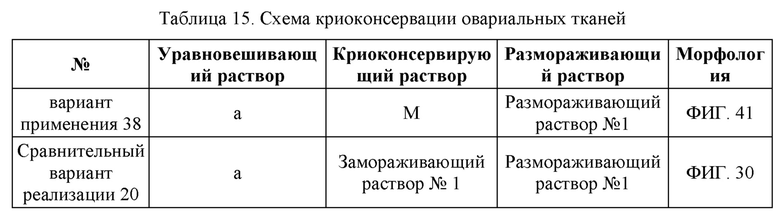
Как можно видеть из ФИГ. 24, 25 и 40 по отношению к сравнительным вариантам реализации, где не применяли биомиметический пептидный материал, подавляющий рост льда (ФИГ. 25 и 30), снимок среза размороженного овариального органа, подвергнутого криоконсервации в криоконсервирующем растворе согласно варианту применения 37, показывает, что исходная структура фолликул остается относительно нетронутой, интерстициальная структура остается относительно нетронутой, цитоплазма клеток относительно однородна и слегка окрашена в относительно небольшом количестве, а сокращения ядер и глубокое окрашивание относительно умеренны, кровеносные сосуды имеют нетронутую структуру стенок и минимальное сужение просвета, цитоплазма клеток эндотелия относительно однородна и слегка окрашена в относительно небольшом количестве, а сокращения ядер и глубокое окрашивание относительно умеренны. Таким образом, вариант применения 37 показывают лучшие эффекты при криоконсервации овариальных органов.
Как можно видеть из ФИГ. 29, 30 и 41, по сравнению со свежими, незамороженными овариальными тканями половозрелых мышей, рассмотренными в Сравнительном варианте реализации 22, схема, предложенная в варианте применения 38, отличаются следующим: структуры фолликул в фазе роста и антральных фолликул остается относительно нетронутой. Можно видеть, что раскрытый в данном описании криоконсервирующий раствор показывает лучший эффект при криоконсервации овариальных тканей, чем криоконсервирующий раствор, традиционно принятый из уровня техники.
Можно видеть, что раскрытый в данном описании криоконсервирующий раствор, приготовленный с применением биомиметического пептидного материала, подавляющего рост льда, может одновременно применяться для криоконсервации ооцитов, эмбрионов, стволовых клеток, репродуктивных органов и тканей, позволяя достигать высоких показателей выживаемости клеток и хорошей биологической активности.
Выше приведены некоторые примеры реализации настоящего изобретения. Однако настоящее изобретение не ограничивается вышеприведенными вариантами воплощениями. Любые модификации, улучшения, аналоги и т.п., сделанные без отступления от существа и объема настоящего изобретения, безусловно подпадают под действие правовой охраны настоящего изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| КРИОКОНСЕРВИРУЮЩИЙ РАСТВОР, НЕ СОДЕРЖАЩИЙ ДМСО, И СПОСОБ ЕГО ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ | 2020 |
|
RU2785227C1 |
| РАЗМОРАЖИВАЮЩАЯ ЖИДКОСТЬ, СПОСОБ ЕЕ ПРИГОТОВЛЕНИЯ И ЕЕ ПРИМЕНЕНИЕ | 2020 |
|
RU2791227C1 |
| КОМПОЗИЦИИ И СПОСОБЫ КРИОКОНСЕРВАЦИИ КЛЕТОК | 2021 |
|
RU2840854C1 |
| СПОСОБЫ ВЫДЕЛЕНИЯ И КУЛЬТИВИРОВАНИЯ ЧЕЛОВЕЧЕСКИХ РЕТИНАЛЬНЫХ КЛЕТОК-ПРЕДШЕСТВЕННИКОВ | 2019 |
|
RU2809003C2 |
| СПОСОБ ВИТРИФИКАЦИИ ОВАРИАЛЬНОЙ ТКАНИ | 2018 |
|
RU2678106C2 |
| СПОСОБ ПОДГОТОВКИ ЖИРОВОЙ ТКАНИ К КРИОКОНСЕРВИРОВАНИЮ | 2016 |
|
RU2655222C2 |
| КОМБИНИРОВАННЫЙ КРИОПРОТЕКТОР "ДИМЕТИЛСУЛЬФОКСИД/РЕОПОЛИГЛЮКИН" ДЛЯ КРИОКОНСЕРВАЦИИ СТВОЛОВЫХ КЛЕТОК И СПОСОБ ИХ КРИОКОНСЕРВАЦИИ ДЛЯ КЛИНИЧЕСКОГО ПРИМЕНЕНИЯ | 2014 |
|
RU2563117C1 |
| КЛЕТКИ-ПРЕДШЕСТВЕННИКИ ПЕЧЕНИ ЧЕЛОВЕКА | 2000 |
|
RU2247565C2 |
| Способ получения ноотропной композиции на основе полипептидных комплексов, выделенных из нейронов и глиальных клеток, полученных методом направленной дифференцировки индуцированных плюрипотентных стволовых клеток человека | 2018 |
|
RU2690498C1 |
| СПОСОБ КРИОКОНСЕРВАЦИИ КЛЕТОК, ИСКУССТВЕННЫЕ КЛЕТОЧНЫЕ КОНСТРУКЦИИ ИЛИ ТРЕХМЕРНЫЕ СЛОЖНЫЕ КОМПЛЕКСЫ ТКАНЕЙ | 2010 |
|
RU2573307C2 |
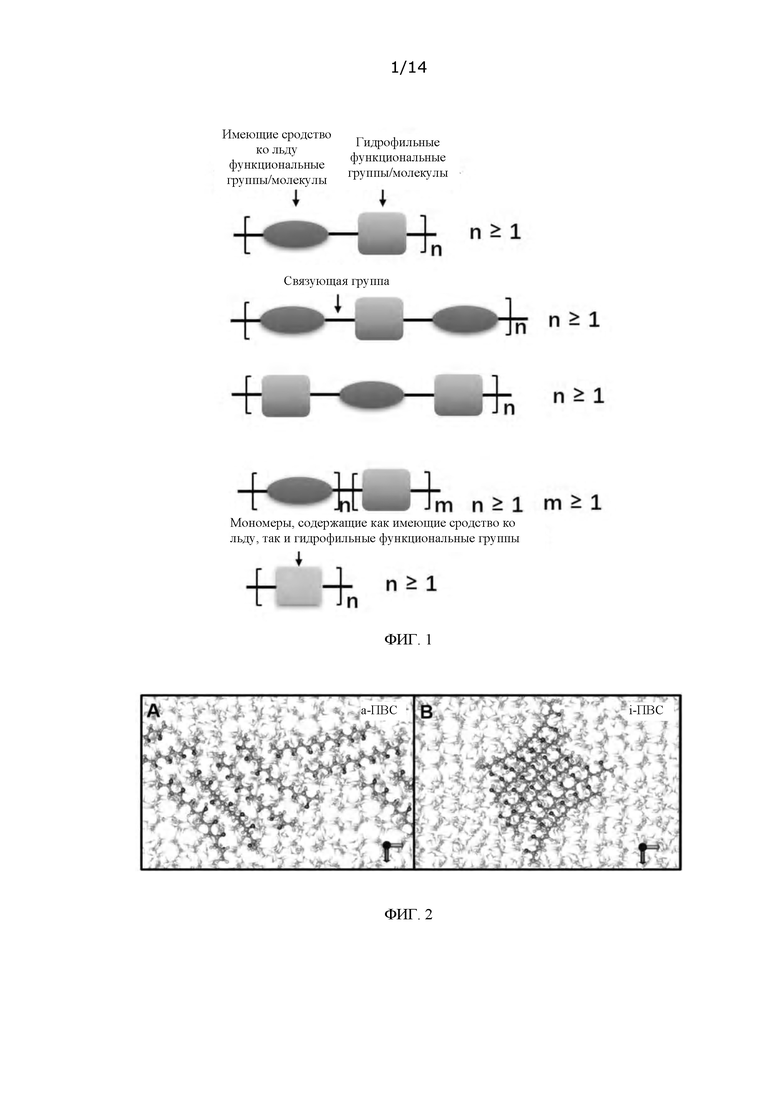
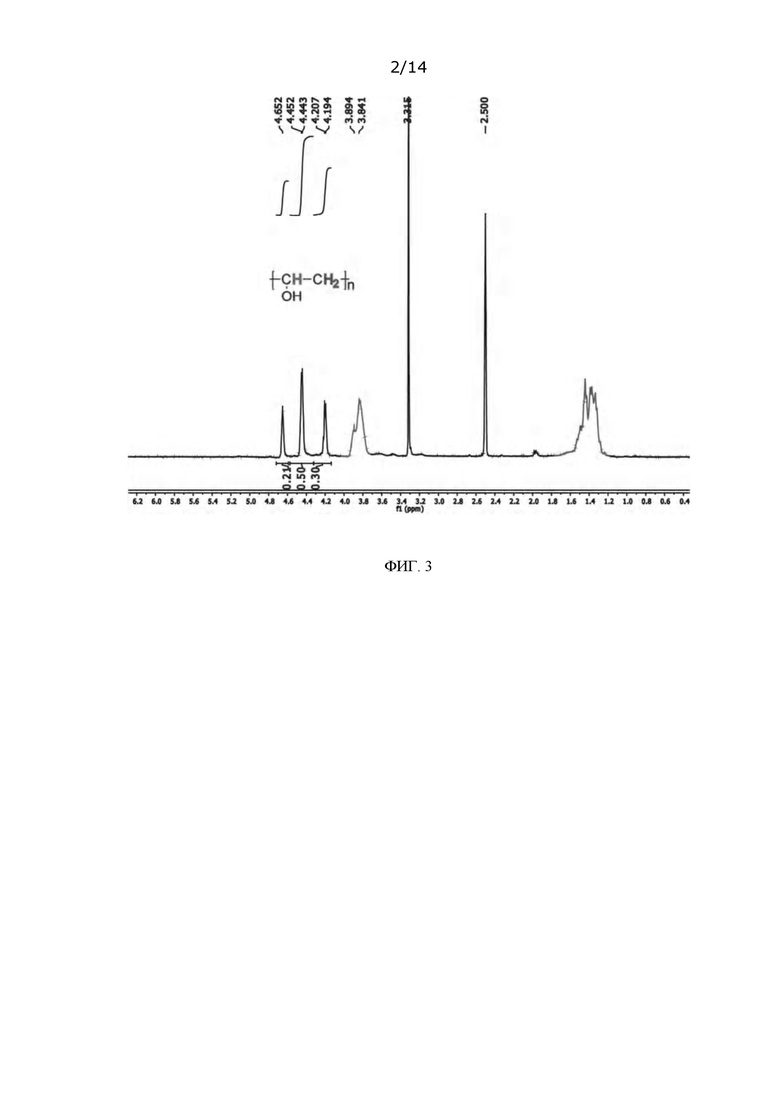
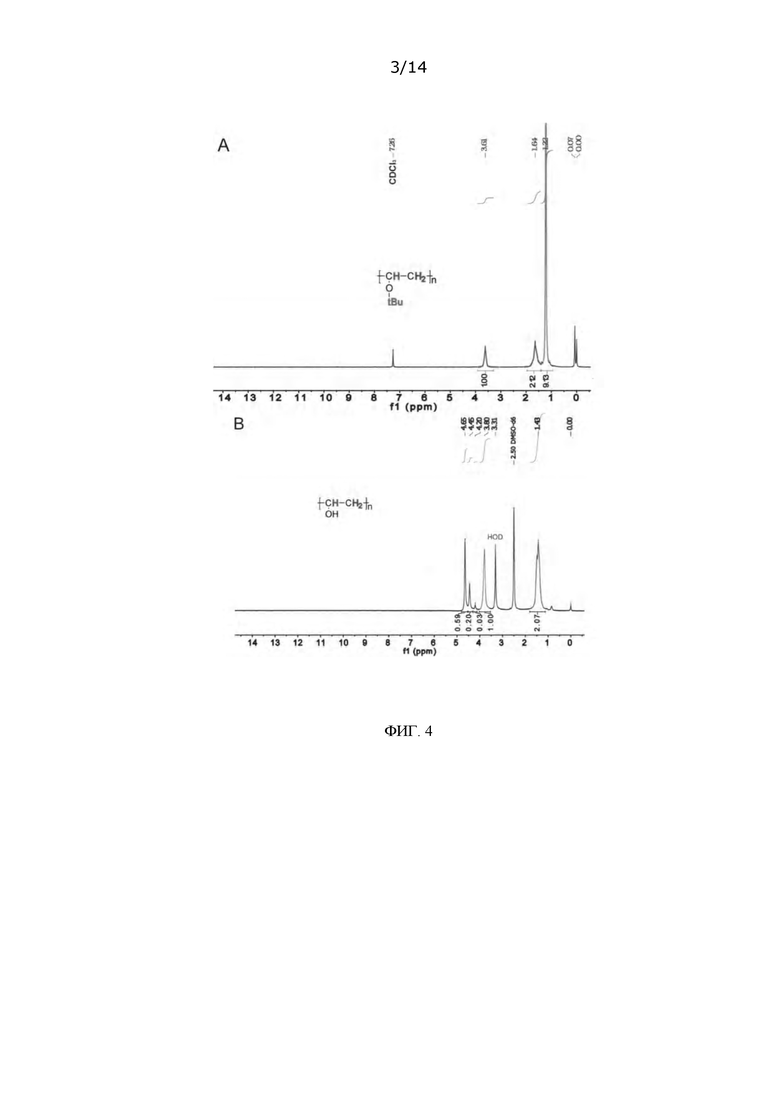
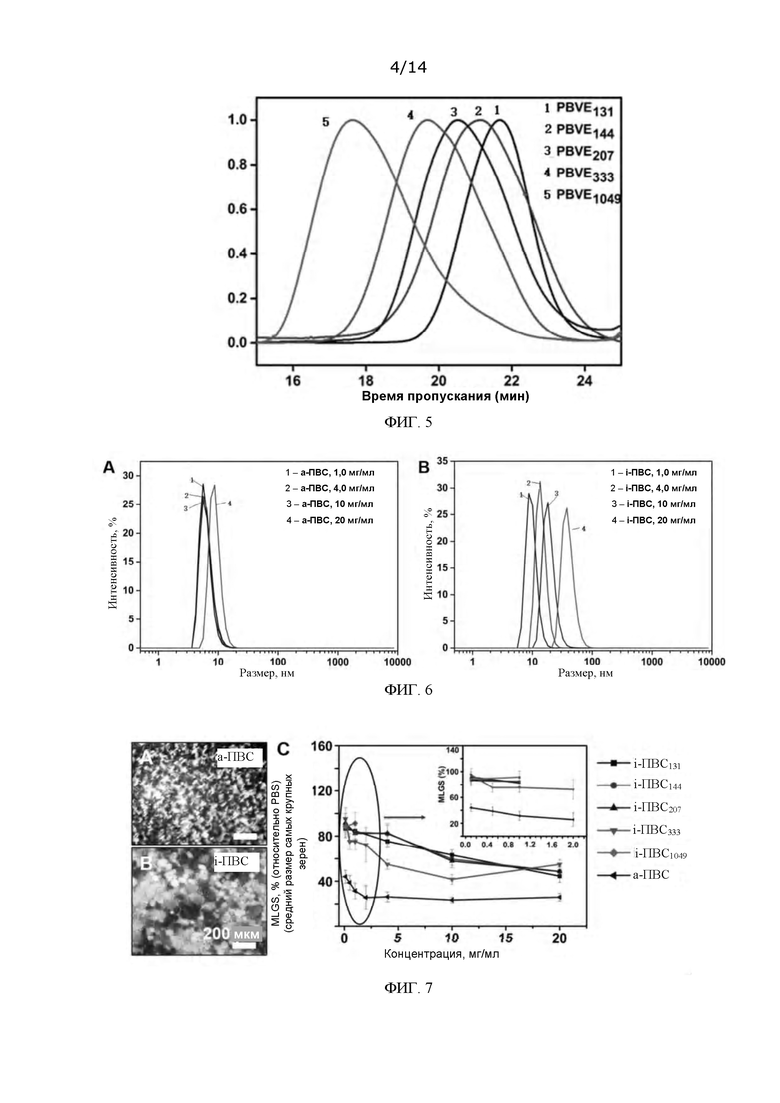
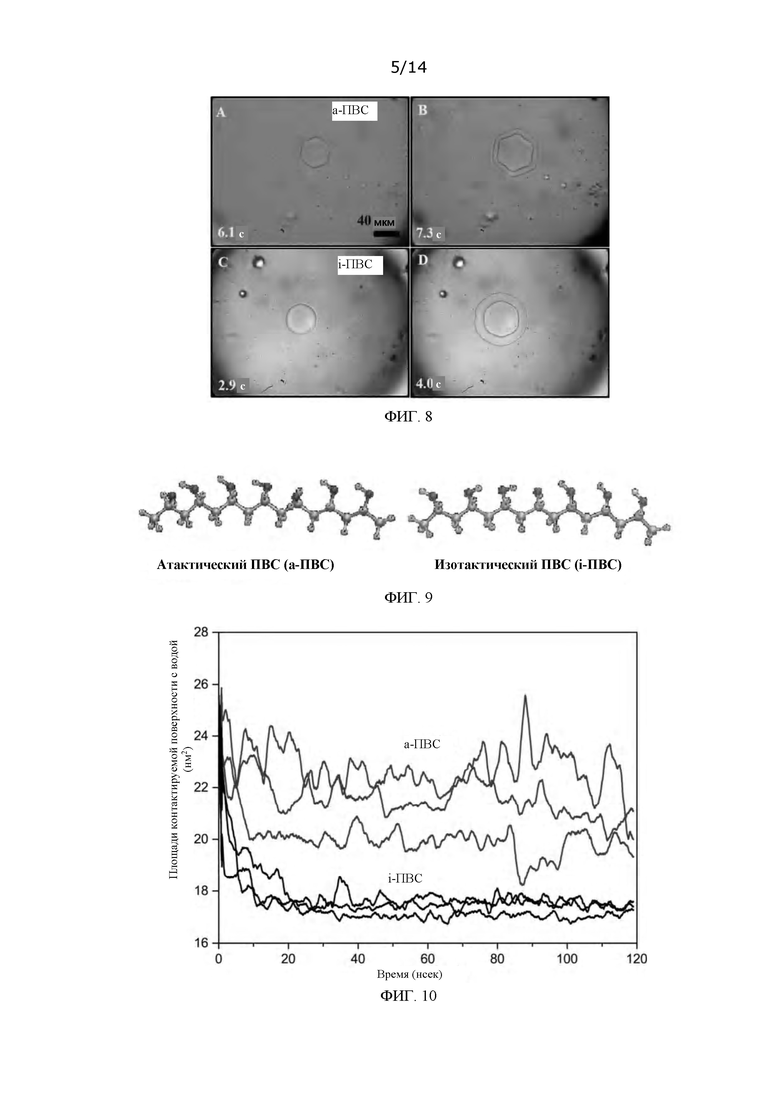
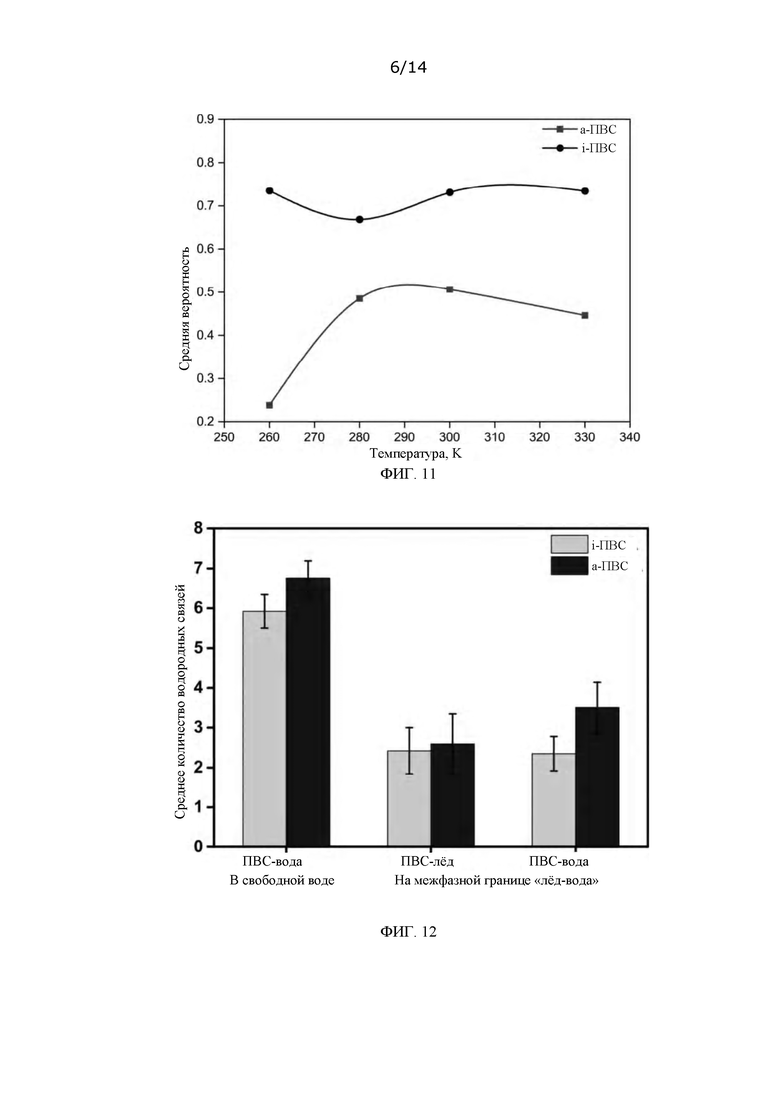
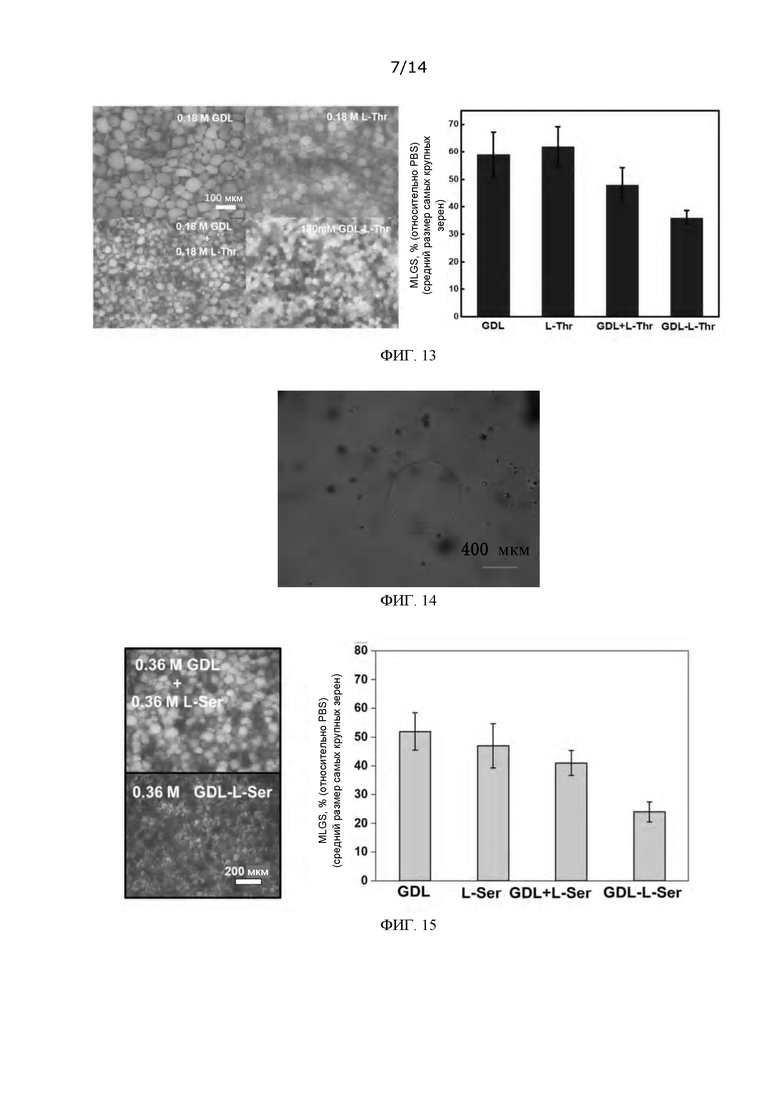
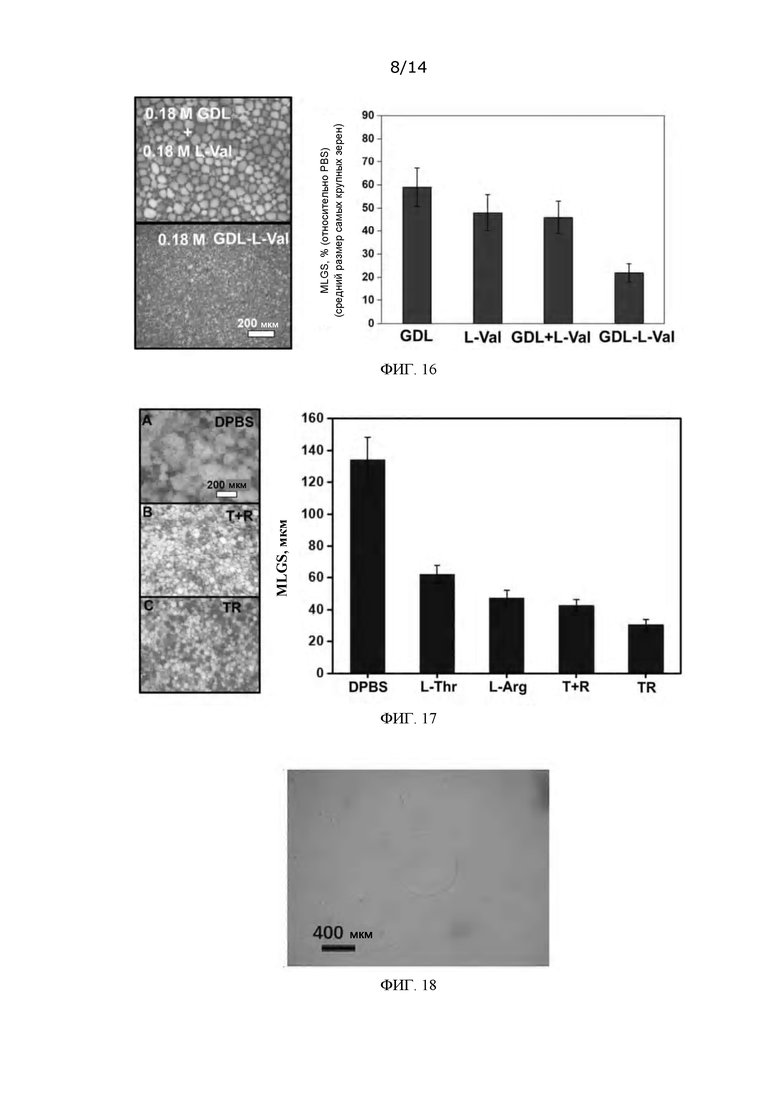
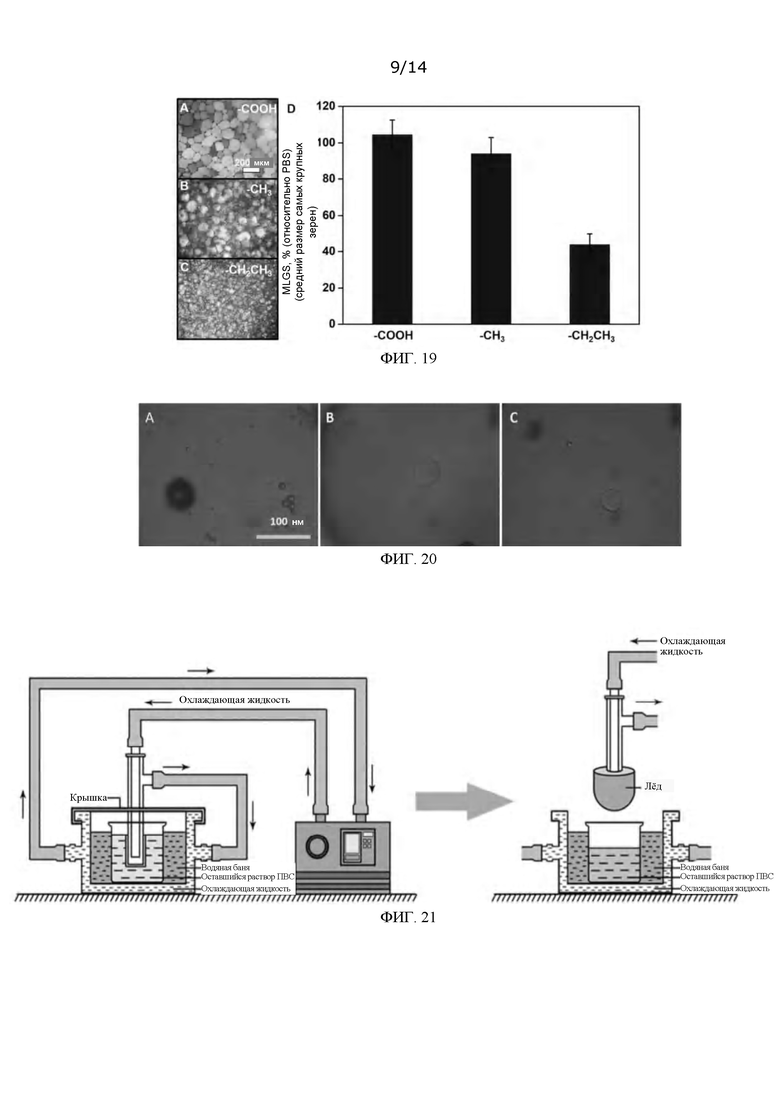
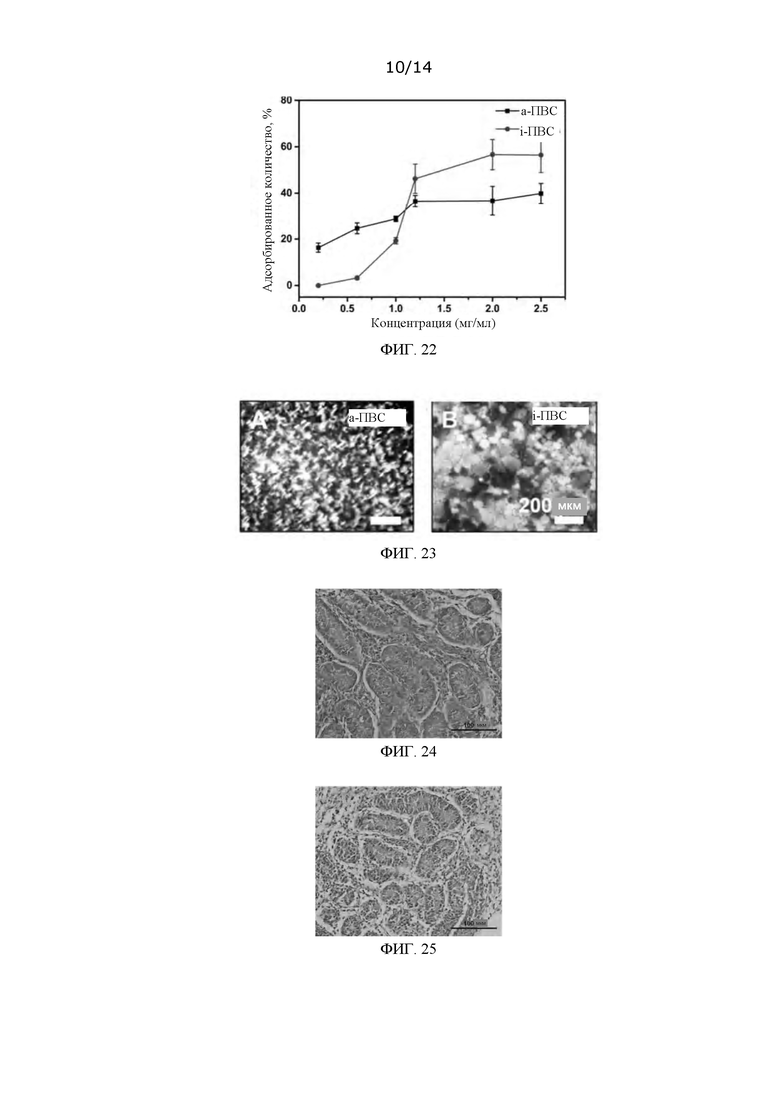
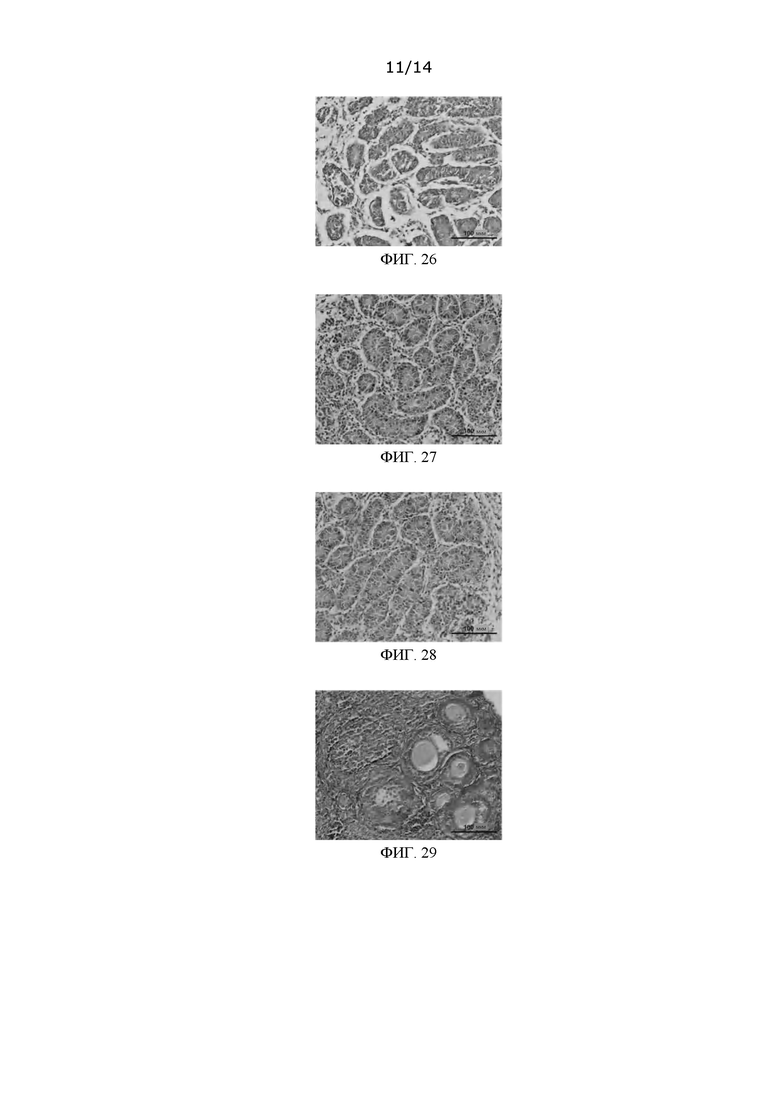
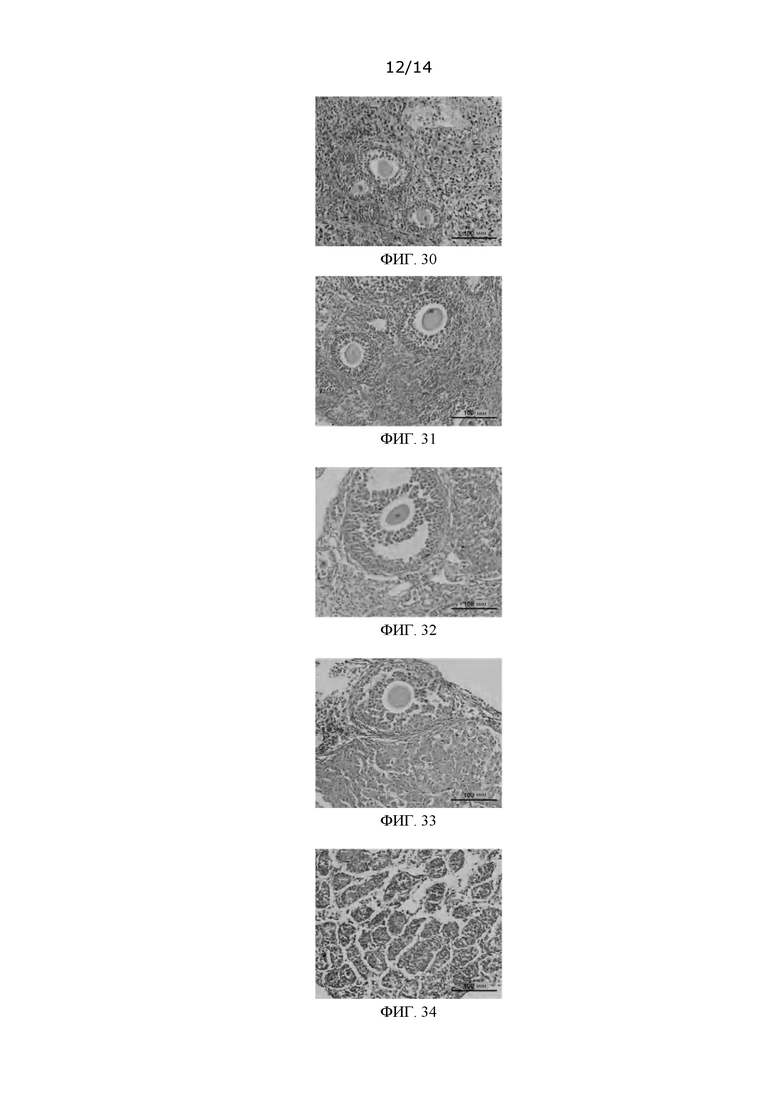
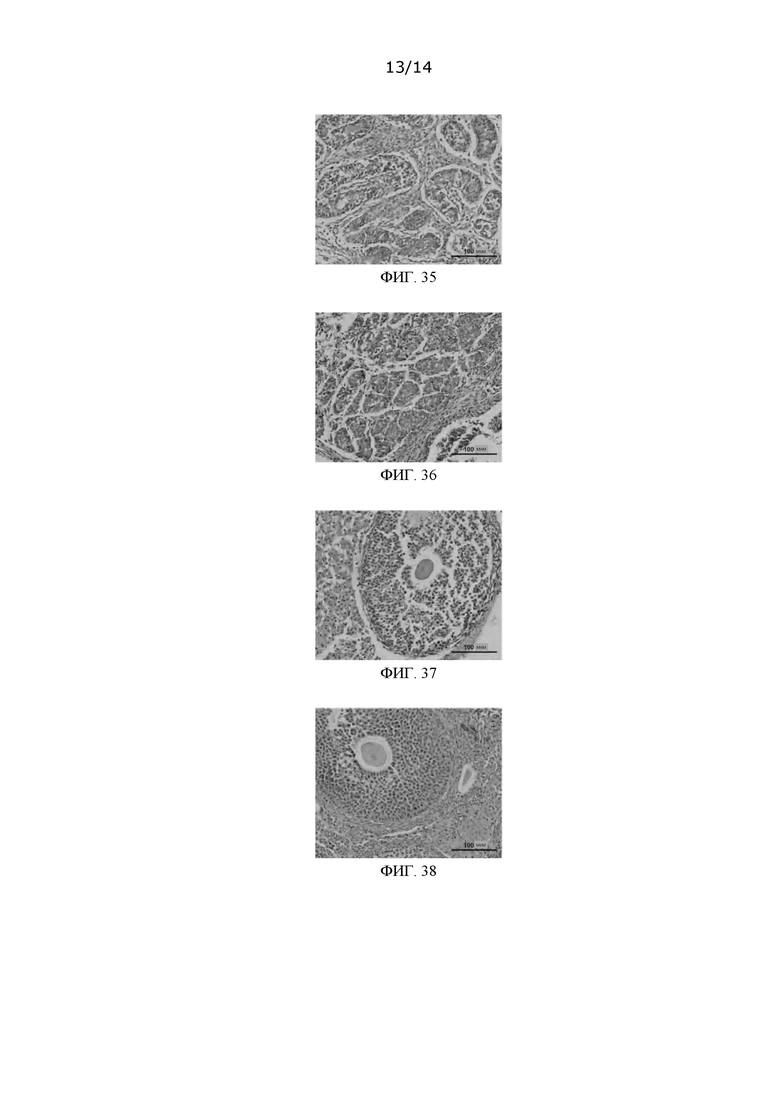

Изобретение относится к области биомедицинских материалов и, в частности, к биомиметическому материалу, подавляющему рост льда. Биомиметический материал получен путем создания библиотеки структур молекул соединений, в которой молекулы содержат гидрофильную группу и группу, имеющую сродство ко льду, путем оценивания показателей способности каждой из молекул соединений распределяться по межфазной границе «лед - вода» с помощью метода молекулярной динамики (MD-моделирования) и путем скрининга молекул соединений с желаемой степенью сродства ко льду и к воде. Предложен механизм сродства материала ко льду и воде, предложено внедрение MD-моделирования в проектирование молекулярной структуры материала, подавляющего рост льда, предложено оценивать сродство спроектированного материала ко льду и воде с помощью MD-моделирования, предложено прогнозирование характеристик подавления роста льда для материала, подавляющего рост льда, и предложена возможность осуществления оптимизации его структуры. Спроектированный и отобранный биомиметический материал обладает хорошей способностью подавлять рост кристаллов льда и может обеспечивать хороший криоконсервирующий эффект в отношении реагентов даже без добавления ДМСО. 7 н. и 37 з.п. ф-лы, 41 ил., 32 табл., 24 пр.
1. Способ молекулярного проектирования материала, подавляющего рост льда, включающий следующие стадии:
(1) создание библиотеки структур молекул соединений, в которой указанные молекулы соединений содержат гидрофильную группу и группу, имеющую сродство ко льду;
(2) моделирование и оценивание способности указанных молекул соединений распределяться по межфазной границе «лёд - вода» с помощью моделирования методом молекулярной динамики (MD); и
(3) скрининг молекул соединений, имеющих сродство ко льду и воде.
2. Способ молекулярного проектирования по п. 1, в котором MD-моделирование на стадии (2) производят с использованием программных пакетов GROMACS, AMBER, CHARMM, NAMD или LAMMPS;
при проведении MD-моделирования на стадии (2) модель молекулы воды предпочтительно выбрана из моделей TIP3P, TIP4P, TIP4P/2005, SPC, TIP3P, TIP5P и SPC/E, предпочтительно модели молекулы воды TIP4P/2005;
при проведении MD-моделирования на стадии (2) параметр силового поля предпочтительно обеспечен с применением одного из силовых полей GROMOS, ESFF, силового поля MM, AMBER, CHARMM, COMPASS, UFF, CVFF и других силовых полей.
3. Способ молекулярного проектирования по п. 1 или 2, в котором при MD-моделировании на стадии (2) моделирование и расчет выполняют учитывая взаимодействие между указанными молекулами соединения, взаимодействие между молекулами соединения и молекулами воды в жидкой фазе и взаимодействие между молекулами соединения и молекулами воды в структуре льда; при этом, например, указанные взаимодействия включают образование водородной связи, ван-дер-ваальсовое взаимодействие, электростатическое взаимодействие, гидрофобное взаимодействие и π-π взаимодействие.
4. Способ молекулярного проектирования по любому из пп. 1-3, в котором при MD-моделировании на стадии (2), когда моделирование и расчет выполняют, учитывая взаимодействия между молекулами, проводят корректировку температуры и давления; при этом предпочтительно температуру и давление корректируют с использованием регулятора температуры V-rescale и регулятора давления;
при проведении MD-моделирования на стадии (2) молекулярную конфигурацию молекул соединения предпочтительно поддерживают путем выбора параметра потенциальной энергии;
при проведении MD-моделирования на стадии (2), если моделируют систему водного раствора, предпочтительно задают периодические граничные условия для направления x, направления у и направления z; при этом, когда моделируют смешанную систему «лёд - вода», периодические граничные условия задают для направления x и направления y;
при проведении MD-моделирования на стадии (2) предпочтительно выбирают кубический или октаэдрический блок воды и предпочтительным является кубический блок с размерами 3,9 × 3,6 × 1,0 нм3.
5. Способ молекулярного проектирования по любому из пп. 1-4, в котором основная цепь молекул соединений представляет собой структуру с углеродной цепью или пептидной цепью.
6. Способ молекулярного проектирования по любому из пп. 1-5, в котором гидрофильная группа представляет собой функциональную группу, способную к образованию нековалентного взаимодействия с молекулой воды, например, путем образования водородной связи, ван-дер-ваальсового взаимодействия, электростатического взаимодействия, гидрофобного взаимодействия или π-π взаимодействия с водой; например, гидрофильная группа может быть выбрана из по меньшей мере одной из таких групп, как гидроксильная группа (-OH), аминогруппа (-NH2), карбоксильная группа (-COOH) и амидогруппа (-CONH2), или, например, из молекул соединений, таких как гидрофильная аминокислота, например пролин (L-Pro), аргинин (L-Arg) и лизин (L-Lys), глюконодельталактон (GDL) и сахарид, и их молекулярных фрагментов;
группа, имеющая сродство ко льду, представляет собой функциональную группу, способную к образованию нековалентного взаимодействия со льдом, например, путем образования водородной связи, ван-дер-ваальсового взаимодействия, электростатического взаимодействия, гидрофобного взаимодействия или π-π взаимодействия со льдом; в качестве иллюстрации группа, имеющая сродство ко льду, может быть выбрана из гидроксила (-OH), аминогруппы (-NH2), фенила (-C6H5), пирролидинила (-C4H8N) или, например, из молекул соединений, таких как аминокислота, имеющая сродство ко льду, такая как глутамин (L-Gln), треонин (L-Thr) и аспарагиновая кислота (L-Asn), бензольное кольцо (C6H6) и пирролидин (C4H9N), и их молекулярных фрагментов.
7. Способ молекулярного проектирования по любому из пп. 1-6, в котором материал, подавляющий рост льда, формируют путем ковалентного связывания блока, содержащего гидрофильную группу, с блоком, содержащим группу, имеющую сродство ко льду, или формируют путем ионного связывания молекулы, содержащей гидрофильную группу, с молекулой, содержащей группу, имеющую сродство ко льду.
8. Способ молекулярного проектирования по любому из пп. 1-7, дополнительно включающий стадию синтеза указанных молекул соединений путем, например, полимеризации, конденсации с отщеплением воды или биологической ферментации бактериями, полученными методами генной инженерии.
9. Материал, подавляющий рост льда, полученный способом молекулярного проектирования по любому из пп. 1-8.
10. Материал, подавляющий рост льда, по п. 9, где материал, подавляющий рост льда, представляет собой ПВС c диадной синдиотактичностью r 45-60% и молекулярной массой 10-500 кДа; при этом предпочтительно ПВС имеет диадную синдиотактичность r 50-55% и молекулярную массу 10-30 кДа.
11. Способ скрининга материала, подавляющего рост льда, включающий: (1) определение сродства материала, подавляющего рост льда, к воде и (2) определение показателей способности материала, подавляющего рост льда, распределяться по межфазной поверхности «лёд - вода», причем стадия (2) обеспечивается путем определения количества материала, подавляющего рост льда, адсорбированного на поверхности льда, в ходе эксперимента по адсорбции материала льдом,
при этом адсорбированное на поверхности льда количество материала, подавляющего рост льда, выражается как (масса материала, подавляющего рост льда, адсорбированного на поверхности льда (m1)) / (общая масса материала, подавляющего рост льда, в исходном растворе, содержащем материал, подавляющий рост льда (m2)) × 100%.
12. Способ скрининга материала, подавляющего рост льда, по п. 11, в котором стадия (1) обеспечивается путем определения растворимости, константы гидратации, степени диспергирования материала, подавляющего рост льда, в воде и/или количества межмолекулярных водородных связей, образованных между молекулой материала, подавляющего рост льда, и молекулой воды.
13. Способ скрининга материала, подавляющего рост льда, по любому из пп. 11, 12, в котором эксперимент по адсорбции материала льдом включает следующие стадии:
S1: приготовление водного раствора материала, подавляющего рост льда, и охлаждение до температуры переохлаждения;
S2: внесение в указанный водный раствор предварительно охлажденного стержня регулирования температуры, так чтобы инициировать рост слоя льда на поверхности стержня регулирования температуры, при этом водный раствор постоянно перемешивают, что обеспечивает возможность равномерной адсорбции материала, подавляющего рост льда, на поверхности слоя льда, а температуру стержня регулирования температуры и температуру водного раствора поддерживают на уровне температуры переохлаждения; и
S3: определение количества материала, подавляющего рост льда, адсорбированного на поверхности льда;
при этом предпочтительно стержень регулирования температуры предварительно охлаждают одним из таких способов, как замораживание жидким азотом, сухим льдом или с помощью охлаждающего устройства со сверхнизкими температурами.
14. Способ скрининга материала, подавляющего рост льда, по любому из пп. 11-13, в котором степень переохлаждения и время адсорбции на протяжении эксперимента по адсорбции материала льдом поддерживают неизменными, так чтобы площадь поверхности полученного льда оставалась неизменной в пределах допустимой погрешности.
15. Способ скрининга материала, подавляющего рост льда, по любому из пп. 13, 14, в котором в материал, подавляющий рост льда, на стадии S1 предварительно введена флуоресцентная метка, например флуоресцеин;
при этом предпочтительно, если сам материал, подавляющий рост льда, способен поглощать в ультрафиолетовом или флуоресцентном спектре, флуоресцентная метка не требуется.
16. Способ скрининга материала, подавляющего рост льда, по любому из пп. 13-15, в котором стадия S3 включает:
S3a: извлечение блока льда после адсорбции, промывание блока льда очищенной водой и плавление блока льда с получением адсорбционного раствора материала, подавляющего рост льда; и
S3b: определение объема V полученного плавлением адсорбционного раствора материала, подавляющего рост льда, определение массо-объемной концентрации c материала, подавляющего рост льда, в адсорбционном растворе и расчет массы m1 материала, подавляющего рост льда, адсорбированного на поверхности льда, посредством формулы m1 = cV.
17. Способ скрининга материала, подавляющего рост льда, по п. 16, в котором на стадии S3b концентрацию c определяют методом спектроскопии в ультрафиолетовой и видимой области спектра.
18. Способ скрининга материала, подавляющего рост льда, по любому из пп. 11-17, где указанный способ применяют для скрининга материала для подавления роста кристаллов льда.
19. Способ скрининга материала, подавляющего рост льда, по любому из пп. 11-18, дополнительно включающий стадию (3): оценку сродства материала к воде и сродства материала ко льду.
20. Устройство для проведения эксперимента по адсорбции материала льдом для применения в способе по п. 13, включающее многослойную полость для размещения жидкости, стержень регулирования температуры и температурный регулятор, где многослойная полость для размещения жидкости последовательно включает изнутри наружу: полость для адсорбции материала льдом, полость бани и полость для размещения охлаждающей жидкости; при этом стержень регулирования температуры размещен в полости для адсорбции материала льдом, а температуру стержня регулирования температуры и полости для размещения жидкости регулируют посредством температурного регулятора.
21. Устройство для проведения эксперимента по адсорбции материала льдом по п. 20, в котором стержень регулирования температуры имеет полую структуру, выполненную из теплопроводящего материала, и полая структура стержня регулирования температуры имеет входное отверстие для жидкости и выходное отверстие для жидкости; температурный регулятор представляет собой жидкостный регулятор температуры и снабжен концевым отверстием для выпуска и концевым отверстием для возврата охлаждающей жидкости; при этом два конца полости для размещения охлаждающей жидкости имеют входное отверстие для жидкости и выходное отверстие для жидкости; причем концевое отверстие для выпуска охлаждающей жидкости температурного регулятора, входное отверстие для жидкости стержня регулирования температуры, выходное отверстие для жидкости стержня регулирования температуры, входное отверстие для жидкости резервуара для размещения охлаждающей жидкости, выходное отверстие для жидкости резервуара для размещения охлаждающей жидкости и концевое отверстие для возврата охлаждающей жидкости температурного регулятора последовательно соединены трубками, по которым протекает охлаждающая жидкость;
при этом предпочтительно указанная многослойная полость для размещения жидкости снабжена крышкой;
при этом предпочтительно при использовании устройства для проведения эксперимента по адсорбции материала льдом полость для адсорбции материала льдом выполнена с возможностью размещения водного раствора материала, подавляющего рост льда, и полость бани в среднем слое выполнена с возможностью размещения среды для бани, находящейся при заданной температуре, например воды для бани, льда для бани или масла для бани; при этом после достижения заданной температуры охлаждающей жидкости охлаждающая жидкость вытекает из температурного регулятора и поступает в полую структуру стержня регулирования температуры, чтобы обеспечить регулирование температуры стержня регулирования температуры, затем вытекает из выходного отверстия для жидкости стержня регулирования температуры и поступает в полость для размещения охлаждающей жидкости в наружном слое с обеспечением поддержания температуры среды бани на заданном уровне, и затем протекает через выходное отверстие для жидкости резервуара для размещения охлаждающей жидкости и концевое отверстие для возврата охлаждающей жидкости температурного регулятора и поступает в температурный регулятор для циркуляции.
22. Криоконсервирующий раствор, содержащий биомиметический материал, подавляющий рост льда, по п. 9 или 10.
23. Криоконсервирующий раствор по п. 22, в котором биомиметический материал, подавляющий рост льда, представляет собой одно из или комбинацию из таких соединений, как поливиниловый спирт (ПВС), аминокислота или полиаминокислота и/или пептидное соединение; при этом криоконсервирующий раствор дополнительно содержит полиол, водорастворимый сахарид (или его производное, такое как водорастворимая целлюлоза) и буфер.
24. Криоконсервирующий раствор по п. 23, который содержит пептидное соединение и, в частности, содержит, на 100 мл, 0,1-50 г пептидного соединения, 0-6,0 г ПВС, 0-9,0 г полиаминокислоты или аминокислоты, 0-15 мл ДМСО, 5-45 мл полиола, водорастворимый сахарид в концентрации 0,1-1,0 моль/л, 0-30 мл сыворотки, при этом остальное количество составляет буфер.
25. Криоконсервирующий раствор по п. 23, который содержит ПВС и, в частности, содержит, на 100 мл, 0,01-6,0 г ПВС, 0-50 г пептидного соединения, 0-9,0 г полиаминокислоты или аминокислоты, 0-15 мл ДМСО, 5-45 мл полиола, водорастворимый сахарид в концентрации 0,1-1,0 моль/л, 0-30 мл сыворотки, при этом остальное количество составляет буфер.
26. Криоконсервирующий раствор по п. 23, который содержит аминокислоту или полиаминокислоту и, в частности, содержит, на 100 мл, 0,1-50 г аминокислоты или полиаминокислоты, 0-6,0 г ПВС, 0-15 мл ДМСО, 5-45 мл полиола, водорастворимый сахарид в концентрации 0,1-1,0 моль/л, 0-30 мл сыворотки, при этом остальное количество составляет буфер.
27. Криоконсервирующий раствор по п. 26, в котором содержание аминокислоты и/или полиаминокислоты в криоконсервирующем растворе составляет 0,5-50 г, предпочтительно 1,0-35 г на 100 мл; при этом, например, содержание аминокислоты может составлять 5,0-35 г, предпочтительно 15-25 г в присутствии аминокислоты; содержание полиаминокислоты может составлять 0,5-9,0 г, предпочтительно 1,0-5,0 г в присутствии полиаминокислоты.
28. Криоконсервирующий раствор по любому из пп. 23-27, в котором полиол может представлять собой полиол, имеющий 2-5 атомов углерода, предпочтительно диол, имеющий 2-3 атома углерода, и/или триол, такой как любой из этиленгликоля, пропиленгликоля и глицерина, предпочтительно этиленгликоль; при этом содержание полиола в криоконсервирующем растворе предпочтительно составляет 5,0-40 мл, например 6,0-20 мл, 9-15 мл, на 100 мл.
29. Криоконсервирующий раствор по любому из пп. 23-27, в котором водорастворимый сахарид представляет собой по меньшей мере один из таких сахаридов, как невосстанавливающий дисахарид, водорастворимый полисахарид, водорастворимая целлюлоза и ангидрид сахарида, и, например, выбран из сахарозы, трегалозы, гидроксипропилметилцеллюлозы и полисахарозы.
30. Криоконсервирующий раствор по любому из пп. 23-27, в котором буфер может быть выбран из по меньшей мере одного из DPBS, HEPES-буферизованного HTF и других буферов для культивирования клеток.
31. Криоконсервирующий раствор по любому из пп. 23-27, в котором содержание ДМСО в криоконсервирующем растворе составляет 0-10 мл, например 1,0-7,5 мл, на 100 мл;
содержание сыворотки в криоконсервирующем растворе составляет 0,1-30 мл, например 5,0-20 мл, на 100 мл;
содержание водорастворимого сахарида в криоконсервирующем растворе составляет 0,1-1,0 моль/л, например 0,1-0,8 моль/л, в 100 мл;
содержание полиола в криоконсервирующем растворе составляет 5,0-40 мл, например 6,0-20 мл, на 100 мл раствора.
32. Криоконсервирующий раствор по любому из пп. 22-31, в котором pH составляет 6,5-7,6.
33. Криоконсервирующий раствор по любому из пп. 23-31, в котором ПВС выбран из одного из или комбинации двух или более из таких ПВС, как изотактический ПВС, синдиотактический ПВС и атактический ПВС, и, например, ПВС характеризуется диадной синдиотактичностью 15-65%, предпочтительно диадной синдиотактичностью 45-65%.
34. Криоконсервирующий раствор по п. 33, в котором ПВС может быть выбран из ПВС, имеющего молекулярную массу 10-500 кДа или более.
35. Криоконсервирующий раствор по любому из пп. 23-31, в котором пептидные соединения получены путем реакции аминокислот, имеющих сродство ко льду, таких как треонин (L-Thr), глутамин (L-Gln) и аспарагиновая кислота (L-Asn), с другими гидрофильными аминокислотами, которые могут быть выбраны из аргинина, пролина и аланина, или с глюконодельталактоном (GDL) или сахаридами.
36. Криоконсервирующий раствор по п. 34, в котором пептидное соединение состоит из не менее чем двух аминокислотных звеньев, например 2-8 аминокислотных звеньев.
37. Криоконсервирующий раствор по любому из пп. 34-36, в котором пептидное соединение имеет структуру согласно любой из формул (1) - (9):
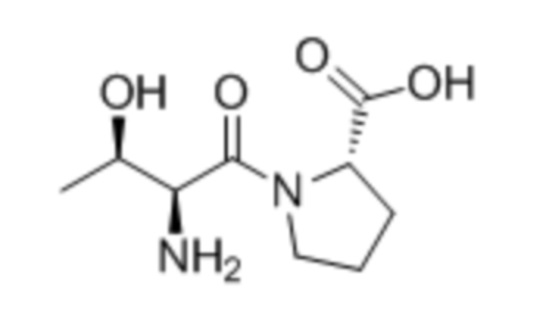
формула (1)
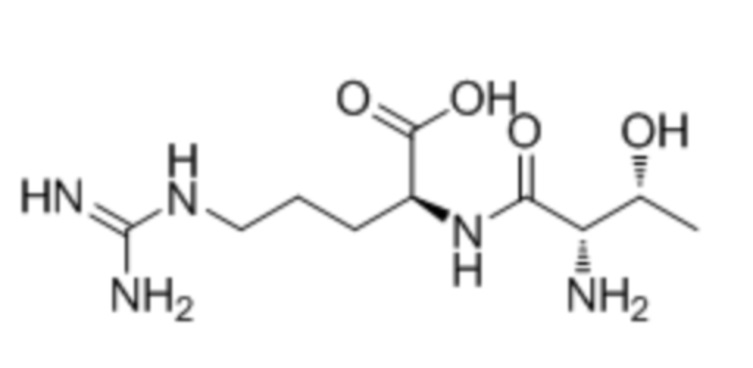
формула (2)
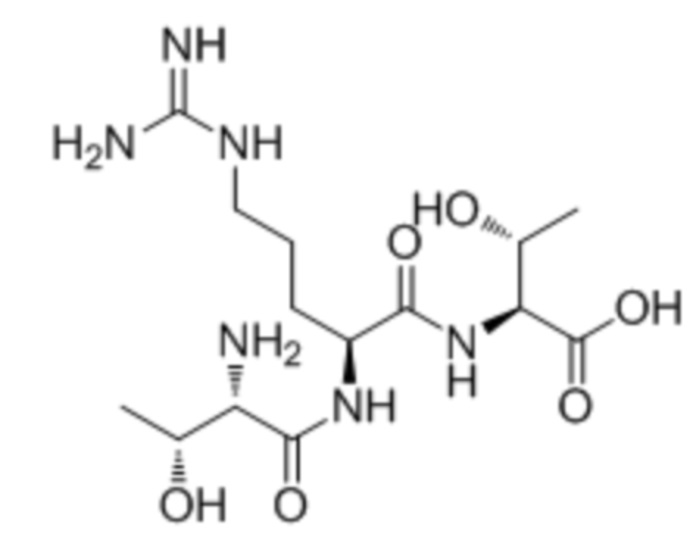
формула (3)
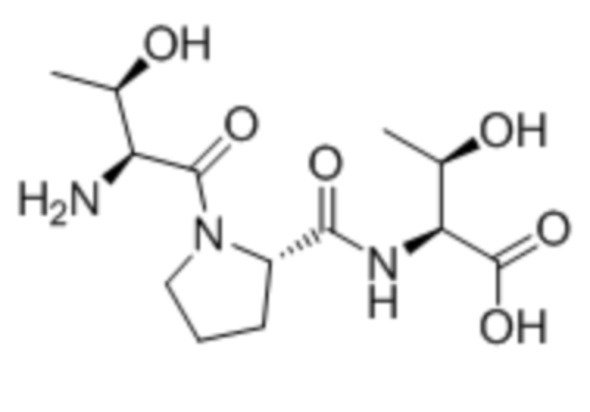
формула (4)
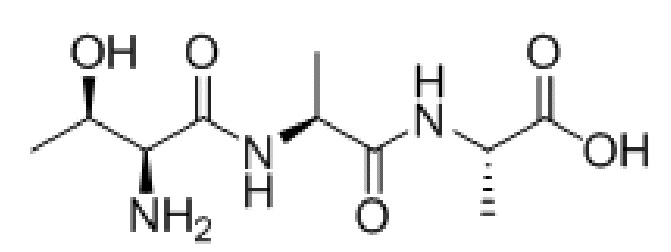
формула (5)
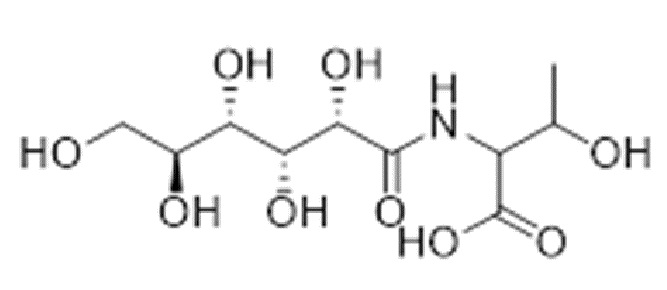
формула (6)
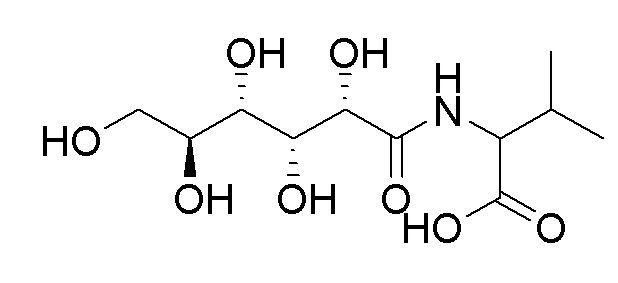
формула (7)
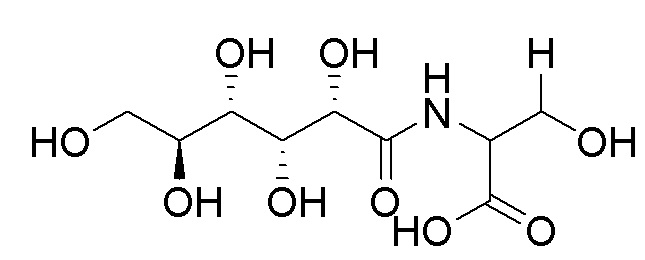
формула (8)
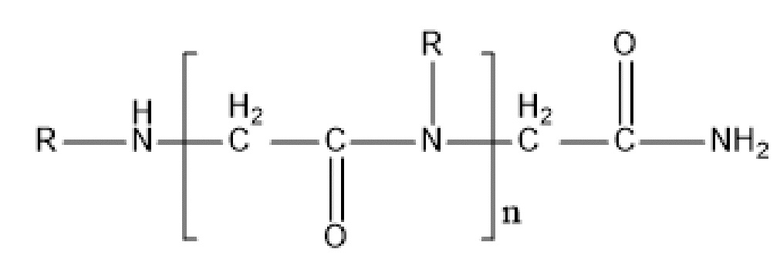
формула (9),
где R в формуле (9) выбран из замещенного алкила и незамещенного алкила, а заместитель может быть выбран из -OH, -NH2, -COOH, -CONH2; например, R представляет собой замещенный или незамещенный C1-6 алкил и предпочтительно R представляет собой -CH3, -CH2CH3, -CH2CH2COOH; n представляет собой целое число, равное не менее 1 и не более 1000.
38. Криоконсервирующий раствор по любому из пп. 23-31, в котором аминокислота представляет собой аминокислоту, содержащую группу, имеющую сродство ко льду, и гидрофильную группу, полиаминокислота представляет собой полиаминокислоту, состоящую из аминокислоты, содержащей группу, имеющую сродство ко льду, и аминокислоты, содержащей гидрофильную группу, и полиаминокислота предпочтительно имеет степень полимеризации 2-40, например степень полимеризации 6, 8, 15 или 20, и, например, представляет собой одно из или комбинацию двух или более из таких полиаминокислот, как поли-L-пролин, поли-L-аргинин; аминокислота выбрана из одной или двух из таких аминокислот, как аргинин, треонин, пролин, лизин, гистидин, глутаминовая кислота, аспарагиновая кислота, глицин, например, комбинации аргинина и треонина; или полиаминокислоту, состоящую из указанных выше аминокислот.
39. Криоконсервирующий реагент, содержащий криоконсервирующий раствор по любому из пп. 22-38 и замораживающий уравновешивающий раствор, содержащий, на 100 мл, 5,0-45 мл полиола, при этом остальное количество составляет буфер.
40. Криоконсервирующий реагент по п. 39, в котором замораживающий уравновешивающий раствор дополнительно необязательно содержит 0-15 мл ДМСО, 0-30 мл сыворотки и/или 0-5,0 г ПВС.
41. Применение криоконсервирующего раствора по любому из пп. 22-38 или криоконсервирующего реагента по п. 39 для криоконсервации клеток, тканей и органов.
42. Применение по п. 41, в котором клетки представляют собой половые клетки или стволовые клетки; например, половые клетки выбраны из ооцитов и сперматозоидов, а стволовые клетки выбраны из эмбриональных стволовых клеток, разнообразных мезенхимальных стволовых клеток (например, мезенхимальных стволовых клеток пуповины, мезенхимальных стволовых клеток жировой ткани и мезенхимальных стволовых клеток костного мозга) и гемопоэтических стволовых клеток.
43. Применение по п. 41, в котором ткань представляет собой овариальную ткань или эмбриональную ткань.
44. Применение по п. 41, в котором орган представляет собой овариальный орган.
| CN 109497044 A, 22.03.2019 | |||
| CN 104839144 A, 19.08.2015 | |||
| CN 107183008 A, 22.09.2017 | |||
| RU 2014113706 A, 20.11.2015 | |||
| СРЕДА ДЛЯ КРИОКОНСЕРВИРОВАНИЯ МЕЗЕНХИМАЛЬНЫХ СТВОЛОВЫХ КЛЕТОК И БИОТРАНСПЛАНТАТ С ЕЕ ИСПОЛЬЗОВАНИЕМ | 2006 |
|
RU2303631C1 |
Авторы
Даты
2023-01-13—Публикация
2020-03-02—Подача