РОДСТВЕННЫЕ ЗАЯВКИ
[001] Настоящая заявка испрашивает приоритет по предварительной заявке на патент США 62/737,622, поданной 27 сентября 2018 года, содержание которой полностью включено посредством отсылки.
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
[002] Изобретение, описанное в настоящем документе, в целом относится к области биологии стволовых клеток и регенеративной медицины. В альтернативных вариантах осуществления в настоящем документе предложены способы выделения первичных клеток сетчатки, полученных или выделенных из человеческого образца. В альтернативных вариантах осуществления предложены композиции и способы лечения, уменьшения тяжести или профилактики заболевания или патологии сетчатки; улучшения фотопического (дневного) зрения; улучшения остроты зрения, улучшения функции желтого пятна, улучшения поля зрения или улучшения скотопического (ночного) зрения путем введения ретинальных клеток-предшественников или регенерации желтого пятна и/или восстановления функции скотопического зрения.
УРОВЕНЬ ТЕХНИКИ
[003] Дегенерация сетчатки глаза относится к ухудшению состояния или дегенерации, вызванной прогрессирующим и необратимым снижением количества и гибелью фоторецепторных клеток в сетчатке. Гибель фоторецепторных клеток может привести к слепоте. Таким образом, в уровне техники существует потребность в эффективных способах лечения для восстановления поврежденных и потерянных фоторецепторных клеток и восстановления зрительной функции.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
[004] В изобретении предложены способы выделения первичных клеток сетчатки, полученных или ранее полученных из образца человека путем: (а) обработки полученного образца или использования уже обработанного образца тканей сетчатки глаза человека гестационного возраста от приблизительно 12 недель до приблизительно 28 недель, (b) механической диссоциации полученного образца, (c) определения жизнеспособности и количества первичных клеток сетчатки, полученных из образца, и (d) подтверждения морфологии полученных первичных клеток сетчатки или использования первичных клеток сетчатки с подтвержденной для создания диссоциированной суспензии клеток и скоплений клеток.
[005] В некоторых вариантах осуществления способов согласно настоящему описанию ткань сетчатки человека получают из одного или пары глазных яблок человека. В некоторых вариантах осуществления способов согласно изобретению глазное яблоко(и) имеет нормальную морфологию, включая интактные глазные яблоки, прозрачную роговицу и/или нормальную форму. В некоторых вариантах осуществления фетальное глазное яблоко (содержащее ткань сетчатки человека) хранят в среде RPMI-1640 с L-глутамином и хранят во льду сразу после изъятия органов у донора. В любом из этих способов сохраненную ткань сетчатки человека доставляют и используют в течение определенного периода времени после изъятия. В различных вариантах осуществления ткань сетчатки человека транспортируют во льду и доставляют в пределах окна транспортировки. В качестве неограничивающего примера окно транспортировки может составлять от приблизительно 1 до приблизительно 26 или более часов (например, 1, 1,5, 2, 2,5, 3, 3,5, 4, 4,5, 5, 5,5, 6, 6,5, 7, 7,5, 8, 8,5, 9, 9,5, 10, 10,5, 11, 11,5, 12, 12,5, 13, 13,5, 14, 14,5, 15, 15,5, 16, 16,5, 17, 17,5, 18, 18,5, 19, 19,5, 20, 20,5, 21, 21,5, 22, 22,5, 23, 23,5, 24, 24,5, 25, 25,5 или 26 часов), например от приблизительно 4,5 до приблизительно 21,5 часов (например, 1, 1,5, 2, 2,5, 3, 3,5, 4, 4,5, 5, 5,5, 6, 6,5, 7, 7,5, 8, 8,5, 9, 9,5, 10, 10,5, 11, 11,5, 12, 12,5, 13, 13,5, 14, 14,5, 15, 15,5, 16, 16,5, 17, 17,5, 18, 18,5, 19, 19,5, 20, 20,5, 21 или 21,5) или от приблизительно 7 до приблизительно 26 часов (например, 7, 7,5, 8, 8,5, 9, 9,5, 10, 10,5, 11, 11,5, 12, 12,5, 13, 13,5, 14, 14,5, 15, 15,5, 16, 16,5, 17, 17,5, 18, 18,5, 19, 19,5, 20, 20,5, 21, 21,5, 22, 22,5, 23, 23,5, 24, 24,5, 25, 25,5 или 26 часов).
[006] В некоторых вариантах осуществления способов согласно изобретению обработка полученного образца в этапе (а) включает: (i) после изъятия органов, извлечение глазного яблока (яблок) из среды RPMI-1640 и промывку от 1 до 5 раз (например, 1 , 2, 3, 4 или 5 раз) охлажденным во льду фосфатно-солевым буфером (PBS) с добавкой антибиотиков, (ii) удаление зрительного нерва и мезенхимальной ткани из глазного яблока для удаления всех экстраокулярных клеток, (iii) промывку глазного яблока охлажденным льдом PBS с добавкой антибиотиков, (iv) прокол глазного яблока по краю роговицы с помощью иглы, (v) круговой разрез по краю роговицы микрохирургическими ножницами, (vi) удаление хрусталика, роговицы и ассоциированного стекловидного тела, (vii) отделение сетчатки от слоя пигментного эпителия сетчатки (ПЭС) с получением отделенной сетчатки, (viii) помещение отделенной сетчатки в чашку Петри, содержащую охлажденную льдом среду или PBS с добавкой антибиотика.
[007] В некоторых вариантах осуществления способов согласно настоящему изобретению механическая диссоциация на этапе (b) включает механическую диссоциацию сетчатки(ок), полученной в этапе (а), путем: (i) переноса сетчатки в коническую пробирку, (ii) механическую диссоциацию сетчатки(ок) с получением диссоциированных сетчаток, (iii) промывки чашки Петри бессывороточной средой с добавкой антибиотика и переноса среды, содержащей любые остаточные диссоциированные фрагменты сетчатки, в коническую пробирку, содержащую диссоциированную сетчатку(ки), (iv) осаждения диссоциированной сетчатки(ок) с помощью центрифугирования и (v) удаления супернатанта. В некоторых вариантах осуществления механическую диссоциацию сетчатки проводят путем ресуспендирования стерильной пипеткой. В некоторых вариантах осуществления диссоциированную сетчатку осаждают с помощью центрифугирования при температуре от приблизительно 10 до приблизительно 1000×g в течение периода от приблизительно 0 до приблизительно 30 минут при температуре от 1 до 50°C.
[008] В некоторых вариантах осуществления способов согласно изобретению этап определения жизнеспособности и количества первичных клеток сетчатки в этапе (c) включает: (i) ресуспендирование осажденной ткани сетчатки, полученной в этапе (b), в охлажденной льдом бессывороточной среде с добавкой антибиотиков, (ii) определение количества и жизнеспособности клеток сетчатки и скоплений клеток сетчатки, полученных в результате механической диссоциации ткани сетчатки, (iii) посев клеток в покрытые фибронектином флаконы или планшеты для культивирования клеток, содержащие бессывороточную среду с добавкой антибиотиков, (iv) инкубирование содержащих клетки сетчатки флаконов или планшетов при температуре от 10 до 50°C. В некоторых вариантах осуществления количество и жизнеспособность клеток определяют с помощью счетчика клеток NC-200. В некоторых вариантах осуществления подсчитанное количество клеток составляет от приблизительно 1 до приблизительно 1000000000 клеток. В некоторых вариантах осуществления процент жизнеспособных подсчитанных клеток составляет от приблизительно 10 до приблизительно 100. В некоторых вариантах осуществления во флаконы или планшеты сеют от приблизительно 1 до приблизительно 1000000000 клеток. В некоторых вариантах осуществления инкубирование флаконов или планшетов, содержащих клетки сетчатки, проводят при 37°C в атмосфере, содержащей от 0 до 30% CO2 и от 0 до 50% O2.
[009] В некоторых вариантах осуществления способов изобретения этап (d) включает подтверждение, что ретинальные клетки, посеянные во флаконы или планшеты для культур клеток, состоят из скоплений ретинальных клеток, состоящих из приблизительно от 1 до приблизительно 100 клеток.
[0010] В некоторых вариантах осуществления способов изобретения антибиотиком, используемым для добавления в PBS или бессывороточную среду, является гентамицин. В некоторых вариантах осуществления антибиотик используется в концентрации от приблизительно 0 до приблизительно 10000 мкг/мл.
[0011] В изобретении предложены способы выделения первичных ретинальных клеток из человеческого образца, включающие: (a) выделение образца сетчатки, включающего множество первичных ретинальных клеток, из человеческого образца, где человеческий образец получен от человека-донора гестационного возраста от приблизительно 12 недель до приблизительно 28 недель, (b) механическую диссоциацию множества первичных ретинальных клеток в ретинальном образце, выделенном в этапе (a), без расщепления множество первичных ретинальных клеток протеазой, с получением в результате выделенной суспензии клеток и скоплений клеток, и (c) определение жизнеспособности, количества и морфологии первичных ретинальных клеток из образца сетчатки, где получают по меньшей мере 30×106 жизнеспособных первичных ретинальных клеток.
[0012] В некоторых вариантах осуществления способов изобретения человеческий образец представляет собой одно или пару человеческих глазных яблок. В некоторых вариантах осуществления глазное яблоко(и) обладает нормальной морфологией, включающей интактное глазное яблоко(и), прозрачную роговицу, нормальную форму или любую комбинацию этого. В некоторых вариантах осуществления человеческий образец помещается в среду для транспортировки культуры клеток после изъятия у человека-донора перед этапом (a). В некоторых вариантах осуществления среда для транспортировки культуры клеток включает RPMI-1640 с L-глутамином или улучшенную DMEM/F12. В некоторых вариантах осуществления среда для транспортировки культуры клеток включает гентамицин в концентрации от приблизительно 0,5 до 50 микрограммов на миллилитр (мл), необязательно среда для транспортировки культуры клеток включает приблизительно 50 микрограммов на миллилитр гентамицина. В некоторых вариантах осуществления человеческий образец хранят приблизительно при 1-8°C непосредственно после помещения в среду для транспортировки культуры клеток, например, помещают в лед.
[0013] В некоторых вариантах осуществления способов изобретения человеческий образец используют в течение от приблизительно 7 до приблизительно 26 часов после изъятия у человека-донора.
[0014] В некоторых вариантах осуществления способов согласно настоящему описанию выделение образца сетчатки из человеческого образца в этапе (а) включает: (i) извлечение одного или пары человеческих глазных яблок из среды для транспортировки культуры, (ii) промывку одного или пары человеческих глазных яблок фосфатно-солевым буфером (PBS) с добавкой антибиотика при температуре приблизительно 1-8°C, (iii) удаление зрительного нерва и мезенхимальной ткани из одного или пары человеческих глазных яблок, (iv) промывку одного или пары человеческих глазных яблок PBS с добавкой антибиотика при температуре приблизительно 1-8°C, (v) прокол каждого из одного или пары глазных яблок по краю роговицы с помощью иглы, (vi) круговой разрез по краю роговицы одного или пары человеческих глазных яблок, (vii) удаление хрусталика, роговицы и ассоциированного стекловидного тела из одного или пары человеческих глазных яблок, (viii) отделение сетчатки(ок) от слоя пигментного эпителия сетчатки (ПЭС) с получением отделенной сетчатки или пары отделенных сетчаток, и (ix) помещение отделенной сетчатки или пары отделенных сетчаток при температуре приблизительно 1-8°C в культуральную среду или PBS, где в культуральную среду или PBS добавлен антибиотик. В некоторых вариантах осуществления этап (ii) повторяют 1-5 раз или 3 раза. В некоторых вариантах осуществления в этапе (iii) удаляют некоторое количество или все экстраокулярные клетки.
[0015] В некоторых вариантах осуществления способов изобретения механическая диссоциация множества первичных ретинальных клеток в этапе (b) включает: (i) перенос образца сетчатки в пробирку, (ii) механическую диссоциацию образца сетчатки с получением множества отделенных первичных ретинальных клеток, (iii) осаждение множества отделенных первичных ретинальных клеток с помощью центрифугирования и (iv) удаление супернатанта. В некоторых вариантах осуществления механическую диссоциацию сетчатки выполняют путем суспендирования с помощью стерильной пипетки. В некоторых вариантах осуществления суспендирование выполняют от 2 до 50 раз, от 2 до 10 раз или от 4 до 8 раз. В некоторых вариантах осуществления множество разделенных первичных ретинальных клеток осаждают с помощью центрифугирования приблизительно при 140×g в течение приблизительно 3 минут при 4°C. В некоторых вариантах осуществления способы включают промывку множества отделенных первичных ретинальных клеток культуральной средой или PBS с добавкой антибиотика после этапа (ii) и перед этапом (iii).
[0016] В некоторых вариантах осуществления способов изобретения множество разделенные первичные ретинальные клетки включают одиночные клетки и скопления клеток.
[0017] В некоторых вариантах осуществления способов изобретения определение жизнеспособности, количества и морфологии первичных ретинальных клеток в этапе (c) включает: (i) ресуспендирование осажденных первичных ретинальных клеток из этапа (b) в охлажденной до приблизительно 1-8°C культуральной среде с добавкой антибиотика, (ii) посев множества отделенных ретинальных клеток в один или более флаконов или планшетов с покрытием для культур клеток, содержащих культуральную среду, где в среду для культивирования клеток необязательно добавлен антибиотик, (iii) инкубирование множества отделенных ретинальных клеток при 10-50°C, где инкубирование необязательно проходит при 37°C, и (iv) определение количества и жизнеспособности первичных ретинальных клеток и скоплений ретинальных клеток. В некоторых вариантах осуществления количество и жизнеспособность первичных ретинальных клеток определяют с помощью счетчика клеток NC-200 при использовании метода подсчета агрегированных клеток, гемоцитометра или трипанового синего. В некоторых вариантах осуществления количество жизнеспособных первичных ретинальных клеток составляет от приблизительно 20×106 до приблизительно 1×109 жизнеспособных первичных ретинальных клеток или от приблизительно 73-147×106 жизнеспособных первичных ретинальных клеток. В некоторых вариантах осуществления процент жизнеспособных клеток от подсчитанных клеток составляет от приблизительно 10% до приблизительно 100% или от приблизительно 68% до приблизительно 85%.
[0018] В некоторых вариантах осуществления способов изобретения посев во флаконы или планшеты производят в этапе (ii) с использованием от приблизительно 1 до приблизительно 1000000000 клеток.
[0019] В некоторых вариантах осуществления способов изобретения множество отделенных ретинальных клеток инкубируют при: (1) приблизительно 37°C в атмосфере с содержанием 0-30% CO2 и 0-50% O2; (2) приблизительно 37°C в атмосфере с содержанием CO2 меньше или равным 5% и O2 меньше или равным 20%; или (3) приблизительно 37°C в атмосфере с содержанием CO2 меньше или равным 5% и O2 меньше или равным 3%. В некоторых вариантах осуществления множество отделенных ретинальных клеток инкубируют при 37°C в атмосфере с содержанием CO2 меньше или равным 5% и O2 меньше или равным 3%.
[0020] В некоторых вариантах осуществления способов изобретения определение жизнеспособности, количества и морфологии первичных ретинальных клеток в этапе (c) включает: (i) визуальное исследование множества отделенных ретинальных клеток под микроскопом и (ii) подтверждение, что множество ретинальных клеток, посеянных во флаконы или планшеты для культур клеток, включает группы скоплений ретинальных клеток, состоящие от приблизительно 2 до приблизительно 1000 клеток.
[0021] В некоторых вариантах осуществления способов изобретения бессывороточная среда включает: (a) улучшенную DMEM/F12, (b) добавку N-2, (c) EGF (рекомбинантный эпидермальный фактор роста человека), (d) bFGF (основной фактор роста фибробластов) и/или (e) GlutaMAX I.
[0022] В некоторых вариантах осуществления способов изобретения культуральная среда не содержит сыворотку. В некоторых вариантах осуществления культуральная среда включает полную среду. В некоторых вариантах осуществления среда включает среду Игла в модификации Дульбекко DMEM/F12, улучшенную DMEM/F12, Knockout DMEM/F12, Нейробазальную среду, ReNcell или среду Ultraculture. В некоторых вариантах осуществления культуральная среда включает улучшенную DMEM/F12. В некоторых вариантах осуществления культуральная среда включает добавку N-2 и GlutaMAX-I. В некоторых вариантах осуществления культуральная среда включает B27, B27 XenoFree или Stempro. В некоторых вариантах осуществления культуральная среда включает добавки, поддерживающие выживание или рост клеток. В некоторых вариантах осуществления добавки, поддерживающие выживание или рост клеток, выбраны из группы, состоящей из L-глутамина, рекомбинантного эпидермального фактора роста человека (EGF), основного фактора роста фибробластов (bFGF), других факторов роста и их комбинации. В некоторых вариантах осуществления антибиотик включает гентамицин в концентрации от приблизительно 0,5 до приблизительно 50 мкг/мл, где концентрация гентамицина необязательно составляет приблизительно 30 мкг/мл.
[0023] В изобретении предложен способ культивирования выделенных первичных человеческих ретинальных клеток для получения популяции неиммортализованных человеческих ретинальных клеток-предшественников, включающий: (a) культивирование суспензии выделенных первичных ретинальных клеток в бессывороточной среде в культуральных флаконах или планшетах, покрытых не содержащим ксеногенных компонентов (xeno-free) фибронектином, орнитином, полилизином или ламинином, при стандартных уровнях кислорода в течение приблизительно 4-6 пассажей, (b) последующее культивирование суспензии в бессывороточной среде при низких уровнях кислорода в течение приблизительно 3-6 пассажей, где клетки пассируют при конфлюентности от 40% до 90% и обрабатывают ферментом при каждом пассаже для диссоциации клеток и добавления свежей культуральной среды, и (c) последующую криоконсервацию клеток, с получением в результате популяции неиммортализованных человеческих ретинальных клеток-предшественников.
[0024] В некоторых вариантах осуществления способов изобретения, после последующего культивирования суспензии при низких уровнях кислорода, клеткам позволяют расти без пассирования в течение некоторого периода времени при стандартных уровнях кислорода. В некоторых вариантах осуществления период времени между пассажами составляет 3-5 дней (например, 3, 4 или 5 дней).
[0025] В некоторых вариантах осуществления способов изобретения ферментативный раствор, используемый для разделения клеток, включает трипсин или эквивалент. В некоторых вариантах осуществления клетки разделяют в первом пассаже с использованием ферментативного раствора, включающего трипсин или эквивалент, и ЭДТА в соотношении приблизительно 1:4. В некоторых вариантах осуществления трипсин или эквивалент и ЭДТА присутствуют в соотношении приблизительно 1:3, 1:3,1, 1:3,2, 1:3,3, 1:3,4, 1:3,5, 1:3,6, 1:3,7, 1:3,8, 1:3,9, 1:4,0, 1:4,1, 1:4,2, 1:4,3, 1:4,4, 1:4,5, 1:4,6, 1:4,7, 1:4,8, 1:4,9 или 1:5,0 в первом пассаже. В некоторых вариантах осуществления клетки разделяют в первом пассаже с использованием ферментативного раствора, включающего трипсин или эквивалент, ЭДТА и DPBS в соотношении приблизительно 1:1:3. В некоторых вариантах осуществления трипсин или эквивалент, ЭДТА и DPBS присутствуют в соотношении приблизительно 1:1:2, 1:1:2,1, 1:1:2,2, 1:1:2,3, 1:1:2,4, 1:1:2,5, 1:1:2,6, 1:1:2,7, 1:1:2,8, 1:1:2,9, 1:1:3,0, 1:1:3,1, 1:1:3,2, 1:1:3,3, 1:1:3,4, 1:1:3,5, 1:1:3,6, 1:1:3,7, 1:1:3,8, 1:1:3,9 или 1:1:4,0 в первом пассаже. В некоторых вариантах осуществления клетки разделяют в первом пассаже в течение 6-10 минут приблизительно при 37°C. В некоторых вариантах осуществления клетки разделяют во втором пассаже с использованием ферментативного раствора, включающего трипсин или эквивалент, ЭДТА и DPBS в соотношении приблизительно 1:1:3. В некоторых вариантах осуществления трипсин или эквивалент, ЭДТА и DPBS присутствуют в соотношении приблизительно 1:1:2, 1:1:2,1, 1:1:2,2, 1:1:2,3, 1:1:2,4, 1:1:2,5, 1:1:2,6, 1:1:2,7, 1:1:2,8, 1:1:2,9, 1:1:3,0, 1:1:3,1, 1:1:3,2, 1:1:3,3, 1:1:3,4, 1:1:3,5, 1:1:3,6, 1:1:3,7, 1:1:3,8, 1:1:3,9 или 1:1:4,0 во втором пассаже. В некоторых вариантах осуществления клетки разделяют во втором пассаже с использованием ферментативного раствора, включающего трипсин или эквивалент и ЭДТА в соотношении приблизительно 1:1. В некоторых вариантах осуществления, трипсин или эквивалент и ЭДТА присутствуют в соотношении приблизительно 1:0,5, 1:0,6, 1:0,7, 1:0,8, 1:0,9, 1:1, 1:1,1, 1:1,2, 1:1,3, 1:1,4 или 1:1,5 во втором пассаже. В некоторых вариантах осуществления клетки разделяют во втором пассаже в течение 4-8 минут приблизительно при 37°C. В некоторых вариантах осуществления клетки разделяют в третьем пассаже и всех последующих пассажах с использованием ферментативного раствора, включающего трипсин или эквивалент и ЭДТА в соотношении приблизительно 1:1. В некоторых вариантах осуществления трипсин или эквивалент и ЭДТА присутствуют в соотношении приблизительно 1:0,5, 1:0,6, 1:0,7, 1:0,8, 1:0,9, 1:1, 1:1,1, 1:1,2, 1:1,3, 1:1,4 или 1:1,5 в третьем и всех последующих пассажах. В некоторых вариантах осуществления клетки разделяют в третьем и всех последующих пассажах в течение 4-8 минут при 37°C. В некоторых вариантах осуществления трипсин или эквивалент включает TrypLE, например TrypLE Express или TrypLE Select. В некоторых вариантах осуществления диссоциацию останавливают добавлением избытка DMEM или PBS. В некоторых вариантах осуществления количество и жизнеспособность клеток определяют после диссоциации. В некоторых вариантах осуществления количество и жизнеспособность клеток определяют с помощью счетчика клеток NC-200.
[0026] В изобретении предложены способы культивирования выделенных первичных человеческих ретинальных клеток для получения популяции неиммортализованных человеческих ретинальных клеток-предшественников, где способы включают: (а) посев в одной или более культуральных флаконов или планшетов с покрытием, содержащих культуральную среду, в первом пассаже множества первичных ретинальных клеток, полученных способом, описанным в настоящем документе, с получением множества культивируемых ретинальных клеток; (b) посев в одной или более культуральных флаконов или планшетов с покрытием, содержащих культуральную среду, во втором пассаже множества культивируемых ретинальных клеток, полученных в первом пассаже; (c) посев в одну или более культуральных флаконов или планшетов с покрытием, содержащих культуральную среду, в третьей пассаже множества культивируемых ретинальных клеток, полученных во втором пассаже; и (d) криоконсервацию множества культивируемых ретинальных клеток, где одну или более культуральных флаконов или планшетов с покрытием засевают при плотности от приблизительно 1×104 клеток на квадратный сантиметр (см2) до приблизительно 2×106 клеток/см2, плотность посева при первом пассаже больше, чем плотность посева при втором пассаже, и плотность посева во втором пассаже больше, чем плотность посева в третьем пассаже, с получением в результате популяции неиммортализованных человеческих ретинальных клеток-предшественников.
[0027] В некоторых вариантах осуществления способов изобретения способы дополнительно включают посев в одну или более культуральных флаконов или планшетов с покрытием, содержащих культуральную среду, в одном или более последующих пассажах множества культивируемых ретинальных клеток, полученных в непосредственно предшествующем пассаже.
[0028] В некоторых вариантах осуществления способов изобретения культуральные флаконы или планшеты покрыты не содержащим ксеногенных компонентов фибронектином, орнитином, полилизином, ламинином или их комбинацией.
[0029] В некоторых вариантах осуществления способов изобретения множество первичных или культивируемых ретинальных клеток культивируют при: (1) приблизительно 37°C в атмосфере, содержащей 0-30% CO2 и 0-50% O2, (2) приблизительно 37°C в атмосфере с содержанием CO2 меньше или равным 5% и содержанием O2 меньше или равным 20%; или (3) приблизительно 37°C в атмосфере с содержанием CO2 меньше или равным 5% и содержанием O2 меньше или равным 3%. В некоторых вариантах осуществления множество первичных или культивируемых ретинальных клеток культивируют приблизительно при 37°C в атмосфере с содержанием CO2 меньше или равным 5% и содержанием O2 меньше или равным 3%. В некоторых вариантах осуществления период времени между двумя последовательными пассажами составляет 2-8 дней, 3-6 дней, 4-5 дней или 3-4 дня. В некоторых вариантах осуществления период времени между двумя последовательными пассажами составляет 3-4 дня.
[0030] В некоторых вариантах осуществления способов согласно изобретению множество первичных ретинальных клеток разделяют в первом пассаже с использованием первого ферментативного раствора, содержащего: (1) трипсин или его эквивалент и этилендиаминтетрауксусную кислоту (ЭДТА), или (2) трипсин или эквивалент, ЭДТА и DPBS. В некоторых вариантах осуществления эквивалентом трипсина является TrypLE. В некоторых вариантах осуществления (1) TrypLE и ЭДТА присутствуют в соотношении 1:4 в первом ферментативном растворе или (2) TrypLE, ЭДТА и DPBS присутствуют в соотношении 1:1:3. В некоторых вариантах осуществления множество первичных ретинальных клеток разделяют в течение приблизительно 5-20 минут, приблизительно 6-10 минут или приблизительно 7-8 минут, приблизительно при 37°C. В некоторых вариантах осуществления множество первичных ретинальных клеток разделяют в течение приблизительно 7-8 минут, приблизительно при 37°C.
[0031] В некоторых вариантах осуществления способов изобретения множество культивируемых ретинальных клеток разделяют во втором пассаже с использованием второго ферментативного раствора, включающего: (1) трипсин или эквивалент, ЭДТА и DPBS, или (2) трипсин или эквивалент и DPBS. В некоторых вариантах осуществления эквивалентом трипсина является TrypLE. В некоторых вариантах осуществления (1) TrypLE, ЭДТА и DPBS присутствуют в соотношении 1:1:3 во втором ферментативном растворе, или (2) TrypLE и DPBS присутствуют в отношении 1:1 во втором ферментативном растворе. В некоторых вариантах осуществления множество культивируемых ретинальных клеток разделяют в течение приблизительно 5-20 минут, приблизительно 6-10 минут или приблизительно 7-8 минут, приблизительно при 37°C. В некоторых вариантах осуществления множество культивируемых ретинальных клеток разделяют в течение приблизительно 5-6 минут приблизительно при 37°C.
[0032] В некоторых вариантах осуществления способов изобретения множество культивируемых ретинальных клеток разделяют по меньшей мере в третьем или последующем пассаже с использованием третьего ферментативного раствора, включающего трипсин или эквивалент и DPBS. В некоторых вариантах осуществления эквивалент трипсина включает TrypLE. В некоторых вариантах осуществления TrypLE и DPBS присутствуют в соотношении 1:1 в третьем ферментативном растворе. В некоторых вариантах осуществления множество культивируемых ретинальных клеток разделяют в течение приблизительно 5-10 минут или приблизительно 5-7 минут приблизительно при 37°C по меньшей мере в третьем или последующем пассаже. В некоторых вариантах осуществления по меньшей мере третий или последующий пассаж включает 3-5 пассажей.
[0033] В некоторых вариантах осуществления способов изобретения способы включают определение количества и жизнеспособности клеток после разделения множества культивируемых ретинальных клеток после второго пассажа. В некоторых вариантах осуществления по меньшей мере 50%, по меньшей мере 60%, по меньшей мере 70%, по меньшей мере 80% или по меньшей мере 90% клеток являются жизнеспособными.
[0034] В некоторых вариантах осуществления способов изобретения c клетки сеют в культуральные флаконы или планшеты при плотности от приблизительно 0,5×106 до приблизительно 3,0×106 клеток/см2 в первом пассаже, от приблизительно 0,1×106 до приблизительно 0,5×106 клеток/см2 во втором пассаже, от приблизительно 0,03×106 до приблизительно 0,2×106 клеток/см2 в третьем пассаже и от приблизительно 10000 до приблизительно 60000 клеток/см2 в четвертом и последующих пассажах.
[0035] В изобретении предложены способы криоконсервации ретинальных клеток-предшественников, полученных с применением способов изобретения, включающие: (i) ферментативное разделение клеток с использованием трипсина, (ii) остановку диссоциации избытком культуральной среды или улучшенной DMEM/F12, (iii) центрифунгирование клеток с ускорением от 10×g до 10000×g в течение 1-30 минут, (iv) ресуспендирование клеток в культуральной среде и определение общего количества и жизнеспособности клеток, (v) добавление среды для криоконсервации с получением конечной концентрации диметилсульфоксида (ДМСО) от 5 до 30%, (vi) деление множества клеток на аликвоты в каждый криофлакон, (vii) замораживание каждого флакона при использовании программируемого криозамораживателя (CRF) и (viii) помещение каждого флакона с клетками в жидкий N2.
[0036] В некоторых вариантах осуществления способов изобретения этап криоконсервации выполняют путем: (a) ферментативного разделения клеток при использовании 1:1 трипсина или эквивалента и DPBS, (b) остановки диссоциации избытком DMEM или PBS, (c) осаждения клеток с помощью центрифугирования при 10-10000 g в течение 1-30 минут, (d) ресуспендирования клеток в бессывороточной среде и определения общего количества и жизнеспособности клеток, (e) добавления среды для криоконсервации с получением конечной концентрации ДМСО от 5 до 30%, (f) деление клеток на аликвоты по 0,2-100×106 клеток в каждый криофлакон, (g) замораживания каждого флакона при -80°C в течение 6-72 часов и (h) помещения каждого флакона с клетками в жидкий N2.
[0037] В некоторых вариантах осуществления способов криоконсервации согласно изобретению эквивалент трипсина в этапе (i) включает TrypLE. В некоторых вариантах осуществления среда для криоконсервации включает культуральную среду и 10% ДМСО. В некоторых вариантах осуществления множество клеток в этапе (vi) составляет от приблизительно 0,5×106 до 50×106 клеток на криофлакон или от приблизительно 0,5×106 до приблизительно 20×106 клеток на мл культуральной среды и ДМСО.
[0038] В некоторых вариантах осуществления способов изобретения клетки и/или скопления клеток культивируют вместе с добавками, которые поддерживают выживание или рост клеток. В некоторых вариантах осуществления добавки, которые поддерживают выживание или рост клеток, выбраны из группы, состоящей из L-глутамина, человеческих рекомбинантных факторов роста, состоящих из EGF и bFGF (Invitrogen) и других факторов роста.
[0039] В альтернативных вариантах осуществления предложены фармацевтические композиции, включающие ретинальную клетку-предшественника или популяцию или множество неиммортализованных человеческих ретинальных клеток-предшественников, выделенных способом согласно любому из предыдущих пунктов, и необязательно также включающие фармацевтически приемлемое вспомогательное вещество.
[0040] В альтернативных вариантах осуществления в настоящем документе предложены наборы, включающие ретинальную клетку-предшественника или популяцию или множество неиммортализованных человеческих ретинальных клеток-предшественников, выделенных способом согласно любому из предыдущих пунктов.
[0041] В альтернативных вариантах осуществления предложены способы лечения, уменьшения тяжести или предупреждения заболевания или патологии сетчатки, улучшения фотопического (дневного) зрения, улучшения коррекции остроты зрения, улучшения функции желтого пятна, улучшения поля зрения или улучшения скотопического (ночного) зрения, включающие: (a) введение или уже выполненное введение нуждающемуся в этом индивиду ретинальной клетки-предшественника или популяции или множества неиммортализованных человеческих ретинальных клеток-предшественников, выделенных способом согласно любому из предыдущих пунктов; или (b) (i) получение или использование уже полученной ретинальной клетки-предшественника или популяции или множества неиммортализованных человеческих ретинальных клеток-предшественников, выделенных способом согласно любому из предыдущих пунктов; и (ii) введение или уже выполненное введение ретинальной клетки-предшественника или популяции или множества неиммортализованных человеческих ретинальных клеток-предшественников нуждающемуся в этом индивиду.
[0042] В альтернативных вариантах осуществления предложены применения ретинальной клетки-предшественника или популяции или множества неиммортализованных человеческих ретинальных клеток-предшественников, выделенных способом согласно любому из предыдущих пунктов, при производстве лекарственного средства для лечения, уменьшения тяжести или предупреждения заболевания или патологии сетчатки, улучшения фотопического (дневного) зрения, улучшения коррекции остроты зрения, улучшения функции желтого пятна, улучшения поля зрения или улучшения скотопического (ночного) зрения.
[0043] В альтернативных вариантах осуществления предложены ретинальные клетки-предшественники или популяция или множество неиммортализованных человеческих ретинальных клеток-предшественников, выделенные способом согласно любому из предыдущих пунктов, для применения при лечении, уменьшении тяжести или предупреждении заболевания или патологии сетчатки, улучшении фотопического (дневного) зрения, улучшении коррекции остроты зрения, улучшении функции желтого пятна, улучшении поля зрения или улучшении скотопического (ночного) зрения.
[0044] Любой из представленных выше аспектов можно комбинировать с любым другим аспектом настоящего изобретения.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[0045] ФИГ. 1 представляет собой линейную диаграмму, на которой показано среднее количество ретинальных клеток-предшественников при каждом пассаже. Ретинальные клетки-предшественники выделяли из образцов глазного яблока с использованием протокола A или протокола B и обрабатывали либо в тот же день (7 часов, 8 часов), либо после транспортировки в течение ночи (24 часа). P означает номер пассажа; d означает номер дня. Точки данных представляют собой теоретический расчет среднего количества всех ретинальных клеток-предшественников, выделенных с использованием одного и того же протокола и культивируемых в одинаковых условиях.
[0046] ФИГ. 2 является таблицей, описывающей условия эксперимента и условия пассажа с использованием Протокола B и сравнивающей их с предыдущим способом культивирования (Протокол A). P означает номер пассажа; d означает номер дня; T означает TrypLE Select (Invitrogen); E означает ЭДТА (Invitrogen); P означает фосфатно-солевой буферный раствор по Дульбекко или DPBS (Invitrogen).
ПОДРОБНОЕ ОПИСАНИЕ
[0047] При транспортировке фетальных глазных яблок (и ассоциированной ткани сетчатки) во льду на большие расстояния время транспортировки может быть довольно значительным. В течение этого времени ткань сетчатки становится все более хрупкой, при этом потенциальная жизнеспособность формирующих ее клеток постепенно снижается. Это создает проблему для производства клеток, когда ткань необходимо получать из удаленной точки, поскольку на получение конечного продукта (в течение любого установленного времени в культуре) влияет количество жизнеспособных клеток, полученных из каждой сетчатки. Однако преимуществом повышенной хрупкости ткани можно воспользоваться и исключить некоторые этапы, которые в ином случае использовались бы для выделения клеток сетчатки. В частности, можно исключить использование трипсина для разрушения ткани сетчатки, так как ткань можно разрушить всего лишь при осторожном суспендировании. Такую операцию легче выполнить, и она сокращает время, затрачиваемое от получения ткани до помещения в инкубатор. Кроме того, использование ЭДТА во время первичного пассирования также снижает нагрузку на клетки в этот критический период при их восстановлении в культуре. При разделении сетчатки на более мелкие фрагменты в ходе последовательных пассажей без попыток разделить их на отдельные клетки на более поздних этапах процесса, жизнеспособность повышается еще больше, и выполнение процесса становится менее рискованным. По мере повышения жизнеспособности клеток трипсин можно систематически вводить в процесс пассирования без отрицательного влияния на выход.
[0048] В частности, если исходная ткань подвергается значительно более длительному времени транспортировки, чем это было ранее, это может отрицательно влиять на ожидаемый выход клеток. Тогда как непосредственно бороться с изменениями в ткани может быть сложно, протокол выделения и раннего культивирования клеток может быть изменен, чтобы устранить источники потери клеток и, таким образом, повысить конечный выход.
[0049] Способы выделения ретинальных клеток, описанные в настоящем документе, обладают множеством преимуществ по сравнению с предыдущими способами, в которых существует длительный временной интервал между получением ткани и началом культивирования ткани. Способы, описанные в настоящем документе, обладают преимуществами, которые включают, без ограничения перечисленным: (1) улучшенный выход, (2) простоту выполнения, поскольку исключается ферментативная стадия, (3) более низкий риск лизиса клеток с выходом ДНК и связанной с этим потерей клеток, (4) более быстрый процесс от выделения ткани до инкубатора и (5) повышение жизнеспособности клеток во время раннего пассирования.
Определения
[0050] Для облегчения понимания данного описания ниже определен ряд терминов. Терминология в настоящем документе используется для описания конкретных вариантов осуществления изобретения, описанного в настоящем документе, но при этом ее использование не ограничивает изобретение, за исключением представленного в формуле изобретения.
[0051] Любой из аспектов и вариантов осуществления, описанных в настоящем документе, можно комбинировать с любым другим аспектом или вариантом осуществления, как раскрыто в настоящем документе.
[0052] Если не определено иное, все технические и научные термины, используемые в настоящем документе, имеют такое же значение, которое обычно известно среднему специалисту в области, к которой относится изобретение. Хотя другие исследования, композиции, способы и наборы, подобные или эквивалентные описанным в настоящем документе, могут применяться при практической реализации настоящего изобретения, в настоящем документе описаны примерные материалы и способы. Следует понимать, что терминология, используемая в настоящем документе, предназначена исключительно для описания конкретных аспектов и не служит для ограничения.
[0053] В настоящем описании "включает", "включающий", "содержащий", "имеющий" и т.п. могут иметь значение в соответствии с Патентным правом США и могут означать "включает", "включающий" и т.п.; термины "состоящий по существу из" или "состоит по существу" также имеют значение в соответствии с Патентным правом США, причем эти термины являются открытыми, допуская присутствие большего, чем было указано, при условии, что основные или новые свойства того, что было указано, не изменяются из-за присутствия большего, чем то, что было указано, но исключают варианты осуществления из предшествующего уровня техники.
[0054] Если прямо не указано или не очевидно из контекста, следует понимать, что при использовании в настоящем документе термины "a", "an" и "the" включают единственное или множественное число.
[0055] Если прямо не указано или не очевидно из контекста, следует понимать, что термин "или" при использовании в настоящем документе является включительным.
[0056] При использовании в настоящем документе в других контекстах термин "приблизительно", если не указано иное, относится к указанному значению, например количеству, дозе, температуре, времени, проценту и т.д., +/-10%, +/-9%, +/-8%, +/-7%, +/-6%, +/-5%, +/-4%, +/-3%, +/-2% или +/-1%.
[0057] При использовании в настоящем документе термины "пациент" или "субъект" и т.п. попеременно используются в настоящем документе для обозначения любого млекопитающего, включая людей, домашних животных и сельскохозяйственных животных, а также зоопарковых, спортивных и домашних животных, таких как собаки, лошади, кошки и животные для использования в сельском хозяйстве, в том числе рогатый скот, овцы, свиньи и козы. Одним из примеров млекопитающего является человек, включая взрослых, детей и пожилых лиц. Субъектом также может быть домашнее животное, включая собак, кошек и лошадей. Примеры сельскохозяйственных животных включают рогатый скот и коз.
[0058] Термины "лечить", "лечение" и т.п. при использовании в настоящем документе, если не указано иное, относятся к лечению, регрессии, ослаблению, облегчению, минимизации, ингибированию процесса, подавлению, остановке и/или предотвращению заболевания, нарушения или состояния, к которым применяется такой термин, или одного или более (то есть не обязательно всех) симптомов такого заболевания, нарушения или состояния, и включает введение любой из композиций, фармацевтических композиций или лекарственных форм, описанных в настоящем документе, для предотвращения появления симптомов или осложнений, облегчения симптомов или осложнений, замедления прогрессирования и/или устранения заболевания, состояния или нарушения. В альтернативных вариантах осуществления лечение обеспечивает излечение или улучшение состояния.
[0059] При использовании в настоящем документе "предупреждение" или "профилактика" означает полное или частичное предотвращение или облегчение, или контроль, или уменьшение или остановку продукции или возникновения состояния или события, например, заболевания, нарушения или состояния, которое нужно предотвратить.
[0060] При использовании в настоящем документе термины "очищенный" или "обогащенный" и т.п. означают, что клетки или популяции клеток удалены из их нормального тканевого окружения и присутствуют в более высокой концентрации по сравнению с нормальным тканевым окружением. Таким образом, "очищенная" или "обогащенная" популяция клеток может дополнительно включать типы клеток в дополнение к ретинальным клеткам-предшественникам и может включать дополнительные тканевые компоненты, при этом термин "очищенный" или "обогащенный" не указывает обязательно на присутствие только клеток-предшественников или исключает присутствие других типов клеток.
[0061] В некоторых вариантах осуществления популяции ретинальных клеток-предшественников, как раскрыто в настоящем документе, могут быть по меньшей мере на 5% чистыми, по меньшей мере на 10% чистыми, по меньшей мере на 15% чистыми, по меньшей мере на 20% чистыми, по меньшей мере на 25% чистыми, по меньшей мере на 30% чистыми, по меньшей мере на 35% чистыми, по меньшей мере на 40% чистыми, по меньшей мере на 45% чистыми, по меньшей мере на 50% чистыми, по меньшей мере на 55% чистыми, по меньшей мере на 60% чистыми, по меньшей мере на 65% чистыми, по меньшей мере на 70% чистыми, по меньшей мере на 75% чистыми, по меньшей мере на 80% чистыми, по меньшей мере на 85% чистыми, по меньшей мере на 90% чистыми, по меньшей мере на 95% чистыми, по меньшей мере на 96% чистыми, по меньшей мере на 97% чистыми, по меньшей мере на 98% чистыми, по меньшей мере на 99% чистыми или чистыми на любое приращение между 5% и 99% (например, 5%, 6%, 7%, 8%, 9%, 10%, 11%, 12%, 13%, 14%, 15%, 16%, 17%, 18%, 19%, 20%, 21%, 22%, 23%, 24%, 25%, 26%, 27%, 28%, 29%, 30%, 31%, 32%, 33%, 34%, 35%, 36%, 37%, 38%, 39%, 40%, 41%, 42%, 43%, 44%, 45%, 46%, 47%, 48%, 49%, 50%, 51%, 52%, 53%, 54%, 55%, 56%, 57%, 58%, 59%, 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% ретинальных клеток-предшественников).
[0062] "Маркер" относится к любой молекуле, которую можно наблюдать или обнаруживать. Например, маркер может включать, без ограничения, нуклеиновую кислоту, такую как транскрипт определенного гена, полипептидный продукт гена, не являющийся продуктом гена полипептид, гликопротеин, углевод, гликолипид, липид, липопротеин или малую молекулу (например, молекулы, имеющие молекулярную массу меньше 10000 дальтон). В альтернативных вариантах осуществления ретинальные клетки-предшественники могут характеризоваться присутствием одного или нескольких маркеров, которые могут экспрессироваться на поверхности клеток в популяции клеток ("маркер клеточной поверхности"), внутри клеток в популяции клеток (т.е. в ядре или цитоплазме клетки) и/или экспрессироваться на уровне РНК или белка в качестве "генетического" маркера.
[0063] Термины "экспрессировать" и "экспрессия" при использовании в настоящем документе относятся к транскрипции и/или трансляции последовательности нуклеиновой кислоты в клетке-хозяине. Уровень экспрессии представляющего интерес требуемого продукта/белка, например маркера, в клетке-хозяине может быть определен или подвергнут "скринингу" либо на основе количества соответствующей мРНК, которая присутствует в клетке, либо количества представляющего интерес требуемого полипептида/белка, кодируемого выбранной последовательностью, как в настоящих примерах. Например, мРНК, транскрибируемая с выбранной последовательности, может быть количественно определена или обнаружена с помощью Нозерн-блот-гибридизации, защиты РНК от действия рибонуклеаз, гибридизации in situ с клеточной РНК, анализа на микроматрицах или с помощью полимеразной цепной реакции с обратной транскрипцией (ОТ-ПЦР). Белки, кодируемые выбранной последовательностью, могут быть обнаружены или определены количественно с помощью различных методов на основе антител, например, метода ИФА, вестерн-блоттинга, радиоиммуноанализа, иммунопреципитации, анализа биологической активности белка, иммуноокрашивания белка (включая, например, иммуногистохимию и иммуноцитохимию), проточной цитометрии или сортировки клеток с активированной флуоресценцией ("FACS") или с помощью гомогенного флуоресцентного анализа с временным разрешением (HTRF).
Ретинальные клетки-предшественники (RPC)
[0064] Выделение, анализ и применение ретинальных клеток-предшественников млекопитающих подробно описаны в заявке WO2012/158910, содержание которой включено в настоящий документ посредством отсылки во всей полноте.
[0065] При эмбриональном развитии позвоночных сетчатка и зрительный нерв формируются в виде отростков развивающегося мозга, поэтому сетчатка считается частью центральной нервной системы (ЦНС) и фактически является мозговой тканью. Сетчатка представляет собой слоистую структуру с несколькими слоями нейронов, соединенных синапсами. От ближайшего к самому дальнему от стекловидного тела, т.е. от ближайшего к передней части головы по направлению к внутренней и задней части головы, слои сетчатки включают: (1) внутреннюю ограничивающую мембрану, включающую подошвы клеток Мюллера, (2) слой нервных волокон, содержащий аксоны ядер ганглионарных клеток, (3) слой ганглионарных клеток, содержащий ядра ганглионарных клеток, аксоны которых становятся волокном зрительного нерва, (4) внутренний сплетениевидный слой, который содержит синапсы между аксонами биполярных клеток и дендритами ганглионарных и амакриновых клеток, (5) внутренний ядерный слой, который содержит ядра и окружающие клеточные тела (перикарионы) биполярных клеток, (6) внешний сплетениевидный слой, содержащий проекции палочек и колбочек, заканчивающиеся сферулой палочки и ножкой колбочки, соответственно, (7) внешний ядерный слой, который содержит тела клеток палочек и колбочек, (8) внешнюю ограничивающую мембрану, которая отделяет части внутренних сегментов фоторецепторов от их клеточного ядра, (9) слой фоторецепторов и (10) пигментный эпителий сетчатки (ПЭС), который представляет собой один слой гексагональных клеток. Нейроны, которые непосредственно чувствительны к свету, представляют собой фоторецепторные клетки, состоящие в основном из двух типов: палочек и колбочек. Палочки функционируют в основном при слабом освещении и обеспечивают черно-белое зрение, а колбочки поддерживают дневное зрение и восприятие цвета. Третий тип фоторецепторов, светочувствительная ганглионарная клетка, важен для рефлексных реакций на яркий дневной свет.
[0066] Донорские фетальные ретинальные клетки (например, ретинальные клетки-предшественники, описанные в настоящем документе) могут оказывать трофическое влияние на сетчатку реципиента, особенно включая колбочки реципиента. Этот трофический эффект является не только нейропротекторным, но также оказывает быстрое восстанавливающее действие на оставшиеся клетки сетчатки реципиента, что определяется улучшением зрительной функции. Донорские клетки способны интегрироваться в сетчатку и, посредством клеточной дифференцировки, заменять фоторецепторы (которые могут присутствовать в ограниченном количестве). Общий эффект заключается в быстром и устойчивом восстановлении и сохранении клинически значимой степени зрительной функции сетчатки, которая в ином случае неизбежно будет утеряна, в результате чего пациент полностью ослепнет. Таким образом, любые из композиций и способов, описанных в настоящем документе, могут применяться для быстрого и устойчивого восстановления и сохранения клинически значимой степени зрительной функции сетчатки у млекопитающего, например человека. Например, любые из композиций и способов, описанных в настоящем документе, могут оказывать клинически значимое трофическое влияние на поврежденную сетчатку или оказывать регенеративное влияние на макулярную и/или скотопическую зрительную функцию.
[0067] Клетки в композициях и популяциях, описанных в настоящем документе, представляют собой популяцию близко родственных клеток, а не выделенный один тип клеток.
[0068] Хотя эти клетки, по сути, не являются стволовыми клетками (потому что они не соответствуют определению для истинных стволовых клеток), они являются незрелыми и/или пластичными. Однако такие клетки не могут (без дополнительной манипуляции) приводить к образованию зародышевого слоя и/или не могут (без дополнительной манипуляции) приводить к образованию всех трех (3) зародышевых слоев.
[0069] Кроме того, эти клетки запрограммированы к образованию ткани или клеток сетчатки. Таким образом, эти клетки могут экспрессировать прогениторные маркеры и ретинальные маркеры.
[0070] Ретинальные клетки-предшественники не плюрипотентные и могут оказаться мультипотентными. Однако, поскольку клетки никогда не культивировали в плюрипотентном состоянии, они более безопасные. Хотя в некоторых вариантах осуществления фетальные ретинальные клетки или клетки RPC млекопитающих могут быть получены искусственно из плюрипотентных клеточных линий, они необязательно не содержат популяцию остаточных плюрипотентных типов клеток.
[0071] Клетки, описанные в настоящем документе, являются ретинальными клетками-предшественниками (RPC), которые можно отличить от нервных прогениторных и/или нервных стволовых клеток (NSC). В частности, такие фетальные ретинальные клетки или клетки RPC млекопитающих являются мультипотентными, но не эквивалентны NSC. Например, фетальные ретинальные клетки или клетки RPC млекопитающих происходят не из головного мозга, а из сетчатки глаза. Кроме того, из фетальных ретинальных клеток или клеток RPC млекопитающих образуются фоторецепторы, тогда как из прогениторных клеток головного мозга фоторецепторы формируются плохо. Аналогичным образом, в отличие от NSC, фетальные ретинальные клетки или клетки RPC млекопитающих являются мультипотентными, но из них не образуются (без дополнительной манипуляции) олигодендроциты. Например, из фетальных ретинальных клеток или клеток RPC млекопитающих образуются (в ходе дифференцировки) ретинальные клетки, включая фоторецепторы, но не образуются олигодендроциты.
[0072] Фетальные ретинальные клетки или клетки RPC млекопитающих получают (или могут быть получены) из фетальной нервной сетчатки млекопитающего, не из реснитчатого края, реснитчатого эпителия или ПЭС. Кроме того, фетальные ретинальные клетки или клетки RPC млекопитающих не развиваются из дифференцированных глиальных клеток Мюллера и, по сути, не являются постмитотическими предшественниками, не являются стволовыми клетками и/или не являются ни одним выделенным типом клеток.
[0073] Фетальные ретинальные клетки или клетки RPC млекопитающих не были обнаружены у эмбриона на ранней стадии развития (например, в бластоцисте). Кроме того, фетальные ретинальные клетки или клетки RPC млекопитающих не обнаружены в каком бы то ни было полезном количестве у нормального зрелого млекопитающего (например, человека).
[0074] Кроме того, ретинальные клетки-предшественники не персистируют в течение всей жизни организма. Однако такие фетальные ретинальные клетки или клетки RPC млекопитающих обнаружены в своей нативной численности в развивающейся (фетальной) сетчатке млекопитающего (например, человека).
[0075] Хотя фетальные ретинальные клетки или RPC млекопитающих являются в основном митотическими при культивировании в условиях пролиферации, малые количества постмитотических клеток также могут быть включены в любую из композиций и популяций, описанных в настоящем документе.
[0076] Фетальные ретинальные клетки или клетки RPC млекопитающих являются иммунологически переносимыми в качестве глазных аллотрансплантатов у неродственных млекопитающих, например, человека. Таким образом, RPC имеют низкую иммуногенность при введении в глаз. В качестве неограничивающего примера такие фетальные ретинальные клетки или клетки RPC млекопитающих можно трансплантировать в полость стекловидного тела или в субретинальное пространство млекопитающего или человека, для лечебной и/или профилактической терапии зрения или болезней сетчатки.
[0077] В альтернативных вариантах осуществления фетальные ретинальные клетки или клетки RPC млекопитающих не связаны с риском (или существенным риском) образования опухоли или другого нежелательного роста клеток.
[0078] Фетальные ретинальные клетки или клетки RPC млекопитающих можно культивировать в виде сфер или адгерентных монослоев, или в виде сфер и затем монослоев, и/или в виде комбинации сфер и монослоев. Однако сферы не требуются, и в некоторых вариантах осуществления клетки пересаживают в виде разделенных клеток, а не в виде сфер, или в виде смеси разделенных клеток и сфер. Фетальные ретинальные клетки или клетки RPC млекопитающих содержат пересаженные клетки, которые сливаются в стекловидном теле и, необязательно, могут становиться сферами.
[0079] В альтернативных вариантах осуществления ретинальные клетки-предшественники и содержащие их популяции клеток не являются бессмертными, причем они не могут быть иммортализованы или принудительно иммортализованы. Хотя клетки не пролиферируют неограниченно, типичные способы культивирования клеток, описанные в данном документе, могут увеличивать скорость и длительность пролиферации и/или могут значительно повышать выход донорских клеток для донорства данной ткани. При использовании в настоящем документе "иммортализованная" клеточная линия является клеточной линией, которая может делиться бесконечно долго, тогда как "неиммортализованная" клеточная линия способна делиться в течение ограниченного количества пассажей. Например, неиммортализованные ретинальные клетки-предшественники могут делиться в течение 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 25, 30 или более пассажей.
[0080] RPC могут быть генетически немодифицированными клетками или они могут быть генетически модифицированы (например, стабильно, транзиентно или индуцируемо трансформированы) с использованием любого способа(ов), известного в уровне техники. Например, ретинальные клетки-предшественники могут быть генетически модифицированы для экспрессии одной или более гетерологичных или экзогенных последовательностей нуклеиновых кислот, представляющих интерес. Последовательность нуклеиновой кислоты может быть "экзогенной", что означает, что она является чужеродной по отношению к клетке, в которую вводят вектор, или что последовательность гомологична последовательности в клетке, но находится в положении внутри нуклеиновой кислоты клетки-хозяина, в котором такая последовательность обычно не присуствует. Последовательности нуклеиновых кислот включают плазмиды, ампликоны, кДНК, мРНК, антисмысловую РНК, миРНК, но не ограничены этими примерами. Термин "ген" относится к функциональной единице нуклеиновой кислоты, кодирующей белок, полипептид или пептид. Как будет понятно специалистам в данной области, данный функциональный термин включает геномные последовательности, последовательности кДНК и менее крупные сконструированные генные сегменты, которые экспрессируют белки, полипептиды, домены, пептиды, слитые белки и мутанты или могут быть адаптированы для их экспрессии.
[0081] Для генетического изменения клеток может использоваться любая методология, известная в данной области. Одним из примеров метода является вставка гена в клетки ткани с помощью рекомбинантного вирусного вектора. Для введения фрагмента экзогенной нуклеиновой кислоты, кодирующего терапевтическое средство, в клетки-мишени и/или ткань могут использовать любой из различных векторов, таких как вирусные векторы, плазмидные векторы, линейная ДНК и т.д., как известно в данной области. Такие векторы могут вводить, например, с использованием любого метода из инфицирования, трансдукции, трансфекции, трансфекции, опосредованной фосфатом кальция, трансфекции, опосредованной DEAE-декстраном, электропорации, трансфекции, опосредованной липосомами, доставки биологических генов, липосомальной доставки генов при использовании фузогенных и анионных липосом (которые являются альтернативой применению катионных липосом), прямой инъекции, рецептор-опосредованного захвата, магнитопорации, ультразвука и других, известных в данной области.
[0082] При использовании в настоящем документе "вектор" относится к несущей молекуле нуклеиновой кислоты, в которую может быть встроена последовательность нуклеиновой кислоты для введения в клетку, где она может реплицироваться. Векторы включают плазмиды, космиды, вирусы (бактериофаги, вирусы животных и вирусы растений) и искусственные хромосомы (например, YAC). Специалист в данной области будет хорошо осведомлен о конструировании вектора с помощью стандартных рекомбинантных технологий, которые описаны в Sambrook et al. (1989) Molecular Cloning: A Laboratory Manual, Cold Spring Harbor, N.Y.; Ausubel et al. (1987) Current Protocols in Molecular Biology, Greene Publ. Assoc. & Wiley-Intersciences. Помимо кодирования модифицированного полипептида, вектор может кодировать немодифицированные полипептидные последовательности, такие как метку или направляющую молекулу. Подходящие векторы, кодирующие такие слитые белки, включают векторы pIN, векторы, кодирующие полигистидиновую метку, и векторы pGEX для применения в создании растворимых слитых белков глутатион-S-трансферазы (GST) для последующей очистки и разделения или отщепления.
[0083] Векторы могут быть сконструированы в первую очередь для введения в клетки гетерологичной молекулы нуклеиновой кислоты, такой как ген, который "функционально связан" или находится под контролем одной или более контрольных последовательностей. "Промотор" относится к одному или нескольким модулям контроля транскрипции, которые сгруппированы вокруг сайта инициации для РНК-полимеразы II и других белков-активаторов транскрипции. Любая комбинация промотора/энхансера (согласно базе данных эукариотических промоторов EPDB) также может использоваться для направления экспрессии представляющей интерес молекулы нуклеиновой кислоты (т.е. конститутивной, индуцируемой, репрессируемой, тканеспецифической). Также векторы могут содержать селективный маркер для облегчения работы с ними in vitro или ex vivo. Векторы также могут содержать сигнал полиаденилирования, который может быть получен из гена гормона роста человека (hGH), гена гормона роста крупного рогатого скота (BGH) или SV40. Кроме того, векторы могут также содержать участки внутренней посадки рибосомы (IRES), которые используются для создания мультигенных или полицистронных информационных последовательностей. Элементы IRES способны обходить модель сканирования рибосом при трансляции, зависимой от 5-метилированных кэпов, и инициировать трансляцию во внутренних участках (Pelletier, J. and Sonenberg, N. (1988) Nature 334(6180): 320-325). Элементы IRES могут быть связаны с гетерологичными открытыми рамками считывания. Несколько открытых рамок считывания могут транскрибироваться вместе, причем каждая из них разделена IRES с получением полицистронных транскриптов. Благодаря элементу IRES каждая открытая рамка считывания доступна рибосомам для эффективной трансляции. Несколько генов могут быть эффективно экспрессироваться с использованием одного промотора/энхансера для транскрипции одного транскрипта.
[0084] В некоторых вариантах осуществления вектор является вирусным вектором. Вирусные векторы, известные в уровне техники, включают, без ограничения перечисленными, аденовирусные векторы, ретровирусные векторы, векторы на основе вируса осповакцины, векторы на основе аденоассоциированного вируса (AAV), векторы на основе вируса полиомы, альфавирусные векторы, рабдовирусные векторы, лентивирусные векторы, векторы на основе вируса Эпштейна-Барр, пикорнавирусные векторы или герпесвирусные векторы. В таких вариантах осуществления, когда вирусный вектор является AAV вектором, может использоваться любой серотип AAV вектора, известный в данной области. Например, AAV вектор может быть AAV1, AAV2, AAV4, AAV5, AAV8 или AAV9. AAV можно псевдотипировать, смешивая капсидный белок и вирусный геном из разных серотипов вируса (например, инвертированные концевые повторы из одного серотипа AAV и капсид из другого серотипа).
[0085] В других вариантах осуществления последовательность нуклеиновой кислоты может быть заключена в липосомный или липидный состав. Липосомы представляют собой везикулярные структуры, характеризующиеся бислойной фосфолипидной мембраной и внутренней водной средой. Многослойные липосомы содержат несколько липидных слоев, которые разделены водной средой. Они образуются спонтанно при суспендировании фосфолипидов в избытке водного раствора. Липидные компоненты подвергаются самоорганизации с образованием замкнутых структур и захватывают воду и растворенные вещества между липидными бислоями (Ghosh, P. C. and Bachhawat, B. K. (1991) Targeted Diagn. Ther. 4: 87-103). Одним из примеров коммерчески доступных липосом или липидных составов является липофектамин (Invitrogen). Другие примеры включают FuGENE (Promega), PromoFectin (PromoKine), Affectene (Qiagen), Polyfect (Qiagen), Superfect (Qiagen) и TransMessenger (Qiagen).
Выделение первичных ретинальных клеток
[0086] В настоящем документе предложены способы выделения, культивирования и/или применения диссоциированных суспензий эмбриональных ретинальных клеток, например, человеческих первичных ретинальных клеток из образца. В различных вариантах осуществления суспензии эмбриональных ретинальных клеток не включают ткань или каркасы. Также предложены способы выделения и анализа ретинальных клеток-предшественников и композиций, содержащих такие клетки, которые получены из донорской ткани, выращены в культуре и включены в композицию для введения субъекту или пациенту.
[0087] Описанные в настоящем документе способы выделения первичных ретинальных клеток из человеческого образца не требуют применения протеазы для расщепления множества первичных ретинальных клеток, что приводит к большему количеству жизнеспособных первичных ретинальных клеток по сравнению со способом, в котором используется протеаза или комбинация механического разделения и обработки протеазой.
[0088] В одном аспекте изобретения предложен способ выделения первичных ретинальных клеток из человеческого образца, включающий: (a) выделение образца сетчатки, включающего множество первичных ретинальных клеток из человеческого образца, (b) механическое разделение множества первичных ретинальных клеток в образце сетчатки, выделенном в этапе (a), с получением в результате разделенной суспензии клеток и скоплений клеток и (c) определение жизнеспособности, количества, морфологии или их комбинации первичных ретинальных клеток из образца сетчатки. Человеческие образцы выделяют у людей-доноров. Возраст донора может составлять от 17 до приблизительно 20 неделей. В некоторых вариантах осуществления способы выделения первичных ретинальных клеток, описанных в настоящем документе, позволяют получать по меньшей мере 30×106 жизнеспособных первичных ретинальных клеток, которые затем культивируют с получением ретинальных клеток-предшественников.
[0089] В некоторых вариантах осуществления образец является глазом или парой глаз, выделенных от млекопитающего, например мыши, крысы, кролика, кошки, собаки, обезьяны, нечеловеческого примата или человека. В некоторых вариантах осуществления образец получен от сельскохозяйственного животного, например лошади, коровы или овцы.
[0090] Образцы, используемые для выделения и/или культивирования популяций клеток, могут быть забраны у здоровых субъектов (т.е. лиц, не страдающих заболеванием сетчатки), у больных субъектов и могут включать не только популяции свежевыделенных клеток сетчатки, но и замороженные популяции клеток сетчатки. Источники включают, без ограничения, целые глаза или ткани сетчатки или другие источники, полученные из эмбриональных, фетальных, детских или взрослых тканей. Способы, описанные в настоящем документе, могут включать дополнительные процедуры обогащения или очистки или этапы выделения клеток путем положительной селекции на другие маркеры, специфические для клеток-предшественников сетчатки. Ретинальные клетки-предшественники и популяции клеток могут быть получены или забраны у любых видов млекопитающих или субъектов, например человека, примата, лошади, крупного рогатого скота, свиньи, собаки, кошки, хорька, кролика, грызуна, например, мыши, крысы, хомяка и т.д.
[0091] В некоторых вариантах осуществления клетки собирают из фетальной сетчатки млекопитающего на стадии, после которой формируется сетчатка, но до того как внешние фоторецепторные сегменты полностью сформируются в сетчатке и до завершения или существенного завершения васкуляризации сетчатки. Стадии, как правило, располагаются между фетальными гестационными возрастами от приблизительно 12 недель до приблизительно 28 недель (например, приблизительно 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27 или 28 недель) человеческого плода. В некоторых вариантах осуществления стадия может соответствовать гестационному возрасту от 17 недель до приблизительно 20 недель. В случае нечеловеческих клеток более крупных млекопитающих, таких как кошачьи или свиные ретинальные клетки-предшественники, стадии, как правило, располагаются между фетальными гестационными возрастами от приблизительно 3 недель до приблизительно 11 недель (например, приблизительно 3, 4, 5, 6, 7, 8, 9, 10 или 11 недель). См., например, Anand-Apte, B. and Hollyfield, J. G. "Developmental Anatomy of the Retinal and Choroidal Vasculature", The Retina and Its Disorders, Besharse, J. and Bok, D., Academic Press, (2001). Однако клетки могут быть также получены из послеродовой или неонатальной ткани млекопитающего.
[0092] В некоторых вариантах осуществления образец представляет собой человеческий образец. В некоторых вариантах осуществления человеческий образец представляет собой одно или пару глазных яблок человека-донора. В некоторых вариантах осуществления гестационный возраст человека-донора составляет от приблизительно 12 недель до приблизительно 28 недель. В некоторых вариантах осуществления гестационный возраст человека-донора составляет от приблизительно 17 недель до приблизительно 20 недель. В некоторых вариантах осуществления использование более узкого возрастного диапазона доноров улучшает единообразие конечного выхода клеток-предшественников сетчатки во время производства.
[0093] В некоторых вариантах осуществления образец представляет собой одно или пару человеческих фетальных глазных яблок. В некоторых вариантах осуществления глазные яблоки обладают нормальной морфологией. Нормальная морфология может быть определена при визуальном наблюдении на предмет таких особенностей, как интактное глазное яблоко(и), прозрачная роговица, нормальная форма или любая комбинация этих особенностей.
[0094] В некоторых вариантах осуществления человеческую ткань сетчатки могут перевозить во льду и доставлять в окне транспортировки. Окно транспортировки может включать удерживание клеток в пункте назначения или пункте отправления в течение некоторого периода времени, например, во льду или в холодильнике при температуре приблизительно 1-8°C или приблизительно 4°C. В некоторых вариантах осуществления окно транспортировки составляет приблизительно 1-40 часов, приблизительно 7-40 часов, приблизительно 1-34 часа, приблизительно 7-34 часа, приблизительно 1-26 часов, приблизительно 4-26 часов, приблизительно 7-26 часов, приблизительно 8-26 часов, приблизительно 4-18 часов, приблизительно 7-18 часов или приблизительно 8-18 часов. В некоторых вариантах осуществления окно транспортировки составляет приблизительно 1 час, приблизительно 2 часа, приблизительно 2,5 часа, приблизительно 3 часа, приблизительно 3,5 часа, приблизительно 4 часа, приблизительно 4,5 часа, приблизительно 5 часов, приблизительно 5,5 часов, приблизительно 6 часов, приблизительно 6,5 часов, приблизительно 7 часов, приблизительно 7,5 часов, приблизительно 8 часов, приблизительно 8,5 часов, приблизительно 9 часов, приблизительно 10 часов, приблизительно 11 часов, приблизительно 12 часов, приблизительно 13, часы, приблизительно 14 часов, приблизительно 15 часов, приблизительно 16 часов, приблизительно 17 часов, приблизительно 18 часов, приблизительно 19 часов, приблизительно 20 часов, приблизительно 21 час, приблизительно 22 часа, приблизительно 23 часа, приблизительно 24 часа, приблизительно 25 часов или приблизительно 26 часов. В качестве неограничивающего примера окно транспортировки может составлять от приблизительно 1 до приблизительно 26 (например, 1, 1,5, 2, 2,5, 3, 3,5, 4, 4,5, 5, 5,5, 6, 6,5, 7, 7,5, 8, 8,5, 9, 9,5, 10, 10,5, 11, 11,5, 12, 12,5, 13, 13,5, 14, 14,5, 15, 15,5, 16, 16,5, 17, 17,5, 18, 18,5, 19, 19,5, 20, 20,5, 21, 21,5, 22, 22,5, 23, 23,5, 24, 24,5, 25, 25,5 или 26), например, от приблизительно 4,5 до приблизительно 21,5 часов (например, 1, 1,5, 2, 2,5, 3, 3,5, 4, 4,5, 5, 5,5, 6, 6,5, 7, 7,5, 8, 8,5, 9, 9,5, 10, 10,5, 11, 11,5, 12, 12,5, 13, 13,5, 14, 14,5, 15, 15,5, 16, 16,5, 17, 17,5, 18, 18,5, 19, 19,5, 20, 20,5, 21 или 21,5) или от приблизительно 7 до приблизительно 26 часов (например, 7, 7,5, 8, 8,5, 9, 9,5, 10, 10,5, 11, 11,5, 12, 12,5, 13, 13,5, 14, 14,5, 15, 15,5, 16, 16,5, 17, 17,5, 18, 18,5, 19, 19,5, 20, 20,5, 21, 21,5, 22, 22,5, 23, 23,5, 24, 24,5, 25, 25,5 или 26 часов).
[0095] В некоторых вариантах осуществления образец помещают в среду для культивирования клеток млекопитающих после забора у донора. Среды для культивирования клеток млекопитающих, которые могут использоваться во время транспортировки образца, включают как базальные среды для культур клеток, так и комплексные среды для культур клеток. Неограничивающие примеры базальных сред для культур клеток, используемых во время транспортировки, включают, без ограничения, минимальную питательную среду Игла, ADC-1, LPM (без бычьего сывороточного альбумина), F10 (Хэма), F12 (Хэма), DCCM1, DCCM2, RPMI 1640, среду BGJ (с и без модификации Фиттона-Джексона), базальную среду Игла (BME - с добавкой солевой основы Эрла), среду Игла в модификации Дульбекко (DMEM - без сыворотки), улучшенную DMEM/F-12, Яманэ, IMEM-20, среду Игла в модификации Глазго (GMEM), среду Лейбовица L-15, среду Маккоя 5А, среду M199 (M199E - с солевой основой Эрла), среду M199 (M199H - с солевой основой Хэнкса), минимальную питательную среду Игла (MEM - с солевой основой Эрла), минимальную питательную среду Игла (MEM-H - с солевой основой Хэнкса) и минимальную питательную среду Игла (MEM-NAA с заменимыми аминокислотами), среди других многочисленных, включая среду 199, CMRL 1415, CMRL 1969, CMRL 1066, NCTC 135, MB 75261, MAB 8713, DM 145, Williams' G, Neuman & Tytell, Higuchi, MCDB 301, MCDB 202, MCDB 501, MCDB 401, MCDB 411, MDBC 153 и Ultraculture. В некоторых вариантах осуществления среда для клеточной культуры, используемая для транспортировки, включает RPMI-1640. В некоторых вариантах осуществления среда для клеточной культуры, используемая для транспортировки, включает RPMI 1640 с добавкой L-глутамина. В некоторых вариантах осуществления среда для клеточной культуры, используемая для транспортировки, включает улучшенную DMEM/F-12. В некоторых вариантах осуществления питательная среда для клеточной культуры, используемая для транспортировки, включает полную среду. Например, питательная среда для клеточной культуры, используемая для транспортировки, включает базальную среду с одной или более из добавок N-2, B27 XenoFree, B27, StemPro, эпидермального фактора роста (EGF), основного фактора роста фибробластов (bFGF) или GlutaMAX I. В некоторых вариантах осуществления среда для клеточной культуры, используемая для транспортировки, включает один или несколько антибиотиков. Например, среда для клеточной культуры, используемая для транспортировки, включает гентамицин в концентрации приблизительно 30-100 микрограммов (мкг) на миллилитр (мл) или от приблизительно 0,5 до приблизительно 50 мкг/мл. В некоторых вариантах осуществления среда для клеточной культуры, используемая для транспортировки, включает гентамицин в концентрации приблизительно 50 мкг/мл.
[0096] В некоторых вариантах осуществления человеческий образец хранят приблизительно при 1-8°C непосредственно после помещения в среду для транспортировки культуры клеток. В некоторых вариантах осуществления человеческий образец хранят приблизительно при 4°C непосредственно после помещения в среду для транспортировки культуры клеток. Например, человеческий образец хранят во льду непосредственно после помещения в среду для транспортировки культуры клеток.
[0097] В изобретении предложены способы выделения образца сетчатки, включающего множество первичных ретинальных клеток из человеческого образца, например, образца, включающего одно или пару глазных яблок от человека-донора гестационного возраста приблизительно 12-28 недель.
[0098] Ретинальные клетки-предшественники могут быть очищены от других компонентов ткани после или параллельно с обработкой образца ткани. Например, клетки-предшественники могут быть очищены от других клеток и компонентов ткани после культивирования образца ткани в условиях, подходящих для роста клеток, и в течение времени, достаточного для того, чтобы клетки могли прикрепиться к чашке для культивирования. В некоторых вариантах осуществления очистка клеток включает получение клеток, которые мигрируют из образца ткани во время культивирования и присутствуют в культуральной среде или слабо прикреплены к фибронектину или другому субстрату или слою питающих клеток. Эти клетки могут быть получены стандартными методами, такими как удаление и центрифугирование среды для осаждения содержащихся в ней клеток и промывка клеток, оставшихся в чашке для культивирования, таким раствором, как фосфатно-солевой буфер (PBS) или сбалансированный солевой раствор Хенкса, для удаления этих клеток, слабо прикрепленных в виде слоя адгерентных клеток. Затем этот промывочный раствор можно центрифугировать с получением клеток. Очистка ретинальных клеток-предшественников и популяций клеток может дополнительно включать отделение клеток от некоторых нерастворимых тканевых компонентов, включая остаточный тканевый материал, такой как липиды. Клетки могут быть отделены от других тканевых компонентов любыми способами, известными и доступными в данной области, включая, например, применение градиентов плотности, центрифугирования, сортировки с помощью проточной цитометрии или магнитного разделения клеток (MACS) и фильтрации, или их комбинаций. Примеры конкретных способов очистки клеток известны и описаны в данной области, например, в патентах США 6,777,231. Методы негативного разделения также могут использоваться для удаления одного или нескольких конкретных типов клеток.
[0099] Ткань может также быть обработана или "разделена". Например, ткань, такую как одно или пара глазных яблок, могут обрабатывать или разрезать для выделения сетчатки, после чего сетчатки разделяют для получения множества первичных ретинальных клеток и скоплений клеток. Затем такие первичные ретинальные клетки и скопления клетки культивируют, как описано в настоящем документе, с получением множества ретинальных клеток-предшественников.
[00100] Таким образом, в изобретении предложены способы выделения образца сетчатки, включающего множество первичных ретинальных клеток, из человеческого образца. Человеческий образец включает, например, одно или пару глазных яблок от человека-донора гестационного возраста приблизительно от 12 до 28 недель. В некоторых вариантах осуществления способы включают: (i) извлечение одного или пары человеческих глазных яблок из среды для транспортировки культуры, (ii) промывку одного или пары человеческих глазных яблок фосфатно-солевым буфером (PBS) с добавкой антибиотика и температурой приблизительно 1-8°C, (iii) удаление зрительного нерва и мезенхимальной ткани из одного или пары человеческих глазных яблок, (iv) промывку одного или пары человеческих глазных яблок PBS с температурой приблизительно 1-8°C и добавкой антибиотика, (v) прокол каждого из одного или пары человеческих глазных яблок по краю с помощью иглы, (vi) круговой разрез по краю роговицы края того или пары человеческих глазных яблок, например с помощью пары микрохирургических ножниц, (vii) удаление хрусталика, роговицы и ассоциированного стекловидного тела из одного или пары человеческих глазных яблок, (viii) отделение сетчатки (сетчаток) от слоя пигментного эпителия сетчатки (ПЭС) с получением отделенной сетчатки или пары отделенных сетчаток, и (ix) помещение отделенной сетчатки или пары отделенных сетчаток в культуральную среду или PBS с температурой приблизительно 1-8°C, где культуральная среда или PBS содержат антибиотик. Промывание (или промывка) образца на различных этапах можно повторить 1-5 раз или больше. Например, образец могут промывать 1, 2, 3, 4 или 5 раз. В некоторых вариантах осуществления образец сетчатки, полученный с применением способов, описанных в настоящем документе, не содержит или по существу не содержит экстраокулярных клеток.
[00101] В некоторых вариантах осуществления образцы сетчатки, выделенные с применением способов, описанных в настоящем документе, разделяют с получением выделенных клеток сетчатки и скоплений клеток сетчатки, которые культивируют с применением ретинальных клеток-предшественников. В некоторых вариантах осуществления диссоциация образца сетчатки является механической. В некоторых вариантах осуществления диссоциация включает: (i) перенос образца сетчатки в пробирку, (ii) механическую диссоциацию образца сетчатки с получением множества разделенных первичных ретинальных клеток, (iii) осаждение множества разделенных первичных ретинальных клеток с помощью центрифугирования, и (iv) удаление супернатанта. Механическая диссоциация может быть осуществлена любыми способами, известными в данной области, включающими, без ограничения, суспендирование стерильной пипеткой. В некоторых вариантах осуществления суспендирование выполняют несколько раз, например от 2 до 50 раз, от 2 до 10 раз или от 2 до 8 раз, или до тех пор, пока образец сетчатки не будет разбит на скопления клеток подходящего размера. В некоторых вариантах осуществления суспендирование проводят от 4 до 8 раз.
[00102] В некоторых вариантах осуществления диссоциация образца сетчатки включает расщепление протеазой. В некоторых вариантах осуществления диссоциация образца сетчатки включает расщепление протеазой и механическую диссоциацию. В некоторых вариантах осуществления протеазой является трипсин. Подходящие композиции трипсина известны средним специалистам в данной области и включают, без ограничения, TrypLE (Thermo Fisher Scientific), TrypLE Select (Invitrogen) и TrypLE Express (Invitrogen). Например, выделенные сетчатки могут пипетировать в неразведенный TrypLE Express. Активность протеаз, таких как трипсин, можно нейтрализовать добавлением избытка среды без протеаз для остановки реакции. Например, 5×, 10×, 15× или 20× избыток культуральной среды можно добавлять к смеси, включающей разделенные сетчатки.
[00103] Диссоциацию могут проводить путем физической диссоциации и/или обработки препаратом фермента, который способствует освобождению клеток от других компонентов ткани с получением "разделенной суспензии" клеток и/или скоплений клеток. Примеры таких ферментов включают, без ограничения перечисленными, матриксные металлопротеиназы, клострипаин, папаин, трипсин, трипсиноподобные протеазы, пепсин, пепсиноподобные протеазы, протеазы нейтрального типа и коллагеназы. Подходящие протеолитические ферменты описаны в патентах США 5,079,160; 6,589,728; 5,422,261; 5,424,208 и 5,322,790. Например, ферментный препарат может включать трипсин отдельно или в комбинации с одним или более дополнительными ферментами. Ферментативную диссоциацию могут проводить в сочетании с физической диссоциацией, например, измельчением, пипетированием, гомогенизацией, растиранием, замораживанием-оттаиванием, осмотическим шоком, для удаления нежелательных клеток или соединительной ткани и, в конечном итоге, с получением культур одиночных клеток или скоплений клеток, которые можно определить по размеру, т.е. "мелкие", "средние" и "крупные". Размер скоплений клеток является субъективным и может изменяться в зависимости от изобретения, раскрытого в настоящем документе. Выделенные первичные ретинальные клетки, описанные в настоящем документе, включают выделенные клетки и скопления клеток. Скопления выделенных первичных ретинальных клеток могут включать приблизительно 2-5000 клеток, 2-4000 клеток, 2-3000 клеток, 2-2000 клеток, 2-1000 клеток, 2-100 клеток, 50-5000 клеток, 50-4000 клеток, 50-3000 клеток, 50-2000 клеток, 50-1000 клеток, 50-100 клеток, 500-5000 клеток или 500-1000 клеток.
[00104] Композиции, включающие множества выделенных первичных ретинальных клеток, могут осаждать с помощью центрифугирования, чтобы сконцентрировать клетки, промыть клетки или заменить среду для культивирования клеток. Например, множества разделенных первичных ретинальных клеток могут промывать культуральной средой или PBS, необязательно с добавкой антибиотика. Множества разделенных первичных ретинальных клеток могут осаждать с помощью центрифугирования от приблизительно 100×g (центробежное ускорение) до приблизительно 1000×g, от приблизительно 100×g до приблизительно 500×g и от приблизительно 140×g до приблизительно 300×g. В некоторых вариантах осуществления множество разделенных первичных ретинальных клеток осаждают с помощью центрифугирования приблизительно при 140×g. В некоторых вариантах осуществления множество разделенных первичных ретинальных клеток осаждают с помощью центрифугирования приблизительно при 300×g. Центрифугирование могут проводить приблизительно от 1 минуты до 30 минут. Например, композиции, включающие множества выделенных первичных ретинальных клеток, могут центрифугировать в течение приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 15, 20, 25 или 30 минут. Центрифугирование могут проводить при любой температуре, требуемой для поддержания жизнеспособности клеток. В некоторых вариантах осуществления композиции, включающие множества выделенных первичных ретинальных клеток, центрифугируют при температуре приблизительно от 0°C до 50°C. В некоторых вариантах осуществления композиции, включающие множества выделенных первичных ретинальных клеток, центрифугируют приблизительно при 4°C. В некоторых вариантах осуществления композиции, включающие множества выделенных первичных ретинальных клеток, центрифугируют приблизительно при 18-24°C. В некоторых вариантах осуществления композиции, включающие множества выделенных первичных ретинальных клеток, центрифугируют приблизительно при 37°C.
[00105] В некоторых вариантах осуществления способов, описанных в настоящем документе, способы включают: (i) ресуспендирование разделенных осажденных первичных ретинальных клеток в культуральной среде с температурой приблизительно 1-8°C с добавкой антибиотика, (ii) посев множества разделенных ретинальных клеток в одну или более флаконов или планшетов для культур клеток с покрытием, содержащих культуральную среду, где в среду для культуры клеток необязательно добавлен антибиотик, (iii) инкубирование множества разделенных ретинальных клеток приблизительно при 10-50°C, где инкубирование необязательно проходит приблизительно при 37°C, и (iv) определение количества и жизнеспособности первичных ретинальных клеток и скоплений ретинальных клеток. Флаконы или планшеты могут засевать при любой подходящей плотности. Например, во флаконы или планшеты могут сеять от приблизительно 1 до приблизительно 1000000000 клеток. В альтернативе флаконы или планшеты могут засевать при плотности от приблизительно 10000 до приблизительно 5×106 клеток на квадратный сантиметр (см2). В качестве другой альтернативы флаконы или планшеты могут засевать при плотности от приблизительно 0,50×106 до приблизительно 2,5×106 клеток на квадратный сантиметр (см2). В качестве другой альтернативы флаконы или планшеты могут засевать при плотности от приблизительно 0,82×106 до приблизительно 2,06×106 клеток на квадратный сантиметр (см2). В качестве другой альтернативы флаконы или планшеты могут засевать при плотности от приблизительно 0,1×106 до приблизительно 20×106 клеток за см2, от приблизительно 1×106 до приблизительно 20×106 клеток за см2, от приблизительно 2×106 до приблизительно 20×106 клеток за см2, от приблизительно 3×106 до приблизительно 20×106 клеток за см2, от приблизительно 4×106 до приблизительно 20×106 клеток за см2, от приблизительно 5×106 до приблизительно 20×106 клеток за см2, от приблизительно 6×106 до приблизительно 20×106 клеток за см2, от приблизительно 7×106 до приблизительно 20×106 клеток за см2, от приблизительно 8×106 до приблизительно 20×106 клеток за см2, от приблизительно 9×106 до приблизительно 20×106 клеток за см2, от приблизительно 10×106 до приблизительно 20×106 клеток за см2, от приблизительно 0,2×106 до приблизительно 10×106 клеток за см2, от приблизительно 0,2×106 до приблизительно 5×106 клеток за см2, от приблизительно 0,2×106 до приблизительно 4×106 клеток за см2, от приблизительно 0,2×106 до приблизительно 3×106 клеток за см2, от приблизительно 0,2×106 до приблизительно 2×106 клеток за см2, от приблизительно 0,5×106 до приблизительно 10×106 клеток за см2, от приблизительно 0,5×106 до приблизительно 5×106 клеток за см2, от приблизительно 0,5×106 до приблизительно 4×106 клеток за см2, от приблизительно 0,5×106 до приблизительно 3×106 клеток за см2 или от приблизительно 0,5×106 до приблизительно 2,5×106 клеток за см2.
[00106] В некоторых вариантах осуществления способы, описанные в настоящем документе, дают от приблизительно 20×106 до приблизительно 1×109 жизнеспособных первичных ретинальных клеток, от приблизительно 20×106 до приблизительно 1×108 жизнеспособных первичных ретинальных клеток, от приблизительно 20×106 до приблизительно 1×107 жизнеспособных первичных ретинальных клеток, от приблизительно 30×106 до приблизительно 1×109 жизнеспособных первичных ретинальных клеток, от приблизительно 30×106 до приблизительно 1×108 жизнеспособных первичных ретинальных клеток, от приблизительно 30×106 до приблизительно 1×107 жизнеспособных первичных ретинальных клеток, от приблизительно 20×106 до приблизительно 147×106 жизнеспособных первичных ретинальных клеток, от приблизительно 20×106 до приблизительно 100×106 жизнеспособных первичных ретинальных клеток или от приблизительно 73×106 до приблизительно 147×106 жизнеспособных первичных ретинальных клеток. В некоторых вариантах осуществления способы, описанные в настоящем документе, дают по меньшей мере приблизительно 20×106 жизнеспособных первичных ретинальных клеток. В некоторых вариантах осуществления способы, описанные в настоящем документе, дают по меньшей мере приблизительно 30×106 жизнеспособных первичных ретинальных клеток. В некоторых вариантах осуществления способы, описанные в настоящем документе, дают по меньшей мере приблизительно 35×106 жизнеспособных первичных ретинальных клеток. В некоторых вариантах осуществления способы, описанные в настоящем документе, дают по меньшей мере приблизительно 30×106 жизнеспособных первичных ретинальных клеток. В некоторых вариантах осуществления способы, описанные в настоящем документе, дают по меньшей мере приблизительно 45×106 жизнеспособных первичных ретинальных клеток. В некоторых вариантах осуществления способы, описанные в настоящем документе, дают по меньшей мере приблизительно 50×106 жизнеспособных первичных ретинальных клеток. В некоторых вариантах осуществления способы, описанные в настоящем документе, дают по меньшей мере приблизительно 20×106 жизнеспособных первичных ретинальных клеток, по меньшей мере приблизительно 30×106 жизнеспособных первичных ретинальных клеток, по меньшей мере приблизительно 40×106 жизнеспособных первичных ретинальных клеток, по меньшей мере приблизительно 50×106 жизнеспособных первичных ретинальных клеток, по меньшей мере приблизительно 60×106 жизнеспособных первичных ретинальных клеток, по меньшей мере приблизительно 70×106 жизнеспособных первичных ретинальных клеток, по меньшей мере приблизительно 80×106 жизнеспособных первичных ретинальных клеток, по меньшей мере приблизительно 90×106 жизнеспособных первичных ретинальных клеток, по меньшей мере приблизительно 100×106 жизнеспособных первичных ретинальных клеток, по меньшей мере приблизительно 120×106 жизнеспособных первичных ретинальных клеток, по меньшей мере приблизительно 140×106 жизнеспособных первичных ретинальных клеток, по меньшей мере приблизительно 145×106 жизнеспособных первичных ретинальных клеток, по меньшей мере приблизительно 147×106 жизнеспособных первичных ретинальных клеток, по меньшей мере приблизительно 150×106 жизнеспособных первичных ретинальных клеток, по меньшей мере приблизительно 170×106 жизнеспособных первичных ретинальных клеток, по меньшей мере приблизительно 190×106 жизнеспособных первичных ретинальных клеток или по меньшей мере приблизительно 200×106 жизнеспособных первичных ретинальных клеток.
Морфология, количество и жизнеспособность клеток
[00107] В настоящем документе предложены способы определения жизнеспособности, количества и морфологии первичных ретинальных клеток из образца сетчатки, и ретинальных клеток-предшественников, полученных из первичных ретинальных клеток.
[00108] Морфологию клеток можно определить с помощью световой микроскопии при использовании любого подходящего метода. Подходящие методы световой микроскопии известны специалистам в данной области и включают, без ограничения перечисленными, дифференциальную интерференционную контрастную микроскопию, микроскопию Номарского, микроскопию с модуляционным контрастом Хоффмана и их вариации, флуоресцентную микроскопию и конфокальную микроскопию. Необязательно может использоваться гистохимическое окрашивание на один или более маркеров выделенных первичных ретинальных клеток.
[00109] Количество и жизнеспособность клеток можно измерять с помощью автоматического счетчика клеток NC200 (Chemometec) и метода подсчета агрегированных клеток. Альтернативно или дополнительно, количество клеток и их жизнеспособность можно измерять с использованием трипанового синего или гемоцитометра.
[00110] В некоторых вариантах осуществления процент жизнеспособных подсчитанных клеток составляет от приблизительно 10% до приблизительно 100% или от приблизительно 68% до приблизительно 85%.
[00111] Фетальные ретинальные клетки или клетки RPC млекопитающих экспрессируют количественно разные профили генов, например, как описано в настоящем документе; или они экспрессируют количественно разные профили растворимых факторов; или они экспрессируют количественно разные профили поверхностных маркеров. Более того, фетальные ретинальные клетки или клетки RPC млекопитающих имеют генный профиль, который не является фиксированным, постоянным или неизменным. Скорее они имеют генный профиль, который в культуре динамически изменяется количественно в зависимости от времени.
[00112] Изобретение, раскрытое в настоящем документе, относится к популяции клеток, содержащей ретинальные клетки-предшественники млекопитающего, которые выделены в соответствии с определенным способом культивирования клеток и которые экспрессируют характеристические маркеры. Популяция клеток может быть культурой клеток, выделенных у млекопитающего и выращенных in vitro. Например, культура может включать суспензию клеток или адгерентных клеток, культивируемых в культуральном планшете, чашке, флаконе или биореакторе. Образец может быть гомогенным или гетерогенным, что может быть определено по экспрессии одного или более маркеров, как определено в настоящем документе. Популяция клеток, описанная в настоящем документе, представляет собой смешанную популяцию клеток и может содержать смесь недифференцированных и дифференцированных клеток. Относительные уровни экспрессии маркеров, характеристических для ретинальных клеток-предшественников, определенных в настоящем документе, у клеток в популяции могут отличаться.
[00113] Ретинальные клетки-предшественники могут характеризоваться по экспрессии молекулярных маркеров, включая маркеры клеточной поверхности и неповерхностные ("генетические") маркеры. Хотя в данной области принято называть клетки "положительными" или "отрицательными" на конкретный маркер, фактические уровни экспрессии определяют количественно. Количество молекул на клеточной поверхности (или расположенных где-либо в другом месте) может отличаться на несколько порядков, но при этом все же может быть охарактеризовано как "положительное". Специалистам в данной области также понятно, что клетка, отрицательная при окрашивании, т.е. когда уровень связывания специфичного к маркеру реагента не отличается заметно от контроля, например, контроля, совпадающего по изотипу, может экспрессировать минорные количества маркера. Анализ уровня мечения ("окрашивания") позволяет проводить тонкие различия между популяциями клеток. Интенсивность окрашивания клеток можно контролировать с помощью проточной цитометрии, где лазеры определяют количественные уровни флуорохрома (которые пропорциональны количеству маркера клеточной поверхности, связанного со специфичными реагентами, например антителами). Проточная цитометрия, или FACS, также может применяться для разделения популяций клеток по интенсивности связывания с конкретным реагентом, а также другим параметрам, таким как размер клеток и светорассеяние. Хотя абсолютный уровень окрашивания может отличаться в зависимости от конкретного флуорохрома и препарата реагента, данные можно нормализовать по контролю.
[00114] Для нормализации распределения по контролю каждую клетку регистрируют как точку данных, имеющую определенную интенсивность окрашивания. Эти точки данных могут отображать на логарифмической шкале, где единицей измерения является условная интенсивность окрашивания. Например, самые яркие окрашенные клетки в образце могут быть на 4 log порядка более интенсивными, чем неокрашенные клетки. При таком отображении клетки, попадающие в наиболее высокий логарифм интенсивности окрашивания, являются яркими, а клетки с самой низкой интенсивностью - отрицательными. Клетки с "низким" положительным окрашиванием имеют уровень окрашивания выше яркости изотипически совпадающего контроля, но не такой интенсивный, как у наиболее ярко окрашенных клеток, обычно встречающиеся в популяции. Низкоположительные клетки могут обладать уникальными свойствами, которые отличаются от отрицательных и ярко окрашенных положительных клеток образца. В альтернативном контроле могут использовать субстрат, имеющий определенную плотность маркера на своей поверхности, например, промышленно изготовленную сферу или линию клеток, которые обеспечивают положительный контроль интенсивности.
[00115] Экспрессия маркеров может изменяться во время культивирования ткани сетчатки, из которой происходят ретинальные клетки-предшественники и популяции клеток. Например, на различия в экспрессии маркеров могут влиять условия культивирования, такие как уровни кислорода (например, показатели атмосферного кислорода или "нормоксические" условия; или условия с низким содержанием кислорода, также известные как "гипоксические" условия). В качестве неограничивающего примера условия с низким содержанием кислорода могут включать приблизительно 0,5-10% кислорода (например, приблизительно 0,5, 1, 1,5, 2, 2,5, 3, 3,5, 4, 4,5, 5, 5,5, 6, 6,5%, 7, 7,5, 8, 8,5, 9, 9,5 или 10%). В некоторых вариантах осуществления условия с низким содержанием кислорода могут включать приблизительно 0,5-5%, приблизительно 1-5% или приблизительно 1-3%. Специалистам в данной области известно, что экспрессия маркеров ретинальных клеток-предшественников и популяций клеток не является статической и может изменяться в зависимости от одного или нескольких условий культивирования, например, культуральной среды, уровней кислорода, количества пассажей, времени культивирования и т.д.
[00116] Ретинальные клетки-предшественники и популяции клеток могут экспрессировать один или больше, два или больше, три или больше, четыре или больше, пять или больше, шесть или больше, семь или больше, восемь или больше, девять или больше, десять или больше, одиннадцать или больше, двенадцать или больше, тринадцать или больше, пятнадцать или больше, шестнадцать или больше, семнадцать или больше, восемнадцать или больше, девятнадцать или больше, двадцать или больше, двадцать пять или больше, тридцать или больше маркеров, определенных в настоящем документе, или любое промежуточное приращение до пятидесяти или более маркеров.
Культивирование первичных ретинальных клеток и ретинальных клеток-предшественников (RPC)
[00117] В настоящем документе предложены способы культивирования первичных ретинальных клеток и ретинальных клеток-предшественников с целью получения популяций ретинальных клеток-предшественников для трансплантации и терапевтических применений.
[00118] Способы, описанные в настоящем документе, могут обеспечивать получение больших количеств жизнеспособных клеток. Например, способы, описанные в настоящем документе, могут давать приблизительно 1 миллиард ретинальных клеток-предшественников или больше при сборе. В некоторых вариантах осуществления по меньшей мере 50%, по меньшей мере 60%, по меньшей мере 70%, по меньшей мере 80% или по меньшей мере 90% клеток являются жизнеспособными.
[00119] В некоторых вариантах осуществления донорские клетки могут культивировать без антибиотиков во избежание изменения клеток. Кроме того, без антибиотиков возможно использовать клетки после очень малого числа пассажей, так как можно исключить скрытую микробную контаминацию. В альтернативных вариантах осуществления применение клеток после малого числа пассажей связано с низким риском перерождения и/или образования опухолей. Кроме того, применение клеток после малого числа пассажей наиболее приближено к естественным клеткам, присутствующим в развивающейся сетчатке.
[00120] В некоторых вариантах осуществления первичные ретинальные клетки и ретинальные клетки-предшественники культивируют с использованием антибиотика. Подходящие антибиотики включают, без ограничения перечисленными, пенициллин, стрептомицин и гентамицин. В некоторых вариантах осуществления антибиотик включает гентамицин. В некоторых вариантах осуществления гентамицин присутствует в концентрации приблизительно 0,5-50 мкг/мл, например, приблизительно 0,5-40 мкг/мл, приблизительно 5-50 мкг/мл или приблизительно 5-35 мкг/мл. В некоторых вариантах осуществления гентамицин присутствует в концентрации приблизительно 50 мкг/мл. В некоторых вариантах осуществления гентамицин присутствует в концентрации приблизительно 30 мкг/мл.
[00121] Для роста и культивирования RPC могут использоваться любые подходящие базальные среды. Культура клеток описывает процесс, с помощью которого клетки выращивают в контролируемых условиях, как правило, вне их естественного окружения. Популяции клеток выращивают или культивируют в любой среде для культивирования клеток, известной в данной области. Термин "базальная среда" относится к любой среде, которая может поддерживать рост клеток. Базальная среда содержит стандартные неорганические соли, такие как цинк, железо, магний, кальций и калий, витамины, глюкозу, буферную систему и ключевые аминокислоты. Базальная среда, которая может использоваться в настоящем изобретении, включает, без ограничения перечисленным, минимальную питательную среду Игла, ADC-1, LPM (без бычьего сывороточного альбумина), F10 (Хэма), F12 (Хэма), DCCM1, DCCM2, RPMI 1640, среду BGJ (с и без модификации Фиттона-Джексона), базальную среду Игла (BME - с добавкой солевой основы Эрла), среду Игла в модификации Дульбекко (DMEM - без сыворотки), Яманэ, IMEM-20, среду Игла в модификации Глазго (GMEM), среду Лейбовица L-15, среду Маккоя 5А, среду M199 (M199E - с солевой основой Эрла), среду M199 (M199H - с солевой основой Хэнкса), минимальную питательную среду Игла (MEM - с солевой основой Эрла), минимальную питательную среду Игла (MEM-H - с солевой основой Хэнкса) и минимальную питательную среду Игла (MEM-NAA с заменимыми аминокислотами), среди других многочисленных, включая среду 199, CMRL 1415, CMRL 1969, CMRL 1066, NCTC 135, MB 75261, MAB 8713, DM 145, Williams' G, Neuman & Tytell, Higuchi, MCDB 301, MCDB 202, MCDB 501, MCDB 401, MCDB 411, MDBC 153 и Ultraculture. В альтернативных вариантах осуществления среды для применения при культивировании ретинальных клеток-предшественников, раскрытых в настоящем документе, представляют собой улучшенную DMEM/F12 и Ultraculture. Некоторые из этих сред коротко описаны в Methods in Enzymology, Volume LVIII, "Cell Culture", стр. 62-72.
[00122] В некоторых вариантах осуществления питательная среда включает среду Игла в модификации Дульбекко DMEM/F12, улучшенную DMEM/F12, Knockout DMEM/F12, нейробазальные среды, ReNcell или Ultraculture. В некоторых вариантах осуществления среда включает DMEM/F12.
[00123] "Кондиционированная среда" относится к среде, которая изменена по сравнению с базовой или базальной средой. Например, кондиционирование среды может включать повышение или снижение уровней молекул, таких как питательные вещества и/или факторы роста, относительно исходных уровней, присутствующих в базовой среде. Среду можно кондиционировать, позволяя клеткам определенных типов расти или поддерживая их в среде при определенных условиях в течение определенного периода времени. Например, среду можно кондиционировать, позволяя ретинальным клеткам-предшественникам размножаться, дифференцироваться или поддерживаться в среде с определенным составом при определенной температуре в течение определенного количества часов. Специалистам в данной области техники будет понятно, что многочисленные комбинации клеток, типов сред, продолжительности и условий окружающей среды можно использовать для получения почти бесконечного множества кондиционированных сред.
[00124] Примеры дополнительных компонентов или добавок для культур клеток включают, без ограничения, ингредиенты, частично или полностью заменяющие сыворотку при поддержании выживания или роста клеток. Например, добавки могут включать инсулин, трансметаллопротеины, микроэлементы, витамины или другие факторы. Эти факторы обычно не включают в состав базальной среды, но их предоставляет сыворотка, обычно используемая при культивировании клеток. Дополнительный компонент или добавка может включать по меньшей мере один или больше из следующих компонентов, которые поддерживают рост клеток: один или более инсулинов или их заменителей, один или более трансметаллопротеинов или их заменителей, один или более микроэлементов (например, селен, железо, цинк, медь, кобальт, хром, иод, фторид, марганец, молибден, ванадий, никель, олово), один или более витаминов (например, витамин C, витамин E, витамин A, группа витаминов B), одна или более солей (например, соли натрия, соли магния, соли кальция или фосфатные соли), один или более буферов (например, фосфатно-солевой буфер, буфер HEPES), одна или более аминокислот (например, L-глутамин), один или более гормонов, гормоноподобные соединения или факторы роста (такие как, например, трансферрин, EGF, NGF, ECGF, PDGF, FGF, IGF, LIF, интерлейкины, интерфероны, TGF и/или VEGF, глюкагон, кортикостероиды, вазопрессин, простагландины и другие факторы роста), сывороточный альбумин или его заменители, один или более углеводов (глюкоза, галактоза, фруктоза, манноза, рибоза, гликолитические метаболиты), один или более антибиотиков и/или антимикотиков (например, пенициллин, стрептомицин, фунгизон) и один или более липидов (например, свободные и связанные с белками жирные кислоты, триглицериды, фосфолипиды, холестерин, этаноламин). Пример дополнительного компонента включает добавку N-2 (N2). Многие коммерческие добавки-заменители сыворотки, такие как KnockOut Serum Replacement (KOSR), N2, B27, StemPro (иногда именуемый в настоящем документе Stempro), добавка инсулин-трансферрин-селен (ITS) и G5, хорошо известны и легко доступны специалистам в данной области техники. Такие добавки характеризуются четко определенными ингредиентами, поэтому концентрации их компонентов могут быть определены на основе их процентного содержания в среде. В некоторых вариантах осуществления культуральная среда включает эпидермальный фактор роста человека (EGF) и основной фактор роста фибробластов (bFGF).
[00125] В качестве неограничивающего примера клетки и/или небольшие клеточные скопления культивируют в стерильном окружении, содержащем бессывороточную среду или среду с сывороткой, а также антибиотики и противогрибковые средства, или без антибиотиков или противогрибковых средств, в течение не больше чем приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 или более пассажей. Клетки и/или небольшие клеточные скопления культивируют в базальной культуральной среде (например, среде Игла в модификации Дульбекко: питательной смеси F-12TM (DMEM/F12TM) или в улучшенной среде DMEM/F12TM (Gibco-Invitrogen-Life Technologies, Carlsbad Calif.)), или в средах ULTRACULTURETM (BioWhittaker-Lonza Walkersville, Inc., Walkersville, MD), необязательно с добавкой N2 (Invitrogen) или B27, или B27 XenoFree (Invitrogen), L-глутамином или GlutaMax, или GlutaMAX-I (Invitrogen), и человеческими рекомбинантными факторами роста, включающими, например, EGF и bFGF (Invitrogen), или другими факторами роста. Например, среда DMEM/F12TM используется для клеток человека, а среда ULTRACULTURETM используется для клеток кошек или собак.
[00126] В некоторых вариантах осуществления клетки и/или скопления клеток культивируют в течение по меньшей мере 1, 2, 3, 4 или 5 пассажей. В некоторых вариантах осуществления клетки и/или скопления клеток культивируют в течение больше чем 5 пассажей. В некоторых вариантах осуществления культуральная среда включает среду Игла в модификации Дульбекко DMEM/F12, улучшенную DMEM/F12, Knockout DMEM/F12, нейробазальные среды, ReNcell и среды Ultraculture. В некоторых вариантах осуществления культуральная среда включает улучшенную DMEM/F12.
[00127] В некоторых вариантах осуществления питательная среда включает улучшенную DMEM/F12, добавку N-2, GlutaMAX I, рекомбинантный человеческий эпидермальный фактор роста (EGF) и основной фактор роста фибробластов (bFGF). В некоторых вариантах осуществления культуральная среда дополнительно включает B27, B27 XenoFree или StemPro. В некоторых вариантах осуществления культуральная среда включает гентамицин в концентрации приблизительно 30 мкг/мл.
[00128] Культуральные среды также необязательно могут включать добавку альбумина, человеческого или кошачьего, или собачьего альбумина, или рекомбинантного альбумина, или альбумина. В качестве неограничивающего примера альбумин могут добавлять в количестве до начальной концентрации приблизительно 1,0 мг/мл.
[00129] Культуры ретинальных клеток-предшественников млекопитающих могут быть получены в среде с пониженным содержанием сыворотки или без сыворотки. Примеры сыворотки включают фетальную бычью сыворотку, телячью сыворотку, сыворотку новорожденных телят, козью сыворотку, лошадиную сыворотку, человеческую сыворотку, кроличью сыворотку, крысиную сыворотку, мышиную сыворотку, помимо прочего. При некоторых условиях культивирования концентрации сыворотки могут изменяться от приблизительно 0,05% об/об до приблизительно 20% об/об (например, 0,05, 0,10, 0,15, 0,20, 0,25, 0,30, 0,35, 0,40, 0,45, 0,50, 0,55, 0,60, 0,65, 0,70, 0,75, 0,80, 0,85, 0,90, 1, 1,5, 2, 2,5, 3, 3,5, 5, 4,5, 5, 5,5, 6, 6,5, 7, 7,5, 8, 8,5, 9, 9,5, 10, 10,5, 11, 11,5, 12, 12,5, 13, 13,5, 14, 14,5, 15, 15,5, 16, 16,5, 17, 17,5, 18, 18,5, 19, 19,5 или 20%). Например, в некоторых процессах дифференцирования концентрация сыворотки в среде может составлять меньше чем приблизительно 0,05% (об/об), меньше, чем приблизительно 0,1% (об/об), меньше чем приблизительно 0,2% (об/об), меньше чем приблизительно 0,3% (об/об), меньше чем приблизительно 0,4% (об/об), меньше чем приблизительно 0,5% (об/об), меньше чем приблизительно 0,6% (об/об), меньше чем приблизительно 0,7% (об/об), меньше чем приблизительно 0,8% (об/об), меньше чем приблизительно 0,9% (об/об), меньше чем приблизительно 1% (об/об), меньше чем приблизительно 2% (об/об), меньше чем приблизительно 3% (об/об), меньше чем приблизительно 4% (об/об), меньше чем приблизительно 5% (об/об), меньше чем приблизительно 6% (об/об), меньше чем приблизительно 7% (об/об), меньше чем приблизительно 8% (об/об), меньше чем приблизительно 9% (об/об), меньше чем приблизительно 10% (об/об), меньше чем приблизительно 15% (об/об) или меньше чем приблизительно 20% (об/об). В некоторых вариантах осуществления ретинальные клетки-предшественники и популяции клеток, включая ретинальные клетки-предшественники, выращивают без сыворотки ("бессывороточный"), без заменителя сыворотки и/или без какого-либо дополнительного компонента.
[00130] Ретинальные клетки-предшественники или популяция клетки, содержащее ретинальные клетки-предшественники, культивируют в условиях отсутствия "ксеногенных" компонентов. "Свободный от ксеногенных компонентов" или "не содержащий ксеногенных компонентов" относится к условиям, когда клетки некоторого вида (например, человеческие клетки) выращивают или культивируют только в присутствии человеческих продуктов или добавок (например, человеческого сывороточного альбумина, человеческой сывороткы), но без продуктов, полученных из других видов. Это особенно важно для клеток, которые применяют для трансплантации у человека. Клетки, которые были подвергнуты контакту с различными неопределенными продуктами животного происхождения, нежелательны для клинических применений из-за повышенного риска отторжения трансплантата, иммунных реакций и вирусных или бактериальных инфекций, прионов и даже неуточненных зоонозов. Кроме того, в случае применения у всех млекопитающих, включая медицинское применение или применение у не относящихся к человеку млекопитающих (например, ветеринарное применение), клетки проверяют на нормальный кариотип или присутствие инфекции или контаминации, например, микоплазмой, грамотрицательными бактериями (например, тест на эндотоксин), грибами и т.п. Клетки могут также иссследовать на туморогенность или перерождение в злокачественный фенотип с помощью анализа активности теломеразы, экспрессии гена hTERT и роста в мягком агаре или образования опухоли у голых мышей. Такие анализы известны в уровне техники и хорошо знакомы квалифицированному специалисту.
[00131] Ретинальные клетки-предшественники или популяции клеток, содержащие ретинальные клетки-предшественники, могут культивировать на слоях питающих клеток (например, эмбриональных или зрелых фибробластов) или в присутствии внеклеточных матриксных каркасов или субстратов, таких как коллаген, энтактин (нидоген), гепаринсульфат-протеогликаны, фибронектин, ламинин, желатин или Matrigel. Например, коллаген PURECOL® известен в качестве стандарта всех коллагенов по чистоте (содержание коллагена >99,9%), функциональности и наиболее близок к нативному коллагену из всех доступных. Коллаген PURECOL® приблизительно на 97% состоит из коллагена I типа, а остальную часть составляет коллаген III типа, и является идеальным для покрытия поверхностей, обеспечивая получение тонких слоев для культивирования клеток, или для применения в качестве твердого геля. Другим примером каркаса или субстрата, известного в данной области, является CELLstart (Invitrogen).
[00132] В некоторых вариантах осуществления условия культивирования клеток могут включать выращивание клеток в инкубаторе, установленном на 37°C, 5% CO2. Первичные ретинальные клетки, ретинальные клетки-предшественники или содержащие их популяции клеток можно культивировать при нормоксических или атмосферных условиях (приблизительно 20% O2) и можно также выращивать в условиях, которые приближенно соответствуют уровням кислорода развивающейся сетчатки плода во время беременности, т.е. при условиях "низкого" содержания O2 или "гипоксических" условиях, например, 0,5%, 1%, 1,5%, 2%, 2,5%, 3%, 3,5%, 4%, 4,5%, 5%, 5,5%, 6%, 6,5%, 7%, 7,5%, 8%, 8,5%, 9%, 9,5% или 10% кислорода или любое промежуточное приращение. В некоторых вариантах осуществления условия культивирования клеток могут включать выращивание клеток в инкубаторе, установленном на: (1) 37°C, при 0-30% CO2 и 0-50% O2, (2) 37°C, с содержанием CO2 меньше или равным 5% и O2 меньше или равным 20%; или (3) 37°C, с содержанием CO2 меньше или равным 5% и O2 меньше или равным 3%.
[00133] Плотность при посеве относится к количеству клеток на объем культуральной среды или к количеству клеток на см2 в адгерентной культуре. Аналогичным термином в данном контексте является "конфлюентность", который обычно используется в качестве показателя количества клеток в чашке или флаконе для культуры клеток и относится к покрытию чашки или флакона клетками. Например, 100-процентная конфлюентность означает, что чашка полностью покрыта клетками, и поэтому не остается свободного места для роста клеток; тогда как 50-процентная конфлюентность означает, что покрыта приблизительно половина чашки и для роста клеток все еще остается свободное место.
[00134] В некоторых вариантах осуществления способы включают первый пассаж, включающий посев клеток в культуральные флаконы или планшеты при плотности от приблизительно 0,5×106 до приблизительно 3,0×106 клеток на квадратный сантиметр (см2), от приблизительно 0,5×106 до приблизительно 5,0×106 клеток/см2, от приблизительно 0,55×106 до приблизительно 4,0×106 клеток/см2, от приблизительно 0,55×106 до приблизительно 3,0×106 клеток/см2, от приблизительно 0,55×106 до приблизительно 2,5×106 клеток/см2 или от приблизительно 0,55×106 до приблизительно 2,1×106 клеток/см2. В некоторых вариантах осуществления первый пассаж включает посев клеток в культуральные флаконы или планшеты при плотности от приблизительно 0,5×106 до приблизительно 3,0×106 клеток/см2. В некоторых вариантах осуществления первый пассаж включает посев клеток в культуральные флаконы или планшеты при плотности от приблизительно 0,59×106 до приблизительно 2,29×106 клеток/см2.
[00135] В некоторых вариантах осуществления способы включают второй пассаж, включающий посев клеток в культуральные флаконы или планшеты при плотности от приблизительно 0,05×106 до приблизительно 1×106 клеток/см2, от приблизительно 0,07×106 до приблизительно 0,80×106 клеток/см2, от приблизительно 0,10×106 до приблизительно 0,5×106 клеток/см2, от приблизительно 0,10×106 до приблизительно 0,4×106 клеток/см2, от приблизительно 0,13×106 до приблизительно 0,35×106 клеток/см2 или от приблизительно 0,14×106 до приблизительно 0,32×106 клеток/см2. В некоторых вариантах осуществления второй пассаж включает посев клеток в культуральные флаконы или планшеты при плотности от приблизительно 0,1×106 до приблизительно 0,5×106 клеток/см2. В некоторых вариантах осуществления второй пассаж включает посев клеток в культуральные флаконы или планшеты при плотности от приблизительно 0,14×106 до приблизительно 0,43×106 клеток/см2.
[00136] В некоторых вариантах осуществления способы включают третий пассаж, включающий посев клеток в культуральные флаконы или планшеты при плотности от приблизительно 0,01×106 до приблизительно 0,5×106 клеток/см2, от приблизительно 0,02×106 до приблизительно 0,45×106 клеток/см2, от приблизительно 0,03×106 до приблизительно 0,40×106 клеток/см2, от приблизительно 0,04×106 до приблизительно 0,30×106 клеток/см2, от приблизительно 0,05×106 до приблизительно 0,20×106 клеток/см2 или от приблизительно 0,05×106 до приблизительно 0,10×106 клеток/см2. В некоторых вариантах осуществления третий пассаж включает посев клеток в культуральные флаконы или планшеты при плотности от приблизительно 0,03×106 до приблизительно 0,2×106 клеток/см2. В некоторых вариантах осуществления третий пассаж включает посев клеток в культуральные флаконы или планшеты при плотности от приблизительно 0,05×106 до приблизительно 0,1×106 клеток/см2.
[00137] В некоторых вариантах осуществления способы включают четвертый и, необязательно, последующие пассажи, где четвертый и последующие пассажи включают посев клеток в культуральные флаконы или планшеты при плотности от приблизительно 10000 до приблизительно 60000 клеток/см2, от приблизительно 10000 до приблизительно 50000 клеток/см2, от приблизительно 10000 до приблизительно 40000 клеток/см2, от приблизительно 20000 до приблизительно 60000 клеток/см2, от приблизительно 20000 до приблизительно 50000 клеток/см2 или от приблизительно 20000 до приблизительно 40000 клеток/см2. В некоторых вариантах осуществления четвертый пассаж включает посев клеток в культуральные флаконы или планшеты при плотности от приблизительно 10000 до приблизительно 60000 клеток/см2. В некоторых вариантах осуществления четвертый проход включает посев клеток в культуральные флаконы или планшеты при плотности от приблизительно 20000 до приблизительно 40000 клеток/см2.
[00138] В некоторых вариантах осуществления способы включают посев клеток в культуральные флаконы при более высоких плотностях, чем при предыдущих пассажах, и при более низких плотностях, чем при последующих пассажах. Без ограничения теорией, считается, что во время первых нескольких пассажей клетки превращаются из скоплений клеток в одиночные клетки, при этом такое постепенное превращение из скоплений в клетки способствует увеличенной жизнеспособности клетки согласно способам, описанным в настоящем документе. В последующих пассажах сеют одиночные клетки, при этом плотность посева быстро снижается, и затем становится постоянной. В качестве неограничивающего примера, клетки сеют в культуральные флаконы или планшеты при плотности от приблизительно 0,5×106 до приблизительно 3,0×106 клеток/см2 в первом пассаже, от приблизительно 0,1×106 до приблизительно 0,5×106 клеток/см2 во втором пассаже, от приблизительно 0,03×106 до приблизительно 0,2×106 клеток/см2 в третьем пассаже и от приблизительно 10000 до приблизительно 60000 клеток/см2 в четвертом и последующих пассажах. В качестве дополнительного неограничивающего примера, клетки сеют в культуральные флаконы или планшеты при плотности от приблизительно 0,59×106 до приблизительно 2,29×106 клеток/см2 в первом пассаже, от приблизительно 0,14×106 до приблизительно 0,32×106 клеток/см2 во втором пассаже, от приблизительно 0,05×106 до приблизительно 0,1×106 клеток/см2 в третьем пассаже и от приблизительно 20000 до приблизительно 40000 клеток/см2 в четвертом и последующих пассажах.
[00139] В некоторых вариантах осуществления период времени между непосредственно последовательными пассажами составляет 2-8 дней, 3-6 дней, 4-5 дней или 3-4 дня. В некоторых вариантах осуществления период времени между пассажами составляет 4 дня. В некоторых вариантах осуществления период времени между непосредственно последовательными пассажами составляет 3 дня.
[00140] В некоторых вариантах осуществления протокол пассирования включает целевые пороговые значения для количеств жизнеспособных клеток, причем культивирование клеток прекращают, если эти целевые пороговые значения не достигаются. Например, культивирование клеток может быть прекращено в конце пассажа 3 (P3), если получено меньше 90 миллионов, 100 миллионов, 110 миллионов, 120 миллионов, 130 миллионов, 140 миллионов или 150 миллионов жизнеспособных клеток. В качестве дополнительного примера культивирование клеток может быть прекращено в конце пассажа 4 (P4), если получено меньше 200 миллионов, меньше 250 миллионов, меньше 300 миллионов, меньше 350 миллионов, меньше 400 миллионов, меньше 450 миллионов или меньше 500 миллионов жизнеспособных клеток.
[00141] Пассирование (также известный как субкультивирование или разделение клеток) включает перенос небольшого количества клеток в новый сосуд. Клетки можно культивировать в течение более длительного времени, если их регулярно разделяют, поскольку это позволяет избежать старения, связанного с длительной высокой плотностью клеток. Суспензионные культуры легко пассировать небольшим количеством культуры, содержащей несколько клеток, разведенных в большем объеме свежей среды. Для адгеретных культур сначала клетки необходимо отделить от поверхности. Обычно это делают при использовании смеси фермента, такой как трипсин-ЭДТА или эквивалент трипсина и ЭДТА, или неферментного раствора, такого как Cell Dissociation Buffer; в любом случае для этой цели доступны различные ферментные или неферментные смеси или препараты. Затем небольшое количество отделенных клеток можно использовать для посева новой культуры.
[00142] В некоторых вариантах осуществления клетки обрабатывают раствором, содержащим трипсин или его эквивалент, который отличается при первом, втором и третьем пассажах. В примерном протоколе клетки обрабатывают первым ферментным раствором, содержащим TrypLE и этилендиаминтетрауксусную кислоту (ЭДТА) в соотношении 1:4, при первом пассаже, вторым ферментным раствором, содержащим TrypLE, ЭДТА и фосфатно-солевой буфер Дульбекко (DPBS) в соотношении 1:1:3, при втором пассаже и третьим ферментным раствором, содержащим TrypLE и DPBS в соотношении 1:1, при третьем и каждом последующем пассаже. В следующем примерном протоколе клетки обрабатывают первым ферментным раствором, содержащим TrypLE, ЭДТА и PBS в соотношении 1:1:3, при первом пассаже, вторым ферментным раствором, содержащим TrypLE и DPBS в соотношении 1:1, при втором пассаже и третьим ферментным раствором, содержащим TrypLE и DPBS в соотношении 1:1, при третьем и каждом последующем пассаже. Клетки могут обрабатывать растворами трипсина или эквивалента в течение приблизительно 5-20 минут, приблизительно 6-10 минут, приблизительно 5-10 минут, приблизительно 7-8 минут или приблизительно 5-7 минут. Жизнеспособность, количество и/или морфология клеток могут определять при любом пассаже. Например, жизнеспособность и количество клеток можно определять при пассажах 3 и 4, чтобы решить, следует ли прекращать культивирование клеток, или для определения плотности посева клеток. Большинство первичных клеточных культур имеют ограниченное время существования и не могут пролиферировать бесконечно. После определенного числа удвоений популяции (так называемого предела Хейфлика) клетки подвергаются процессу старения и перестают делиться, при этом в целом сохраняя жизнеспособность. В некоторых вариантах осуществления ретинальные клетки-предшественники и популяции клеток можно культивировать не больше чем в течение 10 пассажей, например, в течение одного, двух, трех, четырех, пяти, шести, семи, восьми, девяти или десяти пассажей. В некоторых вариантах осуществления RPC пассируют примерно 4-6 (например, 4, 5 или 6) раз в условиях стандартного содержания кислорода и, необязательно, далее культивируют в течение примерно 1-10 (например, 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10) пассажей в условиях низкого содержания кислорода.
[00143] В альтернативных вариантах осуществления клетки могут пассировать (в условиях стандартного содержания кислорода, в условиях низкого содержания кислорода и/или в их любых комбинациях) больше 5 раз, например, шесть, семь, восемь, девять, десять, одиннадцать, двенадцать, тринадцать, четырнадцать, пятнадцать, шестнадцать, семнадцать, восемнадцать, девятнадцать, двадцать или больше пассажей. В некоторых вариантах осуществления ретинальные клетки-предшественники и популяции клеток культивируют приблизительно 5-32 (например, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31 или 32) пассажей. Специалистам в данной области известно, что другие способы, известные в уровне техники, можно применять для культивирования клеток больше 32 пассажей (т.е. 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50 или более пассажей).
[00144] Любой подходящий контейнер, такой как флакон, планшет или многоуровневые флаконы, можно использовать для пассажа клеток с применением способов, описанных в настоящем документе. Примеры флаконов включают флаконы Т25 и Т75. Многоуровневые флаконы CellStacks (CS) представляют собой устанавливаемые друг на друга камеры для культивирования, выпускаемые, например, компанией Corning. В некоторых вариантах осуществления флакон, планшет или многоуровневые флаконы могут иметь покрытие. Флаконы, планшеты и многоуровневые флаконы могут быть покрыты фибронектином, орнитином, полилизином или ламинином, разведенными в фосфатно-солевом буфере Дульбекко (DPBS). В некоторых вариантах осуществления флаконы, планшеты или многоуровневые флаконы покрыты фибронектином. В некоторых вариантах осуществления фибронектин не содержит ксеногенных компонентов. Необязательно флакон, планшет или многоуровневый флакон могут промывать культуральной средой перед помещением в них клеток.
[00145] В различных вариантах осуществления образец клеток исследуют на присутствие патогена, бактерий, эндотоксина, гриба, микоплазмы, вируса, вируса гепатита или вируса ВИЧ. Образец клеток также могут исследовать на наличие нормального кариотипа; жизнеспособность; и/или онкогенность. Необязательно образец клеток не демонстрирует повышенную активность теломеразы.
[00146] В любом из этих способов клетки сетчатки и/или ткань сетчатки могут замораживать либо до, либо после выделения, отбора и/или культивирования. Замораживание клеток могут выполнять при использовании любых криоконсервантов и/или методик, обычно используемых в данной области. Замороженные клетки можно размораживать перед применением с использованием любого протокола, известного в данной области.
[00147] Жизнеспособность клеток могут исследовать до их применения в любом из способов, описанных в настоящем документе. В альтернативных вариантах осуществления, в качестве неограничивающих примеров, перед криоконсервацией по меньшей мере 70% (например, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99 или 100%) клеток являются жизнеспособными. После размораживания, в альтернативных вариантах осуществления, по меньшей мере 70% (например, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99 или 100%) клеток являются жизнеспособными. Аналогичным образом, после восстановления клеточной культуры, в альтернативных вариантах осуществления, по меньшей мере 70% (например, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99 или 100%) клеток являются жизнеспособными. Определение количества жизнеспособных клеток на любой стадии находится в пределах обычного уровня квалификации в данной области.
[00148] Таким образом, в изобретении предложены способы криоконсервации множества ретинальных клеток-предшественников, полученных с применением способов выделения и культивирования, описанных в настоящем документе. В некоторых вариантах осуществления способы включают: (i) ферментативную диссоциацию клеток с использованием трипсина или эквивалента, (ii) остановку диссоциации избытком культуральной среды или улучшенной DMEM/F12, (iii) центрифунгирование клеток с ускорением от 10×g до 10000×g в течение 1-30 минут, (iv) ресуспендирование клеток в культуральной среде и определение общего количества клеток и жизнеспособности, (v) добавление среды для криоконсервации с получением конечной концентрации диметилсульфоксида (ДМСО) от 5 до 30%, (vi) деление множества клеток на аликвоты в каждый криофлакон, (vii) замораживание каждого флакона с использованием программируемого криозамораживателя, и (viii) помещение каждого флакона с клетками в жидкий N2. Может использоваться любой подходящий метод замораживания, известный в уровне техники. Например, клетки могут замораживать с использованием контейнера для замораживания Cryo 1C, помещенного в морозильную камеру на -80°C. В некоторых вариантах осуществления эквивалентом трипсина является TrypLE, такой как TrypLE Express или TrypLE Select (например, ThermoFisher или Invitrogen). В некоторых вариантах осуществления среда для криоконсервации включает культуральную среду и 20% ДМСО. В некоторых вариантах осуществления среду для криоконсервации добавляют к клеткам и культуральной среде клеток в соотношении 1:1 с получением конечной концентрации ДМСО 10%. В некоторых вариантах осуществления множество ретинальных клеток-предшественников делят на аликвоты и замораживают в количестве приблизительно от 0,5×106 до 50×106 клеток на криофлакон. В некоторых вариантах осуществления множество ретинальных клеток-предшественников делят на аликвоты и замораживают в количестве от приблизительно 0,5×106 до приблизительно 40×106 клеток на мл среды (например, культуральной среды с 10% ДМСО), от приблизительно 0,5×106 до приблизительно 20×106 клеток/мл среды, от приблизительно 0,5×106 до приблизительно 10×106 клеток/мл среды, от приблизительно 1×106 до приблизительно 40×106 клеток на мл среды, от приблизительно 1×106 до приблизительно 20×106 клеток/мл среды, от приблизительно 1×106 до приблизительно 10×106 клеток/мл среды, от приблизительно 10×106 до приблизительно 30×106 клеток/мл среды, от приблизительно 10×106 до приблизительно 20×106 клеток/мл среды, от приблизительно 2×106 до приблизительно 10×106 клеток/мл среды, от приблизительно 2×106 до приблизительно 8×106 клеток/мл среды или от приблизительно 2×106 до приблизительно 5×106 клеток/мл среды. В некоторых вариантах осуществления множество ретинальных клеток-предшественников делят на аликвоты и замораживают в количестве от приблизительно 0,5×106 до приблизительно 20×106 клеток/мл среды. В некоторых вариантах осуществления множество ретинальных клеток-предшественников делят на аликвоты и замораживают в количестве от приблизительно 2×106 до приблизительно 8×106 клеток/мл среды. В некоторых вариантах осуществления множество ретинальных клеток-предшественников делят на аликвоты и замораживают в количестве приблизительно 10×106 клеток/мл среды. В некоторых вариантах осуществления криофлакон содержит приблизительно 1 мл, приблизительно 2 мл, приблизительно 3 мл, приблизительно 4 мл, приблизительно 5 мл, приблизительно 6 мл, приблизительно 7 мл, приблизительно 8 мл, приблизительно 9 мл или приблизительно 10 мл среды для криоконсервирования (например, культуральной среды с ДМСО) и ретинальные клетки-предшественники. В некоторых вариантах осуществления криофлакон содержит приблизительно 1 мл среды и ретинальные клетки-предшественники. В некоторых вариантах осуществления криофлакон содержит приблизительно 5 мл среды и ретинальные клетки-предшественники.
[00149] В некоторых вариантах осуществления состав конечного продукта, как было показано, сохраняет оптимальную жизнеспособность (например, по меньшей мере 85%) в течение до 4 часов или больше (например, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24 или больше) при хранении во льду (например, при 0-4°C). Это, в свою очередь, позволяет локально транспортировать препарат клеток в региональные клинические центры.
[00150] Дальнейшее размножение клеток в условиях низкого содержания кислорода можно применять для значительного повышения выхода клеток после каждого изъятия у донора. Например, в некоторых вариантах осуществления клетки могут пассировать в общей сложности 5-12 (т.е. 5, 6, 7, 8, 9, 10, 11 или 12) или более раз. В качестве неограничивающего примера, в одном варианте осуществления, это может включать вторичное размножение в условиях низкого содержания кислорода 3-6 пассажей (т.е. 3, 4, 5 или 6), которое происходит после 4-6 пассажей (т.е. 4, 5 или 6) в условиях стандартного содержания кислорода. Однако специалистам будет очевидно, что общее количество пассажей может составлять приблизительно 1-32 или больше пассажей (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32 или больше), и это может включать вторичное размножение в учловиях низкого содержания кислорода 1-20 или больше пассажей (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19 или 20 или больше). Определение подходящего общего количества пассажей, а также количества пассажей при низком содержании кислорода находится в объеме средней квалификации в данной области. Использование таких вторичных пассажей культуры при низком содержании кислорода значительно повышает выход из рабочего банка hRPC (например, таких, которые получены в результате культивирования в условиях стандартного содержания кислорода). Например, клетки из банка стандартного нормального содержания кислорода могут размораживать и затем размножать еще 1-20 (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19 или 20) пассажей в условиях низкого содержания кислорода.
[00151] Хотя можно использовать меньше пассажей клеток при низком содержании кислорода, полученный выход, скорее всего, будет ниже. Более того, хотя также можно использовать больше пассажей клеток при низком содержании кислорода, это потенциально может вызывать повышенный риск того, что полученный продукт окажется непригодным из-за потенциального фенотипического изменения с потерей эффективности и/или накопления нежелательных генетических аномалий.
[00152] После вторичных пассажей культуры при низком содержании кислорода, в некоторых вариантах осуществления, ретинальные клетки-предшественники подвергаются "периоду восстановления", в котором им позволяют расти в условиях стандартного содержания кислорода в течение короткого периода времени, от 1 часа до 5 дней (т.е. 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 24, 36, 48, 60, 72, 84, 96, 108 или 120 часов). В альтернативных вариантах осуществления в этот период восстановления клеткам позволяют расти, не подвергая дальнейшему пассированию.
[00153] Таким образом, в одном неограничивающем примере ретинальные клетки-предшественники для применения в любых из композиций и способов, описанных в настоящем документе, могут быть получены с применением "гибридного" метода, включающего: (a) культивирование в условиях стандартного содержания кислорода в течение некоторого числа пассажей, с последующим (b) культивированием в условиях низкого содержания кислорода в течение некоторого числа пассажей, необязательно с последующим (c) культивированием в условиях стандартного содержания кислорода в течение заданного периода времени без какого-либо дальнейшего пассирования. Определение подходящего числа пассажей в условиях стандартного содержания кислорода и/или в условиях низкого содержания кислорода, а также подходящей длительности периода восстановления находится в рамках среднего уровня квалификации в данной области.
[00154] Получаемый в результате клеточный продукт, полученный с применением этой новой методики культивирования, был протестирован in vitro и на животных, при этом наблюдали результаты, аналогичные результатам с клеточным продуктом, который не подвергали вторичному культивированию при низком содержании кислорода.
[00155] Специалистам в данной области известно, что добавление такого вторичного компонента низкого содержания кислорода в общий процесс способствует автоматизации способов производства, поскольку не нужны сложные процедуры, такие как начальное разрезание и посев в планшеты, причем выполненное пассирование будет полностью стандартизированным с клетками, которые сильно пролиферируют.
[00156] RPC можно дополнительно получать посредством конверсии существующих RPC в индуцированные плюрипотентные стволовые клетки (иПСК) с последующей экспансией в более примитивном, пролиферативном состоянии. Затем иПСК можно повторно дифференцировать обратно в RPC с использованием любого метода(ов), известного в данной области. В такой ситуации предыдущий эпигенетический импринтинг, представленный в виде RPC, помогает перенаправлять клетки обратно в их исходное состояние, увеличивая, таким образом, выход RPC и/или способствуя безопасности аллогенного продукта с высоким выходом (то есть, путем предотвращения контаминации плюрипотентными клетками). Такая методика экспансии может обеспечить очень большой и потенциально бесконечный (не подверженный старению) источник RPC, полученный из клинически подтвержденных образцов RPC, без необходимости повторного получения фетальной ткани.
[00157] RPC могут быть дополнительно получены из линии плюрипотентных клеток, будь то одна такая линия, полученная из RPC, как указано выше, или нет. Такое происхождение может включать частичную дифференцировку в "эмбриоидные тельца", содержащие примитивные структуры сетчатки, т.е. производные глазного бокала, из которых могут быть получены, очищены и затем размножены RPC.
[00158] Подобные способы могут проводить с использованием аутологичных клеток, когда донорские клетки для иПСК получают из эпителия реснитчатого тела или из радужной оболочки, поскольку обе этих ткани доступны для хирурга и имеют импринтинг развития, который перекрывается с сетчаткой (хотя и не является полностью таким же).
Композиции и составы
[00159] Ретинальные клетки-предшественники и популяции клеток, описанные в настоящем документе, могут быть включены в композицию для введения любыми различными способами, в том числе перорально, парентерально, ингаляционно в виде спрея, назально, наружно, интратекально, интрацеребрально, эпидурально, интракраниально или ректально. Композиции и составы, раскрытые в настоящем документе, могут содержать фармацевтически или ветеринарно приемлемые жидкости, носители, адъюванты и растворители и могут иметь форму жидкостей, таблеток, капсул, имплантатов, аэрозолей, гелей, липосом, наночастиц и т.п.
[00160] Ретинальные клетки-предшественники и популяции клеток могут вводить субъекту в форме фармацевтических или ветеринарных композиций. Фраза "фармацевтически приемлемый" относится к молекулярным единицам и композициям, которые не вызывают нежелательных, аллергических или других неблагоприятных реакций при введении животному или человеку. При использовании в настоящем документе "фармацевтически приемлемый носитель" включает любые возможные водные и неводные носители, которые включают воду, этанол, полиолы (такие как глицерин, пропиленгликоль, полиэтиленгликоль и т.п.) и их подходящие смеси, растительные масла, такие как оливковое масло и пригодные для инъекций органические сложные эфиры, такие как этилолеат.
[00161] Фармацевтически приемлемый носитель необязательно может включать белок (например, человеческий белок), который является белком, который может улучшить выживание клеток в процессе получения.
[00162] Аналогичным образом, любые из композиций или препаратов, раскрытых в настоящем документе, также могут включать вспомогательное вещество HypoThermosol®-FRS (HTS-FRS) (BioLife Solutions, Inc.), которое является доступным в продаже раствором/составом для гипотермического хранения, разработанным для снижения уровня некроза и апоптоза после хранения клеток, подвергающихся длительному гипотермическому (2°C-10°C) хранению (см., например, патент США 6,921,633; патент США 6,632,666; и WO 2005/009766).
[00163] Добавление белка и/или HTS можно использовать для увеличения времени жизнеспособности ретинальных клеток-предшественников в любом из препаратов, раскрытых в настоящем документе, до приблизительно 24 часов (т.е. приблизительно на 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23 или 24 часа).
[00164] Надлежащую текучесть можно поддерживать, например, путем применения материалов для получения покрытия, таких как лецитин, путем поддержания требуемого размера частиц в случае дисперсий и при использовании поверхностно-активных веществ. Такие композиции также могут содержать адъюванты, такие как консерванты, смачивающие вещества, эмульгаторы и дисперсанты. Предотвращение присутствия микроорганизмов можно обеспечивать как процедурами стерилизации, так и путем включения различных антибактериальных и противогрибковых средств, например, парабена, хлорбутанола, сорбиновой кислоты и т.п. Также может быть желательным включать в композиции изотонические вещества, такие как сахара, хлорид натрия и т.п. Кроме того, пролонгированное всасывание инъекционной фармацевтической формы можно обеспечить путем включения веществ, замедляющих абсорбцию, таких как моностеарат алюминия и желатин. Они должны быть стабильными в условиях производства и хранения и должны быть предохранены от контаминирующего действия микроорганизмов, таких как бактерии и грибы. Применение таких сред и веществ для фармацевтически активных субстанций хорошо известно в данной области.
[00165] Субъекту надлежит вводить эффективное количество ретинальных клеток-предшественников или популяций клеток. "Эффективное количество" или "терапевтически эффективное количество" относится к такому количеству композиции, которое производит требуемый эффект. Эффективное количество будет зависеть, например частично, от доставляемой молекулы или вещества (в данном случае ретинальных клеток-предшественников или популяций клеток), от показания, по которому применяют терапевтическое средство, от пути введения и размера (массы тела, площади поверхности тела или размера органа), и состояния (возраста и общего состояния здоровья) субъекта или пациента. Соответственно, лечащий врач или терапевт может подбирать дозу и изменять способ введения для получения оптимального терапевтического эффекта. Эффективное количество конкретного средства для определенной цели можно определять с помощью методов, хорошо известных специалистам в данной области. Для любой композиции, определенной в настоящем документе, эффективное количество может быть оценено первоначально либо в анализах с культурами клеток, либо в моделях на животных, таких как мыши, крысы, кролики, собаки, свиньи или обезьяны. Модель на животных также может использоваться для определения подходящего диапазона концентраций и пути введения. Такую информацию затем можно использовать для определения подходящих доз и способов введения человеку.
[00166] Примеры эффективных количеств композиций, описанных в настоящем документе, включают суспензии клеток в объеме 5 мкл, 10 мкл, 15 мкл, 20 мкл, 25 мкл, 50 мкл, 100 мкл, 150 мкл, 200 мкл, 250 мкл, 300 мкл, 350 мкл, 400 мкл, 450 мкл, 500 мкл или с любым промежуточным приращением, до 5000 мкл (5 мл) (например. 500, 550, 600, 650, 700, 750, 800, 850, 900, 950, 1000, 1050, 1100, 1150, 1200, 1250, 1300, 1350, 1400, 1450, 1500, 1550, 1600, 1650, 1700, 1750, 1800, 1850, 1900, 1950, 2000, 2050, 2100, 2150, 2200, 2250, 2300, 2350, 2400, 2450, 2500, 2550, 2600, 2650, 2700, 2750, 2800, 2850, 2900, 2950, 3000, 3050, 3100, 3150, 3200, 3250, 3300, 3350, 3400, 3450, 3500, 3550, 3600, 3650, 3700, 3750, 3800, 3850, 3900, 3950, 4000, 4050, 4100, 4150, 4200, 4250, 4300, 4350, 4400, 4450, 4500, 4550, 4600, 4650, 4700, 4750, 4800, 4850, 4900, 4950 или 5000 мкл).
[00167] Нижние и верхние границы значений объема лимитированы системой и/или способом доставки. См., например, Kayikcuiglu, O. R. et al, (2006) Retina 26(9): 1089-90. Например, верхняя граница значений объема при введении без витрэктомии составляет приблизительно 200 мкл из-за увеличения внутриглазного давления. Верхняя граница объема при введении с витрэктомией в полость стекловидного тела ограничена объемом полости стекловидного тела и может содержать до 5 мл или больше. Верхняя граница субретинальной инъекции может составлять до 200 мкл из-за отслоения сетчатки. В альтернативных вариантах осуществления эти объемы включают приблизительно от 1000 до 10 миллионов клеток на дозу или 1000-2000 клеток на дозу, 2000-3000 клеток на дозу, 3000-4000 клеток на дозу, 400-5000 клеток на дозу, 5000-6000 клеток на дозу, 6000-7000 клеток на дозу, 7000-8000 клеток на дозу, 8000-9000 клеток на дозу, 9000-10000 клеток на дозу, 10000-15000 клеток на дозу, 15000-20000 клеток на дозу, 20000-25000 клеток на дозу, 25000-30000 клеток на дозу, 30000-35000 клеток на дозу, 35000-40000 клеток на дозу, 40000-45000 клеток на дозу, 45000-50000 клеток на дозу, 50000-55000 клеток на дозу, 55000-60000 клеток на дозу, 60000-65000 клеток на дозу, 65000-70000 клеток на дозу, 70000-75000 клеток на дозу, 75000-80000 клеток на дозу, 80000-85000 клеток на дозу, 85000-90000 клеток на дозу, 90000-95000 клеток на дозу, 95000-100000 клеток на дозу, 100000-125000 клеток на дозу, 125000-150000 клеток на дозу, 150000-200000 клеток на дозу, 200000-250000 клеток на дозу, 250000-300000 клеток на дозу, 300000-350000 клеток на дозу, 350000-400000 клеток на дозу, 400000-450000 клеток на дозу, 450000-500000 клеток на дозу, 500000-550000 клеток на дозу, 550000-600000 клеток на дозу, 600000-650000 клеток на дозу, 650000-700000 клеток на дозу, 700000-750000 клеток на дозу, 750000-800000 клеток на дозу, 800000-850000 клеток на дозу, 850000-900000 клеток на дозу, 900000-950000 клеток на дозу, 950000-1000000 клеток на дозу или любое промежуточное приращение от 1000 клеток и до 10 миллионов клеток на дозу. Дозы, конечно, могут изменяться в зависимости от частоты и длительности введения. В альтернативных вариантах осуществления доза клеток в композициях, описанных в настоящем документе, содержит большое количество клеток в малом объеме, такое как, например, 0,5 миллиона клеток в 100 мкл. Количество клеток можно посчитывать с помощью любого способа, известного в уровне техники, такого как гемоцитометр, спектрофотометрия, счетчиком Коултера, проточная цитометрия и т.д. Дозу могут вводить однократно или могут вводить в течение курса из нескольких процедур лечения.
[00168] Композиции также могут быть изготовлены для парентерального введения в глаз (в частности, в полость стекловидного тела или субретинальное пространство), полость стекловидного тела или субретинальное пространство, сетчатку, головной мозг, нерв или ЦНС путем транссклеральной доставки, или с применением любого способа или протокола, известного в данной области, например, включающих транссклеральную доставку, как описано в патенте США 7,585,517; устройство доставки с замедленным высвобождением для доставки внутрь глаза пациента, как описано в патенте США 7,883,717; устройство для введения в область стекловидного тела глаза, как описано в патентах США 5,378,475 или 5,466,233; или при помощи шприца для подкожных инъекций или введения под углом, например, как описано в публикации заявок на патент США 20110112470 или 20100256597 (в которых описана микроигла для направленного введения в глаз пациента); или посредством гидрогеля гидрофильного полимера с размерами, позволяющими проникать через слезные точки, например, как описано в публикации заявки на патент США 20100209478; или устройство, обеспечивающее доступ в субретинальное пространство в глазу человека, например, как описано в публикации заявки на патент США 20100191176. Парацентез передней камеры глаза также могут выполнять, как определяет специалист в данной области. Способы не требуют ушивания глазного яблока во время и/или после процедуры, особенно в случае интравитреального введения. Однако это может быть необходимо в способах, в которых используют процедуру витрэктомии, например, при введении клеток в субретинальное пространство.
[00169] Композиции, раскрытые в настоящем документе, также могут быть изготовлены для интратекального, внутрицеребрального, эпидурального, подкожного, внутривенного, внутримышечного и/или внутриартериального введения; например, как описано в публикации заявки на патент США 200500480021; путем инъекции, но также включая различные методы инфузии. Введение могут осуществлять с использованием катетеров или насосов, например, интратекального насоса или имплантируемого медицинского устройства. В альтернативных вариантах осуществления способы также могут включать введение или трансплантацию имплантатов и искусственных органов, биореакторные системы, системы культивирования клеток, планшеты, чашки, пробирки, бутылки и флаконы и т.п., содержащие ретинальные клетки-предшественники, популяции клеток или композиции, раскрытые в настоящем документе, такие как описанные в патентах США 7,388,042; 7,381,418; 7,379,765; 7,361,332; 7,351,423; 6,886,568; 5,270,192; и в публикациях заявок на патент США 20040127987; 20080119909; 20080118549; 20080020015; 20070254005; 20070059335; 20060128015.
[00170] Композиции, содержащие ретинальные клетки-предшественники или популяции клеток, необязательно могут вводить совместно с одним или более лекарственными средствами. Неограничивающие примеры лекарственных средств могут включать антиангиогенные средства, такие как ангиостатин, анекортава ацетат, тромбоспондин, ингибиторы VEGF-стимулируемых рецепторов тирозинкиназ и средства против фактора роста эндотелия сосудов (VEGF), такие как ранибизумаб и бевацизумаб, пегаптаниб, сунитиниб и сорафениб, а также любой из множества известных низкомолекулярных ингибиторов и ингибиторов транскрипции, обладающих антиангиогенным действием; классы известных офтальмологических средств, включающие: средства для лечения глаукомы, такие как антагонисты адренергических рецепторов, включающие, например, бета-блокаторы, такие как ацетбутолол, атенолол, бисопролол, карведилол, асмолол, лабеталол, надолол, пенбутолол, пиндолол, пропранолол, метипранолол, бетаксолол, картеолол, левобетаксолол, левобунолол и тимолол; агонисты адренергических рецепторов или симпатомиметические средства, такие как эпинефрин, дипивефрин, клонидин, апарклонидин и бримонидин; парасимпатомиметики или холинергические агонисты, такие как пилокарпин, карбахол, фосфолин-иод и физостигмин, салицилат, ацетилхолинхлорид, эсерин, диизопропилфторфосфат, демекария бромид); мускариновые средства; ингибиторы карбоангидразы, включая средства для наружного и/или системного применения, например, ацетозоламид, бринзоламид, дорзоламид и метазоламид, этоксзоламид, диамокс и дихлорфенамид; мидриатические/циклоплегические средства, такие как атропин, циклопентолат, сукцинилхолин, гоматропин, фенилэфрин, скополамин и тропикамид; простагландины, такие как простагландин F2-альфа, антипростагландины, предшественники простагландинов или аналоги простагландина, такие как биматопрост, латанопрост, травопрост и/или унопростон.
[00171] Другие примеры лекарственных средств также могут включать, без ограничения перечисленными, противовоспалительные средства, в том числе, например, глюкокортикоиды и кортикостероиды, такие как бетаметазон, кортизон, дексаметазон, дексаметазон-21-фосфат, метилпреднизолон, преднизолон-21-фосфат, преднизолона ацетат, преднизолон, флуорометолон, лотепреднол, медризон, флуоцинолона ацетонид, триамцинолона ацетонид, триамцинолон, беклометазон, будесонид, флунизолид, фторметолон, флутиказон, флудрокортизон, гидрокортизон, гидрокортизона ацетат, лотепреднол, римексолон и нестероидные противовоспалительные средства, в том числе, например, аспирин, диклофенак, флурбипрофен, ибупрофен, бромфенак, непафенак и кеторолак, салицилат, индометацин, наксопрен, пироксикам и набуметон, дифлунизал, этодолак, фенопрофен, флурбипрофен, индометацин, кетопрофен, меклофенамат, мефенамовую кислоту, мелоксикам, набуметон, оксапрозин, пироксикам, салсалат, сулиндак и толметин; ингибиторы ЦОГ-2, такие как целекоксиб, рофекоксиб и валдекоксиб; противоинфекционные или противомикробные средства, такие как антибиотики, в том числе, например, тетрациклин, хлортетрациклин, бацитрацин, неомицин, полимиксин, грамицидин, цефалексин, окситетрациклин, хлорамфеникол, рифампицин, ципрофлоксацин, тобрамицин, гентамицин, эритромицин, пенициллин, сульфаниламиды, сульфадиазин, сульфацетамид, сульфаметизол, сульфизоксазол, нитрофуразон, пропионат натрия, аминогликозиды, такие как гентамицин, тобрамицин, амикацин и стрептомицин; фторхинолоны, такие как ципрофлоксацин, гатифлоксацин, левофлоксацин, моксифлоксацин, норфлоксацин, офлоксацин; бацитрацин, эритромицин, фузидовая кислота, неомицин, полимиксин B, грамицидин, триметоприм и сульфацетамид; противогрибковые средства, такие как амфотерицин B, каспофунгин, клотримазол, флуконазол, итраконазол, кетоконазол, вориконазол, тербинафин, нистатин и миконазол; противомалярийные средства, такие как хлорохин, атоваквон, мефлохин, примахин, хинидин и хинин; противомикобактериальные средства, такие как этамбутол, изониазид, пиразинамид, рифампин и рифабутин; и/или противопаразитарные средства, такие как альбендазол, мебендазол, тиобендазол, метронидазол, пирантел, атоваквон, йодохинол, ивермектин, паромицин, празиквантел и триметрексат.
[00172] Другие примеры лекарственных средств также могут включать, без ограничения перечисленными, противовирусные средства, такие как идоксуридин, трифтортимидин, ацикловир, цидофовир, фамцикловир, ганцикловир, валацикловир, валганцикловир, видарабин, трифлуридин и фоскарнет; ингибиторы протеаз, такие как ритонавир, саквинавир, лопинавир, индинавир, атазанавир, ампренавир и нелфинавир; нуклеотидные/нуклеозидные/ненуклеозидные ингибиторы обратной транскриптазы, такие как абакавир, ddl, 3TC, d4T, ddC, тенофовир и эмтрицитабин, делавирдин, эфавиренз и невирапин; другие противовирусные средства, такие как интерфероны, рибавирин и трифлуридин; антибактериальные средства, включая кабапенемы, такие как эртапенем, имипенем и меропенем; цефалоспорины, такие как цефадроксил, цефазолин, цефдинир, цефдиторен, цефалексин, цефаклор, цефепим, цефоперазон, цефотаксим, цефотетан, цефокситин, цефподоксим, цефпрозил, цефтаксидим, цефтибутен, цефтизоксим, цефтриаксон, цефуроксим и лоракарбеф; другие макролиды и кетолиды, такие как азитромицин, кларитромицин, диритромицин и телитромицин; пенициллины (с клавуланатом и без), в том числе амоксициллин, ампициллин, пивампициллин, диклоксациллин, нафциллин, оксациллин, пиперациллин и тикарциллин; тетрациклины, такие как доксициклин, миноциклин и тетрациклин; и/или другие антибактериальные средства, такие как азтреонам, хлорамфеникол, клиндамицин, линезолид, нитрофурантоин и ванкомицин.
[00173] Другие примеры лекарственных средств также могут включать, без ограничения перечисленными, иммуномодулирующие средства, такие как противоаллергические средства, в том числе, например, хромогликат натрия, антазолин, метапирилин, хлорфенирамин, цетризин, пириламин, профенпиридамин; алдеслейкин, адалимумаб, азатиоприн, базиликсимаб, даклизумаб, этанерцепт, гидроксихлорохин, инфликсимаб, лефлуномид, метотрексат, микофенолата мофетил и сульфасалазин; антигистаминные средства, такие как азеластин, эмедастин, лоратадин, дезлоратадин, цетиризин, дифенгидрамин, хлорфенирамин, дексхлорфенирамин, клемастин, ципрогептадин, фексофенадин, гидроксизин, прометазин и левокабастин; иммунологические средства (например, вакцины и иммуностимуляторы); средства, стабилизирующие тучные клетки, такие как кромолин натрия, кетотифен, лодоксамид, недокримил, олопатадин и пемироласт, средства для абляции цилиарного тела, такие как гентимицин и цидофовир; и другие офтальмологические средства, такие как вертепорфин, пропаракаин, тетракаин, циклоспорин и пилокарпин; ингибиторы рецепторов гликопротеинов клеточной поверхности; антиконгестанты, такие как фенилэфрин, нафазолин, тетрагидразолин; липиды или гипотензивные липиды; дофаминергические агонисты и/или антагонисты, такие как хинпирол, фенолдопам и ибопамин; ингибиторы вазоспазма; сосудорасширяющие средства; гипотензивные средства; ингибиторы ангиотензинпревращающего фермента (АПФ); антагонисты рецептора ангиотензина-1, такие как олмесартан; ингибиторы микротрубочек; ингибиторы молекулярных моторов (динеина и/или кинезина); средства, регулирующие актиновый цитоскелет, такие как цитохалазин, латрункулин, свинхолид A, этакриновая кислота, H-7 и ингибиторы Rho-киназы (ROCK); ингибиторы ремоделирования; модуляторы внеклеточного матрикса, такие как трет-бутилгидрохинолон и AL-3037A; агонисты и/или антагонисты аденозиновых рецепторов, такие как N-6-циклофексиладенозин и (R)-фенилизопропиладенозин; агонисты серотонина; гормональные средства, такие как эстрогены, эстрадиол, прогестагенные гормоны, прогестерон, инсулин, кальцитонин, паратиреоидный гормон, пептид и вазопрессин, рилизинг-факторы гипоталамуса; антагонисты фактора роста или факторы роста, в том числе, например, эпидермальный фактор роста, фактор роста фибробластов, фактор роста тромбоцитов, трансформирующий фактор роста бета, соматотропин, фибронектин, фактор роста соединительной ткани, костные морфогенетические белки (BMP), нейротрофический фактор головного мозга (BDNF), цилиарный нейротрофический фактор (CNTF), нейротрофический фактор линии глиальных клеток (GDNF), инсулиноподобный фактор роста (IGF) и фактор роста нервов (NGF); и/или цитокины, такие как интерлейкины, CD44, кохлин, остеопонтин, плеотропин, мидкин, фактор роста эндотелия сосудов (VEGF) и сывороточные амилоиды, такие как сывороточный амилоид А.
[00174] Другие терапевтические средства могут включать, без ограничения перечисленными, нейропротекторные средства, такие как любезол, нимодипин и родственные соединения, включая средства, улучшающие кровообращение, блокаторы натриевых каналов, ингибиторы глутамата, такие как мемантин, нейротрофические факторы, ингибиторы синтазы оксида азота; ловушки свободных радикалов или антиоксиданты; хелатообразующие соединения; ингибиторы связанных с апоптозом протеаз; соединения, которые снижают синтез нового белка; радиотерапевтические средства; средства фотодинамической терапии; средства генотерапии; генетические модуляторы; и средства для лечения синдрома сухого глаза, такие как циклоспорин A, противомикробные средства и гиалуронат натрия; альфа-блокаторы, такие как доксазозин, празозин и теразозин; блокаторы кальциевых каналов, такие как амлодипин, бепридил, дилтиазем, фелодипин, исрадипин, никардипин, нифедипин, нисолдипин и верапамил; другие антигипертензивные средства, такие как клонидин, диазоксид, фенолдопан, гидралазин, миноксидил, нитропруссид, феноксибензамин, эпопростенол, толазолин, трепростинил и средства на основе нитратов; антикоагулянты, включая гепарины и гепариноиды, такие как гепарин, далтепарин, эноксапарин, тинзапарин и фондапаринукс; другие антикоагулянты, такие как гирудин, апротинин, аргатробан, бивалирудин, дезирудин, лепирудин, варфарин и ксимелагатран; и/или антиагрегантные средства, такие как абциксимаб, клопидогрел, дипиридамол, оптифибатид, тиклопидин и тирофибан.
[00175] Другие терапевтические средства могут включать, без ограничения перечисленными, ингибиторы простагландина PDE-5 и другие простагландиновые средства, такие как алпростадил, карбопрост, силденафил, тадалафил и варденафил; ингибиторы тромбина; антитромбогенные средства; средства, препятствующие агрегации тромбоцитов; тромболитики и/или фибринолитики, такие как алтеплаза, анистреплаза, ретеплаза, стрептокиназа, тенектеплаза и урокиназа; антипролиферативные средства, такие как сиролимус, такролимус, эверолимус, зотаролимус, паклитаксел и микофеноловая кислота; гормональные средства, в том числе левотироксин, флуоксиместрон, метилтестостерон, нандролон, оксандролон, тестостерон, эстрадиол, эстрон, эстропипат, кломифен, гонадотропины, гидроксипрогестерон, левоноргестрел, медроксипрогестерон, мегестрол, мифепристон, норэтиндрон, окситоцин, прогестерон, ралоксифен и тамоксифен; противоопухолевые средства, в том числе алкилирующие средства, такие как кармустин, ломустин, мелфалан, цисплатин, фторурацил 3, и средства, подобные прокарбазиновым антибиотикам, такие как блеомицин, даунорубицин, доксорубицин, идарубицин, митомицин и пликамицин; антипролиферативные средства (такие как 1,3-цис-ретиноевая кислота, 5-фторурацил, таксол, рапамицин, митомицин C и цисплатин); антиметаболиты, такие как цитарабин, флударабин, гидроксимочевина, меркаптопурин и 5-флуроурацил (5-ФУ); иммуномодулирующие средства, такие как алдеслейкин, иматиниб, ритуксимаб и тозитумомаб; ингибиторы митоза доцетаксел, этопозид, винбластин и винкристин; радиоактивные вещества, такие как стронций-89; и/или другие противоопухолевые средства, такие как иринотекан, топотекан и митотан.
Введение RPC и способы лечения
[00176] Также в настоящем документе предложены способы и применения культивированных ретинальных клеток-предшественников, полученных в виде суспензии клеток и применяемых в качестве аллогенных трансплантатов для лечения пациентов с заболеванием сетчатки. Например, в настоящем документе предложены клеточные терапии, включающие или состоящие из применения культивированных гетерогенных популяций клеток из незрелой сетчатки млекопитающего, например, человека.
[00177] Популяции клеток и соответствующие композиции, описанные в настоящем документе, могут быть предоставлены субъекту или пациенту множеством различных способов. В качестве неограничивающего примера их могут доставлять локально, например, в участок фактического или потенциального повреждения или заболевания. В некоторых вариантах осуществления их вводят с использованием шприца или иглы для инъекции композиций в участок возможного или фактического повреждения или заболевания. В других вариантах осуществления их вводят системно, например, вводят в кровоток внутривенно или внутриартериально. Конкретный путь введения в значительной степени будет зависеть от локализации и характера заболевания или повреждения, подлежащего лечению или профилактике. Таким образом, способы, описанные в настоящем документе, включают получение популяции или композиции клеток любым известным и доступным способом или путем, включающим, без ограничения перечисленными, внутриглазное, пероральное, парентеральное, внутривенное, внутриартериальное, интраназальное и внутримышечное введение.
[00178] Определение подходящих доз и схем лечения может быть с легкостью выполнено на основе информации, общеизвестной в данной области, и полученной врачом.
[00179] В качестве неограничивающего примера доза клеток может составлять от приблизительно 0,3 до приблизительно 0,5 миллиона клеток (например, 0,3, 0,31, 0,32, 0,33, 0,34, 0,35, 0,36, 0,37, 0,38, 0,39, 0,4, 0,41, 0,42, 0,43, 0,44, 0,45, 0,46, 0,47, 0,48, 0,49 или 0,5 миллиона клеток) или 0,5-3 миллиона клеток (например, 0,5, 0,6, 0,7, 0,8, 0,9, 1,0, 1,1, 1,2, 1,3, 1,4, 1,5, 1,6, 1,7, 1,8, 1,9, 2,0, 2,1, 2,2, 2,3, 2,4, 2,5, 2,6, 2,7, 2,8, 2,9 или 3 миллиона клеток).
[00180] Результаты эффективности, наблюдаемые для обоих диапазонов доз, примерно одинаковы. Однако существует возможный повышенный риск, что при больших дозах (например, 2-9 миллионов клеток) клетки будут персистировать на зрительной оси, приликрепляться к задней мембране хрусталика и/или попадать в переднюю камеру (псевдогипопион), если в глазу пациента ослаблены цилиарные связки. Более того, специалистам в данной области будет очевидна вероятность того, что продолжительность выживания трансплантата может быть пропорциональна дозе и, таким образом, исходному размеру трансплантата.
[00181] Частота введения доз аллогенных hRPC в полость стекловидного тела будет иметь большое значение. В различных вариантах осуществления последующие дозы (т.е. "повторные дозы") можно вводить в один и тот же глаз пациента или в другой глаз. Повторное введение во второй глаз как в моделях на животных, так и у ряда пациентов было выполнено без последующих иммунных осложнений, что позволяет предположить, что введение повторных доз будет хорошо переноситься при двустороннем введении (и, предположительно, в тот же глаз, как выполняли на животных до 3 раз).
[00182] Трансплантаты могут выживать у пациентов с RP в течение года и более. Однако, поскольку они имеют тенденцию исчезать из стекловидного тела приблизительно через 1-1,5 года, это указывает на то, что введение повторной дозы в течение приблизительно 1-2 лет может быть не таким агрессивным и, фактически, в большинстве случаев, в будущем может стать нормой.
[00183] В любом из способов, раскрытых в настоящем документе, лечение может включать одно лечение или несколько (например, 2, 3, 4, 5, 6 или более) курсов лечения. В частности, для профилактических целей в некоторых вариантах осуществления предусмотрено, что очищенные популяции клеток вводят после стресса, который потенциально мог вызывать повреждение сетчатки.
[00184] В одном варианте осуществления популяции и композиции клеток могут вводить локально в виде однократной инъекции в полость стекловидного тела или субретинальное пространство субъекта.
[00185] Хотя композиции и способы, описанные в настоящем документе, не ограничиваются каким-либо конкретным механизмом действия, примерный механизм действия является диффузным и/или трофическим. Доказательства согласуются с концепцией трофического перепрограммирования отмирающих колбочек реципиента, что приводит к переключению с апоптотического пути на восстановление способности световой обработки. Этот процесс может быть прямым или косвенным. Не исключается вовлечение других тканей глаза. Этот механизм позволяет помещать трансплантат из гетерогенной смеси фетальных нервных клеток сетчатки в стекловидное тело или субретинальное пространство.
[00186] Введение в стекловидное тело усиливает лечебный эффект на основе диффузии. Этот механизм может позволить помещать трансплантат из гетерогенных смесей фетальных нервных клеток сетчатки вне зрительной оси, но при этом лечить желтое пятно пациента. Более того, витреальное введение используют для значительного упрощения лечения, поскольку такой пример лечения может повысить доступность для нуждающихся пациентов во всем мире. Кроме того, витреальное введение может способствовать иммунной толерантности, поскольку стекловидное тело удалено от сосудов. Специалистам в данной области будет очевидно, что введение в стекловидное тело позволяет избежать возможных осложнений при субретинальной хирургии, избежать риска общей анестезии, не требует создания отверстия (ретинотомии) в сетчатке (что повышает риск отслоения сетчатки, кровотечения) и/или не требует, чтобы сетчатка пациента подвергалась фокальной отслойке (фокальная отслойка может привести к повреждению или потере фоторецепторов, разрывам сетчатки, кровотечению, полному отслоению сетчатки, а при пигментном ретините (RP) отслойка тонкой, атрофической и адгерентной сетчатки будет сложной/рискованной процедурой).
[00187] В некоторых вариантах осуществления клетки помещают в полость стекловидного тела иглой подходящего размера и длины. В идеальном варианте шприц должен иметь минимальное мертвое пространство (например, 1 микролитр), чтобы повысить эффективность доставки и избежать потери продукта из-за удерживания в шприце. Использование короткой иглы (например, калибра 31G с длиной 5/16 дюйма (~8 мм) или 30G с длиной 1/2 дюйма) обеспечивает максимальное удобство (т.е. подходит для использования в клинических или амбулаторных условиях). Однако использование иглы большей длины (например, 27G или 25G с длиной 5/8 дюйма (~16 мм)) обеспечивает оптимальное размещение (при использовании операционного эндоскопа) дальше назад (кзади) в стекловидном теле, ближе к желтому пятну. Определение подходящего размера и длины иглы является рутинной практикой в данной области. При выборе иглы подходящего размера и длины важно, чтобы жизнеспособность клеток оставалась выше необходимого порогового значения после того, как клетки были пропущены через иглу.
[00188] Помещение клеток в переднюю часть стекловидного тела простое и обеспечивает максимальную безопасность и удобство. Напротив, помещение в заднюю часть стекловидного тела (около заднего полюса) требует непосредственной визуализации конца иглы, чтобы избежать проникающего повреждения сетчатки. Однако это может усилить общий эффект лечения и может обеспечить оптимальное помещение и эффективность.
[00189] Хотя замена клеток сетчатки возможна, она не является необходимой для клинической эффективности. Точно так же миграция донорских клеток в сетчатку возможна, но не является необходимой для клинической эффективности; интеграция донорских клеток в сети сетчатки возможна, но не является необходимой для эффективности; интеграция донорских клеток во внешний ядерный слой/желтое пятно сетчатки реципиента возможна, но не является необходимой для эффективности; и/или интеграция донорских клеток в сетчатку возможна, но не является необходимой для длительного выживания трансплантата.
[00190] В некоторых вариантах осуществления клетки RPC можно вводить в полость стекловидного тела, когда, необязательно, не требуется витрэктомия или субретинальная хирургия. Однако некоторые варианты осуществления могут включать необязательное применение одной или нескольких витрэктомий, кор-витрэктомии и/или витреолитического средства для удаления геля стекловидного тела и оптимизации подвижности и проникновения введенных клеток в заднюю часть стекловидного тела (например, оптимальное положение в непосредственной близости от заднего полюса глаза). В некоторых случаях хирургическая витрэктомия может улучшать размещение клеток в глазу.
[00191] Клетки также могут имплантировать (например, путем инъекции) в субретинальное пространство, или их могут имплантировать (например, путем инъекции) в глаз с применением любой стандартной процедуры внутриглазной инъекции, например, с использованием пути подкожного введения или введения под углом. В некоторых вариантах осуществления ретинотомия, внутриглазной газ или силиконовое масло не требуются.
[00192] В альтернативе, необязательно могут проводить парацентез передней камеры, в зависимости от ситуации, по определению специалиста в данной области. В некоторых вариантах осуществления ушивание глазного яблока во время и/или после процедуры не требуется.
[00193] Любой из способов, раскрытых в настоящем документе, может включать этап введения композиций при поверхностной анестезией непосредственно в полость стекловидного тела без потребности в системной иммунодепрессии у субъекта. Кроме того, хотя тканевое типирование трансплантата и определение совместимости с пациентом или субъектом не требуется, его могут выполнять при необходимости, например, с помощью любых методик тканевого типирования и определения совместимости, известных специалистам в данной области.
[00194] Как уже отмечено, в любом из способов, описанных в настоящем документе, можно использовать только поверхностную анестезию, например, без использования местной, регионарной или общей анестезии. Однако в некоторых случаях во время введения могут дополнительно или альтернативно использовать местную, регионарную или общую анестезию. Примеры подходящих местных анестетиков, подходящих для применения в способах, раскрытых в настоящем документе, включают, без ограничения, меприкаин, пропаракаин, прилокаин, ропивакаин, бензокаин, бупивакаин, бутамбена пикрат, хлорпрокаин, кокаин, дибукаин, диметизохин, диклонин, этидокаин, гексилкаин, кетамин, лидокаин, мепивакаин, прамоксин, прокаин, тетракаин, салицилаты и их производные, сложные эфиры, соли и смеси.
[00195] В некоторых вариантах осуществления не требуется проводить никакой противовоспалительной и/или иммунной депрессии (т.е. системной иммунодепрессии). Кроме того, клинический опыт подтверждает, что это не требуется, так как в некоторых случаях выживание трансплантата можно наблюдать в течение многих месяцев, например, включая 1 год и дольше.
[00196] Впрочем, при необходимости могут включать противовоспалительную и/или иммунодепрессивную терапию в виде послеоперационных капель. Например, пациенты после инъекции могут получать наружные стероидные глазные капли с уменьшением вводимой дозы в течение 1 недели или, в альтернативе, до 2 последующих недель, если имеются клинические показания при подтверждении стойкого воспаления после лечения.
[00197] В альтернативных вариантах осуществления нет никакого строгого постельного режима, поддержания послеоперационного положения и/или потребности в принятии положения "лицом вниз". Такие способы могут выполнять амбулаторно и, скорее всего, не потребуют никакого ночного пребывания в стационаре.
[00198] В некоторых вариантах осуществления изобретения во время введения голову пациента отводят назад из откинутого положения сидя, как можно ближе к горизонтальному положению, чтобы максимально увеличить оседание введенных клеток в геле стекловидного тела по направлению к заднему полюсу глаза, который является наиболее важной для зрения частью сетчатки. Пациенты должны сохранять такое положение примерно 30 минут или дольше, если пациент выдерживает это. Кроме того, после введения пациенты также должны оставаться дома, лежа на спине, смотря вверх.
[00199] Любые из композиций и способов, описанных в настоящем документе, включающие или использующие гетерогенные смеси фетальных нервных клеток сетчатки (например, ретинальных клеток-предшественников), предназначены для лечения, уменьшения тяжести или предотвращения заболевания или патологии сетчатки, например, болезни Ашера, пигментного ретинита (RP), дегенеративного заболевания сетчатки, возрастной макулодистрофии (ВМД), влажной формы ВМД или сухой формы ВМД, географической атрофии, заболевания фоторецепторов сетчатки, диабетической ретинопатии, цистоидного макулярного отека, увеита, отслоения сетчатки, травмы сетчатки, макулярных разрывов, макулярной телеангиэктазии, травматического или ятрогенного повреждения сетчатки, заболевания ганглионарных клеток или клеток зрительного нерва, глаукомы или оптической нейропатии, ишемического заболевания сетчатки, такого как ретинопатии недоношенных, окклюзии сосудов сетчатки или ишемической оптической нейропатии; или для улучшения фотопического (дневного) зрения; или для улучшения коррекции остроты зрения, или улучшения функции желтого пятна, или улучшения поля зрения, или улучшения скотопического (ночного) зрения.
[00200] Аналогичным образом, любые из композиций или способов, описанных в настоящем документе, могут применяться для получения быстрого эффекта, наибольшей остроты зрения с коррекцией, улучшенной функции желтого пятна и/или возможности сохранения или восстановления центральной фиксации.
[00201] Использование или практическое применение любых из композиций и способов, раскрытых в настоящем документе, приводит к различным системным преимуществам, например, изменениям внешнего вида у вылеченных лиц, возможно, из-за соматических улучшений, которые могут быть связаны с влиянием света на циркадные ритмы, функцию гипофиза, высвобождение гормонов, сосудистый тонус и т.д.; улучшенное ощущение зрительных способностей; улучшенная амбулаторная независимость; улучшение самочувствия; и/или улучшение повседневной активности.
[00202] В альтернативных вариантах осуществления использование или практическое применение любых композиций и способов, раскрытых в настоящем документе, не приводит к развитию нежелательного роста клеток, например, опухолей; инфекциям, например, отсутствует эндофтальмит, вероятный при любой внутриглазной процедуре; передаче болезни (однако прионную инфекцию или коровье бешенство может быть сложно исключить); увеиту и/или острому отторжению трансплантата; повышенному внутриглазному давлению; закрытию угла; гипотонии; отслоению сетчатки; и/или неоваскуляризации.
[00203] Применения и способы, описанные в настоящем документе, могут быстро и устойчиво восстанавливать и/или сохранять клинически значимые степени зрительной функции сетчатки у млекопитающих, включая, помимо прочего, улучшенное фотопическое (дневное) зрение, повышенную наибольшую остроту зрения с коррекцией, улучшенную функцию желтого пятна, сохранение или восстановление центральной фиксации, улучшенное поле зрения, улучшение скотопического (ночного) зрения, повышенную или улучшенную чувствительность к звуку и улучшение остроты зрения контралатерального глаза. Другие изменения могут включать различные системные преимущества, например, изменения внешнего вида из-за соматических улучшений, которые могут быть связаны с влиянием света на циркадные ритмы, функцию гипофиза, высвобождение гормонов, сосудистый тонус; улучшенное ощущение зрительных способностей; улучшенную амбулаторную независимость; улучшение самочувствия; и/или улучшение повседневной активности. Такие изменения зрения можно измерять с помощью способов, известных в данной области.
[00204] Улучшение зрения может быть быстрым и может проявляться в течение первой недели после лечения, но может также проявляться в виде постепенного улучшения в течение более длительных периодов времени. Может происходить замещение клеток сетчатки и/или миграция донорских клеток в сетчатку, сеть сетчатки, внешний ядерный слой или желтое пятно, но это не обязательно для клинической эффективности; миграция донорских клеток в сетчатку возможна, но не обязательна для клинической эффективности.
[00205] Измерение изменений зрения, включая улучшение зрения в результате лечения композициями ретинальных клеток-предшественников, раскрытых в настоящем документе, может быть достигнуто с применением стандартных методов офтальмологического обследования, включая, помимо прочего, исследование глазного дна, наибольшую остроту зрения с коррекцией (BCVA), ВГД, осмотр с помощью щелевой лампы, флуоресцентную ангиографию (ФА), оптическую когерентную томографию (ОКТ), стереофотографию глазного дна, электроретинографию (ЭРГ), мелькающую электроретинографию колбочек, периметрию (поле зрения), микропериметрию, адаптацию к темноте, умение преодолевать лабиринт, оптокинетические/оптомоторные реакции, реакции зрачка, зрительные вызванные потенциалы (ЗВП) и сканирующая лазерная офтальмоскопия с адаптивной оптикой (AOSLO).
[00206] Данные, полученные на животных in vivo, также указывают, что интравитреальные RPC являются средством воздействия на несколько типов клеток в пораженной сетчатке, включая, помимо прочего, клетки Мюллера (усиленная активация при дегенерации сетчатки и/или повышенная локальная экспрессия глутаминсинтетазы (ГС)); сосудистый компартмент при диабетической ретинопатии (меньшая проницаемость сосудов (пропотевание) и/или снижение ишемии в результате снижения уровней VEGF внутри сетчатки); усиление рекрутинга макрофагов при дегенерации сетчатки; повышенная локальная экспрессия bFGF (нейротрофического фактора) при дегенерации сетчатки; снижение экспрессии каспазы 3 (что указывает на уменьшение гибели клеток сетчатки). Таким образом, введение RPC также может быть полезным при ряде других заболеваний, нарушений и патологий сетчатки.
[00207] Кроме того, были получены предварительные подтверждения перекрестного эффекта лечения по показателям эффективности во втором глазу, в который не делали инъекцию. В частности, это наблюдали у крыс RCS (гистологическое восстановление фоторецепторов, а также результаты ЭРГ), а также в подгруппе пациентов (проверка остроты зрения), и, по-видимому, это свидетельствует о "гуморальном" лечебном эффекте, который может распространяться за пределы глаза, в который делали инъекцию. Возможно, что этот эффект может быть результатом диффузии цитокинов и/или экзосом через кровоток, иммуномодуляции или того и другого.
[00208] Аналогичным образом, данные in vivo на животных указывают, что однократная интравитреальная инъекция только белка остеопонтина (OPN) воспроизводит некоторые, но не все лечебные эффекты, обеспечиваемые hRPC. Однако эффекты однократной дозы плейотропина (PTN) и/или мидкина отличались от эффектов, наблюдаемых при введении OPN, с точки зрения времени и специфических ответов популяций клеток сетчатки.
[00209] Данные, полученные in vivo на животных, также указывают, что однократная интравитреальная инъекция экзосом, полученных из RPC, в некоторой степени воспроизводит лечебный эффект, обеспечиваемый hRPC.
Наборы и инструкции
[00210] Также предложены наборы, содержащие любую из композиций, описанных в настоящем документе (например, гетерогенную смесь фетальных нервных клеток сетчатки), подходящие для применения в любом из способов, раскрытых в настоящем документе (например, лечение заболевания или патологии сетчатки или получение или выделение гетерогенной смеси фетальных нервных клеток сетчатки), включающие инструкции по их применению. Также предложены наборы, содержащие композицию, продукт производства или смесь или культуру клеток (например, гетерогенную смесь фетальных нервных клеток сетчатки), при этом набор необязательно также включает инструкции по применению любого из способов, описанных в настоящем документе.
[00211] Наборы также могут включать популяцию клеток, содержащую ретинальные клетки-предшественники млекопитающих, описанные в настоящем документе, представленные либо как клетки в культуре, свежие или замороженные, либо включенные в состав композиции для введения субъекту. Аналогичным образом, набор может дополнительно включать инструкции по применению любого из способов, описанных в настоящем документе. В некоторых вариантах осуществления такие наборы могут дополнительно содержать средство, которое связывает один или более маркеров ретинальных клеток-предшественников, описанных в настоящем документе (например, антитело или олигонуклеотидный праймер), и/или базальную или кондиционированную среду. Например, подходящий набор может включать: первый контейнер, содержащий антитело, специфичное к одному или нескольким маркерам, где указанное антитело адаптировано к выделению или обнаружению, например, путем конъюгирования с флуоресцентным маркером или магнитной гранулой; и второй контейнер, содержащий базальную или кондиционированную среду. Наборы могут дополнительно включать один или более дополнительных реагентов, используемых для получения популяции клеток, как предусмотрено в настоящем документе, таких как среда для культивирования клеток, чашки для культивирования клеток, покрытые внеклеточным матриксом, и/или ферменты, подходящие для обработки ткани. Набор также может включать инструкции по применению набора для выделения, очистки и/или экспансии ретинальных клеток-предшественников или популяций клеток, полученных из образца ткани. Аналогичным образом, наборы могут дополнительно содержать средства для получения образца ткани от пациента или донора и/или контейнер для хранения полученного образца ткани.
Ветеринарные применения
[00212] Любые из композиций и способов, описанных в настоящем документе, также могут применять для ветеринарных применений. Например, выращивание кошачьих RPC и терапевтическое применение на сетчатке у кошек с дистрофией и других животных, например, любого домашнего млекопитающего, обычных одомашненных и редких диких млекопитающих, зоопарковых животных, сельскохозяйственных животных, спортивных (например, гончих собак или беговых лошадей) животных, и т.п.
[00213] Существует ряд домашних животных, несущих гены, вызывающие слепоту в результате обширного близкородственного скрещивания. Эти животные включают кошек, собак и лошадей, и, вероятно, другие виды.
[00214] Аналогичным образом, существуют болезни и поражения сетчатки, которые возникают у диких и домашних животных, у которых лечение с применением композиций и способов, описанных в настоящем документе, будет эффективным.
Продукты производства, имплантаты и искусственные органы
[00215] Также предложены имплантаты и искусственные органы, биореакторные системы, системы культивирования клеток, планшеты, чашки, пробирки, бутылки и флаконы и т.п., включающие еще одну из композиций, описанных в настоящем документе, содержащую гетерогенную смесь фетальных невральных ретинальных клеток.
[00216] В качестве неограничивающего примера, в настоящем документе дополнительно предложен биореактор, имплантат, стент, искусственный орган или подобные устройства, содержащие гетерогенную смесь фетальных невральных ретинальных клеток; например, имплантаты, аналогичные или такие, как описанные в патентах США 7,388,042; 7,381,418; 7,379,765; 7,361,332; 7,351,423; 6,886,568; 5,270,192; и публикациях заявок на пат. США 20040127987; 20080119909 (описывает ушные имплантаты); 20080118549 (описывает глазные имплантаты); 20080020015 (описывает биоактивный перевязочный материал); 20070254005 (описывает биопротез сердечного клапана, сосудистые трансплантаты, имплантаты мениска); 20070059335; 20060128015 (описывает имплантаты печени).
ПРОНУМЕРОВАННЫЕ ВАРИАНТЫ ОСУЩЕСТВЛЕНИЯ
[00217] Изобретение может быть определено посредством ссылки на следующие пронумерованные иллюстративные варианты осуществления:
[00218] 1. Способ выделения первичных ретинальных клеток, полученных из человеческого образца, путем:
a) обработки полученного образца человеческих ретинальных тканей ио человека-донора гестационным возрастом от приблизительно 12 недель до приблизительно 28 недель,
b) механической диссоциации полученного образца,
c) определения жизнеспособности и количества первичных ретинальных клеток, полученных из образца, и
d) подтверждения морфологии полученных первичных ретинальных клеток
с получением разделенной суспензии клеток и скоплений клеток.
[00219] 2. Способ согласно варианту осуществления 1, где человеческая ткань сетчатки получена из одного или пары человеческих глазных яблок.
[00220] 3. Способ согласно варианту осуществления 2, где глазное яблоко (яблоки) обладает нормальной морфологией, включающей интактные глазные яблоки, прозрачную роговицу, нормальную форму или любую комбинацию этого.
[00221] 4. Способ согласно варианту осуществления 1, где человеческую ткань сетчатки хранят в среде RPMI-1640 с L-глутамином и сразу помещают в лед после изъятия ткани у человека-донора.
[00222] 5. Способ согласно любому из вариантов осуществления 1-4, где сохраненную человеческую ткань сетчатки доставляют и используют в течение определенного периода времени после изъятия.
[00223] 6. Способ согласно варианту осуществления 5, где определенный период времени включает от приблизительно 7 до приблизительно 26 часов.
[00224] 7. Способ согласно варианту осуществления 1, где этап (a) включает:
a) после изъятия ткани, извлечение глазного яблока (яблок) из среды RPMI-1640 и промывку 1-5 раз охлажденным льдом фосфатно-солевым буфером (PBS) с добавкой антибиотиков,
b) удаление зрительного нерва и мезенхимальной ткани из глазного яблока для удаления всех экстраокулярных клеток,
c) промывку глазного яблока охлажденным льдом PBS с добавкой антибиотиков,
d) прокол глазного яблока по краю роговицы с помощью иглы,
e) круговой разрез по краю роговицы микрохирургическими ножницами,
f) удаление хрусталика, роговицы и ассоциированного стекловидного тела,
g) отделение сетчатки от слоя пигментного эпителия сетчатки (ПЭС) с получением отделенной сетчатки,
h) помещение отделенной сетчатки в чашку Петри, содержащую охлажденную льдом среду или PBS с добавкой антибиотика.
[00225] 8. Способ согласно варианту осуществления 1, где этап (b) включает механическое отделение сетчатки(ок), полученной на этапе (a), путем:
a) переноса сетчатки(ок) к коническую пробирку,
b) механической диссоциации сетчатки(ок) с получением отделенной сетчатки,
c) промывки чашки Петри бессывороточной средой с добавкой антибиотика и переноса среды, содержащей любые остаточные разделенные сетчатки в коническую пробирку, содержащую разделенную сетчатку(и),
d) осаждения разделенной сетчатки(ок) с помощью центрифугирования, и
e) удаления супернатанта.
[00226] 9. Способ согласно варианту осуществления 8, где механическую диссоциацию сетчатки проводят путем суспендирования стерильной пипеткой.
[00227] 10. Способ согласно варианту осуществления 8, где разделенную сетчатку осаждают с помощью центрифугирования при 10-1000 g в течение периода от 0 до 30 минут при 1-50°C.
[00228] 11. Способ согласно варианту осуществления 1, где этап (c) включает:
a) ресуспендирование осажденной ткани сетчатки из этапа (b) в охлажденной льдом бессывороточной среде с добавкой антибиотика,
b) определение количества и жизнеспособности ретинальных клеток и скоплений ретинальных клеток, полученных в результате механической диссоциации ретинальной ткани,
c) посев клеток в покрытые фибронектином флаконы для культур клеток, содержащие бессывороточную среду с добавкой антибиотика,
d) инкубирование флаконов, содержащих ретинальные клетки, при 10-50°C.
[00229] 12. Способ согласно варианту осуществления 11, где количество и жизнеспособность клеток измеряют с помощью счетчика клеток NC-200.
[00230] 13. Способ согласно варианту осуществления 11, где подсчитанное количество клеток составляет от приблизительно 1 до приблизительно 1000000000.
[00231] 14. Способ согласно варианту осуществления 11, где процент жизнеспособных подсчитанных клеток составляет от приблизительно 10 до приблизительно 100.
[00232] 15. Способ согласно варианту осуществления 11, где флаконы засевают от приблизительно 1 до приблизительно 1000000000 клеток.
[00233] 16. Способ согласно варианту осуществления 11, где инкубирование флаконов, содержащих ретинальные клетки, проводят при 37°C и 0-30% CO2 и 0-50% O2.
[00234] 17. Способ согласно варианту осуществления 1, где этап (d) включает подтверждение, что ретинальные клетки, посеянные во флаконы для культуры клеток, состоят из скоплений ретинальных клеток, содержащих от приблизительно 1 до приблизительно 100 клеток.
[00235] 18. Способ согласно любому из вариантов осуществления 1-17, где антибиотиком, используемым для добавления в PBS или бессывороточную среду, является гентамицин.
[00236] 19. Способ согласно любому из вариантов осуществления 1-18, где антибиотик используют в концентрации от приблизительно 0 до приблизительно 10000 мкг/мл.
[00237] 20. Способ согласно любому из вариантов осуществления 1-19, где бессывороточная среда включает:
a) улучшенную DMEM/F12,
b) добавку N-2,
c) EGF (рекомбинантный человеческий эпидермальный фактор роста),
d) bFGF (основной фактор роста фибробластов), и
e) GlutaMAX I.
[00238] 21. Способ культивирования выделенных первичных человеческих ретинальных клеток с получением популяции неиммортализованных человеческих ретинальных клеток-предшественников, включающий:
a) культивирование суспензии выделенных первичных ретинальных клеток в бессывороточной среде в культуральных флаконах или планшетах, покрытых не содержащим ксеногенных компонентов фибронектином, орнитином, полилизином или ламинином, при стандартных уровнях кислорода в течение от приблизительно 4 до 6 пассажей,
b) последующее культивирование суспензии в бессывороточной среде при низких уровнях кислорода в течение еще приблизительно 3-6 пассажей, где клетки пассируют до 40-90% конфлюентности и обрабатывают ферментом при каждом пассаже для отделения клеток, и добавление новой культуральной среды, и
c) последующую криоконсервацию клеток,
с получением в результате популяции неиммортализованных человеческих ретинальных клеток-предшественников.
[00239] 22. Способ согласно варианту осуществления 21, где, после последующего культивирования суспензии при низких уровнях кислорода клеткам позволяют расти без пассирования в течение некоторого периода времени при стандартных уровнях кислорода.
[00240] 23. Способ согласно варианту осуществления 21, где период времени между пассажами составляет 3-5 дней.
[00241] 24. Способ согласно варианту осуществления 21, где ферментативный раствор, используемый для разделения клеток, включает трипсин или эквивалент.
[00242] 25. Способ согласно варианту осуществления 21, где клетки разделяют при пассаже 1 с использованием ферментативного раствора, включающего трипсин или эквивалент, и ЭДТА в соотношении 1:4, в течение 6-10 минут при 37°C.
[00243] 26. Способ согласно варианту осуществления 21, где клетки разделяют при пассаже 2 с использованием ферментативного раствора, включающего трипсин или эквивалент, и DPBS в соотношении 1:1:3, в течение 4-8 минут при 37°C.
[00244] 27. Способ согласно варианту осуществления 21, где клетки разделяют при пассаже 3 и всех последующих пассажах с использованием ферментативного раствора, включающего трипсин или эквивалент, ЭДТА и DPBS в соотношении 1:1, в течение 4-8 минут при 37°C.
[00245] 28. Способ согласно варианту осуществления 21, где диссоциацию останавливают путем добавления избытка DMEM или PBS.
[00246] 29. Способ согласно варианту осуществления 21, где количество и жизнеспособность клеток определяют после диссоциации.
[00247] 30. Способ согласно варианту осуществления 21, где количество и жизнеспособность клеток определяют с помощью счетчка клеток NC-200.
[00248] 31. Способ согласно варианту осуществления 21, где криоконсервацию на этапе (c) выполняют путем:
a) ферментативной диссоциации клеток с использованием трипсин или эквивалента и DPBS в соотношении 1:1,
b) остановки диссоциации избытком DMEM или PBS,
c) осаждения клеток с помощью центрифугирования при 10-10000 g в течение 1-30 минут,
d) ресуспендирования клеток в бессывороточной среде и определения общего количества и жизнеспособности клеток,
e) добавления среды для криоконсервации с получением конечной концентрации ДМСО 5-30%,
f) аликвотирования по 0,2-100×106 клеток в каждый криофлакон,
g) замораживания каждого флакона при -80°C в течение 6-72 часов, и
h) помещения каждого флакона с клетками в жидкий N2.
[00249] 32. Способ согласно варианту осуществления 21, где клетки и/или скопления клеток культивируют вместе с дополнительными компонентами или добавками, поддерживающими выживание или рост клеток.
[00250] 33. Способ согласно варианту осуществления 32, где дополнительные компоненты или добавки, поддерживающие выживание или рост клеток, выбраны из группы, состоящей из L-глутамина, человеческих рекомбинантных факторов роста, состоящих из EGF и bFGF (Invitrogen), и других факторов роста.
ПРИМЕРЫ
Пример 1: Выделение первичных ретинальных клеток: Протокол A
[00251] Выделение первичных человеческих клеток сетчатки производили в соответствии с протоколом, специально оптимизированным для интервала транспортировки от 4,5 до 21,5 часов, где интервал транспортировки измеряется со времени изъятия ткани до времени получения донорской ткани.
1. 1 или пару глазных яблок плода гестационного срока 17–18 недель, в 15 мл пробирке со средой RPMI-1640 и L-глутамином (BioWhittaker), транспортируют во льду и доставляют в течение 4,5–21,5 часов. При получении глазное яблоко(и) осматривают на предмет серьезных аномалий: глазное яблоко интактное, роговица чистая, глазное яблоко имеет нормальную форму. Этапы 2-8 выполняют в ламинарном шкафу с использованием стерильного метода.
2. Целые глазные яблоки промывают 40 мл холодного PBS, содержащего антибиотики (в пробирке 50 мл), 3 раза (в 3 разных пробирках).
3. Зрительный нерв и оставшуюся мезенхимальную ткань удаляют. Этот подход применяют, чтобы избежать возможной контаминации ретинальных образцов клетками, происходящими из мозга. Еще раз промывают холодным PBS, содержащим антибиотики.
4. Под стереомикроскопом делают прокол лимба роговицы с помощью шприца объемом 1 мл с иглой 255/8, глазное яблоко открывают по окружности, делая разрез по лимбу с помощью микрохирургических ножниц, роговицу, хрусталик и ассоциированное с ним стекловидное тело удаляют. Сетчатку осторожно отделяют от ПЭС, собирают в малую чашку Петри, содержащую ~2 мл холодной DMEM/F12.
5. Сетчатку вручную дробят на мелкие фрагменты с помощью наконечника на 1 мл в чашке Петри (2-5 раз), переносят в холодную пробирку с коническим дном объемом 15 мл, чашку Петри 2-3 раза промывают 1 мл холодного PBS, добавляет в 15 мл пробирку, центрифугируют, 1000 об/мин (179×g) 5 минут, полностью удаляют супернатант пипеткой на 10 мл и полированной стеклянной пипеткой.
6. Добавляют 0,8 мл неразведенного TrypLE Express (Invitrogen) на 40 сек при комнатной температуре, мягко и медленно пипетируют 1 мл наконечником (приблизительно 10 раз), добавляют 10 мл холодной свежей среды (без сыворотки) к нейтрализованному TrypLE Express, центрифугируют, 1000 об/мин (179×g) ×4 мин, супернатант удаляют, ресуспендируют осадок в 1,5 мл холодной свежей среды (SM), пипетируют с использованием полированной стеклянной пипетки приблизительно 10 раз, добавляют еще 6,5 мл среды, определяют жизнеспособность клеток и число клеток при окрашивании трипановым синим (Invitrogen), подсчитывают с помощью Countess (Invitrogen) или вручную, приблизительно 1,3×106 клеток/мл, приблизительно 92% живых клеток, приблизительно 10×106 скоплений клеток/всего, приблизительно 80% малых/средних скоплений. Клетки сеют в 2 T75, покрытые фибронектином (см. пример 5), с последующим инкубированием при 37°C и 5% CO2, 3% или 20% O2 (необязательно инкубированием при 37°C, 5-10% CO2 1%-20% O2).
Примечание: подсчет определенных клеток.
• Одиночные клетки: ~6-8 мкм, содержащие 1 клетку.
• Мелкое скопление: ~15-40 мкм, содержащие ~2-30 клетки.
• Среднее скопление: ~40-100 мкм, содержащее ~30-80 клеток.
• Крупное скопление: ~100-150 мкм, содержащее >80 клеток.
В полученной популяции клеток: ~80-90% являются мелкими или средними скоплениями клеток, ~9-18% одиночными клетками, ~1-2% крупными скоплениями.
Если мелкие/средние скопления подсчитывают как "одно", общее число клеток составляет ~ 10×106.
Если одиночные клетки подсчитывают как "одну", общее число клеток составляет ~240×106.
7. Вся процедура: 45 мин~1 ч 10 минут (необязательно в течение 2 часов).
8. Через ~1,5 часа 90% клеток оседают на дно (если ткань свежая, например, после транспортировки 4,5 часа во льду, если нет, например, после транспортировки 21,5 часа во льду, клетки оседают на дно через ~6 часов), 90% являются мелкими фрагментами ткани, 10% являются одиночными клетками. В целом 90% клеток живые (хорошие), плотность клетки будет составлять >10% конфлюентности (лучше ~20%), при оценке с помощью IncuCyte. Делают снимок.
Пример 2: Выделение первичных ретинальных клеток: Протокол B
[00252] Выделение первичных человеческих клеток сетчатки проводили по протоколу, специально оптимизированному для интервала транспортировки 7-26 часов, где интервал транспортировки измеряют со времени изъятия ткани до времени получения донорской ткани.
1. 1 или пару донорских глазных яблок плода гестационного срока 17-20 недель, в пробирке объемом 15 мл, содержащей среду RPMI-1640 с L-глутамином (BioWhittaker), транспортируют во льду и доставляют в окне транспортировки 7-26 часов. Протокол может также работать при более широком транспортном окне. После получения глазное яблоко(и) осматривают на предмет серьезных аномалий: интактное глазное яблоко, прозрачная роговица, глазное яблоко должно иметь нормальную форму. В RPMI-1640 и среду для транспортировки с L-глутамином добавляют 50 мкг/мл гентамицина, чтобы предотвратить потенциальную контаминацию ткани.
Этапы 2-8 выполняют в ламинарном боксе с биозащитой при использовании стерильного метода.
2. Интактные глазные яблоки промывают 40 мл холодного PBS, содержащего антибиотики (в пробирке объемом 50 мл), 3 раза (в 3 разных пробирках). Гентамицин используют в концентрации 30 мкг/мл. Гентамицин используют вместо пенициллина или стрептомицина, чтобы избежать исключения пациентов с аллергиями на антибиотики.
3. Зрительный нерв и оставшуюся мезенхимальную ткань удаляют из глаза (глаз), чтобы избежать возможной контаминации ретинальных образцов экстраокулярными клетками. Еще раз промывают холодным PBS, содержащим антибиотики.
4. Под стереомикроскопом делают прокол глазного яблока по лимбу роговицы с помощью шприца на 1 мл с иглой 255/8, глазное яблоко открывают по окружности, делая разрез по лимбу с помощью микрохирургических ножниц, роговицу, хрусталик и ассоциированное с ним стекловидное тело удаляют. Сетчатку можно осторожно отделить от подлежащего слоя ПЭС, перенести в малую чашку Петри, содержащую приблизительно 2 мл холодной полной среды с гентамицином (30 мкг/мл гентамицина).
5. Сетчатку переносят в коническую пробирку объемом 15 мл. Сетчатку дробят на мелкие фрагменты при использовании мягкого суспендирования наконечником пипетки на 1 мл (4-8 раз). Если остаточная ткань сетчатки присутствует в чашке Петри, чашку промывают 1-2 раза 1 мл холодной полной среды с гентамицином и добавляют в 15 мл пробирку, содержащую ткань сетчатки. Пробирку на 15 мл переносят в центрифугу, центрифугируют при 140×g в течение 3 минут при 4°C, аспирируют и полностью удаляют супернатант.
6. Осадок ресуспендируют в 1,0 мл холодной свежей среды с гентамицином с помощью наконечника на 1 мл пипеткой, осторожно пипетируя суспензию 4-5 раз, добавляют еще 15 мл среды. Жизнеспособность клетки и количество клеток определяют с помощью NC-200 при использовании метода подсчета агрегированных клеток. Этот метод позволяет получать точное число клеток при сохранении скоплений клеток, которые могут быть важны для первичной культуры клеток, и превращении ткани в клетки. Жизнеспособность клеток, по предварительным расчетам, будет попадать в диапазон 68-85%, количество живых клеток должно составить примерно 73-147×106. Клетки сеют в 3× флакона T25 (или 1-2 T75), предварительно покрытые фибронектином (см. Пример 5), с последующим инкубированием при 37°C и 5% CO2, 20% O2. (Примечание: 20% для стадии 1: ткань в фонд культур, что может быть также выполнено в условиях низкого содержания кислорода. Впрочем, цель в данном случае состояла в сохранении нового продукта в максимально близком состоянии к предыдущим продуктам, которые выращивали при уровне кислорода меньше 20%. Этап 2: фонд культур в производственный фонд, выполняли при использовании культивирования при низком уровне кислорода 3%, чтобы продлить пролиферацию клеток.)
7. Клетки исследуют под микроскопом: культуры, как ожидают, преимущественно будут состоять из мелких и средних скоплений плюс некоторые одиночные клетки (последние с высокой вероятностью не будут нежизнеспособными).
8. Продолжительность всей процедуры выделения: приблизительно 30-60 минут (этот протокол, в котором специально не используют ферменты, значительно быстрее и проще, чем протокол выделения, основанный на применении ферментов).
Пример 3: Культура клеток: Протокол A
[00253] Человеческие ретинальные клетки-предшественники культивировали из клеток сетчатки, выделенных согласно способу, описанному в Примере 1:
1. Замена среды: 90% замена среды каждые 2 дня.
2. Пассаж: клетки пассируют при 60-80%, необязательно 40-90%, конфлюентности, с добавлением TrypLE Express (Invitrogen), необязательно трипсина или эквивалента, или TRYP-LE EXPRESS или эквивалента, разводят в 2 раза (эквивалент 0,125%), 5-6 минут, инкубирование при 37°C. Диссоциацию останавливают путем добавления 10 мл старой среды или холодного PBS. Жизнеспособность клеток и число клеток определяют при окрашивании трипановым синим (Invitrogen), подсчитывают с помощью Countess (Invitrogen) или вручную, жизнеспособность клеток >90%. Клетки сеют в новый, покрытый фибронектином флакон/планшет при плотности 1-6,7×104/см2 (ранний пассаж 6,7×104 скоплений/см2), поздний пассаж: 2×104/см2).
3. Замораживание клеток: клетки собирают с использованием TrypLE Express (Invitrogen), необязательно трипсина или эквивалента, или TRYP-LE EXPRESS или эквивалента, разводят в 2 раза (эквивалент 0,125%), 5-6 минут, инкубирование при 37°C. Диссоциацию останавливают путем добавления 10 мл старой среды или холодного PBS, центрифугируют, 1000 об/мин (179×g) в течение 5 минут, ресуспендируют клетки в новой среде или холодном PBS. Жизнеспособность клеток и число клеток определяют при окрашивании трипановым синим (Invitrogen), подсчитывают с помощью Countess (Invitrogen) или вручную. Центрифугируют, 1000 об/мин (179×g) в течение 5 минут, ресуспендируют клетки в среде для замораживания клеток, фасуют аликвотами по 0,5-5×106 клеток в каждый криофлакон (Greiner). Помещают в Cryo 1°C контейнер для замораживания (NALGENE), помещают в замораживатель на -80°C в течение ночи (или дольше, <2 недель), переносят в резервуар с жидким азотом.
4. Размораживание клеток: клетки извлекают из жидкого азота, оставляют в водяной бане при 37°C на 2-3 минуты, пока не исчезнут кристаллы, быстро переносят наконечником на 1 мл в одну холодную пробирку с коническим дном объемом 15 мл, промывают флакон холодной свежей средой 2 раз, медленно добавляют 12 мл холодной свежей среды в пробирку на 15 мл, первый 1 мл - по каплям, мягко встряхивают. Центрифугируют при 800 об/мин (115 g) в течение 3 минут. Удаляют супернатант, ресуспендируют осадок клеток в свежей среде, определяют число и жизнеспособность клеток, как описано выше. Сеют в новый флакон с покрытием и инкубируют при условиях, описанных выше.
5. Подготовка клеток к трансплантации: клетки собирают с использованием TrypLE Express (Invitrogen), необязательно трипсина или эквивалента, или TRYP-LE EXPRESS или эквивалента, разводят в 2 раза (эквивалент 0,125%), 5-6 минут, инкубируют 37°C. Диссоциацию останавливают путем добавления 10 мл старой среды или холодного PBS. Центрифугируют, 1000 об/мин (179×g) в течение 5 минут, ресуспендируют клетки в 10 мл холодной HBSS, жизнеспособность клеток и число клеток определяют при окрашивании трипановым синим (Invitrogen), подсчитывают с помощью Countess (Invitrogen) или вручную. Центрифугируют, 1000 об/мин (179×g) в течение 5 минут, ресуспендируют клетки в холодном HBSS, с получением суспензии клеток для трансплантации, 0,5×106 клеток в 100 мкл HBSS для пациента, 30000 клеток в 2 мкл HBSS для крысы.
Пример 4: Культура клеток: Протокол B
[00254] Человеческие ретинальные клетки-предшественники культивировали из клеток сетчатки, выделенных согласно способу, описанному в Примере 2:
1. Замена среды: замена 100% среды, каждые 2 дня, кроме дня 0-дня 3. Открытые системы, закрытые системы и полузакрытые системы можно использовать при замене среды и пассировании клеток. Среду необязательно можно менять ежедневно.
2. Пассирование: клетки пассируют каждые 4-5 дней при конфлюентности 15-95%, необязательно при конфлюентности 40-95%. Способ отличается числом пассажей. Клетки также могут пассировать каждые 3-4 дня или каждые 3-5 дней.
Пассаж 1: TrypLE Select (Invitrogen) + ЭДТА (Invitrogen) в соотношении 1:4, инкубирование в течение 7-8 минут при 37°C.
Пассаж 2: TrypLE Select (Invitrogen) + ЭДТА (Invitrogen) + DPBS (Invitrogen) в соотношении 1:1:3, инкубирование в течение 5-6 минут при 37°C. T
Пассаж 3 и последующие: TrypLE Select (Invitrogen) + DPBS в соотношении 1:1, инкубирование в течение 5-7 минут при 37°C.
Необязательно могут использовать TrypLE Express, трипсин или эквивалент, или TRYP-LE EXPRESS или эквивалент в 2-кратном разведении (эквивалент 0,125%). Диссоциацию скоплений останавливают путем добавления DMEM или PBS (10 мл). Жизнеспособность клеток и число клеток определяют с помощью NC-200. Ожидаемая жизнеспособность клетки >70%. Клетки сеют в новый флакон/планшет, покрытый фибронектином, при плотности 3-67×104/см2 (ранний пассаж 67x104/cm2, поздний пассаж: 3×104/см2).
3. Криоконсервация: клетки собирают с использованием TrypLE Select/Express (Invitrogen), необязательно трипсина или эквивалента, или TRYP-LE EXPRESS или эквивалента, в 2-кратном разведении (эквивалент 0,125%), в течение 5-7 минут, инкубирование при 37°C. Диссоциацию останавливают путем добавления DMEM или PBS. Затем выполняют центрифугирование. Для пробирки объемом 50 мл: 490×g в течение 7 минут, для флакона с коническим дном объемом 500 мл, 700×g в течение 8 минут, клетки ресуспендируют в свежей среде. Жизнеспособность клеток и число клеток определяют с помощью NC200. Добавляют такое же количество 2× среды для криоконсервации (20% ДМСО) с получением конечной концентрации ДМСО 10% в суспензии клеток. Фасуют аликвотами по 0,5-10×106 клеток в каждый криофлакон (Themofisher или подобный). Помещают в Cryo 1°C контейнер для замораживания (NALGENE), помещают в замораживатель на -80°C в течение ночи (или дольше, <2 недель), переносят в резервуар с жидким азотом.
4. Размораживание клеток: клетки извлекают из жидкого азота, оставляют в водяной бане при 37°C на 2-3 минуты, пока не исчезнут кристаллы, затем быстро переносят в одну холодную пробирку с коническим дном объемом 15 мл с помощью наконечника на 1 мл, промывают флакон холодной свежей средой 1-2 раза, медленно добавляют 9-12 мл холодной свежей среды в пробирку объемом 15 мл, центрифугируют при 1200 об/мин (300 g) в течение 5 минут. Удаляют супернатант, ресуспендируют осадок клеток в свежей среде, определяют число и жизнеспособность клеток, как описано выше. Сеют в новый флакон с покрытием и инкубируют при условиях, описанных выше.
5. Подготовка клеток к трансплантации: клетки собирают с использованием TrypLE Express (Invitrogen), необязательно трипсина или эквивалента, или TRYP-LE EXPRESS или эквивалента, 2-кратное разведение (эквивалент 0,125%), 5-6 минут, инкубирование при 37°C. Диссоциацию останавливают путем добавления DMEM. Суспензию клеток центрифугируют, 300 g ×5 мин, затем клетки ресуспендируют в 0,5-3 мл холодной BSS Plus (или BSS/DPBS/HBSS). Жизнеспособность клеток и число клеток определяют с помощью трипанового синего (Invitrogen), подсчитывают с помощью Countess (Invitrogen) или вручную, или NC200. Центрифугируют, 300 g в течение 5 минут, ресуспендируют клетки в холодной BSS Plus (или BSS/DPBS/HBSS) с получением подходящей дозировки для трансплантации.
Пример 5: Приготовление реагентов и клеточного продукта
Приготовление полной среды (бессывороточной)
[00255] Среду для культуры человеческих ретинальных клеток-предшественников приготавливали с использованием следующих компонентов:
• Улучшенная DMEM/F12 (Invitrogen),
o Необязательно DMEM/F12 (Invitrogen или другой бренд), или KnockOut DMEM/F12 (Invitrogen или другой бренд), или нейробазальная среда (Invitrogen), или UltraCULTURE (Lonza), или ReNcell (Chemicon), или другая эквивалентная среда.
• Добавка N-2 (Invitrogen),
o Необязательно B27 (Invitrogen или другой бренд) xeno-free или B27, не xeno-free, или Stempro (Invitrogen) или другой эквивалент.
• EGF (рекомбинантный человеческий эпидермальный фактор роста): Invitrogen, необязательно другой бренд
• bFGF (основной фактор роста фибробластов): Invitrogen, необязательно другой бренд
• GlutaMAX I: Invitrogen, необязательно L-глутамин (Invitrogen или другой бренд)
• Гентамицин (Invitrogen) для выделения и первого пассажа (~4-5 дней)
[00256] Фермент для пассирования:
• Раствор Версена: Thermo Fisher (Life tech), используют, как описано выше, при пассаже 1 и 2. Раствор Версена представляет собой раствор ЭДТА для использования в качестве мягкого неферментативного реагента для диссоциации клеток. Раствор Версена Gibco® (0,48 мм) содержит 0,2 г ЭДТА (Na4) на литр фосфатно-солевого буфера (PBS).
Приготовление среды для криоконсервации
[00257] Приготавливали среду для криоконсервации культивированных человеческих ретинальных клеток-предшественников, содержащую:
• 90% полной среды
• 10% ДМСО
Покрытие флаконов
Фибронектин человеческой плазмы (Invitrogen), необязательно орнитин, полилизин, ламинин или Матригель, разбавляют в DPBS, в концентрации: 1-5 мкг/см2, оставляют на 1-3 часа для нанесения покрытия в вытяжном шкафу при комнатной температуре, хранят при 4C в течение ночи или до 2 недель. Промывают улучшенной DMEM/F12 перед применением.
Пример 6: Дополнительная версия протокола B культивирования клеток
[00258] Человеческие ретинальные клетки-предшественники культивировали из ретинальных клеток, выделенных согласно способу, описанному в Примере 2:
1. Замена среды: меняют 100% среды, замену производят каждые 2 дня. Открытые системы, закрытые системы и полузакрытые можно использовать при замене среды и пассировании клеток. Среду необязательно можно менять ежедневно.
2. Пассирование: клетки пассируют каждые 4-5 дней при конфлюентности 15-95%, необязательно при конфлюентности 40-95%. Способ отличается числом пассажей. Клетки также могут пассировать каждые 3-4 дня или каждые 3-5 дней.
Пассаж 1: TrypLE Select (Invitrogen) + ЭДТА (Invitrogen) в соотношении 1:4, инкубирование в течение 7-8 минут при 37°C.
Пассаж 2: TrypLE Select (Invitrogen) + ЭДТА (Invitrogen) + DPBS (Invitrogen) в соотношении 1:1:3, инкубирование в течение 5-6 минут при 37°C. T
Пассаж 3 и последующие: TrypLE Select (Invitrogen) + DPBS в соотношении 1:1, инкубирование в течение 5-7 минут при 37°C.
Необязательно могут использовать trypLE Express, трипсин или эквивалент, или TRYP-LE EXPRESS или эквивалент, 2-кратное разведение (эквивалент 0,125%). Диссоциацию скоплений останавливают путем добавления DMEM или PBS (10 мл).
3. Диссоциация: диссоциация скоплений клеток останавливают путем добавления улучшенной DMEM или PBS (10 мл). Жизнеспособность клеток и число клеток определяют с помощью NC-200. Ожидаемая жизнеспособность клетки >70%. Клетки сеют в новые покрытые фибронектином флаконы или многоуровневые флаконы (CS) при плотности 1-200×104/см2 (ранний пассаж 2×106/см2, поздний пассаж: 1×104/см2).
4. Криоконсервация: клетки собирают с использованием TrypLE Select/Express (Invitrogen), необязательно трипсина или эквивалента, или TRYP-LE EXPRESS или эквивалента, в 2-кратном разведении (эквивалент 0,125%), в течение 5-7 минут, инкубирование при 37°C. Диссоциаци останавливают путем добавления DMEM или PBS, и затем клетки центрифугируют. Для пробирки объемом 50 мл: клетки центрифугируют при 490×g в течение 7 минут. Для флакона с коническим дном объемом 500 мл: клетки центрифугируют при 700×g в течение 8 минут. Клетки ресуспендируют в свежей среде. Жизнеспособность клеток и число клеток определяют с помощью NC200. Добавляют такое же количество 2× среды для криоконсервации (20% диметилсульфоксида (ДМСО)) с получением конечного содержания ДМСО 10% в суспензии клеток. Фасуют аликвотами по 0,5-10×106 клеток в каждый криофлакон (Themofisher или подобный). Это соответствует от приблизительно 10×106 до приблизительно 40×106 клеток на мл культуральной среды +10% ДМСО. Клетки помещают в Cryo 1°C контейнер для замораживания (NALGENE) и помещают контейнер в замораживатель на -80°C в течение ночи (или дольше, <2 недель), затем переносят в резервуар с жидким азотом. В альтернативе программируемый замораживатель может использоваться для замораживания клеток перед переносом в жидкий азот.
5. Размораживание клеток: клетки извлекают из жидкого азота, оставляют в водяной бане при 37°C на 2-3 минуты, пока не исчезнут кристаллы, быстро переносят в одну холодную пробирку с коническим дном объемом 15 мл с помощью наконечника на 1 мл. Флакон промывают холодной свежей средой 1-2 раза, затем в пробирку на 15 мл добавляют 9-12 мл холодной свежей среды. Центрифугируют при 1200 об/мин (300 g) в течение 5 минут. Удаляют супернатант, ресуспендируют осадок клеток в свежей среде и определяют количество и жизнеспособность клеток, как описано выше в Примере 2. Клетки сеют в новые покрытые флаконы или многоуровневые флаконы и инкубируют при условиях, описанных выше.
6. Подготовка клеток к трансплантации: клетки собирают с использованием TrypLE Express (Invitrogen), необязательно трипсина или эквивалента, или TRYP-LE EXPRESS или эквивалента, 2-кратное разведение (эквивалент 0,125%), 5-6 минут, инкубирование при 37°C. Диссоциацию останавливают путем добавления полной среды, DMEM или PBS. Суспензию клеток центрифугируют при 300 g в течение 5 минут, и затем клетки ресуспендируют в 0,5-3 мл холодной BSS Plus (или BSS/DPBS/HBSS). Жизнеспособность клеток и число клеток определяют с помощью трипанового синего (Invitrogen), подсчитывают с помощью Countess (Invitrogen), вручную или с помощью NC200. Клетки центрифугируют при 300 g в течение 5 минут и ресуспендируют клетки в холодной BSS Plus (или BSS/DPBS/HBSS) с получением подходящей дозировки для трансплантации.
[00259] Приготовление реагентов/клеточного продукта:
[00260] Приготовление полной среды (бессывороточной):
• В этом протоколе использовали улучшенную DMEM/F12 (Invitrogen). Необязательно может использоваться DMEM/F12 (Invitrogen или другой бренд), KnockOut DEMEM/F12 (Invitrogen или другой бренд), или нейробазальная среда (Invitrogen), UltraCULTURE (Lonza), ReNcell (Chemicon) или другая эквивалентная среда.
• Добавка N-2 (Invitrogen), необязательно B27 (Invitrogen или другой бренд) xeno-free, B27, не xeno-free, или Stempro (Invitrogen) или другой эквивалент.
• EGF (рекомбинантный человеческий эпидермальный фактор роста): Invitrogen, необязательно другого бренда.
• bFGF (основной фактор роста фибробластов): Invitrogen, необязательно другой бренд.
• GlutaMAX I: Invitrogen, необязательно L-глутамин (Invitrogen или другой бренд)
• Гентамицин (Invitrogen) для выделения и первого пассажа (приблизительно 4 дня, хотя гентамицин можно использовать дольше).
[00261] Фермент для пассирования:
• Раствор Версена: Thermo Fisher (Life tech), используемый, как описано выше, при пассажах 1 и 2. Раствор Версена представляет собой раствор ЭДТА для использования в качестве мягкого неферментативного реагента для диссоциации клетки. Раствор Версена Gibco® (0,48 мм) содержит 0,2 г ЭДТА (Na4) на литр фосфатно-солевого буфера (PBS).
[00262] Приготовление среды для криоконсервации:
• 90% полной среды.
• 10% ДМСО (диметилсульфоксида) (Sigma, необязательно другой бренд).
[00263] Покрытие флаконов:
• Использовали фибронектин человеческой плазмы (Invitrogen). В качестве альтернативы необязательно могут использовать орнитин, полилизин, ламинин или Матригель.
• Фибронектин разводят в DPBS.
o Концентрация: 1-5 мкг/см2, оставляют для нанесения покрытия на ночь, до 2 недель, при 4°C или на 1-3 часа в вытяжном шкафу при комнатной температуре, хранят при 4°C в течение ночи или до 2 недель.
o Промывают улучшенной DMEM/F12 перед применением.
o Флаконы также могут использоваться без промывки улучшенной DMEM/F12.
ЭКВИВАЛЕНТЫ
[00264] Подробности одного или нескольких вариантов осуществления изобретения изложены в прилагаемом описании выше. Хотя любые методы и материалы, подобные или эквивалентные описанным в настоящем документе, могут использоваться при практическом применении или тестировании настоящего изобретения, далее описаны примерные методы и материалы.
[00265] Представленное выше описание было представлено исключительно в целях иллюстрации и предназначено для ограничения изобретения не точной раскрытой формой, а только прилагаемой формулой изобретения.
[00266] В изложенное выше могут быть внесены модификации без отступления от основных аспектов изобретения. Хотя изобретение было подробно описано со ссылкой на один или несколько конкретных вариантов осуществления, специалисты в данной области техники поймут, что изменения могут быть внесены в варианты осуществления, конкретно раскрытые в данной заявке, и при этом такие модификации и улучшения будут входить в объем и сущность изобретения. Изобретение, иллюстративно описанное в настоящем документе, может быть подходящим образом осуществлено на практике в отсутствие какого-либо элемента(ов), конкретно не раскрытого в данном документе. Таким образом, например, в каждом случае в настоящем документе любой из терминов "включающий", "состоящий по существу из" и "состоящий из" может быть заменен любым из двух других терминов. Таким образом, использованные термины и выражения используются как описательные, а не ограничивающие термины, эквиваленты показанных и описанных признаков или их части не исключаются, и следует понимать, что в рамках изобретения допускаются различные модификации. Варианты осуществления изобретения представлены в следующей формуле изобретения.
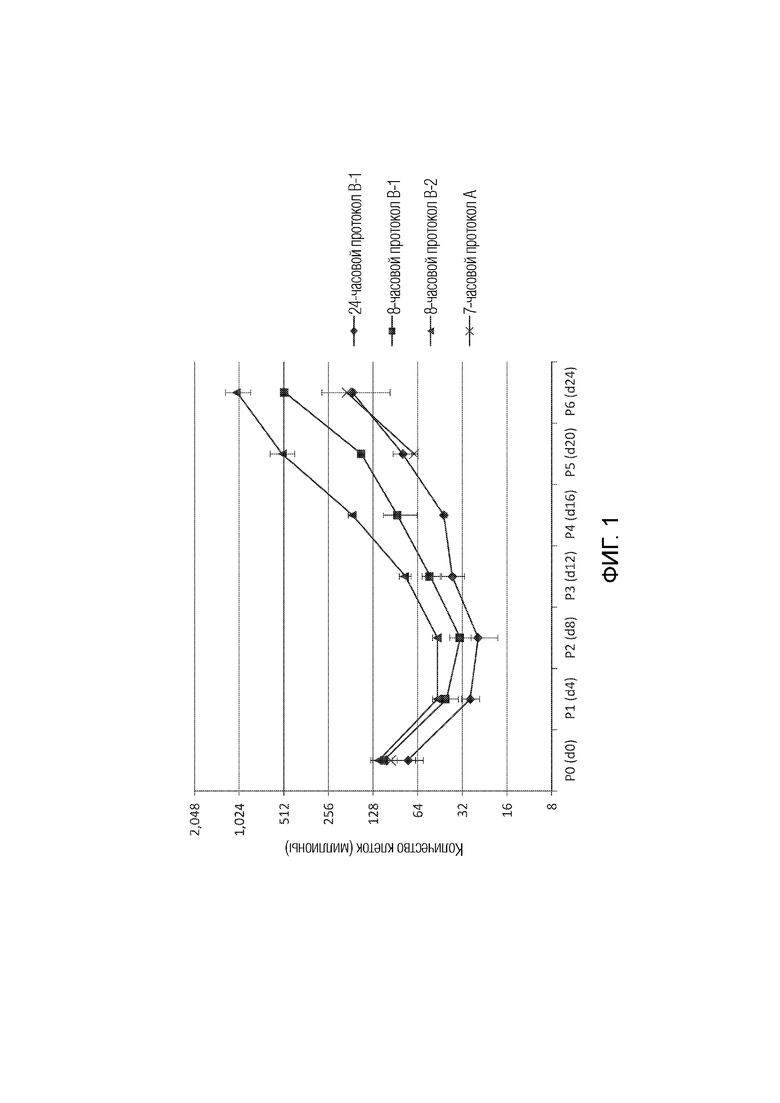
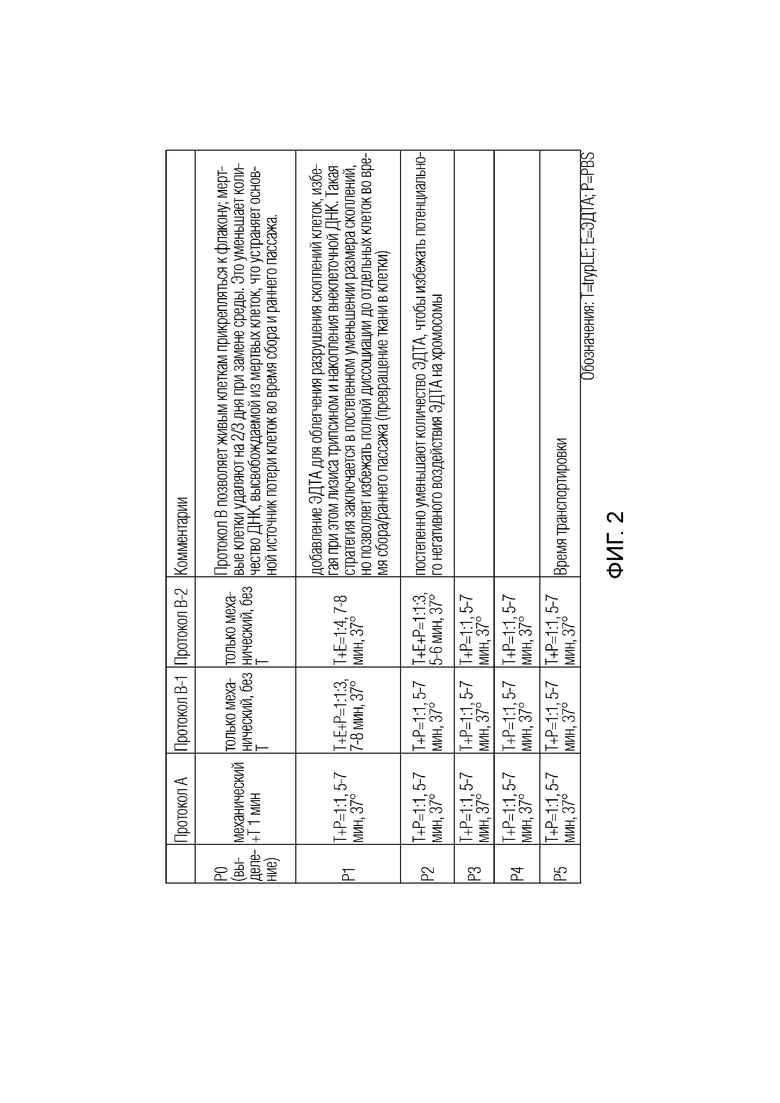
Группа изобретений относится к фармацевтической и медицинской промышленности, а именно к способу выделения первичных ретинальных клеток из человеческого образца и к способу культивирования выделенных первичных человеческих ретинальных клеток для получения популяции неиммортализованных человеческих ретинальных клеток-предшественников. Способ выделения первичных ретинальных клеток из человеческого образца, одного или пары человеческих глазных яблок, полученных от человека-донора, где указанные одно или пара человеческих глазных яблок обладают нормальной морфологией, включающей интактное глазное яблоко(и), прозрачную роговицу, нормальную форму или любую их комбинацию, включает: (a) выделение образца сетчатки, включающего множество первичных ретинальных клеток, из человеческого образца в течение 8 часов после сбора одного или пары глазных яблок от человека-донора, где человек-донор представляет собой плод с гестационным возрастом от 12 недель до 28 недель, (b) механическую диссоциацию множества первичных ретинальных клеток в образце сетчатки, выделенном на этапе (a), без обработки множества первичных ретинальных клеток протеазой, с получением в результате разделенной суспензии клеток и скоплений клеток, и (c) определение жизнеспособности, количества и морфологии первичных ретинальных клеток, полученных из образца сетчатки, где получают по меньшей мере 30×106 жизнеспособных первичных ретинальных клеток. Способ культивирования выделенных первичных человеческих ретинальных клеток для получения популяции неиммортализованных человеческих ретинальных клеток-предшественников включает: (a) посев в один или более культуральных флаконов или планшетов с покрытием, содержащих культуральную среду, в первом пассаже множества первичных ретинальных клеток, полученных вышеописанным способом, с получением множества культивированных ретинальных клеток; (b) посев в один или более культуральных флаконов или планшетов с покрытием, содержащих культуральные среды, во втором пассаже множества культивированных ретинальных клеток, полученных в первом пассаже; (c) посев в одну или более культуральных флаконов или планшетов с покрытием, содержащих культуральную среду, в третьем пассаже множества культивированных ретинальных клеток, полученных во втором пассаже; и (d) криоконсервацию множества культивированных ретинальных клеток; где один или более культуральных флаконов с покрытием засевают при плотности от 0,5×104 клеток на квадратный сантиметр (см2) до 5×106 клеток на см2, плотность посева в первом пассаже больше, чем плотность посева во втором пассаже, и плотность посева во втором пассаже больше, чем плотность посева в третьем пассаже, с получением в результате популяции неиммортализованных человеческих ретинальных клеток-предшественников, где культуральная среда включает улучшенную DMEM/F12, KnockOut DEMEM/F12, UltraCULTURE, ReNcell или нейробазальную среду, и при этом культуральная среда дополнительно дополнена по меньшей мере одним из N-2, B27, Stempro, EGF, bFGF, GlutaMAX I, L-глутамином или гентамицином. Вышеописанные способы, содержащие комбинацию 8-часового ограничения после сбора глазных яблок и исключительно механическую стадию диссоциации, позволяют эффективно повысить количество клеток, снизить риск лизиса клеток, повысить жизнеспособность клеток, повысить конечный выход. 2 н. и 17 з.п. ф-лы, 2 ил., 6 пр.
1. Способ выделения первичных ретинальных клеток из человеческого образца, одного или пары человеческих глазных яблок, полученных от человека-донора, где указанные одно или пара человеческих глазных яблок обладают нормальной морфологией, включающей интактное глазное яблоко(и), прозрачную роговицу, нормальную форму или любую их комбинацию, включающий:
(a) выделение образца сетчатки, включающего множество первичных ретинальных клеток, из человеческого образца в течение 8 часов после сбора одного или пары глазных яблок от человека-донора, где человек-донор представляет собой плод с гестационным возрастом от 12 недель до 28 недель,
(b) механическую диссоциацию множества первичных ретинальных клеток в образце сетчатки, выделенном на этапе (a), без обработки множества первичных ретинальных клеток протеазой, с получением в результате разделенной суспензии клеток и скоплений клеток и
(c) определение жизнеспособности, количества и морфологии первичных ретинальных клеток, полученных из образца сетчатки, где получают по меньшей мере 30×106 жизнеспособных первичных ретинальных клеток.
2. Способ по п.1, где перед этапом (a) человеческий образец помещают в среду для транспортировки культуры клеток, предпочтительно включающей RPMI-1640 с L-глутамином или улучшенную DMEM/F12, необязательно, где среда для транспортировки культуры клеток включает гентамицин в концентрации 0,5-50 микрограммов на миллилитр, где, необязательно, среда для транспортировки культуры клеток включает 50 микрограммов гентамицина на миллилитр.
3. Способ по любому из пп.1, 2, где этап (b) включает:
(i) перенос образца сетчатки в пробирку,
(ii) механическую диссоциацию образца сетчатки с получением множества разделенных первичных ретинальных клеток, предпочтительно путем суспендирования стерильной пипеткой, более предпочтительно путем суспендирования стерильной пипеткой от 2 до 50 раз, от 2 до 10 раз или от 4 до 8 раз,
(iii) осаждение множества разделенных первичных ретинальных клеток с помощью центрифугирования и
(iv) удаление супернатанта.
4. Способ по любому из пп.1-3, где этап (c) включает:
(i) ресуспендирование осажденных первичных ретинальных клеток из этапа (b) в культуральной среде с температурой 1-8°C и добавкой антибиотика,
(ii) посев множества разделенных ретинальных клеток в один или более флаконов или планшетов для культур клеток с покрытием, содержащих культуральную среду, где, необязательно, культуральная среда содержит добавку антибиотика,
(iii) инкубирование множества разделенных ретинальных клеток при 10-50°C, где, необязательно, инкубирование проходит при 37°C, и
(iv) определение количества и жизнеспособности первичных ретинальных клеток и скоплений ретинальных клеток.
5. Способ по п.4, где количество жизнеспособных первичных ретинальных клеток составляет от 30×106 до 1×109 жизнеспособных первичных ретинальных клеток или в пределах 73-147×106 жизнеспособных первичных ретинальных клеток.
6. Способ по любому из пп.4 или 5, где процент жизнеспособных подсчитанных клеток составляет от 10 до 100% или от 68 до 85%.
7. Способ культивирования выделенных первичных человеческих ретинальных клеток для получения популяции неиммортализованных человеческих ретинальных клеток-предшественников, где способ включает:
(a) посев в один или более культуральных флаконов или планшетов с покрытием, содержащих культуральную среду, в первом пассаже множества первичных ретинальных клеток, полученных способом по любому из пп.1-6, с получением множества культивированных ретинальных клеток;
(b) посев в один или более культуральных флаконов или планшетов с покрытием, содержащих культуральные среды, во втором пассаже множества культивированных ретинальных клеток, полученных в первом пассаже;
(c) посев в один или более культуральных флаконов или планшетов с покрытием, содержащих культуральную среду, в третьем пассаже множества культивированных ретинальных клеток, полученных во втором пассаже; и
(d) криоконсервацию множества культивированных ретинальных клеток;
где один или более культуральных флаконов с покрытием засевают при плотности от 0,5×104 клеток на квадратный сантиметр (см2) до 5×106 клеток на см2,
плотность посева в первом пассаже больше, чем плотность посева во втором пассаже, и
плотность посева во втором пассаже больше, чем плотность посева в третьем пассаже,
с получением в результате популяции неиммортализованных человеческих ретинальных клеток-предшественников,
где культуральная среда включает улучшенную DMEM/F12, KnockOut DEMEM/F12, UltraCULTURE, ReNcell или нейробазальную среду, и при этом культуральная среда дополнительно дополнена по меньшей мере одним из N-2, B27, Stempro, EGF, bFGF, GlutaMAX I, L-глутамином или гентамицином.
8. Способ по п.7, дополнительно включающий посев в один или более культуральных флаконов или планшетов с покрытием, содержащих питательную среду, в одном или более дополнительных пассажах множества культивированных ретинальных клеток, полученных в непосредственно предшествующем пассаже.
9. Способ по любому из пп.7 или 8, в котором культуральные флаконы или планшеты покрыты не содержащим ксеногенных компонентов фибронектином, орнитином, полилизином, ламинином или их комбинацией.
10. Способ по любому из пп.7-9, где множество первичных или культивированных ретинальных клеток культивируют при:
(1) 37°C в атмосфере с 0-30% CO2 и 0-50% O2,
(2) 37°C с содержанием CO2 меньше или равным 5% и O2 меньше или равным 20% или
(3) 37°C с содержанием CO2 меньше или равным 5% и O2 меньше или равным 3%.
11. Способ по любому из пп.7-10, в котором период времени между пассажами составляет от 2 до 8 дней, от 3 до 6 дней, от 4 до 5 дней или от 3 до 4 дней.
12. Способ по любому из пп.7-11, где множество первичных ретинальных клеток разделяют в первом пассаже с использованием первого ферментативного раствора, включающего:
(1) трипсин или эквивалент и этилендиаминтетрауксусную кислоту (ЭДТА), необязательно, где TrypLE и ЭДТА присутствуют в соотношении 1:4, или
(2) трипсин или эквивалент, ЭДТА, предпочтительно, TrypLE, ЭДТА и DPBS, необязательно, где TrypLE, ЭДТА и DPBS присутствуют в соотношении 1:1:3.
13. Способ по любому из пп. 7-12, в котором множество культивированных ретинальных клеток диссоциируют при втором пассаже вторым ферментативным раствором, содержащим:
(1) трипсин или его эквивалент, предпочтительно TrypLE, ЭДТА и DPBS, необязательно, где TrypLE, EDTA и DPBS присутствуют в соотношении 1:1:3, или
(2) эквивалент трипсина, предпочтительно TrypLE и DPBS, где необязательно TrypLE и DPBS присутствуют в соотношении 1:1.
14. Способ по п.13, где множество первичных ретинальных клеток разделяют в течение 5-20 минут, 6-10 минут или 7-8 минут при 37°C.
15. Способ по любому из пп.8-14, где множество культивированных ретинальных клеток разделяют в третьем или последующем пассаже с использованием третьего ферментативного раствора, включающего трипсин или эквивалент, предпочтительно TrypLE и DPBS, необязательно, где TrypLE и DPBS присутствуют в соотношении 1:1 в третьем ферментативном растворе.
16. Способ по п. 15, в котором множество культивированных ретинальных клеток разделяют в течение 5-10 минут или 5-7 минут при 37°С по меньшей мере при третьем или последующем пассаже.
17. Способ по любому из пп.7-16, где клетки сеют в культуральные флаконы или планшеты при плотности от 0,5×106 до 3,0×106 клеток/см2 в первом пассаже, от 0,1×106 до 0,5×106 клеток/см2 во втором пассаже, от 0,03×106 до 0,2×106 клеток/см2 в третьем пассаже и от 10000 до 60000 клеток/см2 в четвертом и последующих пассажах.
18. Способ по любому из пп.7-17, где криоконсервация в этапе (d) включает:
(i) ферментативную диссоциацию клеток с использованием трипсина или эквивалента,
(ii) остановку диссоциации избытком культуральной среды или улучшенной DMEM/F12,
(iii) центрифунгирование клеток при 10-10000×g в течение 1-30 минут,
(iv) ресуспендирование клеток в культуральной среде и определение общего количества и жизнеспособности клеток,
(v) добавление среды для криоконсервации с получением конечной концентрации диметилсульфоксида (ДМСО) 5-30%,
(vi) аликвотирование множества клеток в каждый криофлакон,
(vii) замораживание каждого флакона при использовании программируемого криозамораживателя и
(viii) помещение каждого флакона с клетками в жидкий N2.
19. Способ по любому из пп.3-18, где культуральная среда является бессывороточной.
| US 2016319243 А1, 03.11.2016 | |||
| СПОСОБ ПОЛУЧЕНИЯ ДЕДИФФЕРЕНЦИРОВАННЫХ КЛЕТОК РЕТИНАЛЬНОГО ПИГМЕНТНОГО ЭПИТЕЛИЯ ГЛАЗА ВЗРОСЛОГО ЧЕЛОВЕКА | 2009 |
|
RU2409663C1 |
| US 20090238800 A1, 24.09.2009 | |||
| US 6183735 B1, 06.02.2001 | |||
| PENG YANG et al | |||
| In vitro Isolation and Expansion of Human Retinal Progenitor cells //Experimental Neurology, 177, 2002, 326-331. | |||
Авторы
Даты
2023-12-05—Публикация
2019-09-27—Подача