Настоящая заявка испрашивает приоритет на основании заявки на патент №2019102824210 под названием «РАЗМОРАЖИВАЮЩАЯ ЖИДКОСТЬ ДЛЯ КРИОКОНСЕРВАЦИИ И СПОСОБ РАЗМОРАЖИВАНИЯ» и заявки на патент №2019102824155 под названием «ПРИМЕНЕНИЕ РАЗМОРАЖИВАЮЩЕЙ ЖИДКОСТИ ДЛЯ РАЗМОРАЖИВАНИЯ КРИОКОНСЕРВИРОВАННЫХ ООЦИТОВ ИЛИ ЭМБРИОНОВ», поданной в Национальное ведомство по интеллектуальной собственности Китая 9 апреля 2019 года. Эти две предыдущие заявки включены в настоящую заявку в полном объеме посредством ссылки.
ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится к технической области биомедицинских материалов и, в частности, к размораживающему раствору для криоконсервации и способу размораживания.
УРОВЕНЬ ТЕХНИКИ
Криоконсервация представляет собой сохранение биологического материала при сверхнизких температурах, замедляющих или приостанавливающих метаболизм и деление клеток, с возможностью продолжения их развития после восстановления нормальных физиологических температур. С момента ее создания данная технология стала одной из самых незаменимых исследовательских методик в области естественных наук и широко применяется. В последнее время, ввиду нарастающего напряжения в современной жизни, год от года наблюдается тенденция к снижению репродуктивной способности у людей, и, соответственно, сохранение репродуктивной способности становится все более и более насущным. Важным средством сохранения репродуктивной способности становится криоконсервация половых клеток человека (сперматозоидов и ооцитов), гонадных тканей и т.п. Кроме того, по мере старения мировой популяции, быстро растет потребность в криоконсервации донорских клеток, тканей или органов человека, которые могут быть использованы для регенеративной медицины и трансплантации органов. Следовательно, вопрос эффективной криоконсервации ресурсов на основе ценных клеток, тканей и органов на будущие потребности становится научно-технической проблемой, требующей неотложного решения.
В настоящее время наиболее часто используемым способом криоконсервации является витрификация. Во время процесса размораживания необходимо обратить внимание на предотвращение повреждения в результате цикла замораживания-размораживания, такого как кристаллы льда, холодовый шок, влияние растворенного вещества, разрушающее повреждение, перекристаллизация и осмотический шок. Исходя из соображений улучшения показателя выживаемости восстановленных эмбрионов и ооцитов, схема замораживания и размораживания в целом выглядит следующим образом: за счет быстрого процесса размораживания бластулы или ооциты при высоком осмотическим давлении размораживают в культуральных средах с определенным градиентом концентрации криопротектора, тем самым постепенно уменьшая разницу значений осмотического давления внутри и снаружи клеток, снижая скорость изменения объема клеток и предотвращая повреждение клеток или эмбрионов во время процесса размораживания. Большинство размораживающих реагентов, широко используемых в настоящее время в клинической практике, содержат сахарозу, сыворотку и буфер в качестве основных ингредиентов. Однако такие размораживающие растворы не могут обеспечить эффективный контроль роста и перекристаллизации кристаллов льда в процессе размораживания, что приводит к повреждениям клеток. Кроме того, существующие размораживающие растворы характеризуются рядом проблем, такими как короткий срок годности и риски в отношении паразитарных биологических загрязнений, обусловленных точно не установленным составом и легкостью ухудшения качества сыворотки.
РАСКРЫТИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
Для преодоления вышеуказанных недостатков предшествующего уровня техники согласно настоящему изобретению предложен размораживающий раствор для криоконсервации и способ размораживания.
Согласно настоящему изобретению реализованы следующие технические решения:
Размораживающий раствор, содержащий на 100 мл: 0,1-50 г биомиметического материала для подавления нарастания льда, 0-1,0 моль/л водорастворимого сахарида, и остальное составляет буфер, при этом биомиметический материал для подавления нарастания льда представляет собой материал для подавления нарастания льда, содержащий группу, характеризующейся сродством со льдом, и гидрофильную группу.
Согласно настоящему изобретению указанная гидрофильная группа представляет собой функциональную группу, способную к образованию нековалентного взаимодействия с молекулой воды, например, путем образования водородной связи, ван-дер-ваальсового взаимодействия, электростатического взаимодействия, гидрофобного взаимодействия или π-π-взаимодействия с водой; в качестве иллюстрации гидрофильная группа может быть выбрана из по меньшей мере одного из гидроксила (-ОН), амино (-NH2), карбоксила (-СООН) и ациламино (-CONH2) или из молекулы соединения, такого как пролин (L-Pro), аргинин (L-Arg), лизин (L-Lys), гистидин (L-His) и глицин (L-Gly), глюконо-дельта-лактон (GDL) и сахарид, и его молекулярного фрагмента.
Согласно настоящему изобретению указанная группа, характеризующаяся сродством со льдом, представляет собой функциональную группу, способную к образованию нековалентного взаимодействия со льдом, например, путем образования водородной связи, ван-дер-ваальсового взаимодействия, электростатического взаимодействия, гидрофобного взаимодействия или π-π-взаимодействия со льдом; в качестве иллюстрации группа, характеризующаяся сродством со льдом, может быть выбрана из гидроксила (-ОН), амино (-NH2), фенила (-C6H5) и пирролидинила (-C4H8N) или молекулы соединения, такого как глутамин (L-Gln), треонин (L-Thr), аспарагиновая кислота (L-Asn), бензол (C6H6) и пирролидин (C4H9N), и его молекулярного фрагмента.
Согласно настоящему изобретению биомиметический материал для подавления нарастания льда выбран из по меньшей мере одного из или комбинации двух или более из поливинилового спирта (ПВС), аминокислоты, полипептида и полиаминокислоты.
Согласно настоящему изобретению аминокислота может быть выбрана из одного из или комбинации двух или более из аргинина, треонина, пролина, лизина, гистидина, глутамина, аспарагиновой кислоты, глицина и т.п.; полиаминокислота может представлять собой гомополимер (со степенью полимеризации ≥ 2, предпочтительно 2-40, например, 6, 8, 15 и 20) по меньшей мере одного, выбранного из лизина, аргинина, пролина, треонина, гистидина, глутаминовой кислоты, аспарагиновой кислоты, глицина и т.п.
В качестве иллюстрации полипептид представляет собой полипептид, состоящий из двух или более из вышеуказанных аминокислот или гликопептидного производного, образованного в результате реакции аминокислоты с сахаридом (например, глюконолактоном). Например, полипептид представляет собой полипептид, состоящий из 2-8 разных аминокислот, и, например, дипептид, трипептид или тетрапептид. Согласно вариантам реализации настоящего изобретения полипептид представляет собой одно или более из L-Thr-L-Arg (TR), L-Thr-L-Pro (TP), L-Arg-L-Thr (RT), L-Pro-L-Thr (PT), L-Thr-L-Arg-L-Thr (TRT), L-Thr-L-Pro-L-Thr (TPT), L-Ala-L-Ala-L-Thr (AAT) или L-Thr-L-Cys-L-Thr (TCT).
Согласно настоящему изобретению содержание биомиметического материала для подавления нарастания льда составляет 1,0-50 г, 2,0-20 г или 5,0-10 г. Согласно одному варианту реализации настоящего изобретения содержание биомиметического материала для подавления нарастания льда составляет 3,0 г, 4,0 г, 5,0 г, 10 г, 25 г или 30 г.
Согласно одному варианту реализации настоящего изобретения биомиметический материал для подавления нарастания льда содержит 1,0-6,0 г ПВС.
Согласно одному варианту реализации настоящего изобретения биомиметический материал для подавления нарастания льда содержит 1,0-30 г аминокислоты. В качестве иллюстрации аминокислота представлена комбинацией аргинина и треонина, например, содержащей 1,0-20 г, 1,0-10 г или 1,0-5 г аргинина и 1,0-10 г, 1,0-5,0 г или 1,0-2,5 г треонина.
Согласно одному варианту реализации настоящего изобретения биомиметический материал для подавления нарастания льда содержит 0,1-9,0 г полиаминокислоты, например, 1-5,0 г. В качестве иллюстрации поли амино кислота представляет собой поли-L-пролин и/или поли-L-аргинин.
Согласно одному варианту реализации настоящего изобретения биомиметический материал для подавления нарастания льда содержит 1,0-50 г полипептида; например, 1,0-25 г, 1,0-13 г, 1,0-10 г или 1,0-5,0 г.
Согласно одному варианту реализации настоящего изобретения биомиметический материал для подавления нарастания льда представляет собой комбинацию ПВС и аминокислоты, полипептида и/или полиаминокислоты.
Согласно настоящему изобретению содержание водорастворимого сахарида на 100 мл размораживающего раствора составляет 0,1-1,0 моль/л, например, 0,1-0,8 моль/л, 0,2-0,6 моль/л, например, 0,25 моль/л, 0,5 моль/л, 1,0 моль/л.
Размораживающий реагент, содержащий размораживающий раствор I, размораживающий раствор II, размораживающий раствор III и размораживающий раствор IV, причем размораживающие растворы I-IV имеют составы для размораживающего раствора, описанные выше.
В соответствии с размораживающим реагентом согласно настоящему изобретению градиенты концентрации биомиметического материала для подавления нарастания льда в размораживающих растворах I IV конкретно не ограничены. Концентрации биомиметического материала для подавления нарастания льда в размораживающих растворах могут быть одинаковыми или разными. В качестве иллюстративного варианта реализации концентрации биомиметического материала для подавления нарастания льда в размораживающих растворах I-IV являются разными. Например, содержание биомиметического материала для подавления нарастания льда в размораживающем растворе II составляет 50-100% от содержания в размораживающем растворе I, а содержание биомиметического материала для подавления нарастания льда в размораживающем растворе III составляет 50-100% от содержания в размораживающем растворе II.
В размораживающем реагенте согласно настоящему изобретению размораживающие растворы I IV содержат 1,0-6,0 г ПВС; и предпочтительно концентрации ПВС в размораживающих растворах I-IV являются одинаковыми.
В размораживающем реагенте согласно настоящему изобретению концентрация водорастворимого сахарида в размораживающем растворе II составляет 50-100% от концентрации в размораживающем растворе I, концентрация водорастворимого сахарида в размораживающем растворе III составляет 50-100% от концентрации в размораживающем растворе II, а концентрация сахарида в размораживающем растворе IV составляет 0.
Согласно одному варианту реализации размораживающего реагента согласно настоящему изобретению размораживающий раствор I содержит на 100 мл: 1,0-50 г аминокислоты, 1,0-5,0 г ПВС, водорастворимый сахарид в концентрации 1,0 моль/л, и остальное составляет буфер;
размораживающий раствор II содержит на 100 мл: 1,0-25 г аминокислоты, 1,0-5,0 г ПВС, водорастворимый сахарид в концентрации 0,5 моль/л, и остальное составляет буфер;
размораживающий раствор III содержит на 100 мл: 1,0-12,5 г аминокислоты, 1,0-5,0 г ПВС, водорастворимый сахарид в концентрации 0,25 моль/л, и остальное составляет буфер;
размораживающий раствор IV содержит на 100 мл: 0-6,25 г аминокислоты, 1,0-5,0 г ПВС, и остальное составляет буфер.
Согласно одному варианту реализации размораживающего реагента согласно настоящему изобретению размораживающий раствор I содержит на 100 мл: 1,0-5,0 г ПВС, водорастворимый сахарид в концентрации 1,0 моль/л, и остальное составляет буфер;
размораживающий раствор II содержит на 100 мл: 1,0-5,0 г ПВС, водорастворимый сахарид в концентрации 0,5 моль/л, и остальное составляет буфер;
размораживающий раствор III содержит на 100 мл: 1,0-5,0 г ПВС, водорастворимый сахарид в концентрации 0,25 моль/л, и остальное составляет буфер;
размораживающий раствор IV содержит на 100 мл: 1,0-5,0 г ПВС, и остальное составляет буфер.
Согласно одному варианту реализации размораживающего реагента согласно настоящему изобретению размораживающий раствор I содержит на 100 мл: 1,0-9,0 г полиаминокислоты, 0,1-5,0 г ПВС, водорастворимый сахарид в концентрации 1,0 моль/л, и остальное составляет буфер;
размораживающий раствор II содержит на 100 мл: 0,1-4,5 г полиаминокислоты, 1,0-5,0 г ПВС, водорастворимый сахарид в концентрации 0,5 моль/л, и остальное составляет буфер;
размораживающий раствор III содержит на 100 мл: 0,1-2,3 г полиаминокислоты, 1,0-5,0 г ПВС, водорастворимый сахарид в концентрации 0,25 моль/л, и остальное составляет буфер;
размораживающий раствор IV содержит на 100 мл: 0-1,2 г полиаминокислоты, 1,0-5,0 г ПВС, и остальное составляет буфер.
Согласно одному варианту реализации размораживающего реагента согласно настоящему изобретению размораживающий раствор I содержит на 100 мл: 1,0-50 г полипептида, 1,0-5,0 г ПВС, водорастворимый сахарид в концентрации 1,0 моль/л, и остальное составляет буфер;
размораживающий раствор II содержит на 100 мл: 1,0-25 г полипептида, 1,0-5,0 г ПВС, водорастворимый сахарид в концентрации 0,5 моль/л, и остальное составляет буфер;
размораживающий раствор III содержит на 100 мл: 1,0-12,5 г полипептида, 1,0-5,0 г ПВС, водорастворимый сахарид в концентрации 0,25 моль/л, и остальное составляет буфер;
размораживающий раствор IV содержит на 100 мл: 0-6,25 г полипептида, 1,0-5,0 г ПВС, и остальное составляет буфер.
Согласно настоящему изобретению водорастворимый сахарид может представлять собой по меньшей мере одно из невосстанавливающего дисахарида, водорастворимого полисахарида и гликозида, например, выбран из сахарозы и трегалозы, предпочтительно, сахарозы. Водорастворимый сахарид может защищать клеточные мембраны и препятствовать седиментации клеток.
Согласно настоящему изобретению буфер может быть выбран из по меньшей мере одного из DPBS, HEPES-забуференного HTF-буфера и других буферов для культур клеток.
Согласно настоящему изобретению ПВС выбран из одного из или комбинации двух или более ПВС, таких как изотактический ПВС, синдиотактический ПВС и атактический ПВС. Например, ПВС характеризуется синдиотактичностью 15-65%, в частности, например, 40-60% или 53-55%. Предпочтительным является атактический ПВС, например, ПВС с синдиотактичностью 45-65%.
Согласно настоящему изобретению ПВС может быть выбран из ПВС с молекулярной массой 10-500 кДа или более, например, 10-30 кДа, 30-50 кДа, 80-90 кДа или 200-500 кДа.
Согласно настоящему изобретению ПВС может быть выбран из ПВС со степенью гидролиза более 80%, например, 80-99%, 82-87%, 87-89%, 89-99% или 98-99%.
Размораживающий раствор согласно настоящему изобретению может быть получен способами, известными в данной области техники, такими как:
растворение биомиметического материала для подавления нарастания льда в одной части буфера и регулирование рН; растворение водорастворимого сахарида в другой части буфера; и охлаждение двух растворов до комнатной температуры, и смешивание двух растворов.
Способ размораживания криоконсервированных клетки, ткани или органа, включающий:
размораживание криоконсервированных клетки, ткани или органа в размораживающем растворе I при 37°С в течение 3-5 минут, и затем последовательно размораживание криоконсервированной клетки или ткани в размораживающем растворе II, размораживающем растворе III и размораживающем растворе IV в течение 3 5 минут при комнатной температуре.
Размораживающий раствор и размораживающий реагент могут быть применены для размораживания криоконсервированных ооцитов, эмбриона, ткани или органа. Например, ткань или орган представляют собой овариальную ткань или овариальный орган.
Кроме того, согласно настоящему изобретению предложено применение размораживающего раствора и размораживающего реагента, в частности, применение для размораживания криоконсервированных ооцитов, эмбриона, ткани или органа, например, ткань или орган представляет собой овариальную ткань или овариальный орган.
Преимущества
Размораживающий раствор и размораживающий реагент согласно настоящему изобретению получают из биомиметического материала для подавления нарастания льда, характеризующегося сродством со льдом и гидрофильными свойствами, который может обеспечивать эффективный контроль роста кристаллов льда и значительное уменьшение повреждения клеток или тканей, обусловленного изменением температуры в процессе размораживания. Размораживающий раствор и размораживающий реагент характеризуются надлежащей биосовместимостью, не содержат сыворотки животных и характеризуются низкой токсичностью, и, таким образом, характеризуются более низкими рисками в отношении, например, короткого срока годности и включения паразитарных биологических загрязнителей, а также характеризуются наличием преимуществ, заключающихся в сохранении стабильности при пассировании клеток или тканей по сравнению с традиционными размораживающими растворами, содержащими сыворотку. Настоящее изобретение имеет простой состав, характеризуется экономической эффективностью и надлежащей перспективой применения.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
ФИГ. 1 представляет собой фотографию окрашенного среза свежего незамороженного овариального органа;
ФИГ. 2 представляет собой фотографию окрашенного среза овариального органа, размороженного с применением размораживающего раствора из Примера 1;
ФИГ. 3 представляет собой фотографию окрашенного среза свежей незамороженной овариальной ткани; и
ФИГ. 4 представляет собой фотографию окрашенного среза овариальной ткани, размороженной с применением размораживающего раствора из примера 1.
ПОДРОБНОЕ ОПИСАНИЕ
Способ получения согласно настоящему изобретению будет более подробно проиллюстрирован со ссылкой на следующие конкретные примеры. Следует понимать, что следующие примеры представлены лишь с целью типичной иллюстрации и пояснения настоящего изобретения, и их не следует рассматривать как ограничивающие объем правовой охраны настоящего изобретения. Все методики, разрабатываемые на основании вышеуказанного содержания настоящего изобретения, подпадают под объем правовой охраны настоящего изобретения.
Если не указано иное, экспериментальные методы, используемые в следующих примерах, представляют собой традиционные методы. Если не указано иное, реагенты, материалы и т.п., используемые в следующих примерах, являются коммерчески доступными.
ПВС, используемый в примерах настоящего изобретения, характеризуется синдиотактичностью 50-55%, молекулярной массой 13-23 кДа и степенью гидролиза 98%.
В примерах настоящего изобретения поли-L-пролин, используемый в криоконсервирующем растворе, характеризуется степенью полимеризации 15 и молекулярной массой 1475. Поли-L-пролин в размораживающем растворе характеризуется степенью полимеризации 8 и молекулярной массой 795.
В примерах настоящего изобретения использовали следующие замораживающий уравновешивающий раствор и криоконсервирующий раствор:
Криоконсервирующий раствор А (общий объем: 100 мл): 2,0 г ПВС растворяли в 30 мл DPBS на водяной бане при 80°С с использованием магнитной мешалки при нагревании и доводили рН до 7,0 с получением раствора 1; 17 г (0,05 моль) сахарозы (конечная концентрация сахарозы в криоконсервирующем растворе составляла 0,5 моль/л) растворяли под воздействием ультразвука в 25 мл DPBS и после полного растворения сахарозы добавляли 10 мл этиленгликоля с получением раствора 2; после повторного достижения комнатной температуры раствор 1 и раствор 2 хорошо смешивали, регулировали рН, и смесь разбавляли до 100 мл DPBS для последующего применения.
Замораживающий уравновешивающий раствор а (общий объем: 100 мл): 2,0 г ПВС растворяли в 50 мл DPBS на водяной бане при 80°С с использованием магнитной мешалки при нагревании и доводили рН до 7,0 после полного растворения ПВС; к раствору добавляли 7,5 мл этиленгликоля и тщательно перемешивали, регулировали рН и разбавляли смесь до 100 мл с помощью DPBS для последующего применения.
Криоконсервирующий раствор В (общий объем: 100 мл): 2,0 г ПВС растворяли в 25 мл DPBS на водяной бане при 80°С с использованием магнитной мешалки при нагревании и доводили рН до 7,0 с получением раствора 1; 1,5 г поли-L-пролина растворяли под воздействием ультразвука в дополнительных 20 мл DPBS и доводили рН до 7,0 с получением раствора 2; 17 г (0,05 моль) сахарозы (конечная концентрация сахарозы в криоконсервирующем растворе составляла 0,5 моль/л) растворяли под воздействием ультразвука в 25 мл DPBS и после полного растворения сахарозы добавляли 10 мл этиленгликоля с получением раствора 3; после повторного достижения комнатной температуры раствор 1, раствор 2 и раствор 3 хорошо смешивали, регулировали рН и смесь разбавляли до 100 мл DPBS для последующего применения.
Замораживающий уравновешивающий раствор b (аналогичный замораживающему уравновешивающему раствору а; общий объем: 100 мл): 2,0 г ПВС растворяли в 40 мл DPBS на водяной бане при 80°С с использованием магнитной мешалки при нагревании и доводили рН до 7,0 после полного растворения ПВС; к раствору добавляли 7,5 мл этиленгликоля и тщательно перемешивали, регулировали рН и разбавляли смесь до 100 мл с помощью DPBS для последующего применения.
Криоконсервирующий раствор С, содержащий на 1 мл: 10% (об/об) этиленгликоля, 20% (об/об) фетальной бычьей сыворотки, сахарозу в концентрации 0,5 М, и остальное составляет DPBS.
Замораживающий уравновешивающий раствор с, содержащий на 1 мл: 7,5% (об/об) этиленгликоля, 20% (об/об) фетальной бычьей сыворотки, и остальное составляет DPBS.
Пример 1
Размораживающий раствор I содержит на 100 мл:
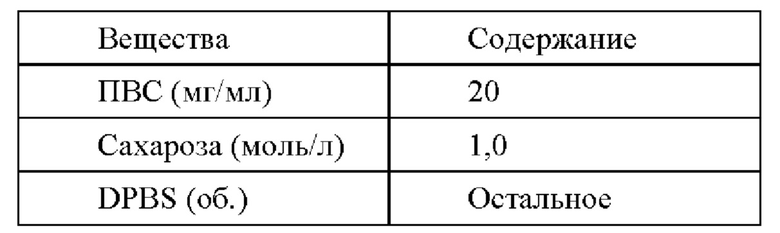
Размораживающий раствор II содержит на 100 мл:
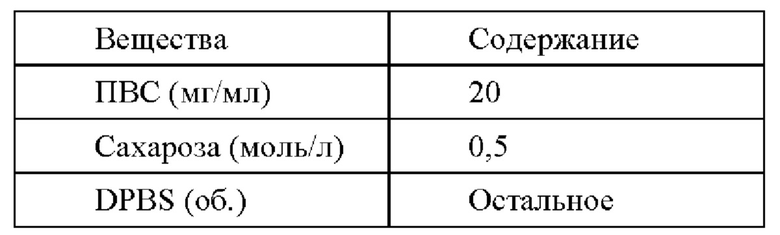
Размораживающий раствор III содержит на 100 мл:
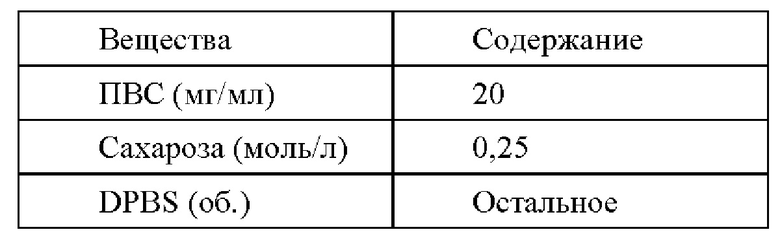
Размораживающий раствор IV содержит на 100 мл:
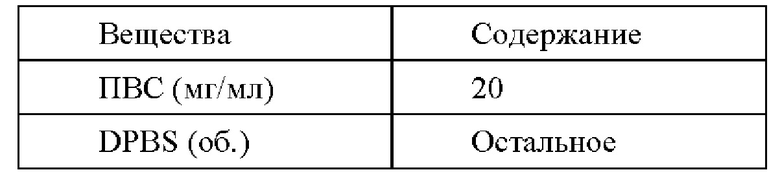
Пример 2
Размораживающий раствор I содержит на 100 мл:
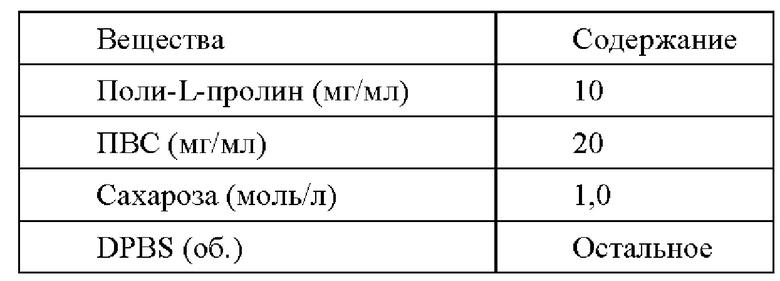
Размораживающий раствор II содержит на 100 мл:
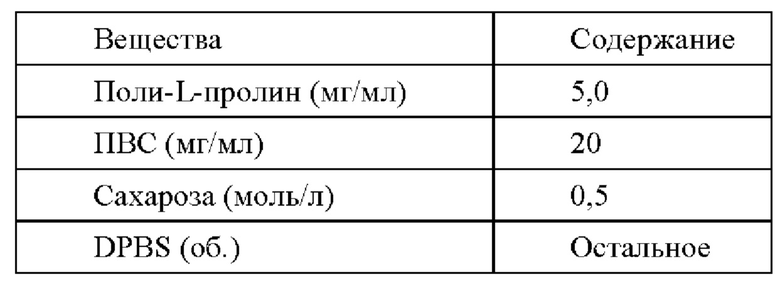
Размораживающий раствор III содержит на 100 мл:
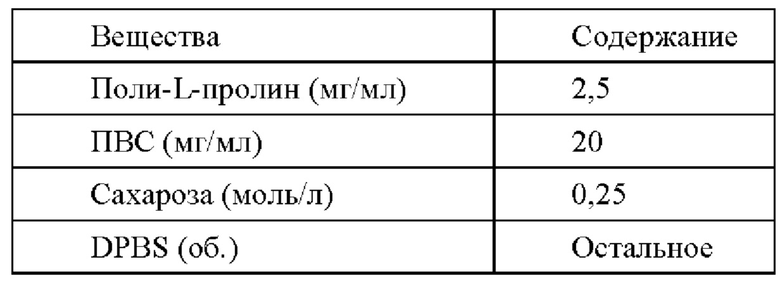
Размораживающий раствор IV содержит на 100 мл:

Сравнительный пример 1:
Размораживающий раствор I содержит: сахарозу в концентрации 1,0 моль/л, 20% сыворотки, и остальное составляет DPBS;
Размораживающий раствор II содержит: сахарозу в концентрации 0,5 моль/л, 20% сыворотки, и остальное составляет DPBS;
Размораживающий раствор III содержит: сахарозу в концентрации 0,25 моль/л, 20% сыворотки, и остальное составляет DPBS;
Размораживающий раствор IV содержит: сахарозу в концентрации 0 моль/л, 20% сыворотки, и остальное составляет DPBS.
Вариант применения 1. Размораживание криоконсервированных ооцитов
Способ криоконсервирования ооцитов согласно настоящему изобретению, в частности, включает следующие стадии: сначала ооциты уравновешивали в замораживающем уравновешивающем растворе в течение 5 минут; затем ооциты уравновешивали в криоконсервирующем растворе в течение 45 секунд; ооциты, уравновешенные в криоконсервирующем растворе, загружали на соломинки; затем соломинки быстро помещали в жидкий азот (-196°С) и закрывали соломинки для криоконсервации.
Ооциты мыши размораживали с помощью размораживающих реагентов, полученных из составов из Примера 1 и Примера 2, и размораживающих реагентов, полученных в Сравнительном примере 1. Способ размораживания ооцитов, в частности, включает следующие стадии: ооциты быстро переносили из жидкого азота в размораживающий раствор I при 37°С и инкубировали в течение 3-5 минут; затем ооциты последовательно инкубировали в размораживающем растворе II, размораживающем растворе III и размораживающем растворе IV в течение 3 минут в каждом при комнатной температуре; затем ооциты переносили в культуральную среду, и инкубировали в инкубаторе с содержанием диоксида углерода 5% при 37°С в течение 2 часов, и рассчитывали показатель выживаемости ооцитов (Таблица 1).
Вариант применения 2. Размораживание криоконсервированных эмбрионов
Способ криоконсервирования эмбрионов согласно настоящему изобретению, в частности, включает следующие стадии: сначала эмбрионы уравновешивали в замораживающем уравновешивающем растворе в течение 8 минут; затем эмбрионы уравновешивали в криоконсервирующем растворе, полученном в соответствии с составом, указанным выше, в течение 50 секунд; эмбрионы, уравновешенные в криоконсервирующем растворе, загружали на соломинки; затем соломинки быстро помещали в жидкий азот (-196°С) и закрывали соломинки для криоконсервации.
Эмбрионы мыши размораживали с помощью размораживающих реагентов, полученных из составов из Примера 1 и Примера 2, и размораживающих реагентов, полученных в Сравнительном примере 1. Способ размораживания эмбрионов, в частности, включает следующие стадии: эмбрионы быстро переносили из жидкого азота в размораживающий раствор I при 37°С и инкубировали в течение 3 5 минут; затем эмбрионы последовательно инкубировали в размораживающем растворе II, размораживающем растворе III и размораживающем растворе IV в течение 3 минут в каждом при комнатной температуре; затем эмбрионы переносили в культуральную среду, и инкубировали в инкубаторе с содержанием диоксида углерода 5% при 37°С в течение 2 часов, и рассчитывали показатель выживаемости эмбрионов (Таблица 2).
Показатель выживаемости в примерах настоящего изобретения представляет собой среднее для показателя выживаемости в 3-12 экспериментах, выполненных в двух повторностях.
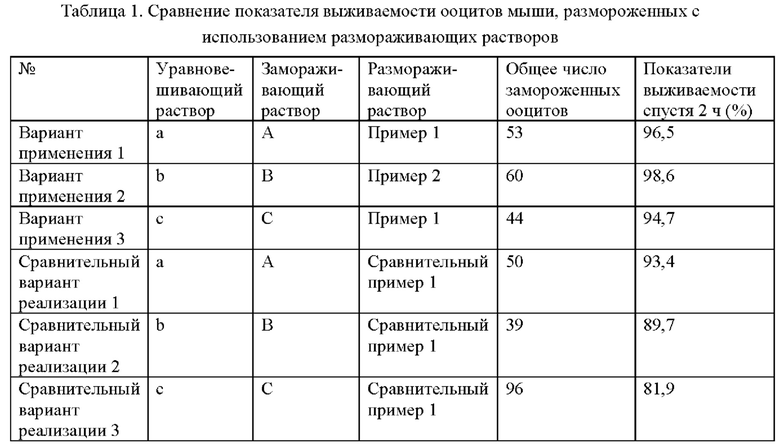
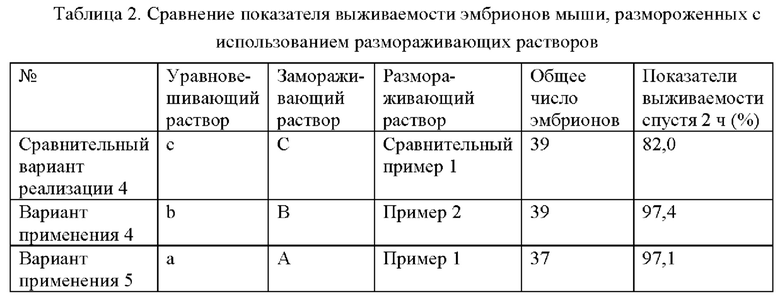
Из данных, приведенных в Таблицах 1 и 2, видно, что показатель выживаемости ооцитов, размороженных с использованием размораживающего реагента согласно настоящему изобретению, составлял более 94%, даже вплоть до 98,6%, и что показатель выживаемости размороженных эмбрионов составлял более 97%, что значительно выше, чем в Сравнительном примере 1 (коммерчески доступные размораживающие растворы), что указывает на то, что эффективность размораживающего реагента превосходила эффективность традиционных размораживающих растворов для витрификации при размораживании ооцитов и эмбрионов. Кроме того, размораживающий реагент согласно настоящему изобретению не содержит сыворотки, характеризуется низким риском в отношении паразитарных биологических загрязнений и т.п. и является более подходящим для сохранения стабильности при пассировании клеток или тканей.
Вариант применения 3. Размораживание криоконсервированных интактных овариальных органов или срезов овариальных тканей
Комбинацию вышеуказанного замораживающего уравновешивающего раствора а и криоконсервирующего раствора А использовали для криоконсервирования среза овариального органа 3-дневных новорожденных мышей и среза овариальной ткани половозрелых мышей, а затем для размораживания использовали вышеуказанный размораживающий раствор из Примера 1. Способ замораживания и размораживания включает следующие стадии: интактные овариальные органы или срезы овариальных тканей уравновешивали в уравновешивающем растворе при комнатной температуре в течение 25 минут, уравновешивали в полученном криоконсервирующем растворе в течение 15 минут и затем загружали на соломинки. Соломинки помещали в жидкий азот для консервации. После размораживания интактные овариальные органы или срезы овариальных тканей инкубировали в культуральных средах (10% FBS+а-МЕМ) в инкубаторе с 5% CO2 при 37°С для размораживания в течение 2 часов, а затем фиксировали 4% параформальдегидом, заливали в парафин и окрашивали НЕ для морфологического исследования.
Результаты представлены на ФИГ. 14, при этом ФИГ. 1 представляет собой фотографию окрашенного среза свежего незамороженного овариального органа; ФИГ. 2 представляет собой фотографию окрашенного среза овариального органа, размороженного с использованием размораживающего раствора из Примера 1; ФИГ. 3 представляет собой фотографию окрашенного среза свежей незамороженной овариальной ткани; и ФИГ. 4 представляет собой фотографию окрашенного среза овариальной ткани, размороженной с использованием размораживающего раствора из Примера 1. Видно, что после размораживания с использованием размораживающего раствора из Примера 1 фолликулярная структура и интерстициальная структура овариальных органов или овариальных тканей оставались относительно интактными, цитоплазма клеток была относительно однородной и слегка окрашенной в относительно большом количестве, а сокращения ядер и глубокое окрашивание были относительно умеренными; структура сосудистой стенки оставалась интактной, разрушение просвета было умеренным, цитоплазма клеток эндотелия была однородной и слегка окрашенной в относительно большом количестве, сокращения ядер и глубокое окрашивание были относительно умеренными, что свидетельствовало о надлежащем размораживающем эффекте.
Выше были описаны конкретные примеры согласно настоящему изобретению. Однако настоящее изобретение не ограничено вышеприведенными примерами. Какие-либо модификации, эквиваленты, улучшения и т.п., выполненные без отступления от сущности и принципа настоящего изобретения, безусловно подпадают под действие правовой охраны настоящего изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| КРИОКОНСЕРВИРУЮЩИЙ РАСТВОР, НЕ СОДЕРЖАЩИЙ ДМСО, И СПОСОБ ЕГО ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ | 2020 |
|
RU2785227C1 |
| БИОМИМЕТИЧЕСКИЙ МАТЕРИАЛ, ПОДАВЛЯЮЩИЙ РОСТ ЛЬДА, И КРИОКОНСЕРВИРУЮЩИЙ РАСТВОР, СОДЕРЖАЩИЙ ЭТОТ МАТЕРИАЛ | 2020 |
|
RU2787934C1 |
| СТАБИЛЬНЫЙ ФАРМАЦЕВТИЧЕСКИЙ ПРЕПАРАТ НА ОСНОВЕ АНТИТЕЛА К PD-1 И ЕГО ПРИМЕНЕНИЕ В МЕДИЦИНЕ | 2016 |
|
RU2731418C2 |
| СПОСОБ ВИТРИФИКАЦИИ ОВАРИАЛЬНОЙ ТКАНИ | 2018 |
|
RU2678106C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ОСНОВЕ АНТИТЕЛА К PD-L1 И ЕЕ ПРИМЕНЕНИЕ | 2018 |
|
RU2766590C2 |
| Компонент катализатора для полимеризации или сополимеризации олефинов, способ его получения и его применение | 2021 |
|
RU2809186C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ АНТИТЕЛО К SOST, И ЕЕ ПРИМЕНЕНИЯ | 2018 |
|
RU2779430C2 |
| КОМПОЗИЦИИ И СПОСОБЫ КРИОКОНСЕРВАЦИИ КЛЕТОК | 2021 |
|
RU2840854C1 |
| МАКРОПОРИСТЫЙ ГЕЛЕВЫЙ МАТЕРИАЛ И ИЗДЕЛИЯ НА ЕГО ОСНОВЕ | 2006 |
|
RU2328313C2 |
| КЕРАТИН BD-10, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ЕГО ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И ПРИМЕНЕНИЕ | 2020 |
|
RU2823655C1 |

Изобретение относится к области сохранения биологического материала, в частности, размораживанию криоконсервированных клеток или тканей. Размораживающий раствор содержит на 100 мл: 0,1-50 г биомиметического материала для подавления нарастания льда, водорастворимый сахарид в концентрации 0-1,0 моль/л, и остальное составляет буфер. Биомиметический материал для подавления нарастания льда представляет собой атактический поливиниловый спирт (ПВС), имеющий синдиотактичность, составляющую 15-65%, молекулярную массу 10-500 кДа, или комбинацию указанного атактического поливинилового спирта (ПВС), аминокислоты, полипептида и/или полиаминокислоты. Аминокислота выбрана из одного из или комбинации двух или более из аргинина, треонина, пролина, лизина, гистидина, глутамина, аспарагиновой кислоты, глицина. Полипептид представляет собой одно или более из L-Thr-L-Arg (TR), L-Thr-L-Pro (TP), L-Arg-L-Thr (RT), L-Pro-L-Thr (PT), L-Thr-L-Arg-L-Thr (TRT), L-Thr-L-Pro-L-Thr (TPT) или L-Thr-L-Cys-L-Thr (TCT). Размораживающий раствор применяют в размораживающем реагенте, который содержит размораживающие растворы I-IV, причем размораживающие растворы I-IV имеют отличные друг от друга составы по количественному содержанию исходных компонентов. Предлагаемый размораживающий раствор обеспечивает эффективный контроль роста кристаллов льда, а также существенное снижение повреждения клеток или ткани, обусловленного неконтролируемым ростом кристаллов льда во время восстановления, снижение рисков в отношении короткого срока годности и включения паразитарных биологических загрязнителей в связи с отсутствием в составе сыворотки животных, способствует сохранению стабильности при пассировании клеток или тканей, обладает низкой токсичностью. 4 н. и 6 з.п. ф-лы, 4 ил., 2 табл., 3 пр.
1. Размораживающий раствор, содержащий на 100 мл:
- 0,1-50 г биомиметического материала для подавления нарастания льда,
- водорастворимый сахарид в концентрации 0-1,0 моль/л, и
- остальное составляет буфер,
при этом биомиметический материал для подавления нарастания льда представляет собой атактический поливиниловый спирт (ПВС), имеющий синдиотактичность, составляющую 15-65%, молекулярную массу 10-500 кДа, или комбинацию указанного атактического поливинилового спирта (ПВС), аминокислоты, полипептида и/или полиаминокислоты,
при этом аминокислота выбрана из одного из или комбинации двух или более из аргинина, треонина, пролина, лизина, гистидина, глутамина, аспарагиновой кислоты, глицина; и
при этом полипептид представляет собой одно или более из L-Thr-L-Arg (TR), L-Thr-L-Pro (TP), L-Arg-L-Thr (RT), L-Pro-L-Thr (PT), L-Thr-L-Arg-L-Thr (TRT), L-Thr-L-Pro-L-Thr (TPT) или L-Thr-L-Cys-L-Thr (TCT).
2. Размораживающий раствор по п. 1, отличающийся тем, что полиаминокислота представляет собой гомополимер (со степенью полимеризации ≥2, предпочтительно 2-40, например, 6, 8, 15 и 20) по меньшей мере одного, выбранного из лизина, аргинина, пролина, треонина, гистидина, глутаминовой кислоты, аспарагиновой кислоты, глицина;
ПВС характеризуется синдиотактичностью, составляющей 45-65 %; и
ПВС характеризуется степенью гидролиза 80-99%, 82-87%, 87-89%, 89-99% или 98-99%.
3. Размораживающий раствор по п. 1 или 2, отличающийся тем, что содержание биомиметического материала для подавления нарастания льда составляет 1,0-30 г;
при этом предпочтительно биомиметический материал для подавления нарастания льда содержит 1,0-6,0 г ПВС;
предпочтительно биомиметический материал для подавления нарастания льда содержит 1,0-30 г аминокислоты, и более предпочтительно аминокислота представляет собой комбинацию аргинина и треонина;
предпочтительно биомиметический материал для подавления нарастания льда содержит 0,1-9,0 г полиаминокислоты;
предпочтительно биомиметический материал для подавления нарастания льда содержит 1,0-50 г полипептида;
предпочтительно биомиметический материал для подавления нарастания льда представляет собой комбинацию атактического ПВС и аминокислоты, полипептида и/или полиаминокислоты.
4. Размораживающий раствор по любому из пп. 1-3, отличающийся тем, что водорастворимый сахарид может представлять собой по меньшей мере одно из невосстанавливающего дисахарида, водорастворимого полисахарида и гликозида, например, выбран из сахарозы, трегалозы, водорастворимой целлюлозы (например, гидроксипропилметилцеллюлозы) и полисахарозы;
предпочтительно буфер может быть выбран из по меньшей мере одного из DPBS, HEPES-забуференного HTF-буфера и других буферов для клеток.
5. Размораживающий реагент, содержащий размораживающий раствор I, размораживающий раствор II, размораживающий раствор III и размораживающий раствор IV, причем размораживающие растворы I-IV имеют отличные друг от друга составы согласно любому из пп. 1-4.
6. Размораживающий реагент по п. 5, отличающийся тем, что предпочтительно концентрация водорастворимого сахарида в размораживающем растворе II составляет 50-100% от концентрации в размораживающем растворе I, концентрация водорастворимого сахарида в размораживающем растворе III составляет 50-100% от концентрации в размораживающем растворе II, а концентрация водорастворимого сахарида в размораживающем растворе IV составляет 0; предпочтительно в размораживающих растворах I-IV, например, концентрации биомиметического материала для подавления нарастания льда являются одинаковыми или разными, например, концентрация биомиметического материала для подавления нарастания льда в размораживающем растворе II составляет 50-100% от концентрации в размораживающем растворе I, концентрация биомиметического материала для подавления нарастания льда в размораживающем растворе III составляет 50-100% от концентрации в размораживающем растворе II, и концентрация биомиметического материала для подавления нарастания льда в размораживающем растворе IV составляет 0;
размораживающие растворы I-IV предпочтительно содержат 1,0-6,0 г атактического ПВС; и предпочтительно концентрации атактического ПВС в размораживающих растворах I-IV являются одинаковыми.
7. Размораживающий реагент по п. 5 или 6, отличающийся тем, что в размораживающем реагенте размораживающий раствор I содержит на 100 мл: 1,0-50 г по меньшей мере одного из аминокислоты и полипептида, 1,0-5,0 г атактического ПВС, водорастворимый сахарид в концентрации 1,0 моль/л, и остальное составляет буфер;
размораживающий раствор II содержит на 100 мл: 1,0-25 г по меньшей мере одного из аминокислоты и полипептида, 1,0-5,0 г атактического ПВС, водорастворимый сахарид в концентрации 0,5 моль/л, и остальное составляет буфер;
размораживающий раствор III содержит на 100 мл: 1,0-12,5 г по меньшей мере одного из аминокислоты и полипептида, 1,0-5,0 г атактического ПВС, водорастворимый сахарид в концентрации 0,25 моль/л, и остальное составляет буфер;
размораживающий раствор IV содержит на 100 мл: 0-6,25 г по меньшей мере одного из аминокислоты и полипептида, 1,0-5,0 г атактического ПВС, и остальное составляет буфер.
8. Размораживающий реагент по п. 5 или 6, отличающийся тем, что размораживающий раствор I содержит на 100 мл: 1,0-5,0 г атактического ПВС, водорастворимый сахарид в концентрации 1,0 моль/л, и остальное составляет буфер;
размораживающий раствор II содержит на 100 мл: 1,0-5,0 г атактического ПВС, водорастворимый сахарид в концентрации 0,5 моль/л, и остальное составляет буфер;
размораживающий раствор III содержит на 100 мл: 1,0-5,0 г атактического ПВС, водорастворимый сахарид в концентрации 0,25 моль/л, и остальное составляет буфер;
размораживающий раствор IV содержит на 100 мл: 1,0-5,0 г атактического ПВС, и остальное составляет буфер;
предпочтительно размораживающий раствор I содержит на 100 мл: 0,1-9,0 г полиаминокислоты, 1,0-5,0 г атактического ПВС, водорастворимый сахарид в концентрации 1,0 моль/л, и остальное составляет буфер;
размораживающий раствор II содержит на 100 мл: 0,1-4,5 г полиаминокислоты, 1,0-5,0 г атактического ПВС, водорастворимый сахарид в концентрации 0,5 моль/л, и остальное составляет буфер;
размораживающий раствор III содержит на 100 мл: 0,1-2,3 г полиаминокислоты, 1,0-5,0 г атактического ПВС, водорастворимый сахарид в концентрации 0,25 моль/л, и остальное составляет буфер;
размораживающий раствор IV содержит на 100 мл: 0-1,2 г полиаминокислоты, 1,0-5,0 г атактического ПВС, и остальное составляет буфер.
9. Способ размораживания криоконсервированной клетки или ткани с использованием размораживающего реагента по любому из пп. 5-8, включающий:
размораживание криоконсервированной клетки или ткани в размораживающем растворе I при 37°C в течение 3-5 минут, и затем последовательно размораживание криоконсервированной клетки или ткани в размораживающем растворе II, размораживающем растворе III и размораживающем растворе IV в течение 3-5 минут при комнатной температуре.
10. Применение размораживающего раствора по любому из пп. 1-4 или размораживающего реагента по любому из пп. 5-8 для размораживания криоконсервированных ооцита, эмбриона, ткани или органа, при этом, например, ткань или орган представляет собой овариальную ткань или овариальный орган.
| CN 109136176 A, 04.01.2019 | |||
| WO 2013117925 A1, 15.08.2013 | |||
| WO 1991010361 A1, 25.07.1991 | |||
| Кипятильник для воды | 1921 |
|
SU5A1 |
Авторы
Даты
2023-03-06—Публикация
2020-03-02—Подача