Настоящее изобретение относится к способу лечения спастичности нижних конечностей у субъекта, в частности, человека в возрасте 18 лет или младше, например от 2 до 17 лет, включающему в себя введение субъекту эффективного количества ботулинического нейротоксина. Изобретение также относится к композиции для применения в лечении спастичности нижних конечностей у пациента, содержащей ботулинический нейротоксин. Кроме того, изобретение относится к средству для применения при определении объема дозы действующего вещества, вводимого субъекту.
УРОВЕНЬ ТЕХНИКИ
Спастичность представляет собой состояние, при котором наблюдается патологическое повышение мышечного тонуса или жесткости в одной или нескольких мышцах, что может мешать их движению. Спастичность обычно вызывается повреждением нервных путей в головном или спинном мозге, которые контролируют движение мышц, и может возникать в связи с церебральным параличом, травмой спинного мозга, рассеянным склерозом, инсультом и травмой головного мозга или головы.
Спастичность нижних конечностей обычно включает спастичность в комплексе икроножной и камбаловидной мышц, расположенном в икре ноги. Эти икроножные мышцы являются главными разгибателями стопы в голеностопном суставе. При ходьбе они выполняют работу по подъему пятки с земли.
Симптомы спастичности могут включать в себя повышение мышечного тонуса, быстрые сокращения мышц, глубокие сухожильные гиперрефлексы и/или мышечные спазмы. Степень спастичности может варьироваться от легкой мышечной жесткости до тяжелых, болезненных и неконтролируемых мышечных спазмов.
Известно, что для лечения спастичности у взрослых применяют ботулинический нейротоксин. Заявителем было обнаружено, что ботулинический нейротоксин может быть применен для лечения спастичности нижних конечностей у субъектов в возрасте 18 лет или младше, например, в возрасте от 2 до 17 лет.
Ботулинический нейротоксин продуцируется Clostridium botulinum в форме большого белкового комплекса, состоящего из самого ботулинического нейротоксина, образующего комплекс с рядом вспомогательных белков. В настоящее время существует семь различных классов ботулинического нейротоксина, а именно: ботулинический нейротоксин серотипов A, B, C, D, E, F и G, все из которых имеют сходные структуры и механизмы действия. Различные серотипы BoNT можно различить на основе инактивации специфическими нейтрализующими антисыворотками, причем такая классификация по серотипу коррелирует с процентом идентичности последовательности на уровне аминокислот. Белки ботулинического нейротоксина заданного серотипа далее делятся на различные подтипы на основе процента идентичности аминокислотной последовательности.
Ботулинический токсин типа A в основном коммерчески доступен от Ipsen (Dysport®, Ipsen Limited, Слау, Великобритания) и Allergan (BOTOX®, Allergan Inc., Ирвин, Калифорния, США), тогда как ботулинический токсин типа B продается Elan (Myobloc®/Neurobloc®, Solstice Neurosciences Inc., Сан–Диего, Калифорния, США).
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится, в частности, к способу лечения спастичности нижних конечностей у субъекта, в частности, человека в возрасте 18 лет или младше, например от 2 до 17 лет, включающему в себя введение субъекту эффективного количества ботулинического нейротоксина. Также изобретение относится к ботулиническому нейротоксину для применения в способе лечения спастичности нижних конечностей, при этом способ включает в себя введение субъекту в возрасте 18 лет или младше эффективного количества ботулинического нейротоксина, и к применению ботулинического нейротоксина в производстве медикамента для лечения спастичности нижних конечностей у субъекта в возрасте 18 лет или младше.
В одном из вариантов осуществления ботулинический нейротоксин относится к типу A, B, C, D, E, F и/или G.
В конкретном варианте осуществления ботулинический нейротоксин относится к типу А.
В одном из вариантов осуществления ботулинический нейротоксин вводят латерально. В конкретном варианте осуществления ботулинический нейротоксин вводят в одну ногу в количестве от 10 до 15 единиц на килограмм общей массы тела субъекта.
В одном из вариантов осуществления ботулинический нейротоксин вводят билатерально. В конкретном варианте осуществления в каждую ногу субъекта вводят индивидуально от 10 до 15 единиц на килограмм общей массы тела субъекта.
В одном из вариантов осуществления общее количество ботулинического нейротоксина, вводимого субъекту за сеанс лечения, составляет 1000 единиц или менее.
В одном из вариантов осуществления ботулинический нейротоксин вводят более чем в одно место в любой отдельной мышце.
В одном из вариантов осуществления не более 0,5 мл Dysport® вводят в любом отдельном месте.
В одном из вариантов осуществления последующий сеанс лечения не проводят в течение 12 недель после другого сеанса лечения. В конкретном варианте осуществления последующий сеанс лечения проводят через 16–22 недели после другого сеанса лечения.
В одном из вариантов осуществления ботулинический нейротоксин вводят субъекту в количестве, по меньшей мере, около 5 единиц на килограмм общей массы тела субъекта. Предпочтительно, ботулинический нейротоксин вводят субъекту в количестве, по меньшей мере, около 10 единиц на килограмм общей массы тела субъекта. Количество ботулинического нейротоксина, вводимого субъекту, может составлять менее чем около 15 единиц на килограмм общей массы тела субъекта (например, менее чем около 12 единиц на килограмм общей массы тела субъекта). Предпочтительно значения, раскрытые в этом параграфе, относятся к количеству единиц, вводимых в одну ногу субъекта.
В одном из вариантов осуществления ботулинический нейротоксин вводят в комплекс икроножной и камбаловидной мышц.
В одном из вариантов осуществления ботулинический нейротоксин вводят латерально в количестве от 10 до 15 единиц на килограмм общей массы тела субъекта, предпочтительно, при этом указанный ботулинический нейротоксин вводят в комплекс икроножной и камбаловидной мышц субъекта. В другом конкретном варианте осуществления ботулинический нейротоксин вводят билатерально в количестве от 20 до 30 единиц на килограмм общей массы тела субъекта, предпочтительно, при этом указанный ботулинический нейротоксин вводят в комплекс икроножной и камбаловидной мышц субъекта.
В одном из вариантов осуществления ботулинический нейротоксин вводят в икроножную мышцу субъекта. В конкретном варианте осуществления ботулинический нейротоксин вводят в индивидуальную икроножную мышцу субъекта в количестве от 6 до 9 единиц на килограмм общей массы тела субъекта. В определенных вариантах осуществления такое количество вводят в каждую икроножную мышцу субъекта.
В одном из вариантов осуществления ботулинический нейротоксин вводят в камбаловидную мышцу субъекта. В конкретном варианте осуществления ботулинический нейротоксин вводят в индивидуальную камбаловидную мышцу в количестве от 4 до 6 единиц на килограмм общей массы тела субъекта. В определенных вариантах осуществления такое количество вводят в каждую камбаловидную мышцу субъекта.
В одном из вариантов осуществления ботулинический нейротоксин вводят посредством инъекции в мышцу. В конкретном варианте осуществления делают до 4 инъекций в икроножную мышцу. В другом конкретном варианте осуществления делают до 2 инъекций в камбаловидную мышцу. В одном из вариантов осуществления места инъекции определяют путем пальпации или с использованием методик направления инъекции, таких как электромиография или электростимуляция.
В одном из вариантов осуществления ботулинический нейротоксин вводят в дозировке, частично определяемой на основании веса субъекта, является ли введение латеральным или билатеральным, будут ли введение выполнять в икроножную и/или камбаловидную мышцу, тяжести спастичности, того, какие мышцы затронуты спастичностью, наличия локальной мышечной слабости и/или анамнеза лечения субъекта ботулиническим нейротоксином.
В конкретном варианте осуществления способ включает в себя этапы: (A) получения веса субъекта; (B) выбора латерального или билатерального введения; (C) в зависимости от веса пациента и того, должно ли введение быть латеральным или билатеральным, определения количества ботулинического нейротоксина для введения субъекту; и (D) введения ботулинического нейротоксина в таком количестве субъекту, нуждающемуся в таком лечении.
Настоящее изобретение также относится, в частности, к средству для применения в определении количества действующего вещества, например ботулинического нейротоксина, для введения субъекту.
В одном из вариантов осуществления средство содержит:
(A) первый элемент, который имеет на нем первую строку чисел, указывающих вес субъекта, и вторую строку чисел, указывающих объем дозы действующего вещества, который следует вводить субъекту, при этом числа в первой строке, указывающие конкретный вес, находятся в продольном или радиальном выравнивании с соответствующими числами во второй строке, указывающими конкретный объем дозы, который следует вводить субъекту, имеющему данный конкретный вес; и
(B) второй элемент;
при этом первый и второй элементы находятся во взаимосвязи друг с другом, так что пользователь может перемещать один элемент для указания объема дозы действующего вещества, который следует вводить субъекту, имеющему конкретный вес.
В одном из вариантов осуществления и первый, и второй элементы представляют собой плоские поверхности, которые находятся в расположении друг относительно друга, допускающем продольное скольжение, при этом второй элемент перекрывает первый элемент и имеет отверстие или отверстия, которые позволяют просматривать строки на первом элементе.
В другом варианте осуществления первый элемент представляет собой плоскую поверхность, а второй элемент представляет собой бегунок в расположении, допускающем продольное скольжение, относительно первого элемента.
В другом варианте осуществления первый элемент представляет собой круглую плоскую поверхность, а второй элемент представляет собой циферблат, который поворачивается вокруг центральной точки первого элемента.
В одном из вариантов осуществления вышеуказанного способа лечения спастичности нижних конечностей у субъекта объем дозы определяют с применением средства, как описано выше.
Изобретение, кроме того, частично относится к композиции для применения в лечении спастичности нижних конечностей у субъекта, в частности, в возрасте 18 лет или младше, например, в возрасте от 2 до 17 лет. Композиция содержит эффективное количество ботулинического нейротоксина.
В одном из вариантов осуществления композиция содержит от 10 до 15 единиц ботулинического нейротоксина на килограмм общей массы тела субъекта на каждую ногу, в которую следует вводить ботулинический нейротоксин.
В одном из вариантов осуществления композиция содержит количество ботулинического нейротоксина, которое следует вводить в индивидуальную икроножную мышцу субъекта, при этом количество составляет от 6 до 9 единиц на килограмм общей массы тела субъекта.
В одном из вариантов осуществления композиция содержит количество ботулинического нейротоксина, которое следует вводить в индивидуальную камбаловидную мышцу субъекта, при этом количество составляет от 4 до 6 единиц на килограмм общей массы тела субъекта.
В одном из вариантов осуществления композиция имеет форму лиофилизированного порошка.
В одном из вариантов осуществления композицию получают путем восстановления лиофилизированного порошка, содержащего ботулинический нейротоксин, в растворе хлорида натрия. В конкретных вариантах осуществления композиция содержит от 300 до 500 единиц ботулинического нейротоксина.
В одном из вариантов осуществления композиция содержит ботулинический нейротоксин и сывороточный альбумин человека.
ОПИСАНИЕ ЧЕРТЕЖЕЙ
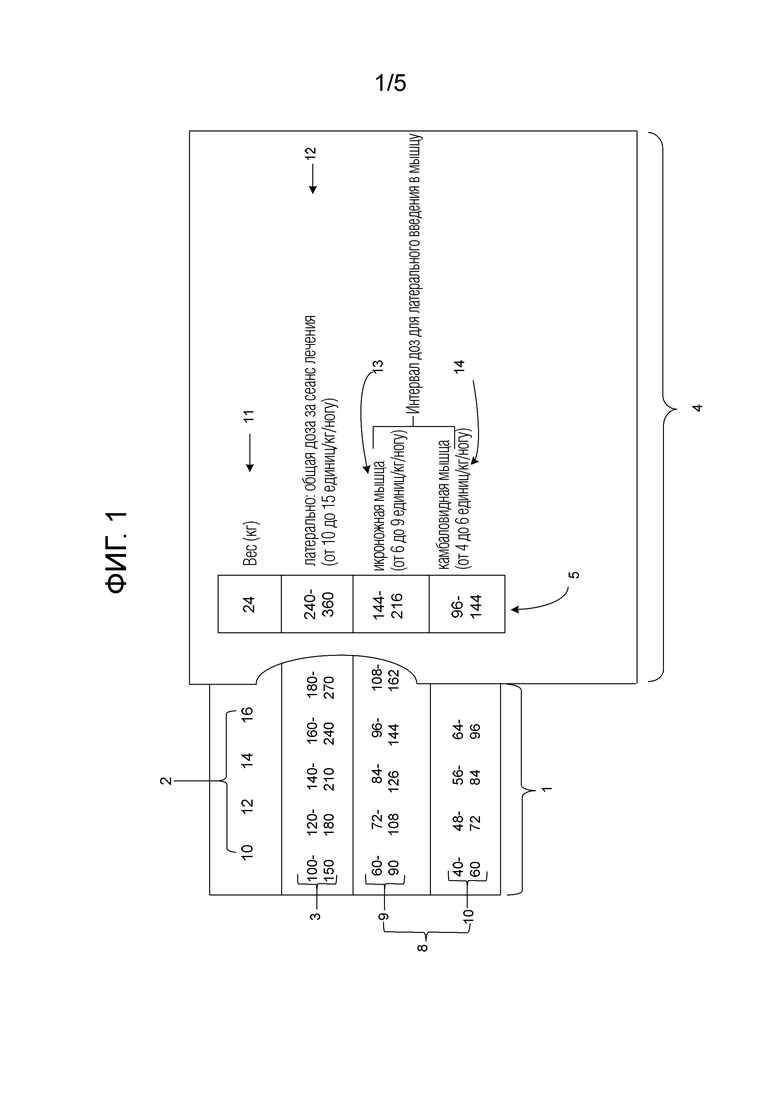
На фиг. 1 изображен вариант осуществления средства по настоящему изобретению. Средство содержит: (A) первый элемент (1), имеющий на нем первую строку чисел (2), указывающих вес субъекта, вторую строку чисел (3), указывающих объем дозы действующего вещества, который следует вводить субъекту, имеющему конкретный вес, и дополнительные строки чисел (8), при этом одна строка указывает объем дозы, который следует вводить в икроножную мышцу ноги субъекта (9), и другая строка указывает объем дозы, который следует вводить в камбаловидную мышцу ноги субъекта (10); и (B) второй элемент (4). Как первый, так и второй элементы представляют собой плоские поверхности и находятся во взаимосвязи друг с другом, так что пользователь может перемещать один элемент для указания объема дозы действующего вещества, который следует вводить субъекту, имеющему конкретный вес. Второй элемент перекрывает первый и имеет отверстие (5), которое позволяет просматривать строки первого элемента. Первая маркировка (11) на втором элементе совмещена со строкой чисел, которые указывают вес субъекта (2), вторая маркировка (12) на втором элементе совмещена со строкой чисел, которые указывают объем дозы действующего вещества, который следует вводить субъекту (3), а третья (13) и четвертая маркировки (14) на втором элементе выровнены, соответственно, со строкой, указывающей объем дозы действующего вещества, который следует вводить в икроножную мышцу ноги субъекта (9), и строкой, указывающей объем дозы действующего вещества, который следует вводить в камбаловидную мышцу ноги субъекта (10).
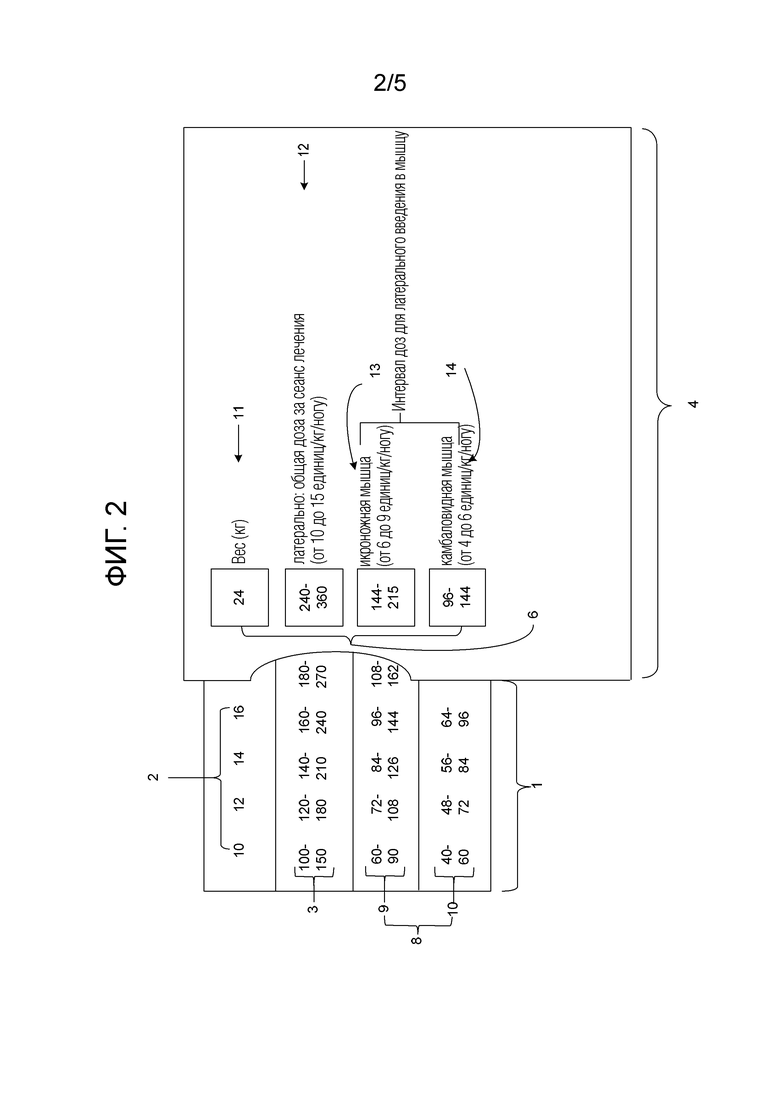
На фиг. 2 изображен другой вариант осуществления средства по настоящему изобретению. Средство содержит: (A) первый элемент (1), имеющий на нем первую строку чисел (2), указывающих вес субъекта, вторую строку чисел (3), указывающих объем дозы действующего вещества, который следует вводить субъекту, имеющему конкретный вес, и дополнительные строки чисел (8), при этом одна строка указывает объем дозы, который следует вводить в икроножную мышцу ноги субъекта (9), и другая строка указывает объем дозы, который следует вводить в камбаловидную мышцу ноги субъекта (10); и (B) второй элемент (4). Как первый, так и второй элементы представляют собой плоские поверхности и находятся во взаимосвязи друг с другом, так что пользователь может перемещать один элемент для указания объема дозы действующего вещества, который следует вводить субъекту, имеющему конкретный вес. Второй элемент перекрывает первый и содержит отверстия (6), каждое из которых позволяет просматривать одну строку на первом элементе. Первая маркировка (11) на втором элементе совмещена со строкой чисел, которые указывают вес субъекта (2), вторая маркировка (12) на втором элементе совмещена со строкой чисел, которые указывают объем дозы действующего вещества, который следует вводить субъекту (3), а третья (13) и четвертая маркировки (14) на втором элементе выровнены, соответственно, со строкой, указывающей объем дозы действующего вещества, который следует вводить в икроножную мышцу ноги субъекта (9), и строкой, указывающей объем дозы действующего вещества, который следует вводить в камбаловидную мышцу ноги субъекта (10).
На фиг. 3 изображен еще один вариант осуществления средства по настоящему изобретению. Средство содержит: (A) первый элемент (1), имеющий на нем первую строку чисел (2), указывающих вес субъекта, и вторую строку чисел (3), указывающих объем дозы действующего вещества, который следует вводить субъекту, имеющему конкретный вес; и (B) второй элемент (4). Первый элемент представляет собой плоскую поверхность, а второй элемент представляет собой бегунок. Второй элемент находится в расположении, допускающем продольное скольжение относительно первого элемента, так что пользователь может обеспечить указание объема дозы действующего вещества, который следует вводить субъекту, имеющему конкретный вес. Бегунок выполнен из прозрачного материала. Первая маркировка (11) на втором элементе совмещена со строкой чисел, которые указывают вес субъекта (2), а вторая маркировка (12) на втором элементе совмещена со строкой чисел, которые указывают объем дозы действующего вещества, который следует вводить субъекту (3). Числа появляются на этикетке (15). Линия (7) присутствует на бегунке, чтобы обеспечить указание конкретного веса и объема дозы, который следует вводить субъекту, имеющему данный конкретный вес.
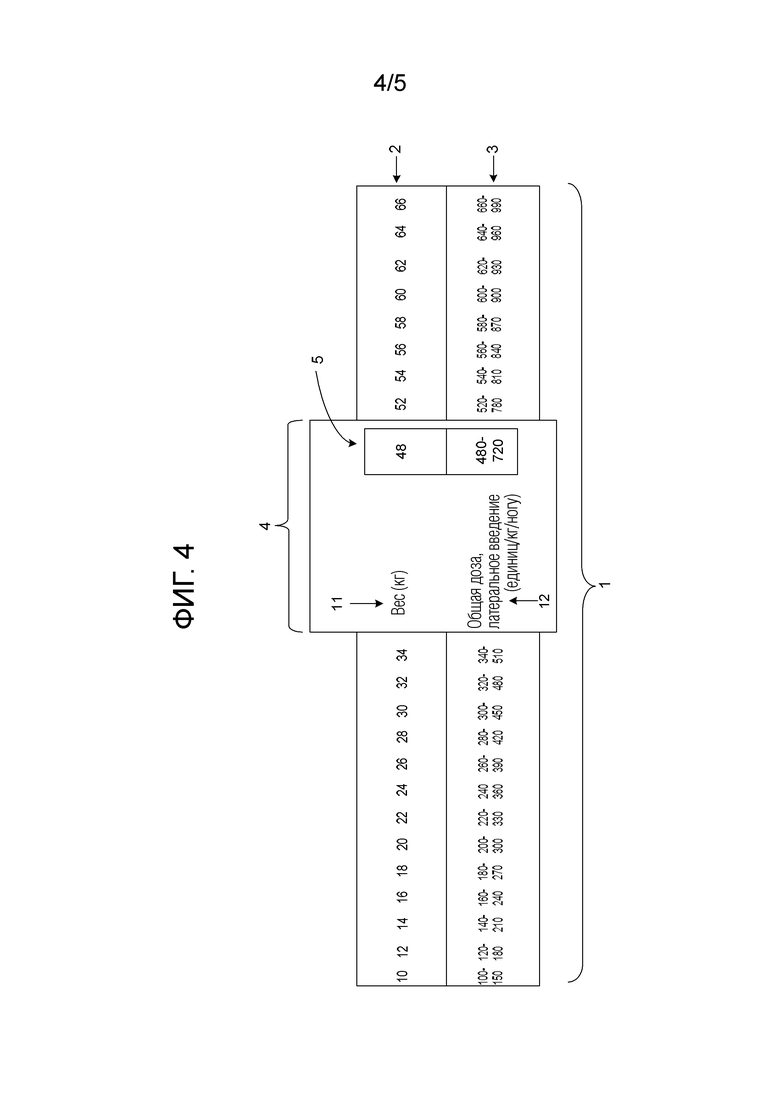
На фиг. 4 изображен еще один вариант осуществления средства по настоящему изобретению. Средство содержит: (A) первый элемент (1), имеющий на нем первую строку чисел (2), указывающих вес субъекта, и вторую строку чисел (3), указывающих объем дозы действующего вещества, который следует вводить субъекту, имеющему конкретный вес; и (B) второй элемент (4). Первый элемент представляет собой плоскую поверхность, а второй элемент представляет собой бегунок. Второй элемент находится в расположении, допускающем продольное скольжение относительно первого элемента, так что пользователь может обеспечить указание объема дозы действующего вещества, который следует вводить субъекту, имеющему конкретный вес. Первая маркировка (11) на втором элементе совмещена со строкой чисел, которые указывают вес субъекта (2), а вторая маркировка (12) на втором элементе совмещена со строкой чисел, которые указывают объем дозы действующего вещества, который следует вводить субъекту (3). Числа появляются на этикетке (15). Бегунок содержит отверстие (5), которое позволяет пользователю просматривать конкретное значение веса и объем дозы, который следует вводить субъекту, имеющему этот конкретный вес.
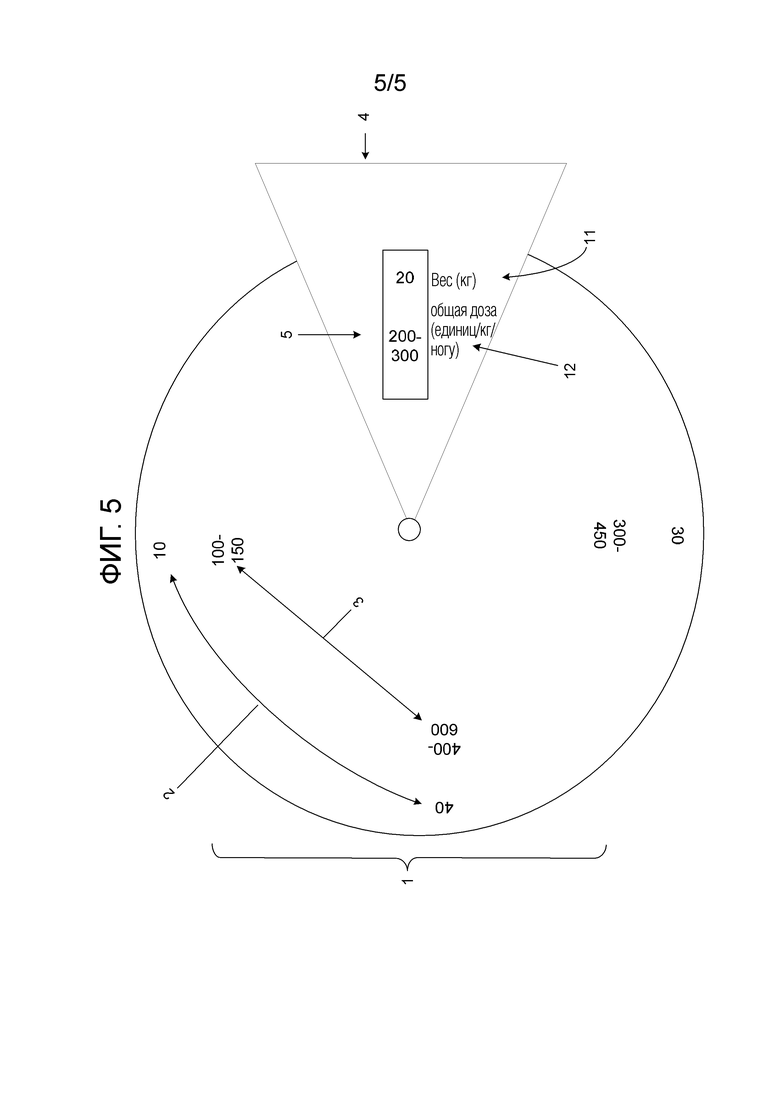
На фиг. 5 изображен еще один вариант осуществления средства по настоящему изобретению. Средство содержит: (A) первый элемент (1), имеющий на нем первую строку чисел (2), указывающих вес субъекта, и вторую строку чисел (3), указывающих объем дозы действующего вещества, который следует вводить субъекту, имеющему конкретный вес; и (B) второй элемент (4). Первый элемент представляет собой круглую плоскую поверхность, а второй элемент представляет собой циферблат, который поворачивается вокруг центральной точки первого элемента, так что пользователь может обеспечить указание объема дозы действующего вещества, который следует вводить субъекту, имеющему конкретный вес. Бегунок содержит отверстие (5), которое позволяет пользователю просматривать конкретное значение веса и объем дозы, который следует вводить субъекту, имеющему данный конкретный вес. Первая маркировка (11) на втором элементе совмещена со строкой чисел, которые указывают вес субъекта (2), а вторая маркировка (12) на втором элементе совмещена со строкой чисел, которые указывают объем дозы действующего вещества, который следует вводить субъекту (3).
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Следует понимать, что настоящее изобретение не ограничено вариантами осуществления, описанными в настоящем описании. Фактически, многочисленные вариации, изменения и замены будут теперь понятны специалистам в данной области техники без отступления от изобретения. Следует понимать, что различные альтернативы вариантам осуществления изобретения, описанным в настоящем описании, будут применяться при практическом применении изобретения.
При описании изобретения, если диапазон значений представлен в отношении варианта осуществления, то подразумевается, что каждое промежуточное значение охватывается в этом варианте осуществления.
Настоящее изобретение относится, в частности, к способу лечения спастичности нижних конечностей у субъекта, в частности, человека в возрасте 18 лет или младше, например, от 2 до 17 лет, включающему в себя введение субъекту эффективного количества ботулинического нейротоксина. Используемый в настоящем описании термин «субъект» относится к млекопитающему, в частности человеку, нуждающемуся в лечении спастичности нижних конечностей. Например, субъект может являться пациентом–человеком, нуждающимся в таком лечении.
Ботулинические нейротоксины представляют собой белки, продуцируемые Clostridium botulinum. Эти белки служат нейротоксинами. При селективном захвате посредством эндоцитоза на нервных окончаниях они блокируют высвобождение синаптических везикул. Существует семь известных серотипов ботулинического нейротоксина, в частности, серотипы A, B, C, D, E, F и G. При использовании в настоящем описании «ботулинический нейротоксин» относится к природным ботулиническим нейротоксинам, в том числе в их форме с высокой степенью чистоты, и рекомбинантно сконструированным ботулиническим нейротоксинам, включая содержащие модификации по сравнению с ботулиническими нейротоксинами дикого типа (например, в их аминокислотной последовательности), сделанные с тем, чтобы они обладали аналогичными или лучшими свойствами, чем ботулинические нейротоксины дикого типа. Ботулинический токсин типа А включает в себя все типы ботулинического токсина типа А, включая А1, А2 и А3. Ботулинический токсин типа С включает в себя все типы ботулинического токсина типа С, включая С1 или С2. То же самое относится, с соответствующими изменениями, к другим серотипам токсинов.
«Ботулинический нейротоксин высокой чистоты» (типа A, B, C, D, E, F или G) относится к ботулиническому нейротоксину, который не содержит комплексов с другими белками.
В одном из вариантов осуществления ботулинический нейротоксин относится к типам A, B, C, D, E, F и/или G или рекомбинантно сконструированному ботулиническому нейротоксину, имеющему аминокислотную последовательность, которая имеет, по меньшей мере, 50%, 60%, 70%, 80%, 90%, 95%, 97%, 98% или 99% идентичности последовательности (предпочтительно, по меньшей мере, 90% идентичности последовательности) с аминокислотной последовательностью ботулинического нейротоксина типов A, B, C, D, E, F или G.
Типичные аминокислотные последовательности для ботулинического нейротоксина типов A, B, C, D, E, F и G представлены под SEQ ID № 1–7, соответственно.
«Процент идентичности последовательности» между двумя или более последовательностями нуклеиновых кислот или аминокислот является функцией числа идентичных позиций, общих для последовательностей. Таким образом, % идентичности может быть рассчитан как количество идентичных нуклеотидов/аминокислот, деленное на общее количество нуклеотидов/аминокислот, умноженное на 100. При вычислении % идентичности последовательности также могут принимать во внимание количество разрывов и длину каждого разрыва, который необходимо внести для оптимизации выравнивания двух или более последовательностей. Сравнения последовательностей и определение процента идентичности между двумя или более последовательностями могут быть выполнены с использованием конкретных математических алгоритмов, таких как BLAST, которые будут знакомы специалисту в данной области техники.
В одном из вариантов осуществления ботулинический нейротоксин относится к типу А, также известному как ботулинический нейротоксин А. Ботулинический нейротоксин А продается под торговым наименованием Dysport® от Ipsen Biopharmaceuticals, Inc. (Баскинг Ридж, Нью–Джерси) и как Botox® от Allergan, Inc. (Парсиппани–Трой Хиллз, Нью–Джерси).
Ботулинический нейротоксин могут вводить латерально. Термин «латерально» и его варианты при использовании в настоящем описании в отношении введения относится к введению ботулинического нейротоксина в одну ногу субъекта.
Таким образом, в одном из вариантов осуществления ботулинический нейротоксин вводят субъекту латерально в количестве, по меньшей мере, около 5 единиц на килограмм общей массы тела субъекта. Предпочтительно, ботулинический нейротоксин вводят субъекту латерально в количестве, по меньшей мере, около 10 единиц на килограмм общей массы тела субъекта. Количество ботулинического нейротоксина, вводимого субъекту латерально, может составлять менее чем около 15 единиц на килограмм общей массы тела субъекта (например, менее около 12 единиц на килограмм общей массы тела субъекта).
В одном из вариантов осуществления ботулинический нейротоксин вводят латерально в количестве от 10 до 15 единиц на килограмм общей массы тела субъекта. Используемый в настоящем описании термин «единица» относится к стандартной дозе Dysport®, которая относится к медианной внутрибрюшинной дозе с LD50 Dysport® для мышей. Отмечено, что медианная внутрибрюшинная доза LD50 Dysport® у мышей необязательно совпадает с медианной внутрибрюшинной дозой LD50 другого содержащего ботулинический нейротоксин продукта, такого как Botox®, поскольку различные фармацевтические препараты производят по–разному. Например, единицы Botox®, как описано в данной области техники, не совпадают с единицами настоящего изобретения, которые являются единицами Dysport®.
Dysport® является инъецируемой формой ботулинического токсина типа А (BoNT–A), которая выделена и очищена из бактерий Clostridium, продуцирующих BoNT–A. Он поставляется в форме лиофилизированного порошка. Dysport® имеет одобренные терапевтические показания к применению в Соединенных Штатах для лечения взрослых с цервикальной дистонией (CD), лечения спастичности верхних конечностей (ULS) у взрослых пациентов и лечения спастичности нижних конечностей у детей для улучшения тонуса и спастичности. Впервые лекарство было зарегистрировано в Великобритании в 1990 году для других целей и лицензировано в более чем 80 странах по восьми различным показаниям, при этом было опубликовано более 1300 рецензируемых публикаций.
Ботулинический нейротоксин также могут вводить билатерально. Термин «билатерально» и его варианты при использовании в настоящем описании в отношении введения относится к введению ботулинического нейротоксина в обе ноги субъекта.
Таким образом, в одном из вариантов осуществления ботулинический нейротоксин вводят субъекту билатерально в количестве, по меньшей мере, около 5 единиц на килограмм общей массы тела субъекта на одну ногу. Предпочтительно, ботулинический нейротоксин вводят субъекту билатерально в количестве, по меньшей мере, около 10 единиц на килограмм общей массы тела субъекта на одну ногу. Количество ботулинического нейротоксина, вводимого субъекту билатерально, может составлять менее около 15 единиц на килограмм общей массы тела субъекта на одну ногу (например, менее около 12 единиц на килограмм общей массы тела субъекта на одну ногу).
В одном из вариантов осуществления ботулинический нейротоксин вводят билатерально в каждую ногу субъекта в количестве от 10 до 15 единиц, от 11 до 14 единиц или от 12 до 13 единиц на килограмм общей массы тела субъекта на одну ногу.
В одном из вариантов осуществления общее количество ботулинического нейротоксина, вводимого субъекту за сеанс лечения, составляет 1000 единиц или менее, 900 единиц или менее, 800 единиц или менее, 700 единиц или менее, 600 единиц или менее или 500 единиц или менее.
В одном из вариантов осуществления последующее лечение ботулиническим нейротоксином после предшествующего такого лечения не проводят в течение 12 недель после предыдущего лечения. Например, последующее лечение могут проводить через 16–22 недели после предшествующего лечения.
Настоящее изобретение предусматривает введение ботулинического нейротоксина, который могут вводить любым способом, например парентерально, внутримышечно, подкожно, внутрикожно или трансдермально. В одном из вариантов осуществления введение может представлять собой инъекцию в мышцу.
Введение может происходить, например, в мышцы комплекса икроножной и камбаловидной мышц. Например, ботулинический нейротоксин могут вводить в икроножную мышцу субъекта. В одном из вариантов осуществления ботулинический нейротоксин вводят в индивидуальную икроножную мышцу в количестве от 6 до 9 единиц или от 7 до 8 единиц на килограмм общей массы тела субъекта. В определенных вариантах осуществления в каждую икроножную мышцу субъекта вводят такое количество. Ботулинический нейротоксин могут также, или альтернативно, вводить в камбаловидную мышцу субъекта. В одном из вариантов осуществления ботулинический нейротоксин вводят в индивидуальную камбаловидную мышцу в количестве от 4 до 6 единиц или около 5 единиц на килограмм общей массы тела субъекта. В определенных вариантах осуществления в каждую камбаловидную мышцу субъекта вводят такое количество.
Введение могут также выполнять более чем в одном месте в любой отдельной мышце. В одном из вариантов осуществления не более 0,5 мл, 0,25 мл или 0,1 мл Dysport® вводят в любом отдельном месте.
Количество вводимого ботулинического нейротоксина могут, например, определять на основании, в частности, таких факторов, как: вес субъекта, является ли введение латеральным или билатеральным, будут ли введение выполнять в икроножную и/или камбаловидную мышцу, тяжести спастичности, того, какие мышцы затронуты спастичностью, наличия локальной мышечной слабости и/или анамнеза лечения субъекта ботулиническим нейротоксином.
Например, когда введение является латеральным, могут вводить общую дозу от 10 до 15 единиц/кг общей массы тела субъекта. Таким образом, могут вводить от 100 до 150 единиц пациенту, имеющему общую массу тела 10 кг, могут вводить от 200 до 300 единиц пациенту, имеющему общую массу тела 20 кг, могут вводить от 300 до 450 единиц пациенту, имеющему общую массу тела 30 кг, могут вводить от 400 до 600 единиц пациенту, имеющему общую массу тела 40 кг, могут вводить от 500 до 750 единиц пациенту, имеющему общую массу тела 50 кг, могут вводить от 600 до 900 единиц пациенту, имеющему общую массу тела 60 кг, и могут вводить от 700 до 1050 единиц пациенту, имеющему общую массу тела 70 кг.
Когда введение является билатеральным, например, могут вводить общую дозу от 20 до 30 единиц/кг общей массы тела субъекта. Таким образом, могут вводить от 200 до 300 единиц пациенту, имеющему общую массу тела 10 кг, могут вводить от 400 до 600 единиц пациенту, имеющему общую массу тела 20 кг, могут вводить от 600 до 900 единиц пациенту, имеющему общую массу тела 30 кг, могут вводить от 800 до 1200 единиц пациенту, имеющему общую массу тела 40 кг, могут вводить от 1000 до 1500 единиц пациенту, имеющему общую массу тела 50 кг, могут вводить от 1200 до 1800 единиц пациенту, имеющему общую массу тела 60 кг, и могут вводить от 1400 до 2100 единиц пациенту, имеющему общую массу тела 70 кг.
Когда спастичность затрагивает икроножную мышцу субъекта, введение ботулинического нейротоксина могут, например, выполнять в икроножную мышцу.
В вариантах осуществления, в которых введение является латеральным, введение в камбаловидную мышцу может, например, составлять от 6 до 9 единиц/кг общей массы тела субъекта. Например, могут вводить от 60 до 90 единиц пациенту, имеющему общую массу тела 10 кг, могут вводить от 120 до 180 единиц пациенту, имеющему общую массу тела 20 кг, могут вводить от 180 до 270 единиц пациенту, имеющему общую массу тела 30 кг, могут вводить от 240 до 360 единиц пациенту, имеющему общую массу тела 40 кг, могут вводить от 300 до 450 единиц пациенту, имеющему общую массу тела 50 кг, могут вводить от 360 до 540 единиц пациенту, имеющему общую массу тела 60 кг, и могут вводить от 420 до 630 единиц пациенту, имеющему общую массу тела 70 кг. В вариантах осуществления, в которых введение является билатеральным, вышеуказанные количества могут индивидуально вводить в икроножную мышцу каждой ноги в вышеуказанных количествах.
Когда спастичность затрагивает камбаловидную мышцу субъекта, введение ботулинического нейротоксина могут, например, выполнять в камбаловидную мышцу. В вариантах осуществления, в которых введение является латеральным, введение в камбаловидную мышцу может, например, составлять от 4 до 6 единиц/кг общей массы тела субъекта. Например, могут вводить от 40 до 60 единиц пациенту, имеющему общую массу тела 10 кг, могут вводить от 80 до 120 единиц пациенту, имеющему общую массу тела 20 кг, могут вводить от 120 до 180 единиц пациенту, имеющему общую массу тела 30 кг, могут вводить от 160 до 240 единиц пациенту, имеющему общую массу тела 40 кг, могут вводить от 200 до 300 единиц пациенту, имеющему общую массу тела 50 кг, могут вводить от 240 до 360 единиц пациенту, имеющему общую массу тела 60 кг, и могут вводить от 280 до 420 единиц пациенту, имеющему общую массу тела 70 кг. В вариантах осуществления, в которых введение является билатеральным, вышеуказанные количества могут индивидуально вводить в камбаловидную мышцу каждой ноги в вышеуказанных количествах.
Субъектом может являться субъект, имеющий спастичность в связи с эквинусом, церебральным параличом, повреждением спинного мозга, рассеянным склерозом, ударом, травмой головного мозга, травмой головы или комбинацией указанного. В одном из вариантов осуществления субъект имеет эквинус. Предпочтительно, субъект имеет спастичность и эквинус. Эквинус может являться динамическим эквинусом (например, динамическая эквинусная деформация стопы).
Уровень спастичности пациента могут, например, измерять с использованием модифицированной шкалы Эшворта (MAS), которая измеряет уровень увеличения сопротивления во время пассивного растяжения мягких тканей. Балл MAS, равный 0, указывает на отсутствие повышения мышечного тонуса. Балл, равный 1, указывает на легкое повышение мышечного тонуса, проявляющееся в напряжении и облегчении, или в минимальном сопротивлении в конце диапазона движения, когда пораженная(–ые) часть(–и) перемещается(–ются) при сгибании или разгибании. Балл, равный 1+, указывает на небольшое повышение мышечного тонуса, выражающееся в напряжении, сопровождаемом минимальным сопротивлением во всем остатке (менее половины) диапазона движения. Балл, равный 2, указывает на более заметное повышение мышечного тонуса в большей части диапазона движения, но пораженная(–ые) часть(–и) легко передвигается(–ются). Балл, равный 3, указывает на значительное повышение пассивного мышечного тонуса и затруднение движения. Балл, равный 4, указывает, что пораженная часть является жесткой при сгибании или разгибании.
В одном из вариантов осуществления количество единиц, вводимых субъекту, может быть прямо пропорционально уровню спастичности субъекта.
Например, когда субъект страдает тяжелой спастичностью в своей икроножной мышце, что показано баллом MAS, составляющим 3 или выше, введение может составлять, например, от 7,5 до 9 единиц/кг общей массы тела субъекта на одну ногу (то есть, от 7,5 до 9 единиц/кг для латерального введения и от 15 до 18 единиц/кг для билатерального введения). В других вариантах осуществления введение может составлять от 8 до 9 единиц/кг на одну ногу, от 8,5 до 9 единиц/кг на одну ногу или от 8,75 до 9 единиц/кг на одну ногу.
Например, когда субъект страдает тяжелой спастичностью в своей икроножной мышце, что показано баллом MAS, составляющим 3 или выше, введение может составлять, например, от 5 до 6 единиц/кг общей массы тела субъекта на одну ногу (то есть, от 5 до 6 единиц/кг для латерального введения и от 10 до 12 единиц/кг для билатерального введения). В других вариантах осуществления введение может составлять от 5,5 до 6 единиц/кг на одну ногу или от 5,75 до 6 единиц/кг на одну ногу.
Напротив, когда субъект страдает менее тяжелой или небольшой спастичностью в своей икроножной мышце, введение может, например, составлять от 6 до 7,5 единиц/кг общей массы тела субъекта на одну ногу (то есть, от 6 до 7,5 единиц/кг для латерального введения и от 12 до 15 единиц/кг для билатерального введения). В других вариантах осуществления введение может составлять от 6 до 7 единиц/кг на одну ногу, от 6 до 6,5 единиц/кг на одну ногу или от 6 до 6,25 единиц/кг на одну ногу.
Когда субъект страдает менее тяжелой или небольшой спастичностью в своей камбаловидной мышце, введение может составлять, например, от 4 до 5 единиц/кг общей массы тела субъекта на одну ногу (то есть от 4 до 5 единиц/кг для латерального введения и от 8 до 10 единиц/кг для билатерального введения). В других вариантах осуществления введение может составлять от 4 до 4,5 единиц/кг на одну ногу или от 4 до 4,25 единиц/кг на одну ногу.
Кроме того, могут вводить более низкую дозу, если у субъекта проявились побочные эффекты после предшествующего лечения ботулиническим нейротоксином или у него присутствуетлокальная мышечная слабость в мышцах, в которые следует вводить ботулинический нейротоксин. Примеры побочных эффектов включают инфекцию дыхательных путей, назофарингит, грипп, фарингит, кашель, гипертермию, бронхит, ринит, ветряную оспу, ушную инфекцию, гастроэнтерит, рвоту, тошноту, боль в ротоглотке, боль в конечностях, мышечную слабость, конвульсии и эпилепсию. Пример такой более низкой дозы составляет от 10 до 12,5 единиц/кг общей массы тела субъекта на одну ногу (то есть, от 10 до 12,5 единиц/кг для латерального введения и от 20 до 25 единиц/кг для билатерального введения). Другие примеры включают от 10 до 12, от 10 до 11,5, от 10 до 11 и от 10 до 10,5 единиц/кг общей массы тела субъекта на одну ногу. Для введения в икроножную мышцу доза может составлять, например, от 6 до 7,5 единиц/кг, от 6 до 7 единиц/кг или от 6 до 6,5 единиц/кг на одну ногу. Для введения в камбаловидную мышцу доза может составлять, например, от 4 до 5 единиц/кг или от 4 до 4,5 единиц/кг на одну ногу.
Альтернативно, могут вводить более высокую дозу, если субъект не демонстрирует желаемого ответа на предшествующее лечение ботулиническим нейротоксином. Ответ субъекта могут, например, измерять с использованием общей оценки врача (PGA) ответа на лечение. PGA измеряет ответ по шкале от –4 до +4, при этом –4 указывает, что ответ заметно хуже, до 0, что указывает на отсутствие изменений, до +4, что указывает, что ответ заметно улучшился. Например, желаемым ответом может быть оценка PGA после лечения, составляющая 0,25 или выше, 0,5 или выше, 1 или выше, 2 или выше, 3 или выше или 4.
Пример такой более высокой дозы составляет от 12,5 до 15 единиц/кг общей массы тела субъекта на одну ногу (то есть от 12,5 до 15 единиц/кг для латерального введения и от 25 до 30 единиц/кг для билатерального введения). Другие примеры включают от 13 до 15, от 13,5 до 15, от 14 до 15 и от 14,5 до 15 единиц/кг общей массы тела субъекта на одну ногу. Для введения в икроножную мышцу доза может составлять, например, от 7,5 до 9 единиц/кг на одну ногу. Для введения в камбаловидную мышцу доза может составлять, например, от 5 до 6 единиц/кг на одну ногу.
В случае локальной мышечной слабости в конкретной мышце, введение могут выполнять в другую мышцу. Например, если субъект страдает локальной мышечной слабостью в икроножной мышце, введение могут выполнять в другую икроножную мышцу субъекта, или в камбаловидную мышцу, или в какую–либо другую подходящую мышцу. Аналогично, если субъект страдает локальной мышечной слабостью в камбаловидной мышце, введение могут выполнять в другую камбаловидную мышцу субъекта, или в икроножную мышцу, или в какую–либо другую подходящую мышцу.
Будет ли введение латеральным или билатеральным, зависит от различных факторов, в том числе от мышц, на которые влияет спастичность пациента, тяжесть спастичности субъекта, наличие локальной мышечной слабости и/или анамнез субъекта в лечении ботулиническим нейротоксином. Например, введение может быть латеральным, если спастичность поражает только одну ногу, и билатеральным, если поражены обе ноги. Кроме того, субъект может иметь спастичность только в одной ноге, но спастичность может являться достаточно тяжелой для того, чтобы можно было применять билатеральное введение. Напротив, субъекта может иметь спастичность в обеих ногах, но локальная мышечная слабость в одной ноге может означать, что является целесообразным латеральное введение только в другую ногу. Кроме того, латеральное, а не билатеральное введение может быть целесообразным в тех случаях, когда у субъекта имелись побочные эффекты, возникающие в результате предшествующего лечения ботулиническим нейротоксином, и билатеральное, а не латеральное введение может быть целесообразным в тех случаях, когда субъект не демонстрировал желаемого ответа после предшествующего латерального лечения и/или лечения более низкой дозой ботулинического нейротоксина.
В одном из вариантов осуществления способ лечения субъекта от спастичности нижних конечностей включает в себя: (A) определение веса субъекта; (B) выбор латерального или билатерального введения; (C) в зависимости от веса пациента и того, должно ли введение быть латеральным или билатеральным, определение количества ботулинического нейротоксина для введения субъекту; и (D) введение ботулинического нейротоксина в таком количестве субъекту. При определении подходящего количества ботулинического нейротоксина способ также может включать в себя рассмотрение того, будут ли введение выполнять в икроножную и/или камбаловидную мышцу, степени спастичности субъекта, какие мышцы затронуты спастичностью, наличия локальной мышечной слабости, анамнеза лечения субъекта ботулиническим нейротоксином, возраста субъекта, роста субъекта, площади поверхности тела субъекта и/или пола субъекта. При определении подходящего объема дозы могут быть сделаны корректировки, как описано выше, с учетом вышеуказанных факторов.
Настоящее изобретение также относится, в частности, к средству для применения в определении количества действующего вещества, например, ботулинического нейротоксина, для введения субъекту.
В одном из вариантов осуществления средство содержит: (A) первый элемент (1), имеющий на нем первую строку чисел (2), указывающих вес субъекта, и вторую строку чисел (3), указывающих объем дозы действующего вещества для введения субъекту; и (B) второй элемент (4). Числа во второй строке указывают конкретный объем дозы, который следует вводить субъекту, имеющему конкретный вес, и находятся в продольном или радиальном выравнивании с соответствующими числами в первой строке, указывающими этот конкретный вес. Первый и второй элементы находятся во взаимосвязи друг с другом, так что пользователь может перемещать один элемент для указания объема дозы действующего вещества, вводимого субъекту, имеющему конкретный вес.
В некоторых вариантах осуществления как первый (1), так и второй (4) элементы представляют собой плоские поверхности, которые находятся в расположении друг относительно друга, допускающем продольное скольжение. Числа в первой строке (2) выровнены продольно с соответствующими числами во второй строке (3). Второй элемент перекрывает первый и содержит отверстие (5), которое позволяет просматривать строки первого элемента. В некоторых вариантах осуществления второй элемент содержит два или более отверстий (6), при этом каждое отверстие позволяет просматривать одну строку на первом элементе. Один элемент может находиться в расположении, допускающем продольное скольжение относительно другого, при этом числа можно просматривать через отверстие или отверстия, указывающие конкретный вес и объем дозы, который следует вводить субъекту, имеющему этот конкретный вес. В некоторых вариантах осуществления первая плоская поверхность складывается вокруг второй плоской поверхности и охватывает ее.
В других вариантах осуществления первый элемент (1) представляет собой плоскую поверхность, а второй элемент (4) представляет собой бегунок, находящийся в расположении, допускающем продольное скольжение относительно первого элемента. Числа в первой строке (2) продольно выровнены с соответствующими числами во второй строке (3). Бегунок может скользить вдоль первого элемента таким образом, что он указывает конкретный вес и объем дозы, который следует вводить субъекту, имеющему этот конкретный вес. Указание может быть выполнено посредством линии (7) на бегунке, которая перекрывает конкретный вес и объем дозы, который следует вводить субъекту, имеющему этот конкретный вес. В таком варианте осуществления бегунок может, например, быть прозрачным или полупрозрачным, чтобы позволить пользователю видеть числа под линией. В качестве альтернативы, бегунок может иметь отверстие (5) или отверстия (6), которые позволяют пользователю просматривать числа на первом элементе.
В дополнительных вариантах осуществления первый элемент (1) представляет собой круглую плоскую поверхность, а второй элемент (4) представляет собой циферблат, который поворачивается вокруг центральной точки первого элемента. Числа в первой строке (2) находятся в радиальном выравнивании с соответствующими числами во второй строке (3). Бегунок может поворачиваться так, что он указывает конкретный вес и объем дозы, который следует вводить субъекту, имеющему этот конкретный вес. Указание может быть выполнено посредством линии (7) на бегунке, которая перекрывает конкретный вес и объем дозы, который следует вводить субъекту, имеющему этот конкретный вес. В таком варианте осуществления бегунок может, например, быть прозрачным или полупрозрачным, чтобы позволить пользователю видеть числа под линией. В качестве альтернативы, бегунок может иметь отверстие (5) или отверстия (6), которые позволяют пользователю просматривать числа на первом элементе.
В некоторых вариантах осуществления средства первый элемент (1) содержит, вместо или в дополнение к вышеуказанной второй строке чисел (3), которые указывают объем дозы действующего вещества, который следует вводить субъекту, одну или более строк чисел (8), которые указывают объем дозы действующего вещества, который следует вводить в конкретные мышцы субъекта. Числа в строке или строках, которые указывают конкретный объем дозы, который следует вводить в мышцу субъекта, имеющего конкретный вес, находятся в продольном или радиальном выравнивании с соответствующими числами в первой строке, указывающими этот конкретный вес. В вариантах осуществления, в которых эти строки (8) являются дополнением к вышеуказанной второй строке чисел (3), которые указывают объем дозы действующего вещества, который следует вводить субъекту, вторая строка чисел представляет общий объем дозы, который следует вводить субъекту.
В одном из вариантов осуществления одна строка чисел указывает объем дозы действующего вещества, который следует вводить в икроножную мышцу ноги (9), а другая строка указывает объем дозы действующего вещества, который следует вводить в камбаловидную мышцу ноги (10).
В вариантах осуществления средства, которые содержат отверстие (5), или два или более отверстий (6), во втором элементе, отверстие может содержать окно, выполненное из прозрачного или полупрозрачного материала.
В вариантах осуществления, в которых второй элемент содержит два или более отверстий (6), каждое отверстие может соответствовать определенной строке на первом элементе. Например, одно отверстие может позволять просматривать числа первой строки (2), другое отверстие может позволять просматривать числа второго строки (3), а третье и четвертое отверстия могут позволять просматривать числа в дополнительных строках (8).
В вариантах осуществления, в которых второй элемент (4) содержит отверстие (5) или отверстия (6), через которые можно просматривать числа в строках на первом элементе (1), или когда второй элемент является прозрачным или полупрозрачным, второй элемент может содержать первую маркировку (11), выровненную со строкой чисел, которые указывают вес субъекта (2), вторую маркировку (12), выровненную со строкой чисел, которые указывают объем дозы действующего вещества, который следует вводить субъекту (3), и третью (13) и четвертую (14) маркировки, выровненные, соответственно, со строкой, указывающей объем дозы действующего вещества, который следует вводить в икроножную мышцу ноги субъекта (9), и строкой, указывающей объем дозы действующего вещества, который следует вводить в камбаловидную мышцу ноги субъекта (10). Маркировки могут идентифицировать каждую строку, соответственно, например, как: «общая масса субъекта»; «объем вещества на одну ногу, который следует вводить субъекту»; «объем вещества, который следует вводить на одну ногу, в икроножную мышцу субъекта», и «объем вещества, который следует вводить на одну ногу, в камбаловидную мышцу субъекта». В вариантах осуществления, в который второй элемент является прозрачным или полупрозрачным, маркировки могут находиться на этикетке (15), чтобы обеспечить лучшую видимость.
В варианте осуществления вышеуказанного способа лечения спастичности нижних конечностей у субъекта объем дозы определяют с применением средства, как описано выше.
Изобретение, кроме того, частично относится к композиции для применения в лечении спастичности нижних конечностей у субъекта, в частности, в возрасте 18 лет или младше, например, в возрасте от 2 до 17 лет. Композиция содержит эффективное количество ботулинического нейротоксина. В определенных вариантах осуществления композиция содержит разбавитель, например раствор хлорида натрия. Раствор может представлять собой, например, 0,9% раствор хлорида натрия.
В определенных вариантах осуществления композиция содержит от 1 до 1000 единиц, от 1 до 750 единиц, от 1 до 500 единиц, от 1 до 400 единиц, от 1 до 300 единиц или от 1 до 200 единиц ботулинического нейротоксина.
В одном из вариантов осуществления композиция содержит ботулинический нейротоксин в количестве 500 единиц и от 1 до 5 мл раствора хлорида натрия, например, 1, 2, 2,5 и 5 мл раствора. В конкретном варианте осуществления композиция содержит 500 единиц и 2,5 мл раствора.
В другом варианте осуществления композиция содержит ботулинический нейротоксин в количестве 300 единиц и от 1 до 3 мл раствора хлорида натрия, например 1, 1,5, 2,5 и 3 мл раствора.
В одном из вариантов осуществления композицию получают путем восстановления лиофилизированного ботулинического нейротоксина в растворе, например, вышеуказанном растворе хлорида натрия. После восстановления композицию можно хранить в холодильнике при температуре от 2 до 8°C и с защитой от света.
В варианте осуществления вышеуказанного способа лечения спастичности нижних конечностей у субъекта, в частности, в возрасте 18 лет или младше, например, в возрасте от 2 до 17 лет, субъекту вводят композицию, как описано выше. Объем вводимой композиции может являться объемом, определенным как подходящий, в соответствии с описанным выше. Например, для композиции, содержащей 500 единиц, разбавленных в 2,5 мл раствора, каждые 0,1 мл композиции будут содержать 20 единиц. Таким образом, объем композиции, который следует вводить субъекту при латеральном лечении, может составлять от 0,05 до 0,075 мл (содержащих от 10 до 15 единиц) на кг общей массы тела субъекта. Таким образом, субъекту с массой тела 50 кг могут вводить от 2,5 до 3,75 мл композиции. Количество композиции, которое следует вводить субъекту при двустороннем лечении, может составлять от 0,1 до 0,15 мл (содержащее от 20 до 30 единиц) на кг общей массы тела субъекта. Субъекту весом 50 кг могут вводить от 5 до 7,5 мл композиции.
В одном из вариантов осуществления композиция дополнительно содержит человеческий сывороточный альбумин. Например, от 1 до 100 мг/мл, от 1 до 50 мг/мл, от 1 до 25 мг/мл или 25 мг/мл.
В одном из вариантов осуществления композиция дополнительно содержит эксципиент. Эксципиент может представлять собой, например, наполнитель, связующее вещество, дезинтегрант, антиадгезив, растворитель, буферный агент, консервант или увлажнитель. Примеры наполнителей включают целлюлозу, лактозу, сахарозу, глюкозу, маннозу и сорбит. Композиция может содержать, например, 10 мг/мл лактозы. Примеры связующих веществ включают желатин, целлюлозу, поливинилпирролидон, крахмал и сахарозу. Примеры дезинтегрантов включают поливинилпирролидон и карбоксиметилцеллюлозу. Примеры консервантов включают парабены. Примеры растворителей включают воду, масла, глицерин, пропиленгликоль и этанол. Примеры буферных агентов включают фосфаты, карбонаты, цитраты и лактаты. Примеры увлажнителей включают глицерин, этиленгликоль и полиэтиленгликоль (ПЭГ).
Варианты осуществления, описанные в настоящем описании в отношении аспекта способа лечения, в равной степени относятся к аспектам ботулинического нейротоксина для применения, применения и композиции для применения (и наоборот).
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
SEQ ID № 1 (BoNT/A – UniProt P10845)
MPFVNKQFNYKDPVNGVDIAYIKIPNVGQMQPVKAFKIHNKIWVIPERDTFTNPEEGDLN
PPPEAKQVPVSYYDSTYLSTDNEKDNYLKGVTKLFERIYSTDLGRMLLTSIVRGIPFWGG
STIDTELKVIDTNCINVIQPDGSYRSEELNLVIIGPSADIIQFECKSFGHEVLNLTRNGY
GSTQYIRFSPDFTFGFEESLEVDTNPLLGAGKFATDPAVTLAHELIHAGHRLYGIAINPN
RVFKVNTNAYYEMSGLEVSFEELRTFGGHDAKFIDSLQENEFRLYYYNKFKDIASTLNKA
KSIVGTTASLQYMKNVFKEKYLLSEDTSGKFSVDKLKFDKLYKMLTEIYTEDNFVKFFKV
LNRKTYLNFDKAVFKINIVPKVNYTIYDGFNLRNTNLAANFNGQNTEINNMNFTKLKNFT
GLFEFYKLLCVRGIITSKTKSLDKGYNKALNDLCIKVNNWDLFFSPSEDNFTNDLNKGEE
ITSDTNIEAAEENISLDLIQQYYLTFNFDNEPENISIENLSSDIIGQLELMPNIERFPNG
KKYELDKYTMFHYLRAQEFEHGKSRIALTNSVNEALLNPSRVYTFFSSDYVKKVNKATEA
AMFLGWVEQLVYDFTDETSEVSTTDKIADITIIIPYIGPALNIGNMLYKDDFVGALIFSG
AVILLEFIPEIAIPVLGTFALVSYIANKVLTVQTIDNALSKRNEKWDEVYKYIVTNWLAK
VNTQIDLIRKKMKEALENQAEATKAIINYQYNQYTEEEKNNINFNIDDLSSKLNESINKA
MININKFLNQCSVSYLMNSMIPYGVKRLEDFDASLKDALLKYIYDNRGTLIGQVDRLKDK
VNNTLSTDIPFQLSKYVDNQRLLSTFTEYIKNIINTSILNLRYESNHLIDLSRYASKINI
GSKVNFDPIDKNQIQLFNLESSKIEVILKNAIVYNSMYENFSTSFWIRIPKYFNSISLNN
EYTIINCMENNSGWKVSLNYGEIIWTLQDTQEIKQRVVFKYSQMINISDYINRWIFVTIT
NNRLNNSKIYINGRLIDQKPISNLGNIHASNNIMFKLDGCRDTHRYIWIKYFNLFDKELN
EKEIKDLYDNQSNSGILKDFWGDYLQYDKPYYMLNLYDPNKYVDVNNVGIRGYMYLKGPR
GSVMTTNIYLNSSLYRGTKFIIKKYASGNKDNIVRNNDRVYINVVVKNKEYRLATNASQA
GVEKILSALEIPDVGNLSQVVVMKSKNDQGITNKCKMNLQDNNGNDIGFIGFHQFNNIAK
LVASNWYNRQIERSSRTLGCSWEFIPVDDGWGERPL
SEQ ID № 2 (BoNT/B – UniProt P10844)
MPVTINNFNYNDPIDNNNIIMMEPPFARGTGRYYKAFKITDRIWIIPERYTFGYKPEDFN
KSSGIFNRDVCEYYDPDYLNTNDKKNIFLQTMIKLFNRIKSKPLGEKLLEMIINGIPYLG
DRRVPLEEFNTNIASVTVNKLISNPGEVERKKGIFANLIIFGPGPVLNENETIDIGIQNH
FASREGFGGIMQMKFCPEYVSVFNNVQENKGASIFNRRGYFSDPALILMHELIHVLHGLY
GIKVDDLPIVPNEKKFFMQSTDAIQAEELYTFGGQDPSIITPSTDKSIYDKVLQNFRGIV
DRLNKVLVCISDPNININIYKNKFKDKYKFVEDSEGKYSIDVESFDKLYKSLMFGFTETN
IAENYKIKTRASYFSDSLPPVKIKNLLDNEIYTIEEGFNISDKDMEKEYRGQNKAINKQA
YEEISKEHLAVYKIQMCKSVKAPGICIDVDNEDLFFIADKNSFSDDLSKNERIEYNTQSN
YIENDFPINELILDTDLISKIELPSENTESLTDFNVDVPVYEKQPAIKKIFTDENTIFQY
LYSQTFPLDIRDISLTSSFDDALLFSNKVYSFFSMDYIKTANKVVEAGLFAGWVKQIVND
FVIEANKSNTMDKIADISLIVPYIGLALNVGNETAKGNFENAFEIAGASILLEFIPELLI
PVVGAFLLESYIDNKNKIIKTIDNALTKRNEKWSDMYGLIVAQWLSTVNTQFYTIKEGMY
KALNYQAQALEEIIKYRYNIYSEKEKSNINIDFNDINSKLNEGINQAIDNINNFINGCSV
SYLMKKMIPLAVEKLLDFDNTLKKNLLNYIDENKLYLIGSAEYEKSKVNKYLKTIMPFDL
SIYTNDTILIEMFNKYNSEILNNIILNLRYKDNNLIDLSGYGAKVEVYDGVELNDKNQFK
LTSSANSKIRVTQNQNIIFNSVFLDFSVSFWIRIPKYKNDGIQNYIHNEYTIINCMKNNS
GWKISIRGNRIIWTLIDINGKTKSVFFEYNIREDISEYINRWFFVTITNNLNNAKIYING
KLESNTDIKDIREVIANGEIIFKLDGDIDRTQFIWMKYFSIFNTELSQSNIEERYKIQSY
SEYLKDFWGNPLMYNKEYYMFNAGNKNSYIKLKKDSPVGEILTRSKYNQNSKYINYRDLY
IGEKFIIRRKSNSQSINDDIVRKEDYIYLDFFNLNQEWRVYTYKYFKKEEEKLFLAPISD
SDEFYNTIQIKEYDEQPTYSCQLLFKKDEESTDEIGLIGIHRFYESGIVFEEYKDYFCIS
KWYLKEVKRKPYNLKLGCNWQFIPKDEGWTE
SEQ ID № 3 (BoNT/C – UniProt P18640)
MPITINNFNYSDPVDNKNILYLDTHLNTLANEPEKAFRITGNIWVIPDRFSRNSNPNLNK
PPRVTSPKSGYYDPNYLSTDSDKDPFLKEIIKLFKRINSREIGEELIYRLSTDIPFPGNN
NTPINTFDFDVDFNSVDVKTRQGNNWVKTGSINPSVIITGPRENIIDPETSTFKLTNNTF
AAQEGFGALSIISISPRFMLTYSNATNDVGEGRFSKSEFCMDPILILMHELNHAMHNLYG
IAIPNDQTISSVTSNIFYSQYNVKLEYAEIYAFGGPTIDLIPKSARKYFEEKALDYYRSI
AKRLNSITTANPSSFNKYIGEYKQKLIRKYRFVVESSGEVTVNRNKFVELYNELTQIFTE
FNYAKIYNVQNRKIYLSNVYTPVTANILDDNVYDIQNGFNIPKSNLNVLFMGQNLSRNPA
LRKVNPENMLYLFTKFCHKAIDGRSLYNKTLDCRELLVKNTDLPFIGDISDVKTDIFLRK
DINEETEVIYYPDNVSVDQVILSKNTSEHGQLDLLYPSIDSESEILPGENQVFYDNRTQN
VDYLNSYYYLESQKLSDNVEDFTFTRSIEEALDNSAKVYTYFPTLANKVNAGVQGGLFLM
WANDVVEDFTTNILRKDTLDKISDVSAIIPYIGPALNISNSVRRGNFTEAFAVTGVTILL
EAFPEFTIPALGAFVIYSKVQERNEIIKTIDNCLEQRIKRWKDSYEWMMGTWLSRIITQF
NNISYQMYDSLNYQAGAIKAKIDLEYKKYSGSDKENIKSQVENLKNSLDVKISEAMNNIN
KFIRECSVTYLFKNMLPKVIDELNEFDRNTKAKLINLIDSHNIILVGEVDKLKAKVNNSF
QNTIPFNIFSYTNNSLLKDIINEYFNNINDSKILSLQNRKNTLVDTSGYNAEVSEEGDVQ
LNPIFPFDFKLGSSGEDRGKVIVTQNENIVYNSMYESFSISFWIRINKWVSNLPGYTIID
SVKNNSGWSIGIISNFLVFTLKQNEDSEQSINFSYDISNNAPGYNKWFFVTVTNNMMGNM
KIYINGKLIDTIKVKELTGINFSKTITFEINKIPDTGLITSDSDNINMWIRDFYIFAKEL
DGKDINILFNSLQYTNVVKDYWGNDLRYNKEYYMVNIDYLNRYMYANSRQIVFNTRRNNN
DFNEGYKIIIKRIRGNTNDTRVRGGDILYFDMTINNKAYNLFMKNETMYADNHSTEDIYA
IGLREQTKDINDNIIFQIQPMNNTYYYASQIFKSNFNGENISGICSIGTYRFRLGGDWYR
HNYLVPTVKQGNYASLLESTSTHWGFVPVSE
SEQ ID № 4 (BoNT/D – UniProt P19321)
MTWPVKDFNYSDPVNDNDILYLRIPQNKLITTPVKAFMITQNIWVIPERFSSDTNPSLSK
PPRPTSKYQSYYDPSYLSTDEQKDTFLKGIIKLFKRINERDIGKKLINYLVVGSPFMGDS
STPEDTFDFTRHTTNIAVEKFENGSWKVTNIITPSVLIFGPLPNILDYTASLTLQGQQSN
PSFEGFGTLSILKVAPEFLLTFSDVTSNQSSAVLGKSIFCMDPVIALMHELTHSLHQLYG
INIPSDKRIRPQVSEGFFSQDGPNVQFEELYTFGGLDVEIIPQIERSQLREKALGHYKDI
AKRLNNINKTIPSSWISNIDKYKKIFSEKYNFDKDNTGNFVVNIDKFNSLYSDLTNVMSE
VVYSSQYNVKNRTHYFSRHYLPVFANILDDNIYTIRDGFNLTNKGFNIENSGQNIERNPA
LQKLSSESVVDLFTKVCLRLTKNSRDDSTCIKVKNNRLPYVADKDSISQEIFENKIITDE
TNVQNYSDKFSLDESILDGQVPINPEIVDPLLPNVNMEPLNLPGEEIVFYDDITKYVDYL
NSYYYLESQKLSNNVENITLTTSVEEALGYSNKIYTFLPSLAEKVNKGVQAGLFLNWANE
VVEDFTTNIMKKDTLDKISDVSVIIPYIGPALNIGNSALRGNFNQAFATAGVAFLLEGFP
EFTIPALGVFTFYSSIQEREKIIKTIENCLEQRVKRWKDSYQWMVSNWLSRITTQFNHIN
YQMYDSLSYQADAIKAKIDLEYKKYSGSDKENIKSQVENLKNSLDVKISEAMNNINKFIR
ECSVTYLFKNMLPKVIDELNKFDLRTKTELINLIDSHNIILVGEVDRLKAKVNESFENTM
PFNIFSYTNNSLLKDIINEYFNSINDSKILSLQNKKNALVDTSGYNAEVRVGDNVQLNTI
YTNDFKLSSSGDKIIVNLNNNILYSAIYENSSVSFWIKISKDLTNSHNEYTIINSIEQNS
GWKLCIRNGNIEWILQDVNRKYKSLIFDYSESLSHTGYTNKWFFVTITNNIMGYMKLYIN
GELKQSQKIEDLDEVKLDKTIVFGIDENIDENQMLWIRDFNIFSKELSNEDINIVYEGQI
LRNVIKDYWGNPLKFDTEYYIINDNYIDRYIAPESNVLVLVQYPDRSKLYTGNPITIKSV
SDKNPYSRILNGDNIILHMLYNSRKYMIIRDTDTIYATQGGECSQNCVYALKLQSNLGNY
GIGIFSIKNIVSKNKYCSQIFSSFRENTMLLADIYKPWRFSFKNAYTPVAVTNYETKLLS
TSSFWKFISRDPGWVE
SEQ ID № 5 (BoNT/E – UniProt Q00496)
MPKINSFNYNDPVNDRTILYIKPGGCQEFYKSFNIMKNIWIIPERNVIGTTPQDFHPPTS
LKNGDSSYYDPNYLQSDEEKDRFLKIVTKIFNRINNNLSGGILLEELSKANPYLGNDNTP
DNQFHIGDASAVEIKFSNGSQDILLPNVIIMGAEPDLFETNSSNISLRNNYMPSNHRFGS
IAIVTFSPEYSFRFNDNCMNEFIQDPALTLMHELIHSLHGLYGAKGITTKYTITQKQNPL
ITNIRGTNIEEFLTFGGTDLNIITSAQSNDIYTNLLADYKKIASKLSKVQVSNPLLNPYK
DVFEAKYGLDKDASGIYSVNINKFNDIFKKLYSFTEFDLRTKFQVKCRQTYIGQYKYFKL
SNLLNDSIYNISEGYNINNLKVNFRGQNANLNPRIITPITGRGLVKKIIRFCKNIVSVKG
IRKSICIEINNGELFFVASENSYNDDNINTPKEIDDTVTSNNNYENDLDQVILNFNSESA
PGLSDEKLNLTIQNDAYIPKYDSNGTSDIEQHDVNELNVFFYLDAQKVPEGENNVNLTSS
IDTALLEQPKIYTFFSSEFINNVNKPVQAALFVSWIQQVLVDFTTEANQKSTVDKIADIS
IVVPYIGLALNIGNEAQKGNFKDALELLGAGILLEFEPELLIPTILVFTIKSFLGSSDNK
NKVIKAINNALKERDEKWKEVYSFIVSNWMTKINTQFNKRKEQMYQALQNQVNAIKTIIE
SKYNSYTLEEKNELTNKYDIKQIENELNQKVSIAMNNIDRFLTESSISYLMKIINEVKIN
KLREYDENVKTYLLNYIIQHGSILGESQQELNSMVTDTLNNSIPFKLSSYTDDKILISYF
NKFFKRIKSSSVLNMRYKNDKYVDTSGYDSNININGDVYKYPTNKNQFGIYNDKLSEVNI
SQNDYIIYDNKYKNFSISFWVRIPNYDNKIVNVNNEYTIINCMRDNNSGWKVSLNHNEII
WTFEDNRGINQKLAFNYGNANGISDYINKWIFVTITNDRLGDSKLYINGNLIDQKSILNL
GNIHVSDNILFKIVNCSYTRYIGIRYFNIFDKELDETEIQTLYSNEPNTNILKDFWGNYL
LYDKEYYLLNVLKPNNFIDRRKDSTLSINNIRSTILLANRLYSGIKVKIQRVNNSSTNDN
LVRKNDQVYINFVASKTHLFPLYADTATTNKEKTIKISSSGNRFNQVVVMNSVGNCTMNF
KNNNGNNIGLLGFKADTVVASTWYYTHMRDHTNSNGCFWNFISEEHGWQEK
SEQ ID № 6 (BoNT/F – UniProt P30996)
MPVAINSFNYNDPVNDDTILYMQIPYEEKSKKYYKAFEIMRNVWIIPERNTIGTNPSDFD
PPASLKNGSSAYYDPNYLTTDAEKDRYLKTTIKLFKRINSNPAGKVLLQEISYAKPYLGN
DHTPIDEFSPVTRTTSVNIKLSTNVESSMLLNLLVLGAGPDIFESCCYPVRKLIDPDVVY
DPSNYGFGSINIVTFSPEYEYTFNDISGGHNSSTESFIADPAISLAHELIHALHGLYGAR
GVTYEETIEVKQAPLMIAEKPIRLEEFLTFGGQDLNIITSAMKEKIYNNLLANYEKIATR
LSEVNSAPPEYDINEYKDYFQWKYGLDKNADGSYTVNENKFNEIYKKLYSFTESDLANKF
KVKCRNTYFIKYEFLKVPNLLDDDIYTVSEGFNIGNLAVNNRGQSIKLNPKIIDSIPDKG
LVEKIVKFCKSVIPRKGTKAPPRLCIRVNNSELFFVASESSYNENDINTPKEIDDTTNLN
NNYRNNLDEVILDYNSQTIPQISNRTLNTLVQDNSYVPRYDSNGTSEIEEYDVVDFNVFF
YLHAQKVPEGETNISLTSSIDTALLEESKDIFFSSEFIDTINKPVNAALFIDWISKVIRD
FTTEATQKSTVDKIADISLIVPYVGLALNIIIEAEKGNFEEAFELLGVGILLEFVPELTI
PVILVFTIKSYIDSYENKNKAIKAINNSLIEREAKWKEIYSWIVSNWLTRINTQFNKRKE
QMYQALQNQVDAIKTAIEYKYNNYTSDEKNRLESEYNINNIEEELNKKVSLAMKNIERFM
TESSISYLMKLINEAKVGKLKKYDNHVKSDLLNYILDHRSILGEQTNELSDLVTSTLNSS
IPFELSSYTNDKILIIYFNRLYKKIKDSSILDMRYENNKFIDISGYGSNISINGNVYIYS
TNRNQFGIYNSRLSEVNIAQNNDIIYNSRYQNFSISFWVRIPKHYKPMNHNREYTIINCM
GNNNSGWKISLRTVRDCEIIWTLQDTSGNKENLIFRYEELNRISNYINKWIFVTITNNRL
GNSRIYINGNLIVEKSISNLGDIHVSDNILFKIVGCDDETYVGIRYFKVFNTELDKTEIE
TLYSNEPDPSILKNYWGNYLLYNKKYYLFNLLRKDKYITLNSGILNINQQRGVTEGSVFL
NYKLYEGVEVIIRKNGPIDISNTDNFVRKNDLAYINVVDRGVEYRLYADTKSEKEKIIRT
SNLNDSLGQIIVMDSIGNNCTMNFQNNNGSNIGLLGFHSNNLVASSWYYNNIRRNTSSNG
CFWSSISKENGWKE
SEQ ID № 7 (BoNT/G – UniProt Q60393)
MPVNIKXFNYNDPINNDDIIMMEPFNDPGPGTYYKAFRIIDRIWIVPERFTYGFQPDQFN
ASTGVFSKDVYEYYDPTYLKTDAEKDKFLKTMIKLFNRINSKPSGQRLLDMIVDAIPYLG
NASTPPDKFAANVANVSINKKIIQPGAEDQIKGLMTNLIIFGPGPVLSDNFTDSMIMNGH
SPISEGFGARMMIRFCPSCLNVFNNVQENKDTSIFSRRAYFADPALTLMHELIHVLHGLY
GIKISNLPITPNTKEFFMQHSDPVQAEELYTFGGHDPSVISPSTDMNIYNKALQNFQDIA
NRLNIVSSAQGSGIDISLYKQIYKNKYDFVEDPNGKYSVDKDKFDKLYKALMFGFTETNL
AGEYGIKTRYSYFSEYLPPIKTEKLLDNTIYTQNEGFNIASKNLKTEFNGQNKAVNKEAY
EEISLEHLVIYRIAMCKPVMYKNTGKSEQCIIVNNEDLFFIANKDSFSKDLAKAETIAYN
TQNNTIENNFSIDQLILDNDLSSGIDLPNENTEPFTNFDDIDIPVYIKQSALKKIFVDGD
SLFEYLHAQTFPSNIENLQLTNSLNDALRNNNKVYTFFSTNLVEKANTVVGASLFVNWVK
GVIDDFTSESTQKSTIDKVSDVSIIIPYIGPALNVGNETAKENFKNAFEIGGAAILMEFI
PELIVPIVGFFTLESYVGNKGHIIMTISNALKKRDQKWTDMYGLIVSQWLSTVNTQFYTI
KERMYNALNNQSQAIEKIIEDQYNRYSEEDKMNINIDFNDIDFKLNQSINLAINNIDDFI
NQCSISYLMNRMIPLAVKKLKDFDDNLKRDLLEYIDTNELYLLDEVNILKSKVNRHLKDS
IPFDLSLYTKDTILIQVFNNYISNISSNAILSLSYRGGRLIDSSGYGATMNVGSDVIFND
IGNGQFKLNNSENSNITAHQSKFVVYDSMFDNFSINFWVRTPKYNNNDIQTYLQNEYTII
SCIKNDSGWKVSIKGNRIIWTLIDVNAKSKSIFFEYSIKDNISDYINKWFSITITNDRLG
NANIYINGSLKKSEKILNLDRINSSNDIDFKLINCTDTTKFVWIKDFNIFGRELNATEVS
SLYWIQSSTNTLKDFWGNPLRYDTQYYLFNQGMQNIYIKYFSKASMGETAPRTNFNNAAI
NYQNLYLGLRFIIKKASNSRNINNDNIVREGDYIYLNIDNISDESYRVYVLVNSKEIQTQ
LFLAPINDDPTFYDVLQIKKYYEKTTYNCQILCEKDTKTFGLFGIGKFVKDYGYVWDTYD
NYFCISQWYLRRISENINKLRLGCNWQFIPVDEGWTE
ПРИМЕРЫ
Пример 1
Эффективность ботулинического нейротоксина в лечении спастичности нижних конечностей оценивали в двойном слепом плацебо–контролируемом многоцентровом исследовании у пациентов в возрасте от 2 до 17 лет, страдающих спастичностью вследствие церебрального паралича, вызывающего динамическую эквинусную деформацию стопы.
В общей сложности 235 пациентов, ранее не получавших и получавших ранее лекарственное средство с оценкой 2–й степени или выше по модифицированной шкале Эшворта на подошвенном сгибателе голеностопного сустава были зарегистрированы для получения Dysport® или плацебо.
Семьдесят девять пациентов получили 10 единиц/кг/ногу, 79 пациентов получили 15 единиц/кг/ногу, и 77 пациентов получили плацебо. Введение выполняли путем инъекции в икроножные и камбаловидные мышцы. Сорок один процент пациентов (n=66) получали билатеральное лечение и получали общую дозу Dysport®, равную 20 единиц/кг (n=37) или 30 единиц/кг (n=29).
Таблица 1
У пациентов измеряли изменение в баллах MAS после лечения и баллах PGA для лечения. Как показано выше, лечение ботулиническим нейротоксином значимо снижает MAS для тонуса мышц голеностопного сустава по сравнению с плацебо. Лечение ботулиническим нейротоксином также привело к значимому повышению среднего балла PGA по сравнению с плацебо.
Пример 2
Пятьсот единиц лиофилизированного Dysport® осторожно смешивают с 2,5 мл 0,9% раствора хлорида натрия, не содержащего консервантов, во флаконе, формируя исходный раствор Dysport®. Дополнительные 2,5 мл 0,9% раствора хлорида натрия без консервантов набирают в 5 мл шприц. Затем шприц используют для извлечения вышеупомянутого раствора Dysport® из флакона без переворачивания. Полученный раствор осторожно перемешивают в шприце с образованием раствора для инъекций 10 единиц/0,1 мл. Раствор хранят в шприце в холодильнике при температуре от 2 до 8°C и с защитой от света. Композицию используют в течение 24 часов и, если она не была использована, утилизируют.
Пример 3
Триста единиц лиофилизированного Dysport® осторожно смешивают с 1,5 мл 0,9% раствора хлорида натрия без консервантов во флаконе, формируя исходный раствор Dysport®. Дополнительные 1,5 мл 0,9% раствора хлорида натрия без консервантов набирают в шприц объемом 3 мл. Затем шприц используют для извлечения вышеупомянутого раствора Dysport® из флакона без переворачивания. Полученный раствор осторожно перемешивают в шприце с образованием раствора для инъекций 10 единиц/0,1 мл. Раствор хранят в шприце в холодильнике при температуре от 2 до 8°C и с защитой от света. Композицию используют в течение 24 часов и, если она не была использована, утилизируют.
Пример 4
Врач, лечащий 10–летнего пациента от тяжелой спастичности нижних конечностей в левой камбаловидной мышце (балл MAS, равный 3), сначала получает вес пациента. Определено, что вес составляет 30 кг. Поскольку у пациента проявляется спастичность в камбаловидной мышце левой ноги, врач определяет, что введение следует выполнять латерально в камбаловидную мышцу левой ноги. Обращаясь к средству дозирования, определяют, что подходящая доза составляет от 120 до 180 единиц. Затем изучают анамнез пациента. Поскольку установлено, что пациент не имел побочных эффектов при предшествующем лечении ботулиническим нейротоксином и уровень спастичности был тяжелым, определяют, что следует ввести 180 единиц.
Раствор Dysport® для инъекций 10 единиц/0,1 мл в шприце готовят, как описано в примере 2. 1,8 мл раствора вводят посредством инъекции в камбаловидную мышцу пациента. Шприц вместе с оставшимся в нем раствором утилизируют.
Вышеуказанные этапы повторяют через 16 недель.
Пример 5
Врач, лечащий 12–летнего пациента от небольшой спастичности нижних конечностей в левой и правой икроножной мышце (балл по шкале MAS 1+), сначала получает вес пациента. Определено, что вес составляет 40 кг. Поскольку у пациента проявляется спастичность в икроножных мышцах обеих ног, врач определяет, что введение следует выполнять билатерально в икроножные мышцы обеих ног. Обращаясь к средству дозирования, определяют, что доза от 240 до 360 единиц на каждую ногу является подходящей. Затем изучают анамнез пациента. Поскольку установлено, что пациент имел побочные эффекты при предшествующем лечении ботулиническим нейротоксином и уровень спастичности был небольшим, было определяют, что 240 единиц следует вводить в каждую ногу.
Раствор Dysport® для инъекций 10 единиц/0,1 мл в шприце готовят, как описано в примере 2. 2,4 мл раствора вводят посредством инъекции в икроножную мышцу каждой ноги пациента. Шприц вместе с оставшимся в нем раствором утилизируют.
Вышеуказанные этапы повторяют через 18 недель.
Пример 6
Врач, лечащий 8–летнего пациента от небольшой спастичности нижних конечностей в левой камбаловидной мышце и правой икроножной мышце (балл MAS, равный 1), сначала получает вес пациента. Определено, что вес составляет 20 кг. Врач определяет, что введение следует выполнять латерально в камбаловидную мышцу левой ноги и латерально в икроножную мышцу правой ноги. Обращаясь к средству дозирования, определяют, что доза от 80 до 120 единиц для левой камбаловидной мышцы и от 120 до 180 единиц для правой икроножной мышцы является подходящей. Затем изучают анамнез пациента. Поскольку установлено, что пациент не имел побочных эффектов при предшествующем лечении ботулиническим нейротоксином и уровень спастичности был средним, определяют, что 100 единиц следует вводить в левую камбаловидную мышцу, и 150 единиц следует вводить в правую икроножную мышцу.
Раствор Dysport® для инъекций 10 единиц/0,1 мл в шприце готовят, как описано в примере 2. Один миллилитр раствора вводят посредством инъекции в левую камбаловидную мышцу и 1,5 мл вводят посредством инъекции в правую икроножную мышцу.
Вышеуказанные этапы повторяют через 17 недель.
Пример 7
Врач, лечащий 8–летнего пациента от небольшой спастичности нижних конечностей в левой камбаловидной мышце и правой икроножной мышце (балл MAS, равный 1), сначала получает вес пациента. Определено, что вес составляет 20 кг. Врач определяет, что введение следует выполнять латерально в камбаловидную мышцу левой ноги и латерально в икроножную мышцу правой ноги. Обращаясь к средству дозирования, определяют, что доза от 80 до 120 единиц для левой камбаловидной мышцы и от 120 до 180 единиц для правой икроножной мышцы является подходящей. Затем изучают анамнез пациента. У пациента наблюдали локальную мышечную слабость в правой икроножной мышце. Тем не менее, пациент не имел побочных эффектов при предшествующем лечении ботулиническим нейротоксином, и уровень спастичности был средним. Определяют, что 100 единиц следует вводить в левую камбаловидную мышцу, и, вследствие мышечной слабости, 120 единиц следует вводить в правую икроножную мышцу.
Раствор Dysport® для инъекций 10 единиц/0,1 мл в шприце готовят, как описано в примере 2. Один миллилитр раствора вводят посредством инъекции в левую камбаловидную мышцу, и 1,2 мл вводят посредством инъекции в правую икроножную мышцу.
Вышеуказанные этапы повторяют через 17 недель.
Пример 8
Врач, лечащий 12–летнего пациента от небольшой спастичности нижних конечностей в левой и правой икроножной мышце (балл по шкале MAS, равный 1+), сначала получает вес пациента. Определено, что вес составляет 40 кг. Поскольку у пациента проявляется спастичность в икроножных мышцах обеих ног, врач определяет, что введение следует выполнять билатерально в икроножные мышцы обеих ног. Обращаясь к средству дозирования, определяют, что доза от 240 до 360 единиц на каждую ногу является подходящей. Затем изучают анамнез пациента. Обнаружено, что у пациента не было побочных эффектов при предшествующем лечении ботулиническим нейротоксином, но такое лечение не привело к желаемому результату (PGA составил 0). Ввиду этого и того, что тяжесть спастичности была средней, было определено, что 360 единиц следует вводить в каждую ногу.
Раствор Dysport® для инъекций 10 единиц/0,1 мл в шприце готовят, как описано в примере 2. 3,6 мл раствора вводят посредством инъекции в икроножную мышцу каждой ноги пациента. Шприц вместе с оставшимся в нем раствором утилизируют.
Вышеуказанные этапы повторяют через 17 недель.
Пример 9
Врач, лечащий 12–летнего пациента от небольшой спастичности нижних конечностей в левой и правой икроножной мышце (балл по шкале MAS, равный 1), сначала получает вес пациента. Определено, что вес составляет 40 кг. Поскольку у пациента проявляется спастичность в икроножных мышцах обеих ног, врач определяет, что введение следует выполнять билатерально в икроножные мышцы обеих ног. Обращаясь к средству дозирования, определяют, что доза 240 до 360 единиц на каждую ногу является подходящей. Затем изучают анамнез пациента. Обнаружено, что у пациента не было побочных эффектов при предшествующем лечении ботулиническим нейротоксином, но такое лечение не привело к желаемому результату (PGA составлял 0,03). Ввиду этого и того, что степень выраженности спастичности была средней, было определено, что 360 единиц следует вводить в каждую ногу.
Раствор Dysport® для инъекций 10 единиц/0,1 мл в шприце готовят, как описано в примере 2. 3,6 мл раствора вводят посредством инъекции в икроножную мышцу каждой ноги пациента. Шприц вместе с оставшимся в нем раствором утилизируют.
Вышеуказанные этапы повторяют через 17 недель.

Изобретение относится к биотехнологии. Представлено средство для применения при определении объема дозы ботулинического нейротоксина, вводимого при лечении спастичности нижних конечностей у субъекта в возрасте 18 лет или моложе, где средство содержит: первый элемент, имеющий первую строку чисел, указывающих вес субъекта, и вторую строку чисел, указывающих объем дозы ботулинического нейротоксина, который следует вводить субъекту, где числа в первой строке, указывающие конкретный вес, находятся в продольном или радиальном выравнивании с соответствующими числами во второй строке, указывающими конкретный объем дозы, который следует вводить субъекту, имеющему этот конкретный вес, где объем дозы соответствует от 5 до 15 единиц на килограмм общей массы тела субъекта на одну ногу. А также второй элемент, перекрывающий первый и имеющий отверстие или отверстия, которые позволяют просматривать строки на первом элементе. При этом первый и второй элементы находятся во взаимосвязи друг с другом. Изобретение позволяет применять его для эффективного определения объема дозы ботулинического нейротоксина, вводимого при лечении спастичности нижних конечностей у субъекта в возрасте 18 лет или моложе. 7 з.п. ф-лы, 5 ил., 1 табл., 9 пр.
1. Средство для применения при определении объема дозы ботулинического нейротоксина, вводимого при лечении спастичности нижних конечностей у субъекта в возрасте 18 лет или моложе, где средство содержит:
первый элемент, имеющий первую строку чисел, указывающих вес субъекта, и вторую строку чисел, указывающих объем дозы ботулинического нейротоксина, который следует вводить субъекту, где числа в первой строке, указывающие конкретный вес, находятся в продольном или радиальном выравнивании с соответствующими числами во второй строке, указывающими конкретный объем дозы, который следует вводить субъекту, имеющему этот конкретный вес, где объем дозы соответствует от 5 до 15 единиц на килограмм общей массы тела субъекта на одну ногу; и
второй элемент, перекрывающий первый и имеющий отверстие или отверстия, которые позволяют просматривать строки на первом элементе;
где первый и второй элементы находятся во взаимосвязи друг с другом, так что пользователь может перемещать один элемент для указания объема дозы ботулинического нейротоксина, который следует вводить субъекту, имеющему конкретный вес; и
где первый элемент дополнительно содержит строку чисел, указывающих объем дозы ботулинического нейротоксина, который следует вводить в конкретную мышцу субъекта, и числа в строке, которые указывают конкретный объем дозы, который следует вводить в мышцу субъекта, имеющего конкретный вес, находятся в продольном или радиальном выравнивании с соответствующими числами в первой строке, указывающими этот конкретный вес,
при этом объем дозы соответствует от 6 до 9 единиц на килограмм общей массы тела субъекта, вводимой в индивидуальную икроножную мышцу субъекта или, где объем дозы соответствует от 4 до 6 единиц на килограмм общей массы тела субъекта, вводимой в индивидуальную камбаловидную мышцу субъекта.
2. Средство по п. 1, в котором первый и второй элементы представляют собой плоские поверхности, которые находятся в расположении друг относительно друга, допускающем продольное скольжение, где числа в первой строке, указывающие конкретный вес, находятся в продольном выравнивании с соответствующими числами во второй строке, указывающими конкретный объем дозы, который следует вводить субъекту, имеющему этот конкретный вес, и второй элемент перекрывает первый элемент и имеет отверстие, которое позволяет просматривать строки на первом элементе, или имеет два или более отверстий, где каждое отверстие позволяет просматривать одну строку на первом элементе, где один элемент может скользить относительно другого, где числа, просматриваемые через отверстие или отверстия, указывают конкретный вес и объем дозы, который следует вводить субъекту, имеющему этот конкретный вес.
3. Средство по п. 1 или 2, в котором первый элемент представляет собой плоскую поверхность, а второй элемент представляет собой бегунок, находящийся в расположении, допускающем продольное скольжение относительно первого элемента, где числа в первой строке, указывающие конкретный вес, находятся в продольном выравнивании с соответствующими числами во второй строке, указывающими конкретный объем дозы, который следует вводить субъекту, имеющему этот конкретный вес, и бегунок можно перемещать вдоль первого элемента так, чтобы он указывал конкретный вес и объем дозы, который следует вводить субъекту, имеющему этот конкретный вес.
4. Средство по п. 1 или 2, в котором первый элемент представляет собой круглую плоскую поверхность, а второй элемент представляет собой циферблат, который поворачивается вокруг центральной точки первого элемента, где числа в первой строке, указывающие конкретный вес, находятся в радиальном выравнивании с соответствующими числами во второй строке, указывающими конкретный объем дозы, который следует вводить субъекту, имеющему этот конкретный вес, где бегунок может поворачиваться так, чтобы он указывал конкретный вес и объем дозы, который следует вводить субъекту, имеющему этот конкретный вес.
5. Средство по п. 3 или 4, в котором указание осуществляется посредством линии на бегунке, которая перекрывает конкретный вес и объем дозы, который следует вводить субъекту, имеющему этот конкретный вес.
6. Средство по п. 3 или 4, в котором указатель представляет собой отверстие в бегунке, которое позволяет просматривать строки на первом элементе, или два или более отверстий, где каждое из отверстий позволяет просматривать одну строку на первом элементе, и где числа, просматриваемые через отверстие или отверстия, указывают конкретный вес и объем дозы, который следует вводить субъекту, имеющему этот конкретный вес.
7. Средство по любому из пп. 1-6, в котором первый элемент дополнительно имеет на нем две строки чисел, где каждая строка указывает объем дозы ботулинического нейротоксина, который следует вводить в разные мышцы субъекта, и числа в строке, которые указывают конкретный объем дозы, который следует вводить в мышцы субъекта, имеющего конкретный вес, находятся в продольном или радиальном выравнивании с соответствующими числами в первой строке, указывающими этот конкретный вес.
8. Средство по любому из пп. 1-6, в котором во второй строке указан общий объем дозы ботулинического нейротоксина, который следует вводить в одну ногу субъекта, и первый элемент дополнительно имеет на нем две дополнительных строки чисел, где одна строка указывает объем дозы ботулинического нейротоксина, который следует вводить в икроножную мышцу ноги, и другая строка указывает объем дозы ботулинического нейротоксина, который следует вводить в камбаловидную мышцу ноги, где числа в строках, которые указывают конкретный объем для введения в мышцы субъекта, имеющего конкретный вес, находятся в продольном или радиальном выравнивании с соответствующими числами в первой строке, указывающими этот конкретный вес.
| Перекатываемый затвор для водоемов | 1922 |
|
SU2001A1 |
| GB 1476668 A, 16.06.1977 | |||
| DE 29814563 U1, 26.11.1998 | |||
| СПОСОБ ПРИГОТОВЛЕНИЯ МЯСНЫХ РУБЛЕНЫХ ПОЛУФАБРИКАТОВ | 2010 |
|
RU2428058C1 |
| GB 734595 A, 03.08.1955 | |||
| CN 201673426 U, 15.12.2010 | |||
| СРЕДСТВА И СПОСОБЫ ОПРЕДЕЛЕНИЯ КОЛИЧЕСТВА ПОЛИПЕПТИДА НЕЙРОТОКСИНА И ЕГО КАТАЛИТИЧЕСКОЙ И ПРОТЕОЛИТИЧЕСКОЙ АКТИВНОСТЕЙ | 2010 |
|
RU2545783C9 |
Авторы
Даты
2023-01-16—Публикация
2018-07-27—Подача