[0001] Настоящая заявка испрашивает преимущество приоритета предварительной заявки на патент США № 62/423618, поданной 17 ноября 2016 года.
Включение посредством ссылки материала, поданного в электронном виде
[0002] Перечень последовательностей в машиночитаемой форме включен посредством ссылки в полном объеме, при этом он подается одновременно с данным документом и имеет следующие характеристики: текстовый файл в формате ASCII под названием «50215PCT_SeqListing.txt», размером 24148 байт, созданный 17 ноября 2017 года.
Область техники, к которой относится изобретение
[0003] Настоящее изобретение относится к способам и материалам для интратекальной доставки рекомбинантного аденоассоциированного вируса 9 (rAAV9), кодирующего метил-CpG-связывающий белок 2 (MECP2). Предусмотрено применение способов и материалов, например, для лечения синдрома Ретта.
Уровень техники
[0004] Синдром Ретта представляет собой Х-сцепленное доминантное нарушение развития нервной системы, которое поражает 1 из 10000 девочек. Гемизиготные особи мужского пола обычно умирают от неонатальной энцефалопатии. Гетерозиготные особи женского пола доживают до взрослого возраста, но у них проявляются тяжелые симптомы, включая микроцефалию, утрату целенаправленных движений рук и речи и двигательные нарушения, которые проявляются после периода визуально нормального развития. Манифестация заболевания приходится на возраст приблизительно 6-18 месяцев.
[0005] Синдром Ретта подразделяют на типичный (или классический) синдром Ретта или атипичный синдром Ретта. Спонтанные мутации гена, кодирующего транскрипционный фактор, метил-CpG-связывающий белок 2 (MECP2), вызывают большинство (~90%) случаев в обоих классах, хотя атипичный синдром Ретта может быть вызван мутациями в генах, отличных от MECP2. На тяжесть заболевания влияют природа мутации MECP2 (например, делеция или точковая мутация) и асимметричная инактивация Х-хромосомы. Транскрипционный фактор MECP2 модулирует транскрипцию тысяч генов. Ранее терапевтические усилия были направлены на мишени, представляющие собой последующие звенья процессов с участием MECP2, включая нейротрансмиттеры, факторы роста и метаболические пути. По меньшей мере в девяти клинических испытаниях, направленных на лечение синдрома Ретта, сообщалось о положительных результатах по различным показателям, но полученные результаты не были независимо подтверждены или не приводили к созданию новых средств лечения [Katz et al, Trends in Neurosciences, 39: 100-113 (2016)]. В настоящее время отсутствуют одобренные средства лечения синдрома Ретта.
[0006] Существуют модельные животные, представляющие собой самцов и самок мышей, где мыши проявляют RTT-подобное поведение [Guy et al., Nature Genetics, 27: 322-326 (2001); Chen et al., Nature Genetics 27: 327-331 (2001); и Katz et al., 5: 733-745 (2012)].
[0007] MECP2 представляет собой ядерный белок массой 52 кДа, который экспрессируется в целом ряде тканей, но характеризуется высоким содержанием в нейронах, и он изучался, прежде всего, в нервной системе. У человека существуют две изоформы MECP2, известные как MECP2A и B (фигура 1) [Weaving et al., Journal of Medical Genetics, 42: 1-7 (2005)]. Две изоформы происходят из транскриптов мРНК, подвергаемых альтернативному сплайсингу, и они имеют различные сайты начала трансляции. MECP2B содержит экзоны 1, 3 и 4 и является преобладающей изоформой в головном мозге. MECP2 обратимо связывается с метилированной ДНК и модулирует экспрессию генов [Guy et al., Annual Review of Cell and Developmental Biology, 27: 631-652 (2011)]. Эти функции связывают с метил-связывающим доменом (MBD) и доменом-репрессором транскрипции (TRD), соответственно [Nan & Bird, Brain & Development, 23, Suppl 1: S32-37 (2001)]. MECP2, первоначально считавшийся репрессором транскрипции, может как индуцировать, так и подавлять экспрессию целевого гена [Chahrour et al., Science, 320: 1224-1229 (2008)]. Предполагается, что MECP2 обеспечивает правильное развитие и поддержание нейронов. В нейронах MECP2 облегчает преобразование синаптической активности в экспрессию генов за счет связывания ДНК и взаимодействия с различными партнерами по связыванию [Ebert et al., Nature, 499: 341-345 (2013) и Lyst et al., Nature Neuroscience, 16: 898-902 (2013)]. В астроцитах недостаточность MECP2 связана с эпизодами апноэ у мышей [Lioy et al., Nature, 475: 497-500 (2011)]. Недостаточность MECP2 может вызывать уменьшение размера головного мозга, увеличение плотности упаковки нейронов и снижение сложности дендритной сети [Armstrong et al., Journal of Neuropathology and Experimental Neurology, 54: 195-201 (1995)]. Важно отметить, что гибель нейронов не сопряжена с недостаточностью MECP2 [Leonard et al., Nature Reviews, Neurology, 13: 37-51 (2017)]. MECP2 также встречается за пределами нервной системы, хотя его уровни в разных тканях варьируются (фигура 2). В недавнем исследовании изучали зависимость симптомов синдрома Ретта у мышей от периферической экспрессии Mecp2 [Ross et al., Human Molecular Genetics, 25: 4389-4404 (2016)]. Периферическая недостаточность была сопряжена с гипоактивностью, усталостью при физической нагрузке и аномалиями костной ткани. У мышей с нокаутом периферического MECP2 отсутствовало большинство поведенческих, сенсорно-двигательных, связанных с походкой и вегетативных (дыхательных и сердечных) фенотипов, сопряженных с RTT.
[0008] Поскольку MECP2 представляет собой X-сцепленный ген, одна копия MECP2 является молчащей вследствие инактивации Х-хромосомы (Xci) у самок. Полагают, что для каждой клетки Xci является случайной, что приводит к химеризму по MECP2 у самок с синдромом Ретта. На тяжесть заболевания влияет то, содержит ли большинство активных Х-хромосом интактный или мутантный ген MECP2. Это называют асимметричной Xci. У самцов Xci не происходит, поэтому недостаточность MECP2 является более сильной, поскольку отсутствуют клетки, которые будут обладать функциональной копией MECP2. На тяжесть заболевания также влияет природа мутации MECP2. В базе данных RettBASE (http://mecp2.chw.edu.au/) описаны более 600 различных мутаций гена MECP2, в том числе делеции, нонсенс-мутации и точковые мутации. Наиболее распространенной мутацией (~9% пациентов) является аллель T185M, при котором затрагивается метил-связывающий домен. Другие распространенные мутации показаны на фигуре 3 [Leonard, выше]. Совместно они составляют более 40% случаев, перечисленных в RettBASE. Крупномасштабные делеции с вовлечением MECP2 обнаруживали в 8-10% случаев [Li et al., Journal of Human Genetics, 52: 38-47 (2007) и Hardwick et al., European Journal of Human Genetics, 15: 1218-1229 (2007)]. Для R133C, R294X и C-концевых мутаций и делеций (ниже TRD), вызывающих более легкую форму заболевания, отмечена генотип-фенотипическая корреляция. Крупные делеции и мутации раннего усечения цепи (R270X, R255X и R168X) сопряжены с тяжелой формой синдрома Ретта. В таблице 1 описаны единые диагностические критерии синдрома Ретта, недавно подготовленные группой интернациональных врачей-клиницистов, специализирующихся на лечении синдрома Ретта [Neul et al., Annals of Neurology, 68: 944-950 (2010)].
Диагностические критерии для RTT 2010
-Диагностика рекомендуется, если наблюдается постнатальное замедление роста головы.
1. Период регрессии с последующим восстановлением или стабилизацией.*
2. Все основные критерии и все критерии исключения
3. Вспомогательные критерии не требуются, хотя зачастую присутствуют при типичном RTT
1. Период регрессии с последующим восстановлением или стабилизацией
2. По меньшей мере 2 из 4 основных критериев
3. 5 из 11 вспомогательных критериев
1. Частичная или полная утрата приобретенных навыков целенаправленных движений рук.
2. Частичная или полная утрата приобретенных навыков устной речи**
3. Нарушения походки: нарушенная (диспраксическая) способность или отсутствие способности.
4. Стереотипные движения рук, такие как автоматические движения в виде выкручивания/сжимания рук, хлопанья/постукивания, помещения рук в рот и моющих/потирающих движений.
1. Повреждение головного мозга вследствие травмы (пери- или постнатальной), нейрометаболическое заболевание или тяжелая инфекция, которая вызывает неврологические проблемы***
2. Чрезвычайно аномальное психомоторное развитие в первые 6 месяцев жизни#
Нарушения дыхания в состоянии бодрствования
Бруксизм в состоянии бодрствования
Нарушенный характер сна
Аномальный мышечный тонус
Периферические вазомоторные расстройства
Сколиоз/кифоз
Замедление роста
Маленькие холодные руки и ступни
Неуместные приступы смеха/крика
Ослабленный ответ на боль
Интенсивное общение глазами - "указывание при помощи глазʺ
[0009] Аденоассоциированный вирус (AAV) представляет собой дефектный по репликации парвовирус, однонитевой ДНК-геном которого имеет длину около 4,7 т. о., включая инвертированный концевой повтор (ITR) длиной 145 нуклеотидов. Нуклеотидная последовательность генома AAV серотипа 2 (AAV2) представлена в Srivastava et al., J Virol, 45: 555-564 (1983), с исправлениями согласно Ruffing et al., J Gen Virol, 75: 3385-3392 (1994). В пределах ITR содержатся действующие в цис-положении последовательности, управляющие репликацией (rep) вирусной ДНК, капсидированием/упаковкой и встраиванием в хромосому клетки-хозяина. Три промотора AAV (названные p5, p19 и p40 за их относительные местоположения на карте) управляют экспрессией двух внутренних открытых рамок считывания AAV, кодирующих гены rep и cap. Два промотора rep (p5 и p19) в сочетании с дифференциальным сплайсингом единственного интрона AAV (по нуклеотидам 2107 и 2227) приводят к образованию четырех белков rep (rep 78, rep 68, rep 52 и rep 40) на основе гена rep. Белки rep обладают свойствами нескольких ферментов, которые, в конечном итоге, ответственны за репликацию вирусного генома. Ген cap экспрессируется за счет промотора p40 и кодирует три капсидных белка VP1, VP2 и VP3. Получение трех родственных капсидных белков обусловлено альтернативным сплайсингом и неконсенсусными сайтами начала трансляции. Единственный консенсусный сайт полиаденилирования расположен в положении 95 на карте генома AAV. Обзор жизненного цикла и генетики AAV приведен в Muzyczka, Current Topics in Microbiology and Immunology, 158: 97-129 (1992).
[0010] AAV обладает уникальными свойствами, которые делают его привлекательным в качестве вектора для доставки чужеродной ДНК в клетки, например, в генной терапии. Вызываемая AAV инфекция клеток в культуре не является цитопатической, а природная инфекция у человека и других животных является скрытой и бессимптомной. Более того, AAV инфицирует множество клеток млекопитающих, что обеспечивает возможность целенаправленного воздействия на множество различных тканей in vivo. Более того, AAV трансдуцирует медленно делящиеся и неделящиеся клетки и может сохраняться фактически в течение периода жизни этих клеток в виде транскрипционно активной ядерной эписомы (внехромосомного элемента). Провирусный геном AAV является инфекционным, поскольку клонирует ДНК в плазмиды, что делает возможным конструирование рекомбинантных геномов. Кроме того, поскольку сигналы, управляющие репликацией AAV, капсидированием и встраиванием генома, содержатся в пределах ITR генома AAV, некоторые или все внутренние участки размером примерно 4,3 т. о. генома (кодирующие белки репликации и структурные капсидные белки, rep-cap) можно заменить чужеродной ДНК, такой как генная кассета, содержащая промотор, представляющую интерес ДНК и сигнал полиаденилирования. Белки rep и cap могут обеспечиваться в транс-конфигурации. Другим важным признаком AAV является то, что он представляет собой исключительно стабильный и крепкий вирус. Он легко выдерживает условия, применяемые для инактивации аденовируса (от 56° до 65°С в течение нескольких часов), что делает менее важным хранение AAV в холодных условиях. AAV даже можно лиофилизировать. Наконец, инфицированные AAV клетки не обладают невосприимчивостью к суперинфекции. Существует множество серотипов AAV, и они характеризуются различным тканевым тропизмом. К известным серотипам относятся, например, AAV1, AAV2, AAV3, AAV4, AAV5, AAV6, AAV7, AAV8, AAV9, AAV10, AAV11, AAV12, AAV13 и AAVrh74. AAV9 описан в патенте США № 7198951 и в Gao et al., J. Virol., 78: 6381-6388 (2004).
[0011] В данной области техники остается потребность в способах и продуктах для доставки полинуклеотидов MECP2 в центральную нервную систему и экспрессии в ней таких полинуклеотидов.
Краткое описание
[0012] В настоящем изобретении предусмотрены способы и материалы, пригодные для лечения синдрома Ретта у пациента, нуждающегося в этом.
[0013] Предусмотрены способы лечения синдрома Ретта у пациента, предусматривающие стадию интратекального введения пациенту рекомбинантного аденоассоциированного вируса 9 (rAAV9), кодирующего метил-CpG-связывающий белок 2 (MECP2), где rAAV9 содержит самокомплементарный геном, кодирующий MECP2B, и где последовательность самокомплементарного генома представляет собой SEQ ID NO:1. В качестве иллюстративного rAAV9 предусмотрен scAAV под названием AVXS-201.
[0014] Предусмотрены способы, которые дополнительно предусматривают стадию интратекального введения пациенту йогексола, йобитридола, йомепрола, йопамидола, йопентола, йопромида, йоверсола или йоксилана или смесей двух или более из них, и/или которые дополнительно предусматривают приведение пациента в положение Тренделенбурга.
Краткое описание графических материалов
[0015] Фигура 1. Диаграмма локуса MECP2 человека. На рисунке показаны альтернативные сайты начала транскрипции (стрелки), экзоны (прямоугольники) и паттерн сплайсинга зрелых мРНК. MECP2B представляет собой изоформу, наиболее распространенную в головном мозге, и кодируется AVXS-201.
[0016] Фигура 2. На графике изображены относительные уровни экспрессии белка MECP2 в различных тканях человека, установленные с помощью иммуногистохимического анализа. Из The Human Protein Atlas (www.proteinatlas.org) с модификациями.
[0017] Фигура 3. Ключевые функциональные домены белка MECP2 и распространенные мутации, обнаруженные у пациентов с синдромом Ретта. MBD=метил-CpG-связывающий домен, TRD=домен репрессии транскрипции, NID=домен взаимодействия NCOR-SMRT (NID) и сигнал ядерной локализации (NLS)
[0018] Фигура 4. Исследование для подтверждения механизма AAV9-опосредованного восстановления экспрессии Mecp2 у самцов мышей с синдромом Ретта. A) Упрощенная схема генома рекомбинантного AAV. B) Дизайн эксперимента. C) Кривая выживания Каплана-Мейера, демонстрирующая увеличение выживания у мышей с синдромом Ретта, обработанных посредством scAAV9.738.Mecp2, по сравнению с животными, обработанными контрольным вектором. D) Опосредованное вектором восстановление Mecp2 улучшает поведенческий фенотип, измеряемый по шкале оценок Берда (вставка 1).
[0019] Фигура 5. Обработка самок мышей с синдромом Ретта с помощью scAAV9.738.Mecp2 обеспечивает физиологические уровни Mecp2 и улучшает аберрантное поведение. A) Дизайн эксперимента. В) Результаты измерений интенсивности флуоресценции на срезах головного мозга, которые были окрашены иммунной меткой для выявления Mecp2, полученных от мышей дикого типа и мышей с синдромом Ретта, обработанных посредством scAAV9.738.Mecp2. Распределение результатов измерения интенсивности является аналогичным у двух групп. C) Оценка фенотипа по шкале Берда демонстрирует уменьшение проявления симптомов у животных, получающих scAAV9.738.Mecp2. D-G) Все из оценок поведения на вращающемся барабане, перевернутой сетке, платформе и поведения при устройстве гнезда, соответственно, демонстрируют улучшение у животных, обработанных посредством scAAV9.738.Mecp2, по сравнению с животными, обработанными контролем.
[0020] Фигура 6. Упрощенная схема, изображающая геномы рекомбинантного AAV первого поколения (A) и переработанного (B, AVXS-201), описанные в данном документе. Цвета указывают на сходства и различия между конструкциями. При переработке scAAV9.738.Mecp2 в AVXS-201 был укорочен промотор, были укорочены промежуточные последовательности между ключевыми элементами, кДНК Mecp2-альфа мыши была заменена на кДНК MECP2B человека, а сигнал полиаденилирования бычьего гормона роста был заменен на более короткий синтетический элемент. Общая цель изменений заключалась в повышении эффективности упаковки при сохранении физиологических уровней экспрессии кДНК MECP2, важной с клинической точки зрения.
[0021] Фигура 7. Дозозависимый ответ на AVXS-201 у Mecp2-/y мышей. A) График Каплана-Мейера для различных доз, применяемых для обработки Mecp2-/y мышей. Медиана выживания у групп с различными дозами имеет цветовую кодировку и обозначена пунктирными линиями. Каждая когорта, которая получала AVXS-201, характеризовалась увеличением выживания относительно мышей с нулевым аллелем, обработанных контролем. B) Данные медианы выживания для каждой группы были нанесены на график, чтобы показать кривую дозозависимого ответа. Пунктирная линия представляет медиану выживания у Mecp2-/y, обработанных посредством PBS. Эти данные согласуются с известными эффектами недостаточности и переизбытка MECP2.
[0022] Фигура 8. Оценка поведения по шкале Берда у Mecp2-/y мышей, обработанных посредством AVXS-201. A) У пораженных мышей, обработанных контролем, с увеличением возраста дефициты накапливаются. Поведенческие дефициты ослабляются при обработке посредством AVXS-201 независимо от дозы. B) На график повторно нанесены те же данные, что и на (A), но показаны только группа, обработанная контролем, и группа, обработанная AVXS-201 в количестве 1,44×1010 vg.
[0023] Фигура 9. У мышей с нулевым аллелем Mecp2, обработанных посредством AVXS-201, восстанавливается способность к самопроизвольным передвижениям. Анализ в тесте "открытое поле" демонстрирует, что мыши с нулевым аллелем, обработанные посредством AVXS-201, проходят (A) большие расстояния и при увеличенной (B) средней скорости по сравнению с мышами с нулевым аллелем, обработанными контролем. C) Показатели на вращающемся барабане в возрасте 3 месяцев также улучшались при умеренных дозах AVXS-201. +=p≤0,001; *=p≤0,05; ζ=p≤0,0001.
[0024] Фигура 10. При терапевтических дозах AVXS-201 приводит к умеренному количеству MECP2. A) Вестерн-блоты гомогенатов полушарий головного мозга от самцов мышей дикого типа (PBS) или Mecp2-/y мышей, которые получены с применением антител к MeCP2. Мышам с нулевым аллелем Mecp2 либо не производили инъекцию (KO), либо они получали указанные дозы AVXS-201. B) Количественная оценка панели A. Целевая терапевтическая доза, составлявшая 1,44×1010 vg, приводила к выработке 11% от уровней белка дикого типа.
[0025] Фигура 11. AVXS-201 хорошо переносится мышами дикого типа. A) График выживания Каплана-Мейера для самцов мышей дикого типа, которые получали ICV введение AVXS-201 в P1. B) Фенотипическая оценка по шкале Берда обработанных мышей и мышей дикого типа демонстрирует, что хорошо переносится широкий диапазон доз. Самая высокая доза (1,13×1011, синяя линия) приводила к легким нарушениям поведения.
[0026] Фигура 12. Обработка посредством AVXS-201 не ухудшает способность к передвижению у животных дикого типа. Анализ в тесте "открытое поле" самцов мышей дикого типа, обработанных посредством AVXS-201, демонстрирует, что (А) пройденные расстояния и (В) средние скорости аналогичны таковым у мышей дикого типа, обработанных контролем. C) Показатели на вращающемся барабане снижались у животных дикого типа, которые получали высокую дозу AVXS-201. +=p≤0,001, *=p≤0,05
[0027] Фигура 13. AVXS-201 приводит к дозозависимому увеличению содержания белка MECP2 в головном мозге дикого типа. A) Вестерн-блоты, полученные с применением антител к MeCP2, демонстрируют дозозависимое повышение общего белка MeCP2 в различных областях головного мозга через 3 недели после ICV инъекции в P1. (Cb=мозжечок, Med=продолговатый мозг, Hipp=гиппокамп, Ctx=кора головного мозга, Mid=средний мозг). TG3 обозначает образцы, взятые от модельной мыши с тяжелой степенью синдрома дупликации MeCP21. B) Количественная оценка панели A. Высокие, а не умеренные, дозы AVXS-201 удваивают экспрессию MECP2 в отдельных областях головного мозга.
[0028] Фигура 14. Интратекальная инфузия AVXS-201 отличным от человека приматам не влияет на прирост массы тела. Три животных, обработанных посредством AVXS-201, показаны красным цветом, а масса тела контрольного субъекта показана синим цветом.
[0029] Фигура 15. Интратекальная инфузия AVXS-201 отличным от человека приматам не влияет на гематологические показатели на протяжении 18 месяцев после инъекции. Значения для трех животных, обработанных посредством AVXS-201, показаны красным цветом, а для контрольных субъектов показаны синим цветом.
[0030] Фигура 16. Интратекальная инфузия AVXS-201 отличным от человека приматам не влияет на биохимические показатели сыворотки на протяжении 12-18 месяцев после инъекции. Печеночные пробы и концентрации электролитов аналогичны у субъектов, обработанными посредством AVXS-201 и контроля. Значения для трех животных, обработанных посредством AVXS-201, показаны красным цветом, а для контрольных субъектов показаны синим цветом.
[0031] Фигура 17. Интратекальная инфузия AVXS-201 отличным от человека приматам не влияет на биохимические показатели сыворотки на протяжении 12-18 месяцев после инъекции. Сердечные и почечные пробы аналогичны у субъектов, обработанных посредством AVXS-201 и контроля. Значения для трех животных, обработанных посредством AVXS-201, показаны красным цветом, а для контрольных субъектов показаны синим цветом.
[0032] Фигура 18. Аналогичные уровни экспрессии MeCP2 во всех участках головного мозга отличных от человека приматов, обработанных посредством AVXS-201 и контроля. Иммуногистохимический анализ с применением антител к MeCP2 не выявил макроскопических аномалий структуры или очевидных отличий в экспрессии MeCP2. OC=затылочная кора, TC=височная кора, LSc=поясничный отдел спинного мозга, Thal=таламус, Hipp=гиппокамп, Cb=мозжечок.
[0033] Фигура 19. Вестерн-блоты областей головного мозга животных, которым вводили инъекцией контроль и AVXS-201, демонстрируют аналогичные уровни MeCP2. Уровни общего MeCP2 показаны зеленым цветом, а контроли загрузки с GAPDH показаны красным цветом. Количественные оценки панелей A и B показаны под их соответствующими блотами. Пунктирными линиями на графиках показаны средние нормализованные значения, обнаруженные у контролей. OC=затылочная кора, TC=височная кора, LSc=поясничный отдел спинного мозга, Thal=таламус, Hipp=гиппокамп, Cb=мозжечок. Значения показаны как среднее ± SEM.
[0034] Фигура 20. In situ гибридизация демонстрирует транскрипт, полученный за счет вектора, во всех исследованных областях головного мозга у животных, обработанных посредством AVXS-201, но не у контрольных животных. На фигуре показаны зонды к Gapdh (красный) и мРНК MECP2, полученная на основе вектора (зеленый), а также мечение ядер (Dapi, синий). OC=затылочная кора, TC=височная кора, LSc=поясничный отдел спинного мозга, Hipp=гиппокамп, Cb=мозжечок. Масштабные полоски=20 мкм.
[0035] Фигура 21. In situ гибридизация демонстрирует транскрипт, полученный за счет вектора, во всех исследованных областях головного мозга у животных, обработанных посредством AVXS-201, но не у контрольных животных через 18 месяцев после инъекции. На фигуре показаны зонды к Gapdh (красный) и мРНК MECP2, полученная на основе вектора (зеленый), а также мечение ядер (Dapi, синий). OC=затылочная кора, TC=височная кора, CA1 и CA3=области гиппокампа, CC=мозолистое тело, Thal=таламус, Cau=хвостатое ядро, Put=скорлупа, SColl=верхнее двухолмие, Med=продолговатый мозг, Cb=мозжечок, Cerv=шейный отдел спинного мозга, Thor=грудной отдел спинного мозга, Lumb=поясничный отдел спинного мозга. Масштабные полоски=20 мкм
Подробное описание
[0036] В одном аспекте настоящего изобретения предусмотрены способы интратекального введения (т. е. введения в пространство под паутинной оболочкой головного или спинного мозга) полинуклеотида, кодирующего MECP2, пациенту, предусматривающие введение rAAV9 с геномом, содержащим полинуклеотид. В некоторых вариантах осуществления геном rAAV9 представляет собой самокомплементарный геном. В других вариантах осуществления геном rAAV9 представляет собой однонитевой геном.
[0037] С помощью способов полинуклеотид, кодирующий MECP2, доставляется в головной и спинной мозг пациента (т. е. в центральную нервную систему пациента). Некоторые целевые области головного мозга, в которые предусмотрена доставка, охватывают без ограничения двигательную зону коры головного мозга и ствол головного мозга. Некоторые целевые клетки центральной нервной системы, в которые предусмотрена доставка, охватывают без ограничения нервные клетки и клетки глии. Примерами клеток глии являются клетки микроглии, олигодендроциты и астроциты.
[0038] Доставка полинуклеотидов, кодирующих MECP2, например, показана при лечении синдрома Ретта.
[0039] "Лечение" предусматривает стадию введения интратекальным путем эффективной дозы или многократных эффективных доз композиции, содержащей rAAV по настоящему изобретению, субъекту-животному (в том числе пациенту-человеку), нуждающемуся в этом. Если дозу вводят до развития нарушения/заболевания, то введение является профилактическим. Если дозу вводят после развития нарушения/заболевания, то введение является терапевтическим. В вариантах осуществления настоящего изобретения эффективная доза представляет собой дозу, которая облегчает (либо устраняет, либо уменьшает) по меньшей мере один симптом, сопряженный с нарушением/болезненным состоянием, подлежащими лечению, ослабляет по меньшей мере один симптом, сопряженный с нарушением/болезненным состоянием, подлежащими лечению, которая замедляет или предупреждает прогрессирование нарушения/болезненного состояния, которая снижает стадию заболевания, которая приводит к ремиссии (частичной или полной) заболевания и/или которая продлевает выживание.
[0040] В случае лечения синдрома Ретта способы приводят к эффекту, включающему без ограничения восстановление целенаправленных движений рук, улучшение речи, уменьшение апноэ, уменьшение судорог, уменьшение тревоги, увеличенную социализацию, повышение IQ, нормализацию характера сна и/или увеличенную подвижность субъекта.
[0041] Также в настоящем изобретении предусмотрены комбинированные варианты лечения. Используемая в данном документе комбинация охватывает как одновременное лечение, так и последовательное лечение. В частности, предусмотрены комбинации способов по настоящему изобретению со стандартным медикаментозным лечением синдрома Ретта, а также комбинации с новыми средствами терапии.
[0042] Хотя предусмотрена доставка индивидууму, нуждающемуся в этом, после рождения, также предусмотрена внутриутробная доставка плоду.
[0043] В другом аспекте настоящего изобретения предусмотрены геномы rAAV. Геномы rAAV содержат один или несколько ITR AAV, фланкирующих полинуклеотид, кодирующий MECP2. Полинуклеотид функционально связан с ДНК транскрипционного контроля, в частности, ДНК промотора и ДНК сигнальной последовательности полиаденилирования, которые являются функциональными в целевых клетках, с образованием "генной кассеты". Генная кассета может содержать промоторы, которые обеспечивают специфическую экспрессию в нейронах или специфическую экспрессию в клетках глии. Примеры охватывают промотор гена нейрон-специфической енолазы и промотор генов фибриллярных кислых белков глии. Также можно применять промоторы, индуцируемые под контролем принимаемого внутрь лекарственного средства. Примеры охватывают без ограничения такие системы, как тетрациклиновая (TET on/off) система [Urlinger et al., Proc. Natl. Acad. Sci. USA 97(14):7963-7968 (2000)] и система, регулируемая экдизоновым рецептором [Palli et al., Eur J. Biochem 270: 1308-1315 (2003]. Генная кассета может дополнительно включать интронные последовательности для облегчения процессинга РНК-транскрипта, когда полинуклеотид экспрессируется в клетках млекопитающих.
[0044] Геномы rAAV по настоящему изобретению не содержат ДНК rep и cap AAV. ДНК AAV в геномах rAAV (например, ITR) может быть получена от любого серотипа AAV, из которого может происходить рекомбинантный вирус, включая без ограничения такие серотипы AAV: AAV1, AAV2, AAV3, AAV4, AAV5, AAV6, AAV7, AAV8, AAV9, AAV10, AAV11, AAV12, AAV13 и AAVrh74. Нуклеотидные последовательности геномов серотипов AAV известны из уровня техники. Например, геном AAV9 приведен в Gao et al., J. Virol., 78: 6381-6388 (2004).
[0045] В другом аспекте настоящего изобретения предусмотрены ДНК-плазмиды, содержащие геномы rAAV по настоящему изобретению. ДНК-плазмиды переносятся в клетки, восприимчивые к инфицированию, с вирусом-помощником AAV (например, аденовирусом, аденовирусом с делецией E1 или герпесвирусом) для сборки генома rAAV в инфекционные вирусные частицы с капсидными белками AAV9. Методики продуцирования частиц rAAV, при которых подлежащий упаковке геном AAV, гены rep и cap и функциональные элементы вируса-помощника обеспечиваются в клетке, являются стандартными в данной области техники. Для продуцирования rAAV необходимо, чтобы в пределах одной клетки (обозначаемой в данном документе как упаковывающая клетка) присутствовали следующие компоненты: геном rAAV, гены rep и cap AAV, отделенные от генома rAAV (т. е. не находящиеся в нем), и функциональные элементы вируса-помощника. Продуцирование псевдотипированного rAAV, например, раскрыто в WO 01/83692, которая включена в данный документ посредством ссылки во всей своей полноте. В различных вариантах осуществления капсидные белки AAV могут быть модифицированы для улучшения доставки рекомбинантного вектора. Модификации, вводимые в капсидные белки, в целом известны из уровня техники. См., например, US 2005/0053922 и US 2009/0202490, раскрытия которых включены в данный документ посредством ссылки во всей своей полноте.
[0046] Способ получения упаковывающей клетки заключается в создании клеточной линии, которая стабильно экспрессирует все необходимые компоненты для продуцирования частиц AAV. Например, в геном клетки встроены плазмида (или несколько плазмид), содержащие геном rAAV без генов rep и cap AAV, гены rep и cap AAV, отделенные от генома rAAV, и селектируемый маркер, такой как ген устойчивости к неомицину. Геномы AAV были введены в бактериальные плазмиды с помощью таких процедур, как GC-наращивание (Samulski et al., 1982, Proc. Natl. Acad. S6. USA, 79:2077-2081), добавление синтетических линкеров, содержащих сайты расщепления рестрикционной эндонуклеазой (Laughlin et al., 1983, Gene, 23:65-73), или путем прямого лигирования тупых концов (Senapathy & Carter, 1984, J. Biol. Chem., 259:4661-4666). Затем линию упаковывающих клеток инфицируют вирусом-помощником, таким как аденовирус. Преимущества этого способа заключаются в том, что клетки можно подвергать отбору, и они подходят для крупномасштабного продуцирования rAAV. В других примерах подходящих способов вместо плазмид используют аденовирус или бакуловирус для введения в упаковывающие клетки геномов rAAV и/или генов rep и cap.
[0047] Обзор общих принципов продуцирования rAAV изложен, например, в Carter, 1992, Current Opinions in Biotechnology, 1533-539; и Muzyczka, 1992, Curr. Topics in Microbial. and Immunol., 158:97-129). Различные подходы описаны в Ratschin et al., Mol. Cell. Biol. 4:2072 (1984); Hermonat et al., Proc. Natl. Acad. Sci. USA, 81:6466 (1984); Tratschin et al., Mol. Cell. Biol. 5:3251 (1985); McLaughlin et al., J. Virol., 62:1963 (1988); и Lebkowski et al., 1988 Mol. Cell. Biol., 7:349 (1988). Samulski et al. (1989, J. Virol., 63:3822-3828); патенте США № 5173414; WO 95/13365 и соответствующем патенте США № 5658776; WO 95/13392; WO 96/17947; PCT/US98/18600; WO 97/09441 (PCT/US96/14423); WO 97/08298 (PCT/US96/13872); WO 97/21825 (PCT/US96/20777); WO 97/06243 (PCT/FR96/01064); WO 99/11764; Perrin et al. (1995) Vaccine 13:1244-1250; Paul et al. (1993) Human Gene Therapy 4:609-615; Clark et al. (1996) Gene Therapy 3:1124-1132; патенте США № 5786211; патенте США № 5871982 и патенте США № 6258595. Вышеперечисленные документы настоящим включены в данный документ посредством ссылки во всей своей полноте, при этом особый акцент делается на те разделы документов, которые относятся к продуцированию rAAV.
[0048] Таким образом, в настоящем изобретении предусмотрены упаковывающие клетки, которые продуцируют дефектный по репликации инфекционный rAAV. В одном варианте осуществления упаковывающие клетки могут представлять собой стабильно трансформированные раковые клетки, такие как клетки HeLa, клетки 293 и клетки PerC.6 (линия, родственная линии 293). В другом варианте осуществления упаковывающие клетки представляют собой клетки, которые не являются трансформированными раковыми клетками, такие как клетки 293 с малым числом пассажей (человеческие эмбриональные клетки почки эмбриона человека, трансформированные с помощью E1 аденовируса), клетки MRC-5 (фибробласты эмбриона человека), клетки WI-38 (фибробласты эмбриона человека), клетки Vero (клетки почки обезьяны) и клетки FRhL-2 (клетки легкого эмбриона макака-резуса).
[0049] Таким образом, в другом аспекте настоящего изобретения предусмотрен rAAV, такой как rAAV9 (т. е. дефектные по репликации инфекционные капсидированные частицы rAAV9), содержащий геном rAAV по настоящему изобретению. Геномы rAAV не содержат ДНК rep и cap AAV, то есть между ITR геномов отсутствует ДНК rep или cap AAV. В некоторых вариантах осуществления геном rAAV представляет собой самокомплементарный геном. В некоторых вариантах осуществления геном rAAV представляет собой однонитевой геном.
[0050] Предусмотрены такие rAAV, как самокомплементарный AAV9 (scAAV9) под названием "AVXS-201". Его генная кассета (нуклеотиды 151-2558 генома AVXS-201, изложенные под SEQ ID NO:1) содержит последовательно: промоторный фрагмент длиной 546 п. о. (SEQ ID NO:2) (нуклеотиды 74085586-74086323 из NC_000086.7 в обратной ориентации) из гена MECP2 мыши, интрон SV40, кДНК MECP2B человека (SEQ ID NO:3) (№ CCDS48193.1 в базе данных CCDS) и синтетическую последовательность сигнала полиаденилирования (SEQ ID NO:4). Генная кассета фланкирована мутантным инвертированным концевым повтором (ITR) AAV2 и инвертированным концевым повтором AAV2 дикого типа, которые совместно делают возможной упаковку самокомплементарных геномов AAV. Геном не содержит ДНК rep и cap AAV, то есть между ITR генома отсутствует ДНК rep или cap AAV.
[0051] Предусмотрены такие rAAV, как scAAV9 под названием "scAAV9.738.Mecp2ʺ. Его генная кассета (нуклеотиды 198-2890 генома scAAV9.738.Mecp2, изложенные под SEQ ID NO:5) содержит последовательно: промоторный фрагмент длиной 738 п. о. (SEQ ID NO:6) (нуклеотиды 74085586-74086323 из NC_000086.7 в обратной ориентации) из гена MECP2 мыши, интрон SV40, кДНК MECP2α мыши (SEQ ID NO:7) (№ CCDS41016.1 в базе данных CCDS) и последовательность сигнала полиаденилирования из гена бычьего гормона роста. Генная кассета фланкирована мутантным инвертированным концевым повтором (ITR) AAV2 и инвертированным концевым повтором AAV2 дикого типа, которые совместно делают возможной упаковку самокомплементарных геномов AAV. Геном не содержит ДНК rep и cap AAV, то есть между ITR генома отсутствует ДНК rep или cap AAV.
[0052] Консервативные нуклеотидные замены в геноме rAAV9 предусмотрены, в том числе без ограничения, в генной кассете генома rAAV9. Например, кДНК MECP2 в генной кассете может характеризоваться 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичностью последовательности с кДНК MECP2α в scAAV9.738.Mecp2 или кДНК MECP2B в AVXS-201.
[0053] В некоторых вариантах осуществления полипептид MECP2, кодируемый rAAV9 по настоящему изобретению, может представлять собой вариант полипептида MECP2. Вариант полипептида сохраняет активность MECP2 и имеет аминокислотную последовательность, которая на по меньшей мере приблизительно 60, 70, 80, 85, 90, 95, 97, 98, 99 или 99,5% идентична аминокислотной последовательности полипептида MECP2, кодируемого кДНК MECP2α в scAAV9.738.Mecp2 или кДНК MECP2B в AVXS-201.
[0054] rAAV можно очищать с помощью способов, стандартных в данной области техники, таких как колоночная хроматография или применение градиентов хлорида цезия. Способы очистки векторов rAAV от вируса-помощника известны из уровня техники и включают способы, раскрытые, например, в Clark et al., Hum. Gene Ther., 10(6): 1031-1039 (1999); Schenpp and Clark, Methods Mol. Med., 69: 427-443 (2002); патенте США № 6566118 и WO 98/09657.
[0055] В другом аспекте настоящего изобретения предусмотрены композиции, содержащие rAAV, такой как rAAV9, кодирующий полипептид MECP2.
[0056] Композиции по настоящему изобретению содержат rAAV в фармацевтически приемлемом носителе. Композиции также могут содержать другие ингредиенты, такие как разбавители и вспомогательные средства. Приемлемые носители, разбавители и вспомогательные средства не оказывают токсического действия на пациентов, принимающих их, а также предпочтительно инертны при используемых дозировках и концентрациях и охватывают буферы, такие как фосфатный, цитратный или на основе других органических кислот; антиоксиданты, такие как аскорбиновая кислота; низкомолекулярные полипептиды; белки, такие как сывороточный альбумин, желатин или иммуноглобулины; гидрофильные полимеры, такие как поливинилпирролидон; аминокислоты, такие как глицин, глутамин, аспарагин, аргинин или лизин; моносахариды, дисахариды и другие углеводы, в том числе глюкозу, маннозу или декстрины; хелатообразующие средства, такие как EDTA; сахароспирты, такие как маннит или сорбит; солеобразующие противоионы, такие как натрий; и/или неионное поверхностно-активные вещества, такие как Tween, плюроники или полиэтиленгликоль (PEG).
[0057] Стерильные инъекционные растворы готовят посредством включения rAAV в требуемом количестве в подходящий растворитель с различными другими ингредиентами, перечисленными выше, если потребуется, с последующей стерилизацией фильтрацией. Как правило, дисперсии получают путем включения простерилизованного активного ингредиента в стерильную среду-носитель, которая содержит основную дисперсионную среду и другие требуемые ингредиенты из перечисляемых выше. В случае стерильных порошков для приготовления стерильных инъекционных растворов предпочтительными способами получения являются вакуумная сушка и методика лиофилизации, которые дают порошок активного ингредиента с любым дополнительным требуемым ингредиентом из их предварительного стерилизованного фильтрацией раствора.
[0058] Титры и дозировки rAAV, подлежащие введению в способах по настоящему изобретению, будут варьироваться в зависимости, например, от конкретного rAAV, способа введения, цели лечения, индивидуума, времени введения и типа(типов) клеток, на которые оказывают целенаправленное воздействие, и их можно определить способами, стандартными для данной области техники. Титры могут находиться в диапазоне от приблизительно 1×106, приблизительно 1×107, приблизительно 1×108, приблизительно 1×109, приблизительно 1×1010, приблизительно 1×1011, приблизительно 1×1012, приблизительно 1×1013 до приблизительно 1×1014 или более устойчивых к ДНКазам частиц (DRP) на мл. Дозировки также могут быть выражены в единицах вирусных геномов (vg). Такие дозировки rAAV могут находиться в диапазоне от приблизительно 1×109 vg или более, приблизительно 1×1010 vg или более, приблизительно 1×1011 vg или более, приблизительно 1×1012 vg или более, приблизительно 6×1012 или более, приблизительно 1×1013 vg или более, приблизительно 1,3×1013 vg или более, приблизительно 1,4×1013 vg или более, приблизительно 2×1013 vg или более, приблизительно 3×1013 vg или более, приблизительно 6×1013 vg или более, приблизительно 1×1014 vg или более, приблизительно 3×1014 или более, приблизительно 6×1014 или более, приблизительно 1×1015 vg или более, приблизительно 3×1015 или более, приблизительно 6×1015 или более, приблизительно 1×1016 или более, приблизительно 3×1016 или более или приблизительно 6×1016 или более. В случае новорожденного дозировки rAAV могут находиться в диапазоне от приблизительно 1×109 vg или более, приблизительно 1×1010 vg или более, приблизительно 1×1011 vg или более, приблизительно 1×1012 vg или более, приблизительно 6×1012 или более, приблизительно 1×1013 vg или более, приблизительно 1,3×1013 vg или более, приблизительно 1,4×1013 vg или более, приблизительно 2×1013 vg или более, приблизительно 3×1013 vg или более, приблизительно 6×1013 vg или более, приблизительно 1×1014 vg или более, приблизительно 3×1014 или более, приблизительно 6×1014 или более, приблизительно 1×1015 vg или более, приблизительно 3×1015 или более, приблизительно 6×1015 или более, приблизительно 1×1016 или более, приблизительно 3×1016 или более или приблизительно 6×1016 или более.
[0059] Способы по настоящему изобретению приводят к трансдукции целевых клеток (включая без ограничения нервные клетки или клетки глии). Термин "трансдукцияʺ используют для обозначения либо in vivo, либо in vitro введения/доставки полинуклеотида в целевую клетку с помощью дефектного по репликации инфекционного rAAV по настоящему изобретению, что приводит к экспрессии в реципиентной клетке функционального полипептида MECP2.
[0060] Трансдукция клеток с применением rAAV по настоящему изобретению приводит к устойчивой экспрессии полипептида MECP2, кодируемого rAAV. В некоторых вариантах осуществления предусмотрен целевой уровень экспрессии, составляющий от приблизительно 75% до приблизительно 125% от нормального (или дикого типа) физиологического уровня экспрессии у субъекта, у которого отсутствует синдром Ретта. Целевой уровень экспрессии может составлять приблизительно 75%, приблизительно 80%, приблизительно 85%, приблизительно 90%, приблизительно 95%, приблизительно 100%, приблизительно 105%, приблизительно 110%, приблизительно 115%, приблизительно 120% или приблизительно 125% от нормального уровня экспрессии.
[0061] В некоторых вариантах осуществления способов лечения по настоящему изобретению пациенту также вводят неионное низкоосмолярное контрастное средство. Такие контрастные средства охватывают без ограничения йобитридол, йогексол, йомепрол, йопамидол, йопентол, йопромид, йоверсол, йоксилан и смеси из двух или более контрастных средств. Таким образом, в некоторых вариантах осуществления способы лечения дополнительно предусматривают введение пациенту йогексола. Неионное низкоосмолярное контрастное средство предусмотрено для увеличения трансдукции целевых клеток в центральной нервной системе пациента. Предусматривается, что трансдукция клеток увеличивается, когда rAAV по настоящему изобретению применяют в комбинации с контрастным средством, описываемым в данном документе, по сравнению с трансдукцией клеток, когда rAAV по настоящему изобретению применяют отдельно. В различных вариантах осуществления трансдукция клеток увеличивается на по меньшей мере приблизительно 1% или по меньшей мере приблизительно 5%, по меньшей мере приблизительно 10%, по меньшей мере приблизительно 20%, по меньшей мере приблизительно 30%, по меньшей мере приблизительно 40%, по меньшей мере приблизительно 50%, по меньшей мере приблизительно 60%, по меньшей мере приблизительно 70%, по меньшей мере приблизительно 80%, по меньшей мере приблизительно 90%, по меньшей мере приблизительно 100%, по меньшей мере приблизительно 120%, по меньшей мере приблизительно 150%, по меньшей мере приблизительно 180%, по меньшей мере приблизительно 200%, по меньшей мере приблизительно 250%, по меньшей мере приблизительно 300%, по меньшей мере приблизительно 350%, по меньшей мере приблизительно 400%, по меньшей мере приблизительно 450%, по меньшей мере приблизительно 500% или более, когда вектор по настоящему изобретению применяют в комбинации с контрастным средством, описываемым в данном документе, по сравнению с трансдукцией вектора по настоящему изобретению, когда его применяют не в комбинации с контрастным средством. В дополнительных вариантах осуществления трансдукция клеток увеличивается на величину, составляющую от приблизительно 10% до приблизительно 50%, или от приблизительно 10% до приблизительно 100%, или от приблизительно 5% до приблизительно 10%, или от приблизительно 5% до приблизительно 50%, или от приблизительно 1% до приблизительно 500%, или от приблизительно 10% до приблизительно 200%, или от приблизительно 10% до приблизительно 300%, или от приблизительно 10% до приблизительно 400%, или от приблизительно 100% до приблизительно 500%, или от приблизительно 150% до приблизительно 300%, или от приблизительно 200% до приблизительно 500%, когда вектор по настоящему изобретению применяют в комбинации с контрастным средством, описываемым в данном документе, по сравнению с трансдукцией вектора по настоящему изобретению, когда его применяют не в комбинации с контрастным средством.
[0062] В некоторых вариантах осуществления предусматривается, что трансдукция клеток увеличивается, когда пациента переводят в положение Тренделенбурга (положение головой вниз). В некоторых вариантах осуществления, например, пациента наклоняют в положение головой вниз на угол, составляющий от приблизительно 1 градуса до приблизительно 30 градусов, от приблизительно 15 до приблизительно 30 градусов, от приблизительно 30 до приблизительно 60 градусов, от приблизительно 60 до приблизительно 90 градусов или от приблизительно 90 до приблизительно 180 градусов) во время интратекальной инфузии вектора или после нее. В различных вариантах осуществления трансдукция увеличивается на по меньшей мере приблизительно 1% или по меньшей мере приблизительно 5%, по меньшей мере приблизительно 10%, по меньшей мере приблизительно 20%, по меньшей мере приблизительно 30%, по меньшей мере приблизительно 40%, по меньшей мере приблизительно 50%, по меньшей мере приблизительно 60%, по меньшей мере приблизительно 70%, по меньшей мере приблизительно 80%, по меньшей мере приблизительно 90%, по меньшей мере приблизительно 100%, по меньшей мере приблизительно 120%, по меньшей мере приблизительно 150%, по меньшей мере приблизительно 180%, по меньшей мере приблизительно 200%, по меньшей мере приблизительно 250%, по меньшей мере приблизительно 300%, по меньшей мере приблизительно 350%, по меньшей мере приблизительно 400%, по меньшей мере приблизительно 450%, по меньшей мере приблизительно 500% или более, когда применяют положение Тренделенбурга, описываемое в данном документе, по сравнению с ситуацией, когда положения Тренделенбурга не применяют.
[0063] В дополнительных вариантах осуществления трансдукция клеток увеличивается на величину, составляющую от приблизительно 10% до приблизительно 50%, или от приблизительно 10% до приблизительно 100%, или от приблизительно 5% до приблизительно 10%, или от приблизительно 5% до приблизительно 50%, или от приблизительно 1% до приблизительно 500%, или от приблизительно 10% до приблизительно 200%, или от приблизительно 10% до приблизительно 300%, или от приблизительно 10% до приблизительно 400%, или от приблизительно 100% до приблизительно 500%, или от приблизительно 150% до приблизительно 300%, или от приблизительно 200% до приблизительно 500%, когда вектор по настоящему изобретению применяют в комбинации с контрастным средством и положением Тренделенбурга, описываемыми в данном документе, по сравнению с трансдукцией вектора по настоящему изобретению, когда его применяют не в комбинации с контрастным средством и положением Тренделенбурга.
[0064] В настоящем изобретении также предусмотрены варианты осуществления способа лечения, где интратекальное введение вектора по настоящему изобретению и контрастного средства в центральную нервную систему пациента, нуждающегося в этом, приводит к увеличению выживания пациента по сравнению с выживанием пациента, когда вектор по изобретению вводят в отсутствие контрастного средства. В различных вариантах осуществления введение вектора по настоящему изобретению и контрастного средства в центральную нервную систему пациента, нуждающегося в этом, приводит к увеличению выживания пациента на по меньшей мере приблизительно 1%, по меньшей мере приблизительно 5%, по меньшей мере приблизительно 10%, по меньшей мере приблизительно 20%, по меньшей мере приблизительно 30%, по меньшей мере приблизительно 40%, по меньшей мере приблизительно 50%, по меньшей мере приблизительно 60%, по меньшей мере приблизительно 70%, по меньшей мере приблизительно 80%, по меньшей мере приблизительно 90%, по меньшей мере приблизительно 100%, по меньшей мере приблизительно 150%, по меньшей мере приблизительно 200% или более по сравнению с выживанием пациента, когда вектор по настоящему изобретению вводят в отсутствие контрастного средства.
[0065] В настоящем изобретении также предусмотрены варианты осуществления способа лечения, где интратекальное введение вектора по настоящему изобретению и контрастного средства в центральную нервную систему пациента, нуждающегося в этом, который приведен в положение Тренделенбурга, приводит к дополнительному увеличению выживания пациента по сравнению с выживанием пациента, когда вектор по настоящему изобретению вводят в отсутствие контрастного средства и положения Тренделенбурга. В различных вариантах осуществления введение вектора по настоящему изобретению и контрастного средства в центральную нервную систему пациента, нуждающегося в этом, который приведен в положение Тренделенбурга, приводит к увеличению выживания пациента на по меньшей мере приблизительно 1%, по меньшей мере приблизительно 5%, по меньшей мере приблизительно 10%, по меньшей мере приблизительно 20%, по меньшей мере приблизительно 30%, по меньшей мере приблизительно 40%, по меньшей мере приблизительно 50%, по меньшей мере приблизительно 60%, по меньшей мере приблизительно 70%, по меньшей мере приблизительно 80%, по меньшей мере приблизительно 90%, по меньшей мере приблизительно 100%, по меньшей мере приблизительно 150%, по меньшей мере приблизительно 200% или более по сравнению с выживанием пациента, когда вектор по настоящему изобретению вводят в отсутствие контрастного средства и положения Тренделенбурга.
Примеры
[0066] Настоящее изобретение проиллюстрировано с помощью нижеприведенного.
Исследования для подтверждения механизма на модельных животных, представляющих собой самок и самцов мышей с синдромом Ретта, демонстрируют терапевтическую эффективность после внутривенного введения scAAV9.738.Mecp2 (пример 1).
Для вектора генной терапии второго поколения, AVXS-201, продемонстрировано увеличение выживания в широком диапазоне доз после интрацеребровентрикулярной (ICV) обработки Mecp2-/y мышей. Максимальное увеличение медианного выживания составляло 477% после обработки посредством AVXS-201 (пример 2).
Самцы Mecp2-/y мышей, обработанные с помощью AVXS-201, демонстрировали стойкое улучшение поведения, как измерено с помощью обобщенной оценки, разработанной для мышей с синдромом Ретта (пример 3).
Фенотипическое преимущество у Mecp2-/y мышей, обработанных с помощью AVXS-201, получают при умеренных уровнях экспрессии белка (пример 4).
Обработка мышей дикого типа с помощью AVXS-201 хорошо переносилась при всех протестированных дозах, что согласуется с тем, что изменения в поведенческих баллах отмечались только в группе с высокими дозами (пример 5 и пример 6).
Интратекальное введение дозы отличным от человека приматам свидетельствует о том, что AVXS-201 является безопасным и хорошо переносится на протяжении 18 месяцев после инъекции (пример 7).
AVXS-201 приводит к широкой экспрессии трансгена на физиологических уровнях в головном и спинном мозге отличных от человека приматов после однократной интратекальной инъекции (пример 8).
Пример 1
Исследование для подтверждения механизма генной терапии синдрома Ретта на самках мышей с синдромом Ретта
[0067] В качестве исследования для подтверждения механизма самцов и самок мышей с симптомами синдрома Ретта обрабатывали посредством внутривенного введения scAAV9.738.Mecp2 [Garg et al., The Journal of Neuroscience: The Official Journal of the Society for Neuroscience, 33: 13612-13620 (2013)]. Рекомбинантный вирусный геном scAAV9.738.Mecp2 (SEQ ID NO:5) содержит промоторный фрагмент длиной 738 п. о. из гена Mecp2 мыши [Adachi et al., Human Molecular Genetics, 14: 3709-3722 (2005)], управляющий экспрессией кДНК Mecp2α мыши (№ CCDS41016.1 в базе данных CCDS), и сигнал полиаденилирования бычьего гормона роста. Генная кассета (нуклеотиды 198-2890 из SEQ ID NO:5) фланкирована мутантным инвертированным концевым повтором (ITR) AAV2 и ITR дикого типа AAV2, которые делают возможной упаковку самокомплементарных геномов AAV.
[0068] Самокомплементарный AAV9 (scAAV9) получали посредством процедур временной трансфекции с применением двухнитевого вектора на основе ITR AAV2 с плазмидой, кодирующей последовательность Rep2Cap9, как описано ранее [Gao et al., J. Virol., 78: 6381-6388 (2004)], совместно с аденовирусной плазмидой-помощником pHelper (Stratagene, Санта-Клара, Калифорния) в клетках 293. Для проведения экспериментов вирус получали тремя отдельными партиями и очищали с помощью двух стадий очистки в градиенте плотности хлорида цезия, диализировали против PBS, и составляли в смесь с 0,001% Pluronic-F68 для предупреждения агрегации вируса, и хранили при 4°C. У всех векторных препаратов определяли титр с помощью количественной ПЦР с применением технологии Taq-Man. Чистоту векторов оценивали с помощью электрофореза в акриламидном геле с добавлением 4-12% додецилсульфата натрия и окрашивания серебром (Invitrogen, Карлсбад, Калифорния).
[0069] Самцов мышей с нулевым аллелем Mecp2 обрабатывали внутривенной инъекцией, содержащей 3×1012 vg либо scAAV9.738.Mecp2, либо контрольного вектора scAAV9, в возрасте 4-6 недель. За животными наблюдали в отношении выживания и еженедельно оценивали в отношении фенотипического балла [Guy et al., Science, 315: 1143-1147 (2007)].
Компоненты фенотипической оценки из публикации Guy et al. 2007.
A. Подвижность. За мышью наблюдают при помещении ее на стол, а затем при осторожном прикосновении к ней рукой. 0=как у мыши дикого типа. 1=уменьшенное движение по сравнению с мышью дикого типа: увеличенный период замирания при первом помещении на стол и более длительные периоды, проводимые в неподвижном состоянии. 2=отсутствует самопроизвольное передвижение при помещении на стол; мышь может двигаться в ответ на нежное подталкивание или при помещении неподалеку гранулы корма. (Примечание: мыши могут стать более активными, когда находятся в условиях своей собственной клетки).
B. Походка. 0=как у мыши дикого типа. 1=при ходьбе или беге задние конечности раздвинуты шире, чем у мыши дикого типа, при этом уменьшено поднятие таза, что приводит к "ковыляющейʺ походке. 2=более серьезные аномалии: тремор при поднятии ног, ходьба назад или походка 'прыгающего кролика' за счет одновременного поднятия обеих задних ног.
C. Поджатие задних конечностей. За мышью наблюдают, когда она находится в подвешенном состоянии и ее удерживают за основание хвоста. 0=ноги раскинуты наружу. 1=задние конечности приближены друг к другу (без соприкосновения), или одна нога приближена к туловищу. 2=обе ноги сильно сокращены, либо касаются друг друга, либо касаются туловища.
D. Тремор. За мышью наблюдают, когда она стоит на уплощенной ладони руки. 0=тремор отсутствует. 1=прерывистый легкий тремор. 2*=постоянный тремор или прерывистый сильный тремор
E. Дыхание. Наблюдают за движением боков, когда животное стоит на месте. 0=нормальное дыхание. 1=периоды регулярного дыхания, чередующиеся с короткими периодами более частого дыхания или с паузами в дыхании. 2*=очень нерегулярное дыхание - одышка или гиперпноэ.
F. Общее состояние. У мышей определяют показатели общего самочувствия, такие как состояние шерсти, глаза, положение тела. 0=чистая блестящая шерсть, чистые глаза, нормальное положение. 1=глаза тусклые, шерсть тусклая/неухоженная, несколько сгорбленное положение. 2*=глаза покрыты корками или сужены, пилоэрекция, сгорбленная поза.
[0070] На фигуре 4 показано, что группа, обработанная посредством scAAV9.738.Mecp2, не достигла медианного выживания в период проведения эксперимента на момент публикации, но превосходила животных, обработанных контролем, более чем на 10 недель. Животные, обработанные посредством scAAV9.738.Mecp2, также характеризовались более низким поведенческим баллом по сравнению с животными, обработанными контролем. Эксперимент повторяли с пораженными самками мышей (фигура 5). Животных обрабатывали IV введением либо scAAV9.738.Mecp2, либо контроля, как перед этим поступали с самцами. Самок обрабатывали в возрасте 10-12 месяцев, когда у мышей с синдромом Ретта появлялись симптомы. За животными наблюдали в течение примерно 6 месяцев после инъекции и тестировали в отношении их фенотипического балла. Важно отметить, что для самок мышей с синдромом Ретта не характерна ранняя смертность, как в случае самцов с более тяжелым проявлением синдрома [Guy et al., Nature Genetics, 27: 322-326 (2001)]. Обработка посредством scAAV9.738.Mecp2 останавливала прогрессирование заболевания, и было показано снижение тяжести заболевания, при этом баллы уменьшались почти до 1. Это составляло резкий контраст с животными, обработанными контролем, которые закончили эксперимент с фенотипическими баллами примерно 6, что указывало на ухудшение симптомов (фигура 5C). Все данные, полученные на вращающемся барабане, в тесте "перевернутая сетка", тесте на платформе, а также на основе способности к устройству гнезда, подтверждали улучшение поведения у животных, обработанных посредством scAAV9.738.Mecp2, по сравнению с животными, обработанными контролем. Посмертный анализ головного мозга от самок, обработанных посредством scAAV9.738.Mecp2, показал, что показатели интенсивности флуоресценции при экспрессии MECP2 были идентичны таковым в головном мозге мышей дикого типа, что свидетельствовало о том, что экспрессия трансгена, вводимого в качестве генной терапии, была на примерно физиологических уровнях.
Пример 2
Доклинические исследования эффективности AVXS-201
[0071] Для повышения эффективности упаковки и для включения кДНК MECP2 человека, важной с клинической точки зрения, при сохранении физиологических уровней генной экспрессии повторно конструировали scAAV9.738.Mecp2 с более коротким промотором, кДНК MECP2B человека и синтетическим сигналом полиаденилирования. Повторно сконструированный геном упаковывался в капсиды AAV9, как описано ниже, и полученный scAAV затем получил название "AVXS-201ʺ (фигура 6). AVXS-201 изначально назывался "AAV9-P545-MeCP2''.
Последовательность промоторной области (промоторный фрагмент гена MeCP2 мыши) (SEQ ID NO:2)
GTGAACAACGCCAGGCTCCTCAACAGGCAACTTTGCTACTTCTACAGAAAATGATAATAAAGAAATGCTGGTGAAGTCAAATGCTTATCACAATGGTGAACTACTCAGCAGGGAGGCTCTAATAGGCGCCAAGAGCCTAGACTTCCTTAAGCGCCAGAGTCCACAAGGGCCCAGTTAATCCTCAACATTCAAATGCTGCCCACAAAACCAGCCCCTCTGTGCCCTAGCCGCCTCTTTTTTCCAAGTGACAGTAGAACTCCACCAATCCGCAGCTGAATGGGGTCCGCCTCTTTTCCCTGCCTAAACAGACAGGAACTCCTGCCAATTGAGGGCGTCACCGCTAAGGCTCCGCCCCAGCCTGGGCTCCACAACCAATGAAGGGTAATCTCGACAAAGAGCAAGGGGTGGGGCGCGGGCGCGCAGGTGCAGCAGCACACAGGCTGGTCGGGAGGGCGGGGCGCGACGTCTGCCGTGCGGGGTCCCGGCATCGGTTGCGCGCGCGCTCCCTCCTCTCGGAGAGAGGGCTGTGGTAAAACCCGTCCGGAAAAC
Последовательность кодирующей области (cds MeCP2B человека) (SEQ ID NO:3)
ATGGCCGCCGCCGCCGCCGCCGCGCCGAGCGGAGGAGGAGGAGGAGGCGAGGAGGAGAGACTGGAAGAAAAGTCAGAAGACCAGGACCTCCAGGGCCTCAAGGACAAACCCCTCAAGTTTAAAAAGGTGAAGAAAGATAAGAAAGAAGAGAAAGAGGGCAAGCATGAGCCCGTGCAGCCATCAGCCCACCACTCTGCTGAGCCCGCAGAGGCAGGCAAAGCAGAGACATCAGAAGGGTCAGGCTCCGCCCCGGCTGTGCCGGAAGCTTCTGCCTCCCCCAAACAGCGGCGCTCCATCATCCGTGACCGGGGACCCATGTATGATGACCCCACCCTGCCTGAAGGCTGGACACGGAAGCTTAAGCAAAGGAAATCTGGCCGCTCTGCTGGGAAGTATGATGTGTATTTGATCAATCCCCAGGGAAAAGCCTTTCGCTCTAAAGTGGAGTTGATTGCGTACTTCGAAAAGGTAGGCGACACATCCCTGGACCCTAATGATTTTGACTTCACGGTAACTGGGAGAGGGAGCCCCTCCCGGCGAGAGCAGAAACCACCTAAGAAGCCCAAATCTCCCAAAGCTCCAGGAACTGGCAGAGGCCGGGGACGCCCCAAAGGGAGCGGCACCACGAGACCCAAGGCGGCCACGTCAGAGGGTGTGCAGGTGAAAAGGGTCCTGGAGAAAAGTCCTGGGAAGCTCCTTGTCAAGATGCCTTTTCAAACTTCGCCAGGGGGCAAGGCTGAGGGGGGTGGGGCCACCACATCCACCCAGGTCATGGTGATCAAACGCCCCGGCAGGAAGCGAAAAGCTGAGGCCGACCCTCAGGCCATTCCCAAGAAACGGGGCCGAAAGCCGGGGAGTGTGGTGGCAGCCGCTGCCGCCGAGGCCAAAAAGAAAGCCGTGAAGGAGTCTTCTATCCGATCTGTGCAGGAGACCGTACTCCCCATCAAGAAGCGCAAGACCCGGGAGACGGTCAGCATCGAGGTCAAGGAAGTGGTGAAGCCCCTGCTGGTGTCCACCCTCGGTGAGAAGAGCGGGAAAGGACTGAAGACCTGTAAGAGCCCTGGGCGGAAAAGCAAGGAGAGCAGCCCCAAGGGGCGCAGCAGCAGCGCCTCCTCACCCCCCAAGAAGGAGCACCACCACCATCACCACCACTCAGAGTCCCCAAAGGCCCCCGTGCCACTGCTCCCACCCCTGCCCCCACCTCCACCTGAGCCCGAGAGCTCCGAGGACCCCACCAGCCCCCCTGAGCCCCAGGACTTGAGCAGCAGCGTCTGCAAAGAGGAGAAGATGCCCAGAGGAGGCTCACTGGAGAGCGACGGCTGCCCCAAGGAGCCAGCTAAGACTCAGCCCGCGGTTGCCACCGCCGCCACGGCCGCAGAAAAGTACAAACACCGAGGGGAGGGAGAGCGCAAAGACATTGTTTCATCCTCCATGCCAAGGCCAAACAGAGAGGAGCCTGTGGACAGCCGGACGCCCGTGACCGAGAGAGTTAGCTGA
Последовательность полиA (синтетическая) (SEQ ID NO:4)
AATAAAAGATCTTTATTTTCATTAGATCTGTGTGTTGGTTTTTTGTGTG
[0072] scAAV9 получали посредством процедур временной трансфекции с применением двухнитевого вектора на основе ITR AAV2 с плазмидой, кодирующей последовательность Rep2Cap9, как описано ранее [Gao et al., выше], совместно с аденовирусной плазмидой-помощником pHelper (Stratagene, Санта-Клара, Калифорния) в клетках 293. Для проведения экспериментов вирус получали тремя отдельными партиями и очищали с помощью двух стадий очистки в градиенте плотности хлорида цезия, диализировали против PBS, и составляли в смесь с 0,001% Pluronic-F68 для предупреждения агрегации вируса, и хранили при 4°C. У всех векторных препаратов определяли титр с помощью количественной ПЦР с применением технологии Taq-Man. Чистоту векторов оценивали с помощью электрофореза в акриламидном геле с добавлением 4-12% додецилсульфата натрия и окрашивания серебром (Invitrogen, Карлсбад, Калифорния).
[0073] Исследования эффективности и подбора дозы проводили на той же линии мышей с синдромом Ретта, что и на фигуре 4. Дозы в примере 1 и примеры 2 не сопоставимы из-за усовершенствований в способах определения титра. В экспериментах примера 1 применяли оптический способ определения титра вирусных препаратов, в то время как в исследованиях примера 2 и далее применяли более точный способ определения титра методом цифровой капельной ПЦР. Для имитации предложенного клинического пути доставки в виде интратекального введения эти инъекции проводили как интрацеребровентрикулярную (ICV) инъекцию детенышам в день 1 после рождения. Интратекальную доставку выбрали для доставки AVXS-201 непосредственно в нервную систему, которая является ключевым местом действия синдрома Ретта. За детенышами наблюдали в отношении их естественной жизни и оценивали в отношении выживания, обобщенного фенотипического балла, поведения в тесте "открытое поле" и на вращающемся барабане. Данные по выживанию в диапазоне доз в двулогарифмическом масштабе показаны на фигуре 7. Результаты, показанные на фигуре 7, демонстрируют, что комбинация векторов и методик, применяемых в способах лечения по настоящему изобретению, обеспечивает улучшенный результат. Все протестированные дозы увеличивали медианное выживание по сравнению с Mecp2y/- мышами, обработанными контролем, при этом наблюдаемое максимальное индивидуальное выживание достигло 500 дней (и продолжается) по сравнению с 93 днями у мышей с синдромом Ретта, обработанных контролем. Самая большая медианная продолжительность жизни (315 дней) достигалась при умеренной дозе 1,44×1010 vg на животное. Данные показывают колоколообразный дозозависимый ответ (фигура 7В), что отличает результаты, полученные в данном документе, от эффектов неправильной дозировки (число копий гена) MECP2, наблюдаемых ранее [см., например, Lombardi et al., The Journal of Clinical Investigation, 125: 2914-2923 (2015)]. Важно отметить, что даже при самой высокой протестированной дозе обработка посредством AVXS-201 не укорачивала выживание Mecp-/y мышей по сравнению с обработкой контролем.
[0074] В дополнение к оценке выживания, обработанных и контрольных мышей еженедельно оценивали в отношении фенотипов синдрома Ретта (фенотипы, изложенные в предыдущем примере). У необработанные самцов фенотип быстро прогрессировал от балла 0 до среднего пика 5,25 к 10-недельному возрасту (фигура 8). В отличие от этого, у всех обработанных групп фенотипические баллы достигали только балла приблизительно 2 к 17-недельному возрасту, за исключением группы с 5,56×1010 vg, которая через 18 недель достигла балла 5. Обработанных и контрольных животных также оценивали в тестах "открытое поле" и на вращающемся барабане (фигура 9). Уменьшение самопроизвольного передвижения является симптомом синдрома Ретта у самцов мышей. Анализ в тесте "открытое поле" проводили для оценки самопроизвольного передвижения и скорости, когда группы достигали возраста 2-3 месяца. Пораженные животных характеризовались практически 43% уменьшением общего пройденного расстояния по сравнению с мышами дикого типа. Значительное увеличение пройденного расстояния отмечали у всех, за исключением двух, групп, обработанных посредством AVXS-201, по сравнению с нокаутными по Mecp2 самцами, обработанными контролем. Также значимо увеличивалась скорость в сравнении с нокаутными мышами, обработанными контролем. Это показывает, что обработка посредством AVXS-201 модельных мышей, представляющих собой самцов с синдромом Ретта, улучшала исследовательское поведение и способность к передвижению. Обработанных и контрольных животных тестировали в возрасте 3 месяцев в отношении показателей на вращающемся барабане, которые являются мерой координации движений. Животных тестировали в течение трех последовательных дней, и баллы усредняли по дням и дозе. Полученные данные представлены на фигуре 9С. У Mecp-/y мышей, обработанных контролем, показатели на вращающемся барабане были значимо хуже, чем у однопометников дикого типа, обработанными контролем. Показатели на вращающемся барабане значимо улучшались в сравнении с контрольной обработкой в когортах 7,00×109 и 1,44×1010 vg.
Пример 3
Экспрессия белка MECP2 за счет AVXS-201 в головном мозге обработанных мышей с синдромом Ретта
[0075] Через 3 недели после инъекции самцов дикого типа, обработанных посредством PBS, необработанных животных с синдромом Ретта и животных с синдромом Ретта, обработанных вектором, подвергали эвтаназии для проверки уровней белка MECP2 в головном мозге после ICV инъекции AVXS-201 в день 1 после рождения. Одно полушарие головного мозга гомогенизировали и анализировали с помощью вестерн-блоттинга для отслеживания экспрессии MECP2. Репрезентативный блот и результаты количественной оценки показаны на фигуре 10. После нормализации относительно головного мозга мышей дикого типа, обработанных PBS, группа нокаутных мышей и группа с дозой 1,75×109 vg AVXS-201 характеризовались отсутствием детектируемых уровней MECP2. Обработка посредством 3,50×109 vg и 7,00×109 vg приводила к детектируемым уровням MECP2, которые достигали ~1% и 3,6% от уровней дикого типа, соответственно. Наиболее эффективная доза, при измерении по увеличению медианного выживания (1,44×1010 vg), приводила к ~11% от уровней MeCP2 дикого типа. Доза 5,56×1010 vg, изученная с помощью вестерн-блоттинга, приводила к уровням MECP2, составляющим ~54% от уровней дикого типа, тогда как при дозе 1,13×1011 достигались более чем 2-кратные уровни от уровней дикого типа. Эти данные показывают, что уровень экспрессии белка и его распределение во всех участках головного мозга являются ключевыми для прогнозирования эффективности генной терапии посредством MECP2.
Пример 4
Обработка мышей дикого типа посредством AVXS-201 безопасна и хорошо переносится
[0076] Важной проблемой, касающейся заместительной терапии посредством MECP2, была оценка влияния на клетки, экспрессирующие интактную копию MECP2. AVXS-201 разрабатывали с учетом сказанного выше путем включения фрагмента промотора гена Mecp2 мыши для поддержки физиологической регуляции трансгена MECP2. Для тестирования безопасности AVXS-201 проводили анализ выживания и поведения на когортах мышей дикого типа, которые получали ICV инъекции AVXS-201 в P1, как в случае самцов мышей с синдромом Ретта.
[0077] В общей сложности 131 самца мышей дикого типа обрабатывали различными ICV дозами AVXS-201 и наблюдали в отношении выживания (фигура 11). При целевой терапевтической дозе (1,44×1010 vg) ни одного случая смерти не регистрировали, при этом 21 обработанное животное оставалось живым вплоть до P342. Ни одного случая смерти не регистрировали в группе, обработанной PBS, и по одному случаю смерти регистрировали в каждой из групп, обработанных посредством 3,50×109, 2,78×1010 и 1,13×1011 vg. Оценка поведения с применением критериев из вставки 1 показывает, что группы, обработанные вектором, в большинстве характеризовались средними фенотипическими баллами <1. Средние совокупные баллы >1 отмечали лишь у двух групп с самыми высокими дозами (5,56×1010 и 1,13×1011 vg). Исследование в тесте "открытое поле" в возрасте 2-3 месяцев не показало статистической разницы между самцами дикого типа, обработанными вектором и PBS (фигура 12). Интересно отметить, что у когорты, обработанной 1,13×1011 vg, обнаружили значимое снижение показателей на вращающемся барабане в сравнении с мышами дикого типа, обработанными контролем, в возрасте трех месяцев. Эти данные позволяют предположить токсический эффект сверхэкспрессии MECP2 при самой высокой дозе AVXS-201. Взятые вместе, эти данные свидетельствуют о том, что в случае “наихудшего сценария”, если при обработке посредством AVXS-201 трансдуцируются только клетки дикого типа, при целевой терапевтической дозе наблюдается минимальное воздействие на выживание и поведение животных.
Пример 5
Физиологические уровни MECP2 сохраняются в головном мозге мышей дикого типа, обработанных терапевтическими дозами AVXS-201
[0078] Для дополнительного исследования уровней, сопряженных с симптоматической сверхэкспрессией MECP2, самцы мышей дикого типа получали ICV инъекции PBS или AVXS-201 P1 из расчета терапевтической целевой дозы 1,44×1010 vg или самой высокой тестируемой дозы 1,13×1011 vg. Животных подвергали эвтаназии через 3 недели после инъекции и головной мозг животных собирали для проведения вестерн-блоттинга. Для целей сравнения блоттинг тканей производили параллельно с образцами головного мозга мышиной модели со сверхэкспрессией MECP2 под названием Tg3. Головной мозг рассекали на отдельные области (Cb=мозжечок, Med=продолговатый мозг, Hipp=гиппокамп, Ctx=кора головного мозга и Mid=средний мозг; фигура 13) и эти отдельные области гомогенизировали для проведения блоттинга. Данные нормализовали относительно уровней MECP2 в головном мозге мышей дикого типа, обработанных посредством PBS. При обработке целевой терапевтической дозой (1,44×1010 vg) для всех исследованных областей характерны уровни MECP2, составляющие от 1 до 1,5x от уровней в тканях животных дикого типа. При высокой дозе (1,13×1011 vg) уровни находились в диапазоне 1,31-2,56x от уровней дикого типа, но не достигала 2,31-3,93x уровней, характерных для тканей от Tg3. Эти данные, вместе с данными по поведению и выживанию, продемонстрированными ранее, вселяют уверенность в том, что при введении в целевой дозе AVXS-201 экспрессирует белок практически на физиологических уровнях. Важно отметить, что при введении терапевтической дозы не наблюдали приближение к 2-кратным уровням белка, которые сопряжены с синдромом дупликации MECP2. Это показывает безопасность подхода замещения MECP2 с применением генной терапии.
Пример 6
Масса тела, гематологические и биохимические показатели сыворотки у отличных от человека приматов не были отягощены вплоть до 18 месяцев после интратекальной инъекции AVXS-201
[0079] Для изучения безопасности и переносимости AVXS-201 и сопряженной с ними процедуры интратекальной инъекции за тремя обработанными самцами яванского макака наблюдали в течение 18 месяцев после инъекции. Параметры введения дозы показаны в таблице 2.
[0080] Двух животных обрабатывали предполагаемой терапевтической дозой (эквивалент ~1,44×109 vg на кг массы тела) и одно получало в ~2 раза более низкую дозу (эквивалент ~7,00×108 vg на кг массы тела). Процедура интратекальной инъекции была ранее описана в Meyer et al., Molecular Therapy: The Journal of the American Society of Gene Therapy, 23: 477-487 (2015). Вкратце, вектор смешивали с контрастным средством для проверки распределения вектора. Подвергнутого анестезии субъекта помещали в положение лежа на боку и готовили место для инъекции по средней линии спины на уровне ~L4/5 (ниже конуса спинного мозга). В стерильных условиях вводили иглу для спинномозговой пункции со стилетом и катетеризацию подпаутинного пространства подтверждали при вытекании прозрачной CSF из иглы. Для снижения давления в подпаутинном пространстве сливали 0,8 мл CSF и сразу же после этого инъецировали раствор с вектором. После инъекции животных удерживали в положении Тренделенбурга и их тело наклоняли головой вниз в течение 10 минут. Подвергаемым обработке животным дозу вводили в возрасте 6 или 12 месяцев, данные о массе тела, числе форменных элементов крови и биохимических показателях сыворотки собирали ежемесячно в течение первых 6 месяцев после инъекции и раз в два месяца впоследствии. Масса тела показана на фигуре 14, число форменных элементов крови показано на фигуре 15, а биохимические показатели сыворотки показаны на фигурах 16 и 17, при этом они нанесены на график со значениями от обработанных контролем животных из той же колонии в фонде Маннхеймера (Хомстед, Флорида). Таким образом, масса тела, число клеток и показатели сыворотки крови у обработанных вектором животных соответствовали таковым у обработанных контролем животных. У рассматриваемого животного отсутствовали значения, которые в значительной степени отклонялись от значений контроля на протяжении более чем 2 последовательных наблюдений, за исключением уровня амилазы, который был выше у двух обработанных вектором животных на исходном уровне. Эти данные показывают, что AVXS-201 и процедура интратекальной инъекцией безопасны и хорошо переносятся.
Пример 7
Гистопатологический анализ тканей отличных от человека приматов после интратекальной инъекции AVXS-201
[0081] В дополнение к in vivo анализу (пример 6) и посмертному анализу (пример 8) образцы висцеральных тканей и тканей нервной системы от животных 15C38, 15C49 и 15C34 (таблица 1) отправляли в GEMpath Inc. (Лонгмонт, Колорадо) для заливки парафином, изготовления срезов и окрашивания гематоксилином и эозином. Остальные животные (таблица 8.2) все еще живы, и их ткани будут отправлены на анализ по окончании исследования. Микроскопические препараты были проанализированы и отчеты подготовлены сертифицированным ветеринарным патоморфологом из экспертного совета компании GEMpath. Ткани, из которых отбирали образцы и которые изучали, показаны в таблице 3. В гистологическом заключении отмечается, что обработка посредством AVXS-201 не индуцировала развития очагов поражения в каких-либо из указанных в протоколе тканях на момент времени 6 недель или 18 месяцев.

Пример 8
Физиологические уровни MeCP2 в головном мозге отличных от человека приматов после интратекальной инъекции AVXS-201
[0082] Два 12-месячных самца яванского макака получали интратекальные инъекции, содержащие 7,7×1012 vg/кг AVXS-201, как описано выше. Животных поддерживали в течение шести недель после инъекции, а потом подвергали эвтаназии для анализа экспрессии MeCP2. Выбранные области головного мозга анализировали в отношении общей экспрессии MeCP2 с помощью иммуногистохимического анализа (фигура 18). Явного повышения содержания MeCP2 не выявляли ни в кортикальных и подкорковых областях, ни вблизи места инъекции (поясничный отдел спинного мозга). Важно отметить, что эти данные также не показали никаких чрезвычайных аномалий в тканях животных, которые получали инъекцию AVXS-201. Для дополнительного исследования экспрессии трансгена области головного мозга гомогенизировали и сравнивали с ретроспективной контрольной тканью животных из той же колонии (фигура 19). Образцы затылочной и височной коры, гипоталамуса, поясничного отдела спинного мозга, таламуса, миндалины, гиппокампа и мозжечка анализировали с помощью вестерн-блоттинга в отношении общей экспрессии MeCP2. Для всех исследованных областей превышение уровня экспрессии MeCP2 ≥2x в сравнении с контролями не было показано ни для одной из областей. Повышение содержания MeCP2 выявили в гипоталамусе и миндалине, которые являются областями, расположенными вблизи 3го желудочка и бокового желудочка, соответственно, но не в мозжечке. Кроме того, в поясничном отделе спинного мозга, который расположен вблизи места инъекции, не показано повышение уровней MeCP2. Эти данные позволяют предположить, что комбинация дозы вируса и конструкции экспрессии регулируют экспрессию MECP2. Кроме того, in situ гибридизацию (ISH) проводили для обнаружения полученного за счет вектора транскрипта и определения его распределения в головном мозге через 6 недель и 18 месяцев после инъекции (фигуры 20 и 21). Для всех исследованных областей головного и спинного мозга (затылочная кора, височная кора, гиппокамп, мозолистое тело, таламус, хвостатое ядро, скорлупа, верхнее двухолмие, варолиев мост, продолговатый мозг, мозжечок, шейный, грудной и поясничный отделы спинного мозга) показана экспрессия транскрипта, полученного за счет вектора, который отсутствовал в тканях животных, обработанных контролем. Эти данные показывают специфичность зонда для ISH в отношении транскрипта MECP2, полученного за счет вектора, и показывают, что промоторная конструкция AVXS-201 функциональна в ткани нервной системы NHP. Эти данные показывают, что при введении посредством люмбальной пункции AVXS-201 широко распределяется по всем областям ЦНС и экспрессируется на физиологических уровнях.
Раскрытие из предварительной заявки на патент № 62/423618
Генная терапия синдрома Ретта
Генная терапия, направленная на восстановление транскрипционного фактора MeCP2, по-видимому, является реалистичной стратегией для лечения синдрома Ретта, прогрессирующего нарушения развития нервной системы, приводящего к выраженному аутистическому поведению, утрате двигательной функции и ранней смерти. Авторы настоящего изобретения разработали аденоассоциированный вирус серотипа 9 (AAV9), экспрессирующий MECP2 человека под контролем усеченного эндогенного промотора. Задача данной работы заключается в оценке эффективности и безопасности данного вектора на мышах (с нулевым аллелем MeCP2 и дикого типа) и отличных от человека приматах. В рамках продолжения исследования нашей целью является перенесение данного лечения из лаборатории к постели больного.


--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> КАСПАР, Брайан, К. et al.
<120> ИНТРАТЕКАЛЬНАЯ ДОСТАВКА РЕКОМБИНАНТНОГО АДЕНОАССОЦИИРОВАННОГО ВИРУСА,
КОДИРУЮЩЕГО МЕТИЛ-CPG-СВЯЗЫВАЮЩИЙ БЕЛОК 2
<130> 28335/50215PCT
<160> 8
<170> PatentIn версия 3.5
<210> 1
<211> 2558
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<220>
<221> другой_признак
<223> Геном AVXS-201
<220>
<221> другой_признак
<222> (1)..(106)
<223> Мутантный ITR
<220>
<221> другой_признак
<222> (151)..(699)
<223> Промоторный фрагмент из 546 нуклеотидов
<220>
<221> другой_признак
<222> (729)..(827)
<223> Интрон SV40
<220>
<221> другой_признак
<222> (848)..(2344)
<223> cds hMECP2B
<220>
<221> другой_признак
<222> (2345)..(2393)
<223> Синтетический pA
<220>
<221> другой_признак
<222> (2418)..(2558)
<223> ITR
<400> 1
ctgcgcgctc gctcgctcac tgaggccgcc cgggcaaagc ccgggcgtcg ggcgaccttt 60
ggtcgcccgg cctcagtgag cgagcgagcg cgcagagagg gagtggaatt cacgcgtgga 120
tctgaattca attcacgcgt ggtaccacgc gtgaacaacg ccaggctcct caacaggcaa 180
ctttgctact tctacagaaa atgataataa agaaatgctg gtgaagtcaa atgcttatca 240
caatggtgaa ctactcagca gggaggctct aataggcgcc aagagcctag acttccttaa 300
gcgccagagt ccacaagggc ccagttaatc ctcaacattc aaatgctgcc cacaaaacca 360
gcccctctgt gccctagccg cctctttttt ccaagtgaca gtagaactcc accaatccgc 420
agctgaatgg ggtccgcctc ttttccctgc ctaaacagac aggaactcct gccaattgag 480
ggcgtcaccg ctaaggctcc gccccagcct gggctccaca accaatgaag ggtaatctcg 540
acaaagagca aggggtgggg cgcgggcgcg caggtgcagc agcacacagg ctggtcggga 600
gggcggggcg cgacgtctgc cgtgcggggt cccggcatcg gttgcgcgcg cgctccctcc 660
tctcggagag agggctgtgg taaaacccgt ccggaaaacg cgtcgaaggg cgaattctgc 720
agataactgg taagtttagt cttttttgtc ttttatttca ggtcccggat ccggtggtgg 780
tgcaaatcaa agaactgctc ctcagtcgat gttgccttta cttctaggcc tgtacggaag 840
tgttactatg gccgccgccg ccgccgccgc gccgagcgga ggaggaggag gaggcgagga 900
ggagagactg gaagaaaagt cagaagacca ggacctccag ggcctcaagg acaaacccct 960
caagtttaaa aaggtgaaga aagataagaa agaagagaaa gagggcaagc atgagcccgt 1020
gcagccatca gcccaccact ctgctgagcc cgcagaggca ggcaaagcag agacatcaga 1080
agggtcaggc tccgccccgg ctgtgccgga agcttctgcc tcccccaaac agcggcgctc 1140
catcatccgt gaccggggac ccatgtatga tgaccccacc ctgcctgaag gctggacacg 1200
gaagcttaag caaaggaaat ctggccgctc tgctgggaag tatgatgtgt atttgatcaa 1260
tccccaggga aaagcctttc gctctaaagt ggagttgatt gcgtacttcg aaaaggtagg 1320
cgacacatcc ctggacccta atgattttga cttcacggta actgggagag ggagcccctc 1380
ccggcgagag cagaaaccac ctaagaagcc caaatctccc aaagctccag gaactggcag 1440
aggccgggga cgccccaaag ggagcggcac cacgagaccc aaggcggcca cgtcagaggg 1500
tgtgcaggtg aaaagggtcc tggagaaaag tcctgggaag ctccttgtca agatgccttt 1560
tcaaacttcg ccagggggca aggctgaggg gggtggggcc accacatcca cccaggtcat 1620
ggtgatcaaa cgccccggca ggaagcgaaa agctgaggcc gaccctcagg ccattcccaa 1680
gaaacggggc cgaaagccgg ggagtgtggt ggcagccgct gccgccgagg ccaaaaagaa 1740
agccgtgaag gagtcttcta tccgatctgt gcaggagacc gtactcccca tcaagaagcg 1800
caagacccgg gagacggtca gcatcgaggt caaggaagtg gtgaagcccc tgctggtgtc 1860
caccctcggt gagaagagcg ggaaaggact gaagacctgt aagagccctg ggcggaaaag 1920
caaggagagc agccccaagg ggcgcagcag cagcgcctcc tcacccccca agaaggagca 1980
ccaccaccat caccaccact cagagtcccc aaaggccccc gtgccactgc tcccacccct 2040
gcccccacct ccacctgagc ccgagagctc cgaggacccc accagccccc ctgagcccca 2100
ggacttgagc agcagcgtct gcaaagagga gaagatgccc agaggaggct cactggagag 2160
cgacggctgc cccaaggagc cagctaagac tcagcccgcg gttgccaccg ccgccacggc 2220
cgcagaaaag tacaaacacc gaggggaggg agagcgcaaa gacattgttt catcctccat 2280
gccaaggcca aacagagagg agcctgtgga cagccggacg cccgtgaccg agagagttag 2340
ctgaaataaa agatctttat tttcattaga tctgtgtgtt ggttttttgt gtggcatgct 2400
ggggagagat cgatctgagg aacccctagt gatggagttg gccactccct ctctgcgcgc 2460
tcgctcgctc actgaggccg ggcgaccaaa ggtcgcccga cgcccgggct ttgcccgggc 2520
ggcctcagtg agcgagcgag cgcgcagaga gggagtgg 2558
<210> 2
<211> 549
<212> ДНК
<213> Mus musculus
<400> 2
gtgaacaacg ccaggctcct caacaggcaa ctttgctact tctacagaaa atgataataa 60
agaaatgctg gtgaagtcaa atgcttatca caatggtgaa ctactcagca gggaggctct 120
aataggcgcc aagagcctag acttccttaa gcgccagagt ccacaagggc ccagttaatc 180
ctcaacattc aaatgctgcc cacaaaacca gcccctctgt gccctagccg cctctttttt 240
ccaagtgaca gtagaactcc accaatccgc agctgaatgg ggtccgcctc ttttccctgc 300
ctaaacagac aggaactcct gccaattgag ggcgtcaccg ctaaggctcc gccccagcct 360
gggctccaca accaatgaag ggtaatctcg acaaagagca aggggtgggg cgcgggcgcg 420
caggtgcagc agcacacagg ctggtcggga gggcggggcg cgacgtctgc cgtgcggggt 480
cccggcatcg gttgcgcgcg cgctccctcc tctcggagag agggctgtgg taaaacccgt 540
ccggaaaac 549
<210> 3
<211> 1497
<212> ДНК
<213> Homo sapiens
<220>
<221> другой_признак
<223> cds MeCP2B
<400> 3
atggccgccg ccgccgccgc cgcgccgagc ggaggaggag gaggaggcga ggaggagaga 60
ctggaagaaa agtcagaaga ccaggacctc cagggcctca aggacaaacc cctcaagttt 120
aaaaaggtga agaaagataa gaaagaagag aaagagggca agcatgagcc cgtgcagcca 180
tcagcccacc actctgctga gcccgcagag gcaggcaaag cagagacatc agaagggtca 240
ggctccgccc cggctgtgcc ggaagcttct gcctccccca aacagcggcg ctccatcatc 300
cgtgaccggg gacccatgta tgatgacccc accctgcctg aaggctggac acggaagctt 360
aagcaaagga aatctggccg ctctgctggg aagtatgatg tgtatttgat caatccccag 420
ggaaaagcct ttcgctctaa agtggagttg attgcgtact tcgaaaaggt aggcgacaca 480
tccctggacc ctaatgattt tgacttcacg gtaactggga gagggagccc ctcccggcga 540
gagcagaaac cacctaagaa gcccaaatct cccaaagctc caggaactgg cagaggccgg 600
ggacgcccca aagggagcgg caccacgaga cccaaggcgg ccacgtcaga gggtgtgcag 660
gtgaaaaggg tcctggagaa aagtcctggg aagctccttg tcaagatgcc ttttcaaact 720
tcgccagggg gcaaggctga ggggggtggg gccaccacat ccacccaggt catggtgatc 780
aaacgccccg gcaggaagcg aaaagctgag gccgaccctc aggccattcc caagaaacgg 840
ggccgaaagc cggggagtgt ggtggcagcc gctgccgccg aggccaaaaa gaaagccgtg 900
aaggagtctt ctatccgatc tgtgcaggag accgtactcc ccatcaagaa gcgcaagacc 960
cgggagacgg tcagcatcga ggtcaaggaa gtggtgaagc ccctgctggt gtccaccctc 1020
ggtgagaaga gcgggaaagg actgaagacc tgtaagagcc ctgggcggaa aagcaaggag 1080
agcagcccca aggggcgcag cagcagcgcc tcctcacccc ccaagaagga gcaccaccac 1140
catcaccacc actcagagtc cccaaaggcc cccgtgccac tgctcccacc cctgccccca 1200
cctccacctg agcccgagag ctccgaggac cccaccagcc cccctgagcc ccaggacttg 1260
agcagcagcg tctgcaaaga ggagaagatg cccagaggag gctcactgga gagcgacggc 1320
tgccccaagg agccagctaa gactcagccc gcggttgcca ccgccgccac ggccgcagaa 1380
aagtacaaac accgagggga gggagagcgc aaagacattg tttcatcctc catgccaagg 1440
ccaaacagag aggagcctgt ggacagccgg acgcccgtga ccgagagagt tagctga 1497
<210> 4
<211> 49
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<220>
<221> другой_признак
<223> Последовательность полиA
<400> 4
aataaaagat ctttattttc attagatctg tgtgttggtt ttttgtgtg 49
<210> 5
<211> 3093
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<220>
<221> другой_признак
<223> Геном scAAV9.738.Mecp1
<220>
<221> другой_признак
<222> (1)..(106)
<223> Мутантный ITR
<220>
<221> другой_признак
<222> (198)..(936)
<223> Промоторный фрагмент из 738 нуклеотидов
<220>
<221> другой_признак
<222> (941)..(1037)
<223> Интрон SV40
<220>
<221> другой_признак
<222> (1138)..(2643)
<223> cds MeCP2
<220>
<221> другой_признак
<222> (2709)..(2890)
<223> pA BGH
<220>
<221> другой_признак
<222> (2953)..(3093)
<223> ITR
<400> 5
ctgcgcgctc gctcgctcac tgaggccgcc cgggcaaagc ccgggcgtcg ggcgaccttt 60
ggtcgcccgg cctcagtgag cgagcgagcg cgcagagagg gagtggaatt cacgcgtgga 120
tctgaattca attcacgcgt ggtaccgagc tcggatccac tagtaacggc cgccagtgtg 180
ctggaattcg cccttaatat caaaccatct gattcaacaa tgacagaccg atctcttatg 240
ggcttggcac acaccatctg cccattataa acgtctgcaa agaccaaggt ttgatatgtt 300
gattttactg tcagccttaa gagtgcgaca tctgctaatt tagtgtaata atacaatcag 360
tagacccttt aaaacaagtc ccttggcttg gaacaacgcc aggctcctca acaggcaact 420
ttgctacttc tacagaaaat gataataaag aaatgctggt gaagtcaaat gcttatcaca 480
atggtgaact actcagcagg gaggctctaa taggcgccaa gagcctagac ttccttaagc 540
gccagagtcc acaagggccc agttaatcct caacattcaa atgctgccca caaaaccagc 600
ccctctgtgc cctagccgcc tcttttttcc aagtgacagt agaactccac caatccgcag 660
ctgaatgggg tccgcctctt ttccctgcct aaacagacag gaactcctgc caattgaggg 720
cgtcaccgct aaggctccgc cccagcctgg gctccacaac caatgaaggg taatctcgac 780
aaagagcaag gggtggggcg cgggcgcgca ggtgcagcag cacacaggct ggtcgggagg 840
gcggggcgcg acgtctgccg tgcggggtcc cggcatcggt tgcgcgcgcg ctccctcctc 900
tcggagagag ggctgtggta aaacccgtcc ggaaaaactg gtaagtttag tctttttgtc 960
ttttatttca ggtcccggat ccggtggtgg tgcaaatcaa agaactgctc ctcagtggat 1020
gttgccttta cttctaggcc tgtacggaag tgttacttct gctctaaaag ctgcggaatt 1080
gtacccgcgg ccgatccacc ggttttaagg gccgaggcgg ccagatcttt cgaagatatg 1140
gccgccgctg ccgccaccgc cgccgccgcc gccgcgccga gcggaggagg aggaggaggc 1200
gaggaggaga gactggagga aaagtcagaa gaccaggatc tccagggcct cagagacaag 1260
ccactgaagt ttaagaaggc gaagaaagac aagaaggagg acaaagaagg caagcatgag 1320
ccactacaac cttcagccca ccattctgca gagccagcag aggcaggcaa agcagaaaca 1380
tcagaaagct caggctctgc cccagcagtg ccagaagcct cggcttcccc caaacagcgg 1440
cgctccatta tccgtgaccg gggacctatg tatgatgacc ccaccttgcc tgaaggttgg 1500
acacgaaagc ttaaacaaag gaagtctggc cgatctgctg gaaagtatga tgtatatttg 1560
atcaatcccc agggaaaagc ttttcgctct aaagtagaat tgattgcata ctttgaaaag 1620
gtgggagaca cctccttgga ccctaatgat tttgacttca cggtaactgg gagagggagc 1680
ccctccagga gagagcagaa accacctaag aagcccaaat ctcccaaagc tccaggaact 1740
ggcaggggtc ggggacgccc caaagggagc ggcactggga gaccaaaggc agcagcatca 1800
gaaggtgttc aggtgaaaag ggtcctggag aagagccctg ggaaacttgt tgtcaagatg 1860
cctttccaag catcgcctgg gggtaagggt gagggaggtg gggctaccac atctgcccag 1920
gtcatggtga tcaaacgccc tggcagaaag cgaaaagctg aagctgaccc ccaggccatt 1980
cctaagaaac ggggtagaaa gcctgggagt gtggtggcag ctgctgcagc tgaggccaaa 2040
aagaaagccg tgaaggagtc ttccatacgg tctgtgcatg agactgtgct ccccatcaag 2100
aagcgcaaga cccgggagac ggtcagcatc gaggtcaagg aagtggtgaa gcccctgctg 2160
gtgtccaccc ttggtgagaa aagcgggaag ggactgaaga cctgcaagag ccctgggcgt 2220
aaaagcaagg agagcagccc caaggggcgc agcagcagtg cctcctcccc acctaagaag 2280
gagcaccatc atcaccacca tcactcagag tccacaaagg cccccatgcc actgctccca 2340
tccccacccc cacctgagcc tgagagctct gaggacccca tcagcccccc tgagcctcag 2400
gacttgagca gcagcatctg caaagaagag aagatgcccc gaggaggctc actggaaagc 2460
gatggctgcc ccaaggagcc agctaagact cagcctatgg tcgccaccac taccacagtt 2520
gcagaaaagt acaaacaccg aggggaggga gagcgcaaag acattgtttc atcttccatg 2580
ccaaggccaa acagagagga gcctgtggac agccggacgc ccgtgaccga gagagttagc 2640
tgaatcggcg ccgctagcgc ggccgcgttt aaaccctgca ggtctagaaa gcttatcgat 2700
accgtcgact agagctcgct gatcagcctc gactgtgcct tctagttgcc agccatctgt 2760
tgtttgcccc tcccccgtgc cttccttgac cctggaaggt gccactccca ctgtcctttc 2820
ctaataaaat gaggaaattg catcgcattg tctgagtagg tgtcattcta ttctgggggg 2880
tggggtgggg caggacagca agggggagga ttgggaagac aatagcaggc atgctgggga 2940
gagatcgatc tgaggaaccc ctagtgatgg agttggccac tccctctctg cgcgctcgct 3000
cgctcactga ggccgggcga ccaaaggtcg cccgacgccc gggctttgcc cgggcggcct 3060
cagtgagcga gcgagcgcgc agagagggag tgg 3093
<210> 6
<211> 739
<212> ДНК
<213> Mus musculus
<220>
<221> другой_признак
<223> Промотор MECP2
<400> 6
tatcaaacca tctgattcaa caatgacaga ccgatctctt atgggcttgg cacacaccat 60
ctgcccatta taaacgtctg caaagaccaa ggtttgatat gttgatttta ctgtcagcct 120
taagagtgcg acatctgcta atttagtgta ataatacaat cagtagaccc tttaaaacaa 180
gtcccttggc ttggaacaac gccaggctcc tcaacaggca actttgctac ttctacagaa 240
aatgataata aagaaatgct ggtgaagtca aatgcttatc acaatggtga actactcagc 300
agggaggctc taataggcgc caagagccta gacttcctta agcgccagag tccacaaggg 360
cccagttaat cctcaacatt caaatgctgc ccacaaaacc agcccctctg tgccctagcc 420
gcctcttttt tccaagtgac agtagaactc caccaatccg cagctgaatg gggtccgcct 480
cttttccctg cctaaacaga caggaactcc tgccaattga gggcgtcacc gctaaggctc 540
cgccccagcc tgggctccac aaccaatgaa gggtaatctc gacaaagagc aaggggtggg 600
gcgcgggcgc gcaggtgcag cagcacacag gctggtcggg agggcggggc gcgacgtctg 660
ccgtgcgggg tcccggcatc ggttgcgcgc gcgctccctc ctctcggaga gagggctgtg 720
gtaaaacccg tccggaaaa 739
<210> 7
<211> 1563
<212> ДНК
<213> Mus musculus
<220>
<221> другой_признак
<223> MECP2 альфа
<400> 7
gtacccgcgg ccgatccacc ggttttaagg gccgaggcgg ccagatcttt cgaagatatg 60
gccgccgctg ccgccaccgc cgccgccgcc gccgcgccga gcggaggagg aggaggaggc 120
gaggaggaga gactggagga aaagtcagaa gaccaggatc tccagggcct cagagacaag 180
ccactgaagt ttaagaaggc gaagaaagac aagaaggagg acaaagaagg caagcatgag 240
ccactacaac cttcagccca ccattctgca gagccagcag aggcaggcaa agcagaaaca 300
tcagaaagct caggctctgc cccagcagtg ccagaagcct cggcttcccc caaacagcgg 360
cgctccatta tccgtgaccg gggacctatg tatgatgacc ccaccttgcc tgaaggttgg 420
acacgaaagc ttaaacaaag gaagtctggc cgatctgctg gaaagtatga tgtatatttg 480
atcaatcccc agggaaaagc ttttcgctct aaagtagaat tgattgcata ctttgaaaag 540
gtgggagaca cctccttgga ccctaatgat tttgacttca cggtaactgg gagagggagc 600
ccctccagga gagagcagaa accacctaag aagcccaaat ctcccaaagc tccaggaact 660
ggcaggggtc ggggacgccc caaagggagc ggcactggga gaccaaaggc agcagcatca 720
gaaggtgttc aggtgaaaag ggtcctggag aagagccctg ggaaacttgt tgtcaagatg 780
cctttccaag catcgcctgg gggtaagggt gagggaggtg gggctaccac atctgcccag 840
gtcatggtga tcaaacgccc tggcagaaag cgaaaagctg aagctgaccc ccaggccatt 900
cctaagaaac ggggtagaaa gcctgggagt gtggtggcag ctgctgcagc tgaggccaaa 960
aagaaagccg tgaaggagtc ttccatacgg tctgtgcatg agactgtgct ccccatcaag 1020
aagcgcaaga cccgggagac ggtcagcatc gaggtcaagg aagtggtgaa gcccctgctg 1080
gtgtccaccc ttggtgagaa aagcgggaag ggactgaaga cctgcaagag ccctgggcgt 1140
aaaagcaagg agagcagccc caaggggcgc agcagcagtg cctcctcccc acctaagaag 1200
gagcaccatc atcaccacca tcactcagag tccacaaagg cccccatgcc actgctccca 1260
tccccacccc cacctgagcc tgagagctct gaggacccca tcagcccccc tgagcctcag 1320
gacttgagca gcagcatctg caaagaagag aagatgcccc gaggaggctc actggaaagc 1380
gatggctgcc ccaaggagcc agctaagact cagcctatgg tcgccaccac taccacagtt 1440
gcagaaaagt acaaacaccg aggggaggga gagcgcaaag acattgtttc atcttccatg 1500
ccaaggccaa acagagagga gcctgtggac agccggacgc ccgtgaccga gagagttagc 1560
tga 1563
<210> 8
<211> 6087
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<220>
<221> другой_признак
<223> Плазмида для продуцирования AVXS-201
<220>
<221> другой_признак
<222> (1)..(106)
<223> Мутантный ITR
<220>
<221> другой_признак
<222> (151)..(699)
<223> Промоторный фрагмент из 546 нуклеотидов
<220>
<221> другой_признак
<222> (729)..(829)
<223> Интрон SV40
<220>
<221> другой_признак
<222> (848)..(2344)
<223> hMECP2B
<220>
<221> другой_признак
<222> (2345)..(2393)
<223> Синтетический pA
<220>
<221> другой_признак
<222> (2418)..(2558)
<223> ITR
<220>
<221> другой_признак
<222> (3309)..(4259)
<223> Ген устойчивости к канамицину
<220>
<221> другой_признак
<222> (4325)..(4939)
<223> Точка начала репликации pMB1
<400> 8
ctgcgcgctc gctcgctcac tgaggccgcc cgggcaaagc ccgggcgtcg ggcgaccttt 60
ggtcgcccgg cctcagtgag cgagcgagcg cgcagagagg gagtggaatt cacgcgtgga 120
tctgaattca attcacgcgt ggtaccacgc gtgaacaacg ccaggctcct caacaggcaa 180
ctttgctact tctacagaaa atgataataa agaaatgctg gtgaagtcaa atgcttatca 240
caatggtgaa ctactcagca gggaggctct aataggcgcc aagagcctag acttccttaa 300
gcgccagagt ccacaagggc ccagttaatc ctcaacattc aaatgctgcc cacaaaacca 360
gcccctctgt gccctagccg cctctttttt ccaagtgaca gtagaactcc accaatccgc 420
agctgaatgg ggtccgcctc ttttccctgc ctaaacagac aggaactcct gccaattgag 480
ggcgtcaccg ctaaggctcc gccccagcct gggctccaca accaatgaag ggtaatctcg 540
acaaagagca aggggtgggg cgcgggcgcg caggtgcagc agcacacagg ctggtcggga 600
gggcggggcg cgacgtctgc cgtgcggggt cccggcatcg gttgcgcgcg cgctccctcc 660
tctcggagag agggctgtgg taaaacccgt ccggaaaacg cgtcgaaggg cgaattctgc 720
agataactgg taagtttagt cttttttgtc ttttatttca ggtcccggat ccggtggtgg 780
tgcaaatcaa agaactgctc ctcagtcgat gttgccttta cttctaggcc tgtacggaag 840
tgttactatg gccgccgccg ccgccgccgc gccgagcgga ggaggaggag gaggcgagga 900
ggagagactg gaagaaaagt cagaagacca ggacctccag ggcctcaagg acaaacccct 960
caagtttaaa aaggtgaaga aagataagaa agaagagaaa gagggcaagc atgagcccgt 1020
gcagccatca gcccaccact ctgctgagcc cgcagaggca ggcaaagcag agacatcaga 1080
agggtcaggc tccgccccgg ctgtgccgga agcttctgcc tcccccaaac agcggcgctc 1140
catcatccgt gaccggggac ccatgtatga tgaccccacc ctgcctgaag gctggacacg 1200
gaagcttaag caaaggaaat ctggccgctc tgctgggaag tatgatgtgt atttgatcaa 1260
tccccaggga aaagcctttc gctctaaagt ggagttgatt gcgtacttcg aaaaggtagg 1320
cgacacatcc ctggacccta atgattttga cttcacggta actgggagag ggagcccctc 1380
ccggcgagag cagaaaccac ctaagaagcc caaatctccc aaagctccag gaactggcag 1440
aggccgggga cgccccaaag ggagcggcac cacgagaccc aaggcggcca cgtcagaggg 1500
tgtgcaggtg aaaagggtcc tggagaaaag tcctgggaag ctccttgtca agatgccttt 1560
tcaaacttcg ccagggggca aggctgaggg gggtggggcc accacatcca cccaggtcat 1620
ggtgatcaaa cgccccggca ggaagcgaaa agctgaggcc gaccctcagg ccattcccaa 1680
gaaacggggc cgaaagccgg ggagtgtggt ggcagccgct gccgccgagg ccaaaaagaa 1740
agccgtgaag gagtcttcta tccgatctgt gcaggagacc gtactcccca tcaagaagcg 1800
caagacccgg gagacggtca gcatcgaggt caaggaagtg gtgaagcccc tgctggtgtc 1860
caccctcggt gagaagagcg ggaaaggact gaagacctgt aagagccctg ggcggaaaag 1920
caaggagagc agccccaagg ggcgcagcag cagcgcctcc tcacccccca agaaggagca 1980
ccaccaccat caccaccact cagagtcccc aaaggccccc gtgccactgc tcccacccct 2040
gcccccacct ccacctgagc ccgagagctc cgaggacccc accagccccc ctgagcccca 2100
ggacttgagc agcagcgtct gcaaagagga gaagatgccc agaggaggct cactggagag 2160
cgacggctgc cccaaggagc cagctaagac tcagcccgcg gttgccaccg ccgccacggc 2220
cgcagaaaag tacaaacacc gaggggaggg agagcgcaaa gacattgttt catcctccat 2280
gccaaggcca aacagagagg agcctgtgga cagccggacg cccgtgaccg agagagttag 2340
ctgaaataaa agatctttat tttcattaga tctgtgtgtt ggttttttgt gtggcatgct 2400
ggggagagat cgatctgagg aacccctagt gatggagttg gccactccct ctctgcgcgc 2460
tcgctcgctc actgaggccg ggcgaccaaa ggtcgcccga cgcccgggct ttgcccgggc 2520
ggcctcagtg agcgagcgag cgcgcagaga gggagtggcc cccccccccc cccccccggc 2580
gattctcttg tttgctccag actctcaggc aatgacctga tagcctttgt agagacctct 2640
caaaaatagc taccctctcc ggcatgaatt tatcagctag aacggttgaa tatcatattg 2700
atggtgattt gactgtctcc ggcctttctc acccgtttga atctttacct acacattact 2760
caggcattgc atttaaaata tatgagggtt ctaaaaattt ttatccttgc gttgaaataa 2820
aggcttctcc cgcaaaagta ttacagggtc ataatgtttt tggtacaacc gatttagctt 2880
tatgctctga ggctttattg cttaattttg ctaattcttt gccttgcctg tatgatttat 2940
tggatgttgg aatcgcctga tgcggtattt tctccttacg catctgtgcg gtatttcaca 3000
ccgcatatgg tgcactctca gtacaatctg ctctgatgcc gcatagttaa gccagccccg 3060
acacccgcca acactatggt gcactctcag tacaatctgc tctgatgccg catagttaag 3120
ccagccccga cacccgccaa cacccgctga cgcgccctga cgggcttgtc tgctcccggc 3180
atccgcttac agacaagctg tgaccgtctc cgggagctgc atgtgtcaga ggttttcacc 3240
gtcatcaccg aaacgcgcga gacgaaaggg cctcgtgata cgcctatttt tataggttaa 3300
tgtcatgaga ttatcaaaaa ggatcttcac ctagatcctt ttaaattaaa aatgaagttt 3360
taaatcaatc taaagtatat atgagtaaac ttggtctgac agttagaaaa actcatcgag 3420
catcaaatga aactgcaatt tattcatatc aggattatca ataccatatt tttgaaaaag 3480
ccgtttctgt aatgaaggag aaaactcacc gaggcagttc cataggatgg caagatcctg 3540
gtatcggtct gcgattccga ctcgtccaac atcaatacaa cctattaatt tcccctcgtc 3600
aaaaataagg ttatcaagtg agaaatcacc atgagtgacg actgaatccg gtgagaatgg 3660
caaaagttta tgcatttctt tccagacttg ttcaacaggc cagccattac gctcgtcatc 3720
aaaatcactc gcatcaacca aaccgttatt cattcgtgat tgcgcctgag cgaggcgaaa 3780
tacgcgatcg ctgttaaaag gacaattaca aacaggaatc gagtgcaacc ggcgcaggaa 3840
cactgccagc gcatcaacaa tattttcacc tgaatcagga tattcttcta atacctggaa 3900
cgctgttttt ccggggatcg cagtggtgag taaccatgca tcatcaggag tacggataaa 3960
atgcttgatg gtcggaagtg gcataaattc cgtcagccag tttagtctga ccatctcatc 4020
tgtaacatca ttggcaacgc tacctttgcc atgtttcaga aacaactctg gcgcatcggg 4080
cttcccatac aagcgataga ttgtcgcacc tgattgcccg acattatcgc gagcccattt 4140
atacccatat aaatcagcat ccatgttgga atttaatcgc ggcctcgacg tttcccgttg 4200
aatatggctc atactcttcc tttttcaata ttattgaagc atttatcagg gttattgtct 4260
catgaccaaa atcccttaac gtgagttttc gttccactga gcgtcagacc ccgtagaaaa 4320
gatcaaagga tcttcttgag atcctttttt tctgcgcgta atctgctgct tgcaaacaaa 4380
aaaaccaccg ctaccagcgg tggtttgttt gccggatcaa gagctaccaa ctctttttcc 4440
gaaggtaact ggcttcagca gagcgcagat accaaatact gttcttctag tgtagccgta 4500
gttaggccac cacttcaaga actctgtagc accgcctaca tacctcgctc tgctaatcct 4560
gttaccagtg gctgctgcca gtggcgataa gtcgtgtctt accgggttgg actcaagacg 4620
atagttaccg gataaggcgc agcggtcggg ctgaacgggg ggttcgtgca cacagcccag 4680
cttggagcga acgacctaca ccgaactgag atacctacag cgtgagctat gagaaagcgc 4740
cacgcttccc gaagggagaa aggcggacag gtatccggta agcggcaggg tcggaacagg 4800
agagcgcacg agggagcttc cagggggaaa cgcctggtat ctttatagtc ctgtcgggtt 4860
tcgccacctc tgacttgagc gtcgattttt gtgatgctcg tcaggggggc ggagcctatg 4920
gaaaaacgcc agcaacgcgg cctttttacg gttcctggcc ttttgctggc cttttgctca 4980
catgttcttt cctgcgttat cccctgattc tgtggataac cgtattaccg cctttgagtg 5040
agctgatacc gctcgccgca gccgaacgac cgagcgcagc gagtcagtga gcgaggaagc 5100
ggaagagcgc ccaatacgca aaccgcctct ccccgcgcgt tggccgattc attaatgcag 5160
ctggcgtaat agcgaagagg cccgcaccga tcgcccttcc caacagttgc gcagcctgaa 5220
tggcgaatgg cgattccgtt gcaatggctg gcggtaatat tgttctggat attaccagca 5280
aggccgatag tttgagttct tctactcagg caagtgatgt tattactaat caaagaagta 5340
ttgcgacaac ggttaatttg cgtgatggac agactctttt actcggtggc ctcactgatt 5400
ataaaaacac ttctcaggat tctggcgtac cgttcctgtc taaaatccct ttaatcggcc 5460
tcctgtttag ctcccgctct gattctaacg aggaaagcac gttatacgtg ctcgtcaaag 5520
caaccatagt acgcgccctg tagcggcgca ttaagcgcgg cgggtgtggt ggttacgcgc 5580
agcgtgaccg ctacacttgc cagcgcccta gcgcccgctc ctttcgcttt cttcccttcc 5640
tttctcgcca cgttcgccgg ctttccccgt caagctctaa atcgggggct ccctttaggg 5700
ttccgattta gtgctttacg gcacctcgac cccaaaaaac ttgattaggg tgatggttca 5760
cgtagtgggc catcgccctg atagacggtt tttcgccctt tgacgttgga gtccacgttc 5820
tttaatagtg gactcttgtt ccaaactgga acaacactca accctatctc ggtctattct 5880
tttgatttat aagggatttt gccgatttcg gcctattggt taaaaaatga gctgatttaa 5940
caaaaattta acgcgaattt taacaaaata ttaacgctta caatttaaat atttgcttat 6000
acaatcttcc tgtttttggg gcttttctga ttatcaaccg gggtacatat gattgacatg 6060
ctagttttac gattaccgtt catcgcc 6087
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| СРЕДСТВА И СПОСОБ ПОЛУЧЕНИЯ ВИРУСНЫХ ВЕКТОРОВ И ВАРИАНТЫ ИХ ПРИМЕНЕНИЯ | 2018 |
|
RU2818529C2 |
| ВИРУСНЫЕ ВЕКТОРЫ НА ОСНОВЕ AAV И ПУТИ ИХ ПРИМЕНЕНИЯ | 2019 |
|
RU2796274C2 |
| ОПОСРЕДОВАННЫЙ АДЕНОАССОЦИИРОВАННЫМ ВИРУСОМ ПЕРЕНОС ГЕНОВ В ЦЕНТРАЛЬНУЮ НЕРВНУЮ СИСТЕМУ | 2014 |
|
RU2801511C1 |
| ОПОСРЕДОВАННЫЙ АДЕНОАССОЦИИРОВАННЫМ ВИРУСОМ ПЕРЕНОС ГЕНОВ В ЦЕНТРАЛЬНУЮ НЕРВНУЮ СИСТЕМУ | 2014 |
|
RU2692251C2 |
| ВЕКТОР НА ОСНОВЕ АДЕНОАССОЦИИРОВАННОГО ВИРУСА ДЛЯ ТЕРАПЕВТИЧЕСКОЙ ДОСТАВКИ В ЦЕНТРАЛЬНУЮ НЕРВНУЮ СИСТЕМУ | 2016 |
|
RU2804953C2 |
| ВЕКТОР НА ОСНОВЕ АДЕНОАССОЦИИРОВАННОГО ВИРУСА ДЛЯ ТЕРАПЕВТИЧЕСКОЙ ДОСТАВКИ В ЦЕНТРАЛЬНУЮ НЕРВНУЮ СИСТЕМУ | 2016 |
|
RU2751952C2 |
| ПОЛУЧЕНИЕ УЛУЧШЕННОЙ ЧЕЛОВЕЧЕСКОЙ PAH ДЛЯ ЛЕЧЕНИЯ ТЯЖЕЛОЙ PKU С ПОМОЩЬЮ ГЕННОЙ ЗАМЕСТИТЕЛЬНОЙ ТЕРАПИИ, НАПРАВЛЕННОЙ НА ПЕЧЕНЬ | 2019 |
|
RU2839587C2 |
| ОПТИМИЗИРОВАННЫЕ ГЕНЫ И ЭКСПРЕССИОННЫЕ КАССЕТЫ CLN1, И ИХ ПРИМЕНЕНИЕ | 2017 |
|
RU2764919C2 |
| ГЕННАЯ ТЕРАПИЯ НЕЙРОДЕГЕНЕРАТИВНЫХ НАРУШЕНИЙ | 2021 |
|
RU2836835C2 |
| ГЕННАЯ ТЕРАПИЯ НЕЙРОДЕГЕНЕРАТИВНЫХ НАРУШЕНИЙ | 2010 |
|
RU2603740C2 |
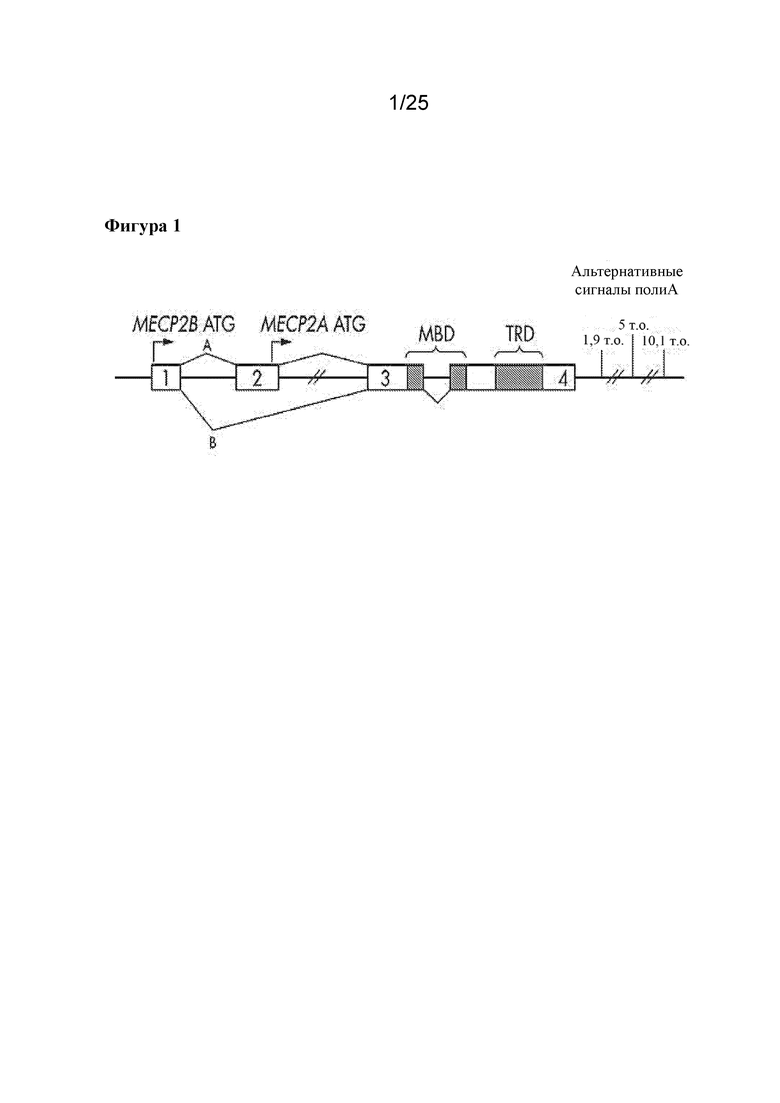
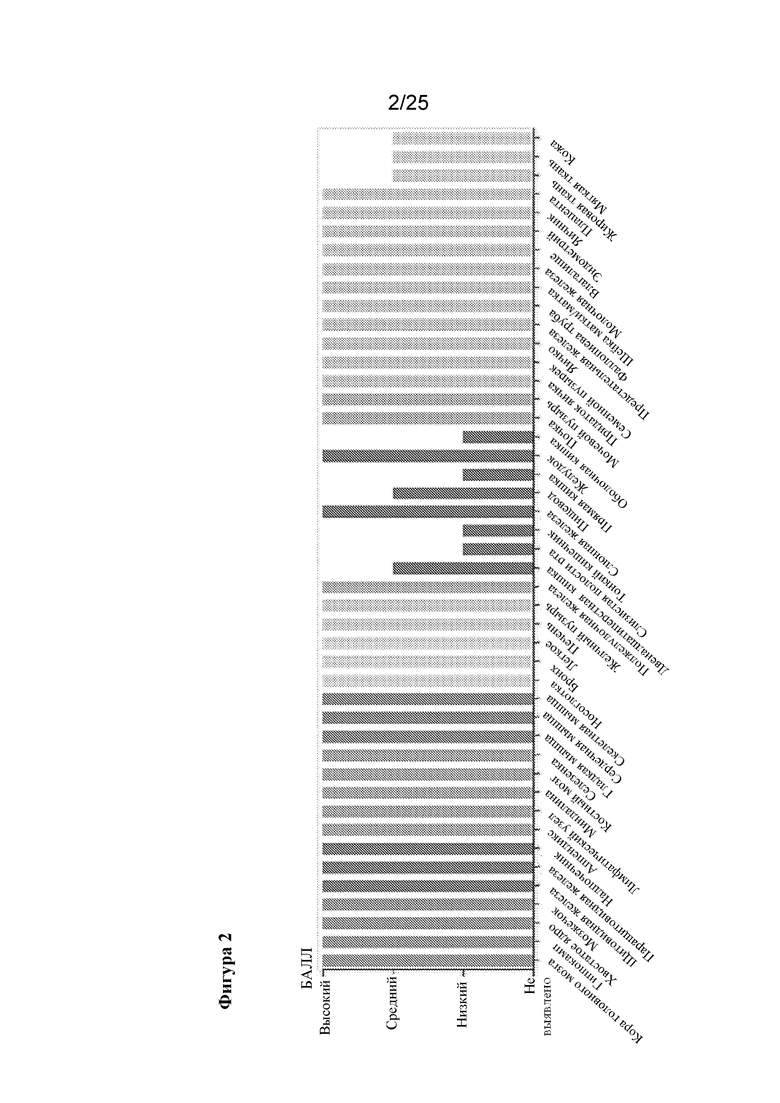

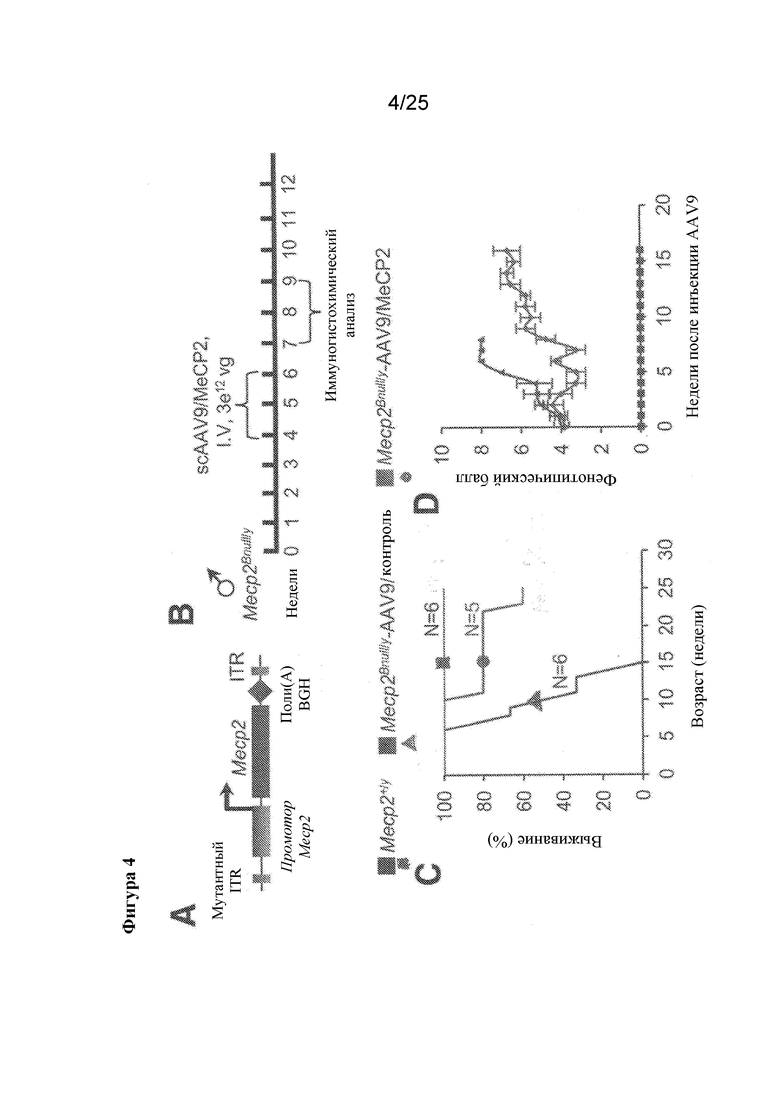
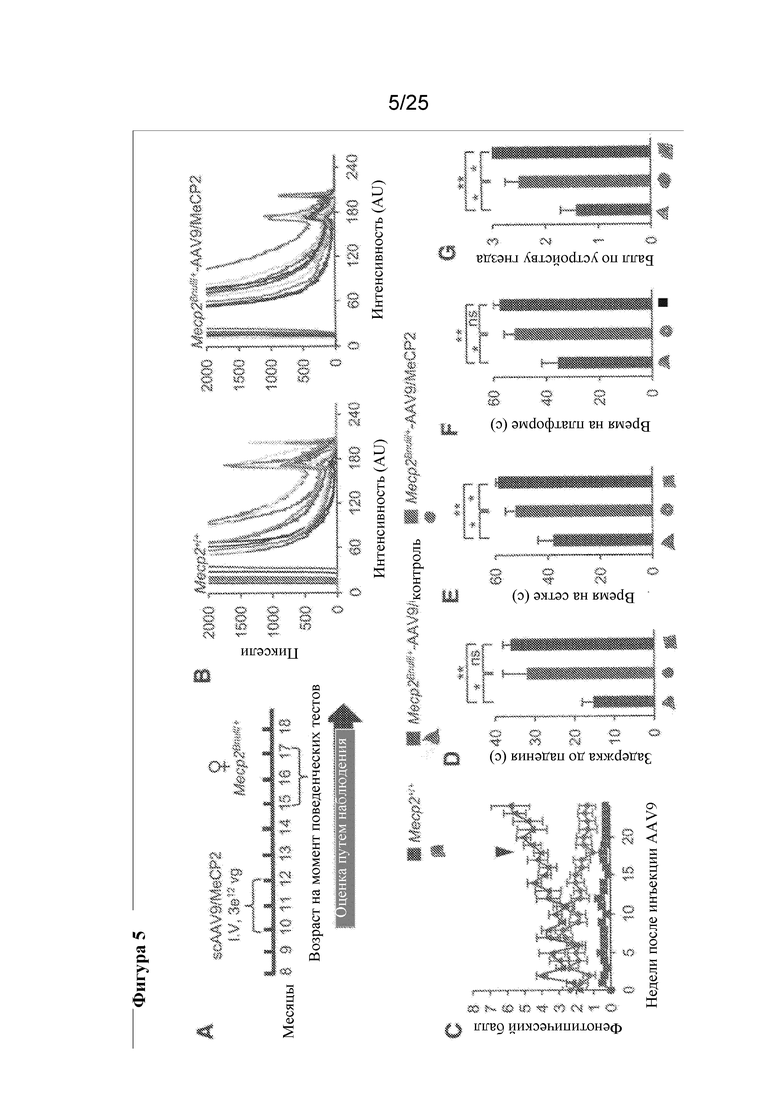

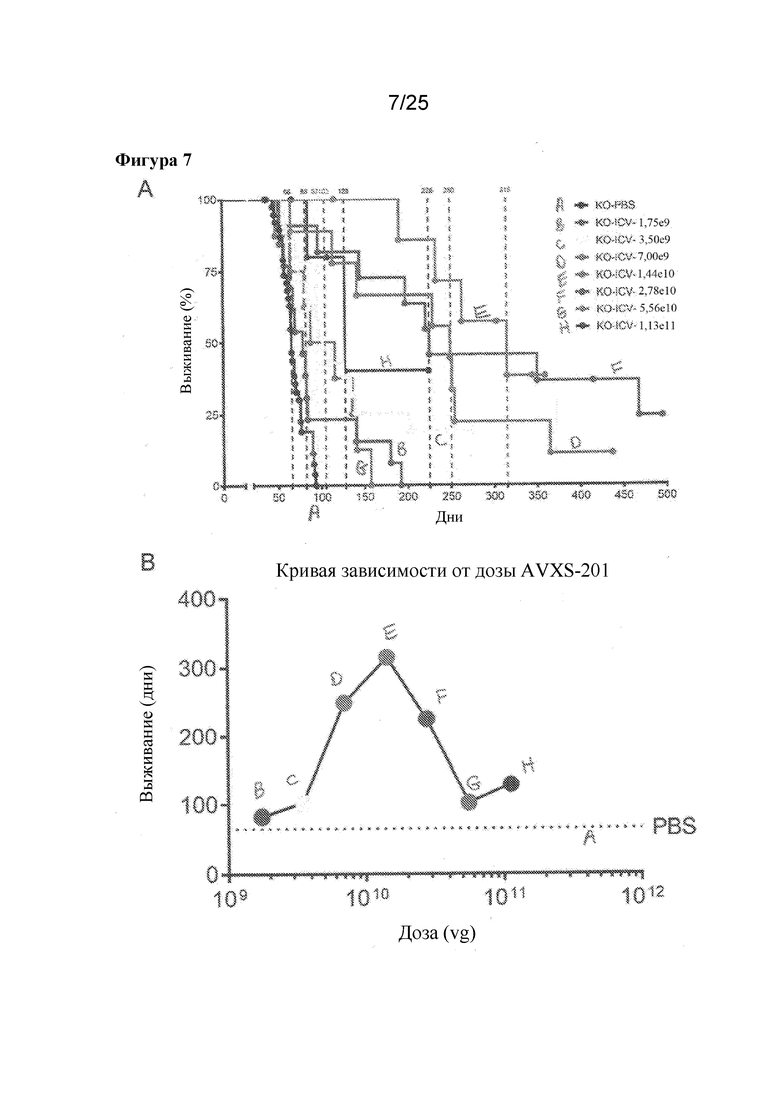
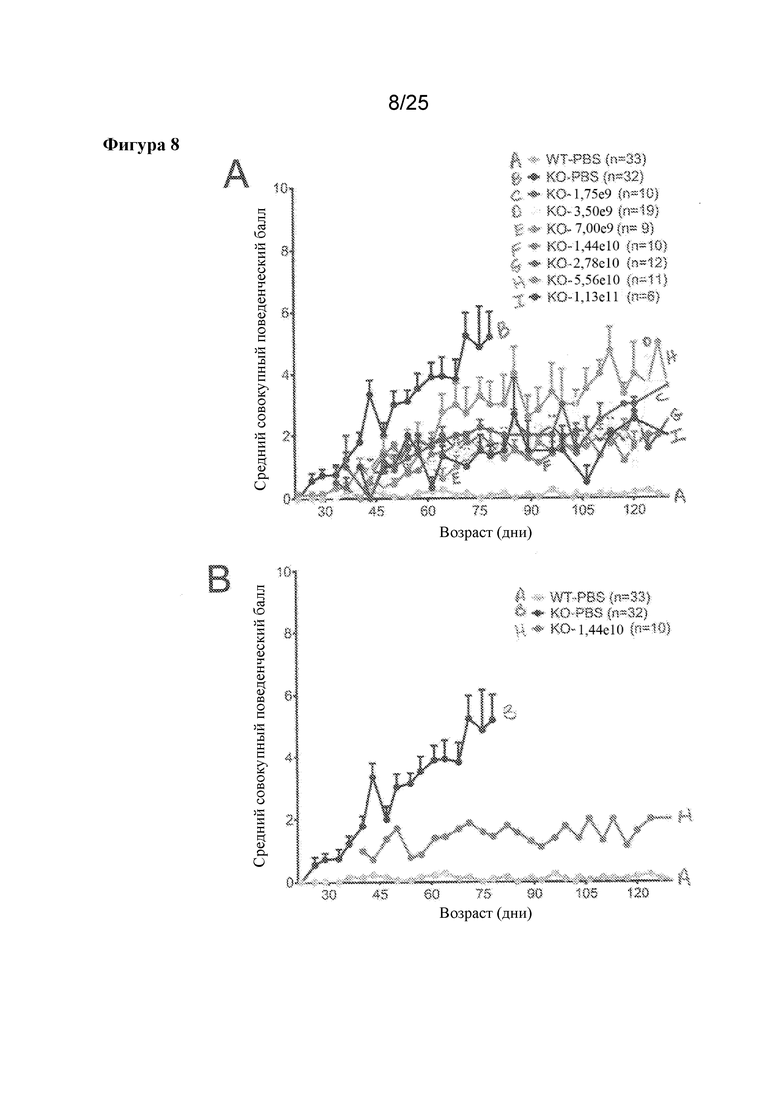
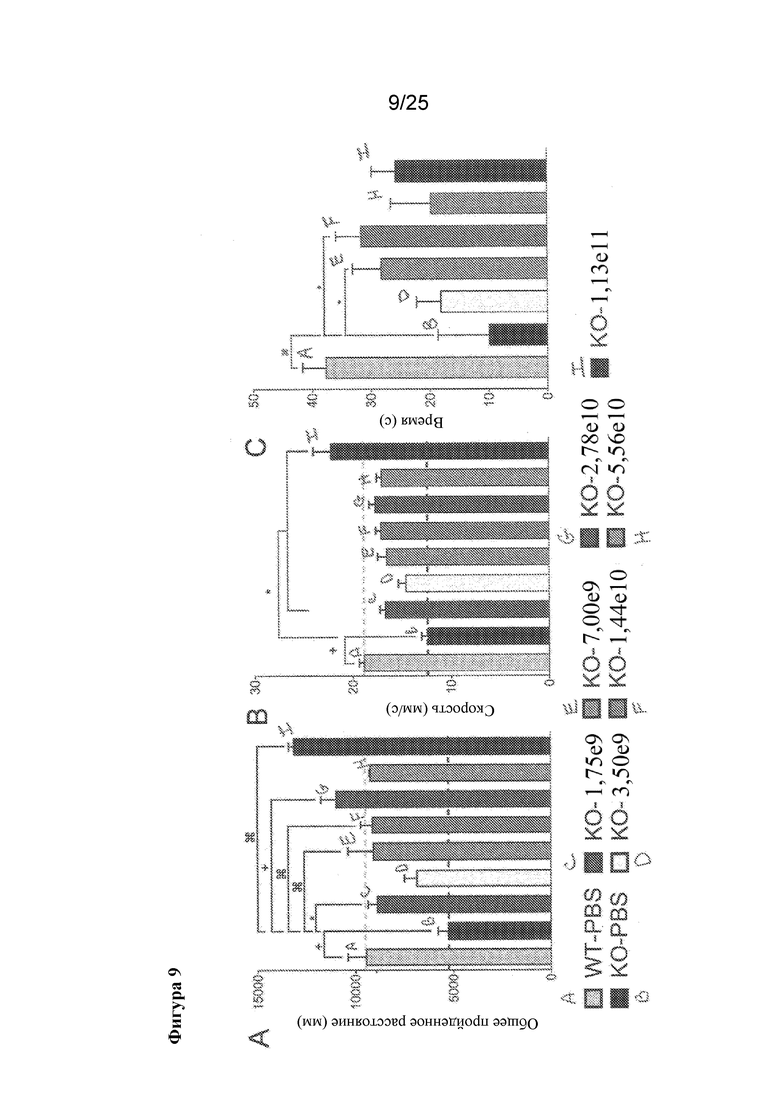

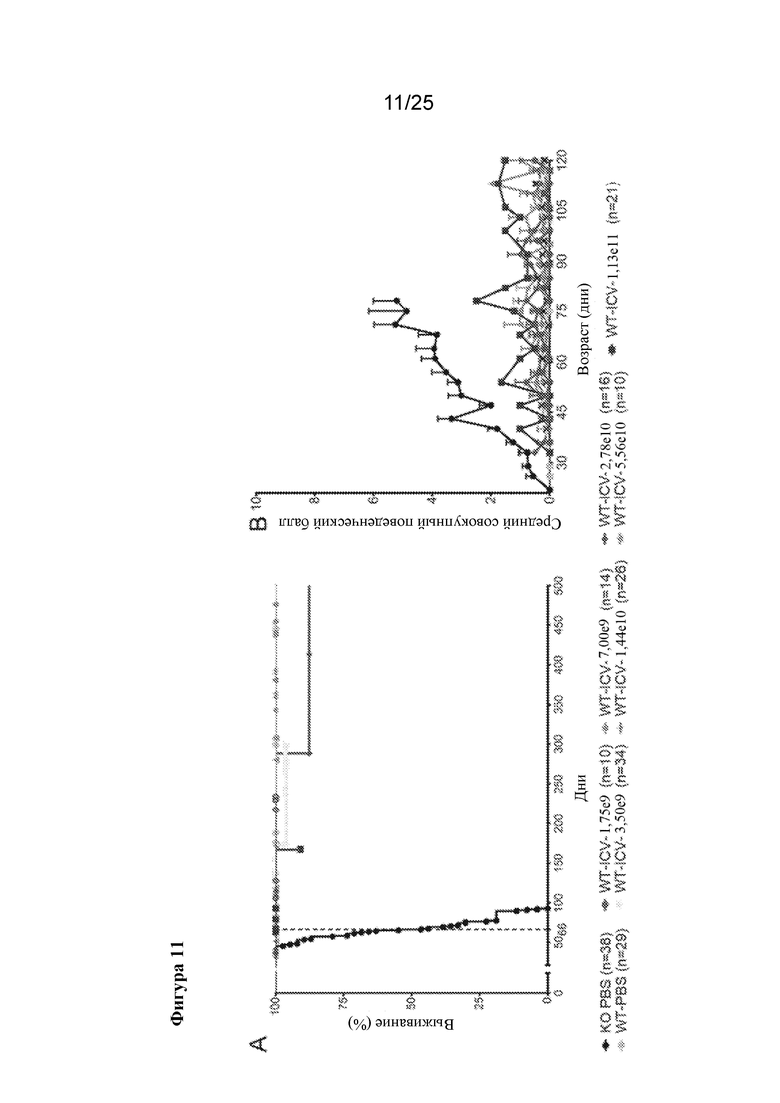
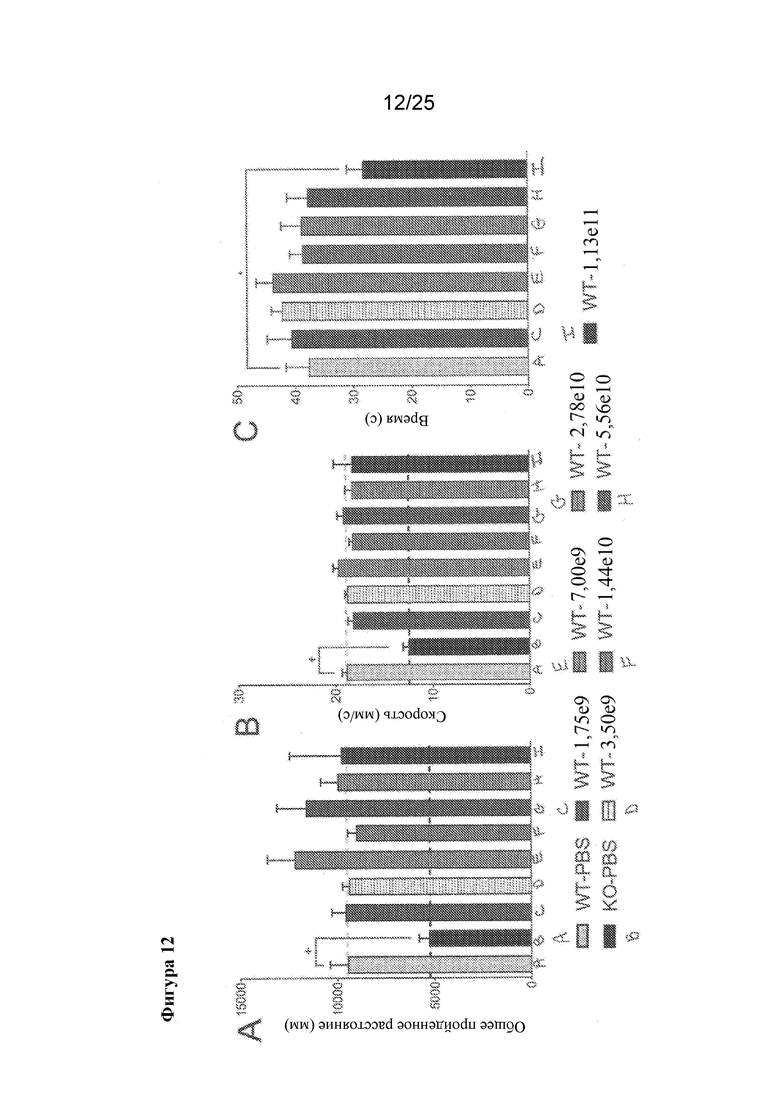

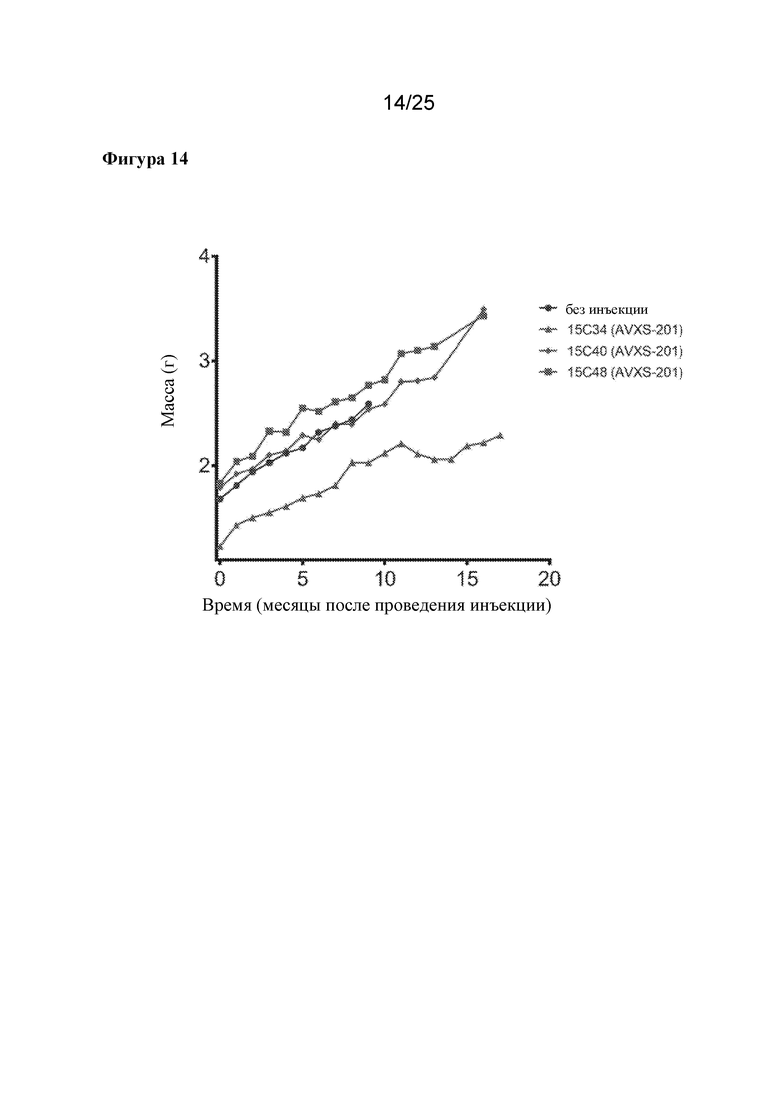
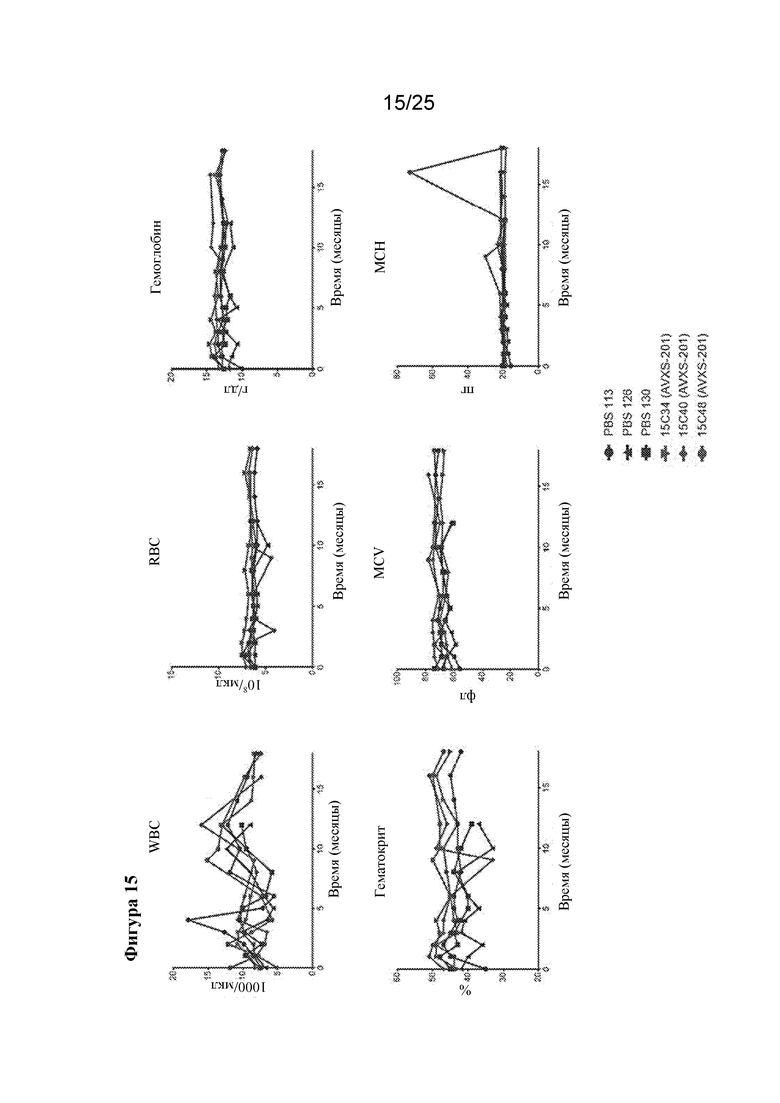
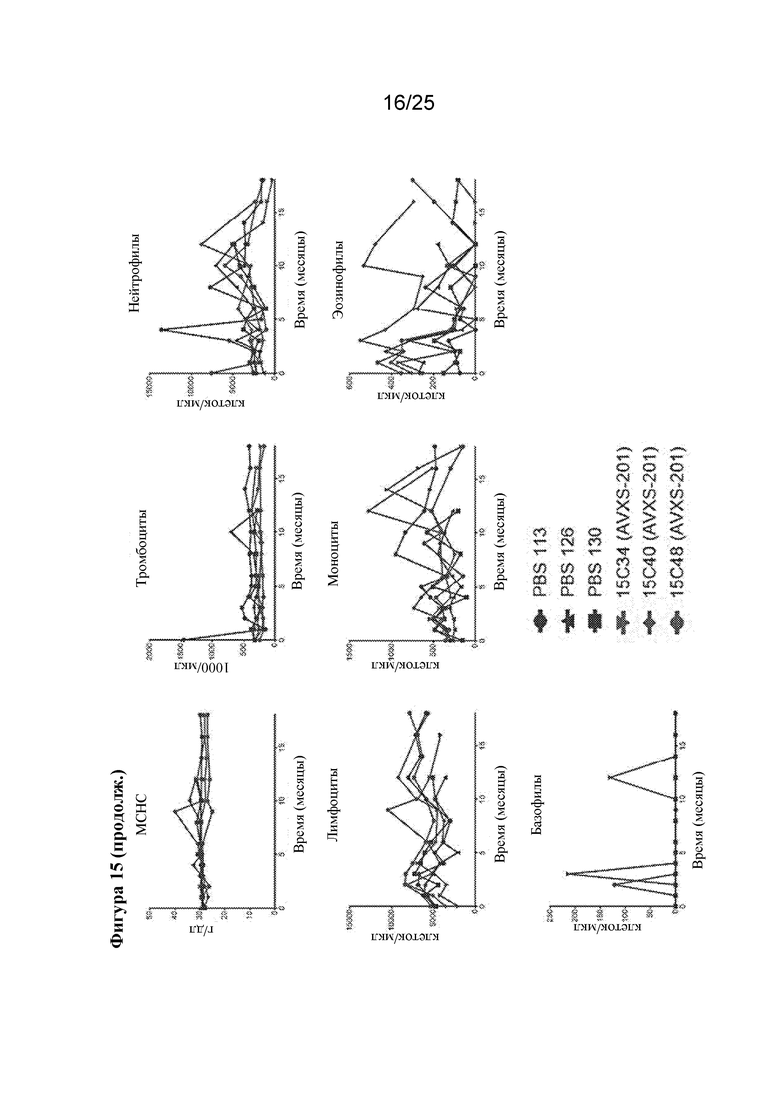

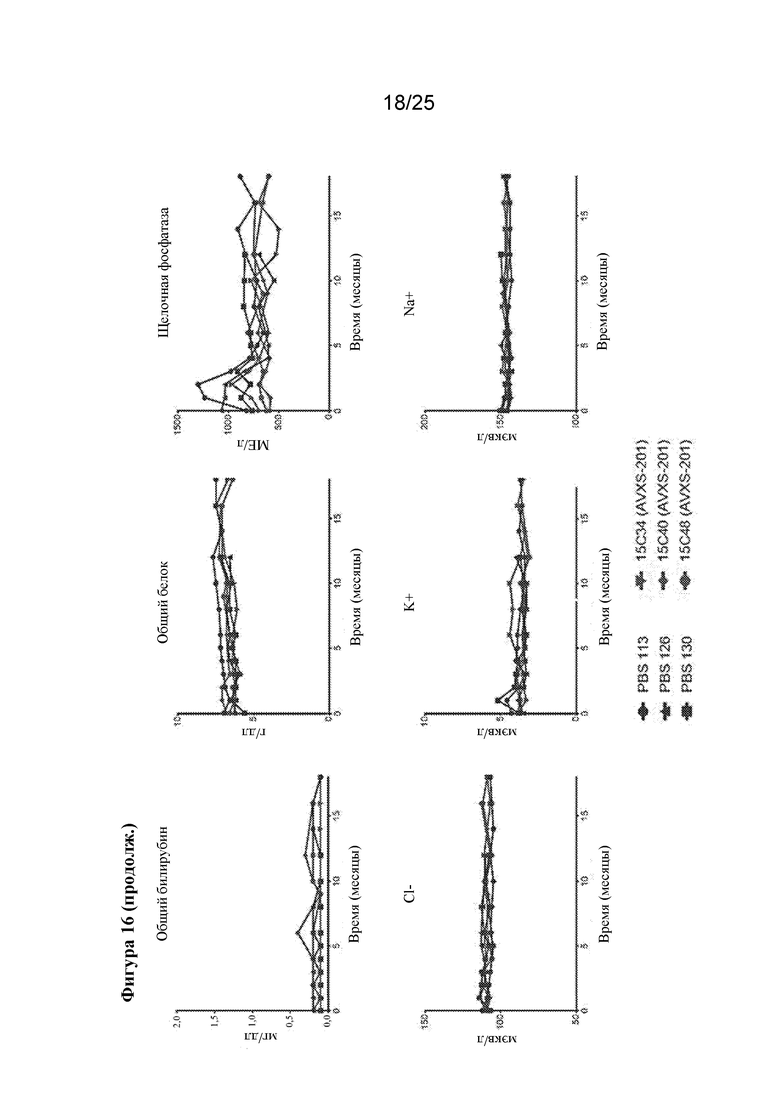
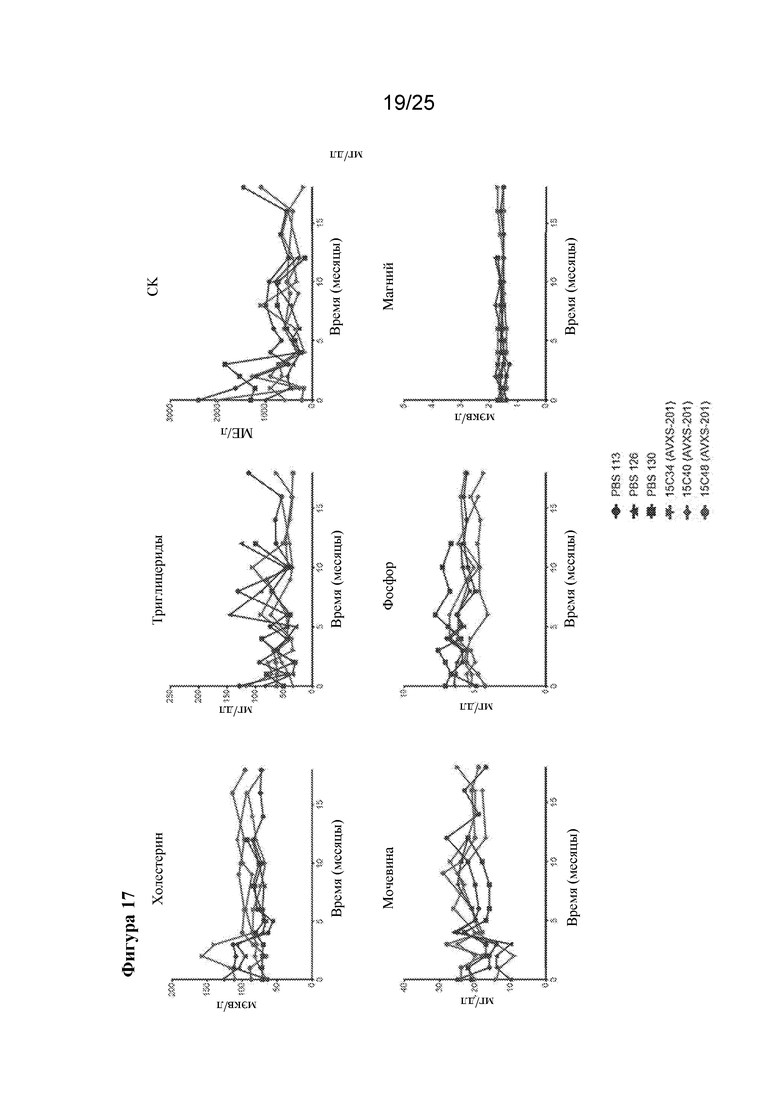
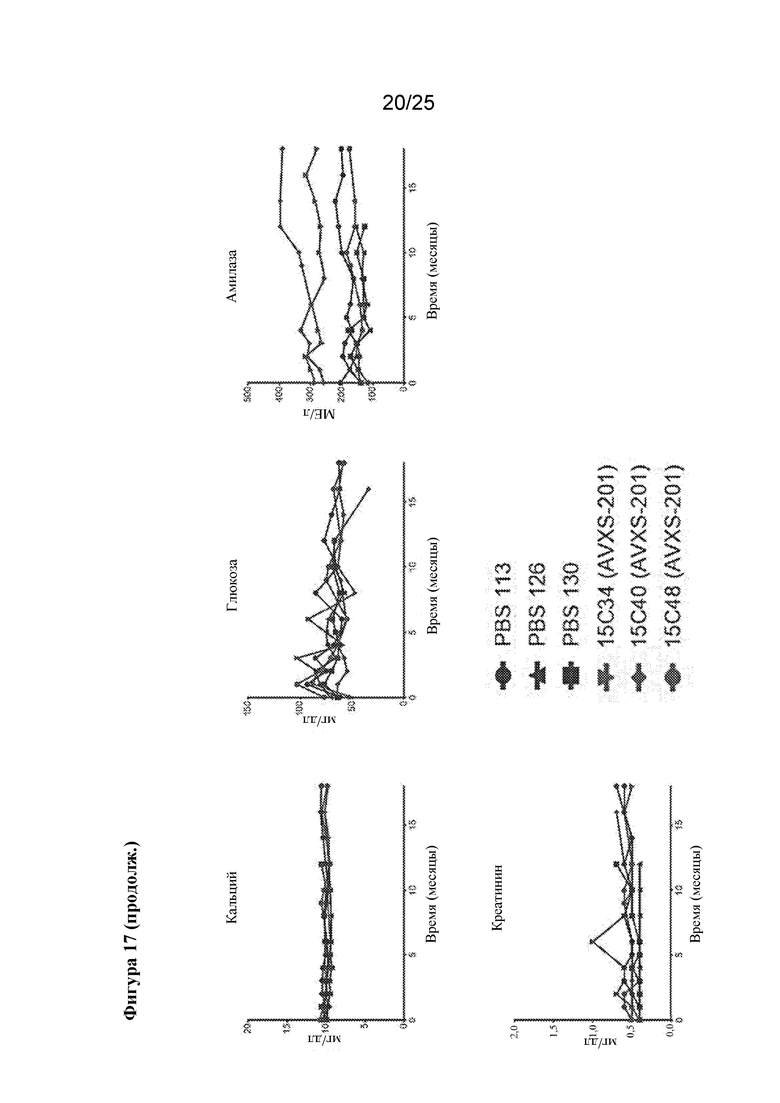
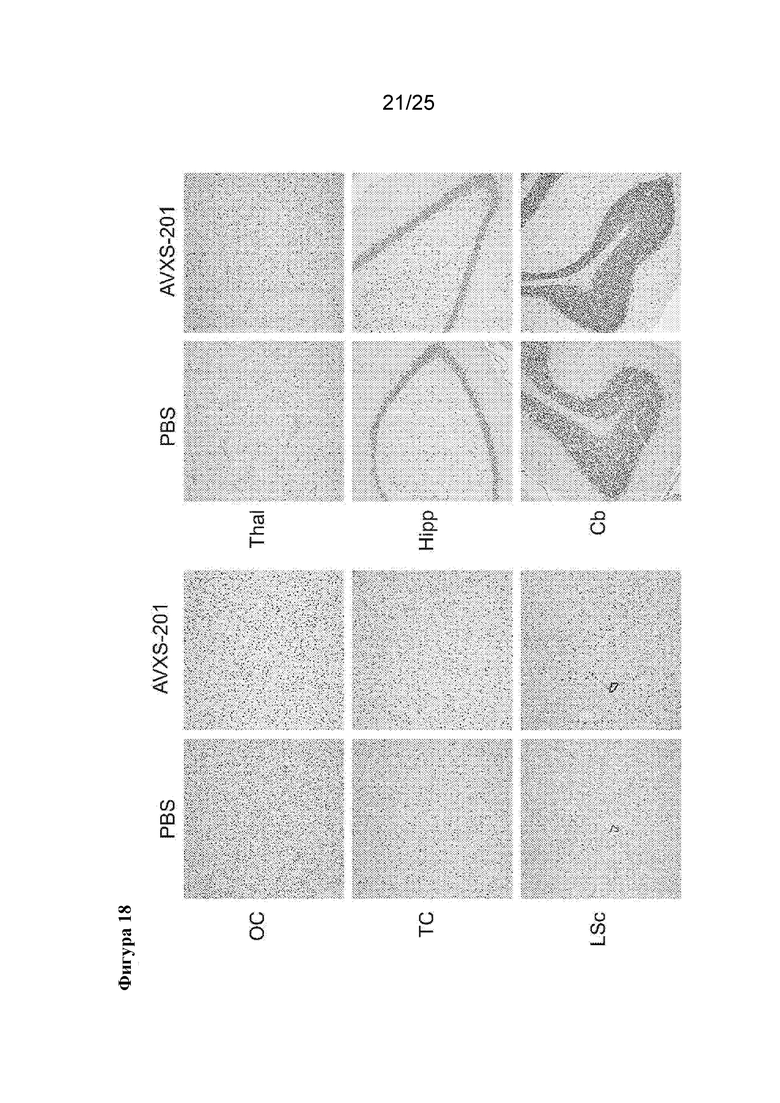
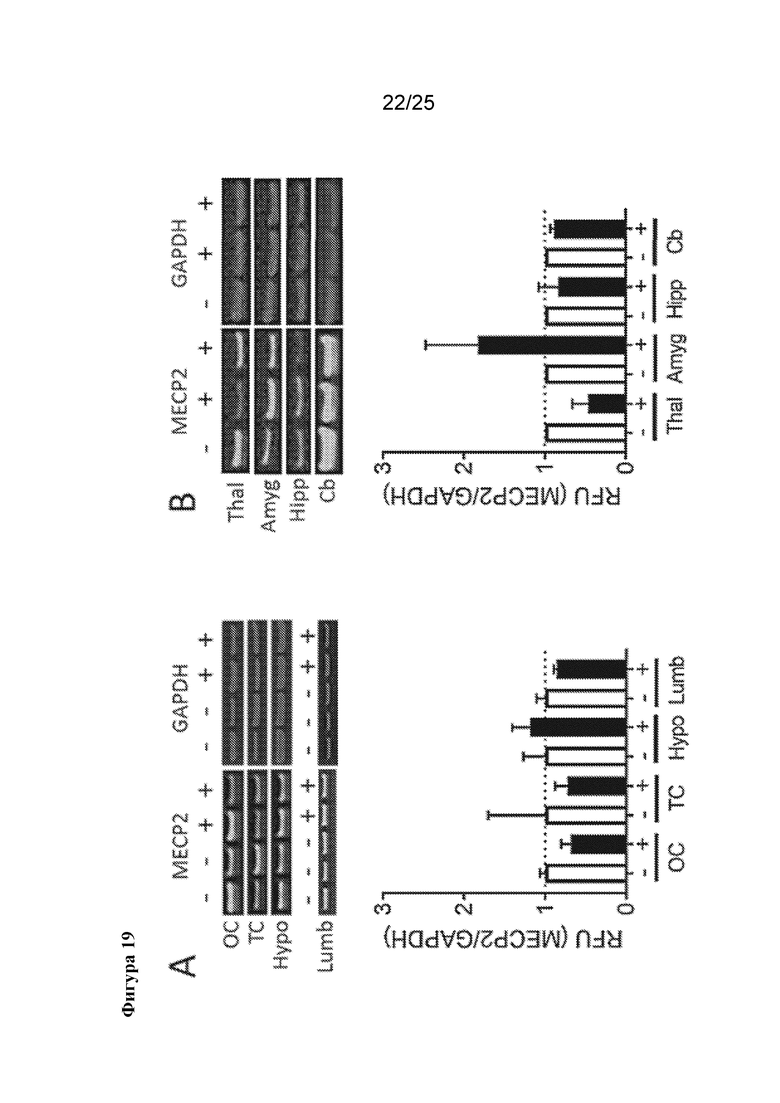
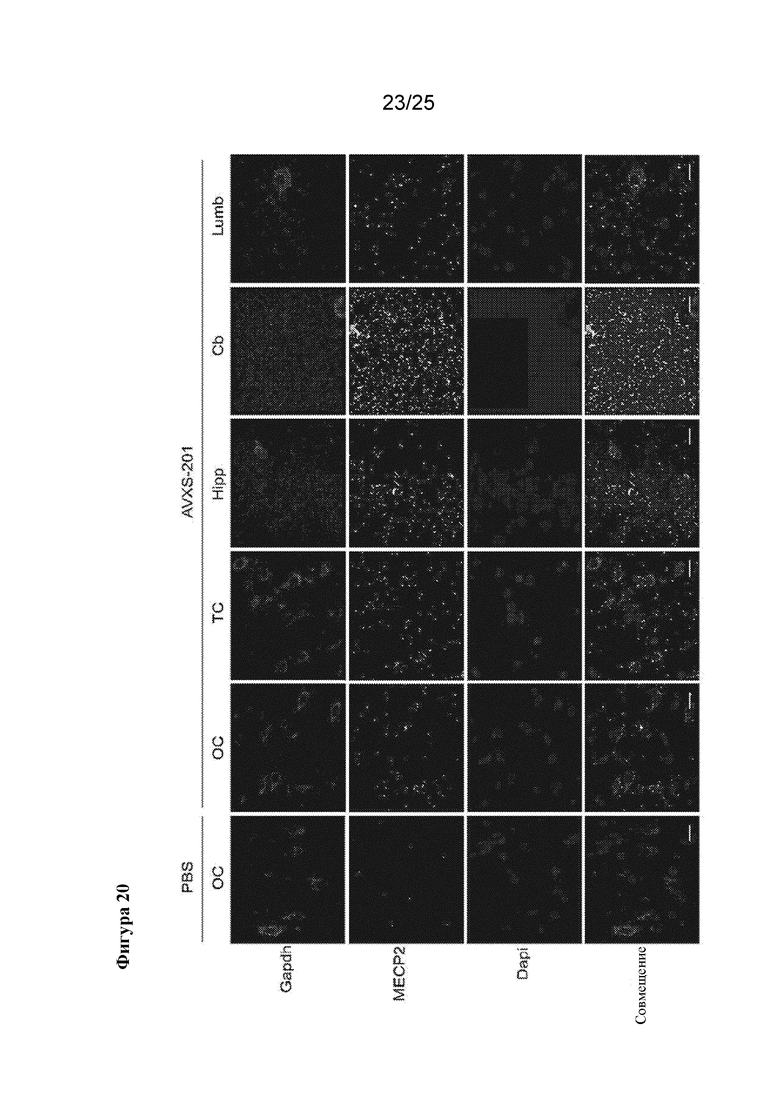
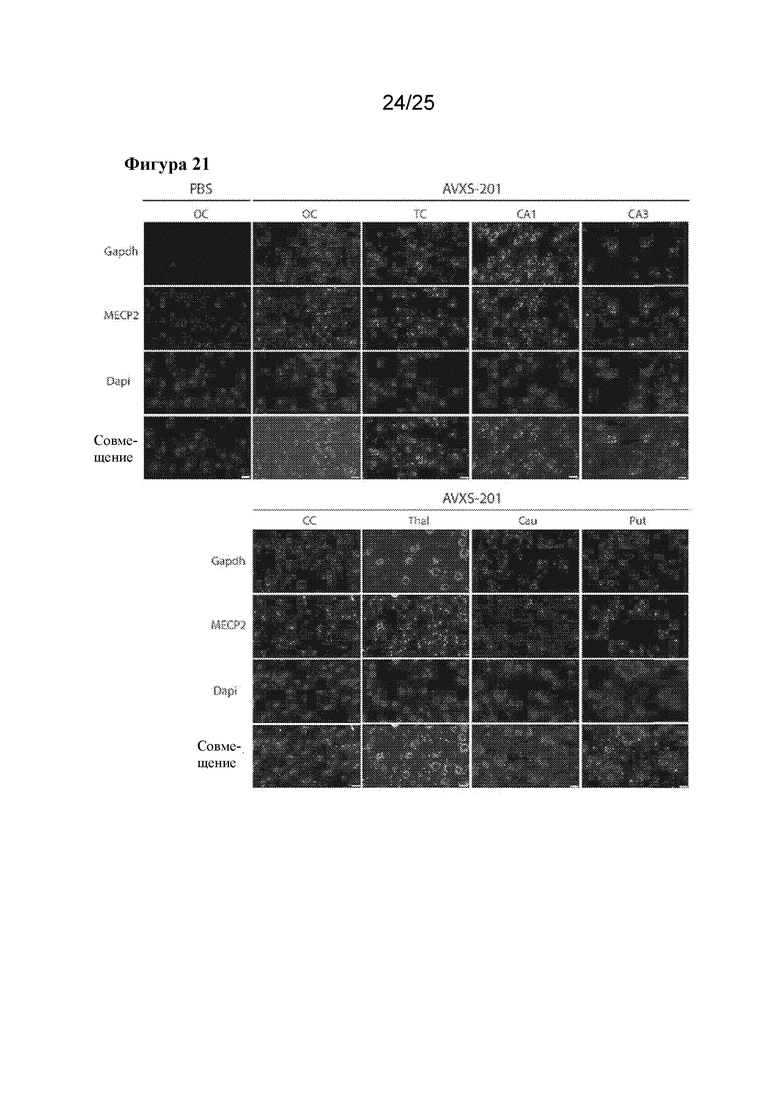
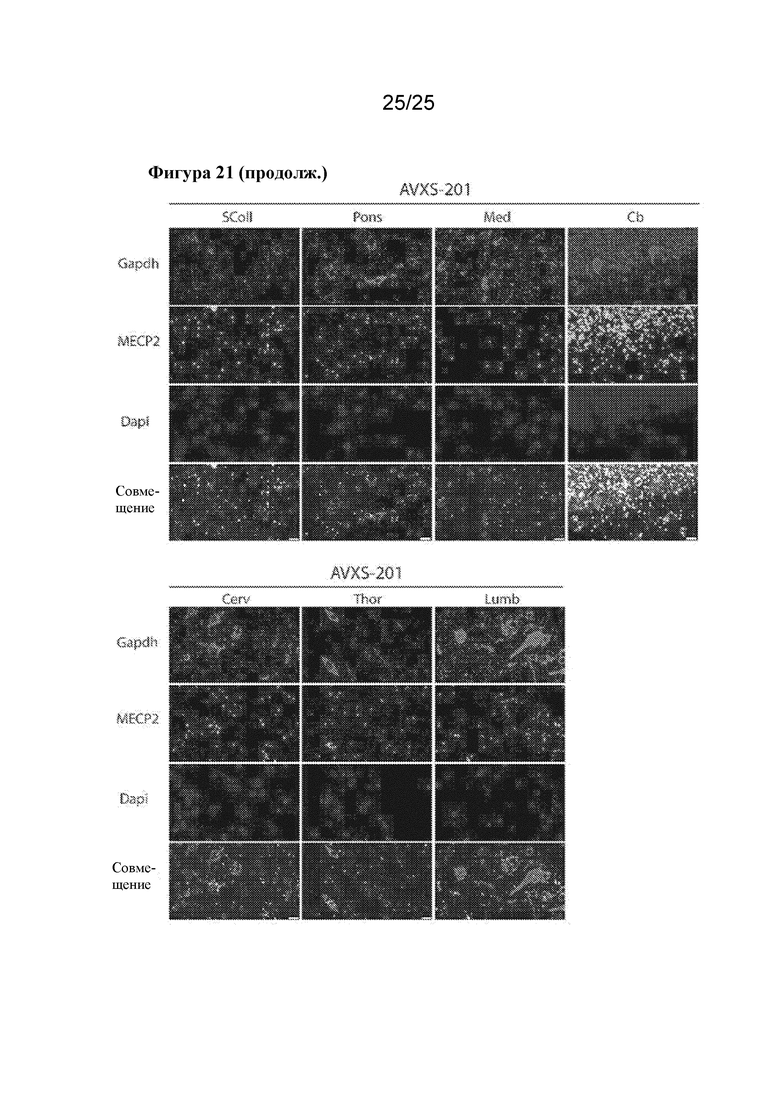
Изобретение относится к биотехнологии. Представлен аденоассоциированный вирусный вектор (AAV) для экспрессии метил-CpG-связывающего белка 2 (MECP2) для лечения синдрома Ретта. Вирусный вектор содержит генную кассету, содержащую промотор, состоящий из SEQ ID NO: 2, интрон SV20, полинуклеотидную последовательность, кодирующую метил-CpG-связывающий белок 2 (MECP2), с последовательностью SEQ ID NO: 3 и синтетический сигнал полиаденилирования. Генная кассета фланкирована мутантным инвертированным концевым повтором и интактным инвертированным концевым повтором AAV2. Представлена вирусная частица, содержащая AAV вектор, фармацевтическая композиция для лечения синдрома Реттаэ, содержащая эффективное количество AAV вектора или вирусной частицы и фармацевтически приемлемый носитель. Представлен способ лечения синдрома Ретта, применение AAV вектора, вирусной частицы или фармацевтической композиции для лечения синдрома Ретта у пациента, а также самокомплементарный аденоассоциированный вирус серотипа 9 (scAAV9) для экспрессии метил-CpG-связывающего белка 2 (MECP2) для лечения синдрома Ретта. Изобретение позволяет доставку полинуклеотидов MECP2 в центральную нервную систему и экспрессию в ней таких полинуклеотидов для создания средства лечения синдрома Ретта. 6 н. и 16 з.п. ф-лы, 3 табл., 21 ил., 8 пр.
1. Аденоассоциированный вирусный вектор (AAV) для экспрессии метил-CpG-связывающего белка 2 (MECP2) для лечения синдрома Ретта,
где вирусный вектор содержит генную кассету, содержащую промотор, состоящий из SEQ ID NO: 2, интрон SV20, полинуклеотидную последовательность, кодирующую метил-CpG-связывающий белок 2 (MECP2), с последовательностью SEQ ID NO: 3 и синтетический сигнал полиаденилирования,
где генная кассета фланкирована мутантным инвертированным концевым повтором и интактным инвертированным концевым повтором AAV2.
2. AAV вектор по п.1, где ААV вектор представляет собой самокомплементарный (scAAV).
3. AAV вектор по п.1 или 2, дополнительно содержащий синтетическую сигнальную последовательность полиаденилирования.
4. AAV вектор по любому из пп.1-3, где сигнальная последовательность полиаденилирования содержит SEQ ID NO: 4.
5. AAV вектор по любому из пп.1-4, содержащий по порядку мутантный ITR AAV2, промотор, состоящий из SEQ ID NO: 2, интрон SV40, полинуклеотидную последовательность, кодирующую MECP2, синтетическую сигнальную последовательность полиаденилирования и ITR AAV2 дикого типа.
6. AAV вектор по п.5, где полинуклеотидная последовательность, кодирующая MECP2, содержит SEQ ID NO: 3, и сигнальная последовательность полиаденилирования содержит SEQ ID NO: 4.
7. AAV вектор по любому из пп.1-6, содержащий полинуклеотидную последовательность SEQ ID NO: 1.
8. Вирусная частица, содержащая AAV вектор по любому из пп.1-7.
9. Вирусная частица по п.8, дополнительно содержащая один или несколько капсидных белков.
10. Вирусная частица по п.8 или 9, где вирус представляет собой AAV.
11. Вирусная частица п.10, где AAV представляет собой AAV9.
12. Фармацевтическая композиция для лечения синдрома Ретта, содержащая
i) эффективное количество AAV вектора по любому из пп.1-7 или вирусную частицу по любому из пп.8-11 и
ii) фармацевтически приемлемый носитель.
13. Фармацевтическая композиция по п.12, где композиция входит в состав для интратекального (ИТ) введения.
14. Фармацевтическая композиция по п.12 или 13 дополнительно содержащая неионное, низкоосмолярное контрастное средство.
15. Фармацевтическая композиция по п.12 или 13 для применения в комбинации с неионным, низкоосмолярным контрастным средством.
16. Фармацевтическая композиция по п.14 или 15, где неионное, низкоосмолярное контрастное средство содержит один или несколько из йобитридола, йогексола, йомепрола, йопамидола, йопентола, йопромида, йоверсола и йоксилана.
17. Фармацевтическая композиция по п.14 или 15, где неионное, низкоосмолярное контрастное средство содержит йогексол.
18. Способ лечения синдрома Ретта, включающий введение пациенту терапевтически эффективного количества AVV вектора по любому из пп.1-7, вирусной частицы по любому из пп.8-11 или фармацевтической композиции по любому из пп.12-17.
19. Способ по п.18, где AAV вектор, вирусную частицу или фармацевтическую композицию вводят интратекальным (ИТ) путем введения.
20. Применение AAV вектора по любому из пп.1-7, вирусной частицы по любому из пп.8-11 или фармацевтической композиции по любому из пп.12-17 для лечения синдрома Ретта у пациента.
21. Применение по п.20, где AAV вектор, вирусную частицу или фармацевтическую композицию вводят интратекальным (ИТ) путем введения.
22. Самокомплементарный аденоассоциированный вирус серотипа 9 (scAAV9) для экспрессии метил-CpG-связывающего белка 2 (MECP2) для лечения синдрома Ретта, где scAAV9 содержит полинуклеотид, содержащий SEQ ID NO: 1.
| Токарный резец | 1924 |
|
SU2016A1 |
| Многоступенчатая активно-реактивная турбина | 1924 |
|
SU2013A1 |
| Колосоуборка | 1923 |
|
SU2009A1 |
| БОГОСЛОВСКАЯ Е.В | |||
| Безопасность использования ретровирусных векторов в генной терапии | |||
| Вестник РАМН, 2012, N10, с.55-61. | |||
Авторы
Даты
2023-01-16—Публикация
2017-11-17—Подача