Изобретение относится к аналитической химии, в частности к способам люминесцентного определения тербия, и может быть использовано для определения следовых количеств тербия при анализе высокочистых лантанидов.
Известны способы люминесцентного определения тербия в комплексе с органическими реагентами:
Патент РФ № 2412435 «Люминесцентный способ определения тербия». Изобретение относится к области аналитической химии - к способам люминесцентного определения тербия, и может быть использовано для определения следовых количеств тербия при анализе высококачественных лантанидов и в природных водах. В качестве комплексообразователя используется органический реагент (R) - дифениловый эфир сульфосалициловой кислоты (ДЭСК), и в раствор люминесцирующего комплексного соединения тербия с ДЭСК приливают поверхностно-активное вещество (ПАВ) - цетилпиридиний бромистый, в соотношениях Tb:K:ПАВ=1:2:13 и слабыми растворами аммиака и соляной кислоты создают рН=7,5±0,1. Достигается повышение точности, чувствительности и селективности анализа.
Патент РФ № 2194013 «Люминесцентный способ определения тербия». Изобретение относится к аналитической химии, в частности к способам люминесцентного определения тербия. Тербий переводят в люминесцирующее комплексное соединение с органическим реагентом (R) - метиловым эфиром S-(4-броманилидом) сульфосалициловой кислоты в присутствии катионного поверхностно-активного вещества (ПАВ) хлорида децилпиридиния. Соотношение Tb:R:ПАВ=1: 2: 13, рН 7,9±0,08. Способ отличается высокой селективностью и воспроизводимостью. Он позволяет одновременно определять Tb, Dy, Sm, Eu в оксидах лантаноидов.
Патент РФ № 2506569 «Люминесцентный способ определения тербия». Изобретение относится к области аналитической химии, а именно к способу люминесцентного определения тербия. Способ включает перевод тербия в люминесцирующее соединение с органическим реагентом. В качестве реагента используют 1,2-диоксибензол-3,5-дисульфокислоту (ДБСК) и в раствор люминесцирующего комплексного соединения тербия с ДБСК добавляют этилендиаминтетрауксусную кислоту (ЭДТА) в соотношении Tb:ДБСК:ЭДТА=1:1:1 при рН=12,0-13,0.
Недостатками предложенных способов являются - недостаточная чувствительность, селективность и устойчивость во времени стояния и облучения, а также высокая трудоемкость получения комплексного соединения и продолжительность анализа.
Задача, решаемая изобретением, заключается в снижении предела обнаружения, повышение устойчивости, чувствительности, селективности и снижение продолжительности анализа.
Результат достигается тем, что тербий переводят в люминесцирующее комплексное соединение с органическим реагентом (R) - офлоксацином (ОФ), соотношение Tb:R=1:2, при рН=3,0±0,1.
Пример 1.
Для получения растворов хлоридов лантанидов, их оксиды предварительно прокаливали в течение одного часа в муфельной печи при температуре 650-700°C и охлаждают в эксикаторе. Навеску оксидов лантанидов по расчетам их 10-3 М концентраций обрабатывают соляной кислотой и Н2О2, а затем раствор выпаривают. Сухой остаток рездкоземельных элементов (РЗЭ) растворяют в дистиллированной воде. Растворы с меньшей концентрацией реагента готовили соответствующим разбавлением. Концентрацию стандартного раствора хлорида тербия контролировали комплексонометрическим методом. Титрование производили в присутствии уротропина, в качестве индикатора использовали арсеназо I. Раствор нолицина с концентрацией 10-3 М готовят соответствующим разбавлением концентрированного этанольного раствора. Кислотность среды создают добавлением водного раствора аммиака до рН рН=5,9±0,1. Для определения содержания тербия в оксидах РЗЭ применяли метод добавок.
При добавлении к раствору тербия раствора нолицина, установлении рН=5,9±0,1 и облучении УФ-светом наблюдается свечение зеленого цвета, характерное для ионов тербия.
Пример 2.
Для получения растворов хлоридов лантанидов, их оксиды предварительно прокаливали в течение одного часа в муфельной печи при температуре 650-700°C и охлаждают в эксикаторе. Навеску оксидов лантанидов по расчетам их 10-5 М концентраций обрабатывают соляной кислотой и Н2О2, а затем раствор выпаривают. Сухой остаток рездкоземельных элементов (РЗЭ) растворяют в дистиллированной воде. Растворы с меньшей концентрацией реагента готовили соответствующим разбавлением. Концентрацию стандартного раствора хлорида тербия контролировали комплексонометрическим методом. Титрование производили в присутствии уротропина, в качестве индикатора использовали арсеназо I.
Растворы офлоксацина (ОФ) готовили из точной навески 0,0903 г, растворяли в этиловом спирте, отфильтровали раствор и переносили в мерную колбу на 50 мл.
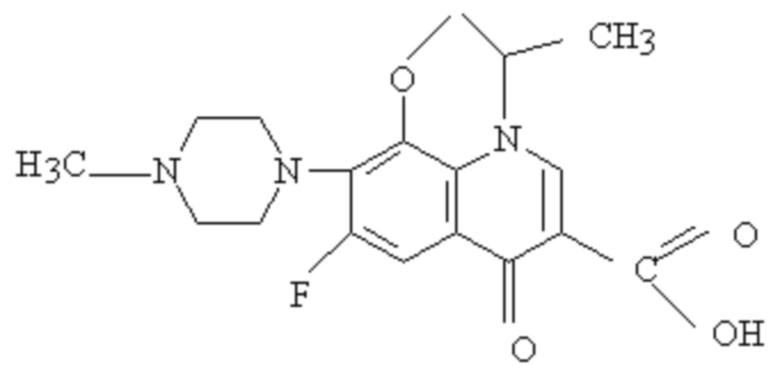
C18H20FN3O4 (ОФ)
МВ=361 г/моль
9-фтор-2,3-дигидро-3-метил-10-(4-метил-1-пиперазинил)-7-оксо-7Н пиридо (1,2,3-de)-1,4-бензоксазин-6-карбоновая кислота.
В ходе проведенных поисковых работ обнаружена яркая люминесцентная реакция Tb с офлоксацином (ОФ) зеленого цвета.
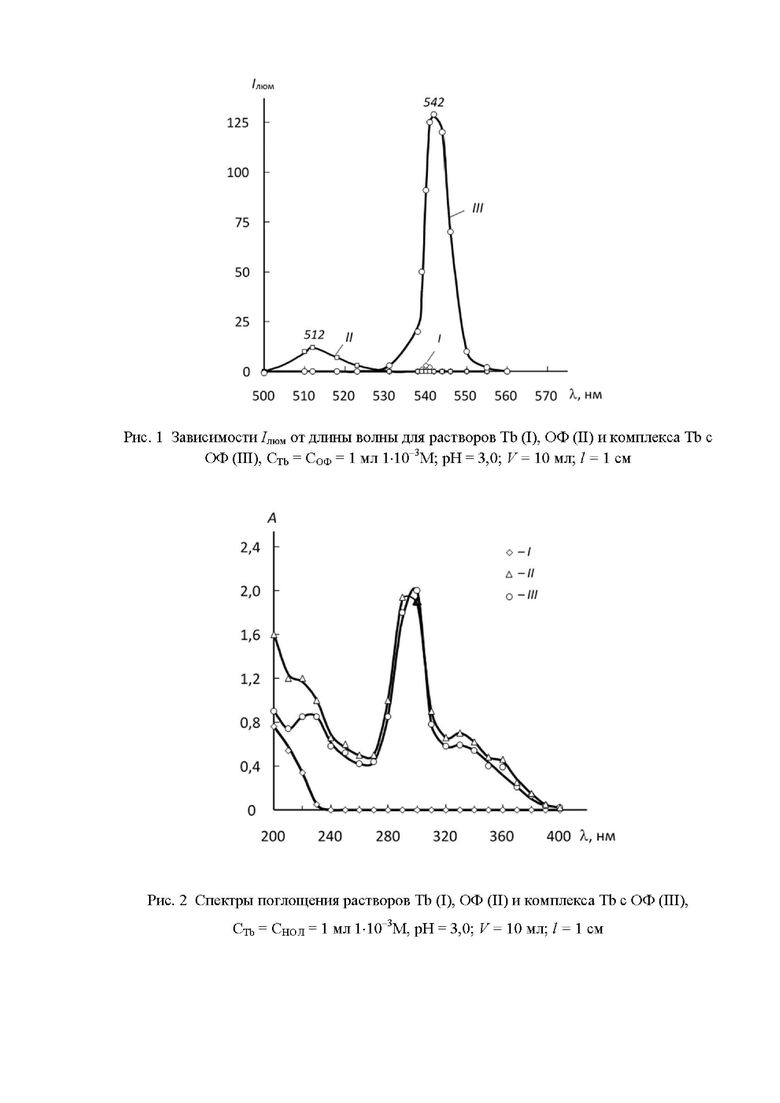
Исследована зависимость интенсивности люминесценции ионов Tb в комплексе с ОФ от длин волн в интервале 500-600 нм электромагнитного спектра (рис. 1).
Как видно из рис. 1, растворы комплексов тербия с ОФ максимально люминесцируют при длине волны λ = 542 нм. Спектры поглощения растворов комплекса тербия с ОФ изучали спектрофотометрически по всему электромагнитному спектру.
Как показали полученные данные, поглощательная способность растворов комплекса Tb с ОФ установлена в УФ- области в интервале 200-380 нм (рис. 2 ). Как видно из рис.2, максимальное поглощение световой энергии растворами реагента и комплекса Tb с ОФ наблюдается в интервале длин волн 280-310 нм. Раствор ОФ максимально поглощает при λ = 290 нм, а у раствора комплекса Tb с ОФ поглощательная способность выше и максимум поглощения расположен правее при λ = 300 нм. В области максимального поглощения растворами реагента и комплекса световой энергии в интервале 250-370 нм растворы Tb не поглощают.
Состав комплекса Tb с Оф установлен методами молярных отношений и изомолярных серий равным Tb:ОФ = 1:2.
C Tb = СОФ = 1 мл 1⋅10-3М; λ = 542 нм; V = 10 мл; l = 1 см
Проведено исследование влияния различных факторов на интенсивность свечения растворов комплекса Tb с ОФ для выявления оптимальных условий люминесцирующего комплексообразования.
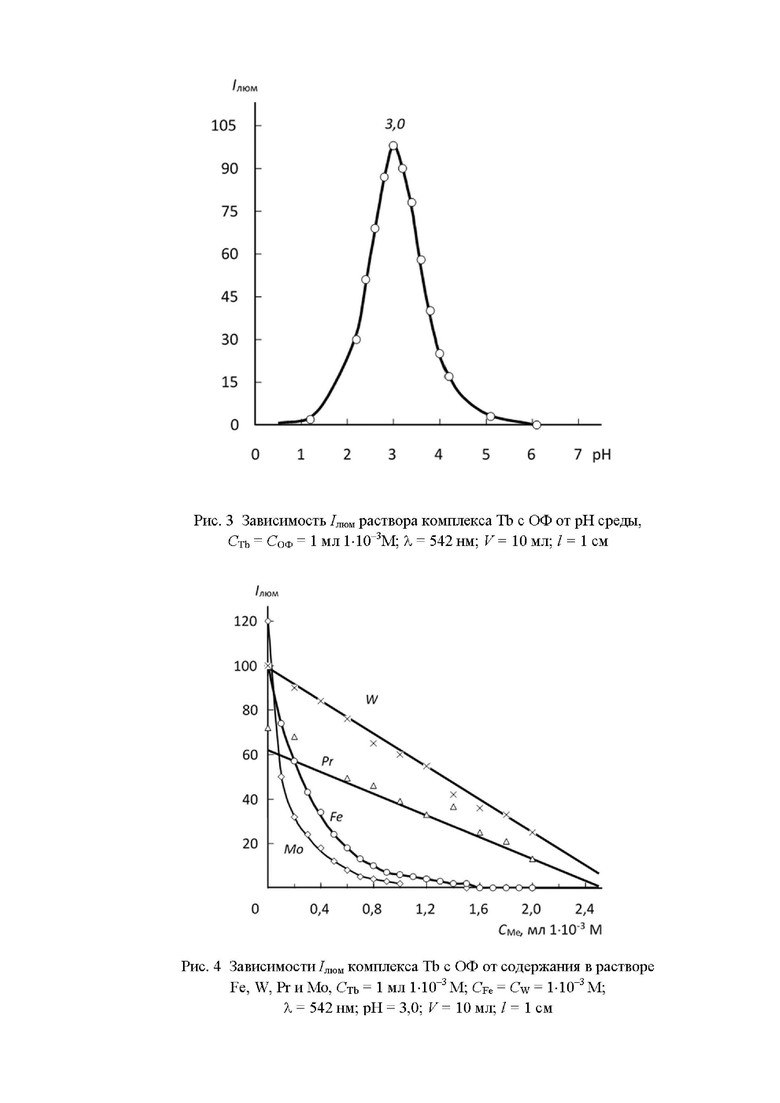
Изучена зависимость интенсивности люминесценции комплекса Tb с ОФ от рН раствора, создаваемого добавлением разбавленных растворов соляной кислоты HCI (1:10) и аммиака NH4OH (1:10). Люминесцирующий комплекс образуется в достаточно узком интервале рН =2,0-4,0 с максимумом при рН = 3,0 (рис. 3).
3,0
Iлюм,мм
Изучен характер зависимости Iлюм Tb с ОФ от времени созревания и устойчивости комплекса от времени облучения раствора УФ-светом. Iлюм раствора комплекса Tb с ОФ повышается в течение 10 мин, и далее раствор устойчив более суток, затем Iлюм раствора медленно снижается. При постоянном облучении раствора комплекса Tb с ОФ УФ-светом Iлюм снижается в первые 20 мин, затем остается постоянной более 3-х часов и далее наблюдается медленное снижение Iлюм.
Исследовано влияние других РЗЭ на Iлюм Tb с ОФ. Для этой цели брали при подобранных условиях проведения люминесцентной реакции концентрации Tb и других элементов Ме:Эл = 1:1, концентрацию ОФ увеличивали в 2 раза, т.е. СОФ = 3 мл 1⋅10 -3 М, создавали рН = 3,0; объём доводили до 10 мл и через 10 мин измеряли Iлюм раствора. Свечению Tb с ОФ не мешает Eu. Другие РЗЭ снижают Iлюм в разной степени до 30% (табл. 1). Исследование влияния сопутствующих d-элементов на Iлюм Tb с ОФ (табл. 2) показало, что они в различной степени снижают Iлюм до 2-6 %.
Рассмотрим случай, когда ион Tb присутствует, имея постоянную концентрацию, а элемент-гаситель - переменную, и СМе = 0,5 мл1⋅10-3М (рис. 4).
CTb = С
РЗЭ = 0,5 мл 1⋅10-3М; СОФ = 3 мл 1⋅10-3М; λ = 545 нм;
pH = 5,9; V = 10 мл; l = 1 см
CTb = Cd-эл = 0,5 мл 1⋅10-3 М; СОФ = 3 мл 1⋅10-3М; λ = 542 нм;
pH = 3,0; V = 10 мл; l = 1cм
1⋅10-3М
Как видно из рис. 4, молибден и железо - элементы-гасители: при увеличении их содержания в растворе комплекса наблюдается резкое снижение Iлюм Tb с ОФ. Элементы Pr и W незначительно снижают Iлюм Tb с ОФ, при увеличении их концентрации наблюдается линейное снижение Iлюм Tb с ОФ.
Нижний предел обнаружения Tb с офлоксацином составляет 7,5⋅10-9 г/мл Tb.
| название | год | авторы | номер документа |
|---|---|---|---|
| Люминесцентный способ определения тербия с ципрофлоксацином | 2022 |
|
RU2784738C1 |
| Люминесцентный способ определения европия с офлоксацином | 2023 |
|
RU2837079C1 |
| Люминесцентный способ определения тербия с нолицином | 2022 |
|
RU2794672C1 |
| Люминесцентный способ определения тербия с метилэтиловым эфиром сульфосалициловой кислоты | 2020 |
|
RU2747594C1 |
| Люминесцентный способ определения тербия с ципролетом | 2022 |
|
RU2784340C1 |
| Люминесцентный способ определения европия с ципролетом | 2023 |
|
RU2837076C1 |
| Люминесцентный способ определения самария с метакрилатом гуанидина | 2023 |
|
RU2799664C1 |
| Люминесцентный способ определения неодима с метакрилатом гуанидина | 2023 |
|
RU2825005C1 |
| ЛЮМИНЕСЦЕНТНЫЙ СПОСОБ ОПРЕДЕЛЕНИЯ ТЕРБИЯ | 2009 |
|
RU2412435C1 |
| ЛЮМИНЕСЦЕНТНЫЙ СПОСОБ ОПРЕДЕЛЕНИЯ ТЕРБИЯ | 2012 |
|
RU2506569C1 |
Изобретение относится к аналитической химии, в частности к способам люминесцентного определения тербия. Тербий переводят в люминесцирующее комплексное соединение с органическим реагентом (R) - офлоксацином. Соотношение Tb:R=1:2 при рН=3,0±0,1. Нижний предел обнаружения Tb с офлоксацином составляет 7,5⋅10–9 г/мл Tb. Технический результат - высокая селективность, точность и воспроизводимость, а также возможность одновременно определять Tb, Dy, Sm, Eu в оксидах лантаноидов. 4 ил., 2 табл.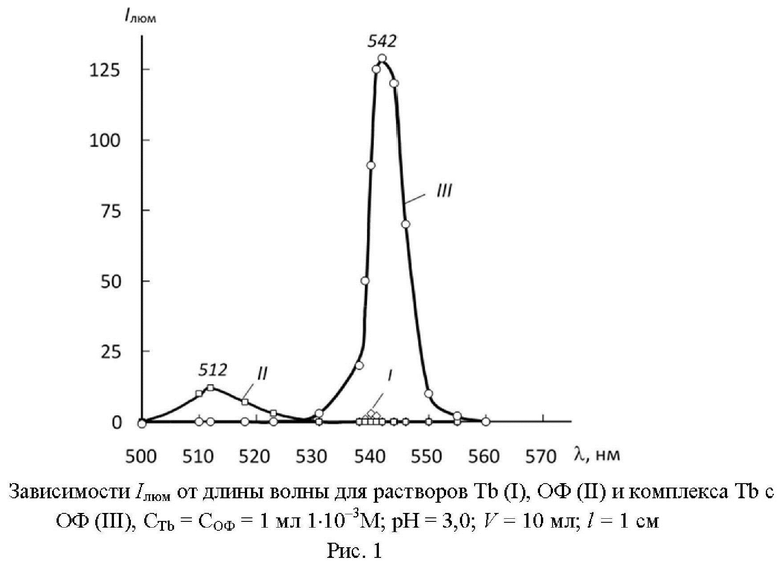
Люминесцентный способ определения тербия, включающий перевод его в люминесцирующее комплексное соединение с органическим реагентом (R), отличающийся тем, что в качестве органического реагента используют офлоксацин в соотношениях Tb:R=1:2 при рН=3,0±0,1, при этом растворы комплексов тербия с офлоксацином максимально люминесцируют при длине волны λ = 542 нм.
| AU 2020203239 A1, 11.06.2020 | |||
| CN 111122843 A, 08.05.2020 | |||
| US 8993246 B2, 31.03.2015 | |||
| CN 101196483 A, 11.06.2008 | |||
| Способ определения тербия | 1983 |
|
SU1108350A1 |
Авторы
Даты
2023-01-30—Публикация
2022-08-03—Подача