Изобретение относится к области медицинской химии и касается поиска новых химических соединений, обладающих антикоагулянтным действием. Изобретение может найти применение в медицине и ветеринарии.
Известно, что одним из тяжелых осложнений вирусных, в том числе COVID-19 (SARS-CoV-2), и бактериальных заболеваний является гиперцитокинемия, которая приводит к повреждению эндотелия легочных сосудов и нарушению всех его защитных функций, прежде всего снижению выделения оксида азота и простациклина PGI2, подавляющих активацию и адгезию лейкоцитов. Генерация тромбина приводит к образованию фибрина, активации тромбоцитов и эндотелиальных клеток через PAR-1 рецепторы, это способствует увеличению фактора фон Виллебранда (VWF), усилению воспалительной реакции, вызывая активацию Р-селектина, лейкоцитов и гладких мышц эндотелия и провоцирует высвобождение множественных цитокинов [1].
Гиперцитокинемия, которую описывают как «цитокиновый шторм» при COVID-19 (SARS-CoV-2) и других бактериальных заболеваниях, связана с выраженной реакцией иммунной системы, характеризующейся быстрой пролиферацией и повышенной активностью Т-клеток, макрофагов и естественных киллеров с высвобождением защитными клетками различных воспалительных цитокинов и химических медиаторов. Все это приводит к гиперкоагуляционному статусу, который проявляется развитием макро- и микросоудистых тромбозов венозного и артериального русла [2, 3]. Такое состояние является частым осложнением протекания коронавирусной инфекции COVID-19 (SARS-CoV-2), при этом значительную часть летальных случаев формирует диссеминированное внутрисосудистое свертывание или ДВС-синдром, который развивается на фоне цитокинового шторма [4].
Множественный тромбоз сосудов и системные нарушения ведут к полиорганной недостаточности, характерной для тяжелого течения COVID-19. Среди средств для предотвращения тромбозов при данной патологии лидирующее место занимают антикоагулянты [5].
Прорывом в современной медицине явились инновационные разработки ведущих мировых фармацевтических компаний по созданию прямых оральных антикоагулянтов (ПОАК), которые избирательно ингибируют только один фактор свертывания крови: показатель влияния на внутренний путь свертывания крови - фактор F IIa или показатель влияния на внешний путь активации свертывающей системы крови - фактор F Ха.
Зарегистрированные в Российской Федерации для применения ПОАК по механизму действия можно разделить на две группы: прямые ингибиторы тромбина - F IIa фактора (дабигатран этексилат) и прямые ингибиторы фактора Ха (апиксабан, ривароксабан, эдоксабан).
Дабигатран этексилат (торговое название - «Прадакса®», производитель - Boehringer Ingelheim International) - пролекарство, которое после приема внутрь быстро трансформируется сывороточной эстеразой в дабигатран - прямой ингибитор фактора F IIa (тромбина). Препарат оказывает ингибирующее воздействие, как на свободный тромбин, так и на тромбин, связанный с фибриновым сгустком, а также на вызванную тромбином агрегацию тромбоцитов, обладая антикоагулянтным действием.
Механизм действия препаратов апиксабана, ривароксабана и эдоксбана связан с обратимым ингибированием свободного и связанного с тромбом фактора FXa. Для реализации своей прямой функции им не требуется наличие антитромбина.
Апиксабан (торговое название - «Эликвис®», производитель - Bristol-Myers Squibb Company) обратимо и селективно блокирует активный центр F X. Апиксабан не оказывает непосредственного прямого влияния на агрегацию тромбоцитов, но опосредованно ингибирует агрегацию, индуцированную тромбином.
Снижение коагуляционного звена гемостаза крови является главной стратегией для предотвращения тромботических состояний, в том числе в условиях экспериментального цитокинового шторма, который возникает при тяжелых формах вирусной инфекции COVID-19. Использование современных оральных антикоагулянтов дабигатрана этексилата и апиксабана существенно снижает риск развития таких осложнений. Однако эти препараты закупаются за рубежом и имеют высокую стоимость.
У имеющихся в настоящее время прямых антикоагулянтов имеются и недостатки, которые ограничивают их применение [6].
Поиск и изучение новых соединений, влияющих на коагуляционное звено гемостаза, развитие исследований, направленных на создание высокоэффективных селективных антикоагулянтов, в современных эпидемических условиях особенно актуально.
Сущность изобретения
Задача предлагаемого изобретения - поиск нового соединения с высокой антикоагулянтной активностью, превосходящей ингибитор FIIa фактора дабигатрана этексилата по способности удлинять тромбиновое время, в том числе в условиях цитокиновой интоксикации при COVID-19.
Об антикоагулянтном действии соединений пирроло[2,1-ƒ][1,2,4]триазинового ряда сведений нет [7].
Техническим результатом данного изобретения является создание нового химического соединения - диметил 7-метил-2-(n-толил)-4-фенилпирроло[2,1-ƒ][1,2,4] триазин-5,6-дикарбоксилата формулы (4):
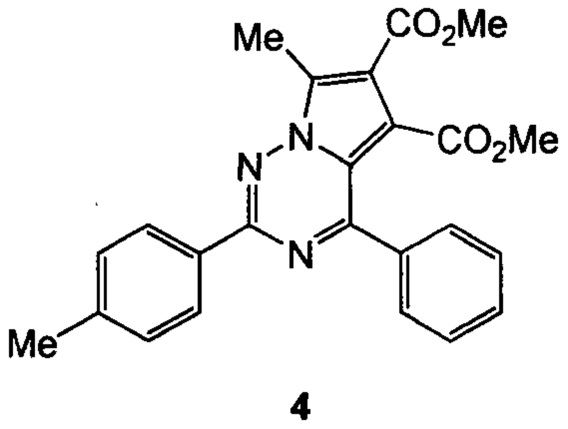
Соединение 4, его физико-химические характеристики, а также способ его получения в литературе не описаны.
Сущность изобретения поясняется следующими материалами:
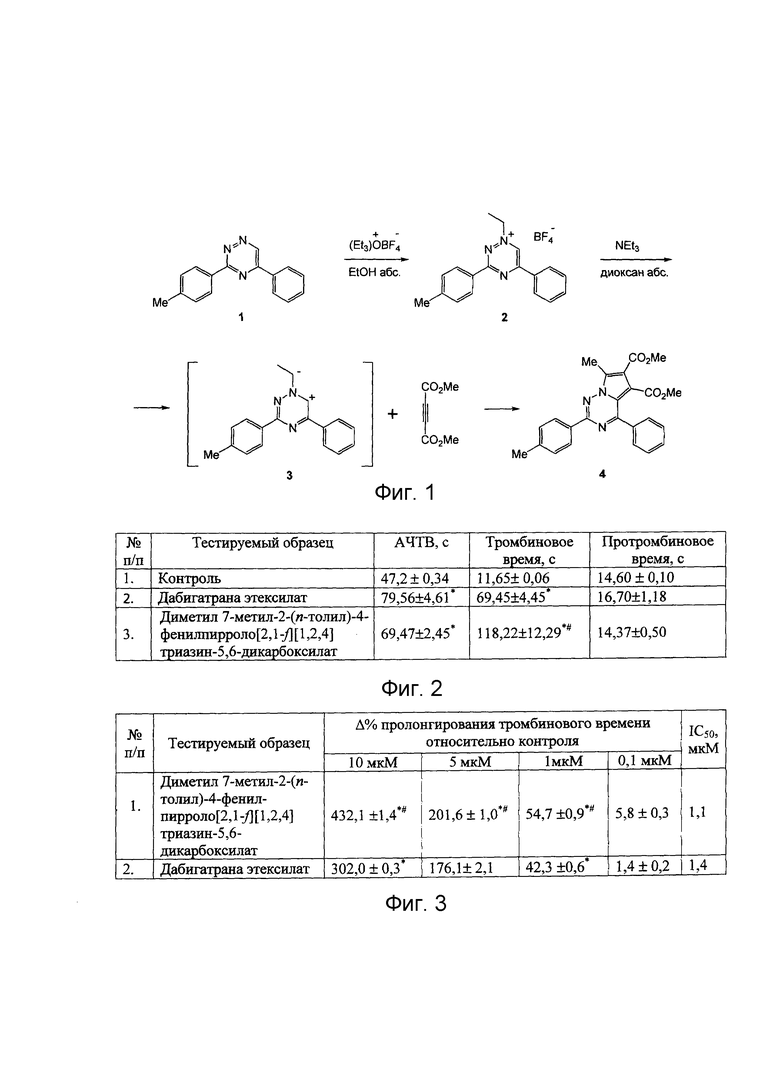
На Фиг. 1 представлена схема получения диметил 7-метил-2-(n-толил)-4-фенилпирроло[2,1-ƒ][1,2,4]триазин-5,6-дикарбоксилата (4)
На Фиг. 2 представлена таблица, в которой приведены данные о влиянии диметил 7-метил-2-(n-толил)-4-фенилпирроло[2,1-ƒ][1,2,4]триазин-5,6-дикарбоксилата и препарата сравнения дабигатрана этексилата в концентрации 100 мкМ на параметры коагулограммы крови кроликов (М±m) (n=6). Примечание: * - (р≤0,05) изменения статистически значимы по отношению к контролю, критерий ANOVA; # - (р≤0,05) изменения статистически значимы по отношению к препарату сравнения дабигатрана этексилату, критерий ANOVA; n - число тестируемых животных
На Фиг. 3 представлена таблица, в которой приведены данные о IC50 диметил 7-метил-2-(n-толил)-4-фенилпирроло[2,1-ƒ][1,2,4]триазин-5,6-дикарбоксилата и препарата сравнения дабигатрана этексилата по влиянию на тромбиновое время интактной крови кроликов (М±m) (n=6). Примечание: * - (р<0,05) данные достоверны относительно контроля, критерий ANOVA; # - (р≤0,05) изменения статистически значимы по отношению к препарату сравнения дабигатрана этексилату, критерий ANOVA; n - число тестируемых животных.
На Фиг. 4 представлена таблица, в которой приведены данные о влиянии диметил 7-метил-2-(n-толил)-4-фенилпирроло[2,1-ƒ][1,2,4]триазин-5,6-дикарбоксилата и препаратов сравнения апиксабана и дабигатрана этексилата в концентрации 100 мкМ на параметры коагулограммы крови кроликов, обработанной LPS токсином (М±m) (n=6). Примечание: * - (р≤0,05) изменения статистически значимы по отношению к контролю LPS, критерий ANOVA; n - число тестируемых животных.
На Фиг. 5 представлена таблица, в которой приведены данные о влиянии IC50 диметил 7-метил-2-(n-толил)-4-фенилпирроло[2,1-ƒ][1,2,4]триазин-5,6-дикарбоксилата и препарата сравнения дабигатрана этексилата повлиянию на тромбиновое время в условии LPS -интоксикации (М±m) (n=6). Примечание: * - (р<0,05) данные достоверны относительно контроля, критерий ANOVA4; #- (р*<0,05) изменения статистически значимы по отношению к препарату сравнения дабигатрана этексилату, критерий ANOVA; n - число тестируемых животных.
1. Способ получения диметил 7-метил-2-(n-толил)-4-фенилпирроло[2,1-ƒ][1,2,4]триазин-5,6-дикарбоксилата (4).
Соединение формулы (4) может быть получено в две стадии по модифицированной методике [8] из доступного 3-(n-толил)-5-фенил-1,2,4-триазина (1) [9].
3-(n-Толил)-5-фенил-1,2,4-триазин 1 обрабатывают реагентом Меервейна и получают N(1)-1,2,4-триазиниевую соль 2. Далее из N(1)-1,2,4-триазиниевой соли 2 под действием триэтиламина в среде абсолютного диоксана генерируют in situ илид 3, который вступает в реакцию 1,3-диполярного циклоприсоединения с диметиацетилендикарбоксилатом с образованием целевого соединения - пирроло[2,1-ƒ][1,2,4]триазина 4 (Фигура 1).
Характеристики нового соединения приведены в примере конкретного выполнения. Структура полученного соединения подтверждена ЯМР 1Н и 13С спектрами, масс-спектром и элементным анализом.
Спектры ЯМР 1H и 13С зарегистрированы на приборе Bruker Avance (600 МГц) в ДМСО-d6 с сигналом растворителя в качестве внутреннего стандарта при 25°С. Химические сдвиги (5) приведены в миллионных долях (м.д.), а константы спин-спинового взаимодействия (J) - в герцах.
Масс-спектр зарегистрирован на спектрометре Varian МАТ-311А. Условия съемки: ускоряющее напряжение 3кВ, энергия ионизирующих электронов 70 эВ, прямой ввод образца в источник.
Элементный анализ выполнен на автоматическом CHNS-O анализаторе РЕ 2400 серия II (Perkin Elmer).
Температуры плавления соединений определяют на приборе Stuart SMP3 (Barloworld Scientific).
Пример 1. Синтез диметил 7-метил-2-(n-толил)-4-фенилпирроло[2,1-ƒ][1,2,4]триазин-5,6-дикарбоксилата (4).
Стадия 1. Получение 1-этил-3-(n-толил)-5-фенил-1,2,4-триазиния тетрафторбората (2).
К раствору 1,4 г (7,28 ммоль) тетрафторбората триэтилоксония в 15,0 мл абсолютного дихлорэтана добавляют 1,2 г (4,85 ммоль) 3-(n-толил)-5-фенил-1,2,4-триазина (1). Реакционную массу выдерживают при комнатной температуре 4 ч, выпавший осадок отфильтровывают и перекристаллизовывают из абсолютного этанола.
Стадия 2. Получение диметил 7-метил-2-(n-толил)-4-фенилпирроло[2,1-ƒ][1,2,4]триазин-5,6-дикарбоксилата (4).
К суспензии, содержащей 1,0 г (2,75 ммоль) 1-этил-3-(n-толил)-5-фенил-1,2,4-триазиния тетрафторбората (2) в 6 мл абсолютного диоксана и 0,47 г (3,30 ммоль) диметилацетилендикарбоксилата, по каплям добавляют 0,31 г (3,03 ммоль) триэтиламина. Реакционную массу выдерживают сутки при комнатной температуре. Выпавший осадок отфильтровывают и перекристаллизовывают из этанола. Выход 479 мг (42%). Кристаллический осадок желтого цвета. Т пл. = 173-175°С (EtOH).
Найдено, %: С 69,42; Н 5,23; N 9,97. Вычислено, % для C24H21N3O4 (М 415,44): С 69,39; Н 5,10; N 10,11.
Спектр ЯМР 1Н (600 МГц, ДМСО-d6): 8,30 (д, 2 Н, СН3-C6H4, J=8,1 Гц); 7.71-7.74 (м, 2 Н, Ph); 7,63-7,66 (м, 1Н, Ph); 7,52-7,62 (м, 2 Н, Ph); 7,38 (д, 2 Н, CH3-C6H4, J=8,1 Гц); 3,84 (с, 3Н, О-СН3); 3,40 (с, 3Н, O-СН3); 2,85 (с, 3Н, С-СН3); 2,40 (с, 3Н, CH3-С6Н4).
Спектр ЯМР 13С (600 МГц, ДМСО-d6): 164,67; 163,87; 162,34; 154,61; 141,38; 136,56; 132,09; 131,44; 131,41; 129,68; 128,80; 128,64; 127,73; 117,80; 116,28; 112,71; 52,40; 21,43; 10,42.
Масс-спектр, m/z(%): 416 [М+1]+(28), 416 [М]+(100), 384 (21), 383 (39), 352 (22), 296 (23), 207 (16).
2. Антикоагулянтное действие диметил 7-метил-2-(n-толил)-4-фенилпирроло[2,1-ƒ][1,2,4]триазин-5,6-дикарбоксилата в экспериментах in vitro
Материалы и методы
Исследования выполняли на 6 кроликах породы «Шиншилла», весом 3,5-4 кг. Влияние диметил 7-метил-2-(n-толил)-4-фенилпирроло[2,1-ƒ][1,2,4]триазин-5,6-дикарбоксилата (4) на параметры коагулограммы крови кроликов определяли хронометрически, на гемокоагулометре «SOLAR» (Белоруссия) с использованием наборов реактивов производства («Технология-стандарт», Россия), методиками, которые основаны на автоматическом определении клоттингового времени (времени свертывания). Для калибровки прибора и проведения тестов использовалась нормальная калибровочная плазма. Все коагуляционные анализы проводились на бедной тромбоцитами плазме кроликов, которую получали путем центрифугирования богатой тромбоцитами плазмы при 3000 об/мин в течение 15 минут. В качестве препарата сравнения при изучении антикоагулянтной активности in vitro, использовали прямой оральный антикоагулянт-ингибитор тромбина (фактор IIa) - дабигатрана этексилат (Берингер Ингельхайм Фарма ГмбХ и Ко., Германия).
Диметил 7-метил-2-(n-толил)-4-фенилпирроло[2,1-ƒ][1,2,4]триазин-5,6-дикарбоксилат (4) и препарат сравнения исследовали в концентрации 100 мкМ. Величину эффекта на параметр коагулограммы оценивали по показателю IC50 (концентрация, в которой соединение удлиняет параметр на 50% относительно контроля). Для расчета данного параметра исследуемое вещество и препарат сравнения изучали также в концентрациях: 10, 5, 1 и 0,1 мкМ. При исследовании влияния тестируемых образцов на параметры коагулограммы в качестве растворителя реагентов использовали физиологический раствор. В контрольные образцы плазмы добавляли физиологический раствор.
Для определения протромбинового времени в кювету коагулометра вносили 100 мкл бедной тромбоцитами плазмы, 10 мкл исследуемого вещества и данную смесь помещали в отделение для инкубации при температуре 37°С на 5 минут. Затем данную пробирку помещали в кюветное отделение и вносили магнитный якорь. С этого момента начинали обратный отсчет времени (60 секунд) - время инкубации плазмы в автоматическом режиме при работающей магнитной мешалке. По окончании инкубационного времени в кювету дозатором вносили 200 мкл тромбопластин-кальциевой смеси со стандартизированной активностью. Время свертывания считывалось с дисплея коагулометра.
Для определения тромбинового времени 100 мкл исследуемой, бедной тромбоцитами плазмы и магнитный якорь вносили в кювету. После инкубации пробы (120 с при 37°С) в нее добавляли 100 мкл стандартизированного по активности рабочего раствора тромбина. Для исследования влияния соединения на активность тромбина тестируемое вещество в концентрации 100 мкМ в объеме 10 мкл вносили в кювету коагулометра, содержащую 100 мкл рабочего раствора тромбина, и инкубировали в течение 5 минут при комнатной температуре.
При определении активированного частичного тромбопластинового времени (АЧТВ) регистрировали время свертывания рекальцифицированной плазмы в условиях контактной и фосфолипидной активации. Для этого к 100 мкл бедной тромбоцитами плазме добавляли 100 мкл кефалин-каолиновой суспензии. После проведения инкубации полученной смеси в кювету вносили 100 мкл 0,28% раствора хлорида кальция (25 мМ). Для исследования влияния тестируемого соединения на активность тромбопластина его в концентрации 100 мкМ в объеме 10 мкл вносили в кювету коагулометра, содержащую 200 мкл разведенного тромбопластина, и помещали в термостат на 5 минут при температуре +37°С.
При исследовании влияния диметил 7-метил-2-(n-толил)-4-фенилпирроло[2,1-ƒ][1,2,4]триазин-5,6-дикарбоксилата и препаратов сравнения на показатели коагулограммы для создания гиперцитокинемии LPS-токсин ингкубировали с цельной кровью до получения опытных образцов бедной тромбоцитами плазмы в конечной концентрации 10 мкМ и производили измерения.
Статистическую обработку данных проводили при помощи программного обеспечения Graph Pad Prism 8.0. (критерий one-way ANOVA с поправкой Бонферрони, р<0,05), расчет показателя IC50, величину среднего значения и стандартного отклонения в каждой группе определяли с использованием встроенных функций MS Excel 2020.
Пример 1. Изучение влияния диметил 7-метил-2-(n-толил)-4-фенилпирроло[2,1-ƒ][1,2,4]триазин-5,6-дикарбоксилата на параметры коагулограммы (протромбиновое время, тромбиновое время, АЧТВ) in vitro.
Изучение воздействия диметил 7-метил-2-(n-толил)-4-фенилпирроло[2,1-ƒ][1,2,4]триазин-5,6-дикарбоксилата на коагуляционные характеристики интактной крови кроликов in vitro в концентрации 100 мкМ представлены в Фигуре 1. Так, в контроле показатель АЧТВ составил 47,2 с. При этом препарат сравнения дабигатрана этексилат достоверно удлинял данный показатель относительно контроля в 1,7 раза. Диметил 7-метил-2-(n-толил)-4-фенилпирроло[2,1-ƒ][1,2,4]триазин-5,6-дикарбоксилат статистически значимо пролонгировал АЧТВ относительно контрольных значений в 1,5 раза (Фигура 2).
Контрольные показатели тромбинового времени составили 11,65 с. Дабигатрана этексилат в концентрации 100 мкМ статистически значимо увеличивал продолжительность данного показателя относительно контрольных значений в 6 раз. Диметил 7-метил-2-(n-толил)-4-фенилпирроло[2,1-ƒ][1,2,4]триазин-5,6-дикарбоксилат оказывал выраженное достоверное антитромбиновое действие, удлиняя параметр тромбинового времени относительно значений, полученных в контроле в 10,1 раза и превосходя при этом препарат сравнения дабигатрана этексилат в 1,7 раза.
Показатель протромбинового времени в контроле составил 14,6 с. Дабигатрана этексилат и диметил 7-метил-2-(n-толил)-4-фенилпирроло[2,1-ƒ][1,2,4]триазин-5,6-дикарбоксилат практически не изменяли данный показатель относительно контрольных значений.
Таким образом, при исследовании влияния диметил 7-метил-2-(n-толил)-4-фенилпирроло[2,1-ƒ][1,2,4]триазин-5,6-дикарбоксилата на параметры коагулограммы крови кроликов была выявлена его высокая антитромбиновая активность.
В связи с этим изучено влияние данного вещества и ингибитора тромбина (IIa фактора) дабигатрана этексилата на показатель тромбинового времени в различных концентрациях для расчета IC50 (Фигура 3).
Тромбиновое время под влиянием диметил 7-метил-2-(n-толил)-4-фенилпирроло[2,1-ƒ][1,2,4]триазин-5,6 дикарбоксилата составило 62,0 с, что на 432,1%, превышает показатели контрольных значений. При уменьшении концентрации исследуемого вещества до 5; 1 и 0,1 мкМ тромбиновое время составило 35,1; 18,0 и 12,3 с соответственно. Таким образом, в концентрации 5 мкМ данный параметр относительно значения, полученного в контроле, пролонгировался на 201,6% а в концентрациях 1 и 0,1 мкМ на 54,7 и 5,8% соответственно. IC50 диметил 7-метил-2-(n-толил)-4-фенилпирроло[2,1-ƒ][1,2,4]триазин-5,6 дикарбоксилата составило 1,1 мкМ.
Тромбиновое время под влиянием препарата сравнения дабигатрана этексилата в концентрации 10 мкМ составило 46,8 с, что соответствует увеличению его относительно контроля на 302,0%. При дальнейшем уменьшении концентрации до 5 и 1 мкМ показатель тромбинового времени удлинялся на 176,1 и 42,3% соответственно. В концентрации 0,1 мкМ дабигатрана этексилат не оказывал влияние на данный параметр. IC50 препарата сравнения составило 1,4 мкМ.
Пример 2. Изучение влияния диметил 7-метил-2-(n-толил)-4-фенилпирроло[2,1-ƒ][1,2,4]триазин-5,6-дикарбоксилата на параметры коагулограммы (протромбиновое время, тромбиновое время, АЧТВ) в условиях ЛПС-интоксикации in vitro
Изучено влияние диметил 7-метил-2-(n-толил)-4-фенилпирроло[2,1-ƒ][1,2,4] триазин-5,6-дикарбоксилата на параметры коагулограммы крови кроликов, обработанной ЛПС-токсином. Влияние исследуемого соединения и препарата сравнения на показатели коагулограммы при гиперцитокинемии in vitro представлены на Фигуре 4.
Контрольные показатели параметров коагулограммы крови кроликов, обработанной ЛПС - токсином, статистически значимо не менялись относительно образцов интактной крови, за исключением тромбинового времени, которое достоверно уменьшалось в 1,3 раза и составило 9,13 с.
Показатель АЧТВ в условиях гиперцитокинемии составил 50,1 с. При этом дабигатрана этексилат в концентрации 100 мкМ достоверно удлинял данный показатель относительно контроля с ЛПС в 2,9 раза. Диметил 7-метил-2-(n-толил)-4-фенилпирроло[2,1-ƒ][1,2,4]триазин-5,6-дикарбоксилат также достоверно пролонгировал АЧТВ в 1,3 раза, уступая при этом препарату сравнения.
В условиях гиперцитокинемии тромбиновое время уменьшалось и составило 9,1 с. Дабигатрана этексилат статистически значимо в 13,7 раза увеличивал время образования тромбина. Диметил 7-метил-2-(n-толил)-4-фенилпирроло[2,1-ƒ][1,2,4]триазин-5,6-дикарбоксилат проявил высокую антитромбиновую активность, в 15,9 раз удлиняя тромбиновое время относительно контрольного значения крови, обработанной ЛПС-токсином и превосходя при этом препарат сравнения в 1,2 раза.
Показатель протромбинового времени в контроле составил 15,1 с. Дабигатрана этексилат и диметил 7-метил-2-(n-толил)-4-фенилпирроло[2,1-ƒ][1,2,4]триазин-5,6-дикарбоксилата в условиях ЛПС - интоксикации также не оказывали влияния на протромбиновое время.
Изучена антитромбиновая активность диметил 7-метил-2-(n-толил)-4-фенилпирроло[2,1-ƒ][1,2,4]триазин-5,6-дикарбоксилата и дабигатрана этексилата для расчета IC50 в условиях гиперцитокинемии (Фигура 5).
Тромбиновое время под влиянием диметил 7-метил-2-(n-толил)-4-фенилпирроло[2,1-ƒ][1,2,4]триазин-5,6-дикарбоксилата в концентрации 10 мкМ составило 45,3 с, что соответствует его увеличению на 396,7% относительно контрольных образцов крови, обработанных ЛПС-токсином. При снижении концентрации соединения до 5; 1 и 0,1 мкМ показатели тромбинового времени также снижались и составили 31,1; 16,6 и 11,3 с соответственно. IC50 антитромбиновой активности диметил 7-метил-2-(n-толил)-4-фенилпирроло[2,1-ƒ][1,2,4]триазин-5,6-дикарбоксилата в условиях гиперцитокинемии составило 0,35 мкМ.
Тромбиновое время под действием дабигатрана этексилата в концентрации 10 мкМ составило 35,8 с, что соответствует его увеличению на 292,0%. В концентрации 5 мкМ препарат сравнения пролонгировал изучаемый параметр на 208,6%. Показатель тромбинового времени при этом соответствовал 28,2 с. При дальнейшем уменьшении концентрации до 1 и 0,1 мкМ тромбиновое время снижалось до 13,9 и 10,6 с, что на 51,7 и 16,3% соответственно превышало контрольные значения. Показатель IC50 антитромбиновой активности дабигатрана этексилата в условиях гиперцитокинемии был равен 0,76 мкМ.
Заключение
В результате проведенных исследований было изучено влияние прямого орального антикоагулянта дабигатрана этексилата и производного диметил 7-метил-2-(n-толил)-4-фенилпирроло[2,1-ƒ][1,2,4]триазин-5,6-дикарбоксилата на различные параметры коагулограммы. Исследуемые соединения не оказывали влияние на показатель протромбинового времени, что свидетельствует об отсутствии у них способности нарушать активность факторов свертывания внешнего пути активации. Однако, было выявлено, что данные соединения достоверно удлиняют тромбиновое время, действие на которое позволяет оценить кинетику конечного этапа свертывания крови - скорость превращения фибриногена в фибрин. При этом диметил 7-метил-2-(n-толил)-4-фенилпирроло[2,1-ƒ][1,2,4]триазин-5,6-дикарбоксилат по значению IC50 антитромбиновой активности превосходит препарат сравнения - ингибитор тромбина дабигатрана этексилат в 1,3 раза.
В экспериментах было показано, что экзогенный липополисахарид (ЛПС), вызывая эндотоксемию, приводит к провоспалительному и прокоагулянтному состоянию [10, 11].
В результате проведенных экспериментов было показано, что при обработке цельной крови кроликов ЛПС-токсином происходило достоверное снижение показателя тромбинового времени, что указывает на активацию коагулянтного звена гемостаза. В условиях гиперцитокинемии диметил 7-метил-2-(n-толил)-4-фенилпирроло[2,1-ƒ][1,2,4]триазин-5,6-дикарбоксилат проявил более высокую антитромбиновую активность по сравнению с таковой на интактной крови кроликов и превосходил по IC50 препарат сравнения дабигатрана этексилат в 2,2 раза.
Таким образом, способность диметил 7-метил-2-(n-толил)-4-фенилпирроло[2,1-ƒ][1,2,4]триазин-5,6-дикарбоксилата удлинять тромбиновое время указывает на наличие у данного соединения антикоагулянтного действия, а усиление его в условиях гиперцитокинемии может внести существенный вклад в снижение риска развития COVID-19-ассоциированных тромбозов.
Список литературы
1) Mitchell W.B. Thromboinflammation in COVID-19 acute lung injury. Pediatric Respiratory Reviews. 2020, 35, 20-24.
2) Wong J.P., Viswanathan S., Wang M., Sun L.Q., Clark G.C. & D'Elia R.V. Current and future developments in the treatment of virus-induced hypercytokinemia. Future Medicinal Chemistry. 2017, 9(2), 169-178.
3) Li H., Liu L., Zhang D., Xu J., Dai H., Tang N. SARS CoV-2 and viral sepsis: observations and hypotheses. Lancet. 2020, (395), 1517-1520.
4) Fajgenbaum D.C. & June C.H. Cytokine Storm. New England Journal of Medicine. 2020, 383(23), 2255-2273.
5) Tang N., Bai H., Chen X., Gong J., Li D., Sun Z. Anticoagulant treatment is associated with decreased mortality in severe coronavirus disease 2019 patients with coagulopathy. J. Thromb. Haemost. 2020, 18(05), 1094-1099.
6) 6 Testa S., Prandoni P., Paoletti O., Morandini R., Tala M., Dellanoce C, Giorgi-Pierfranceschi M., Betti M., Battista Danzi G., Pan A., Palareti G. Directoral anticoagulant plasma levels' striking increase in severe COVID-19 respiratory syndrome patients treated with antiviral agents: The Cremona experience. Thromb. Haemost. 2020, 18(6), 1320-1323.
7) Ott, G.R., Favor D.A. Pyrrolotriazines: From C-nucleoside stokinases and back again, the remark able journey of a versatilenitrogenheterocycle. Bioorganic & Medicinal Chemistry Letters. 2017, 27 (18), 4238-4246.
8) Chupakhin O.N., Rudakov B.V., Alexeev S.G., Shorshnev S.V., Charushin V.N. 1-Alkyl-1,2,4-triazinium Ylidesas 1,3-Dipolesina Cycloaddition Reaction with Diethyl Acetylenedicarboxylate. Mendeleev Commun. 1992, 2 (3), 85-86.
9) Tang D., Wang J., Wu P., Guo X., Li J.-H., Yang S., Chen B.-H. Synthesis of 1,2,4-Triazine Derivatives via [4+2] Domino Annulations Reactions in Onepot. RSC Advances. 2016,6(15), 12514-12518.
10) Yang, X., Cheng X., Tang Y., Qiu X., Wang Y., Kang H. et al. Bacterial endotoxin activates the coagulation cascade through gasdermin D-dependent phosphatidylserine exposure. Immunity. 2019, 51, 983-996.
11) Zhang H., Zeng L., Xie M., Liu J., Zhou В., WuR. et al. TMEM173 drives lethal coagulation in sepsis. Cell Host Microbe. 2020, 27, 556-570.
| название | год | авторы | номер документа |
|---|---|---|---|
| ЛЕКАРСТВЕННОЕ СРЕДСТВО, ОБЛАДАЮЩЕЕ АНТИКОАГУЛЯНТНОЙ (ИНГИБИТОР IIA ФАКТОРА), АНТИТРОМБОТИЧЕСКОЙ, ПРОТИВОВОСПАЛИТЕЛЬНОЙ АКТИВНОСТЯМИ И СОДЕРЖАЩЕЕ 5,7-ДИ(ТИОФЕН-2-ИЛ)-4,5-ДИГИДРО-[1,2,4]ТРИАЗОЛО[1,5-а]ПИРИМИДИН | 2022 |
|
RU2798587C1 |
| Диметил 7-метил-2-(пирролидин-1-ил)-4-фенилпирроло[2,1-ƒ][1,2,4]триазин-5,6-дикарбоксилат и диметил 7-метил-2-(4-R-фенил)-4-(4-R-фенил)пирроло[2,1-ƒ][1,2,4]триазин-5,6-дикарбоксилаты, обладающие противовирусной активностью | 2021 |
|
RU2790376C1 |
| ДНК-АПТАМЕРЫ, ВЗАИМОДЕЙСТВУЮЩИЕ С ПРОТРОМБИНОМ | 2018 |
|
RU2703799C1 |
| СПОСОБ ДИАГНОСТИКИ ТРОМБИНЕМИИ У ПАЦИЕНТОВ С ИНФЕКЦИЕЙ COVID-19 | 2022 |
|
RU2794035C1 |
| Способ профилактики венозной тромбоэмболии у больных раком шейки матки | 2016 |
|
RU2641058C1 |
| Аминопроизводные диарилпиримидинов как ингибиторы высвобождения оксида азота и интерлейкина 6 | 2022 |
|
RU2812550C1 |
| 3-Бензил-5-метил-6-(фенилтио)-[1,2,4]триазоло[1,5-a]пиримидин-7(3H)-он, обладающий противовирусной активностью в отношении коронавируса SARS-CoV2 | 2022 |
|
RU2808622C1 |
| ПРИМЕНЕНИЕ ЗАМЕЩЕННЫХ 2-(2-(4,4,6-ТРИМЕТИЛ-2-ОКСО-4Н-ПИРРОЛО[3,2,1-IJ]ХИНОЛИН-1(2Н)-ИЛИДЕН)ГИДРАЗИНИЛ)ТИАЗОЛ-4(5Н)-ОНОВ В КАЧЕСТВЕ ИНГИБИТОРОВ ФАКТОРОВ СВЕРТЫВАНИЯ КРОВИ XA И XIA И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2023 |
|
RU2819271C1 |
| НОВОЕ 2-СТИРИЛПРОИЗВОДНОЕ 4-(2,6-ДИМЕТИЛ-4-ОКСО-5-ФЕНИЛ-4Н-ПИРИМИДИН-1-ИЛ)-БЕНЗСУЛЬФАМИДА, ОБЛАДАЮЩЕЕ ЭНДОТЕЛЕОПРОТЕКТОРНОЙ АКТИВНОСТЬЮ | 2017 |
|
RU2652993C1 |
| Способ оптимизации лабораторной диагностики тромбинемии у пациентов с инфекцией COVID-19 | 2022 |
|
RU2789822C1 |
Изобретение относится к новому диметил 7-метил-2-(n-толил)-4-фенилпирроло[2,1-ƒ][1,2,4]триазин-5,6-дикарбоксилату 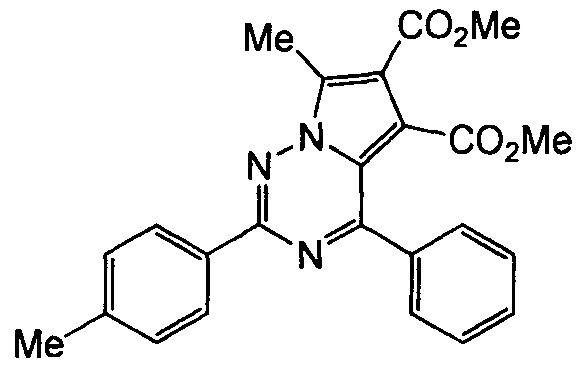 .
.
Технический результат: получено новое соединение, обладающее антикоагулянтным действием, которое может быть использовано для предотвращения тромботических состояний при тяжелых формах вирусной инфекции. 5 ил., 3 пр.
Диметил 7-метил-2-(n-толил)-4-фенилпирроло[2,1-ƒ][1,2,4]триазин-5,6-дикарбоксилат формулы
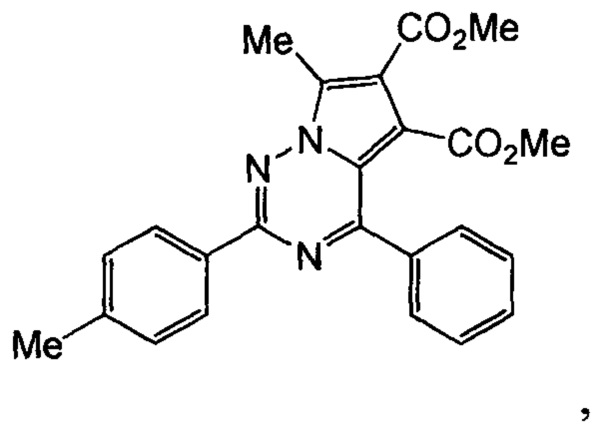
обладающий антикоагулянтным действием.
| Способ получения продукта, заменяющего деготь | 1932 |
|
SU33626A1 |
| Brian M | |||
| Fox et al, Discovery of pyrrolopyridazines as novel DGAT1 inhibitors, Bioorganic & Medicinal Chemistry Letters, 20, 6030-6033, 2010 | |||
| US7211666B2, 01.05.2007 | |||
| Nataliya N | |||
| Mochulskaya et al, Intermolecular and intramolecular cycloaddition reactions of 1-ethyl-1,2,4-triazinium salts with alkynes, Mendeleev Comm., | |||
Авторы
Даты
2023-02-17—Публикация
2022-03-22—Подача