Изобретение относится к области ветеринарии и может быть использовано для курсового лечения когнитивной дисфункции мелких домашних животных, в частности собак и кошек.
Предлагается способ курсового применения тразодона сукцината для лечения когнитивной дисфункции у пожилых собак и кошек, заключающийся во введении животному, нуждающемуся в таком лечении, тразодона сукцината: в первые три дня приема - в разовой дозе 3-6 мг/кг 2 раза в день с интервалом 12 часов, в последующие дни приема - в разовой дозе 6-10 мг/кг 2 раза в день с интервалом 12 часов, с продолжительностью курса не менее 6 недель.
Способ позволяет эффективно купировать прогрессирующие признаки когнитивной дисфункции у пожилых кошек и собак, такие, как чрезмерная беспричинная вокализация, нарушение цикла сна и бодрствования, нарушение ориентации в пространстве и социального поведения, нарушение памяти, нечистоплотное поведение, тревожность, повышенная привязанность и др. без снижения уровня безопасности для организма животного при длительном применении.
Введение
Достижения ветеринарной медицины, а также улучшения условий содержания домашних животных привели к большим демографическим изменениям в популяции питомцев: теперь и собаки и кошки живут гораздо дольше. Нередко среди животных встречаются особи, возраст которых пересек черту 10 и более лет, приближаясь ко второму десятку или уже даже перешел за эту черту. Поскольку у животных-компаньонов возрастное развитие происходит быстрее, чем у их владельцев, последние в большинстве своем неизбежно сталкиваются с процессом старения питомцев и все чаще вынуждены обращаться к ветеринарным врачам с жалобами на физические и умственные нарушения, возникающие у домашних животных в связи со старением.
Кошки.
В настоящее время выяснено, что приблизительно 30-50% домашних кошек имеют возраст старше 7 лет, из которых старше 12 лет - 13% [Laflamme D.P., Abood S.K., Fascetti A.J., Fleeman L.M., Freeman L.M., Michel K.E., Bauer C., Kemp B.L., Doren J.R., Willoughby K.N. Pet feeding practices of dog and cat owners in the United States and Australia. J. Am. Vet. Med Assoc. 2008; 232:687-694. doi: 10.2460/javma.232.5.687].
Одной из основных проблем содержания пожилых кошек, с которой сталкиваются владельцы животных - это нарушения поведения, связанные с возрастом. Обследование кошек 7-11 лет выявило 36% животных с поведенческими нарушениями, и этот показатель возрастает до 88% в возрастной популяции от 16 до 19 лет [Landsberg G. Behavior problems of older cats, in Schaumburg I (ed): Proceedings of the 135th Annual Meeting of the American Veterinary Medical Association, San Diego, CA, 1998, pp 317-320]. Последние исследования показали, что у 28 % домашних кошек в возрасте от 11 до 14 лет регистрируются гериатрические поведенческие нарушения, и этот показатель увеличивается до более чем 50%, а для кошек от 15 лет и старше этот показатель составляет более 50%. Самые частые нарушения в пожилой возрастной группе проявляются чрезмерной вокализацией и патологическим стереотипным поведением [Gunn-Moore D.A., Moffat K., Christie L.A., et al.: Cognitive dysfunction and the neurobiology of aging in cats. J Small Anim Pract 48:546-553, 2007; Moffat K.S., Landsberg G.M.: An investigation of the prevalence of clinical signs of cognitive dysfunction syndrome (CDS) in cats [abstract]. J Am Anim Hosp Assoc 39:512, 2003].
При анализе поведения пожилых кошек старше 10 лет обнаруживается частая встречаемость таких поведенческих нарушений, как нечистоплотное поведение, чрезмерная вокализация (в том числе и ночная), агрессия к животным и людям, дезориентация, бесцельное блуждание, тревожность [The effects of aging on behavior in senior pets. [Электронный ресурс]: Информационный ресурс Veterian Key. - Режим доступа: https://veteriankey.com/the-effects-of-aging-on-behavior-in-senior-pets/#bibl].
Собаки.
Сравнение популяций собак в 1960 и в 1994 гг. показало, что за указанный промежуток времени, завершившийся более 20 лет назад, доля возрастных собак уже увеличилась с 24 до 34% (Watson, 1996). Соответственно, возрос процент старых собак, поступающих в ветеринарные клиники для лечения. Так, анализ возрастного состава пациентов клиники при ветеринарном колледже Эдинбургского университета в 1991 показал, что 34,9% из 20786 принятых на лечение собак были старше 7 лет. Результатом этих изменений стал и заметный рост числа возрастных поведенческих проблем собак, с которыми обращаются в ветеринарные клиники. В одном из исследований собак в возрасте 11-16 лет было определено, что у 28% собак 11-12 лет и 68% собак 14-16 лет присутствует хотя бы один признак синдрома когнитивной дисфункции (Nielson JC, Hart BL, Cliff KD et al. Prevalence of behavioral changes associated with agerelated cognitive impairment in dogs. J Am Vet Med Assoc 2001; 218: 1787-1791).
По данным опроса, проведенного в основном с помощью Интернета (n=497), распространенность СКД (синдром когнитивной дисфункции) у собак в возрасте 8-10 лет составила 3,4%, в возрасте 10-12 лет - 5%, в возрасте 12-14 лет - 23,3‰ а в возрасте >14 лет - 41% (Salvin, Н.Е., McGreevy, P.D., Sachdev, P.S., & Valenzuela, М.J. (2010). Under diagnosis of canine cognitive dysfunction: a cross-sectional survey of older companion dogs. Veterinary journal (London, England: 1997), 184(3), 277-81. doi: 10.1016/j.tvjl.2009.11.007). Распространенными клиническими признаками снижения когнитивных способностей у собак являются дезориентация, изменение взаимодействия с людьми и другими животными, изменение циклов сна и бодрствования, несоблюдение чистоты в доме, изменения активности - сначала снижение, затем усиление беспокойного поведения или бесцельного хождения и др. (Landsberg, Gary М., Wayne L. Hunthausen, Lowell J. Ackerman, and Gary M. Landsberg. "The Effects of Aging on Behavior in Senior Pets." Behavior Problems of the Dog and Cat. Edinburgh: Saunders/Elsevier, 2013. 211-35; Landsberg, G.M., Deporter, Т., & Araujo, J.A. (2011). Clinical signs and management of anxiety, sleeplessness, and cognitive dysfunction in the senior pet. The Veterinary clinics of North America. Small animal practice, 41(3), 565-90. doi: 10.1016/j.cvsm.2011.03.017).
Несмотря на то, что численность состарившихся домашних животных постоянно растет, общий уровень освещения в литературе возрастных поведенческих расстройств как у собак, так и у кошек остается относительно низким. Этим можно объяснить недостаточную информированность владельцев о потенциальном влиянии старения на поведение их питомцев и о возможных вариантах лечения.
Таким образом, создание новых способов курсового лечения когнитивной дисфункции у пожилых МДЖ с использованием современных фармацевтических средств, продолжает оставаться актуальной и важной задачей.
Уровень техники.
Возрастные когнитивные расстройства у МДЖ трудно поддаются лечению, однако существует спектр медикаментов и пищевых добавок, позволяющих не только замедлить прогрессирование заболевания, но и улучшить качество жизни животных.
В настоящее время для улучшения когнитивной функции ветеринарными врачами рекомендуются специальные диеты, включающие бета-каротин, витамины Е и С, селен, L-карнитин, например, Purina One Vibrant Maturity (Deivis, M. (2002). Geriatriya sobak i koshek. Moscow, Akvarium Print, 96; Landsberg G.M., Nicho J., Araujo J. Cognitive Dysfunction Syndrome A Disease of Canine and Feline Brain Aging // Veterinary Clinics of North America: Small Animal Practice. 2012. V. 42. №4. P. 749-768. 5. Gunn-Moore D.A. Cogni). Известно также использование для кошек препарата пирибедил, клинические исследования которого подтвердили его эффективность в улучшении когнитивных функций (Герунова Л.К., Гунбин А.В. Синдром когнитивной дисфункции собак и кошек // Современная наука - агропромышленному производству. Тюмень, 2014. 167 с.). Однако, несмотря на эффективность данного препарата, при его использовании были выявлены побочные эффекты в виде рвоты и атаксии. Среди большого количества лекарственных средств, используемых по проблематике когнитивной дисфункции у домашних животных в Европе, предпочтение отдается трем препаратам, а именно, селегилину, ницерголину и пропентофиллину.
Селегилин (Аниприл, Pfizer Animal Health) и Селгиан (CEVA Animal Health) - препараты, одобренные для лечения синдрома когнитивной дисфункции (СКД) у собак и кошек. Селегилин - селективный и необратимый ингибитор моноаминоксидазы (МАО). Считается, что он обладает нейропротективным действием, возможно, за счет повышения активности супероксиддисмутазы и каталазы, нейтрализующих свободные радикалы, которая может снижаться при повреждении/дегенерации нервов (Carillo МС, Ivy GO, Milgram NW, et al. Deprenyl increases activity of superoxide dismutase in striatum of dog brain. Life Sci 1994; 54:1483-9; Milgram NW, Ivy GO, Head E, et al. The effect of L-deprenyl on behavior, cognitive function and biogenic amines in the dog. Neurochem Res 1993; 18(12): 1211-9).
Селегилин назначают один раз в сутки, собакам по 0,5 мг/кг, кошкам по 1 мг/кг. Препарат обладает следующими важными эффектами: способствует повышению уровня нейромедиаторов, особенно дофамина, усиливает катехоламинергическую активность и замедляет развитие нейродегенеративных процессов, будучи избирательным ингибитором МАО типа В, замедляет распад фенилэтиламина, дофамина, тирамина и норадреналина, но не серотонина, подавляет обратный захват указанных нейромедиаторов. Собакам, страдающим слабоумием, прием селегилина назначают на длительный срок, при этом стойкий терапевтический эффект достигается после 6 недель приема. Однако уже в первую неделю приема владельцы сообщают о таких побочных эффектах препарата, как рвота и диарея (Британская ассоциация по ветеринарии мелких домашних животных, Руководство по поведенческой медицине собак и кошек под редакцией Д. Хорвитц, Д. Миллса и С. Хит, перевод с английского под редакцией канд. вет. наук Ж.В. Вараксиной, канд. биол. наук М.Д. Гроздовой и канд. хим. наук И.Я. Корсаковой, Москва, «Софион», 2005).
Клинические испытания ницерголина в случаях старческих поведенческих изменений у собак дали обнадеживающие результаты: отмечалось улучшение восприятия и реакций на визуальные раздражители, а также корректировалось нечистоплотное поведение в доме, расстройство сна и снижение аппетита (Британская ассоциация по ветеринарии мелких домашних животных, Руководство по поведенческой медицине собак и кошек под редакцией Д. Хорвитц и др., Москва, «Софион», 2005). Однако прием ницерголина часто сопровождался такими побочными эффектами как тошнота и снижение артериального давления (Ю.Э. Азимова Субъективные когнитивные нарушения: современный взгляд на проблему Материал опубликован в №2 журнала Поликлиника, Москва, 2017, режим доступа: https://www.pfizerprofi.ru/sites/default/files/yu.e._azimova_subektivnye_kognitivnye_narusheniya-_sovremennyy_vzglyad_na_problemu.pdf).
Дозы ницерголина, применяемые собакам составляют от 0,25 до 2 мг/кг массы тела 3 раза в день, кошкам - от 4 до 6 мг/кг массы тела 3 раза в день (режим доступа: https://pandia.ru/text/77/465/8248-3.php).
Рекомендованный ветеринарами к применению препарат кломипрамин (трициклический антидепрессант, обладающий свойством ингибирования обратного захвата серотонина), который в силу механизма своего действия особенно эффективен, если ведущим клиническим признаком является нечистоплотное поведение в доме, а также в тех случаях, когда преобладает расстройство цикла сон/бодрствование (Британская ассоциация по ветеринарии мелких домашних животных, Руководство по поведенческой медицине собак и кошек под редакцией Д. Хорвитц и др., Москва, «Софион», 2005).
Кломипрамин хлоргидрат используется как для собак (P.A. Mertens, N.H, Dodman, Kleintierpraxis, 1996, 41: 313-392; R.A. Eckstein и B.L. Hart, J. Am. An. Hosp. Assoc., 1996, 32: 225-230), так и для кошек (L.S. Saxyer et. all., J. Am. Vet. Med. Assoc., 1999, 214: 71-74; K. Seksel, M.J. Lindeman, Aust. Vet. J., 1998, 76: 317-321). Многие специалисты рекомендуют применение кломипрамина в дозе 1-5 мг на животное каждые 12-24 часа (Simpson, 1998). Недостатком данного препарата является то, что он противопоказан пациентам с больными сердцем и почками, а престарелые домашние питомцы часто страдают заболеваниями сердечно-сосудистой и мочевыделительной системы. Также побочными эффектами от применения кломипрамина являются депрессия и снижение аппетита (Overall, 1997).
Таким образом, практически все вышеперечисленные лекарственные средства обладают, в той или иной степени, отрицательным влиянием на организм пожилого животного и требуют постоянного контроля специфических биохимических показателей крови, а также проведения других контрольных исследований.
Анализ патентных документов показывает, что лечение когнитивной дисфункции у МДЖ сегодня является актуальной проблемой, в связи с чем в последнее время активно разрабатываются и препараты, и способы лечения, улучающие когнитивные функции у собак и кошек пожилого возраста.
Известна международная заявка, в которой раскрывается способ лечения для улучшения когнитивной функции у субъекта (который, в частности, может представлять собой кошку или собаку), включающий введение субъекту терапевтически эффективного количества антагониста кальциевых каналов Т-типа, в качестве которого может быть использован спектр препаратов, в том числе, тразодон (WO 2018200850 А1, 01.11.2018). Однако в данной заявке не раскрывается ни использование тразодона в форме сукцината, ни его курсовое применение в определенных дозах с конкретным режимом приема и длительностью курса применительно к пожилым собакам и кошкам с нарушением когнитивных функций. Более того, практикующие ветврачи ряда стран рекомендуют владельцам кошек и собак в различных стрессовых ситуациях использовать тразодон непосредственно в виде известных сегодня медицинских препаратов, которые в своем составе в качестве действующего вещества содержат гидрохлорид тразодона (режим доступа: http://www.dvm360.com:John Ciribassi, 01.05.2015; Jennifer L. Garcia; 16.02.2017; Kathryn Primm 27.06.2016 и др.). В свете этого, не является неожиданностью тот факт, что присущие известным коммерческим препаратам многочисленные побочные эффекты, и прежде всего, глубокий сон, вялость, заторможенность, нарушение координации движений и др., наблюдаемые в течение нескольких часов после применения тразодон-содержащего препарата, отмечаются и при попытках использования этих препаратов для кошек и собак (Д.В. Белоглазов, С.В. Мукасеев, О.А. Зейналов «Тразодона сукцинат - новые возможности фармакологической коррекции ситуационных поведенческих отклонений у собак и кошек, Российский ветеринарный журнал, 2021, № 4, с. 5-13. DOI: 10.32416/2500-4379-2021-4-5-13). При этом примеры, представленные в заявке WO 2018200850 А1, направлены на изучение влияния конкретного антагониста кальциевых каналов Т-типа- МК-8998 (Сувекалтамид) на один из основных клеточных механизмов, лежащих в основе обучения и развития памяти, на мышах. Кроме того, в данной заявке сообщается о лечении пациента с легкими когнитивными нарушениями, где на фоне основного лечения (или без него) вводят МК-8998, Мибефрадил или Эфонидипин, достигая при этом улучшения нейропсихических показателей.
В источниках WO 0121178 А2, 29.03.2001 и WO 2006138385 А2, 28.12.2006 раскрываются способы лечения поведенческих проблем у собак, связанных со старением, заключающиеся во введении эффективного количества пропентофиллина (WO 0121178 А2) и ингибитора холинэстеразы фенсерина (WO 2006138385 А2), введение которых корректирует симптомы, связанные с синдромом когнитивной дисфункции у собак. При этом известно, что при использовании пропентофиллина могут возникнуть такие побочные эффекты, как рвота, кардиологические нарушения и кожная аллергия (http://mri.cts-mrp.eu/Veterinary/Downloads/NL_V_0313_001_FinalSPC.pdf), а использование ингибиторов холинэстеразы может привести к повышению уровня ацетилхолина, тем самым вызвав расстройство желудка, повышенное слюноотделение и слезотечение, учащенное мочеиспускание, замедление сердцебиения, диарею и низкое кровяное давление (https://www.singlecare.com/blog/cholinesterase-inhibitors/).
В указанных патентных документах не раскрывается ни использование тразодона сукцината ни его курсовое применение для лечения когнитивной дисфункции у пожилых собак и кошек в определенных дозах с конкретным режимом приема и длительностью курса.
Известен способ предупреждения или замедления проявления одного или нескольких возрастных проявлений у домашних животных, особенно связанных с синдромами когнитивной дисфункции, заключающийся во введении животным эффективного количества S-аденозил-L-метионина или одной из его солей в количестве от 1 до 50 мг/кг массы тела в день в течении длительного периода времени, в частности, в примерах описания раскрывается курсовое применение активного вещества по изобретению. Так в примере 1 раскрывается курсовое применения S-аденозил-L-метионина в дозе 2,5 мг/кг веса в день однократно, ежедневно в течении 4-х месяцев у собак возрастом более 7 лет с поведенческими расстройствами, связанными с синдромом когнитивной дисфункции, в примере 3 раскрывается применение S-аденозил-L-метионина в минимальной (12,9 мг/кг сутки), средней (18 мг/кг в сутки) и максимальной (22,5 мг/кг/сутки) дозе в сутки в течении 3-х месяцев у кошек с четко установленными когнитивными расстройствами, возраст которых составлял от 12,5 до 19 лет (US 2008199520 А1, 21.08.2008).
В данной заявке, однако, не раскрывается ни использование в способе тразодона сукцината, ни его курсовое применение, обеспечивающее эффективное лечение когнитивной дисфункции у пожилых собак и кошек в указанных дозах с конкретным режимом приема препарата и длительностью курса.
В настоящее время проводятся обширные исследования по поиску препаратов и способов лечения когнитивной дисфункции у мелких домашних животных, которые являлись бы максимально эффективными и не обладали бы побочными эффектами предшествующего уровня техники.
Основываясь на том, что проблема когнитивной дисфункции у МДЖ все больше приобретает масштабный характер и требует эффективный подход к ее решению, заявитель счел целесообразным разработать способ курсового применения для лечения когнитивной дисфункции у пожилых собак и кошек, который являлся бы высокоэффективным для данной категории животных.
Настоящее изобретение решает указанные выше проблемы, предлагая эффективную схему курсового применения тразодона сукцината для лечения когнитивной дисфункции у пожилых кошек и собак, обеспечивающую отсутствие побочных эффектов при длительном использовании.
Раскрытие изобретения
Поставленная задача создания эффективного и безопасного способа лечения когнитивной дисфункции у МДЖ была решена путем разработки курса применения для этой цели препарата, содержащего в качестве ДВ янтарно-кислую соль тразодона (сукцинат тразодона).
Тразодон известен как антидепрессант, участвующий в обмене серотонина и при этом представляющий собой пример мультимодальных препаратов, т.е. препаратов, обладающих более чем одним механизмом действия. Он одновременно является антагонистом группы серотониновых рецепторов, преимущественно типа 5-НТ2, с отчетливой дозозависимой функциональностью (способностью по мере увеличения дозы усиливать определенный эффект или присоединять к нему новые эффекты в силу различного сродства к различным их типам), и ингибитором обратного захвата серотонина из синаптического пространства (Чабан О.С и др., Международный неврологический журнал. № 2(56); 2013; https://medi.ru/info/11157).
Известно, что серотониновая система имеет решающее значение в регуляции поведенческих и когнитивных функций у млекопитающих [Harvey Р.J., Li X., Li Y., Bennett D.J. 5-HT2 receptor activation facilitates a persistent sodium current and repetitive firing in spinal motoneurons of rats with and without chronic spinal cord injury. J. Neurophysiol. 2006; 96: 1158-1170. doi: 10.1152/jn.01088.2005.]. Она обеспечивает регуляцию поведения в различных ситуациях или путем подавления усвоенных моделей поведения, которые были бы неуместны, или путем корректировки времени ответов для обеспечения более адаптированного поведения [Jacobs B.L., Azmitia Е.С. Structure and function of the brain serotonin system. Physiol. Rev. 1992; 72: 165-229. doi: 10.1152/physrev.1992.72.1.165.; Soubrié P. Reconciling the role of central serotonin neurons in human and animal behavior. Behav. Brain Sci. 1986; 9: 319-335].
Основными поведенческими проявлениями, регулируемыми серотонином у человека и животных, являются:
- двигательное поведение;
- активность действий;
- двигательная активность морды и головы, обеспечивающая уход за телом, жевание, кусание;
- состояние сна и бодрствования;
- пищевое поведение;
- контроль социального взаимодействия и статуса;
- агрессивное поведение;
- тревожность;
- обучение и память;
- импульсивное и компульсивное поведение.
В контексте настоящего изобретения важно отметить, что роль серотонина не ограничивается регуляцией важных физиологических процессов, таких как сон, аппетит, боль и двигательная активность, а модулирует и высшие функции мозга, включая обучение и эмоциональное поведение.
При этом сегодня установлена четкая корреляция между изменениями в эмоциональном поведении человека при старении со снижением как количества серотониновых рецепторов, так и уровня в крови пациента серотонина. [Blazer D., Williams CD. 1980. Epidemiology of dysphoria and depression in the elderly population. Am J Psychiatry 137:439-444; Mann J.J., Arango V., Underwood M.D. 1990. Serotonin and suicidal behavior. Ann NY Acad Sci 600:476-485.; Meltzer C.C., Smith G., De Kosky S.T., Pollock B.G Serotonin in Aging, Late-Life Depression, and Alzheimer's Disease: The Emerging Role of Functional Imaging Neuropsychopharmacology volume 18, pages 407-430 (1998)].
Полученные экспериментальные данные побудили медиков исследовать влияние различных препаратов, активирующих уровень серотонина, на поведенческие и психологические симптомы, характерные для пожилых пациентов. Одним из препаратов, показавшим отличные результаты в части высоких стандартов безопасности и переносимости при лечении «возрастных» пациентов с неврологическими заболеваниями, оказался тразодон. Показано, что у пациентов с болезнью Альцгеймера тразодон помогает справиться с поведенческими симптомами, а также действует как нейрозащитный агент [Cuomo A., Bianchetti A., Cagnin A., De Berardis D. Di Fazio I, Antonelli R, Trazodone: a multifunctional antidepressant. Evaluation of its properties and real-world use Journal of Gerontology and Geriatrics Vol. 69: Issue 2 - June 2021]. В ряде исследований также было обнаружено, что тразодон улучшает поведенческие симптомы у 80% включенных в исследование пациентов пожилого возраста с деменцией [Tingle D.: Trazodone in dementia (letter). J Clin Psychiatry 1986; 47:482; Pinner E., Rich C.L.: Effects of trazodone on aggressive behavior in seven patients with organic mental disorders. Am J Psychiatry 1988; 145:1295-6; Lebert F., Pasquier F., Petit H.: Behavioral effects of trazodone in Alzheimer's disease. J Clin Psychiatry 1994; 55:536-538].
Результаты, полученные при использовании тразодона в медицине, послужили отправной точкой для начала исследований, связанных с возможностью его применения домашним животным при поведенческих нарушениях, связанных с возрастом [Cognitive disorder common in older dogs [Электронный ресурс]: Режим доступа:
https://www.abqjournal.com/1005470/cognitive-disorder-common-in-older-dogs.html]. Однако на сегодняшний день опыт использования тразодона для этих целей ограничивается единичными случаями и не дает необходимой для его внедрения в ветеринарную практику информации. Кроме того, как и в остальных случаях по применению тразодона животным, здесь до недавнего времени использовались исключительно коммерческие медицинские препараты (Trittiko, Desyrel, Oleptro и др.), содержащие тразодон в форме гидрохлорида.
На сегодняшний день на мировом ветеринарном рынке существует единственный тразодон-содержащий препарат, предназначенный для животных (кошек и собак). Данный лекарственный препарат выпускается под торговым названием Экспресс Успокоин® таблетки и в качестве действующего вещества содержит тразодона сукцинат, преимущества применения которого для коррекции поведения мелких домашних животных в стрессовых ситуациях раскрыты нами в патенте RU 2706700 С1, 20.11.2019 и недавно опубликованной обзорной статье (Д.В. Белоглазов, С.В. Мукасеев, О.А. Зейналов «Тразодона сукцинат - новые возможности фармакологической коррекции ситуационных поведенческих отклонений у собак и кошек, Российский ветеринарный журнал, 2021, №4, с. 5-13. DOI: 10.32416/2500-4379-2021-4-5-13).
Объединение в молекуле сукцината тразодона целевого действия тразодона с уникальными свойствами янтарной кислоты позволило добиться высокой эффективности при снижении вероятности проявления побочных эффектов, характерных для медицинских препаратов на основе гидрохлорида тразодона, альтернативы которым до недавнего времени не было.
С учетом имеющихся литературных данных и результатов собственных исследований, при решении задачи лечения когнитивной дисфункции у МДЖ представлялось перспективным разработать новый эффективный способ курсового применения лекарственного препарата на основе тразодона сукцината.
Разработанный нами при создании настоящего изобретения способ курсового применения тразодона сукцината при когнитивных расстройствах у МДЖ, в частности, у собак и кошек, подробно раскрытый в разделе описания «Осуществление изобретения», обеспечивает высокую терапевтическую эффективность без снижения уровня безопасности при длительном его применении (технический результат).
Осуществление изобретения
Изобретение проиллюстрировано примерами, которые дополнительно раскрывают изобретение, но не предназначены для ограничения объема и не должны толковаться как такое ограничение
Практически разработка способа включала следующие этапы:
- обследование и отбор животных в эксперимент;
- коррекция поведения с применением исследуемого препарата с контролем (плацебо);
- анализ динамики физиологических показателей животных, участвующих в исследовании;
- наблюдение за животными после отмены препарата;
- установление продолжительности и качество ремиссии;
- анализ полученных данных;
- заключение о безопасности и эффективности курсового применения тразодона сукцината.
Животные
Планом клинического исследования было предусмотрено включение 24-х собак, весом 8,2±5,6 кг и 24-х кошек, весом 3,8±1,4 кг, испытывающих проблему поведения в пожилом возрасте на протяжении не менее 6 месяцев. На время проведения исследования животные находились в привычных квартирных условиях. В эксперименте участвовали домашние собаки и кошки любой породы и пола, в возрасте от 7 лет с выявленным нежелательным поведением длительностью не менее 6 месяцев. Для собак такое поведение включало дезориентацию в пространстве, изменения социального поведения, снижение активности, тревожность, нарушение цикла сна и бодрствования, нечистоплотное поведение, потерю навыков выполнения команд. Для кошек чрезмерную вокализацию, нарушение цикла сна и бодрствования, нарушение ориентации в пространстве, изменение социального поведения, нечистоплотное поведение и тревожность.
Собаки и кошки, в силу возраста, имели по несколько хронических заболеваний, в частности, у собак были зарегистрированы такие заболевания как холецистит, холангит, уролитиаз, хроническая почечная недостаточность, гастроэнтерит/гастродуоденит, цистит, поликистоз почки, отит, у кошек - холецистит, холангит, мочекаменная болезнь, хроническая почечная недостаточность, гастроэнтерит, герпесвирусная инфекция, дерматит идиопатический и отит. До начала исследования все животные, участвующие в эксперименте, подвергались лечению вышеуказанных хронических заболеваний без использования психотропных лекарственных средств и БАД для коррекции поведения и, на момент исследования, по хроническим заболеваниям находились в стадии ремиссии.
Все владельцы животных ранее обращались за ветеринарной помощью по поводу прогрессирующего изменения поведения животного и отмечали ухудшение качества собственной жизни в связи с постоянными нежелательными поведенческими проявлениями у питомца. Диагноз устанавливался на основании выраженности когнитивных нарушений у пожилых собак и кошек с учетом данных анамнеза, оценки целевых показателей поведения собаки и кошки без введения тразодона сукцината.
В испытаниях использовалось лекарственное средство, включающее тразодон сукцинат и фармацевтические приемлемые вспомогательные вещества (см. патент RU 2706700 СТ).
I. Скрининговое обследование животных до начала лечения.
Пример 1. Определение общего состояния организма по показателям общего и биохимического анализа крови у собак
В опыте использовали 24 собаки возрастом от 7 лет и более, которые рандомно были поделены на две группы (опытная (12 особей) и контрольная (12 особей)), у собак брали кровь утром натощак, доступ к воде при этом не ограничивали.
Результаты исследования крови представлены в таблицах 1 и 2.
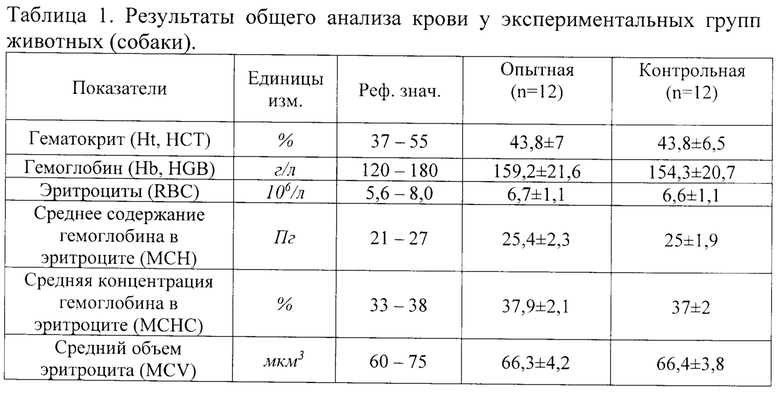
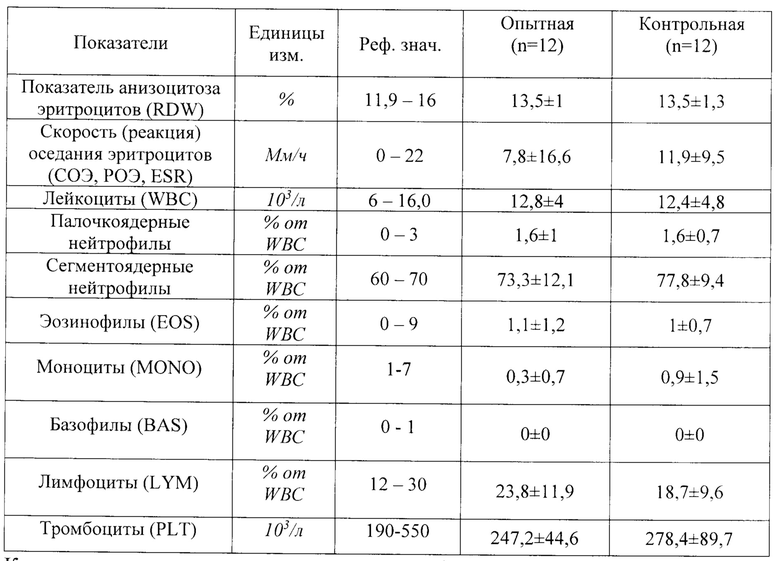
Как следует из данных, представленных в таблице 1 значимых различий между результатами общего анализа крови в опытной и контрольной группе собак не выявлено.
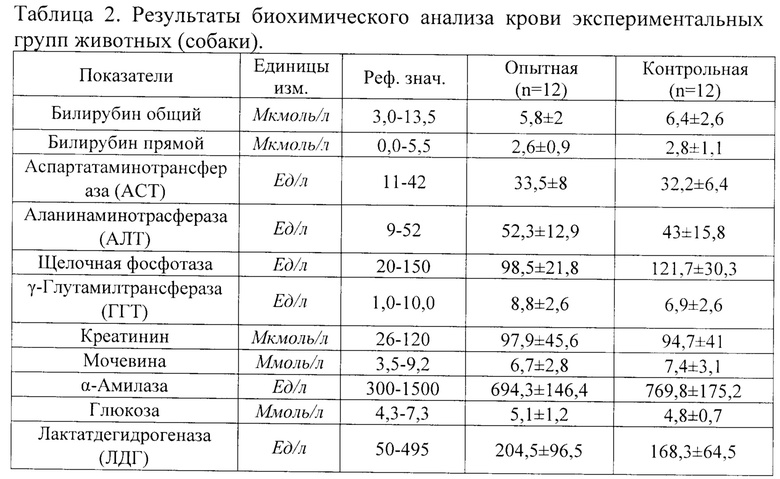

Как следует из данных, представленных в таблице 2 значимых различий между результатами биохимического анализа крови в опытной и контрольной группе собак не выявлено.
Таким образом, все показатели находились в пределах физиологической нормы.
Пример 2. Исследование выраженности признаков когнитивной дисфункции у собак на момент включения в исследование.
В опыте использовали 24 собаки возрастом более 7 лет, которые рандомно были поделены на две группы (опытная (12 особей) и контрольная (12 особей)) у которых фиксировались признаки когнитивной дисфункции в баллах, где 1 балл означал наличие признака, 0 отсутствие признака. Результаты исследования представлены в таблице 3.
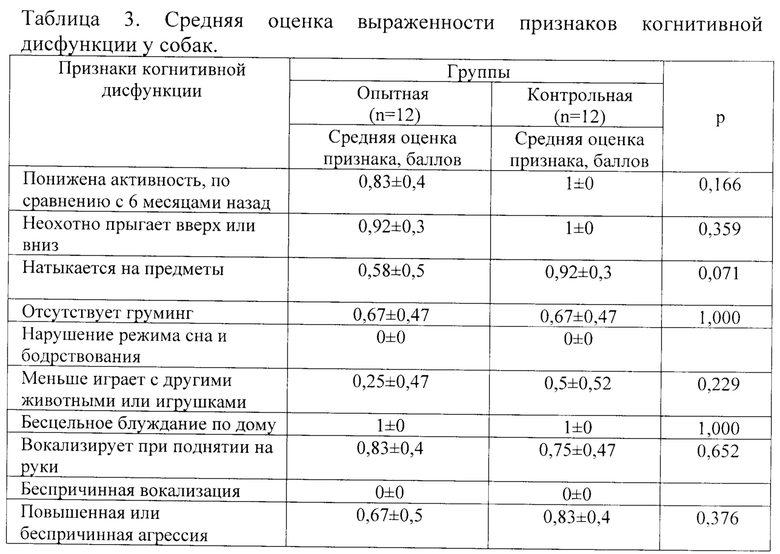
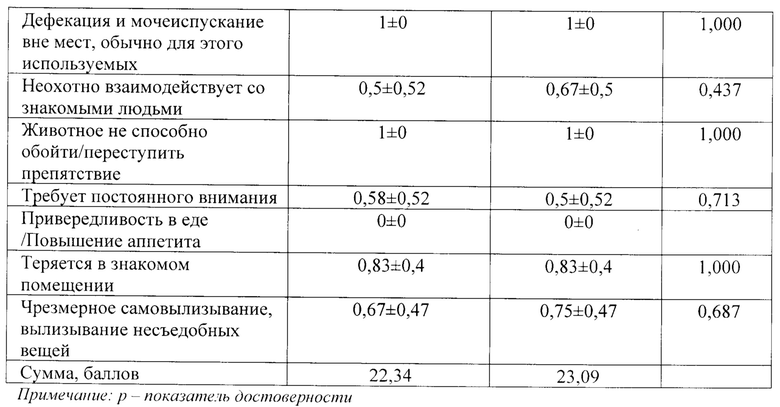
Исходя из показателей, представленных в таблице 3, значимых различий в целевых показателях поведения собак между двумя группами не выявлено.
Пример 3. Определение общего состояния организма по показателям общего и биохимического анализа крови у кошек.
В опыте использовали 24 кошки возрастом более 7 лет, которые были рандомно поделены на две группы (опытная (12 особей) и контрольная (12 особей)), у кошек брали кровь утром натощак, доступ к воде при этом не ограничивали. Результаты исследования крови представлены в таблицах 4 и 5.
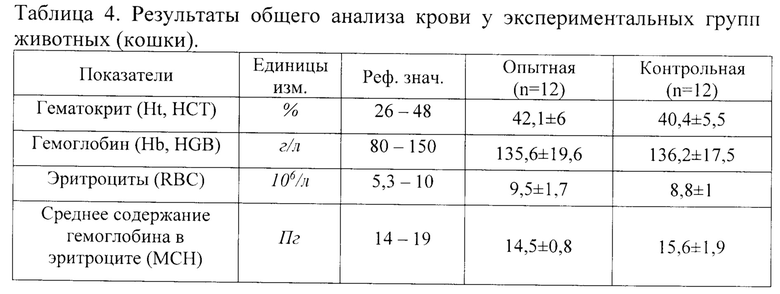

Как следует из данных, представленных в таблице 4, значимых различий между результатами общего анализа крови в опытной и контрольной группе кошек не выявлено.


Как следует из данных, представленных в таблице 5, значимых различий между результатами биохимического анализа крови в опытной и контрольной группе кошек не выявлено.
Таким образом, все показатели находились в пределах физиологической нормы.
Пример 4. Исследование выраженности клинических признаков когнитивной дисфункции у кошек на момент включения в исследование.
В опыте использовали 24 кошки возрастом более 7 лет, которые были рандомно поделены на две группы (опытная (12 особей) и контрольная (12 особей)) у которых фиксировались признаки когнитивной дисфункции в баллах, где 1 балл означал наличие признака, 0 отсутствие признака. Результаты исследования представлены в таблице 6.

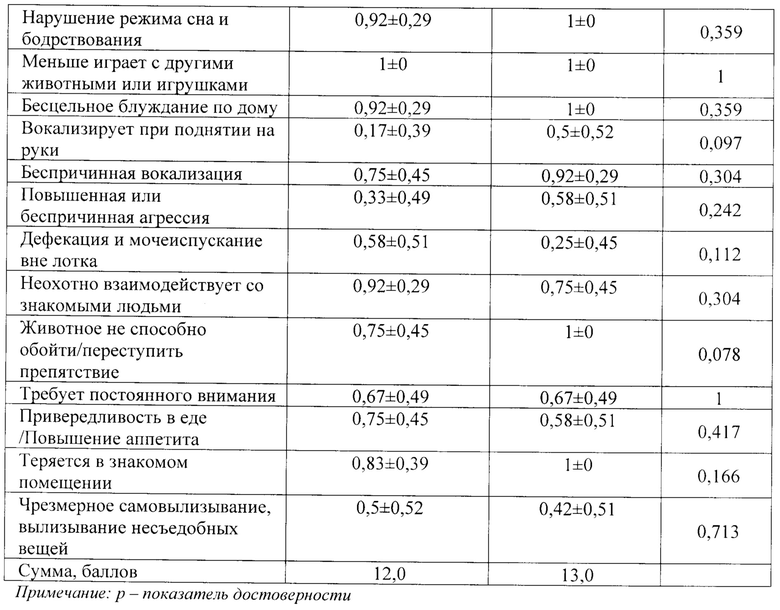
Исходя из данных, представленных в таблице 6, значимых различий в целевых показателях поведения кошек между двумя группами не выявлено.
II. ОЦЕНКА ЭФФЕКТИВНОСТИ И БЕЗОПАСНОСТИ КУРСОВОГО ПРИМЕНЕНИЯ ТРАЗОДОНА СУКЦИНАТА
1. Общие положения.
В эксперименте использовались разнополые собаки и кошки возрастом более 7 лет в количестве по 24 особи, собаки весом 8,2±5,6 кг, кошки весом 3,8±1,4 кг, испытывающих проблему поведения на протяжении не менее 6 месяцев. Животные были разделены на 2 группы: опытную (кошки и собаки по 12 особей), в которой применяли тразодон сукцинат и контрольную (кошки и собаки по 12 особей), в которой применяли плацебо. Для улучшения восприятия опытная группа далее по тексту именуется как «Группа 1», контрольная группа - «Группа 2».
Группам экспериментальных животных вводили исследуемый лекарственный препарат или плацебо по одинаковой схеме в одно и то же время (800 и 2000).
Все животные Группы 1 в первые три дня получали тразодона сукцината в виде разовой дозой 3-6 мг/кг веса животного 2 раза в день с интервалом в 12 часов, а начиная с четвертого дня лечения и до его завершения (до 6 недель) разовая доза препарата составляла 6-10 мг/кг и также применялась два раза в день с интервалом в 12 часов, после чего препарат отменяли и вели наблюдение за животными для определения качества и продолжительности ремиссии.
Животные Группы 2 получали препарат плацебо по аналогичной схеме. В качестве плацебо использовался состав, включающий лактозу моногидрат, натрий кроскармеллозу, повидон, кремния диоксид коллоидный безводный, магния стеарат, пищевую добавку со вкусом мяса.
Оценка эффективности лечения проводилась по динамике снижения выраженности негативной симптоматики поведения собак и кошек во время применения курса тразодона сукцината.
Показатели эффективности применения оценивались с помощью непараметрических методик (Манна-Уитни, Вилкоксона). Статистическая значимость различий оценивалась на уровне р≤0,05. Данные по безопасности оценивались по частоте выявления нежелательных реакций. Определение длительности и качества ремиссии проводилось по отрицательной динамике выраженности негативной симптоматики поведения собак и кошек после отмены тразодона сукцината:
Оценка безопасности применения исследуемого препарата включала следующие показатели:
- частота возникновения нежелательных реакций;
- удовлетворительное состояние пациента по результатам осмотра;
- удовлетворительное состояние пациента по результатам биохимического и общего клинического анализа крови.
Выбор параметров эффективности и безопасности основывался на литературных данных [Gunn-Moore D.A., Cognitive Dysfunction in Cats: Clinical Assessment and Management. Top Companion Anim Med. 2011 Feb; 26(1):17-24.] и анамнестических данных, полученных от владельцев испытуемых животных.
2. Экспериментальное исследование эффективности курсового применения сукцината тразодона при когнитивной дисфункции.
Пример 5. Оценка эффективности курсового лечения сукцинатом тразодона пожилых собак по поведенческим признакам.
Результаты оценки эффективности лечения по динамике снижения выраженности негативной симптоматики поведения собак во время применения курса тразодона сукцината представлены в таблице 7.
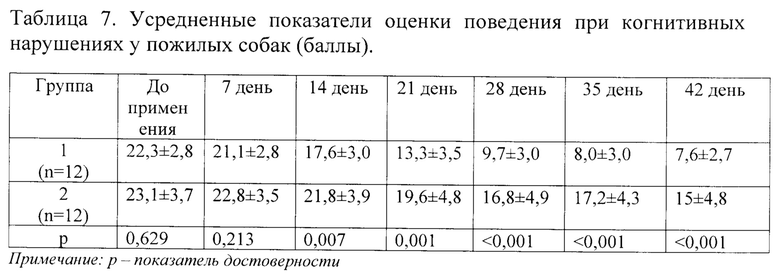
Как следует из таблицы 7 статистически достоверное изменение в поведении пожилых собак начинается со второй недели терапии, далее выраженность признаков когнитивной дисфункции достоверно снижается вплоть до окончания применения тразодона сукцината (6 недель).
Пример 6. Оценка эффективности курсового лечения сукцинатом тразодона пожилых кошек по поведенческим признакам.
Результаты оценки эффективности лечения по динамике снижения выраженности негативной симптоматики поведения кошек во время применения курса тразодона сукцината представлены в таблице 8.
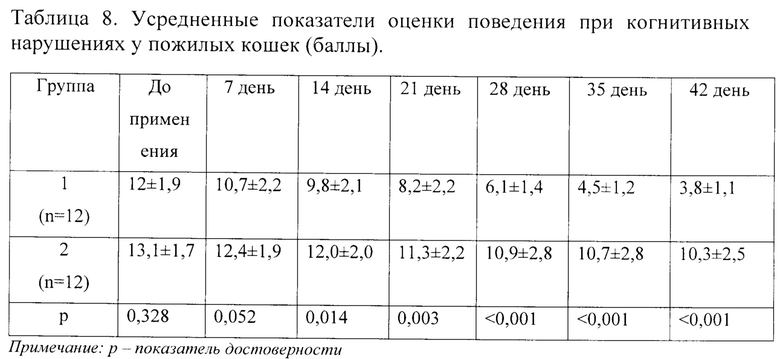
Как следует из таблицы 8 статистически достоверное изменение в поведении пожилых кошек начинается со второй недели терапии, далее выраженность признаков когнитивной дисфункции достоверно снижается вплоть до окончания применения тразодона сукцината (6 недель).
Таким образом, курсовое применение тразодона сукцината в заявленных режимах и дозах показало высокий терапевтический эффект для собак и кошек старше 7 лет с прогрессирующими признаками когнитивной дисфункции, заключающийся в снижении чрезмерной вокализации, нормализации цикла сна и бодрствования, ориентации в пространстве и социального поведения, устранении нечистоплотного поведения, тревожности и др.
Пример 7. Оценка длительности ремиссии после отмены тразодона сукцината у собак.
В опыте оценивалась длительность и качество ремиссии после отмены тразодона сукцината у собак Группы 1 и Группы 2 через 14, 28, 42, 56, 70 и 84 дня. Результаты исследования приведены в таблице 9.
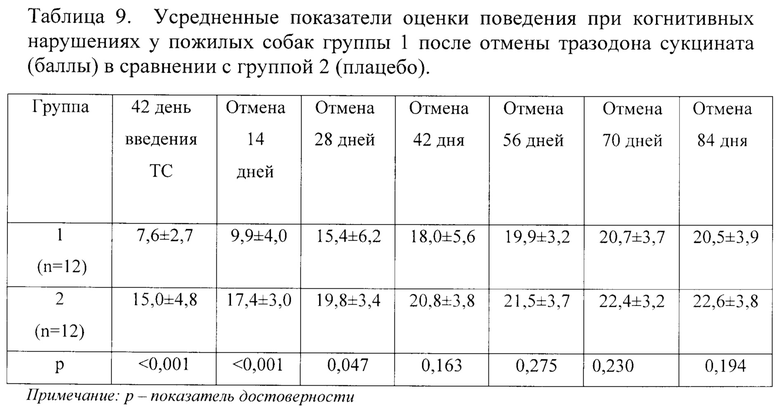
После завершения 6-ти недельного курса зарегистрировано постепенное восстановление показателей поведения до уровня, приближающегося к исходному. Исходный уровень оценки целевых показателей поведения 22,3±2,8 балла (таблица 7), уровень оценки целевых показателей собак после отмены препарата на 84 день составил 20,5±3,9 балла (таблица 9). Таким образом, после отмены тразодона сукцината наблюдается постепенное возвращение признаков когнитивной дисфункции у собак. Статистически значимая разница отмечается через 2 недели после отмены исследуемого препарата. Соответственно средний срок продолжительности ремиссии в данном исследовании можно установить в 2 недели.
Пример 8. Оценка длительности ремиссии после отмены тразодона сукцината у кошек.
В опыте оценивалась длительность ремиссии после отмены тразодона сукцината у кошек Группы 1 и Группы 2 через 14, 28, 42, 56, 70 и 84 дня. Результаты исследования приведены в таблице 10.

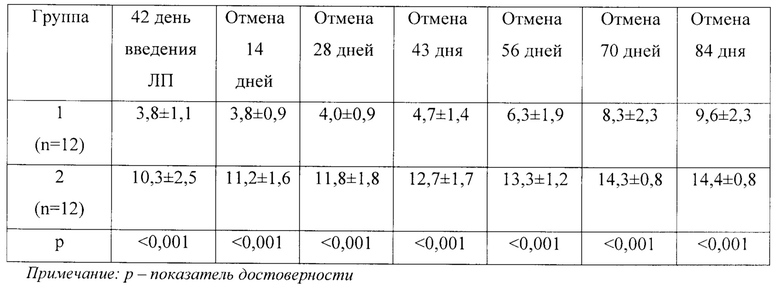
При отмене препарата (на 43 день) зарегистрировано постепенное восстановление показателей поведения до уровня, приближающегося к исходному. Исходный уровень оценки целевых показателей поведения 12,0±1,9 балла (таблица 8), уровень оценки целевых показателей кошек после отмены препарата на 84 день составил 9,6±2,3 балла (таблица 10). После отмены препарата наблюдается постепенное возвращение признаков поведения при когнитивных нарушениях. Статистически значимая разница отмечается через 8 недель после отмены исследуемого препарата. Соответственно средний срок продолжительности ремиссии в данном исследовании можно установить в 8 недель.
Таким образом, курсовое применение тразодона сукцината в заявленных режимах и дозах позволяет добиться ремиссии для собак в течении 2-х недель, для кошек 8-ми недель, что подтверждает высокий терапевтический эффект для собак и кошек старше 7 лет с прогрессирующими признаками когнитивной дисфункции.
3. Экспериментальное исследование безопасности курсового применения сукцината тразодона при когнитивной дисфункции.
Безопасность курсового применения тразодона сукцината на целевых животных {Группа 1 и Группа 2, описанные ранее) оценивали по динамике гематологических показателей у собак и кошек на 21 день введения препарата и на 43 день исследования (первый день отмены тразодона сукцината).
Пример 9. Влияние тразодона сукцината на динамику гематологических показателей у собак.
Общий анализ крови (OAK) и биохимический анализ крови (БАК) проводился у всех животных натощак, доступ к воде при этом не ограничивали. Как в группе 1, так и группе 2 в установленные контрольные сроки исследования брали кровь: на 21 день введения тразодона сукцината и на 43 день исследования (первый день отмены тразодона сукцината).
Результаты сравнения данных ОАК на 21 день введения тразодона сукцината представлены в таблице 11, результаты сравнения данных ОАК на 43 день исследования (первый день отмены тразодона сукцината после 6-ти недельного курса) представлены в таблице 12.
Результаты сравнения данных БАК на 21 день введения тразодона сукцината представлены в таблице 13, результаты сравнения данных БАК на 43 день исследования (первый день отмены тразодона сукцината после 6-ти недельного курса) представлены в таблице 14.
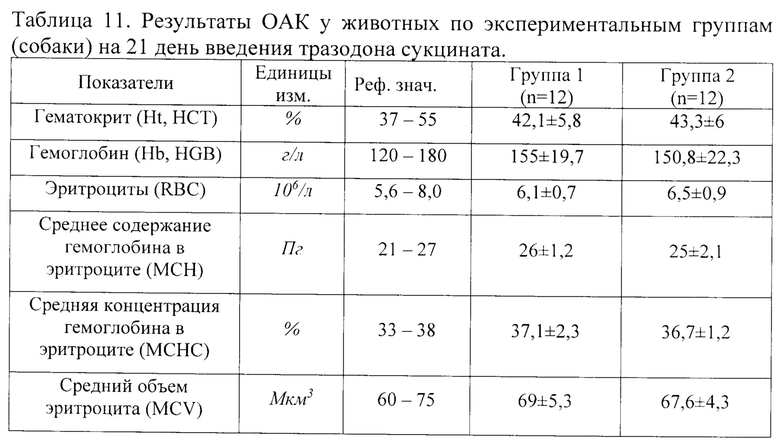
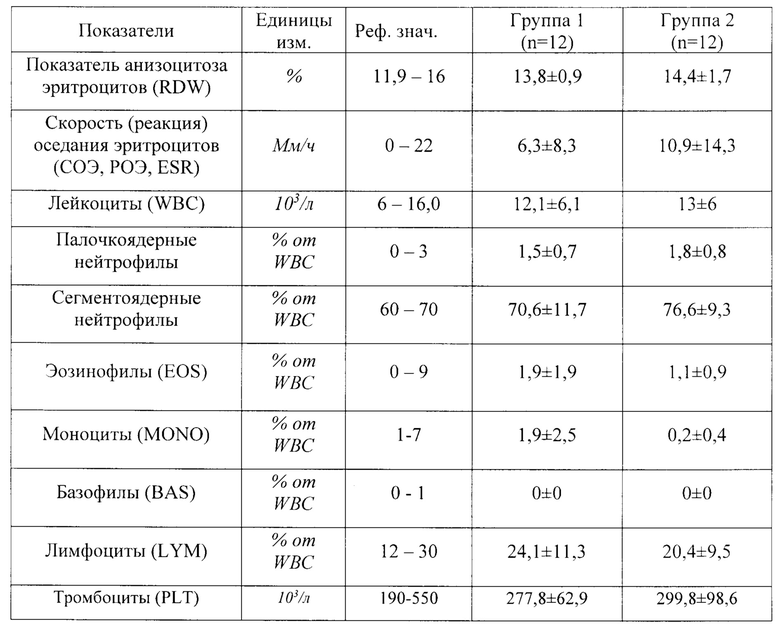
Как следует из данных, представленных в таблице 11 результаты исследований ОАК не выявили значимых различий по показателям крови между Группами 1 и 2. Средние значения всех показателей в обеих группах находились в пределах физиологической нормы.
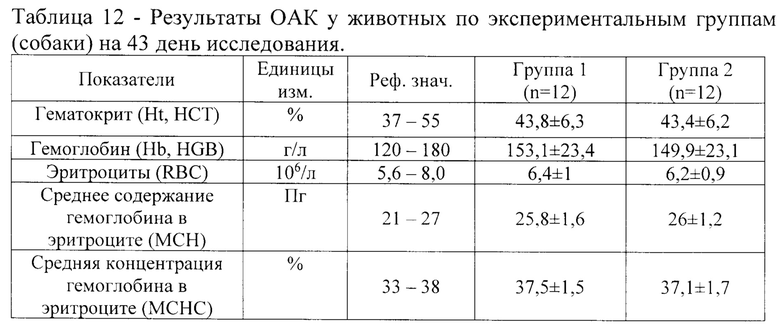
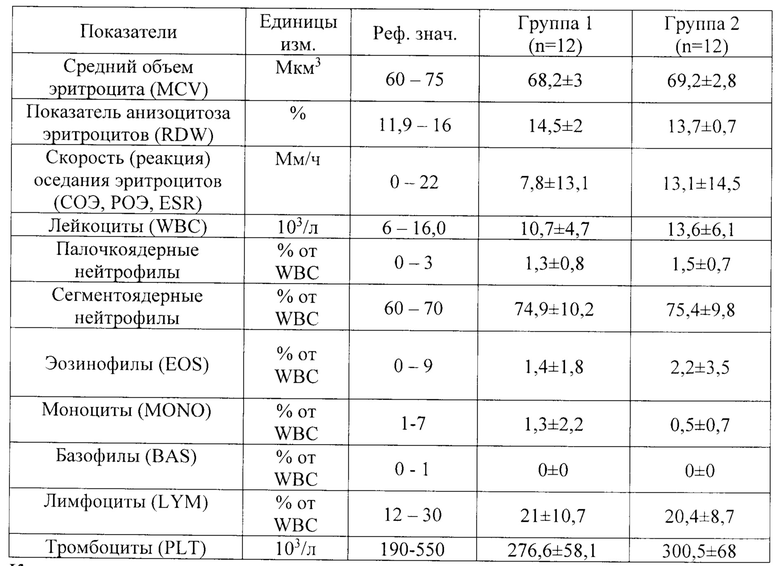
Как следует из данных, представленных в таблице 12 результаты исследований ОАК не выявили значимых различий по показателям крови между Группами 1 и 2. Средние значения всех показателей в обеих группах находились в пределах физиологической нормы.
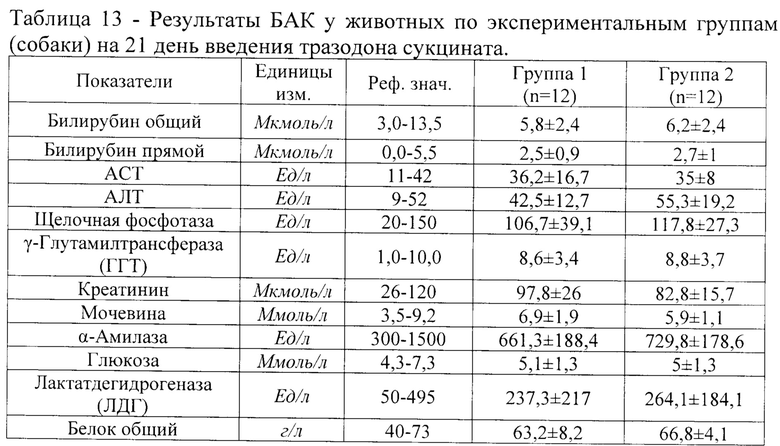
Как следует из данных, представленных в таблице 13 результаты исследований БАК не выявили значимых различий по показателям крови между Группами 1 и 2. Средние значения всех показателей в обеих группах находились в пределах физиологической нормы.
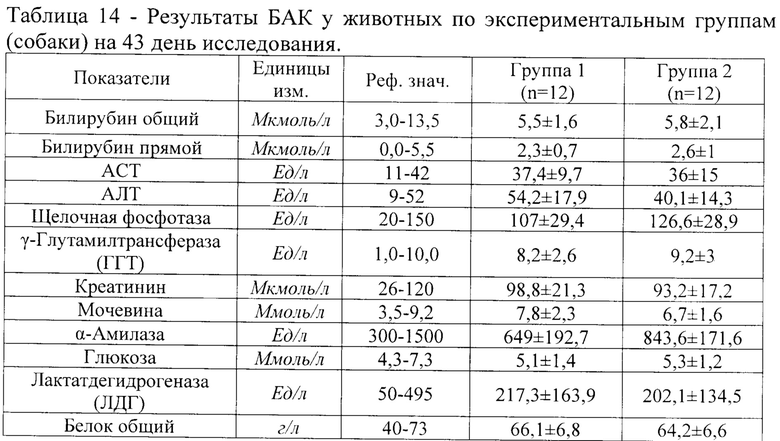
Как следует из данных, представленных в таблице 14 результаты исследований БАК не выявили значимых различий по показателям крови между Группами 1 и 2. Средние значения всех показателей в обеих группах находились в пределах физиологической нормы.
Таким образом, нежелательных реакций, связанных с применением курса тразодона сукцината, а также после отмены препарата, не зарегистрировано.
Пример 10. Влияние тразодона сукцината на динамику гематологических показателей у кошек.
Общий анализ крови (ОАК) и биохимический анализ крови (БАК) проводился у всех животных натощак, доступ к воде при этом не ограничивали. Как в Группе 1, так и Группе 2 в установленные контрольные сроки исследования брали кровь: на 21 день введения тразодона сукцината и на 43 день исследования (первый день отмены тразодона сукцината).
Результаты сравнения данных ОАК на 21 день введения тразодона сукцината представлены в таблице 15, результаты сравнения данных ОАК на 43 день исследования (первый день отмены тразодона сукцината после 6-ти недельного курса) представлены в таблице 16.
Результаты сравнения данных БАК на 21 день введения тразодона сукцината представлены в таблице 17, результаты сравнения данных БАК на 43 день исследования (первый день отмены тразодона сукцината после 6-ти недельного курса) представлены в таблице 18.
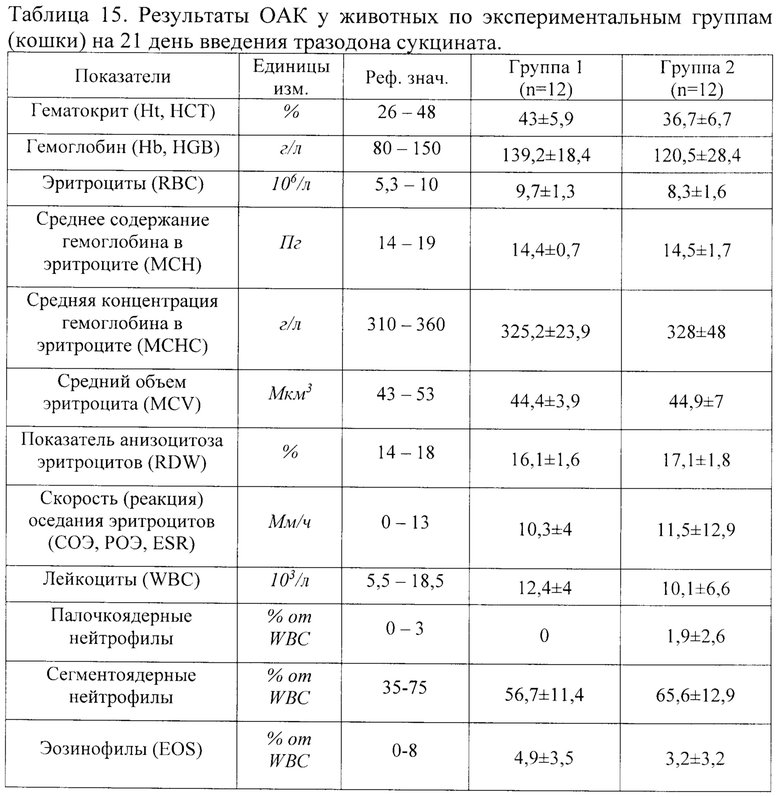
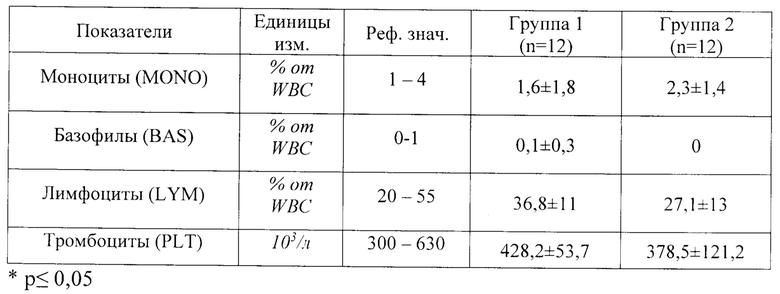
Как следует из данных по исследованию ОАК, представленных в таблице 15, значимых различий по показателям между группами при введении тразодона сукцината на 21 день исследования не выявлено. Средние значения всех показателей в обеих группах находятся в пределах физиологической нормы.
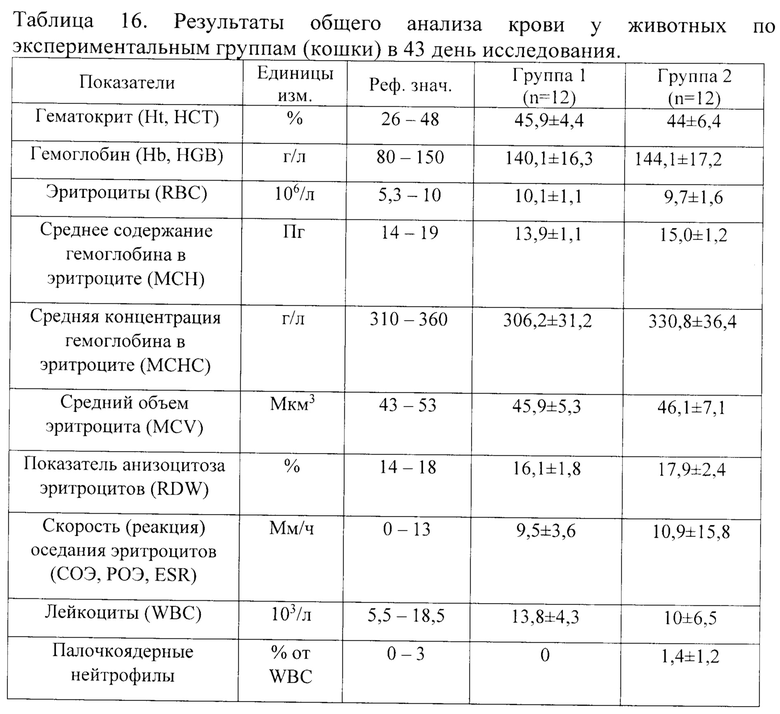
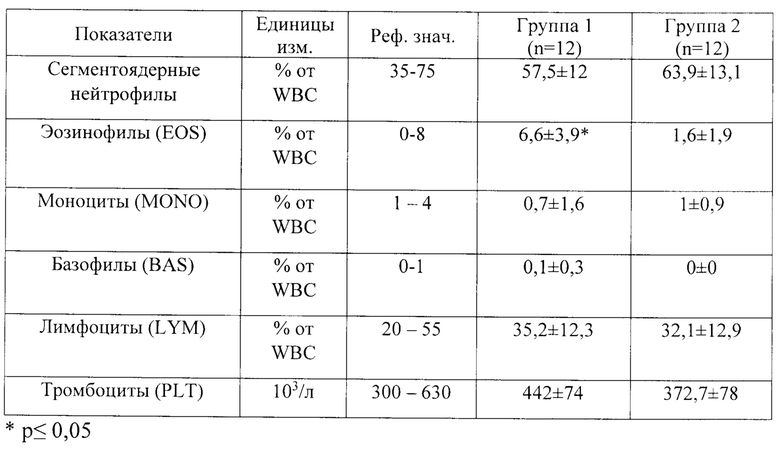
Как следует из данных по исследованию ОАК, представленных в таблице 16, значимых различий по показателям между группами на 43 день исследования не выявлено. Средние значения всех показателей в обеих группах находятся в пределах физиологической нормы.
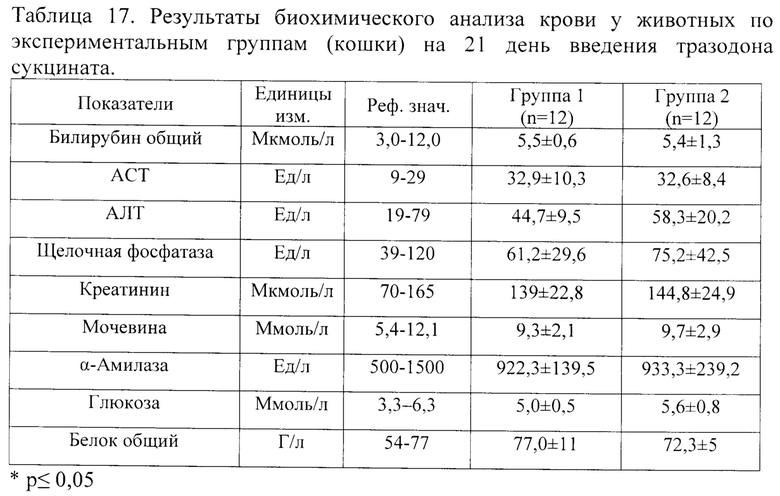
Как следует из данных по исследованию БАК, представленных в таблице 17, значимых различий по показателям между группами при введении тразодона сукцината на 21 день исследования не выявлено. Средние значения всех показателей в обеих группах находятся в пределах физиологической нормы.
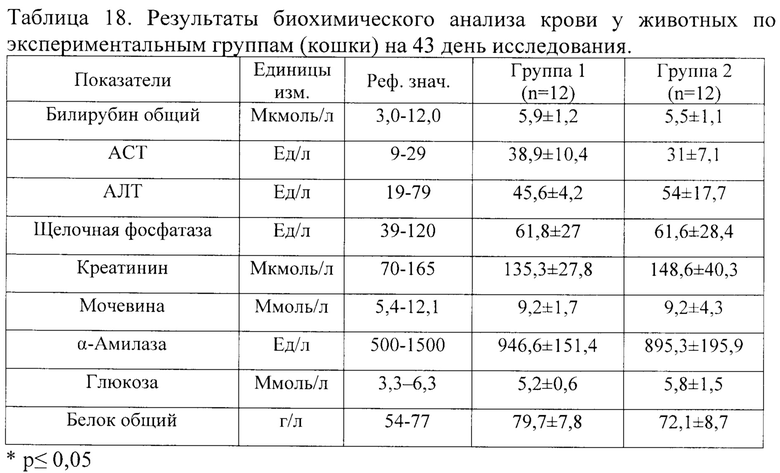
Как следует из данных по исследованию БАК, представленных в таблице 18, значимых различий по показателям между группами на 43 день исследования не выявлено. Средние значения всех показателей в обеих группах находятся в пределах физиологической нормы.
Таким образом, нежелательных реакций, связанных с применением курса тразодона сукцината, а также после его отмены, не зарегистрировано. Пример 11. Оценка хронической токсичности тразодона сукцината на собаках по влиянию длительного применения на биохимические показатели крови.
Исследования проводились в приюте «БИМ-Хотеичи» в период с апреля 2021 года по апрель 2022 года.
В эксперименте участвовали 18 собак породы метис, возрастом 1-7 лет, массой тела 14-26 кг, которые были помещены на 7 дней в вольеры для карантина и адаптации с ежедневным контрольным осмотром ветеринарным врачом для выявления проявлений отклонений в здоровье. По результатам осмотра все животные были клинически здоровы. Животные содержались при стандартном освещении и комнатной температуре, получали одинаковый рацион, который был сбалансирован по основным питательным веществам в соответствии с нормами кормления и имели свободный доступ к питьевой воде.
Безопасность длительного применения тразодона сукцината оценивалась по динамике изменения массы тела животных в течении 180 дней и последующем наблюдении за изменением биохимических показателей крови до 12 месяцев включительно.
Животных распределяли по группам случайным образом, используя в качестве критерия массу тела, так, чтобы средние показатели массы тела не отличались между группами более чем на 20%.
Были сформированы 3 группы животных (2 опытные и 1 контрольная по 6 голов в каждой). Каждому животному, включённому в исследование, предварительно был имплантирован микрочип, в памяти которого содержится код, состоящий из комбинации букв и цифр, позволяющий однозначно идентифицировать животное.
Собакам Групп 1 и 2 задавали тразодон сукцинат два раза в день в одно и тоже время за час до еды в течение 360 дней в дозах:
Группа 1 (n=6)- 10,0-11,5 (10,8±0,54) мг/кг
Группа 2 (n=6)- 12,6-16,0 (14,4±1,4) мг/кг
Собакам Группы плацебо (n=6) скармливали состав, включающий лактозу моногидрат, натрий кроскармеллозу, повидон, кремния диоксид коллоидный безводный, магния стеарат, пищевую добавку со вкусом мяса.
Кровь у животных брали натощак, доступ к воде при этом не ограничивали. Результаты исследования биохимических показателей крови вплоть до 360 дней приведены в таблице 19.
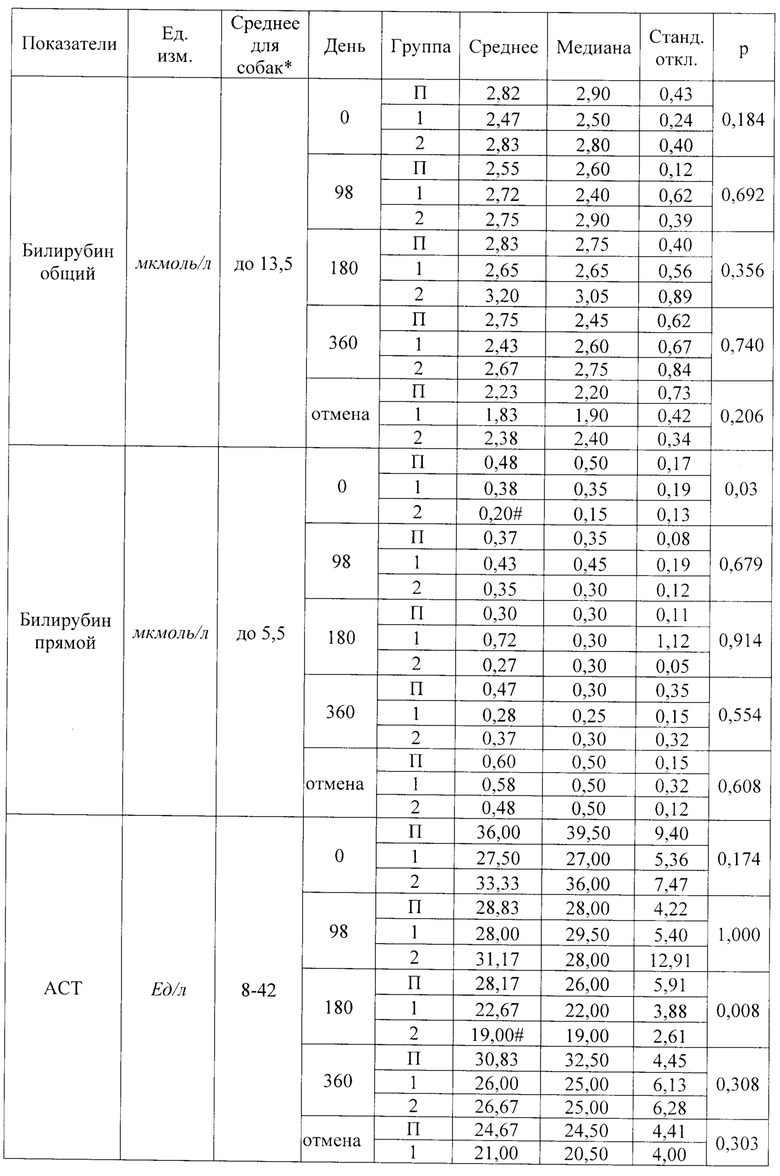
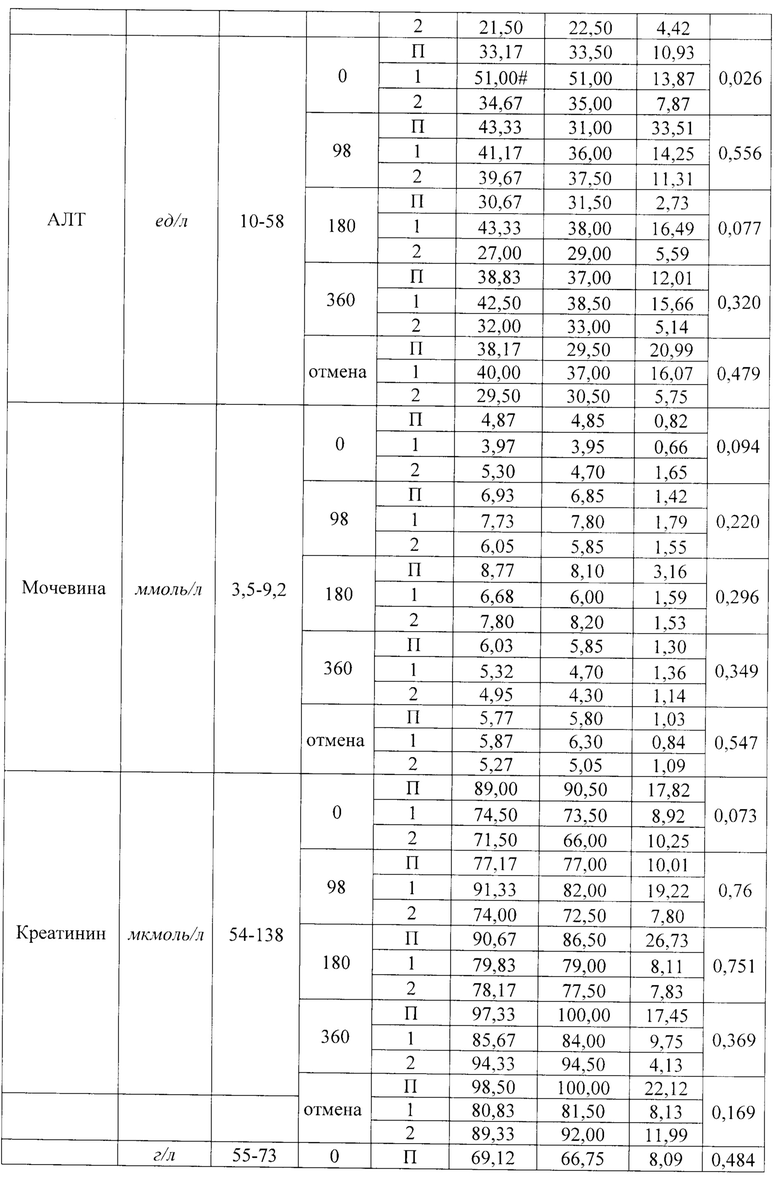
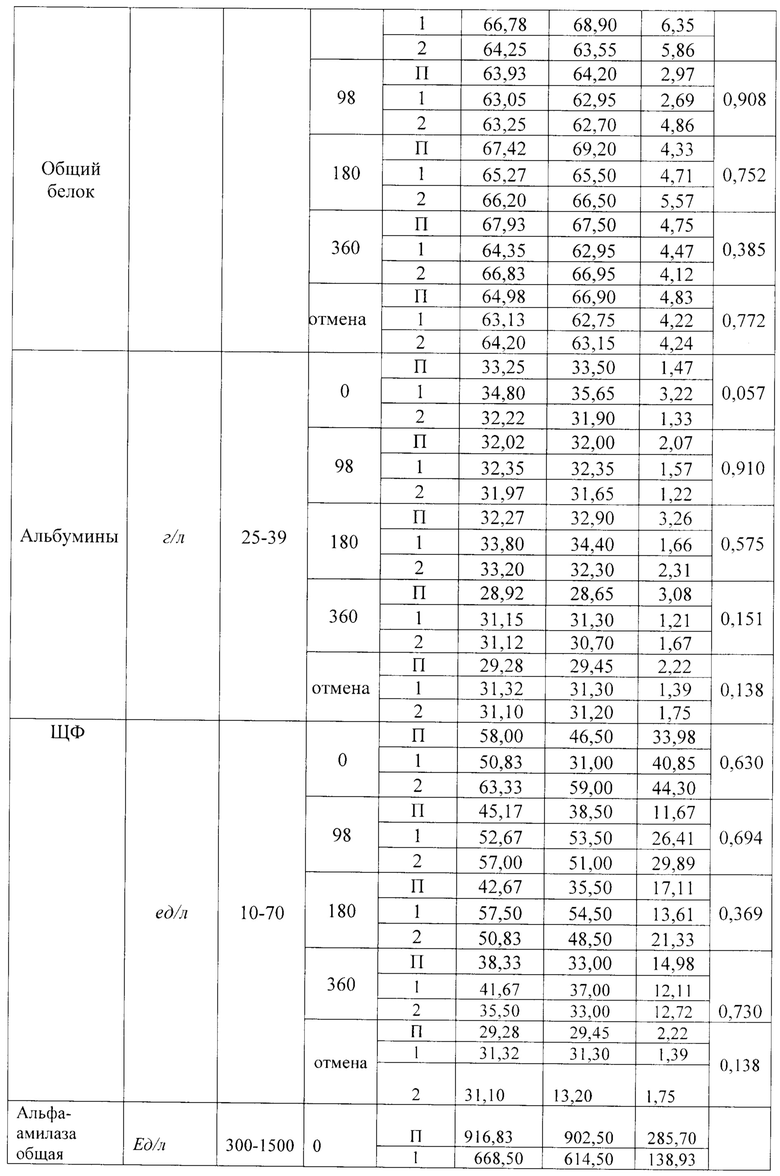
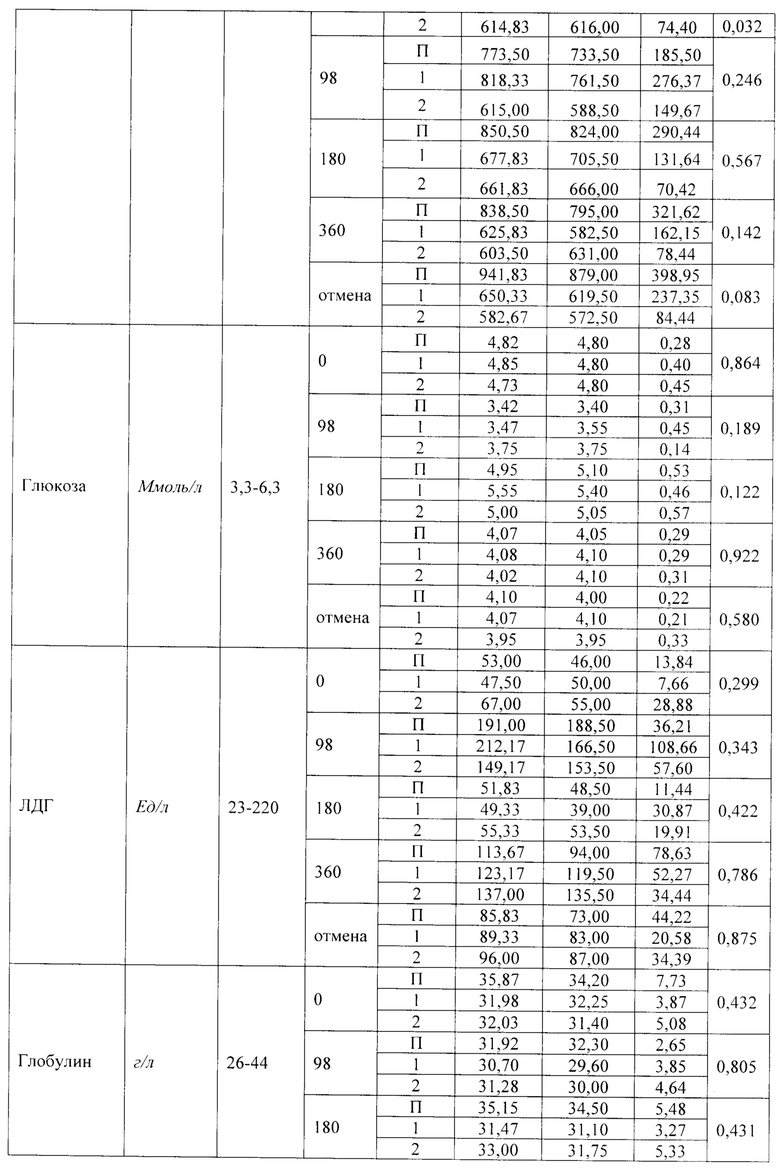
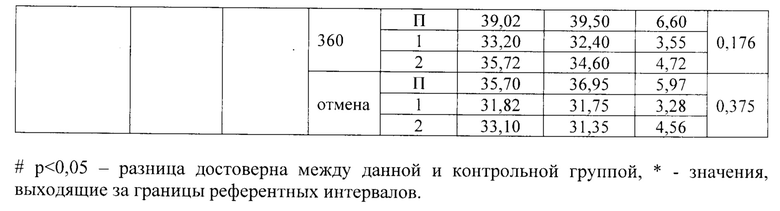
Результаты БАК собак, приведенные в таблице 19, свидетельствуют об отдельных статистически достоверных отличиях между опытными группами и контролем по некоторым показателям, которые в целом находились в пределах референтных значений. Данные различия не являются клинически значимыми.
При отмене исследуемого препарата нежелательных реакций организма, по биохимическим показателям, не выявлено.
Таким образом, суточная доза 20-23 мг/кг и 25-32 мг/кг тразодона сукцината, превышающие терапевтические дозы более чем в 3 раза, применяемая в течение 360 дней собакам, не оказывает отрицательного влияния на общее состояние животных.
Пример 12. Определение влияния длительного применения тразодона сукцината на массу тела собак.
Для оценки влияния тразодона сукцината на массу тела животных проводили контрольное взвешивание собак на 14, 98, 112 и 180 сутки приема препарата. Собаки, участвующие в эксперименте, были те же, что и в примере 11. Результаты исследования представлены в таблице 20.
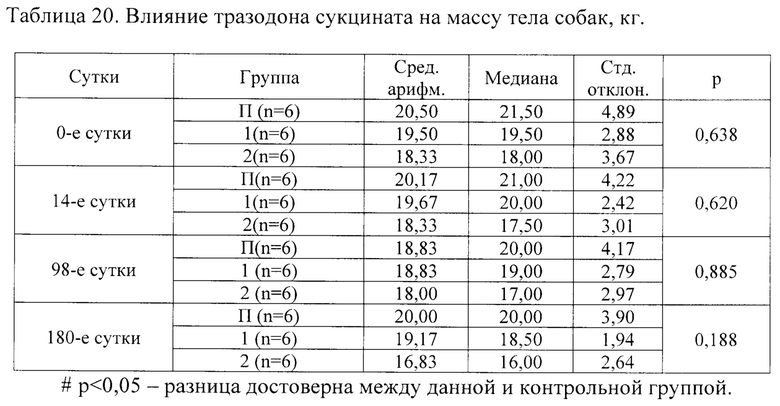
Как следует из данных представленных в таблице 20, статистически достоверных отличий в динамике массы тела собак на 14, 98 и 180 сутки ежедневного введения тразодона сукцината в сравнении с показателями группы П (плацебо), в которой тразодона сукцинат не применялся, не установлено.
В результате ежедневного наблюдения за животными в течение экспериментального периода было установлено, что:
- ежедневное пероральное введение тразодона сукцината собакам в течение 360 дней в средней дозе 10,8 мг/кг массы тела животного 2 раза в день не приводит к изменениям в общем состоянии животных;
- ежедневное пероральное введение тразодона сукцината собакам в течение 360 дней в средней дозе 14,4 мг /кг массы тела животного 2 раза в день не приводит к изменениям в общем состоянии животных.
Собаки опытных групп потребляли корм и воду в тех же количествах, что и животные контрольной группы, были активны, беспокойство и вялость у животных не регистрировали, состояние шерстного покрова и видимых слизистых оболочек не изменялось и было в норме. На протяжении всего эксперимента гибели животных не регистрировали.
Пример 13. Оценка хронической токсичности тразодона сукцината на кошках по влиянию на биохимические показатели крови.
Исследования проводились в приюте «БИМ-Хотеичи» в период с апреля 2021 по апрель 2022 года.
В эксперименте участвовали 18 кошек породы метис, возрастом 2-7 лет, массой тела 3,5-6 кг, которые были помещены на 14 дней в вольеры для карантина и адаптации с ежедневным контрольным осмотром ветеринарным врачом для выявления проявлений отклонений в здоровье. По результатам осмотра все животные были клинически здоровы. Животные содержались при стандартном освещении и комнатной температуре, получали одинаковый рацион, который был сбалансирован по основным питательным веществам в соответствии с нормами кормления и имели свободный доступ к питьевой воде.
Безопасность длительного применения тразодона сукцината оценивалась по динамике изменения массы тела животных в течении 180 дней и последующем наблюдении за изменением биохимических показателей крови до 12 месяцев включительно.
Животных распределяли по группам случайным образом, используя в качестве критерия массу тела, так, чтобы средние показатели массы тела не отличались между группами более чем на 20%.
Были сформированы 3 группы животных (2 опытные и 1 контрольная по 6 голов в каждой). Каждому животному, включённому в исследование, предварительно был имплантирован микрочип, в памяти которого содержится код, состоящий из комбинации букв и цифр, позволяющий однозначно идентифицировать животное.
Кошкам Групп 1 и 2 задавали тразодон сукцинат два раза в день в одно и тоже время за час до еды в течение 360 дней в дозах:
Группа 1 (n=6)- 8,0-10,0 (9±0,6) мг/кг
Группа 2 (n=6)- 12,0-13,7 (12,6±0,9) мг/кг
Кошкам Группы плацебо (n=6) скармливали состав, включающий лактозу моногидрат, натрий кроскармеллозу, повидон, кремния диоксид коллоидный безводный, магния стеарат, пищевую добавку со вкусом мяса. Кровь у животных брали натощак, доступ к воде при этом не ограничивали. Результаты исследования биохимических показателей крови вплоть до года приведены в таблице 21.
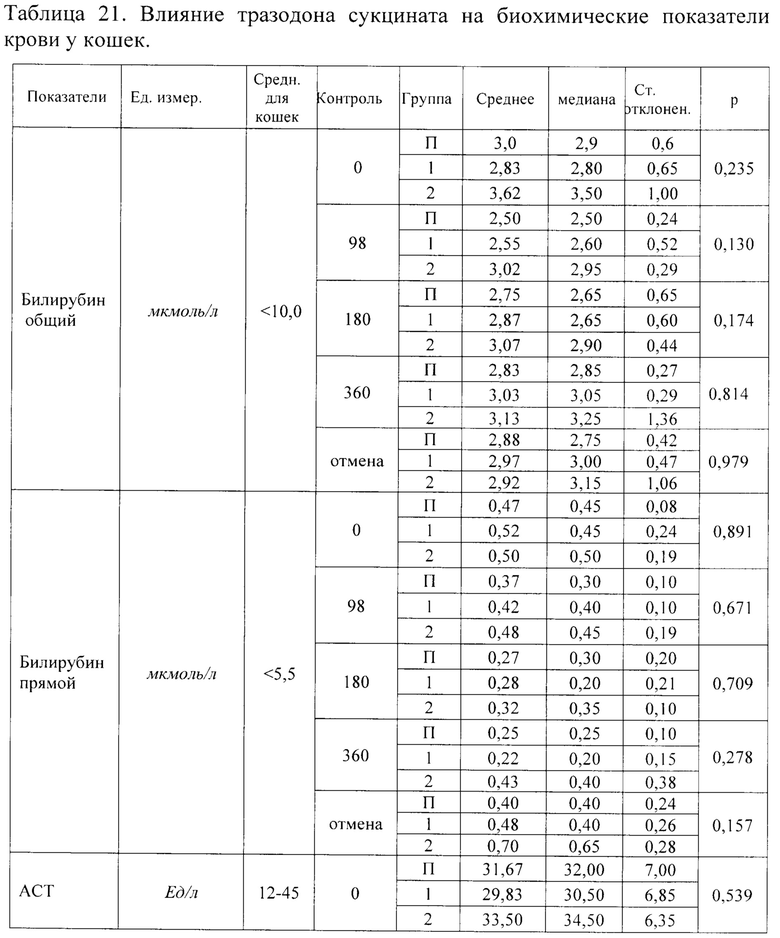
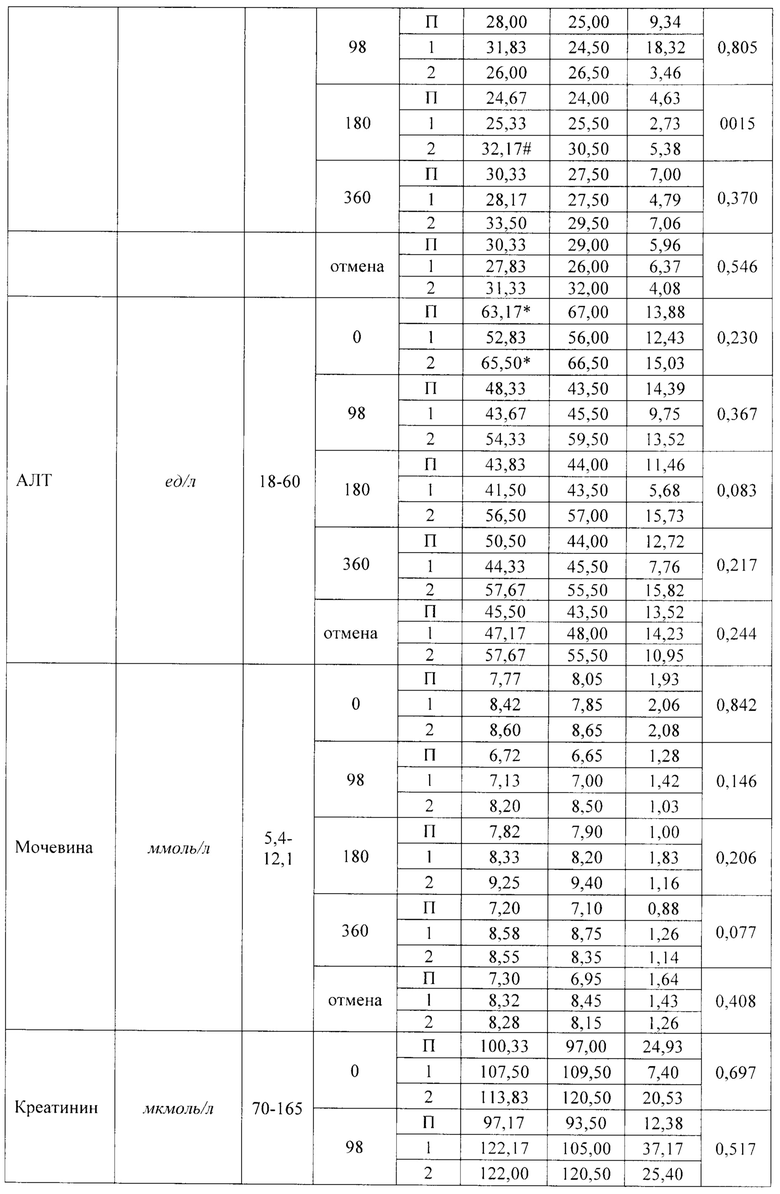
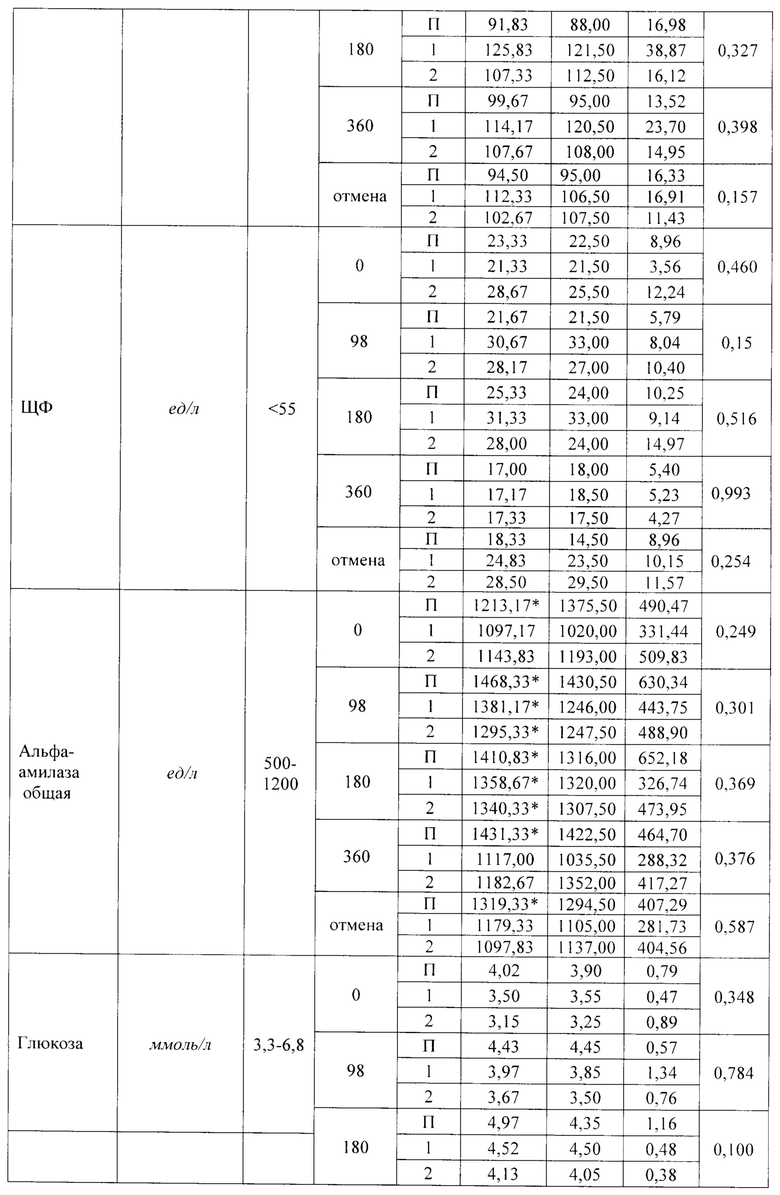
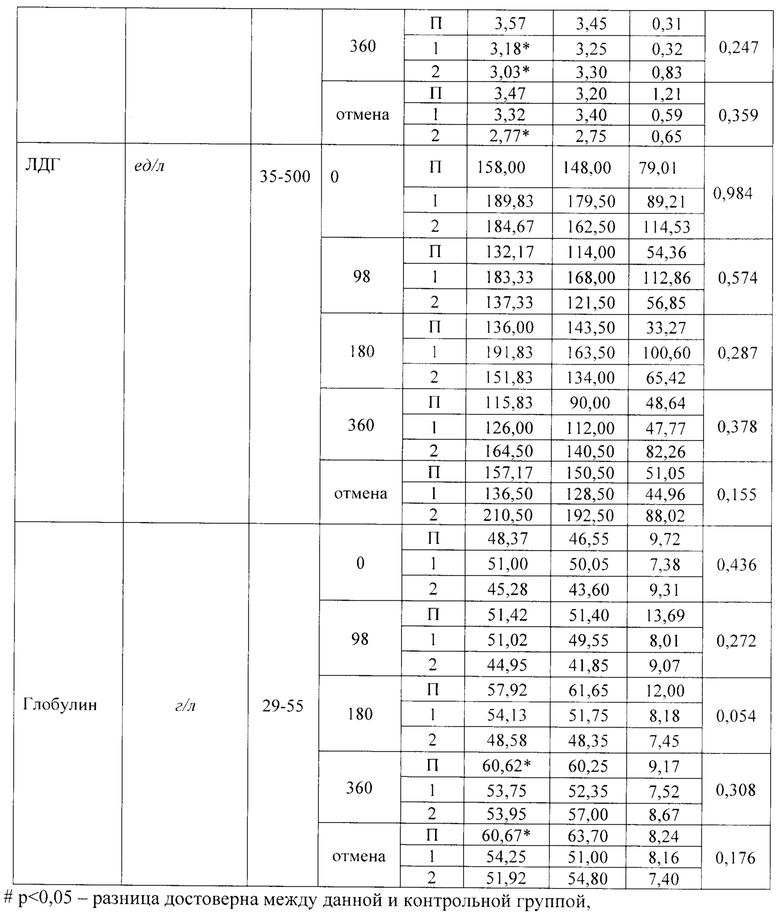
Результаты, приведенные в таблице 21 свидетельствуют об отдельных статистически достоверных отличиях между опытными группами и контролем по некоторым показателям, которые находились в пределах референтных значений. Клинического значения данные различия не имеют.
Незначительное увеличение значения показателя альфа-амилазы во всех группах при отсутствии каких-либо негативных симптомов, клинического значения не имеет. При отмене исследуемого препарата нежелательных реакций организма, по биохимическим показателям, не выявлено.
Пример 14. Определение хронической токсичности тразодона сукцината на кошках по влиянию на массу тела.
Для оценки влияния тразодона сукцината на массу тела животных проводили контрольное взвешивание кошек на 14, 98 и 180 сутки приема препарата. Кошки использовались те же, что и в примере 13. Результаты исследования представлены в таблице 22.
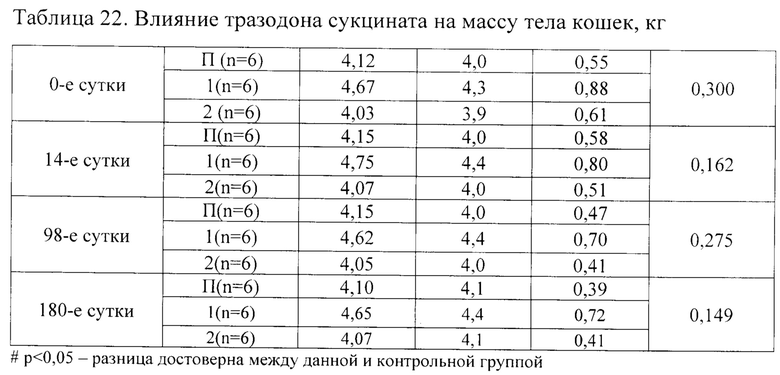
Как следует из данных представленных в таблице 22, статистически достоверных отличий в динамике массы тела кошек на 14, 98 и 180 сутки ежедневного введения тразодона сукцината в сравнении с показателями группы П (плацебо), в которой тразодон сукцинат не применялся, не установлено.
В результате ежедневного наблюдения за животными в течение экспериментального периода было установлено, что:
- ежедневное пероральное введение тразодона сукцината в течение 360 дней в средней дозе 9,0 мг/кг массы тела животного 2 раза в день не приводит к изменениям в общем состоянии животных;
- ежедневное пероральное введение тразодона сукцината в течение 360 дней в средней дозе 12,6 мг /кг массы тела животного 2 раза в день не приводит к изменениям в общем состоянии животных.
Таким образом, суточная доза 18 мг/кг и 25 мг/кг тразодона сукцината, превышающие терапевтические дозы более чем в 3 раза, применяемая в течение 360 дней кошкам, не оказывает отрицательного влияния на общее состояние животных.
Кошки опытных групп потребляли корм и воду в тех же количествах, что и животные контрольной группы, были активны, беспокойство и вялость у животных не регистрировали, состояние шерстного покрова и видимых слизистых оболочек не изменялось и было в норме. На протяжении всего эксперимента гибели животных не регистрировали.
ЗАКЛЮЧЕНИЕ
Суммируя изложенное, можно заключить, что результатом настоящего изобретения является разработка нового высокоэффективного способа курсового применения лекарственного средства на основе тразодона сукцината, обеспечивающего лечение когнитивной дисфункции у пожилых МДЖ (собак, кошек) без снижения уровня безопасности препарата при длительном применении.
Настоящее изобретение относится к области ветеринарной медицины, а именно к способу курсового применения лекарственного средства на основе тразодона сукцината для лечения когнитивной дисфункции у пожилых собак и кошек, заключающемуся во введении животному, нуждающемуся в таком лечении, указанного средства в первые три дня приема в разовой дозе 3-6 мг/кг веса, 2 раза в день с интервалом в 12 часов, а начиная с четвертого дня приема, в разовой дозе 6-10 мг/кг веса 2 раза в день с интервалом в 12 часов, при общей продолжительности курса не менее 6-ти недель. Настоящее изобретение обеспечивает высокую терапевтическую эффективность без снижения уровня безопасности при длительном его применении. 22 табл., 14 пр.
Способ курсового применения лекарственного средства на основе тразодона сукцината для лечения когнитивной дисфункции у пожилых собак и кошек, заключающийся во введении животному, нуждающемуся в таком лечении, указанного средства в первые три дня приема в разовой дозе 3-6 мг/кг веса 2 раза в день с интервалом в 12 часов, а начиная с четвертого дня приема - в разовой дозе 6-10 мг/кг веса 2 раза в день с интервалом в 12 часов, при общей продолжительности курса не менее 6-ти недель.
| Фармацевтическая композиция для коррекции поведения кошек и собак в стрессовых ситуациях | 2019 |
|
RU2706700C1 |
| Д.В | |||
| Белоглазов и др., Тразодона сукцинат - новые возможности фармакологической коррекции ситуационных поведенческих отклонений у собак и кошек / Российский ветеринарный журнал, 2021, N.4, стр.2-13 | |||
| WO 2018200850 A1, 01.11.2018 | |||
| Lorena Sordo et al., Cognitive Dysfunction in Cats: Update on Neuropathological and | |||
Авторы
Даты
2023-03-22—Публикация
2022-08-12—Подача