Область техники, к которой относится изобретение
Изобретение относится к медицине, а именно к сердечно-сосудистой хирургии.
Уровень техники
При проведении исследования способа ингибирования развития гиперплазии интимы в области дистального анастомоза в эксперименте на животных использовались свиньи породы Крупная белая, мужского пола, весом от 90 до 100 кг, физически здоровые.
В отношении снижения активности неоинтимальной гиперплазии давно доказана эффективность применения цитостатических препаратов в эндоваскулярной хирургии, где для решения данной проблемы широко используется лекарственное покрытие цитостатическими препаратами стентов и баллонов. Несмотря на то, что в эндоваскулярной хирургии данные лекарственные препараты широко используются, нет клинически доказанных эффективных методов локального использования лекарственных препаратов в открытой хирургии.
Известно несколько способов местной доставки цитостатических препаратов, в частности паклитаксела, в периферические сосуды, это стенты и баллоны с лекарственным покрытием.
Прототипом нашего способа является локальная доставка жидкости в сосудистое русло (Катетерная инфузия растворов) - LLD.
Местная доставка жидкости - катетерная инфузия растворов, содержащих паклитаксел, была исследована как метод доставки в качестве дополнения или альтернативы стентам и балонам. Три препарата для внутриартериальной местной доставки паклитаксела включают этанол-Кремофор (полиэтоксилированное касторовое масло), йопромидное контрастное вещество и наночастицы альбумина. Теоретически она может обеспечить равномерную доставку высоких доз лекарства к стенке сосуда без необходимости в постоянном металлическом имплантате или полимерном материале-носителе. В отличие от балонов, LLD доставляется под низким давлением. Было исследовано множество катетерных устройств для LLD паклитаксела. Основные категории включают катетеры для доставки с остановкой потока, в которых используется один или несколько окклюзионных баллонов, пористые и микропористые инфузионные баллоны с одним или несколькими слоями, а также катетеры для микроинфузий, в которых используются иглы для вливания раствора непосредственно в стенку сосуда или периваскулярное пространство.
Данные способы имеют следующие недостатки:
- невозможность использования стентов и балонов с лекарственным покрытием в открытой хирургии
- непродолжительный эффект от катетерной инфузии растворов
- неоднородность воздействия по длине и окружности сосуда
- локальный и системный токсический эффект
В заявленном способе перечисленные недостатки устранены.
Раскрытие изобретения
Целью настоящего изобретения является: разработка способа ингибирования развития гиперплазии интимы в области дистального анастомоза
Задачами изобретения являются: увеличение длительности проходимости зон сосудистых реконструкций после открытых оперативных вмешательств и снижения активности неоинтимальной гиперплазии в области дистального анастомоза
Техническим результатам исследования является: изоляция аппликации с цитостатическим препаратом от окружающих тканей, для того чтобы препарат мог проникать только в одном направлении (в стенку сосуда), исключая его токсическое воздействие на окружающие ткани, что также позволит осуществить более равномерное воздействие препарата на «проблемную» зону сосуда.
Осуществление изобретения.
Заявленный технический результат может быть достигнут следующим образом:
Перед операцией всем лабораторным животным в качестве антибактериальной профилактики за 30 минут до кожного разреза внутривенно вводили цефазолин 2.0.
Животное вводится в наркоз с помощью гидрохлорида ксилазина в дозировке 0,2 мл/кг, общая анестезия животных обеспечивается гидрохлоридом тилетамина в сочетании с гидрохлоридом золезепама в дозировке 10 мг/кг.
Перед пережатием артерий внутривенно вводится 7500 ЕД гепарина
Пересекается поверхностная бедренная артерия и формируется артериальный анастомоз проксимального и дистального участков ПБА по типу «конец в бок» с использованием нити пролен 8/0 на атравматической игле.
В области анастомоза периадветициально накладывается аппликация с лекарственным пропитыванием.
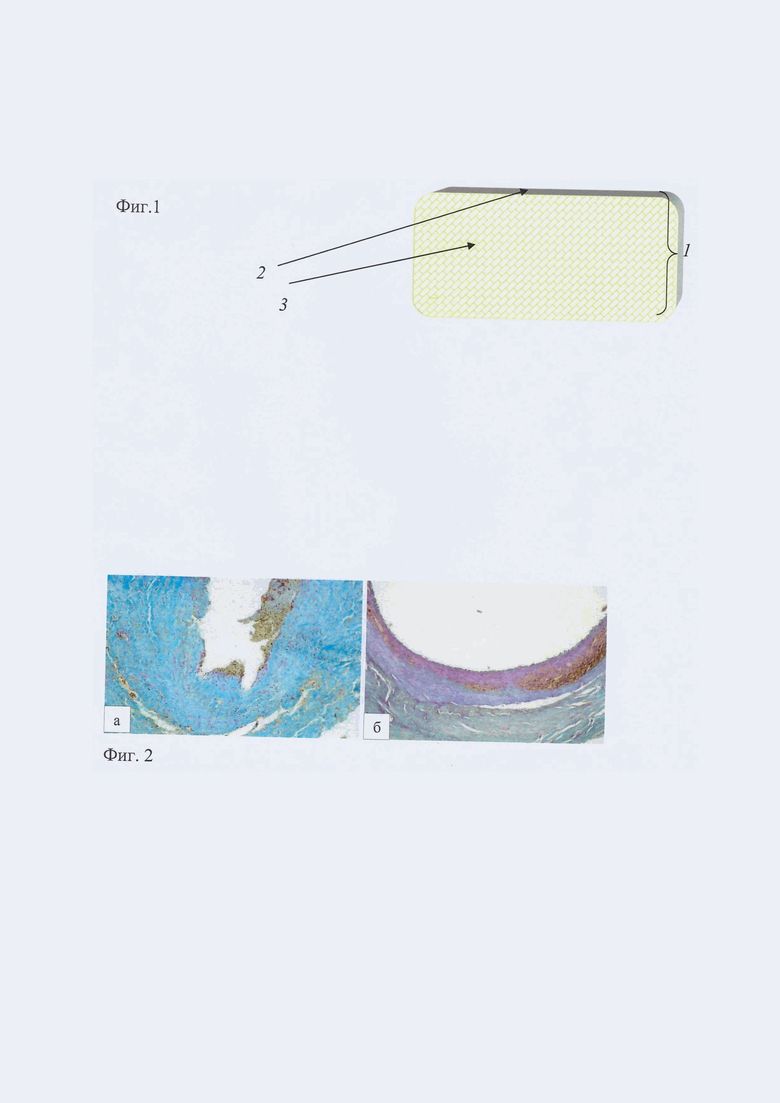
Аппликация проводится с использованием полупроницаемой мембраны (фиг.1). Мембрана с лекарственным пропитыванием изготавливается в стерильных условиях следующим образом: в качестве основы используется гемостатическая целлюлозная ткань (фиг.1 1.) . Перед операцией у лабораторного животного производится забор 10 мл крови, с помощью центрифуги получают плазму. В плазме растворяется цитостатический препарат паклитаксел.
После чего целлюлозную ткань пропитывают полученным раствором паклитаксела (фиг.1 3 )в расчете 3 мкг паклитаксела 1 мембрану. Одну сторону ткани (мембраны) покрывают медицинским вазелином (фиг.1. 2 ) в качестве изолирующего материала для исключения проникновения лекарственного препарата в окружающие ткани (фиг.1)
Мембрана помещалается в области сосудистого анастомоза стороной, свободной от вазелина - к сосудистой стенке.
В послеоперационном периоде всем животным для антитромботической профлактики подкожно вводится эноксапарин натрия 0.1 мл на 10 кг массы тела 2 раза в сутки.
Через 2 недели проводятся повторные операции под общей анестезией по забору области реконструкций. Полученные препараты изучаются гистологически, при микроскопии срезов используется гематоксилин-эозин и трихромное окрашивание по Маллори, оценивается выраженность неоинтимальной гиперплазии.
Конкретный пример реализации технического решения.
Проведен анализ результатов 6 экспериментальных операций на магистральных сосудах 3 лабораторных животных (свинья), которым были проведены артериальные реконструкции в условиях вивария ФГБОУ ВО Тверской ГМУ Минздрава России в 2019 г. Период наблюдения составил 2 недели. Использовались свиньи породы Крупная белая, мужского пола, весом от 90 до 100 кг, физически здоровые.
Перед операцией всем лабораторным животным в качестве антибактериальной профилактики за 30 минут до кожного разреза внутривенно вводили цефазолин 2.0.
Операции выполнены с применением неингаляционного наркоза гидрохлоридом ксилазина в дозировке 0,2 мл/кг, общая анестезия животных обеспечивалась гидрохлоридом тилетамина в сочетании с гидрохлоридом золезепама в дозировке 10 мг/кг.
Перед пережатием артерий внутривенно вводили 7500 ЕД гепарина (в связи с наличием у свиней выраженной склонности к гиперкоагуляции).
У каждого животного операция производилась одномоментно на обеих задних конечностях. После пересечения поверхностной бедренной артерии (ПБА) формировали артериальный анастомоз проксимального и дистального участков ПБА по типу «конец в бок» с использованием нити пролен 8/0 на атравматической игле. Таким образом в дистальном участке артерии создавали гемодинамический удар для провоцирования развития неоинтимальной гиперплазии. На левой конечности в области анастомоза периадветициально накладывали аппликацию с лекарственным пропитыванием, на правой - без лекарственного пропитывания. (Фиг. 5.).
Аппликация проводилась с использованием полупроницаемой мембраны. Мембрана была двух видов: с лекарственным пропитыванием и без него. Мембрана с лекарственным пропитыванием изготавливалась в стерильных условиях следующим образом: в качестве основы использовалась гемостатическая целлюлозной ткань. Перед операцией у лабораторного животного производился забор 10 мл крови, с помощью центрифуги получали плазму. В плазме растворяли цитостатический препарат паклитаксел.
После чего целлюлозную ткань пропитывали полученным раствором паклитаксела в расчете 3 мкг паклитаксела 1 мембрану. Одну сторону ткани (мембраны) покрывали медицинским вазелином в качестве изолирующего материала для исключения проникновения лекарственного препарата в окружающие ткани. Мембрана без лекарственного пропитывания изготавливалась аналогичным образом, но без использования цитостатического препарата.
Мембрана помещалась в области сосудистого анастомоза стороной, свободной от вазелина - к сосудистой стенке.
В послеоперационном периоде всем животным для антитромботической профлактики подкожно вводили эноксапарин натрия 0.1 мл на 10 кг массы тела 2 раза в сутки.
Через 2 недели проводились повторные операции под общей анестезией по забору области реконструкций. Полученные препараты изучались гистологически, при микроскопии срезов использовались гематоксилин-эозин и трихромное окрашивание по Маллори, оценивалась выраженность неоинтимальной гиперплазии.
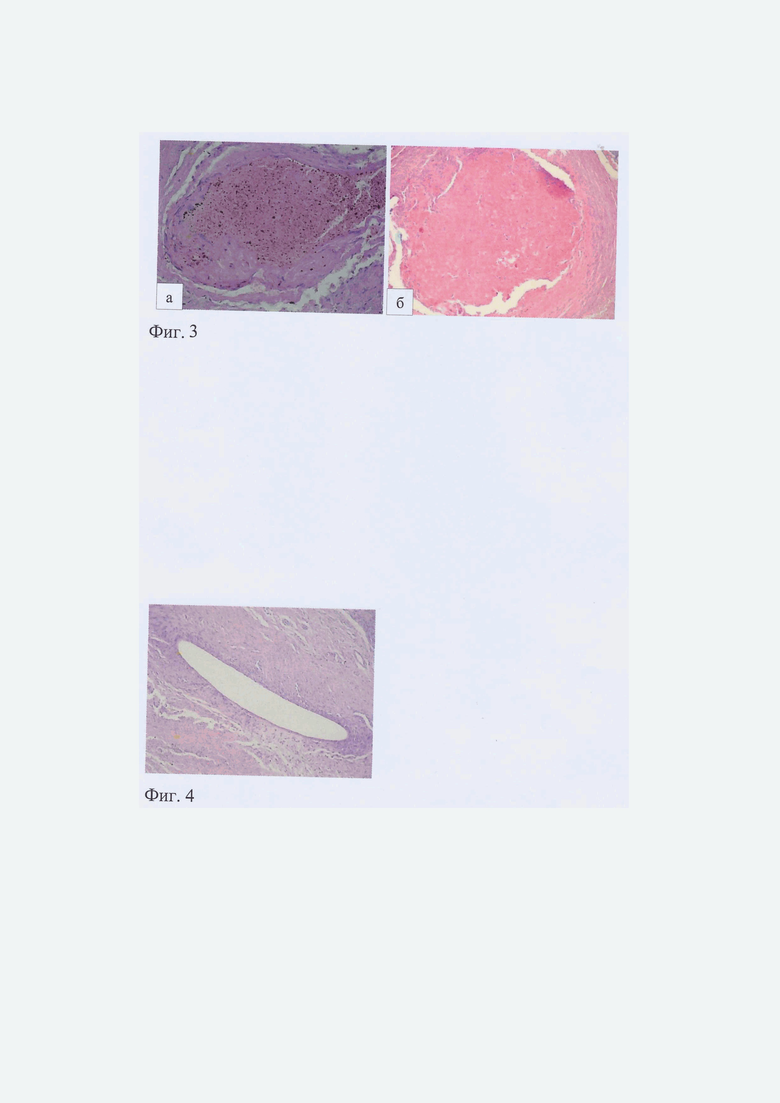
Трихромное окрашивание по Маллори показало существенные структурные различия в строении сосудистой стенки. В участках реконструкции артерии без применения паклитаксела, выявлено утолщение интимы и средней оболочки за счет диффузного разрастания коллагеновых волокон, свидетельствующего о формировании выраженного склероза (фиг. 2а). В случае обработки зоны анастомоза паклитакселем, в субэндотелиальном слое на границе с медиальной оболочкой зафиксирована густая сеть эластических волокон. Средняя оболочка представлена чередующими пучками эластических волокон, гладких мышечных клеток и коллагеновых волокон. Степень выраженности последних увеличивалась от центра к периферии (фиг. 2б). Такое строение артериальной стенки в зоне анастомоза можно расценить как морфологический эквивалент реституции (полной регенерации).
При изучении состояния интимы отмечено ее утолщение. В препаратах анастомоза, не обработанного лекарственным средством, на отдельных участках обнаружено отсутствие эндотелиальной выстилки, отек и пропитывание фибрином субэндотелиального слоя с дефектами базальной мембраны (фиг. 3а). В других участках наблюдалась очаговая гиперплазия эндотелия с формированием гофрированного рельефа внутренней поверхности (фиг. 3б). Просвет сосуда обтурирован тромбом, фиксированным к эндотелию (фиг. 3б).
В препаратах после применения паклитаксела участки анастомоза были полностью выстланы неоинтимой. Базальная мембрана четко контурировалась по всему периметру, гиперплазия эндотелия носила очаговый характер без формирования складок, признаки пристеночного тромбоза отсутствовали (фиг.4).
Сравнение морфологического строения стенки артерий в зоне анастомоза в зависимости от использования цитостатического препарата представлено в таблице 1.
Морфологическое строение артериальной стенки в зоне анастомоза в зависимости от использования паклитаксела
Фибриноидный некроз, дефекты базальной мембраны
Использованная нами в экспериментальной работе методика аппликации зоны анастомоза цитостатическим препаратом Паклитаксел показала положительные результаты в отношении ингибирования развития НИГ. При микроскопическом исследовании зон анастомоза с применением паклитаксела, артериальные стенки оказались полностью выстланы неоинтимой, гиперплазия эндотелия носила очаговый характер без формирования складок, тромботические массы полностью отсутствовали. В то же время, микроскопический анализ артериальной стенки, реконструированной без использования паклитаксела, зафиксирована морфологическая картина продуктивного воспаления, наблюдалась очаговая гиперплазия эндотелия с формированием гофрированного рельефа внутренней поверхности, а также тромботические массы, фиксированные к эндотелию.
Новизна заявленного способа заключается в том, что
- впервые использована полупроницаемая мембрана, пропитанная раствором паклитаксела, в качестве аппликации зоны сосудистого анастомоза;
- впервые разработан способ местной доставки цитостатического препарата, исключающий системное действие препарата;
- впервые разработан и испытан в эксперименте на лабораторных животных метод фармакологически активной аппликации зоны хирургического анастомоза;
- стоимость данного метода ниже, чем при использовании стентов и балонов с лекарственным покрытием.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ профилактики рестеноза после шунтирующих операций на артериях нижних конечностей | 2023 |
|
RU2826614C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ПОЗДНИХ ТРОМБОТИЧЕСКИХ РЕОККЛЮЗИЙ | 2010 |
|
RU2438591C1 |
| ЭНДОЛЮМИНАЛЬНЫЙ ПРОТЕЗ, СОДЕРЖАЩИЙ ЛЕЧЕБНОЕ СРЕДСТВО | 2004 |
|
RU2360646C2 |
| ЛОКАЛЬНАЯ СОСУДИСТАЯ ДОСТАВКА ПРОБУКОЛА, ОДНОГО ИЛИ В КОМБИНАЦИИ С СИРОЛИМУСОМ, ДЛЯ ЛЕЧЕНИЯ РЕСТЕНОЗА, УЯЗВИМЫХ БЛЯШЕК, ААА (АНЕВРИЗМЫ БРЮШНОЙ АОРТЫ) И ИНСУЛЬТА | 2008 |
|
RU2481084C2 |
| УСТРОЙСТВО ДЛЯ ЛОКАЛЬНОЙ И/ИЛИ РЕГИОНАРНОЙ ДОСТАВКИ С ПРИМЕНЕНИЕМ ЖИДКИХ СОСТАВОВ ТЕРАПЕВТИЧЕСКИ АКТИВНЫХ ВЕЩЕСТВ | 2009 |
|
RU2596092C2 |
| УСТРОЙСТВО ДЛЯ ЛОКАЛЬНОЙ И/ИЛИ РЕГИОНАРНОЙ ДОСТАВКИ С ПРИМЕНЕНИЕМ ЖИДКИХ СОСТАВОВ ТЕРАПЕВТИЧЕСКИ АКТИВНЫХ ВЕЩЕСТВ | 2009 |
|
RU2513153C2 |
| МЕДИЦИНСКОЕ УСТРОЙСТВО, ДОСТАВЛЯЮЩЕЕ ЛЕКАРСТВЕННОЕ СРЕДСТВО, СПОСОБ ЕГО ПОЛУЧЕНИЯ И СПОСОБ ДОСТАВКИ ЛЕКАРСТВЕННОГО СРЕДСТВА | 2010 |
|
RU2573045C2 |
| СПОСОБ ОЦЕНКИ ФУНКЦИОНАЛЬНОГО СОСТОЯНИЯ ЭНДОТЕЛИЯ ЭКСПЕРИМЕНТАЛЬНЫХ ЖИВОТНЫХ ПОСЛЕ РЕКОНСТРУКТИВНЫХ ОПЕРАЦИЙ НА БРЮШНОЙ АОРТЕ | 2012 |
|
RU2503961C2 |
| Способ лечения истинной аневризмы плечевой артерии у детей | 2024 |
|
RU2831899C1 |
| СТЕНТ, ВЫДЕЛЯЮЩИЙ РАПАМИЦИН | 2010 |
|
RU2563429C2 |

Изобретение относится к экспериментальной медицине, а именно к сердечно-сосудистой хирургии. Одномоментно пересекают поверхностную бедренную артерию (ПБА) на обеих задних конечностях свиньи породы Крупная белая мужского пола. Формируют артериальный анастомоз проксимального и дистального участков ПБА по типу «конец в бок». На левую конечность в области анастомоза периадветициально накладывают аппликацию с лекарственным пропитыванием, причем аппликацию проводят с использованием полупроницаемой мембраны, на которую нанесен раствор паклитаксела в расчете 3 мкг паклитаксела на 1 мембрану. Одну сторону мембраны покрывают медицинским вазелином, мембрану помещают в область сосудистого анастомоза стороной, свободной от вазелина, к сосудистой стенке. Аналогичным образом на правую конечность накладывают аппликацию без лекарственного пропитывания. Через 2 недели проводят повторные операции по забору области реконструкций для гистологического исследования. Способ обеспечивает изоляцию аппликации с цитостатическим препаратом от окружающих тканей, для проникновения препарата только в стенку сосуда, исключая его токсическое воздействие на окружающие ткани, что также позволит осуществить более равномерное воздействие препарата на «проблемную» зону сосуда, обеспечивает увеличение длительности проходимости зон сосудистых реконструкций после открытых оперативных вмешательств и снижение активности неоинтимальной гиперплазии в области анастомоза. 5 ил., 1 табл., 1 пр.
Способ исследования ингибирования развития гиперплазии интимы в области сосудистого анастомоза в эксперименте на свиньях породы Крупная белая мужского пола, включающий одномоментное пересечение поверхностной бедренной артерии (ПБА) на обеих задних конечностях свиньи, затем формируют артериальный анастомоз проксимального и дистального участков ПБА по типу «конец в бок», на левую конечность в области анастомоза периадветициально накладывают аппликацию с лекарственным пропитыванием, причем аппликацию проводят с использованием полупроницаемой мембраны, на которую нанесен раствор паклитаксела в расчете 3 мкг паклитаксела на 1 мембрану, одну сторону мембраны покрывают медицинским вазелином, мембрану помещают в область сосудистого анастомоза стороной, свободной от вазелина, к сосудистой стенке; аналогичным образом на правую конечность накладывают аппликацию без лекарственного пропитывания, через 2 недели проводят повторные операции по забору области реконструкций для гистологического исследования, при микроскопии срезов используют гематоксилин-эозин и трихромное окрашивание по Маллори, оценивают выраженность неоинтимальной гиперплазии.
| TAKAHISA MASAKI et al | |||
| Inhibition of neointimal hyperplasia in vascular grafts by sustained perivascular delivery of paclitaxel, Kidney International, 2004, vol.66, is.5, pp.2061-2069 | |||
| ИНГИБИТОР ГИПЕРПЛАЗИИ ИНТИМЫ СОСУДОВ | 2005 |
|
RU2339381C2 |
| СПОСОБ ПРОФИЛАКТИКИ ТРОМБОТИЧЕСКИХ ОСЛОЖНЕНИЙ ПОСЛЕ РЕКОНСТРУКТИВНЫХ СОСУДИСТЫХ ХИРУРГИЧЕСКИХ ВМЕШАТЕЛЬСТВ | 2004 |
|
RU2308227C2 |
| ПРИСПОСОБЛЕНИЕ ДЛЯ НАВИВАНИЯ ЛЕНТЫ НА ЛЕНТОЧНОМ ТКАЦКОМ СТАНКЕ | 1930 |
|
SU20563A1 |
| US 20070026034 A1, 01.02.2007 | |||
| КОМОВ К.В | |||
| Профилактика гиперплазии неоинтимы | |||
Авторы
Даты
2023-04-04—Публикация
2022-06-29—Подача