Изобретение относится к области нанотехнологий, а именно к способам получения фотокатализаторов на основе гетероструктур для разложения веществ, загрязняющих воздух и воду, и может быть использовано в химической, фармацевтической и биосинтетической промышленности.
В настоящее время наиболее часто в качестве фотокатализаторов предлагают использовать чистый и/или модифицированный диоксид титана (TiO2), который относительно дешев и практически нетоксичен [1, 2]. С его помощью можно окислить до углекислого газа и воды практически любые органические соединения, т.к. окислительный потенциал дырки на поверхности TiO2 составляет около 3 эВ. Несмотря на большое количество предложений по использованию в качестве фотокатализатора диоксида титана имеются работы, посвященные использованию других широкозонных полупроводниковых металлоксидов и их композиций, включая оксиды олова, меди и цинка [3, 4]. Причем фотокатализаторы на основе ZnO и гетероструктур из металлооксидов с различной шириной запрещенной зоны на его основе обладают рядом преимуществ в сравнении с TiO2, включая сочетание повышенной фотокаталитической активности с экологической стабильностью.
Известен способ получения фотокатализатора на основе оксида цинка [1], заключающийся в растворении хлорида цинка в водном растворе многоатомного спирта в процессе гидротермальной обработки и введении в раствор щелочи с последующим отделением получившегося осадка частиц оксида цинка, их промывкой и сушкой. Способ отличается тем, что в водном растворе содержится этиленгликоль с концентрацией от 23 до 27%, в котором при температуре раствора от 60 до 80°С с помощью механического перемешивания растворяют от 23 до 27 мл 2М водного раствора хлорида цинка, обеспечивая его концентрацию в растворе от 0,04 до 0,06 моль/литр, после чего добавляют гидроксид калия из расчета от 40 до 50 грамм на литр раствора и, поддерживая температуру, продолжают перемешивание смеси в течение от 1 до 3 часов до полного растворения гидроксида калия. Затем смесь остывает естественным способом до комнатной температуры и подвергается центрифугированию до полного осаждения частиц. Недостатком такого способа являются ограничения по размеру частиц, используемых в качестве фотокатализатора (580 нм и менее), а также низкая скорость фотокаталитического разложения при очистке воды от фенола в опыте с воздействием дневного освещения (требуется длительность процесса фотокатализа до 25 часов). Кроме того, эффективность реализации способа демонстрируется только для водного раствора фенола с концентрацией 1 мг/л, а способность разложения иных токсичных соединений или загрязнителей, встречающиеся в виде примесей в сточных водах, авторами не подтверждается.
Известен способ получения фотокатализатора на основе механоактивированного порошка оксида цинка [2]. Способ заключается в том, что порошок ZnO подвергают интенсивной механической обработке в воздушной среде, отличающийся тем, что скорость измельчения в размольных барабанах планетарной шаровой мельницы составляет 250 оборотов в минуту, соотношение массы порошка и шаров 10:1, время измельчения 1 минута. Недостатком такого способа является относительно высокая загрузка фотокатализатора 0,5 г/дм3, а также рассмотрение ограниченного спектра веществ, подверженных фотокаталитическому разложению.
Предложен способ получения фотокатализатора из порошка оксида цинка массового производства [3]. Способ заключается в том, что частицы ZnO, например, цинковых белил, подвергают дополнительной обработке, обеспечивающей повышение их фотокаталитической активности, отличающийся тем, что в процессе дополнительной обработки порошок диспергируют в содержащей аммиак-гидрат дистиллированной воде до растворения находящегося в порошке гидроксида цинка и образования водорастворимой комплексной соли гидроксид гексааммиакат цинка. Затем отстаивают или центрифугируют полученную суспензию для отделения частиц от жидкости, промывают полученный осадок частиц дистиллированной водой. На последнем этапе разделяют полученную суспензию отстаиванием, центрифугированием на две фракции с размером частиц 200 нм и менее, и с размером частиц более 200 нм, после чего полученные суспензии декантируют и высушивают до постоянного веса осадка, при этом частицы размером менее 200 нм используют в качестве фотокатализатора. Недостатком такого способа являются ограничения по размеру частиц (200 нм и менее), используемых в качестве фотокатализатора, а также низкая скорость фотокаталитического разложения при очистке воды от фенола в опыте с длиной волны света более 410 нм (требуется длительность процесса фотокатализа до 70 часов).
Описан способ получения фотокатализатора на основе наноструктурированного оксида цинка, допированного медью [4]. Способ включает введение смеси кислородсодержащего соединения цинка и кислородсодержащего соединения меди в этиленгликоль, вакуумную фильтрацию, промывание ацетоном, сушку и последующее прокаливание. Способ отличается тем, что смесь кристаллического оксида цинка и кристаллического карбоната меди, взятых в стехиометрическом соотношении, добавляют в этиленгликоль, содержащий концентрированную муравьиную кислоту в количестве 9-14 объемных % от общего объема этиленгликоля и предварительно нагретый до 50°С, при этом этиленгликоль берут в избытке 10-15% от стехиометрического соотношения смеси оксида цинка и карбоната меди. Недостатком такого способа является то, что получаемый в соответствии с ним материал Zn1-xCuxO, где 0,02≤х≤0,20 представляет собой преимущественно твердый раствор с морфологией частиц в виде нановолокон или наносфер. При этом несмотря на то, что зафиксирована примесь CuO, образование гетероперехода ZnO/CuO не показано. Кроме того, фотокаталитическая активность Zn0,95Cu0,05O и Zn0,975Cu0,025O является относительно низкой при использовании УФ излучения (требуется длительность процесса фотокатализа 13 часов и более).
Наиболее близким по технической сущности к предлагаемому решению является способ повышения фотокаталитической активности оксида цинка [5], который заключается в том, что с использованием растворного метода формируют гетероструктуру из металлооксидов с различной шириной запрещенной зоны ZnO/Cu2O. Недостатком такого способа является низкая эффективность фотокаталитического разложения, а также сложная многостадийная технология получения фотокатализатора.
Технический результат изобретения состоит в том, что за счет формирования фотокатализатора в виде гетероструктуры из металлооксидов с различной шириной запрещенной зоны, в которой оксид цинка получен в виде иерархической структуры, на ветвях которой расположены нанокристаллиты оксида меди (I) Cu2O и оксида меди (II) CuO, повышается фотокаталитическая активность.
Сущность предлагаемого способа заключается в том, что с использованием золь-гель технологии формируют гетероструктуру ZnO/Cu2O-CuO в рамках одностадийного синтеза, причем атомное содержание оксидов меди составляет 0,15 ат.%, температура отжига в воздушной среде 600°С, время отжига 30 мин.
В рамках заявляемого способа для приготовления пленкообразующего золя использовали следующие прекурсоры: 2-метоксиэтанол CH3OCH2CH2OH объемом 20 мл, 2-аминоэтанол H2NCH2CH2OH объемом 3,2 мл, дигидрат ацетата цинка (CH3COO)2Zn·2H2O массой 10 и дигидрат ацетата меди (CH3COO)2Cu⋅2H2O, массу которой варьировали, чтобы обеспечить атомное содержание меди 0,5 ат.% и 0,15 ат.%. Все прекурсоры производства Sigma-Aldrich (США) смешивали в круглодонной колбе и перемешивали в течение 15 мин при комнатной температуре, что обеспечивало одностадийность синтеза. Затем перемешивание проводилось в течение 60 мин с помощью магнитной мешалки при температуре 60°С. После процессов перемешивания золь созревал в течение 24 ч при комнатной температуре.
Формирование гетероструктуры ZnO/Cu2O-CuO проводили путем нанесения полученного золя на кремниевые подложки методом центрифугирования с использованием центрифуги марки 80-2 при частоте вращения 300 об/мин и длительности процесса 1 мин. На заключительном этапе осуществляли отжиг в воздушной среде при температуре 600°С в течение 30 мин.
Фотокаталитические свойства фотокатализатора на основе гетероструктуры ZnO/Cu2O-CuO, а также немодифицированного ZnO, выступающего в качестве образца сравнения, исследовали при освещении светом в ультрафиолетовом и видимом диапазоне длин волн растворов модельного красителя (бриллиантового зеленого) концентрацией 20 ppm. При этом в раствор объемом 50 мл помещали кремниевые подложки размером 1,5 см × 2,5 см, УФ-лампа Sylvania 18W BLB Т8 (диапазон излучения 315-400 нм) размещалась на 10 см выше поверхности раствора. В процессе проведения фотокаталитических тестов из растворов через равные промежутки времени забирались пробы объемом 2 мл, которые после центрифугирования и фильтрования анализировались с помощью спектрофотометра Evolution 300 Thermo Scientific на длине волны, соответствующей максимальному поглощению красителя (625 нм). После проведения измерений пробы возвращались обратно в раствор. Во все время проведения эксперимента раствор перемешивался с помощью магнитной мешалки со скоростью вращения 400 оборотов в минуту.
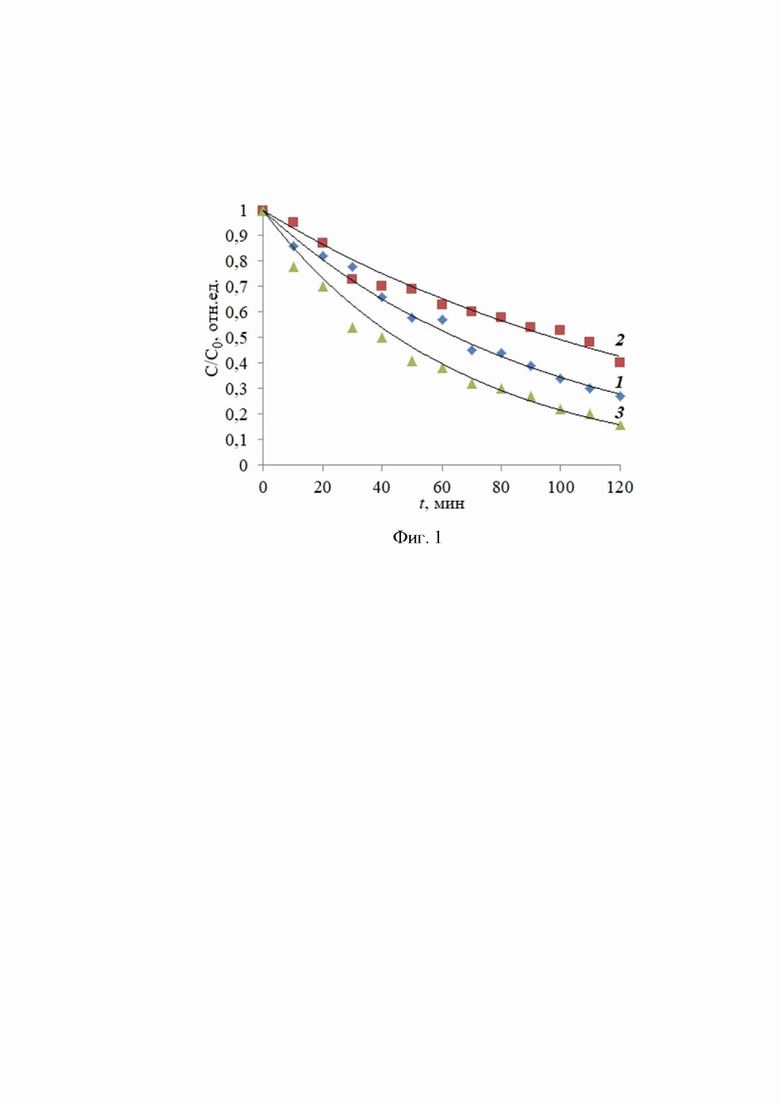
На фиг. 1 представлены кинетические кривые фотокаталитического расщепления бриллиантового зеленого на немодифицированном оксиде цинка (кривая 1) и на гетероструктуре ZnO/Cu2O-CuO с различным содержанием меди (кривая 2 - 0,05 ат.%; кривая 3 - 0,15 ат.%). Из фиг. 1 видно, что в зависимости от содержания меди скорость фотокаталитического расщепления может как увеличиваться (кривая 3) по сравнению с эталонным образцом, так и уменьшаться (кривая 2), в том числе до значений меньше, чем характерных для немодифицированного ZnO. Константа скорости фотокаталитического расщепления (k) бриллиантового зеленого для немодифицированного оксида цинка k1=0,011 мин-1, для гетероструктуры ZnO/Cu2O-CuO с содержанием меди 0,05 ат.% k2=0,007 мин-1, а при содержании меди 0,15 ат.% k3=0,015 мин-1, что указывает на повышение фотокаталитической активности.
На фиг. 2 представлены данные растровой электронной микроскопии (РЭМ) для фотокатализаторов на основе гетероструктуры ZnO/Cu2O-CuO с содержанием меди 0,15 ат.%. Из фиг. 2 видно, что для оксида цинка характерная иерархическая структура, которую образуют перекрывающиеся ветви различного размера. Фрактальная размерность такой структуры согласно методу подсчета кубов составляет 2,46, а согласно методу триангуляции 2,55, что однозначно отвечает ее иерархической пространственной организации.
На фиг. 3 представлены РЭМ-изображения нанокристаллитов Cu2O (фиг. 3а) и CuO (фиг 3б), а также картины дифракции обратноотраженных электронов в обозначенных крестом областях. Анализ РЭМ-изображений показывает в рамках заявляемого способа при атомном содержании меди 0,15 ат.%, температуре отжига в воздушной среде 600°С и времи отжига 30 мин формируется гетероструктуры из металлооксидов с различной шириной запрещенной зоны. Причем оксид цинка получен в виде иерархической структуры (фиг. 2), на ветвях которой расположены нанокристаллиты, которые согласно данным дифракции обратноотраженных электронов представляют Cu2O (фиг. 3в) и CuO (фиг. 3г).
Представленные данные по фотокаталитической активности немодифицированного оксида цинка в ультрафиолетовом диапазоне излучения свидетельствуют о наличии у него фотокаталитических свойств (константа скорости фотокаталитического расщепления бриллиантового зеленого k1=0,011 мин-1). Введение 0,05 ат.% меди в матрицу оксида цинка приводит к замедлению фотокаталитического расщепления и уменьшению константы скорости до величины k2=0,007 мин-1. Вероятно, это связано с формированием твердого раствора на основе оксида цинка, в котором атомы катионов меди выступают в роли центров рекомбинации фотогенерированных носителей заряда: электроны и дырки не достигают поверхности, а рекомбинируют в объеме. Повышение концентрации меди до 0,15 ат.% существенно меняет картину: эффективность фотокаталитического расщепления повышается, константа скорости реакции увеличивается до величины k3=0,015 мин-1. По всей видимости, это связано с образованием на поверхности ветвей из оксида цинка нанокристаллитов из оксида меди (I) Cu2O и оксида меди (II) CuO, что отвечает формированию гетероструктуры ZnO/Cu2O-CuO. Это, в свою очередь, повышает эффективность разделения фотогенерированных носителей заряда на сформированном гетеропереходе [10, 11]. Следует однако отметить, что часть меди остается в решетке ZnO, формируя твердый раствор и понижая эффективность фотокатализа. Однако эти процессы не вносят решающего вклада: интегрально наблюдается общее повышение фотокаталитической активности. Формирование нанокристаллитов меди подтверждается данными РЭМ и дифракции обратноотраженных электронов.
Заявляемый способ может найти применение в химической и биосинтетической промышленности для фотокаталитического расщепления загрязнителей водной и воздушной среды с последующим их разложением на простые и экологически безвредные химические соединения (в том числе углекислый газ и воду), а также в фармацевтической промышленности для утилизации лекарственных препаратов с истекшим сроком годности.
Источники информации
1. Li Z., Wang S., Wu J., Zhou W. Recent progress in defective TiO2 photocatalysts for energy and environmental applications // Renewable and Sustainable Energy Reviews. 2022. V. 156. P. 111980.
2. Qutub N., Singh P., Sabir S., Sagadevan S., Oh W.C. Enhanced photocatalytic degradation of Acid Blue dye using CdS/TiO2 nanocomposite // Scientific Reports. 2022. V. 12. N.1. P. 1-18.
3. Abdullah F.H., Bakar N.H.H.A., Bakar M.A. Current advancements on the fabrication, modification, and industrial application of zinc oxide as photocatalyst in the removal of organic and inorganic contaminants in aquatic systems // Journal of hazardous materials. 2022. V. 424. P. 127416.
4. Крупкин Е.И., Аверин И.А., Пронин И.А., Карманов А.А., Якушова Н.Д. Получение наноструктурированных пленок оксида цинка и исследование их фотокаталитических свойств // Нано- и микросистемная техника. 2019. Т. 21. № 1. С. 23-34.
5. Патент РФ № 2678983 Способ получения фотокатализатора на основе оксида цинка // Бюл. № 4 от 05.02.2019.
6. Патент РФ № 2627496 Способ получения фотокатализатора на основе механоактивированного порошка оксида цинка // Бюл. № 22 от 08.08.2017.
7. Патент РФ № 2733474 Способ получения фотокатализатора из порошка оксида цинка массового производства // Бюл. № 28 от 01.10.2020.
8. Патент РФ № 2771385 Способ получения фотокатализатора на основе наноструктурированного оксида цинка, допированного медью // Бюл. № 13 от 04.05.2022.
9. He Z., Xia Y., Tang B., Jiang X., Su J. Fabrication and photocatalytic property of ZnO/Cu2O core-shell nanocomposites // Materials Letters. 2016. V. 184. P. 148-151.
10. Goktas S., Goktas A. A comporative study on recent progress in efficient ZnO based nanocomposite and heterojunction photocatalysts: A review // Journal of Alloys and Compounds. 2021. V. 863. P. 158734.
11. Kumari V., Sharma S., Sharma A., Kumari K., Kumari N. Hydrotermal synthesis conditions effect on hierhal ZnO/CuO hybrid materials and their photocatalytics activity // Journal of Material Science: Materials and Electronics. 2021. V. 32. N. 7. P. 9596-9610.
| название | год | авторы | номер документа |
|---|---|---|---|
| Композитный порошковый фотокатализатор и способ его получения | 2023 |
|
RU2829486C1 |
| Способ получения фотокатализатора на основе наноструктурированного оксида цинка, допированного медью | 2021 |
|
RU2771385C1 |
| Способ получения фотокаталитически активной пленки | 2018 |
|
RU2675808C1 |
| Способ получения фотокатализатора на основе оксида цинка | 2018 |
|
RU2678983C1 |
| СПОСОБ ПОЛУЧЕНИЯ ФОТОКАТАЛИЗАТОРА ИЗ ПОРОШКА ОКСИДА ЦИНКА МАССОВОГО ПРОИЗВОДСТВА | 2019 |
|
RU2733474C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЦЕОЛИТСОДЕРЖАЩИХ КОМПОЗИТОВ НА ОСНОВЕ ОКСИДА ЦИНКА | 2020 |
|
RU2750653C1 |
| Способ получения многослойных нанокомпозитных пленок CuO/C с сенсорными свойствами в широком спектральном оптическом диапазоне | 2023 |
|
RU2810420C1 |
| КАТАЛИЗАТОР, СПОСОБ ЕГО ПРИГОТОВЛЕНИЯ И СПОСОБ ФОТОКАТАЛИТИЧЕСКОГО ПОЛУЧЕНИЯ ВОДОРОДА | 2015 |
|
RU2603190C1 |
| Способ формирования фотокаталитического покрытия на основе висмутата стронция на стеклокерамическом носителе | 2022 |
|
RU2813885C1 |
| СПОСОБ ПОЛУЧЕНИЯ ФОТОКАТАЛИЗАТОРА НА ОСНОВЕ МЕХАНОАКТИВИРОВАННОГО ПОРОШКА ОКСИДА ЦИНКА | 2016 |
|
RU2627496C1 |


Изобретение относится к области нанотехнологий, а именно, к способам получения фотокатализаторов на основе гетероструктур для разложения веществ, загрязняющих воздух и воду, и может быть использовано в химической, фармацевтической и биосинтетической промышленности. Способ заключается в том, что с использованием золь-гель технологии формируют гетероструктуру из металлооксидов в рамках одностадийного синтеза. При этом для получения оксида цинка в виде иерархической структуры, на ветвях которой расположены нанокристаллиты Cu2O и CuO, атомное содержание меди составляет 0,15 ат.%, температура отжига в воздушной среде 600°С, время отжига 30 мин. Технический результат изобретения состоит в том, что за счет формирования фотокатализатора в виде гетероструктуры ZnO/Cu2O-CuO повышается фотокаталитическая активность. 3 ил.
Способ получения фотокатализатора на основе гетероструктуры ZnO/Cu2O-CuO, заключающийся в том, что с использованием золь-гель технологии формируют гетероструктуру из металлооксидов в рамках одностадийного синтеза, отличающийся тем, что для получения оксида цинка в виде иерархической структуры, на ветвях которой расположены нанокристаллиты Cu2O и CuO, атомное содержание меди составляет 0,15 ат.%, температура отжига в воздушной среде 600°С, время отжига 30 мин.
| Способ получения фотокатализатора на основе оксида цинка | 2018 |
|
RU2678983C1 |
| Гырдасова О.И | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Гырдасова, Л.А | |||
| Пасечник, В.Н | |||
| Красильников, В.Т | |||
| Суриков, М.В | |||
| Кузнецов // Физико-химические аспекты изучения кластеров, наноструктур и наноматериалов, 2020, Вып | |||
| Способ гальванического снятия позолоты с серебряных изделий без заметного изменения их формы | 1923 |
|
SU12A1 |
| Телеграфный коммутатор | 1921 |
|
SU792A1 |
| CN 106732617 B, | |||
Авторы
Даты
2023-04-11—Публикация
2022-09-16—Подача