Изобретение относится к области получения фотокаталитически активных полупроводниковых плёнок.
Известен способ получения слоёв фотопреобразователя для солнечных батарей из оксида меди, состоящий в периодическом обмакивании стеклянной подложки в ацетонитрильный раствор иодида одновалентной меди с последующим окислением полученной плёнки на подложке до оксида двухвалентной меди в щелочном водном растворе (Zuo Ch., Ding L., “Solution-processed Cu2O and CuO as hole transport material for efficient perovskite solar cells”, SMALL, 2015, v.11, 41, p. 5528-5532).
Недостатком известного способа является многостадийность, использование токсичного ацетонитрила.
Известен способ нанесения слоя фотоактивного оксида меди на поверхность стекла из суспензии наночастиц оксида меди(II) в растворе хлороформа и метанола (2:1)(Yee-Fun Lim, Joshua J. Choi, Tobias Hanrath “Facile synthesis of colloidal CuO nanocrytals for light-harvesting application”, Journal of Nanomaterials, 2012, v.2012, article ID 393160).
Недостатками известного способа также являются многостадийность, длительность и использование токсичных реагентов.
Известен способ осаждение частиц фотоактивного оксида меди на поверхность гранулированных подложек из упорядоченного мезопористого углерода. Способ включает приготовление отдельно суспензии углерода в абсолютном спирте (А) и приготовление раствора нитрата меди в фурфуриловом спирте (Б), смешение растворов А и Б, многократную фильтрацию, а затем карбонизацию полученного углеродного композита при 5500С на воздухе до конечного продукта с содержанием оксида меди 0,8 – 15 масс. %(A. Tuerdi, Abdukader A.P. Chen ”Systhesisof composite photocatalyst based on the ordered mesoporous carbon-CuO nanocomplex”, Materials Letters, 2017, v.209. pp. 235-239).
Недостатками известного способа являются его многостадийность и длительность процесса (весь цикл приготовления занимает 13-14 часов), необходимость применения токсичных органических реактивов, дополнительная высокотемпературная обработка материала.
Известен способ получения слоев фотокатализатора оксида меди на стеклянную подложку, состоящий в нанесении подслоя из наночастиц оксида меди толщиной 100 нм путём обмакивания субстрата раствор ацетата меди(II) в смеси 2-метоксиэтанола и моноэтаноламина. После двухчасовой сушки поверхности и часовой термообработки при 350 0С полученного материала, его помещают в водный раствор нитрата меди(II) в гексамине и наращивают слой активного материала при температуре 900С в течение 4 часов. В зависимости от концентрации меди в растворе, частицы возникающего Cu(OH)2, превращаются в оксид CuO и осаждаются на поверхность субстрата в виде слоя с различной морфологией (нанолисты, нанолистья). Для синтеза слоёв фотокативного оксида меди, согласно описанию прототипа, характерно нескольких стадий синтеза, использование твердофазного материала-предшественника Cu(OH)2 (прекурсора), который и превращают в активный оксид CuO (A. Kushwahaa, R.S. Moakhara, G. K. L. Goha, G.K. Dalapatia “Morphologically tailored CuO photocathode using aqueous solution technique for enhanced visible light driven water splitting”, Jonal of photochemistry and photobiology A: Chemistry, 2017, v. 337, pp. 54-61).
Недостатками известного способа также являются многостадийность и длительность процесса, необходимость применения токсичных органических реагентов.
Известен способ получения композиционного фотокаталитического материала на основе оксида меди. Способ включает следующие стадии: замачивание медной сетки в соляной кислоте; затем, помещение медной сетки в этанол для очистки; помещение очищенной медной сетки в печь сопротивления и обжиг с последующим нанесением на гибкую подложку (Патент CN 107497430; МПК B01J 23/72, B01J 23/72, B01J 37/08, C02F 1/30, C02F 101/38; 2017г.).
Недостатком известного способа является ограниченная область использования фотокаталитического материала за счет получения его в сетчатой форме.
Наиболее близким по технической сущности к предлагаемому способу является способ получения фотокаталитического материала, содержащего фотокаталитический слой, состоящий из фотокаталитических частиц на основе диоксида титана, оксида или гидроксида меди, неорганических частиц, не обладающих фотокаталитической активностью, и связки и нанесенный на неорганическую подложку, например, из стекла. Способ заключается в получении смеси исходный компонентов, тщательном ее перемешивании с использованием растворителя в шаровой мельнице до крупности частиц не более 0,5 мм и нанесении на подложку, например, путем напыления или окунания с последующей сушкой при температуре 150-200оС на воздухе. В качестве исходного соединения меди могут быть использованы, например, хлорид меди, ацетат меди, нитрат меди, сульфат меди (Заявка WO2018110173; МПК B01J 23/72, B01J 35/02, B32B 9/00, C09D 1/00, C09D 201/00, C09D 5/16; 2018 г.)(прототип).
Однако входящий в состав фотокаталитического покрытия, полученного известным способом, оксид или гидроксид меди не проявляет фотокаталитической активности, проявляя только бактерицидные свойства. Кроме того, в способе используются токсичные органические соединения в качестве прекурсоров при приготовлении связки и растворителя.
Таким образом, перед авторами стояла задача разработать простой одностадийный способ получения фотокаталитически активной пленки, обеспечивающий высокую фотокаталитическую способность.
Поставленная задача решена в способе получения фотокаталитически активной пленки, включающем осаждение ионов Cu+2 в виде оксида меди или гидроксида меди из раствора неорганической соли меди на подложку, в котором осаждение ведут из раствора аммиаката хлорида меди (II) с концентрацией 0,3 – 3,0 моль/л при температуре 45-75оС при концентрации свободного аммиака 4,0 – 11,2 моль/л.
При этом в качестве неорганической подожки используют силикагель, стекло, никелевую фольгу.
В настоящее время из патентной и научно-технической литературы не известен способ получения фотокаталитически активной пленки путем осаждения из раствора аммиаката хлорида меди (II) с концентрацией 0,3 – 3,0 моль/л при температуре 45-75оС при концентрации свободного аммиака 4,0 – 11,2 моль/л.
Авторами предлагается способ получения фотокаталитически активной пленки путем формирования слоя катализатора на основе оксида меди или гидроксида меди на подложке в результате термического разложения аммиачного комплекса в щелочной среде. Целью исследования авторов являлось создание одностадийного гидрохимического способа получения слоя CuO или Cu(OH)2 на подложке из стекла или металла в результате термического разложения аммиачных комплексов Cu(II) в щелочной среде. С этой целью авторами было установлено влияние температуры, состава раствора, природы положки (диэлектрик, металл) на состав получаемого слоя CuO, исключающее появление в нём Cu2O. Авторами также получены сведения о фотокаталитической активности получаемых слоёв CuO в сравнении с порошками - аналогами, теоретически и экспериментально показана причина повышенной эффективности фотокатализаторов в виде слоёв на носителе, связанная с поглощением фотонного излучения объёмом фотокатализатора. Оценку условий формирования CuO в объёме раствора электролита при термогидролизе аммиачных комплексов меди авторы провели путём термодинамического исследования температурной эволюции полей преобладания фаз CuO/Cu(OH)2 в координатах “pH – Eh – концентрация Cu(II)”, где Eh – относительный редокс-потенциал системы, В. Используя программу HSC Chemistry v.8. авторы получили сведения о влияние состава раствора на следующие гетерогенные равновесия, приводящие к синтезу фотокатализатора CuO в закрытой системе (1 – 3),
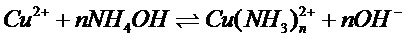
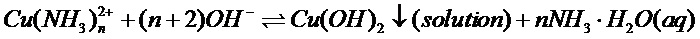
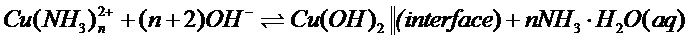
Реакция (1) описывает образование аммиачных комплексов Cu(II) в растворе, реакции (2,3) характеризуют образование фазы оксида/гидроксида меди(II) в объёме раствора (2) и на поверхности раздела фаз раствор - твёрдое, “||(interface)” . С учётом эволюции 29 химических форм частиц меди включая фазы Cu, CuO, Cu2O, Cu(OH)2, аква-ионы Cu(I,II), их гидроксо-, аммиачные моно- и димерные комплексы установлено, что основой термогидролиза является термическая нестабильность тетра-аммиачного комплекса меди(II) в диапазоне 25 - 95 0C. Верхняя граница устойчивости комплекса Cu(NH3)4+2(aq) относительно фаз Cu(OH)2/CuO при 25 0C соответствует pH 11.2-11.5, а с ростом температуры она сдвигается в область меньших рН. Повышение температуры ведёт к медленному выделению фазы Cu(OH)2/CuO в объёме раствора и на поверхностях раздела фаз «раствор-стенка стеклянного реактора», При этом авторами выявлены оптимальные условия проведения процесса. Необходимо отметить, что величина удельной фотокаталитической активности определяет скорость фотоокисления (k) в расчете на единицу массы катализатора (k имеет размерность 1\с, г). Поскольку фотоактивный материал, в частности на основе CuO или Cu(OH)2 реагирует с электромагнитным излучением, которое проникает на глубину, зависящую от массы катализатора, с увеличением массы увеличивается и доля катализатора, не участвующая во взаимодействии с излучением из-за его полного поглощения. Поэтому величина k зависит от массы слоя фотокатализатора на поверхности подложки. В предлагаемом способе используют в качестве фотоактивного материала в виде пленки оксида меди или гидроксида меди на подложке из диэлектрика ( стекло, силикагель) или металла(никелевая фольга) в количестве, обеспечивающем наибольшую величину удельной скорости фотоокисления k на единицу массы фотоактивного материала. На фиг. 1 приведена зависимость относительной скорости фотоокисления субстрата – пары “гидрохинон-бензохинон” с концентрацией 0,4 ммоль/л от массовой толщины слоя фотокатализатора – оксида меди (II) на стеклянной подложке – стенке стеклянного катализатора. Из приведенных данных следует, что при содержании фотокатализатора более 100 мкг на 1 см2 поверхности подложки эффективность катализатора уменьшается. Таким образом, авторами были определены условия проведения процесса, обеспечивающие содержание фотокатализатора на поверхности подложки не более 100 мкг/см2. Такими условиями являются использование раствора аммиаката хлорида меди (II) с концентрацией 0,3 – 3,0 моль/л при концентрации свободного аммиака 4,0 – 11,2 моль/л. При увеличении концентрации аммиаката хлорида меди (II) более 3,0 моль/л с увеличением концентрации свободного аммиака более 11,2 моль/л наблюдается снижение до нуля выхода оксида или гидроксида меди в плёнку. Нижний предел концентрации аммиаката хлорида меди (II) 0,3 моль/л и нижний предел концентрации свободного аммиака 4,0 моль/л определены из условий целесообразности, поскольку при дальнейшем снижении концентрации также снижается эффективность фотокатализа за счет недостаточного содержания фотокатализатора.
На фиг. 2 приведены сравнительные данные по фотокаталитической активности при окислении субстрата, используемых в виде пленки на подложки из стекла или никелевой фольги (позиции а, б, в, г) или в виде порошка (позиции д, е, ж). Субстрат – пара “гидрохинон - бензохинон” с концетрацией 0,4 ммоль/л в воде; источник света – УФ-лампа с длиной волны 253 нм; средний размер частиц порошков материалов – CuO (27,0 мкм), TiO2 (1,4 мкм), SiO2 (28 мкм). Из приведенных данных следует, что наибольшей каталитической активностью обладает пленка на основе CuO на подложке из стекла.
Предлагаемый способ может быть осуществлен следующим образом. Берут раствор аммиаката хлорида меди (II) с концентрацией 0,3 – 3,0 моль/л при концентрации свободного аммиака 4,0 – 11,2 моль/л, нагревают раствор до температуры 45-75оС и осуществляют осаждение в течение 20-120 минут на подложку из неорганического материала (стекло, силикагель, никелевая фольга). Полученную фотоактивную пленку подвергают КР-спектроскопии, рентгенофазовому анализу, масс-спектрометрическому анализу.
Предлагаемый способ иллюстрируется следующими примерами.
Пример 1. В стакан из термостойкого стекла ёмкостью 50 мл заливают 25 мл 0.3 моль/л раствора аммиаката меди(II) c концентрацией свободного аммиака 4.0 моль/л. Стакан нагревают в термостате до температуры 75 0С в течение 30 минут. После этого на внутренней поверхности стенки стакана возникает равномерный слой черного цвета. Состав слоя на поверхности стекла по данным КР-спектроскопии отвечает фазе CuO ( колебательные моды при 282 cm-1 относится к Ag колебаниям, а моды при 332 cm-1 и 616 cm-1 относят к моде Bg CuO. Данные рентгенофазового анализа (РФА) указывают на фазу CuO: пространственная группа C12/c1, параметры решётки (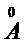
Пример 2. В стакан из термостойкого стекла ёмкостью 50 мл заливают 25 мл 0.3 моль/л, раствора аммиаката меди(II) c концентрацией свободного аммиака 4.0 моль/л. Стакан нагревают в термостате до температуры 75 0С в течение 20 минут. После этого на внутренней поверхности стенки стакана возникает равномерный слой черного цвета. Состав слоя на поверхности стекла по данным КР-спектроскопии отвечает фазе CuO. Массовое содержание CuO в расчёте на единицу поверхности стекла, по данными измерения методом масс-спектрометрии с индуктивно связанной плазмой, составляет 50.1 мкг Cu /см2.
Пример 3. В стакан из термостойкого стекла ёмкостью 50 мл заливают 25 мл 3,0 моль/л, раствора аммиаката меди(II) c концентрацией свободного аммиака 11,2 моль/л. Стакан нагревают в термостате до температуры 45 0С в течение 120 минут. В термостат помещают 1.0 г порошка измельчённого силикагеля фракции 0.3-0.5 мм. После указанного времени поверхность частиц силикагеля приобретает голубую окраску. Состав слоя на поверхности частиц силикагеля по данным рентгенофазового анализа отвечает фазе Cu(OН)2, пространственная группа Cmc21, параметры решётки (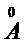
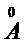
Пример 4. В стакан из термостойкого стекла ёмкостью 50 мл заливают 25 мл 0.3 моль/л, раствора аммиаката меди(II) c концентрацией свободного аммиака 4.0 моль/л. Стакан нагревают в термостате до температуры 45оС в течение 120 минут. В термостат помещают пластинку размером 1.5х1.5х0.05 см из никелевой фольги, предварительно обезжиренную. После указанного времени поверхность пластинки приобретает черную окраску за счёт формирования на её поверхности слоя оксида меди. По данным КР-спектроскопии образца в нем обнаруживается фаза CuO согласно с колебательными модами при 282 cm-1 ( Ag колебания), 332 cm-1 и 616 cm-1 (мода Bg ) CuO. Массовое содержание CuO в расчёте на единицу поверхности стекла, по данными измерения методом масс-спектрометрии с индуктивно связанной плазмой, составляет 50.1 мкг Cu /см2.
Таким образом, авторами предлагается способ получения фотокаталитической активной пленки в одну стадию как на плоских образцах стекла, металлической фольги, так и на порошкообразных материалах, например, на порошке силикагеля.
| название | год | авторы | номер документа |
|---|---|---|---|
| ЗОЛЬ ФОТОКАТАЛИТИЧЕСКИ АКТИВНОГО ОКСИДА ТИТАНА, КОМПОЗИЦИЯ ПОКРЫТИЯ И ДЕТАЛЬ С ЕГО ИСПОЛЬЗОВАНИЕМ | 2007 |
|
RU2404852C1 |
| КАТАЛИЗАТОР, СПОСОБ ЕГО ПРИГОТОВЛЕНИЯ И СПОСОБ ФОТОКАТАЛИТИЧЕСКОГО ПОЛУЧЕНИЯ ВОДОРОДА | 2015 |
|
RU2603190C1 |
| СПОСОБ ПОЛУЧЕНИЯ ФОТОКАТАЛИЗАТОРА НА ОСНОВЕ ГЕТЕРОСТРУКТУРЫ ZnO/CuO-CuO С ПОВЫШЕННОЙ ФОТОКАТАЛИТИЧЕСКОЙ АКТИВНОСТЬЮ | 2022 |
|
RU2794093C1 |
| СПОСОБ ПОЛУЧЕНИЯ ТИТАНАТНОГО ФОТОКАТАЛИЗАТОРА, АКТИВНОГО В ВИДИМОЙ ОБЛАСТИ СПЕКТРА | 2011 |
|
RU2466791C1 |
| ФОТОКАТАЛИТИЧЕСКОЕ ПОКРЫТИЕ | 2015 |
|
RU2581359C1 |
| Способ получения фотоактивного композита с бактерицидными свойствами | 2018 |
|
RU2683321C1 |
| СПОСОБ ПОЛУЧЕНИЯ ТЕРМОСТАБИЛЬНОГО ФОТОКАТАЛИЗАТОРА НА ОСНОВЕ ДИОКСИДА ТИТАНА | 2014 |
|
RU2563239C1 |
| Способ получения смешанного фотокатализатора на основе оксида титана | 2021 |
|
RU2760442C1 |
| Способ получения антибактериального покрытия Cu-Ti-O экстракционно-пиролитическим методом | 2022 |
|
RU2801505C1 |
| Способ получения фотокатализатора на основе наноструктурированного оксида цинка, допированного медью | 2021 |
|
RU2771385C1 |

Изобретение относится к области получения фотокаталитически активных полупроводниковых пленок. Предложен способ получения фотокаталитически активной пленки, включающий осаждение ионов Cu+2 в виде оксида меди или гидроксида меди из раствора неорганической соли меди на подложку. Осаждение ведут из раствора аммиаката хлорида меди(II) с концентрацией 0,3-3,0 моль/л при температуре 45-75°С при концентрации свободного аммиака 4,0-11,2 моль/л. При этом в качестве подложки используют силикагель, стекло, никелевую фольгу. Способ позволяет получать фотокаталитически активную пленку в одну стадию как на плоских образцах стекла, металлической фольги, так и на порошкообразных материалах, например на порошке силикагеля. 3 ил., 4 пр.
1. Способ получения фотокаталитически активной пленки, включающий осаждение ионов Cu+2 в виде оксида меди или гидроксида меди из раствора неорганической соли меди на подложку, отличающийся тем, что осаждение ведут из раствора аммиаката хлорида меди(II) с концентрацией 0,3-3,0 моль/л при температуре 45-75°С при концентрации свободного аммиака 4,0-11,2 моль/л.
2. Способ по п.1, отличающийся тем, что в качестве подложки используют силикагель, стекло, никелевую фольгу.
| Способ получения цианистых соединений | 1924 |
|
SU2018A1 |
| ФОТОКАТАЛИЗАТОР НА ОСНОВЕ ОКСИДА ТИТАНА И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2012 |
|
RU2508938C1 |
| Способ нанесения медного покрытия на поверхность стекла | 1979 |
|
SU1036697A1 |
| CN 102580742 A, 18.07.2012 | |||
| US 20130281283 A1, 24.10.2013. | |||
Авторы
Даты
2018-12-25—Публикация
2018-10-29—Подача