Изобретение относится к области нанотехнологий, а именно к способам получения фотокатализаторов для разложения веществ, загрязняющих воздух и воду, и может быть использовано в химической, фармацевтической и биосинтетической промышленности.
В настоящее время наиболее часто в качестве фотокатализаторов предлагают использовать чистый и/или модифицированный диоксид титана (TiO2), который относительно дешев и практически нетоксичен. С его помощью можно окислить до углекислого газа и воды практически любые органические соединения, т.к. окислительный потенциал дырки на поверхности TiO2 составляет около 3 эВ.
Известен способ получения фотокатализатора на основе диоксида титана [1], заключающийся в приготовлении водного раствора сульфата титанила с концентрацией 0,1-1,0 моль/л, добавлении в раствор кислоты до получения концентрации 0,15-1 моль/л с последующим гидролизом полученного раствора в гидротермальных условиях при температуре в диапазоне 100-250°С в течение 0,5-24 часа и последующем высушиванием полученной суспензии пористого диоксида титана. Недостатком такого способа является относительно большая длительность процесса синтеза TiO2 в форме мезопористых частиц с высокой удельной поверхностью (малым размером частиц), а также низкая скорость фотокаталитического окисления.
Описан фотокатализатор на основе наноразмерной η-модификации диоксида титана [2], отличающийся тем, что в качестве диоксида титана применяют наноразмерную метастабильную η-модификацию диоксида титана с площадью удельной поверхности 4,5-16 м2/г. Данный способ позволяет повысить фотокаталитическую активность TiO2, однако его недостатком является малые величины константы скорости реакции разложения, а как следствие этого - низкая скорость фотокаталитического окисления.
Известен способ приготовления фотокатализатора на основе η-модификации диоксида титана, допированного ванадием, активного в видимой области спектра [3]. Он заключается в том, что допирование диоксида титана проводят путем введения водных растворов нитратов ванадила (VO(NO3)2) в реакционную смесь в ходе синтеза диоксида титана из сольватированного сульфата титанила после формирования полупродукта гидролиза сульфата титанила - устойчивого гидрозоля диоксида титана. Полученная таким способом η-модификация диоксида титана имеет повышенную чувствительность к видимому свету при одновременном повышении фотокаталитической активности, однако скорость фотокаталитического окисления, в том числе модельного красителя метилового оранжевого, составляет достаточно низкую величину.
Также известен способ получения термостабильного фотокатализатора на основе диоксида титана [4], включающий осаждение гидроксида титана из водного раствора его неорганической соли, отделение, отмывку, растворение в перекиси водорода, установление требуемого рН раствора, осаждение гидратированного диоксида титана из раствора пероксокомплекса, отмывку, сушку, термическую обработку. При этом гидратированный диоксид титана осаждают из водного раствора пероксокомплекса титана этиловым спиртом или ацетоном. Недостатком такого способа является относительно большая длительность процесса синтеза TiO2 (свыше 24 ч), а также относительно низкая скорость фотокаталитического окисления.
Описан способ приготовления титаноксидного фотокатализатора, активного в видимой области спектра [5], который включает сенсабилизацию диоксида титана введением активизирующей добавки (органические красители и окрашенные координационные соединения). Добавку вводят в реакционную смесь в ходе синтеза диоксида титана гидролизом сольватированного сульфата титанила на стадии коагуляции одновременно с коагулянтом. Такой способ повышает энергоэффективность технологии получения фотокатализатора, однако его недостатком является низкая скорость фотокаталитического окисления некоторых видов органических загрязнителей.
Несмотря на большое количество предложений по использованию в качестве фотокатализатора диоксида титана имеются работы, посвященные использованию других широкозонных полупроводниковых металлоксидов и их композиций. Так известен способ получения фотокатализатора SnO [6], который включает в себя приготовление раствора хлорида олова(II) с последующим его гидролизом в присутствии концентрированного аммиака, помещение его в микроволновую печь (2450 МГц) с мощностью излучения 539 Вт в течение 5-15 минут, центрифугирование полученного оксида олова(II) и сушку при температуре 90°С. Гидролиз проводится в щелочной среде, способствующей формированию аммиачного коллоидного раствора гидроксоформы олова(II) с последующей термической деструкцией под микроволновым воздействием в отсутствие гидротермальной обработки. Используется следующее соотношение компонентов в процессе получения коллоидного раствора, мас. %: металлическое олово - от 1,5 до 1,8; 36%-ный раствор соляной кислоты - от 48,2 до 57,8; 25%-ный раствор аммиака - остальное. Недостатком такого способа является узкий спектр веществ, подверженных фотокаталитическому разложению (азотсодержащие органические загрязнители), а также низкая скорость фотокаталитического окисления.
Описан композитный фотокатализатор для очистки воды и воздуха [7], который состоит из адсорбента, диоксида кремния и фотокатализатора, при этом каждая гранула представляет собой трехслойную частицу, состоящую из внутреннего слоя - частицы активированного угля или оксида алюминия, или цеолита, промежуточного слоя - диоксида кремния и наружного слоя - диоксида титана анатазной модификации. В качестве наружного слоя композитный фотокатализатор содержит диоксид титана с добавками благородных металлов, таких как серебро, золото, платина или палладий, или их смеси в количестве не более 5% от массы диоксида титана. Недостатком такого фотокатализатора является существенная сложность технологии его получения, а также низкая скорость фотокаталитического окисления.
Из литературных данных известна высокая эффективность использования оксида цинка (ZnO) в качестве фотокатализатора для разложения активных красителей, фенола, хлорфенола и других загрязняющих веществ [8, 9]. Также большое количество работ посвящено исследованию влияния различных способов модификации (легирование полупроводниками, металлами и неметаллами) на каталитические свойства материалов на основе ZnO [10, 11].
Наиболее близким по технической сущности к предлагаемому решению является способ увеличения фотокаталитической активности порошков оксида цинка [12], который заключается в том, что порошки оксида цинка подвергают интенсивной механической обработке в планетарной шаровой мельнице в воздушной среде. Недостатком такого способа является низкая скорость фотокаталитического окисления получаемых фотокатализаторов.
Технический результат изобретения состоит в том, что за счет механоактивации порошков оксида цинка увеличивается их фотокаталитическая активность.
Сущность предлагаемого способа заключается в том, что порошки оксида цинка подвергают интенсивной механической обработке в воздушной среде при заданных технологических параметрах (скорости и времени измельчения, соотношения массы шаров и порошка).
В рамках заявляемого способа коммерческие порошки ZnO (>99.0%, Acros Organics, США) были подвергнуты интенсивной механической обработке в планетарной шаровой мельнице Planetary Micro Mill PULVERISETTE 7 premium line в воздушной атмосфере. В процессе измельчения использовались следующие параметры:
- шары из нержавеющей стали диаметром 5 мм;
- скорость измельчения в размольных барабанах - 250 оборотов в минуту;
- соотношение массы порошка и шаров - 10:1;
- время измельчения - 1, 3, 5 и 7 минут.
Фотокаталитические свойства коммерческих и механоактивированных порошков ZnO были исследованы при освещении светом в ультрафиолетовом и видимом диапазоне длин волн растворов модельного красителя (бриллиантового зеленого) концентрацией 20 ppm. При этом загрузка катализатора составляла 0.5 г/дм3, объем раствора - 250 мл. УФ-лампа Sylvania 18W BLB Т8 (диапазон излучения 315-400 нм) размещалась на 10 см выше поверхности раствора. После приготовления растворов в них добавлялись исследуемые порошки ZnO с дальнейшим перемешиванием в течение 30 минут в темноте до образования однородной суспензии. В процессе проведения фотокаталитических тестов из растворов через равные промежутки времени забирались пробы объемом 2 мл, которые после центрифугирования и фильтрования анализировались с помощью спектрофотометра Evolution 300 Thermo Scientific на длине волны, соответствующей максимальному поглощению красителя (625 нм). После проведения измерений пробы возвращались обратно в раствор. Во все время проведения эксперимента раствор перемешивался с помощью магнитной мешалки со скоростью вращения 400 оборотов в минуту.
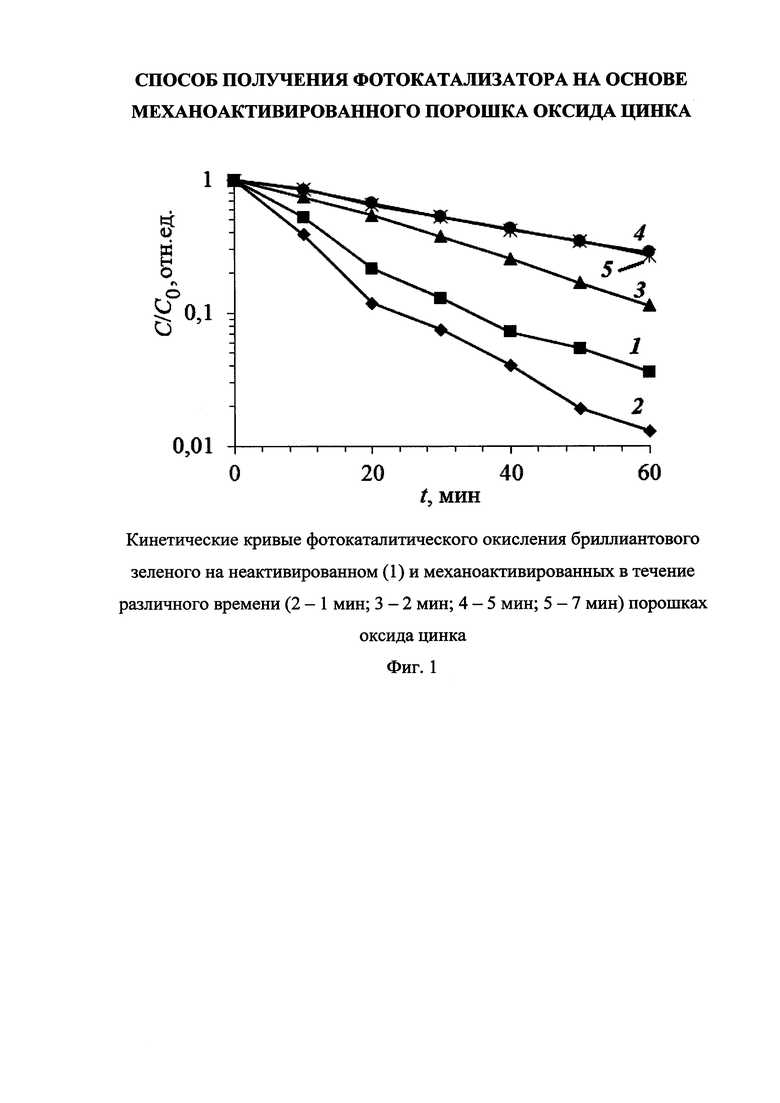
На фиг. 1 представлены кинетические кривые фотокаталитического окисления бриллиантового зеленого на неактивированном (кривая 1) и механоактивированных в течение различного времени порошках оксида цинка (кривая 2-1 мин; кривая 3-3 мин; кривая 4-5 мин; кривая 5-7 мин.). Из фиг. 1 видно, что при механоактивации порошков оксида цинка скорость фотокаталитического окисления сначала повышается (кривая 2), а затем уменьшается (кривая 3-5), в том числе до значений меньше чем характерных для неактивированного порошка, после чего наступает «насыщение» (кривые 4 и 5).
На фиг. 2 представлены данные растровой электронной микроскопии для порошков: неактивированного (фиг. 2, а) и активированного в течение 7 минут (фиг. 2, б) оксида цинка. Результатом обработки коммерческих порошков оксида цинка в планетарной мельнице является уменьшение среднего размера зерен и, как следствие, увеличение площади контакта порошков с молекулами красителя, что должно приводить к увеличению фотокаталитической активности материала. Тем не менее, это не всегда так, поскольку при интенсивной механообработке увеличивается концентрация собственных точечных дефектов, выступающих в качестве центров рекомбинации. В ZnO существует большое количество типов точечных дефектов, таких как вакансии в подрешетке кислорода, вакансии в подрешетке цинка, междоузельный кислород и цинк, антиструктурные замещения. Общепринятым является тот факт, что основной тип собственных точечных электрически активных дефектов в ZnO при низких парциальных давлениях кислорода - это двукратно ионизированные вакансии в подрешетке кислорода, благодаря которым материал обязан существенной электропроводностью при низких температурах.
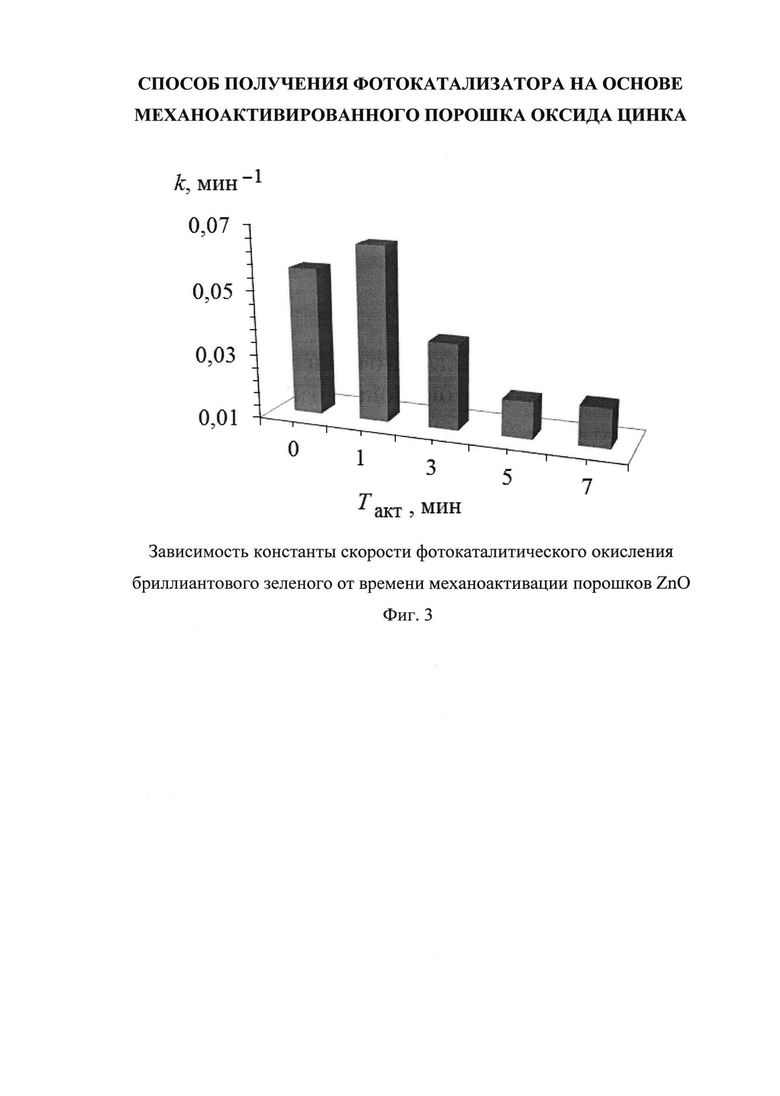
На фиг. 3 представлена зависимость константы скорости фотокаталитического окисления (k) бриллиантового зеленого от времени механоактивации порошков ZnO. Из фиг. 3 видно, что константа скорости при механоактивации образца в течение 1 минуты возрастает, что может быть связано с увеличением удельной площади поверхности образца и довольно малой концентрацией дефектов. Однако при дальнейшем увеличении времени механоактивации константа скорости уменьшается, что связано с подавлением фотокаталитической активности из-за рекомбинации носителей заряда на образовавшихся дефектах. В этом случае дальнейшее увеличение площади поверхности нивелируется возникающими рекомбинационными процессами.
Заявляемый способ может найти применение в химической и биосинтетической промышленности для фотокаталитического окисления загрязнителей водной и воздушной среды с последующим их разложением на простые и экологически безвредные химические соединения (в том числе углекислый газ и воду), а также в фармацевтической промышленности для утилизации лекарственных препаратов с истекшим сроком годности.
Источники информации
1. Патент РФ №2408427, МПК B01J 37/08, C01G 23/053, B01D 53/86, B01J 21/06, C02F 1/30, В82В 3/00 Способ получения фотокатализатора на основе диоксида титана / Зверева И.А., Чурагулов Б.Р., Иванов В.К., Баранчиков А.Е., Шапорев А.С., Миссюль А.Б. // Бюл. №1 от 10.01.2011 г.
2. Патент РФ №2469788, МПК B01J 21/06, В82В 1/00, B01J 20/00, C01G 23/00, C02F 1/32 Фотокатализатор на основе наноразмерной η-модификации диоксида титана / Савинкина Е.В., Оболенская Л.Н., Кузьмичева Г.М., Дорохов А.В. // Бюл. №35 от 20.12.2012.
3. Патент РФ №2540336, МПК B01J 37/34, B01J 37/08, B01J 21/06, B01J 37/00 Способ приготовления фотокатализатора на основе η-модификации диоксида титана, допированного ванадием, активного в видимой области спектра / Кузмичева Г.М., Гайнанова А.А., Кабачков Е.Н., Садовская Н.В., Дорохов А.В. // Бюл. №4 от 10.02.2015.
4. Патент РФ №2563239, МПК B01J 37/03, B01J 37/06, B01J 37/08, В0 1J 21/06 Способ получения термостабильного фотокатализатора на основе диоксида титана / Кривцов И.В., Авдин В.В., Илькаева М.В. // Бюл. №26 от 20.09.2015.
5. Патент РФ №2520100, МПК C01G 23/053, B01J 21/06 Способ приготовления титаноксидного фотокатализатора, активного в видимой области спектра // Савинкина Е.В., Оболенская Л.Н., Кузьмичева Г.М. // Бюл. №17 от 20.06.2014.
6. Патент РФ №2538203, МПК B01J 37/34, B01J 23/14, C02F 1/30 Способ получения фотокатализатора SnO / Пичугина А.А., Козик В.В., Кузнецова С.А. // Бюл. №1 от 10.01.2015.
7. Патент РФ №2478413, МПК B01D 21/06, B01J 21/08, B01J 21/18, B01J 23/38, B01D 53/86, C02F 1/30 Композитный фотокатализатор для очистки воды и воздуха / Козлов Д.В., Селищев Д.С., Колинько П.А., Козлова Е.А. // Бюл. №10 от 10.04.2013.
8. Behnajady М., Modishahla N, Hamzavi R. // Journal of Hazardous Materials. 2006. V. 133. PP. 226-232.
9. Lathasree S., Rao A.N., Siva-Sankar В., Sadasivam В., Rengaraj K. // J. Mol. Catal. A: Chem. 2004. V. 223. PP. 101-105.
10. Пронин И.А., Донкова Б.В., Димитров Д.Ц., Аверин И.А., Пенчева Ж.А., Мошников В.А. // Физика и техника полупроводников. 2014. Т. 48. №7. С. 868-874.
11. Ullah R., Dutta J. Photocatalytic degradation of organic dyes with manganese-doped ZnO nanoparticles // Journal of Hazardous Materials. 2008. V. 156. PP. 194-200.
12.  V.,
V.,  A., Wilkening M., Becker K.D., Heitjans P. Mechanochemical reactions and syntheses of oxides // Chem. Soc. Rev. 2013. V. 42. PP. 7507-7520.
A., Wilkening M., Becker K.D., Heitjans P. Mechanochemical reactions and syntheses of oxides // Chem. Soc. Rev. 2013. V. 42. PP. 7507-7520.
| название | год | авторы | номер документа |
|---|---|---|---|
| Композитный порошковый фотокатализатор и способ его получения | 2023 |
|
RU2829486C1 |
| СПОСОБ ПОЛУЧЕНИЯ ФОТОКАТАЛИЗАТОРА НА ОСНОВЕ ГЕТЕРОСТРУКТУРЫ ZnO/CuO-CuO С ПОВЫШЕННОЙ ФОТОКАТАЛИТИЧЕСКОЙ АКТИВНОСТЬЮ | 2022 |
|
RU2794093C1 |
| СПОСОБ ПОЛУЧЕНИЯ ФОТОКАТАЛИЗАТОРА ИЗ ПОРОШКА ОКСИДА ЦИНКА МАССОВОГО ПРОИЗВОДСТВА | 2019 |
|
RU2733474C1 |
| Способ приготовления металл-нанесенного катализатора для процесса фотокаталитического окисления монооксида углерода | 2016 |
|
RU2637120C1 |
| ФОТОКАТАЛИТИЧЕСКИЙ СОРБИРУЮЩИЙ ТКАНЕВЫЙ МАТЕРИАЛ | 2014 |
|
RU2562485C1 |
| СПОСОБ ПОЛУЧЕНИЯ ФОТОКАТАЛИЗАТОРА SnO | 2013 |
|
RU2538203C1 |
| СПОСОБ ПОЛУЧЕНИЯ ТИТАНАТНОГО ФОТОКАТАЛИЗАТОРА, АКТИВНОГО В ВИДИМОЙ ОБЛАСТИ СПЕКТРА | 2011 |
|
RU2466791C1 |
| СПОСОБ ПОЛУЧЕНИЯ КРИСТАЛЛИЧЕСКОГО ДИОКСИДА ТИТАНА В СТРУКТУРНОЙ МОДИФИКАЦИИ АНАТАЗ | 2014 |
|
RU2575026C1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ ТИТАНОКСИДНОГО ФОТОКАТАЛИЗАТОРА, АКТИВНОГО В ВИДИМОЙ ОБЛАСТИ СПЕКТРА | 2012 |
|
RU2520100C1 |
| СПОСОБ ПОЛУЧЕНИЯ ВОЛОКНИСТОГО ФИЛЬТРУЮЩЕ-СОРБИРУЮЩЕГО МАТЕРИАЛА С ПОКРЫТИЕМ ИЗ НАНОРАЗМЕРНОГО ДИОКСИДА ТИТАНА И ВОЛОКНИСТО ФИЛЬТРУЮЩЕ-СОРБИРУЮЩИЙ МАТЕРИАЛ | 2023 |
|
RU2824859C1 |

Изобретение относится к области нанотехнологий, а именно к способам получения фотокатализаторов для разложения веществ, загрязняющих воздух и воду, и может быть использовано в химической, фармацевтической и биосинтетической промышленности. Способ заключается в том, что порошок ZnO подвергают интенсивной механической обработке в воздушной среде. При этом скорость измельчения в размольных барабанах планетарной шаровой мельницы составляет 250 оборотов в минуту, соотношение массы порошка и шаров 10:1, время измельчения 1 минута. Технический результат изобретения состоит в том, что за счет механоактивации порошков оксида цинка при заданных технологических параметрах увеличивается их фотокаталитическая активность. 3 ил.
Способ получения фотокатализатора на основе механоактивированного порошка оксида цинка, заключающийся в том, что порошок ZnO подвергают интенсивной механической обработке в воздушной среде, отличающийся тем, что скорость измельчения в размольных барабанах планетарной шаровой мельницы составляет 250 оборотов в минуту, соотношение массы порошка и шаров 10:1, время измельчения 1 минута.
| SEPELAK V | |||
| ET AL., Mechanochemical reactions and syntheses of oxides, Chem | |||
| Soc | |||
| Rev., 2013, 42, 7507-7520 | |||
| СПОСОБ ПОЛУЧЕНИЯ НАНОПОРОШКА КАРБИДА КРЕМНИЯ | 2012 |
|
RU2493937C1 |
| Способ приготовления скелетного никелевого катализатора для гидрирования органических соединений | 1988 |
|
SU1599083A1 |
| EP 2898951 A1, 29.07.2015. | |||
Авторы
Даты
2017-08-08—Публикация
2016-07-05—Подача