В данной заявке испрашивается приоритет по предварительной заявке США №62/628564, поданной 9 февраля 2018 года, которая полностью включена в данный документ посредством ссылки.
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
В данной заявке содержится перечень последовательностей, который был представлен в электронном виде в формате ASCII и полностью включен в данный документ посредством ссылки. Указанная копия ASCII, созданная 4 февраля 2019 года, называется 50474-161WO2_Sequence_Listing_2.4.19_ST25 и имеет размер 47,396 байт.
ОБЛАСТЬ ТЕХНИКИ
Данное изобретение относится к терапевтическим и диагностическим способам воспалительных заболеваний, опосредованных тучными клетками, включая астму.
УРОВЕНЬ ТЕХНИКИ
Астму канонически описывают как аллергическое воспалительное заболевание дыхательных путей, которое клинически характеризуется эпизодической обратимой обструкцией дыхательных путей. Терапевтическое обоснование для нацеливания на медиаторы аллергического воспаления при астме подтверждается клинической эффективностью, достигаемой препаратами против цитокинов 2-го типа, например, анти-ИЛ-5. Эти исследования подтвердили терапевтическую стратегию нацеливания на путь 2-го типа, чтобы обеспечить значимое улучшение клинических показателей, особенно у субъектов, отобранных на основе биомаркеров 2-го типа. Несмотря на эти достижения, остается значительный интерес к открытию и разработке новых способов лечения астмы, обладающих большей эффективностью при астме с высоким уровнем биомаркеров 2-го типа, а также для пациентов с астмой с низким уровнем биомаркеров 2-го типа, для которых, как ожидается, разработанные в настоящее время способы лечения обеспечивают меньшее улучшение клинических показателей.
Инфильтрация тучных клеток гладких мышц дыхательных путей является определяющим патофизиологическим признаком астмы. IgE/FcεRl-зависимые и IgE/FcεRI-независимые механизмы стимулируют высвобождение связанных с астмой растворимых медиаторов тучных клеток. Демонстрируя терапевтическую важность нацеливания на тучные клетки, XOLAIR® (омализумаб), препарат на основе монокпонального антитела против IgE, эффективен в ослаблении обострений астмы.
В данной области остается потребность в улучшенных терапевтических и диагностических подходах к астме и другим воспалительным заболеваниям, опосредованным тучными клетками.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Данное изобретение относится, среди прочего, к способам лечения пациентов с воспалительным заболеванием, опосредованным тучными клетками, способам определения того, могут ли пациенты с воспалительным заболеванием, опосредованным тучными клетками, отвечать на терапию (например, терапию, включающую выбранный агент из группы, состоящей из антагониста триптазы, антагониста Fc-эпсилона-рецептора (FcεR), антитела, истощающего IgE+ В-кпетки, антитела, истощающего тучные клетки или базофилы, антагониста активируемого протеазой рецептора 2 (PAR2), антагониста IgE и их комбинации), способам выбора терапии для пациента с воспалительным заболеванием, опосредованным тучными клетками, способам оценки ответа пациента с воспалительным заболеванием, опосредованным тучными клетками, и способам контроля ответа пациента с воспалительным заболеванием, опосредованным тучными клетками.
В одном аспекте изобретение относится к способу лечения пациента с воспалительным заболеванием, опосредованным тучными клетками, который был идентифицирован как имеющий (i) генотип, содержащий количество активных аллелей триптазы, которое равно или превышает эталонное количество активных аллелей триптазы; или (ii) уровень экспрессии триптазы в образце от пациента, который равен или превышает эталонный уровень триптазы, причем способ включает применение у пациента с воспалительным заболеванием, опосредованным тучными клетками, терапии, включающей агент, выбранный из группы, состоящей из антагониста триптазы, антагониста IgE, антитела, истощающего IgE+ В-клетки, антитела, истощающего тучные клетки или базофилы, антагониста активируемого протеазой рецептора 2 (PAR2), и их комбинации.
В другом аспекте изобретение относится к способу определения того, может ли пациент с воспалительным заболеванием, опосредованным тучными клетками, отвечать на терапию, включающую агент, выбранный из группы, состоящей из антагониста триптазы, антагониста IgE, антитела, истощающего IgE+ В-клетки, антитела, истощающего тучные клетки или базофилы, антагониста активируемого протеазой рецептора 2 (PAR2), и их комбинации, причем способ включает: (а) определение в образце от пациента с воспалительным заболеванием, опосредованным тучными клетками, количества активных аллелей триптазы у пациента; и (b) идентификацию пациента, имеющего вероятность ответа на терапию, включающую агент, выбранный из группы, состоящей из антагониста триптазы, антагониста IgE, антитела, истощающего IgE+ В-клетки, антитела, истощающего тучные клетки или базофилы, антагониста PAR2, и их комбинации, на основании количества активных аллелей триптазы у пациента, причем количество активных аллелей триптазы, равное или превышающее эталонное количество активных аллелей триптазы, указывает на то, что пациент имеет повышенную вероятность ответа на терапию.
В другом аспекте изобретение относится к способу определения того, может ли пациент с воспалительным заболеванием, опосредованным тучными клетками, отвечать на терапию, включающую агент, выбранный из группы, состоящей из антагониста триптазы, антагониста IgE, антитела, истощающего IgE+ В-клетки, антитела, истощающего тучные клетки или базофилы, антагониста активируемого протеазой рецептора 2 (PAR2), и их комбинации, причем способ включает: (а) определение уровня экспрессии триптазы в образце от пациента с воспалительным заболеванием, опосредованным тучными клетками; и (b) идентификацию пациента, имеющего вероятность ответа на терапию, включающую агент, выбранный из группы, состоящей из антагониста триптазы, антагониста IgE, антитела, истощающего IgE+ В-клетки, антитела, истощающего тучные клетки или базофилы, антагониста PAR2, и их комбинации, на основании уровня экспрессии триптазы в образце от пациента, причем уровень экспрессии триптазы в образце, равный или превышающий эталонный уровень триптазы, указывает на то, что пациент имеет повышенную вероятность ответа на терапию.
В некоторых вариантах осуществления любого из предшествующих аспектов способ дополнительно включает применение у пациента данной терапии.
В некоторых вариантах осуществления любого из предшествующих аспектов пациент был идентифицирован как имеющий уровень биомаркера 2-го типа в образце от пациента, который ниже эталонного уровня биомаркера 2-го типа. В некоторых вариантах осуществления агент применяют у пациента в виде монотерапии.
В некоторых вариантах осуществления любого из предшествующих аспектов пациент был идентифицирован как имеющий уровень биомаркера 2-го типа в образце от пациента, который равен или выше эталонного уровня биомаркера 2-го уровня. В некоторых вариантах осуществления способ дополнительно включает введение ингибитора пути TH2 пациенту.
В другом аспекте изобретение относится к способу лечения пациента с воспалительным заболеванием, опосредованным тучными клетками, который был идентифицирован как имеющий (i) генотип, содержащий количество активных аллелей триптазы, которое ниже эталонного количества активных аллелей триптазы; или (ii) уровень экспрессии триптазы в образце от пациента, который ниже эталонного уровня триптазы, причем способ включает применение у пациента с воспалительным заболеванием, опосредованным тучными клетками, терапии, включающей антагонист IgE или антагонист Fc-эпсилон-рецептора (FcεR).
В другом аспекте изобретение относится к способу определения того, может ли пациент с воспалительным заболеванием, опосредованным тучными клетками, отвечать на терапию, включающую антагонист IgE или антагонист FcεR, при этом способ включает: (а) определение в образце от пациента с воспалительным заболеванием, опосредованным тучными клетками, количества активных аллелей триптазы у пациента; и (b) идентификацию пациента, имеющего вероятность ответа на терапию, включающую антагонист IgE или антагонист FcεR, на основании количества активных аллелей триптазы у пациента, причем количество активных аллелей триптазы ниже эталонного количества активных аллелей триптазы указывает на то, что пациент имеет повышенную вероятность ответа на терапию.
В другом аспекте изобретение относится к способу определения того, может ли пациент с воспалительным заболеванием, опосредованным тучными клетками, отвечать на терапию, включающую антагонист IgE или антагонист FcεR, при этом способ включает: (а) определение уровня экспрессии триптазы в образце от пациента с воспалительным заболеванием, опосредованным тучными клетками; и (b) идентификацию пациента, имеющего вероятность ответа на терапию, включающую антагонист IgE или антагонист FcεR, на основании уровня экспрессии триптазы в образце от пациента, причем уровень экспрессии триптазы в образце от пациента ниже эталонного уровня триптазы указывает на то, что пациент имеет повышенную вероятность ответа на терапию.
В некоторых вариантах осуществления любого из предшествующих аспектов способ дополнительно включает применение у пациента данной терапии.
В некоторых вариантах осуществления любого из предшествующих аспектов пациент был идентифицирован как имеющий уровень биомаркера 2-го типа в образце от пациента, который равен или выше эталонного уровня биомаркера 2-го уровня. В некоторых вариантах осуществления способ дополнительно включает введение пациенту дополнительного ингибитора пути TH2.
В другом аспекте изобретение относится к способу выбора терапии для пациента с воспалительным заболеванием, отобранным тучными клетками, причем способ включает: (а) определение в образце от пациента с воспалительным заболеванием, опосредованным тучными клетками, количества активных аллелей триптазы у пациента; и
(b) выбор для пациента: (i) терапии, включающей агент, выбранный из группы, состоящей из антагониста триптазы, антагониста IgE, антитела, истощающего IgE+ В-клетки, антитела, истощающего тучные клетки или базофилы, антагониста активируемого протеазой рецептора 2 (PAR2), и их комбинации, если количество активных аллелей триптазы у пациента равно или выше эталонного количества активных аллелей триптазы, или (ii) терапию, включающую антагонист IgE или антагонист FcεR, если количество активных аллелей триптазы у пациента ниже эталонного количества активных аллелей триптазы.
В другом аспекте изобретение относится к способу выбора терапии для пациента с воспалительным заболеванием, отобранным тучными клетками, причем способ включает: (а) определение уровня экспрессии триптазы в образце от пациента с воспалительным заболеванием, отобранным тучными клетками; и (b) выбор для пациента: (i) терапии, включающей агент, выбранный из группы, состоящей из антагониста триптазы, антагониста IgE, антитела, истощающего IgE+ В-клетки, антитела, истощающего тучные клетки или базофилы, антагониста активируемого протеазой рецептора 2 (PAR2), и их комбинации, если уровень экспрессии триптазы в образце от пациента равен или выше эталонного уровня триптазы, или (ii) терапии, включающей антагонист IgE или антагонист FcεR, если уровень экспрессии триптазы в образце от пациента ниже эталонного уровня триптазы.
В некоторых вариантах осуществления любого из предшествующих аспектов способ дополнительно включает введение терапии, выбранной в соответствии с (b), пациенту.
В некоторых вариантах осуществления любого из предшествующих аспектов пациент был идентифицирован как имеющий уровень биомаркера 2-го типа в образце от пациента, который ниже эталонного уровня биомаркера 2-го типа. В некоторых вариантах осуществления агент применяют у пациента в виде монотерапии.
В некоторых вариантах осуществления любого из предшествующих аспектов пациент был идентифицирован как имеющий уровень биомаркера 2-го типа в образце от пациента, который равен или выше эталонного уровня биомаркера 2-го типа, и способ дополнительно включает выбор комбинированной терапии, включающей ингибитор пути TH2. В некоторых вариантах осуществления способ дополнительно включает введение ингибитора пути TH2 (или дополнительного ингибитора пути TH2) пациенту.
В другом аспекте изобретение относится к способу оценки ответа пациента с воспалительным заболеванием, опосредованным тучными клетками, на лечение терапией, включающей агент, выбранный из группы, состоящей из антагониста триптазы, антагониста IgE, антитела, истощающего IgE+ В-клетки, антитела, истощающего тучные клетки или базофилы, антагониста активируемого протеазой рецептора 2 (PAR2), и их комбинации, причем способ включает: (а) определение уровня экспрессии триптазы в образце от пациента с воспалительным заболеванием, опосредованным тучными клетками, в течение или после применения терапии, включающей агент, выбранный из группы, состоящей из антагониста триптазы, антагониста IgE, антитела, истощающего IgE+ В-клетки, антитела, истощающего тучные клетки или базофилы, антагониста PAR2, и их комбинации, у пациента; и (b) поддержание, корректировку или прекращение лечения на основе сравнения уровня экспрессии триптазы в образце с эталонным уровнем триптазы, причем изменение уровня экспрессии триптазы в образце от пациента по сравнению с эталонным уровнем указывает на ответ на лечение терапией. В некоторых вариантах осуществления изменение представляет собой повышение уровня экспрессии триптазы, и лечение продолжают. В некоторых вариантах осуществления изменение представляет собой снижение уровня экспрессии триптазы, и лечение корректируют или прекращают.
В другом аспекте изобретение относится к способу контроля ответа пациента с воспалительным заболеванием, опосредованным тучными клетками, которое лечится терапией, включающей агент, выбранный из группы, состоящей из антагониста триптазы, антагониста IgE, антитела, истощающего IgE+ В-клетки, антитела, истощающего тучные клетки или базофилы, антагониста активируемого протеазой рецептора 2 (PAR2), и их комбинации, причем способ включает: (а) определение уровня экспрессии триптазы в образце от пациента в течение или после применения терапии, включающей агент, выбранный из группы, состоящей из антагониста триптазы, антагониста IgE, антитела, истощающего IgE+ В-клетки, антитела, истощающего тучные клетки или базофилы, антагониста PAR2, и их комбинации, у пациента; и (b) сравнение уровня экспрессии триптазы в образце от пациента с эталонным уровнем триптазы, таким образом, отслеживая ответ пациента, проходящего лечение терапией. В некоторых вариантах осуществления изменение представляет собой повышение уровня триптазы, и лечение продолжают. В некоторых вариантах осуществления изменение представляет собой снижение уровня экспрессии триптазы, и лечение корректируют или прекращают.
В другом аспекте изобретение относится к агенту, выбранному из группы, состоящей из антагониста триптазы, антагониста IgE, антитела, истощающего IgE+ В-клетки, антитела, истощающего тучные клетки или базофилы, антагониста PAR2, и их комбинации, для применения в способе лечения пациента с воспалительным заболеванием, опосредованным тучными клетками, в котором (i) было определено, что генотип пациента содержит количество активных аллелей триптазы, которое равно или выше эталонного количества активных аллелей триптазы; или (ii) было определено, что образец от пациента имеет уровень экспрессии триптазы, который равен или выше эталонного уровня триптазы. В некоторых вариантах осуществления было определено, что пациент имеет уровень биомаркера 2-го типа в образце от пациента, который ниже эталонного уровня биомаркера 2-го типа, и агент предназначен для применения в виде монотерапии. В некоторых вариантах осуществления пациент был идентифицирован как имеющий уровень биомаркера 2-го типа в образце от пациента, который равен или выше эталонного уровня биомаркера 2-го типа, и агент предназначен для применения в комбинации с ингибитором пути TH2. В некоторых вариантах осуществления антагонист триптазы представляет собой антитело против триптазы, например, любое антитело против триптазы, описанное в данном документе. В некоторых вариантах осуществления антагонист IgE представляет собой антитело против IgE. например, любое из антител против IgE, описанных в данном документе.
В другом аспекте изобретение относится к агенту, выбранному из антагониста IgE или антагониста FcεR, для применения в способе лечения пациента с воспалительным заболеванием, опосредованным тучными клетками, в котором (i) определено, что генотип пациента содержит количество активных аллелей триптазы ниже эталонного количества активных аллелей триптазы; или (ii) было определено, что образец от пациента имеет уровень экспрессии триптазы, который ниже эталонного уровня триптазы. В некоторых вариантах осуществления было определено, что пациент имеет уровень биомаркера 2-го типа в образце от пациента, который равен или выше эталонного уровня биомаркера 2-го типа, а антагонист IgE или антагонист FcεR предназначен для применения в комбинации с дополнительным ингибитором пути TH2.
В другом аспекте изобретение обеспечивает применение агента, выбранного из группы, состоящей из антагониста триптазы, антагониста IgE, антитела, истощающего IgE+ В-клетки, антитела, истощающего тучные клетки или базофилы, антагониста PAR2, и их комбинации, при изготовлении лекарственного препарата для лечения пациента с воспалительным заболеванием, опосредованным тучными клетками, в котором (i) было определено, что генотип пациента содержит количество активных аллелей триптазы, которое равно или выше эталонного количества активных аллелей триптазы; или (ii) было определено, что образец от пациента имеет уровень экспрессии триптазы, который равен или выше эталонного уровня триптазы. В некоторых вариантах осуществления было определено, что пациент имеет уровень биомаркера 2-го типа в образце от пациента, который ниже эталонного уровня биомаркера 2-го типа, и агент предназначен для применения в виде монотерапии. В некоторых вариантах осуществления пациент был идентифицирован как имеющий уровень биомаркера 2-го типа в образце от пациента, который равен или выше эталонного уровня биомаркера 2-го типа, и агент предназначен для применения в комбинации с ингибитором пути TH2. В некоторых вариантах осуществления антагонист триптазы представляет собой антитело против триптазы, например, любое антитело против триптазы,описанное в данном документе. В некоторых вариантах осуществления антагонист IgE представляет собой антитело против IgE. например, любое из антител против IgE, описанных в данном документе. В некоторых вариантах осуществления антагонист триптазы следует вводить в комбинации с антагонистом IgE. В некоторых вариантах осуществления агент представляет собой антагонист триптазы, а лекарственный препарат составляют для введения с антагонистом IgE.
В другом аспекте изобретение обеспечивает применение антагониста IgE или антагониста FcεR при изготовлении лекарственного препарата для лечения пациента с воспалительным заболеванием, опосредованным тучными клетками, в котором (i) было определено, что генотип пациента содержит количество активных аллелей триптазы, которое ниже эталонного количества активных аллелей триптазы; или (ii) было определено, что образец от пациента имеет уровень экспрессии триптазы, который ниже эталонного уровня триптазы. В некоторых вариантах осуществления было определено, что пациент имеет уровень биомаркера 2-го типа в образце от пациента, который равен или выше эталонного уровня биомаркера 2-го типа, а антагонист IgE или антагонист FcεR предназначен для применения в комбинации с дополнительным ингибитором пути TH2.
В некоторых вариантах осуществления любого из предшествующих аспектов количество активных аллелей триптазы определяют путем секвенирования локусов TPSAB1 и TPSB2 генома пациента. В некоторых вариантах осуществления секвенирование представляет собой секвенирование по Сэнгеру или массовое параллельное секвенирование. В некоторых вариантах осуществления локус TPSAB1 секвенируют при помощи способа, включающего (i) амплификацию нуклеиновой кислоты от субъекта в присутствии первого прямого праймера, содержащего нуклеотидную последовательность 5'-CTG GTG TGC AAG GTG ААТ GG-3' (SEQ ID NO: 31) и первого обратного праймера, содержащего нуклеотидную последовательность 5'-AGG ТСС AGC ACT CAG GAG GA 3' (SEQ ID NO: 32), с образованием ампликона TPSAB1 и (ii) секвенирование ампликона TPSAS1B некоторых вариантах осуществления секвенирование ампликона TPSAB1 включает применение первого прямого праймера и первого обратного праймера. В некоторых вариантах осуществления локус TPSB2 секвенируют при помощи способа, включающего (i) амплификацию нуклеиновой кислоты от субъекта в присутствии второго прямого праймера, содержащего нуклеотидную последовательность 5'-GCA GGT GAG ССТ GAG AGT СС-3' (SEQ ID NO: 33), и второго обратного праймера, содержащего нуклеотидную последовательность 5'-GGG АСС ТТС АС С TGC ТТС AG-3' (SEQ ID NO: 34), для получения ампликона TPSB2 и (ii) секвенирования ампликона TPSB2. В некоторых вариантах осуществления секвенирование ампликона TPSB2 включает применение второго прямого праймера и обратного праймера для секвенирования, содержащего нуклеотидную последовательность 5'-CAG CCA GTG АСС CAG САС-3' (SEQ ID NO: 35).
В некоторых вариантах осуществления любого из предшествующих аспектов количество активных аллелей триптазы определяется по формуле: 4 - сумма количества аллелей α-триптазы и βIII-триптазы со сдвигом рамки (βIIIFS) в генотипе пациента В некоторых вариантах осуществления альфа-триптазу определяют путем обнаружения ОНП с733 G>А в TPSAB1, содержащем нуклеотидную последовательность
CTGCAGGCGGGCGTGGTCAGCTGGG[G/A]CGAGGGCTGTGCCCAGCCCAACCGG (SEQ ID NO: 36), где присутствие А в с733> указывает на альфа-триптазу. В некоторых вариантах осуществления бета-IIIFS-триптазу определяют путем обнаружения мутации c980_981insC в TPSB2, содержащей нуклеотидную последовательность CACACGGTCACCCTGCCCCCTGCCTCAGAGACCTTCCCCCCC (SEQ ID NO: 37).
В некоторых вариантах осуществления любого из предшествующих аспектов эталонное количество активных аллелей триптазы определяют в группе пациентов с воспалительным заболеванием, опосредованным тучными клетками. В некоторых вариантах осуществления эталонное количество активных аллелей триптазы равно 3.
В некоторых вариантах осуществления любого из предшествующих аспектов количество активных аллелей триптазы у пациента равно 3 или 4.
В некоторых вариантах осуществления любого из предшествующих аспектов количество активных аллелей триптазы у пациента равно 0, 1 или 2.
В некоторых вариантах осуществления любого из предшествующих аспектов триптаза представляет собой бета-I-триптазу, бета-II-триптазу, бета-III-триптазу, альфа-I-триптазу или их комбинацию.
В некоторых вариантах осуществления любого из предшествующих аспектов уровень экспрессии триптазы представляет собой уровень экспрессии белка. В некоторых вариантах осуществления уровень экспрессии белка триптазы представляет собой уровень экспрессии активной триптазы. В некоторых вариантах осуществления уровень экспрессии белка триптазы представляет собой уровень экспрессии общей триптазы. В некоторых вариантах осуществления уровень экспрессии белка измеряют с применением иммуноанализа, иммуноферментного анализа (ИФА), вестерн-блоттинга или масс-спектрометрии. В некоторых вариантах осуществления уровень экспрессии триптазы представляет собой уровень экспрессии мРНК. В некоторых вариантах осуществления уровень экспрессии мРНК измеряют при помощи метода полимеразной цепной реакции (ПЦР) или микроматричного чипа. В некоторых вариантах осуществления метод ПЦР представляет собой кПЦР.
В некоторых вариантах осуществления любого из предшествующих аспектов эталонный уровень триптазы представляет собой уровень, определенный в группе индивидуумов с воспалительным заболеванием, опосредованным тучными клетками. В некоторых вариантах осуществления эталонный уровень триптазы представляет собой медианный уровень.
В некоторых вариантах осуществления любого из предшествующих аспектов образец от пациента выбран из группы, состоящей из образца крови, образца ткани, образца мокроты, образца бронхиального лаважа, образца жидкости слизистой оболочки (MLF), бронхосорбционного образца и назосорбционного образца. В некоторых вариантах осуществления образец крови представляет собой образец цельной крови, образец сыворотки, образец плазмы или их комбинацию. В некоторых вариантах осуществления образец крови представляет собой образец сыворотки или образец плазмы.
В некоторых вариантах осуществления любого из предшествующих аспектов агент представляет собой антагонист триптазы. В некоторых вариантах осуществления антагонист триптазы представляет собой антагонист альфа-триптазы или антагонист бета-триптазы. В некоторых вариантах осуществления антагонист триптазы представляет собой антагонист бета-триптазы. В некоторых вариантах осуществления антагонист бета-триптазы представляет собой антитело против бета-триптазы или его антигенсвязывающий фрагмент. В некоторых вариантах осуществления антитело содержит следующие шесть гипервариабельных областей (HVR): (а) HVR-H1, содержащую аминокислотную последовательность DYGMV (SEQ ID NO: 1); (b) HVR-H2, содержащую аминокислотную последовательность FISSGSSTVYYADTMKG (SEQ ID NO: 2); (с) HVR-H3, содержащую аминокислотную последовательность RNYDDWYFDV (SEQ ID NO: 3); (d) HVR-L1, содержащую аминокислотную последовательность SASSSVTYMY (SEQ ID NO: 4); (е) HVR-L2, содержащую аминокислотную последовательность RTSDLAS (SEQ ID: 5); и (f) HVR-L3, содержащую аминокислотную последовательность QHYHSYPLT (SEQ ID NO: 6). В некоторых вариантах осуществления антитело содержит (а) вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, имеющую по меньшей мере 90%, по меньшей мере 95% или по меньшей мере 99% идентичность последовательности с аминокислотной последовательностью SEQ ID NO: 7; (b) вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, имеющую по меньшей мере 90%, по меньшей мере 95% или по меньшей мере 99% идентичность с аминокислотной последовательностью SEQ ID NO: 8; или (с) домен VH как в (а) и домен VL как в (b). В некоторых вариантах домен VH содержит аминокислотную последовательность SEQ ID NO: 7. В некоторых вариантах домен VL содержит аминокислотную последовательность SEQ ID NO: 8. В некоторых вариантах домен VH содержит аминокислотную последовательность SEQ ID NO: 7, и домен VL содержит аминокислотную последовательность SEQ ID NO: 8. В некоторых вариантах осуществления антитело содержит (а) тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 9, и (b) легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 10. В некоторых вариантах осуществления антитело содержит (а) тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 11, и (b) легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 10. В некоторых вариантах осуществления антитело содержит следующие шесть HVR: (a) HVR-H1, содержащую аминокислотную последовательность GYAIT (SEQ ID NO: 12); (b) HVR-H2, содержащую аминокислотную последовательность GISSAATTFYSSWAKS (SEQ ID NO: 13); (с) HVR-H3, содержащую аминокислотную последовательность DPRGYGAALDRLDL (SEQ ID NO: 14); (d) HVR-L1, содержащую аминокислотную последовательность QSIKSVYNNRLG (SEQ ID NO: 15); (е) HVR-L2, содержащую аминокислотную последовательность ETSILTS (SEQ ID: 16); и (f) HVR-L3, содержащую аминокислотную последовательность AGGFDRSGDTT (SEQ ID NO: 17). В некоторых вариантах осуществления антитело содержит (а) вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, имеющую по меньшей мере 90%, по меньшей мере 95% или по меньшей мере 99% идентичность последовательности с аминокислотной последовательностью SEQ ID NO: 18; (b) вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, имеющую по меньшей мере 90%, по меньшей мере 95% или по меньшей мере 99% идентичность с аминокислотной последовательностью SEQ ID NO: 19; или (с) домен VH как в (а) и домен VL как в (b). В некоторых вариантах осуществления домен VH содержит аминокислотную последовательность SEQ ID NO: 18. В некоторых вариантах осуществления домен VL содержит аминокислотную последовательность SEQ ID NO: 19. В некоторых вариантах осуществления домен VH содержит аминокислотную последовательность SEQ ID NO: 18, и домен VL содержит аминокислотную последовательность SEQ ID NO: 19. В некоторых вариантах осуществления антитело содержит (а) тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 20, и (b) легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 21. В некоторых вариантах осуществления антитело содержит (а) тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 22, и (b) легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 21. В некоторых вариантах осуществления терапия дополнительно включает антагонист IgE.
В некоторых вариантах осуществления любого из предшествующих аспектов агент представляет собой антагонист FcεR. В некоторых вариантах осуществления антагонист FcεR представляет собой ингибитор тирозинкиназы Брутона (ВТК). В некоторых вариантах осуществления ингибитор ВТК представляет собой GDC-0853, акалабрутиниб, GS-4059, спебрутиниб, BGB-3111 или НМ71224. В некоторых вариантах осуществления агент представляет собой антитело, истощающее IgE+ В-клетки. В некоторых вариантах осуществления антитело, истощающее IgE+ В-клетки, представляет собой антитело против домена М1.
В некоторых вариантах осуществления любого из предшествующих аспектов агент представляет собой антитело, истощающее тучные клетки или базофилы.
В некоторых вариантах осуществления любого из предшествующих аспектов агент представляет собой антагонист PAR2.
В некоторых вариантах осуществления любого из аспектов, описанных в данном документе, терапия или комбинация содержит антагонист триптазы (например, антитело против триптазы, включая любое из антител против триптазы, описанных в данном документе) и антагонист IgE (например, антитело против IgE, включая любое из антител против IgE, описанных в данном документе, например, омализумаб (например, XOLAIR®)).
В некоторых вариантах осуществления любого из описанных в данном документе аспектов агент представляет собой антагонист IgE. В некоторых вариантах осуществления антагонист IgE представляет собой антитело против IgE. В некоторых вариантах осуществления антитело против IgE представляет собой антитело, блокирующее IgE, и/или антитело, истощающее IgE. В некоторых вариантах осуществления антитело против IgE содержит следующие шесть HVR: (а) HVR-H1, содержащую аминокислотную последовательность GYSWN (SEQ ID NO: 40); (b) HVR-H2, содержащую аминокислотную последовательность SITYDGSTNYNPSVKG (SEQ ID NO: 41); (с) HVR-H3, содержащую аминокислотную последовательность GSHYFGHWHFAV (SEQ ID NO: 42); (d) HVR-L1, содержащую аминокислотную последовательность RASQSVDYDGDSYMN (SEQ ID NO: 43); (е) HVR-L2, содержащую аминокислотную последовательность AASYLES (SEQ ID: 44); и (f) HVR-L3, содержащую аминокислотную последовательность QQSHEDPYT (SEQ ID NO: 45). В некоторых вариантах осуществления антитело против IgE содержит (а) вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, имеющую по меньшей мере 90%, по меньшей мере 95% или по меньшей мере 99% идентичность последовательности с аминокислотной последовательностью SEQ ID NO: 38; (b) вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, имеющую по меньшей мере 90%, по меньшей мере 95% или по меньшей мере 99% идентичность с аминокислотной последовательностью SEQ ID NO: 39; или (с) домен VH как в (а) и домен VL как в (b). В некоторых вариантах осуществления домен VH содержит аминокислотную последовательность SEQ ID NO: 38. В некоторых вариантах осуществления домен VL содержит аминокислотную последовательность SEQ ID NO: 39. В некоторых вариантах осуществления домен VH содержит аминокислотную последовательность SEQ ID NO: 38, и домен VL содержит аминокислотную последовательность SEQ ID NO: 39. В некоторых вариантах осуществления антитело против IgE представляет собой омализумаб (XOLAIR®) или ХтАЬ7195. В некоторых вариантах осуществления антитело против IgE представляет собой омализумаб (XOLAIR®).
В некоторых вариантах осуществления любого из предшествующих аспектов биомаркер 2-го типа представляет собой связанный с клеткой TH2 цитокин, периостин, количество эозинофилов, профиль эозинофилов, FeNO или IgE. В некоторых вариантах осуществления цитокин, связанный с клеткой TH2, представляет собой ИЛ-13, ИЛ-4, ИЛ-9 или ИЛ-5. В некоторых вариантах осуществления ингибитор пути TH2 ингибирует любую мишень, выбранную из индуцируемой интерлейкином-2 Т-клеточной киназы (ITK), тирозинкиназы Брутона (ВТК), Янус киназу 1 (JAK1) (например, руксолитиниба, тофацитиниба, оклацитиниба, барицитиниба, филготиниба, гандотиниба, лестауртиниба, момелотиниба, пакринитиба, упадацитиниба, пефитиниба и федратиниба), GATA-связывающего белка 3 (GATA3), ИЛ-9 (например, MEDI-528), ИЛ-5 (например, меполизумаба, CAS №196078-29-2; ресилизумаба), ИЛ-13 (например, IMA-026, IMA-638 (также называемого анрукинзумабом, INN №910649-32-0; QAX-576; ловушкой для ИЛ-4/ИЛ-13) тралокинумаба (также называемого САТ-354, CAS №1044515-88-9); AER-001, АВТ-308 (также называемого гуманизированным антителом 13С5.5)), ИЛ-4 (например, AER-001, ловушки для ИЛ-4/ИЛ-13), OX40L, TSLP, ИЛ-25, ИЛ-33 и IgE (например, XOLAIR®, QGE-031 и MEDI-4212); и рецепторов, например: рецептора ИЛ-9, рецептора ИЛ-5 (например, MEDI-563 (бенилизумаба, CAS №1044511-01-4)), альфа рецептора ИЛ-4 (например, AMG-317, AIR-645), альфа-1 рецептора ИЛ-13 (например, R-1671) и альфа-2 рецептора ИЛ-13, ОХ40, TSLP-R, ИЛ-7R-альфа (корецептора для TSLP), ИЛ-17RB (рецептора для ИЛ-25), ST2 (рецептора для ИЛ-33), CCR3, CCR4, CRTH2 (например, AMG-853, АР768, АР-761, MLN6095, АСТ129968), FcεRI, Fc£RII/CD23 (рецепторов для IgE), Flap (например, GSK2190915), Syk киназы (R-343, PF3526299); CCR4 (AMG-761), TLR9 (QAX-935) и мультицитокинового ингибитора CCR3, ИЛ-5, ИЛ-3 и ГМ-КСФ (например, TPI ASM8).
В некоторых вариантах осуществления любого из предшествующих аспектов способ дополнительно включает введение пациенту дополнительного терапевтического агента. В некоторых вариантах осуществления дополнительный терапевтический агент выбран из группы, состоящей из кортикостероида, антагониста, связывающего ось ИЛ-33, антагониста TRPA1, бронходилататора или лекарственного препарата для контроля симптомов астмы, иммуномодулятора, ингибитора тирозинкиназы и ингибитора фосфодиэстеразы. В некоторых вариантах осуществления дополнительный терапевтический агент представляет собой кортикостероид. В некоторых вариантах осуществления кортикостероид представляет собой ингаляционный кортикостероид.
В некоторых вариантах осуществления любого из предшествующих аспектов воспалительное заболевание, опосредованное тучными клетками, выбрано из группы, состоящей из астмы, атопического дерматита, хронической спонтанной крапивницы (CSU), системной анафилаксии, мастоцитоза, хронической обструктивной болезни легких (ХОБЛ), идиопатического фиброза легких (IPF) и эозинофильного эзофагита. В некоторых вариантах осуществления воспалительное заболевание, опосредованное тучными клетками, представляет собой астму. В некоторых вариантах осуществления астма представляет собой от умеренной до тяжелой. В некоторых вариантах осуществления астма не контролируется кортикостероидами. В некоторых вариантах осуществления астма представляет собой астму с высоким уровнем TH2 или астму с низким уровнем TH2.
В другом аспекте изобретение относится к набору для идентификации пациента с воспалительным заболеванием, опосредованным тучными клетками, который имеет вероятность ответа на терапию, включающую агент, выбранный из группы, антагониста триптазы, антагониста IgE, антитела, истощающего IgE+ В-клетки, антитела, истощающего тучные клетки или базофилы, антагониста активируемого протеазой рецептора 2 (PAR2), и их комбинации, причем набор содержит: (а) реагенты для определения количества активных аллелей триптазы у пациента или для определения уровня экспрессии триптазы в образце от пациента; и, необязательно, (b) инструкции по применению реагентов для идентификации пациента с воспалительным заболеванием, опосредованным тучными клетками, который имеет вероятность ответа на терапию, включающую агент, выбранный из группы, состоящей из антагониста триптазы, антагониста IgE, антитела, истощающего IgE+ В-клетки, антитела, истощающего тучные клетки или базофилы, антагониста PAR2, и их комбинации. В некоторых вариантах осуществления агент представляет собой антагонист триптазы, и терапия дополнительно включает антагонист IgE. В некоторых вариантах осуществления терапия включает антагонист триптазы и антагонист IgE.
В другом аспекте изобретение относится к набору для идентификации пациента с воспалительным заболеванием, опосредованным тучными клетками, который имеет вероятность ответа на терапию, включающую антагонист IgE или антагонист FcεR, причем набор содержит: (а) реагенты для определения количества активных аллелей триптазы у пациента или для определения уровня экспрессии триптазы в образце от пациента; и, необязательно, (b) инструкции по применению реагентов для идентификации пациента с воспалительным заболеванием, опосредованным тучными клетками, который имеет вероятность ответа на терапию, включающую антагонист IgE или антагонист FcεR.
В некоторых вариантах осуществления любого из предшествующих аспектов набор дополнительно содержит реагенты для определения уровня биомаркера 2-го типа в образце от пациента.
В другом аспекте изобретение относится к агенту, выбранному из группы, состоящей из антагониста триптазы, антагониста IgE, антитела, истощающего IgE+ В-клетки, антитела, истощающего тучные клетки или базофилы, антагониста PAR2, и их комбинации, для применения в способе лечения пациента с воспалительным заболеванием, опосредованным тучными клетками, в котором (i) было определено, что генотип пациента содержит количество активных аллелей триптазы, которое равно или выше эталонного количества активных аллелей триптазы; или (ii) было определено, что образец от пациента имеет уровень экспрессии триптазы, который равен или выше эталонного уровня триптазы. В некоторых вариантах осуществления было определено, что пациент имеет уровень биомаркера 2-го типа в образце от пациента, который ниже эталонного уровня биомаркера 2-го типа, и агент предназначен для применения в виде монотерапии. В некоторых вариантах осуществления пациент был идентифицирован как имеющий уровень биомаркера 2-го типа в образце от пациента, который равен или выше эталонного уровня биомаркера 2-го типа, и агент предназначен для применения в комбинации с ингибитором пути TH2.
В другом аспекте изобретение относится к агенту, выбранному из антагониста IgE или антагониста FcεR, для применения в способе лечения пациента с воспалительным заболеванием, опосредованным тучными клетками, в котором (i) определено, что генотип пациента содержит количество активных аллелей триптазы ниже эталонного количества активных аллелей триптазы; или (ii) было определено, что образец от пациента имеет уровень экспрессии триптазы, который ниже эталонного уровня триптазы. В некоторых вариантах осуществления было определено, что пациент имеет уровень биомаркера 2-го типа в образце от пациента, который равен или выше эталонного уровня биомаркера 2-го типа, а антагонист IgE или антагонист FcεR предназначен для применения в комбинации с дополнительным ингибитором пути TH2.
В другом аспекте изобретение обеспечивает применение агента, выбранного из группы, состоящей из антагониста триптазы, антагониста IgE, антитела, истощающего IgE+ В-клетки, антитела, истощающего тучные клетки или базофилы, антагониста PAR2, и их комбинации, при изготовлении лекарственного препарата для лечения пациента с воспалительным заболеванием, опосредованным тучными клетками, в котором (i) было определено, что генотип пациента содержит количество активных аллелей триптазы, которое равно или выше эталонного количества активных аллелей триптазы; или (ii) было определено, что образец от пациента имеет уровень экспрессии триптазы, который равен или выше эталонного уровня триптазы. В некоторых вариантах осуществления было определено, что пациент имеет уровень биомаркера 2-го типа в образце от пациента, который ниже эталонного уровня биомаркера 2-го типа, и агент предназначен для применения в виде монотерапии. В некоторых вариантах осуществления пациент был идентифицирован как имеющий уровень биомаркера 2-го типа в образце от пациента, который равен или выше эталонного уровня биомаркера 2-го типа, и агент предназначен для применения в комбинации с ингибитором пути TH2.
В другом аспекте изобретение обеспечивает применение антагониста IgE или антагониста FcεR при изготовлении лекарственного препарата для лечения пациента с воспалительным заболеванием, опосредованным тучными клетками, в котором (i) было определено, что генотип пациента содержит количество активных аллелей триптазы, которое ниже эталонного количества активных аллелей триптазы; или (ii) было определено, что образец от пациента имеет уровень экспрессии триптазы, который ниже эталонного уровня триптазы. В некоторых вариантах осуществления было определено, что пациент имеет уровень биомаркера 2-го типа в образце от пациента, который равен или выше эталонного уровня биомаркера 2-го типа, а антагонист IgE или антагонист FcεR предназначен для применения в комбинации с дополнительным ингибитором пути TH2.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
На Фиг. 1 представлен график, демонстрирующий количество активных аллелей триптазы для пациентов с умеренной или тяжелой астмой. Количество активных аллелей триптазы наносят на столбчатую диаграмму для субъектов с умеренной или тяжелой астмой из BOBCAT, EXTRA и MILLY.
На Фиг. 2А и 2В представлена серия графиков, демонстрирующих, что общий уровень белка триптазы периферической крови связан с количеством копий триптазы при умеренной или тяжелой астме. Анализ количества белка, полученного от определенного гена, (pQTL) проводили для общей триптазы плазмы из исследования BOBCAT (Фиг. 2А) и общей сывороточной триптазы из исследования MILLY (Фиг. 2В). Аппроксимирующая прямая (95% ДИ) показана серым цветом. Р-значение r2 из линейной регрессии отмечается на графиках, r2 представляет собой коэффициент определения линейной регрессии, который принимает значение от 0 до 1; возрастающие значения указывают на долю дисперсии, описываемой независимой переменной.
На Фиг. 3 представлена серия графиков, демонстрирующих эффективность лечения ОФВ1 при астме от терапии антителом против IgE (омализумаб (XOLAIR®)) на основе количества копий активных триптаз. Процентное изменение ОФВ1 от исходного уровня оценивали у субъектов из исследования EXTRA на основе количества аллелей активных триптаз (левая панель, 1 или 2; правая панель, 3 или 4).
На Фиг. 4А-4С представлена серия графиков, демонстрирующих, что биомаркеры астмы 2-го типа не коррелируют с количеством активных аллелей триптазы при умеренной или тяжелой астме. Уровни биомаркера 2-го типа периостина в сыворотке (Фиг. 4А), фракция оксида азота в выдыхаемом воздухе (FeNO) (Фиг. 4В) и количество эозинофилов в крови (Фиг. 4С) были оценены в отношении количества активной триптазы в когорте с умеренной или тяжелой астмой из BOBCAT, EXTRA, и MILLY.
ПОДРОБНОЕ ОПИСАНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
I. Определения
Термин «около», используемый в данном документе, относится к обычному диапазону погрешностей для соответствующего значения и хорошо известный специалисту в данной области техники. В данном документе применение «около» по отношению к величине или параметру включает (и описывает) варианты осуществления, которые относятся непосредственно к этой величине или параметру по существу.
Термины «биомаркер» и «маркер» используются в данном документе взаимозаменяемо для обозначения молекулярного маркера на основе ДНК, РНК, белка, углеводов или гликолипидов, экспрессию или присутствие которого в образце субъекта или пациента можно обнаружить стандартными способами (или способами, описанными в данном документе) и полезны, например, для идентификации, например, вероятности восприимчивости или чувствительности млекопитающего, подвергаемого лечению, или для мониторинга ответа субъекта на лечение. Экспрессия такого биомаркера может быть определена как более высокая или более низкая в образце, полученном от пациента, который имеет повышенную или пониженную вероятность ответа на терапию, по сравнению с эталонным уровнем (включая, например, средний уровень экспрессии биомаркера в образцах из группы/популяции пациентов (например, пациентов с астмой), уровень биомаркера в образцах из группы/популяции контрольных индивидуумов (например, здоровых индивидуумов) или уровень в образце, ранее полученном от индивидуума в предыдущий раз). В конкретных вариантах осуществления биомаркер, как описано в данном документе, представляет собой количество активных аллелей триптазы или уровень экспрессии триптазы.
В контексте данного документа термин «триптаза» относится к любой нативной триптазе из любого источника, относящегося к позвоночным, включая млекопитающих, таких как приматы (например, люди) и грызуны (например, мыши и крысы), если не указано иное. Триптаза также известна в данной области техники как туч но клеточная триптаза, тучноклеточная протеаза II, триптаза кожи, триптаза легких, триптаза гипофиза, тучноклеточная нейтральная протеиназа и тучноклеточная сериновая протеиназа II. Термин «триптаза» включает альфа-триптазу (кодируется у человека с помощью TPSAB1), бета-триптазу (кодируется у человека с помощью TPSAB1 и TPSB2; см. ниже), дельта-триптазу (кодируется у человека с помощью TPSD1), гамма-триптазу (кодируется у человека с помощью TPSG1) и эпсилон-триптазу (кодируется у человека с помощью PRSS22). Белки альфа (α)-, бета (β)- и гамма (γ)- триптазы растворимы, в то время как белки эпсилон (ε)-триптазы прикреплены к мембране. Бета- и гамма-триптаза представляют собой активные сериновые протеазы, хотя они имеют разные специфичности. Белки альфа- и дельта (δ)-триптазы представляют собой в значительной степени неактивные протеазы, поскольку они имеют остатки в критическом положении, которые отличаются от типичных активных сериновых протеаз. Иллюстративную полноразмерную последовательность белка альфа-триптазы можно найти под номером доступа NCBI GenBank ACZ98910.1. Иллюстративные полноразмерные последовательности белка гамма-триптазы можно найти под номером доступа Uniprot Q9NRR2 или номером доступа GenBank Q9NRR2.3, AAF03695.1, NP_036599.3 или AAF76457.1. Иллюстративные полноразмерные последовательности белка дельта-триптазы можно найти под номером доступа Uniprot Q9BZJ3 или номером доступа GenBank NP_036349.1. Несколько генов триптазы сгруппированы на человеческой хромосоме 16р13.3. Термин охватывает «полноразмерную» непроцессированную триптазу, а также любую форму триптазы, возникающую в результате процессинга в клетке. Бета-триптаза представляет собой основную триптазу, экспрессируемую в тучных клетках, в то время как альфа-триптаза представляет собой основную триптазу, экспрессируемую в базофилах. Альфа-триптаза и бета-триптаза, как правило, содержит лидерную последовательность из приблизительно 30 аминокислот и каталитическую последовательность из приблизительно 245 аминокислот (см., например, Schwartz, Immunol. Allergy Clin. N. Am. 26:451-463, 2006).
В контексте данного документа термин «бета-триптаза» относится к любой нативной бета-триптазе из любого источника, относящегося к позвоночным, включая млекопитающих, таких как приматы (например, люди) и грызуны (например, мыши и крысы), если не указано иное. Бета-триптаза представляет собой сериновую протеазу, которая является основным компонентом секреторных гранул тучных клеток. В контексте данного документа термин охватывает бета-1-триптазу (кодируемую геном TPSAB1, который также кодирует альфа-1-триптазу), бета-2-триптазу (кодируемую геном TPSB2) и бета-3-триптазу (также кодируемую геном TPSB2). Иллюстративная последовательность бета-1-триптазы человека показана в SEQ ID NO: 23 (см. также номер доступа GenBank NP_003285.2). Иллюстративная последовательность бета-2-триптазы человека показана в SEQ ID NO: 24 (см. также номер доступа GenBank AAD13876.1). Иллюстративная последовательность бета-3-триптазы человека показана в SEQ ID NO: 25 (см. также номер доступа GenBank NP_077078.5). Термин бета-триптаза охватывает «полноразмерную» непроцессированную бета-триптазу, а также бета-триптазу, полученную в результате посттрансляционных модификаций, включая протеолитичесий процессинг. Предполагается, что полноразмерная бета-триптаза процессируется в две протеолитические стадии. Во-первых, происходит автокаталитическое межмолекулярное расщепление в R-3, особенно при кислотном рН и в присутствии полианиона (например, гепарина или декстрансульфата). Затем оставшийся продипептид удаляется (вероятно, дипептидилпептидазой I). Для полноразмерной человеческой бета-1-триптазы, со ссылкой на SEQ ID NO: 23 ниже, подчеркнутые аминокислотные остатки, которые соответствуют нативной лидерной последовательности, и выделенные жирным шрифтом и серым цветом аминокислотные остатки, которые соответствуют продомену, расщепляются с образованием зрелого белка (см., например, Sakai et al. J. Clin. Invest. 97:988-995, 1996)

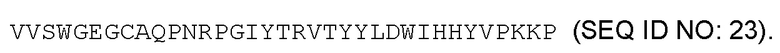
Зрелая ферментативно активная бета-триптаза, как правило, представляет собой гомотетрамер или гетеротетрамер, хотя сообщалось об активном мономере (см., например, Fukuoka et al. J. Immunol. 176:3165, 2006). Субъединицы тетрамера бета-триптазы удерживаются вместе посредством гидрофобных и полярных взаимодействий между субъединицами и стабилизируются полианионами (в частности, гепарином и декстрансульфатом). Термин «триптаза» может относиться ктетрамеру триптазе или мономеру триптазе. Иллюстративные последовательности для зрелой человеческой бета-1-, бета-2- и бета-3-триптазы приведены в SEQ ID NO: 26, SEQ ID NO: 27, и SEQ ID NO: 28, соответственно. Активный сайт каждой субъединицы обращен в центральную пору тетрамера, размеры которой составляют приблизительно 50×30 ангстрем (см., например, Pereira et al. Nature 392:306-311, 1998). Размер центральной поры, как правило, ограничивает доступ активных сайтов ингибиторами. Иллюстративные субстраты бета-триптазы включают, но не ограничиваются ими, PAR2, С3, фибриноген, фибронектин и кининоген.
Термины «олигонуклеотид» и «полинуклеотид» используются взаимозаменяемо и относятся к молекуле, состоящей из двух или более дезоксирибонуклеотидов или рибонуклеотидов, предпочтительно более трех. Его точный размер будет зависеть от многих факторов, которые, в свою очередь, зависят от конечной функции или использования олигонуклеотида. Олигонуклеотид может быть получен синтетическим путем или путем клонирования. Химеры дезоксирибонуклеотидов и рибонуклеотидов также могут входить в объем данного изобретения.
Термин «генотип» относится к описанию аллелей гена, содержащихся в индивидууме или образце. В контексте данного изобретения не делается различий между генотипом индивидуума и генотипом образца, полученного от индивидуума. Хотя обычно генотип определяется из образцов диплоидных клеток, генотип может быть определен из образца гаплоидных клеток, таких как сперматозоид.
Положение нуклеотида в геноме, при котором в популяции возможно более одной последовательности, обозначается в данном документе как «полиморфизм» или «полиморфный сайт». Полиморфный сайт может представлять собой, например, нуклеотидную последовательность из двух или более нуклеотидов, вставленный нуклеотид или нуклеотидную последовательность, удаленный нуклеотид, или нуклеотидную последовательность, или микросателлит. Полиморфный сайт, длина которого составляет два или более нуклеотидов, может составлять 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15 или более, 20 или более, 30 или более, 50 или более, 75 или более, 100 или более, 500 или более, или около 1000 нуклеотидов в длину, где все или некоторые из нуклеотидных последовательностей различаются в пределах области.
Термин «однонуклеотидный полиморфизм» или «ОНП» относится к замене одного основания в последовательности ДНК, которая приводит к генетической изменчивости. Однонуклеотидные полиморфизмы могут происходить в любой области гена. В некоторых случаях полиморфизм может привести к изменению последовательности белка. Изменение последовательности белка может повлиять на функцию белка или нет.
Когда в полиморфном сайте присутствуют две, три или четыре альтернативные нуклеотидные последовательности, каждая нуклеотидная последовательность называется «полиморфным вариантом» или «вариантом нуклеиновой кислоты». Каждый возможный вариант в последовательности ДНК упоминается как «аллель». Как правило, первая идентифицированная аллельная форма произвольно обозначена как контрольная форма, а другие аллельные формы обозначены как альтернативные или вариантные аллели.
Термин «количество активных аллелей триптазы» относится к количеству активных аллелей триптазы в генотипе субъекта. В некоторых вариантах осуществления количество активных аллелей триптазы можно определить путем учета инактивирующих мутаций TPSAB1 и TPSB2. Поскольку у каждого диплоидного субъекта будет две копии каждого из TPSAB1 и TPSB2, количество активных аллелей триптазы может быть определено по формуле 4 - сумма количества аллелей альфа-триптазы и бета-III-триптазы со сдвигом рамки (бета-IIIFS) в генотипе субъекта. В некоторых вариантах осуществления количество активных аллелей триптазы у субъекта представляет собой целое число в диапазоне от 0 до 4 (например, 0, 1, 2, 3 или 4).
Термин «эталонное количество активных аллелей триптазы» относится к количеству активных аллелей триптазы, с которым сравнивается другое количество активных аллелей триптазы, например, для диагностического, предиктивного, прогностического и/или терапевтического определения. Количество эталонных активных аллелей триптазы может быть определено в эталонном образце, эталонной популяции и/или может быть предварительно заданным значением (например, пороговым значением, которое ранее было определено для значимого (например, статистически значимого) разделения первой субпопуляции индивидуумов от второй субпопуляции индивидуумов (например, с точки зрения ответа на терапию (например, терапию, включающую агент, выбранный из группы, состоящей из антагониста триптазы, антагониста IgE, антагониста FcεR, антитела, истощающего IgE+ В-клетки, антитела, истощающего тучные клетки или базофилы, антагониста PAR2 и их комбинации)). В некоторых вариантах осуществления эталонное количество активных аллелей триптазы представляет собой предварительно определенное значение. Количество эталонных активных аллелей триптазы в одном варианте осуществления было предварительно определяют при определенном заболевании, которым страдает пациент (например, воспалительном заболевании, опосредованным тучными клетками, таким как астма). В некоторых вариантах осуществления количество активных аллелей триптазы определяют по общему распределению значений при исследуемом определенном заболевании или в данной популяции. В некоторых вариантах осуществления эталонное количество активных аллелей триптазы представляет собой целое число в диапазоне от 0 до 4 (например, 0, 1, 2, 3 или 4). В конкретных вариантах осуществления эталонное количество активных аллелей триптазы равно 3.
Термины «уровень», «уровень экспрессии» или «экспрессионный уровень» используются взаимозаменяемо и, как правило, относятся к количеству полинукпеотида, или аминокислотного продукта, или белка в биологическом образце. «Экспрессия», как правило, относится к процессу, посредством которого кодированная генами информация преобразуется в структуры, присутствующие и функционирующие в клетке. Следовательно, согласно изобретению «экспрессия» гена может относиться к транскрипции в полинукпеотид, трансляции в белок или даже к посттрансляционной модификации белка. Фрагменты транскрибированного полинуклеотида, транслированного белка или посттрансляционно модифицированного белка также следует рассматривать как экспрессированные, независимо от того, происходят ли они от транскрипта, полученного путем альтернативного сплайсинга или деградированного транскрипта, или от посттрансляционного процессинга белка, например, путем протеолиза. «Экспрессированные гены» включают те, которые транскрибируются в полинуклеотид в виде мРНК и затем транслируются в белок, а также те, которые транскрибируются в РНК, но не транслируются в белок (например, переносят и рибосомные РНК).
В определенных вариантах осуществления термин «эталонный уровень» в данном документе относится к предварительно определенному значению. Специалист в данной области техники поймет, что эталонный уровень заранее определен и установлен так, чтобы соответствовать требованиям, например, в отношении специфичности и/или чувствительности. Эти требования могут варьироваться, например, от регулирующего органа к регулирующему органу. Может быть так, например, что чувствительность или специфичность анализа, соответственно, должны быть установлены на определенные пределы, например, 80%, 90% или 95%. Эти требования также могут быть определены с точки зрения положительных или отрицательных прогностических значений. Тем не менее, основываясь на представленных в данном изобретении идеях, всегда можно будет достичь эталонного уровня, отвечающего этим требованиям. В одном варианте осуществления эталонный уровень определяют у здоровых индивидуумов. Эталонное значение в одном варианте осуществления было предварительно определяют при определенном заболевании, которым страдает пациент (например, воспалительном заболевании, опосредованным тучными клетками, таким как астма). В некоторых вариантах осуществления эталонный уровень может быть установлен на любой процент, например, от 25% до 75% от общего распределения значений при исследуемом определенном заболевании. В других вариантах осуществления эталонный уровень может быть установлен, например, на медиану, тертили, квартили или квинтили, как определено из общего распределения значений при исследуемом определенном заболевании или в данной популяции. В одном варианте осуществления эталонный уровень устанавливают равным медианному значению, как определено из общего распределения значений при исследуемом определенном заболевании. В одном варианте осуществления эталонный уровень может зависеть от пола пациента, например, у мужчин и женщин могут быть разные эталонные уровни.
В некоторых вариантах осуществления термин «на эталонном уровне» относится к уровню маркера (например, триптазы), который является таким же, как уровень, обнаруженный при помощи способов, описанных в данном документе, из эталонного образца.
В некоторых вариантах осуществления термин «увеличение» или «выше» относится к уровню, равному эталонному уровню, или к общему увеличению на 5%, 10%, 20%, 25%, 30%, 40%, 50%, 60%. 70%, 80%, 85%, 90%, 95%, 100% или более уровня маркера (например, триптазы), обнаруженного при помощи способов, описанных в данном документе, по сравнению с уровнем из эталонного образца.
В определенных вариантах осуществления термин «уменьшение» или «ниже» в данном документе относится к уровню ниже эталонного уровня или к общему снижению на 5%, 10%, 20%, 25%, 30%, 40%, 50%, 60%, 70%, 80%, 85%, 90%, 95%, 96%, 97%, 98%, 99% или более уровня маркера (например, триптазы), обнаруженного при помощи способов, описанных в данном документе, по сравнению с уровнем из эталонного образца.
«Нарушение» или «заболевание» представляет собой любое патологическое состояние, для которого было бы полезно лечение или диагностика способом согласно изобретению. Данный термин охватывает хронические и острые расстройства или заболевания, включая те патологические состояния, которые увеличивают предрасположенность млекопитающего к рассматриваемому расстройству. Примеры заболеваний, подлежащих лечению, включают воспалительные заболевания, опосредованные тучными клетками, такие как астма.
«Воспалительное заболевание, опосредованное тучными клетками» относится к заболеваниям или расстройствам, которые по меньшей мере частично опосредованы тучными клетками, таким как астма (например, аллергическая астма), крапивница (например, хроническая спонтанная крапивница (CSU) или хроническая идиопатическая крапивница (CIU)), экзема, зуд, аллергия, атопическая аллергия, анафилаксия, анафилактический шок, аллергический бронхолегочный аспергиллез, аллергический ринит, аллергический конъюнктивит, а также аутоиммунные расстройства, включая ревматоидный артрит, ювенильный ревматоидный артрит, псориатический артрит, панкреатит, псориаз, бляшковидный псориаз, каплевидный псориаз, инверсный псориаз, пустулезный псориаз, эритродермический псориаз, паранеопластические аутоиммунные заболевания, аутоиммунный гепатит, буллезный пемфигоид, миастения гравис, воспалительное заболевание кишечника, болезнь Крона, язвенный колит, целиакия, тиреоидит (например, болезнь Грейвса), синдром Шегрена, болезнь Гийена-Барре, феномен Рейно, болезнь Аддисона, заболевания печени (например, первичный билиарный цирроз, первичный склерозирующий холангит, неалкогольная жировая болезнь печени и неалкогольный стеатогепатит) и диабет (например, диабет I типа).
В некоторых вариантах осуществления астма представляет собой хроническую персистирующую тяжелую астму с серьезными явлениями ухудшения симптомов (приступы или обострения), которые могут быть опасными для жизни. В некоторых вариантах осуществления астма представляет собой атопическую (также известную как аллергическую) астму, неаллергическую астму (например, часто вызываемую респираторной вирусной инфекцией (например, гриппом, парагриппом, риновирусом, человеческим метапнеемовирусом и респираторным синцитиальным вирусом) или вдыхаемым раздражителем (например, загрязнителями воздуха, смогом, частицами дизельного топлива, летучими химическими веществами и газами в помещении или на улице, или даже холодным сухим воздухом).
В некоторых вариантах осуществления астма является эпизодической или вызванной физической нагрузкой астмой из-за острого или хронического первичного или вторичного воздействия «дыма» (как правило, сигарет, сигар или трубок), вдыхания или «парения» (табака, марихуаны или других подобных веществ), или астмой, вызванной недавним приемом аспирина или родственных нестероидных противовоспалительных препаратов (НПВП). В некоторых вариантах осуществления астма представляет собой легкую или нелеченную кортикостероидами астму, недавно диагностированную и нелеченную астму или ранее не требующую хронического применения ингаляционных местных или системных стероидов для контроля симптомов (кашля, стерторозного дыхания, диспноэ/одышки или боли в груди). В некоторых вариантах осуществления астма представляет собой хроническую, резистентную к кортикостероидам астму, рефрактерную к кортикостероидам астму, астму, неконтролируемую кортикостероидами или другими лекарственными препаратами для контроля хронической астмы.
В некоторых вариантах осуществления астма представляет собой астму от умеренной до тяжелой. В определенных вариантах осуществления астма представляет собой астму с высоким уровнем TH2. В некоторых вариантах осуществления астма представляет собой тяжелую астму. В некоторых вариантах осуществления астма представляет собой атопическую астму, аллергическую астму, неаллергическую астму (например, вследствие инфекции и/или респираторно-синцитиального вируса (РСВ)), астму, вызванную физической нагрузкой, чувствительную к аспирину/индуцированную аспирином астму, легкую астму, умеренную или тяжелую астму, нелеченную кортикостероидами астму, хроническую астму, резистентную к кортикостероидам астму, рефрактерную к кортикостероидам астму, недавно диагностированную и нелеченную астму, астму, вызванную курением, астму, неконтролируемую кортикостероидами. В некоторых вариантах осуществления астма представляет собой эозинофильную астму. В некоторых вариантах осуществления астма представляет собой аллергическую астму. В некоторых вариантах осуществления индивидуум был определен как положительный по эозинофильному воспалению (EIP). Смотрите WO 2015/061441. В некоторых вариантах осуществления астмой представляет собой астму с высоким уровнем периостина (например, при которой уровень периостина по меньшей мере любой из около 20 нг/мл, 25 нг/мл или 50 нг/мл сыворотки). В некоторых вариантах осуществления астма представляет собой астму с высоким уровнем эозинофилов (например по меньшей мере любым количеством из около 150, 200, 250, 300, 350, 400 эозинофилов/мл крови). В некоторых вариантах осуществления индивидуум был определен как отрицательный по эозинофильному воспалению (EIN). Смотрите WO 2015/061441. В некоторых вариантах осуществления астма представляет собой астму с низким уровнем периостина (например, с уровнем периостина менее чем около 20 нг/мл сыворотки). В некоторых вариантах осуществления астма представляет собой астму с низким уровнем эозинофилов (например, менее чем около 150 эозинофилов/мкл крови или менее чем около 100 эозинофилов/мкл крови).
В контексте данного документа термин «астма с высоким уровнем TH2» относится к астме, которая демонстрирует высокие уровни одного или более цитокинов, связанных с клетками TH2, например, ИЛ-13, ИЛ-4, ИЛ-9 или ИЛ-5, или которая проявляет воспаление, связанное с цитокином TH2. В некоторых вариантах осуществления термин «астма с высоким уровнем TH2» может использоваться взаимозаменяемо с астмой с высоким уровнем эозинофилов, астмой с высоким уровнем Т-хелперных лимфоцитов 2-го типа, астмой 2-го типа, или астмой, вызванной TH2. В некоторых вариантах осуществления пациент с астмой был определен как положительный по эозинофильному воспалению (EIP). См., например, публикацию международной патентной заявки № WO 2015/061441, которая полностью включена в данный документ посредством ссылки. В определенных вариантах осуществления было установлено, что индивидуум имеет повышенные уровни по меньшей мере одного из генов эозинофильного профиля по сравнению с контрольным или эталонным уровнем. Смотрите WO 2015/061441. В определенных вариантах осуществления астма с высоким TH2 представляет собой астму с высоким уровнем периостина. В некоторых вариантах осуществления у индивидуума имеется высокий уровень периостина в сыворотке. В определенных вариантах осуществления индивидуум представляет собой индивидуума восемнадцати лет и более. В определенных вариантах осуществления у индивидуума был определен повышенный уровень сывороточного периостина по сравнению с контрольным или эталонным уровнем. В некоторых вариантах осуществления контрольный или эталонный уровень представляет собой медианный уровень периостина в популяции. В определенных вариантах осуществления у индивидуума было определено 20 нг/мл или выше сывороточного периостина. В определенных вариантах осуществления у индивидуума было определено 25 нг/мл или выше сывороточного периостина. В определенных вариантах осуществления у индивидуума было определено 50 нг/мл или выше сывороточного периостина. В определенных вариантах осуществления контрольный или эталонный уровень сывороточного периостина составляет 20 нг/мл, 25 нг/мл или 50 нг/мл. В некоторых вариантах осуществления астма представляет собой астму с высоким уровнем эозинофилов. В некоторых вариантах осуществления у индивидуума был определено повышенное количество эозинофилов по сравнению с контрольным или эталонным уровнем. В некоторых вариантах осуществления контрольный или эталонный уровень представляет собой медианный уровень популяции. В определенных вариантах осуществления у индивидуума было определено 150 или выше эозинофилов/мкл крови. В определенных вариантах осуществления у индивидуума было определено 200 или выше эозинофилов/мкл крови. В определенных вариантах осуществления у индивидуума было определено 250 или выше эозинофилов/мкл крови. В определенных вариантах осуществления у индивидуума было определено 300 или выше эозинофилов/мкл крови. В определенных вариантах осуществления у индивидуума было определено 350 или выше эозинофилов/мкл крови. В определенных вариантах осуществления у индивидуума было определено 400 или выше эозинофилов/мкл крови. В определенных вариантах осуществления у индивидуума было определено 450 или выше эозинофилов/мкл крови. В определенных вариантах осуществления у индивидуума было определено 500 или выше эозинофилов/мкл крови. В определенных предпочтительных вариантах осуществления у индивидуума было определено 300 или выше эозинофилов/мкл крови. В определенных вариантах осуществления эозинофилы представляют собой эозинофилы периферической крови. В определенных вариантах осуществления эозинофилы представляют собой эозинофилы мокроты. В определенных вариантах осуществления индивидуум демонстрирует повышенный уровень FeNO (фракцию оксида азота в выдыхаемом воздухе) и/или повышенный уровень IgE. Например, в некоторых случаях индивидуум демонстрирует уровень FeNO выше около 250 частей на миллиард (част/млрд), выше около 275 част/млрд, выше около 300 част/млрд, выше около 325 част/млрд, выше около 325 част/млрд или выше около 350 част/млрд. В некоторых случаях у индивидуума уровень IgE выше 50 МЕ/мл. В качестве обзора астмы с высоким уровнем TH2 смотри, например, Fajt et al. J. Allergy Clin. Immunol. 135(2):299-310, 2015.
В контексте данного документа термин «астма с низким уровнем TH2» или «астма с невысоким уровнем TH2» относится к астме, которая демонстрирует низкие уровни одного или более связанных с клетками TH2 цитокинов, например, ИЛ-13, ИЛ-4, ИЛ-9, или ИЛ-5, или демонстрирует воспаление, которое не связано с цитокином TH2. В некоторых вариантах осуществления термин «астма с низким уровнем TH2» может использоваться взаимозаменяемо с астмой с низким уровнем эозинофилов. В некоторых вариантах осуществления пациент с астмой был определен как отрицательный по эозинофильному воспалению (EIN). Смотри, например, WO 2015/061441. В определенных вариантах осуществления астма с низким TH2 представляет собой астму с низким уровнем периостина. В определенных вариантах осуществления индивидуум представляет собой индивидуума восемнадцати лет и более. В определенных вариантах осуществления у индивидуума был определен сниженный уровень сывороточного периостина по сравнению с контрольным или эталонным уровнем. В некоторых вариантах осуществления контрольный или эталонный уровень представляет собой медианный уровень периостина в популяции. В определенных вариантах осуществления у индивидуума было определено менее 20 нг/мл сывороточного периостина. В некоторых вариантах осуществления астма представляет собой астму с низким уровнем эозинофилов. В некоторых вариантах осуществления у индивидуума был определено сниженное количество эозинофилов по сравнению с контрольным или эталонным уровнем. В некоторых вариантах осуществления контрольный или эталонный уровень представляет собой медианный уровень популяции. В определенных вариантах осуществления у индивидуума было определено менее 150 эозинофилов/мкп крови. В определенных вариантах осуществления у индивидуума было определено менее 100 эозинофилов/мкп крови. В определенных вариантах осуществления у индивидуума было определено менее 300 эозинофилов/мкп крови.
В контексте данного документа термин «биомаркер 2-го типа» относится к биомаркеру, который связан с воспалением TH2. Неограничивающие примеры биомаркеров 2-го типа включают цитокин, связанный с клеткой TH2 (например, ИЛ-13, ИЛ-4, ИЛ-9 или ИЛ-5), периостин, количество эозинофилов, профиль эозинофилов, FeNO или IgE.
Термин «введение» означает введение композиции пациенту (например, пациенту, страдающему воспалительным заболеванием, опосредованным тучными клетками, таким как астма). Композиции, используемые в описанных в данном документе способах, могут вводиться, например, парентерально, внутрибрюшинно, внутримышечно, внутривенно, внутрикожно, чрескожно, внутриартериально, внутриочагово, интракраниально, внутрисуставно, внутрь простаты, внутриплеврально, интратрахеально, интратекально, интраназально, интравагинально, ректально, местно, внутриопухолево, подкожно, субконъюнктивально, интравезикулярно, мукозально, интраперикардиально, внутрипуповинно, интраокулярно, интрабитально, перорально, местно, трансдермально, интравитреально, периокулярно, в конъюнктивальную полость, в субтеноновое пространство, внутрикамерно, субретинально, ретробульбарно, внутриканально, путем ингаляции, инъекции, имплантации, инфузии, непрерывной инфузии, локализованной перфузии непосредственно в целевых клетках, при помощи катетера, путем лаважа, в кремах или в липидных композициях. Парентеральное введение включает внутримышечное, внутривенное, внутриартериальное, внутрибрюшинное или подкожное введение. Композиции, используемые в способах, описанных в данном документе, можно также вводить системно или локально. Способ введения может изменяться в зависимости от различных факторов (например, соединения или композиции для введения, степени тяжести патологического состояния, заболевания или нарушения, подлежащего лечению).
Термины «терапевтический агент» или «агент» относятся к любому агенту, который используется для лечения заболевания, например, воспалительного заболевания, опосредованного тучными клетками, например, астмы. Терапевтический агент может представлять собой, например, полипептид(ы) (например, антитело, иммуноадгезин или пептитело), аптамер, небольшую молекулу, которая может связываться с белком, или молекулу нуклеиновой кислоты, которая может связываться с молекулой нуклеиновой кислоты, кодирующей мишень (например, киРНК) и тому подобное.
Термины «ингибиторы» и «антагонисты», используемые в данном документе взаимозаменяемо, относятся к соединениям или агентам, которые ингибируют или уменьшают биологическую активность молекулы, с которой они связываются. Ингибиторы включают антитела, синтетические пептиды или пептиды с нативной последовательностью, иммуноадгезины и низкомолекулярные ингибиторы, которые связываются, например, стриптазой или IgE. В некоторых вариантах осуществления ингибитор (например, антитело) ингибирует активность антигена на по меньшей мере 10% в присутствии ингибитора по сравнению с активностью в отсутствие ингибитора. В некоторых вариантах осуществления ингибитор ингибирует активность на по меньшей мере 20%, по меньшей мере 30%, по меньшей мере 40%, по меньшей мере 50%, по меньшей мере 60%, по меньшей мере 70%, по меньшей мере 80%, по меньшей мере 90%, или 100%.
В контексте данного документа термин «антагонист триптазы» относится к соединениям или агентам, которые ингибируют или снижают биологическую активность триптазы (например, альфа-триптазы (например, альфа-I-триптазы) или бета-триптазы (например, бета-I-триптазы, бета-II-триптазы, или бета-III-триптаза)). В некоторых вариантах осуществления антагонист триптазы представляет собой антитело против триптазы или низкомолекулярный ингибитор.
Термины «антитело против триптазы», и «антитело, которое связывается с триптазой», и «антитело, которое специфически связывает триптазу» относятся к антителу, которое способно связывать триптазу с достаточной аффиностью, чтобы антитело можно было применять в качестве диагностического и/или терапевтического агента для нацеливания на триптазу. В одном варианте осуществления степень связывания антитела против триптазы с неродственным белком, не являющимся триптазой, составляет менее чем около 10% от связывания антитела с триптазой, как измерено, например, с помощью радиоиммунологического анализа (РИА). В определенных вариантах осуществления антитело, которое связывается стриптазой, имеет константу диссоциации (Kd) ≤ 1 мкМ, ≤ 100 нМ, ≤ 10 нМ, ≤ 1 нМ, ≤ 0,1 нМ, ≤ 0,01 нМ, или ≤ 0,001 нМ (например, 10-8М или менее, например, от 10-8М до 10-13М, например, от 10-9М до 10-13М). В определенных вариантах осуществления антитело против триптазы связывается с эпитопом триптазы, который является консервативным среди триптаз разных видов. Иллюстративные антитела против триптазы описаны в данном документе и в предварительной заявке на патент США №62/457222 и публикации международной патентной заявки № WO 2018/148585, которые включены в данный документ посредством ссылки во всей своей полноте.
Термин «FcεRI» относится к любому нативному FcεRI (также известному в данной области техники как высокоаффинный рецептор к IgE или FCER1) из любого источника, относящегося к позвоночным, включая млекопитающих, таких как приматы (например, люди) и грызуны (например, мыши и крысы), если не указано другое. FcεRI представляет собой тетрамерный рецепторный комплекс, который связывает Fc-белок тяжелой цепи ε IgE. FcεRI состоит из одной α-цепи, одной β-цепи и двух γ-цепей. Аминокислотная последовательность иллюстративного человеческого полипептида FcεRIα приведена под номером доступа UniProt Р12319. Аминокислотная последовательность иллюстративного человеческого полипептида FcεRIβ приведена под номером доступа UniProt Q01362. Аминокислотная последовательность иллюстративного человеческого полипептида FcεRIγ приведена под номером доступа UniProt Р30273.
Термин «FcεRII» относится к любому природному FcεRII (также известному в данной области техники как CD23, FCER2 или низкоаффинный рецептор к IgE) из любого источника, относящегося к позвоночным, включая млекопитающих, таких как приматы (например, люди) и грызуны (например, мыши и крысы), если не указано иное. Термин охватывает «полноразмерный» непроцессированный FcεRII, а также любую форму FcεRII, возникающую в результате процессинга в клетке. Термин также охватывает природные варианты FcεRII, например, сплайс-варианты или аллельные варианты. Аминокислотная последовательность иллюстративного человеческого полипептида FcεRII приведена под номером доступа UniProt Р06734.
В контексте данного документа термин «антагонист Fc-эпсилон-рецептора (FcεR)» относится к соединениям или агентам, которые ингибируют или уменьшают биологическую активность FcεR (например, FcεRI или FcεRII). Антагонист FcεR может ингибировать активность FcεR или нуклеиновой кислоты (например, гена или мРНК, транскрибированной с гена) или полипептида, который участвует в сигнальной трансдукции FcεR. Например, в некоторых вариантах осуществления антагонист FcεR ингибирует тирозин-протеинкиназу Lyn (Lyn), тирозинкиназу Брутона (ВТК), тирозин-протеинкиназу Fyn (Fyn), связанную с селезенкой тирозинкиназу (Syk), линкер для активации Т-клеток (LAT), белок-2, связанный с рецептором фактора роста (Grb2), белок «son of sevenless» (Sos), Ras, Raf-1, митоген-активируемую протеинкиназу 1 (MEK), митоген-активируемую протеинкиназу 1 (ERK), цитозольную фосфолипазу А2 (cPLA2), арахидонат-5-липоксигеназу (5-LO), арахидонат-5-липоксигеназа-активирующий белок (FLAP), фактор обмена гуаниновых нуклеотидов VAV (Vav), Rac, киназу-3 митоген-активируемой протеинкиназы, киназу-7 митоген-активируемой протеинкиназы, р38 МАР-киназу (р38), c-Jun-N-концевую киназу (JNK), белок-2, ассоциированный с белком-2, который связан с рецептором фактора роста (Gab2), фосфатидилинозитол-4,5-бисфосфат-3-киназу (PI3K), фосфолипазу С гамма (PLCγ), протеинкиназу С (PKC), 3-фосфоинозитид-зависимую протеинкиназу 1 (PDK1), RAC серин/треонин-протеинкиназу (АКТ), гистамин, гепарин, интерлейкин (ИЛ) -3, ИЛ-4, ИЛ-13, ИЛ-5, гранулоцитарно-макрофагальный колониестимулирующий фактор (ГМ-КСФ), фактор некроза опухоли-альфа (ФНО-α), лейкотриены (например, LTC4, LTD4 и LTE4) и простагландины (например, PDG2). В некоторых вариантах осуществления антагонист FcεR представляет собой ингибитор ВТК, например, GDC-0853, акалабрутиниб, GS-4059, спебрутиниб, BGB-3111 или НМ71224.
«В-клетка» представляет собой лимфоцит, который созревает в костном мозге и включает наивные В-клетки, В-клетки памяти или эффекторные В-клетки (плазматические клетки). В данном документе В-клетка может быть нормальной или незлокачественной.
Термин «антитело, истощающего IgE+ В-клетки» относится к антителу, которое может уменьшать количество IgE+ В-клеток у субъекта и/или препятствовать одной или более функциям IgE+ В-клеток. «IgE+ В-клетка» относится к В-клетке, которая экспрессирует мембранную форму В-клеточного рецептора к IgE. В некоторых вариантах осуществления IgE+ В-клетка представляет собой переключенную на синтез IgE В-клетку или В-клетку памяти. Человеческий мембранный IgE содержит внеклеточный сегмент из 52 аминокислот, называемый прайм-сегментом М1 (также известный как М1', me.1 или CemX), который не экспрессируется в секретируемых антителах к IgE. В некоторых вариантах осуществления антитело, истощающее IgE+ В-клетки, представляет собой антитело против М1' (например, килизумаб). В некоторых вариантах осуществления антитело против М1' представляет собой любое антитело против M1', описанное в публикации международной патентной заявки №WO 2008/116149.
«Тучная клетка» представляет собой тип гранулоцитарной иммунной клетки. Тучные клетки обычно присутствуют в слизистых и эпителиальных тканях по всему организму. Тучные клетки содержат цитоплазматические гранулы, которые хранят медиаторы воспаления, в том числе триптазу (особенно бета-триптазу), гистамин, гепарин и цитокины. Тучные клетки могут быть активированы перекрестным связыванием антиген/IgE/FcεRI, которое может привести к дегрануляции и высвобождению медиаторов воспаления. Тучная клетка может быть тучной клеткой слизистой оболочки или тучной клеткой соединительной ткани. Смотри, например, Krystel-Whittemore et al. Front. Immunol. 6:620, 2015.
«Базофил» представляет собой тип гранулоцитарной иммунной клетки. Базофилы, как правило, присутствуют в периферической крови. Базофилы могут быть активированы посредством перекрестного сшивания антиген/IgE/FcεRI для высвобождения молекул, таких как гистамины, триптаза (особенно альфа-триптаза), лейкотриены и цитокины. Смотри, например, Siracusa et al. J. Allergy Clin. Immunol. 132(4)789-801, 2013.
Термин «антитело, истощающее тучные клетки или базофилы» относится к антителу, которое может снижать количество или биологическую активность тучных клеток или базофилов у субъекта и/или препятствовать одной или более функциям тучных клеток или базофилов. В некоторых вариантах осуществления антитело представляет собой антитело, истощающее тучные клетки. В других вариантах осуществления антитело представляет собой антитело, истощающее базофилы. В еще других вариантах осуществления антитело истощает тучные клетки и базофилы. В некоторых вариантах осуществления антитело, истощающее тучные клетки или базофилы, представляет собой антитело против Siglec8.
Термин «активируемый протеазой рецептор 2 (PAR2)» относится к любому нативному PAR2 (также известному в данной области техники как F2R-подобный рецептор-1 трипсина (F2RL1) или связанный с G-белком рецептор 11 (GPR11)) из любого источника, относящегося к позвоночным, включая млекопитающих, таких как приматы (например, люди) и грызуны (например, мыши и крысы), если не указано иное. Термин охватывает «полноразмерный» непроцессированный PAR2, а также любую форму PAR2, возникающую в результате процессинга в клетке. Термин также охватывает природные PAR2, например, сплайс-варианты или аллельные варианты. Последовательность нуклеиновой кислоты иллюстративного человеческого PAR2 приведена в RefSeq под номером доступа NM_005252. Аминокислотная последовательность иллюстративного белка, кодируемого человеческим PAR2, приведена в UniProt под номером доступа Р55085.
Термин «антагонист PAR2» относится к молекуле, которая уменьшает, блокирует, ингибирует, отменяет или препятствует биологической активности или сигнальной трансдукции PAR2. Как правило, PAR2 активируется путем протеолитического расщепления его N-конца, который демаскирует связанный пептидный лиганд, который связывает и активирует трансмембранный рецепторный домен. Иллюстративные антагонисты PAR2 включают низкомолекулярные ингибиторы (например, K-12940, K-14585, GB83, GB88, AZ3451 и AZ8838), растворимые рецепторы, киРНК и антитела против PAR2 (например, МАВ3949 и Fab3949). См., например, Cheng et al. Nature 545:112-115, 2017; Kanke et al. Br. J. Pharmacol. 158(1):361-371, 2009; и Lohman et al. FASEB J. 26(7):2877-2887, 2012.
Термин «антагонист IgE» относится к молекуле, которая уменьшает, блокирует, ингибирует, отменяет или препятствует биологической активности IgE. Такие антагонисты включают, но не ограничиваются ими, антитела против IgE, рецепторы IgE, антитела против рецепторов IgE, варианты антител к IgE, лиганды для рецепторов IgE и их фрагменты. В некоторых вариантах осуществления антагонист IgE способен нарушать или блокировать взаимодействие между IgE (например, человеческим IgE) и рецептором FcεRI с высокой аффинностью, например, на тучных клетках или базофилах.
«Антитело против IgE» включает любое антитело, которое специфически связывается с IgE таким образом, чтобы не вызывать перекрестное сшивание, когда IgE связан с рецептором с высокой аффинностью на тучных клетках и базофилах. Иллюстративные антитела против IgE включают rhuMabE25 (Е25, омализумаб (XOLAIR®)), Е26, Е27, а также CGP-5101 (Hu-901), антитело к НА (гемагглютинин), лигелизумаб и тализумаб. Аминокислотные последовательности вариабельных доменов тяжелой и легкой цепей гуманизированных антител против IgE Е25, Е26 и Е27 описаны, например, в патенте США №6172213 и WO 99/01556. Антитело CGP-5101 (Hu-901) описано в Corne et al. J. Clin. Invest. 99(5): 879-887, 1997; WO 92/17207; и №№депонирования в ATCC BRL-10706, BRL-11130, BRL-11131, BRL-11132 и BRL-11133. Антитело к НА описано в US №60/444229, WO 2004/070011, и WO 2004/070010.
В контексте данного документа термин «интерлейкин-33 (ИЛ-33)» относится к любому нативному ИЛ-33 из любого источника, относящегося к позвоночным, включая млекопитающих, таких как приматы (например, люди) и грызуны (например, мыши и крысы), если не указано иное. ИЛ-33 также упоминается в данной области техники как ядерный фактор наружных эндотелиальных венул (NF-HEV; см., например, Baekkevold et al. Am. J. Pathol. 163(1): 69-79, 2003), DVS27, C9orf26, и член 11 семейства интерлейкина-1 (IL-1F11). Термин охватывает «полноразмерный» непроцессированный ИЛ-33, а также любую форму ИЛ-33, возникающую в результате процессинга в клетке. Человеческий полноразмерный непроцессированный ИЛ-33 содержит 270 аминокислот (АК) и может также упоминаться как ИЛ-331-270. Процессированные формы человеческого ИЛ-33 включают, например, ИЛ-3395-270, ИЛ-3399-270, ИЛ-33109-270, ИЛ-33112-270, ИЛ-331-178, и ИЛ-33179-270 (Lefrangais et al. Proc. Natl. Acad. Sci. 109(5): 1673-1678, 2012 и Martin, Semin. Immunol. 25: 449-457, 2013). В некоторых вариантах осуществления процессированные формы человеческого ИЛ-33, например, ИЛ-3395-270, ИЛ-3399-270, ИЛ-33109-270, или другие формы, процессированные протеазами, такими как кальпаин, протеиназа-3, нейтрофильная эластаза и катепсин G, может иметь повышенную биологическую активность по сравнению с полноразмерным ИЛ-33. Термин также охватывает природные варианты ИЛ-33, например, сплайс-варианты (например, конститутивно активный сплайс-вариант spIL-33, в котором отсутствует экзон 3, Hong et al. J. Biol. Chem. 286(22): 20078-20086, 2011) или аллельные варианты. ИЛ-33 может присутствовать в клетке (например, в ядре) или в форме секретируемого цитокина. Полноразмерный белок ИЛ-33 содержит ДНК-связывающий мотив спираль-поворот-спираль, включая последовательность ядерной локализации (АК 1-75 человеческого ИЛ-33), который содержит хроматин-связывающий мотив (АК 40-58 человеческого ИЛ-33). Формы ИЛ-33, которые процессируются и секретируются, лишены этих N-концевых мотивов. Аминокислотная последовательность иллюстративного человеческого ИЛ-33 может быть найдена, например, под номером доступа UniProt 095760.
Под «осью ИЛ-33» понимают нуклеиновую кислоту (например, ген или мРНК, транскрибируемую с гена) или полипептид, который участвует в сигнальной трансдукции ИЛ-33. Например, ось ИЛ-33 может включать лиганд ИЛ-33, рецептор (например, ST2 и/или ИЛ-IRAcP), адаптерные молекулы (например, MyD88) или белки, которые связываются с рецепторными молекулами и/или адаптерными молекулами (например, киназы, такие как киназа-1, связанная с рецептором интерлейкина-1 (IRAK1), и киназа-4, связанная с рецептором интерлейкина-1 (IRAK4), или лигазы убиквитина Е3, такие как фактор-6, связанный с рецептором ФНО (TRAF6)).
«Антагонист, связывающий ось ИЛ-33» относится к молекуле, которая ингибирует взаимодействие партнера по связыванию оси ИЛ-33 с одним или более его партнерами по связыванию. В контексте данного документа антагонист, связывающий ось ИЛ-33, включает антагонисты, связывающие ИЛ-33, антагонисты, связывающие ST2, и антагонисты, связывающие ИЛ-IRAcP. Иллюстративные антагонисты, связывающие ось ИЛ-33, включают антитела против ИЛ-33 и их антигенсвязывающие фрагменты (например, антитела против ИЛ-33, такие как ANB-020 (AnaptysBio Inc.) или любое из антител, описанных в ЕР 1725261, US 8187596, WO 2011/031600, WO 2014/164959, WO 2015/099175, WO 2015/106080 или WO 2016/077381, каждый из которых включен в данный документ посредством ссылки в полном объеме); полипептиды, которые связывают ИЛ-33 и/или его рецептор (ST2 и/или ИЛ-IRAcP) и блокируют взаимодействие лиганд-рецептор (например, белки ST2-Fc; иммуноадгезины, пептиды и растворимые ST2 или их производные); антитела против рецептора ИЛ-33 (например, антитела против ST2, например, AMG-282 (Amgen) или STLM15 (Janssen) или любое из антител против ST2, описанных в WO 2013/173761 или WO 2013/165894, каждый из которых включен в данный документ посредством ссылки во всей своей полноте, или белки ST2-Fc, такие как белки, описанные в WO 2013/173761; WO 2013/165894 или WO 2014/152195, каждый из которых включен в данный документ посредством ссылки во всей своей полноте); и антагонисты рецептора ИЛ-33, такие как низкомолекулярные ингибиторы, аптамеры, которые связывают ИЛ-33, и нуклеиновые кислоты, которые гибридизуются в жестких условиях с последовательностями нуклеиновых кислот оси ИЛ-33 (например, короткие интерферирующие РНК (киРНК) или РНК коротких палиндромных повторов, регулярно расположенных группами, (CRISPR-PHK или сгРНК)).
Термин «антагонист, связывающий ST2» относится к молекуле, которая ингибирует взаимодействие ST2 с ИЛ-33, ИЛ-IRAcP и/или второй молекулой ST2. Антагонист, связывающий ST2, может представлять собой белок, такой как «белок ST2-Fc», который включает домен, связывающий ИЛ-33, (например, весь или часть белка ST2 или ИЛ-IRAcP) и мультимеризирующий домен (например, Fc-часть иммуноглобулина, например, домен Fc IgG, выбранный из изотипов IgG1, IgG2, IgG3 и IgG4, а также любого аллотипа в каждой группе изотипов), которые присоединены друг к другу прямо или косвенно через линкер (например, линкер серин-глицин (SG), линкер глицин-глицин (GG) или их вариант (например, линкер SGG, GGS, SGS или GSG)) и включает, но не ограничивается ими, белки ST2-Fc и их варианты, описанные в WO 2013/173761, WO 2013/165894 и WO 2014/152195, каждый из которых включен в данный документ посредством ссылки во всей своей полноте.
«Ингибитор пути TH2» или «ингибитор TH2» представляет собой агент, который ингибирует путь TH2. Примеры ингибитора пути TH2 включают ингибиторы активности любой из мишеней, выбранных из индуцируемой интерлейкином-2 Т-клеточной киназы (ITK), тирозинкиназы Брутона (ВТК), Янус-киназу 1 (JAK1) (например, руксолитиниба, тофацитиниба, оклацитиниба, барицитиниба, филготиниба, гандотиниба, лестауртиниба, момелотиниба, пакринитиба, упадацитиниба, пефитиниба и федратиниба), GATA-связывающего белка 3 (GATA3), ИЛ-9 (например, MEDI-528), ИЛ-5 (например, меполизумаба, CAS №196078-29-2; резилизумаба), ИЛ-13 (например, IMA-026, IMA-638 (также называемого анрукинзумабом, INN №910649-32-0; QAX-576; ловушкой для ИЛ-4/ИЛ-13), тралокинумаба (также называемого САТ-354, CAS №1044515-88-9); AER-001, АВТ-308 (также называемого гуманизированным антителом 13С5.5)), ИЛ-4 (например, AER-001, ловушки для ИЛ-4/ИЛ-13), OX40L, TSLP, ИЛ-25, ИЛ-33 и IgE (например, XOLAIR®, QGE-031 и MEDI-4212); и рецепторов, например: рецептора ИЛ-9, рецептора ИЛ-5 (например, MEDI-563 (бенилизумаба, CAS №1044511-01-4)), альфа рецептора ИЛ-4 (например, AMG-317, AIR-645), альфа-1 рецептора ИЛ-13 (например, R-1671) и альфа-2 рецептора ИЛ-13, ОХ40, TSLP-R, ИЛ-7R-альфа (корецептора для TSLP), ИЛ-17RB (рецептора для ИЛ-25), ST2 (рецептора для ИЛ-33), CCR3, CCR4, CRTH2 (например, AMG-853, АР768, АР-761, MLN6095, АСТ129968), FcεRI, FcεRII/CD23 (рецепторы для IgE), Flap (например, GSK2190915), Syk киназы (R-343, PF3526299); CCR4 (AMG-761), TLR9 (QAX-935) и мультицитокинового ингибитора CCR3, ИЛ-5, ИЛ-3 и ГМ-КСФ (например, TPI ASM8). Примеры ингибиторов вышеупомянутых мишеней раскрыты, например, в WO 2008/086395; WO 2006/085938; US 7615213; US 7501121; WO 2006/085938; WO 2007/080174; US 7807788; WO 2005/007699; WO 2007/036745; WO 2009/009775; WO 2007/082068; WO 2010/073119; WO 2007/045477; WO 2008/134724; US 2009/0047277; и WO 2008/127271.
Термины «пациент» или «субъект» относятся к любому отдельному животному, более конкретно млекопитающему (включая таких животных, отличных от человека, как, например, кошки, собаки, лошади, кролики, коровы, свиньи, овцы, животные зоопарка и приматы, отличные от человека), для которых требуется диагностика или лечение. Еще более конкретно, в данном документ пациент представляет собой человека.
Термин «малая молекула» относится к органической молекуле, имеющей молекулярную массу от 50 дальтон до 2500 дальтон.
Термин «эффективное количество» относится к количеству лекарственного средства или терапевтического агента (например, антагониста триптазы, антагониста FcεR, антитела, истощающего IgE+ В-клетки, антитела, истощающего тучные клетки или базофилы, антагониста PAR2, антагониста IgE, или их комбинации (например, антагониста триптазы и антагониста IgE)), эффективному для лечения заболевания или расстройства (например, воспалительного заболевания, опосредованного тучными клетками, например, астмы) у субъекта или пациента, такого как млекопитающее, например, человек.
В контексте данного документа термин «терапия» или «лечение» относится к клиническому вмешательству при попытке изменить естественное течение заболевания у индивидуума или клетки, подвергаемых лечению, и может осуществляться для профилактики или в процессе клинического проявления патологии. Желательные эффекты лечения включают предотвращение возникновения или рецидива заболевания, ослабление симптомов, уменьшение любых прямых или косвенных патологических последствий заболевания, уменьшение скорости прогрессирования заболевания, улучшение или смягчение болезненного состояния, а также ремиссию или улучшение прогноза. К числу тех, кто нуждается в лечении, могут относиться те, кто уже страдает этим расстройством, а также те, кто подвержен риску заболевания, или те, у кого это заболевание необходимо предотвратить. Пациент может успешно «лечиться» от астмы, если, например, после получения астматической терапии у пациента наблюдается заметное и/или измеримое уменьшение или отсутствие одного или более из следующих факторов: рецидивирующего синдрома бронхиальной обструкции, кашля, затрудненного дыхания, сдавленности в груди, симптомов, которые возникают или ухудшаются ночью, симптомов, которые вызываются холодным воздухом, физическими упражнениями или воздействием аллергенов.
«Ответ» пациента или «восприимчивость» пациента на лечение или терапию, например, терапию, включающую антагонист триптазы, антагонист FcεR, антитело, истощающее IgE+ В-клетки, антитело, истощающее тучные клетки или базофилы, антагонист PAR2, антагонист IgE или их комбинацию (например, антагонист триптазы и антагонист IgE), относится к клиническому или терапевтическому эффекту, получаемому пациентом с астмой или риском ее развития от или в результате лечения. Специалист в данной области техники легко может определить, восприимчив ли пациент. Например, пациент, страдающий астмой, который отвечает на терапию, включающую антагонист триптазы, антагонист FcεR, антитело, истощающее IgE+ В-клеток, антитело, истощающее тучных клеток или базофилов, антагонист PAR2, антагонист IgE или их комбинацию (например, антагониста триптазы и антагониста IgE), могут демонстрировать наблюдаемое и/или измеримое уменьшение в или отсутствие одного или более симптомов астмы, например, рецидивирующего синдрома бронхиальной обструкции, кашля, затрудненного дыхания, сдавленности в груди, симптомов, которые возникают или ухудшаются ночью, симптомов, которые вызываются холодным воздухом, физическими упражнениями или воздействием аллергенов. В некоторых вариантах осуществления ответ может представлять собой улучшение функции легких, например, улучшение в FEV1%.
Термины «образец» и «биологический образец» используются взаимозаменяемо для обозначения любого биологического образца, полученного от индивидуума, включая жидкости организма, ткани тела (например, образцы легких), назальные образцы (включая назальные мазки или полипы носовой полости), мокроту, назосорбционные образцы, бронхосорбционные образцы, клетки или другие источники. Жидкости организма включают, например, жидкость бронхиального лаважа (BAL), жидкость слизистой оболочки (MLF; включая, например, назальную MLF или бронхиальную MLF), лимфу, сыворотку, цельную свежую кровь, замороженную цельную кровь, плазму (включая свежую или замороженную), сыворотку (включая свежую или замороженную), мононуклеарные клетки периферической крови, мочу, слюну, сперму, синовиальную жидкость и спинномозговую жидкость. В данной области техники хорошо известны способы получения биопсии тканей и биологических жидкостей у млекопитающих.
Термин «антитело» применяется в данном документе в самом широком смысле и включает различные структуры антител, включая, но не ограничиваясь этим, моноклональные антитела, поликлональные антитела, мультиспецифические антитела (например, биспецифические антитела) и фрагменты антител, до тех пор, пока они демонстрируют необходимую антигенсвязывающую активность.
Антитело «с созревшей аффинностью» представляет собой антитело с одним или более изменениями в одной или более HVR и/или каркасных областях, которые приводят к улучшению аффинности антитела к антигену по сравнению с исходным антителом, которое не обладает этим изменением(ями). Предпочтительные антитела с созревшей аффинностью будут иметь наномолярную или даже пикомолярную аффинность к целевому антигену. Антитела с созревшей аффинностью получают способами, известными в данной области техники. Например, в Marks et al. Bio/Technology 10:779-783, 1992 описано созревание аффинности путем перестановки доменов VH и VL. Случайный мутагенез HVR и/или каркасные остатки описаны в: Barbas et al. Proc. Natl. Acad. Sci. USA 91:3809-3813, 1994; Schieret al. Gene 169:147-155, 1995; Yelton et al. J. Immunol. 155:1994-2004, 1995; Jackson et al. J. Immunol. 154(7):3310-3319, 1995; и Hawkins et al. J. Mol. Biol. 226:889-896, 1992.
В контексте данного документа «акцепторная каркасная область человека» представляет собой каркасную область, которая содержит аминокислотную последовательность каркасной области вариабельного домена легкой цепи (VL) или каркасной области вариабельного домена тяжелой цепи (VH), которая получена из каркасной области иммуноглобулина человека или консенсусной каркасной области человека, как определено ниже. Акцепторная каркасная область человека, «полученная из» каркасной области иммуноглобулина человека или консенсусной каркасной области человека, может содержать такую же самую аминокислотную последовательность, как и указанная, или может содержать изменения в аминокислотной последовательности. В некоторых вариантах осуществления количество аминокислотных изменений составляет 10 или менее, 9 или менее, 8 или менее, 7 или менее, 6 или менее, 5 или менее, 4 или менее, 3 или менее, или 2 или менее. В некоторых вариантах осуществления последовательность акцепторной человеческой каркасной области VL идентична последовательности каркасной области VL иммуноглобулина человека или последовательности консенсусной каркасной области человека.
Термин «аффинность» относится к силе суммарных общих нековалентных взаимодействий между одиночным сайтом связывания молекулы (например, антитела) и ее партнера по связыванию (например, антигена). Если не указано иное, используемый в данном документе термин «аффинность связывания» относится к действительной аффинности связывания, которая отражает взаимодействие в соотношении 1:1 между членами связывающей пары (например, антителом и антигеном). Аффинность молекулы X к ее партнеру Y обычно может быть представлена константой диссоциации (Kd). Аффинность можно измерить с помощью общепринятых в данной области техники способов, в том числе тех, которые описаны в данном документе. Конкретные иллюстративные и типичные варианты осуществления изобретения, относящиеся к измерению аффинности связывания, описаны далее.
«Антитело, которое связывается с тем же эпитопом», что и эталонное антитело, относится к антителу, которое связывается с перекрывающимся набором аминокислотных остатков антигена по сравнению с эталонным антителом или блокирует связывание эталонного антитела с его антигеном в конкурентном анализе на 50% или более, 60% или более, 70% или более, 80% или более или 90% или более. В некоторых вариантах осуществления набор аминокислотных остатков, с которыми связывается антитело, может полностью перекрываться или частично перекрываться с набором аминокислотных остатков, с которыми связывается эталонное антитело. В некоторых вариантах осуществления антитело, которое связывается с тем же эпитопом, что и эталонное антитело, блокирует связывание эталонного антитела с его антигеном в конкурентном анализе на 50% или более, 60% или более, 70% или более, 80% или более, или 90% или более, и наоборот, эталонное антитело блокирует связывание антитела с его антигеном в конкурентном анализе на 50% или более, 60% или более, 70% или более, 80% или более или 90% или более. В данном документе предлагается иллюстративный конкурентный анализ.
«Фрагменты антител» включают часть интактного антитела, предпочтительно антигенсвязывающую или вариабельную область интактного антитела. Примеры фрагментов антител включают Fab-, Fab'-, F(ab')2- и Fv-фрагменты; димеры; линейные антитела (см. патент США №5641870, пример 2; Zapata et al. Protein Eng. 8(10):1057-1062, 1995); молекулы одноцепочечных антител и мультиспецифические антитела, образованные из фрагментов антител.
При расщеплении антител папаином образуются два идентичных антигенсвязывающих фрагмента, называемые «Fab»-фрагментами, и остаточный «Fc»-фрагмент, название которого отражает его способность к легкой кристаллизации. Fab-фрагмент состоит из целой L-цепи вместе с доменом вариабельной области Н-цепи (VH) и первым константным доменом одной тяжелой цепи (CH1). Обработка антитела пепсином позволяет выделить одиночный большой F(ab')2-фрагмент, который приблизительно соответствует двум Fab-фрагментам с бивалентной антигенсвязывающей активностью, соединенным дисульфидной связью, и сохраняющий способность к перекрестному сшиванию антигена. Fab'-фрагменты отличаются от Fab-фрагментов тем, что имеют несколько дополнительных остатков на карбоксильном конце домена СН1, включая один или более цистеинов из шарнирной области антитела. В данном документе Fab'-SH представляет собой обозначение Fab', в котором цистеиновый(е) остаток(и) константных доменов несет свободную тиольную группу. F(ab')2-фрагменты антител первоначально получали как пары Fab'-фрагментов, которые соединены между собой цистеинами шарнирной области. Также известны другие химические соединения фрагментов антитела.
В контексте данного документа термин «Fc-область» употребляется для обозначения С-концевой области тяжелой цепи иммуноглобулина, которая содержит по меньшей мере часть константной области. Данный термин включает нативные последовательности Fc-областей и варианты Fc-областей. В одном варианте осуществления Fc-область тяжелой цепи человеческого IgG находится в пределах от Cys226 или от Pro230 до карбоксильного конца тяжелой цепи. Однако, Fc-область может содержать или не содержать С-концевой лизин (Lys447). Если не указано иное, нумерация аминокислотных остатков Fc-области или константной области соответствует системе нумерации EU, также называемой индексом EU, как описано в Kabat et al. Sequences of Proteins of Immunological Interest, 5th Ed. Public Health Service, National Institutes of Health, Bethesda, MD, 1991.
«Fv» состоит из димера одного домена вариабельной области тяжелой цепи и одного домена вариабельной области легкой цепи, жестко связанных посредством нековалентных связей. При фолдинге этих двух доменов наружу выступают шесть гипервариабельных петель (по 3 петли на каждой Н- и L-цепи), аминокислотные остатки которых участвуют в связывании антигена и придают антителу специфичность по отношению к связыванию антигена. В то же время даже один вариабельный домен (или половина Fv, содержащая только три Н, специфичные к антигену) обладает способностью распознавать и связывать антиген, хотя часто с более низкой аффинностью, чем целый сайт связывания.
«Одноцепочечные Fv», также имеющие аббревиатуру «sFv» или «scFv», представляют собой фрагменты антител, которые содержат домены VH и VL антител, связанные в одну полипептидную цепь. Предпочтительно, полипептид sFv также содержит полипептидный линкер между доменами VH и VL, позволяющий sFv образовывать структуру, необходимую для связывания с антигеном. Для обзора sFv смотри Pluckthun in The Pharmacology of Monoclonal Antibodies, vol. 113, Rosenburg and Moore eds., Springer-Verlag, New York, pp. 269-315, 1994.
Термин «диатела» относится к небольшим фрагментам антител, полученным путем конструирования sFv-фрагментов (см. предыдущий абзац) с короткими линкерами (около 5-10 остатков) между доменами VH и VL, благодаря чему достигается межцепочечное, а не внутрицепочечное сопряжение V-доменов, приводящее к образованию бивалентного фрагмента, т.е. фрагмента, несущего два антигенсвязывающих сайта. Биспецифические антитела представляют собой гетеродимеры двух «кроссоверных» sFv-фрагментов, в которых VH -и VL-домены двух антител представлены на разных полипептидных цепях. Диатела более подробно описаны, например, в ЕР 404097; WO 93/11161; и Hollinger et al. Proc. Natl. Acad. Sci. USA 90:6444-6448, 1993.
«Блокирующее» антитело или «антагонистическое» антитело представляет собой антитело, которое ингибирует или снижает биологическую активность антигена, который он связывает.Некоторые блокирующие антитела или антагонистические антитела в значительной степени или полностью ингибируют биологическую активность антигена. Например, что касается антител против триптазы, в некоторых вариантах осуществления активность может представлять собой ферментативную активность триптазы, например, активность протеазы. В других случаях активность может представлять собой опосредованную триптазой стимуляцию пролиферации клеток гладких мышц бронхов и/или коллагенового сокращения. В других случаях активностью может быть высвобождение гистамина тучными клетками (например, высвобождение гистамина, запускаемого IgE, и/или высвобождение гистамина, запускаемого триптазой). В некоторых вариантах осуществления антитело может ингибировать биологическую активность антигена, который оно связывает на по меньшей мере около 1%, около 5%, около 10%, около 20%, около 25%, около 30%, около 35%, около 40%. около 45%, около 50%, около 55%, около 60%, около 65%, около 70%, около 75%, около 80%, около 85%, около 90%, около 95%, около 96%, около 97%, около 98%, около 99% или около 100%.
«Класс» антитела относится к типу константного домена или константной области, содержащейся в его тяжелой цепи. Существует пять основных классов антител: IgA, IgD, IgE, IgG и IgM, и некоторые из них могут быть дополнительно подразделены на подклассы (изотипы), например, IgG1, IgG2, IgG3, IgG4, IgA1, и IgA2. Константные домены тяжелой цепи, которые соответствуют различным классам иммуноглобулинов, называются α, δ, ε, γ, и μ, соответственно.
«Эффекторные функции» антитела относятся к той биологической активности, которая относится к Fc-области (например, нативной последовательности Fc-области или варианту аминокислотной последовательности Fc-области) антитела, и варьируются в зависимости от изотипа антитела. Примеры эффекторных функций антитела включают: связывание C1q и комплементзависимую цитотоксичность; связывание с рецептором Fc; антителозависимую клеточно-опосредованную цитотоксичность (АЗКЦ); фагоцитоз; снижение экспрессии клеточных поверхностных рецепторов (например, В-клеточного рецептора) и активацию В-клеток.
«Антителозависимая клеточно-опосредованная цитотоксичность» или «АЗКЦ» относится к форме цитотоксичности, при которой секретируемый Ig, связанный с Fc-рецепторами (FcR), присутствующими на определенных цитотоксических клетках (например, натуральных клетках-киллерах (NK-клетках), нейтрофилах и макрофагах), позволяет этим цитотоксическим эффекторным клеткам специфически связываться с несущей антиген целевой клеткой и впоследствии уничтожать целевую клетку цитотоксинами. Антитела «приводят в готовность» цитотоксические клетки и абсолютно необходимы для такого уничтожения. Первичные клетки для опосредования АЗКЦ, NK-клетки, экспрессируют только FcγRIII, тогда как моноциты экспрессируют FcγRI, FcγRII и FcγRIII. Экспрессия FcR на гемопоэтических клетках приведена в таблице 3 на странице 464 в Ravetch et al. Аппи. Rev. Immunol. 9:457-492, 1991. Для оценки активности АЗКЦ представляющей интерес молекулы может быть проведен анализ АЗКЦ in vitro, описанный в патенте США №5500362 или 5821337. Эффекторные клетки, пригодные для такого анализа, включают мононуклеарные клетки периферической крови (МКПК) и натуральные клетки-киллеры (NK). В качестве альтернативы или дополнения, АЗКЦ-активность молекулы, представляющей интерес, можно оценить in vivo, например, в животной модели, например, согласно описанию в публикации Clynes et al. Proc. Natl. Acad. Sci. USA 95:652-656, 1998.
Термины «Fc-рецептор» или «FcR» описывают рецептор, который связывается с Fc-областью антитела. Предпочтительный FcR представляет собой нативную последовательность человеческого FcR. Кроме того, предпочтительный FcR представляет собой тот, который связывает антитело IgG (гамма-рецептор) и включает рецепторы подклассов FcγRI, FcγRII и FcγRIII, включая аллельные варианты и альтернативно сплайсированные формы этих рецепторов. Рецепторы FcγRII включают FcγRIIA («активирующий рецептор») и FcγRIIB («ингибирующий рецептор»), которые содержат аналогичные аминокислотные последовательности, отличающиеся преимущественно цитоплазматическими доменами. Активирующий рецептор FcγRIIA содержит иммунорецепторный тирозиновый активирующий мотив (ITAM) в своем цитоплазматическом домене. Ингибирующий рецептор FcγRIIB содержит иммунорецепторный тирозиновый ингибирующий мотив (ITIM) в своем цитоплазматическом домене (см. обзор М. в Daeron, Annu. Rev. Immunol. 15:203-234, 1997). Обзор FcR приведен в публикациях Ravetch et al. Аппи. Rev. Immunol. 9:457-492, 1991; Capel et al. Immunomethods 4:25-34, 1994; и de Haas et al. J. Lab. Clin. Med. 126:330-41, 1995. Другие FcR, включая те, которые будут идентифицированы в будущем, включены в термин «FcR» в данном документе. Этот термин также включает неонатальный рецептор, FcRn, отвечающий за перенос материнских IgG в плод (см., например, Guyer et al. J. Immunol. 117:587, 1976; and Kim et al. J. Immunol. 24:249, 1994).
«Эффекторные клетки человека» представляют собой лейкоциты, которые экспрессируют один или более FcR и осуществляют эффекторные функции. Предпочтительно, такие клетки экспрессируют по меньшей мере FcγRIII и осуществляют эффекторную функцию АЗКЦ (ADCC). Примеры лейкоцитов человека, которые опосредуют АЗКЦ, включают мононуклеарные клетки периферической крови МКПК, натуральные клетки-киллеры (NK), моноциты, цитотоксические Т-клетки, и нейтрофилы; причем МКПК и NK-клетки являются предпочтительными. Эффекторные клетки могут быть выделены из нативного источника, например, из крови.
«Комплементзависимая цитотоксичность» или «КЗЦ» относится к лизису клетки-мишени в присутствии комплемента. Активация классического пути комплемента инициируется связыванием первого компонента системы комплемента (C1q) с антителами (соответствующего подкласса), которые связаны со своим распознаваемым антигеном. Для оценки активации комплемента, может быть выполнен анализ CDC, например, как описано в Gazzano-Santoro et al. J. Immunol. Methods 202:163, 1996.
«Эпитоп» представляет собой часть антигена, с которой антитело селективно связывается. Для полипептидного антигена линейный эпитоп может представлять собой пептидную часть в приблизительно 4-15 (например, 4, 5, 6, 7, 8, 9, 10, 11, 12, аминокислотных остатков. Нелинейный конформационный эпитоп может содержать остатки полипептидной последовательности, расположенные в непосредственной близости в трехмерной (3D) структуре белка. В некоторых вариантах осуществления эпитоп содержит аминокислоты, которые находятся в пределах 4 ангстрем  от любого атома антитела. В некоторых вариантах осуществления эпитоп содержит аминокислоты, которые находятся в пределах
от любого атома антитела. В некоторых вариантах осуществления эпитоп содержит аминокислоты, которые находятся в пределах  или
или  от любого атома антитела. Аминокислотные остатки антитела, которые связываются с антигеном (то есть паратопом), могут быть определены, например, путем определения кристаллической структуры антитела в комплексе с антигеном или путем осуществления обмена водород/дейтерий.
от любого атома антитела. Аминокислотные остатки антитела, которые связываются с антигеном (то есть паратопом), могут быть определены, например, путем определения кристаллической структуры антитела в комплексе с антигеном или путем осуществления обмена водород/дейтерий.
Термины «полноразмерное антитело», «интактное антитело» и «полное антитело» взаимозаменяемо употребляются в данном документе для обозначения антитела, имеющего структуру, в значительной степени сходную со структурой нативного антитела, или содержащего тяжелые цепи, которые содержат Fc-область, согласно определению в данном документе.
«Человеческое антитело» представляет собой антитело, которое имеет аминокислотную последовательность, которая соответствует таковой из антитела, вырабатываемого человеком, и/или была создана с помощью любых технологий получения человеческих антител. Из этого определения антитела человека, в частности, исключено гуманизированное антитело, содержащее антигенсвязывающие остатки нечеловеческого происхождения.
«Консенсусная каркасная область человека» представляет собой каркасную область, которая содержит наиболее часто встречающиеся аминокислотные остатки при выборе последовательностей каркасной области VL или VH иммуноглобулина человека. Как правило, последовательности VL или VH иммуноглобулина человека выбирают из последовательностей подгруппы вариабельных доменов. Как правило, подгруппа последовательностей представляет собой подгруппу по классификации Kabat et al. Sequences of Proteins of Immunological Interest, Fifth Edition, NIH Publication 91-3242, Bethesda MD, vols. 1-3, 1991. В одном варианте осуществления для VL подгруппа представляет собой подгруппу каппа III или каппа IV, согласно Kabat et al. выше. В одном варианте осуществления для VH подгруппа представляет собой подгруппу III, согласно Kabat et al. выше.
«Гуманизированные» формы не относящихся к человеку видов (например, грызунов) антител представляют собой химерные антитела, которые содержат минимальную последовательность, полученную из иммуноглобулина, не принадлежащего к человеческому роду. В большинстве случаев, гуманизированные антитела представляют собой иммуноглобулины человека (реципиентное антитело), в которых остатки гипервариабельной области реципиента заменены остатками гипервариабельной области нечеловеческих видов (донорское антитело), такого как мышь, крыса, кролик или примат, отличный от человека, имеющего требуемую специфичность, аффинность и активность антитела. В некоторых случаях остатки каркасной области (FR) иммуноглобулина человека заменены соответствующими остатками нечеловеческого происхождения. Кроме того, гуманизированные антитела могут содержать остатки, которые отсутствуют в реципиентном антителе или в донорном антителе. Эти модификации осуществляют для дополнительного улучшения характеристик антитела. В общем, гуманизированное антитело будет содержать практически все из по меньшей мере одного, а обычно двух вариабельных доменов, в которых все или практически все гипервариабельные петли соответствуют таким областям иммуноглобулина нечеловеческого происхождения, а все или практически все FR соответствуют таким областям последовательности иммуноглобулина человека. Гуманизированное антитело также необязательно будет содержать по меньшей мере часть константной области иммуноглобулина (Fc), как правило, из человеческого иммуноглобулина. Для получения дополнительной информации см. Jones et al. Nature 321:522-525, 1986; Riechmann et al. Nature 332:323-329, 1988; и Presta, Curr. Op.Struct. Biol. 2:593-596, 1992.
«Иммуноконъюгат» представляет собой антитело, конъюгированное с одной или более гетерологичными молекулами, включая, но не ограничиваясь этим, цитотоксический агент.
Термин «выделенное», когда используется для описания различных антител, описанных в данном документе, относится к антителу, которое идентифицировано и отделено и/или выделено из клетки или культуры клеток, в которой оно экспрессировано. Загрязняющие компоненты окружающей природной среды представляют собой вещества, которые как правило могут мешать диагностическому или терапевтическому применению полипептида, и могут включать ферменты, гормоны и другие белковые или небелковые растворенные вещества. В некоторых вариантах осуществления антитело является очищенным до более чем 95% или 99% чистоты, определяемой, например, методом электрофореза (например, электрофореза в полиакриламидном геле в присутствии додецилсульфата натрия (ДСН-ПААГ-электрофореза), изоэлектрического фокусирования (ИЭФ), капиллярного электрофореза) или методом хроматографии (например, ионообменной или обращенно-фазовой ВЭЖХ). Для обзора способов оценки чистоты антител, см., например, Flatman et al. J. Chromatogr. В 848:79-87, 2007. В предпочтительных вариантах осуществления антитело будет очищено (1) до степени, достаточной для получения по меньшей мере 15 остатков на N-концевой или внутренней аминокислотной последовательности путем использования секвенатора с вращающейся чашкой или (2) до гомогенности, полученной методом ДСН-ПААГ электрофореза в невосстанавливающих или восстанавливающих условиях, используя окрашивание красителем Кумасси синим или, предпочтительно, серебром. Выделенное антитело включает антитела, полученные in situ внутри рекомбинантных клеток, поскольку по меньшей мере один компонент из полипептидного природного окружения будет отсутствовать. В то же время, выделенный полипептид, как правило, будет получен с использованием по меньшей мере одной стадии очистки.
В контексте данного документа термин «моноклональное антитело» относится к антителу, полученному из популяции в значительной степени гомогенных антител, т.е., отдельные антитела, составляющие популяцию, являются идентичными и/или связывают один эпитоп на антигене за исключением возможных вариантных антител, например, содержащих мутации природного происхождения или возникших во время получения препарата моноклональных антител, при этом такие варианты в общем случае присутствуют в незначительном количестве. В отличие от препаратов поликлональных антител, которые, как правило, содержат различные антитела против различных детерминант (эпитопов), каждое моноклональное антитело из препарата моноклонального антитела направлено против одной детерминанты антигена. Таким образом, определение «моноклональный» указывает на характеристику антитела, полученного по существу из однородной популяции антител, и не должно быть истолковано как необходимость получения антитела каким-либо конкретным способом. Например, моноклональные антитела для использования согласно данному изобретению можно получить с помощью различных способов, включая, без ограничений, метод гибридомы, методы рекомбинантных ДНК, методы фагового дисплея и способы с использованием трансгенных животных, полностью или частично содержащих локусы человеческого иммуноглобулина, причем такие способы и другие иллюстративные способы получения моноклональных антител описаны в данном документе. В определенных вариантах осуществления термин «моноклональное антитело» охватывает биспецифические антитела.
Термин «двухвалентное антитело» относится к антителу, которое имеет два сайта связывания для антигена. Двухвалентное антитело может быть, без ограничения, в формате IgG или в формате F(ab')2.
Термин «мультиспецифическое антитело» используется в самом широком смысле и охватывает антитело, которое связывается с двумя или более детерминантами или эпитопами на одном антигене или двумя или более детерминантами или эпитопами на более чем одном антигене. Такие мультиспецифические антитела включают, но не ограничиваются, полноразмерные антитела, антитела, обладающие двумя или более доменами VL и VH, фрагментами антител, такими как Fab, Fv, dsFv, scFv, диатела, биспецифические диатела и триатела, фрагменты антитела, которые ковалентно или нековалентно связаны. Термин «полиэпитопная специфичность» относится к способности специфически связываться с двумя или более различными эпитопами на одной или разных мишенях. В определенных вариантах осуществления мультиспецифическое антитело представляет собой биспецифическое антитело. «Двойная специфичность» или «биспецифичность» относится к способности специфически связываться с двумя разными эпитопами на одной или разных мишенях. Однако, в отличие от биспецифических антител, антитела с двойной специфичностью имеют два антигенсвязывающих плеча, которые идентичны в аминокислотной последовательности и каждое Fab-плечо способно распознавать два антигена. Двойная специфичность позволяет антителам взаимодействовать с высокой аффинностью с двумя разными антигенами как одна молекула Fab или IgG. В соответствии с одним из вариантов осуществления мультиспецифичное антитело связывается с каждым эпитопом с аффинностью от 5 мкМ до 0,001 пМ, от 3 мкМ до 0,001 пМ, от 1 мкМ до 0,001 пМ, от 0,5 мкМ до 0,001 пМ или от 0,1 мкМ до 0,001 пМ. Термин «моноспецифический» относится к способности связывать только один эпитоп.
«Голое антитело» относится к антителу, которое не конъюгировано с гетерологичным фрагментом (например, цитотоксическим фрагментом) или радиоактивной меткой. Голое антитело может присутствовать в фармацевтической композиции.
Что касается связывания антитела с целевой молекулой, термин «связывает» или «связывание» или «специфическое связывание» или «специфически связывает» или является «специфическим к» конкретному полипептиду или эпитопу на конкретном целевом полипептиде означает связывание, которое измеряемо отличается от неспецифического взаимодействия. Специфическое связывание может быть измерено, например, при помощи определения связывания молекулы по сравнению со связыванием контрольной молекулы. Например, специфическое связывание может определяться конкуренцией с контрольной молекулой, которая сходна с мишенью, к примеру, при избытке немеченой мишени. В этом случае связывание считается специфическим, если связывание меченой мишени с зондом конкурентно ингибируется избытком немеченой мишени. Термин «специфическое связывание» или «специфически связывается с» или является «специфическим к» конкретному полипептиду или эпитопу на конкретном целевом полипептиде, как используется в данном документе, может быть проиллюстрирован, например, при помощи молекулы, имеющей Кодля мишени КИМ или ниже, альтернативно 10-5М или ниже, альтернативно 10-6 М или ниже, альтернативно 10-7 М или ниже, альтернативно 10-8 М или ниже, альтернативно 10-9 М или ниже, альтернативно 10-10 М или ниже, альтернативно 10-11 М или ниже, альтернативно 10-12 М или ниже, или KD в диапазоне от 10-4 М до 10-8 М, или от 10-8 М до 10-10 М, или от 10-7 М до 10-9 М. Как будет понятно специалисту в данной области техники, значения аффинности и KD связаны обратной зависимостью. Высокая аффинность для антигена измеряется низким значением KD. В одном варианте осуществления термин «специфическое связывание» относится к связыванию, при котором молекула связывается с конкретным полипептидом или эпитопом на конкретном полипептиде без значительного связывания с любым другим полипептидом или полипептидным эпитопом.
Термин «вариабельный» относится к тому факту, что среди антител некоторые сегменты вариабельных доменов сильно различаются по последовательностям. Вариабельный или «V»-домен опосредуют антигенное связывание и определяет специфичность конкретного антитела к своему конкретному антигену. При этом вариабельность неравномерно распределена по 110-аминокислотному участку вариабельных доменов. На самом деле, V-области состоят из относительно инвариантных фрагментов, называемых каркасными областями (FR), из 15-30 аминокислот, разделенных более короткими областями с чрезвычайной вариабельностью, называемыми «гипервариабельными областями», которые составляют в длину 9-12 аминокислот.Термин «гипервариабельная область» или «HVR», если используется в данном документе, относится к аминокислотным остаткам антитела, которые отвечают за связывания антигена. Гипервариабельная область, как правило, содержит аминокислотные остатки из числа, например, приблизительно около остатков 24-34 (L1), 50-56 (L2) и 89-97 (L3) в VL, и приблизительно около остатков 26-35 (Н1), 49-65 (Н2) и 95-102 (Н3) в VH (в одном варианте осуществления Н1 состоит из приблизительно около 31-35 остатков); Kabat et al. выше) и/или этих остатков из «гипервариабельной петли» (например, 26-32 (L1), 50-52 (L2), и 91-96 (L3) в VL, и 26-32 (Н1), 53-55 (Н2), и 96-101 (Н3) в VH; Chothia et al. J. Mol. Biol. 196:901-917, 1987. Каждый из вариабельных доменов нативных тяжелых и легких цепей содержит четыре FR, преимущественно принимающих конфигурацию бета-листа, соединенных тремя гипервариабельными областями, которые образуют петли, соединяющие структуру бета-листа, а в некоторых случаях - образующие часть структуры бета-листа. Гипервариабельные области в каждой цепи удерживаются вместе в непосредственной близости от FR и вместе с гипервариабельными областями другой цепи способствуют образованию антигенсвязывающего сайта антител (см. Kabat et al. выше).
Соответственно, последовательности HVR и FR, как правило, располагаются в следующем порядке в VH (или VL): FR1-H1(L1)-FR2-H2(L2)-FR3-H3(L3)-FR4. Константные домены не вовлечены непосредственно в связывание антитела с антигеном, однако проявляют различные эффекторные функции, такие как участие антитела в антителозависимой клеточной токсичности (АЗКЦ).
Термины «нумерация остатков вариабельного домена по Кабату» или «нумерация аминокислотных положений по Кабату» и их вариации относятся к системе нумерации, используемой для вариабельных доменов тяжелой цепи или вариабельных доменов легкой цепи при составлении антител в Kabat et al. выше. При использовании этой системы нумерации, фактическая линейная аминокислотная последовательность может содержать меньше или больше аминокислот, что соответствует укорочению или вставкам в FR или HVR вариабельного домена. Например, вариабельный домен тяжелой цепи может включать единичную аминокислотную вставку (остаток 52а в соответствии с Кабат) после остатка 52 в Н2 и вставленные аминокислотные остатки (например, остатки 82а, 82b и 82с и т.д. в соответствии с Кабат) после FR аминокислотного остатка 82 тяжелой цепи. Нумерация остатков по Кабату может быть определена для данного антитела путем выравнивания гомологичных областей последовательности антитела со «стандартной» пронумерованной последовательностью по Кабату.
Система нумерации по Кабату в общем случае используется для обозначения остатка в вариабельном домене (приблизительно, остатки 1-107 легкой цепи и остатки 1-113 тяжелой цепи) (например, Kabat et al. выше). «Система нумерации EU» или «индекс EU», как правило, используется при рассмотрении аминокислотного остатка в константной области тяжелой цепи иммуноглобулина (например, индекс EU, представленный в Kabat et al. выше). «Индекс EU в соответствии с Кабат» относится к нумерации остатков EU человеческого антитела IgG1. Если не указано иначе, ссылки на номера остатков в вариабельном домене антител означают нумерацию остатков по системе нумерации по Кабату. Если не указано иное, то в данном документе ссылки на номера остатков в константном домене антител означают нумерацию остатков согласно системе нумерации EU (например, см. предварительную заявку США №60/640323, фигуры для нумерации EU).
«Процент (%) идентичности аминокислотных последовательностей» по отношению к полипептидным последовательностям, указанным в данном документе, определяется как процент аминокислотных остатков в кандидатной последовательности, которые идентичны аминокислотным остаткам в сравниваемом полипептиде, после выравнивания последовательностей и введения, в случае необходимости, гэпов для достижения максимальной процентной идентичности последовательностей, и без учета каких-либо консервативных замен как части идентичности последовательностей. Выравнивание с целью определения процента идентичности аминокислотных последовательностей может осуществляться различными способами, которые известны специалистам в данной области техники, например, с использованием общедоступных компьютерных программ, таких как программные обеспечения BLAST, BLAST-2, ALIGN, или Megalign (DNASTAR). Специалисты в данной области техники могут определить нужные параметры для выравнивания, включая любые алгоритмы, необходимые для достижения максимального выравнивания по всей длине сравниваемых последовательностей.
Для целей данного документа, тем не менее, значения % идентичности аминокислотной последовательности получены с использованием программы для сравнения последовательностей ALIGN-2. Компьютерная программа для выравнивания последовательностей ALIGN-2 была разработана Genentech, Inc. а исходная программа была подана вместе с документацией пользователя в Бюро регистрации авторских прав США, Вашингтон, округ Колумбия, 20559, где она зарегистрирована под номером регистрации авторского права США TXU510087. Программа ALIGN-2 находится в свободном доступе в Genentech, Inc., Южный Сан-Франциско, штат Калифорния. Для применения в операционной системе UNIX, предпочтительно цифровую версию UNIX V4.0D, программу ALIGN-2 нужно скомпилировать. Все параметры сравнения последовательностей устанавливаются программой ALIGN-2 и остаются неизменными.
В тех случаях, когда для сравнения аминокислотных последовательностей используется ALIGN-2, % идентичности аминокислотной последовательности данной аминокислотной последовательности А к, с, или по отношению к данной аминокислотной последовательности В (что в альтернативном варианте может быть сформулировано как данная аминокислотная последовательность А, которая имеет или содержит определенный % идентичности аминокислотной последовательности к, с или по отношению к данной аминокислотной последовательности В) рассчитывают следующим образом:
100 умножить на соотношение X/Y
, где X представляет собой число аминокислотных остатков, оцененных программой выравнивания последовательностей ALIGN-2 как идентичные совпадения при программном выравнивании А и В, и где Y представляет общее количество аминокислотных остатков в В. Следует понимать, что там, где длина аминокислотной последовательности А не равняется длине аминокислотной последовательности В, % идентичности аминокислотной последовательности А к В не будет равен % идентичности аминокислотной последовательности В к А. Если специально не указано иное, все значения % идентичности аминокислотных последовательностей, которые используется в данном документе, получают, как описано в предыдущем абзаце с использованием компьютерной программы ALIGN-2.
Под «массовым параллельным секвенированием» или «массово-параллельным секвенированием», также известным в данной области техники как «секвенирование нового поколения» или «секвенирование второго поколения», подразумевается любой подход высокопроизводительного секвенирования нуклеиновых кислот. Эти подходы обычно включают параллельное секвенирование большого количества (например, тысяч, миллионов или миллиардов) пространственно разделенных, клонально амплифицированных матриц ДНК или отдельных молекул ДНК. Смотри, например, Metzker, Nature Reviews Genetics 11: 31-36, 2010.
Термин «листок-вкладыш в упаковке» используется для обозначения инструкций, которые обычно вкладывают в коммерческие упаковки терапевтических продуктов для продажи, содержащие информацию о показаниях, использовании, дозах, приеме, комбинированной терапии, противопоказаниях и/или предупреждениях, которые касаются использования таких терапевтических продуктов.
Термины «фармацевтический состав» и «фармацевтическая композиция» используются в данном документе взаимозаменяемо и относятся к препарату, который находится в такой форме, чтобы обеспечить биологическую активность активного ингредиента, содержащегося в нем, и который не содержит дополнительных компонентов, которые являются неприемлемо токсичными для субъекта, которому вводят состав. Такие составы являются стерильными.
«Стерильная» фармацевтическая композиция является асептической или свободной от, или практически не содержит любых живых микроорганизмов и их спор.
«Фармацевтически приемлемый носитель» относится к ингредиенту в фармацевтической композиции, отличному от активного ингредиента, который нетоксичен для субъекта. Фармацевтически приемлемый носитель включает, но не ограничивается ими, буфер, наполнитель,стабилизатор или консервант.
«Набор» представляет собой любое изделие (например, упаковку или контейнер), содержащее по меньшей мере один реагент, например, зонд для определения количества активных аллелей триптазы у пациента или для определения уровня экспрессии биомаркера (например, триптазы), как описано в данном документе, и/или лекарственный препарат для лечения воспалительного заболевания, опосредованного тучными клетками, например, астмы. Изделие предпочтительно продвигается, распространяется или продается в качестве единицы для выполнения способов согласно данному изобретению.
II. Терапевтические способы и применения согласно изобретению
Данное изобретение обеспечивает способы лечения пациента с воспалительным заболеванием, опосредованным тучными клетками (например, астмой). В некоторых вариантах осуществления способы согласно изобретению включают применение терапии у пациента на основании присутствия и/или уровня экспрессии биомаркера согласно изобретению, например, триптазы (например, количества активных аллелей триптазы у пациента и/или уровня экспрессии триптазы). В некоторых вариантах осуществления способы включают применение терапии, например, терапии, включающей антагонист триптазы, антагонист Fc-эпсилона-рецептора (FcεR), антитело, истощающее IgE+ В-клетки, антитело, истощающее тучные клетки или базофилы, антагонист активируемого протеазой рецептора 2 (PAR2), антагонист IgE или их комбинацию (например, антагонист триптазы и антагонист IgE). В некоторых вариантах осуществления терапия включает терапию, направленную на тучные клетки (например, антагонист триптазы, антагонист IgE, антитело, истощающее IgE+ В-клетки, антитело, истощающее тучные клетки или базофилы, и/или антагонист PAR2). В некоторых вариантах осуществления терапия включает антагонист триптазы (например, антитело против триптазы, например, любое антитело против триптазы, описанное в данном документе или в WO 2018/148585) и антагонист IgE (например, антитело против IgE, например, омализумаб (XOLAIR®)).
Например, изобретение относится к способу лечения пациента с воспалительным заболеванием, опосредованным тучными клетками, который включает применение пациенту с воспалительным заболеванием, опосредованным тучными клетками, к терапии, направленной на тучные клетки (например, терапии, включающей агент, выбранный из группы, состоящей из антагониста триптазы, антагониста IgE, антитела, истощающего IgE+ В-клетки, антитела, истощающего тучные клетки или базофилы, антагониста PAR2 и их комбинации (например, антагониста триптазы и антагониста IgE)), причем (i) было определено, что генотип пациента содержит количество активных аллелей триптазы, которое равно или выше эталонного количества активных аллелей триптазы; или (ii) было определено, что образец от пациента имеет уровень экспрессии триптазы, который равен или выше эталонного уровня триптазы. Например, в некоторых вариантах осуществления генотип пациента был определен как содержащий количество активных аллелей триптазы, которое равно или выше эталонного количества активных аллелей триптазы. В других вариантах осуществления было определено, что образец от пациента имеет уровень экспрессии триптазы, который равен или выше эталонного уровня триптазы.
В другом аспекте изобретение относится к способу лечения пациента с воспалительным заболеванием, опосредованным тучными клетками, который был идентифицирован как имеющий (i) генотип, содержащий количество активных аллелей триптазы, которое равно или выше эталонного количества активных аллелей триптазы; или (ii) уровень экспрессии триптазы в образце от пациента, который равен или выше эталонного уровня триптазы, причем способ включает применение пациенту с воспалительным заболеванием, опосредованным тучными клетками, терапии, направленной на тучные клетки, (например, терапии, включающей агент, выбранный из группы, состоящей из антагониста триптазы, антагониста IgE, антитела, истощающего IgE+ В-клетки, антитела, истощающего тучные клетки или базофилы, антагониста PAR2 и их комбинации (например, антагониста триптазы и антагониста IgE)). Например, в некоторых вариантах осуществления генотип пациента был идентифицирован как содержащий количество активных аллелей триптазы, которое равно или выше эталонного количества активных аллелей триптазы. В других вариантах осуществления было идентифицировано, что пациент имеет уровень экспрессии триптазы в образце от пациента, который равен или выше эталонного уровня триптазы.
В другом аспекте изобретение относится к способу лечения пациента с воспалительным заболеванием, опосредованным тучными клетками, причем способ включает: (а) получение образца, содержащего нуклеиновую кислоту, от пациента; (b) проведение генотипирования образца и выявление присутствия количества активных аллелей триптазы, которое равно или выше эталонного уровня триптазы; (с) идентификацию пациента, имеющего количество активных аллелей триптазы, которое равно или выше эталонного уровня триптазы, как имеющего повышенную вероятность получения пользы от лечения с помощью терапии, направленной на тучные клетки, (например, терапии, включающей антагонист триптазы, антагонист IgE, антитело, истощающее IgE+ В-клетки, антитело, истощающее тучные клетки или базофилы, антагонист PAR2 и их комбинацию (например, антагонист триптазы и антагонист IgE)); и (d) применение терапии, направленной на тучные клетки, (например, терапии, включающей антагонист триптазы, антагонист IgE, антитело, истощающее IgE+ В-клетки, антитело, истощающее тучные клетки или базофилы, антагонист PAR2 и их комбинацию (например, антагонист триптазы и антагонист IgE)) у пациента.
В еще одном дополнительном аспекте изобретение относится к способу лечения пациента с воспалительным заболеванием, опосредованным тучными клетками, причем способ включает: (а) получение образца, содержащего нуклеиновую кислоту или белок, от пациента; (b) проведение анализа экспрессии и определение уровня экспрессии триптазы, который равен или выше эталонного уровня триптазы; (с) идентификацию пациента, имеющего уровень экспрессии триптазы, который равен или выше эталонного уровня триптазы, как имеющего повышенную вероятность получения пользы от лечения с помощью терапии, направленной на тучные клетки (например, терапии, включающей антагонист триптазы, антагонист IgE, антитело, истощающее IgE+ В-клетки, антитело, истощающее тучные клетки или базофилы, антагонист PAR2 и их комбинацию (например, антагонист триптазы и антагонист IgE)); и (d) применение терапии, направленной на тучные клетки, (например, терапии, включающей антагонист триптазы, антагонист IgE, антитело, истощающее IgE+ В-клетки, антитело, истощающее тучные клетки или базофилы, антагонист PAR2 и их комбинацию (например, антагонист триптазы и антагонист IgE)) у пациента. В некоторых вариантах осуществления образец содержит белок, и анализ экспрессии представляет собой ИФА или иммуноанализ.
В некоторых вариантах осуществления любого из предшествующих способов пациент был идентифицирован как имеющий уровень биомаркера 2-го типа в образце от пациента, который ниже эталонного уровня биомаркера 2-го типа. В некоторых вариантах осуществления агент применяют у пациента в виде монотерапии.
В некоторых вариантах осуществления любого из предшествующих способов пациент был идентифицирован как имеющий уровень биомаркера 2-го типа в образце от пациента, который равен или выше эталонного уровня биомаркера 2-го уровня. В некоторых вариантах осуществления способ дополнительно включает введение ингибитора пути TH2 пациенту.
В другом аспекте изобретение относится к способу лечения пациента с воспалительным заболеванием, опосредованным тучными клетками, который включает применение у пациента с воспалительным заболеванием, опосредованным тучными клетками, терапии, включающей антагонист IgE или антагонист FcεR, причем (i) было определено, что генотип пациента содержит количество активных аллелей триптазы, которое ниже эталонного количества активных аллелей триптазы; или (ii) было определено, что образец от пациента имеет уровень экспрессии триптазы, который ниже эталонного уровня триптазы. Например, в некоторых вариантах осуществления генотип пациента был определен как содержащий количество активных аллелей триптазы, которое ниже эталонного количества активных аллелей триптазы. В других вариантах осуществления было определено, что образец от пациента имеет уровень экспрессии триптазы, который ниже эталонного уровня триптазы.
В другом аспекте изобретение относится к способу лечения пациента с воспалительным заболеванием, опосредованным тучными клетками, который был идентифицирован как имеющий (i) генотип, содержащий количество активных аллелей триптазы, которое ниже эталонного количества активных аллелей триптазы; или (ii) уровень экспрессии триптазы в образце от пациента, который ниже эталонного уровня триптазы, причем способ включает применение у пациента с воспалительным заболеванием, опосредованным тучными клетками, терапии, включающей антагонист IgE или антагонист FcεR. Например, в некоторых вариантах осуществления было определено, что генотип пациента содержит количество активных аллелей триптазы, которое ниже эталонного количества активных аллелей триптазы. В других вариантах осуществления было идентифицировано, что пациент имеет уровень экспрессии триптазы в образце от пациента, который ниже эталонного уровня триптазы.
В другом аспекте изобретение относится к способу лечения пациента с воспалительным заболеванием, опосредованным тучными клетками, причем способ включает: (а) получение образца, содержащего нуклеиновую кислоту, от пациента; (b) проведение генотипирования образца и определение присутствия количества активных аллелей триптазы, которое ниже эталонного уровня триптазы; (с) идентификацию пациента, имеющего количество активных аллелей триптазы, которое ниже эталонного уровня триптазы, как имеющего повышенную вероятность получения пользы от лечения антагонистом IgE или антагонистом FcεR; и (d) введение антагониста IgE или антагониста FcεR пациенту.
В еще одном дополнительном аспекте изобретение относится к способу лечения пациента с воспалительным заболеванием, опосредованным тучными клетками, причем способ включает: (а) получение образца, содержащего нуклеиновую кислоту или белок, от пациента; (b) проведение анализа экспрессии и определение уровня экспрессии триптазы, который ниже эталонного уровня триптазы; (с) идентификацию пациента с уровнем экспрессии триптазы, который ниже эталонного уровня триптазы, как имеющего повышенную вероятность получения пользы от лечения антагонистом IgE или антагонистом FcεR; и (d) введение антагониста IgE или антагониста FcεR пациенту. В некоторых вариантах осуществления образец содержит белок, и анализ экспрессии представляет собой ИФА или иммуноанализ.
В некоторых вариантах осуществления любого из предшествующих способов пациент был идентифицирован как имеющий уровень биомаркера 2-го типа в образце от пациента, который равен или выше эталонного уровня биомаркера 2-го уровня. В некоторых вариантах осуществления способ дополнительно включает введение пациенту дополнительного ингибитора пути TH2.
В некоторых вариантах осуществления любого из предшествующих способов количество активных аллелей триптазы определяют путем секвенирования локусов TPSAB1 и TPSB2 генома пациента. Можно использовать любой подходящий подход секвенирования, например секвенирование по Сэнгеру или массовое параллельное секвенирование (например, ILLUMINA®). В некоторых вариантах осуществления локус TPSAB1 секвенируют при помощи способа, включающего (i) амплификацию нуклеиновой кислоты от субъекта в присутствии первого прямого праймера, содержащего нуклеотидную последовательность 5'-CTG GTG TGC AAG GTG ААТ GG-3' (SEQ ID NO: 31) и первого обратного праймера, содержащего нуклеотидную последовательность 5'-AGG ТСС AGC ACT CAG GAG GA 3' (SEQ ID NO: 32) для получения ампликона TPSAB1, и (ii) секвенирования ампликона TPSAB1. В некоторых вариантах осуществления секвенирование ампликона TPSAB1 включает использование первого прямого праймера и первого обратного праймера. В некоторых вариантах осуществления локус TPSB2 секвенируют при помощи способа, включающего (i) амплификацию нуклеиновой кислоты от субъекта в присутствии второго прямого праймера, содержащего нуклеотидную последовательность 5'-GCA GGT GAG ССТ GAG AGT СС-3' (SEQ ID NO: 33), и второго обратного праймера, содержащего нуклеотидную последовательность 5'-GGG АСС ТТС АСС TGC ТТС AG-3' (SEQ ID NO: 34) для получения ампликона TPSB2, и (ii) секвенирования ампликона TPSB2. В некоторых вариантах осуществления секвенирование ампликона TPSB2 включает использование второго прямого праймера и обратного праймера для секвенирования, содержащего нуклеотидную последовательность 5'-CAG CCA GTG АСС CAG САС-3'(SEQ ID NO: 35). В некоторых вариантах осуществления количество активных аллелей триптазы может быть определено путем выявления присутствия любой вариации в локусах TPSAB1 и TPSB2 генома пациента. В некоторых вариантах осуществления количество активных аллелей триптазы определяется по формуле: 4 - сумма количества аллелей альфа-триптазы и бета-III-триптазы со сдвигом рамки (бета-IIIFS) в генотипе пациента В некоторых вариантах осуществления альфа-триптазу определяют путем обнаружения ОНП с733 G>A в TPSAB1. В некоторых вариантах осуществления обнаружение ОНП с733 G>А в TPSAB1 включает обнаружение генотипа пациента с полиморфизмом
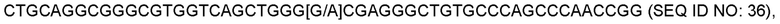
причем присутствие А в ОНП с733 G>А указывает на альфа-триптазу. В некоторых вариантах осуществления бета-IIIFS-триптазу определяют путем обнаружения мутации c980_981insC в TPSB2. В некоторых вариантах осуществления обнаружение мутации c980_981insC в TPSB2 включает обнаружение нуклеотидной последовательности

В некоторых вариантах осуществления любого из предшествующих способов количество активных аллелей триптазы у пациена равно 3 или 4. В некоторых вариантах осуществления количество активных аллелей триптазы равно 3. В других вариантах осуществления количество активных аллелей триптазы равно 4.
В других вариантах осуществления любого из предшествующих способов количество активных аллелей триптазы у пациента равно 0, 1 или 2. В некоторых вариантах осуществления количество активных аллелей триптазы равно 0. В некоторых вариантах осуществления количество активных аллелей триптазы равно 1. В других вариантах осуществления количество активных аллелей триптазы равно 2.
В некоторых вариантах осуществления любого из предшествующих способов эталонное количество активных аллелей триптазы может быть определено в эталонном образце, эталонной популяции и/или может быть предварительно заданным значением (например, пороговым значением, которое ранее было определено для значимого (например, статистически значимого) разделения первой субпопуляции индивидуумов от второй субпопуляции индивидуумов (например, с точки зрения ответа на терапию (например, терапию, включающую агент, выбранный из группы, состоящей из антагониста триптазы, антагониста IgE, антагониста FcεR, антитела, истощающего IgE+ В-клетки, антитела, истощающего тучные клетки или базофилы, антагониста PAR2 и их комбинации (например, антагониста триптазы и антагонисат IgE))). В некоторых вариантах осуществления эталонное количество активных аллелей триптазы представляет собой предварительно определенное значение. В некоторых вариантах осуществления эталонное количество активных аллелей триптазы предварительно определяют при воспалительном заболевании, опосредованном тучными клетками, которым страдает пациент (например, при астме). В определенных вариантах осуществления количество активных аллелей триптазы определяют по общему распределению значений при исследуемом воспалительном заболевании, опосредованным тучными клетками, (например, астмой), или в данной популяции. В некоторых вариантах осуществления эталонное количество активных аллелей триптазы представляет собой целое число в диапазоне от 0 до 4 (например, 0, 1, 2, 3 или 4). В конкретных вариантах осуществления эталонное количество активных аллелей триптазы равно 3.
В любом из предыдущих способов генотип пациента может быть определен с помощью любого из способов или анализов, описанных в данном документе, (например, в Разделе IV подробного описания сущности изобретения или в Примере 1), или известных в данной области техники.
В некоторых вариантах осуществления любого из предшествующих аспектов биомаркер 2-го типа представляет собой связанный с клеткой TH2 цитокин, периостин, количество эозинофилов, профиль эозинофилов, FeNO или IgE. В некоторых вариантах осуществления цитокин, связанный с клеткой TH2, представляет собой ИЛ-13, ИЛ-4, ИЛ-9 или ИЛ-5.
В некоторых вариантах осуществления любого из предшествующих способов уровень экспрессии биомаркера (например, триптазы) представляет собой уровень экспрессии белка. Например, в некоторых вариантах осуществления уровень экспрессии белка измеряли с использованием иммуноанализа (например, мультиплексного иммуноанализа), ИФА, вестерн-блоттинга или масс-спектрометрии. См., например, Раздел V подробного описания сущности изобретения. В некоторых вариантах осуществления уровень экспрессии белка триптазы представляет собой уровень экспрессии активной триптазы. В других вариантах осуществления уровень экспрессии белка триптазы представляет собой уровень экспрессии общей триптазы.
В других вариантах осуществления любого из предшествующих способов уровень экспрессии биомаркера (например, триптазы) представляет собой уровень экспрессии мРНК. Например, в некоторых вариантах осуществления уровень экспрессии мРНК измеряли с использованием метода ПЦР (например, кПЦР) или микроматричного чипа. См., например, Раздел V подробного описания сущности изобретения.
В любом из предшествующих способов или применений уровень экспрессии биомаркера согласно изобретению (например, триптазы) в образце, полученном от пациента, может быть изменен на/в по меньшей мере около 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 100%, 2 раза, 3 раза, 4 раза, 5 раз, 6 раз, 7 раз, 8 раз, 9 раз, 10 раз, 11 раз, 12 раз, 13 раз, 14 раз, 15 раз, 16 раз или более относительно эталонного уровня биомаркера. Например, в некоторых вариантах осуществления уровень экспрессии биомаркера согласно изобретению в образце, полученном от пациента, может быть увеличен на/в по меньшей мере около 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 100%, 2 раза, 3 раза, 4 раза, 5 раз, 6 раз, 7 раз, 8 раз, 9 раз, 10 раз, 11 раз, 12 раз, 13 раз, 14 раз, 15 раз, 16 раз или более относительно эталонного уровня биомаркера. В других вариантах осуществления уровень экспрессии биомаркера согласно изобретению в образце, полученном от пациента, может быть уменьшен на/в по меньшей мере около 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 100%, 2 раза, 3 раза, 4 раза, 5 раз, 6 раз, 7 раз, 8 раз, 9 раз, 10 раз, 11 раз, 12 раз, 13 раз, 14 раз, 15 раз, 16 раз или более относительно эталонного уровня биомаркера.
В некоторых вариантах осуществления эталонный уровень может быть установлен на любой процентиль между, например, 20-м процентилем и 99-м процентилем (например, 20-й, 25-й, 30-й, 35-й, 40-й, 45-й, 50-й, 55-й, 60-й, 65-й, 70-й, 75-й, 80-й, 85-й, 90-й, 95-й или 99-й процентиль) общего распределения уровня экспрессии биомаркера (например, триптазы), например, у здоровых субъектов или в группе пациентов с расстройством (например, воспалительным заболеванием, опосредованным тучными клетками, (например, астмой)). В конкретных вариантах осуществления эталонный уровень может быть установлен на 25-й процентиль общего распределения значений в популяции пациентов с астмой. В других конкретных вариантах осуществления эталонный уровень может быть установлен на 50-й процентиль общего распределения значений в популяции пациентов с астмой. В других вариантах осуществления эталонный уровень может быть медианой общего распределения значений в популяции пациентов с астмой.
Любой подходящий образец, полученный от пациента, может быть использован в любом из предыдущих способов. Например, в некоторых вариантах осуществления образец, полученный от пациента, представляет собой образец крови (например, образец цельной крови, образец сыворотки, образец плазмы или их комбинацию), образец ткани, образец мокроты, образец бронхиального лаважа, образец жидкости слизистой оболочки (MLF), бронхосорбционный образец и назосорбционный образец.
Изобретение также относится к терапии, направленной на тучные клетки, (например, агенту, выбранному из группы, состоящей из антагониста триптазы, антагониста IgE, антитела, истощающего IgE+ В-клетки, антитела, истощающего тучные клетки или базофилы, антагониста PAR2, и их комбинации (например, антагониста триптазы и антагониста IgE)) для применения в способе лечения пациента с воспалительным заболеванием, опосредованным тучными клетками, в котором (i) было определено, что генотип пациента содержит количество активных аллелей триптазы, которое равно или выше эталонного количества активных аллелей триптазы; или (ii) было определено, что образец от пациента имеет уровень экспрессии триптазы, который равен или выше эталонного уровня триптазы. В некоторых вариантах осуществления было определено, что пациент имеет уровень биомаркера 2-го типа в образце от пациента, который ниже эталонного уровня биомаркера 2-го типа, и агент предназначен для применения в виде монотерапии. В некоторых вариантах осуществления пациент был идентифицирован как имеющий уровень биомаркера 2-го типа в образце от пациента, который равен или выше эталонного уровня биомаркера 2-го типа, и агент предназначен для применения в комбинации с ингибитором пути TH2.
В другом аспекте изобретение относится к применению терапии, направленной на тучные клетки, (например, агента, выбранного из группы, состоящей из антагониста триптазы, антагониста IgE, антитела, истощающего IgE+ В-клетки, антитела, истощающего тучные клетки или базофилы, антагониста PAR2, и их комбинации (например, антагониста триптазы и антагониста IgE)) при изготовлении лекарственного средства для лечения пациента с воспалительным заболеванием, опосредованным тучными клетками, в котором (i) было определено, что генотип пациента содержит количество активных аллелей триптазы, которое равно или выше эталонного количества активных аллелей триптазы; или (и) было определено, что образец от пациента имеет уровень экспрессии триптазы, который равен или выше эталонного уровня триптазы. В некоторых вариантах осуществления было определено, что пациент имеет уровень биомаркера 2-го типа в образце от пациента, который ниже эталонного уровня биомаркера 2-го типа, и агент предназначен для применения в виде монотерапии. В некоторых вариантах осуществления пациент был идентифицирован как имеющий уровень биомаркера 2-го типа в образце от пациента, который равен или выше эталонного уровня биомаркера 2-го типа, и агент предназначен для применения в комбинации с ингибитором пути TH2.
В еще одном аспекте изобретение относится к антагонисту IgE или антагонисту FcεR для применения в способе лечения пациента с воспалительным заболеванием, опосредованным тучными клетками, в котором (i) определено, что генотип пациента содержит количество активных аллелей триптазы ниже эталонного количества активных аллелей триптазы; или (ii) было определено, что образец от пациента имеет уровень экспрессии триптазы, который ниже эталонного уровня триптазы. В некоторых вариантах осуществления было определено, что пациент имеет уровень биомаркера 2-го типа в образце от пациента, который равен или выше эталонного уровня биомаркера 2-го типа, а антагонист IgE или антагонист FcεR предназначен для применения в комбинации с ингибитором пути TH2.
В дополнительном аспекте изобретение обеспечивает применение антагониста IgE или антагониста FcεR при изготовлении лекарственного препарата для лечения пациента с воспалительным заболеванием, опосредованным тучными клетками, в котором (i) было определено, что генотип пациента содержит количество активных аллелей триптазы, которое ниже эталонного количества активных аллелей триптазы; или (ii) было определено, что образец от пациента имеет уровень экспрессии триптазы, который ниже эталонного уровня триптазы. В некоторых вариантах осуществления было определено, что пациент имеет уровень биомаркера 2-го типа в образце от пациента, который равен или выше эталонного уровня биомаркера 2-го типа, а антагонист IgE или антагонист FcεR предназначен для применения в комбинации с ингибитором пути TH2.
Любой из предшествующих способов или применений может включать введение антагониста триптазы пациенту. Антагонист триптазы может быть антагонистом альфа-триптазы (например, антагонист альфа-1-триптазы) или антагонист бета-триптазы (например, бета-1-триптаза, бета-2-триптаза и/или антагонист бета-3-триптазы). В некоторых вариантах осуществления антагонист триптазы представляет собой антагонист альфа-триптазы и антагонист бета-триптазы. В некоторых вариантах осуществления антагонист триптазы (например, антагонист альфа-триптазы и/или антагонист бета-триптазы) представляет собой антитело против триптазы (например, антитело против альфа-триптазы и/или антитело против бета-триптазы). Можно использовать любое антитело против триптазы, описанное в Разделе VII ниже.
Любой из предшествующих способов или применений может включать введение антагониста FcεR пациенту. В некоторых вариантах осуществления антагонист FcεR ингибирует FcεRIα, FcεRIβ и/или FcεRIγ. В других вариантах осуществления антагонист FcεR ингибирует FcεRII. В еще других вариантах осуществления антагонист FcεR ингибирует член сигнального пути FcεR. Например, в некоторых вариантах осуществления антагонист FcεR ингибирует тирозин-протеинкиназу Lyn (Lyn), тирозинкиназу Брутона (ВТК), тирозин-протеинкиназу Fyn (Fyn), связанную с селезенкой тирозинкиназу (Syk), линкер для активации Т-клеток (LAT), белок-2, связанный с рецептором фактора роста (Grb2), белок «son of sevenless» (Sos), Ras, Raf-1, митоген-активируемую протеинкиназу 1 (MEK), митоген-активируемую протеинкиназу 1 (ERK), цитозольную фосфолипазу А2 (cPLA2), арахидонат-5-липоксигеназу (5-LO), арахидонат-5-липоксигеназа-активирующий белок (FLAP), фактор обмена гуаниновых нуклеотидов VAV (Vav), Rac, киназу-3 митоген-активируемой протеинкиназы, киназу-7 митоген-активируемой протеинкиназы, р38 МАР-киназу (р38), c-Jun-N-концевую киназу (JNK), белок-2, ассоциированный с белком-2, который связан с рецептором фактора роста (Gab2), фосфатидилинозитол-4,5-бисфосфат-3-киназу (PI3K), фосфолипазу С гамма (PLCγ), протеинкиназу С (PKC), 3-фосфоинозитид-зависимую протеинкиназу 1 (PDK1), RAC серин/треонин-протеинкиназу (АКТ), гистамин, гепарин, интерлейкин (ИЛ) -3, ИЛ-4, ИЛ-13, ИЛ-5, гранулоцитарно-макрофагальный колониестимулирующий фактор (ГМ-КСФ), фактор некроза опухоли-альфа (ФНО-α), лейкотриены (например, LTC4, LTD4 и LTE4) и простагландины (например, PDG2). В некоторых вариантах осуществления антагонист FcεR представляет собой ингибитор ВТК (например, GDC-0853, акалабрутиниб, GS-4059, спебрутиниб, BGB-3111 или НМ71224).
Любой из предшествующих способов или применений может включать введение агента, истощающего IgE+ В-клетки, (например, антитела, истощающего IgE+ В-клетки) пациенту. В некоторых вариантах осуществления антитело, истощающее IgE+ В-клетки, представляет собой антитело против домена М1. Может быть использовано любое подходящее антитело против домена M1', например, любое антитело против домена M1', описанное в публикации международной патентной заявки №WO 2008/116149, которая полностью включена в данный документ посредством ссылки. В некоторых вариантах осуществления антитело против домена М1' является афукозилированным. В некоторых вариантах осуществления антитело против домена М1' представляет собой килизумаб или 47Н4 (см., например, Brightbill et al. J. Clin. Invest. 120(6):2218-2229, 2010).
Любой из предшествующих способов или применений может включать введение агента, истощающего тучные клетки или базофилы, (например, антитела, истощающего тучные клетки или базофилы) пациенту. В некоторых вариантах осуществления антитело истощает тучные клетки. В других вариантах осуществления антитело истощает базофилы. В еще других вариантах осуществления антитело истощает тучные клетки и базофилы.
Любой из предшествующих способов или применений может включать введение антагониста PAR2 пациенту. Иллюстративные антагонисты PAR2 включают низкомолекулярные ингибиторы (например, K-12940, K-14585, пептид FSLLRY-NH2 (SEQ ID NO: 30), GB88, AZ3451 и AZ8838), растворимые рецепторы, киРНК и антитела против PAR2 (например, МАВ3949 и Fab3949).
Любой из предшествующих способов или применений может включать введение антагониста IgE пациенту. В некоторых вариантах осуществления антагонист IgE представляет собой антитело против IgE. Можно использовать любое подходящее антитело против IgE. Например, антитело против IgE может представлять собой любое антитело против IgE, описанное в патенте США №8961964, которое полностью включено в данный документ посредством ссылки. Иллюстративные антитела против IgE включают омализумаб (XOLAIR®), Е26, Е27, CGP-5101 (Hu-901), НА, лигелизумаб и тализумаб. В конкретных вариантах осуществления антитело против IgE представляет собой омализумаб (XOLAIR®).
Аминокислотная последовательность вариабельного (VH) домена тяжелой цепи омализумаба (XOLAIR®) представляет собой следующее (аминокислотные последовательности HVR-H1, -Н2 и -Н3 подчеркнуты):

Аминокислотная последовательность вариабельного (VL) домена легкой цепи омализумаба (XOLAIR®) представляет собой следующее (аминокислотные последовательности HVR-L1, -L2 и -L3 подчеркнуты):
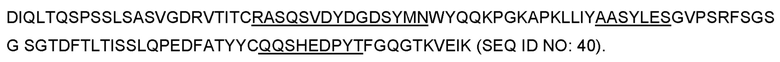
Соответственно, в некоторых вариантах осуществления антитело против IgE содержит одну, две, три, четыре, пять или все шесть из следующих шести HVR: (a) HVR-H1, содержащую аминокислотную последовательность GYSWN (SEQ ID NO: 40); (b) HVR-H2, содержащую аминокислотную последовательность SITYDGSTNYNPSVKG (SEQ ID NO: 41); (c) HVR-H3, содержащую аминокислотную последовательность GSHYFGHWHFAV (SEQ ID NO: 42); (d) HVR-L1, содержащую аминокислотную последовательность RASQSVDYDGDSYMN (SEQ ID NO: 43); (e) HVR-L2, содержащую аминокислотную последовательность AASYLES (SEQ ID: 44); и (f) HVR-L3, содержащую аминокислотную последовательность QQSHEDPYT (SEQ ID NO: 45). В некоторых вариантах осуществления антитело против IgE содержит (а) домен VH, содержащий аминокислотную последовательность, имеющую по меньшей мере 90%, по меньшей мере 95% или по меньшей мере 99% идентичность последовательности с аминокислотной последовательностью SEQ ID NO: 38; (b) домен VL, содержащий аминокислотную последовательность, имеющую по меньшей мере 90%, по меньшей мере 95% или по меньшей мере 99% идентичность с аминокислотной последовательностью SEQ ID NO: 39; или (с) домен VH как в (а) и домен VL как в (b). В некоторых вариантах осуществления домен VH содержит аминокислотную последовательность SEQ ID NO: 38. В некоторых вариантах осуществления домен VL содержит аминокислотную последовательность SEQ ID NO: 39. В некоторых вариантах осуществления домен VH содержит аминокислотную последовательность SEQ ID NO: 38, и домен VL содержит аминокислотную последовательность SEQ ID NO: 39. Любое из антител против IgE, описанных в данном документе, можно использовать в комбинации с любым антителом против триптазы, описанным в данном документе, например, в Разделе VII ниже.
Любой из предшествующих способов или применений может включать введение ингибитора пути TH2 пациенту. В некоторых вариантах осуществления ингибитор пути TH2 ингибирует любую из мишеней, выбранных из индуцируемой интерлейкином-2 Т-клеточной киназы (ITK), тирозинкиназы Брутона (ВТК), Янус-киназу 1 (JAK1) (например, руксолитиниба, тофацитиниба, оклацитиниба, барицитиниба, филготиниба, гандотиниба, лестауртиниба, момелотиниба, пакринитиба, упадацитиниба, пефитиниба и федратиниба), GATA-связывающего белка 3 (GATA3), ИЛ-9 (например, MEDI-528), ИЛ-5 (например, меполизумаба, CAS №196078-29-2; резилизумаба), ИЛ-13 (например, IMA-026, IMA-638 (также называемого анрукинзумабом, INN №910649-32-0; QAX-576; ловушкой для ИЛ-4/ИЛ-13), тралокинумаба (также называемого САТ-354, CAS №1044515-88-9); AER-001, АВТ-308 (также называемого гуманизированным антителом 13С5.5)), ИЛ-4 (например, AER-001, ловушки для ИЛ-4/ИЛ-13), OX40L, TSLP, ИЛ-25, ИЛ-33 и IgE (например, XOLAIR®, QGE-031 и MEDI-4212); и рецепторов, например: рецептора ИЛ-9, рецептора ИЛ-5 (например, MEDI-563 (бенилизумаба, CAS №1044511-01-4)), альфа рецептора ИЛ-4 (например, AMG-317, AIR-645), альфа-1 рецептора ИЛ-13 (например, R-1671) и альфа-2 рецептора ИЛ-13, ОХ40, TSLP-R, ИЛ-7R-альфа (корецептора для TSLP), ИЛ-17RB (рецептора для ИЛ-25), ST2 (рецептора для ИЛ-33), CCR3, CCR4, CRTH2 (например, AMG-853, АР768, АР-761, MLN6095, АСТ129968), FcεRI, Fc£RII/CD23 (рецепторы для IgE), Flap (например, GSK2190915), Syk киназы (R-343, PF3526299); CCR4 (AMG-761), TLR9 (QAX-935) и мультицитокинового ингибитора CCR3, ИЛ-5, ИЛ-3 и ГМ-КСФ (например, TPI ASM8).
Любой из предшествующих способов или применений может включать введение дополнительного терапевтического агента пациенту. В некоторых вариантах осуществления дополнительный терапевтический агент выбран из группы, состоящей из ингибитора пути TH2, кортикостероида, антагониста, связывающего ось ИЛ-33, антагониста TRPA1, бронходилататора или лекарственного препарата для контроля симптомов астмы, иммуномодулятора, ингибитора тирозинкиназы и ингибитора фосфодиэстеразы. Такие комбинированные методы лечения описаны ниже.
В некоторых вариантах осуществления дополнительный терапевтический агент представляет собой терапию астмы, как описано ниже. Умеренную астму в настоящее время лечат ежедневно ингалируемым противовоспалительным кортикостероидом или ингибитором тучных клеток, таким как кромолин-натрий или недокромил, а также ингаляционным бета2-агонистом по мере необходимости (3-4 раза в день) для облегчения обострения симптомов астмы на фоне лечения, или астмы, вызванной аллергенами или физической нагрузкой. Иллюстративные ингаляционные кортикостероиды включают QVAR®, PULMICORT®, SYMBICORT®, AEROBID®, FLOVENT®, FLONASE®, ADVAIR® и AZMACORT®. Дополнительные методы лечения астмы включают бронходилататоры длительного действия (LAND). В определенных вариантах осуществления LAND представляет собой бета-2-агонист пролонгированного действия (LABA), антагонист лейкотриеновых рецепторов (LTRA), мускариновый антагонист длительного действия (LAMA), теофиллин или пероральные кортикостероиды (OCS). Иллюстративные LABD включают SYMBICORT®, ADVAIR®, BROVANA®, FORADIL®, PERFOROMIST™, и SEREVENT®.
В некоторых вариантах осуществления любой из предшествующих способов или применений дополнительно включает введение бронходилататора или лекарственного препарата для контроля симптомов астмы. В некоторых вариантах осуществления бронходилататор или лекарственный препарат для контроля астмы представляет собой р2-адренергический агонист, такой как р2-агонист короткого действия (SABA) (такой как альбутерол), или р2-адренергический агонист длительного действия (LABA). В некоторых вариантах осуществления LABA представляет собой сальметерол, абедитерол, индакатерол, вилантерол и/или формотерол (формотерола фумарата дегидрат). В некоторых вариантах осуществления лекарственный препарат от астмы представляет собой антагонист лейкотриеновых рецепторов (LTRA). В некоторых вариантах осуществления LTRA представляет собой монтелукаст, зафирлукаст и/или зилеутон. В некоторых вариантах осуществления бронходилататор или лекарственный препарат для контроля астмы представляет собой мускариновый антагонист, такой как (холинергический) антагонист ацетилхолиновых мускариновых рецепторов длительного действия (LAMA). В некоторых вариантах осуществления LAMA представляет собой гликопирроний. В некоторых вариантах осуществления бронходилататор или лекарственный препарат для контроля астмы представляет собой агонист ионного канала, такого как рецептор горького вкуса (такой как TAS2R).
В некоторых вариантах осуществления любой из предшествующих способов или применений дополнительно включает введение бронходилататора. В некоторых вариантах осуществления бронходилататор представляет собой ингаляционный бронходилататор. В некоторых вариантах осуществления ингаляционный бронходилататор представляет собой β2-адренергический агонист. В некоторых вариантах осуществления р2-адренергический агонист представляет собой β2-адренергический агонист короткого действия (SABA). В некоторых вариантах осуществления SABA представляет собой битолтерол, фенотерол, изопротеренол, левальбутерол, метапротеренол, пирбутерол, прокатерол, ритодрин, альбутерол и/или тербуталин. В некоторых вариантах осуществления β2-адренергический агонист представляет собой β2-адренергический агонист длительного действия (LABA). В некоторых вариантах осуществления LABA представляет собой арформотерол, бамбутерол, кленбутерол, формотерол, сальметерол, абедитерол, кармотерол, индакатерол, олодатерол и/или вилантерол. В некоторых вариантах осуществления ингаляционный бронходилататор представляет собой антагонист мускариновых рецепторов. В некоторых вариантах осуществления антагонист мускариновых рецепторов представляет собой антагонист мускариновых рецепторов короткого действия (SAMA). В некоторых вариантах осуществления SAMA представляет собой ипратропия бромид. В некоторых вариантах осуществления антагонист мускариновых рецепторов представляет собой антагонист мускариновых рецепторов длительного действия (LAMA). В некоторых вариантах осуществления LAMA представляет собой тиотропия бромид, гликопиррония бромид, умеклидиния бромид, аклидиния бромид и/или ревефенацин. В некоторых вариантах осуществления ингаляционный бронходилататор представляет собой комбинацию SABA/SAMA. В некоторых вариантах осуществления комбинация SABA/SAMA представляет собой альбутерол/ипратропий. В некоторых вариантах осуществления ингаляционный бронходилататор представляет собой комбинацию LABA/LAMA. В некоторых вариантах осуществления комбинация LABA/LAMA представляет собой формотерол/аклидиний, формотерол/гликопирроний, формотерол/тиотропий, индакатерол/гликопирроний, индакатерол/тиотропий, олодатерол/тиотропий, сальметерол/тиотропин и/или вилантерол/умеклидиний. В некоторых вариантах осуществления ингаляционный бронходилататор представляет собой бифункциональный бронходилататор. В некоторых вариантах осуществления бифункциональный бронходилататор представляет собой мускариновый антагонист/β2-агонист (МАВА). В некоторых вариантах осуществления МАВА представляет собой батефентерол, THRX 200495, AZD2115, LAS 190792, TEI3252, PF-3429281 и/или PF-4348235. В некоторых вариантах осуществления ингаляционный бронходилататор представляет собой агонист TAS2R. В некоторых вариантах осуществления бронходилататор представляет собой небулизированный SABA. В некоторых вариантах осуществления небулизированный SABA представляет собой альбутерол и/или левальбутерол. В некоторых вариантах осуществления бронходилататор представляет собой небулизированный LABA. В некоторых вариантах осуществления небулизированный LABA представляет собой арформотерол и/или формотерол. В некоторых вариантах осуществления бронходилататор представляет собой небулизированный SAMA. В некоторых вариантах осуществления небулизированный SAMA представляет собой ипратропий. В некоторых вариантах осуществления бронходилататор представляет собой небулизированный LAMA. В некоторых вариантах осуществления небулизированный LAMA представляет собой гликопирроний и/или ревефенацин. В некоторых вариантах осуществления бронходилататор представляет собой комбинацию небулизированных SABA/SAMA. В некоторых вариантах осуществления комбинация небулизированных SABA/SAMA представляет собой альбутерол/ипратропий. В некоторых вариантах осуществления бронходилататор представляет собой антагонист лейкотриеновых рецепторов (LTRA). В некоторых вариантах осуществления LTRA представляет собой монтелукаст, зафирлукаст и/или зилеутон. В некоторых вариантах осуществления бронходилататор представляет собой метилксантин. В некоторых вариантах осуществления метилксантин представляет собой теофиллин.
В некоторых вариантах осуществления любой из предшествующих способов или применений дополнительно включает введение иммуномодулятора. В некоторых вариантах осуществления способ дополнительно включает введение кромолина. В некоторых вариантах осуществления способ дополнительно включает введение метилксантина. В некоторых вариантах осуществления метилксантин представляет собой теофиллин или кофеин.
В некоторых вариантах осуществления любой из предшествующих способов или применений дополнительно включает введение одного или более кортикостероидов, таких как ингаляционный кортикостероид (ICS) или пероральный кортикостероид. Неограничивающие иллюстративные кортикостероиды включают ингаляционные кортикостероиды, такие как беклометазона дипропионат, будесонид, циклесонид, флунизолид, флутиказона пропионат, флутиказона фуроат, мометазон, и/или триамцинолона ацетонид, и пероральные кортикостероиды, такие как метилпреднизолон, преднизолон и преднизон. В некоторых вариантах осуществления кортикостероид представляет собой ICS. В некоторых вариантах осуществления ICS представляет собой беклометазон, будесонид, флунизолид, флутиказона фуроат, флутиказона пропионат, мометазон, циклесонид и/или триамцинолон. В некоторых вариантах осуществления способ дополнительно включает введение комбинации ICS/LABA и/или LAMA. В некоторых вариантах осуществления комбинация ICS/LABA и/или LAMA представляет собой флутиказона пропионат/сальметерол, будесонид/формотерол, мометазон/формотерол, флутиказона фуроат/вилантерол, флутиказона пропионат/формотерол, беклометазон/формотерол, флутиказона фуроат/умецилидиум, флутиказона фуроат/вилантерол/умеклидиний, флутиказон/сальметерол/тиотропий, беклометазон/формотерол/гликопирроний, будесонид/формотерол/гликопирроний, и/или будесонид/формотерол/тиотропий. В некоторых вариантах осуществления способ дополнительно включает введение небулизированного кортикостероида. В некоторых вариантах осуществления небулизированный кортикостероид представляет собой будесонид. В некоторых вариантах осуществления способ дополнительно включает введение перорального или внутривенного кортикостероида. В некоторых вариантах осуществления пероральный или внутривенный кортикостероид представляет собой преднизон, преднизолон, метилпреднизолон и/или гидрокортизон.
В некоторых вариантах осуществления любой из предшествующих способов или применений дополнительно включает введение одного или боле активных ингредиентов, выбранных из аминосалицилата; стероида; биологического препарата; тиопурина; метотрексата; ингибитора кальциневрина, например, циклоспорина или такролимуса; и антибиотика. В некоторых вариантах осуществления способ включает введение дополнительного активного ингредиента в составе для перорального или местного применения. Примеры аминосалицилатов включают 4-аминосалициловую кислоту, сульфасалазин, бальсалазид, олсалазин и мезалазин в таких формах, как покрытый Eudragit-S, рН-зависимый мезаламин, покрытый этилцеллюлозой мезаламин, и мультиматричный мезаламин с контролируемым высвобождением. Примеры стероидов включают кортикостероиды или глюкокортикостероиды. Примеры кортикостероидов включают преднизон и гидрокортизон, или метилпреднизолон или кортикостероид второго поколения, например, будесонид или азатиоприн; например, в таких формах, как клизма с гидрокортизоном или гидрокортизон в виде пены. Примеры биологических препаратов включают этанерцепт; антитело к фактору некроза опухоли-альфа, например инфликсимаб, адалимумаб или цертолизумаб; антитело к ИЛ-12 и ИЛ-23, например, устекинумаб; ведолизумаб; этролизумаб и натализумаб. Примеры тиопуринов включают азатиоприн, 6-меркаптопурин и тиогуанин. Примеры антибиотиков включают ванкомицин, рифаксимин, метронидазол, триметоприм, сульфаметоксазол, диаминодифенилсульфон и ципрофлоксацин; и противовирусные агенты, такие как ганцикловир.
В некоторых вариантах осуществления любой из предшествующих способов или применений дополнительно включает введение противофибротического агента. В некоторых вариантах осуществления противофибротический агент ингибирует синтез коллагена, стимулированного трансформирующим фактором роста-бета (ТФР-β), уменьшает внеклеточный матрикс и/или блокирует пролиферацию фибробластов. В некоторых вариантах осуществления противофибротический агент представляет собой пирфенидон. В некоторых вариантах осуществления противофибротический агент представляет собой PBI-4050. В некоторых вариантах осуществления противофибротический агент представляет собой типелукаст.
В некоторых вариантах осуществления любой из предшествующих способов или применений дополнительно включает введение ингибитора тирозинкиназы. В некоторых вариантах ингибитор тирозинкиназы ингибирует тирозинкиназу, которая опосредует выработку одного или нескольких фиброгенных факторов роста. В некоторых вариантах осуществления фиброгенный фактор роста представляет собой фактор роста тромбоцитов, фактор роста эндотелия сосудов и/или фактор роста фибробластов. В некоторых вариантах осуществления ингибитор тирозинкиназы представляет собой иматиниб и/или нинтеданиб. В некоторых вариантах осуществления ингибитор тирозинкиназы представляет собой нинтеданиб. В некоторых вариантах осуществления способ дополнительно включает введение противодиарейного агента. В некоторых вариантах осуществления противодиарейный агент представляет собой лоперамид.
В некоторых вариантах осуществления любой из предшествующих способов или применений дополнительно включает введение антитела. В некоторых вариантах осуществления антитело представляет собой антитело против интерлейкина (ИЛ)-13. В некоторых вариантах осуществления антитело против ИЛ-13 представляет собой тралокинумаб. В некоторых вариантах осуществления антитело представляет собой антитело против ИЛ-4 / против ИЛ-13. В некоторых вариантах осуществления антитело против ИЛ-4 / против ИЛ-13 представляет собой SAR 156597. В некоторых вариантах осуществления антитело представляет собой антитело против фактора роста соединительной ткани (CTGF). В некоторых вариантах осуществления антитело против CTGF представляет собой FG-3019. В некоторых вариантах осуществления антитело представляет собой антитело против лизилоксидазоподобного-2 белка (LOXL2). В некоторых вариантах осуществления антитело против LOXL2 представляет собой симтузумаб. В некоторых вариантах осуществления антитело представляет собой антитело против рецептора интегрина αvβ6. В некоторых вариантах осуществления антитело против рецептора интегрина αvβ6 представляет собой STX-100. В некоторых вариантах осуществления антитело представляет собой моноклональное антитело.
В некоторых вариантах осуществления любой из предшествующих способов или применений дополнительно включает введение антагониста рецептора лизофосфатидной кислоты-1 (LPA1). В некоторых вариантах осуществления антагонист рецептора LPA1 представляет собой BMS-986020. В некоторых вариантах осуществления способ дополнительно включает введение ингибитора галектина-3. В некоторых вариантах осуществления ингибитор галектина-3 представляет собой TD-139.
В некоторых вариантах осуществления любой из предшествующих способов или применений дополнительно включает применение паллиативной терапии. В некоторых вариантах осуществления паллиативная терапия включает один или более антибиотиков, анксиолитиков, кортикостероидов и опиоидов. В некоторых вариантах осуществления антибиотик представляет собой антибиотик широкого спектра действия. В некоторых вариантах осуществления антибиотик представляет собой пенициллин, ингибитор β-лактамаз и/или цефалоспорин. В некоторых вариантах осуществления антибиотик представляет собой пиперациллин/тазобактам, цефиксим, цефтриаксон и/или цефдинир. В некоторых вариантах осуществления анксиолитик представляет собой алпразолам, буспирон, хлорпромазин, диазепам, мидазолам, лоразепам и/или прометазин. В некоторых вариантах осуществления кортикостероид представляет собой глюкокортикостероид. В некоторых вариантах осуществления глюкокортикостероид представляет собой преднизон, преднизолон, метилпреднизолон и/или гидрокортизон. В некоторых вариантах осуществления опиоид представляет собой морфин, кодеин, дигидрокодеин и/или диаморфин.
В некоторых вариантах осуществления любой из предшествующих способов или применений дополнительно включает введение антибиотика. В некоторых вариантах осуществления антибиотик представляет собой макролид. В некоторых вариантах осуществления макролид представляет собой азитромицин и/или кларитромицин. В некоторых вариантах осуществления антибиотик представляет собой доксициклин. В некоторых вариантах осуществления антибиотик представляет собой триметоприм/сульфаметоксазол. В некоторых вариантах осуществления антибиотик представляет собой цефалоспорин. В некоторых вариантах осуществления цефалоспорин представляет собой цефепим, цефиксим, цефподоксим, цефпрозил, цефтазидим и/или цефуроксим. В некоторых вариантах осуществления антибиотик представляет собой пенициллин. В некоторых вариантах осуществления антибиотик представляет собой амоксициллин, ампициллин и/или пивампициллин. В некоторых вариантах осуществления антибиотик представляет собой комбинацию ингибитора пенициллина/β-лактамаз. В некоторых вариантах осуществления комбинация ингибитора пенициллина/β-лактамаз представляет собой амоксициллин/клавуланат и/или пиперациллин/тазобактам. В некоторых вариантах осуществления антибиотик представляет собой фторхинолон. В некоторых вариантах осуществления фторхинолон представляет собой ципрофлоксацин, гемифлоксацин, левофлоксацин, моксифлоксацин и/или офлоксацин.
В некоторых вариантах осуществления любой из предшествующих способов или применений дополнительно включает введение ингибитора фосфодиэстеразы. В некоторых вариантах осуществления ингибитор фосфодиэстеразы представляет собой ингибитор фосфодиэстеразы 5-го типа. В некоторых вариантах осуществления ингибитор фосфодиэстеразы представляет собой аванафил, бензамиденафил, дазантафил, икариин, ломенафил, мироденафил, силденафил, тадалафил, уденафил и/или варденафил. В некоторых вариантах осуществления ингибитор PDE представляет собой ингибитор PDE-4. В некоторых вариантах осуществления ингибитор PDE-4 представляет собой рофлумиласт, циломиласт, тетомиласт и/или CHF6001. В некоторых вариантах осуществления ингибитор PDE представляет собой ингибитор PDE-3/PDE-4. В некоторых вариантах осуществления ингибитор PDE-3/PDE-4 представляет собой RPL-554.
В некоторых вариантах осуществления любой из предшествующих способов или применений дополнительно включает введение цитотоксического и/или иммуносупрессивного агента. В некоторых вариантах осуществления цитотоксический и/или иммуносупрессивный агент представляет собой азатиоприн, колхицин, циклофосфамид, циклоспорин, метотрексат, пеницилламин и/или талидомид. В некоторых вариантах осуществления способ дополнительно включает введение агента, который восстанавливает истощенные уровни глутатиона в легких. В некоторых вариантах осуществления агент, который восстанавливает истощенные уровни глутатиона в легких, представляет собой N-ацетилцистеин. В некоторых вариантах осуществления способ дополнительно включает введение антикоагулянта. В некоторых вариантах осуществления антикоагулянт представляет собой варфарин, гепарин, активированный белок С и/или ингибитор пути тканевого фактора.
В некоторых вариантах осуществления любой из предшествующих способов или применений дополнительно включает введение антагониста рецепторов эндотелина. В некоторых вариантах осуществления антагонист рецепторов эндотелина представляет собой бозентан, макитентан и/или амбризентан. В некоторых вариантах осуществления способ дополнительно включает введение антагониста ФНО-α. В некоторых вариантах осуществления антагонист ФНО-α включает один или более из этанерцепта, адалимумаба, инфликсимаба, цертолизумаба и голимумаба. В некоторых вариантах осуществления способ дополнительно включает введение интерферона гамма-1b.
В некоторых вариантах осуществления любой из предшествующих способов или применений дополнительно включает введение ингибитора интерлейкина (ИЛ). В некоторых вариантах осуществления ингибитор ИЛ представляет собой ингибитор ИЛ-5. В некоторых вариантах осуществления ингибитор ИЛ-5 представляет собой меполизумаб и/или бенилизумаб. В некоторых вариантах осуществления ингибитор ИЛ представляет собой ингибитор ИЛ-17А. В некоторых вариантах осуществления ингибитор ИЛ-17А представляет собой CNTO-6785.
В некоторых вариантах осуществления любой из предшествующих способов или применений дополнительно включает введение ингибитора р38 митоген-активируемой протеинкиназы (МАРК). В некоторых вариантах осуществления ингибитор р38 МАРК представляет собой лозмапимод и/или AZD-7624. В некоторых вариантах осуществления способ дополнительно включает введение антагониста CXCR2. В некоторых вариантах осуществления антагонист CXCR2 представляет собой данириксин.
В некоторых вариантах осуществления любой из предшествующих способов или применений дополнительно включает вакцинацию. В некоторых вариантах осуществления вакцинация представляет собой вакцинацию против пневмококков и/или гриппа. В некоторых вариантах осуществления вакцинация представляет собой вакцинацию против Streptococcus pneumoniae и/или гриппа. В некоторых вариантах осуществления способ дополнительно включает применение противовирусной терапии. В некоторых вариантах осуществления противовирусная терапия представляет собой осельтамивир, перамивир и/или занамивир.
В некоторых вариантах осуществления любой из предшествующих способов или применений дополнительно включает предотвращение гастроэзофагеального рефлюкса и/или повторяющейся микроаспирации.
В некоторых вариантах осуществления любой из предшествующих способов или применений дополнительно включает вентиляционную поддержку. В некоторых вариантах осуществления вентиляционная поддержка представляет собой механическую вентиляцию. В некоторых вариантах осуществления вентиляционная поддержка представляет собой неинвазивную вентиляцию. В некоторых вариантах осуществления вентиляционная поддержка представляет собой оксигенотерапию. В некоторых вариантах осуществления способ дополнительно включает легочную реабилитацию.
В некоторых вариантах осуществления любой из предшествующих способов или применений дополнительно включает трансплантацию легких. В некоторых вариантах осуществления трансплантация легких представляет собой трансплантацию одного легкого. В некоторых вариантах осуществления трансплантация легких представляет собой двустороннюю трансплантацию легких.
В некоторых вариантах осуществления любого из предшествующих способов или применений дополнительно включает нефармакологическое вмешательство. В некоторых вариантах осуществления нефармакологическое вмешательство представляет собой прекращение курения, здоровое питание и/или регулярные физические упражнения. В некоторых вариантах осуществления способ дополнительно включает применение фармакологической помощи для прекращения курения. В некоторых вариантах осуществления фармакологическая помощь для прекращения курения представляет собой никотин-заместительную терапию, бупропион и/или варениклин. В некоторых вариантах осуществления нефармакологическое вмешательство представляет собой пульмональную терапию. В некоторых вариантах осуществления пульмональная терапия представляет собой легочную реабилитацию и/или оксигенотерапию. В некоторых вариантах осуществления нефармакологическое вмешательство представляет собой операцию на легких. В некоторых вариантах осуществления операция на легких представляет собой операцию по уменьшению объема легких, трансплантацию одного легкого, двустороннюю трансплантацию легкиз или буллэктомию. В некоторых вариантах осуществления нефармакологическое вмешательство представляет собой применение устройства. В некоторых вариантах осуществления устройство представляет собой спираль для уменьшения объема легких, трансбронхиальный стент и/или систему поддержки носового дыхания.
Комбинированная терапия может обеспечивать «синергизм» и подтверждает «синергетический» эффект, то есть, эффект, достигаемый, когда активные компоненты, используемые вместе, дают больший эффект, чем сумма эффектов, которые приводят к результатам при использовании соединений по отдельности. Синергетический эффект может быть достигнут, когда активные ингредиенты: (1) совместно составлены и введены или доставлены одновременно в комбинированном стандартном лекарственном составе; (2) доставлены путем чередования, или параллельно в виде отдельных составов; или (3) при помощи какой-либо другой схемы. Комбинированное введение включает совместное введение с использованием отдельных составов или одного фармацевтического состава и последовательное введение в любом порядке, где предпочтительно существует период времени, в течение которого оба (или все) активные вещества одновременно проявляют свои биологические активности. При доставке чередующейся терапии, синергетический эффект может быть достигнут, когда соединения вводят или доставляют последовательно, например, с помощью различных инъекций в отдельных шприцах. Как правило, во время чередующейся терапии эффективную дозировку каждого активного ингредиента вводят последовательно, то есть последовательно, тогда как при комбинированной терапии эффективные дозировки двух или более активных ингредиентов вводят вместе. При последовательном введении комбинацию можно вводить в два или более приемов.
Такие комбинированные способы лечения, отмеченные выше, включают комбинированное введение (где два или более терапевтических агентов включено в один или разные составы) и раздельное введение, в этом случае введение агента (например, антагониста триптазы, антагониста FcεR, антитела, истощающего IgE+ В-клетки, антитела, истощающего тучные клетки или базофилы, антагониста PAR2, антагониста IgE или их комбинации (например, антагониста триптазы и антагониста IgE)) или его фармацевтической композиции может происходить до, одновременно и/или после введения дополнительного терапевтического агента(ов). В одном варианте осуществления введение агента (например, антагониста триптазы, антагониста FcεR, антитела, истощающего IgE+ В-клетки, антитела, истощающего тучные клетки или базофилы, антагониста PAR2, антагониста IgE или их комбинации (например, антагониста триптазы и антагониста IgE)) или его фармацевтической композиции, и введение дополнительного терапевтического агента происходит в течение около одного месяца; или в течение около одной, двух или трех недель; или в течение одного, двух, трех, четырех, пяти или шести суток; или в течение около 1, 2, 3, 4, 5, 6, 7, 8 или 9 часов; или в течение около 1,5,10, 20, 30, 40 или 50 минут друг от друга. Для вариантов осуществления, включающих последовательное введение, агент (например, антагонист триптазы, антагонист Fc-эпсилон-рецептора (FcεR), антитело, истощающее IgE+ В-клетки, антитело, истощающее тучные клетки или базофилы, антагонист активируемого протеазой рецептора 2 (PAR2), антагонист IgE или их комбинацию (например, антагонист триптазы и антагонист IgE)) можно вводить до или после введения дополнительного терапевтического агента(ов).
В любом из предшествующих способов или применений терапия (например, терапия, включающая антагонист триптазы, антагонист FcεR, антитело, истощающее IgE+ В-клетки, антитело, истощающее тучные клетки или базофилы, антагонист PAR2, антагонист IgE или их комбинацию (например, антагонист триптазы и антагонист IgE)) и любой дополнительный терапевтический агент можно вводить любым подходящим способом, в том числе парентерально, внутрибрюшинно, внутримышечно, внутривенно, внутрикожно, чрескожно, внутриартериально, внутриочагово, интракраниально, внутрисуставно, внутрь простаты, внутриплеврально, интратрахеально, интратекально, интраназально, интравагинально, ректально, местно, внутриопухолево, подкожно, субконъюнктивально, интравезикулярно, мукозально, интраперикардиально, внутрипуповинно, интраокулярно, интрабитально, перорально, местно, трансдермально, интравитреально, периокулярно, в конъюнктивальную полость, в субтеноновое пространство, внутрикамерно, субретинально, ретробульбарно, внутриканально, путем ингаляции, инъекции, имплантации, инфузии, непрерывной инфузии, локализованной перфузии непосредственно в целевых клетках, при помощи катетера, путем лаважа, в кремах или в липидных композициях. Введение может быть системным или местным. Кроме того, антагонист может быть соответствующим образом введен путем импульсной инфузии, например, при снижении дозы антагониста.
Любой терапевтический агент, например, антагонист триптазы, антагонист FcεR, антитело, истощающее IgE+ В-клетки, антитело, истощающее тучные клетки или базофилы, антагонист PAR2, антагонист IgE, их комбинация (например, антагонист триптазы и антагонист IgE), любой дополнительный терапевтический агент или их фармацевтические композиции будут составлены, дозированы и введены таким образом, чтобы это соответствовало надлежащей медицинской практике. Такие дозировки известны в данной области техники. Факторы, подлежащие рассмотрению в этом контексте, включают конкретное расстройство, которое лечат, конкретное млекопитающее, которое лечат, клиническое состояние отдельного пациента, причину расстройства, место доставки агента, способ введения, график введения и другие факторы, известные врачам. Антагонист триптазы, антагонист FcεR, антитело, истощающее IgE+ В-клетки, антитело, истощающее тучные клетки или базофилы, антагонист PAR2, антагонист IgE или их фармацевтическая композиция необязательна, но, возможно, составлены с одним или более агентами, используемыми в настоящее время для предотвращения или лечения рассматриваемого в данном документе расстройства. Эффективное количество таких других агентов зависит от количества антитела, присутствующего в составе, типа расстройства или лечения и других факторов, обсуждаемых выше. Они, как правило, используются в тех же дозировках и с путями введения, как описано в данном документе, или приблизительно от 1 до 99% дозировок, описанных в данном документе, или в любой дозировке и любым путем, который эмпирически/клинически определен как подходящий.
В качестве одного примера, для предотвращения или лечения заболевания, подходящую дозировку антитела (например, антитела против триптазы, антитела против IgE (например, XOLAIR®), антитела, истощающего IgE+ В-клетки (например, антитела против домена М1' (например, квилизумаба)), антитела, истощающего тучные клетки или базофилы, или антитела против PAR2) (при использовании отдельно или в комбинации с одним или более другими дополнительными терапевтическими агентами) будет зависеть от типа заболевания подлежащего лечению, типа антитела, степени тяжести и течения заболевания, вводится ли антитело в профилактических или терапевтических целях, предшествующей терапии, истории болезни пациента и ответа на антитело, и усмотрения лечащего врача. Антитело легко вводить пациенту одноразово или в течение серии курсов лечения. В зависимости от типа и тяжести заболевания, от 1 мкг/кг до 15 мг/кг (например, от 0,1 мг/кг до 10 мг/кг) антитела могут быть начальной потенциальной дозой для введения пациенту, будь то, например, одно или более отдельных введений или непрерывная инфузия. Одна типичная суточная доза может находится в диапазоне от около 1 мкг/кг до 200 мг/кг или более в зависимости от вышеуказанных факторов. В случае повторных введений в течение нескольких суток или более, в зависимости от состояния, лечение, как правило, проводят до достижения желаемой степени подавления симптомов заболевания. Одна иллюстративная доза антитела должна находиться в диапазоне от около 0,05 мг/кг до около 10 мг/кг. Таким образом, пациенту может быть введена одна или более доз около 0,5 мг/кг, 2,0 мг/кг, 4,0 мг/кг или 10 мг/кг (или любая их комбинация). Такие дозы можно вводить периодически, например, каждую неделю, каждые две недели, каждые три недели или каждые четыре недели (например, так, чтобы пациент получал от около двух до около двадцати или, например, около шести доз антитела). Например, дозу можно вводить один раз в месяц. Может быть введена начальная более высокая нагрузочная доза, за которой следует одна или несколько более низких доз. Однако, могут быть полезными другие схемы приема лекарственного средства. Эффективность такой терапии легко контролировать при помощи традиционных методик и методов анализа. В некоторых случаях можно вводить дозу от около 50 мг/мл до около 200 мг/мл, например, около 50 мг/мл, около 60 мг/мл, около 70 мг/мл, около 80 мг/мл, около 90 мг/мл, около 100 мг/мл, около 110 мг/мл, около 120 мг/мл, около 130 мг/мл, около 140 мг/мл, около 150 мг/мл, около 160 мг/мл, около 170 мг/мл, около 180 мг/мл, около 190 мг/мл или около 200 мг/мл антитела. В некоторых вариантах осуществления дозировка XOLAIR® (омализумаба) для пациентов с астмой может быть определена на основании массы тела и уровней IgE перед лечением с использованием подходов, известных в данной области техники. XOLAIR® (омализумаб) можно вводить при помощи подкожной инъекции каждые четыре недели в дозе 300 или 150 мг на дозу для лечения CIU.
В любом из предшествующих способов или применений в некоторых вариантах осуществления воспалительное заболевание, опосредованное тучными клетками, выбрано из группы, состоящей из астмы, атопического дерматита, крапивницы (например, CSU или CIU), системной анафилаксии, мастоцитоза, хронической обструктивной болезни легких (ХОБЛ), идиопатического легочного фиброза (IPF) и эозинофильного эзофагита.
В некоторых вариантах осуществления любого из предшествующих способов или применений воспалительное заболевание, опосредованное тучными клетками, представляет собой астму. В некоторых вариантах осуществления астма представляет собой хроническую персистирующую тяжелую астму с серьезными явлениями ухудшения симптомов (приступы или обострения), которые могут быть опасными для жизни. В некоторых вариантах осуществления астма представляет собой атопическую (также известную как аллергическую) астму, неаллергическую астму (например, часто вызываемую респираторной вирусной инфекцией (например, гриппом, парагриппом, риновирусом, человеческим метапнеемовирусом и респираторным синцитиальным вирусом) или вдыхаемым раздражителем (например, загрязнителями воздуха, смогом, частицами дизельного топлива, летучими химическими веществами и газами в помещении или на улице, или даже холодным сухим воздухом).
В некоторых вариантах осуществления любого из предшествующих способов или применений астма является эпизодической или вызванной физической нагрузкой астмой из-за острого или хронического первичного или вторичного воздействия «дыма» (как правило, сигарет, сигар или трубок), вдыхания или «парения» (табака, марихуаны или других подобных веществ), или астмой, вызванной недавним приемом аспирина или родственных НПВП. В некоторых вариантах осуществления астма представляет собой легкую или нелеченную кортикостероидами астму, недавно диагностированную и нелеченную астму или ранее не требующую хронического применения ингаляционных местных или системных стероидов для контроля симптомов (кашля, стерторозного дыхания, диспноэ/одышки или боли в груди). В некоторых вариантах осуществления астма представляет собой хроническую, резистентную к кортикостероидам астму, рефрактерную к кортикостероидам астму, или астму, неконтролируемую кортикостероидами, или другими лекарственными препаратами для контроля хронической астмы.
В некоторых вариантах осуществления любого из предшествующих способов или применений астма представляет собой астму от умеренной до тяжелой. В определенных вариантах осуществления астма представляет собой астму с высоким уровнем TH2. В некоторых вариантах осуществления астма представляет собой тяжелую астму. В некоторых вариантах осуществления астма представляет собой атопическую астму, аллергическую астму, неаллергическую астму (например, вследствие инфекции и/или респираторно-синцитиального вируса (РСВ)), астму, вызванную физической нагрузкой, чувствительную к аспирину/индуцированную аспирином астму, легкую астму, умеренную или тяжелую астму, нелеченную кортикостероидами астму, хроническую астму, резистентную к кортикостероидам астму, рефрактерную к кортикостероидам астму, недавно диагностированную и нелеченную астма, астму, вызванную курением, астму, неконтролируемую кортикостероидами. В некоторых вариантах осуществления астма представляет собой эозинофильную астму. В некоторых вариантах осуществления астма представляет собой аллергическую астму. В некоторых вариантах осуществления индивидуум был определен как положительный по эозинофильному воспалению (EIP). Смотри WO 2015/061441. В некоторых вариантах осуществления астмой представляет собой астму с высоким уровнем периостина (например, при которой уровень периостина по меньшей мере любой из около 20 нг/мл, 25 нг/мл или 50 нг/мл сыворотки). В некоторых вариантах осуществления астма представляет собой астму с высоким уровнем эозинофилов (например по меньшей мере любым количеством из около 150, 200, 250, 300, 350, 400 эозинофилов/мл крови). В определенных вариантах осуществления астма представляет собой астму с низким уровнем TH2. В некоторых вариантах осуществления индивидуум был определен как отрицательный по эозинофильному воспалению (EIN). Смотри WO2015/061441. В некоторых вариантах осуществления астма представляет собой астму с низким уровнем периостина (например, с уровнем периостина менее чем около 20 нг/мл сыворотки). В некоторых вариантах осуществления астма представляет собой астму с низким уровнем эозинофилов (например, менее чем около 150 эозинофилов/мкп крови или менее чем около 100 эозинофилов/мкп крови).
Например, в конкретных вариантах осуществления любого из предшествующих способов или применений астма представляет собой астму от умеренной до тяжелой. В некоторых вариантах осуществления астма не контролируется кортикостероидами. В некоторых вариантах осуществления астма представляет собой астму с высоким уровнем TH2 или астму с низким уровнем TH2. В конкретных вариантах осуществления астма представляет собой астму с высоким уровнем TH2.
III. Диагностические способы согласно данному изобретению
Данное изобретение относится к способам определения того, могут ли пациенты с воспалительным заболеванием, опосредованным тучными клетками, (например, астму), отвечать на терапию (например, терапию, включающую агент, выбранный из группы, состоящей из антагониста триптазы, антагониста Fc-эпсилона-рецептора (FcεR), антитела, истощающего IgE+ В-клетки, антитела, истощающего тучные клетки или базофилы, антагониста активируемого протеазой рецептора 2 (PAR2), антагониста IgE и их комбинации (например, антагониста триптазы и антагониста IgE)), способам выбора терапии для пациента с воспалительным заболеванием, опосредованным тучными клетками, способам оценки ответа пациента с воспалительным заболеванием, опосредованным тучными клетками, и способам контроля ответа пациента с воспалительным заболеванием, опосредованным тучными клетками. В некоторых вариантах осуществления терапия представляет собой терапию, направленную на тучные клетки (например, терапию, которая включает антагонист триптазы, антагонист IgE, антитело, истощающее IgE+ В-клетки, антитело, истощающее тучные клетки или базофилы, и/или антагонист PAR2). В некоторых вариантах осуществления терапия включает антагонист триптазы (например, антитело против триптазы, например, любое антитело против триптазы, описанное в данном документе или в WO 2018/148585) и антагонист IgE (например, антитело против IgE, например, омализумаб (XOLAIR®)).
Присутствие и/или уровень экспрессии биомаркера согласно изобретению (например, количества активных аллелей триптазы и/или триптазы) могу быть определены с использованием любого из описанных в данном документе анализов или с помощью любого метода или анализа, известных в данной области техники. В некоторых вариантах осуществления способы дополнительно включают применение терапии у пациента, например, как описано в Разделе II подробного описания сущности изобретения выше. Способы могут проводиться в различных форматах анализа, включая анализы, определяющие генетическую информацию (например, секвенирование ДНК или РНК), экспрессию гена или белка (например, полимеразную цепную реакцию (ПЦР) и иммуноферментные анализы) и биохимические анализы, определяющие соответствующую активность, например, как описано ниже.
Например, в одном аспекте изобретение относится к способу определения того, может ли пациент с воспалительным заболеванием, опосредованным тучными клетками, отвечать на терапию, направленную на тучные клетки, (например, терапию, включающую агент, выбранный из группы, состоящей из антагониста триптазы, антагониста IgE, антитела, истощающего IgE+ В-клетки, антитела, истощающего тучные клетки или базофилы, антагониста PAR2 и их комбинации (например, антагониста триптазы и антагониста IgE)), причем способ включает: (а) определение в образце от пациента с воспалительным заболеванием, опосредованным тучными клетками, количества активных аллелей триптазы у пациента; и (b) идентификацию пациента, имеющего вероятность ответа на терапию, направленную на тучные клетки, (например, терапию, включающую агент, выбранный из группы, состоящей из антагониста триптазы, антагониста IgE, антитела, истощающего IgE+ В-клетки, антитела, истощающего тучные клетки или базофилы, антагониста PAR2, и их комбинации (например, антагониста триптазы и антагониста IgE)), на основании количества активных аллелей триптазы у пациента, причем количество активных аллелей триптазы, равное или превышающее эталонное количество активных аллелей триптазы, указывает что пациент имеет повышенную вероятность ответа на терапию. В некоторых вариантах осуществления способ дополнительно включает применение терапии у пациента.
В другом примере изобретение относится к способу определения того, может ли пациент с воспалительным заболеванием, опосредованным тучными клетками, отвечать на терапию, направленную на тучные клетки, (например, терапию, включающую агент, выбранный из группы, состоящей из антагониста триптазы, антагониста IgE, антитела, истощающего IgE+ В-клетки, антитела, истощающего тучные клетки или базофилы, антагониста активируемого протеазой рецептора 2 (PAR2) и их комбинации (например, антагониста триптазы и антагониста IgE)), причем способ включает: (а) определение уровня экспрессии триптазы в образце от пациента с воспалительным заболеванием, опосредованным тучными клетками; и (b) идентификацию пациента, имеющего вероятность ответа на терапию, направленную на тучные клетки, (например, терапию, включающую агент, выбранный из группы, состоящей из антагониста триптазы, антагониста IgE, антитела, истощающего IgE+ В-клетки, антитела, истощающего тучные клетки или базофилы, антагониста PAR2, и их комбинации (например, антагониста триптазы и антагониста IgE)), на основании уровня экспрессии триптазы в образце от пациента, причем уровень экспрессии триптазы в образце, равный или превышающий эталонный уровень триптазы, указывает на то, что пациент имеет повышенную вероятность ответа на терапию. В некоторых вариантах осуществления способ дополнительно включает применение терапии у пациента.
В некоторых вариантах осуществления любого из предшествующих способов пациент был идентифицирован как имеющий уровень биомаркера 2-го типа в образце от пациента, который ниже эталонного уровня биомаркера 2-го типа. В некоторых вариантах осуществления агент применяют у пациента в виде монотерапии.
В некоторых вариантах осуществления любого из предшествующих способов пациент был идентифицирован как имеющий уровень биомаркера 2-го типа в образце от пациента, который равен или выше эталонного уровня биомаркера 2-го уровня. В некоторых вариантах осуществления способ дополнительно включает введение ингибитора пути TH2 пациенту.
В другом аспекте изобретение относится к способу определения того, может ли пациент с воспалительным заболеванием, опосредованным тучными клетками, отвечать на терапию, включающую антагонист IgE или антагонист FcεR, который включает (а) определение в образце от пациента с воспалительным заболеванием, опосредованным тучными клетками, количества активных аллелей триптазы у пациента; и (b) идентификацию пациента, имеющего вероятность ответа на терапию, включающую антагонист IgE или антагонист FcεR, на основании количества активных аллелей триптазы пациента, причем количество активных аллелей триптазы ниже эталонного количества активных аллелей триптазы указывает на то, что пациент имеет повышенную вероятность ответа на терапию. В некоторых вариантах осуществления способ дополнительно включает применение терапии у пациента.
В другом примере изобретение относится к способу определения того, может ли пациент с воспалительным заболеванием, опосредованным тучными клетками, отвечать на терапию, включающую антагонист IgE или антагонист FcεR, который включает (а) определение уровня экспрессии триптазы в образце от пациента с воспалительным заболеванием, опосредованным тучными клетками; и (b) идентификацию пациента, имеющего вероятность ответа на терапию, включающую антагонист IgE или антагонист FcεR, на основании уровня экспрессии триптазы в образце от пациента, причем уровень экспрессии триптазы в образце от пациента ниже эталонного уровня триптазы указывает на то, что пациент имеет повышенную вероятность ответа на терапию. В некоторых вариантах осуществления способ дополнительно включает применение терапии у пациента.
В некоторых вариантах осуществления любого из предшествующих способов пациент был идентифицирован как имеющий уровень биомаркера 2-го типа в образце от пациента, который равен или выше эталонного уровня биомаркера 2-го уровня. В некоторых вариантах осуществления способ дополнительно включает введение пациенту дополнительного ингибитора пути TH2.
В дополнительном примере изобретение относится к способу выбора терапии для пациента с воспалительным заболеванием, опосредованным тучными клетками, который включает (а) определение в образце от пациента с воспалительным заболеванием, опосредованным тучными клетками, количества активных аллелей триптазы у пациента; и: (b) выбор для пациента: (i) терапии, направленной на тучные клетки (например, терапии, включающей агент, выбранный из группы, состоящей из антагониста триптазы, антагониста IgE, антитела, истощающего IgE+ В-клетки, антитела, истощающего тучные клетки или базофилы, антагониста PAR2, и их комбинации (например, антагониста триптазы и антагониста IgE)), если количество активных аллелей триптазы у пациента равно или выше эталонного количества активных аллелей триптазы, или (и) терапию, включающую антагонист IgE или антагонист FcεR, если количество активных аллелей триптазы у пациента ниже эталонного количества активных аллелей триптазы. В некоторых вариантах осуществления способ дополнительно включает применение терапии, выбранной в соответствии с (b), у пациента.
В еще одном примере изобретение относится к способу выбора терапии для пациента с воспалительным заболеванием, опосредованным тучными клетками, который включает (а) определение уровня экспрессии триптазы в образце от пациента с воспалительным заболеванием, опосредованным тучными клетками; и (b) выбор для пациента: (i) терапии, направленной на тучные клетки, (например, терапии, включающей агент, выбранный из группы, состоящей из антагониста триптазы, антагониста IgE, антитела, истощающего IgE+ В-клетки, антитела, истощающего тучные клетки или базофилы, антагониста PAR2, и их комбинации (например, антагониста триптазы и антагониста IgE)), если уровень экспрессии триптазы в образце от пациента равен или выше эталонного уровня триптазы, или (ii) терапии, включающей антагонист IgE или антагонист FcεR, если уровень экспрессии триптазы в образце от пациента ниже эталонного уровня триптазы. В некоторых вариантах осуществления способ дополнительно включает применение терапии, выбранной в соответствии с (b), у пациента.
В некоторых вариантах осуществления любого из предшествующих аспектов пациент был идентифицирован как имеющий уровень биомаркера 2-го типа в образце от пациента, который ниже эталонного уровня биомаркера 2-го типа. В некоторых вариантах осуществления агент применяют у пациента в виде монотерапии.
В некоторых вариантах осуществления любого из предшествующих аспектов пациент был идентифицирован как имеющий уровень биомаркера 2-го типа в образце от пациента, который равен или выше эталонного уровня биомаркера 2-го типа, и способ дополнительно включает выбор комбинированной терапии, включающей ингибитор пути TH2. В некоторых вариантах осуществления способ дополнительно включает введение ингибитора пути TH2 (или дополнительного ингибитора пути TH2) пациенту.
Изобретение также относится к способу оценки ответа пациента с воспалительным заболеванием, опосредованным тучными клетками, на лечение терапией, направленной на лечение тучными клетками (например, терапией, включающей агент, выбранный из группы, состоящей из антагониста триптазы, антагониста IgE, антитела, истощающего IgE+ В-клетки, антитела, истощающего тучные клетки или базофилы, антагониста PAR2 и их комбинации (например, антагониста триптазы и антагониста IgE)), причем способ включает: (а) определение уровня экспрессии триптазы в образце от пациента с воспалительным заболеванием, опосредованным тучными клетками, в течение или после применения терапии, направленной на тучные клетки, (например, терапии, включающей агент, выбранный из группы, состоящей из антагониста триптазы, антагониста IgE, антитела, истощающего IgE+ В-кпетки, антитела, истощающего тучные клетки или базофилы, антагониста PAR2, и их комбинации (антагониста триптазы и антагониста IgE)), у пациента; и (b) поддержание, корректировку или прекращение лечения на основе сравнения уровня экспрессии триптазы в образце с эталонным уровнем триптазы, причем изменение уровня экспрессии триптазы в образце от пациента по сравнению с эталонным уровнем указывает на ответ на лечение терапией. В некоторых вариантах осуществления изменение представляет собой повышение уровня экспрессии триптазы, и лечение продолжают. В других вариантах осуществления изменение представляет собой снижение уровня экспрессии триптазы, и лечение корректируют или прекращают.
В другом примере изобретение относится к способу контроля ответа пациента с воспалительным заболеванием, опосредованным тучными клетками, которого лечат терапией, направленной на тучные клетки, (например, терапией, включающей агент, выбранный из группы, состоящей из антагониста триптазы, антагониста IgE, антитела, истощающего IgE+ В-кпетки, антитела, истощающего тучные клетки или базофилы, антагониста PAR2 и их комбинации (например, антагониста триптазы и антагониста IgE)), причем способ включает: (а) определение уровня экспрессии триптазы в образце от пациента в течение или после применения терапии, направленной на тучные клетки, (например, терапии, включающей агент, выбранный из группы, состоящей из антагониста триптазы, антагониста IgE, антитела, истощающего IgE+ В-клетки, антитела, истощающего тучные клетки или базофилы, антагониста PAR2, и их комбинации (например, антагониста триптазы и антагониста IgE), у пациента); и (b) сравнение уровня экспрессии триптазы в образце от пациента с эталонным уровнем триптазы, таким образом, отслеживая ответ пациента, проходящего лечение терапией. В некоторых вариантах осуществления изменение представляет собой повышение уровня экспрессии триптазы, и лечение продолжают.В других вариантах осуществления изменение представляет собой снижение уровня экспрессии триптазы, и лечение корректируют или прекращают.
В некоторых вариантах осуществления любого из предшествующих способов количество активных аллелей триптазы определяют путем секвенирования локусов TPSAB1 и TPSB2 генома пациента. Можно использовать любой подходящий подход секвенирования, например секвенирование по Сэнгеру или массовое параллельное секвенирование (например, ILLUMINA®). В некоторых вариантах осуществления локус TPSAB1 секвенируют при помощи способа, включающего (i) амплификацию нуклеиновой кислоты от субъекта в присутствии первого прямого праймера, содержащего нуклеотидную последовательность 5'-CTG GTG TGC AAG GTG ААТ GG-3' (SEQ ID NO: 31) и первого обратного праймера, содержащего нуклеотидную последовательность 5'AGG ТСС AGC ACT CAG GAG GA-3' (SEQ ID NO: 32) для получения ампликона TPSAB1, и (ii) секвенирования ампликона TPSAB1. В некоторых вариантах осуществления секвенирование ампликона TPSAB1 включает использование первого прямого праймера и первого обратного праймера. В некоторых вариантах осуществления локус TPSB2 секвенируют при помощи способа, включающего (i) амплификацию нуклеиновой кислоты от субъекта в присутствии второго прямого праймера, содержащего нуклеотидную последовательность 5'-GCA GGT GAG ССТ GAG AGT СС-3' (SEQ ID NO: 33), и второго обратного праймера, содержащего нуклеотидную последовательность 5-GGG АСС ТТС АСС TGC ТТС AG-3' (SEQ ID NO: 34) для получения ампликона TPSB2, и (ii) секвенирования ампликона TPSB2. В некоторых вариантах осуществления изобретения секвенирование ампликона TPSB2 включает применение второго прямого праймера и обратного праймера для секвенирования, содержащего нуклеотидную последовательность 5'-CAG CCA GTG АСС CAG САС-3' (SEQ ID NO: 35). В некоторых вариантах осуществления количество активных аллелей триптазы может быть определено путем определения присутствия любых вариаций в локусах TPSAB1 и TPSB2 генома пациента. В некоторых вариантах осуществления количество активных аллелей триптазы определяется по формуле: 4 - сумма количества аллелей альфа-триптазы и бета-III-триптазы со сдвигом рамки (бета-IIIFS) в генотипе пациента В некоторых вариантах осуществления альфа-триптазу определяют путем обнаружения ОНП с733 G>C в TPSAB1. В некоторых вариантах осуществления обнаружение ОНП с733 G> А в TPSAB1 включает обнаружение генотипа пациента с полиморфизмом CTGCAGGCGGGCGTGGTCAGCTGGG[G/A]CGAGGGCTGTGCCCAGCCCAACCGG (SEQ ID NO: 36), причем присутствие А в ОНП с733 G> А указывает на альфа-триптазу. В некоторых вариантах осуществления бета-IIIFS-триптазу обнаруживают путем обнаружения мутации c980_981insC в TPSB2. В некоторых вариантах осуществления обнаружение мутации c980_981insC в TPSB2 включает обнаружение нуклеотидной последовательности CACACGGTCACCCTGCCCCCTGCCTCAGAGACCTTCCCCCCC (SEQ ID NO: 37). В некоторых вариантах осуществления любого из предшествующих способов количество активных аллелей триптазы у пациена равно 3 или 4. В некоторых вариантах осуществления количество активных аллелей триптазы равно 3. В других вариантах осуществления количество активных аллелей триптазы равно 4.
В других вариантах осуществления любого из предшествующих способов количество активных аллелей триптазы у пациента равно 0, 1 или 2. В некоторых вариантах осуществления количество активных аллелей триптазы равно 0. В некоторых вариантах осуществления количество активных аллелей триптазы равно 1. В других вариантах осуществления количество активных аллелей триптазы равно 2.
В некоторых вариантах осуществления любого из предшествующих способов эталонное количество активных аллелей триптазы может быть определено в эталонном образце, эталонной популяции и/или может быть предварительно заданным значением (например, пороговым значением, которое ранее было определено для значимого (например, статистически значимого) разделения первой субпопуляции индивидуумов от второй субпопуляции индивидуумов (например, с точки зрения ответа на терапию (например, терапию, включающую агент, выбранный из группы, состоящей из антагониста триптазы, антагониста IgE, антагониста FcεR, антитела, истощающего IgE+ В-клетки, антитела, истощающего тучные клетки или базофилы, антагониста PAR2 и их комбинации (например, антагониста триптазы и антагонисат IgE))). В некоторых вариантах осуществления эталонное количество активных аллелей триптазы представляет собой предварительно определенное значение. В некоторых вариантах осуществления эталонное количество активных аллелей триптазы предварительно определяют при воспалительном заболевании, опосредованном тучными клетками, которым страдает пациент (например, при астме). В определенных вариантах осуществления количество активных аллелей триптазы определяют по общему распределению значений при исследуемом воспалительном заболевании, опосредованным тучными клетками, (например, астмой), или в данной популяции. В некоторых вариантах осуществления эталонное количество активных аллелей триптазы представляет собой целое число в диапазоне от 0 до 4 (например, 0, 1, 2, 3 или 4). В конкретных вариантах осуществления эталонное количество активных аллелей триптазы равно 3.
Любой из предшествующих способов может включать определение уровня экспрессии одного или более биомаркеров 2-го типа. В некоторых вариантах осуществления биомаркер 2-го типа представляет собой связанный с клеткой TH2 цитокин, периостин, количество эозинофилов, профиль эозинофилов, FeNO или IgE. В некоторых вариантах осуществления цитокин, связанный с клеткой TH2, представляет собой ИЛ-13, ИЛ-4, ИЛ-9 или ИЛ-5.
В любом из предыдущих способов генотип пациента может быть определен с помощью любого из способов или анализов, описанных в данном документе, (например, в Разделе IV подробного описания сущности изобретения или в Примере 1), или известных в данной области техники.
В некоторых вариантах осуществления любого из предшествующих способов уровень экспрессии биомаркера представляет собой уровень экспрессии белка. Например, в некоторых вариантах осуществления уровень экспрессии белка измеряют с использованием иммуноанализа (например, мультиплексного иммуноанализа), ИФА, вестерн-блоттинга или масс-спектрометрии. В некоторых вариантах осуществления уровень экспрессии белка триптазы представляет собой уровень экспрессии активной триптазы. В других вариантах осуществления уровень экспрессии белка триптазы представляет собой уровень экспрессии общей триптазы.
В других вариантах осуществления любого из предшествующих способов уровень экспрессии биомаркера представляет собой уровень экспрессии мРНК. Например, в некоторых вариантах осуществления уровень экспрессии мРНК измеряют с использованием метода ПЦР (например, кПЦР) или микроматричного чипа.
В некоторых вариантах осуществления любого из предшествующих способов эталонный уровень биомаркера представляет собой уровень биомаркера, определенный в группе индивидуумов, страдающих астмой. Например, в некоторых вариантах осуществления эталонный уровень представляет собой медианный уровень.
Любой подходящий образец, полученный от пациента, может быть использован в любом из предыдущих способов. Например, в некоторых вариантах осуществления образец, полученный от пациента, представляет собой образец крови (например, образец цельной крови, образец сыворотки, образец плазмы или их комбинацию), образец ткани, образец мокроты, образец бронхиального лаважа, образец жидкости слизистой оболочки (MLF), бронхосорбционный образец и назосорбционный образец.
В любом из предшествующих способов уровень экспрессии биомаркера согласно изобретению (например, триптазы) в образце, полученном от пациента, может быть изменен на/в по меньшей мере около 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 100%, 2 раза, 3 раза, 4 раза, 5 раз, 6 раз, 7 раз, 8 раз, 9 раз, 10 раз, 11 раз, 12 раз, 13 раз, 14 раз, 15 раз, 16 раз или более относительно эталонного уровня биомаркера. Например, в некоторых вариантах осуществления уровень экспрессии биомаркера согласно изобретению в образце, полученном от пациента, может быть увеличен на/в по меньшей мере около 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 100%, 2 раза, 3 раза, 4 раза, 5 раз, 6 раз, 7 раз, 8 раз, 9 раз, 10 раз, 11 раз, 12 раз, 13 раз, 14 раз, 15 раз, 16 раз или более относительно эталонного уровня биомаркера. В других вариантах осуществления уровень экспрессии биомаркера согласно изобретению в образце, полученном от пациента, может быть уменьшен на/в по меньшей мере около 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 100%, 2 раза, 3 раза, 4 раза, 5 раз, 6 раз, 7 раз, 8 раз, 9 раз, 10 раз, 11 раз, 12 раз, 13 раз, 14 раз, 15 раз, 16 раз или более относительно эталонного уровня биомаркера.
В некоторых вариантах осуществления любого из предшествующих способов эталонный уровень может быть установлен на любой процентиль между, например, 20-м процентилем и 99-м процентилем (например, 20-й, 25-й, 30-й, 35-й, 40-й, 45-й, 50-й, 55-й, 60-й, 65-й, 70-й, 75-й, 80-й, 85-й, 90-й, 95-й или 99-й процентиль) общего распределения уровня экспрессии биомаркера (например, триптазы), например, у здоровых субъектов или у пациентов с расстройством (например, воспалительным заболеванием, опосредованным тучными клетками, (например, астмой)). В некоторых вариантах осуществления эталонный уровень может быть установлен на 25-й процентиль общего распределения значений в популяции пациентов с астмой. В других вариантах осуществления эталонный уровень может быть установлен на 50-й процентиль общего распределения значений в популяции пациентов с воспалительным заболеванием, опосредованным тучными клетками, (например, астмой). В еще других вариантах осуществления эталонный уровень может представлять собой медиану общего распределения значений в популяции пациентов с воспалительным заболеванием, опосредованным тучными клетками, (например, астмой).
В любом из предшествующих способов пациент может иметь повышенный уровень биомаркера TH2 относительно эталонного уровня. В некоторых вариантах осуществления биомаркер TH2 выбран из группы, состоящей из сывороточного периостина, фракции оксида азота в выдыхаемом воздухе (FeNO), количества эозинофилов в мокроте и количества эозинофилов в периферической крови. В некоторых вариантах осуществления биомаркер TH2 представляет собой сывороточный периостин. Например, пациент может иметь уровень сывороточного периостина около 20 нг/мл или выше (например, около 20 нг/мл, около 25 нг/мл, около 30 нг/мл, около 35 нг/мл, около 40 нг/мл, около 45 нг/мл, около 50 нг/мл или выше). В других вариантах осуществления пациент может иметь уровень сывороточного периостина около 50 нг/мл или выше (например, около 50 нг/мл, около 55 нг/мл, около 60 нг/мл, около 65 нг/мл, около 70 нг/мл, около 75 нг/мл, около 80 нг/мл или выше). Уровни сывороточного периостина могут быть определены с использованием любого подходящего способа, например, иммуноферментного анализа (ИФА). В данном документе описаны подходящие подходы.
В некоторых вариантах осуществления любого из предшествующих способов терапия включает антагонист триптазы. Антагонист триптазы может быть антагонистом альфа-триптазы (например, антагонист альфа-1-триптазы) или антагонист бета-триптазы (например, бета-1-триптаза, бета-2-триптаза и/или антагонист бета-3-триптазы). В некоторых вариантах осуществления антагонист триптазы представляет собой антагонист альфа-триптазы и антагонист бета-триптазы. В некоторых вариантах осуществления антагонист триптазы (например, антагонист альфа-триптазы и/или антагонист бета-триптазы) представляет собой антитело против триптазы (например, антитело против альфа-триптазы и/или антитело против бета-триптазы). Можно использовать любое антитело против триптазы, описанное в Разделе VII ниже.
В некоторых вариантах осуществления любого из предшествующих способов терапия включает антагонист FcεR. В некоторых вариантах осуществления антагонист FcεR ингибирует FcεRlα, FcεRlβ и/или FcεRlγ. В других вариантах осуществления антагонист FcεR ингибирует FcεRlI. В еще других вариантах осуществления антагонист FcεR ингибирует член сигнального пути FcεR. Например, в некоторых вариантах осуществления антагонист FcεR ингибирует тирозин-протеинкиназу Lyn (Lyn), тирозинкиназу Брутона (ВТК), тирозин-протеинкиназу Fyn (Fyn), связанную с селезенкой тирозинкиназу (Syk), линкер для активации Т-клеток (LAT), белок-2, связанный с рецептором фактора роста (Grb2), белок «son of sevenless» (Sos), Ras, Raf-1, митоген-активируемую протеинкиназу 1 (MEK), митоген-активируемую протеинкиназу 1 (ERK), цитозольную фосфолипазу А2 (cPLA2), арахидонат-5-липоксигеназу (5-LO), арахидонат-5-липоксигеназа-активирующий белок (FLAP), фактор обмена гуаниновых нуклеотидов VAV (Vav), Rac, киназу-3 митоген-активируемой протеинкиназы, киназу-7 митоген-активируемой протеинкиназы, р38 МАР-киназу (р38), c-Jun-N-концевую киназу (JNK), белок-2, ассоциированный с белком-2, который связан с рецептором фактора роста (Gab2), фосфатидилинозитол-4,5-бисфосфат-3-киназу (PI3K), фосфолипазу С гамма (PLCy), протеинкиназу С (РКС), 3-фосфоинозитид-зависимую протеинкиназу 1 (PDK1), RAC серин/треонин-протеинкиназу (АКТ), гистамин, гепарин, интерлейкин (ИЛ) -3, ИЛ-4, ИЛ-13, ИЛ-5, гранулоцитарно-макрофагальный колониестимулирующий фактор (ГМ-КСФ), фактор некроза опухоли-альфа (ФНО-а), лейкотриены (например, LTC4, LTD4 и LTE4) и простагландины (например, PDG2). В некоторых вариантах осуществления антагонист FcεR представляет собой ингибитор ВТК (например, GDC-0853, акалабрутиниб, GS-4059, спебрутиниб, BGB-3111 или НМ71224).
В некоторых вариантах осуществления любого из предшествующих способов терапия включает агент, истощающий IgE+ В-клетки (например, антитело, истощающее IgE+ В-клетки). В некоторых вариантах осуществления антитело, истощающее IgE+ В-клетки, представляет собой антитело против домена М1. Может быть использовано любое подходящее антитело против домена MV, например, любое антитело против домена MV, описанное в публикации международной патентной заявки №WO 2008/116149, которая полностью включена в данный документ посредством ссылки. В некоторых вариантах осуществления антитело против домена М1' является афукозилированным. В некоторых вариантах осуществления антитело против домена М1' представляет собой килизумаб или 47Н4 (см., например,, Brightbill et al. J. Clin. Invest. 120(6):2218-2229, 2010).
В некоторых вариантах осуществления любого из предшествующих способов терапия включает агент, истощающий тучные клетки или базофилы (например, антитело, истощающее тучные клетки или базофилы). В некоторых вариантах осуществления антитело истощает тучные клетки. В других вариантах осуществления антитело истощает базофилы. В еще других вариантах осуществления антитело истощает тучные клетки и базофилы.
В некоторых вариантах осуществления любого из предшествующих способов терапия включает антагонист PAR2. Иллюстративные антагонисты PAR2 включают низкомолекулярные ингибиторы (например, К-12940, К-14585, пептид FSLLRY-NH2 (SEQ ID NO: 30), GB88, AZ3451 и AZ8838), растворимые рецепторы, киРНК и антитела против PAR2 (например, МАВ3949 и Fab3949).
В некоторых вариантах осуществления любого из предшествующих способов терапия включает антагонист IgE. В некоторых вариантах осуществления антагонист IgE представляет собой антитело против IgE. Можно использовать любое подходящее антитело против IgE. Иллюстративные антитела против IgE включают омализумаб (XOLAIR®), Е26, Е27, CGP-5101 (Ни-901), НА, лигелизумаб и тализумаб. В некоторых вариантах осуществления антитело против IgE содержит одну, две, три, четыре, пять или все шесть из следующих шести HVR: (a) HVR-H1, содержащую аминокислотную последовательность GYSWN (SEQ ID NO: 40); (b) HVR-H2, содержащую аминокислотную последовательность SITYDGSTNYNPSVKG (SEQ ID NO: 41); (с) HVR-H3, содержащую аминокислотную последовательность GSHYFGHWHFAV (SEQ ID NO: 42); (d) HVR-L1, содержащую аминокислотную последовательность RASQSVDYDGDSYMN (SEQ ID NO: 43); (е) HVR-L2, содержащую аминокислотную последовательность AASYLES (SEQ ID: 44); и (f) HVR-L3, содержащую аминокислотную последовательность QQSHEDPYT (SEQ ID NO: 45). В некоторых вариантах осуществления антитело против IgE содержит (а) домен VH, содержащий аминокислотную последовательность, имеющую по меньшей мере 90%, по меньшей мере 95% или по меньшей мере 99% идентичность последовательности с аминокислотной последовательностью SEQ ID NO: 38; (b) домен VL, содержащий аминокислотную последовательность, имеющую по меньшей мере 90%, по меньшей мере 95% или по меньшей мере 99% идентичность с аминокислотной последовательностью SEQ ID NO: 39; или (с) домен VH как в (а) и домен VL как в (b). В некоторых вариантах осуществления домен VH содержит аминокислотную последовательность SEQ ID NO: 38. В некоторых вариантах осуществления домен VL содержит аминокислотную последовательность SEQ ID NO: 39. В некоторых вариантах осуществления домен VH содержит аминокислотную последовательность SEQ ID NO: 38, и домен VL содержит аминокислотную последовательность SEQ ID NO: 39. Любое из антител против IgE, описанных в данном документе, можно использовать в комбинации с любым антителом против триптазы, описанным в данном документе, например, в Разделе VII ниже. В конкретных вариантах осуществления антитело против IgE представляет собой омализумаб (XOLAIR®).
В некоторых вариантах осуществления любого из предшествующих способов терапия включает ингибитор пути TH2. В некоторых вариантах осуществления ингибитор пути TH2 ингибирует любую из мишеней, выбранных из индуцируемой интерлейкином-2 Т-клеточной киназы (ITK), тирозинкиназы Брутона (ВТК), Янус-киназу 1 (JAK1) (например, руксолитиниба, тофацитиниба, оклацитиниба, барицитиниба, филготиниба, гандотиниба, лестауртиниба, момелотиниба, пакринитиба, упадацитиниба, пефитиниба и федратиниба), GATA-связывающего белка 3 (GATA3), ИЛ-9 (например, MEDI-528), ИЛ-5 (например, меполизумаба, CAS №196078-29-2; резилизумаба), ИЛ-13 (например, IMA-026, IMA-638 (также называемого анрукинзумабом, INN №910649-32-0; QAX-576; ловушкой для ИЛ-4/ИЛ-13), тралокинумаба (также называемого САТ-354, CAS №1044515-88-9); AER-001, АВТ-308 (также называемого гуманизированным антителом 13С5.5)), ИЛ-4 (например, AER-001, ловушки для ИЛ-4/ИЛ-13), OX40L, TSLP, ИЛ-25, ИЛ-33 и IgE (например, XOLAIR®, QGE-031 и MEDI-4212); и рецепторов, например: рецептора ИЛ-9, рецептора ИЛ-5 (например, MEDI-563 (бенилизумаба, CAS №1044511-01-4)), альфа рецептора ИЛ-4 (например, AMG-317, AIR-645), альфа-1 рецептора ИЛ-13 (например, R-1671) и альфа-2 рецептора ИЛ-13, ОХ40, TSLP-R, ИЛ-7R-альфа (корецептора для TSLP), ИЛ-17RB (рецептора для ИЛ-25), ST2 (рецептора для ИЛ-33), CCR3, CCR4, CRTH2 (например, AMG-853, АР768, АР-761, MLN6095, АСТ129968), FcεRI, FcεRIl/CD23 (рецепторы для IgE), Flap (например, GSK2190915), Syk киназы (R-343, PF3526299); CCR4 (AMG-761), TLR9 (QAX-935) и мультицитокинового ингибитора CCR3, ИЛ-5, ИЛ-3 и ГМ-КСФ (например, TPI ASM8).
В некоторых вариантах осуществления любого из предшествующих способов астма представляет собой хроническую персистирующую тяжелую астму с серьезными явлениями ухудшения симптомов (приступы или обострения), которые могут быть опасными для жизни. В некоторых вариантах осуществления астма представляет собой атопическую (также известную как аллергическую) астму, неаллергическую астму (например, часто вызываемую респираторной вирусной инфекцией (например, гриппом, парагриппом, риновирусом, человеческим метапневмовирусом и респираторным синцитиальным вирусом) или вдыхаемым раздражителем (например, загрязнителями воздуха, смогом, частицами дизельного топлива, летучими химическими веществами и газами в помещении или на улице, или даже холодным сухим воздухом).
В некоторых вариантах осуществления любого из предшествующих способов астма является эпизодической или вызванной физической нагрузкой астмой из-за острого или хронического первичного или вторичного воздействия «дыма» (как правило, сигарет, сигар или трубок), вдыхания или «парения» (табака, марихуаны или других подобных веществ), или астмой, вызванной недавним приемом аспирина или родственных НПВП. В некоторых вариантах осуществления астма представляет собой легкую или нелеченную кортикостероидами астму, недавно диагностированную и нелеченную астму или ранее не требующую хронического применения ингаляционных местных или системных стероидов для контроля симптомов (кашля, стерторозного дыхания, диспноэ/одышки или боли в груди). В некоторых вариантах осуществления астма представляет собой хроническую, резистентную к кортикостероидам астму, рефрактерную к кортикостероидам астму, или астму, неконтролируемую кортикостероидами, или другими лекарственными препаратами для контроля хронической астмы.
В некоторых вариантах осуществления любого из предшествующих способов астма представляет собой астму от умеренной до тяжелой. В определенных вариантах осуществления астма представляет собой астму с высоким уровнем TH2. В некоторых вариантах осуществления астма представляет собой тяжелую астму. В некоторых вариантах осуществления астма представляет собой атопическую астму, аллергическую астму, неаллергическую астму (например, вследствие инфекции и/или респираторно-синцитиального вируса (РСВ)), астму, вызванную физической нагрузкой, чувствительную к аспирину/индуцированную аспирином астму, легкую астму, умеренную или тяжелую астму, нелеченную кортикостероидами астму, хроническую астму, резистентную к кортикостероидам астму, рефрактерную к кортикостероидам астму, недавно диагностированную и нелеченную астму, астму, вызванную курением, астму, неконтролируемую кортикостероидами. В некоторых вариантах осуществления астма представляет собой астму с высоким уровнем Т-хелперных лимфоцитов 2-го типа (TH2), астму 2-го типа (TH2), или астму, вызванную 2 типом (12). В некоторых вариантах осуществления астма представляет собой эозинофильную астму. В некоторых вариантах осуществления астма представляет собой аллергическую астму. В некоторых вариантах осуществления индивидуум был определен как положительный по эозинофильному воспалению (EIP). Смотри WO 2015/061441. В некоторых вариантах осуществления астмой представляет собой астму с высоким уровнем периостина (например, при которой уровень периостина по меньшей мере любой из около 20 нг/мл, 25 нг/мл или 50 нг/мл сыворотки). В некоторых вариантах осуществления астма представляет собой астму с высоким уровнем эозинофилов (например по меньшей мере любым количеством из около 150, 200, 250, 300, 350, 400 эозинофилов/мл крови). В некоторых вариантах осуществления астма представляет собой астму с низким уровнем TH2 или астму, вызванную не TH2. В некоторых вариантах осуществления индивидуум был определен как отрицательный по эозинофильному воспалению (EIN). Смотри WO 2015/061441. В некоторых вариантах осуществления астма представляет собой астму с низким уровнем периостина (например, с уровнем периостина менее чем около 20 нг/мл сыворотки). В некоторых вариантах осуществления астма представляет собой астму с низким уровнем эозинофилов (например, менее чем около 150 эозинофилов/мкл крови или менее чем около 100 эозинофилов/мкл крови).
Например, в конкретных вариантах осуществления любого из предшествующих способов астма представляет собой астму от умеренной до тяжелой. В некоторых вариантах осуществления астма не контролируется кортикостероидами. В некоторых вариантах осуществления астма представляет собой астму с высоким уровнем TH2 или астму с низким уровнем TH2. В конкретных вариантах осуществления астма представляет собой астму с высоким уровнем TH2.
Следует понимать, что любой из способов лечения пациента, описанных в данном документе, например, в Разделе II подробного описания сущности изобретения выше, может использоваться в вариантах осуществления, причем способ включает применение терапии (например, терапии, включающей агент, выбранный из группы, состоящей из антагониста триптазы, антагониста Fc-эпсилон-рецептора (FcεR), антитела, истощающего IgE+ В-клетки, антитела, истощающего тучные клетки или базофилы, антагониста активируемого протеазой рецептора 2 (PAR2), антагониста IgE и их комбинации) у пациента. Например, в некоторых вариантах осуществления способ включает применение терапии, включающей агент, выбранный из группы, состоящей из антагониста триптазы, антагониста Fc-эпсилон-рецептора (FcεR), антитела, истощающего IgE+ В-клетки, антитела, истощающего тучные клетки или базофилы, антагониста активируемого протеазой рецептора 2 (PAR2), антагониста IgE и их комбинации. В других вариантах осуществления способ включает применение терапии, включающей антагонист IgE.
IV. Обнаружение полиморфизмов нуклеиновых кислот
В нескольких вариантах осуществления способы лечения и диагностики, обеспечиваемые изобретением, включают определение генотипа пациента при одном или более полиморфизмах, например, для определения количества активных аллелей триптазы у пациента. Методики обнаружения для оценки нуклеиновых кислот на наличие полиморфизма (например, ОНП (например, ОНП с733 G>A при TPSAB1, CTGCAGGCGGGCGTGGTCAGCTGGG[G/A]CGAGGGCTGTGCCCAGCCCAACCGG (SEQ ID NO: 36) (см. также rs145402040) или вставку (например, мутацию c980_981insC в TPSB2, CACACGGTCACCCTGCCCCCTGCCTCAGAGACCTTCCCCCCC (SEQ ID NO: 37), на которую указывает жирный и подчеркнутый нуклеотид С)), включают процедуры, хорошо известные в области молекулярной генетики. Многие, но не все, способы включают амплификацию нуклеиновых кислот. В данной области техники содержатся исчерпывающие указания по выполнению амплификации. Иллюстративные ссылки включают руководства, такие как Erlich, ed., PCR Technology: Principles and Applications for DNA Amplification, Freeman Press, 1992; Innis et al. eds., PCR Protocols: A Guide to Methods and Applications, Academic Press, 1990; Ausubel, ed., Current Protocols in Molecular Biology, 1994-1999, включая дополнительные обновления до апреля 2004; и Sambrook et al. eds., Molecular Cloning, A Laboratory Manual, 2001. Общие способы обнаружения однонуклеотидных полиморфизмов раскрыты в Kwok, ed., Single Nucleotide Polymorphisms: Methods and Protocols, Humana Press, 2003.
Хотя в способах, как правило, используются стадии ПЦР, могут также использоваться другие протоколы амплификации. Подходящие способы амплификации включают лигазную цепную реакцию (см., например, Wu et al. Genomics 4:560-569, 1988); анализ замещения цепи (см., например, Walker et al. Proc. Natl. Acad. Sci. USA 89:392-396, 1992; патент США №5455166); и несколько систем амплификации, основанных на транскрипции, включающих способы, описанные в патенте США №№5437990; 5409818; и 5399491; систему амплификации, основанную на транскрипции, (TAS) (Kwoh et al. Proc. Natl. Acad. Sci. USA 86:1173-1177, 1989); и самоподдерживающуюся репликацию последовательностей (3SR) (Guatelli et al. Proc. Natl. Acad. Sci. USA 87:1874-1878, 1990; WO 1992/08800). Альтернативно, можно использовать способы, в которых амплифицируют образец до детектируемого уровня, такие как Qβ-репликазная амплификация (Kramer et al. Nature 339:401-402, 1989; Lomeli et al. Clin. Chem. 35:1826-1831, 1989). Обзор известных способов амплификации можно найти, например, в работе Abramson et al. Curr. Opin. Biotech. 4:41-47, 1993.
Обнаружение генотипа, гаплотипа, ОНП, микросателлитного локуса или другого полиморфизма индивидуума может быть выполнено с использованием олигонуклеотидных праймеров и/или зондов. Олигонуклеотиды могут быть получены при помощи любого подходящего способа, как правило, химического синтеза. Олигонуклеотиды могут быть синтезированы с использованием коммерчески доступных реагентов и приборов. Альтернативно, их можно приобрести у коммерческих источников. Способы синтеза олигонуклеотидов хорошо известны в данной области техники (см., например, Narang et al. Meth. Enzymol. 68:90-99, 1979; Brown et al. Meth. Enzymol. 68:109-151, 1979; Beaucage et al. Tetra. Lett. 22:1859-1862, 1981; и твердофазный метод, описанный в патенте США №4458066). Кроме того, модификации описанных выше способов синтеза могут быть использованы для желательного воздействия на поведение фермента по отношению к синтезированным олигонуклеотидам. Например, включение модифицированных фосфодиэфирных связей (например, фосфоротиоата, метилфосфонатов, фосфоамидата или боранофосфата) или связей, отличных от производного фосфористой кислоты, в олигонуклеотид может быть использовано для предотвращения расщепления в выбранном сайте. Кроме того, использование 2'-амино-модифицированных Сахаров способствует замещению по сравнению с расщеплением олигонуклеотида при гибридизации с нуклеиновой кислотой, которая также является матрицей для синтеза новой цепи нуклеиновой кислоты.
Генотип индивидуума (например, пациента с воспалительным заболеванием, опосредованным тучными клетками, (например, астмой)) может быть определен с использованием многих способов обнаружения, которые хорошо известны в данной области техники. Большинство анализов включают один из нескольких общих протоколов: секвенирования, гибридизации с использованием аллель-специфических олигонуклеотидов, удлинения праймера, аллель-специфического лигирования или способов электрофоретического разделения, например, одноцепочечного конформационного полиморфизма (SSCP) и гетеродуплексного анализа. Иллюстративные анализы включают 5'-нуклеазный анализ, управляемое матрицей включение окрашенных терминаторов, анализы аллель-специфичных олигонуклеотидов методом молекулярных маячков, анализ удлинения цепи на одно основание и оценка ОНП с помощью пирофосфатного секвенирования в режиме реального времени. Анализ амплифицированных последовательностей может быть выполнен с использованием различных методов, таких как технология микрочипов, флуоресцентные поляризационные анализы и времяпролетная масс-спектрометрия с лазерной ионизацией и десорбцией из жидкой матрицы (MALDI-TOF). Два способа, которые также могут быть использованы, представляют собой анализы, основанные на инвазивном расщеплении с помощью Flap-нуклеаз и методологии, использующие замыкающие кольца зонды.
Определение присутствия или отсутствия определенного аллеля обычно проводят путем анализа образца нуклеиновой кислоты, полученного от индивидуума, подлежащего анализу. Часто образец нуклеиновой кислоты содержит геномную ДНК. Геномную ДНК, как правило, получают из образцов крови, но также может быть получена из других клеток или тканей.
Также возможно проанализировать образцы РНК на наличие полиморфных аллелей. Например, мРНК может быть использована для определения генотипа индивидуума в одном или более полиморфных сайтах. В этом случае образец нуклеиновой кислоты получают из клеток, в которых экспрессируется целевая нуклеиновая кислота, например, из Т-хелперных клеток 2-го типа (Th2) и тучных клеток. Такой анализ может быть выполнен при помощи сначала обратной транскрипции целевой РНК с использованием, например, вирусной обратной транскриптазы, а затем амплификации полученной кДНК; или с использованием комбинированной высокотемпературной полимеразной цепной реакции с обратной транскрипцией (ОТ-ПЦР), как описано в патенте США №№5310652; 5322770; 5561058; 5641864; и 5693517.
Образец может быть взят у пациента, у которого подозревают воспалительное заболевание, опосредованное тучными клетками, или у которого диагностировано заболевание, опосредованное тучными клетками, и, следовательно, который, вероятно, нуждается влечении, или у нормального человека, у которого не подозревают какое-либо расстройство. Для определения генотипов в способах согласно данному изобретению можно использовать образцы пациентов, такие как образцы, содержащие клетки, или нуклеиновые кислоты, продуцируемые этими клетками. Жидкости или выделения организма, используемые в качестве образцов в данном изобретении, включают, например, кровь, мочу, слюну, стул, плевральную жидкость, лимфатическую жидкость, мокроту, BAL, жидкость слизистой оболочки (MLF) (например, MLF, полученную путем назосорбции или бронхосорбции), асцит, секрет простаты, спинномозговую жидкость (CSF) или любое другое выделение организма или его производное. Под словом кровь подразумевается цельная кровь, плазма, сыворотка или любое производное крови. Образец нуклеиновой кислоты для использования в способах, описанных в данном документе, может быть получен из любого типа клеток или ткани субъекта. Например, жидкость организма субъекта (например, кровь) может быть получена при помощи известных способов. Альтернативно, тесты на нуклеиновую кислоту можно проводить на сухих образцах (например, волосах или коже).
Образец может быть замороженным, свежим, фиксированным (например, фиксированным формалином), центрифугированным и/или залитым (например, залитым в парафин) и т.д. Образец клеток, конечно, может быть подвергнуть различным хорошо известным способам подготовки и хранения после сбора (например, экстракции нуклеиновой кислоты и/или белка, фиксации, хранению, замораживанию, ультрафильтрации, концентрированию, выпариванию, центрифугированию и т.д.) до оценки генотипа в образце. Аналогичным образом, биопсии также могут быть подвергнуты способам подготовки и хранения после сбора, например, фиксации.
Часто используемые методологии для анализа образцов нуклеиновых кислот для обнаружения присутствия полиморфизмов, таких как ОНП или вставки, которые полезны в данном изобретении, кратко описаны ниже. Однако любой способ, известный в данной области техники, может быть использован в изобретении для обнаружения присутствия единичных нуклеотидных замен.
а. Секвенирование ДНК и удлинения цепи на одно основание
Полимофизмы, например, ОНП или вставки, могут быть обнаружены путем прямого секвенирования. Способы включают, например, способы на основе дидезокси-секвенирования (например, секвенирование по Сэнгеру) и другие способы, такие как способ Максама-Гилберта (см., например, Sambrookand Russell, выше). В некоторых вариантах осуществления подход секвенирования представляет собой секвенирование по Сэнгеру.
Подход секвенирования может представлять собой подход массового параллельного секвенирования (например, секвенирование ILLUMINA®). Другие способы обнаружения включают PYROSEQUENCING™ продуктов олигонуклеотидной длины. В таких способах часто используют способы амплификации, такие как ПЦР. Например, при пиросеквенировании праймер для секвенирования гибридизуется с одноцепочечной, амплифицированной с помощью ПЦР ДНК-матрицей и инкубируется с ферментами, ДНК-полимеразой, АТФ-сульфурилазой, люциферазой и апиразой, а также с субстратами, аденозин-5'-фосфосульфатом (АФС) и люциферином. В реакцию добавляют первый из четырех дезоксинуклеотидтрифосфатов (дНТФ). ДНК-полимераза катализирует включение дезоксинуклеотидтрифосфата в цепь ДНК, если он комплементарен основанию в матричной цепи. Каждое событие включения сопровождается выделением пирофосфата (ПФ) в количестве, эквимолярном количеству включенного нуклеотида. АТФ-сульфурилаза количественно превращает ПФ в АТФ в присутствии АФС. Эта АТФ опосредует обусловленное люциферазой превращение люциферина в оксилюциферин, который генерирует видимый свет в количествах, которые пропорциональны количеству АТФ. Свет, генерируемый в реакции, катализируемой люциферазой, детектируется камера на приборах с зарядовой связью (ПЗС) и рассматривается как пик в PYROGRAM™. Каждый световой сигнал пропорционален количеству включенных нуклеотидов. Апираза, фермент, разлагающий нуклеотиды, постоянно расщепляет неинкорпорированные дНТФ и избыток АТФ. Когда деградация завершается, добавляется другой дНТФ.
В некоторых вариантах осуществления секвенирование РНК (РНК-секвенирование), также упоминаемое как полнотранскриптомное секвенирование методом дробовика (WTSS), может использоваться для обнаружения полиморфизмов (например, ОНП или вставок). Смотри, например, Wang et al. Nature Reviews Genetics 10:57-63, 2009.
Другой аналогичный способ для характеристики ОНП не требует использования полной ПЦР, но, как правило, использует только удлинение праймера на одну флуоресцентно меченую молекулу дидезоксирибонуклеиновой кислоты (ддНТФ), которая комплементарна нуклеотиду, подлежащему исследованию. Нуклеотид в полиморфном сайте может быть идентифицирован путем обнаружения праймера, который удлинен на одно основание и флуоресцентно помечен (например, Kobayashi et al, Mol. Cell. Probes, 9:175-182, 1995).
b. Аллель-специфическая гибридизация
Этот способ, также обычно называемый аллель-специфической гибридизацией олигонуклеотидов (ASO) (например, Stoneking et al. Am. J. Hum. Genet. 48:70-382, 1991; Saiki et al. Nature 324, 163-166, 1986; EP 235726; и WO 1989/11548), основан на различении двух молекул ДНК, отличающихся по одному основанию, путем гибридизации олигонуклеотидного зонда, специфичного для одного из вариантов, с амплифицированным продуктом, полученным в результате амплификации образца нуклеиновой кислоты. В этом способе, как правило, используются короткие олигонуклеотиды, например, длиной 15-20 оснований. Зонды предназначены для дифференциальной гибридизации одного варианта с другим. Принципы и руководство по разработке такого зонда доступны в данной области техники. Условия гибридизации должны быть достаточно жесткими, чтобы существовала значительная разница в интенсивности гибридизации между аллелями и чтобы при этом получали по существу бинарный ответ, при котором зонд гибридизуется только с одним из аллелей. Некоторые зонды конструируют для гибридизации с сегментом целевой ДНК таким образом, что полиморфный сайт выравнивается с центральным положением зонда (например, в олигонуклеотиде из 15 оснований в положении 7; в олигонуклеотиде из 16 оснований в положении 8 или 9), но в таком конструкте нет необходимости.
Количество и/или присутствие аллеля можно определить путем измерения количества аллель-специфического олигонуклеотида, который гибридизуется с образцом. Как правило, олигонуклеотид помечен меткой, такой как флуоресцентная метка. Например, аллель-специфический олигонуклеотид гибризуют с иммобилизованными олигонуклеотидами, представляющими последовательности ОНП. После жестких условий гибридизации и отмывки измеряют интенсивность флуоресценции для каждого олигонуклеотида с ОНП.
В одном варианте осуществления нуклеотид, присутствующий в полиморфном сайте, идентифицируют путем гибридизации в условиях последовательность-специфической гибридизации с олигонуклеотидным зондом или праймером, точно комплементарным одному из полиморфных аллелей в области, охватывающей этот полиморфный сайт. Зонд или праймер, которые гибридизуют последовательность, и условия последовательность-специфической гибридизации выбраны таким образом, чтобы одно несовпадение в полиморфном сайте дестабилизировало гибридизационный дуплекс в достаточной степени, чтобы он эффективно не образовывался. Таким образом, в условиях последовательность-специфической гибридизации стабильные дуплексы будут образовываться только между зондом или праймером и точно комплементарной аллельной последовательностью. Таким образом, олигонуклеотиды длиной от около 10 до около 35 нуклеотидов, обычно длиной от около 15 до около 35 нуклеотидов, которые точно комплементарны аллельной последовательности в области, которая охватывает полиморфный сайт, входят в объем изобретения.
В альтернативном варианте осуществления нуклеотид, присутствующий в полиморфном сайте, идентифицируют путем гибридизации в достаточно жестких условиях гибридизации с олигонуклеотидом, по существу комплементарным одному из аллелей ОНП в области, охватывающей полиморфный сайт, и точно комплементарным аллелю в полиморфном сайте. Поскольку несовпадения, которые возникают в неполиморфных сайтах, представляют собой несовпадения с обеими последовательностями аллелей, разница в количестве несовпадений в дуплексе, образованном с последовательностью целевого аллеля, и в дуплексе, сформированном с соответствующей последовательностью нецелевого аллеля, является такой же, как когда используется олигонуклеотид, точно комплементарный последовательности целевого аллеля. В данном варианте осуществления условия гибридизации ослабляют в достаточной степени, чтобы позволить образование стабильных дуплексов с целевой последовательностью, при этом сохраняя достаточную жесткость, чтобы исключить образование стабильных дуплексов с нецелевыми последовательностями. При таких достаточно жестких условиях гибридизации стабильные дуплексы будут образовываться только между зондом или праймером и целевым аллелем. Таким образом, олигонуклеотиды длиной от около 10 до около 35 нуклеотидов, как правило, длиной от около 15 до около 35 нуклеотидов, которые являются по существу комплементарными последовательности аллеля в области, которая охватывает полиморфный сайт, и являются точно комплементарными последовательности аллеля в полиморфном сайте, входят в объем изобретения.
Использование по существу, а не точно комплементарных олигонуклеотидов, может быть желательным в форматах анализа, в которых ограничена оптимизация условий гибридизации. Например, в типичном формате анализа на основе иммобилизованного олигонуклеотида с несколькими мишенями, зонды или праймеры для каждой мишени иммобилизованы на одной твердой подложке. Гибридизации проводят одновременно путем приведения в контакт твердой подложки с раствором, содержащим целевую ДНК. Поскольку все гибридизации проводят в идентичных условиях, условия гибридизации нельзя оптимизировать отдельно для каждого зонда или праймера. Включение несовпадений в зонд или праймер можно использовать для регуляции стабильности дуплекса, когда формат анализа не позволяет регулировать условия гибридизации. Влияние конкретного введенного несовпадения на стабильность дуплекса хорошо известно, и стабильность дуплекса обычно может быть оценена и эмпирически определена, как описано выше. Подходящие условия гибридизации, которые зависят от точного размера и последовательности зонда или праймера, могут быть выбраны эмпирически с использованием руководства, представленного в данном документе и хорошо известного в данной области техники. Использование олигонуклеотидных зондов или праймеров для выявления различий в единичных парах оснований в последовательности описано, например, в Conner et al. Proc. Natl. Acad. Sci. USA 80:278-282, 1983, и патентах США №№5468613 и 5604099.
Пропорциональное изменение в стабильности между абсолютно совпадающим гибридизационным дуплексом и гибридизационным дуплексом с несовпадением по одному основанию зависит от длины гибридизованных олигонуклеотидов. Дуплексы, образованные с более короткими последовательностями зондов, дестабилизируются пропорционально в большей степени из-за присутствия несовпадений. Олигонуклеотиды длиной от около 15 до около 35 нуклеотидов часто используют специфическое для последовательности обнаружение. Кроме того, поскольку концы гибридизованного олигонуклеотида подвергаются непрерывной случайной диссоциации и повторному отжигу из-за термической энергии, несовпадение на обоих концах дестабилизирует гибридизационный дуплекс меньше, чем несовпадение, возникающее внутри гибридизационного дуплекса. Для распознавания одного изменения пары оснований в целевой последовательности выбирается последовательность зонда, которая гибридизуется с целевой последовательностью так, что во внутренней области зонда возникает полиморфный сайт.
Приведенные выше критерии для выбора последовательности зонда, которая гибридизуется с конкретным аллелем, применимы к гибридизующей области зонда, то есть той части зонда, которая участвует в гибридизации с целевой последовательностью. Зонд может быть связан с дополнительной последовательностью нуклеиновой кислоты, такой как поли-Т-хвост, используемый для иммобилизации зонда, без существенного изменения гибридизационных характеристик зонда. Специалист в данной области техники поймет, что для использования в данных способах зонд, связанный с дополнительной последовательностью нуклеиновой кислоты, которая не комплементарна целевой последовательности и, таким образом, не участвует в гибридизации, по существу эквивалентен несвязанному зонду.
Подходящие форматы анализа для обнаружения гибридов, образованных между зондами и последовательностями целевой нуклеиновой кислоты в образце, известны в данной области техники и включают форматы анализа на основе иммобилизованной мишени (дот-блот) и анализы на основе иммобилизованного зонда (обратный дот-блот или линейный блот). Форматы дот-блот и обратного дот-блот анализов описаны в патенте США №№5310893; 5451512; 5468613; и 5604099.
В формате дот-блот амплифицированная целевую ДНК иммобилизуют на твердой подложке, такой как нейлоновая мембрана. Комплекс мембрана-мишень инкубируют с меченым зондом в подходящих условиях гибридизации, негибридизованный зонд удаляют отмывкой в подходящих жестких условиях, и мембрану исследуют на присутствие связанного зонда.
В формате обратного дот-блота (или линейного блота) зонды иммобилизуют на твердой подложке, такой как нейлоновая мембрана или титрационный микропланшет. Целевую ДНК метят, как правило, во время амплификации путем включения меченых праймеров. Могут быть помечены один или оба праймера. Комплекс мембрана-зонд инкубируют с меченой амплифицированной целевой ДНК в подходящих условиях гибридизации, негибридизованную целевую ДНК удаляют отмывкой в подходящих жестких условиях, и мембрану исследуют на наличие связанной целевой ДНК. В этом примере описан анализ обнаружения на основе обратного линейного блота.
Аллель-специфический зонд, специфический для одного из вариантов полиморфизма, часто используется вместе с аллель-специфическим зондом для другого варианта полиморфизма. В некоторых вариантах осуществления зонды иммобилизуют на твердой подложке, и анализируют целевую последовательность у индивидуума, используя оба зонда одновременно. Примеры чипов нуклеиновых кислот описаны в WO 95/11995. Для анализа охарактеризованных полиморфизмов можно использовать тот же чип или другой чип. В WO 95/11995 также описаны подчипы, которые оптимизированы для обнаружения вариантов форм предварительно охарактеризованного полиморфизма. Такой подчип можно использовать для обнаружения присутствия полиморфизмов, описанных в данном документе.
с. Аллель-специфические праймеры
Полиморфизмы, такие как ОНП или вставки, также обычно обнаруживают с использованием способов аллель-специфической амплификации или удлинения праймеров. Эти реакции, как правило, включают использование праймеров, которые предназначены для специфического нацеливания на полиморфизм посредством несовпадения на 3'-конце праймера. Присутствие несовпадения влияет на способность полимеразы удлинять праймер, когда у полимеразы отсутствует активность по исправлению ошибок. Например, для обнаружения последовательности аллеля с использованием способа на основе аллель-специфической амплификации или удлинения праймера конструируют праймер, комплементарный одному аллелю полиморфизма, так что З'-концевой нуклеотид гибридизуется в полиморфном положении. Присутствие конкретного аллеля может быть определено по способности праймера инициировать удлинение. Если З'-конец не совпадает, удлинение затрудняется.
В некоторых вариантах осуществления праймер используется вместе со вторым праймером в реакции амплификации. Второй праймер гибридизуется в сайте, не связанном с полиморфным положением. Амплификация происходит от двух праймеров, приводящих к обнаруживаемому продукту, указывающему на наличие конкретной аллельной формы. Способы на основе аллель-специфической амплификации или удлинения праймера описаны, например, в WO 93/22456 и патенте США №№5137806; 5595890; 5639611; и 4851331.
Используя генотипирование на основе аллель-специфической амплификации, идентификация аллелей требует только обнаружения присутствия или отсутствия амплифицированных целевых последовательностей. Способы обнаружения амплифицированных целевых последовательностей хорошо известны в данной области техники. Например, описанные анализы методом гель-электрофореза и гибридизации зондов часто используются для обнаружения присутствия нуклеиновых кислот.
В альтернативном беззондовом способе амплифицированную нуклеиновую кислоту обнаруживают путем отслеживания увеличения общего количества двухцепочечной ДНК в реакционной смеси, как описано, например, в патенте США №5994056; и европейских патентных публикациях №№487218 и 512334. Обнаружение двухцепочечной целевой ДНК зависит от повышенной флуоресценции, которую проявляют различные ДНК-связывающие красители, например, SYBR Green, когда связаны с двухцепочечной ДНК.
Как понятно специалисту в данной области техники, способы аллель-специфической амплификации могут быть выполнены в реакциях, в которых используются множественные аллель-специфические праймеры для нацеливания на конкретные аллели. Праймеры для таких мультиплексных применений обычно метят различимыми метками или выбирают так, чтобы продукты амплификации, полученные из аллелей, различались по размеру. Так, например, оба аллеля в одном образце могут быть идентифицированы с использованием одной амплификации с помощью гель-анализа продукта амплификации.
Как и в случае аллель-специфических зондов, аллель-специфический олигонуклеотидный праймер может быть точно комплементарен одному из полиморфных аллелей в области гибридизации или может иметь некоторые несовпадения в положениях, отличных от З'-конца олигонуклеотида так, что несовпадения встречаются в неполиморфных сайтах в обеих последовательностях аллелей.
d. Обнаруживаемые зонды
i) Зонды 5'-нуклеазного анализа
Генотипирование также может быть выполнено с использованием «TAQMAN®» или «5'-нуклеазного анализа», как описано в патенте США №№5210015; 5487972; и 5804375; и Holland et al. Proc. Natl. Acad. Sci. USA 88:7276-7280, 1988. В анализе TAQMAN® меченые детекторные зонды, которые гибридизуются в амплифицированной области, добавляются во время реакции амплификации. Зонды модифицированы таким образом, чтобы они не действовали в качестве праймеров для синтеза ДНК. Амплификацию проводят с использованием ДНК-полимеразы, обладающей 5'-3'-экзонуклеазной активностью. Во время каждой стадии синтеза амплификации любой зонд, который гибридизуется с целевой нуклеиновой кислотой ниже от удлиняемого праймера, деградирует из-за 5'-3'-экзонуклеазной активности ДНК-полимеразы. Таким образом, синтез новой целевой цепи также приводит к деградации зонда, а накопление продукта деградации обеспечивает показатель контроля синтеза целевых последовательностей.
Гибридизационный зонд может представляет собой аллель-специфический зонд, который дифференцирует аллели ОНП. Альтернативно, способ может быть осуществлен с использованием аллель-специфического праймера и меченого зонда, который связывается с амплифицированным продуктом.
В 5'-нуклеазном анализе можно использовать любой способ, подходящий для обнаружения продукта деградации. Часто детекторный зонд метят двумя флуоресцентными красителями, один из которых способен тушить флуоресценцию другого красителя. Красители прикрепляются к зонду, обычно один прикрепляется к 5'-концу, а другой прикрепляется к внутреннему сайту, так что тушение происходит, когда зонд находится в негибридизованном состоянии, и таком, что расщепление зонда ДНК-полимеразой с 5'-3'-экзонуклеазной активности происходит между двумя красителями. Амплификация приводит к расщеплению зонда между красителями с сопутствующим устранением тушения и увеличением флуоресценции, наблюдаемой от первоначально потушенного красителя. Накопление продукта разложения контролируется путем измерения увеличения реакции флуоресценции. В патентах США №№5491063 и 5571673 описаны альтернативные способы обнаружения деградации зонда, которая происходит одновременно с амплификацией.
ii) Вторичная структура зондов
Зонды, обнаруживаемые при вторичном структурном изменении, также подходят для обнаружения полиморфизма, в том числе ОНП. Примеры вторичной структуры или структуры «петля-на-стебле» зондов включают молекулярные маяки или праймер/зонды SCORPION®. Зонды типа «молекулярный маяк» представляют собой зонды на основе одноцепочечной олигонуклеиновой кислоты, которые могут образовывать шпилечную структуру, в которой флуорофор и тушитель, как правило, располагаются на противоположных концах олигонуклеотида. На обоих концах зонда короткие комплементарные последовательности позволяют формировать внутримолекулярный стебель, который позволяет флуорофору и тушителю находиться в непосредственной близости. Петлевая часть молекулярного маяка является комплементарной представляющей интерес целевой нуклеиновой кислоте. Связывание этого зонда с представляющей интерес целевой нуклеиновой кислотой образует гибрид, который отодвигает ствол. Это вызывает изменение конформации, которое отодвигает флуорофор и тушитель друг от друга и приводит к более интенсивному флуоресцентному сигналу. Однако зонды типа «молекулярного маяка» очень чувствительны к небольшому изменению последовательности в целевом зонде (см., например, Tyagi et al. Nature Biotech. 14:303-308, 1996; Tyagi et al. Nature Biotech. 16:49-53, 1998; Piatek et al. Nature Biotech. 16: 359-363, 1998; Marras et al. Genetic Analysis: Biomolecular Engineering 14:151-156,1999; Tapp et al, BioTechniques 28: 732-738, 2000). Праймер/зонд SCORPION® включает зонд со структурой «стебель-петля», ковалентно связанный с праймером.
е. Электрофорез
Продукты амплификации, полученные с использованием полимеразной цепной реакции, могут быть проанализированы с использованием денатурирующего градиентного гель-электрофореза. Различные аллели могут быть идентифицированы на основании различных зависимых от последовательности свойств плавления и электрофоретической миграции ДНК в растворе (см., например, Erlich, ed., PCR Technology, Principles and Applications for DNA Amplification, W. H. Freeman and Co., 1992).
Различение полиморфизмов микросателлитов можно проводить с помощью капиллярного электрофореза. Капиллярный электрофорез позволяет легко идентифицировать количество повторов в конкретном аллеле микросателлита. Применение капиллярного электрофореза для анализа полиморфизмов ДНК хорошо известно специалистам в данной области техники (см., например, Szantai et al. J Chromatogr A. 1079(1-2):41-9, 2005; Bjorheim et al. Electrophoresis 26(13):2520-30, 2005 и Mitchelson, Mol. Biotechnol. 24(1):41-68, 2003).
Идентичность аллельного варианта также может быть получена путем анализа движения нуклеиновой кислоты, содержащей полиморфную область в полиакриламидных гелях, содержащих градиент денатурирующего вещества, который анализируется с использованием денатурирующего градиентного гель-электрофореза (DGGE) (см., например, Myers et al. Nature 313:495-498, 1985). Когда DGGE используется в качестве метода анализа, ДНК будет модифицирована, чтобы гарантировать, что она не полностью денатурируется, например, путем добавления GC-зажима приблизительно 40 п. н. GC-богатой ДНК с высокой температурой плавления при помощи ПЦР. В дополнительном варианте осуществления вместо градиента денатурирующего агента используется температурный градиент для идентификации различий в подвижности контрольной ДНК и ДНК образца (см., например, Rosenbaum et al. Biophys. Chem. 265:1275, 1987).
f. Анализ одноцепочечного конформационного полиморфизма
Аллели целевых последовательностей могут быть дифференцированы с использованием анализа одноцепочечного конформационного полиморфизма, который идентифицирует различия в основаниях путем изменения электрофоретической миграции одноцепочечных продуктов ПЦР, как описано, например, в Orita et al. Proc. Nat. Acad. Sci. 86, 2766-2770, 1989; Cotton Mutat. Res. 285:125-144, 1993; и Hayashi Genet. Anal. Tech. Appl. 9:73-79, 1992. Продукты амплифицированной ПЦР могут быть получены, как описано выше, и нагреты или денатурированы иным способом для образования одноцепочечных продуктов амплификации. Одноцепочечные нуклеиновые кислоты могут повторно образовывать или образовывать вторичные структуры, которые частично зависят от последовательности оснований. Различная электрофоретическая подвижность одноцепочечных продуктов амплификации может быть связана с различием в последовательностях оснований между целевыми аллелями, и результирующее изменение электрофоретической подвижности позволяет обнаруживать даже изменение одного основания. Фрагменты ДНК могут быть помечены или обнаружены с помощью меченых зондов. Чувствительность анализа может быть повышена путем использования РНК (а не ДНК), в которой вторичная структура более чувствительна к изменению последовательности. В другом предпочтительном варианте осуществления в указанном способе используется гетеродуплексный анализ для разделения двухцепочечных гетеродуплексных молекул на основе изменений электрофоретической подвижности (см., например, Keen et al. Trends Genet. 7:5-10, 1991).
В способах обнаружения ОНП часто используются меченые олигонуклеотиды. Олигонуклеотиды могут быть помечены путем включения метки, определяемой спектроскопическим, фотохимическим, биохимическим, иммунохимическим или химическим способом. Полезные метки включают флуоресцентные красители, радиоактивные метки, например 32Р, электронно-плотные реагенты, ферменты, такие как пероксидаза или щелочная фосфатаза, биотин или гаптены, и белки, для которых доступны антисыворотка или моноклональные антитела. Методики мечения хорошо известны в данной области техники (см., например, Current Protocols in Molecular Biology, выше; Sambrook et al., выше).
g. Дополнительные способы определения генотипа индивидуума при полиморфизмах
Можно использовать технологию ДНК-микрочипов, например, инструменты в виде ДНК-чипов, микрочипы высокой плотности для методов высокопроизводительного скрининга и микрочипы низкой плотности. Способы изготовления микрочипов известны в данной области техники и включают различные технологии и процессы осаждения или нанесения пятен на струйных и микроструйных аппаратах, фотолитографические процессы синтеза олигонуклеотидов in situ или на чипе, а также способы получения ДНК-зондов при помощи электрофокусирования. Методы гибридизации ДНК-микрочипов были успешно применены в областях анализа экспрессии генов и генотипирования для точечных мутаций, однонуклеотидных полиморфизмов (ОНП) и коротких тандемных повторов (STR). Дополнительные методы включают микрочипы с интерферирующими РНК и комбинации микрочипов и других методов, такие как лазерная захватывающая микродиссекция (LCM), сравнительная геномная гибридизация (CGH), матричная CGH и иммунопреципитация хроматина (ChIP). См., например, Не et al. Adv. Exp. Med. Biol. 593:117-133, 2007 и Heller Annu. Rev. Biomed. Eng. 4:129-153, 2002.
В некоторых вариантах осуществления защита от расщепляющих агентов (таких как нуклеаза, гидроксиламин или тетроксид осмия и с пиперидином) может использоваться для обнаружения несовпадающих оснований в гетеродуплексах РНК/РНК, ДНК/ДНК или РНК/ДНК (см., например, Myers et al. Science 230:1242, 1985). В целом, метод «расщепления ошибочно спаренных оснований» начинается с обеспечения гетеродуплексов, образованных гибридизацией контрольной нуклеиновой кислоты, которая необязательно помечена, например, РНК или ДНК, содержащей нуклеотидную последовательность аллельного варианта гена, с нуклеиновой кислоты образца, например, РНК или ДНК, полученной из образца ткани. Двухцепочечные дуплексы обрабатывают агентом, который расщепляет одноцепочечные области дуплекса, такие как дуплексы, сформированные на основе несовпадений пар оснований между контрольной цепью и цепью из образца. Например, дуплексы РНК/ДНК могут быть обработаны РНКазой, а гибриды ДНК/ДНК могут быть обработаны нуклеазой S1 для ферментативного расщепления несовпадающих областей. Альтернативно, дуплексы ДНК/ДНК или РНК/ДНК могут быть обработаны гидроксиламином или тетроксидом осмия и пиперидином для расщепления несовпадающих областей. После расщепления несовпадающих областей полученный материал затем разделяют по размеру на денатурирующих полиакриламидных гелях, чтобы определить, имеют ли контрольная нуклеиновая кислота и нуклеиновая кислота из образца идентичную нуклеотидную последовательность или в каких нуклеотидах они различны. См., например, патент США №6455249, Cotton et al. Proc. Natl. Acad. Sci. USA 85:4397-4401, 1988; Saleeba et al. Meth. Enzymol. 217:286-295, 1992.
В некоторых случаях присутствие специфического аллеля в ДНК субъекта может быть показано с помощью рестрикционного анализа. Например, специфический нуклеотидный полиморфизм может приводить к нуклеотидной последовательности, содержащей сайт рестрикции, который отсутствует в нуклеотидной последовательности другого аллельного варианта.
В другом варианте осуществления идентификацию аллельного варианта проводят с помощью лигирования олигонуклеотидных зондов (OLA), как описано, например, в патенте США №4998617 и Laridegren et al. Science 241:1077-1080, 1988. В протоколе OLA используются два олигонуклеотида, которые сконструированы так, чтобы они могли гибридизоваться с примыкающими последовательностями одной цепи мишени. Один из олигонуклеотидов связан с разделяющим маркером, например, биотинилированием, а другой детектируемо помечен. Если в целевой молекуле обнаружена точная комплементарная последовательность, олигонуклеотиды гибридизуются таким образом, что их концы примыкают друг к другу, и создают субстрат для лигирования. Затем лигирование позволяет выделить меченый олигонуклеотид с использованием авидина или другого биотинового лиганда. В данной области техники также известен анализ обнаружения нуклеиновых кислот, который сочетает в себе свойства ПЦР и OLA (см., например, Nickerson et al. Proc. Natl. Acad. Sci. USA 87:8923-8927, 1990). В данном способе ПЦР используется для экспоненциальной амплификации целевой ДНК, которая затем детектируется с помощью OLA.
Одноосновный полиморфизм может быть обнаружен с использованием специального резистентного к экзонуклеазе нуклеотида, как описано, например, в патенте США №. 4656127. Согласно этому способу праймеру, комплементарному последовательности аллеля, непосредственно находящейся 3' к полиморфному сайту, разрешается гибридизовать с целевой молекулой, полученной от конкретного животного или человека. Если полиморфный сайт в целевой молекуле содержит нуклеотид, который комплементарен присутствующему конкретному резистентному к экзонуклеазе производному нуклеотида, то это производное будет включено в конец гибридизованного праймера. Такое включение делает праймер резистентным к экзонуклеазе и тем самым позволяет его обнаруживать. Поскольку идентичность резистентного к экзонуклеазе производного образца известна, обнаружение того, что праймер стал резистентным к экзонуклеазам, демонстрирует, что нуклеотид, присутствующий в полиморфном сайте целевой молекулы, был комплементарен производному нуклеотида, используемого в реакции. Преимущество этого способа состоит в том, что он не требует определения большого количества данных посторонних последовательностей.
Метод на основе раствора также может быть использован для определения идентичности нуклеотида полиморфного сайта (см., например, WO 1991/02087). Как указано выше, используется праймер, который комплементарен последовательностям аллелей, непосредственно находящимся 3' к полиморфному сайту. Способ определяет идентичность нуклеотида этого сайта с использованием меченых дидезоксинуклеотидных производных, которые, будучи комплементарны нуклеотиду полиморфного сайта, будут включены в конец праймера.
Альтернативный способ, который можно использовать, описан в WO 92/15712. В этом способе используется смеси меченых терминаторов и праймера, который комплементарен последовательности, находящимся в 3' к полиморфному сайту. Меченый терминатор, который включен таким образом, определяется по нуклеотиду, присутствующему в полиморфном сайте оцениваемой целевой молекулы, и комплементарен ему. Способ, как правило, представляет собой анализ гетерогенной фазы, в котором праймер или целевая молекула иммобилизованы на твердой фазе.
Были описаны многие другие процедуры направляемого праймером включения нуклеотидов для анализа полиморфных сайтов в ДНК (Komher et al. Nucl. Acids. Res. 17:7779-7784, 1989; Sokolov Nucl. Acids Res. 18:3671, 1990; Syvanen et al. Genomics 8:684-692, 1990; Kuppuswamy et al. Proc. Natl. Acad. Sci. USA 88:1143-1147, 1991; Prezant et al. Hum. Mutat. 1:159-164, 1992; Ugozzoli et al. GATA 9:107-112, 1992; Nyren et al. Anal. Biochem. 208:171-175, 1993). Все эти способы основаны на включении меченых дезоксинуклеотидов для дифференциации оснований в полиморфном сайте.
V. Определение уровня экспрессии биомаркеров
Терапевтические и диагностические способы согласно изобретению могут включать определение уровня экспрессии одного или более биомаркеров (например, триптазы). Определение уровня биомаркеров может быть выполнено любым из способов, известных в данной области техники или описанных ниже.
Экспрессия описанных в данном документе биомаркеров (например, триптазы) может быть обнаружена с использованием любого способа, известного в данной области техники. Например, образцы тканей или клеток млекопитающих могут быть легко проанализированы, например, на мРНК или ДНК представляющего интерес биомаркера, используя Нозерн-дот, дот-блот или ПЦР-анализ, гибридизацию на чипах, анализ методом защиты от РНКаз или с использованием ДНК-микрочипов с ОНП, которые имеются в продаже, в том числе снимки ДНК-микрочипов. Например, анализы методом ПЦР в режиме реального времени (ПЦР-РВ), такие как анализы методом количественной ПЦР, хорошо известны в данной области техники. В иллюстративном варианте осуществления изобретения способ обнаружения мРНК представляющего интерес биомаркера (например, триптазы) в биологическом образце включает получение кДНК из образца путем обратной транскрипции с использованием по меньшей мере одного праймера; амплификацию кДНК, полученной таким образом; и обнаружение присутствия амплифицированной кДНК. Кроме того, такие способы могут включать одну или более стадий, которые позволяют определить уровни мРНК в биологическом образце (например, путем одновременного исследования уровней сравнительной контрольной последовательности мРНК гена «домашнего хозяйства», например, члена семейства актина). Необязательно, может быть определена последовательность амплифицированной кДНК.
Другие способы, которые можно использовать для обнаружения нуклеиновых кислот, для применения в изобретении, включают высокопроизводительный анализ экспрессии последовательности РНК, включая геномный анализ на основе РНК, такой как, например, РНК-секвенирование.
В одном конкретном варианте осуществления экспрессия биомаркера (например, триптазы) может быть выполнена с помощью технологии ОТ-ПЦР. Зонды, используемые для ПЦР, могут быть помечены детектируемым маркером, таким как, например, радиоизотоп, флуоресцентное соединение, биолюминесцентное соединение, хемилюминесцентное соединение, металлохелат или фермент. Такие зонды и праймеры можно использовать для обнаружения присутствия экспрессированного биомаркера в образце. Как будет понятно специалисту в данной области техники, очень много различных праймеров и зондов могут быть получены на основе последовательностей, предложенных в данном документе, и эффективно использоваться для амплификации, клонирования, и/или определения наличия и/или уровней биомаркера.
Другие способы включают протоколы, которые исследуют или обнаруживают мРНК биомаркера (например, триптазы) в образце ткани или клетки с помощью технологий микрочипов. С использованием микрочипов нуклеиновых кислот тестируемые и контрольные образцы мРНК из тестируемых и контрольных образцов ткани подвергают обратной транскрипции и метят для получения кДНК-зондов. Затем зонды гибридизуют с чипом нуклеиновых кислот, иммобилизованных на твердой подложке. Чип сконфигурирован так, что последовательность и положение каждого элемента чипа известны. Например, выборка генов, которые потенциально могут экспрессироваться при определенных болезненных состояниях, может располагаться на твердой подложке. Гибридизация меченого зонда с конкретным элементом чипа указывает на то, что образец, из которого был получен зонд, экспрессирует этот ген. Анализ дифференциальной экспрессии генов пораженной ткани может обеспечить ценную информацию. В технологии микрочипов используются методы гибридизации нуклеиновых кислот и вычислительной технологии для оценки профиля экспрессии мРНК тысяч генов в одном эксперименте (см., например, WO 2001/75166). См., например, патент США №№5700637, 5445934, и 5807522, Lockart, Nat. Biotech. 14:1675-1680, 1996; и Cheung et al. Nat. Genet. 21(Suppl):15-19, 1999 для обсуждения изготовления чипа.
Кроме того, может быть использован способ профилирования и обнаружения ДНК с использованием микрочипов, описанный в европейском патенте ЕР 1753878. Этот способ быстро идентифицирует и дифференцирует различные последовательности ДНК с использованием анализа коротких тандемных повторов (STR) и ДНК-микрочипов. В одном варианте осуществления меченая целевая последовательность STR гибридизуется с ДНК-микрочипом, несущим комплементарные зонды. Эти зонды различаются по длине для охвата диапазона возможных STR. Меченые одноцепочечные участки ДНК-гибридов селективно удаляют с поверхности микрочипы с использованием ферментативного расщепления после гибридизации. Количество повторов в неизвестной мишени определяется на основе структуры целевой ДНК, которая остается гибридизованной с микрочипом.
Одним из примеров микрочиповой системы является система Affymetrix GENECHIP®, которая имеется в продаже и содержит чипы, изготовленные путем прямого синтеза олигонуклеотидов на стеклянной поверхности. Могут использоваться и другие системы, известные специалисту в данной области техники.
Имеется много ссылок для предоставления указаний по применению вышеуказанных способов (Kohler et al. Hybridoma Techniques, Cold Spring Harbor Laboratory, 1980; Tijssen, Practice and Theory of Enzyme Immunoassays, Elsevier, 1985; Campbell, Monoclonal Antibody Technology, Elsevier, 1984; Hurrell, Monoclonal Hybridoma Antibodies: Techniques and Applications, CRC Press, 1982; and Zola, Monoclonal Antibodies: A Manual of Techniques, pp. 147-158, CRC Press, Inc., 1987). Нозерн-блот анализ является общепринятым методом, хорошо известным в данной области техники, и описан, например, в Sambrook et al., выше. Типичные протоколы для оценки статуса генов и генных продуктов можно найти, например, в Ausubel et al., выше.
Что касается обнаружения белковых биомаркеров, доступны различные анализы белка, включая, например, способы на основе антител, а также масс-спектроскопию и другие подобные способы, известные в данной области техники. Например, в случае способов на основе антител образец можно приводить в контакт с антителом, специфическим для биомаркера (например, триптазы), в условиях, достаточных для образования комплекса антитело-биомаркер, а затем детектировать комплекс. Обнаружение присутствия белкового биомаркера может быть выполнено рядом способов, таких как вестерн-блот (с или без иммунопреципитации), 2-мерный электрофорез в полиакриламидном геле в присутствии додецилсульфата натрия (ДСН-ПААГ), иммунопреципитация, флуоресцентно-активированная сортировка клеток (FACS™), проточная цитометрия и иммуноферментный анализ (ИФА) для анализа широкого спектра тканей и образцов, включая плазму или сыворотку. Доступен широкий спектр методик иммуноанализа с использованием такого формата анализа, см., например, патенты США №№4016043; 4424279; и 4018653. К ним относятся как одностадийные, так и двустадийные или сэндвич-анализы неконкурентных типов, а также традиционные анализы конкурентного связывания. Эти анализы также включают прямое связывание меченого антитела с целевым биомаркером.
Сэндвич-анализы являются одними из самых полезных и обычно используемых анализов. Существует ряд вариаций сэндвич-анализа, и все они охвачены данным изобретением. Вкратце, в типичном прямом анализе немеченое антитело иммобилизуют на твердой подложке, и исследуемый образец приводят в контакт со связанной молекулой. После подходящего периода инкубации, в течение периода времени, достаточного для образования комплекса антитело-антиген, затем добавляют второе специфическое к антигену антитело, меченное репортерной молекулой, способной генерировать детектируемый сигнал, и инкубируют, давая время достаточное для образования другого комплекса антитело-антиген-меченое антитело. Любой непрореагировавший материал вымывают, а присутствие антигена определяют путем наблюдения сигнала, генерируемого репортерной молекулой. Результаты могут быть либо качественными, путем простого наблюдения видимого сигнала, либо могут быть количественно оценены путем сравнения с контрольным образцом, содержащим известные количества биомаркера.
Варианты прямого анализа включают одновременный анализ, в котором и образец, и меченое антитело добавляют одновременно к связанному антителу. Эти методы хорошо известны специалистам в данной области техники, включая любые незначительные изменения, которые будут очевидны. В типичном прямом сэндвич-анализе первое антитело, обладающее специфичностью к биомаркеру, или ковалентно, или пассивно связано с твердой поверхностью. Твердая поверхность, как правило, представляет собой стекло или полимер, наиболее часто используемые полимеры - целлюлозу, полиакриламид, нейлон, полистирол, поливинилхлорид или полипропилен. Твердые подложки могут быть в форме пробирок, гранул, дисков или микропланшетов или любой другой поверхности, подходящей для проведения иммуноанализа. Процессы связывания хорошо известны в данной области техники и обычно состоят из поперечного сшивания, ковалентно связывания или физического адсорбирования, комплекс полимер-антитело промывают при подготовке к тестированию образца. Затем аликвоту исследуемого образца добавляют в твердофазный комплекс и инкубируют в течение достаточного периода времени (например, 2-40 минут или в течение ночи, если это более удобно) и в подходящих условиях (например, от комнатной температуры до 40°С, например от 25°С до 32°С включительно), чтобы обеспечить связывание любой субъединицы, присутствующей в антителе. После периода инкубации твердую фазу с субъединицей антитела промывают, сушат и инкубируют со вторым антителом, специфическим для части биомаркера. Второе антитело связано с репортерной молекулой, которая используется для определения связывания второго антитела с молекулярным маркером.
Альтернативный способ включает иммобилизацию целевых биомаркеров в образце, а затем воздействие на иммобилизованную мишень специфическим антителом, которое может быть помечено или может быть не помечено репортерной молекулой. В зависимости от количества мишени и силы сигнала репортерной молекулы, связанная мишень может быть обнаружена путем прямого мечения антителом. Альтернативно, второе меченое антитело, специфическое к первому антителу, подвергается воздействию комплекса мишень - первое антитело с образованием тройного комплекса мишень - первое антитело - второе антитело. Комплекс обнаруживают по сигналу, испускаемому репортерной молекулой. Под «репортерной молекулой», как используется в данном описании, подразумевается молекула, которая по своей химической природе обеспечивает аналитически идентифицируемый сигнал, который позволяет обнаруживать антигенсвязанное антитело. Наиболее часто используемые репортерные молекулы в этом типе анализа представляют собой либо ферменты, флуорофоры, либо молекулы, содержащие радионуклиды (то есть радиоизотопы), и хемилюминесцентные молекулы.
В случае иммуноферментного анализа (EIA) фермент конъюгируют со вторым антителом, обычно с помощью глутаральдегида или периодата. Однако, как будет легко понятно, существует большое разнообразие различных методов конъюгации, которые легко доступны для специалиста в данной области техники. Примеры обычно используемых ферментов, подходящих для способов согласно данному изобретению, включают пероксидазу хрена, глюкозооксидазу, бета-галактозидазу и щелочную фосфатазу. Субстраты для использования со специфическими ферментами обычно выбирают для получения при гидролизе соответствующего фермента обнаруживаемого изменения цвета. Также возможно использовать флуорогенные субстраты, которые дают флуоресцирующий продукт, а не хромогенные субстраты, упомянутые выше. Во всех случаях меченное ферментом антитело добавляют к первому комплексу антитело-молекулярный маркер, дают возможность связываться, а затем избыток реагента отмывают.Раствор, содержащий соответствующий субстрат, затем добавляют к комплексу антитело-антиген-антитело. Субстрат будет реагировать с ферментом, связанным со вторым антителом, давая качественный визуальный сигнал, который может быть дополнительно количественно измерен, как правило, спектрофотометрически, для определения количества биомаркера (например, триптазы), который присутствовал в образце. Альтернативно, флуоресцентные соединения, такие как флуоресцеин и родамин, могут быть химически связаны с антителами без изменения их способности к связыванию. При активации светом определенной длины волны меченное флуорохромом антитело адсорбирует световую энергию, индуцируя состояние возбудимости в молекуле с последующим излучением света характерного цвета, визуально определяемого с помощью светового микроскопа. Как и в EIA, флуоресцентно меченное антитело может связываться с первым комплексом антитело-молекулярный маркер. После отмывки несвязанного реагента оставшийся тройной комплекс затем подвергают воздействию света соответствующей длины волны, наблюдаемая флуоресценция указывает на присутствие представляющего интерес молекулярного маркера. Методы иммунофлуоресценции и EIA очень хорошо известны в данной области техники. Однако также могут быть использованы другие репортерные молекулы, такие как радиоизотопные, хемилюминесцентные или биолюминесцентные молекулы.
В некоторых вариантах осуществления уровень активной триптазы в образце (например, в крови (например, в сыворотке или плазме), BAL или MLF) может быть определен с использованием ИФА-анализа активной триптазы, например, как описано в примере 6 предварительной заявки на патент США №62/457722. Концентрация активной триптазы человека (тетрамера) может быть определена при помощи ИФА-анализа. Вкратце, клон моноклонального антитела, распознающий триптазу человека, используют в качестве захватывающего антитела (например, моноклональное антитело В12, описанное в Fukuoka et al. выше, или клон антитела E88AS). Можно использовать любое подходящее антитело, связывающее человеческую триптазу. Рекомбинантная активная человеческая бета-1-триптаза очищается и используется в качестве исходного материала для приготовления стандартов анализа. Стандарты анализа, контроли и разведенные образцы инкубировали с 500 мкг/мл ингибитора трипсина сои (SBTI; Sigma кат.№10109886001) в течение 10 минут, а затем метили с помощью зонда на основе активности (АВР) (G0353816) в течение 1 часа. Низкомолекулярный ингибитор триптазы (G02849855) добавляют в течение 20 минут, чтобы остановить мечение АВР. В зависимости от захватывающего антитела, используемого в анализе, эту смесь можно инкубировать с антителом против триптазы человека, которое способно диссоциировать тетрамер триптазы (например, hu31A.v11 или В12), перед добавлением в планшет для ИФА с захватывающим антителом в течение 1 ч, промывают 1х фосфористым солевым раствором - TWEEN® (PBST) и инкубируют с реагентом SA-HRP (стрептавидин-конъюгированная пероксидаза хрена, каталожный номер General Electric (GE) RPN4401V) в течение 2 часов. Колориметрический сигнал генерируют путем применения субстрата HRP, тетраметилбензидина (ТМВ), и реакцию останавливают добавлением фосфорной кислоты. Планшеты считывают на планшет-ридере (например, планшет-ридере SpectraMax® М5) при 450 нм для определения поглощения и 650 нм для эталонного поглощения. Аналогичный анализ может быть проведен для определения уровня активной триптазы яванского макака (макак-крабоед) в образце (например, в крови (например, в сыворотке или плазме), BAL или MLF), например, с использованием клона антитела 13G6 в качестве захватывающего антитела.
В некоторых вариантах осуществления уровень общей триптазы в образце (например, в крови (например, в сыворотке или плазме), BAL или MLF) может быть определен с использованием ИФА-анализа общей триптазы, например, как описано в примере 6 предварительной заявки на патент США №62/457722. Вкратце, концентрацию общей триптазы человека можно определить с помощью ИФА-анализа. Антитело, распознающее человеческую триптазу, используют в качестве захватывающего антитела (например, клона антитела В12). Моноклональное антитело, распознающее человеческую триптазу, используют в качестве детектирующего антитела (например, клона антитела E82AS). Рекомбинантная активная человеческая бета-1-триптаза очищается и используется в качестве исходного материала для приготовления стандартов анализа. В зависимости от захватывающего антитела, используемого в анализе, эту смесь можно инкубировать с антителом против триптазы человека, которое способно диссоциировать тетрамер триптазы (например, hu31A.v11 или В12), перед добавлением в планшет для ИФА с захватывающим антителом в течение 2 часов и затем промывают 1х PBST. Биотинилированное детектирующее антитело добавляют в течение 1 часа. Затем добавляется реагент SA-HRP в течение 1 часа. Колориметрический сигнал генерируют путем применения ТМВ, и реакцию останавливают добавлением фосфорной кислоты. Планшеты считывают на планшет-ридере (например, планшет-ридере SpectraMax® М5) при 450 нм для определения поглощения и 650 нм для эталонного поглощения. Аналогичный анализ может быть проведен для определения уровня общей триптазы яванского макаки (макак-крабоед) в образце (например, в крови (например, в сыворотке или плазме), BAL или MLF), например, с использованием клона антитела 13G6 в качестве захватывающего антитела и клона антитела E88AS в качестве анализа на обнаружение.
В некоторых вариантах осуществления иллюстративный эталонный уровень для общей триптазы в крови (например, в сыворотке или плазме) может составлять около 1 нг/мл, около 2 нг/мл, около 3 нг/мл, около 4 нг/мл, около 5 нг/мл, около 6 нг/мл, около 7 нг/мл, около 8 нг/мл, около 9 нг/мл или около 10 нг/мл. Например, в некоторых вариантах осуществления иллюстративный эталонный уровень для общей триптазы в плазме составляет около 3 нг/мл. В другом примере в некоторых вариантах иллюстративный эталонный уровень для общей триптазы в сыворотке составляет около 4 нг/мл. Например, в некоторых вариантах осуществления субъект может иметь уровень общей триптазы, который равен или выше эталонного уровня, если уровень общей триптазы субъекта (например, в крови (например, в сыворотке или плазме) составляет около 1 нг/мл или выше, около 2 нг/мл или выше, около 3 нг/мл или выше, около 4 нг/мл или выше, около 5 нг/мл или выше, около 6 нг/мл или выше, около 7 нг/мл или выше, около 8 нг/мл или выше, около 9 нг/мл или выше, или около 10 нг/мл или выше. Например, в некоторых вариантах осуществления субъект может иметь уровень общей триптазы, который равен или выше эталонного уровня, если уровень общей триптазы в плазме составляет 3 нг/мл или выше. В другом примере в некоторых вариантах осуществления субъект может иметь уровень общей триптазы, который равен или выше эталонного уровня, если уровень общей триптазы в сыворотке субъекта составляет 4 нг/мл или выше.
В некоторых вариантах осуществления данного изобретения для определения уровня периостина в образце, полученном от пациента, используют анализ общего периостина, как описано в публикации международной патентной заявки № WO 2012/083132, которая полностью включена в данный документ посредством ссылки. Например, может быть использован ИФА-анализ с захватом периостина, который является очень чувствительным (чувствительность приблизительно 1,88 нг/мл), называемый анализом Е4 в WO 2012/083132. Антитела распознают изоформы периостина 1-4 (SEQ ID NO: 5-8 в WO 2012/083132) с наномолярной аффинностью. В других вариантах осуществления анализ периостина ELECSYS®, описанный в WO 2012/083132, можно использовать для определения уровня периостина в образце, полученном от пациента.
В некоторых вариантах осуществления иллюстративный эталонный уровень для уровней периостина составляет 20 нг/мл, например, при использовании анализа Е4, описанного выше. Например, при использовании анализа Е4 пациент может иметь уровень периостина, равный или превышающий эталонный уровень, если уровень периостина пациента (например, в сыворотке или плазме) составляет 20 нг/мл или выше, 21 нг/мл или выше, 22 нг/мл или выше, 23 нг/мл или выше, 24 нг/мл или выше, 25 нг/мл или выше, 26 нг/мл или выше, 27 нг/мл или выше, 28 нг/мл или выше, 29 нг/мл или выше, 30 нг/мл или выше, 31 нг/мл или выше, 32 нг/мл или выше, 33 нг/мл или выше, 34 нг/мл или выше, 35 нг/мл или выше, 36 нг/мл или выше, 37 нг/мл или выше, 38 нг/мл или выше, 39 нг/мл или выше, 40 нг/мл или выше, 41 нг/мл или выше, 42 нг/мл или выше, 43 нг/мл или выше, 44 нг/мл или выше, 45 нг/мл или выше, 46 нг/мл или выше, 47 нг/мл или выше, 48 нг/мл или выше, 49 нг/мл или выше, 50 нг/мл или выше, 51 нг/мл или выше, 52 нг/мл или выше, 53 нг/мл или выше, 54 нг/мл или выше, 55 нг/мл или выше, 56 нг/мл или выше, 57 нг/мл или выше, 58 нг/мл или выше, 59 нг/мл или выше, 60 нг/мл или выше, 61 нг/мл или выше, 62 нг/мл или выше, 63 нг/мл или выше, 64 нг/мл или выше, 65 нг/мл или выше, 66 нг/мл или выше, 67 нг/мл или выше, 68 нг/мл или выше, 69 нг/мл или выше, или 70 нг/мл или выше.
При использовании анализа Е4 пациент может иметь уровень периостина, равный или меньший, чем эталонный уровень, если уровень периостина пациента (например, в сыворотке или плазме) составляет 20 нг/мл или ниже, 19 нг/мл или ниже, 18 нг/мл или ниже, 17 нг/мл или ниже, 16 нг/мл или ниже, 15 нг/мл или ниже, 14 нг/мл или ниже, 13 нг/мл или ниже, 12 нг/мл или ниже, 11 нг/мл или ниже, 10 нг/мл или ниже, 9 нг/мл или ниже, 8 нг/мл или ниже, 7 нг/мл или ниже, 6 нг/мл или ниже, 5 нг/мл или ниже, 4 нг/мл или ниже, 3 нг/мл или ниже, 2 нг/мл или ниже, или 1 нг/мл или ниже.
В других вариантах осуществления иллюстративный эталонный уровень для уровней периостина (например, в сыворотке или плазме) составляет 50 нг/мл, например, при использовании анализа периостина ELECSYS®, описанного выше. Например, при использовании анализа периостина ELECSYS® пациент может иметь уровень периостина, равный или превышающий эталонный уровень, если уровень периостина у пациента составляет 50 нг/мл или выше, 51 нг/мл или выше, 52 нг/мл или выше, 53 нг/мл или выше, 54 нг/мл или выше, 55 нг/мл или выше, 56 нг/мл или выше, 57 нг/мл или выше, 58 нг/мл или выше, 59 нг/мл или выше 60 нг/мл или выше, 61 нг/мл или выше, 62 нг/мл или выше, 63 нг/мл или выше, 64 нг/мл или выше, 65 нг/мл или выше, 66 нг/мл или выше, 67 нг/мл или выше, 68 нг/мл или выше, 69 нг/мл или выше, 70 нг/мл или выше, 71 нг/мл или выше, 72 нг/мл или выше, 73 нг/мл или выше, 74 нг/мл или выше, 75 нг/мл или выше, 76 нг/мл или выше, 77 нг/мл или выше, 78 нг/мл или выше, 79 нг/мл или выше, 80 нг/мл или выше, 81 нг/мл или выше, 82 нг/мл или выше, 83 нг/мл или выше, 84 нг/мл или выше, 85 нг/мл или выше, 86 нг/мл или выше, 87 нг/мл или выше, 88 нг/мл или выше, 89 нг/мл или выше, 90 нг/мл или выше, 91 нг/мл или выше ее, 92 нг/мл или выше, 93 нг/мл или выше, 94 нг/мл или выше, 95 нг/мл или выше, 96 нг/мл или выше, 97 нг/мл или выше, 98 нг/мл или выше или 99 нг/мл или выше.
При использовании анализа периостина ELECSYS® пациент может иметь уровень периостина, равный или меньший, чем эталонный уровень, если уровень периостина у пациента (например, в сыворотке или плазме) составляет 50 нг/мл или ниже, 49 нг/мл или ниже, 48 нг/мл или ниже, 47 нг/мл или ниже, 46 нг/мл или ниже, 45 нг/мл или ниже, 44 нг/мл или ниже, 43 нг/мл или ниже, 42 нг/мл или ниже, 41 нг/мл или ниже, 40 нг/мл или ниже, 39 нг/мл или ниже, 38 нг/мл или ниже, 37 нг/мл или ниже, 36 нг/мл или ниже, 35 нг/мл или ниже, 34 нг/мл или ниже, 33 нг/мл или ниже, 32 нг/мл или ниже, 31 нг/мл или ниже, 30 нг/мл или ниже, 29 нг/мл или ниже, 28 нг/мл или ниже, 27 нг/мл или ниже, 26 нг/мл или ниже, 25 нг/мл или ниже, 24 нг/мл или ниже, 23 нг/мл или ниже, 22 нг/мл или ниже, 21 нг/мл или ниже, 20 нг/мл или ниже, 19 нг/мл или ниже, 18 нг/мл или ниже, 17 нг/мл или ниже, 16 нг/мл или ниже, 15 нг/мл или ниже, 14 нг/мл или ниже, 13 нг/мл или ниже, 12 нг/мл или ниже, 11 нг/мл или ниже, 10 нг/мл или ниже, 9 нг/мл или ниже, 8 нг/мл или ниже, 7 нг/мл или ниже, 6 нг/мл или ниже, 5 нг/мл или ниже, 4 нг/мл или ниже, 3 нг/мл или ниже, 2 нг/мл или ниже, или 1 нг/мл или ниже.
VI. Наборы
Для использования при обнаружении присутствия и/или уровня экспрессии биомаркеров (например, триптазы) в изобретении также предложены наборы или промышленные изделия. Такие наборы можно использовать для определения того, может ли пациент с воспалительным заболеванием, опосредованным тучными клетками, (например, астмой), отвечать на терапию, например, терапию, включающую агент, выбранный из группы, состоящей из антагониста триптазы, антагониста IgE, антагониста FcεR, антитела, истощающего IgE+ В-клетки, антитело, истощающего тучные клетки или базофилы, антагонист PAR2 и их комбинации (например, антагониста триптазы и антагониста IgE) или терапию, включающую антагонист IgE или антагонист Fc-эпсилон-рецептора (FcεR), и/или можно использовать для оценки или контроля ответа пациента с астмой на лечение терапией. В некоторых вариантах осуществления наборы могут использоваться для определения количества активных аллелей триптазы у пациента. В других вариантах осуществления наборы могут использоваться для определения уровня экспрессии триптазы (например, активной или общей триптазы) в образце от пациента. Такие наборы могут быть использованы для осуществления любого из способов изобретения.
Например, изобретение обеспечивает набор для идентификации пациента с воспалительным заболеванием, опосредованным тучными клетками, который имеет вероятность ответа на терапию, направленную на тучные клетки, (например, терапию, включающую агент, выбранный из группы, состоящей из антагониста триптазы, антагониста IgE, антагониста FcεR, антитела, истощающего IgE+ В-клетки, антитела, истощающего тучные клетки или базофилы, антагониста PAR2 и их комбинации (например, антагониста триптазы и антагониста IgE)), причем набор включает: (а) реагенты для определения количества активных аллелей триптазы у пациента или для определения уровня экспрессии триптазы в образце от пациента; и, необязательно, (b) инструкции по применению реагентов для идентификации пациента с воспалительным заболеванием, опосредованным тучными клетками, который имеет вероятность ответа на терапию, направленную на тучные клетки, (например, терапию, включающую агент, выбранный из группы, состоящей из антагониста триптазы, антагониста IgE, антагониста FcεR, антитела, истощающего IgE+ В-клетки, антитела, истощающего тучные клетки или базофилы, антагониста PAR2, и их комбинации (например, антагониста триптазы и антагониста IgE)). В некоторых вариантах осуществления набор содержит реагенты для определения количества активных аллелей триптазы у пациента. В других вариантах осуществления набор содержит реагенты для определения уровня экспрессии триптазы в образце от пациента.
В другом примере изобретение обеспечивает набор для идентификации пациента с воспалительным заболеванием, опосредованным тучными клетками, который имеет вероятность ответа на терапию, включающую антагонист IgE или антагонист FcεR, который включает (а) реагенты для определения количества активных аллелей триптазы у пациента или для определения уровня экспрессии триптазы в образце от пациента; и, необязательно, (b) инструкции по применению реагентов для идентификации пациента с воспалительным заболеванием, опосредованным тучными клетками, который имеет вероятность ответа на терапию, включающую антагонист IgE или антагонист FcεR.
Любые подходящие реагенты для определения количества активных аллелей триптазы у пациента или для определения уровня экспрессии триптазы можно использовать в любом из предшествующих наборов, включая, например, олигонуклеотиды, полипептиды (например, антитела) и тому подобное.
В некоторых вариантах осуществления набор дополнительно содержит реагенты для определения уровня биомаркера 2-го типа в образце от пациента.
Например, в некоторых вариантах осуществления реагент содержит олигонуклеотид. Олигонуклеотиды, «специфические для» генетического локуса, связываются или с полиморфной областью локуса, или связываются рядом с полиморфной областью локуса. Для олигонуклеотидов, которые должны использоваться в качестве праймеров для амплификации, праймеры являются смежными, если они достаточно близки, чтобы их можно было использовать для получения полинуклеотида, содержащего полиморфную область. В одном варианте осуществления олигонуклеотиды являются смежными, если они связываются в пределах приблизительно 1-2 т.п.н., например, менее чем 1 т.п.н. от полиморфизма. Специфические олигонуклеотиды способны гибридизоваться с последовательностью и в подходящих условиях не будут связываться с последовательностью, отличающейся одним нуклеотидом.
Олигонуклеотиды, независимо от того, используются ли они в качестве зондов или праймеров, содержащиеся в наборе, могут быть детектируемо помечены. Метки могут быть обнаружены или непосредственно, например, для флуоресцентных меток, или косвенно. Непрямое обнаружение может включать любой способ обнаружения, известный специалисту в данной области техники, включая взаимодействия биотина и авидина, связывание антител и тому подобное. Флуоресцентно меченные олигонуклеотиды также могут содержать тушащую молекулу. Олигонуклеотиды могут быть связаны с поверхностью. В некоторых вариантах осуществления поверхность представляет собой диоксид кремния или стекло. В некоторых вариантах осуществления поверхность представляет собой металлический электрод.
В других вариантах осуществления реагент для определения уровня экспрессии триптазы может представлять собой полипептид, например, антитело. В некоторых вариантах осуществления антитело может быть детектируемо помечено.
Еще другие наборы согласно изобретению содержат по меньшей мере один реагент, необходимый для проведения анализа. Например, набор может содержать фермент. Альтернативно, набор может содержать буфер или любой другой необходимый реагент. Наборы могут включать все или некоторые из положительных контролей, отрицательных контролей, реагентов, праймеров, маркеров секвенирования, зондов и антител, описанных в данном документе, для определения количества активных аллелей триптазы у пациента или определения уровня экспрессии триптазы в образце от пациента.
Любой из предшествующих наборов может содержать носитель, разделенный на части для размещения в герметично закрывающихся одном или более контейнерах, таких как флаконы, пробирки и тому подобное, причем каждый из контейнеров содержит один из отдельных элементов, которые должны использоваться в способе. Например, один из контейнеров может содержать зонд, который имеет или может быть детектируемо помечен. Такой зонд может представлять собой антитело или олигонуклеотид, специфические для белка или транскрипта, соответственно. Если набор используется для гибридизации нуклеиновой кислоты для обнаружения целевой нуклеиновой кислоты, то набор также может иметь контейнеры, содержащие нуклеотид(ы) для амплификации последовательности целевой нуклеиновой кислоты, и/или контейнер, содержащий репортер, такой как биотин-связывающий белок (например, авидин или стрептавидин), связанный с репортерной молекулой, такой как ферментативная, флуоресцентная или радиоизотопная метка.
Такие наборы обычно содержат контейнер, описанный выше, и один или более других контейнеров, содержащих материалы, желательные с коммерческой и потребительской точки зрения, включая буферы, разбавители, фильтры, иглы, шприцы и вкладыши в упаковку с инструкциями по применению. На контейнере может присутствовать этикетка, указывающая на то, что композиция используется для конкретного применения, и может также указывать на направления для использования как in vivo, так и in vitro, такие как описанные выше.
Наборы согласно изобретению имеют ряд вариантов осуществления. Типичным вариантом осуществления является набор, содержащий контейнер, этикетку на указанном контейнере и композицию, содержащуюся в указанном контейнере, причем композиция содержит первичное антитело, которое связывается с белковым биомаркером (например, триптазой), а этикетка на указанном контейнере указывает на то, что композицию можно использовать для оценки присутствия таких белков в образце, и при этом набор включает инструкции по использованию антитела для оценки присутствия биомаркерных белков в конкретном типе образца. Набор может дополнительно содержать набор инструкций и материалов для приготовления образца и нанесения антитела на образец. Набор может включать как первичное, так и вторичное антитело, причем вторичное антитело конъюгировано с меткой, например, ферментативной меткой.
Другим вариантом осуществления является набор, содержащий контейнер, этикетку на указанном контейнере и композицию, содержащуюся в указанном контейнере, причем композиция содержит один или более полинуклеотидов, которые гибридизуются с комплементом биомаркера (например, триптазы) в жестких условиях, а этикетка на указанном контейнере указывает на то, что композицию можно использовать для оценки присутствия биомаркера (например, триптазы) в образце, и при этом набор включает инструкции по использованию полинуклеотида(ов) для оценки присутствия биомаркера РНК или ДНК в конкретном типе образца.
Другие необязательные компоненты набора включают один или более буферов (например, блокирующий буфер, промывочный буфер, субстратный буфер и т.д.), Другие реагенты, такие как субстрат (например, хромоген), которые химически изменены при помощи ферментативной метки, раствор для демаскировки антигена, контрольные образцы (положительный и/или отрицательный контроли), контрольный(е) микроскопический препарат(-ы) и т.д. Наборы могут также включать инструкции для интерпретации результатов, полученных с использованием набора.
В других конкретных вариантах осуществления для наборов на основе антител, набор может содержать, например: (1) первое антитело (например, прикрепленное к твердой подложке), которое связывается с биомаркерным белком (например, триптазой); и, необязательно, (2) второе, другое антитело, которое связывается или с белком, или с первым антителом и конъюгируется с детектируемой меткой.
Для наборов на основе олигонуклеотидов, набор может содержать, например: (1) олигонуклеотид, например, детектируемый меченый олигонуклеотид, который гибридизуется с геном триптазы (например, TPSAB1 или TPSB2), и/или последовательность нуклеиновой кислоты, кодирующую последовательность нуклеиновой кислоты биомаркерного белка (например, триптазы) или (2) пару праймеров, применяемых для амплификации молекулы нуклеиновой кислоты биомаркера. Набор также может содержать, например, буферный агент, консервант или стабилизирующий белок агент. Набор может дополнительно содержать компоненты, необходимые для обнаружения детектируемой метки (например, фермент или субстрат). Набор также может содержать контрольный образец или серию контрольных образцов, которые можно анализировать и сравнивать с тестируемым образцом. Каждый компонент набора может быть заключен в отдельный контейнер, а все различные контейнеры могут находиться в одной упаковке вместе с инструкциями для интерпретации результатов анализов, выполненных с использованием набора.
Любой из предшествующих наборов может дополнительно включать один или более терапевтических агентов, включая любой из антагонистов триптазы, антагонистов FcεR, антител, истощающих IgE+ В-клетки, антител, истощающих тучные клетки или базофилы, антагонистов PAR2, антагонистов IgE и их комбинаций (например, антагониста триптазы и антагониста IgE) и/или дополнительных терапевтических агентов, описанных в данном документе.
VII. Композиции и фармацевтические составы
В одном аспекте изобретение основано, в частности, на открытии, что биомаркеры согласно изобретению (например, количество активных аллелей триптазы у пациента и/или уровень экспрессии триптазы) могут использоваться для идентификации пациентов с воспалительным заболеванием, опосредованным тучными клетками, имеющих вероятность ответа на терапию (например, терапию, включающую агент, выбранный из группы, состоящей из антагониста триптазы, антагониста Fc-эпсилон-рецептора (FcεR), антитела, истощающего IgE+ В-клетки, антитела, истощающего тучные клетки или базофилы, антагониста активируемого протеазой рецептора 2 (PAR2), антагониста IgE и их комбинации (например, антагониста триптазы и антагониста IgE)). Эти агенты и их комбинации полезны для лечения воспалительных заболеваний, опосредованных тучными клетками, например, как часть любого из способов, описанных в данном документе, например, в разделах II и III выше. В некоторых вариантах осуществления терапия представляет собой терапию, направленную на тучные клетки. Любой подходящий антагонист триптазы (например, антитело против триптазы), антагонист Fc-эпсилон-рецептора (FcεR), антитело, истощающее IgE+ В-клетки, антитело, истощающее тучные клетки или базофилы, антагонист активируемого протеазой рецептора 2 (PAR2) и/или антагонист IgE могут использоваться в способах и анализах, описанных в данном документе. Неограничивающие примеры, подходящие для использования в способах и анализах изобретения, описаны дополнительно ниже.
А. Антитела
Любое подходящее антитело может быть использовано в способах, описанных в данном документе, например, антитела против триптазы, антитела против FcεR, антитела, истощающие IgE+ В-клетки, антитела, истощающие тучные клетки или базофилы, антитела против PAR2 и/или антитела против IgE. Предполагается, что такие антитела против триптазы, антитела против FcεR, антитела, истощающие IgE+ В-клетки, антитела, истощающие тучные клетки или базофилы, антитела против PAR2 и/или антитела против IgE для применения в любом из перечисленных выше вариантов осуществления могут иметь любые признаки, по отдельности или в комбинации, описанные в разделах а-с и 1-7 ниже.
а. Антитела против триптазы
Любое подходящее антитело против триптазы можно использовать в способах согласно изобретению. Например, антитело против триптазы может представлять собой любое антитело против триптазы, описанное в предварительной заявке на патент США №62/457722, которая полностью включена в данный документ посредством ссылки.
В некоторых вариантах осуществления антитело против триптазы (например, антитело против бета-триптазы) может содержать по меньшей мере одну, по меньшей мере две, по меньшей мере три, по меньшей мере четыре, по меньшей мере пять или все шесть гипервариабельных областей (HVR), выбранных из (a) HVR-H1, содержащей аминокислотную последовательность DYGMV (SEQ ID NO: 1); (b) HVR-H2, содержащей аминокислотную последовательность FISSGSSTVYYADTMKG (SEQ ID NO: 2); (с) HVR-H3, содержащей аминокислотную последовательность RNYDDWYFDV (SEQ ID NO: 3); (d) HVR-L1, содержащей аминокислотную последовательность SASSSVTYMY (SEQ ID NO: 4); (е) HVR-L2, содержащей аминокислотную последовательность RTSDLAS (SEQ ID: 5); и (f) HVR-L3, содержащей аминокислотную последовательность QHYHSYPLT (SEQ ID NO: 6), или комбинации одной или более из указанных выше HVR и одного или более их вариантов, имеющих по меньшей мере около 80% идентичность последовательности (например, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, или 99% идентичность) с любой из SEQ ID NO: 1-6. Например, в некоторых вариантах осуществления антитело против триптазы содержит (a) HVR-H1, содержащую аминокислотную последовательность DYGMV (SEQ ID NO: 1); (b) HVR-H2, содержащую аминокислотную последовательность FISSGSSTVYYADTMKG (SEQ ID NO: 2); (с) HVR-H3, содержащую аминокислотную последовательность RNYDDWYFDV (SEQ ID NO: 3); (d) HVR-L1, содержащую аминокислотную последовательность SASSSVTYMY (SEQ ID NO: 4); (е) HVR-L2, содержащую аминокислотную последовательность RTSDLAS (SEQ ID: 5); и (f) HVR-L3, содержащую аминокислотную последовательность QHYHSYPLT (SEQ ID NO: 6).
В некоторых вариантах осуществления антитело против триптазы (например, антитело против бета-триптазы) может содержать (а) вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, имеющую по меньшей мере 90% идентичность последовательности с (например, по меньшей мере 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичность последовательности) или аминокислотную последовательность SEQ ID NO: 7; (b) вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, имеющую по меньшей мере 90% идентичность последовательности с (например, по меньшей мере 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичность последовательности) или аминокислотную последовательность SEQ ID NO: 8; или (с) домен VH как в (а) и домен VL как в (b). Например, в некоторых вариантах осуществления домен VH содержит аминокислотную последовательность SEQ ID NO: 7. В некоторых вариантах осуществления домен VL содержит аминокислотную последовательность SEQ ID NO: 8. В конкретных вариантах осуществления домен VH содержит аминокислотную последовательность SEQ ID NO: 7, и домен VL содержит аминокислотную последовательность SEQ ID NO: 8.
В некоторых вариантах осуществления антитело против триптазы (например, антитело против бета-триптазы) может содержать (а) тяжелую цепь, содержащую аминокислотную последовательность, имеющую по меньшей мере 90% идентичность последовательности с (например, по меньшей мере 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичность последовательности) или аминокислотную последовательность SEQ ID NO: 9; и (b) легкую цепь, содержащую аминокислотную последовательность, имеющую по меньшей мере 90% идентичность последовательности с (например, по меньшей мере 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичность последовательности) или аминокислотную последовательность SEQ ID NO: 10. Например, в некоторых вариантах осуществления антитело против триптазы (например, антитело против бета-триптазы) содержит (а) тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 9, и (b) легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 10.
В других вариантах осуществления антитело против триптазы (например, антитело против бета-триптазы) может содержать (а) тяжелую цепь, содержащую аминокислотную последовательность, имеющую по меньшей мере 90% идентичность последовательности с (например, по меньшей мере 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичность последовательности) или аминокислотную последовательность SEQ ID NO: 11; и (b) легкую цепь, содержащую аминокислотную последовательность, имеющую по меньшей мере 90% идентичность последовательности с (например, по меньшей мере 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичность последовательности) или аминокислотную последовательность SEQ ID NO: 10. Например, в некоторых вариантах осуществления антитело против триптазы (например, антитело против бета-триптазы) содержит (а) тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 11, и (b) легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 10.
В еще других вариантах осуществления антитело против триптазы (например, антитело против бета-триптазы) содержит по меньшей мере одну, по меньшей мере две, по меньшей мере три, по меньшей мере четыре, по меньшей мере пять или все шесть гипервариабельных областей (HVR), выбранных из (a) HVR-H1, содержащей аминокислотную последовательность GYAIT (SEQ ID NO: 12); (b) HVR-H2, содержащую аминокислотную последовательность GISSAATTFYSSWAKS (SEQ ID NO: 13); (с) HVR-H3, содержащую аминокислотную последовательность DPRGYGAALDRLDL (SEQ ID NO: 14); (d) HVR-L1, содержащую аминокислотную последовательность QSIKSVYNNRLG (SEQ ID NO: 15); (е) HVR-L2, содержащую аминокислотную последовательность ETSILTS (SEQ ID: 16); и (f) HVR-L3, содержащую аминокислотную последовательность AGGFDRSGDTT (SEQ ID NO: 17), или комбинации одной или более из указанных выше HVR и одного или более их вариантов, имеющих по меньшей мере около 80% идентичность последовательности (например, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, или 99% идентичность) с любой из SEQ ID NO: 12-17. Например, в некоторых вариантах осуществления антитело против триптазы содержит (а) HVR-H1, содержащую аминокислотную последовательность GYAIT (SEQ ID NO: 12); (b) HVR-H2, содержащую аминокислотную последовательность GISSAATTFYSSWAKS (SEQ ID NO: 13); (с) HVR-H3, содержащую аминокислотную последовательность DPRGYGAALDRLDL (SEQ ID NO: 14); (d) HVR-L1, содержащую аминокислотную последовательность QSIKSVYNNRLG (SEQ ID NO: 15); (e) HVR-L2, содержащую аминокислотную последовательность ETSILTS (SEQ ID: 16); и (f) HVR-L3, содержащую аминокислотную последовательность AGGFDRSGDTT (SEQ ID NO: 17).
В некоторых вариантах осуществления антитело против триптазы (например, антитело против бета-триптазы) содержит (а) вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, имеющую по меньшей мере 90% идентичность последовательности с (например, по меньшей мере 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичность последовательности) или аминокислотную последовательность SEQ ID NO: 18; (b) вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, имеющую по меньшей мере 90% идентичность последовательности с (например, по меньшей мере 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичность последовательности) или аминокислотную последовательность SEQ ID NO: 19; или (с) домен VH как в (а) и домен VL как в (b). Например, в некоторых вариантах осуществления домен VH содержит аминокислотную последовательность SEQ ID NO: 18. В некоторых вариантах осуществления домен VL содержит аминокислотную последовательность SEQ ID NO: 19. В конкретных вариантах осуществления домен VH содержит аминокислотную последовательность SEQ ID NO: 18, и домен VL содержит аминокислотную последовательность SEQ ID NO: 19.
В некоторых вариантах осуществления любого из предшествующих способов антитело против триптазы (например, антитело против бета-триптазы) содержит (а) тяжелую цепь, содержащую аминокислотную последовательность, имеющую по меньшей мере 90% идентичность последовательности с (например, по меньшей мере 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичность последовательности) или аминокислотную последовательность SEQ ID NO: 20; и (b) легкую цепь, содержащую аминокислотную последовательность, имеющую по меньшей мере 90% идентичность последовательности с (например, по меньшей мере 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичность последовательности) или аминокислотную последовательность SEQ ID NO: 21. Например, в некоторых вариантах осуществления антитело против триптазы (например, антитело против бета-триптазы) содержит (а) тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 20, и (b) легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 21.
В других вариантах осуществления любого из предшествующих способов антитело против триптазы (например, антитело против бета-триптазы) содержит (а) тяжелую цепь, содержащую аминокислотную последовательность, имеющую по меньшей мере 90% идентичность последовательности с (например, по меньшей мере 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичность последовательности) или аминокислотную последовательность SEQ ID NO: 22; и (b) легкую цепь, содержащую аминокислотную последовательность, имеющую по меньшей мере 90% идентичность последовательности с (например, по меньшей мере 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичность последовательности) или аминокислотную последовательность SEQ ID NO: 21. Например, в некоторых вариантах осуществления антитело против триптазы (например, антитело против бета-триптазы) содержит (а) тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 22, и (b) легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 21.
В некоторых вариантах осуществления антитело против триптазы представляет собой антитело, которое связывается с тем же эпитопом, что и любое из предшествующих антител.
Любое из антител против триптазы, описанных в данном документе, можно вводить в комбинации с любым из антител против IgE, описанных в подразделе С ниже, включая омализумаб (XOLAIR®).
b. Антитела, истощающие IgE+ В-клетки
Любое подходящее антитело, истощающее IgE+ В-клетки, может быть использовано в способах согласно изобретению. В некоторых вариантах осуществления антитело, истощающее IgE+ В-клетки, представляет собой антитело против М1' (например, килизумаб). В некоторых вариантах осуществления антитело против М1' представляет собой любое антитело против М1', описанное в публикации международной патентной заявки № WO 2008/116149.
c. Антитела против IgE
Любое подходящее антитело против IgE может быть использовано в способах согласно изобретению. Иллюстративные антитела против IgE включают rhuMabE25 (Е25, омализумаб (XOLAIR®)), Е26, Е27, а также CGP-5101 (Ни-901), антитело к НА (гемагглютинин), лигелизумаб и тализумаб. Аминокислотные последовательности вариабельных доменов тяжелой и легкой цепей гуманизированных антител против IgE Е25, Е26 и Е27 описаны, например, в патенте США №6172213 и WO 99/01556. Антитело CGP-5101 (Ни-901) описано в Corne et al. J. Clin. Invest. 99(5): 879-887, 1997; WO 92/17207; и №№депонирования в АТСС BRL-10706, BRL-11130, BRL-11131, BRL-11132 и BRL-11133. Антитело к НА описано в US №60/444229, WO 2004/070011, и WO 2004/070010.
Например, в некоторых вариантах осуществления антитело против IgE содержит одну, две, три, четыре, пять или все шесть из следующих шести HVR: (a) HVR-H1, содержащую аминокислотную последовательность GYSWN (SEQ ID NO: 40); (b) HVR-H2, содержащую аминокислотную последовательность SITYDGSTNYNPSVKG (SEQ ID NO: 41); (с) HVR-H3, содержащую аминокислотную последовательность GSHYFGHWHFAV (SEQ ID NO: 42); (d) HVR-L1, содержащую аминокислотную последовательность RASQSVDYDGDSYMN (SEQ ID NO: 43); (е) HVR-L2, содержащую аминокислотную последовательность AASYLES (SEQ ID: 44); и (f) HVR-L3, содержащую аминокислотную последовательность QQSHEDPYT (SEQ ID NO: 45). В некоторых вариантах осуществления антитело против IgE содержит (а) домен VH, содержащий аминокислотную последовательность, имеющую по меньшей мере 90% идентичность последовательности (например, по меньшей мере 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичность последовательности) с аминокислотной последовательностью SEQ ID NO: 38; (b) домен VL, содержащий аминокислотную последовательность, имеющую по меньшей мере 90% идентичность последовательности (например, по меньшей мере 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичность последовательности) с аминокислотной последовательностью SEQ ID NO: 39; или (с) домен VH как в (а) и домен VL как в (b). В некоторых вариантах осуществления домен VH содержит аминокислотную последовательность SEQ ID NO: 38. В некоторых вариантах осуществления домен VL содержит аминокислотную последовательность SEQ ID NO: 39. В некоторых вариантах осуществления домен VH содержит аминокислотную последовательность SEQ ID NO: 38, и домен VL содержит аминокислотную последовательность SEQ ID NO: 39. Любое из антител против IgE, описанных в данном документе, можно использовать в комбинации с любым антителом против триптазы, описанным в подразделе А выше.
1. Аффинность антител
В определенных вариантах осуществления антитело, предложенное в данном документе, (например, антитело против триптазы, антитело против FcεR, антитело, истощающее IgE+ В-клетки, антитело, истощающее тучные клетки или базофилы, антитело против PAR2 или антитело против IgE) имеет константу диссоциации (KD)≤1 мкМ, ≤100 нМ, ≤10 нМ, ≤1 нМ, ≤0,1 нМ, ≤0,01 нМ, ≤1 пМ или ≤0,1 пМ (например, 10-6 М или менее, например, от 10-6 М до 10-9 М или менее, например, от 10-9 М до 10-13 М или менее). Например, в некоторых вариантах осуществления антитело против триптазы связывается стриптазой (например, триптазой человека, например бета-триптазой человека) с KD около 100 нМ или ниже (например, 100 нМ или ниже, 10 нМ или ниже, 1 нМ или ниже, 100 пМ или ниже, 10 пМ или ниже, 1 пМ или ниже, или 0,1 пМ или ниже). В некоторых вариантах осуществления антитело связывает триптазу (например, триптазу человека, например, бета-триптазу человека) с KD 10 нМ или ниже (например, 10 нМ или ниже, 1 нм или ниже, 100 пМ или ниже, 10 пМ или ниже, 1 пМ или ниже, или 0,1 пМ или ниже). В некоторых вариантах осуществления антитело связывает триптазу (например, триптазу человека, например, бета-триптазу человека) с KD 1 нМ или ниже (например, 1 нМ или ниже, 100 пМ или ниже, 10 пМ или ниже, 1 пМ или ниже, или 0,1 пМ или ниже). В некоторых вариантах осуществления любое из антител против триптазы, описанных выше или в данном документе, связывается с триптазой (например, триптазой человека, например, бета-триптазой человека) с KD около 0,5 нМ или ниже (например, 0,5 нМ или ниже, 400 пМ или ниже, 300 пМ или ниже, 200 пМ или ниже, 100 пМ или ниже, 50 пМ или ниже, 25 пМ или ниже, 10 пМ или ниже, 1 пМ или ниже, или 0,1 пМ или ниже). В некоторых вариантах осуществления антитело связывается с триптазой (например, триптазой человека, например, бета-триптазой человека) с KD от около 0,1 нМ до около 0,5 нМ (например, около 0,1 нМ, около 0,2 нМ, около 0,3 нМ, около 0,4 нМ, или около 0,5 нМ). В некоторых вариантах осуществления антитело связывает триптазу (например, триптазу человека, например, бета-триптазу человека) с KD около 0,4 нМ. В некоторых вариантах осуществления антитело связывает триптазу (например, триптазу человека, например, бета-триптазу человека) с KD около 0,18 нМ. Любое из других антител, описанных в данном документе, может связываться со своим антигеном с аффинностями, как описано выше в отношении антител против триптазы.
В одном варианте осуществления KD измеряют с помощью анализа связывания антигена, меченного радиоактивным изотопом (РИА). В одном варианте осуществления РИА выполняли с использованием версии Fab представляющего интерес антитела и его антигена. Например, аффинность связывания Fab в растворе в отношении антигена измеряют, уравновешивая Fab минимальной концентрацией (125I)-меченного антигена в присутствии ряда титров немеченого антигена, затем иммобилизуя связанный антиген на планшете, покрытом антителом против Fab, (см., например, Chen et al. J. Mol. Biol. 293:865-881, 1999). Чтобы определить условия анализа, многолуночные планшеты MICROTITER® (Thermo Scientific) покрывали в течение ночи захватывающим антителом против Fab (Cappel Labs) в концентрации 5 мкг/мл в 50 мкМ растворе карбоната натрия (рН 9,6), а затем блокировали 2% (мас./об.) раствором бычьего сывороточного альбумина в PBS в течение от двух до пяти часов при комнатной температуре (около 23°С). В неадсорбентном планшете (Nunc №269620) смешивали 100 пМ или 26 пМ [125I]-антигена с серийными разведениями целевого Fab (например, в соответствии с оценкой антитела против ФРЭС, Fab-12, в Presta et al. Cancer Res. 57:4593-4599, 1997). Затем представляющий интерес Fab инкубировали в течение ночи; однако инкубацию можно продолжать в течение более длительного периода (например, около 65 часов), чтобы обеспечить достижение равновесия. Затем смесь переносили на планшет для захвата и инкубировали при комнатной температуре (например, в течение часа). Затем раствор удаляют и планшет промывают восемь раз 0,1% раствором полисорбата 20 (TWEEN®-20) в PBS. После высыхания планшетов добавляли 150 мкл/лунку сцинтиллятора (MICROSCINT-20™; Packard), а планшеты считывали на счетчике гамма-излучения TOPCOUNT™ (Packard) в течение десяти минут. Концентрации каждого Fab, обеспечивавшие связывание, меньшее или равное 20% от максимального, отбирали для использования в конкурентном анализе связывания.
В соответствии с другим вариантом осуществления KD измеряют методом поверхностного плазмонного резонанса BIACORE®. Например, анализ с использованием BIACORE®-2000 или BIACORE ®-3000 (BIAcore, Inc., Пискатауэй, Нью-Джерси) выполняли при 25°С с чипами СМ5 с иммобилизованным антигеном при 10 единицах ответа (RU). В одном варианте осуществления биосенсорные чипы на основе карбоксиметилированного декстрана (СМ5, BIACORE, Inc.) активируются N-этил-N'-(3-диметиламинопропил)-карбодиимид гидрохлоридом (EDC) и N-гидроксисукцинимидом (NHS) в соответствии с инструкциями изготовителя. Антиген разводят 10 мМ ацетата натрия, рН 4,8, до 5 мкг/мл (~0,2 мкМ) перед инжекцией при скорости потока 5 мкл/минута для достижения приблизительно 10 единиц ответа (RU) связанного белка. После введения антигена вводили 1 М раствор этаноламина для блокирования непрореагировавших групп. Для измерений кинетики двукратные серии разведений Fab (от 0,78 нМ до 500 нМ) вводили в PBS с 0,05% полисорбат 20 (TWEEN®-20) сурфактантом (PBST) при 25°С при расходе приблизительно 25 мкл/мин. Скорости ассоциации (kon) и диссоциации (koff) рассчитывали как простые однозначные модели связывания Лангмюра (программное обеспечение BIACORE® Evaluation версии 3.2) путем одновременной подгонки сенсограмм ассоциации и диссоциации. Равновесную константу диссоциации (KD) рассчитывали как отношение koff/kon. См., например, Chen et al. (J. Mol. Biol. 293:865-881, 1999). Если скорость превышает 106 M-1s-1 из вышеописанного способа поверхностного плазмонного резонанса, то скорости прямой реакции могут быть определены с помощью метода затухания флуоресценции, который измеряет повышение или понижение интенсивности флуоресцентного излучения (возбуждение = 295 нм; излучение = 340 нм, 16 нм полоса пропускания) при температуре 25°С 20 нМ антитела против антигена (Fab-форма) в PBS, при рН 7,2, в присутствии увеличивающихся концентраций антигена, что измеряется спектрометром, таким как спектрофотометр с устройством остановки потока (Aviv Instruments) или спектрометр SLM-AMINCO™ 8000 серии (ThermoSpectronic) с перемешивающей кюветой.
В некоторых вариантах осуществления KD измеряют с использованием анализа BIACORE® SPR. В некоторых вариантах для анализа методом SPR (поверхностный плазмонный резонанс) можно использовать BIAcore® T200 или эквивалентное устройство. В некоторых вариантах осуществления сенсорные чипы СМ5 серии S BIAcore® (или эквивалентные сенсорные чипы) иммобилизуют моноклональным мышиным антителом против человеческого IgG (Fc), и впоследствии антитела против триптазы захватывают в проточной ячейке. Последовательные 3-кратные разведения His-меченого мономера бета-1-триптазы человека (SEQ ID NO: 128) вводят при скорости потока 30 мкл/мин. Каждый образец анализируют с 3-минутной ассоциацией и 10-минутной диссоциацией. Анализ проводится при 25°С.После каждой инъекции чип регенерируют с использованием 3 М MgCl2. Ответ связывания корректируют путем вычитания единиц ответа (RU) из проточной ячейки, захватывающей нерелевантный IgG с аналогичной плотностью. Для анализа кинетики используется модель Ленгмюра 1:1 с одновременной аппроксимацией значений kon и koff.
2. Фрагменты антител
В некоторых вариантах осуществления антитело, предложенное в данном документе, (например, антитело против триптазы, антитело против FcεR, антитело, истощающее IgE+ В-клетки, антитело, истощающее тучные клетки или базофилы, антитело против PAR2 или антитело против IgE) представляет собой фрагмент антитела. Фрагменты антител включают, без ограничений, Fab-, Fab'-, Fab'-SH-, F(ab')2-, Fv и scFv-фрагменты и другие фрагменты, описанные ниже. Для обзора некоторых фрагментов антител см. Hudson et al. Nat. Med. 9:129-134 (2003). Для обзора scFv-фрагментов см., например, Pluckthun, in The Pharmacology of Monoclonal Antibodies, vol. 113, Rosenburg and Moore eds., (Springer-Verlag, New York), pp. 269-315 (1994); см. также WO 93/16185; патенты США №№5571894 и 5587458. Обсуждение Fab- и F(ab')2-фрагментов, содержащих остатки эпитопа связывания рецептора реутилизации и имеющих увеличенное in vivo время полужизни, смотрите в патенте США №5869046.
Диатела представляют собой фрагменты антител с двумя антигенсвязывающими сайтами, которые могут быть двухвалентными или биспецифическими. См., например, ЕР 404097; WO 1993/01161; Hudson et al. Nat. Med. 9:129-134, 2003; и Hollinger et al. Proc. Natl. Acad. Sci. USA 90: 6444-6448, 1993. Триатела и тетратела также описаны в Hudson et al. Nat. Med. 9:129-134, 2003.
Однодоменные антитела представляют собой фрагменты антител, которые содержат весь или часть вариабельного домена тяжелой цепи, или весь или часть вариабельного домена легкой цепи антитела. В некоторых вариантах осуществления однодоменное антитело представляет собой человеческое однодоменное антитело (см., например, патент США №6248516 В1).
Фрагменты антител могут быть получены различными способами, включая, без ограничений, протеолитическое расщепление интактного антитела, а также получение при помощи рекомбинантных клеток-хозяев (например, Е. coli или фага), как описано в данном документе.
3. Химерные и гуманизированные антитела
В некоторых вариантах осуществления антитело, предложенное в данном документе, (например, антитело против триптазы, антитело против FcεR, антитело, истощающее IgE+ В-клетки, антитело, истощающее тучные клетки или базофилы, антитело против PAR2 или антитело против IgE) представляет собой химерное антитело. Некоторые химерные антитела описаны, например, в патенте США №4816567; и Morrison et al. Proc. Natl. Acad. Sci. USA, 81:6851-6855, 1984). В одном примере химерное антитело содержит нечеловеческую вариабельную область (например, вариабельную область, полученную от мыши, крысы, хомяка, кролика или отличного от человека примата, такого как обезьяна) и человеческую константную область. В дополнительном примере, химерное антитело представляет собой антитело с «переключенным классом», в котором класс или подкласс был изменен по сравнению с исходным антителом. Термин «химерные антитела» включает антигенсвязывающие фрагменты таких антител.
В определенных вариантах осуществления химерное антитело представляет собой гуманизированное антитело. Как правило, антитело нечеловеческого происхождения гуманизируют с целью снижения иммуногенности для человека, сохраняя при этом специфичность и аффинность исходного антитела нечеловеческого происхождения. Как правило, гуманизированное антитело содержит один или более вариабельных доменов, в которых HVR (или их части) получают из нечеловеческого антитела, a FR (или их части) получают из последовательностей человеческих антител. Гуманизированное антитело необязательно также будет содержать по меньшей мере часть человеческой константной области. В некоторых вариантах осуществления некоторые остатки FR в гуманизированном антителе замещены соответствующими остатками нечеловеческого антитела (например, антитела, из которого получены остатки HVR), например, для восстановления или улучшения специфичности или аффинности антитела.
Гуманизированные антитела и способы их получения рассмотрены, например, в Almagro et al. Front. Biosci. 13:1619-1633, 2008, и дополнительно описаны, например, в Riechmann et al. Nature 332:323-329, 1988; Queen et al. Proc. Natl. Acad. Sci. USA 86:10029-10033, 1989; патентах США №№. 5821337, 7527791, 6982321, и 7087409; Kashmiri et al. Methods 36:25-34, 2005 (где описано прививание определяющей специфичность области (SDR)); Padlan, Mol. Immunol. 28:489-498, 1991 (где описано «изменение поверхности»); Dall'Acqua et al. Methods 36:43-60, 2005 (где описана «перетасовка FR»); и Osbourn et al. Methods 36:61-68, 2005 и Klimka et al. Br. J. Cancer, 83:252-260, 2000 (где описан подход «направленного отбора» к перетасовке FR).
Человеческие каркасные области, которые можно использовать для гуманизации, включают, но не ограничиваются ими: каркасные области, выбранные с использованием метода «наилучшего соответствия» (см., например, Sims et al. J. Immunol. 151:2296, 1993); каркасные области, полученные из консенсусной последовательности антител человека конкретной подгруппы вариабельных областей легкой или тяжелой цепи (см., например, Carter et al. Proc. Natl. Acad. Sci. USA, 89:4285, 1992; и Presta et al. J. Immunol., 151:2623, 1993); зрелые каркасные области человека (соматически мутированные) или каркасные области зародышевой линии человека (см., например, Almagro et al. Front. Biosci. 13:1619-1633, 2008); и каркасные области, полученные в результате скрининга библиотек FR (см., например, Baca et al. J. Biol. Chem. 272:10678-10684, 1997 и Rosok et al. J. Biol. Chem. 271:22611-22618, 1996).
4. Человеческие антитела
В некоторых вариантах осуществления антитело, предложенное в данном документе, (например, антитело против триптазы, антитело против FcεR, антитело, истощающее IgE+ В-клетки, антитело, истощающее тучные клетки или базофилы, антитело против PAR2 или антитело против IgE) представляет собой человеческое антитело. Человеческие антитела могут быть получены с использованием различных способов, известных в данной области техники. Человеческие антитела описаны в общих чертах у van Dijk et al. Curr. Opin. Pharmacol. 5:368-74, 2001 и Lonberg, Curr. Opin. Immunol. 20:450-459, 2008.
Человеческие антитела можно получить путем введения иммуногена трансгенному животному, модифицированному с целью продукции интактных человеческих антител или интактных антител с человеческими вариабельными областями в ответ на антигенную стимуляцию. Такие животные, как правило, содержат все или часть локусов иммуноглобулина человека, которые замещают эндогенные локусы иммуноглобулина или которые находятся во внехромосомном пространстве или случайным образом интегрированы в хромосомы животного. Как правило, у таких трансгенных мышей инактивированы эндогенные локусы иммуноглобулинов. Обзор способов получения антител человека из трансгенных животных см. в Lonberg, Nat. Biotech. 23:1117-1125, 2005. Также см., например, патенты США №№6075181 и 6150584, описывающие технологию XENOMOUSE™; патент США №5770429, описывающий технологию HUMAB®; патент США №7041870, описывающий технологию К-М MOUSE®, и публикацию патентной заявки США № US 2007/0061900, описывающую технологию VELOCIMOUSE®. Человеческие вариабельные области из интактных антител, образованных такими животными, могут дополнительно модифицироваться, например, путем объединения с разными человеческими консервативными областями.
Человеческие антитела также можно получать при помощи способов на основе гибридом. Были описаны клеточные линии человеческой миеломы и мышино-человеческой гетеромиеломы для получения человеческих моноклональных антител. (См., например, Kozbor J. Immunol. 133:3001, 1984; Brodeur et al. Monoclonal Antibody Production Techniques and Applications, pp.51-63 (Marcel Dekker, Inc., New York, 1987); и Boerner et al. J. Immunol. 147: 86, 1991). Человеческие антитела, полученные с использованием технологии человеческой В-клеточной гибридомы, описаны в Li et al. Proc. Natl. Acad. Sci. USA, 103:3557-3562, 2006. Дополнительные способы включают способы, описанные, например, в патенте США №7189826 (где описано получение моноклональных антител IgM человека из гибридомных клеточных линий) и в статье Ni, Xiandai Mianyixue, 26(4):265-268, 2006 (где описаны гибридомы типа человек-человек). Технология с использованием человеческих гибридом (технология «Триома») также описана в Vollmers et al. Histology and Histopathology 20(3):927-937, 2005 и Vollmers et al. Methods and Findings in Experimental and Clinical Pharmacology 27(3):185-91, 2005.
Человеческие антитела также можно получать путем выделения последовательностей вариабельного домена клона Fv из библиотек фагового дисплея человеческого происхождения. Такие последовательности вариабельного домена можно затем объединять с требуемым константным доменом человека. Методики отбора человеческих антител из библиотек антител описаны ниже.
5. Антитела, полученные из библиотек
Антитела согласно изобретению могут быть выделены путем скрининга комбинаторных библиотек антител с необходимой активностью или свойствами. Например, в данной области техники известно множество способов получения библиотек фагового дисплея и скрининга таких библиотек в отношении антител, обладающих необходимыми связывающими характеристиками. Такие способы рассмотрены, например, в публикации Hoogenboom et al. in Methods in Molecular Biology 178:1-37 (O'Brien et al., ed., Human Press, Totowa, NJ, 2001) и дополнительно описаны, например, в статьях McCafferty et al. Nature 348:552-554, 1990; Clackson et al. Nature 352: 624-628, 1991; Marks et al. J. Mol. Biol. 222: 581-597, 1992; Marks et al. in Methods in Molecular Biology248:161-175 (Lo, ed., Human Press, Totowa, NJ, 2003); Sidhu et al. J. Mol. Biol. 338(2): 299-310, 2004; Lee et al. J. Mol. Biol. 340(5): 1073-1093, 2004; Fellouse, Proc. Natl. Acad. Sci. USA 101 (34):12467-12472, 2004; и Lee et al. J. Immunol. Methods 284(1-2): 119-132, 2004.
В некоторых методах фагового дисплея репертуары генов VH и VL отдельно клонируют при помощи полимеразной цепной реакции (ПЦР) и повторно комбинируют случайным образом в фаговых библиотеках, которые затем можно подвергнуть скринингу на антигенсвязывающий фаг, как описано в Winter et al. Ann. Rev. Immunol., 12: 433-455, 1994. Фаг, как правило, представляет фрагменты антител, как одноцепочечные фрагменты Fv (scFv), так и фрагменты Fab. Библиотеки из иммунизированных источников позволяют получить антитела с высокой аффинностью к иммуногену без необходимости конструирования гибридом. В качестве альтернативы, можно клонировать наивный репертуар (например, от человека) для получения единого источника антител к широкому спектру чужеродных антигенов и аутоантигенов без иммунизации, как описано в статье Griffiths et al. EMBO J. 12: 725-734, 1993. И наконец, наивные библиотеки также можно создавать синтетически, путем клонирования неперестроенных V-генных сегментов из стволовых клеток и применения ПЦР-праймеров, содержащих случайную последовательность, для кодирования гипервариабельных областей HVR3 и для осуществления перестройки in vitro, как описано в статье Hoogenboom et al. J. Mol. Biol., 227: 381-388, 1992. Патентные публикации, в которых описаны фаговые библиотеки антител человека, включают, например: патент США №5750373, и публикации патентов США №№2005/0079574, 2005/0119455, 2005/0266000, 2007/0117126, 2007/0160598, 2007/0237764, 2007/0292936, и 2009/0002360.
Антитела или фрагменты антител, выделенные из библиотек человеческих антител, считаются в данном документе человеческими антителами или фрагментами человеческих антител.
6. Мультиспецифические антитела В некоторых вариантах осуществления антитело, предложенное в данном документе, (например, антитело против триптазы, антитело против FcεR, антитело, истощающее IgE+ В-клетки, антитело, истощающее тучные клетки или базофилы, антитело против PAR2 или антитело против IgE) представляет собой мультиспецифическое антитело, например, биспецифичесское антитело. Мультиспецифические антитела представляют собой моноклональные антитела, которые имеют специфичности связывания в отношении по меньшей мере двух различных сайтов. Например, что касается антител против триптазы, в некоторых вариантах осуществления биспецифические антитела могут связываться с двумя различными эпитопами триптазы. В некоторых вариантах осуществления одна из специфичностей связывания относится ктриптазе, а другая относится к любому другому антигену (например, второй биологической молекуле). В некоторых вариантах осуществления биспецифические антитела могут связываться с двумя различными эпитопами триптазы. В других вариантах осуществления одна из специфичностей связывания относится ктриптазе (например, триптазе человека, например, бета-триптазе человека), а другая относится к любому другому антигену (например, второй биологической молекуле, например, ИЛ-13, ИЛ-4, ИЛ-5, ИЛ-17, ИЛ-33, IgE, прайм-сегменту М1, CRTH2 или TRPA). Соответственно, биспецифическое антитело может иметь специфичность связывания для триптазы и ИЛ-13; триптазы и IgE; триптазы и ИЛ-4; триптазы и ИЛ-5; триптазы и ИЛ-17 или триптазы и ИЛ-33. В частности, биспецифическое антитело может иметь специфичность связывания для триптазы и ИЛ-13 или триптазы и ИЛ-33. В других конкретных вариантах осуществления биспецифическое антитело может иметь специфичность связывания для триптазы и IgE. Биспецифические антитела могут быть получены в виде полноразмерных антител или фрагментов антител.
Методики для получения мультиспецифических антител включают, но не ограничиваются рекомбинантной коэкспрессией двух пар тяжелой цепи-легкой цепи иммуноглобулинов, имеющих разную специфичность (см. Milstein et al. Nature 305: 537, 1983; WO 93/08829; и Traunecker et al. EMBO J. 10: 3655,1991), и метод конструирования «выступ-во-впадину» (см., например, в патенте США №5731168). Мультиспецифические антитела также могут быть получены путем конструирования с использованием эффекта электростатического взаимодействия для получения молекул Fc-гетеродимерных антител (WO 2009/089004А1); путем перекрестного связывания двух или более антител или фрагментов (см., например, патент США №4676980, и Brennan et al. Science, 229: 81, 1985); с использованием лейциновых застежек для создания биспецифических антител (см., например, Kostelny et al. J. Immunol., 148(5):1547-1553, 1992); с использованием технологии «диател» для получения фрагментов биспецифических антител (см., например, Hollinger et al. Proc. Natl. Acad. Sci. USA 90:6444-6448, 1993); и с использованием одноцепочечных Fv (sFv) димеров (см., например, Gruberet al. J. Immunol. 152: 5368, 1994); и получение триспецифических антител, как описано, например, в Tutt et al. J. Immunol. 147: 60, 1991.
Сконструированные антитела стремя или более функциональными антигенсвязывающими сайтами, включая «антитела-осьминоги», также включены в данный документ (см., например, US 2006/0025576 А1).
В данном документе антитело или фрагмент также включает «Fab двойного действия» или «DAF», содержащий антигенсвязывающий сайт, который связывается с триптазой, а также другим, отличающимся антигеном (см., например, US 2008/0069820).
Выступы-во-впадины
Использование «выступов-во-впадины» в качестве способа получения полиспецифических антител описано, например, в патенте США №№5731168, WO2009/089004, US2009/0182127, US2011/0287009, Marvin and Zhu, Acta Pharmacol. Sin. (2005) 26(6):649-658, и Kontermann (2005) Acta Pharmacol. Sin. 26:1-9. Краткое неограничивающее обсуждение приводится ниже.
«Выпуклость» относится к по меньшей мере одной боковой цепи аминокислоты, которая выступает из поверхности взаимодействия первого полипептида и, следовательно, может располагаться в компенсаторной полости на соседней поверхности взаимодействия (т.е. поверхности взаимодействия второго полипептида), чтобы стабилизировать гетеромультимер, и тем самым способствуют образованию гетеромультимера, например, образованию гомомультимера. Выпуклость может присутствовать на исходной поверхности взаимодействия или может быть введена синтетически (например, путем изменения нуклеиновой кислоты, кодирующей поверхность взаимодействия). В некоторых вариантах осуществления нуклеиновую кислоту, кодирующую поверхность взаимодействия первого полипептида, изменяют для кодирования выпуклости. Для достижения этого нуклеиновую кислоту, кодирующую по меньшей мере один «исходный» аминокислотный остаток на поверхности взаимодействия первого полипептида, заменяют нуклеиновой кислотой, кодирующей по меньшей мере один «импортированный» аминокислотный остаток, который имеет больший объем боковой цепи, чем исходный аминокислотный остаток. Следует иметь в виду, что может быть несколько исходных и соответствующих импортированных остатков. Объемы боковых цепей различных аминокислотных остатков показаны, например, в таблице 1 патента США 2011/0287009 или в таблице 1 патента США №7642228.
В некоторых вариантах осуществления импортированные остатки для образования выпуклости представляют собой природные аминокислотные остатки, выбранные из аргинина (R), фенилаланина (F), тирозина (Y) и триптофана (W). В некоторых вариантах осуществления импортированный остаток представляет собой триптофан или тирозин. В некоторых вариантах исходный остаток для образования выпуклости имеет небольшой объем боковой цепи, например, аланин, аспарагин, аспарагиновая кислота, глицин, серии, треонин или валин. См., например, патент США №7642228.
«Полость» относится к по меньшей мере одной боковой цепи аминокислоты, которая углублена от поверхности взаимодействия второго полипептида и, следовательно, вмещает соответствующий выступ на соседней поверхности взаимодействия первого полипептида. Полость может присутствовать на исходной поверхности взаимодействия или может быть введена синтетически (например, путем изменения нуклеиновой кислоты, кодирующей поверхность взаимодействия). В некоторых вариантах осуществления нуклеиновую кислоту, кодирующую поверхность взаимодействия второго полипептида, изменяют для кодирования полости. Для достижения этого нуклеиновую кислоту, кодирующую по меньшей мере один «исходный» аминокислотный остаток на поверхности взаимодействия второго полипептида, заменяют ДНК, кодирующей по меньшей мере один «импортированный» аминокислотный остаток, который имеет меньший объем боковой цепи, чем исходный аминокислотный остаток. Следует иметь в виду, что может быть несколько исходных и соответствующих импортированных остатков. В некоторых вариантах осуществления импортированные остатки для образования полости представляют собой природные аминокислотные остатки, выбранные из аланина (А), серина (S), треонина (Т) и валина (V). В некоторых вариантах осуществления импортированный остаток представляет собой серии, аланин или треонин. В некоторых вариантах исходный остаток для образования полости имеет большой объем боковой цепи, например, тирозин, аргинин, фенилаланин или триптофан.
Выпуклость «позиционируется» в полости, что означает, что пространственное расположение выпуклости и полости на поверхности взаимодействия первого полипептида и второго полипептида, соответственно, и размеры выпуклости и полости таковы, что выпуклость может быть расположена в полости без значительного нарушения нормальной ассоциации первого и второго полипептидов на поверхности взаимодействия. Поскольку выпуклости, такие как Tyr, Phe и Trp, как правило, не проходят перпендикулярно от оси поверхности взаимодействия и имеют предпочтительные конформации, выравнивание выпуклости с соответствующей полостью может, в некоторых случаях, основываться на моделировании пары выпуклость/полость на основании трехмерной структуры, такой как структура, полученная с помощью рентгеновской кристаллографии или ядерного магнитного резонанса (ЯМР). Это может быть достигнуто с использованием широко распространенных в данной области техники методов.
В некоторых вариантах осуществления мутация по типу «выступ» и в константной области IgG1 представляет собой T366W. В некоторых вариантах осуществления мутация по типу «впадина» в константной области IgG1 содержит одну или более мутаций, выбранных из T366S, L368A и Y407V. В некоторых вариантах осуществления мутация по типу «впадина» в константной области IgG1 содержит T366S, L368A и Y407V.
В некоторых вариантах осуществления мутация по типу «выступ» и в константной области IgG4 представляет собой T366W.B некоторых вариантах осуществления мутация по типу «впадина» в константной области IgG4 содержит одну или более мутаций, выбранных из T366S, L368A и Y407V.B некоторых вариантах осуществления мутация по типу «впадина» в константной области IgG4 содержит T366S, L368A и Y407V.
7. Варианты антител
В определенных вариантах осуществления рассматриваются варианты аминокислотных последовательностей антител, предложенных в данном документе. Например, может быть желательно улучшить аффинность связывания и/или другие биологические свойства антитела, такие как ингибирующая активность. Варианты аминокислотных последовательностей антитела можно получить путем внесения соответствующих модификаций в нуклеотидную последовательность, кодирующую антитело, или путем пептидного синтеза. Такие модификации включают, например, делеции, и/или вставки, и/или замены остатков в аминокислотных последовательностях антитела. Для получения конечного конструкта можно выполнить любые комбинации делеций, вставок и замен, при условии, что конечный конструкт обладает требуемыми характеристиками, например, связыванием антигена.
а) Варианты замен, вставок и делеций
В некоторых вариантах осуществления предложены варианты антител, имеющих одну или более аминокислотных замен. Сайты, представляющие интерес для мутагенеза с заменами, включают HVR и FR. Консервативные замены показаны в Таблице 1 под заголовком «предпочтительные замены». Более существенные изменения представлены в Таблице 1 под заголовком «иллюстративные замены», и как дополнительно описано ниже со ссылкой на классы аминокислотных боковых цепей. Аминокислотные замены можно вносить в представляющее интерес антитело, и проводить скрининг полученных продуктов в отношении необходимой активности, например, сохранения/улучшения связывания антигена, снижения иммуногенности или улучшения АЗКЦ или КЗЦ.
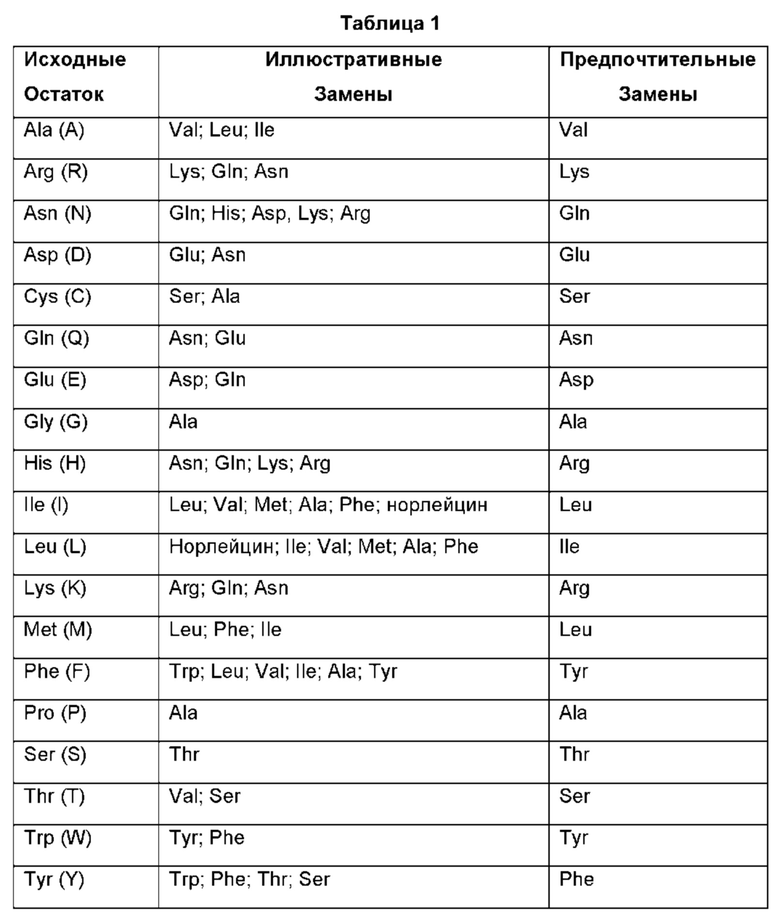

Аминокислоты можно поделить на группы в соответствии с общими свойствами боковых цепей:
(1) гидрофобные: Норлейцин, Met, Ala, Val, Leu, Ile;
(2) нейтральные гидрофильные: Cys, Ser, Thr, Asn, Gln;
(3) кислые: Asp, Glu;
(4) основные: His, Lys, Arg;
(5) остатки, которые влияют на ориентацию цепи: Gly, Pro;
(6) ароматические: Trp, Tyr, Phe.
Неконсервативные замены представляют собой замену члена одного из указанных классов членом другого класса.
Один тип заменяемого варианта включает замену одного или более остатков гипервариабельной области исходного антитела (например, гуманизированное или человеческое антитело). Как правило, полученный вариант(ы), выбранный для дальнейшего изучения, будет иметь модификации (например, улучшения) определенных биологических свойств (например, повышенную аффинность, пониженную иммуногенность) по сравнению с исходным антителом, и/или будет иметь по существу сохраненные определенные биологические свойства исходного антитела. Иллюстративным замещающим вариантом является антитело с созревшей аффинностью, которое традиционно можно получить, например, применяя методы созревания на основе фагового дисплея, такие как те, что описаны в данном документе. Вкратце один или более аминокислотных остатков HVR подвергают мутации и вариантные антитела экспонируют на поверхности фага и проводят скрининг в отношении конкретного вида биологической активности (например, аффинности связывания).
Изменения (например, замещения) могут быть сделаны в HVR, например, для улучшения аффинности антитела. Такие изменения могут быть произведены в «горячих точках» HVR, т.е. остатках, кодируемых кодонами, которые подвергаются мутации с высокой частотой во время процесса соматического созревания (см., например, Chowdhury, Methods Mol. Biol. 207:179-196, 2008), и/или остатках, которые приводят в контакт с антигеном, с тестированием полученного варианта VH или VL на аффинность связывания. Созревание аффинности путем конструирования и повторного отбора из вторичных библиотек было описано, например, в Hoogenboom et al. in Methods in Molecular Biology 178:1 -37 (O'Brien et al. ed., Human Press, Totowa, NJ, 2001). В некоторых вариантах осуществления аффинного созревания, многообразие вводится в вариабельные гены, выбранные для созревания любым из множества способов (например, ПЦР пониженной точности, перестановкой цепи или олигонуклеотид-направленным мутагенезом). Затем создают вторичную библиотеку. Затем проводят скрининг библиотеки для идентификации любых вариантов антител с требуемой аффинностью. Другой способ для внесения разнообразия включает подходы, направленные на HVR, в которых несколько аминокислотных остатков HVR (4-6 аминокислотных остатков подряд) являются рандомизированными. Остатки HVR, вовлеченные в связывание антигена, могут быть специфически идентифицированы, например, с использованием аланин-сканирующего мутагенеза или моделирования. Мишенями в частности являются HVR-H3 и HVR-L3.
В некоторых вариантах осуществления замены, вставки или делеции могут совершаться внутри одной или более HVR при условии, что такие изменения существенно не снижают способность антитела связывать антиген. Например, в HVR можно проводить консервативные замены (например, консервативные замены, предложенные в данном документе), которые существенно не снижают аффинность связывания. Такие изменения могут быть, например, за пределами остатков, контактирующих с антигеном, в HVR. В некоторых вариантах осуществления в вариантах последовательностей VH и VL, приведенных ранее, каждый HVR или не изменен, или содержит не более одной, двух или трех аминокислотных замен.
Удобный способ выявления остатков или областей антитела, которые могут быть мишенями для мутагенеза, называется «аланин-сканирующим мутагенезом», описанным в Cunningham et al. Science 244:1081-1085, 1989. В данном способе аминокислотный остаток или группу целевых аминокислотных остатков (например, заряженные аминокислотные остатки, такие как Arg, Asp, His, Lys и Glu) идентифицируют и заменяют нейтральной или отрицательно заряженной аминокислотой (например, Ala или полиаланином) для определения влияния на взаимодействие антитела с антигеном. Дополнительные замены могут быть внесены в те расположения аминокислот, которые проявляли функциональную чувствительность к исходным заменам. В альтернативном или дополнительном варианте используют кристаллическую структуру комплекса антиген-антитело для идентификации точек контакта между антителом и антигеном. Такие контактные остатки и расположенные рядом остатки можно использовать в качестве мишеней или удалять из кандидатов для замены. Варианты могут быть скринированы для определения присутствия в них желаемых свойств.
Вставки аминокислотной последовательности включают N- и/или С-концевые гибриды, имеющие длину в диапазоне от одного остатка до полипептидов, содержащих сто или более остатков, а также вставки внутри последовательности одного или более аминокислотных остатков. Примеры концевых вставок включают антитело с N-концевым остатком метионила. Другие инсерционные варианты молекулы антитела включают слияние N- или С-конца антитела с ферментом (например, для терапии ADEPT) или полипептидом, который увеличивает время полужизни в сыворотке крови.
b) Варианты гликозилирования
В определенных вариантах осуществления антитело, предложенное в данном документе, изменено с целью увеличения или уменьшения степени гликозилирования антитела. Добавление или удаление сайтов гликозилирования в антителе легко осуществить путем изменения аминокислотной последовательности, приводящего к созданию или удалению одного или более сайтов гликозилирования.
Если антитело содержит Fc-область, то можно изменять присоединенный к ней углевод. Нативные антитела, вырабатываемые клетками млекопитающих, как правило, содержат разветвленный, биантеннальный олигосахарид, который в общем случае присоединен посредством N-связи к Asn297 домена СН2 области Fc. См., например, Wright et al. TIBTECH 15:26-32, 1997. Олигосахарид может содержать различные углеводы, например, маннозу, N-ацетилглюкозамин (GlcNAc), галактозу и сиаловую кислоту, а также фукозу, присоединенную к GlcNAc в «стволе» биантеннальной олигосахаридной структуры. В некоторых вариантах осуществления можно выполнить модификации олигосахарида в антителе согласно изобретению с целью создания вариантов антител с определенными улучшенными свойствами.
В одном варианте осуществления предложены варианты антител, в которых углеводная структура, присоединенная (или непосредственно, или опосредованно) к области Fc, имеет сниженное содержание фукозы. Например, количество фукозы в таком антителе может составлять от 1% до 80%, от 1% до 65%, от 5% до 65% или от 20% до 40%. Количество фукозы определяют, рассчитывая среднее количество фукозы в сахарной цепи Asn297 относительно общего количества гликоструктур, присоединенных к Asn 297 (например, комплексных, гибридных или содержащих большое количество маннозы структур), согласно данным масс-спектрометрии MALDI-TOF, как описано, например, в WO 2008/077546. Asn297 относится к остатку аспарагина, расположенному в положении 297 в области Fc (согласно нумерации EU остатков области Fc); при этом Asn297 также может быть расположен на около±3 аминокислот выше или ниже положения 297, т.е. между положениями 294 и 300, вследствие незначительных вариаций последовательностей в антителах. Такие фукозилированные варианты могут обладать улучшенной функцией АЗКЦ. См., например, патентные публикации США №№. 2003/0157108 и 2004/0093621. Примеры публикаций, связанных с «дефукозилированными» или «фукозодефицитными» вариантами антитела включают: US 2003/0157108; WO 2000/61739; WO 2001/29246; US 2003/0115614; US 2002/0164328; US 2004/0093621; US 2004/0132140; US 2004/0110704; US 2004/0110282; US 2004/0109865; WO 2003/085119; WO 2003/084570; WO 2005/035586; WO 2005/035778; WO 2005/053742; WO 2002/031140; Okazaki et al. J. Mol. Biol. 336:1239-1249, 2004; Yamane-Ohnuki et al. Biotech. Bioeng. 87: 614, 2004. Примеры линий клеток, способных вырабатывать дефукозилированные антитела, включают клетки СНО 1_ес13 с дефицитом фукозилирования белка (Ripka et al. Arch. Biochem. Biophys. 249:533-545, 1986; US 2003/0157108; и WO 2004/056312 A1, особенно в Примере 11), и нокаутные линии клеток, такие как нокаутные клетки СНО по гену альфа-1,6-фукозилтрансферазы, FUT8, (см., например, Yamane-Ohnuki et al. Biotech. Bioeng. 87: 614, 2004; Kanda et al. Biotechnol. Bioeng. 94(4):680-688, 2006; и WO 2003/085107).
Кроме того, предлагаются варианты антител с олигосахаридами, разделенными пополам, например, в которых биантеннальный олигосахарид, присоединенный к Fc-области антитела, разделен пополам с помощью GlcNAc. Такие варианты антител могут обладать сниженным уровнем фукозилирования и/или улучшенной функцией АЗКЦ. Примеры таких вариантов антител описаны, например, в заявке WO 2003/011878; в патенте США №6602684; и US 2005/0123546. Также предлагаются варианты антител с по меньшей мере одним остатком галактозы в олигосахариде, присоединенном к Fc-области. Такие варианты антител могут обладать улучшенной функцией КЗЦ. Такие варианты антител описаны, например, в WO 1997/30087; WO 1998/58964; и WO 1999/22764.
с) Варианты Fc-области
В определенных вариантах осуществления в Fc-область антитела, предложенного в данном документе, могут быть введены одна или более аминокислотных модификаций, тем самым обеспечивая создание варианта Fc-области. Вариант Fc-области может содержать последовательность человеческой Fc-области (например, человеческой Fc-области IgG1, IgG2, IgG3 или IgG4), содержащую аминокислотную модификацию (например, замену) в одном или более аминокислотных положениях.
В определенных вариантах осуществления данное изобретение обеспечивает вариант антитела, который обладает некоторыми, но не всеми эффекторными функциями, что делает его подходящим кандидатом для практических применений, в которых важное значение имеет период полужизни антитела in vivo, хотя отдельные эффекторные функции (такие как комплемент и АЗКЦ) не являются необходимыми или являются вредными. Цитотоксические анализы могут быть проведены in vitro и/или in vivo для подтверждения восстановления/ослабления активности КЗЦ и/или АЗКЦ. Например, чтобы убедиться в отсутствии связывания антитела с FcγR (и, следовательно, отсутствии активности АЗКЦ) при сохранении способности связывания с FcRn, можно выполнить анализы связывания с Fc-рецептором (FcR). Первичные клетки для опосредования АЗКЦ экспрессируют только FcγRIII, тогда как моноциты экспрессируют FcγRI, FcγRII и FcγRIII. Экспрессия FcR на гемопоэтических клетках приведена в таблице 3 на странице 464 в Ravetch et al. Annu. Rev. Immunol. 9:457-492, 1991. Неограничивающие примеры анализов in vitro для оценки активности АЗКЦ представляющей интерес молекулы описаны в патенте США №5500362 (см., например, Hellstrom et al. Proc. Natl. Acad. Sci. USA 83:7059-7063, 1986 и Hellstrom et al. Proc. Natl. Acad. Sci. USA 82:1499-1502, 1985; патент США. №5821337 (см. Bruggemann et al. J. Exp. Med. 166:1351-1361, 1987). В альтернативном варианте могут быть использованы нерадиоактивные методы анализа (см., например, нерадиоактивный анализ цитотоксичности ACTI™ для проточной цитометрии (CellTechnology, Inc. Маунтин-Вью, Калифорния; и нерадиоактивный анализ цитотоксичности CytoTox 96® (Promega, Мадисон, Висконсин). Эффекторные клетки, пригодные для такого анализа, включают мононуклеарные клетки периферической крови (МКПК) и натуральные клетки-киллеры (NK). В альтернативном или дополнительном варианте активность АЗКЦ представляющей интерес молекулы можно оценить in vivo, например, на животной модели, как раскрыто в Clynes et al. Proc. Natl. Acad. Sci. USA 95:652-656, 1998. Также можно проводить анализ связывания C1q, чтобы подтвердить, что антитело неспособно связывать C1q и, следовательно, у него отсутствует активность КЗЦ. См., например, анализ связывания C1q и С3с методом ИФА в WO 2006/029879 и WO 2005/100402. Для оценки активации комплемента может быть проведен анализ КЗЦ (см., например, Gazzano-Santoro et al. J. Immunol. Methods 202:163, 1996; Cragg et al. Blood 101:1045-1052, 2003; и Cragg et al. Blood 103:2738-2743, 2004). Определение связывания с FcRn и in vivo клиренса/времени полужизни также может быть выполнено с использованием способов, известных в данной области техники (см., например, Petkova et al. Intl. Immunol. 18(12):1759-1769, 2006).
Антитела со сниженной эффекторной функцией включают те, которые содержат замены одного или более из остатков 238, 265, 269, 270, 297, 327 и 329 Fc-области (патенты США №6737056). Такие мутанты Fc включают мутантов Fc с заменами в двух или более аминокислотных положениях 265, 269, 270, 297 и 327, в том числе так называемые мутанты Fc «DANA» с заменой остатков 265 и 297 на аланин (патент США 7332581).
Описаны некоторые модификации антитела с улучшенным или уменьшенным связыванием с FcR. (См., например, патент США №6737056; WO 2004/056312; и Shields et al. J. Biol. Chem. 9(2): 6591-6604, 2001).
В некоторых вариантах осуществления вариант антитела содержит Fc-область с одной или более аминокислотными заменами, которые улучшают АЗКЦ, например, с заменами в положениях 298, 333 и/или 334 Fc-области (нумерация остатков по системе EU).
В некоторых вариантах осуществления изменения сделаны в Fc-области, что привело к изменению (то есть или к улучшению, или к ухудшению) связывания C1q и/или комплементзависимой цитотоксичности (КЗЦ), например, как описано в патенте США №6194551, WO 99/51642, и Idusogie et al. J. Immunol. 164: 4178-4184, 2000.
Антитела с увеличенным временем полужизни и улучшенным связыванием с неонатальным Fc-рецептором (FcRn), который отвечает за перенос материнских IgG к плоду (Guyer et al. J. Immunol. 117:587, 1976 and Kim et al. J. Immunol. 24:249, 1994), описаны в US2005/0014934.flaHHbie антитела содержат область Fc с одной или более заменами в ней, которые улучшают связывание области Fc с FcRn. Такие варианты Fc включают варианты с заменами одного или более остатков Fc-области: 238, 256, 265, 272, 286, 303, 305, 307, 311, 312, 317, 340, 356, 360, 362, 376, 378, 380, 382, 413, 424 или 434, например, замену аминокислотного остатка 434 в Fc-области (патент США №7371826).
Смотрите также Duncan et al. Nature 322:738-40, 1988; патентах США №№5648260 и 5624821; и WO 94/29351 в отношении других примеров вариантов Fc-области.
d) Варианты антител, сконструированные с цистеином
В некоторых вариантах осуществления может быть желательным создание антитела, сконструированные с цистеином, например, «ThioMAb», в которых один или более остатков антитела замещены остатками цистеина. В конкретных вариантах осуществления замещенные остатки расположены в доступных участках антитела. Таким образом, в результате замены таких остатков на цистеин, группы, реакционноспособные к тиолу, располагаются в доступных участках антитела и могут быть использованы для конъюгации антитела с другими фрагментами, такими как фрагменты лекарственного средства или фрагменты лекарственное средство-линкер, для создания иммуноконъюгата, как описано далее в данном документе. В некоторых вариантах осуществления цистеином можно заменить один или более из следующих остатков: V205 (нумерация по Кабату) в легкой цепи, А118 (нумерация EU) в тяжелой цепи и S400 (нумерация EU) в области Fc тяжелой цепи. Антитела, сконструированные с цистеином, могут быть получены, как описано, например, в патенте США №7521541.
e) Производные антитела
В определенных вариантах осуществления антитело, предложенное в данном документе, может быть дополнительно модифицировано для включения дополнительных небелковых компонентов, которые известны в данной области техники и общедоступны. Фрагменты, пригодные для получения производных антитела, включают, без ограничений, водорастворимые полимеры. Неограничивающие примеры водорастворимых полимеров включают, без ограничений, полиэтиленгликоль (ПЭГ), сополимеры этиленгликоля/пропиленгликоля, карбоксиметилцеллюлозу, декстран, поливиниловый спирт, поливинилпирролидон, поли-1,3-диоксолан, поли-1,3,6-триоксан, сополимер этилена/малеинового ангидрида, полиаминокислоты (либо гомополимеры, либо статистические сополимеры), декстран или поли(п-винилпирролидон) полиэтиленгликоль, гомополимеры пропропиленгликоля, сополимеры оксида/этиленоксида, полиоксиэтилированные полиолы (например, глицерин), поливиниловый спирт и их смеси. Пропиональдегид полиэтиленгликоля может иметь преимущество при производстве вследствие его стабильности в воде. Указанный полимер может обладать любой молекулярной массой и быть разветвленным или неразветвленным. Количество полимеров, присоединенных к антителу, может изменяться и, в случае присоединения более одного полимера, они могут представлять собой одинаковые или разные молекулы. В целом, количество и/или тип полимеров, используемых для дериватизации, можно определить с учетом факторов, включающих, без ограничений, конкретные свойства или функции антитела, подлежащие улучшению, независимо от того, будет ли производное антитела использоваться в терапии при определенных условиях и тому подобное.
В другом варианте осуществления изобретения предложены конъюгаты антитела и небелкового компонента, которые можно избирательно нагревать путем облучения. В одном варианте осуществления изобретения небелковый компонент представляет собой углеродную нанотрубку (Kam et al. Proc. Natl. Acad. Sci. USA 102: 11600-11605, 2005). Излучение может иметь любую длину волны и включает, без ограничений, длины волн, которые не наносят вред обычным клеткам, но которые нагревают небелковый компонент до температуры, при которой клетки, расположенные близко к антитело-небелковому компоненту, погибают.
В. Фармацевтические составы
Терапевтические составы, включающие терапевтические агенты, используемые в соответствии сданным изобретением, (например, любой из антагонистов триптазы (например, антитела против триптазы, включая любые антитела против триптазы, описанные в данном документе), антагонисты FcεR, антитела, истощающие IgE+ В-клетки, антитела, истощающие тучные клетки или базофилы, антагонисты PAR2, антагонисты IgE (например, антитела против IgE, например, омализумаб (XOLAIR®)) и их комбинации (например, антагонист триптазы (например, антитело против триптазы, включая любое из антител против триптазы, описанные в данном документе) и антагонист IgE (например, антитело против IgE, например, омализумаб (XOLAIR®))) и/или дополнительные терапевтические агенты, описанные в данном документе), получают для хранения путем смешивания терапевтического агента(ов), имеющую желаемую степень чистоты, с необязательными фармацевтически приемлемыми вспомогательными веществами, наполнителями или стабилизаторами в форме лиофилизированных составов или водных растворов. Для получения общей информации о составах см., например, Gilman et al. (eds.) The Pharmacological Bases of Therapeutics, 8th Ed., Pergamon Press, 1990; A. Gennaro (ed.), Remington's Pharmaceutical Sciences, 18th Edition, Mack Publishing Co., Pennsylvania, 1990; Avis et al. (eds.) Pharmaceutical Dosage Forms: Parenteral Medications Dekker, New York, 1993; Lieberman et al. (eds.) Pharmaceutical Dosage Forms: Tablets Dekker, New York, 1990; Lieberman et al. (eds.), Pharmaceutical Dosage Forms: Disperse Systems Dekker, New York, 1990; and Walters (ed.) Dermatological and Transdermal Formulations (Drugs and the Pharmaceutical Sciences), Vol.119, Marcel Dekker, 2002.
Приемлемые носители, вспомогательные вещества или стабилизаторы являются нетоксичными для реципиентов при используемых дозировках и концентрациях и включают буферы, такие как фосфат, цитрат и другие органические кислоты; антиоксиданты, включая аскорбиновую кислоту и метионин; консерванты (такие как хлорид октадецилдиметилбензиламмония; хлорид гексаметония; хлорид бензалкония, хлорид бензетония; фенол, бутиловый или бензиловый спирт; алкилпарабены, такие как метил или пропилпарабен; катехол; резорцинол; циклогексанол; 3-пентанол; и м-крезол); низкомолекулярные (менее чем около 10 остатков) полипептиды; белки, такие как сывороточный альбумин, желатин или иммуноглобулины; гидрофильные полимеры, такие как поливинилпирролидон; аминокислоты, такие как глицин, глутамин, аспарагин, гистидин, аргинин или лизин; моносахариды, дисахариды и другие углеводы, включая глюкозу, маннозу или декстрины; хелатообразующие агенты, такие как ЭДТК; сахара, такие как сахароза, маннит, трегалоза или сорбит; солеобразующие противоионы, такие как натрий; комплексы металлов (например, комплексы Zn-белок); и/или неионные поверхностно-активные вещества, такие как TWEEN™, PLURONICS™ или полиэтиленгликоль (ПЭГ).
Композиция в данном документе также может содержать более одного активного соединения, предпочтительно соединения с взаимодополняющими активностями, не оказывающими нежелательного действия друг на друга. Тип и эффективные количества таких лекарственных средств зависят, например, от количества и типа терапевтического агента(ов), присутствующего в составе, и от клинических параметров субъектов.
Активные ингредиенты также можно помещать в микрокапсулы, полученные, например, методом коацервации или межфазной полимеризации, например, в микрокапсулы из гидроксиметилцеллюлозы или желатина и микрокапсулы из поли(метилметакрилата), соответственно; в коллоидные системы для доставки лекарственных препаратов (например, в липосомы, микросферы альбумина, микроэмульсии, наночастицы и нанокапсулы) или в макроэмульсии. Такие методы раскрыты в Remington's Pharmaceutical Sciences 16th edition, Osol, A. Ed. (1980).
Можно изготовить препараты с замедленным высвобождением. Подходящие примеры препаратов с замедленным высвобождением включают полупроницаемые матрицы из твердых гидрофобных полимеров, содержащие антагонист, причем матрицы представлены в форме, например, пленок или микрокапсул. Примеры матриц с контролируемым высвобождением включают полиэфиры, гидрогели (например, поли(2-гидроксиэтилметакрилат) или поливиниловый спирт)), полилактиды (патент США №3773919), сополимеры L-глутаминовой кислоты и у этил-L-глютамата, неразлагаемый этиленвинилацетат, разлагаемые сополимеры молочной кислоты и гликолевой кислоты, такие как LUPRON DEPOT™ (инъецируемые микросферы, состоящие из сополимера молочной кислоты и гликолевой кислоты и ацетата лейпролида), и поли-D-(-)-3-гидроксимасляную кислоту.
Составы, используемые для введения in vivo, должны быть стерильными. Данное условие легко достижимо проведением фильтрации через мембраны для стерильной фильтрации.
ПРИМЕРЫ
Следующие примеры приведены для иллюстрации, но не для ограничения заявленного в настоящее время изобретения.
Пример 1: Материалы и методы
A) Количество активных аллелей триптазы
ПЦР с последующим секвенированием геномной ДНК по Сэнгеру использовали для определения количества активных аллелей триптазы, как описано ранее (Trivedi et al. J. Allergy Clin. Immunol. 124:1099-1105 e1-4, 2009). Вкратце, количество активных аллелей триптазы оценивали как количество оставшихся активных генов триптазы после подсчета дефицитных аллелей триптазы, то есть тех, которые определяют как α и βIIIFS. Генотипы автоматически определялись по соотношению интенсивности двух аллелей (А/В). Пациентам присваивали группу генотипа на основе этого соотношения. Генотипы подтверждались визуальным осмотром хроматограмм для 5% популяции без ошибок. Данные о пациентах, которые не были правильно распределены, проверялись визуально. Генотипирование по количеству активных аллелей триптазы было проведено на субъектах европейского происхождения с астмой, определенных методом главных компонент данных ОНП по всему геному, как описано ранее (Ramirez-Carrozzi et al. J. Allergy Clin. Immunol. 135:1080-1083 e3, 2015).
Для генотипирования α-триптазы, прямой праймер 5'-CTG GTG TGC AAG GTG ААТ GG-3 '(SEQ ID NO: 31) и обратный праймер 5'-AGG ТСС AG С ACT CAG GAG GA-3' (SEQ ID NO: 32) использовали для амплификации части локуса TPSAB1. Условия ПЦР были следующими: полимеразу Qiagen HOTSTARTAQ® Plus использовали в условиях амплификатора при 95°С в течение 5 минут, затем 35 циклов при 94°С в течение 60 секунд, 58°С в течение 60 секунд и 72 С в течение 2 минут. После проведения ПЦР для очистки использовали реагент для очистки продукта EXOSAP-IT™. Для секвенирования использовали одинаковые прямой и обратный праймеры. Секеенирование проводили с использованием терминатора BIG-DYE® на анализаторе ДНК ABI 3730XL, произведенном Applied Biosystems.
Для генотипирования βIIIFS-триптазы, прямой праймер 5'-GCA GGT GAG ССТ GAG AGT СС 3 '(SEQ ID NO: 33) и обратный праймер 5-GGG АСС ТТС АСС TGC ТТС AG-3' (SEQ ID NO: 34) использовали для амплификации части локуса TPSB2. Условия ПЦР были следующими: Полимеразу Qiagen HOTSTARTAQ® Plus использовали в условиях амплификатора при 95°С в течение 5 минут, затем 35 циклов при 94°С в течение 60 секунд, 60°С в течение 60 секунд и 72°С в течение 2 минут. После проведения ПЦР для очистки использовали реагент для очистки продукта EXOSAP-IT™. Для секвенирования использовали прямой праймер 5-GCA GGT GAG ССТ GAG AGT СС-3 '(SEQ ID NO: 33) и обратный праймер 5'-CAG CCA GTG АСС CAG CAC-3' (SEQ ID NO: 35). Секвенирование проводили с использованием терминатора BIG-DYE® на анализаторе ДНК ABI 3730XL, произведенном Applied Biosystems.
B) Клинические когорты
EXTRA (идентификатор ClinicalTrials.gov: NCT00314574) было рандомизированным, двойным слепым, плацебо-контролируемым исследованием Xolair (анти-IgE) у пациентов в возрасте от 12 до 75 лет с персистирующей умеренной или тяжелой астмой. Полная информация о дизайне исследования была опубликована ранее (Hanania et al. Ann. Intern. Med. 154:573-582, 2011; Hanania et al. Am. J. Respir. Crit. Care Med. 187:804-811, 2013; Choy et al. J. Allergy Clin. Immunol. 138:1230-1233 e8, 2016). Короче говоря, после 2-4-недельного вводного периода подходящие пациенты были рандомизированы в соотношении 1:1 для получения XOLAIR® (омализумаб) или плацебо (в дополнение к высоким дозам ингаляционных кортикостероидов (ICS) и агонистов бета-адренорецепторов (LABA) длительного действия, с или без дополнительных контролирующих лекарств) в течение 48 недель.
BOBCAT (Arron et al. Eur. Respir. J. 43:627-629, 2014; Choy et al. supra; Huang et al. J. Allergy Clin. Immunol. 136:874-884, 2015; Jia et al. J. Allergy Clin. Immunol. 130:647-654, 2012) было многоцентровым наблюдательным исследованием, проведенным в Соединенных Штатах, Канаде и Соединенном Королевстве для 67 взрослых пациентов с умеренной и тяжелой астмой. Необходимыми критериями включения были диагноз умеренной или тяжелой астмы (подтвержденный объемом форсированного выдоха за 1 секунду (FEV1) между 40% и 80% от прогнозируемого значения, а также доказательства в течение последних 5 лет >12% обратимости обструкции дыхательных путей с чувствительностью к бронходилататору короткого действия или метахолину (провокационная концентрация вызывает 20%-ное снижение FEV1 (РС20) <8 мг/мл), которая не контролируется (что определяется по меньшей мере 2 обострениями в предыдущем году или баллом > 1,50 согласно опроснику для оценки контроля симптомов астмы (ACQ) в версии из 5 пунктов (ACQ-5) при получении схемы введения (> 6 недель) стабильной высокой дозы ICS (>1000 мг флутиказона или эквивалент в сутки)) с или без LABA.
MILLY (идентификатор ClinicalTrials.gov: NCT00930163) было рандомизированным, двойным слепым, плацебо-контролируемым исследованием лебрикизумаба (антитела против ИЛ-13) у взрослых, у которых была астма, которая не контролировалась должным образом, несмотря на терапию ингаляционными глюкокортикоидами (Corren et al. N. Engl. J. Med. 365:1088-1098, 2011).
С) ИФА общей триптазы
Уровни триптазы в сыворотке или плазме измеряли с использованием сэндвич-варианта иммуноферментного анализа (ИФА) с 2 моноклональными антителами, способными обнаруживать мономеры и тетрамеры человеческих β1-, β2-, β3- и α1-триптаз. Вкратце, 384-луночные планшеты покрывали моноклональным антителом против триптазы в концентрации 1,0 мкг/мл в фосфатно-солевом буфере (PBS) в течение ночи при 4°С, а затем блокировали 90 мкл блокирующего буфера (1х PBS + 1% бычьего сывороточного альбумина (BSA)) в течение не менее 1 ч при комнатной температуре. Образцы сыворотки или плазмы разбавляли 1:100 в аналитическом буфере (1Х PBS рН 7,4, 0,35 М NaCl, 0,5% BSA, 0,05% TWEEN® 20 (полисорбат 20), 0,25% 3-[(3-холамидопропил)диметиламмонио]-1-пропансульфонат (CHAPS), 5 мМ этилендиаминтетрауксусной кислоты (EDTA) и 15 миллионных долей (м.д.) PROCLIN™ (антимикробный препарат широкого спектра действия)) и добавляли в трех повторностях в планшеты после промывки и инкубировали при перемешивании при комнатной температуре в течение 2 часов при комнатной температуре. Рекомбинантную β1-триптазу использовали для установления стандартного диапазона (7,8-500 пг/мл) в анализе. После промывки добавляли биотинилированное антитело против человеческой триптазы (0,5 мкг/мл) в разбавителе для анализа (1х PBS, рН 7,4, 0,5% BSA, 0,05% TWEEN® 20) и инкубировали в течение 1 часа при комнатной температуре. Цвет проявлялся после промывки стрептавидин-пероксидазой и субстратом тетраметилбензидином (ТМВ). Данные были интерпретированы на основе стандартной кривой с 4-параметрической моделью аппроксимации (4Р). Предел обнаружения этого анализа составлял приблизительно 7,8 пг/мл.
D) Статистические методы
Для построения графиков и анализа использовали программное обеспечение R (RCoreTeam, R: A Language an Environment for Statistical Computing, 2014).
Пример 2: Количество активных генов триптазы неоднородно при умеренной и тяжелой астме
Триптаза представляет собой гранулярный белок, который сильно экспрессируется в тучных клетках и является важным медиатором астмы, оказывающим заметное влияние на функцию легких. Гены, кодирующие ферментативно активную триптазу, TSPAB1 и TPSB2, являются полиморфными, и мы ранее описали частоты и характер наследования общих, инактивирующих мутаций с потерей функции (Trivedi et al. J. Allergy Clin. Immunol. 124:1099-1105 e1-4, 2009). Несмотря на появление современных полногемных анализов, включая ОНП-чипы высокой плотности и секвенирование нового поколения, локусы триптазы не были хорошо изучены, поскольку высокая гомология и повторяющаяся природа этой области не подходят для этих методологий, что таким образом требует прямого повторного секвенирования. Мы предположили, что количество активных аллелей триптазы, определяемое путем учета инактивирующих мутаций TSPAB1 и TPSB2, будет влиять на экспрессию триптазы, происходящей из тучных клеток, и прогнозировать клинический ответ на терапию, связанную с тучными клетками, например, XOLAIR® (омализумаб), антитело против IgE.
Мы оценили количество активных аллелей триптазы у пациентов европейского происхождения с умеренной и тяжелой астмой из исследований BOBCAT, EXTRA и MILLY (см. Пример 1). В соответствии с предыдущими докладами о популяциях Земли (Trivedi et al. J. Allergy Clin. Immunol. 124:1099-1105 e1-4, 2009), мутации с потерей функции были распространены у участников нашего исследования (Фиг. 1); 88,3% субъектов (408 из 462) имели по меньшей мере одну мутацию с потерей функции, что дало 1, 2 или 3 оставшиеся активные копии триптазы. Субъектов с нулевыми активными копиями в этих исследованиях не наблюдали, а те, у кого была одна активная копия, встречались относительно редко (<1%, 3 из 462). В нашей когорте преобладали субъекты, имеющие две или три активные копии триптазы (88%, 405 из 462); распространенность двух или трех активных копий была сопоставимой (43%, 199 или 462; и 45%, 206 из 462, соответственно).
Наблюдаемое распределение количества активных аллелей триптазы согласуется с данными о том, что специфические аллели TPSAB1 и TPSB2 находятся в неравновесном сцеплении, что приводит к тому, что дисфункциональные аллели триптазы совместно наследуются с функциональными аллелями (Trivedi et al. выше). Таким образом, субъекты с нулем или четырьмя активными аллелями триптазы, как ожидается, будут редки. Таким образом, количество активных аллелей триптазы неоднородно у пациентов с умеренной или тяжелой астмой.
Пример 3: Количество активных аллелей триптазы представляет собой меру белка, полученного от определенного гена, (pQTL) для астматических уровней триптазы периферической крови
Затем мы оценили взаимосвязь количества активных копий триптазы с общими уровнями триптазы периферической крови при умеренной или тяжелой астме из исследований BOBCAT (Фиг. 2А) и MILLY (Фиг. 2В). Значительный pQTL (Р <0,0001) наблюдали в каждом исследовании, дополнительно связывая, что количество активных аллелей триптазы является основной детерминантой экспрессии триптазы, и что субъекты с астмой с повышенным количеством активных аллелей триптазы связаны с повышенными уровнями экспрессии триптазы. Таким образом, эти данные демонстрируют, что уровень экспрессии триптазы периферической крови (например, в образцах крови) коррелирует с количеством активных аллелей триптазы у субъекта. На основании этой корреляции ожидается, что уровень экспрессии триптазы, например, в крови (например, в сыворотке или плазме) можно использовать для прогнозирования ответа на лечение, например, на терапию анти-IgE или другие терапевтические вмешательства.
Пример 4: Количество активных аллелей триптазы прогнозирует астматический ответ FEV1 на терапию анти-IgE
На основании данных о том, что количество активных аллелей триптазы коррелирует с экспрессией активной триптазы из первичных тучных клеток ex vivo и с уровнями общей триптазы в периферической крови у больных астмой (см. Пример 3), мы предположили, что количество активных аллелей триптазы будет предсказывать клинический ответ к терапии, связанной с тучными клетками, при астме. XOLAIR® (омализумаб) является одобренной терапией моноклональными антителами против IgE для уменьшения обострений при атопической астме. Поскольку блокирование IgE приводит к улучшению клинической астмы за счет снижения IgE/FcεRI-зависимой дегрануляции из тучных клеток, мы провели апостериорный анализ улучшения FEV1 по сравнению с исходным уровнем на основе количества активных аллелей триптазы. Поскольку два и три активных аллеля триптазы наблюдались преимущественно (88%) при астме, и поэтому субъекты с одним или четырьмя активными аллелями триптазы относительно редки, мы делили нашу исследуемую популяцию на части с 1 или 2 активными аллелями триптазы и 3 или 4 активными аллелями триптазы для улучшения статистической мощности.
Субъекты, имеющие один или два активных аллеля триптазы, получили значительное процентное улучшение FEV1 к 12 неделе лечения анти-IgE (Фиг. 3, среднее значение ± стандартная ошибка = 11,3 (3, 19,6)%, Р=0,009). Напротив, субъекты с тремя или четырьмя активными аллелями триптазы не получали эффекта относительно FEV1 от терапии анти-IgE (Фиг. 3). Эти наблюдения были устойчивыми в течение 48 недель исследования. Таким образом, у пациентов-астматиков с одним или двумя активными аллелями триптазы отмечалось значительное улучшение функции легких при лечении анти-IgE (XOLAIR®) по сравнению с субъектами, имеющими три или четыре копии.
Туч но клеточная триптаза, как было показано, непосредственно влияет на гладкую мускулатуру дыхательных путей, повышая сократительную способность и дифференцировку клеток in vitro, и, следовательно, является важным астматическим медиатором обструкции дыхательных путей. Эти данные предполагают, что терапия анти-IgE может быть наиболее эффективной у субъектов, которые экспрессируют низкие уровни тучноклеточной триптазы, которые могут высвобождаться как IgE/FcεRI-зависимой дегрануляцией, так и IgE/FcεRI-независимыми механизмами. Эти данные также указывают на то, что количество активных аллелей триптазы можно использовать в качестве прогностического биомаркера для прогнозирования ответа на терапевтические вмешательства при астме. Например, пациенты с низким количеством активных аллелей триптазы, вероятно, получат пользу от терапии XOLAIR® (омализумабом). В других примерах пациенты с высоким количеством активных аллелей триптазы могут получать пользу от терапии антагонистами триптазы (например, антителами против триптазы).
Пример 5: Количество активных аллелей триптазы не ассоциируется с биомаркерами 2-го типа при умеренной или тяжелой астме
Предыдущие исследования показали, что уровни экспрессии биомаркеров 2-го типа, обогащенные для лечения, приносят пользу, то есть снижают частоту обострений, при терапии XOLAIR® (омализумабом) при астме (Hanania et al. Am. J. Respir. Crit. Care Med. 187:804-811, 2013). Чтобы выяснить, как количество активных аллелей триптазы связано с биомаркерами воспаления 2-го типа, мы оценили уровни периостина в сыворотке, фракцию оксида азота в выдыхаемом воздухе (FeNO) и количество эозинофилов в крови по отношению к количеству активных аллелей триптазы у субъектов на исходном уровне из исследований BOBCAT, EXTRA и MILLY и не обнаружили никакой взаимосвязи (Фиг. 4А-4С). Эти данные указывают на то, что по количеству активных аллелей триптазы и биомаркерам 2-го типа независимо выделяют различные субпополяции астматиков. Независимость количества активных копий триптазы от уровней биомаркеров воспаления 2-го типа позволяет предположить, что оценка количества активных копий триптазы дает уникальную информацию относительно биологии триптазы и тучных клеток. Например, субъекты, у которых повышено количество активных аллелей триптазы и низкие уровни биомаркеров 2-го типа (например, астма с низким уровнем TH2), могут получить пользу от терапии, направленной на тучные клетки (например, терапии, включающей антагонист триптазы, антитело, истощающее IgE+ В-клетки, антитело, истощающее тучные клетки или базофилы, или антагонист активируемого протеазой рецептора 2 (PAR2)). Наоборот, субъекты с повышенным количеством активных аллелей триптазы и высокими уровнями биомаркеров 2-го типа (например, астмой с высоким уровнем TH2) могут получить пользу от лечения ингибитором пути TH2 и/или терапии, направленной на тучные клетки.
Другие варианты осуществления
Хотя вышеизложенное изобретение в целях однозначности понимания было описано с некоторыми подробностями в качестве иллюстрации и примеров, описание и примеры не следует воспринимать как ограничивающие объем изобретения. Содержание всех патентов и научной литературы, упоминаемых в данном документе, в явной форме и в полном объеме включено посредством ссылки.
| название | год | авторы | номер документа |
|---|---|---|---|
| АНТИТЕЛА ПРОТИВ ТРИПТАЗЫ, ИХ КОМПОЗИЦИИ И ПРИМЕНЕНИЯ | 2018 |
|
RU2771485C2 |
| КОМПОЗИЦИИ И СПОСОБЫ ДЛЯ ЛЕЧЕНИЯ И ДИАГНОСТИКИ АСТМЫ | 2009 |
|
RU2607569C2 |
| СПОСОБЫ ДИАГНОСТИКИ И ЛЕЧЕНИЯ, СВЯЗАННЫЕ С ИНГИБИРОВАНИЕМ TH2 | 2011 |
|
RU2578468C2 |
| СПОСОБЫ ДИАГНОСТИКИ И ЛЕЧЕНИЯ, СВЯЗАННЫЕ С ИНГИБИРОВАНИЕМ ТН2 | 2011 |
|
RU2737245C2 |
| СПОСОБЫ ДИАГНОСТИКИ И ЛЕЧЕНИЯ, СВЯЗАННЫЕ С ИНГИБИРОВАНИЕМ TH2 | 2020 |
|
RU2832013C2 |
| АПОПТОТИЧЕСКИЕ АНТИТЕЛА ПРОТИВ IgE | 2008 |
|
RU2500686C2 |
| СПОСОБЫ ЛЕЧЕНИЯ ЭОЗИНОФИЛЬНОГО ЭЗОФАГИТА С ПОМОЩЬЮ ИНГИБИТОРА ИЛ-4Р | 2014 |
|
RU2679141C2 |
| СПОСОБЫ ЛЕЧЕНИЯ ИЛИ ПРЕДУПРЕЖДЕНИЯ АСТМЫ ПОСРЕДСТВОМ ВВЕДЕНИЯ АНТАГОНИСТА IL-4R | 2020 |
|
RU2832774C2 |
| ПРИМЕНЕНИЕ АНТАГОНИСТОВ IL-13 ДЛЯ ЛЕЧЕНИЯ АТОПИЧЕСКОГО ДЕРМАТИТА | 2017 |
|
RU2752785C2 |
| СПОСОБЫ ИЗБИРАТЕЛЬНОГО ЛЕЧЕНИЯ АСТМЫ С ИСПОЛЬЗОВАНИЕМ АНТАГОНИСТОВ IL-13 | 2015 |
|
RU2694980C2 |

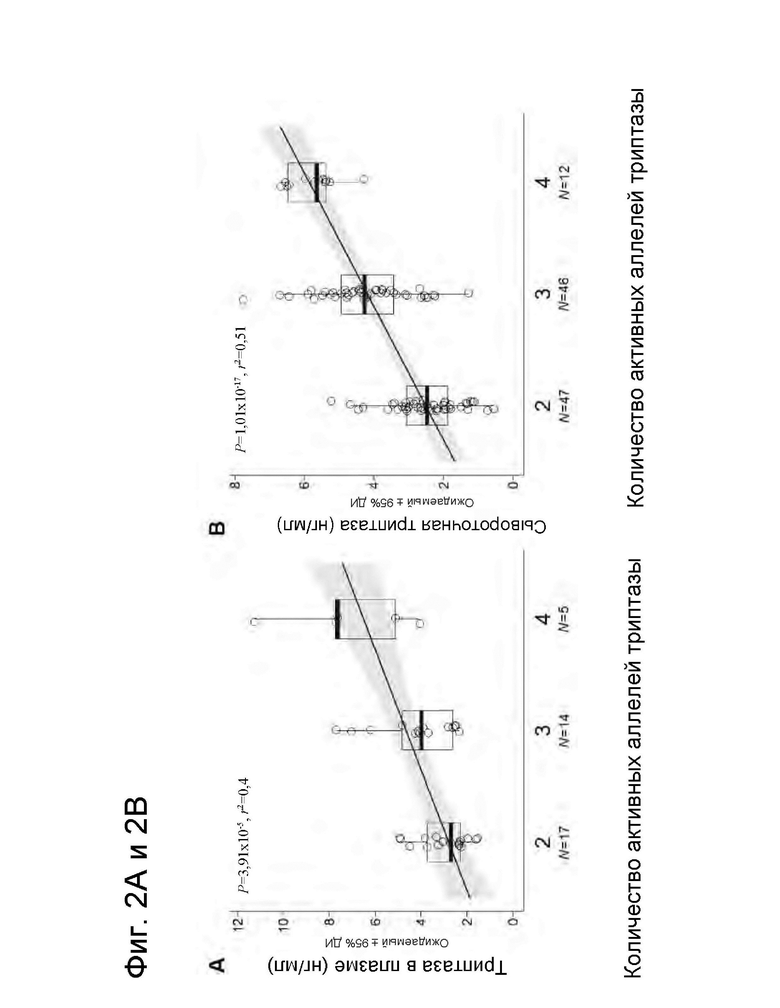
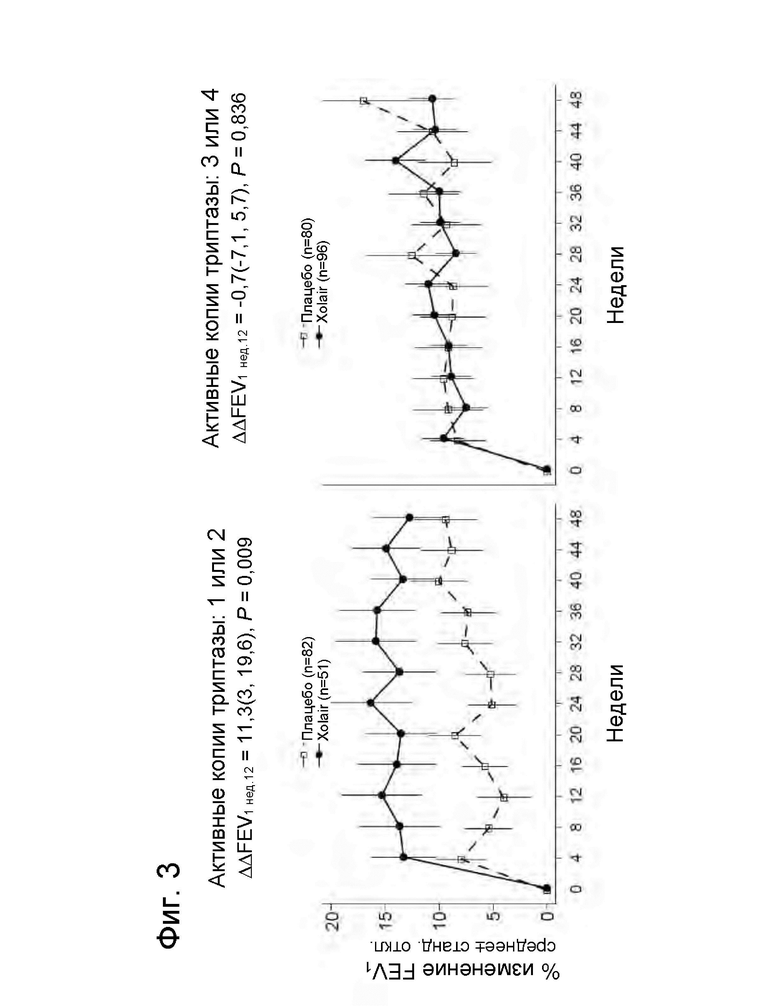
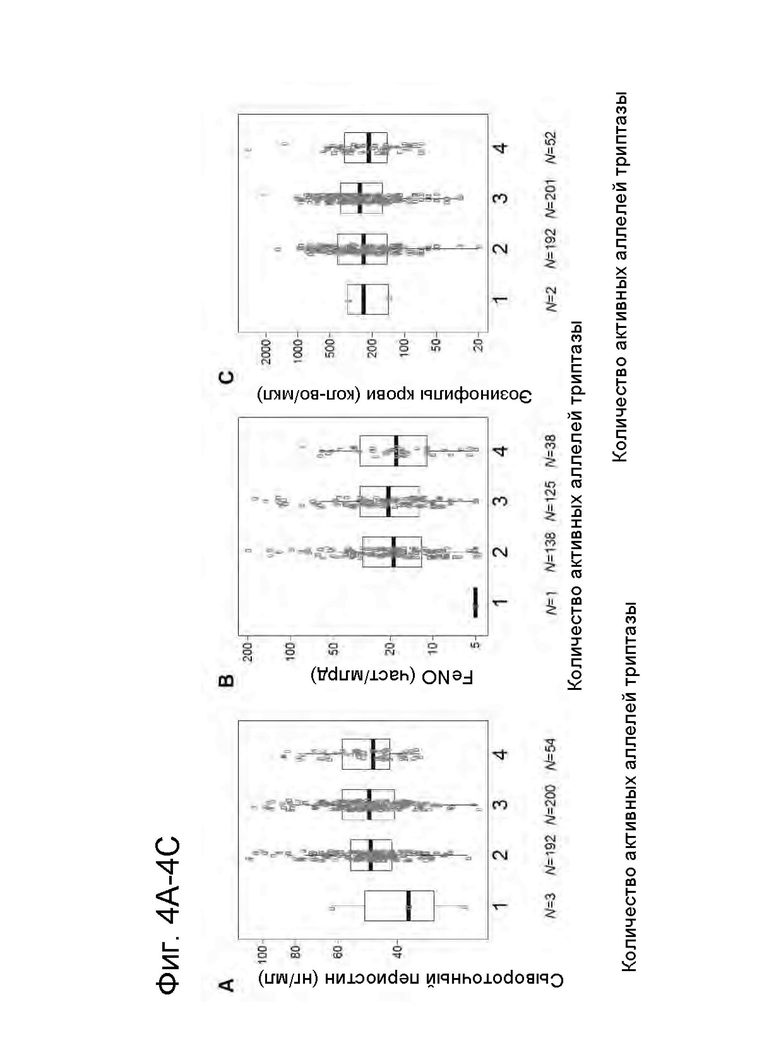
Группа изобретений относится к биотехнологии. Представлены: способ лечения пациентов с воспалительным заболеванием, опосредованным тучными клетками, способы определения того, могут ли пациенты с воспалительным заболеванием, опосредованным тучными клетками, отвечать на терапию, например терапию, включающую агент, выбранный из группы, состоящей из антагониста триптазы, антагониста Fc-эпсилона-рецептора (FcεR), антитела, истощающего IgE+ В-клетки, антитела, истощающего тучные клетки или базофилы, антагониста активируемого протеазой рецептора 2 (PAR2), антагониста IgE и их комбинации, способы выбора терапии для пациента с воспалительным заболеванием, опосредованным тучными клетками. Также указаны: способ мониторинга ответа пациента с воспалительным заболеванием, опосредованным тучными клетками, набор для идентификации пациента с воспалительным заболеванием, опосредованным тучными клетками, применение антагониста триптазы для изготовления лекарственного препарата для лечения пациента с воспалительным заболеванием и способы лечения пациента с астмой. Изобретение позволяет создать новые эффективные терапевтические и диагностические способы лечения воспалительных заболеваний, опосредованных тучными клетками. 10 н. и 133 з.п. ф-лы, 1 табл., 4 ил., 5 пр.
1. Способ лечения пациента с воспалительным заболеванием, опосредованным тучными клетками, который был идентифицирован как имеющий (i) генотип, содержащий количество активных аллелей триптазы равное 3 или 4; или (ii) уровень экспрессии триптазы в образце от пациента, который равен или превышает уровень триптазы, который соответствует количеству активных аллелей триптазы равному 3 или 4, причем способ включает применение у пациента с воспалительным заболеванием, опосредованным тучными клетками, терапии, включающей антагонист триптазы.
2. Способ определения того, может ли пациент с воспалительным заболеванием, опосредованным тучными клетками, отвечать на терапию, включающую антагонист триптазы, причем способ включает:
(а) определение в образце от пациента с воспалительным заболеванием, опосредованным тучными клетками, что количества активных аллелей триптазы у пациента равно 3 или 4; и затем
(b) идентификацию пациента, имеющего вероятность ответа на терапию, включающую антагонист триптазы, при этом количество активных аллелей триптазы равное 3 или 4 указывает на то, что пациент имеет повышенную вероятность ответа на терапию.
3. Способ определения того, может ли пациент с воспалительным заболеванием, опосредованным тучными клетками, отвечать на терапию, включающую антагонист триптазы, причем способ включает:
(а) определение уровня экспрессии триптазы в образце от пациента с воспалительным заболеванием, опосредованным тучными клетками; и
(b) идентификацию пациента, имеющего вероятность ответа на терапию, включающую антагонист триптазы, если уровень экспрессии триптазы в образце от пациента соответствует уровню экспрессии количества активных аллелей триптазы равному 3 или 4, причем уровень экспрессии триптазы в образце, равный или превышающий указанный уровень экспрессии триптазы, указывает на то, что пациент имеет повышенную вероятность ответа на терапию.
4. Способ по п. 2 или 3, дополнительно включающий применение данной терапии у пациента.
5. Способ по любому из пп. 1-4, в котором пациент был идентифицирован как имеющий уровень биомаркера 2-го типа в образце от пациента, который ниже эталонного уровня биомаркера 2-го типа, где эталонный уровень биомаркера 2-го типа представляет собой уровень биомаркера у индивидуумов, у которых отсутствует указанное воспалительное заболевание, опосредованное тучными клетками.
6. Способ по п. 5, в котором антагонист триптазы применяют у пациента в виде монотерапии.
7. Способ по любому из пп. 1-4, в котором пациент был идентифицирован как имеющий уровень биомаркера 2-го типа в образце от пациента, который равен или выше эталонного уровня биомаркера 2-го типа, где эталонный уровень биомаркера 2-го типа представляет собой уровень биомаркера у индивидуумов, у которых отсутствует указанное воспалительное заболевание, опосредованное тучными клетками.
8. Способ по п. 7, в котором способ дополнительно включает применение у пациента дополнительного ингибитора пути TH2.
9. Способ выбора терапии для пациента с воспалительным заболеванием, опосредованным тучными клетками, причем способ включает:
(а) определение в образце от пациента с воспалительным заболеванием, опосредованным тучными клетками, количества активных аллелей триптазы у пациента; и
(b) выбор для пациента терапии, включающей антагонист триптазы, если количество активных аллелей триптазы у пациента равно 3 или 4.
10. Способ выбора терапии для пациента с воспалительным заболеванием, опосредованным тучными клетками, причем способ включает:
(а) определение уровня экспрессии триптазы в образце от пациента с воспалительным заболеванием, опосредованным тучными клетками; и
(b) выбор для пациента терапии, включающей антагонист триптазы, если уровень экспрессии триптазы в образце от пациента соответствует уровню экспрессии триптазы количества активных аллелей триптазы равному 3 или 4.
11. Способ по п. 9 или 10, дополнительно включающий применение терапии, выбранной в соответствии с (b), у пациента.
12. Способ по любому из пп. 9-11, в котором пациент был идентифицирован как имеющий уровень биомаркера 2-го типа в образце от пациента, который ниже эталонного уровня биомаркера 2-го типа, где эталонный уровень биомаркера 2-го типа представляет собой уровень биомаркера у индивидуумов, у которых отсутствует указанное воспалительное заболевание, опосредованное тучными клетками.
13. Способ по п. 12, в котором антагонист триптазы применяют у пациента в виде монотерапии.
14. Способ по любому из пп. 9-11, в котором пациент был идентифицирован как имеющий уровень биомаркера 2-го типа в образце от пациента, который равен или выше эталонного уровня биомаркера 2-го типа, где эталонный уровень биомаркера 2-го типа представляет собой уровень биомаркера у индивидуумов, у которых отсутствует указанное воспалительное заболевание, опосредованное тучными клетками, и способ дополнительно включает выбор комбинированной терапии, включающей ингибитор пути TH2.
15. Способ по п. 14, в котором способ дополнительно включает применение у пациента ингибитора пути TH2.
16. Способ мониторинга ответа пациента с воспалительным заболеванием, опосредованным тучными клетками, которое лечится терапией, включающей антагонист триптазы, причем способ включает:
(а) определение уровня экспрессии триптазы в образце от пациента во время или после применения терапии, включающей антагонист триптазы; и
(b) сравнение уровня экспрессии триптазы в образце от пациента с эталонным уровнем триптазы, где эталонный уровень триптазы соответствует уровню экспрессии триптазы количества активных аллелей триптазы равному 3 или 4, таким образом, отслеживая ответ пациента, проходящего лечение терапией.
17. Способ по любому из пп. 1, 2, 4-9 и 11-15, в котором количество активных аллелей триптазы определяют путем секвенирования локусов TPSAB1 и TPSB2 генома пациента.
18. Способ по п. 17, в котором секвенирование представляет собой секвенирование по Сэнгеру или массовое параллельное секвенирование.
19. Способ по п. 17 или 18, в котором локус TPSAB1 секвенируют при помощи способа, включающего (i) амплификацию нуклеиновой кислоты от субъекта в присутствии первого прямого праймера, содержащего нуклеотидную последовательность SEQ ID NO: 31, и первого обратного праймера, содержащего нуклеотидную последовательность SEQ ID NO: 32, для получения ампликона TPSAB1 и (ii) секвенирование ампликона TPSAB1.
20. Способ по п. 19, в котором секвенирование ампликона TPSAB1 включает применение первого прямого праймера и первого обратного праймера.
21. Способ по любому из пп. 17-20, в котором локус TPSB2 секвенируют при помощи способа, включающего (i) амплификацию нуклеиновой кислоты от субъекта в присутствии второго прямого праймера, содержащего нуклеотидную последовательность SEQ ID NO: 33, и второго обратного праймера, содержащего нуклеотидную последовательность SEQ ID NO: 34, для получения ампликона TPSB2 и (ii) секвенирование ампликона TPSB2.
22. Способ по п. 21, в котором секвенирование ампликона TPSB2 включает применение второго прямого праймера и обратного праймера для секвенирования, содержащего нуклеотидную последовательность SEQ ID NO: 35.
23. Способ по любому из пп. 1, 2, 4-9, 11-15 и 17-22, в котором количество активных аллелей триптазы определяют по формуле: 4 - сумма количества аллелей α-триптазы и βIII-триптазы со сдвигом рамки (βIIIFS) в генотипе пациента.
24. Способ по п. 23, в котором альфа-триптазу определяют путем обнаружения ОНП c733 G> A в TPSAB1, содержащем нуклеотидную последовательность SEQ ID NO: 36, причем присутствие А в ОНП c733 G> A указывает на альфа-триптазу.
25. Способ по п. 23 или 24, в котором бета-IIIFS-триптазу определяют путем обнаружения мутации c980_981insC в TPSB2, содержащем нуклеотидную последовательность SEQ ID NO: 37.
26. Способ по любому из пп. 1, 3-8 и 10-16, в котором триптаза представляет собой бета-I-триптазу, бета-II-триптазу, бета-III-триптазу, альфа-I-триптазу или их комбинацию.
27. Способ по любому из пп. 1, 3-8, 10-16 и 26, в котором уровень экспрессии триптазы представляет собой уровень экспрессии белка.
28. Способ по п. 27, в котором уровень экспрессии белка триптазы представляет собой уровень экспрессии активной триптазы.
29. Способ по п. 27, в котором уровень экспрессии белка триптазы представляет собой уровень экспрессии общей триптазы.
30. Способ по любому из пп. 27-29, в котором уровень экспрессии белка измеряют с применением иммуноанализа, иммуноферментного анализа (ИФА), вестерн-блоттинга или масс-спектрометрии.
31. Способ по любому из пп. 1, 3-8, 10-16 и 26, в котором уровень экспрессии триптазы представляет собой уровень экспрессии мРНК.
32. Способ по п. 31, в котором уровень экспрессии мРНК измеряют с применением метода полимеразной цепной реакции (ПЦР) или микроматричного чипа.
33. Способ по п. 32, в котором метод ПЦР представляет собой кПЦР.
34. Способ по любому из пп. 1-33, в котором образец от пациента выбран из образца крови, образца ткани, образца мокроты, образца бронхиального лаважа, образца жидкости слизистой оболочки (MLF), бронхосорбционного образца и назосорбционного образца.
35. Способ по п. 34, в котором образец крови представляет собой образец цельной крови, образец сыворотки, образец плазмы или их комбинацию.
36. Способ по п. 35, в котором образец крови представляет собой образец сыворотки или образец плазмы.
37. Способ по любому из пп.1-36, в котором антагонист триптазы представляет собой антагонист альфа-триптазы или антагонист бета-триптазы.
38. Способ по п. 37, в котором антагонист триптазы представляет собой антагонист бета-триптазы.
39. Способ по п. 37 или 38, в котором антагонист бета-триптазы представляет собой антитело против бета-триптазы или его антигенсвязывающий фрагмент.
40. Способ по п. 39, в котором антитело содержит следующие шесть гипервариабельных областей (HVR):
(a) HVR-H1, содержащую аминокислотную последовательность SEQ ID NO: 1;
(b) HVR-H2, содержащую аминокислотную последовательность SEQ ID NO: 2;
(c) HVR-H3, содержащую аминокислотную последовательность SEQ ID NO: 3;
(d) HVR-L1, содержащую аминокислотную последовательность SEQ ID NO: 4;
(e) HVR-L2, содержащую аминокислотную последовательность SEQ ID NO: 5; и
(f) HVR-L3, содержащую аминокислотную последовательность SEQ ID NO: 6.
41. Способ по п. 39 или 40, в котором антитело содержит (а) вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, имеющую по меньшей мере 90%, по меньшей мере 95% или по меньшей мере 99% идентичность последовательности с аминокислотной последовательностью SEQ ID NO: 7; (b) вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, имеющую по меньшей мере 90%, по меньшей мере 95% или по меньшей мере 99% идентичность с аминокислотной последовательностью SEQ ID NO: 8; или (c) домен VH, как в (a), и домен VL, как в (b).
42. Способ по п. 41, в котором домен VH содержит аминокислотную последовательность SEQ ID NO: 7.
43. Способ по п. 41, в котором домен VL содержит аминокислотную последовательность SEQ ID NO: 8.
44. Способ по п. 41, в котором домен VH содержит аминокислотную последовательность SEQ ID NO: 7 и домен VL содержит аминокислотную последовательность SEQ ID NO: 8.
45. Способ по любому из пп. 39-42, в котором антитело содержит (а) тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 9, и (b) легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 10.
46. Способ по любому из пп. 39-44, в котором антитело содержит (а) тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 11, и (b) легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 10.
47. Способ по п. 39, в котором антитело содержит следующие шесть HVR:
(a) HVR-H1, содержащую аминокислотную последовательность SEQ ID NO: 12;
(b) HVR-H2, содержащую аминокислотную последовательность SEQ ID NO: 13;
(c) HVR-H3, содержащую аминокислотную последовательность SEQ ID NO: 14;
(d) HVR-L1, содержащую аминокислотную последовательность SEQ ID NO: 15;
(e) HVR-L2, содержащую аминокислотную последовательность SEQ ID NO: 16; и
(f) HVR-L3, содержащую аминокислотную последовательность SEQ ID NO: 17.
48. Способ по п. 39 или 47, в котором антитело содержит (а) домен VH, содержащий аминокислотную последовательность, имеющую по меньшей мере 90%, по меньшей мере 95% или по меньшей мере 99% идентичность последовательности с аминокислотной последовательностью SEQ ID NO: 18; (b) домен VL, содержащий аминокислотную последовательность, имеющую по меньшей мере 90%, по меньшей мере 95% или по меньшей мере 99% идентичность с аминокислотной последовательностью SEQ ID NO: 19; или (c) домен VH, как в (a), и домен VL, как в (b).
49. Способ по п. 48, в котором домен VH содержит аминокислотную последовательность SEQ ID NO: 18.
50. Способ по п. 48, в котором домен VL содержит аминокислотную последовательность SEQ ID NO: 19.
51. Способ по п. 48, в котором домен VH содержит аминокислотную последовательность SEQ ID NO: 18 и домен VL содержит аминокислотную последовательность SEQ ID NO: 19.
52. Способ по любому из пп. 39 или 47-51, в котором антитело содержит (а) тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 20, и (b) легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 21.
53. Способ по любому из пп. 39 или 47-51, в котором антитело содержит (а) тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 22, и (b) легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 21.
54. Способ по любому из пп. 1-53, в котором терапия дополнительно включает антагонист IgE.
55. Способ по п. 54, в котором антагонист IgE представляет собой антитело против IgE.
56. Способ по п. 55, в котором антитело против IgE представляет собой антитело, блокирующее IgE, и/или антитело, истощающее IgE.
57. Способ по п. 56, в котором антитело против IgE содержит следующие шесть HVR:
(a) HVR-H1, содержащую аминокислотную последовательность SEQ ID NO: 40;
(b) HVR-H2, содержащую аминокислотную последовательность SEQ ID NO: 41;
(c) HVR-H3, содержащую аминокислотную последовательность SEQ ID NO: 42;
(d) HVR-L1, содержащую аминокислотную последовательность SEQ ID NO: 43;
(e) HVR-L2, содержащую аминокислотную последовательность SEQ ID NO: 44; и
(f) HVR-L3, содержащую аминокислотную последовательность SEQ ID NO: 45.
58. Способ по п. 56 или 57, в котором антитело против IgE содержит (а) домен VH, содержащий аминокислотную последовательность, имеющую по меньшей мере 90%, по меньшей мере 95% или по меньшей мере 99% идентичность последовательности с аминокислотной последовательностью SEQ ID NO: 38; (b) домен VL, содержащий аминокислотную последовательность, имеющую по меньшей мере 90%, по меньшей мере 95% или по меньшей мере 99% идентичность с аминокислотной последовательностью SEQ ID NO: 39; или (c) домен VH, как в (a), и домен VL, как в (b).
59. Способ по п. 58, в котором домен VH содержит аминокислотную последовательность SEQ ID NO: 38.
60. Способ по п. 58, в котором домен VL содержит аминокислотную последовательность SEQ ID NO: 39.
61. Способ по п. 58, в котором домен VH содержит аминокислотную последовательность SEQ ID NO: 38 и домен VL содержит аминокислотную последовательность SEQ ID NO: 39.
62. Способ по любому из пп. 55-61, в котором антитело против IgE представляет собой омализумаб (XOLAIR®) или XmAb7195.
63. Способ по п. 62, в котором антитело против IgE представляет собой омализумаб (XOLAIR®).
64. Способ по любому из пп. 5-8, 12-15 и 17-63, в котором биомаркер 2-го типа представляет собой связанный с клеткой TH2 цитокин, периостин, количество эозинофилов, профиль эозинофилов, FeNO или IgE.
65. Способ по п. 64, в котором связанный с клеткой TH2 цитокин представляет собой ИЛ-13, ИЛ-4, ИЛ-9 или ИЛ-5.
66. Способ по любому из пп. 5-8, 12-15 и 17-65, в котором ингибитор пути TH2 ингибирует индуцируемую интерлейкином-2 Т-клеточную киназу (ITK), тирозинкиназу Брутона (BTK), Янус-киназу 1 (JAK1), GATA-связывающий белок 3 (GATA3), ИЛ-9, ИЛ-5, ИЛ-13, ИЛ-4, ИЛ-33, OX40L, TSLP, ИЛ-25, рецептор ИЛ-9, рецептор ИЛ-5, альфа рецептор ИЛ-4, альфа-1 рецептор ИЛ-13, альфа-2 рецептор ИЛ-13, OX40, TSLP-R, ИЛ-7R-альфа, ИЛ-17RB, ST2, CCR3, CCR4, CRTH2, Flap, Syk-киназу; CCR4, TLR9 или ГМ-КСФ.
67. Способ по любому из пп. 1, 4-8 и 11-66, дополнительно включающий применение у пациента дополнительного терапевтического агента.
68. Способ по п. 67, в котором дополнительный терапевтический агент выбран из антитела, истощающего IgE+ B-клетки, антитела, истощающего тучные клетки или базофилы, антагониста активируемого протеазой рецептора 2 (PAR2), кортикостероида, антагониста, связывающего ось ИЛ-33, антагониста TRPA1, бронходилататора или лекарственного препарата для контроля симптомов астмы, иммуномодулятора, ингибитора тирозинкиназы и ингибитора фосфодиэстеразы.
69. Способ по п. 68, в котором дополнительный терапевтический агент представляет собой кортикостероид.
70. Способ по п. 68 или 69, в котором кортикостероид представляет собой ингаляционный кортикостероид.
71. Способ по любому из пп. 1-70, в котором воспалительное заболевание, опосредованное тучными клетками, выбрано из астмы, атопического дерматита, хронической спонтанной крапивницы (CSU), системной анафилаксии, мастоцитоза, хронической обструктивной болезни легких (ХОБЛ), идиопатического фиброза легких (IPF) и эозинофильного эзофагита.
72. Способ по п. 71, в котором воспалительное заболевание, опосредованное тучными клетками, представляет собой астму.
73. Способ по п. 72, в котором астма представляет собой астму от умеренной до тяжелой.
74. Способ по любому из пп. 71-73, в котором астма не контролируется кортикостероидами.
75. Способ по любому из пп. 71-74, в котором астма представляет собой астму с высоким уровнем TH2 или астму с низким уровнем TH2.
76. Набор для идентификации пациента с воспалительным заболеванием, опосредованным тучными клетками, который имеет вероятность ответа на терапию, включающую антагонист триптазы, причем набор содержит:
(а) реагенты для определения количества активных аллелей триптазы у пациента или для определения уровня экспрессии триптазы в образце от пациента; и, необязательно,
(b) инструкции по применению реагентов для идентификации пациента с воспалительным заболеванием, опосредованным тучными клетками, который имеет вероятность ответа на терапию, включающую антагонист триптазы.
77. Набор по п. 76, в котором терапия дополнительно включает антагонист IgE.
78. Набор по п. 76 или 77, дополнительно содержащий реагенты для определения уровня биомаркера 2-го типа в образце от пациента.
79. Применение антагониста триптазы для изготовления лекарственного препарата для лечения пациента с воспалительным заболеванием, опосредованным тучными клетками, причем (i) было определено, что генотип пациента содержит количество активных аллелей триптазы, которое равно 3 или 4; или (ii) было определено, что образец от пациента имеет уровень экспрессии триптазы, который равен или выше эталонного уровня триптазы, где эталонный уровень триптазы соответствует уровню экспрессии триптазы количества активных аллелей триптазы равному 3 или 4.
80. Применение по п. 79, в котором было определено, что пациент имеет уровень биомаркера 2-го типа в образце от пациента, который ниже эталонного уровня биомаркера 2-го типа, где эталонный уровень биомаркера 2-го типа представляет собой уровень биомаркера у индивидуумов, у которых отсутствует указанное воспалительное заболевание, опосредованное тучными клетками, и лекарственный препарат предназначен для применения в виде монотерапии.
81. Применение по п. 79, в котором пациент был идентифицирован как имеющий уровень биомаркера 2-го типа в образце от пациента, который равен или выше эталонного уровня биомаркера 2-го типа, где эталонный уровень биомаркера 2-го типа представляет собой уровень биомаркера у индивидуумов, у которых отсутствует указанное воспалительное заболевание, опосредованное тучными клетками, и лекарственный препарат предназначен для применения в комбинации с ингибитором пути TH2.
82. Применение по любому из пп. 79-81, в котором количество активных аллелей триптазы определяют путем секвенирования локусов TPSAB1 и TPSB2 генома пациента.
83. Применение по п. 82, в котором секвенирование представляет собой секвенирование по Сэнгеру или массовое параллельное секвенирование.
84. Применение по п. 82 или 83, в котором локус TPSAB1 секвенируют при помощи способа, включающего (i) амплификацию нуклеиновой кислоты от субъекта в присутствии первого прямого праймера, содержащего нуклеотидную последовательность SEQ ID NO: 31, и первого обратного праймера, содержащего нуклеотидную последовательность SEQ ID NO: 32, для получения ампликона TPSAB1 и (ii) секвенирование ампликона TPSAB1.
85. Применение по п. 84, в котором секвенирование ампликона TPSAB1 включает применение первого прямого праймера и первого обратного праймера.
86. Применение по любому из пп. 82-85, в котором локус TPSB2 секвенируют при помощи способа, включающего (i) амплификацию нуклеиновой кислоты от субъекта в присутствии второго прямого праймера, содержащего нуклеотидную последовательность SEQ ID NO: 33, и второго обратного праймера, содержащего нуклеотидную последовательность SEQ ID NO: 34, для получения ампликона TPSB2 и (ii) секвенирование ампликона TPSB2.
87. Применение по п. 86, в котором секвенирование ампликона TPSB2 включает применение второго прямого праймера и обратного праймера для секвенирования, содержащего нуклеотидную последовательность SEQ ID NO: 35.
88. Применение по любому из пп. 79-87, в котором количество активных аллелей триптазы определяют по формуле: 4 - сумма количества аллелей α-триптазы и βIII-триптазы со сдвигом рамки (βIIIFS) в генотипе пациента.
89. Применение по п. 88, в котором альфа-триптазу определяют путем обнаружения ОНП c733 G> A в TPSAB1, содержащем нуклеотидную последовательность SEQ ID NO: 36, причем присутствие А в ОНП c733 G> A указывает на альфа-триптазу.
90. Применение по п. 88 или 89, в котором бета-IIIFS-триптазу определяют путем обнаружения мутации c980_981insC в TPSB2, содержащем нуклеотидную последовательность SEQ ID NO: 37.
91. Применение по любому из пп. 79-90, в котором триптаза представляет собой бета-I-триптазу, бета-II-триптазу, бета-III-триптазу, альфа-I-триптазу или их комбинацию.
92. Применение по любому из пп. 79-91, в котором уровень экспрессии триптазы представляет собой уровень экспрессии белка.
93. Применение по п. 92, в котором уровень экспрессии белка триптазы представляет собой уровень экспрессии активной триптазы.
94. Применение по п. 92, в котором уровень экспрессии белка триптазы представляет собой уровень экспрессии общей триптазы.
95. Применение по любому из пп. 92-94, в котором уровень экспрессии белка измеряют с применением иммуноанализа, ИФА, вестерн-блоттинга или масс-спектрометрии.
96. Применение по любому из пп. 79-91, в котором уровень экспрессии триптазы представляет собой уровень экспрессии мРНК.
97. Применение по п. 96, в котором уровень экспрессии мРНК измеряют с применением метода ПЦР или микроматричного чипа.
98. Применение по п. 97, в котором метод ПЦР представляет собой кПЦР.
99. Применение по любому из пп. 79-98, в котором образец от пациента выбран из образца крови, образца ткани, образца мокроты, образца бронхиального лаважа, образца жидкости слизистой оболочки (MLF), бронхосорбционного образца и назосорбционного образца.
100. Применение по п. 99, в котором образец крови представляет собой образец цельной крови, образец сыворотки, образец плазмы или их комбинацию.
101. Применение по п. 100, в котором образец крови представляет собой образец сыворотки или образец плазмы.
102. Применение по любому из пп. 79-101 , в котором антагонист триптазы представляет собой антагонист альфа-триптазы или антагонист бета-триптазы.
103. Применение по п. 102, в котором антагонист триптазы представляет собой антагонист бета-триптазы.
104. Применение по п. 102 или 103, в котором антагонист бета-триптазы представляет собой антитело против бета-триптазы или его антигенсвязывающий фрагмент.
105. Применение по п. 104, в котором антитело содержит следующие шесть гипервариабельных областей (HVR):
(a) HVR-H1, содержащую аминокислотную последовательность SEQ ID NO: 1;
(b) HVR-H2, содержащую аминокислотную последовательность SEQ ID NO: 2;
(c) HVR-H3, содержащую аминокислотную последовательность SEQ ID NO: 3;
(d) HVR-L1, содержащую аминокислотную последовательность SEQ ID NO: 4;
(e) HVR-L2, содержащую аминокислотную последовательность SEQ ID NO: 5; и
(f) HVR-L3, содержащую аминокислотную последовательность SEQ ID NO: 6.
106. Применение по п. 104 или 105, в котором антитело содержит (а) домен VH, содержащий аминокислотную последовательность, имеющую по меньшей мере 90%, по меньшей мере 95% или по меньшей мере 99% идентичность последовательности с аминокислотной последовательностью SEQ ID NO: 7; (b) домен VL, содержащий аминокислотную последовательность, имеющую по меньшей мере 90%, по меньшей мере 95% или по меньшей мере 99% идентичность с аминокислотной последовательностью SEQ ID NO: 8; или (c) домен VH, как в (a), и домен VL, как в (b).
107. Применение по п. 106, в котором домен VH содержит аминокислотную последовательность SEQ ID NO: 7.
108. Применение по п. 106, в котором домен VL содержит аминокислотную последовательность SEQ ID NO: 8.
109. Применение по п. 106, в котором домен VH содержит аминокислотную последовательность SEQ ID NO: 7 и домен VL содержит аминокислотную последовательность SEQ ID NO: 8.
110. Применение по любому из пп. 104-109, в котором антитело содержит (а) тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 9, и (b) легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 10.
111. Применение по любому из пп. 104-109, в котором антитело содержит (а) тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 11, и (b) легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 10.
112. Применение по п. 104, в котором антитело содержит следующие шесть HVR:
(a) HVR-H1, содержащую аминокислотную последовательность SEQ ID NO: 12;
(b) HVR-H2, содержащую аминокислотную последовательность SEQ ID NO: 13;
(c) HVR-H3, содержащую аминокислотную последовательность SEQ ID NO: 14;
(d) HVR-L1, содержащую аминокислотную последовательность SEQ ID NO: 15;
(e) HVR-L2, содержащую аминокислотную последовательность SEQ ID NO: 16; и
(f) HVR-L3, содержащую аминокислотную последовательность SEQ ID NO: 17.
113. Применение по п. 104 или 112, в котором антитело содержит (а) домен VH, содержащий аминокислотную последовательность, имеющую по меньшей мере 90%, по меньшей мере 95% или по меньшей мере 99% идентичность последовательности с аминокислотной последовательностью SEQ ID NO: 18; (b) домен VL, содержащий аминокислотную последовательность, имеющую по меньшей мере 90%, по меньшей мере 95% или по меньшей мере 99% идентичность с аминокислотной последовательностью SEQ ID NO: 19; или (c) домен VH, как в (a), и домен VL, как в (b).
114. Применение по п. 113, в котором домен VH содержит аминокислотную последовательность SEQ ID NO: 18.
115. Применение по п. 113, в котором домен VL содержит аминокислотную последовательность SEQ ID NO: 19.
116. Применение по п. 113, в котором домен VH содержит аминокислотную последовательность SEQ ID NO: 18 и домен VL содержит аминокислотную последовательность SEQ ID NO: 19.
117. Применение по любому из пп. 104 и 112-116, в котором антитело содержит (а) тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 20, и (b) легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 21.
118. Применение по любому из пп. 104 и 112-116, в котором антитело содержит (а) тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 22, и (b) легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 21.
119. Применение по любому из пп. 79-118, в котором антагонист триптазы следует применять в комбинации с антагонистом IgE.
120. Применение по п. 119, в котором антагонист IgE представляет собой антитело против IgE.
121. Применение по п. 120, в котором антитело против IgE представляет собой антитело, блокирующее IgE, и/или антитело, истощающее IgE.
122. Применение по п. 121, в котором антитело против IgE содержит следующие шесть HVR:
(a) HVR-H1, содержащую аминокислотную последовательность SEQ ID NO: 40;
(b) HVR-H2, содержащую аминокислотную последовательность SEQ ID NO: 41;
(c) HVR-H3, содержащую аминокислотную последовательность SEQ ID NO: 42;
(d) HVR-L1, содержащую аминокислотную последовательность SEQ ID NO: 43;
(e) HVR-L2, содержащую аминокислотную последовательность SEQ ID NO: 44; и
(f) HVR-L3, содержащую аминокислотную последовательность SEQ ID NO: 45.
123. Применение по п. 121 или 122, в котором антитело против IgE содержит (а) домен VH, содержащий аминокислотную последовательность, имеющую по меньшей мере 90%, по меньшей мере 95% или по меньшей мере 99% идентичность последовательности с аминокислотной последовательностью SEQ ID NO: 38; (b) домен VL, содержащий аминокислотную последовательность, имеющую по меньшей мере 90%, по меньшей мере 95% или по меньшей мере 99% идентичность с аминокислотной последовательностью SEQ ID NO: 39; или (c) домен VH, как в (a), и домен VL, как в (b).
124. Применение по п. 123, в котором домен VH содержит аминокислотную последовательность SEQ ID NO: 38.
125. Применение по п. 123, в котором домен VL содержит аминокислотную последовательность SEQ ID NO: 39.
126. Применение по п. 123, в котором домен VH содержит аминокислотную последовательность SEQ ID NO: 38 и домен VL содержит аминокислотную последовательность SEQ ID NO: 39.
127. Применение по любому из пп. 120-126, в котором антитело против IgE представляет собой омализумаб (XOLAIR®) или XmAb7195.
128. Применение по п. 127, в котором антитело против IgE представляет собой омализумаб (XOLAIR®).
129. Применение по любому из пп. 80-128, в котором биомаркер 2-го типа представляет собой связанный с клеткой TH2 цитокин, периостин, количество эозинофилов, профиль эозинофилов, FeNO или IgE.
130. Применение по п. 129, в котором связанный с клеткой TH2 цитокин представляет собой ИЛ-13, ИЛ-4, ИЛ-9 или ИЛ-5.
131. Применение по любому из пп. 81-130, в котором ингибитор пути TH2 ингибирует индуцируемую интерлейкином-2 Т-клеточную киназу (ITK), тирозинкиназу Брутона (BTK), Янус-киназу 1 (JAK1), GATA-связывающий белок 3 (GATA3), ИЛ-9, ИЛ-5, ИЛ-13, ИЛ-4, ИЛ-33, OX40L, TSLP, ИЛ-25, рецептор ИЛ-9, рецептор ИЛ-5, альфа рецептор ИЛ-4, альфа-1 рецептор ИЛ-13, альфа-2 рецептор ИЛ-13, OX40, TSLP-R, ИЛ-7R-альфа, ИЛ-17RB, ST2, CCR3, CCR4, CRTH2, Flap, Syk-киназу; CCR4, TLR9 или ГМ-КСФ.
132. Применение по любому из пп. 79-131, в котором лекарственный препарат составляют для применения с дополнительным терапевтическим агентом.
133. Применение по п. 132, в котором дополнительный терапевтический агент выбран из антитела, истощающего IgE+ B-клетки, антитела, истощающего тучные клетки или базофилы, антагониста активируемого протеазой рецептора 2 (PAR2), кортикостероида, антагониста, связывающего ось ИЛ-33, антагониста TRPA1, бронходилататора или лекарственного препарата для контроля симптомов астмы, иммуномодулятора, ингибитора тирозинкиназы и ингибитора фосфодиэстеразы.
134. Применение по п. 133, в котором дополнительный терапевтический агент представляет собой кортикостероид.
135. Применение по п. 133 или 134, в котором кортикостероид представляет собой ингаляционный кортикостероид.
136. Применение по любому из пп. 79-135, в котором воспалительное заболевание, опосредованное тучными клетками, представляет собой астму, атопический дерматит, хроническую спонтанную крапивницу (CSU), системную анафилаксию, мастоцитоз, ХОБЛ, идиопатический фиброз легких (IPF) и эозинофильный эзофагит.
137. Применение по п. 136, в котором воспалительное заболевание, опосредованное тучными клетками, представляет собой астму.
138. Применение по п. 137, в котором астма представляет собой астму от умеренной до тяжелой.
139. Применение по любому из пп. 136-138, в котором астма не контролируется кортикостероидами.
140. Применение по любому из пп. 136-139, в котором астма представляет собой астму с высоким уровнем TH2 или астму с низким уровнем TH2.
141. Способ лечения пациента с астмой, включающий определение того, что пациент имеет i) генотип, содержащий количество активных аллелей триптазы равное 3 или 4; или (ii) уровень экспрессии триптазы в образце от пациента, который равен или превышает уровень триптазы, который соответствует количеству активных аллелей триптазы равному 3 или 4, и введение антагониста триптазы указанному пациенту для лечения астмы.
142. Способ лечения пациента с астмой, включающий определение того, что пациент имеет либо (i) генотип, содержащий количество активных аллелей триптазы равное 1 или 2; или (ii) уровень экспрессии триптазы в образце от пациента, который равен или превышает уровень триптазы, который соответствует количеству активных аллелей триптазы равному 1 или 2, и применение анти-IgE терапии у указанного пациента для лечения астмы.
143. Способ по п. 142, где анти-IgE терапия представляет собой омализумаб (XOLAIR®).
| OH S.W | |||
| et al., Tryptase inhibition blocks airway inflammation in a mouse asthma model, J Immunol., 2002, Volume 168, Issue 4, pp | |||
| Пуговица для прикрепления ее к материи без пришивки | 1921 |
|
SU1992A1 |
| LIU X | |||
| et al., Induction of Mast Cell Accumulation by Tryptase via a Protease Activated Receptor-2 and ICAM-1 Dependent Mechanism, Mediators Inflamm., 2016, Volume 2016 | |||
| WO 2013020132 A1, 07.02.2013 | |||
| RU | |||
Авторы
Даты
2023-05-02—Публикация
2019-02-08—Подача