ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение относится к комплексам, содержащим нацеливающееся на PSMA соединение, связанное с радионуклидом, таким как 212Pb или 227Th. Эти соединения и содержащие их фармацевтические композиции можно использовать в областях применения, связанных с медициной. Такие области применения включают лечение рака предстательной железы, а комплексы позволяют осуществлять двойное нацеливание на разные формы рака. Нацеливающиеся на PSMA пептидные и пептидомиметические производные мочевины конъюгированы с хелаторами для образования комплекса с 212Pb и 227Th для применения в радиотерапии. Их можно применять при одиночном и двойном нацеливании.
УРОВЕНЬ ТЕХНИКИ
Рак предстательной железы является одной из наиболее частых причин связанной с раком смертности у мужчин. Существует большая потребность в новом и эффективном лечении, особенно при гормонорезистентном заболевании на поздней стадии. Скелетные метастазы являются частой проблемой на поздней стадии заболевания, и поэтому для пациентов, страдающих раком предстательной железы на поздней стадии со скелетными метастазами, в качестве специфического в отношении кости средства терапии был представлен излучатель альфа-частиц 223Ra (Ксофиго).
Хотя в качестве остеотропа 223Ra и демонстрирует значительную клиническую эффективность у пациентов, его активность ограничена метастазами в кости и не предусматривает целенаправленного воздействия на метастазы в мягких тканях.
Существует несколько молекул-носителей, обеспечивающих нацеливание радиолиганда на простат-специфический мембранный антиген (PSMA). Меченный лютецием-177 PSMA-617 (177Lu-PSMA-617) представляет собой соединение, находящееся на самой последней стадии клинической разработки для применения в радионуклидной терапии.
Данная молекула функционирует подходящим образом и обеспечивает соответствующие значения соотношения накопления в опухолевой и нормальной тканях для более долгоживущих (т. е. с периодом полураспада в несколько дней) радионуклидов, в том числе 177Lu и 225Ac, но при этом в ранние моменты времени (обычно через несколько часов после инъекции) характеризуется высоким накоплением в почках. В случае с более короткоживущими радионуклидами, такими как 212Pb (период полураспада 10,6 часа), первоначальное накопление в почках представляет собой проблему потенциальной токсичности.
Поэтому предпочтительно применять PSMA-лиганд с меньшим накоплением в почках, причем это не должно нарушать накопление в опухоли. Молекулы PSMA-лиганда состоят из (1) PSMA-связывающей области, (2) линкерной области и (3) хелатора, при этом линкерная область соединяет (1) и (3). Линкерную область также используют для регулирования размера молекулы
и полярности и т. д. в целях оказания влияния на свойства распределения in vivo. PSMA-связывающая область (мотив), используемая в PSMA-617, представляет собой структуру, которую можно обнаружить в нескольких молекулах данного класса, разработанных несколькими разными авторами изобретений и исследователями, в том числе в PSMA-11 и PSMA I&T, а также в меченных посредством 131I и 211At PSMA-связывающих лигандах.
Требуются новые соединения, которые содержат PSMA-область, поскольку в настоящее время все лиганды при тестировании обладают недостатками, в том числе относительно низкую радиобиологическую эффективность (RBE) и субоптимальное биораспределение.
Также существует потребность в улучшенном излучателе альфа-частиц, который может целенаправленно воздействовать как на метастазы в кости, так и на метастазы в мягких тканях.
Настоящее изобретение относится к соединениям, которые обеспечивают преодоление данных проблем.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Один аспект настоящего изобретения относится к комплексу по настоящему изобретению, где соединение X связано с радионуклидом, таким как 212Pb или 227Th, с помощью хелатирующего фрагмента Z.
В одном варианте осуществления настоящего изобретения радионуклидом является 212Pb.
В другом варианте осуществления настоящего изобретения радионуклидом является 227Th.
Хелатирующий фрагмент Z может быть выбран из группы, состоящей из ациклических хелаторов, циклических хелаторов, криптандов, краун-эфиров, порфиринов или циклических или нециклических полифосфонатов, DOTMP, EDTMP, бисфосфоната, DOTA, производного DOTA, памидроната, конъюгированного с DOTA, TCМC, производного TCMC, памидроната, конъюгированного с TCMC, DOTA, конъюгированной с антителом, TCMC, конъюгированного с антителом, HBED-CC, NOTA, NODAGA, TRAP, NOPO, PCTA, DFO, DTPA, CHX-DTPA, AAZTA, DEDPA и оксо-Do3A.
В одном варианте осуществления настоящего изобретения линкером является DOTA или производное DOTA.
В другом варианте осуществления настоящего изобретения линкером является TCMC или производное TCMC.
В случае 227Th особенно подходящими являются октадентатные гидроксипиридинон-содержащие лиганды, как например 3,2-HOPO.
Один аспект настоящего изобретения относится к радиофармацевтической композиции в соответствии с настоящим изобретением для применения в качестве лекарственного препарата.
Один аспект настоящего изобретения относится к радиофармацевтической композиции в соответствии с настоящим изобретением для применения в лечении заболевания мягких тканей и/или скелета.
В одном варианте осуществления настоящего изобретения заболевание скелета выбрано из группы, состоящей из скелетных метастазов при формах рака молочной железы, предстательной железы, почек, легкого, кости или множественной миеломе или не относящихся к раку заболеваний, вызывающих нежелательную кальцификацию, включая анкилозирующий спондилит.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
Описание фигур
На фигуре 1 показано биораспределение 212Pb через 2 часа после инъекции меченного 212Pb p-SCN-Bn-TCMC-PSMA-лиганда 1 и PSMA-617 соответственно в присутствии 224Ra.
На фигуре 2 показана выживаемость мышей с ксенотрансплантатом на основе PSMA-положительных C4-2 после обработки солевым раствором, 52 МБк 177Lu-OSMA-617 и 0,32 МБк 212Pb-p-SCN-Bn-TCMC-PSMA-лиганда 1.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Некоторые используемые аббревиатуры
Пептидный миметик, также называемый пептидомиметиком, представляет собой небольшую подобную белковой цепь, разработанную для имитации пептида. Как правило, они образуются либо в результате модификации существующего пептида, либо в результате разработки схожих систем, которые имитируют пептиды, таких как пептоиды и β-пептиды. Независимо от подхода, измененная химическая структура разработана для обеспечения преимущественного регулирования молекулярных свойств, таких как стабильность или биологическая активность. Это может иметь значение при разработке соединений, подобных лекарственным средствам, на основе существующих пептидов. Данные модификации включают вносимые в пептид изменения, которые не будут встречаться в природе (такие как измененные остовы и включение не встречающихся в природе аминокислот). Исходя из их сходства с пептидом-предшественником, пептидомиметики можно сгруппировать в четыре класса (A–D), где A характеризуется наибольшим сходством, а D характеризуется наименьшим сходством. Классы A и B включают пептидоподобные остовы, в то время как классы C и D включают малые молекулы.
PSMA — простат-специфический мембранный антиген. Синонимами PSMA являются простат-специфический раковый антиген, PSM, FGCP, FOLH, GCP2, mGCP, GCPII, NAALAD1, NAALA-даза, FOLH1, глутаматкарбоксипептидаза 2, глутаматкарбоксипептидаза II, мембранная глутаматкарбоксипептидаза, N-ацетилированная-альфа-связанная кислая дипептидаза I, петроилполи-гамма-глутаматкарбоксипептидаза, фолилполи-гамма-глутаматкарбоксипептидаза, фолатгидролаза 1, простат-специфический мембранный антиген, ингибирующий рост клеток белок 27.
DOTMP — 1,4,7,10-тетраазациклододекан-1,4,7,10-тетра(метиленфосфоновая кислота).
EDTMP — этилендиаминтетра(метиленфосфоновая кислота).
EDTA — этилендиаминтетрауксусная кислота.
p-SCN-Bn-DOTA — 2-(4-изотиоцианатобензил)-1,4,7,10-тетраазациклододекан-1,4,7,10-тетрауксусная кислота.
DOTA — 1,4,7,10-тетраазациклододекан-1,4,7,10-тетрауксусная кислота, а также используется для обозначения бензил-1,4,7,10-тетраазациклододекан-1,4,7,10-тетрауксусной кислоты (например, конъюгированной с моноклональным антителом).
p-SCN-Bn-TCMC — 2-(4-изотиоцианотобензил)-1,4,7,10-тетрааза-1,4,7,10-тетра-(2-карбамонилметил)циклододекан.
TCMC — 1,4,7,10-тетрааза-1,4,7,10-тетра-(2-карбамонилметил)циклододекан, а также используется для обозначения бензил-1,4,7,10-тетрааза-1,4,7,10-тетра-(2-карбамонилметил)циклододекана (например, конъюгированного с моноклональным антителом).
mAb — моноклональное антитело.
HOPO — Me-3,2-HOPO, октадентат-гидроксипиридинон для образования комплекса с 227Th, 4-((4-(3-(бис(2-(3-гидрокси-1-метил-2-оксо-1,2-дигидропиридин-4-карбоксамидо)этил)амино)-2-((бис(2-(3-гидрокси-1-метил-2-оксо-1,2-дигидропиридин-4-карбоксамидо)этил)амино)метил)пропил)фенил)амино)-4-оксобутановая кислота и производные.
Лиганд 1 — p-SCN-Bn-TCMC-PSMA-лиганд 1, p-SCN-Bn-TCMC-PSMA и т. д.
Лиганд 2 — p-SCN-Bn-DOTA-PSMA-лиганд 2, p-SCN-Bn-DOTA-PSMA и т. д.
Те же аббревиатуры в дальнейшем используются для кислот, солей или частично или полностью диссоциированных версий хелаторов.
Настоящее изобретение относится к растворам со свойствами одиночного или двойного нацеливания, основанным на низкомолекулярном производном мочевины в качестве средства, нацеливающегося на раковые клетки предстательной железы, предназначенного для переноса 212Pb.
Его можно применять с очищенным 212Pb или в обеспечивающем двойное нацеливание растворе, где 224Ra будет действовать в качестве средства лечения скелета, а 212Pb-производное мочевины будет действовать в качестве средства системной терапии против клеток, экспрессирующих PSMA-антиген, который связан главным образом с метастатическим раком предстательной железы на поздних стадиях и в некоторой степени также с другими типами рака.
В данной области известно, что основанные на мочевине соединения, конъюгированные с хелаторной группой, могут способствовать нацеливанию радионуклидов на клетки, экспрессирующие PSMA. К радионуклидам, которые были оценены в отношении радиотерапевтических целей с использованием нацеливания на PSMA, относятся 177Lu, 211At, 213Bi и 225Ac.
Настоящее изобретение относится к области меченных радионуклидом терапевтических средств. В соответствии с настоящим изобретением раскрыты меченные радионуклидом производные основанных на мочевине ингибиторов простат-специфического мембранного антигена (PSMA).
Таким образом, настоящее изобретение относиться к комплексу, содержащему соединение X, связанному с радионуклидом, таким как 212Pb или 227Th, где соединение X представляет собой пептидное или пептидомиметическое производное мочевины, подходящее для нацеливания на экспрессирующие PSMA клетки и ткани.
Линкер
Один аспект настоящего изобретения относится к комплексу по настоящему изобретению, где соединение X связано с радионуклидом, таким как 177Lu, 213Bi, 225Ac, 212Pb или 227Th, с помощью хелатирующего фрагмента Z.
В одном варианте осуществления настоящего изобретения радионуклидом является 212Pb.
В другом варианте осуществления настоящего изобретения радионуклидом является 227Th.
В другом варианте осуществления настоящего изобретения радионуклидом является 177Lu.
В дополнительном варианте осуществления настоящего изобретения радионуклидом является 213Bi или 212Bi.
В еще одном варианте осуществления настоящего изобретения радионуклидом является 225Ac.
Следует понимать, что комплексообразующее средство, или линкер, или хелатирующий фрагмент Z в соответствии с настоящим изобретением может также охватывать производные вышеупомянутых соединений (такие как производные EDTMP, DOTA, например p-SCN-Bn-DOTA, и TCMC, например p-SCN-Bn-TCMC). Конечно, следует понимать, что такие производные должны сохранять способность образовывать комплекс с 212Pb с более высокой константой устойчивости, чем с 224Ra.
Хелатирующий фрагмент Z может быть выбран из группы, состоящей из ациклических хелаторов, циклических хелаторов, криптандов, краун-эфиров, порфиринов или циклических или нециклических полифосфонатов, DOTMP, EDTMP и производных бисфосфоната, DOTA, производного DOTA, такого как p-SCN-Bn-DOTA, памидроната, конъюгированного с DOTA, TCМC, производного TCMC, такого как p-SCN-Bz-TCMC, памидроната, конъюгированного с TCMC, DOTA, конъюгированной с антителом, TCMC, конъюгированного с антителом, HBED-CC, NOTA, NODAGA, TRAP, NOPO, PCTA, DFO, DTPA, CHX-DTPA, AAZTA, DEDPA и оксо-Do3A.
В одном варианте осуществления настоящего изобретения линкером является DOTA или производное DOTA, такое как p-SCN-Bn-DOTA.
В другом варианте осуществления настоящего изобретения линкером является TCMC или производное TCMC, такое как p-SCN-Bn-TCMC.
Комплексообразующее средство может быть связано посредством углеродного остова, который обеспечивает возможность взаимодействия всех «связывающих плечей» молекулы хелатора с металлом. Альтернативно, в качестве линкера может быть использовано одно из плеч.
Подходящие хелаторы включают производные DOTA, такие как п-изотиоцианатобензил-1,4,7,10-тетраазациклододекан-1,4,7,10-тетрауксусная кислота (p-SCN-Bz-DOTA) и DOTA-NHS-сложный эфир.
Таким образом, в случае p-SCN-Bn-DOTA или p-SCN-Bn-TCMC комплексообразующее средство может быть связано с остальной частью соединения посредством углеродного остова (С-остова).
В одном варианте осуществления линкер представляет собой октадентатные гидроксипиридинон-содержащие лиганды, как например 3,2-HOPO. Такие лиганды, как правило, будут содержать по меньшей мере одну хелатирующую группу следующей структуры в виде замещенного пиридина (I):
-17-R, I,
где R представляет собой необязательную N-замещающую группу, и, таким образом, она может отсутствовать или может быть выбрана из углеводородных, ОН-, О-углеводородных, SH- и S-углеводородных групп, при этом любой или каждый углеводородный фрагмент независимо выбран из коротких гидрокарбильных групп, таких как С1-С8-углеводород, в том числе С1-С8-алкильная, -алкенильная или -алкинильная группы, или может представлять собой ОН- или О-углеводород. R также может предусматривать линкерный фрагмент, как указано ниже, и/или может содержать связующий фрагмент, как также указано ниже.
В формуле I каждая из групп R2 – R6 может быть независимо выбрана из Н, ОН, =О, короткого углеводорода (описанного в данном документе), линкерного фрагмента (описанного в данном документе) и/или связующего фрагмента (описанного в данном документе). Как правило, по меньшей мере одна из групп R – R6 будет представлять собой ОН. Как правило, по меньшей мере одна из групп R2 – R6 будет представлять собой =О.
Как правило, по меньшей мере одна из групп R – R6 будет представлять собой линкерный фрагмент. Предпочтительно ровно одна из групп R2 – R6 будет представлять собой =О. Предпочтительно ровно одна из групп R – R6 будет представлять собой ОН. Предпочтительно ровно одна из групп R – R6 будет представлять собой линкерный фрагмент (описанный в данном документе). Остальные группы R – R6 могут являться любыми из указанных в данном документе фрагментов, но предпочтительно представляют собой H. Если линкерный фрагмент или любые дополнительные линкерные, матричные или хелатирующие группы, присоединенные к линкерному фрагменту, не предусматривают связующий фрагмент, то одна из групп R – R6 предпочтительно представляет собой связующий фрагмент (описанный в данном документе).
В предпочтительном варианте осуществления одна из групп R – R6 будет представлять собой ОН, и одна из групп от R2 и далее будет представлять собой =О, а группы ОН и =О будут расположены на соседних атомах кольца.
Таким образом, в предпочтительном варианте осуществления ОН и =О могут располагаться при атомах 1,2; 2,3; 3,2; 3,4;
или 4,3 соответственно (как и следует ожидать,нумерация проводится от азота).
Особенно предпочтительными являются октадентатные лиганды, имеющие по меньшей мере один хелатирующий фрагмент, где группы OH и =О присутствуют в положениях 3 и 2 соответственно. Октадентатные лиганды могут иметь 2, 3 или 4 такие хелатирующие группы, причем особенно предпочтительными являются 2 или 4 такие группы.
В конкретном варианте осуществления нацеливающийся на PSMA комплекс на основе производного мочевины помечен 212Pb или 227Th, находясь при этом в смеси с остеотропным 224Ra или 223Ra соответственно, для обеспечения двойного нацеливания за счет (1) нацеливания на клеточный PSMA и (2) нацеливания на синтез кости, связанный со скелетными метастазами, с помощью катионов радия.
Комплексообразующие средства для 227Th, в том числе описанные в WO2011098611, US20170319721, Ramdahl et al. (Bioorganic & Medicinal Chemistry Letters
Volume 26, Issue 17, 1 September 2016, Pages 4318-4321) и Hagemann et al. (Mol Cancer Ther. 2016 Oct;15(10):2422-2431. Epub 2016 Aug 17), конъюгированы с производным мочевины для обеспечения нацеливания на PSMA. Упомянутые в данном документе комплексообразующие средства, таким образом, включены посредством ссылки.
Таким образом, один вариант осуществления настоящего изобретения относится к нацеливающемуся на PSMA производному мочевины, содержащему группу TCMC, как например p-SCN-Bn-TCMC, для хелатирования 212Pb.
Другой вариант осуществления настоящего изобретения относится к нацеливающемуся на PSMA производному мочевины, содержащему HOPO для хелатирования 227Th.
Дополнительный вариант осуществления настоящего изобретения относится к нацеливающемуся на PSMA производному мочевины, содержащему DOTA, как например p-SCN-Bn-TCMC, меченному либо 212Pb, либо 227Th.
В еще одном варианте осуществления комплексообразующее средство не образует комплекс с 224Ra или по сути не образует комплекс с 224Ra в фармацевтической композиции.
В еще одном дополнительном варианте осуществления комплексообразующее средство образует комплекс с 212Pb с более высокой константой устойчивости, чем с 224Ra.
В одном варианте осуществления константа устойчивости для 212Pb в по меньшей мере два раза превышает сродство к 224Ra, как например в по меньшей мере четыре раза выше, как например в по меньшей мере 8 раз выше или как например в по меньшей мере 10 раз выше.
В одном варианте осуществления указанное комплексообразующее средство выбрано из группы, состоящей из конъюгированной с лигандом DOTA, такой как конъюгированная с лигандом p-SCN-Bn-DOTA, или конъюгированного с лигандом TCMC, такого как конъюгированный с лигандом p-SCN-Bn-TCMC.
Лиганд может представлять собой антитело или полипептид.
В дополнительном варианте осуществления количество 224Ra и 212Pb находится в радиоактивном равновесии.
В еще одном дополнительном варианте осуществления отношение активности (в МБк) 212Pb к 224Ra составляет от 0,5 до 2, как например, 0,8–1,5, или, как например, 0,8–1,3, или предпочтительно, как например, 0,9–1,15.
В настоящем контексте термин «радиоактивное равновесие» относится к тому, что соотношение в МБк между двумя радионуклидами остается одинаковым или по сути одинаковым с течением времени. Термин «отношение активности», например 212Pb к 224Ra, относится к выраженному в МБк отношению 212Pb к 224Ra. На фигуре 5 представлена таблица (таблица 2), в которой показана динамика этого отношения активности с течением времени. Можно видеть, что через два дня устанавливалось радиоактивное равновесие, составляющее 1,1, для отношения активности 212Pb к 224Ra (7,3, деленное на 6,8). Таким образом, на фигуре 5 также можно видеть, что приблизительно через 2 дня достигалось радиоактивное равновесие между 212Pb и 224Ra.
В контексте настоящего изобретения термины «комплексообразующее средство», «акцептор», «линкер», «хелатирующий фрагмент Z» и «хелатирующее средство» используют взаимозаменяемо. Данные термины относятся к средствам, способным образовывать комплексы с 212Pb, предпочтительно путем хелатирования и со значительной прочностью, исходя из результатов измерения в тест-системах, при этом наличие такого комплекса не оказывает значительного влияния на радий, исходя из результатов измерения в тест-системах.
Тест-системы включают определение биораспределения in vivo, а также in vitro катионообменник или обеспечивающий удерживание в зависимости от размера и центробежное концентрирование картридж для выявления связывания радионуклида с комплексом хелат-антитело. Альтернативно, в качестве тест-системы можно применять тонкослойную хроматографию.
В настоящем контексте термин «акцептирование» (или комплексообразование) определяют как по меньшей мере 50% связывание в соответствии с результатами тонкослойной хроматографии (TLC), разделения центробежным концентрированием или в соответствии с профилями биораспределения.
Это означает, например, на по меньшей мере 50% меньшее накопление в крови 212Pb с низкомолекулярным хелатором. В случае конъюгированного с антителом хелатора, где накопление в крови не является надежным показателем, предусматривается по меньшей мере 50% связывание согласно результатам TLC-анализов.
В одном варианте осуществления настоящего изобретения предусмотрено по меньшей мере 60% связывание.
В другом варианте осуществления настоящего изобретения предусмотрено по меньшей мере 70% связывание.
В другом варианте осуществления настоящего изобретения предусмотрено по меньшей мере 80% связывание.
В другом варианте осуществления настоящего изобретения предусмотрено по меньшей мере 85% связывание.
В другом варианте осуществления настоящего изобретения предусмотрено по меньшей мере 90% связывание.
Соединение или соединения также могут обладать способностью образовывать комплекс с большим количеством радионуклидов, чем только с 212Pb.
В одном варианте осуществления настоящего изобретения соединение и/или комплекс представлены в концентрации от 1 нг/мл до 1 г/мл.
В другом варианте осуществления настоящего изобретения соединение и/или комплекс представлены в концентрации от 100 нг до 10 мг/мл.
Комплекс может содержать одно, два, три, четыре, пять или более соединений.
В одном варианте осуществления представлен раствор объемом от 100 мкл до 1000 мл, как например от 500 мкл до 100 мл, от 1 мл до 10 мл.
В одном варианте осуществления настоящего изобретения радиоактивность раствора составляет от 1 кБк до 1 ГБк, как например от 10 кБк до 100 МБк, как например от 100 кБк до 10 МБк.
В другом варианте осуществления настоящего изобретения радиоактивность раствора составляет от 100 кБк до 100 МБк.
В другом варианте осуществления настоящего изобретения комплексообразующее средство конъюгировано с соединением, выбранным из группы, состоящей из пептидов и пептидомиметических производных мочевины, имеющих сродство к PSMA.
В другом варианте осуществления настоящего изобретения комплексообразующее средство представляет собой хелатор TCMC, такой как p-SCN-Bn-TCMC, или DOTA, такую как p-SCN-Bn-DOTA, конъюгированное с соединением, выбранным из группы, состоящей из моноклонального антитела, поликлонального антитела, фрагмента антитела, синтетического белка, пептида, гормона или производного гормона или витамина или производного витамина.
Для целей введения дозы можно использовать чистый раствор 212Pb. Альтернативно, можно использовать 224Ra в смеси с 212Pb, применяя последний в целях обеспечения двойного нацеливания, т. е. 224Ra нацеливается на метастазы в кости, а 212Pb нацеливается на системный рак за счет своего носителя в виде производного мочевины. В случае введения растворов, содержащих 224Ra, они могут быть подвергнуты хранению в течение некоторого времени, например в течение 1 дня или более предпочтительно по меньшей мере двух дней, например 1–2 дней или 1–3 дней, для обеспечения достижения равновесия между 224Ra и 212Pb/212Bi. Это будет обеспечивать значения отношения активности 212Pb к 224Ra, составляющие от 0,83 до 1,14. Это может быть достигнуто, например, производителем путем простого выдерживания продукта в течение дня или около того перед транспортировкой.
Альтернативно, 212Pb можно добавлять в растворы 224Ra с получением определенного отношения радионуклидов. Например, если опухолевая нагрузка мягких тканей намного превышает опухолевую нагрузку скелета, можно использовать чистый препарат 212Pb или раствор с высоким отношением 212Pb к 224Ra.
Неперекрывающийся профиль побочных эффектов катионов радия и излучателей альфа-частиц, конъюгированных с PSMA-связывающими производными мочевины, делает смесь катиона 224Ra и 212Pb-PSMA-нацеливающего средства особенно привлекательной для двойного нацеливания. Это связано с тем, что для получения противоопухолевой активности можно применять более низкую величину дозы каждого соединения, поскольку, по меньшей мере в случае представленной скелетом составляющей, два разных соединения будут целенаправленно воздействовать на поражения независимо друг от друга.
Важно сохранять радий в основном в виде несвязанного или слабо связанного в комплекс катиона, поскольку это обеспечивает максимальное накопление в кости и в метастазах в кости, а также обеспечивает благоприятное выведение элиминируемого продукта, в основном происходящее через кишечник.
При добавлении комплексообразующего средства в раствор радия дочернему продукту можно придать тропность к кости или опухоли, а также повысить терапевтический потенциал раствора радия вместо его представляющего опасность для здоровья воздействия. Однако, именно комплексообразующее средство не должно оказывать негативного влияния на остеотропные свойства радия. Например, способность TCMC-меченного производного мочевины акцептировать 212Pb, образующийся в растворе радия во время транспортировки и хранения между местом изготовления и больницами, где собираются вводить данный продукт.
Хотя такую подверженность можно уменьшить путем добавления ингибиторов радиолиза, нацеливающиеся на опухоль пептиды и пептидомиметики зачастую более подвержены радиолизу, и их, вероятно, следует поставлять в формате набора, предусматривающего их добавление в отдаленный на промежуток от нескольких часов до нескольких минут момент времени до введения растворов 224Ra с относительно длительным сроком годности.
В данной области известно, что каликсарены и EDTA в некоторой степени могут образовывать комплекс с радием, а также образовывать комплекс со свинцом и висмутом. Однако в настоящей работе авторы настоящего изобретения обнаружили хелаторы, которые оставляют радий в основном несвязанным или слабо связанным в комплекс, что определяют по результатам измерения биораспределения in vivo, и при этом способны быстро и с соответствующей стабильностью образовывать комплекс с наиболее долгоживущим дочерним продуктом 212Pb. Избирательное комплексообразование можно использовать для получения по меньшей мере свинца, тропного к кости или опухоли, при сохранении благоприятных свойств радия в отношении лечения склеротических заболеваний, таких как скелетные метастазы. Комплекс с 212Pb, который нацелен на кость или опухолевые клетки, образует излучатель альфа-частиц 212Bi вследствие распада 212Pb. Таким образом, для облучения целевых клеток или ткани в качестве непрямого излучателя альфа-частиц применяют излучатель бета-частиц 212Pb. Другие потенциальные хелаты, которые могут быть пригодны для акцептирования образующегося из 224Ra дочернего нуклида, помимо TCMC и DOTA, включают без ограничения порфирины, производные DTPA и DTPA, а также связанную с карбоксилом DOTA.
Свинец-212 является наиболее долгоживущим из дочерних продуктов распада 224Ra, и он является наиболее важным для связывания в комплекс, так как он генерирует in vivo короткоживущий излучатель альфа-частиц 212Bi. Если 212Pb-хелат накапливается в кости или в опухолевых клетках, 212Bi также, вероятно, будет удерживаться в мишени. В растворе 224Ra в равновесии с дочерними продуктами распада атомов 212Pb будет более чем в 10 раз больше в сравнении с атомами 212Bi. Таким образом, количество излучения, генерируемого атомами 212Bi в этих растворах, является небольшим и, вероятно, не имеет токсикологического значения по сравнению с цепочкой распада 224Ra и 212Bi. Количество 212Bi сравнимо с количеством 211Pb, который косвенно производит альфа-частицу в цепочке 223Ra, и это не было существенной проблемой для регистрации и клинического применения 223Ra в равновесии с дочерними продуктами распада.
Тем не менее, если будет необходима высокая степень хелатирования также и 212Bi в инъекционном растворе, по меньшей мере в некоторых случаях может потребоваться добавление стабилизирующего средства, такого как NaI или HI, поскольку висмут имеет склонность в водных растворах находиться в состоянии, которое менее подходит для хелатирования.
По сравнению с одобренным на данный момент генерирующим альфа-частицы фармацевтическим средством для лечения скелетных метастазов, т. е. 223Ra, описанные в данном документе новые растворы могут обеспечить в одном из вариантов осуществления продукт с улучшенными свойствами для лечения скелетных метастазов, поскольку можно осуществлять нацеливание дочернего нуклида на циркулирующие в кровотоке раковые клетки и, до некоторой степени, также на метастазы в мягких тканях. Это может предупредить рецидив в результате обусловленной CTC реколонизации скелета раковыми клетками.
Другой аспект заключается в том, что более короткий период полураспада 224Ra по сравнению с 223Ra действительно может принести некоторую пользу по мере внедрения радия в костный матрикс. Вследствие высокой плотности минеральной составляющей кости длина пробега альфа-частиц сильно снижена в кости по сравнению с мягкими тканями. При применении генерирующего альфа-частицы фармацевтического средства с тропностью к объему может иметь значение процесс внедрения, особенно в областях с быстрой минерализацией, таких как костные раковые метастазы.
Следовательно, 224Ra может обеспечить улучшение противоопухолевой дозы, поскольку в среднем его внедренное количество на момент распада будет меньшим.
Заболевания, при которых можно применять новые растворы 212Pb с 224Ra или без него, включают без ограничения первичные и метастатические формы рака, аутоиммунные заболевания и атеросклероз. Данный препарат можно вводить внутривенно или местно, в том числе внутрибрюшинно или в условиях перфузии конечности.
Хелаторы, применяемые в новых растворах, могут быть ациклическими, а также циклическими хелаторами и криптандами, краун-эфирами, порфиринами или циклическими или нециклическими полифосфонатами, в том числе DOTMP и EDTMP. В качестве акцептора в растворе 224Ra также можно применять бисфосфонат, например, памидронат, конъюгированный с DOTA, TCMC или подобным.
Можно утверждать, что количество 212Pb в терапевтическом растворе 224Ra может быть от умеренного до незначительного (т. е. в состоянии равновесия приблизительно в 1,1 раза превышающее 224Ra). Если предполагается дозировка 224Ra, схожая с дозировкой, выполняемой для 223Ra у пациентов, но с поправкой на разницу в периоде полураспада, то вводимая доза будет составлять ориентировочно 150 кБк на кг массы тела.
В состоянии равновесия это может быть переведено в дозу конъюгата 212Pb-антитело, равную 11,5 МБк на 5 литров крови у пациента весом 70 кг (если 212Pb хелатирован количественно). Количество циркулирующих в кровотоке опухолевых клеток обычно составляет менее 10 клеток на мл, поэтому в 5 л крови в общей сложности содержится менее 50000 опухолевых клеток. Если лишь 1 из 100000 введенных молекул конъюгата 212Pb-антитело связывается с опухолевыми клетками, это будет означать по меньшей мере 0,0023 Бк на клетку, что эквивалентно примерно 127 связанным атомам 212Pb на клетку, что было бы в высшей степени разрушительным, поскольку ранее сообщалось, что в среднем 25 связанных с клеткой 212Pb на клетку приводило к уничтожению 90% клеточной популяции.
Соединения
Один аспект настоящего изобретения относится к соединению X, связанному с хелатирующим фрагментом Z, которое определено формулой I:
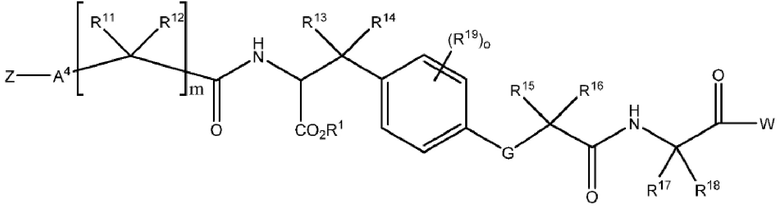
формула I,
или его фармацевтически приемлемой соли,
где
W представляет собой нацеливающийся на PSMA лиганд;
A4 представляет собой связь или двухвалентный связывающий фрагмент, содержащий 1–10 атомов углерода в цепи, кольце или их комбинации, где по меньшей мере один атом углерода необязательно заменен на О, -NR3- или -С(О)-;
G представляет собой C=O, C=S, C-NH2 или C-NR3;
R1 представляет собой водород или защитную группу для карбоксикислотной группы;
R3 выбран из группы, состоящей из водорода, алкила, циклоалкила, гетероциклоалкила, арила, алкиларила и гетероарила;
каждый из R11, R12, R13, R14, R15 и R16 независимо представляет водород, алкил, алкоксил, или
каждый из R17 и R18 независимо представляет водород, алкил, арил или алкиларил;
R19 выбран из группы, состоящей из алкила, алкоксила, галогенида, галогеналкила и
CN;
m представляет собой целое число от 1 до 6; и
o представляет собой целое число от 0 до 4, при этом если o больше 1, то каждый R19 является одинаковым или различается.
Один аспект настоящего изобретения относится к комплексу в соответствии с настоящим изобретением или его фармацевтически приемлемой соли, где
A4 представляет собой связь, (CH2)n, -HC(O)-, -(OCH2CH2)n-, -(HCH2CH2)n-, -H(CO)CH2-, -HC(О)CH2(OCH2CH2)n- или -HC(О)CH2(HCH2CH2)n-; и
L представляет собой связь, (CH2)n, -(OCH2CH2)n-, -(HCH2CH2)n- или -C(О)(CH2)n-;
при этом n независимо равняется 1, 2 или 3.
Один аспект настоящего изобретения относится к комплексу в соответствии с настоящим изобретением или его фармацевтически приемлемой соли, где A4 представляет собой связь, -(OCH2CH2)n- или -HC(О)CH2(OCH2CH2)n-; и
L представляет собой связь или -(OCH2CH2)n-;
при этом n независимо равняется 1 или 2.
Один аспект настоящего изобретения относится к комплексу в соответствии с настоящим изобретением или его фармацевтически приемлемой соли, где
W характеризуется структурой:

где каждый из R20 и R21 независимо представляет собой аминокислотный остаток, связанный посредством своей аминогруппы с соседней группой -C(O)-.
Один аспект настоящего изобретения относится к комплексу в соответствии с настоящим изобретением или его фармацевтически приемлемой соли, где
W характеризуется структурой:

где R представляет собой водород или защитную группу для карбоксикислотной группы.
Один аспект настоящего изобретения относится к комплексу в соответствии с настоящим изобретением или его фармацевтически приемлемой соли, характеризующимся структурой:
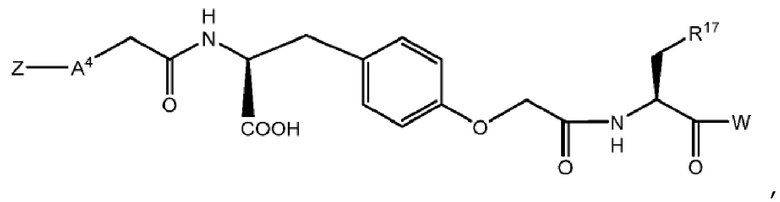
или его фармацевтически приемлемой соли,
где R17 представляет собой арил.
Один аспект настоящего изобретения относится к комплексу в соответствии с настоящим изобретением или его фармацевтически приемлемой соли, где комплекс представляет собой PSMA-617:
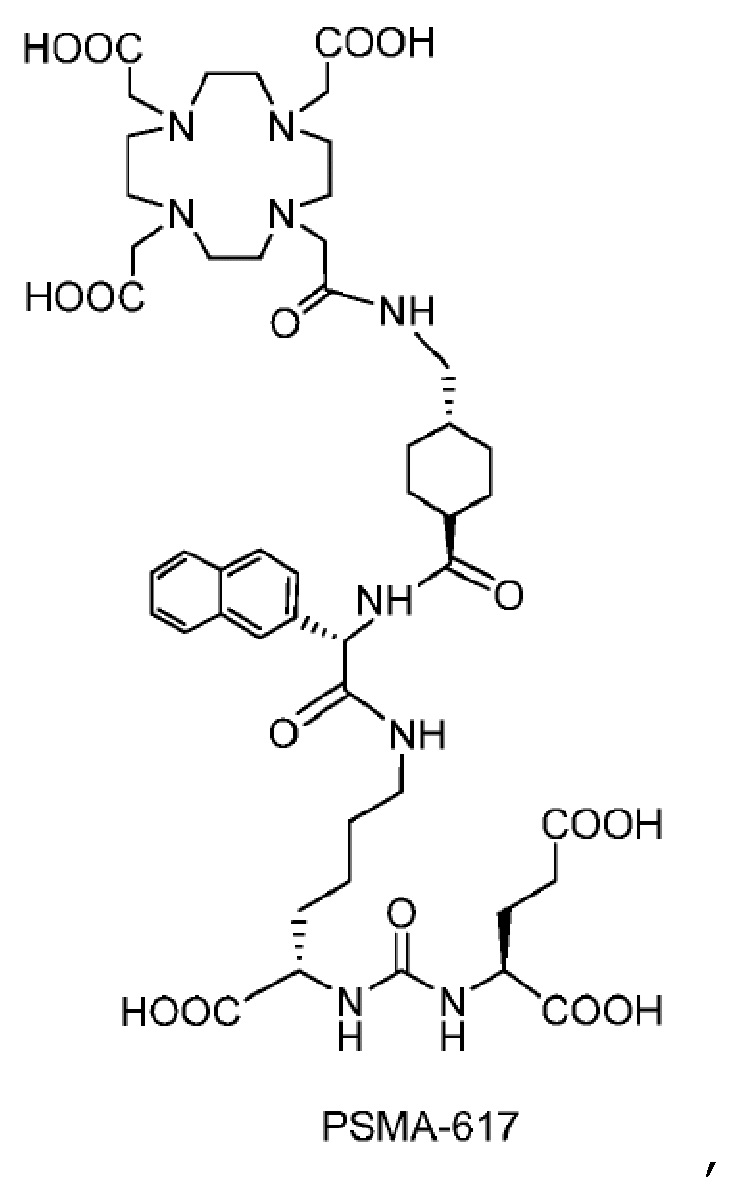
при этом радионуклид, такой как 212Pb, связан/хелатирован с четырьмя N.
Один аспект настоящего изобретения относится к комплексу в соответствии с настоящим изобретением, в котором DOTA-звено, такое как p-SCN-Bz-DOTA, заменено на TCMC-звено, такое как p-SCN-Bz-TCMC.
Линкер в PSMA-617 также может быть ковалентно связан с C-атомом в остове вместо связи с N, как можно видеть на приведенной выше фигуре.
Таким образом, производное мочевины может быть конъюгировано с DOTA или TCMC посредством связи с С-атомом остова или связи с N-атомом.
В случае конъюгации p-SCN-Bn-DOTA или p-SCN-Bn-TCMC посредством связи с С-остовом соединение представляет собой:
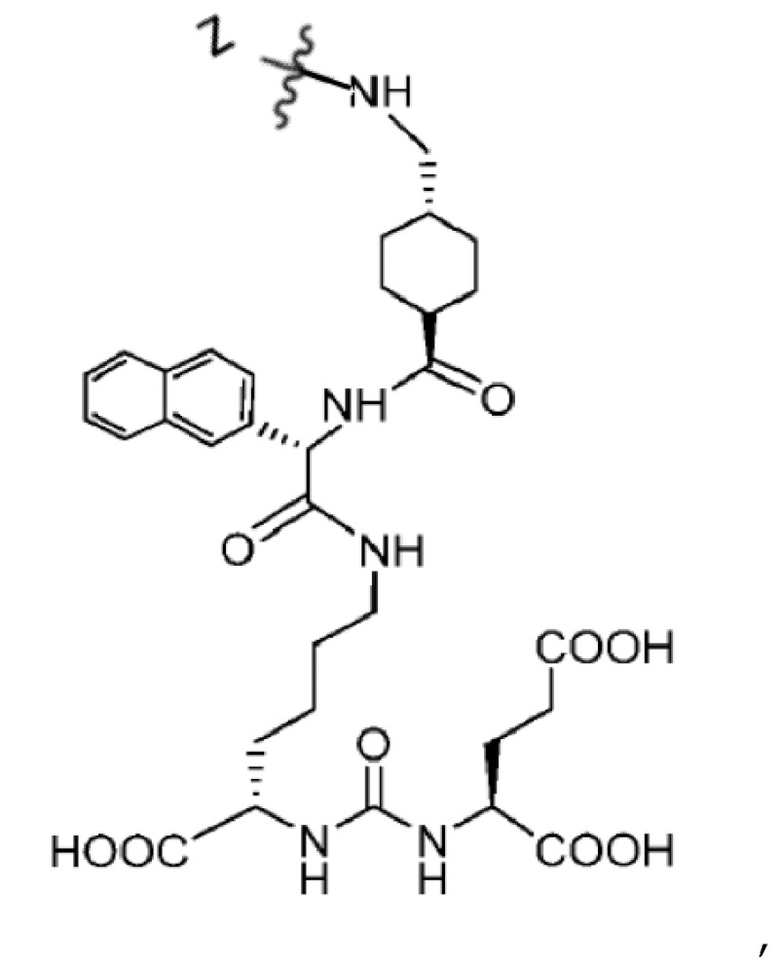
где Z представляет собой:
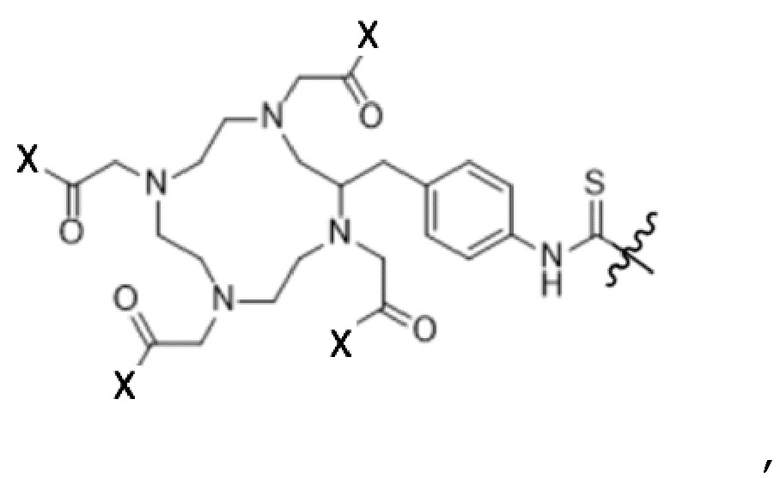
и где X представляет собой -OH или NH2.
X представляет собой -OH в случае p-SCN-Bn-DOTA, и X представляет собой NH2 в случае p-SCN-Bn-TCMC.
Это означает, что формула для связанных посредством C-остова p-SCN-Bn-DOTA или p-SCN-Bn-TCMC будет представлять собой:
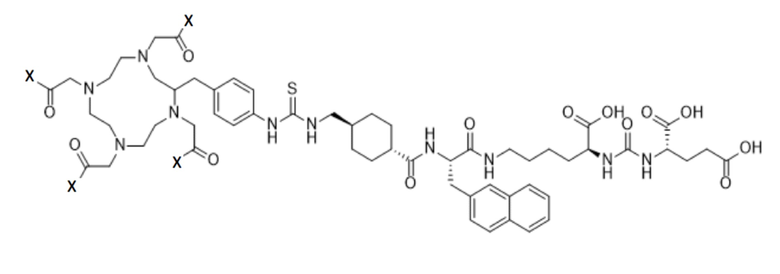 ,
,
где X представляет собой -OH или NH2.
Связанная посредством C-остова p-SCN-Bn-DOTA представляет собой:
 ,
,
p-SCN-Bn-DOTA-PSMA-лиганд 2.
Таким образом, один аспект настоящего изобретения относится к соединению, которое представляет собой p-SCN-Bn-DOTA-PSMA-лиганд 2.
Связанный посредством C-остова p-SCN-Bn-TCMC представляет собой:
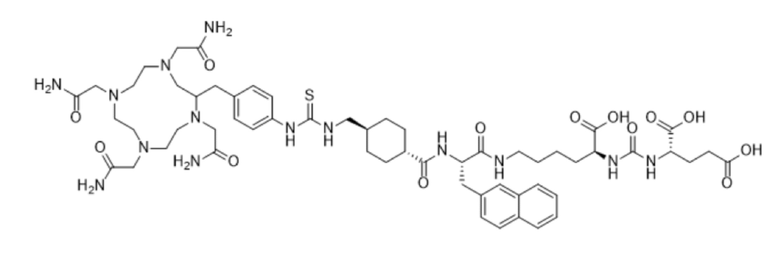 ,
,
p-SCN-Bn-TCMC-PSMA-лиганд 1.
Таким образом, один аспект настоящего изобретения относится к соединению, которое представляет собой p-SCN-Bn-TCMA-PSMA-лиганд 1 или p-SCN-Bn-DOTA-PSMA-лиганд 2, которые раскрыты выше и в примерах.
P-SCN-Bn-TCMC-PSMA-лиганд (лиганд 1) и p-SCN-Bn-DOTA-PSMA-лиганд (лиганд 2) (как показано в примерах) связан посредством углеродного остова (C-остова) с остальной частью соединения и имеет удлиненную линкерную область, включающую изотиоцианатобензильный линкер, а также в нем используется замещенный по углероду хелатор со всеми 4 хелатирующими плечами, являющимися свободными, в отличие от PSMA-617, который имеет более короткую линкерную область, и в нем используется одно из хелаторных плеч в качестве точки присоединения линкера. В последующих примерах, приведенных в данном документе, показано, что эти различия вызывают существенно различающееся биораспределение меченного радионуклидом продукта, что делает его более подходящим для нацеливания 212Pb на PSMA-экспрессирующие опухоли, поскольку он обеспечивает сниженное воздействие на почки по сравнению с PSMA-617.
В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению, такие как p-SCN-Bn-TCMC-PSMA-лиганд 1 и p-SCN-Bn-DOTA-PSMA-лиганд 2, могут быть представлены в форме соли трифторуксусной кислоты.
Совместно с 212Pb в комплексах по настоящему изобретению также можно применять CTT1401 и CTT1403 и их производные (Choy et al, 2017) с вариантами TCMC или DOTA.
При получении PSMA-связывающего производного мочевины в соответствии с настоящим изобретением с легкодоступной аминогруппой или другой группой, подходящей для конъюгации, p-SCN-Bn-TCMC можно конъюгировать с PSMA-связывающим соединением. Может потребоваться последующая очистка перед включением радиоактивной метки в виде 212Pb с наличием 224Ra в растворе или без него.
Таким образом, в одном варианте осуществления настоящего изобретения линкером является p-SCN-Bn-TCMC. Один вариант осуществления настоящего изобретения относится к комплексу в соответствии с настоящим изобретением, где линкером-хелатором является p-SCN-Bn-TCMC. Один вариант осуществления настоящего изобретения относится к комплексу в соответствии с настоящим изобретением, где линкером является p-SCN-Bn-DOTA. Другими словами, -p-SCN-Bn- является концевой частью линкерной области, которая присоединена к хелаторной группе TCMC или DOTA посредством углеродного остова.
Для продления периода полувыведения лекарственных средств можно применять человеческий сывороточный альбумин. Таким образом, в одном варианте осуществления 212Pb-меченное PSMA-связывающее производное мочевины в соответствии с настоящим изобретением дополнительно содержит группу, которая может связываться с альбумином с увеличением периода полувыведения из кровотока меченного радионуклидом продукта.
Дополнительный вариант осуществления настоящего изобретения относится к комплексу в соответствии с настоящим изобретением, где 212Pb-меченное PSMA-связывающее производное мочевины в соответствии с настоящим изобретением дополнительно содержит человеческий сывороточный альбумин, который был непосредственно конъюгирован с комплексом или ассоциирован с комплексом, например, посредством липосом.
Фармацевтические композиции
Один вариант осуществления настоящего изобретения относится к раствору, содержащему соединение и/или комплекс по настоящему изобретению. Раствор также может представлять собой фармацевтическую композицию.
Обычно важным элементом фармацевтической композиции является буферный раствор, который в значительной степени поддерживает химическую целостность радиолиганда и является физиологически приемлемым для инфузии пациентам.
В одном варианте осуществления настоящего изобретения фармацевтическая композиция содержит один или более фармацевтически приемлемых носителей и/или вспомогательных веществ.
Приемлемые фармацевтические носители включают без ограничения нетоксичные буферы, наполнители, изотонические растворы и т.д. Более конкретно, фармацевтический носитель может представлять собой без ограничения нормальный физиологический раствор (0,9%), полунормальный физиологический раствор, лактатный раствор Рингера, 5% декстрозу, 3,3% декстрозу/0,3% физиологический раствор. Физиологически приемлемый носитель может содержать антирадиолитический стабилизатор, например аскорбиновую кислоту, которая защищает целостность радиофармацевтического препарата во время хранения и транспортировки.
Один аспект настоящего изобретения относится к фармацевтической композиции, содержащей комплекс в соответствии с настоящим изобретением и разбавитель, носитель, поверхностно-активное вещество и/или вспомогательное вещество.
Один аспект настоящего изобретения относится 212Pb-меченному лиганду в качестве отдельно взятого средства. Им будет являться соединение по настоящему изобретению, связанное в комплекс с 212Pb, и без наличия каких-либо дополнительных радионуклидов, таких как 224Ra.
Один аспект настоящего изобретения относится к обеспечивающему двойное нацеливание раствору, содержащему 212Pb-меченный лиганд и катионный или слабо связанный в комплекс 224Ra. Им будет являться соединение по настоящему изобретению, связанное в комплекс с 212Pb, совместно с 224Ra, присутствующим в виде катионного или слабо связанного в комплекс 224Ra.
Один аспект настоящего изобретения относится к фармацевтической композиции, содержащей соединение и/или комплекс в соответствии с настоящим изобретением, которая дополнительно содержит 224Ra. 224Ra может быть катионным. Добавление 224Ra делает возможным двойное нацеливание, например, при его присутствии совместно с 212Pb.
Один аспект настоящего изобретения относится к фармацевтической композиции, содержащей комплекс в соответствии с настоящим изобретением, где радиоактивность составляет от 100 кБк до 100 МБк на дозу.
Один аспект настоящего изобретения относится к фармацевтической композиции, содержащей комплекс в соответствии с настоящим изобретением, где количество 224Ra и 212Pb находится в радиоактивном равновесии.
Один аспект настоящего изобретения относится к фармацевтической композиции, содержащей комплекс в соответствии с настоящим изобретением, где отношение активности (МБк) 212Pb к 224Ra составляет от 0,5 до 2, как например, 0,8–1,5, или, как например, 0,8–1,3, или предпочтительно, как например, 0,9–1,15.
Наборы
Раствор следует изготавливать физиологически пригодным для инъекций либо в централизованном месте изготовления, либо путем получения из системы набора, состоящей обычно из 2–4 флаконов, при этом являясь физиологически пригодным для инъекции после объединения содержимого флаконов набора.
Один аспект настоящего изобретения относится к набору, содержащему первый флакон, содержащий радиофармацевтическую композицию в соответствии с настоящим изобретением, и второй флакон, содержащий нейтрализующий раствор для регулирования рН и/или изотоничности радиофармацевтической композиции перед введением пациенту.
В случае, например, моноклонального антитела, обычно рекомендуют поддерживать собственную дозу генерирующего альфа-частицы радиофармацевтического раствора на уровне ниже 0,5 кГр, чтобы избежать снижения связывающих свойств ввиду радиолиза. Так, в случае концентрированных растворов, предназначенных для отправки в удаленные пункты, в зависимости от устойчивости к радиолизу генерируемого радиолиганда рекомендуют использовать систему набора, которая предусматривает добавление конъюгированного с хелатором лиганда в раствор 224Ra (включающий дочерние продукты распада) в отдаленный на промежуток от нескольких часов до 10 минут момент времени до момента введения.
Один аспект настоящего изобретения относится к набору, содержащему первый флакон, содержащий раствор 224Ra; второй флакон, содержащий комплексообразующее средство, выбранное из группы, состоящей из p-SCN-Bn-DOTA-PSMA-лиганда, p-SCN-Bn-TCMC-PSMA-лиганда, ациклических хелаторов, циклических хелаторов, криптандов, краун-эфиров, порфиринов или циклических или нециклических полифосфонатов, DOTMP, EDTMP, производных бисфосфоната, DOTA, производного DOTA, памидроната, конъюгированного с DOTA, TCMC, производного TCMC, памидроната, конъюгированного с TCMC, DOTA, конъюгированной с антителом, TCMC, конъюгированного с антителом, HBED-CC, NOTA NODAGA, TRAP, NOPO, PCTA, DFO, DTPA, CHX-DTPA, AAZTA, DEDPA и оксо-Do3A, при этом комплексообразующее средство способно образовывать комплекс с образующимся из 224Ra дочерним нуклидом, таким как 212Pb, и при этом комплексообразующее средство не образует комплекс с 224Ra в фармацевтическом растворе; и необязательно инструкции по смешиванию содержимого первого флакона и второго флакона, тем самым получая фармацевтическую композицию, готовую для введения пациенту через промежуток длительностью от 1 минуты до 12 часов после смешивания.
В одном варианте осуществления настоящего изобретения представлен набор, предназначенный для применения в качестве лекарственного препарата.
В конкретном варианте осуществления термин «раствор 224Ra» следует понимать как 224Ra, который представлен в растворе в свободной форме и не связан, например, с поверхностью, такой как смола.
В одном варианте осуществления набор содержит третий флакон, содержащий нейтрализующий раствор для регулирования рН и/или изотоничности радиофармацевтического раствора перед введением пациенту.
В еще одном предпочтительном варианте осуществления количество 224Ra и 212Pb находится в радиоактивном равновесии в первом флаконе.
В еще одном предпочтительном варианте осуществления отношение активности (МБк) 212Pb к 224Ra в первом флаконе составляет от 0,5 до 2, как например, 0,8–1,5, или, как например, 0,8–1,3, или, как например, 0,9–1,15.
В еще одном варианте осуществления первый флакон характеризуется радиоактивностью в диапазоне от 100 кБк до 100 МБк.
В одном варианте осуществления настоящего изобретения конъюгированный с хелатором лиганд добавляют в раствор 224Ra (включающий дочерние продукты распада) за 30 мин. – 5 часов до инъекции, как например за 1–3 часа до инъекции.
В одном варианте осуществления настоящего изобретения конъюгированный с хелатором лиганд добавляют в раствор 224Ra (включающий дочерние продукты распада) за 1 мин. – 20 мин. до инъекции.
В одном варианте осуществления настоящего изобретения конъюгированный с хелатором лиганд добавляют в раствор 224Ra (включающий дочерние продукты распада) за 1 мин. – 10 мин. до инъекции.
Также часть настоящего изобретения составляет набор с меченным хелатом белком или пептидом в одном флаконе и раствором 224Ra в другом флаконе, который предусматривает смешивание содержимого этих двух флаконов за 12 часов – 1 минуту перед введением. В одном варианте осуществления смешивание происходит за несколько часов (как например 5) – 30 минут перед введением пациенту с целью связывания 212Pb и/или 212Bi с хелатом.
В одном варианте осуществления настоящего изобретения содержимое обоих флаконов смешивают за 30 мин. – 1 час перед инъекцией.
В одном варианте осуществления настоящего изобретения содержимое обоих флаконов смешивают за 1 мин. – 20 мин. перед инъекцией.
В варианте осуществления настоящего изобретения содержимое обоих флаконов смешивают за 1 мин. – 10 мин. перед инъекцией.
Необязательно можно использовать третий флакон, содержащий жидкость, применяемую для разведения и регулирования изотоничности перед введением радиофармацевтического раствора. Этот третий флакон может содержать EDTMP, который при необходимости может хелатировать 212Bi.
Области применения, связанные с медициной
Один аспект настоящего изобретения относится к радиофармацевтической композиции в соответствии с настоящим изобретением для применения в качестве лекарственного препарата.
В одном варианте осуществления настоящего изобретения заболевание представляет собой рак.
Один аспект настоящего изобретения относится к радиофармацевтической композиции в соответствии с настоящим изобретением для применения в лечении заболевания мягких тканей и/или скелета. Лечение направлено на характеризующееся экспрессией PSMA заболевание, в том числе на заболевание мягких тканей и скелета.
В одном варианте осуществления настоящего изобретения заболевание скелета выбрано из группы, состоящей из метастазов в мягких тканях или скелете при формах рака молочной железы, предстательной железы, почек, легкого, кости или множественной миеломе.
В одном варианте осуществления настоящего изобретения рак представляет собой рак предстательной железы. Рак также может представлять собой рак молочной железы. Рак может представлять собой рак почки. Рак также может представлять собой рак легкого. Рак также может представлять собой рак кости. Рак также может представлять собой множественную миелому. Рак может представлять собой метастазы, обусловленные этими типами рака.
В одном варианте осуществления настоящего изобретения раствор вводят в дозе в диапазоне 50–150 кБк на кг массы тела, как например 50–100 кБк на кг массы тела.
Один аспект настоящего изобретения относится к способу лечения злокачественного или незлокачественного заболевания путем введения радиофармацевтической композиции в соответствии с настоящим изобретением нуждающемуся в этом индивидууму.
Ее можно применять с очищенным 212Pb-меченным лигандом или в обеспечивающем двойное нацеливание растворе, где 224Ra будет действовать в качестве средства лечения скелета, а 212Pb-меченное производное мочевины будет действовать в качестве средства системной терапии против клеток, экспрессирующих PSMA-антиген, который связан с метастатическим раком предстательной железы на поздних стадиях.
Таким образом, комплексы и растворы по настоящему изобретению можно применять в лечении метастатического рака предстательной железы.
Другой вариант осуществления настоящего изобретения относится к фармацевтическому раствору со свойствами двойного нацеливания, где 212Pb связан в комплекс с основанным на мочевине средством, нацеливающимся на PSMA, как описано в настоящем документе, а катионный 224Ra нацеливается на метастазы в кости посредством имитирующего кальций включения в кость.
Способы получения
Один аспект настоящего изобретения относится к способу получения радиофармацевтической композиции в соответствии с настоящим изобретением, при этом способ предусматривает получение первого раствора, где количество 224Ra и 212Pb находится в радиоактивном равновесии; получение второго раствора, содержащего комплексообразующее средство, которое выбрано из группы, состоящей из p-SCN-Bn-DOTA-PSMA-лиганда, p-SCN-Bn-TCMC-PSMA-лиганда, ациклических хелаторов, циклических хелаторов, криптандов, краун-эфиров, порфиринов или циклических или нециклических полифосфонатов, DOTMP, EDTMP, бисфосфоната, DOTA, производного DOTA, памидроната, конъюгированного с DOTA, TCMC, производного TCMC, памидроната, конъюгированного с TCMC, DOTA, конъюгированной с антителом, TCMC, конъюгированного с антителом, HBED-CC, NOTA NODAGA, TRAP, NOPO, PCTA, DFO, DTPA, CHX-DTPA, AAZTA, DEDPA и оксо-Do3A, при этом комплексообразующее средство способно образовывать комплекс с образующимся из 224Ra дочерним нуклидом, таким как 212Pb, и при этом комплексообразующее средство не образует комплекс с 224Ra; и смешивание первой композиции и второй композиции, тем самым получая фармацевтическую композицию в соответствии с настоящим изобретением.
Производные PSMA
PSMA (также называемый простат-специфическим раковым антигеном, PSM, FGCP, FOLH, GCP2, mGCP, GCPII, NAALAD1, NAALA-дазой, FOLH1, глутаматкарбоксипептидазой 2, глутаматкарбоксипептидазой II, мембранной глутаматкарбоксипептидазой, N-ацетилированной-альфа-связанной кислой дипептидазой I, петроилполи-гамма-глутаматкарбоксипептидазой, фолилполи-гамма-глутаматкарбоксипептидазой, фолатгидролазой 1, простат-специфическим мембранным антигеном, ингибирующим рост клеток белком 27) представляет собой мембранный антиген эпителиальных клеток предстательной железы в виде трансмембранного белка II типа и состоит из короткого NH2-концевого цитоплазматического домена, гидрофобной трансмембранной области и крупного внеклеточного домена. PSMA представляет собой фермент, который у людей кодируется геном FOLH1 (фолатгидролазы 1). GCPII человека содержит 750 аминокислот и имеет вес примерно 84 кДа.
Экспрессия PSMA ограничена несколькими здоровыми тканями, такими как слезные и слюнные железы, проксимальные почечные канальцы, придаток яичка, яичник, внутренняя сторона подвздошной и тощей кишок и астроциты в центральной нервной системе (CNS); в здоровой предстательной железе экспрессируется сравнительно малое количество PSMA, при этом экспрессия ограничена апикальным эпителием секреторных протоков. В данных незлокачественных тканях накопление нацеленных на PSMA зондов может ограничиваться интактным гематоэнцефалическим барьером, здоровой внутренней стороной проксимальной части тонкого кишечника и сокращенной цитоплазматической экспрессией PSMA в нормальной предстательной железе. PSMA чаще всего ассоциирован с андроген-независимой метастазирующей опухолью с высокой степенью злокачественности, хотя PSMA экспрессируется при большинстве первичных опухолей предстательной железы независимо от андрогенного статуса.
Низкомолекулярные ингибиторы PSMA являются связывающими цинк соединениями, и их можно классифицировать на три типа: 1) фосфонатные, фосфатные и фосфорамидатные соединения, 2) тиолы и 3) мочевины. Производные мочевины, судя по всему, обладают особенно интересными свойствами в качестве носителя для радионуклидов с целью диагностики и терапии.
Настоящее изобретение относиться к применению 212Pb-меченных производных мочевины. Их можно сочетать с андроген-депривационной терапией для усиления экспрессии PSMA для улучшенного накопления радиолиганда (Bakht et al, 2017).
Уровень активности
Если 212Pb-меченное производное мочевины применяют отдельно, уровень активности часто будет составлять от 1 до 500 МБк на пациента, еще чаще будет составлять 10–100 МБк на пациента.
Если 224Ra находится в равновесии с 212Pb, связанным в комплекс с PSMA-связывающим производным мочевины, дозировка часто будет составлять от 0,1 МБк до 100 МБк на пациента, еще чаще будет составлять от 1 до 20 МБк на пациента.
В конкретном варианте осуществления нацеливающийся на PSMA комплекс на основе производного мочевины в соответствии с настоящим изобретением помечен с помощью 227Th, который генерирует остеотропный 223Ra для обеспечения двойного нацеливания.
227Th может быть чистым или содержать различные количества 223Ra, например 10%, 50%, 100% или 250% 223Ra в сравнении с 227Th.
Общие сведения
Следует понимать, что любой признак и/или аспект, рассмотренный выше в связи с соединениями по настоящему изобретению, по аналогии применим к описанным в данном документе способами.
Последующие фигуры и примеры представлены ниже для иллюстрации настоящего изобретения. Они предназначены для иллюстрации и не должны трактоваться как каким-либо образом ограничивающие.
ПРИМЕРЫ
В следующих примерах используемая ксенотрансплантатная модель представляет собой модель опухоли с промежуточным уровнем накопления PSMA-лиганда в мышиных ксенотрансплантатах при использовании 177Lu-PSMA-617, обычно составляющим 10–15% от введенной дозы на грамм (% ID/г), в отличие от модели PC3 PIP, используемой другими исследователями, которая показывает уровень накопления в мышиных ксенотрансплантатах, обычно составляющий 30–40% ID/г.
Пример 1. Новые PSMA-связывающие хелатирующие лиганды в сравнении с PSMA-617
Предпосылки. Существует несколько молекул-носителей, обеспечивающих нацеливание радиолиганда на простат-специфический мембранный антиген (PSMA). Меченный лютецием-177 PSMA-617 (177Lu-PSMA-617) представляет собой соединение, находящееся на самой последней стадии клинической разработки для применения в радионуклидной терапии. Данная молекула хорошо функционирует и обеспечивает соответствующие значения соотношения накопления в опухолевой и нормальной тканях для более долгоживущих (т. е. с периодом полураспада в несколько дней) радионуклидов, в том числе 177Lu и 225Ac, но при этом в ранние моменты времени (обычно через несколько часов после инъекции) характеризуется высоким накоплением в почках. В случае с более короткоживущими радионуклидами, такими как 212Pb (период полураспада 10,6 часа), первоначальное накопление в почках представляет собой проблему потенциальной токсичности. Поэтому предпочтительно применять PSMA-лиганд с меньшим накоплением в почках, причем это не должно нарушать накопление в опухоли. Молекулы PSMA-лиганда состоят из (1) PSMA-связывающей области, (2) линкерной области и (3) хелатора, при этом линкерная область соединяет (1) и (3). Линкерную область также используют для регулирования размера молекулы и полярности в целях оказания влияния на свойства распределения in vivo. PSMA-связывающая область (мотив), используемая в PSMA-617, представляет собой структуру, которая может быть обнаружена в нескольких молекулах данного класса, разработанных несколькими разными авторами изобретений и исследователями, в том числе в PSMA-11 и PSMA I&T, а также в меченных посредством 131I и 211At PSMA-связывающих лигандах.
Как можно видеть, p-SCN-Bn-TCMC-PSMA-лиганд 1 имеет удлиненную линкерную область, включающую изотиоцианатобензильный линкер, а также в нем используется замещенный по углероду хелатор со всеми 4 хелатирующими плечами, являющимися свободными, в отличие от PSMA-617, который имеет более короткую линкерную область, и в нем используется одно из хелаторных плеч в качестве точки присоединения линкера. В последующих примерах, приведенных в данном документе, показано, что эти различия вызывают существенно различающееся биораспределение меченного радионуклидом продукта, что делает p-SCN-Bn-TCMC-PSMA-лиганд 1 более подходящим для нацеливания 212Pb на PSMA-экспрессирующие опухоли, поскольку он обеспечивает сниженное воздействие на почки по сравнению с PSMA-617.
Материалы и способы. Предшественники PSMA-лигандов для мечения радионуклидом синтезировала субподрядная лаборатория, осуществляющая коммерческий синтез.
PSMA-617 синтезировали в соответствии с процедурами, описанными в литературе. Предшественники p-SCN-Bn-TCMC синтезировали в соответствии с процедурами, описанными в литературе. На заключительной стадии синтеза TCMC-PSMA-лиганд синтезировали путем конъюгирования p-SCN-Bn-TCMC с аминогруппой промежуточного соединения PSMA-связывающего лиганда. Как PSMA-617, так и TCMC-Bn-PSMA-лиганд 1 очищали с помощью HPLC до чистоты> 98%, и высушивали, и хранили в виде солей трифторуксусной кислоты. Структуры и массы молекул определяли с помощью анализа 1Н-ЯМР и MS.
Соль трифторуксусной кислоты и p-SCN-Bn-TCMC-PSMA-лиганда 1 имеет химическую формулу C65H86F12N14O21S и молекулярную массу 1659,52 г/моль.
Химическое название (по номенклатуре IUPAC): (((1S)-1-карбокси-5-((2S)-3-(нафталин-2-ил)-2-((1R,4S)-4-((3-(4-((1,4,7,10-тетракис(2-амино-2-оксоэтил)-1,4,7,10-тетраазациклододекан-2-ил)метил)фенил)тиоуреидо)метил)циклогексан-1-карбоксамидо)пропанамидо)пентил)карбамоил)-L-глутаминовая кислота; трифторуксусная кислота(1:4).
Соль трифторуксусной кислоты и PSMA-617 имеет химическую формулу C57H75F12N9O24 и молекулярную массу 1498,25 г/моль.
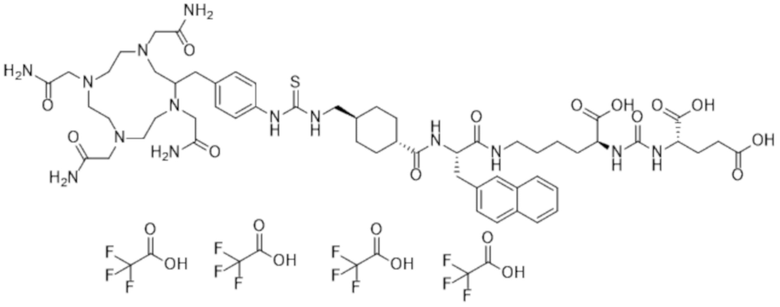
Соль трифторуксусной кислоты и p-SCN-Bn-TCMC-PSMA-лиганда 1.
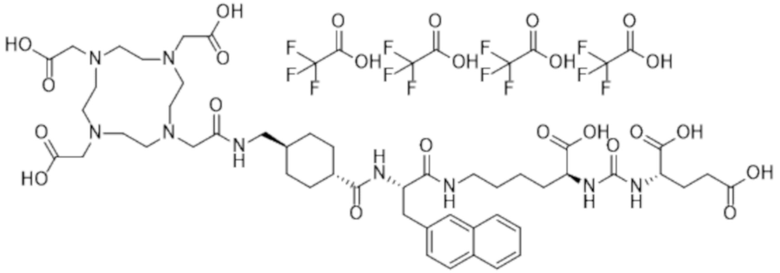
Соль трифторуксусной кислоты и PSMA-617.
Как можно видеть, p-SCN-Bn-TCMC-PSMA-лиганд 1 имеет удлиненную линкерную область, включающую бензильный линкер, а также в нем используется замещенный по углероду хелатор со всеми 4 хелатирующими плечами, являющимися свободными, в отличие от PSMA-617, который имеет более короткую линкерную область, и в нем используется одно из хелаторных плеч в качестве точки присоединения линкера. В последующих примерах показано, что эти химические различия вызывают существенно различающееся биораспределение меченного радионуклидом продукта, что делает его более подходящим для нацеливания 212Pb на PSMA-экспрессирующие опухоли, поскольку он обеспечивает сниженное воздействие на почки по сравнению с PSMA-617.
Подводя итог, описана новая молекула с идентичной PSMA-связывающей областью, но с отличающейся линкерной областью и отличающимися хелатирующими свойствами по сравнению с PSMA-617.
Пример 2
Замещенный по углероду p-SCN-Bn-DOTA-PSMA-лиганд 2 для мечения с помощью радиоактивных изотопов 212Pb, 212Bi, 213Bi, 225Ac, 227Th, 177Lu и т. д.
По сравнению с PSMA-617 лиганд имеет больший размер и группу p-SCN-Bn-DOTA, то есть имеет как отличающуюся область линкера, так и отличающуюся версию хелатора DOTA, где все четыре плеча хелатора свободны для обеспечения хелатирования радионуклидов по сравнению с PSMA-617.
p-SCN-Bn-DOTA-PSMA-лиганд 2 является DOTA-аналогом p-SCN-Bn-TCMC-PSMA-лиганда 1, описанного в примере 1, и имеет углеродный линкер, обеспечивающий связывание с остовом хелатора, оставляя хелаторные группы свободными для взаимодействия с радиоактивной меткой, и поэтому ожидается, что он улучшит стабильность хелата после мечения радионуклидом по сравнению с меченным радионуклидом PSMA-617. Ввиду наличия дополнительного липофильного бензильного звена в линкерной области и большего размера молекулы ожидается меньшее накопление в почках по сравнению с PSMA-617. Эту молекула можно синтезировать таким же образом, как p-SCN-Bn-TCMC-PSMA-лиганд 1, используя предшественник на основе DOTA вместо предшественника на основе TCMC на последней стадии синтеза.

Соль трифторуксусной кислоты и p-SCN-Bn-DOTA-PSMA-лиганда 2.
Соль трифторуксусной кислоты и p-SCN-Bn-DOTA-PSMA-лиганда 2 имеет химическую формулу C65H82F12N10O25S и молекулярную массу 1663,46 г/моль.
Являясь присоединенной к DOTA посредством замещения по углероду, эта молекула характеризуется свойствами, крайне подходящими для мечения с помощью радиоактивных изотопов 212Pb, 212Bi, 213Bi, 225Ac, 227Th, а также с помощью совместимых с позитронно-эмиссионной томографией (PET) радионуклидов, как например 68Ga.
Таким образом, описана новая PSMA-связывающая молекула, представляющая собой p-SCN-Bn-DOTA-PSMA-лиганд 2, подходящая для радиолигандной визуализации и терапии.
Подводя итог, замещенный по углероду p-SCN-Bn-DOTA-PSMA-лиганд 2 описан как характеризующийся отличными от PSMA-617 свойствами в отношении размера и хелатирующих свойств.
Пример 3. Протестированные радионуклиды
Лютеций-177 приобретали в виде готового к использованию 177LuCl3, растворенного в разведенной HCl. Свинец-212 получали из растворов на основе 224Ra. Радий-224 получали из 228Th, связанного с актинидной смолой (Eichrom Technologies, LLC), путем элюирования колонки, содержащей актинидную смолу с иммобилизованным 228Th, с помощью 1 М HCl. Элюат очищали на второй колонке с Ac-смолой, и элюат выпаривали досуха, используя флакон для выпаривания с крышкой с входным и выходным отверстиями для газа, помещенный в блок нагревателя при примерно 110◦C, и небольшой поток газообразного азота для выпаривания растворителя. Когда флакон для выпаривания становился свободным от растворителя, добавляли 0,1 М HCl для растворения остатка, обычно 200–400 мкл.
Пример 4. Мечение радиоактивными изотопами PSMA-связывающих лигандов
Как правило, растворы 177Lu и 224Ra/212Pb доводили с помощью HCl с 10% 5 М ацетата аммония до желаемого объема и рН 5–6. PSMA-связывающие лиганды растворяли в 0,1 М HCl с 0,5 М ацетата аммония до концентрации 1 мг/мл. Как правило, использовали концентрацию, составляющую 20 мкг на 1 мл радиоактивного раствора. Реакционную смесь инкубировали на шейкере в течение 15–30 минут, причем мечение, как правило, оценивали с помощью тонкослойной хроматографии. Мечение с помощью свинца-212 проводили при комнатной температуре или 37oC с использованием p-SCN-Bn-TCMC-PSMA-лиганда 1, в то время как 177Lu-мечение и 212Pb-мечение PSMA-617 проводили при 90oC. Типичные выходы для мечения с помощью радионуклидов находились в диапазоне 90–100% при использовании тестируемых соединений и радионуклидов, обеспечивая концентрацию 1 мкг на 20 мкл или выше.
Подводя итог, мечение радионуклидами обоих лигандов осуществляли с успехом. Новый p-SCN-Bn-TCMC-PSMA-лиганд 1 можно было подвергать мечению радионуклидом 212Pb при комнатной температуре в отличие от 177Lu-PSMA-617, который требовал мечения при повышенной температуре.
Пример 5. Анализы посредством тонкослойной хроматографии
Тонкослойную хроматографию (TLC) проводили с использованием хроматографических полосок (модель № 150-772, Biodex Medical Systems Inc, Ширли, Нью-Йорк, США). Буфер для составления (FB), состоящий из 7,5% человеческого сывороточного альбумина и 5 мМ EDTA в DPBS и доведенный до примерно pH 7 с помощью NaOH, смешивали с конъюгатами антител в соотношениях 2:1 в течение по меньшей мере 5 минут перед нанесением на полоски для определения свободного радионуклида. Небольшой химический стакан с приблизительно 0,5 мл 0,9% NaCl использовали для размещения в нем полосок с нанесенным пятном образца. К полоске обычно добавляли 1–4 мкл образца на приблизительно 10% выше нижнего края полоски. После того, как фронт растворителя перемещался на приблизительно 20% от верхнего края полоски, полоску разрезали пополам, и каждую половину помещали в пробирку объемом 5 мл для регистрации излучения. В этой системе меченный радионуклидом лиганд остается в нижней половине, тогда как радионуклид, связанный в комплекс с EDTA, мигрирует в верхнюю половину. Было подтверждено, что свободные катионы как 212Pb, так и 177Lu образовывали комплекс с EDTA и перемещались в верхнюю часть.
Подводя итог, использовали систему TLC, позволяющую быстро определять выход мечения радионуклидом, которая эффективно различала радиолиганд и свободный радионуклид.
Пример 6. Отделение 212Pb от растворов 224Ra
Меченный радионуклидом лиганд может быть использован в качестве компонента в обеспечивающих двойное нацеливание растворах 224Ra, где 224Ra нацеливается на заболевание скелета, а лиганд нацеливается на системное метастатическое заболевание. Альтернативно, генерирующие растворы 224Ra можно использовать для получения 212Pb-меченного лиганда путем мечения in situ, то есть лиганд образует комплекс с 212Pb в присутствии 224Ra. К 40 мкл растворов радия-224/212Pb в 0,5 М ацетата аммония с рН 5–6 добавляли 2 мкл (1 мкг/мкл) либо p-SCN-Bn-TCMC-PSMA-лиганда 1, либо PSMA-617, и проводили реакцию, как описано, для генерирования 212Pb-меченных лигандов. Для очистки 212Pb-PSMA-лиганда к продукту добавляли около 10 мкл буфера для составления, состоящего из 7% бычьего сывороточного альбумина, 10 мМ EDTA и 10 мг/мл аскорбиновой кислоты. После этого реакционную смесь добавляли в колонку Sephadex G-10 PD MiniTrap G-10 (GE Healthcare Life Sciences) и элюировали с помощью 0,9% NaCl. Элюат, содержащий 212Pb, как правило фракции, элюированные после внесения 0,7–1,5 мл, собирали и анализировали на гамма-радиометре, и проводили анализ посредством TLC и анализ связывания с радиолигандом. Процедура очистки продукта характеризовалась высоким радиохимическим выходом (обычно >80%) и высокой радиохимической чистотой, при этом, как правило, 224Ra составлял менее 0,4% по сравнению с 212Pb-меченным лигандом.
Подводя итог, p-SCN-Bn-TCMC-PSMA-лиганд 1 и PSMA-617 можно подвергать мечению радионуклидом 212Pb в присутствии 224Ra, что приводит к получению обеспечивающего двойное нацеливание раствора для комбинированного нацеливания на метастазы в костях с помощью 224Ra и системного нацеливания на опухолевые клетки с помощью 212Pb-меченного PSMA-лиганда.
Было также обнаружено, что при использовании гель-фильтрационной колонки Sephadex G-10 оба протестированных 212Pb-меченных PSMA-лиганда могут быть отделены от 224Ra в растворе с уровнем извлечения выше 80% и проникновением 224Ra менее 0,4%, что обеспечивает получение высокоочищенного 212Pb-меченного PSMA-радиолиганда для независимого нацеливания на PSMA.
Пример 7. Анализ стабильности 212Pb-меченных лигандов in vitro.
Меченный радионуклидом лиганд в растворе 224Ra/212Pb смешивали 1:1 с PBS или бычьим сывороточным альбумином и инкубировали при 37oC в течение периода вплоть до 48 часов. Анализы посредством TLC проводили через 1 ч., 4 ч., 24 ч. и 48 ч. инкубации.
Данные приведены в таблице 1 и показывают, что 212Pb после его генерации из 224Ra непрерывно реагирует с лигандом и поддерживает высокий процент радиохимической чистоты даже через 48 часов. Таким образом, PSMA-лиганды совместимы с использованием раствора 224Ra для получения радиолиганда in situ, который подходит для централизованного изготовления и транспортировки к конечному пользователю.
Таблица 1. Радиохимическая чистота 212Pb-TCMC-PSMA-лиганда 1 и 212Pb-PSMA-617 в PBS и FBS
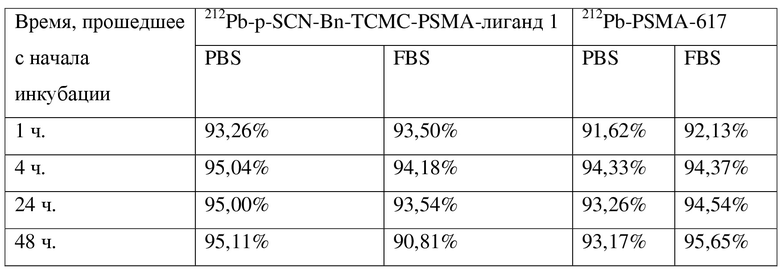
Заключение. Данные показывают, что p-SCN-Bn-TCMC-PSMA-лиганд 1 и PSMA-617, меченные с помощью 212Pb, стабильны в растворах 224Ra в течение длительного периода времени, что указывает на совместимость с централизованным изготовлением и транспортировкой к конечному пользователю готового к использованию продукта. Такие растворы могут быть использованы для противоракового лечения.
Пример 8. Связывание раковых клеток предстательной железы p-SCN-Bn-TCMC-PSMA-лигандом-1 и PSMA-617, меченными с помощью 212Pb
Фракции связанных клеток измеряли путем добавления приблизительно 1 нг радиолиганда к 0,2 мл клеток C4-2 (5 × 107 клеток на мл) в пробирке объемом 5 мл и инкубирования в течение 1 часа перед измерением индуцированной активности, промывали клетки 3 раза с помощью 0,5 мл 0,5% бычьего сывороточного альбумина в DPBS, и затем проводили повторную регистрацию излучения промытого клеточного осадка. Из нескольких экспериментов было обнаружено, что % связывания находился в диапазоне 40–53% после вычитания неспецифического связывания. Неспецифическое связывание измеряли путем блокирования клеток избытком 10 мкг/мл немеченого лиганда перед добавлением радиолиганда. Не было обнаружено существенного различия в связывании клеток между меченными радионуклидом p-SCN-Bn-TCMC-PSMA-лигандом 1 и PSMA-617. Подводя итог, радиолиганды меченных радионуклидом p-SCN-Bn-TCMC-PSMA-лиганда 1 и PSMA-617 имели сходные свойства связывания клеток in vitro, указывая на то, что p-SCN-Bn-TCMC-PSMA-лиганд 1 обладает соответствующей антигенсвязывающей способностью.
Пример 9. Радиолитическая стабильность p-SCN-Bn-TCMC-PSMA-лиганда 1, оцененная с помощью анализа способности радиолиганда связывать раковые клетки предстательной железы и анализа посредством TLC.
В таблице 2 показаны фракции связанных клеток, измеренные путем добавления приблизительно 1 нг радиолиганда к 0,2 мл клеток C4-2 (5 × 107 клеток на мл) в пробирке объемом 5 мл и инкубирования в течение 1 часа перед измерением индуцированной активности, промывания клеток 3 раза с помощью 0,5 мл 0,5% бычьего сывороточного альбумина в DPBS, и затем проведения повторной регистрации излучения промытого клеточного осадка. Начальная активность в растворе составляла около 5 МБк/мл, обеспечивая поглощенную дозу излучения в растворе, составляющую приблизительно 1,8 Гр через 24 ч. и 3,3 Гр через 48 часов. Данные (таблица 2) указывают на небольшое снижение при самом длительном времени воздействия, но в целом наблюдали относительно сильную устойчивость лиганда к радиолизу, которая совместима с централизованным изготовлением и транспортировкой к конечному пользователю генерирующего раствора на основе 224Ra с осуществлением или без осуществления удаления 224Ra до введения продукта.
Таблица 2. Связывающая способность 212Pb-p-SCN-Bn-TCMC-PSMA-лиганда 1 при выдерживании в растворе 224Ra

Заключение. Данные указывают на то, что 212Pb-p-SCN-Bn-TCMC-PSMA-лиганд 1 стабилен в растворах 224Ra в течение длительного периода времени, и PSMA-лиганд способен образовывать с комплекс 212Pb по мере его генерирования из 224Ra во время хранения, а при условии, что поглощенная доза излучения поддерживается на уровне ниже приблизительно 2 кГр, такие растворы можно использовать для противоракового лечения.
Пример 10. Биораспределение меченных радионуклидом лигандов у голых мышей с PSMA-позитивными ксенотрансплантатами C4-2.
Биораспределение растворов 224Ra/212Pb с p-SCN-Bn-TCMC-PSMA-лигандом 1 и PSMA-617, меченными с помощью 212Pb и 177Lu, сравнивали после внутривенной инъекции голым мышам с ксенотрансплантатами C4-2 в различные моменты времени после инъекции. Каждая группа обычно состояла из трех мышей. 212Pb-мечение превышало 92% для продуктов. Молярная концентрация лиганда была значительно ниже для 177Lu-PSMA-617, поскольку для 177Lu использовался гораздо более высокий уровень радионуклида по сравнению с 212Pb. Примерно 16 кБк 224Ra/212Pb инъецировали каждому животному, то есть примерно 0,2 нмоль лиганда на мышь. Животным давали наркоз и умерщвляли с помощью смещения шейных позвонков с последующим препарированием и сбором образцов ткани, крови и мочи. Образцы взвешивали и излучение регистрировали с помощью гамма-радиометра.
Пример 11. Сравнение связывания опухолью и накопления почками p-SCN-Bn-TCMC-PSMA-лиганда 1 и PSMA-617, меченных 212Pb, у мышей
Биораспределение растворов 224Ra/212Pb с p-SCN-Bn-TCMC-PSMA-лигандом 1 и PSMA-617, меченными 212Pb, сравнивали после внутривенной инъекции голым мышам с ксенотрансплантатами C4-2 через 4 ч. после инъекции. Предусматривали по три мыши в каждой группе. 212Pb-мечение превышало 92% для обоих продуктов. Молярная концентрация была одинаковой для обоих продуктов, то есть 12,5 нмоль на МБк. Примерно 16 кБк 224Ra/212Pb инъецировали каждому животному, то есть примерно 0,2 нмоль лиганда на мышь. Животным давали наркоз и умерщвляли с помощью смещения шейных позвонков с последующим препарированием и сбором образцов ткани, крови и мочи. Образцы взвешивали и излучение регистрировали с помощью гамма-радиометра. Результаты. Через четыре часа после инъекции отношения 212Pb-p-SCN-Bn-TCMC-PSMA-лиганда 1 к PSMA-617 были следующими: 1,35 для опухоли; 0,20 для почки; 1,21 для крови; 2,67 для печени; 0,71 для селезенки. Путем регистрирования излучения от образцов после 3 дней хранения подтверждали, что биораспределение 224Ra не было существенно изменено ни одним из PSMA-направленных лигандов. Обсуждение. 212Pb p-SCN-Bn-TCMC-PSMA-лиганд 1 продемонстрировал существенно отличное от 212Pb-PSMA-617 биораспределение, и особенно достойным внимания является крайне низкое и благоприятное соотношение для накопления в почках, поскольку почки, как ожидается, будут основной дозолимитирующей нормальной тканью, связанной с PSMA-радиолигандной терапией с использованием относительно короткоживущих излучателей альфа-частиц (фигура 1). Подводя итог, 212Pb-p-SCN-Bn-TCMC-PSMA-лиганд 1 показывает очень многообещающее биораспределение в ранних временных точках по сравнению с PSMA-617, что важно при использовании короткоживущих радионуклидов, таких как 212Pb.
Пример 12. Сравнение связывания опухолью и накопления почками 212Pb-меченного p-SCN-Bn-TCMC-PSMA-лиганда 1 и 177Lu-меченного PSMA-617 у мышей
Способы. Накопление в опухоли и почках 212Pb-меченного p-SCN-Bn-TCMC-PSMA-лиганда 1 и 177Lu-меченного PSMA-617 сравнивали через 1 час и 4 часа после внутривенной инъекции продуктов голым мышам с ксенотрансплантатами C4-2, как описано в примере 9. Результаты. Опухоли и почки являлись тканями, накапливающими наибольшее количество радиоактивности. В качестве примеров накопление опухолью и почками 212Pb-p-SCN-Bn-TCMC-PSMA составляло в среднем 13,9 и 8,1 процента от введенной дозы на грамм (% ID/г) соответственно через 4 часа после инъекции. Накопление опухолью и почками 177Lu-PSMA-617 составляло в среднем 13,6 и 17,4% ID/г соответственно через 4 часа после инъекции. Следует отметить, что молярное количество введенного лиганда было намного ниже для PSMA-617, что, как известно, снижает накопление в почках, однако, тем не менее, новое 212Pb-меченное соединение показало меньшее накопление в почках. Соотношения накопления опухолью по сравнению с почками на отметке 4 часа были следующими: 1,7 для 212Pb-p-SCN-Bn-TCMC-PSMA-лиганда 1; 0,8 для 177Lu-PSMA-617.
Средние соотношения накопления опухолью по сравнению с почками, определенные через 1 час после введения, составляли 0,40 для 212Pb-p-SCN-Bn-TCMC-PSMA-лиганда 1 и 0,17 для 177Lu-PSMA-617. Подводя итог, несмотря на более высокий показатель молярной концентрации лиганда для 212Pb-p-SCN-Bn-TCMC-PSMA-лиганда 1, он показал лучшее соотношение накопления опухолью по сравнению с почками, чем 177Lu-PSMA-617, что указывает на то, что он может хорошо подходить для радиолигандной терапии излучателем альфа-частиц на основе 212Pb.
Пример 13. Биораспределение раствора с одиночным нацеливанием, содержащего 212Pb-p-SCN-Bn-TCMC-PSMA-лиганд 1, у мышей с PSMA-позитивными ксенотрансплантатами
Используя раствор 212Pb/224Ra для реакции с p-SCN-Bn-TCMC-PSMA-лигандом 1, как описано, очищенный 212Pb-p-SCN-Bn-TCMC-PSMA-лиганд 1 очищали с использованием гель-фильтрационной колонки Sephadex G-10, и приблизительно 30 кБк и 300 нг очищенного радиолигандного продукта инъецировали каждому животному. Данные показаны в таблице 3. Как можно видеть, почечная активность снижается относительно быстро, в то время как накопление опухолью показывает хорошее удержание. Соотношения накопления опухолью по сравнению с тканями (таблица 4) указывает на пригодность для радиолигандного нацеливания с помощью 212Pb.
Подводя итог, 212Pb-p-SCN-Bn-TCMC-PSMA-лиганд 1 демонстрирует соответствующие свойства нацеливания для использования в радиолигандной терапии, направленной против PSMA-экспрессирующего рака предстательной железы.
Таблица 3. Биораспределение для 212Pb-p-SCN-Bn-TCMC-PSMA-лиганда 1 в различные моменты времени после инъекции
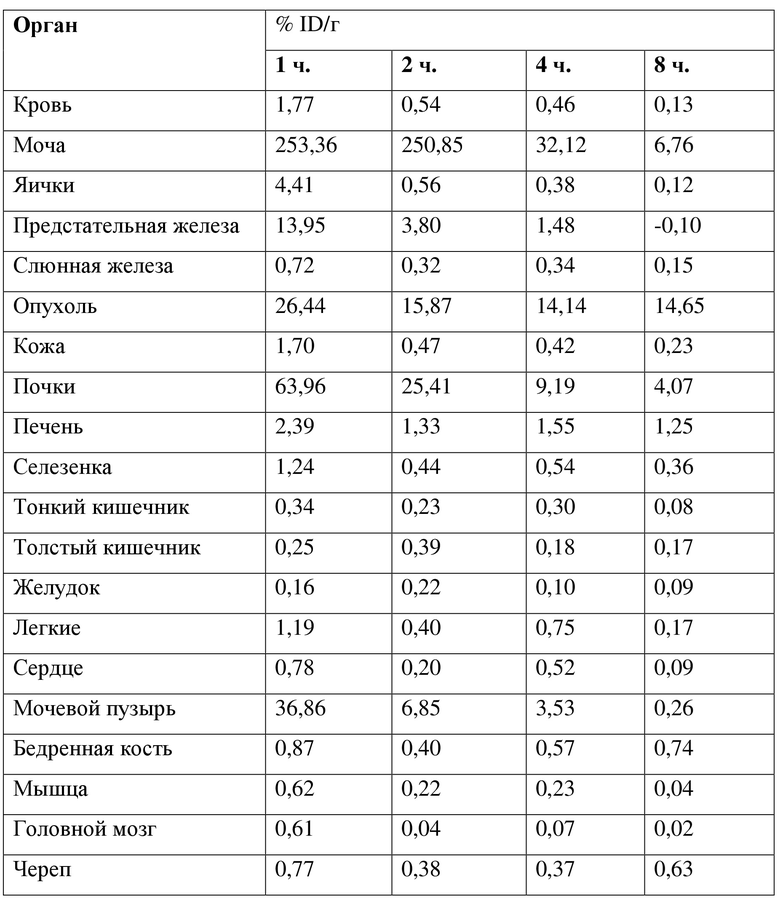
Таблица 4. Соотношения накопления опухолью по сравнению с тканью для 212Pb-p-SCN-Bn-TCMC-PSMA-лиганда 1 в различные моменты времени

Пример 14. Дозировка
Вырабатываемая энергия излучения для двух нуклидов в основном исходит от альфа-частиц, и поэтому в следующей оценке рассматриваются только альфа-частицы.
212Pb и короткоживущие дочерние продукты распада вырабатывают в среднем 7,8 МэВ альфа-излучения на атом 212Pb. Период полураспада 212Pb составляет 10,6 ч.
213Bi и короткоживущие дочерние продукты распада вырабатывают в среднем 8,4 МэВ альфа-излучения на атом 213Bi. Период полураспада 213Bi составляет 46 мин.
Предполагается, что эквивалентная доза для альфа-частиц составляет 5 Зв/Гр.
Таким образом, 1 Бк 212Pb вырабатывает эквивалентную дозу альфа-частиц, составляющую 1 x (10,6 x 60/46) x 7,8 / 8,4 = 12,6 Бк 213Bi, при полном распаде.
Сообщалось, что слюнные железы, почки и красный костный мозг являются дозолимитирующими тканями для 213Bi и 225Ac в комплексе с PSMA-617 (Kratochwil, et al, 2018).
На основании визуализации PSMA-617, меченного радионуклидами, подходящими для обнаружения с помощью позитронно-эмиссионной томографии, предполагается, что максимальный процент накопления будет достигнут во временной точке 30 минут, когда 70% атомов 213Bi по сравнению с 90% 212Pb достигнут и подвергнутся распаду в опухоли (т. е. относительная фракция распада).
Предполагается, что относительная фракция распада для дозолимитирующих тканей составляет 70% для всех тканей при использовании 213Bi-PSMA-617. Предполагается, что 50% накопленного 212Pb-PSMA-617 будет подвергаться распаду в слюнных железах, 30% в почках и 20% в костном мозге.
С учетом поправки на энергию на один Бк и относительную фракцию распада для PSMA-617, меченного 212Pb и 213Bi, расчетные дозы для 212Pb-PSMA-617 будут такими, как представленов таблице 5 вместе с ранее опубликованными данными для PSMA-617, меченного 213Bi и 225Ac. Кроме того, с помощью сравнения полученных от мышей данных в отношении 212Pb-p-SCN-Bn-TCMC-PSMA-лиганда 1 и 212Pb-PSMA-617 и предполагая, что коэффициент накопления тканями у человека будет аналогичным, дозиметрическая оценка для 212Pb-p-SCN-Bn-TCMC-PSMA-лиганда 1 представлена в таблице 5.
Таблица 5. Оценка дозы, при условии аналогичной стабильности и аффинности продуктов независимо от радионуклида

aИз Kratochwil et al 2017. bИз Kratochwil et al 2018. cПри условии, что накопление такое же, как и для 212Pb-PSMA-617, за исключением накопления почками, которое, как предполагается, снижается на 50%.
Сообщалось, что PSMA-617, меченный как 225Ac, так и 213Bi, использовали клинически, и он показал значительную противоопухолевую активность. На основании оценок в этом примере показано, что 212Pb-меченный ингибитор PSMA на основе мочевины является крайне перспективным терапевтическим средством, направленным против рака, экспрессирующего PSMA.
Пример 15. Дозиметрическая оценка для двойного нацеливания катионом 224Ra и 212Pb-меченным производным мочевины, нацеливающимся на PSMA
Использовали 224Ra в равновесии с 212Pb-меченным производным мочевины, связывающим PSMA.
Для дозы 150 кБк 224Ra общая введенная активность будет составлять 10,5 МБк на человека весом 70 кг. Используя опубликованные данные дозиметрии для катионного 223Ra у пациентов с раком простаты и делая поправку на разницу в периоде полураспада между 224Ra и 223Ra, предполагая одинаковое биораспределение и учитывая разные значения времени удержания в различных тканях, обнаружили, что 224Ra на один введенный МБк будет обеспечивать 0,006 Гр для почек, 0,029 Гр для слюнных желез, 0,26 Гр для красного костного мозга и, по оценкам, накопление опухолями, в 5 раз превышающее накопление для красного костного мозга, т. е. 1,3 Гр.
Для дозы альфа-частиц предполагается эквивалентная доза 5 Зв/Гр, и данные переведены в Зв на единицу введенной дозы (10,5 МБк/пациент) в таблице 6.
Таблица 6. Оценка дозы для катиона 224Ra + 212Pb-меченное производное мочевины, связывающее PSMA*

*Предполагая соотношение 1:1 между 224Ra и 212Pb.
aИз Lassmann et al, 2002. bСледует отметить, что красный костный мозг главным образом облучается отложениями Ra на поверхности кости, и ввиду небольшой длины пробега альфа-частиц с поверхностей кости существенные участки красного костного мозга находятся вне зоны досягаемости альфа-частиц с поверхности кости. Для дозы альфа-частиц предполагается эквивалентная доза 5.
Пример 15. Оценочная дозиметрия для 227Th-меченного производного мочевины, связывающего PSMA
В этом примере предполагается, что p-SCN-Bn-DOTA-PSMA-лиганд 2 или версия этой молекулы, полученная из HOPO, помечены 177Lu. Текущие оценки основаны на адаптации данных из исследований 223Ra у пациентов и 225Ac-PSMA-617 у пациентов с раком простаты (Chittenden et al., 2015, Kratochwil et al, 2017, 2018).
Для излучения альфа-частиц предполагается эквивалентная доза 5 Зв/Гр.
Предполагается, что 223Ra, генерируемый в тканях, подвергнется распаду локально. Предполагается, что 40% 223Ra, генерируемого в результате циркуляции 227Th во всем теле, удерживается в скелете. Рассматривается только доза альфа-частиц, поскольку она составляет 95% или больше от общей выработанной энергии излучения.
Для ткани с более длительным временем удержания меченного радионуклидом производного мочевины, связывающего PSMA, (слюнной железы, почек и опухолей) предполагается, что совокупная активность 223Ra, продуцируемого из 227Th, составляет 20% от 227Th, а для красного костного мозга составляет 5%.
Предполагается, что 20% и 5% радия, генерируемого из 227Th в различных тканях, находятся в равновесии с излучающими альфа-частицы дочерними радионуклидами, поэтому каждый распад радия в сущности генерирует 26,4 МэВ альфа-излучения, в то время как 227Th отдельно генерирует 5,9 МэВ альфа-излучения.
Поскольку для 225Ac и 227Th значения времени удержания ниже, чем периоды полураспада, предполагается, что совокупная активность для 227Th всего лишь на 10% выше, чем для 225Ac (не считая дочерних продуктов распада 225Ac) во всех органах. Предполагается в общей сложности 27,7 МэВ альфа-излучения на атом 225Ac в результате распада материнского нуклида и излучающих альфа-частицы дочерних продуктов распада.
Предполагается также, что применительно к дозе для красного костного мозга и дозе для опухоли скелета последняя увеличивается в 2 раза по сравнению с дозой для красного костного мозга вследствие накопления скелетом 223Ra, генерируемого во время системной циркуляции и т. д. продуктом с 227Th.
Данные представлены в таблице 7. Данные указывают на благоприятное соотношение накопления опухолью по сравнению с тканью для 227Th-меченного производного мочевины, связывающего PSMA.
Таблица 7. Оценочная дозиметрия эквивалентных доз для критически значимых органов и опухолей для 227Th-меченного производного мочевины, связывающего PSMA (МБк/пациент)
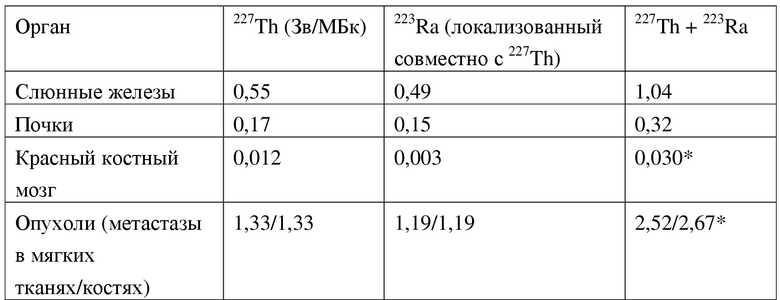
*Включает добавленную скелетную дозу 223Ra, генерируемого из 227Th во время фазы циркуляции.
Данные в таблице 7 представляют 227Th-меченное производное мочевины, связывающее PSMA (например, PSMA-617), которое очищают от 223Ra перед инъекцией. Альтернативно, можно использовать раствор продукта с 227Th, предусматривающий наличие различных количеств 223Ra, для увеличения дозы в отношении метастазов в кости, например, если заболевание костей является крайне доминирующим по сравнению с заболеванием мягких тканей.
Предполагается, что продукты, описанные в данном документе, могут использоваться в виде однократной процедуры лечения или в виде повторяющихся процедур лечения.
Подводя итог, дозиметрические оценки для меченных 212Pb или 227Th производных мочевины, нацеливающихся на PSMA, указывают на многообещающие соотношения накопления опухолью по сравнению с тканями, что указывает на возможную клиническую эффективность при применении.
Пример 16. Сравнительный эксперимент в отношении терапии с помощью 177Lu-PSMA-617 и 212Pb-p-SCN-Bn-TCMC-PSMA-лиганда 1, проводимый на голых мышах с ксенотрансплантатами С4-2
Самцам голых мышей в боковые области инокулировали PSMA-позитивные клетки предстательной железы человека линии C4-2 и спустя 2 недели, когда опухоли имели диаметр 5–7 мм. Группы, предусматривающие по 8 животных в каждой, получали физиологический раствор, 52 МБк 177Lu-PSMA-617 или 320 кБк 212Pb-p-SCN-Bn-TCMC-PSMA-лиганда 1. Животных умерщвляли, когда размер опухоли достигал 20 мм, ввиду требований в отношении благополучия животных. Показатели дозиметрии опухоли рассчитывали на основе следующих предположений: для 177Lu-PSMA-617 эффективный период полураспада в опухоли составлял 3 дня, 10% инъецированной дозы на грамм подвергается распаду в опухоли, и 80% излучения от распадов в опухолях поглощается опухолями, и энергия излучения составляет 0,15 МэВ на распад. Предполагали, что эффективный период полураспада для 212Pb составлял 10,6 ч., 10% от введенной дозы на грамм подвергается распаду в опухоли, и 100% радиации в опухоли поглощается опухолью, удержание 212Pb и дочерних продуктов распада в опухолях составляет 100%, и энергия излучения составляет 8 МэВ на распад. Опухолевая дозиметрия активности инъецированных субстанций в среднем показала поглощенную опухолью дозу, составляющую 35,9 Гр, для получавшей 177Lu-PSMA-617 группы и поглощенную опухолью дозу, составляющую 2,06 Гр, для получавшей 212Pb-p-SCN-Bn-TCMC-PSMA-лиганда 1 группы соответственно.
Результаты. В день 30 после проведения обработки следующие данные показали выживаемость, составляющую 0%, 12,5% и 75% для получавших физиологический раствор, 177Lu-PSMA-617 и 212Pb-p-SCN-Bn-TCMC-PSMA-лиганд 1 групп соответственно (фигура 2). Медианная выживаемость составила 15 дней, 20 дней и >30 дней (не достигнута) для получавших физиологический раствор, 177Lu-PSMA-617 и 212Pb-p-SCN-Bn-TCMC-PSMA-лиганд 1 групп соответственно.
Подводя итог, данные указывают на сильную задержку роста опухоли при использовании 212Pb-p-SCN-Bn-TCMC-PSMA-лиганда 1 по сравнению с 177Lu-PSMA-617 даже несмотря на то, что оценки дозы излучения показывают, что доза излучения в пересчете на Гр, которую доставляет 177Lu-PSMA-617, является в 17 раз выше. Таким образом, радиобиологическая эффективность (RBE) 212Pb-p-SCN-Bn-TCMC-PSMA-лиганда 1 по отношению к 177Lu-PSMA-617 составляла не менее 17. Такая высокая радиобиологическая эффективность для терапевтических уровней излучателя альфа-частиц была весьма неожиданной, так как обычно ожидается, что RBE для излучателей альфа-частиц по отношению к излучателям бета-частиц будет составлять 2–5.
Ссылки
An efficient chelator for complexation of thorium-227.
Ramdahl T, Bonge-Hansen HT, Ryan OB, Larsen S, Herstad G, Sandberg M, Bjerke RM, Grant D, Brevik EM, Cuthbertson AS
Bioorg Med Chem Lett. 2016 Sep 1; 26(17):4318-21.In Vitro and In Vivo Efficacy of a Novel CD33-Targeted Thorium-227 Conjugate for the Treatment of Acute Myeloid Leukemia.
Hagemann UB, Wickstroem K, Wang E, Shea AO, Sponheim K, Karlsson J, Bjerke RM, Ryan OB, Cuthbertson AS
Mol Cancer Ther. 2016 Oct; 15(10):2422-2431.
Chittenden SJ., A phase 1, open-label study of the biodistribution, pharmacokinetics, and dosimetry of 223Ra -dicloride in patinets with hormone-refractory prostate cancer and skeletal metastases. J Nucl Med 56: 1304-1309 (2015).
Kratochwil C et al., Targeted α-therapy of metastatic castration resistant prostate cancer with 225Ac-PSMA-617: Dosimetry estimate and empirical dose finding J Nucl Med 58: 1624-1631 (2017).
Kratochwil C et al., Targeted α-therapy of mCRPC: Dosimetry estimate of 213Bismuth-PSMA-617. Eur J Nucl Med Mol Imaging 45:31-37 (2018)
Huang SS, Heston WDW. Should Low Molecular Weight PSMA Targeted Ligands Get Bigger and Use Albumin Ligands for PSMA Targeting? Theranostics 7: (7) 1940-1941 (2017)
Choy CJ et al., 177Lu-Labeled Phosphoramidate-Based PSMA Inhibitors: The Effect of an Albumin Binder on Biodistribution and Therapeutic Efficacy in Prostate Tumor-Bearing Mice. Theranostics. 2017;7(7):1928–1939. doi:10.7150/thno.18719.
Lassmann, M et al., Therapy of ankylosing spondylitis with 224Ra-radium chloride:Dosimetry and risk considerations. Radiat Environ Biophys 41: 173-178 (2002).
ПУНКТЫ
1. Соединение X, где соединение X представляет собой производное мочевины, подходящее для нацеливания на клетки и ткани, экспрессирующие PSMA.
2. Комплекс, содержащий соединение X, связанное с 212Pb, 177Lu, 213Bi, 225Ac или 227Th, где соединение X представляет собой производное мочевины, подходящее для нацеливания на клетки и ткани, экспрессирующие PSMA.
3. Соединение по п. 1 или комплекс по п. 2, где соединение X связано с 212Pb или 227Th с помощью хелатирующего фрагмента Z.
4. Соединение или комплекс по любому из пп. 1–3, где хелатирующий фрагмент Z выбран из группы, состоящей из ациклических хелаторов, циклических хелаторов, криптандов, краун-эфиров, порфиринов или циклических или нециклических полифосфонатов, DOTMP, EDTMP, бисфосфоната, DOTA, производного DOTA, такого как p-SCN-Bn-DOTA, памидроната, конъюгированного с DOTA, TCMC, производного TCMC, такого как p-SCN-Bn-TCMC, памидроната, конъюгированного с TCMC, DOTA, конъюгированной с антителом, TCMC, конъюгированного с антителом, HBED-CC, NOTA, NODAGA, TRAP, NOPO, PCTA, DFO, DTPA, CHX-DTPA, AAZTA, DEDPA и оксо-Do3A.
4. Соединение или комплекс по любому из пп. 1–4, где линкер представляет собой DOTA или производное DOTA.
5. Соединение или комплекс по любому из пп. 1–4, где линкер представляет собой производное DOTA, такое как p-SCN-Bn-DOTA.
6. Соединение или комплекс по любому из пп. 1–4, где линкер представляет собой TCMC или производное TCMC.
7. Соединение или комплекс по любому из пп. 1–4 или п. 6, где линкер представляет собой производное TCMC, такое как p-SCN-Bn-TCMC.
8. Соединение или комплекс по любому из пп. 1–7, где линкер представляет собой октадентатный гидроксипиридинон-содержащий лиганд, такой как 3,2-HOPO.
9. Соединение или комплекс по любому из пп. 1–8, где соединение X, связанное с хелатирующим фрагментом Z, определено формулой I:
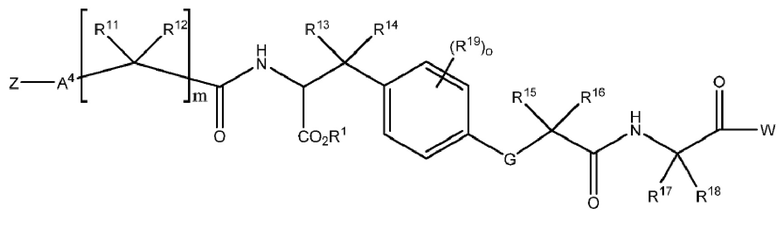
формула I,
или его фармацевтически приемлемая соль,
где
W представляет собой нацеливающийся на PSMA лиганд;
A4 представляет собой связь или двухвалентный связывающий фрагмент, содержащий 1–10 атомов углерода в цепи, кольце или их комбинации, где по меньшей мере один атом углерода необязательно заменен на О, -NR3- или -С(О)-;
G представляет собой C=O, C=S, C-NH2 или C-NR3;
R1 представляет собой водород или защитную группу для карбоксикислотной группы;
R3 выбран из группы, состоящей из водорода, алкила, циклоалкила, гетероциклоалкила, арила, алкиларила и гетероарила;
каждый из R11, R12, R13, R14, R15 и R16 независимо представляет водород, алкил, алкоксил, или
каждый из R17 и R18 независимо представляет водород, алкил, арил или алкиларил;
R19 выбран из группы, состоящей из алкила, алкоксила, галогенида, галогеналкила и
CN;
m представляет собой целое число от 1 до 6; и
o представляет собой целое число от 0 до 4, при этом если o больше 1, то каждый R19 является одинаковым или различается.
10. Соединение или комплекс по любому из пп. 1–9 или его фармацевтически приемлемая соль, где
A4 представляет собой связь, (CH2)n, -HC(O)-, -(OCH2CH2)n-, -(HCH2CH2)n-, -H(CO)CH2-, -HC(О)CH2(OCH2CH2)n- или -HC(О)CH2(HCH2CH2)n-; и
L представляет собой связь, (CH2)n, -(OCH2CH2)n-, -(HCH2CH2)n- или -C(О)(CH2)n-;
при этом n независимо равняется 1, 2 или 3.
11. Соединение или комплекс по любому из пп. 1–10 или его фармацевтически приемлемая соль, где A4 представляет собой связь, -(OCH2CH2)n- или -HC(О)CH2(OCH2CH2)n-; и
L представляет собой связь или -(OCH2CH2)n-;
при этом n независимо равняется 1 или 2.
12. Соединение или комплекс по любому из пп. 1–11 или его фармацевтически приемлемая соль, где
W характеризуется структурой:

где каждый из R20 и R21 независимо представляет собой аминокислотный остаток, связанный посредством своей аминогруппы с соседней группой -C(O)-.
13. Соединение или комплекс по любому из пп. 1–12 или его фармацевтически приемлемая соль, где
W характеризуется структурой:

где R представляет собой водород или защитную группу для карбоксикислотной группы.
14. Соединение или комплекс по любому из пп. 1–13 или его фармацевтически приемлемая соль, характеризующиеся структурой:

или его фармацевтически приемлемая соль,
где R17 представляет собой арил.
15. Соединение или комплекс по любому из пп. 1–14 или его фармацевтически приемлемая соль, где комплекс представляет собой PSMA-617:
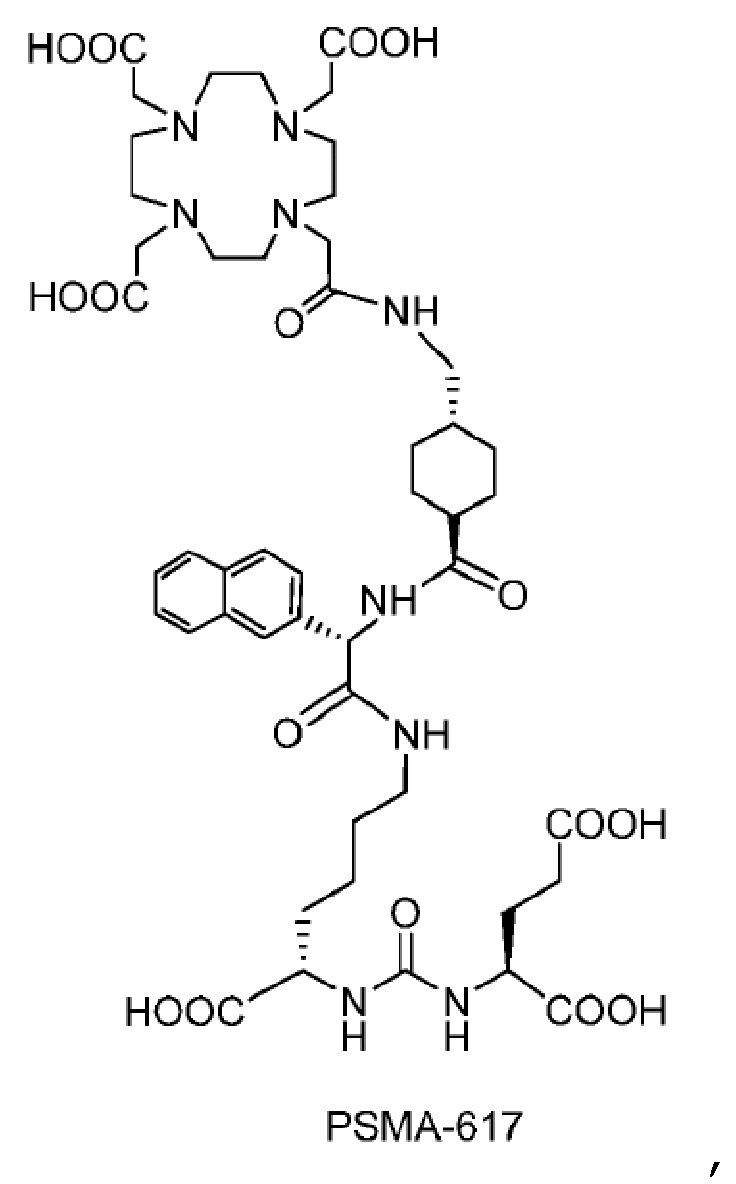
при этом радионуклид, такой как 212Pb, может быть связан/хелатирован с четырьмя N.
16. Соединение или комплекс п. 15, где DOTA-звено заменено на TCMC-звено.
17. Соединение или комплекс по пп. 15–16, где DOTA представляет собой p-SCN-Bn-DOTA и TCMC представляет собой p-SCN-Bn-TCMC.
18. Соединение или комплекс по пп. 15–17, где p-SCN-Bn-DOTA или p-SCN-Bn-TCMC связаны с С-атомом остова производного мочевины (PSMA).
19. Соединение или комплекс по пп. 15–18, где соединение представляет собой связанные посредством C-остова p-SCN-Bn-DOTA или p-SCN-Bn-TCMC:

где Z представляет собой:

и где X представляет собой -OH или NH2.
20. Соединение или комплекс по пп. 15–19, где соединение представляет собой связанные посредством C-остова p-SCN-Bn-DOTA или p-SCN-Bn-TCMC:
 ,
,
где X представляет собой -OH или NH2.
21. Соединение или комплекс по пп. 15–20, где соединение представляет собой связанную посредством C-остова p-SCN-Bn-DOTA, то есть p-SCN-Bn-DOTA-PSMA-лиганд 2:
 .
.
22. Соединение или комплекс по пп. 15–20, где соединение представляет собой связанный посредством C-остова p-SCN-Bn-TCMC, то есть p-SCN-Bn-TCMC-PSMA-лиганд 1:
 .
.
23. Нацеливающееся на PSMA производное мочевины, содержащее группу TCMC для хелатирования 212Pb.
24. Нацеливающееся на PSMA производное мочевины, содержащее HOPO для хелатирования 227Th.
25. Нацеливающееся на PSMA производное мочевины, содержащее DOTA, меченное либо 212Pb, либо 227Th.
26. Фармацевтическая композиция, содержащая соединение или комплекс по пп. 1–21 и/или нацеливающееся на PSMA производное мочевины по пп. 15–17 и разбавитель, носитель, поверхностно-активное вещество и/или вспомогательное вещество.
27. Радиофармацевтическая композиция по п. 26, дополнительно содержащая 224Ra.
28. Радиофармацевтическая композиция по любому из пп. 26–27, где радиоактивность составляет от 100 кБк до 100 МБк на дозу.
29. Радиофармацевтическая композиция по любому из пп. 26–28, где количество 224Ra и 212Pb находится в радиоактивном равновесии.
30. Радиофармацевтическая композиция по любому из пп. 26–29, где отношение активности (МБк) 212Pb к 224Ra составляет от 0,5 до 2, как например, 0,8–1,5, или, как например, 0,8–1,3, или предпочтительно, как например, 0,9–1,15.
31. Набор, содержащий:
- первый флакон, содержащий радиофармацевтическую композицию по любому из пп. 26–30, и
- второй флакон, содержащий нейтрализующий раствор для регулирования рН и/или изотоничности радиофармацевтической композиции перед введением пациенту.
32. Набор, содержащий:
- первый флакон, содержащий раствор, содержащий 224Ra, 212Pb и/или 227Th;
- второй флакон, содержащий комплексообразующее средство, выбранное из группы, состоящей из ациклических хелаторов, циклических хелаторов, криптандов, краун-эфиров, порфиринов или циклических или нециклических полифосфонатов, DOTMP, EDTMP, производных бисфосфоната, DOTA производного DOTA, памидроната, конъюгированного с DOTA, TCMC, производного TCMC, памидроната, конъюгированного с TCMC, DOTA, конъюгированной с антителом, TCMC, конъюгированного с антителом, HBED-CC, NOTA, NODAGA, TRAP, NOPO, PCTA, DFO, DTPA, CHX-DTPA, AAZTA, DEDPA и оксо-Do3A или соединения по любому из пп. 1–21,
при этом комплексообразующее средство способно образовывать комплекс с образующимся из 224Ra дочерним нуклидом, таким как 212Pb, и при этом комплексообразующее средство не образует комплекс с 224Ra в фармацевтическом растворе; и
- необязательно инструкции по смешиванию содержимого первого флакона и второго флакона, тем самым получая фармацевтическую композицию, готовую для введения пациенту через промежуток длительностью от 1 минуты до 12 часов после смешивания.
33. Набор по любому из пп. 31–32, где набор предназначен для использования в качестве лекарственного препарата.
34. Радиофармацевтическая композиция по любому из пп. 18–22 для применения в качестве лекарственного препарата.
35. Радиофармацевтическая композиция по любому из пп. 18–22 для применения в лечении заболевания скелета.
36. Радиофармацевтическая композиция для применения по п. 35, где заболевание скелета выбрано из группы, состоящей из скелетных метастазов при формах рака молочной железы, предстательной железы, почек, легкого, кости или множественной миеломе или не относящихся к раку заболеваний, вызывающих нежелательную кальцификацию, включая анкилозирующий спондилит.
37. Радиофармацевтическая композиция для применения по любому из пп. 34–36, где раствор вводится в дозе в диапазоне 50–150 кБк на кг массы тела, как например 50–100 кБк на кг массы тела.
38. Способ лечения злокачественного или незлокачественного заболевания путем введения радиофармацевтической композиции, описанной в пп. 26–30, нуждающемуся в этом индивидууму.
39. Способ получения радиофармацевтической композиции по любому из пп. 26–30, включающий:
а) получение первого раствора, где количество 224Ra и 212Pb находится в радиоактивном равновесии;
b) получение второго раствора, содержащего комплексообразующее средство, которое выбрано из группы, состоящей из ациклических хелаторов, циклических хелаторов, криптандов, краун-эфиров, порфиринов или циклических или нециклических полифосфонатов, DOTMP, EDTMP, бисфосфоната, DOTA производного DOTA, памидроната, конъюгированного с DOTA, TCMC, производного TCMC, памидроната, конъюгированного с TCMC, DOTA, конъюгированной с антителом, TCMC, конъюгированного с антителом, HBED-CC, NOTA, NODAGA, TRAP, NOPO, PCTA, DFO, DTPA, CHX-DTPA, AAZTA, DEDPA и оксо-Do3A, при этом комплексообразующее средство способно образовывать комплекс с образующимся из 224Ra дочерним нуклидом, таким как 212Pb, и при этом комплексообразующее средство не образует комплекс с 224Ra; и
c) смешивание первой композиции и второй композиции, тем самым получая фармацевтическую композицию по любому из пп. 26–30.
| название | год | авторы | номер документа |
|---|---|---|---|
| РАДИОФАРМАЦЕВТИЧЕСКИЕ РАСТВОРЫ С ПРЕДПОЧТИТЕЛЬНЫМИ СВОЙСТВАМИ | 2016 |
|
RU2741794C2 |
| Лиофилизат на основе лигандов к простат-специфическому мембранному антигену (ПСМА) для приготовления радиофармацевтической композиции в форме раствора для инъекций для лечения рака предстательной железы, радиофармацевтическая композиция на ее основе для лечения рака предстательной железы и способ приготовления радиофармацевтической композиции | 2023 |
|
RU2817970C1 |
| ПСМА-ТАРГЕТНОЕ СОЕДИНЕНИЕ И ЕГО КОМПЛЕКС С РАДИОНУКЛИДАМИ ДЛЯ ТЕРАНОСТИКИ ОПУХОЛЕЙ, ЭКСПРЕССИРУЮЩИХ ПСМА | 2022 |
|
RU2803734C1 |
| Комплексные соединения, содержащие в своем составе радионуклид Th, а также бисфосфонатный фрагмент, способы их получения, а также потенциальное применение в качестве действующего вещества в составе остеотропного радиофармацевтического лекарственного препарата | 2020 |
|
RU2767567C1 |
| Способ повышения уровней экспрессии антигенов | 2014 |
|
RU2681953C2 |
| Новые радиоиммуноконъюгаты и их применения | 2011 |
|
RU2664475C1 |
| СОЕДИНЕНИЕ, ЦЕЛЕНАПРАВЛЕННО ВОЗДЕЙСТВУЮЩЕЕ НА ПРОСТАТСПЕЦИФИЧЕСКИЙ МЕМБРАННЫЙ АНТИГЕН, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ЕГО ПРИМЕНЕНИЕ | 2022 |
|
RU2832300C2 |
| НОВЫЕ РАДИОИММУНОКОНЪЮГАТЫ И ИХ ПРИМЕНЕНИЯ | 2011 |
|
RU2560587C9 |
| РАДИОТЕРАПЕВТИЧЕСКИЕ ЧАСТИЦЫ И СУСПЕНЗИИ | 2016 |
|
RU2770073C2 |
| СПОСОБ ПОЛУЧЕНИЯ КОМПЛЕКСА ПСМА-ТАРГЕТНОГО СОЕДИНЕНИЯ НА ОСНОВЕ МОЧЕВИНЫ Lu-PS-161 И КОМПЛЕКС | 2023 |
|
RU2808636C1 |

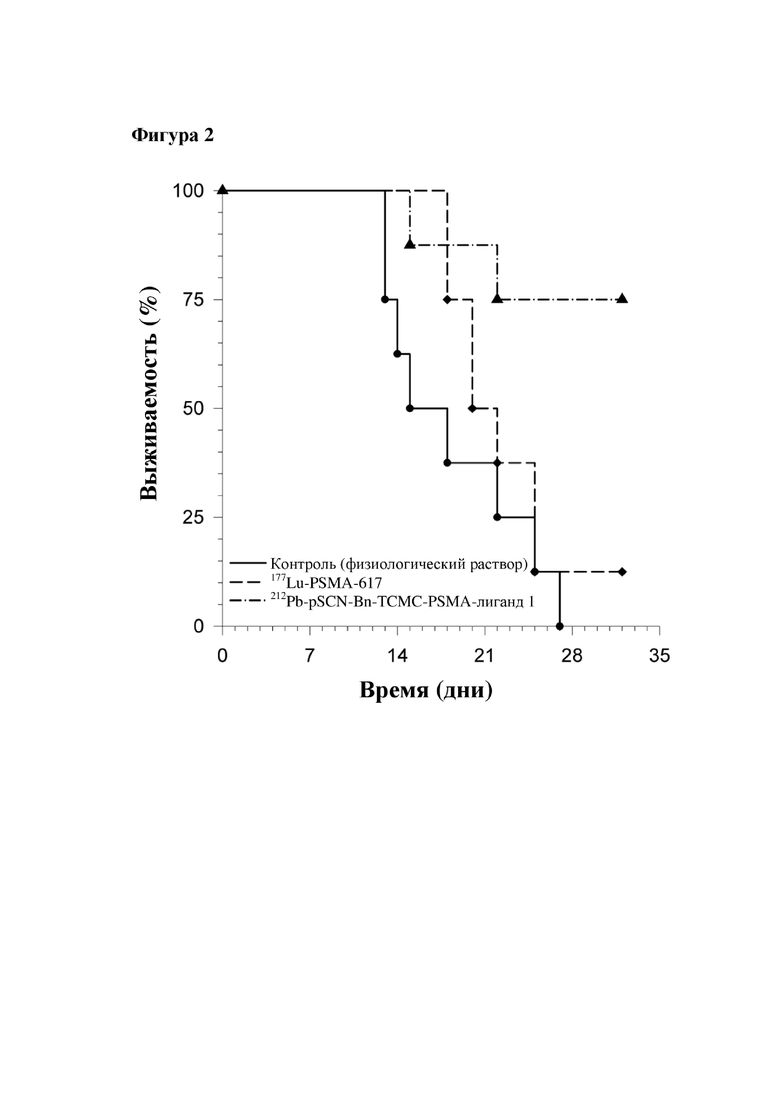
Настоящее изобретение относится к соединению, содержащему направленное на PSMA звено и хелатирующее звено, где направленное на PSMA звено связано посредством углеродного остова с хелатирующим звеном и где соединение характеризуется формулой

где X представляет собой -NH2 или -ОН. Также предложены комплекс для использования в радиолигандной терапии, содержащий вышеуказанное соединение, связанное в комплекс с радионуклидом, выбранным из группы, состоящей из 212Pb, 212Bi, 213Bi, 225Ас или 227Th, фармацевтическая композиция, содержащая комплекс, применение фармацевтической композиции, способ лечения заболевания, характеризующегося экспрессией PSMA, и наборы. Изобретение позволяет получить комплексные соединения с высокой радиобиологической эффективностью, которые могут применяться для лечения заболевания, характеризующегося экспрессией PSMA. 8 н. и 10 з.п. ф-лы, 2 ил., 7 табл., 17 пр.
1. Соединение, содержащее направленное на PSMA звено и хелатирующее звено, где направленное на PSMA звено связано посредством углеродного остова с хелатирующим звеном и где соединение характеризуется формулой
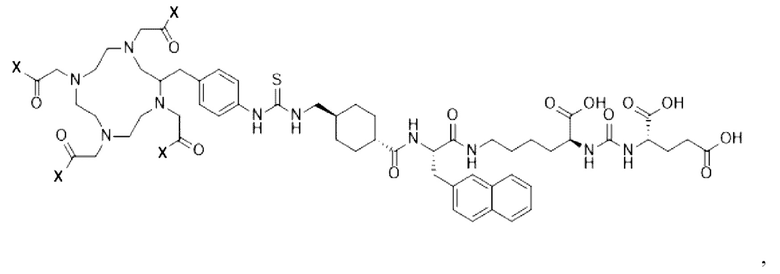
где X представляет собой -NH2 или -ОН.
2. Соединение по п. 1, где соединение представляет собой

p-SCN-Bn-TCMC-PSMA-лиганд 1.
3. Соединение по п. 1, где соединение представляет собой
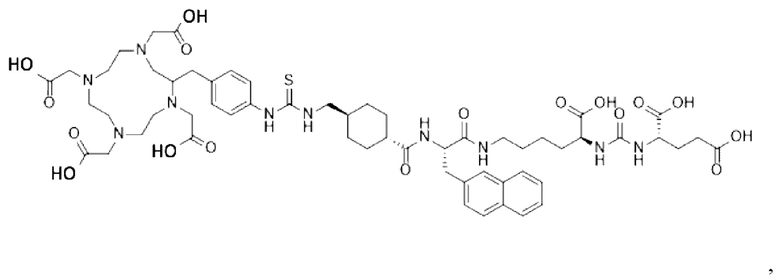
p-SCN-Bn-DOTA-PSMA-лиганд 2.
4. Комплекс для использования в радиолигандной терапии, содержащий соединение по любому из пп. 1-3, связанное в комплекс с радионуклидом, выбранным из группы, состоящей из 212Pb, 212Bi, 213Bi, 225Ас или 227Th.
5. Комплекс по п. 4, где соединение по п. 2 (p-SCN-Bn-TCMC-PSMA-лиганд 1) связано в комплекс с 212Pb.
6. Комплекс по п. 4, где соединение по п. 3 (p-SCN-Bn-DOTA-PSMA-лиганд 2) связано в комплекс с 212Pb, 212Bi, 213Bi, 225Ас или 227Th.
7. Фармацевтическая композиция для использования в радиолигандной терапии, направленной против PSMA-экспрессирующего рака предстательной железы, содержащая комплекс по любому из пп. 4-6 и разбавитель, носитель, поверхностно-активное вещество и/или вспомогательное вещество.
8. Фармацевтическая композиция по п. 7, дополнительно содержащая 224Ra.
9. Фармацевтическая композиция по п. 8, где количество 224Ra и 212Pb находится в радиоактивном равновесии.
10. Фармацевтическая композиция по любому из пп. 7-9, где отношение активности (МБк) 212Pb к 224Ra составляет от 0,5 до 2, как например 0,8-1,5, или, как например, 0,8-1,3, или предпочтительно, как например, 0,9-1,15.
11. Фармацевтическая композиция по любому из пп. 7-10, где композиция вводится в дозе, предусматривающей радиоактивность от 100 кБк до 100 МБк на дозу.
12. Применение фармацевтической композиции по любому из пп. 7-11 в качестве лекарственного препарата для использования в радиолигандной терапии, направленной против PSMA-экспрессирующего рака предстательной железы.
13. Применение фармацевтической композиции по любому из пп. 7-11 в лечении характеризующегося экспрессией PSMA заболевания, в том числе заболевания мягких тканей и скелета.
14. Применение по п. 13, где заболевание скелета выбрано из группы, состоящей из скелетных метастазов при формах рака молочной железы, предстательной железы, почек, легкого, кости или множественной миеломе.
15. Применение по любому из пп. 12-14, где раствор вводится в дозе в диапазоне 50-150 кБк/кг массы тела.
16. Способ лечения заболевания, характеризующегося экспрессией PSMA, путем введения фармацевтической композиции по любому из пп. 7-11 нуждающемуся в этом индивидууму.
17. Набор, содержащий:
- первый флакон, содержащий фармацевтическую композицию по любому из пп. 7-11, и
- второй флакон, содержащий нейтрализующий раствор для регулирования рН и/или изотоничности фармацевтической композиции перед введением пациенту.
18. Набор для получения комплекса, содержащий:
- первый флакон, содержащий раствор, содержащий 224Ra, 212Pb и/или 227Th;
- второй флакон, содержащий соединение по любому из пп. 1-3.
| KRATOCHWIL C | |||
| et al., Targeted Alpha Therapy of mCRPC with 225Ac-PSMA-617: Dosimetry Estimate and Empirical Dose Finding, The Journal of Nuclear Medicine, 13.04.2017, p | |||
| Двойная пневматическая шина | 1923 |
|
SU1624A1 |
| SATHEKGE M | |||
| et al., 213Bi-PSMA-617 targeted alpha-radionuclide therapy in metastatic castration-resistant prostate cancer, European Journal of Nuclear Medicine and | |||
Авторы
Даты
2023-05-03—Публикация
2018-12-13—Подача