Изобретение относится к области медицинской химии, а именно, к новому органическому соединению, конкретно к 2-((1H-1,2,4-триазо-3-ил)тио)-3-метил-6-(проп-1-ен-2-ил)циклогекс-3-ен-1-олу, описываемому формулой 1,
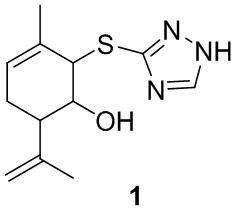
которое может применяться для лечения болезни Паркинсона.
Болезнь Паркинсона - это тяжелое прогрессирующее заболевание центральной нервной системы, характеризующееся тремором, гипокинезией, мышечной ригидностью и постуральной неустойчивостью. Главной причиной болезни и проявляющихся симптомов является необратимая гибель дофаминовых нейронов, преимущественно, в черной субстанции мозга, ведущая к дефициту содержания дофамина в головном мозге и разбалансировке нейромедиаторных систем [1]. Чаще всего болезнь Паркинсона поражает людей в пожилом возрасте - в 55-65 лет. Однако известны случаи, когда болезнь диагностировалась и у молодых людей в возрасте 30-40 лет. Существует и так называемая ювенильная форма, при которой заболевание поражает подростков в возрасте до 20 лет.
В настоящее время нет лекарственных средств, способных предотвратить или хотя бы замедлить потерю дофаминовых нейронов, и главной задачей терапии является купирование симптомов, позволяющее добиться приемлемого качества жизни в течение максимально длительного времени. Для лечения болезни Паркинсона чаще всего применяются средства, в состав которых входит предшественник дофамина L-ДОФА (леводопа). Эти средства используются как заместительная терапия, т.к. патогенез развития данного заболевания связан с прогрессирующим разрушением и гибелью нейронов, продуцирующих нейромедиатор дофамин, что приводит к резкому снижению содержания дофамина в головном мозге. Недостатками препаратов, содержащих L-ДОФА, являются [2,3]: 1)недостаточно высокая эффективность; 2) наличие большого количества побочных эффектов (анорексия, рвота, тахикардия, дискинезия, психические нарушения и т.д.); 3) колебания реакции на препарат, заключающиеся во флуктуации двигательных симптомов (синдром «включения-выключения»); 4) L- ДОФА не останавливает прогрессирование заболевания и в какой-то момент наступает стадия, когда из-за побочных эффектов невозможно подобрать эффективную дозу.
Для снижения дозы и уменьшения побочных эффектов L-ДОФА обычно комбинируют с другими препаратами: ингибиторы периферической допа-декарбоксилазы (карбидопа), средства, снижающие стимулирующее действие кортикальных глутаматных рецепторов, которое развивается на фоне снижения уровня дофамина (мидантан), либо агонисты дофаминовых рецепторов (ропинирол), ингибиторы МАО-В (селегин) и центральные холиноблокирующие средства, которые, однако, не устраняют полностью указанные недостатки [2, 3], а без применения L-ДОФА на поздних стадиях развития болезни эти препараты недостаточно эффективны.
Таким образом, поиск новых высокоэффективных и низкотоксичных противопаркинсонических средств продолжает оставаться актуальным в настоящее время.
Ранее нами была продемонстрирована высокая противопаркинсоническая активность 3-метил-6-(проп-1-ен-2-ил)циклогекс-3-ен-1,2-диола 2, который в дозе 20 мг/кг устранял симптомы паркинсонического синдрома, вызванного введением мышам нейротоксина МФТП [4]. Весьма желательным является повышение активности, то есть снижение действующей дозы.
Задача, на решение которой направлено изобретение, заключается в создании нового соединения, обладающего высокой противопаркинсонической активностью и имеющего потенциал замедлять прогрессирование заболевания.
Поставленная задача решается использованием в качестве противопаркинсонического средства соединения 1

Соединение 1 может быть получено из 3-метил-6-(проп-1-ен-2-ил)циклогекс-3-ен-1,2-диола 2 в соответствии со Схемой 1 через предварительное образование ацетата 3 и эпоксида 4.
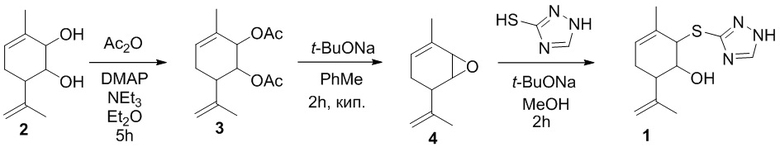
Схема 1.
Исходное соединение 2 может быть синтезировано исходя из широко распространенного в растительном сырье монотерпена α-пинена с использованием доступных реагентов [5], или другими способами (например, из карвона в соответствии с работой [4]) (Схема 2).

Схема 2.
Способность соединения поддерживать дофаминовые нейроны in vitro исследовалась на нейронах среднего мозга, выделенных из эмбрионов мышей. Дофаминовые нейроны метили антителами, специфичными к ключевому ферменту синтеза дофамина, тирозингидроксилазе (TH), визуализировали с помощью системы Cell Insight и подсчитывали с помощью программного обеспечения Cell Profiler. Показано (Фиг. 1), что соединение 1 в дозе 1 нМ способствует выживанию культивируемых эмбриональных дофаминовых нейронов на уровне препарата сравнения глиального нейротрофического фактора GDNF в дозе 50 нг/мл.
Для изучения противопаркинсонической активности in vivo широко используется нейротоксин 1-метил-4-фенил-1,2,3,6-тетрагидропиридин (МФТП), при парентеральных способах введения вызывающий гибель дофаминовых нейронов головного мозга, и, как следствие, развитие паркинсонического синдрома у людей, обезьян и грызунов [6]. Индукцию паркинсонического синдрома осуществляли четырехкратным внутрибрюшинным введением МФТП в дозе 20 мг/кг самцам мышей линии C57Bl/6. Соединение 1 вводили мышам перорально в дозе 1 мг/кг через 24 часа после последней инъекции МФТП, после чего была изучена способность соединения 1 устранять симптомы экспериментального паркинсонизма в поведенческих тестах «на вешалке» и «открытое поле».
Тест «на вешалке» широко используется для оценки параметров двигательно-координационной активности у мышей. Животных подвешивали передними лапами в центре нижней горизонтальной перекладины вешалки. Положение тела животного наблюдали в течение 120 сек и оценивали по шкале от 0 до 7, где 0 указывает на наихудший возможный результат (падение в течение 10 сек), а 7 - наилучший возможный результат (активное движение до вершины вешалки). Кроме того, состояние моторной системы характеризовалось измерением времени активного движения. Мыши контрольной группы быстрее достигают вершины по сравнению с животными c экспериментальным паркинсонизмом. За первые 60 с теста все мыши контрольной группы (10 из 10 мышей) достигали вершины вешалки и получали 7 баллов. В сравнении, только 2 мыши с индуцированным паркинсонизмом из группы МФТП достигали вершины, а средний балл к 60-ой секунде был всего 3.6±1.0 (P = 0.02) (Фиг. 2А). В то же время, соединение 1 значительно улучшает балл по сравнению с группой МФТП до 6.7±0.2 (P = 0.0324). Кроме того, в группе МФТП было зафиксировано 4 падения к 60-ой и еще 2 падения к 120-ой секунде теста. В других группах падений не было. МФТП влияет на двигательную активность мышей, сокращая общее время активных движений и увеличивая время замирания. Мыши контрольной группы были на 46% более активны, чем мыши с МФТП-индуцированным паркинсонизмом. Воздействие соединением 1 на мышей с паркинсонизмом увеличивает время движения на 40%. (Фиг. 2Б).
В эксперименте «открытое поле» было установлено, что введение нейротоксина МФТП приводит к достоверному снижению двигательной активности у мышей. В тоже время, введение соединения 1 в дозе 1 мг/кг снижает моторный дефицит и увеличивает двигательную активность на 20% относительно мышей с индуцированным паркинсонизмом (Фиг. 3).
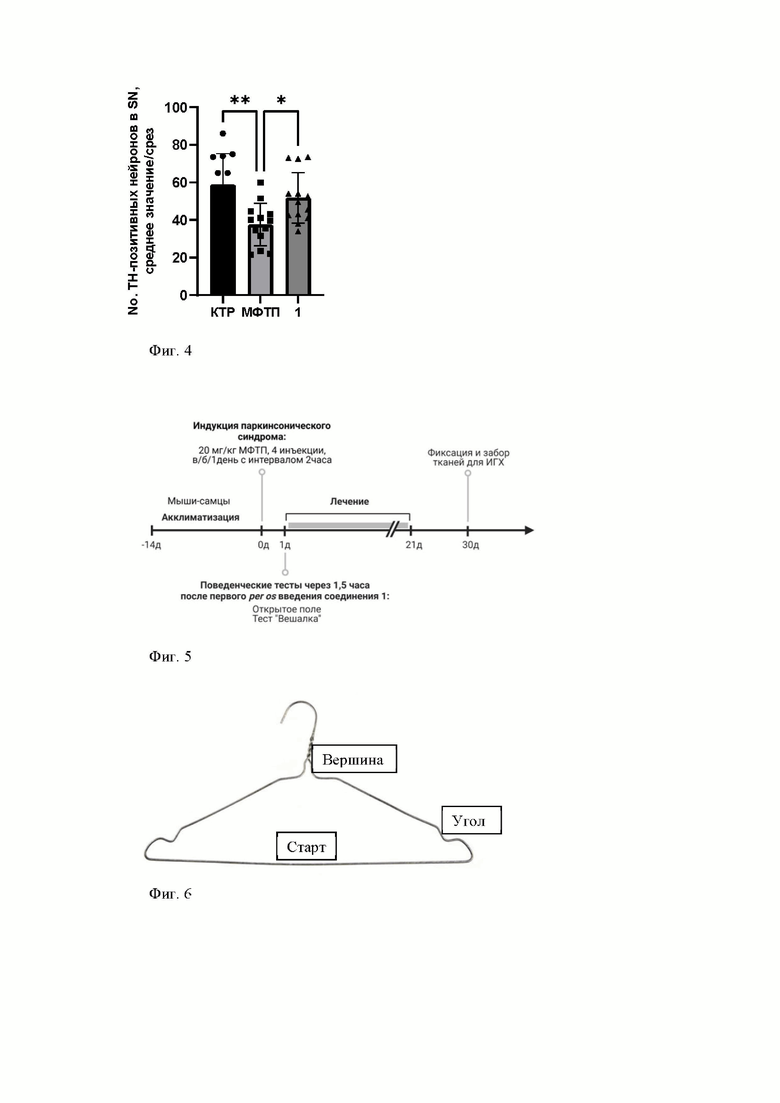
Для оценки способности соединения 1 восстанавливать поврежденные нейроны, его вводили мышам с индуцированным паркинсоническим синдромом в течение 21 дня (5 ежедневных введений в неделю в течение 3 недель). Через 30 дней после введения МФТП мышей умерщвляли и извлекали головной мозг. Оказалось, что введение МФТП уменьшает количество TH-позитивных нейронов в черной субстанции головного мозга (Фиг. 4). Введение соединения 1 в дозе 1 мг/кг мышам с индуцированным МФТП паркинсоническим синдромом значительно увеличивало количество TH-позитивных нейронов по сравнению с мышами, получавшими МФТП (P = 0.04), подтверждая потенциал соединения 1 замедлять прогрессирование болезни Паркинсона.
Исследование острой токсичности проводили по методу Кербера, среднесмертельная доза для соединения 1 составила 234 мг/кг.
Таким образом, можно заключить, что соединение 1 обладает высокой противопаркинсонической активностью, устраняя двигательные симптомы паркинсонического синдрома и способствуя восстановлению поврежденных дофаминовых нейронов головного мозга мышей, и может, после проведения соответствующих испытаний, использоваться в чистом виде или в качестве компонента новых высокоэффективных лекарственных форм для лечения болезни Паркинсона.
Изобретение иллюстрируется следующими примерами.
Пример 1. Синтез соединения 1
Смесь 0.8 г (8.3 ммоль) трет-бутоксида натрия и 10 мл толуола нагревали до температуры кипения растворителя на глицериновой бане. После этого добавили по каплям в реакционную смесь раствор 0.53 г (2.1 ммоль) диацетата (1R,2R,6S)-3-метил-6-(проп-1-ен-2-ил)циклогекс-3-ен-1,2-диола 3 в 5 мл толуола. Смесь перемешивали при кипячении с обратным холодильником при 110°С в течение 2 часов. Затем добавили 30 мл гексана, отфильтровали выпавший осадок, растворитель упарили в вакууме. Получили (1S,5S,6R)-2-метил-5-(проп-1-ен-2-ил)-7-оксабицикло[4.1.0]гепт-2-ен 4. Добавили 0.2 г (2.06 ммоль) 1Н-1,2,4-триазол-3-тиола к раствору 0.198 г (2.06 ммоль) трет-бутоксида натрия в 10 мл метанола. Через 5 мин к смеси при перемешивании добавляли раствор 0.25 г (1.68 ммоль) соединения 4 в 10 мл метанола. Реакционную смесь перемешивали в течение 2 часов при комнатной температуре. Затем растворитель отогнали, и остаток экстрагировали этилацетатом (3×10 мл). Органическую фазу сушили над Na2SO4, отфильтровали и упарили от растворителя в вакууме. Получили 0.253 г (выход 60%) соединения 1.
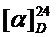 =-34.6(c=0.67, CHCl3).1H-NMR (600 MHz, CDCl3, δ, ppm): 1.72 (3H, s, CH3-10), 1.79 (3H, s, CH3-7), 2.0-2.09 (1H, m, CH2-3), 2.21-2.34 (1H, m, CH2-3), 2.60 (1H, dd, J(4a,3a)=11.9 Hz, J(4a,3e)=5.2 Hz, CH-4), 4.11 (1H, br.s, CH-6), 4.27 (1H, s, CH-5), 4.82 (1H, s, CH2-9), 4.87 (1H, s, CH2-9), 5.69 (1H, s, CH-2), 8.23 (1H, s, CH-12).13C-NMR (150 MHz, CDCl3, δ, ppm): 145.53 (C, C-11), 145.48 (C, C-8), 127.22 (CH, C-12), 127.18 (C, C-1), 111.25 (CH2, C-9), 70.57 (CH, C-5), 52.42 (CH, C-6), 38.80 (CH, C-4), 24.47 (CH2, C-3), 22.05 (CH3, C-10), 21.91 (CH3, C-7). HR-MS: 251.1085 (M+, C12H17O1N332S1+; calc. 251.1087).
=-34.6(c=0.67, CHCl3).1H-NMR (600 MHz, CDCl3, δ, ppm): 1.72 (3H, s, CH3-10), 1.79 (3H, s, CH3-7), 2.0-2.09 (1H, m, CH2-3), 2.21-2.34 (1H, m, CH2-3), 2.60 (1H, dd, J(4a,3a)=11.9 Hz, J(4a,3e)=5.2 Hz, CH-4), 4.11 (1H, br.s, CH-6), 4.27 (1H, s, CH-5), 4.82 (1H, s, CH2-9), 4.87 (1H, s, CH2-9), 5.69 (1H, s, CH-2), 8.23 (1H, s, CH-12).13C-NMR (150 MHz, CDCl3, δ, ppm): 145.53 (C, C-11), 145.48 (C, C-8), 127.22 (CH, C-12), 127.18 (C, C-1), 111.25 (CH2, C-9), 70.57 (CH, C-5), 52.42 (CH, C-6), 38.80 (CH, C-4), 24.47 (CH2, C-3), 22.05 (CH3, C-10), 21.91 (CH3, C-7). HR-MS: 251.1085 (M+, C12H17O1N332S1+; calc. 251.1087).
Пример 2. Нейропротекторный эффект соединения 1 на первичной культуре дофаминовых нейронов.
Культуру первичных дофаминовых (DA) нейронов получали из эмбрионов E13.5 мышей линии NMRI. Нужную часть среднего мозга иссекали под микроскопом (стереомикроскоп Olympus SZX10), поместив эмбрион в раствор Дульбекко (0.1 g/lMgCl2.6H2O, 0.1 g/lCaCl2, 8 g/lNaCl, 0.2 g/lKCl, 1.4 g/lNa2HPO4.2H2O, 0.2 g/lKH2PO4), содержащий 2% БСА. Далее кусочки ткани трижды промывали сбалансированным солевым раствором Хэнкса без Ca2+, Mg2+ (HBSS: Gibco, Life Technologies) и инкубировали в растворе трипсина с концентрацией 5 мг/мл в HBSS в течение 20 минут при 37°C. Ферментативную активность трипсина блокировали 50% эмбриональной бычьей сывороткой. Для снижения вязкости раствор также обрабатывали ДНКазой I (10 мг/мл). Диссоциацию клеток осуществляли механическим способом с помощью многократного пипетирования пипеткой Пастера из силиконизированного стекла. Клеточную суспензию центрифугировали, осадок клеток промывали 3 раза средой для культивирования [(Dulbecco's MEM/Nut mix F12 (Invitrogen/Gibco 21331-020), с добавлением заменителя сыворотки 1xN2 (Invitrogen/Gibco 17502-048), 33 мМ D -Глюкозы (Sigma G-8769), 0,5 мМ L-глютамина (Invitrogen/Gibco 25030-032) и 100 мкг/мл примоцина (InvivoGen)]. Полученный клеточных осадок ресуспендировали в культуральной среде и определяли количество живых клеток по исключению красителя трипанового синего с помощью автоматического счетчика клеток TC20 (BIO-RAD). В лунках 96-луночного планшета Costar, высверливали островок диаметром около 3 мм, который покрывали поли-L-орнитином (0.5 мг/мл в 0.15 М боратном буфере, рН 8.7, на ночь при 4°C). На этот островок высевали около 30 000 клеток, выделенных из среднего мозга эмбрионов мыши. Соединение 1 в концентрации 1 нМ и GDNF (Icosagen, 50 нг/мл) растворяли в культуральной среде, содержащей 1% ДМСО, и добавляли в лунки (в трех повторностях) в течение 1 ч после посева. Клетки инкубировали в течение 5 дней в инкубаторе для клеточных культур при 37°C. питательную среду заменяли свежей порцией через 2.5 дня после посева.
После 5-ти дней инкубации, клетки фиксировали 4% PFA в течение 20 минут и трижды промывали PBS с последующей пермеабилизацией 0,2% Triton X-100 в PBS в течение 15 минут. Неспецифические сайты связывания антител блокировали 5% лошадиной сывороткой в 0,2% Triton X-100 в PBS в течение 1 часа после чего клетки инкубировали в течение ночи при 4°C с антителом против тирозингидроксилазы (TH) (1:500 в блокирующем растворе, 50 Millipore Cat# MAB318 Lot# RRID:AB_2201528). Затем клетки трижды промывали PBS и инкубировали со вторичным антителом, конъюгированным с Alexa Fluor 688 (разведенном в блокирующем растворе 1:500), в течение 1 часа при комнатной температуре. Несвязавшиеся антитела отмывали PBS и окрашивали ядра клеток 0.2 мкг/мл 4',6-диамидино-2-фенилиндолом (DAPI) в PBS в течение 10 минут при комнатной температуре. Наконец, клетки трижды промывали PBS и хранили в PBS до визуализации не более 2 суток.
Клетки визуализировали с помощью Cell Insight CX5 High Content Screening (HCS) (Life Technologies). Изображения анализировали с использованием программного обеспечения для анализа изображений Cell Profiler (BROAD Institute). Соединение анализировали в трех повторностях в четырех независимых экспериментах.
Показано, что соединение 1 в дозе 1 нМ способствует выживанию культивируемых эмбриональных дофаминовых нейронов на уровне препарата сравнения GDNF в дозе 50 нг/мл.
Пример 3. Изучение противопаркинсонической активности соединения 1 in vivo.
Для исследования противопаркинсонической активности соединения 1 была использована фармакологическая модель болезни Паркинсона, индуцированная внутрибрюшинным введением нейротоксина МФТП, который разрушает дофаминовые нейроны головного мозга.
Эксперименты проводились на мышах-самцах линии С57В1/6 разделенных на группы по 8 животных в каждой. Индукцию паркинсонического синдрома осуществляли путем внутрибрюшинного введения МФТП в дозе 20 мг/кг (4 раза каждые 2 часа), группе интактного контроля вводили физраствор (КТР). Соединение 1 в дозе 1 мг/кг вводили перорально через 24 часа после последней инъекции нейротоксина (Фиг. 5).
Проявление моторного дефицита оценивали в тестах «открытое поле» и «вешалка» на следующий день через 1.5 часа после первого введения соединения 1 в дозе 1 мг/кг ).
Исследование животных в тесте «Открытое поле»
Тест «открытое поле» используют для оценки влияния потенциальных противопаркинсонических препаратов на двигательную и исследовательскую активность экспериментальных животных в условиях свободного перемещения в тестовой арене (TruScan, США) в течение 2 минут. Результаты экспериментов приведены на Фиг. 3.
В эксперименте было установлено, МФТП достоверно снижает двигательно-исследовательскую активность у мышей. В тоже время введение соединения 1 в дозе 1 мг/кг снижает моторный дефицит (Фиг. 3), что проявилось в достоверном увеличении двигательной активности на 20% относительно не леченных мышей с паркинсонизмом.
Моторный дефицит, вызванный введением нейротоксина, также оценивали с помощью теста «вешалка». Этот тест обычно используется для оценки силы и координации конечностей. Испытание проводили, как описано ранее [7] с некоторыми изменениями в системе начисления баллов.
Процедура тестирования: животное помещали передними лапами на середину нижней горизонтальной перекладины. Далее регистрировали перемещения животного в течение 120 с и оценивали по шкале от 0 до 7 баллов, учитывая расположение животного на ключевых элементах тестовой конструкции (Фиг. 6), следующим образом:
0 - животное упало в течение 10 с;
1 - висит на перекладине одной лапой;
2 - висит на перекладине двумя лапами;
3 - висит на перекладине тремя лапами;
4 - висит на всех четырех лапах;
5 - держится за перекладину четырьмя лапами и обвивает ее хвостом, пытаясь взобраться выше на перекладину;
6 - активное передвижение по нижней перекладине до угла вешалки;
7 - доходит до вершины вешалки.
Также оценивали общее время движения и моменты замирания в пределах 120 с и дополнительно регистрировали число упавших мышей в течение каждых 60 с.
Мыши контрольной группы быстрее достигают вершины по сравнению с животными с MФТП-индуцированным паркинсонизмом.
Все мыши без экспериментального паркинсонизма достигали вершины вешалки уже к 60-ой секунде эксперимента, за это же время только 2 мыши из 10 с экспериментальным паркинсонизмом достигали вершины. Оценка КТР мышей составила 7 баллов, тогда как у мышей, которым вводили только МФТП, оценка составила 3.6 ± 1.0 (P = 0.0202) (Фиг. 2А). В то же время соединение 1 значительно улучшало оценку по сравнению с группой МФТП до 6.7±0.2 (P = 0.0324). Кроме того, в группе МФТП было зарегистрировано 4 падения к 60-ой и еще 2 падения к 120-ой секунде теста. В других группах падений не было. МФТП влияет на двигательную активность мышей, сокращая общее время активных движений и увеличивая время замирания. Мыши контрольной группы (КТР) были на 46% более активны, чем мыши с МФТП-индуцированным паркинсонизмом. Воздействие соединением 1 на мышей с паркинсонизмом увеличивает время движения на 40%. (Фиг. 2Б).
Пример 4. Нейроресторативный эффект соединения 1 при МФТП-индуцированном паркинсонизме in vivo.
БП - это нейродегенеративное заболевание, характеризующееся типичными моторными проявлениями (тремор, постуральная нестабильность, брадикинезия), вызванными снижением концентрации дофамина в путамене, в результате дегенерации аксонов и тел дофаминовых нейронов в SN.
Поэтому следующим этапом в эксперименте было исследование влияния соединения 1 на дофаминовые нейроны в SN у мышей с МРТР-индуцированным паркинсонизмом. Схема эксперимента см. Пример 2.
Через 7 дней после последнего введения соединения 1 мышам вводили внутрибрюшинно хлоралгидрат в дозе 325 мг/кг и проводили транскардиальную перфузию раствором PBS, а затем 4% параформальдегидом в PBS в соответствии с [8], вынимали головной мозг, обрабатывали и заливали в парафиновые блоки на гистологическом комплексе Microm (Германия). Затем мозг, фиксированный PFA и залитый парафином, разрезали на срезы толщиной 5 мкм, который укладывали на предметные стекла для микроскопии (3-4 среза на стекло). В каждом 5-м из полученных гистологических препаратов с помощью ИГХ определяли уровень экспрессии TH. Срезы депарафинизировали с последующим высокотемпературным демаскированием антигена в цитратном буфере. Эндогенную пероксидазу инактивировали 30-минутной инкубацией срезов с 3% H2O2. Срезы блокировали 5% нормальной козьей сывороткой, а затем инкубировали с моноклональными антителами к ТН (1:2000, Millipore Cat# MAB318 Lot# RRID:AB_2201528) в течение ночи при +4°C. Срезы промывали и наносили биотинилированные лошадиные антимышиные вторичные антитела (1:200, кат. № BA-2001, Vector Laboratories, Burlingame, CA, USA) на 1 час с последующей промывкой. Срезы обрабатывали наборами для окрашивания ABC и DAB (Vector Laboratories, Калифорния, США) в соответствии с инструкциями производителя для визуализации связанных антител.
Срезы сканировали с помощью автоматизированного сканера (3DHistech, Будапешт, Венгрия; http://www.biocenter.helsinki.fi/bi/histoscanner/index.html). Считали количество ТН-позитивных нейронов в SN c помощью программного обеспечения ImageJ (NIH) отдельно для левой и правой стороны, и высчитывали среднее.
Введение МФТП уменьшает количество TH-позитивных нейронов в черной субстанции головного мозга на 36% (Фиг. 3). Введение соединения 1 в дозе 1 мг/кг мышам с МФТП-индуцированным паркинсонизмом значительно увеличивало количество TH-позитивных нейронов на 37%, восстанавливая количество нейронов до уровня интактного контроля.
Пример 5. Исследование острой токсичности.
Исследование острой токсичности соединения 1 проведено на мышах стока СD-1. Каждой группе внутрижелудочно вводили испытуемое соединение в дозах 100-500 мг/кг. Длительность наблюдений за животными составляла 10 суток с момента введения препаратов. Устанавливались дозы, при которых наступала 100% гибель животных, и при которых животные в 100% случаев выживали. Расчет LD50 и проводился по методу Кербера [9].
Вычисление острой токсичности по методу Кербера осуществляется с помощью формулы:
LD50 = LD100 - ∑ (z × d) / m
LD100- доза, при которой реагировали все животные (погибали);
z - половина суммы числа животных в опытах с испытанием двух последующих доз;
d - разница числового значения двух доз, стоящих рядом;
m - число животных в каждой группе.
Введение соединения 1 в дозе 100 мг/кг не привело к гибели животных, общее действие выражалось в незначительном угнетении центральной нервной системы. Введение соединения 1 в дозе 200 мг/кг вызвало гибель 40% животных в группе, а в дозе 150 мг/кг вызвало гибель 50% животных в группе в течение первых суток, остальные животные на протяжении эксперимента выжили. Доза, при которой наблюдалась 100% гибель животных (абсолютно смертельная доза (LD100)) составила 500 мг/кг (таб. 1).
LD50 соединения 1 = 234 мг/кг.
Исходя из классификации по степени воздействия на организм вредных веществ согласно ГОСТ 12.1.007-76 (Система стандартов безопасности труда (ССБТ). Вредные вещества. Классификация и общие требования безопасности), соединение 1, относится к 3-му классу умеренно опасных веществ.
Краткое описание чертежей:
Фиг. 1. Влияние соединения 1 на выживаемость первичных дофаминовых нейронов среднего мозга. Данные представлены как среднее значение ± стандартная ошибка среднего, n=4-10 на группу, ** P< 0.01 в сравнении с группой интактного контроля (КТР), ANOVA с Dunnett'spost-hoc test
Фиг. 2. Влияние соединения 1 на моторную координацию мышей с МФТП-индуцированным паркинсонизмом: оценивали баллы по шкале от 0 до 7 (A); продолжительность двигательной активности (Б). Данные представлены как среднее значение ± стандартная ошибка среднего. N = 10 мышей на группу. * P<0.05, ** P<0.01 по сравнению с группой МФТП, ANOVA с Dunnett's post-hoc test
КТР- контрольная группа (мыши без паркинсонизма)
Фиг. 3. Влияние соединения 1 на время двигательной активности у мышей с МФТП-индуцированным паркинсонизмом в тесте «открытое поле». Данные представлены в виде среднего значения ± стандартная ошибка среднего, N = 10. *P <0.05, ***Р< 0.001 по сравнению с группой МФТП, ANOVA с Dunnett's post-hoc test
Фиг. 4. Влияние соединения 1 на количество ТН-позитивных клеток в SN у мышей с МФТП-индуцированным паркинсонизмом. Данные представлены в виде среднего значения на срез ± стандартная ошибка среднего, N = 3-6 на группу. * P <0.05, ** P <0.01 по сравнению с группой MФTП, ANOVA с Dunnett's post-hoc test
Фиг. 5. Схема эксперимента. ИГХ -иммуногистохимическое исследование
Фиг. 6. Ключевые для оценки состояния животного элементы конструкции в тесте «вешалка»
Источники информации
1. Dauer, W., Przedborski, S. Parkinson's disease: mechanisms and models // Neuron. - 2003. - V.39, №6. - P. 889 - 909.
2. Венгеровский А.И. Лекции по фармакологии для врачей и провизоров. Томск: STT. 1998. С. 181-186.
3. Аминофф М.Д. Фармакотерапия паркинсонизма и других двигательных нарушений. В кн.: Базисная и клиническая фармакология. Т. 1. Под ред. Катцунга Б.Г. М.: Бином. 2007. С. 539-555.
4. Ardashov O. V., Pavlova A. V., Il’ina I. V., Morozova E. A., Korchagina D. V., Karpova E. V., Volcho K. P., Tolstikova T. G., Salakhutdinov N. F. Highly Potent Activity of (1R,2R,6S)-3-Methyl-6-(prop-1-en-2-yl)cyclohex-3-ene-1,2-diol in Animal Models of Parkinson’s Disease. J. Med. Chem., 2011, 54, 3866-3874.
5. Il’ina I.V., Volcho K.P., Korchagina D.V., Barkhash V.A., Salakhutdinov N.F. Helv. Chim. Acta, 2007, V. 90, № 2, P. 353-368.
6. Jackson-Lewis, V.; Przeborski, S. Protocol for the MPTP mouse model of Parkinson’s disease. Nat. Protoc., 2007, 2, 141-151.
7. Mätlik K., Võikar V., Vilenius C., Kulesskaya N., Andressoo J.-O. Two-Fold Elevation of Endogenous GDNF Levels in Mice Improves Motor Coordination without Causing Side-Effects. Sci. Rep.,2018, 8, 11861.
8. Gage, G.J.; Kipke, D.R.; Shain, W. Whole Animal Perfusion Fixation for Rodents. JoVE (Journal of Visualized Experiments) 2012, e3564, doi:10.3791/3564.
9. Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ / под общей ред. член-корр. РАМН, проф. Р. У. Хабриева. М.: Медицина, 2005. 832 с.
| название | год | авторы | номер документа |
|---|---|---|---|
| 2-((1-(4R-Бензил)-1H-1,2,3-триазол-4-ил)метокси)-3-метил-6-(проп-1-ен-2-ил)циклогекс-3-ен-1-ол в качестве противопаркинсонического средства | 2023 |
|
RU2812081C1 |
| ЭПОКСИДЫ 3-МЕТИЛ-6-(ПРОП-1-ЕН-2-ИЛ)ЦИКЛОГЕКС-3-ЕН-1,2-ДИОЛА-НОВЫЕ ПРОТИВОПАРКИНСОНИЧЕСКИЕ И ПРОТИВОСУДОРОЖНЫЕ СРЕДСТВА | 2014 |
|
RU2571299C1 |
| СРЕДСТВО ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ БОЛЕЗНИ ПАРКИНСОНА | 2006 |
|
RU2324492C1 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ БОЛЕЗНИ ПАРКИНСОНА | 2009 |
|
RU2418577C1 |
| 2-МЕТОКСИ-4[(3aR,7aS)-3,3,6-ТРИМЕТИЛ-1,3,3a,4,5,7a-ГЕКСАГИДРО-2-БЕНЗОФУРАН-1-ИЛ]ФЕНОЛ - НОВОЕ СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ БОЛЕЗНИ ПАРКИНСОНА | 2010 |
|
RU2436782C1 |
| Адамантильные производные бензимидазола, обладающие антипаркинсонической активностью | 2023 |
|
RU2820315C1 |
| ИНЪЕКЦИОННАЯ ЛЕКАРСТВЕННАЯ ФОРМА ДЛЯ ЛЕЧЕНИЯ БОЛЕЗНИ ПАРКИНСОНА, СПОСОБ ЕЕ ПРИГОТОВЛЕНИЯ И ПРИМЕНЕНИЕ | 2011 |
|
RU2520758C2 |
| Пептид, обладающий нейропротекторной активностью на модели МФТП-индуцированного паркинсонизма и фармацевтическая композиция на его основе | 2017 |
|
RU2662429C1 |
| СПОСОБ ЛЕЧЕНИЯ СИНДРОМА ПАРКИНСОНИЗМА | 1994 |
|
RU2057529C1 |
| Способ получения средства, способного блокировать развитие экспериментального паркинсонизма | 2017 |
|
RU2675697C2 |
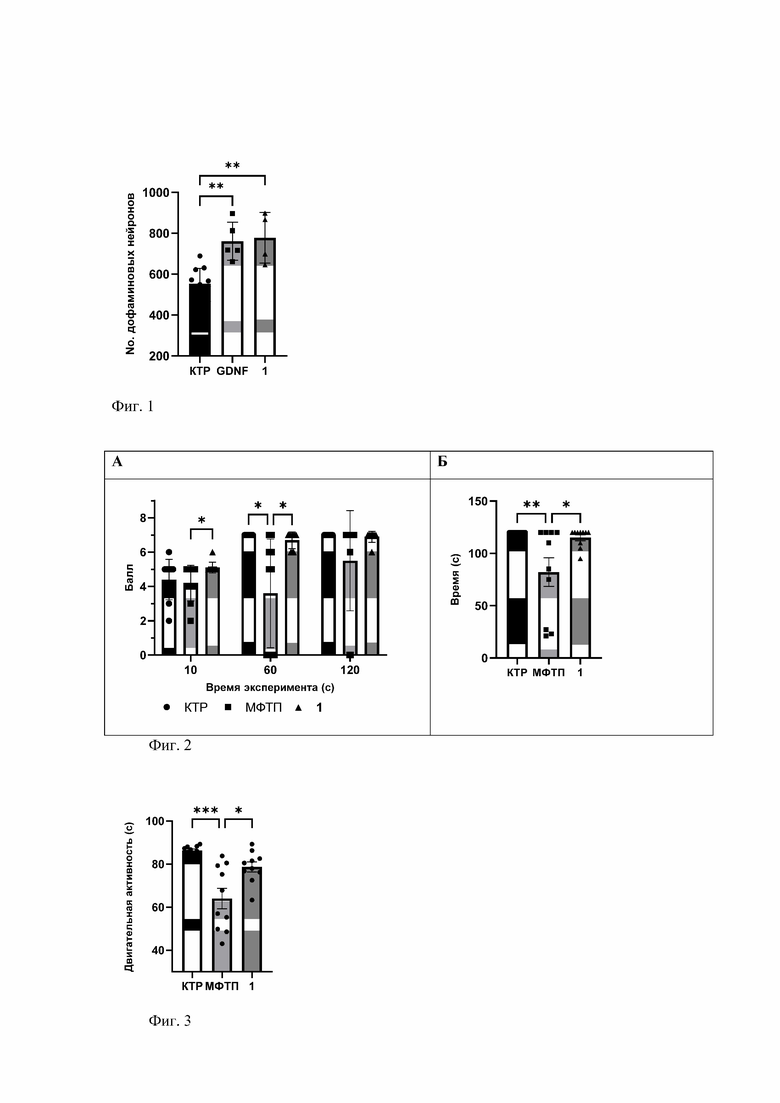
Изобретение относится к новому соединению 2-((1H-1,2,4-триазо-3-ил)тио)-3-метил-6-(проп-1-ен-2-ил)циклогекс-3-ен-1-олу формулы 1

Технический результат: получено новое соединение, обладающее противопаркинсонической активностью, которое может быть использовано в медицине. 6 ил., 1 табл., 5 пр.
2-((1H-1,2,4-Триазо-3-ил)тио)-3-метил-6-(проп-1-ен-2-ил)циклогекс-3-ен-1-ол формулы 1
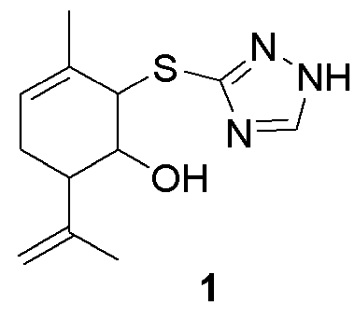
в качестве противопаркинсонического средства.
| Ardashov O | |||
| V., Pavlova A | |||
| V., Il’ina I | |||
| V., Morozova E | |||
| A., Korchagina D | |||
| V., Karpova E | |||
| V., Volcho K | |||
| P., Tolstikova T | |||
| G., Salakhutdinov N | |||
| F | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| J | |||
| Med | |||
| Chem., 54, 3866-3874, 2011 | |||
| 3-МЕТИЛ-6-(ПРОП-1-ЕН-2-ИЛ)ЦИКЛОГЕКС-3-ЕН-1,2-ДИОЛ В КАЧЕСТВЕ АНАЛЬГЕЗИРУЮЩЕГО СРЕДСТВА | 2009 |
|
RU2409351C1 |
| Адамантилсодержащие производные 1,2,4-триазола и 1,3,4-тиадиазола, имеющие монотерпеноидные фрагменты, используемые в качестве ингибиторов фермента тирозил-ДНК-фосфодиэстеразы 1 | 2020 |
|
RU2761880C1 |
Авторы
Даты
2023-05-29—Публикация
2022-09-12—Подача