Изобретение относится к области ветеринарии, а именно ветеринарной фармакологии и хирургии, и может быть использовано с целью сокращения сроков заживления плоскостных ран, а также профилактики инфицирования раневой поверхности.
Раны являются одними из самых частых травматических повреждений как у людей, так и у животных. Раны зачастую осложняются развитием вторичных инфекций кожи и мягких тканей вследствие первичного нарушения анатомической целостности кожного покрова, нарушения трофики и т.д. [4]
Микробный статус ран может быть классифицирован следующим образом:
1. контаминация - микроорганизмы присутствуют и фиксируются к ткани без размножения (изначально);
2. колонизация - микроорганизмы присутствуют и размножаются, клинически значимая иммунологическая реакция организма хозяина (изначально) отсутствует;
3. критическая колонизация - размножение микроорганизмов без классических признаков инфекции, но с задержкой заживления раны из-за образования токсинов или рана колонизируется резистентными к антибиотикам штаммами без признаков инфекции;
4. локальная инфекция - клинически наблюдаемая иммунологическая реакция организма хозяина с типичными признаками инфекции, включая гиперемию (эритема 1-2 см от края раны), с тенденцией к увеличению, отек, повышение локальной температуры кожи/глубжележащих тканей, боль, дисфункция, увеличение количества экссудата и его вязкости, в некоторых случаях возможно появление необычного запаха, задержка заживления раны;
5. системная инфекция - в дополнение к симптомам локальной инфекции наблюдаются признаки системной реакции организма хозяина, такие как лейкоцитоз, увеличение уровня C-реактивного белка в крови, и лихорадка [14].
Актуальной задачей является поиск альтернативных решений для профилактики и лечения бактериальных инфекций с ограниченным использованием системных антибиотиков. Современные нанотехнологии и нанопродукты за последние годы прочно вошли в практическую медицину. Нанотехнологии успешно применяются в медицине в направлении экологичного производства лекарств нового поколения, более эффективных и с минимальными побочными эффектами. Наночастицы металлов, главным образом микроэлементов, обладая бактерицидным действием, уже нашли свое применение в медицине, однако, к сожалению, еще не вполне распространены в ветеринарии [4-8].
Известен способ лечения инфицированных ран у животных, включающий очищение кожи от загрязнения, подсушивание и нанесение на кожу спиртового раствора клея БФ-8 и бромацида, взятых в соотношении 100:1, тонким слоем до образования пленки толщиной 2-5 мм (Патент RU №2383333, опубликованный 10.03.2010). Способ обеспечивает повышение лечебного эффекта не только животным с гнойно-ферментированным типом очищения раны, но и раненым животным с гнойно-секвестрационным и секвестрационным типами очищения раны. Однако, используемые авторами вещества обладают высокой токсичностью, и помимо этого, образовавшаяся пленка делает невозможным контроль раневого процесса и может привести к развитию анаэробной инфекции.
Задачей изобретения является разработка наиболее эффективного способа сокращения сроков регенерации плоскостной раны при одновременной профилактике инфицирования раневой поверхности.
Техническим результатом заявленного изобретения является ускорение регенеративного и минимизация воспалительного процессов при заживлении плоскостной раны.
Для сокращения сроков регенерации плоскостной раны при одновременной профилактике инфицирования раневой поверхности применялось антисептическое средство на основе наночастиц оксида цинка (изготовитель - ООО «Лаборатория биомедицинской инженерии») в совокупности с лекарственным препаратом «Суиферровит-А».
Антисептическое средство содержит в 1 л раствора:
ZnO - 13,88 мг/л (0,03%);
Цетилпиридиния хлорид (ЦПХ) - 0,07%;
Дистиллированная вода - 99,9%.
Лекарственный препарат «Суиферровит-А» представляет собой комбинацию ферментативного гидролизата растительного белка, витаминов группы В и железо(III)-декстранового коллоида (включающего ковалентно связанные атомы меди, кобальта и селена). В 1 мл раствора содержится:
Железо (III) в составе наночастиц железодекстранового коллоида - 7,0-8,0 мг;
Медь (II) включенная в кристаллическую решетку неорганического ядра наночастиц железодекстранового коллоида - 0,015 мг;
Кобальт (II) включённый в кристаллическую решетку неорганического ядра наночастиц железодекстранового коллоида - 0,025 мг;
Селен (IV) включённый в кристаллическую решетку неорганического ядра наночастиц железодекстранового коллоида - 0,019 - 0,024 мг;
Витамин В1 - 0,03 мг;
Витамин В2 - 0,012 мг;
Витамин В5 - 0,003 мг;
Витамин РР (В3) - 0,30 мг;
Витамин В6 (пантотенат кальция) - 0,016 мг;
Комплекс незаменимых аминокислот и низших пептидов - 47-53 мг.
Указанный технический результат достигается следующим образом. Лабораторным животным, а именно белым беспородным крысам, проводили обработку путем орошения раневой поверхности указанным антисептическим средством 2 раза в сутки до полного заживления раны, помимо этого, осуществляли однократное подкожное введение лекарственного препарата «Суиферровит-А» в дозе 0,1 мл в первый день лечения.
В результате проведенных экспериментов была доказана высокая эффективность разработанного способа. Для этого было сформировано 4 группы животных обоего пола по 10 лабораторных крыс в каждой. Содержание, кормление и манипуляции над подопытными животными осуществлялось в соответствии с положением Европейской конвенции о защите позвоночных животных, которые используются в эксперименте (Страсбург, 1986) и Правилами лабораторной практики в Российской Федерации (приказ Минздрава России от 19.06.2003 №267). Для обработки ран первой подопытной группе (контроль) применяли изотонический раствор натрия хлорида, второй группе (опыт 1) - раствором хлоргексидина биглюконата 0,05%, третьей группе (опыт 2) - антисептическим средством, содержащим наночастицы ZnO, четвертой группе (опыт 3) - антисептическим средством, содержащим наночастицы ZnO совместно с подкожным введением препарата «Суиферровит-А».
При этом на протяжении всего эксперимента проводили оценку общего состояния лабораторных животных, потребления корма и воды, поведения. На 1, 3, 7, 10, 13, 17 и 21 сутки проводили измерение площади раневой поверхности.
На 10 сутки для гистологического исследования у одной из подопытных крыс всех 4 групп брали фрагменты кожи с захватом раны. Далее эти крысы выводились из эксперимента путем ингаляции диэтилового эфира. Материал фиксировался в 10 % нейтральном формалине, обезвоживался в ряде спиртов возрастающей крепости и заливался в парафин по общепринятой методике. Срезы толщиной 5-7 мкм окрашивали гематоксилином и эозином. На препаратах оценивали наличие и выраженность воспалительного инфильтрата в дерме, выраженность процессов грануляции и эпителизации.
Процент уменьшения площади раны (ПУП) считали по следующей формуле.
ПУП = (A-B)/A*100%,
где A - Исходная площадь раневой поверхности;
B - Площадь раневой поверхности на момент измерения.
Наблюдение за остальными лабораторными крысами велось еще 11 суток до полной репарации кожной поверхности. На 21 сутки все животные подвергались эвтаназии путем ингаляции диэтилового эфира.
В таблице 1 представлены результаты убыли площади раневой поверхности лабораторных крыс 4-х подопытных групп, показана динамика заживления ран в различные сроки наблюдения.
*p < 0,05
По данным, представленным в таблице 1, можно сделать вывод о том, что наиболее интенсивно заживление ран происходило в 3 опытной группе, где лабораторным крысам применяли антисептик на основе наночастиц оксида цинка совместно с препаратом «Суиферровит-А», и рана полностью зажила на 17 сутки эксперимента. Наиболее низкие темпы заживления раны наблюдались в контрольной группе, где применяли изотонический раствор натрия хлорида. Группы опыт 1 и опыт 2 показали похожие результаты: на 17 сутки раны ПУП составили 98,31% и 98,61% соответственно. Во всех группах к 21-м суткам завершалось полное заживление и очищение раны.
Далее на 10 сутки эксперимента провели взятие материала для гистологического исследования. Для этого у одной лабораторной крысы из каждой группы, введенной в наркоз, с помощью хирургических инструментов провели взятие фрагмента кожи с захватом раны, изготовили препарат и исследовали его с помощью микроскопа.
Контроль. В гистологических препаратах, окрашенных гематоксилином и эозином, выявляется кожа, состоящая из трёх четко выраженных слоёв: эпидермиса, дермы и части гиподермы. Морфологическая картина кожи в разных её участках имеет определенные локальные особенности. В центральной части гистологического среза со стороны эпидермиса наблюдается дефект, полностью затрагивающий эпидермис и часть дермы. Морфологическая картина дефекта характерна для процесса посттравматического заживления раны под струпом в фазу пролиферации и начала созревания грануляционной ткани с выраженным размножением молодых клеток соединительной ткани, начальными процессами фиброгенеза и эпителизации. Воспалительный процесс при этом выражен умеренно.
Среди клеток грануляционной ткани преобладают округлые фибробласты с гиперхромными ядрами, между которыми встречаются нейтрофилы, располагающиеся в ткани диффузно. Наибольшая концентрация нейтрофилов наблюдается под струпом в верхних двух третях грануляции.
В межклеточном веществе визуализируются тонкие слабооксифильные пучки коллагеновых волокон и мелкозернистое аморфное межклеточное вещество.
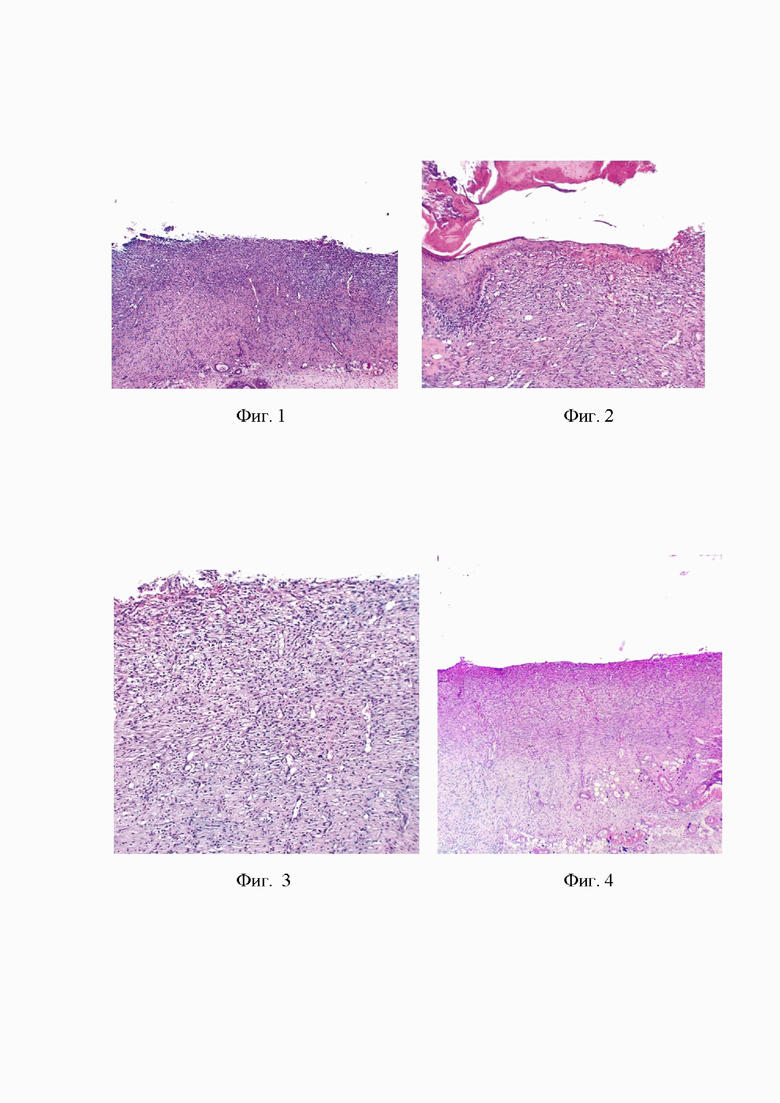
Также диффузно в грануляционной ткани визуализируются многочисленные новообразованные тонкостенные кровеносные сосуды, относительно равномерно расположенные по всей площади грануляции. Большинство сосудов находятся в состоянии кровенаполнения (Фиг. 1, Контроль. Грануляция раны. Гематоксилин и эозин. Окуляр Х10, объектив Х10).
На краю раны распознаются эпидермальные наползания. Краевая эпителизация дефекта слабая. В эпителиальном пласте не прослеживалась четкая дифференцировка слоев клеток. Видна небольшая контракция - инвагинация краев здоровой кожи в краевые зоны дефекта (Фиг. 2. Контроль. Эпителизация раны. Гематоксилин и эозин. Окуляр Х10, объектив Х10).
Опыт 1 и Опыт 2. В гистологических препаратах, окрашенных гематоксилином и эозином, выявляется кожа, состоящая из трёх четко выраженных слоёв: эпидермиса, дермы и части гиподермы. Морфологическая картина кожи в разных её участках имеет определенные локальные особенности. В центральной части гистологического среза со стороны эпидермиса наблюдается дефект, полностью затрагивающий эпидермис и часть дермы. Морфологическая картина дефекта характерна для процесса посттравматического заживления раны под струпом в фазу пролиферации и умеренного созревания грануляционной ткани с выраженным размножением молодых клеток соединительной ткани, начальными процессами фиброгенеза и эпителизации. Воспалительный процесс при этом выражен умеренно.
Среди клеток грануляционной ткани наравне с округлыми фибробластами с гиперхромными ядрами присутствуют и фиброциты с вытянутыми овальными ядрами, между которыми встречаются нейтрофилы, располагающиеся в ткани диффузно. Наибольшая концентрация нейтрофилов наблюдается под струпом в верхних двух третях грануляции.
В межклеточном веществе визуализируются тонкие слабооксифильные пучки коллагеновых волокон и мелкозернистое аморфное межклеточное вещество.
Также диффузно в грануляционной ткани визуализируются многочисленные новообразованные тонкостенные кровеносные сосуды, относительно равномерно расположенные по всей площади грануляции. Большинство сосудов находятся в состоянии кровенаполнения (Фиг. 3. Опыт 1. Грануляция раны. Гематоксилин и эозин. Окуляр Х10, объектив Х10 и рис. 4. Опыт 2. Грануляция раны. Гематоксилин и эозин. Окуляр Х10, объектив Х10).
На краю раны распознаются эпидермальные наползания. Краевая эпителизация дефекта умеренная. В эпителиальном пласте не прослеживалась четкая дифференцировка слоев клеток. Видна небольшая контракция - инвагинация краев здоровой кожи в краевые зоны дефекта (Фиг. 5. Опыт 1. Эпителизация раны. Гематоксилин и эозин. Окуляр Х10, объектив Х10 и фиг. 6 Опыт 2. Эпителизация раны. Гематоксилин и эозин. Окуляр Х10, объектив Х10).
Опыт 3. В гистологических препаратах, окрашенных гематоксилином и эозином, выявляется кожа, состоящая из трёх четко выраженных слоёв: эпидермиса, дермы и части гиподермы. Морфологическая картина кожи в разных её участках имеет определенные локальные особенности. В центральной части гистологического среза со стороны эпидермиса наблюдается дефект, полностью затрагивающий эпидермис и часть дермы. Морфологическая картина дефекта характерна для процесса посттравматического заживления раны под струпом в фазу пролиферации и выраженного созревания грануляционной ткани с характерным размножением молодых клеток соединительной ткани, их дифференцировкой, развивающимися процессами фиброгенеза и эпителизации. Воспалительный процесс при этом выражен очень слабо.
Среди клеток грануляционной ткани преобладают фиброциты с крупными гипохромными вытянутыми ядрами, среди которых встречаются и округлые фибробласты с гиперхромными ядрами. Нейтрофилы встречаются редко в виде единичных клеток. В основном они наблюдаются под струпом в верхней четверти грануляции.
В межклеточном веществе визуализируются толстые оксифильные пучки коллагеновых волокон и мелкозернистое аморфное межклеточное вещество.
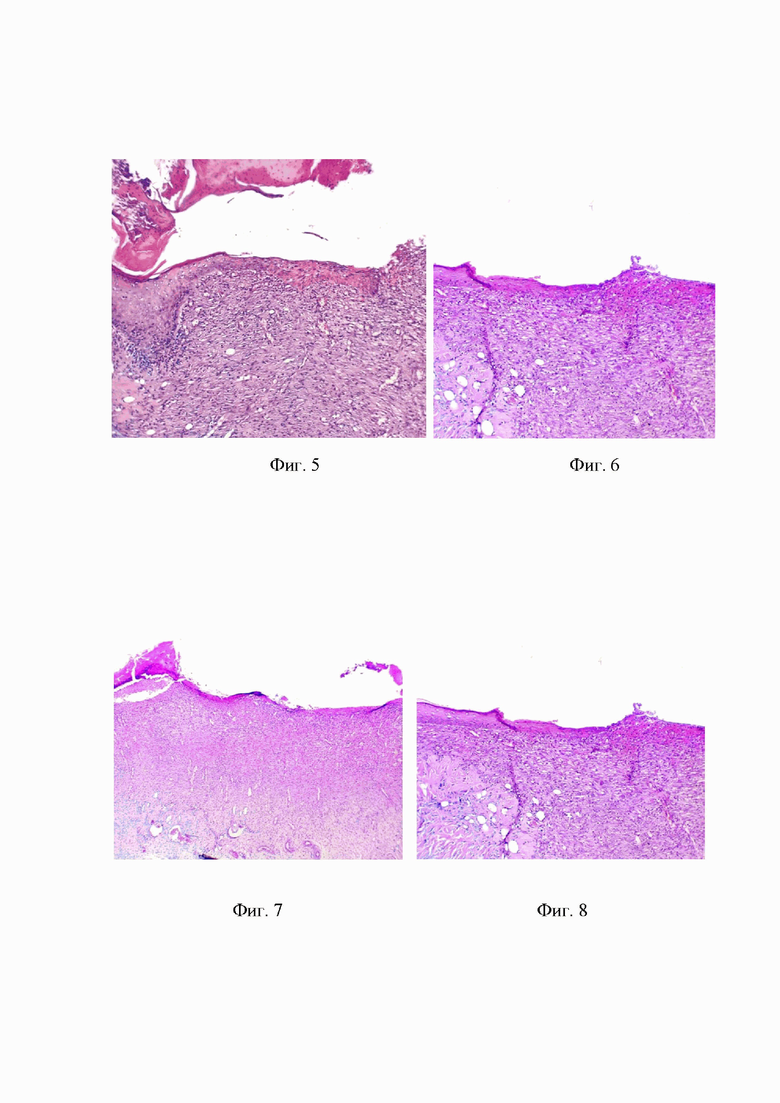
Также диффузно в грануляционной ткани визуализируются многочисленные новообразованные тонкостенные кровеносные сосуды, относительно равномерно расположенные по всей площади грануляции. Большинство сосудов находятся в состоянии кровенаполнения (Фиг. 7. Опыт 3. Грануляция раны. Гематоксилин и эозин. Окуляр Х10, объектив Х10).
На краю раны распознаются эпидермальные наползания. Краевая эпителизация дефекта достаточно сильная. В эпителиальном пласте не прослеживалась четкая дифференцировка слоев клеток. Видна небольшая контракция - инвагинация краев здоровой кожи в краевые зоны дефекта Фиг. 8. Опыт 3. Эпителизация раны. Гематоксилин и эозин. Окуляр Х10, объектив Х10).
Таким образом, анализ результатов проведенных экспериментов позволил сделать вывод о том, что обработка раневой поверхности антисептическим средством на основе наночастиц оксида цинка при одновременном подкожном введении препарата «Суиферровит-А» способствовало ускорению сокращению сроков регенерации плоскостной раны, минимизации воспалительного процесса, профилактике инфицирования раневой поверхности.
Литература
1. Аль З., Малинкина О.Н., Зудина И.В., Ковалева Я.О., Ксенофонтова О.Ю., Островский Н.В. Оценка ранозаживляющей активности l- и d-изоформ аскорбиновой кислоты и их солей с хитозаном на модели ожоговой раны у крыс // Современные проблемы науки и образования. - 2016. - № 6. - С. 236.
2. Брайловская Т.В., Федорина Т.А. Морфологическая характеристика течения раневого процесса при экспериментальном моделировании резаных и рвано-ушибленных кожных ран // Биомедицина. - 2009. - №1. - С. 68-74.
3. Габриелян Л.С., Трчунян А.А. Антибактериальные свойства наночастиц серебра и мембранотропные механизмы их действия // Журнал Белорусского государственного университета. Биология. 2020. № 3. С. 64-71.
4. Гельфанд Б.Р. и др. (ред.) Хирургические инфекции кожи и мягких тканей. Российские национальные рекомендации. Москва: Издательство МАИ; 2015, 109 с. Режим доступа: http://nasci.ru/?id=3392&download=1.
5. ГОСТ Р 53434-2009 - Принципы надлежащей лабораторной практики.
6. Кривошапка А.В., Криворотько Д.Н., Стародубцев Д.С. Влияние ранозаживляющих лекарственных средств на уровень провоспалительных цитокинов при экспериментальном термическом ожоге у крыс Архивариус. - 2015. - Т. 2. - № 3(3). - С. 52-55.
7. Кулешов С.М., Кулешов Р.С. Ранозаживляющее действие биологически активных препаратов органического происхождения // Научный журнал КубГАУ. - 2007. - №26(2).
8. Приказ МЗ РФ № 708н от 23.августа 2010 г. «Правила лабораторной практики в Российской Федерации».
9. Приказ МЗ СССР № 1045-73 от 06.04.1973 г. «Санитарные правила по устройству, оборудованию и содержанию экспериментально биологических клиник (вивариев)».
10. Приказ МЗ СССР № 755 от 12.08.77 г. «Правила проведения работ с использованием экспериментальных животных».
11. Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ. Под ред. Р.У. Хабриева. - 2 изд., перераб. и доп. - М.: ОАО Издательство «Медицина», 2005 - 832 с.
12. Тржецинский С.Д., Мозуль В.И., Жернова Г.А., Фурса Н.С. Ранозаживляющая активность мази, содержащей эфирное масло травы тысячелистника пойменного // Актуальні питання фармацевтичної і медичної науки та практики. - 2014. - № 2(15). - С. 50-53.
13. Knetsch M.L.W., Koole L.H. Новые стратегии в разработке антимикробных покрытий: пример увеличения использования серебра и наночастиц серебра // Полимеры Базель. - 2011; - №3. - С. 340-366.
14. Kramer A., Dissemond J., Kim S., Willy C., Mayer D., Papke R., Tuchmann F., Assadian O. Consensus on Wound Antisepsis: Update 2018. Skin Pharmacol Physiol. 2018; 31(1): 28-58. doi: 10.1159/000481545.
15. Leung Y.H., Ng A.M.C., Xu X., Shen Z., Gethings L.A., Wong M.T., Chan C.M.N., Guo M.Y., Ng Y.H., Djurišić A.B., Lee P.K.H., Chan W.K., Yu L.H., Phillips D.L., Ma A.P.Y., Leung F.C.C. Mechanisms of antibacterial activity of MgO: non-ROS mediated toxicity of MgO nanoparticles towards Escherichia coli // Small. 2014 Mar 26; 10(6):1171-83. doi: 10.1002/smll.201302434. Epub 2013 Dec 17.
16. Nagy A. 1, Harrison A., Sabbani S., Munson R.S. Jr, Dutta P.K., Waldman W.J. Silver nanoparticles embedded in zeolite membranes: release of silver ions and mechanism of antibacterial action // Int J Nanomedicine. 2011; 6:1833-52. doi: 10.2147/IJN.S24019. Epub 2011 Sep 6.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ЛЕЧЕНИЯ ГЛУБОКОГО ОЖОГА КОЖИ | 2008 |
|
RU2372922C1 |
| Ранозаживляющая мазь для лечения термических ожогов | 2022 |
|
RU2787377C1 |
| Способ лечения ран мягких тканей с использованием измельченных слайсов пантов марала | 2024 |
|
RU2831889C1 |
| ТЕХНОЛОГИЯ РЕГЕНЕРАТИВНОЙ БИОПЛАСТИКИ ДЕФЕКТОВ ПОКРОВНЫХ ТКАНЕЙ | 2013 |
|
RU2547386C1 |
| Лекарственный препарат в виде золя для лечения заболевания и/или состояния, характеризующегося нарушением целостности кожного покрова, и способ его получения | 2019 |
|
RU2742752C1 |
| СПОСОБ ОПЕРАТИВНОГО ЛЕЧЕНИЯ ОЖОГОВЫХ РАН | 2018 |
|
RU2673806C1 |
| ПРОТИВООЖОГОВЫЙ ГЕЛЬ | 2011 |
|
RU2481121C2 |
| СПОСОБ ПОЛУЧЕНИЯ ИСКУССТВЕННОЙ МАТРИЦЫ КОЖИ | 2003 |
|
RU2252787C1 |
| КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ РАН | 2008 |
|
RU2370270C1 |
| Комплексное соединение иона Co и полиакриловой кислоты, обладающее гемостатическими, антимикробными и ранозаживляющими свойствами | 2021 |
|
RU2767853C1 |
Изобретение относится к области ветеринарии, а именно ветеринарной фармакологии и хирургии, и может быть использовано для регенерации плоскостных ран у крыс. Для этого обрабатывают раневую поверхность путем орошения антисептическим средством на основе наночастиц оксида цинка, содержащим в 1 л раствора: ZnO 0,03% цетилпиридиния хлорид – 0,07 %, дистиллированная вода – 99,9%, 2 раза в сутки до полного заживления раны вместе с однократным подкожным введением лекарственного препарата «Суиферровит-А» в дозе 0,1 мл в первый день лечения. Изобретение способствует ускорению регенеративного и минимизации воспалительного процессов при заживлении плоскостной раны. 8 ил., 1 табл.
Способ регенерации плоскостных ран у крыс, включающий обработку раневой поверхности путем орошения антисептическим средством на основе наночастиц оксида цинка, содержащим в 1 л раствора: ZnO 0,03% цетилпиридиния хлорид – 0,07 %, дистиллированная вода – 99,9%, 2 раза в сутки до полного заживления раны вместе с однократным подкожным введением лекарственного препарата «Суиферровит-А» в дозе 0,1 мл в первый день лечения.
| РАНОЗАЖИВЛЯЮЩЕЕ ВЕЩЕСТВО | 1997 |
|
RU2143908C1 |
| Композиция для лечения заболеваний кожи и косметического использования | 2019 |
|
RU2724342C1 |
| СПОСОБ ЛЕЧЕНИЯ ИНФИЦИРОВАННЫХ РАН У ЖИВОТНЫХ | 2007 |
|
RU2383333C2 |
| MELNIKOVA N | |||
| et al | |||
| The New Pharmaceutical Compositions of Zinc Oxide Nanoparticles and Triterpenoids for the Burn Treatment / Pharmaceuticals, 2020, 13, 207, 19 pages | |||
| AKBAR N | |||
| et al | |||
| Zinc oxide nanoparticles conjugated with clinically‑approved medicines as | |||
Авторы
Даты
2023-05-29—Публикация
2022-09-29—Подача