Изобретение относится к новому химическому соединению, а именно к 2-этил-6-метилпиридинол-3-ил-тиооктаноату формулы (1):
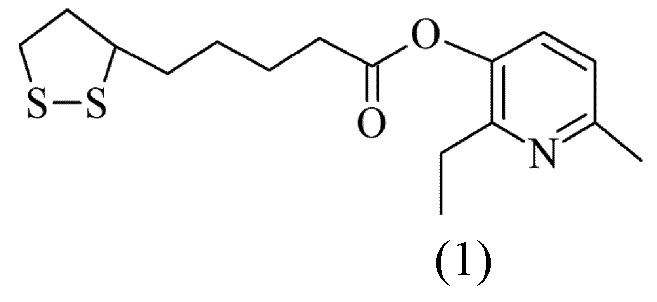
Данное соединение проявляет антигипоксическую активность и может использоваться в качестве биологически активного вещества, обладающего антигипоксической активностью.
Предлагаемое изобретение относится к органической химии и медицине, в частности к новому химическому соединению, проявляющему антигипоксическую активность.
Соли 2-этил-6-метил-3-оксипиридина широко позиционируются в качестве лекарственных средств (ЛС) с антигипоксической активностью. Известны фармакологические композиции на основе солей 2-этил-6-метил-3-оксипиридина с органическими карбоновыми кислотами [Патент РФ №RU 2284993 C2, 2002], нитроксисукцината 2-этил-6-метил-3-оксипиридина [Патент РФ №RU2394815 C2, 2008], сукцината 2-этил-6-метил-3-оксипиридина [Патент РФ №RU 2497522 C1, 2012], проявляющие антигипоксическую активность. Однако, широко декларируемая зависимость антигипоксического потенциала солей 2-этил-6-метил-3-оксипиридина от их антиокислительной активности не всегда находит подтверждение в экспериментальных и клинических исследованиях [И.А. Волчегорский, И.Ю. Мирошниченко, Л.М. Рассохина, М.П. Малкин, Росс. физиол. журн. им. И.М. Сеченова, 105(3), 363-374 (2019); И.А. Волчегорский, М.Г. Москвичева, Е.Н. Чащина, Клиническая медицина, 82(11), 31-35 (2004)]. Известны ситуации, при которых соответствующие лекарственные средства оказывают разнонаправленное влияние на устойчивость к гипоксии различного генеза [И.А. Волчегорский, И.Ю. Мирошниченко, Л.М. Рассохина, М.П. Малкин, Росс. физиол. журн. им. И.М. Сеченова, 105(3), 363-374 (2019)]. Данное обстоятельство иллюстрирует целесообразность поиска дериватов 2-этил-6-метил-3-оксипиридина с оптимальным профилем антигипоксического действия. Одним из перспективных подходов к решению этой задачи является этерификация 2-этил-6-метил-3-оксипиридина тиоктовой (α-липоевой) кислотой.
В качестве прототипов и препаратов сравнения использованы известные лекарственные средства, обладающие антигипоксическим действием: эмоксипин (2-этил−6-метил-3-оксипиридина гидрохлорид) и тиоктовая (α-липоевая) кислота [Новиков В. Е., Лосенкова С. О. Обзоры по клинической фармакологии и лекарственной терапии. 2004. Т. 3. №. 1.С. 2-14; И.А. Волчегорский, И.Ю. Мирошниченко, Л.М. Рассохина, М.П. Малкин, Росс. физиол. журн. им. И.М. Сеченова, 105(3), 363-374 (2019)].
Задачей изобретения является расширение арсенала биологически активных веществ, в том числе обладающих антигипоксической активностью. Технический результат - получение практически нетоксичного биологически активного нового химического вещества, обладающего антигипоксической активностью.
Сущность изобретения: сложный эфир тиоктовой (α-липоевой) кислоты и 2-этил-6-метил-3-оксипиридина (2-этил-6-метилпиридинол-3-ил-тиооктаноат) формулы (1):
 ,
,
проявляющий антигипоксическую активность.
Указанное соединение и его свойства в литературе не описаны.
Заявляемое соединение синтезируют взаимодействием тиоктовой кислоты и 2-этил-6-метил-3-оксипиридина в соответствии с нижеприведенной схемой:
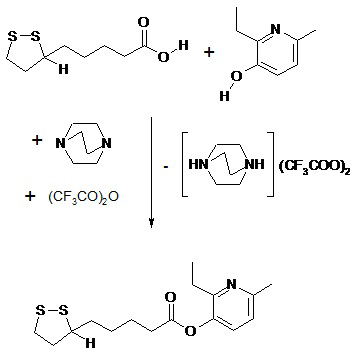
На первом (предэтерификационном) этапе синтеза получают смешанный ангидрид тиоктовой и трифторуксусной кислот, который используется на втором (этерификационном) этапе: добавление 2-этил-6-метил-3-оксипиридина гидрохлорида к смешанному ангидриду при температуре 55 - 60 градусов Цельсия после промывания 0,005 М раствором соляной кислоты и дистиллированной водой с последующим удалением воды и летучих примесей на роторном испарителе. Для получения хроматографически гомогенного продукта эфир подвергается экстракции гексаном, остатки которого удаляются с помощью роторного испарителя. Химическую однородность полученного вещества оценивают методом тонкослойной хроматографии на пластинах типа "Сорбфил" или аналогичных. В качестве элюента используют смесь н-гептан - изопропанол в соотношении 5/1. Проявление хроматограмм проводится в парах йода. После получения хроматографически гомогенного продукта оценивается его агрегатное состояние и растворимость.
Пример 1
Синтез заявляемого соединения
В качестве исходных реагентов используют (R, S)- тиоктовую (α-липоевую) кислоту (NuSci, США); СAS № 1077-28-7. 2-этил-6-метил-3-оксипиридин – основание получают из субстанции-порошка метилэтилпиридинола гидрохлорида (2-этил-6-метил-3-оксипиридина гидрохлорида) [ЗАО «Обнинская химико-фармацевтическая компания», Россия]). К насыщенному водному раствору 2-этил-6-метил-3-оксипиридина гидрохлорида добавляют эквивалентное количество натриевой щёлочи, выпавший осадок отфильтровывают на холоде, промывают на фильтре охлаждённой водой, высушивают в эксикаторе над твёрдым KOH.
В стеклянную коническую колбу помещают 20,62 г (0,100 моль) тиоктовой (α-липоевой) кислоты, 12,0 г триэтилендиамина (0,107 моль) и 75 мл 1,2-дихлорэтана (ДХЭ). Колбу герметично закрывают и взвешивают на технических весах. Затем содержимое колбы перемешивают, добиваясь полного растворения твёрдых компонентов, и помещают колбу в водяную баню со льдом. После охлаждения раствора в колбу добавляют 22,5 г (0,107 моль; около 15 мл) трифторуксусного ангидрида (ТФУА), предварительно охлаждённого в бане со льдом. ТФУА вносят порциями по 2-3 мл (3-4,5 г) с периодичностью 2-3 минуты. После прибавления каждой порции ТФУА колбу герметично закрывают и энергично перемешивают её содержимое, не допуская локального перегрева. Количество внесенного ТФУА контролируют, взвешивая колбу с реакционной смесью после прибавления каждой порции ангидрида. По завершении добавления ТФУА колбу с реакционной смесью помещают в водяную баню (40–43 °С), где выдерживают в течение 10-12 минут при периодическом перемешивании. На этом этапе синтеза формируется смешанный ангидрид тиоктовой и трифторуксусной кислот.
Колбу с полученным ангидридом помещают в баню со льдом и после охлаждения раствора добавляют в него 13,72 г (0,100 моль) 2-этил-6-метил-3-оксипиридина, предварительно растёртого в порошок и высушенного в вакуум-эксикаторе. Сосуд с реакционной смесью помещают в водяную баню (56–60°С) и энергично перемешивают содержимое колбы до полного растворения 2-этил-6-метил-3-оксипиридина. Полученный раствор выдерживают ещё 20 минут при той же температуре, затем охлаждают до комнатной температуры и после этого выливают в 1,0 литра холодной (+3 - +5 °С) дистиллированной воды. После интенсивного перемешивания в течение 5-ти минут смесь отстаивают до разделения фаз. Верхнюю («водную») фазу, содержащую соль триэтилендиамина и трифторуксусной кислоты, удаляют декантированием. Нижнюю фазу, содержащую раствор целевого продукта (2-этил-6-метилпиридинол-3-ил-тиооктаноата) в ДХЭ, трижды промывают 1,0 литром дистиллированной воды комнатной температуры. Затем раствор полученного эфира дважды промывают 0,005 М раствором соляной кислоты (по 1,0 л) и дважды водой (по 1,0 л). По окончании промывки раствор эфира переносят в колбу роторного испарителя, с помощью которого удаляют растворитель при температуре 25-35°С. В качестве альтернативного подхода можно «высушивать» раствор в потоке воздуха в вытяжном шкафу. В обоих случаях «выход» целевого продукта составляет не менее 85% от расчетных значений.
Полученный эфир может содержать незначительные количества 2-этил-6-метил-3-оксипиридина гидрохлорида, тиоктовой кислоты и триэтилендиамина. Для получения хроматографически гомогенного целевого вещества полученный эфир экстрагируют кипящим н-гексаном. В процессе охлаждения гексанового экстракта целевой эфир выделяется в виде ярко-жёлтого масла. По окончании экстракции холодный н-гексан осторожно декантируют из приёмной колбы и удаляют его остатки на роторном испарителе (40-45 °С). Все этапы синтеза и очистки целевого соединения проводят в вытяжном шкафу.
Химическую однородность полученного вещества оценивают методом тонкослойной хроматографии на пластинах типа «Сорбфил». При элюировании смесью н-гептан – изопропанол (5:1) с последующим проявлением парами йода Rf целевого эфира составляет 0,61. При недостаточной чистоте продукта процедуру очистки необходимо повторить.
Спектральные характеристики соединения формулы (1).
Сложный эфир тиоктовой (α-липоевой) кислоты и 2-этил-6-метил-3-оксипиридина (2-этил-6-метилпиридинол-3-ил-тиооктаноат)
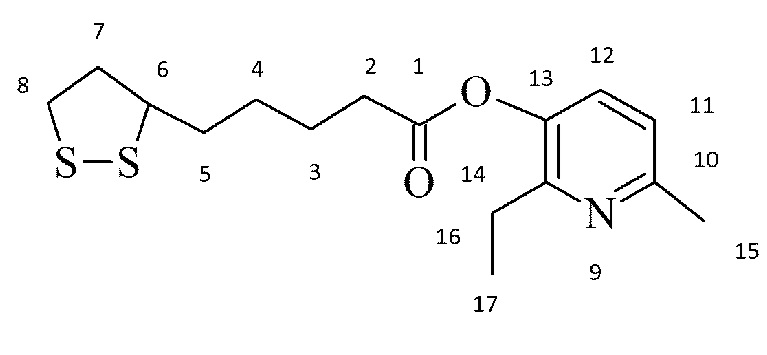 (1)
(1)
Маслообразная вязкая жидкость жёлтого цвета со слабым специфическим запахом.
ИК-спектр (v, см-1) в KBr: 1761.4 c. (v C(1)=O), 1228.3 c., 1153.5 c., 1123,1 c. широкая «эфирная полоса» [симм. и асимм. v C(1)O-C(13)].
Спектр ЯМР 1H (500.13 МГц; Т=293.5К) 1Н (δ, м.д., J, Гц): 1.27 (трипл. 3H, C(17)H3, J=7.6); 1.61(мультипл. 2H, С(4)H2, J=8.3); 1.78 (мультипл. 2H, С(5)H2, J=4.0); 1.87 (мультипл. 2H, С(3)H2, J=7.3); 1.97 (секст. 1H, C(7)H2(2), J=7.3); 2.52 (квинт. 1H, C(7)H2(1), J=6.2); 2.57 (сингл. 3H, C(15)H3); 2.66 (трипл. 2H, C(2)H2, J=7.5); 2.74 (квадр. 2H, C(16)H2, J=7.6); 3.17 (секст. 1H, C(8)H2(1), J=5.0); 3.25 (секст. 1H, C(8)H2(2), J=4.7); 3.64 (квинт. 1H, C(6)H, J=6.8); 7.06 (дубл. 1H, C(11)H, J=8.2); 7.28 (дубл. 1H, C(12)H, J=8.2).
УФ-спектр (раствор в 95% этаноле): λmax 332 нм -S-S- n→σ* переход.
По данным криометрического анализа молекулярная масса целевого продукта, растворенного в бензоле, составила 324±3 г/моль при расчетном значении 325,34 г/моль.
Физико-химические свойства
2-этил-6-метилпиридинол-3-ил-тиооктаноат представляет собой маслообразную вязкую жидкость интенсивного жёлтого цвета, при низких температурах застывающую в стеклоподобную прозрачную массу. В жидком виде полученное вещество имеет показатель преломления n25-27=1,546±0,001, нерастворимо в воде, постепенно гидролизуется при контакте с нейтральными, щелочными и кислыми растворами. Целевое соединение мало растворимо в алифатических углеводородах, умеренно растворимо в бензоле, хорошо растворимо в хлороформе, ДХЭ, диметилсульфоксиде, этиловом спирте, изопропиловом спирте, ацетоне, диоксане, а также в разбавленных растворах сильных кислот (при рН выше 1,65 выпадает из растворов в виде эмульсии).
Полученному сложному эфиру было присвоено лабораторное название «тиоксипин», состоящее из аффикса «тио» и корня «ксипин», соответственно обозначающих ацильный и спиртовой компоненты целевого вещества.
Пример 2
Оценка токсичности заявляемого соединения
Токсикологические исследования выполнены в соответствии с рекомендациями по изучению острой токсичности химических веществ [А.Н. Миронов, Н.Д. Бунятян, А.Н. Васильев и др., Руководство по проведению доклинических исследований лекарственных средств, Гриф и К, Москва (2012); М.Л. Беленький, Элементы количественной оценки фармакологического эффекта, Медицина, Ленинград (1963); И.В. Березовская, Хим.-фарм. журн., 37(3), 32-34 (2003)]. Острую токсичность тиоксипина оценивали после его однократного внутрибрющинного введения с последующим наблюдением за животными в течении 4-х недель. Этот раздел работы был выполнен на самках лабораторных грызунов двух видов (крысы популяции Вистар массой 200±20 г и белые беспородные мыши массой 30±3 г). В обоих случаях регистрировали летальность животных после введения тиоксипина в 7 различных дозах, каждую из которых испытывали на 10 животных. Животным вводили тиоксипин и «вещества сравнения» в виде эмульсий, приготовленных на среде, состоящей из водного раствора NaCl (9 г/л) и Твин-80 (10,9 г/л). рН вводимых эмульсий не выходил за пределы 7,2 – 7,6. В экспериментах на крысах эмульсию тиоксипина вводили в объеме 25 мл/кг. Соответствующая величина в экспериментах на мышах составила 50 мл/кг. Изучаемые дозы тиоксипина рассчитывали исходя из вычисленных ранее эквивалентов средней терапевтической дозы (ЭСТД=72,5 мкмоль/кг) 2-этил-6-метил-3-оксипиридина гидрохлорида (эмоксипина) [И.А. Волчегорский, Л.М. Рассохина, И.Ю. Мирошниченко, Эксперим. и клин. фармакол., 74(12), 27-32 (2011).]. В токсикологическом разделе исследования тиоксипин вводили в дозах, эквимолярных 4,77 – 25,5 ЭСТД эмоксипина для крыс и 4,47 – 13,06 ЭСТД для мышей.
Параллельно оценивали острую токсичность «веществ сравнения»: смеси 2-этил-6-метил-3-оксипиридина гидрохлорида и тиоктовой кислоты, вводимых в дозах эквимолярных дозировкам тиоксипина. Полученные данные были обработаны пробит-анализом [D.J. Finney, Probit analysis: a statistical treatment of the sigmoid response curve, Cambridge university press, Cambridge (1952)]. Результаты выражали в виде LD50, её стандартной ошибки (s) и дополнительно рассчитанного 95% доверительного интервала (95% ДИ). Статистическое сопоставление LD50 тиоксипина и «вещества сравнения» проводили с помощью токсикологической версии t – критерия. Вывод о влиянии этерификации на токсичность смеси компонентов тиоксипина делали только при однонаправленных статистически значимых изменениях LD50, установленных как в экспериментах на мышах, так и на крысах.
Результаты представлены в таблице 1.
Во всех сериях токсикологического раздела исследования гибель животных отмечалась только в течении первых двух суток с момента введения изучаемых веществ. Полученные данные позволили отнести тиоксипин к классу малотоксичных соединений [И.В. Березовская, Хим.-фарм. журн., 37(3), 32-34 (2003).]. Об этом свидетельствуют показатели острой токсичности (в размерности мг/кг), установленные в экспериментах на мышах и крысах. В обоих случаях LD50 тиоксипина соответствовала диапазону 101 – 1000 мг/кг, характеризующему низкую токсичность химических веществ при внутрибрюшинном введении. Важно заметить, что эквимолярная смесь тиоктовой кислоты и эмоксипина продемонстрировала более высокую токсичность в сравнении с продуктом их этерификации. Это проявилось статистически значимым уменьшением LD50 смеси свободных компонентов тиоксипина в сравнении с LD50 их сложноэфирного деривата. Данная закономерность была установлена как в экспериментах на мышах, так и на крысах. В первом случае, LD50 тиоксипина (в размерности мкмоль/кг) превышала соответствующий показатель смеси его свободных компонентов в 1,63 раза, во втором – в 1,27 раза.
Пример 3
Оценка антигипоксической активности заявляемого соединения на моделях гипоксической, гиперкапнической, гемической и гистотоксической гипоксии.
Данный раздел исследования выполнен на мышах обоего пола. Каждая экспериментальная группа, численностью 10 мышей, включала 5 самцов и 5 самок. В качестве «веществ сравнения» использовали 2-этил-6-метил-3-оксипиридина гидрохлорид, тиоктовую кислоту и их эквимолярную смесь. Тиоксипин и «вещества сравнения» в эквимолярных тиоксипину дозах вводили внутрибрюшинно за 30 минут до моделирования острой гипоксии. Животным вводили тиоксипин и «вещества сравнения» в виде эмульсий, приготовленных на среде, состоящей из водного раствора NaCl (9 г/л) и Твин-80 (0,84 г/л). рН вводимых эмульсий не выходил за пределы 7,2 – 7,6. Тиоксипин применяли в дозах эквимолярных 0,5; 1,0 и 2,0 ЭСТД эмоксипина. Мыши контрольной группы получали эквиобъемное количество среды [Твин-80 (0,84 г/л) на водном растворе NaCl (9 г/л)], использовавшейся для эмульгирования тиоксипина и «веществ сравнения». Для моделирования острой гипоксической гипоксии использовали тест «асфиксии утопления» [Кулинский В.И., Ольховский И.А., Ковалевский А.Н., Бюл. эксперим. биол. и мед. 101(6), 669–671(1986).]. Для воспроизведения гиперкапнической гипоксии мышей помещали в индивидуальные, герметически закрывающиеся стеклянные емкости объемом 200 мл. Гемическую гипоксию вызывали однократным введением нитрита натрия в дозе 200 мг/кг (20 мл/кг 1% раствора NaNO, подкожно). [А.Н. Миронов, Н.Д. Бунятян, А.Н. Васильев и др., Руководство по проведению доклинических исследований лекарственных средств, Гриф и К, Москва (2012).]. Гистотоксическую гипоксию индуцировали разовой инъекцией нитропруссида натрия в дозе 20 мг/кг (20 мл/кг 0,1% раствора, внутрибрюшинно) [А.И. Курбанов, Н.Н. Самойлов, Е.Н. Стратиенко и др., Психофармакол. и биол. наркол. 6(1–2), 1164–1170 (2006).]. Во всех случаях критерием устойчивости к острой гипоксии являлось время от момента её индукции до гибели животных. Статистический анализ этого раздела исследования выполнен с использованием пакета прикладных компьютерных программ SPSS-17.0. Данные обработаны методами дескриптивной статистики и представлены в виде медианы (Me) и диапазона между «нижним» (LQ, 25 процентиль) и «верхним» (UQ, 75 процентиль) квартилями. О значимости межгрупповых различий судили по U-критерию Манна-Уитни. Вывод об антигипоксическом действии изучаемых веществ делали при статистически значимом увеличении латентности гибели мышей, установленном не менее чем на двух моделях острой гипоксии. Значимость межгрупповых различий по летальности оценивали по точному критерию Фишера. Все разделы статистического анализа соответствовали критериям intersection-union test, исключающего применение поправок на множественные сравнения. Проверка статистических гипотез выполнялась при критическом уровне значимости Р=0,05.
Результаты представлены в таблице 2.
Снижение токсичности смеси тиоктовой кислоты и эмоксипина в результате их этерификации сопровождалось относительным нарастанием антигипоксической активности полученного эфира. Наиболее ярко это проявилось на модели острой гипоксической гипоксии (асфиксии утопления), устойчивость к которой значимо нарастала после введения тиоксипина в средней (ЭСТД) и максимальной (2ЭСТД) дозах. Антигипоксическое действие тиоксипина нарастало в прямой зависимости от дозы и достигало наибольшей выраженности (151% от медианы контроля) при использовании максимальной дозировки. Смесь тиоктовой кислоты и эмоксипина в дозе, эквимолярной 2ЭСТД тиоксипина, тоже вызывала статистически значимый антигипоксический эффект, увеличивая латентность гибели мышей до 120% от медианы контрольных значений. По выраженности антигипоксического действия тиоксипин в максимальной дозе существенно превосходил смесь своих свободных компонентов в эквимолярной дозировке (Р=0,037). Наличие антигипоксической активности у изучаемого эфира было подтверждено на модели гиперкапнической гипоксии, устойчивость к которой возрастала до 143% от медианы контроля под действием тиоксипина в максимальной дозе. Увеличение латентности гибели мышей, установленное на 2-х моделях гипоксии под действием тиоксипина, позволяет рассматривать его в качестве истинного антигипоксанта. Влияние тиоксипина на устойчивость к гистотоксической гипоксии качественно отличалось от его протекторных эффектов при гипоксической и гиперкапнической гипоксии. Это проявилось снижением латентности гибели мышей до 68 % от медианы контроля под действием тиоксипина в дозе ½ЭСТД. Аналогичный эффект вызывала тиоктовая кислота в эквимолярной дозировке. Ни одно из изучаемых веществ не оказало значимого влияния ни на частоту гибели мышей (Р = 0,47 - 0,56), ни на продолжительность жизни погибших животных (Р=0,19-0,93) при воспроизведении гемической гипоксии.
Таблица 1
Сравнительный анализ острой токсичности тиоксипина (2-этил-6-метилпиридинол-3-ил-тиооктаноата) и эквимолярной смеси его свободных компонентов (тиоктовой кислоты и 2-этил-6-метил-3-оксипиридина гидрохлорида)
мкмоль/кг(мг/кг)
(пробит)
95% ДИ (887 - 1146 мкмоль/кг)
330,9 ± 20,63 мг/кг
95% ДИ (288 - 373 мг/кг)
95% ДИ (658 – 941 мкмоль/кг)
95% ДИ (1131 – 1495 мкмоль/кг)
427,41± 29,28 мг/кг
95% ДИ (368 – 487 мг/кг)
95% ДИ (649 – 964 мкмоль/кг)
Примечание к табл. 1.
1. * - значимые отличия от группы «тиоксипин» по результатам сопоставления LD50 в размерности мкмоль/кг (Р<0,05 по t-критерию)
Таблица 2
Влияние тиоксипина (2-этил-6-метилпиридинол-3-ил-тиооктаноата) и его свободных компонентов (тиоктовой кислоты, 2-этил-6-метил-3-оксипиридина гидрохлорида и их эквимолярной смеси) на устойчивость к острой гипоксии
Группы
0,84 г/л на 0,9% NaCl
(28-35)
(1314-1984)
(1933-2915)
10
(1510-2452)
(29-36)
(1163-2087)
(1853-2710)
10
(1003-1635)
(33-43)
(1622-2442)
(1899-2537)
10
(1265-1730)
(35-51)
(2157-3158)
(2309-4680)
10
(1167-1948)
(29-37)
(1103-1752)
(1867-2399)
10
(992- 2146)
(28-34)
(1647-2888)
(1783-2569)
10
(1299- 1677)
(27-31)
(1303-2181)
(2093-2614)
10
(1477- 2151)
(31-46)
(1183-2095)
(1943-2392)
10
(1110-1700)
(32-38)
(1547-2122)
(1897-2786)
10
(1042-1948)
(29-38)
(1507-2297)
(2415-2965)
10
(954-1885)
(27-35)
(1312-1718)
(2010-3221)
10
(1156-1692)
(28-34)
(1559-2530)
(1959-3611)
10
(1516-1970)
(32-39)
(1232-2125)
(1980-3176)
10
(1127-1784)
Примечания к табл. 2
1. Эксперименты проведены на белых беспородных мышах обоего пола, каждая группа состояла из 5 самцов и 5 самок; во всех сериях (за исключением «гемической гипоксии») моделирование острой гипоксии приводило к 100% летальности мышей. Количество животных серии «гемическая гипоксия» представлено дробью, в числителе которой число погибших животных, а в знаменателе общая численность животных в группе; ни одна из групп этой серии не отличалась от контроля по частоте гибели мышей (Р = 0,47 - 0,56, точный критерий Фишера).
2. * - статистически значимые отличия от контроля (Р<0,05 по U-критерию Мана-Уитни)
3. ** - истинное антигипоксическое действие (по критерию антигипоксической активности, установленной не менее чем на 2-х моделях гипоксии).
| название | год | авторы | номер документа |
|---|---|---|---|
| 3-(N,N-ДИМЕТИЛКАРБАМОИЛОКСИ)-2-ЭТИЛ-6-МЕТИЛПИРИДИНА СУКЦИНАТ, ОБЛАДАЮЩИЙ АНТИГИПОКСИЧЕСКОЙ АКТИВНОСТЬЮ | 1993 |
|
RU2095350C1 |
| КОМПЛЕКСНОЕ СОЕДИНЕНИЕ 6-МЕТИЛУРАЦИЛА С ЯНТАРНОЙ КИСЛОТОЙ, ПРОЯВЛЯЮЩЕЕ АНТИГИПОКСИЧЕСКУЮ АКТИВНОСТЬ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2003 |
|
RU2259357C2 |
| КОМБИНИРОВАННЫЕ ЛЕКАРСТВЕННЫЕ ПРЕПАРАТЫ, СОСТОЯЩИЕ ИЗ СОЛЕЙ 2-ЭТИЛ-3-(N, N-ДИМЕТИЛКАРБАМОИЛОКСИ)-6-МЕТИЛПИРИДИНА С ОРГАНИЧЕСКИМИ И НЕОРГАНИЧЕСКИМИ КИСЛОТАМИ И ЯНТАРНОЙ КИСЛОТЫ, ОБЛАДАЮЩИЕ АНТИГИПОКСИЧЕСКОЙ, АНТИАМНЕСТИЧЕСКОЙ И ПРОТИВОСУДОРОЖНОЙ АКТИВНОСТЬЮ | 2009 |
|
RU2440115C2 |
| Средство, проявляющее антигипоксическую активность | 2022 |
|
RU2809486C2 |
| ВЕЩЕСТВО, ПОВЫШАЮЩЕЕ УСТОЙЧИВОСТЬ К ОСТРОЙ ГИПОБАРИЧЕСКОЙ ГИПОКСИИ | 2001 |
|
RU2191016C1 |
| 1-(1,1-ДИОКСОТИЕТАНИЛ-3)-2-МОРФОЛИНОБЕНЗИМИДАЗОЛА ГИДРОХЛОРИД, ПОВЫШАЮЩИЙ УСТОЙЧИВОСТЬ К ОСТРОЙ ГИПОКСИИ С ГИПЕРКАПНИЕЙ | 2002 |
|
RU2225867C1 |
| ПРИМЕНЕНИЕ 2-АМИНО-7-БРОМ-4-АЦЕТИЛТИАЗОЛО[5,4-b]ИНДОЛА ДЛЯ ЗАЩИТЫ ОРГАНИЗМА ОТ ГИПОБАРИЧЕСКОЙ И ГЕМИЧЕСКОЙ ГИПОКСИИ И/ИЛИ ПЕЧЕНИ ОТ ОТРАВЛЕНИЯ ЧЕТЫРЕХХЛОРИСТЫМ УГЛЕРОДОМ | 2004 |
|
RU2318828C2 |
| ГИДРОХЛОРИД 3-(2-ДИЭТИЛАМИНОЭТИЛТИО)-1,2,4-ТРИАЗИНО[5,6-B] ИНДОЛА, ПОВЫШАЮЩИЙ УСТОЙЧИВОСТЬ ОРГАНИЗМА К ГИПОКСИИ | 1981 |
|
SU978567A1 |
| ВЕЩЕСТВО, ПРОЯВЛЯЮЩЕЕ АНТИГИПОКСИЧЕСКОЕ И АНТИГИПОТЕРМИЧЕСКОЕ СВОЙСТВА | 1983 |
|
SU1832499A3 |
| ПРЕПАРАТ ДЛЯ ВЕТЕРИНАРНОГО ПРИМЕНЕНИЯ, ОБЛАДАЮЩИЙ АНТИОКСИДАНТНОЙ, АНТИГИПОКСИЧЕСКОЙ АКТИВНОСТЯМИ И СТИМУЛИРУЮЩИЙ ОБОНЯНИЕ | 2017 |
|
RU2672917C2 |
Изобретение относится к органической химии и медицине, в частности к новому химическому соединению, а именно к сложному эфиру тиоктовой (α-липоевой) кислоты и 2-этил-6-метил-3-оксипиридина (2-этил-6-метилпиридинол-3-ил-тиооктаноату) формулы (1). Техническим результатом изобретения является получение нетоксичного биологически активного нового химического вещества, обладающего антигипоксической активностью. 1 з.п. ф-лы, 2 табл., 3 пр.
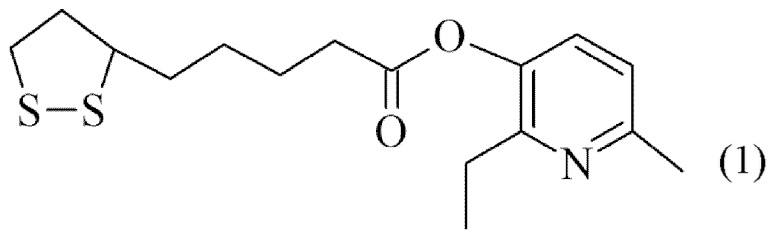
1. Сложный эфир тиоктовой (α-липоевой) кислоты и 2-этил-6-метил-3-оксипиридина (2-этил-6-метилпиридинол-3-ил-тиооктаноат) формулы (1)
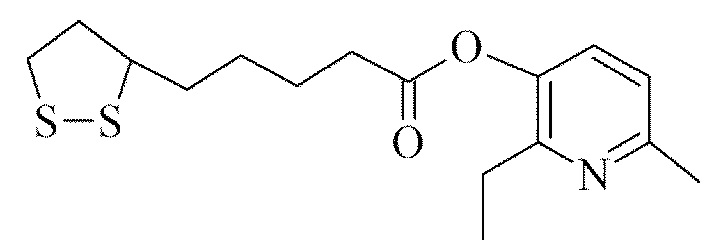 (1).
(1).
2. Соединение по п.1, проявляющее антигипоксическую активность.
| НОВИКОВ В.Е | |||
| и др., Фармакология производных 3-оксипиридина, Обзоры по клин | |||
| фармакол | |||
| и лек | |||
| терапии, 2004, т.3, N.1, c.2-14 | |||
| ВОЛЧЕГОРСКИЙ И.А | |||
| и др., Влияние производных 3-оксипиридина и янтарной кислоты на физическую работоспособность мышей и их устойчивость к острой гипоксии различного генеза, Российский физиологический журнал им | |||
| И.М |
Авторы
Даты
2023-06-13—Публикация
2023-03-21—Подача