Способ относится к медицине, а именно к ее разделам: патологической анатомии, экспериментальной онкологии и патологии.
Рак молочной железы (РМЖ) – чрезвычайно разнообразная группа опухолей с точки зрения гистологии, молекулярного фенотипа и клинического прогноза. Даже несмотря на то, что многие виды РМЖ имеют достаточно хороший прогноз при лечении с выраженным лечебным патоморфозом опухоли, многие аспекты патогенеза рака молочной железы (МЖ) все еще остаются неизвестными.
Инвазивный РМЖ (IDC) является наиболее распространенным типом рака молочной железы как у людей, так и у большинства млекопитающих. Протоковый РМЖ (Ductal carcinoma, DC) представляет собой гетерогенную группу злокачественных новообразований, локализующихся внутри молочных протоков. Протоковый рак также подразделяется на подклассы в зависимости от морфологии и гистофизиологических характеристик опухоли. Дольковая карцинома (Lobular carcinoma, LC) встречается реже, чем протоковый рак, но, как правило, поражает обе МЖ.
Стоит отметить, что как протоковый, так и дольковый раки (так и многие другие варианты РМЖ) МЖ часто гормонально-зависимые опухоли, формирующиеся на фоне хронической гиперэстрогенемии и дисгормональной патологии молочной железы.
Наиболее близким является способ моделирования РМЖ у лабораторных животных путем введения канцерогена N-нитрозо-N-метилмочевины (NMU) (самкам крыс Wistar выполняли однократную внутрибрюшинную инъекцию NMU в дозе 35 мг/кг массы тела, в возрасте 50 дней. NMU разводили в 0,9% раствора натрия хлорида, подкисленном до рН 4 раствором уксусной кислоты, затем крыс взвешивали еженедельно и ежедневно пальпировали на предмет опухолей молочной железы), который принимается нами за прототип (Maren M. Chan, Xin Lu, Faisal M. Merchant, J.Dirk Iglehart, Penelope L. Miron, Gene expression profiling of NMU-induced rat mammary tumors: cross species comparison with human breast cancer, Carcinogenesis, Volume 26, Issue 8, August 2005, Pages 1343–1353, https://doi.org/10.1093/carcin/bgi100).
Недостатком прототипа является то, что опухоли, полученные вышеописанным способом, морфогенетически далеки от опухолей молочной железы, возникающей у человека, поскольку, как правило, не ассоциированы с дисгормональной патологией МЖ и хронической гиперэстрогенемией.
Технический результат заключается в разработке способа моделирования экспериментального рака молочной железы у крыс, морфогенетически максимально приближенного к раку человеческого типа, на фоне предсуществующей дисгормональной патологии МЖ и хронической гиперэстрогенемии.
Технический результат достигается тем, что на первом этапе взрослым половозрелым девственным самкам крыс линии Wistar внутримышечно в нижнюю конечность вводят по 0,5 мл масляного раствора синестрола, в концентрации 20 мг/мл, 1 раз в неделю в течение месяца, затем, спустя 2 недели после последнего введения раствора эстрогена, животным вводят по 0,5 мл 0,02% раствора N-нитрозо-N-метилмочевины в основание паховых молочных желез, преимущественно в проекции сосково-ареолярной области частотой 1 раз в неделю в течение 6 недель.
Животных выводят из эксперимента спустя 12 недель после последнего введения раствора N-нитрозо-N-метилмочевины. Выведение животных из эксперимента осуществляют с помощью передозировки средств для наркоза, в частности эфира.
Таким образом, после проведения первого этапа у животного создается хроническая гиперэстрогенемия и в молочной железе развивается фиброзно-кистозная болезнь, и затем, добиваются канцерогенеза опухолей молочной железы, путем введения N-нитрозо-N-метилмочевины.
ИЗОБРЕТЕНИЕ ПОЯСНЯЕТСЯ ФИГУРАМИ (Фиг. 1-3)
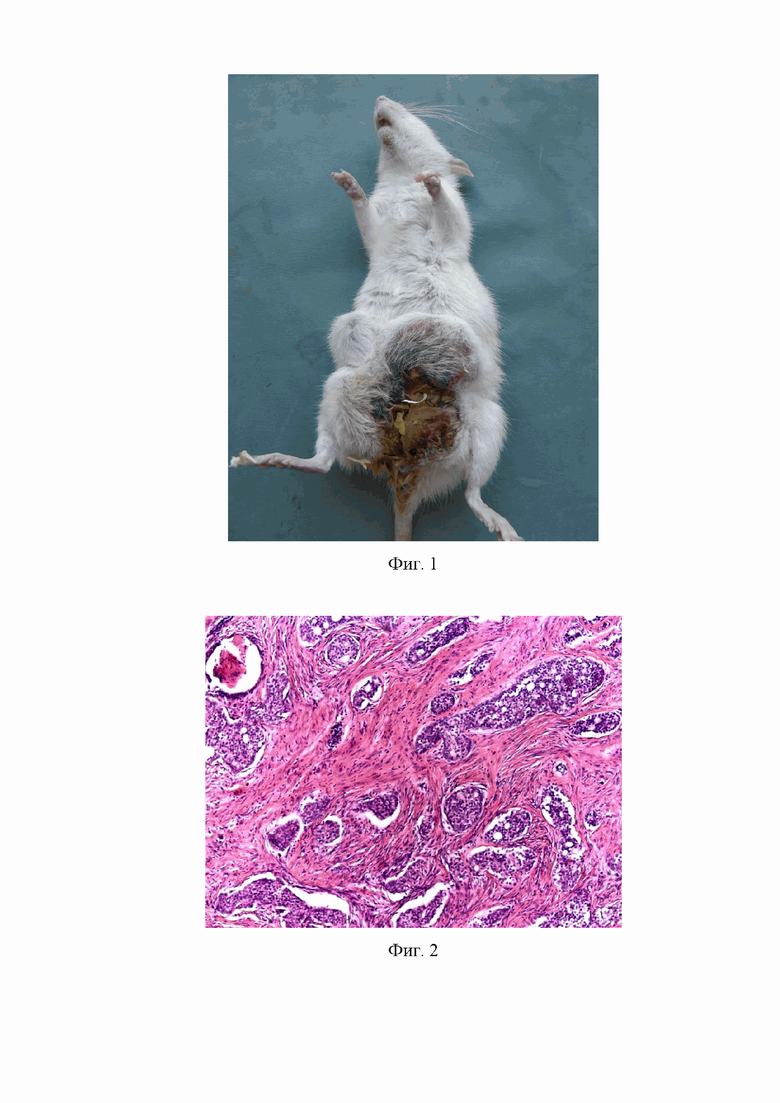
На фиг. 1 - Макроскопический вид N-Нитрозо-N-метилмочевина-индуцированного РМЖ у крысы. В проекции МЖ определяется крупный изъязвленный узел диаметром 3.4 см серовато-красного цвета.
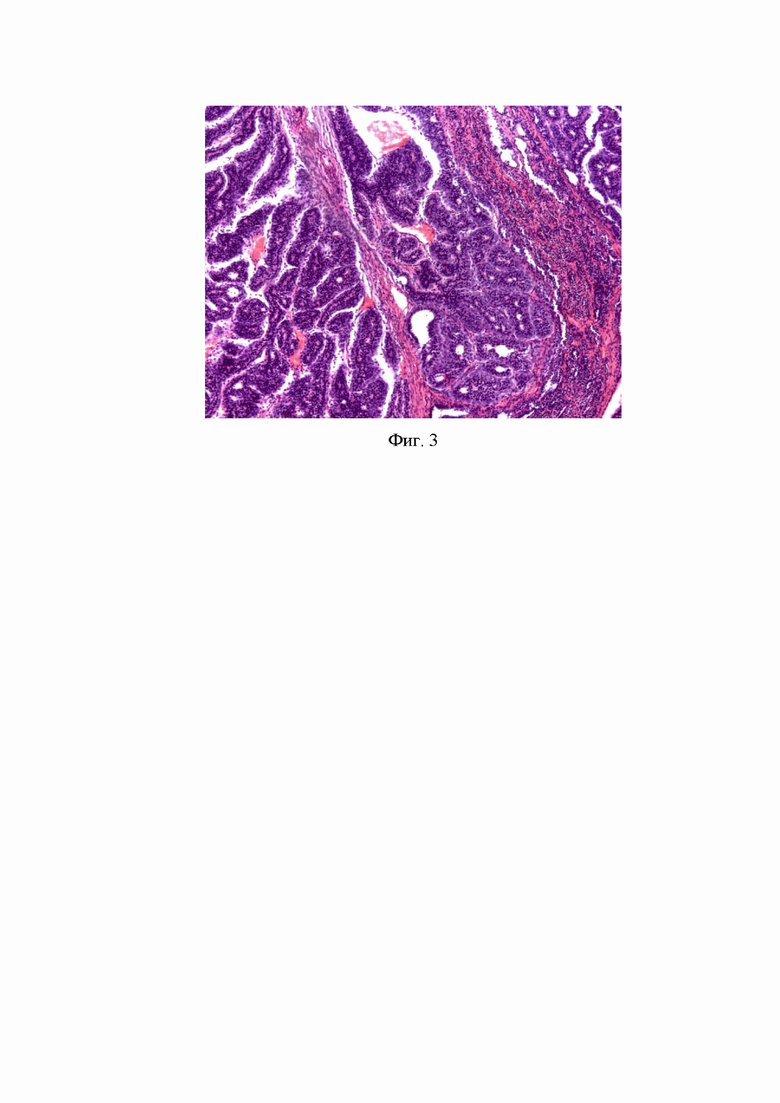
На фиг. 2 - Гистологическая характеристика N-Нитрозо-N-метилмочевина -индуцированного РМЖ у крысы.
На фиг. 3 - Гистологическая характеристика N-Нитрозо-N-метилмочевина -индуцированного РМЖ у крысы.
Опухоль построена из множества атипичных круглых и полиморфных клеток, формирующих атипичные протоковые структуры. Определяется выраженная стромальная инвазия опухоли с десмопластической реакцией стромы. Рак молочной железы, идентичный протоковому раку, возникающему у человека.
Способ используется следующим образом, на первом этапе взрослым половозрелым девственным самкам крыс линии Wistar внутримышечно в нижнюю конечность вводят по 0,5 мл масляного раствора синестрола, в концентрации 20 мг/мл, 1 раз в неделю в течение месяца.
Затем, спустя 2 недели после последнего введения раствора эстрогена, животным вводят по 0,5 мл 0,02% раствора N-нитрозо-N-метилмочевины в основание паховых молочных желез, преимущественно в проекции сосково-ареолярной области частотой 1 раз в неделю в течение 6 недель.
Животных выводят из эксперимента спустя 12 недель после последнего введения раствора N-нитрозо-N-метилмочевины. Выведение животных из эксперимента осуществляют с помощью передозировки средств для наркоза, в частности эфира.
Таким образом, после проведения первого этапа у животного создается хроническая гиперэстрогенемия и в молочной железе развивается фиброзно-кистозная болезнь, и затем, добиваются канцерогенеза опухолей молочной железы, путем введения N-нитрозо-N-метилмочевины. Полученная модель рака молочной железы крысы, морфологически наиболее приближена к раку молочной железы человека.
ПРИМЕР ЭКСПЕРИМЕНТАЛЬНОГО ИСПОЛЬЗОВАНИЯ
Исследование проводилось на базе Института Морфологии человека им. акад. А.П. Авцына.
Крысам линии Wistar, девственным самкам в возрасте 50 дней, в количестве 20 особей, внутримышечно в нижнюю конечность вводили по 0,5 мл масляного раствора синестрола, в концентрации 20 мг/мл, 1 раз в неделю в течение месяца. Затем, спустя 2 недели после последнего введения раствора эстрогена, животным вводили по 0,5 мл 0,02% раствора N-нитрозо-N-метилмочевины в основание паховых молочных желез, преимущественно в проекции сосково-ареолярной области частотой 1 раз в неделю в течение 6 недель.
Животных выводили из эксперимента спустя 12 недель после последнего введения раствора N-нитрозо-N-метилмочевины, с помощью передозировки средств для наркоза, в частности эфира. Опухоли молочной железы иссекали, фиксировали в 10% растворе нейтрального формалина, после чего изготавливали гистологические препараты по стандартной методике и окрашивали гематоксилином и эозином. Полученные препараты изучали посредством световой микроскопии. Опухоль построена из множества атипичных круглых и полиморфных клеток, формирующих атипичные протоковые структуры. Определяется выраженная стромальная инвазия опухоли с десмопластической реакцией стромы, что морфологически характерно для протокового рака молочной железы человека.
Таким образом, предложенная нами методика получения N-Нитрозо-N-метилмочевина-индуцированного экспериментального рака молочной железы у крыс позволяет смоделировать эпителиальные опухоли молочной железы животных, по гистогенетическим характеристикам, наиболее приближенные к опухолям МЖ, встречающихся у человека. При этом достигается четкая экспериментальная модель человеческого РМЖ на фоне хронической гиперэстрогенемии и дисгормональной патологии МЖ.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПРЕДУПРЕЖДЕНИЯ И ПОДАВЛЕНИЯ РОСТА РАКА МОЛОЧНОЙ ЖЕЛЕЗЫ В ЭКСПЕРИМЕНТЕ | 2005 |
|
RU2301073C2 |
| Способ препекторальной реконструкции молочных желез после кожесохраняющей мастэктомии | 2022 |
|
RU2802144C1 |
| Способ отсроченной препекторальной реконструкции после мастэктомии при раке молочной железы с помощью перманентного имплантата | 2024 |
|
RU2831000C1 |
| СПОСОБ ПОДКОЖНОЙ РАДИКАЛЬНОЙ МАСТЭКТОМИИ ПО ПОВОДУ РАКА | 2004 |
|
RU2267297C1 |
| СПОСОБ ЛЕЧЕНИЯ РАКА ПЕДЖЕТА МОЛОЧНОЙ ЖЕЛЕЗЫ | 2006 |
|
RU2325920C1 |
| СПОСОБ ОРГАНОСОХРАНЯЮЩЕГО ЛЕЧЕНИЯ РАКА МОЛОЧНОЙ ЖЕЛЕЗЫ | 2012 |
|
RU2481075C1 |
| Способ кожесохранной мастэктомии с реконструкцией деэпидермизированным кожно-жировым лоскутом и свободной пересадкой сосково-ареолярного комплекса при птозированных молочных железах | 2024 |
|
RU2830358C2 |
| СПОСОБ МОДЕЛИРОВАНИЯ ГИНЕКОМАСТИИ В ЭКСПЕРИМЕНТЕ | 2006 |
|
RU2330327C1 |
| СПОСОБ ЛЕЧЕНИЯ РАКА МОЛОЧНОЙ ЖЕЛЕЗЫ | 2009 |
|
RU2411953C1 |
| СПОСОБ ПРОФИЛАКТИКИ КАНЦЕРОГЕННОГО ДЕЙСТВИЯ МЕТИЛНИТРОЗОМОЧЕВИНЫ У ЭКСПЕРИМЕНТАЛЬНЫХ ЖИВОТНЫХ | 2009 |
|
RU2410114C1 |
Изобретение относится к области медицины, а именно к способу моделирования N-нитрозо-N-метилмочевина-индуцированного рака молочной железы у крыс на фоне хронической гиперэстрогенемии. Способ моделирования N-нитрозо-N-метилмочевина-индуцированного рака молочной железы у крыс на фоне хронической гиперэстрогенемии, включающий введение N-нитрозо-N-метилмочевины крысам линии Wistar, отличающийся тем, что на первом этапе взрослым половозрелым девственным самкам крыс линии Wistar внутримышечно в нижнюю конечность вводят по 0,5 мл масляного раствора синестрола, в концентрации 20 мг/мл, 1 раз в неделю в течение месяца, затем, спустя 2 недели после последнего введения раствора эстрогена, животным вводят по 0,5 мл 0,02% раствора N-нитрозо-N-метилмочевины в основание паховых молочных желез, преимущественно в проекции сосково-ареолярной области частотой 1 раз в неделю в течение 6 недель. Вышеуказанное изобретение позволяет моделировать экспериментальный рак молочной железы у крыс, морфогенетически максимально приближенный к раку человеческого типа, на фоне предсуществующей дисгормональной патологии МЖ и хронической гиперэстрогенемии. 3 ил., 1 пр.
Способ моделирования N-нитрозо-N-метилмочевина-индуцированного рака молочной железы у крыс на фоне хронической гиперэстрогенемии, включающий введение N-нитрозо-N-метилмочевины крысам линии Wistar, отличающийся тем, что на первом этапе взрослым половозрелым девственным самкам крыс линии Wistar внутримышечно в нижнюю конечность вводят по 0,5 мл масляного раствора синестрола, в концентрации 20 мг/мл, 1 раз в неделю в течение месяца, затем, спустя 2 недели после последнего введения раствора эстрогена, животным вводят по 0,5 мл 0,02% раствора N-нитрозо-N-метилмочевины в основание паховых молочных желез, преимущественно в проекции сосково-ареолярной области частотой 1 раз в неделю в течение 6 недель.
| CHAN, M.M., et al | |||
| Gene expression profiling of NMU-induced rat mammary tumors: cross species comparison with human breast cancer | |||
| Carcinogenesis | |||
| Способ обработки целлюлозных материалов, с целью тонкого измельчения или переведения в коллоидальный раствор | 1923 |
|
SU2005A1 |
| Прибор для получения стереоскопических впечатлений от двух изображений различного масштаба | 1917 |
|
SU26A1 |
| Телефонный трансформатор | 1922 |
|
SU1343A1 |
| CARRERA, M.P., et al | |||
| Renin-Angiotensin System-Regulating Aminopeptidase Activities Are Modified in the Pineal Gland of Rats with Breast Cancer Induced by | |||
Авторы
Даты
2023-06-14—Публикация
2022-11-01—Подача