Изобретение относится к области медицины, а именно к биологическим препаратам, состоящим из молекул, присутствующих в нормальных физиологических условиях в организме человека.
Плазма крови, являющаяся одним из многочисленных компонентов донорской крови, может быть использована в качестве самостоятельного терапевтического препарата (свежезамороженная плазма), а также в качестве исходного сырья для получения многочисленных фармацевтических продуктов ее фракционирования. В процессе переработки смесь плазмы нескольких сотен здоровых доноров предварительно проходит контроль на отсутствие маркеров гемотрансмиссивных инфекций методами иммуноферментного анализа и полимеразной цепной реакции [1], затем от одного до пяти этапов низкотемпературного фракционирования с использованием спиртовых осадителей в соответствии с методом Кона, в результате чего получают нативные белки плазмы крови, к которым относятся фибриноген, иммуноглобулины, составляющие основную массу белков, альфа- и бета-глобулины и альбумин [2]. На стадии выделения альбуминов также получают побочный продукт – супернатант, представляющий собой водно-спиртовой раствор, содержащий органические и минеральные соединения, которые могут быть использованы для создания широкого спектра лекарственных препаратов, биологических добавок и компонентов питательных сред. Получаемый ценный супернатант ранее не подвергался более глубокой переработке для получения дополнительных продуктов фракционирования плазмы, помимо перечисленных ранее. Биологически активный пептидно-аминокислотный препарат, описываемый в предлагаемом изобретении, изготавливается из данного побочного продукта – супернатанта.
Известен способ получения кислого альфа-1-гликопротеина, при котором балластный осадок сыворотки крови человека гомогенизируют в воде и растворяют в гидрооксиде натрия. Полученный раствор охлаждают до 3-15°С и вносят в него этанол. После центрифугирования смеси надосадочную жидкость одновременно концентрируют и подвергают диафильтрации на полых волокнах с последующим хроматографическим выделением целевого продукта [3].
Недостатком данного способа является низкий выход конечного продукта – 0,3 грамма из литра исходной плазмы, что делает невозможным в условиях постоянного дефицита донорской крови организацию массового производства получаемого препарата.
Известен способ выделения природных антимикробных пептидов (АМП) из лейкоцитарно-эритоцитарно-тромбоцитарной массы крови, предварительно подверженной гемолизу трипсином [4]. Выделение АМП проводят методом жидкостной хроматографии на разделительной колонке с трехкратным использованием Сефадекса G-25. Способ позволяет оптимизировать технологию выделения наиболее полной фракции естественных низкомолекулярных пептидов, содержащих АМП, несколько раз использовать Сефадекс G-25 после промывки, регенерации и высушивания, повысить биологическую ценность АМП.
Недостатком известного способа является необходимость использования значительного количества перекиси водорода, а также использование в качестве исходного сырья эритроцитов, одного из важнейших компонентов крови.
Известен способ получения из крови эмбрионов коров биологически активного препарата, представляющего собой смесь неустановленного состава, которая содержит высокоактивные низкомолекулярные пептиды, аминокислоты, производные нуклеиновых кислот и другие компоненты. Способ заключается в том, что предварительно замороженную при температуре -18±2°С кровь эмбрионов коров размораживают, сепарируют и подвергают ультрафильтрации с использованием двух последовательно подключаемых мембран с пределами задержания 100 и 10 кДа соответственно. Изобретение позволяет повысить специфические свойства лекарственного препарата, выделенного из крови крупного рогатого скота, и получаемой на его основе фармацевтической композиции, используемой при лечении нарушений церебрального кровообращения, обмена веществ, нарушений периферического кровообращения, термических и лучевых поражений тканей, а также при лечении ран, язв и воспалительных процессов без образования келоидных рубцов [5].
К недостаткам данного способа относится ксеногенность получаемого биологически активного препарата по отношению к организму человека, а также лишь частичное использование представляющих фармацевтический интерес компонентов крови, выделенных на стадии сепарации сырья.
Наиболее близким к заявляемому изобретению по совокупности существенных признаков, является способ получения депротеинизированного гомодеривата крови телят под торговым названием «Актовегин» [6]. Данный препарат представляет собой депротеинизированный, не содержащий эндотоксинов и антигенов, ультрафильтрат крови телят, содержащий более 200 биоактивных компонентов. Процесс его производства заключается в том, что кровь телят подвергают предварительной подготовке, технологические этапы которой производителями не приводятся и причислены к «ноу-хау», и депротеинизации путем двухстадийной ультрафильтрации с использованием сит с отсечением по молекулярной массе 5кДа. Далее сырье подвергают вакуумной перегонке, фильтрованию оставшегося осадка через фильтр с пористостью 0,45 мкм и титрованию до рН 6,4 с последующей стерилизующей фильтрацией через фильтры с пористостью 0,45 мкм и 0,2 мкм.
Недостатком указанного способа является ксеногенность получаемого препарата, что повышает риск возникновения негативных последствий у принимающих терапию пациентов.
Задача, на решение которой направлено заявленное изобретение, заключается в разработке биологически активного пептидно-аминокислотного препарата, обладающего нейропротективными свойствами и применяющегося при лечении пациентов с острой и хронической цереброваскулярной патологией, постинсультными когнитивными нарушениями и периферической ишемией.
Техническим результатом настоящего изобретения является получение биологически активного пептидно-аминокислотного препарата, лишенного ксеногенности и обладающего повышенной нейропротекторной активностью, а также достижение более полной переработки человеческой плазмы крови и повышение выхода конечного продукта по сравнению с известными способами.
Указанный технический результат в способе получения биологически активного пептидно-аминокислотного препарата на основе плазмы крови человека достигается за счет того, что супернатант, полученный в процессе выделения нативных белков из плазмы крови человека, фильтруют через мембранные фильтры с порогом отсечения по молекулярной массе в пределах 10 ÷ 30 кДа и концентрируют до суспензионного состояния посредством вакуумной перегонки на ротационном испарителе или с использованием хроматографических методов, после чего образовавшуюся суспензию подвергают вакуумной сушке в среде инертного газа при температуре 55°С или супернатант подвергают конвекционной, лиофильной или распылительной сушке сразу до получения сухого остатка, который затем диспергируют до визуальной однородности и перерастворяют в воде для инъекций с использованием ультразвукового диспергатора, при этом осуществляют контроль рН в диапазоне от 5,0 до 6,0. Полученный раствор пептидно-аминокислотного препарата подвергают трехкратной ультрафильтрации с использованием мембранных фильтров сначала пористостью 5 и 0,45 мкм, после чего его стерилизуют с помощью фильтров пористостью 0,22 мкм.
Новизна способа заключается в том, что для изготовления биологически активного пептидно-аминокислотного препарата используется супернатант, получаемый на V стадии выделения методом Кона нативных белков из плазмы крови человека.
В основе изготовления биологически активного пептидно-аминокислотного препарата лежит использование супернатанта, побочного продукта выделения нативных белков из плазмы крови человека [2], представляющего собой водно-спиртовой раствор, богатый аминокислотами, пептидами, протеинами, питательными веществами, минеральными соединениями, а также другими органическими и неорганическими веществами. Используемая для фракционирования плазма представляет собой смесь плазмы нескольких сотен здоровых доноров, прошедшая стадию контроля отсутствия маркеров гемотрансмиссивных инфекций и лишенная групповой и резус-принадлежности.
На практике способ получения биологически активного пептидно-аминокислотного препарата на основе человеческой плазмы крови осуществляют следующим образом.
Супернатант, полученный после выделения нативных белков из плазмы крови здоровых доноров, фильтруют через мембранные фильтры с порогом отсечения по молекулярной массе в пределах 10 ÷ 30 кДа и концентрируют с использованием вакуумной перегонки на ротационном испарителе или с использованием различных хроматографических методов (ионообменной хроматографии, гидрофобной хроматографии на сорбенте Sepharose, гель-фильтрационной хроматографии на сорбенте Sephadex G-10) до суспензионного состояния. Далее суспензию подвергают вакуумной сушке в среде инертного газа при температуре не более 55°С во избежание окисления аминокислот и денатурации пептидов. Возможны также варианты концентрирования супернатанта до сухого состояния, заключающиеся в том, что раствор подвергают конвекционной сушке в сушильном шкафу при температуре 55°С либо лиофильной сушке при температуре -100°С, либо распылительной сушке в потоке азота. После этого сухой остаток диспергируют до визуальной однородности и перерастворяют в воде для инъекций с использованием ультразвукового диспергатора для предотвращения конгломерации частиц сухого остатка. В процессе перерастворения осуществляют контроль уровня кислотности среды для поддержания стабильности химического состава: рН должен находиться в диапазоне от 5,0 до 6,0. Полученный раствор пептидно-аминокислотного препарата подвергают трехкратной ультрафильтрации: с целью достижения визуальной прозрачности и однородности раствор сначала пропускают через мембранные фильтры пористостью 5 мкм и 0,45 мкм, затем стерилизуют раствор с использованием фильтров пористостью 0,22 мкм. В результате получают биологически активный пептидно-аминокислотного препарат из побочного продукта фракционирования плазмы крови человека. Выход сухого остатка с 1 л исходного раствора супернатанта представлен в таблице 1 и в среднем составляет 6,6 г.
Таблица 1
Выбор порога отсечения, обеспечивающего получение исключительно пептидно-аминокислотной фракции с молекулярной массой до 30 кДа, подтверждается литературными данными и обусловлен необходимостью депротеинизации исходного раствора для получения препарата с целью исключения вероятности развития иммунного ответа организма.
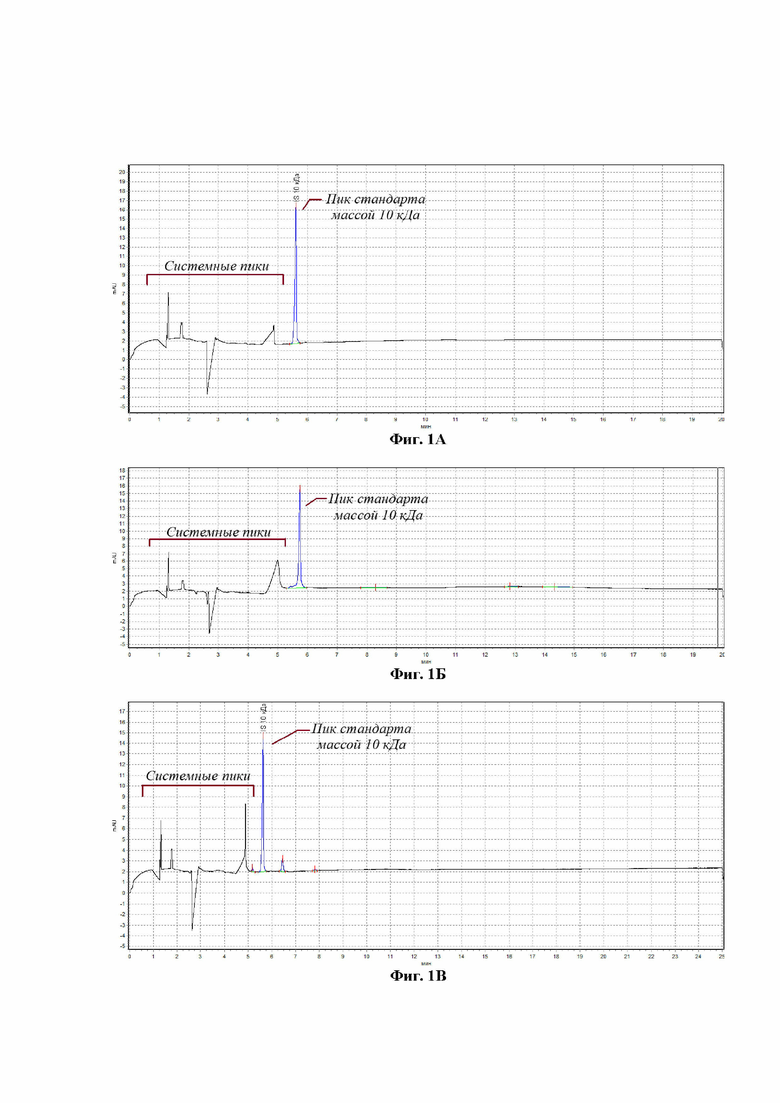
Определение границы отделения компонентов по молекулярной массе и контроль чистоты пептидно-аминокислотного препарата осуществляли методом капиллярного гель-электрофореза с использованием системы «Капель-105М» путем разделения SDS-белковых комплексов по методике ПУ 49-2016 издания 2018 г. компании ООО «Люмэкс-Маркетинг». Результаты электрофоретического анализа пептидно-аминокислотных препаратов, изготовленных из супернатанта, прошедшего предварительно стадию ультрафильтрации через мембраны с порогом отсечения по молекулярной массе в пределах 10 ÷ 30 кДа, представлены на Фиг. 1А и 1Б соответственно. На фигурах 1А, 1Б и 1В показано полное отсутствие белков с молекулярной массой выше 10 кДа как в препарате сравнения Актовегине, так и в пептидно-аминокислотном препарате, получаемом заявленным способом с использованием мембранных фильтров с выбранным порогом отсечения. Исходя из данных, полученных в ходе электрофоретического анализа, подкрепленных научно-технической литературой, можно сделать вывод о достаточности выбранного порога отсечения не менее 10 и не более 30 кДа.
Подлинность и чистоту пептидно-аминокислотного препарата определяли методами высокоэффективной жидкостной хроматографии (ВЭЖХ), биуретовой реакции, капиллярного электрофореза, спектрофотометрии и спектральным методом анализа с индуктивно связанной плазмой.
В Таблице 2 представлена сравнительная характеристика средних показателей качества трех серий пептидно-аминокислотного препарата на основе плазмы крови человека, полученного заявленным способом, и препарата сравнения.
Таблица 2
возникновение сине-фиолетового окрашивания
глицин,
аргинин,
серин,
аланин,
тирозин,
лизин
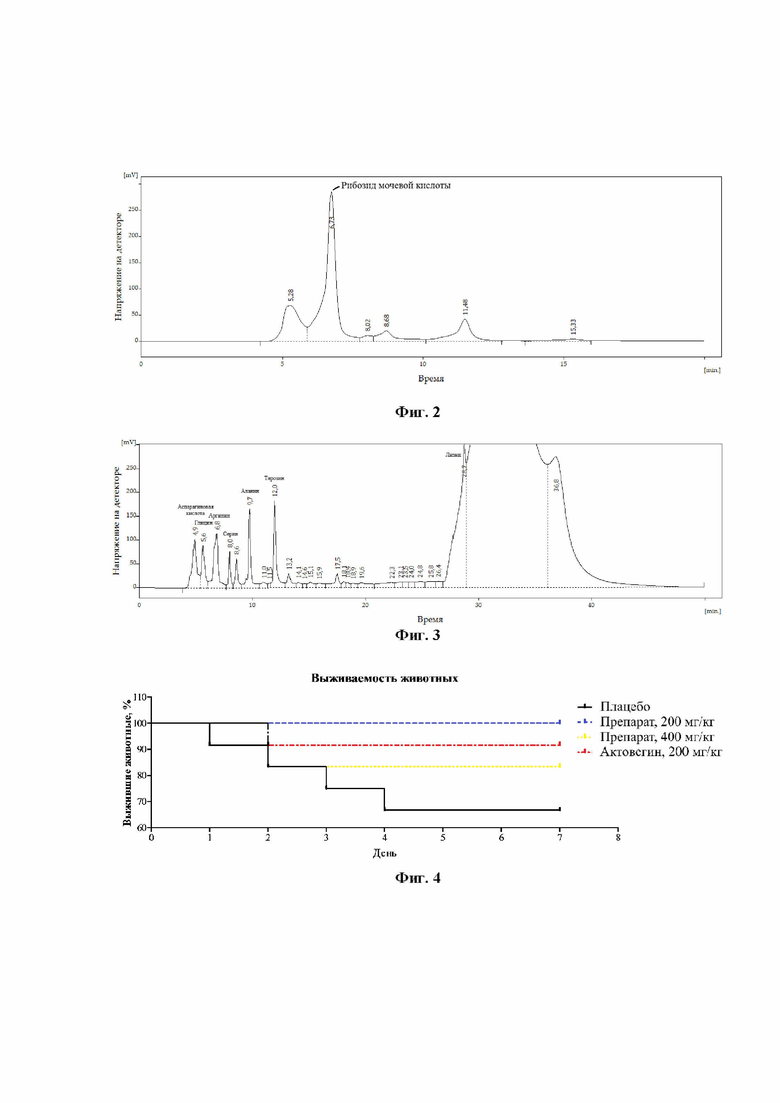
На Фиг. 2 представлена хроматограмма пептидно-аминокислотного препарата, полученная методом ВЭЖХ в условиях изократического режима элюирования со скоростью потока подвижной фазы (фосфатный буфер с метанолом, 82:18) 0,5 мл/мин. Результаты анализа показывают наличие в составе препарата рибозида мочевой кислоты.
Результаты хроматографического качественного анализа пептидно-аминокислотного препарата на содержание аминокислот представлены на Фиг. 3. Хроматограмма (Фиг. 3) получена методом ВЭЖХ в условиях градиентного элюирования с использованием ацетатного буфера и органического растворителя с добавлением модификатора. Исследуемые образцы препарата предварительно проходили пробоподготовку с применением фенилизотиоцианата. Таким образом, в состав пептидно-аминокислотного препарата входит около семи незаменимых аминокислот.
Для оценки нейропротекторных свойств и эффективности получаемого предлагаемым способом пептидно-аминокислотного препарата выполнены экспериментальные исследования по изучению выживаемости лабораторных животных на модели ишемии головного мозга.
В одной серии эксперимент проводился на 60 самцах белых лабораторных крыс весом 250-300 г, возрастом 3-4 месяца. Количество животных (n = 12 в каждой из групп) было достаточным для того, чтобы оценить характер и частоту проявления регистрируемых эффектов, и провести надлежащую статистическую обработку. Помимо этого, количество животных было минимально достаточным с точки зрения этических принципов. Эксперименты выполнены в пяти сериях опытов.
В первый день исследования выполнялось моделирование патологии методом необратимой одномоментной окклюзии общих сонных артерий. Далее на протяжении семи дней тестируемый препарат вводился животным из опытной группы внутримышечно в дозах 200 или 400 мг/кг/сут; животным из группы сравнения вводился препарат сравнения «Актовегин» в дозе 200 мг/кг/сут. Крысам из контрольной группы аналогично вводились эквивалентные объемы физиологического раствора.
В работе использовались методы, широко применяемые в доклинических исследованиях фармакодинамических свойств церебропротективных лекарственных средств. В ходе исследования контролировались такие показатели, как психоневрологическое состояние животных, нарушения сенсомоторных функций, уровень локального мозгового кровотока и когнитивные функции крыс. Сведения о выживаемости животных после необратимой перевязки общих сонных артерий, представленные в виде кривой, построенной методом Каплана-Мейера, представлены на Фиг. 4.
Из результатов эксперимента, представленных на Фиг. 4 следует, что наибольший процент выживаемости, составляющий 100%, соответствует группе животных, которой вводили пептидно-аминокислотный препарат в дозах 200 мг/кг/сут, наименьший (66,67%) – группе, которой вводили плацебо. Процент выживаемости в группе животных, получавших препарат Актовегин, составляет 91,67%. Исходя из полученных данных, можно сделать вывод о наличии положительного эффекта у крыс, перенесших необратимую перевязку общих сонных артерий, от введения пептидно-аминокислотного препарата и препарата «Актовегин» в отличие от плацебо.
Полученные результаты исследований по изучению возможности использования биологически активного пептидно-аминокислотного препарата на основе плазмы крови человека, изготавливаемого предложенным авторами способом, при ишемии головного мозга у крыс, вызванной необратимой перевязкой общих сонных артерий, позволяют утверждать, что данный препарат обладает существенным нейропротекторным действием и не уступает по эффективности препарату сравнения Актовегину в отношении влияния на выживаемость животных и сроки восстановления их моторных и неврологических функций.
Предлагаемый способ обеспечивает получение биологически активного пептидно-аминокислотного препарата со стабильным составом за счет удаления в процессе фильтрации протеиновой фракции плазмы крови с молекулярной массой более 30 кДа, что исключает опасность развития побочных эффектов, в первую очередь аутоиммунизации.
Преимуществом настоящего изобретения является исключение ксеногенности получаемого конечного биологически активного пептидно-аминокислотного препарата на основе плазмы крови человека, обладающего также повышенной нейропротекторной активностью, а также обеспечение более эффективной переработки исходного сырья и высокого выхода пептидно-аминокислотного продукта, составляющего в среднем 6,6 г с 1 л супернатанта, по сравнению с известными способами.
Источники информации
1. Национальный стандарт РФ ГОСТ Р 52249-2009 "Правила производства и контроля качества лекарственных средств" (утв. и введен в действие приказом Федерального агентства по техническому регулированию и метрологии от 20 мая 2009 г. N 159-ст).
2. Тхай С. В., Русанов В. М., Уйба В. В. Производство препаратов крови : особенности технологии, организации и технического обеспечения / С. В. Тхай, В. М. Русанов, В. В. Уйба. – Москва : Медпрактика-М, 2014. – 151 с.
3. Авторское свидетельство №1662039, Способ получения кислого альфа-1-гликопротеина, МПК A61K39/00, / Лютов А. Г., Еникеева С. А., Алешкин В. А., Новикова Л. И., Хакимова Ф. З. ; патентообладатель Уфимский научно-исследовательский институт вакцин и сывороток имени И.И. Мечникова, опубл. 10.02.1996.
4. Патент RU №2729016, Способ выделения природных антимикробных пептидов из лейкоцитарно-эритоцитарно-тромбоцитарной массы крови, МПК C07K1/12, C12P21/06, G01N30/02. / Базиков И. А., Мальцев А. Н., Батурин В. А., Рамеш К. Гоял, А. Наджирул Амин, Ефременко А. А., патентообладатели Базиков И. А., Федеральное государственное бюджетное образовательное учреждение высшего образования "Ставропольский государственный медицинский университет" Министерства здравоохранения Российской Федерации (ФГБОУ ВО СтГМУ Минздрава Росси, опубл. 04.08.2020.
5. Патент EA № 000633В1, Способ получения из крови эмбрионов коров биологически активного препарата и фармацевтическая композиция на его основе с радиопротекторной, антигипоксической, иммуномоделирующей, ранозаживляющей и противогерпетической активностью, / Пленина Л. В., Хлюстов С. В., Федорова Н. И., Бабук Л. В., Федулов А. С., Марченко Л. Н., патентообладатель Предприятие диагностических и лекарственных препаратов «Диалек», опубл. 29.12.1999.
6. Способ получения депротеинизированного гомодеривата крови телят под торговым названием «Актовегин», Machicao, F. Pleiotropic neuroprotective and metabolic effects of Actovegin's mode of action / F. Machicao, D. F. Muresanu, H. Hundsberger [et al.] // Journal of the Neurological Sciences. – 2012. – V. 322. – P. 222-227.
Изобретение относится к области медицины, а именно к способу получения биологически активного пептидно-аминокислотного препарата на основе плазмы крови человека. Способ получения биологически активного пептидно-аминокислотного препарата на основе плазмы крови человека заключается в том, что супернатант, полученный в процессе выделения нативных белков из плазмы крови доноров, фильтруют через мембранные фильтры с порогом отсечения по молекулярной массе в пределах 10÷30 кДа и концентрируют до суспензионного состояния, после чего образовавшуюся суспензию подвергают вакуумной сушке в среде инертного газа при температуре 55°С до получения сухого остатка, который затем диспергируют до визуальной однородности и перерастворяют в воде для инъекций с использованием ультразвукового диспергатора, при этом осуществляют контроль рН в диапазоне от 5,0 до 6,0, полученный раствор пептидно-аминокислотного препарата подвергают трехкратной ультрафильтрации с использованием мембранных фильтров сначала пористостью 5 и 0,45 мкм, после чего его стерилизуют с помощью фильтров пористостью 0,22 мкм. Вышеуказанное изобретение позволяет получить биологически активный пептидно-аминокислотный препарат, лишенный ксеногенности и обладающий повышенной нейропротекторной активностью, достигнуть более полной переработки человеческой плазмы крови и повысить выход конечного продукта по сравнению с известными способами. 3 з.п. ф-лы, 4 ил., 2 табл.
1. Способ получения биологически активного пептидно-аминокислотного препарата на основе плазмы крови человека, заключающийся в том, что супернатант, полученный в процессе выделения нативных белков из плазмы крови доноров, фильтруют через мембранные фильтры с порогом отсечения по молекулярной массе в пределах 10÷30 кДа и концентрируют до суспензионного состояния, после чего образовавшуюся суспензию подвергают вакуумной сушке в среде инертного газа при температуре 55°С до получения сухого остатка, который затем диспергируют до визуальной однородности и перерастворяют в воде для инъекций с использованием ультразвукового диспергатора, при этом осуществляют контроль рН в диапазоне от 5,0 до 6,0, полученный раствор пептидно-аминокислотного препарата подвергают трехкратной ультрафильтрации с использованием мембранных фильтров сначала пористостью 5 и 0,45 мкм, после чего его стерилизуют с помощью фильтров пористостью 0,22 мкм.
2. Способ получения биологически активного пептидно-аминокислотного препарата на основе плазмы крови человека по п. 1, заключающийся в том, что супернатант концентрируют до суспензионного состояния посредством вакуумной перегонки на ротационном испарителе.
3. Способ получения биологически активного пептидно-аминокислотного препарата на основе плазмы крови человека по п. 1, заключающийся в том, что супернатант концентрируют до суспензионного состояния с использованием хроматографических методов.
4. Способ получения биологически активного пептидно-аминокислотного препарата на основе плазмы крови человека по п. 1, заключающийся в том, что суспензию подвергают конвекционной, лиофильной или распылительной сушке.
| MACHICAO, F., et al | |||
| Pleiotropic neuroprotective and methabolic effects of Actovegin's mode of action | |||
| Ледорезный аппарат | 1921 |
|
SU322A1 |
| ПРИСПОСОБЛЕНИЕ ДЛЯ ПРЕВРАЩЕНИЯ КИНЕТИЧЕСКОЙ ЭНЕРГИИ КАПЕЛЬНЫХ, ПАРООБРАЗНЫХ И ГАЗООБРАЗНЫХ ЖИДКОСТЕЙ В ЭНЕРГИЮ ДАВЛЕНИЯ | 1923 |
|
SU633A1 |
| EP 976759 A2, 02.02.2000 | |||
| WO 2017058877 A1, 06.04.2017 | |||
| WO 2011149472 A1, 01.12.2011 | |||
| EP 2968455 B1, 17.07.2019. | |||
Авторы
Даты
2023-07-07—Публикация
2022-12-28—Подача