Изобретение относится к области медицины и может быть использовано для устранения острых судорожных состояний различной этиологии.
Судорожные состояния могут быть вызваны разными причинами, из которых наиболее распространенными являются эпилепсия, воздействие химических веществ, гипоксия и другие факторы. В острых случаях может развиваться судорожный синдром - опасное жизнеугрожающее состояние, требующее экстренной помощи пострадавшим. [1. Болезни нервной системы: Руководство для врачей в 2-х томах. Под ред. Яхно Н. Н., Штульмана Д. Р. М.: Медицина, 2008, 744 с]. Судорожный синдром часто сопровождается потерей сознания, острым нарушением дыхания и кровообращения, отеком мозга и другими осложнениями, нередко приводящими к смерти. Скоротечность летальных осложнений требует оказания первой помощи немедленно, то есть в течение нескольких минут (на догоспитальном этапе). Это обстоятельство диктует требования к препаратам первой помощи при судорожном синдроме, которые должны оказывать быстрый эффект и при этом быть простыми в употреблении.
Современная фармакология располагает широким набором противосудорожных средств, но ни одно из них в полной степени не удовлетворяет требованиям, предъявляемым к препаратам первой помощи [2. Ивченко Е.В., Кузьмин А.А., Федонюк В.П. и др. Итоги и перспективы совершенствования средств и методов медицинской защиты от неблагоприятных факторов химической природы // Военно-медицинский журнал - 2019. -Т. 340, №9. - С.14-21].
Например, такие противосудорожные средства, как производные барбитуровой кислоты (фенобарбитал, бензонал), назначаются перорально [3. Машковский М. Д. Лекарственные средства. 16 изд., М.; Новая Волна, 2012, с. 35-37], что не позволяет их использовать на фоне уже развившихся судорог.Препараты другой группы - вальпроаты, широко используемые для лечения эпилепсии, недостаточно активны и обладают замедленным эффектом [4. Карпова В.И., Пылаева О.А., Мухин К.Ю., Петрухин А.С. Вальпроевая кислота и ее соли - от истории открытия до клинической практики (исторический очерк) // Русский журнал детской неврологии. -2011. - Vol.6(3). - С.36-46. 5. Tasso S.M., Moon S.Ch., Brano-Blancha L.E., Estiu G.L. Characterization of the anticonvulsant profile of valpromide derivatives//Bioorg. Med. Chem. -2004. - Vol.12 (14).-P. 3857-3869. 6. Haines K.M., Matson L.M., Dunn E.N., Ardinger C.E., Stubbs R.L., Bibi D., McDonough J.H., Bialer M. Comparative efficacy of valnoctamide and sec-butylpropylacetamide (SPD) in terminating nerve agent-induced seizures in pediatric rats//Epilepsia. -2019. -60 (2). -P. 315-321], поэтому могут рассматриваться скорее как средства профилактического и курсового назначения. Атропин и его аналоги, применяемые при отравлениях фосфо-рорганическими отравляющими веществами, эффективны далеко не при всех типах судорог, и к тому же довольно токсичны [7. Под ред. Куценко С.А. Военная токсикология, радиобиология и медицинская защита. - Санкт-Петербург: Фолиант, 2004, 528 с. 8. Alozi М., Rawas-Qalaji М. Treating organophosphates poisoning: management challenges and potential solutions // Crit Rev Toxicol.- 2020.- Vol.50(9).- P. 764-779].
Наконец, наиболее перспективная группа антиконвульсантов - бензодиазепины, также обладают рядом существенных недостатков. Препараты этой группы мало растворимы в воде, что затрудняет создание инъекционных форм с высокой концентрацией активного вещества, которые были бы эффективны при внутримышечном введении при генерализованных судорогах. В частности, феназепам выпускается в виде 0,1%-ного раствора (per. №: ЛСР-001772/09 от 10.03.09), диазепам (сибазон) - в виде 0,5%-ного раствора [9. Машковский М. Д. Лекарственные средства. 16 изд., М.; Новая Волна, 2012, с. 75], также как и мидазолам [10. Видаль. Электронный справочник лекарственных средств. 2014 г. ]. Средний разовый объем раствора сибазона при внутримышечной инъекции составляет 2 мл (соответствует 10 мг препарата), а этого далеко не всегда достаточно для устранения судорожного синдрома у человека.
Существует возможность альтернативного пути введения бензодиазепиновых препаратов - путем интраназальной доставки. В этом случае в качестве носителя используются неводные растворители [11. Чой Йонг Мун, Ли Лианли, Ким Квон Хо. Назальные противосудорожные композиции и способ введения противосудорожных агентов. Патент РФ №2264209]. Данный подход был реализован при разработке противосудорожного препарата VALTOCO® (Neurelis, США), который представляет собой назальный спрей на основе диазепама. VALTOCO позволяет вводить от 1 мг до 10 мг диазепама, при этом скорость достижения эффекта даже выше, чем при внутримышечном введении. Однако интраназальный путь также не является универсальным, так как имеет ограничения по объему введения, а кроме того, его эффективность резко снижается при наличии выделений из носа.
Задачей настоящего изобретения является получение противосудорожного средства, обладающего более высокой эффективностью по сравнению с прототипом, и пригодного как для инъекционного введения, так и интраназального введения. В качестве прототипа было выбрано официнальное противосудорожное средство: Сибазон 0.5% для внутримышечных инъекций.
Согласно изобретению заявляемое средство (фармацевтическая композиция) представляет собой раствор препарата бензодиазепиновой группы в диэтиламиде никотиновой кислоты (ДЭАНК). ДЭАНК известен также как никетамид, который является активным началом лекарственного препарата кордиамин.
Заявителю не известны какие-либо источники информации, в которых бы содержались сведения об идентичных технических решениях, что позволяет сделать вывод о соответствии заявленного изобретения условию патентоспособности «Новизна».
Как показывают приведенные ниже примеры, заявленное вещество обеспечивает важный технический результат, состоящий в значительном сокращении времени наступления фармакологического эффекта, а также существенном снижении побочных явлений.
Заявителем не выявлены какие-либо источники информации, содержащие сведения о влиянии признаков изобретения на достигаемый вследствие их реализации технический результат. Это, по мнению заявителя, свидетельствует о соответствии данного технического решения условию патентоспособности «Изобретательский уровень».
Реализация изобретения поясняется примерами.
Пример 1. Получение заявляемой фармацевтической композиции
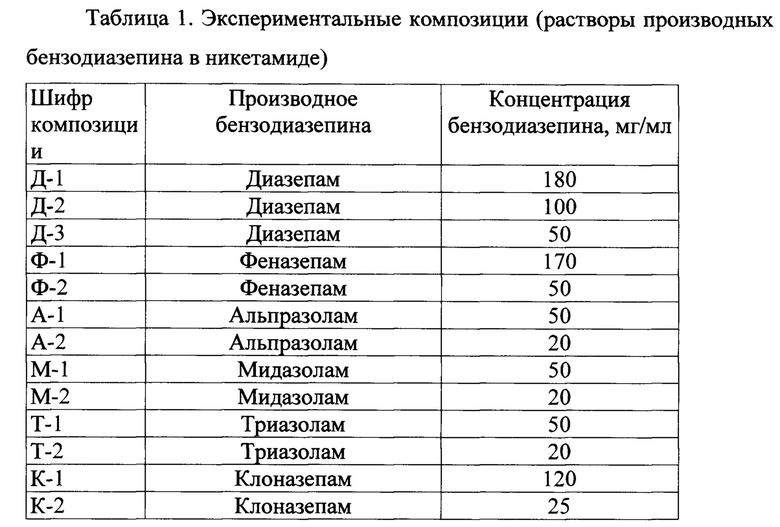
В мерную колбу вместимостью 10 мл помещали расчетное количество субстанции производного бензодиазепина (диазепама, феназепама, альпразолама, мидазолама, триазолама или клоназепама). Добавляли 7-8 мл ДЭАНК (чистой субстанции никетамида) и перемешивали при 50°С до полного растворения исходного бензодиазепина. После этого доводили объем раствора до метки добавлением ДЭАНК и перемешивали. Состав полученных экспериментальных композиций приведен в таблице 1.
Пример 2. Определение противосудорожной активности заявляемой фармацевтической композиции в условиях внутримышечного введения
Исследование противосудорожной активности проводили на белых нелинейных крысах массой 180-220 г, возраста 13-14 недель, прошедших карантин и предварительную отборку. Крыс рандомизировали по группам, каждая экспериментальная группа включала по 10 животных.
Судорожный синдром у крыс моделировали с помощью известного судорожного агента - камфоры [12. Воронина Т.А. Неробкова Л.Н. Методические рекомендации по доклиническому изучению противосудорожной активности лекарственных средств // Руководство по проведению доклинических исследований лекарственных средств. Часть первая. - М.: Гриф и К, 2012. - с. 235-250], которую вводили животным внутрибрюшинно в растворе N-метилпирролидона с содержанием камфоры 0.5 г/мл. Доза камфоры составляла 1 г/кг, что вызывало 100% гибель животных.
Лечение судорог (введение противосудорожного средства) начинали через 0,5 мин после введения конвульсанта. Заявляемые противосудорожные вещества и прототип вводили внутримышечно. Оценку эффективности лечения проводили по таким критериям, как выживаемость крыс и латентное время судорог, то есть время начала судорог от момента введения конвульсанта. Сравнение проводили с группой животных контроля, которые не получали лечения.
Результаты представлены в таблице 2.
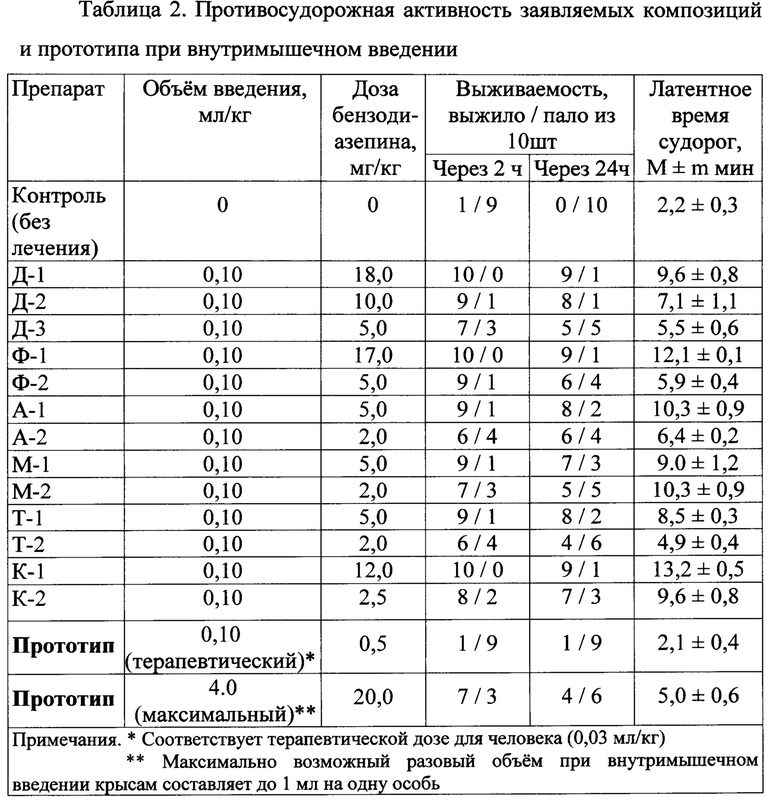
Как видно из полученных результатов, заявляемые средства значительно превосходят прототип, введенный в терапевтическом объеме (0,1 мл/кг) - как по выживаемости животных, так и по отсрочке времени наступления судорог. Даже в том случае, когда прототип был введен в максимально возможной дозе (4 мл/кг), заявляемые средства были более эффективны, особенно по времени отсрочки судорог. При этом следует отметить, что использованный в примере максимальный объем раствора прототипа (4 мл/кг) при внутримышечном введении возможен для крыс, но неприемлем для человека. Так, например, рекомендуемая разовая доза диазепама при внутримышечном введении человеку содержится в 2 мл 0,5% раствора, то есть 0,03 мл/кг.
Пример 3. Определение противосудорожной активности заявляемой фармацевтической композиции при интраназальном введении
Эксперименты были проведены на той же модели судорожного синдрома, что и в Примере 2. Заявляемые противосудорожные вещества и прототип вводили крысам интраназально с помощью механического дозатора с варьируемым объемом дозирования (от 1,0 мкл до 20,0 мкл, предел точности ±3,0%). В качестве контроля использовали группу животных, не получавших лечения. Результаты исследования представлены в таблице 3.
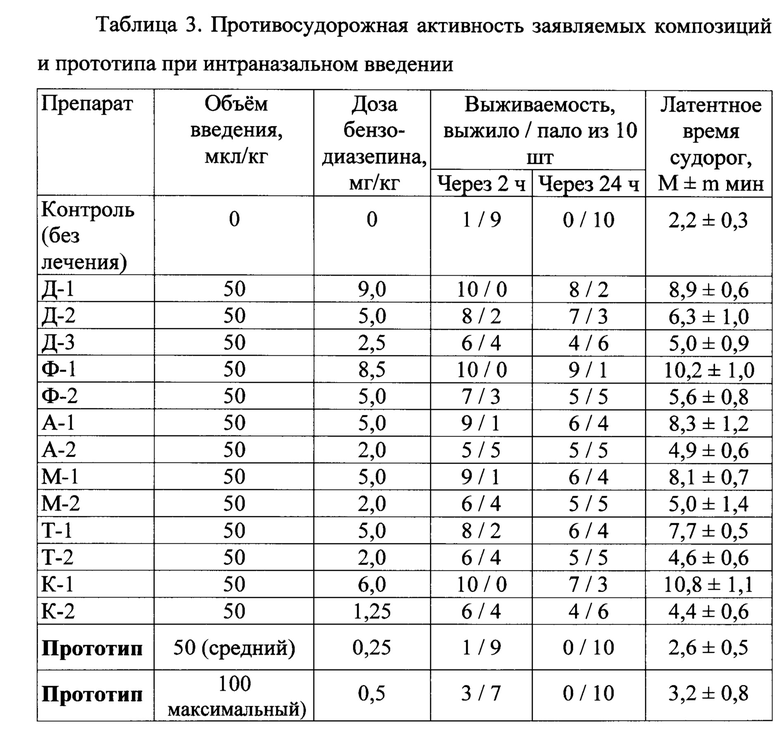
Из полученных результатов видно, что заявляемые средства, вводимые интраназально, значительно повышают выживаемость крыс при судорожном синдроме, и в 2-5 раз увеличивают латентное время начала судорог. Напротив, прототип при назальном введении малоэффективен, так как даже в максимально возможной дозе он практически не снижает летальность у крыс, и не дает достоверной отсрочки начала судорог.
Таким образом, заявляемые средства обладают значительным преимуществом перед прототипом и могут быть использованы для купирования острых судорожных состояний.
| название | год | авторы | номер документа |
|---|---|---|---|
| СРЕДСТВО ТЕРАПИИ СУДОРОЖНОГО СИНДРОМА | 2001 |
|
RU2191017C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ С ПРОТИВОСУДОРОЖНОЙ АКТИВНОСТЬЮ ДЛЯ ПАРЕНТЕРАЛЬНОГО ВВЕДЕНИЯ | 2011 |
|
RU2463052C1 |
| НАЗАЛЬНЫЕ ПРОТИВОСУДОРОЖНЫЕ КОМПОЗИЦИИ И СПОСОБ ВВЕДЕНИЯ ПРОТИВОСУДОРОЖНЫХ АГЕНТОВ | 2000 |
|
RU2264209C2 |
| КОМПОЗИЦИЯ ДЛЯ ТЕРАПИИ СУДОРОЖНОГО СИНДРОМА | 2006 |
|
RU2314829C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ПАРОКСИЗМАЛЬНЫХ СОСТОЯНИЙ | 2011 |
|
RU2469722C1 |
| СРЕДСТВО ДЛЯ КУПИРОВАНИЯ СЕРИЙНЫХ СУДОРОЖНЫХ ПРИПАДКОВ | 1990 |
|
RU2080863C1 |
| СРЕДСТВО ТЕРАПИИ СУДОРОЖНОГО СИНДРОМА | 2006 |
|
RU2314828C1 |
| ПРОФИЛАКТИЧЕСКИЙ ИЛИ ТЕРАПЕВТИЧЕСКИЙ АГЕНТ ПРОТИВ ДЕПРЕССИИ ИЛИ ТРЕВОЖНОГО РАССТРОЙСТВА | 2006 |
|
RU2413510C2 |
| ПРОИЗВОДНОЕ ПИРРОЛИДИНАЦЕТАМИДА ИЛИ ЕГО КОМБИНАЦИЯ ДЛЯ ЛЕЧЕНИЯ РАССТРОЙСТВ ЦНС | 2000 |
|
RU2261093C2 |
| ГИДРОХЛОРИД (1-МЕТИЛПИПЕРИДИН-4-ИЛ)-2-ПРОПИЛПЕНТАНОАТА, ОБЛАДАЮЩИЙ ХОЛИНОЛИТИЧЕСКОЙ И ПРОТИВОСУДОРОЖНОЙ АКТИВНОСТЬЮ | 2019 |
|
RU2714135C1 |
Изобретение относится к области биохимии и медицины, а именно к фармацевтической композиции для лечения судорожного синдрома. Фармацевтическая композиция для лечения судорожного синдрома представляет собой раствор фармацевтической субстанции бензодиазепиновой группы в диэтиламиде никотиновой кислоты (никетамиде), где фармацевтическую субстанцию бензодиазепиновой группы выбирают из группы диазепама с концентрацией от 50 до 180 мг/мл, феназепама с концентрацией от 50 до 170 мг/мл, альпразолама с концентрацией от 20 до 50 мг/мл, мидазолама с концентрацией от 20 до 50 мг/мл, триазолама с концентрацией от 20 до 50 мг/мл, клоназепама с концентрацией от 25 до 120 мг/мл. Вышеописанное изобретение позволяет значительно сократить время наступления фармакологического эффекта, а также существенно снизить побочные явления. 3 табл., 3 пр.
Фармацевтическая композиция для лечения судорожного синдрома, отличающаяся тем, что она представляет собой раствор фармацевтической субстанции бензодиазепиновой группы в диэтиламиде никотиновой кислоты (никетамиде), где фармацевтическую субстанцию бензодиазепиновой группы выбирают из группы диазепама с концентрацией от 50 до 180 мг/мл, феназепама с концентрацией от 50 до 170 мг/мл, альпразолама с концентрацией от 20 до 50 мг/мл, мидазолама с концентрацией от 20 до 50 мг/мл, триазолама с концентрацией от 20 до 50 мг/мл, клоназепама с концентрацией от 25 до 120 мг/мл.
| Интернет-источник Лекарственный справочник ГЭОТАР "Сибазон", найдено 17.01.2019, ссылка на источник: https://web.archive.org/web/20190117193250/http://www.lsgeotar.ru/sibazon-8267.html | |||
| ZAVALA F | |||
| Benzodiazepines, Anxiety and Immunity / Pharmacol | |||
| Ther | |||
| Электрическое сопротивление для нагревательных приборов и нагревательный элемент для этих приборов | 1922 |
|
SU1997A1 |
| Фальцовая черепица | 0 |
|
SU75A1 |
| ПЕЧНОЙ ЖЕЛЕЗНЫЙ РУКАВ (ТРУБА) | 1920 |
|
SU199A1 |
| СКРЯБИН В.Ю | |||
| и др | |||
| Особенности фармакокинетики, фармакодинамики | |||
Авторы
Даты
2023-08-01—Публикация
2022-10-07—Подача