Область техники, к которой относится изобретение
Изобретение относится к медицине, а именно, к хирургии и может быть использовано в лечении прогрессирующей нутритивной недостаточности у больных после гастрошунтирования по Ру.
Уровень техники
Желудочное шунтирование по Ру сегодня является наиболее популярным способом коррекции морбидного ожирения. Методика позволяет добиться стойкой редукции избыточной массы тела до 70% [Welbourn R., Hollyman M., Kinsman R., Dixon J., Liem R., Ottosson J., Ramos A., Våge V., Al-Sabah S., Brown W., Cohen R., Walton P., Himpens J. Bariatric surgery worldwide: baseline demographic description and one-year outcomes from the fourth IFSO Global Registry Report 2018. Obes Surg. 2019 Mar; 29 (3):782-795]. Однако известны и неблагоприятные исходы отключенного желудка и двенадцатиперстной кишки (ДПК) из пищеварения, которые приводят к излишней нежелательной потере веса и сопровождаются постоянными гипогликемическими кризами, обморочными состояниями, диареей и нарастающей кахексией. Прогрессирующие метаболические нарушения после бариатрических операций встречаются в 17% случаев и являются показанием к «ревизионным» вмешательствам [Kermansaravi M., Shahmiri S.S., Davarpanah Jazi A.H., Valizadeh R., Weiner R.A., Chiappetta S. Reversal to normal anatomy after one-anastomosis/mini gastric bypass, indications and results: a systematic review and meta-analysis. Surg Obes Relat Dis. 2021 Aug;17 (8) :1489-1496]. Широко распространены два варианта реконструктивных операций, это укорочение длины билиопанкреатической петли с перемещением межкишечного анастомоза проксимальнее к малой культе желудка и возврат к нормальной анатомии, то есть разобщение гастроэнтеро- и энтероэнтероанастомоза с восстановлением физиологического пассажа пищи [Abu-Abeid A., Goren O., Eldar S.M., Vitiello A., Berardi G., Lahat G., Dayan D. Revisional surgery of one anastomosis gastric bypass for severe protein-energy malnutrition. nutrients. 2022 Jun 6;14(11):2356]. Однако существующие способы удлинения «питательной» петли тонкой кишки не устраняют белково-энергетический дефицит и не избавляют больных от диареи [Khrucharoen U., Juo Y.Y., Chen Y., Dutson E.P. Indications, operative techniques, and outcomes for revisional operation following mini-gastric bypass-one anastomosis gastric bypass: a systematic review. Obes. Surg. 2020;30:1564–1573], а восстановление анатомической целостности желудка и естественного пассажа пищи способствует повторному набору веса. Кроме того, ревизионная хирургия с восстановлением физиологического пассажа пищи по данным M. Musella et al., (2022) сопровождается тяжелым рефлюкс-эзофагитом [Musella M., Vitiello A., Susa A. et al. Revisional surgery after one anastomosis/minigastric bypass: an Italian multi-institutional survey. OBES SURG 32, 256-265; 2022]. Поэтому необходим дальнейший поиск варианта реконструкции желудочно-кишечного тракта, который бы предотвратил пищеварительные расстройства, вызванные гастрошунтированием, и обеспечил пациентам достойное качество жизни.
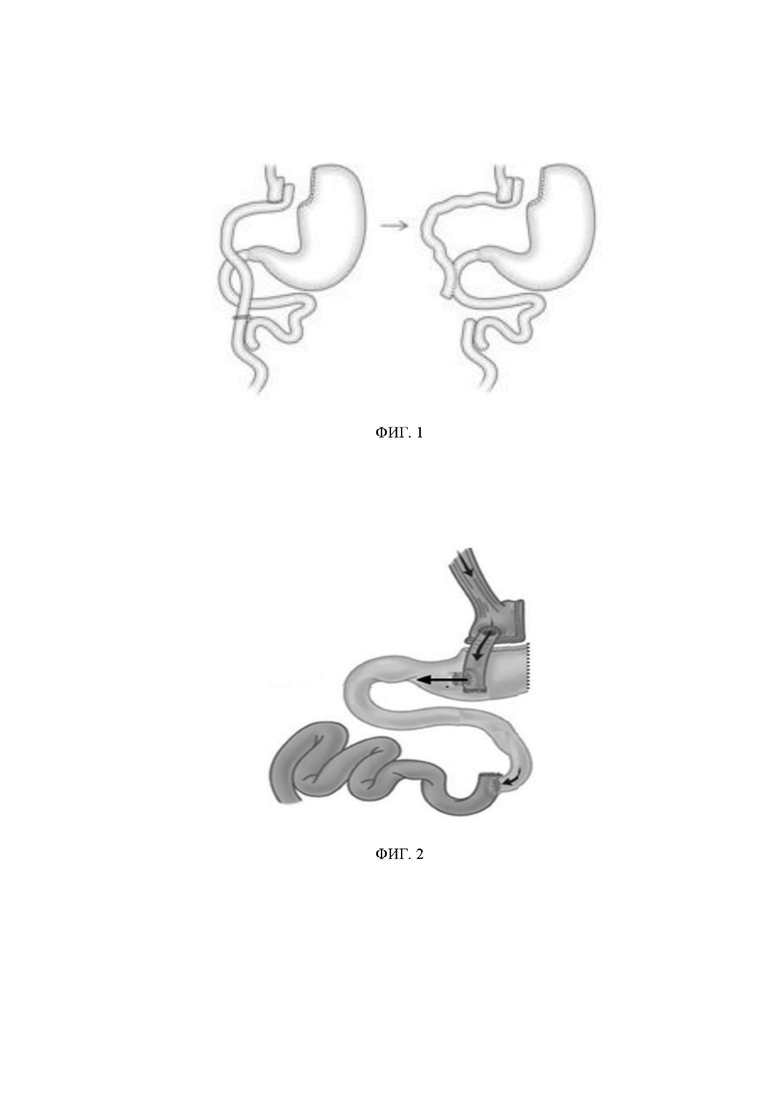
Из уровня техники известен способ хирургического лечения прогрессирующей нутритивной недостаточности после гастрошунтирования по Ру [Ceneviva R., Salgado Júnior W., Marchini J.S. A new revisional surgery for severe protein-calorie malnutrition after Roux-en-Y gastric bypass: successful duodenojejunal reconstruction using jejunal interposition. Surg Obes Relat Dis. 2016 Feb;12(2):e21-3] (фиг. 1). В публикации описан способ хирургического лечения пациентки в связи с прогрессирующей белково-энергетической недостаточностью, развившейся через год после гастрошунтирования по Ру. Согласно способу, выше межкишечного соустья пересекали отводящую петлю гастроэнтероанастомоза, не нарушая его целостность. После чего дистальный отдел длинного сегмента (50 см) соединяли с нисходящей частью двенадцатиперстной кишки. В отдаленном периоде лабораторные показатели пришли в норму, кроме ферритина, который постоянно снижался. Снижение ферритина связано с тем, что при выключении желудка из пассажа пищи происходит снижение абсорбции витамина В и железа в организме, что проявляется дефицитом железосвязывающих белков [Дворецкий Л.И., Яшков Ю.И., Ивлева О.В. Анемия у больных после билиопанкреатического шунтирования. Клиническая медицина. 2017. 95 (8). 742-748].
Недостатком вышеуказанного способа является формирование тонко-дуоденального соустья с нисходящей частью двенадцатиперстной кишки ниже привратника, что не устраняет быстрый пассаж пищи по кишечнику и не предотвращает тяжелый демпинг-синдром с характерными его проявлениями. Кроме того, использование длинного сегмента кишки - 50 см, может приводить к его перегибам в отдаленном периоде и вызывать непроходимость [Sousa J.E.S., Troncon L.E.A., Andrade J.I., Ceneviva R. Comparison between Henley jejunal interposition and Roux-en-Y anastomosis as concerns enterogastric biliary reflux levels. Ann Surg. 1988; 5: 597-600].
Наиболее близким к заявленному изобретению является способ хирургического лечения прогрессирующей нутритивной недостаточности после гастрошунтирования по Ру [Sampaio-Neto J., Branco-Filho A.J., Nassif L.S., Nassif A.T., Masi F.D., Gasperin G. Proposal of a revisional surgery to treat severe nutritional deficiency post-gastric bypass. Arq Bras Cir Dig. 2016. 29 Suppl 1(Suppl 1). 98-101] (фиг. 2). При осуществлении способа авторы мобилизовали отключенный желудок из брюшных сращений, пересекали желудочно-селезеночные сосуды и резецировали дно и тело желудка на уровне антрального отдела. После чего на 10 см дистальнее ранее сформированного гастроэнтероанастомоза пересекали отводящею кишку и соединяли с культей антрального отдела желудка анастомозом «бок в бок» на расстоянии 4 см от привратника. Таким образом, для восстановления естественного пассажа пищи использовали короткий тощекишечный сегмент 10 см. Далее пересекали билиопанкреатическую петлю в зоне ранее сформированного межкишечного анастомоза, дефект в отводящей петле ушивали и формировали новое межкишечное соустье между приводящей и отводящей петлей «конец в бок».
Недостатком вышеуказанного способа являются:
1. Транспозиция короткого тощекишечного сегмента длиной 10 см не устраняет заброс желудочного и дуоденального содержимого в пищевод через малую культю желудка. В отдаленном периоде автор предложенной методики у 50% больных выявил изжогу [Sampaio-Neto J., Branco-Filho A.J., Nassif L.S., Nassif A.T., Masi F.D., Gasperin G. Proposal of a revisional surgery to treat severe nutritional deficiency post-gastric bypass. Arq Bras Cir Dig. 2016. 29 Suppl 1(Suppl 1). 98-101].
2. Формирование анастомоза отводящей кишки с антральным отделом желудка вблизи привратника (на расстояние 4 см от него) является причиной развития щелочного рефлюкс-эзофагита, что в последующем может привести к раку пищевода [Bolton J.S., Conway W.C. Postgastrectomy syndromes. Surg Clin N Am 2011; 91:1105].
3. Денервированная дистальная культя желудка неизбежно приводит к атонии и гастростазу, что в последующем проявляется анастомозитом или стриктурой гастроэнтероанастомоза [Jung H.J., Lee J.H., Ryu K.W., Lee J.Y., Kim C.G., Choi I.J., Kim Y.W., Bae J.M. The influence of reconstruction methods on food retention phenomenon in the remnant stomach after a subtotal gastrectomy. J Surg Oncol. 2008 Jul 1;98(1):11-4].
Технической проблемой, решение которой обеспечивается при осуществлении изобретения, является создание способа хирургического лечения нутритивной недостаточности у больных после гастрошунтирования по Ру, лишенного перечисленных выше недостатков.
Раскрытие сущности изобретения
Техническим результатом, на достижение которого направлено заявленное изобретение, является восстановление естественного пассажа пищи при помощи перемещения отводящей петли гастроэнтероанастомоза в культю желудка, сформированную в виде трубки. Предложенный способ позволяет надежно предотвратить заброс желудочного и кишечного содержимого в пищевод и обеспечить порционную эвакуацию пищи в нижележащие отделы ЖКТ.
Предложенный способ позволяет минимальным количеством оперативных приемов восстановить пассаж пищи через двенадцатиперстную кишку. Используемый сегмент тощей кишки в изоперистальтическом положении выполняет функцию барьера между слизистой культи желудка и пищеводов, за счет перистальтической активности и направленности сегмента пища перемещается в каудальном направлении, предотвращая регургитацию, образуя, тем самым, искусственный клапан. Изобретение также направлено на профилактику гастростаза денервированной культи желудка после предыдущей операции. При формировании культи желудка в виде трубки шириной до 4 см пища практически в ней не задерживается и порционно эвакуируется в двенадцатиперстную кишку, благодаря функции привратника. Заявленное изобретение также направлено на уменьшение риска повторного набора веса, резецируется ранее отключенный (не функционирующий) желудок, оставляя культю длинной 12 см и шириной 4 см, что практически лишает его резервуарной функции.
Технический результат способа хирургического лечения прогрессирующей нутритивной недостаточности после гастрошунтирования по Ру, достигается за счет транспозиции отводящей петли гастроэнтероанастомоза в культю желудка, при этом отводящую петлю пересекают на 20 см дистальнее гастроэнтероанастомоза, затем выполняют мобилизацию и резекцию желудка, формируя из него трубку с примерными размерами - длиной 12 см и шириной 4 см, с питанием на правых желудочно-сальниковых сосудах, далее дистальный конец отводящей петли соединяют с культей желудка «конец в конец», далее разобщают межкишечный анастомоз и восстанавливают непрерывность тонкой кишки, формируют анастомоз между бывшей приводящей и отводящей кишкой «конец в конец».
Использование заявляемого способа позволяет восстановить естественный пассаж пищи, избежать не желаемый повторный набор веса, предотвратить послеоперационный рефлюкс-эзофагит.
Краткое описание чертежей
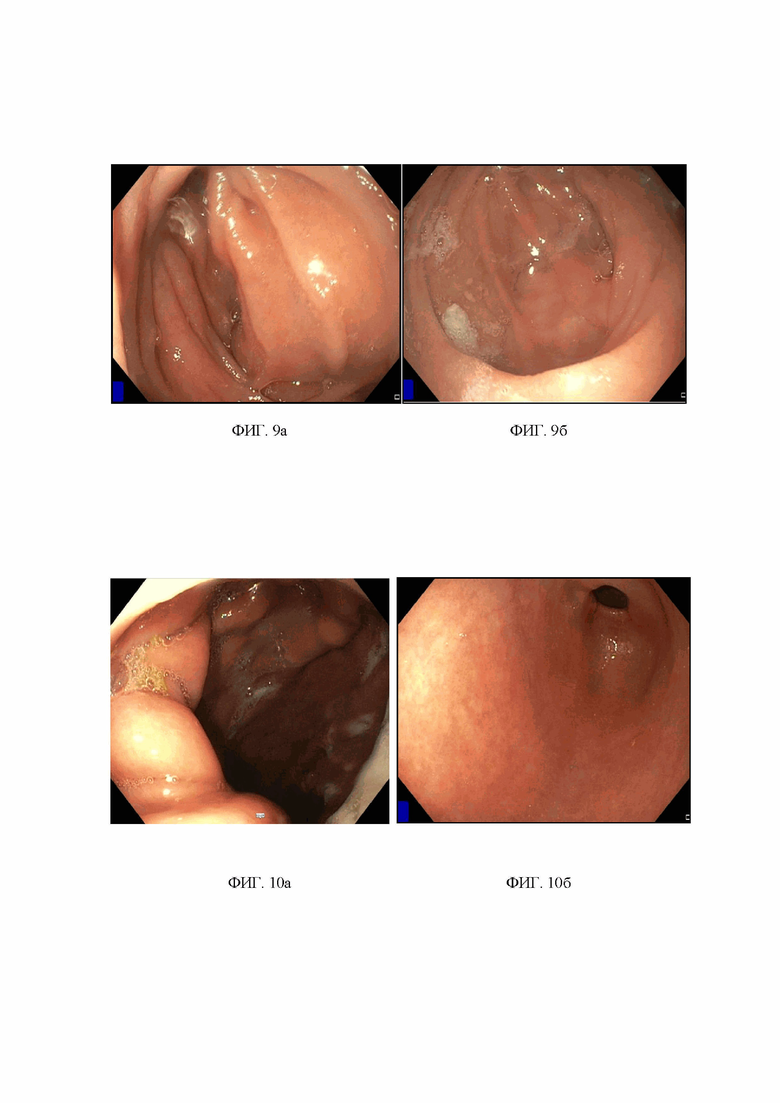
Изобретение поясняется чертежами, рентгенограммами и интраоперационными фотографиями, где на фиг.1 схематично представлена операция по R. Ceneviva; на фиг. 2 схематично представлен окончательный вариант реконструкции по J. Sampaio-Neto; на фиг. 3 – рентгенограммы больной Г. 48 лет до реконструктивной операции: а) – прямая проекция сразу после перорального приема сульфата бария, б) – прямая проекция через 30 минут после перорального приема сульфата бария; на фиг. 4 - интраоперационная фотография после мобилизации Ру петли и культи желудка: а) – отключенный желудок, б) – гастроэнтероанастомоз; на фиг. 5 - интраоперационное фото окончательного варианта транспозиции отводящей петли гастроэнтероанастомоза в культю желудка (заявленный способ): а) – культя желудка, сформированная в виде трубки, б) – тощекишечный сегмент; на фиг 6 - схема операции больной Г. 48 лет: а) – схема ранее выполненной операции гастрошунтирование по Ру, б) – транспозиция отводящей петли в культю желудка, предлагаемый вариант; на фиг. 7 - рентгенограммы больной Г. 48 лет через 6 месяцев после реконструктивной операции: а) – прямая проекция сразу после перорального приема сульфата бария, б) – прямая проекция через 2 часа после перорального приема сульфата бария; на фиг. 8 – результаты эндоскопического исследования, фотография пищеводно-тонкокишечного анастомоза, больной Г. 48 лет через год после операции; на фиг. 9 - эндоскопическое исследование больной Г. 48 лет через 1 год после операции: а) проксимальный отдел тощекишечной вставки, б) дистальный отдел кишечной вставки ближе к еюногастроанастомозу; на фиг. 10 эндоскопическое исследование больной Г. 48 лет через 1 год после операции: а) гастроэнтероанастомоз, б) культя желудка.
Осуществление изобретения
Способ осуществляют следующим образом.
При выполнении транспозиции отводящей петли гастроэнтероанастомоза в культю желудка после гастрошунтирования по Ру используют следующую последовательность хирургических этапов.
Операцию выполняют через лапаротомный доступ. После чего производят мобилизацию культи желудка от спаек и рубцовых сращений возникающих после предыдущей операции. В последующем перевязывают левую желудочную артерию и вену, правую желудочную артерию. Выполняют резекцию желудка при помощи линейного сшивающего степлера под прямым углом со стороны малой кривизны, избегания слепых карманов с питанием на правых желудочно-сальниковых сосудах. Механический шов укрывают непрерывным серо-серозным швом. Ширина желудочной трубки должна быть 4 см, длинна от 12 до 15 см.
Далее, отступив 20 см от гастроэнтероанастомоза, пересекают отводящую кишку на зажимах Кохера, мобилизую брыжейку кишки с таким расчетом, чтобы не повредить ее питающий сосуд. После чего дистальную часть сегмента тонкой кишки соединяют с проксимальной частью культи желудка однорядным анастомозом «конец в конец», отдельными узловыми швами. Принципиальное значение имеет длина перемещенного сегмента, которая должна быть не менее 20 см и не более 25 см, так как короткая кишечная вставка не выполняет функцию антирефлюксного барьера, а более длинный сегмент может стать причиной непроходимости пищи вследствие его перегиба в отдаленном периоде.
Затем выполняют разобщение ранее сформированного межкишечного анастомоза, приводящую (билиопанкератическую) петлю отсекают от общей (питательной) петли тонкой кишки линейным степлером. Механический шов общей петли тонкой кишки укрывают непрерывным серо-серозным швом. Целостность тонкого кишечника восстанавливают однорядным швом «конец в конец», формируют анастомоз между проксимальным отделом бывшей отводящей петли и дистальным отделом приводящей.
Пример. Больная Г. 48 лет поступила с жалобами на слабость, отеки конечностей, вздутие живота, обморочные состояния после каждого приема пищи, диарею 8-12 раз в сутки. Из анамнеза в 2018 года по поводу морбидного ожирения, индекс массы тела (ИМТ) составлял – 43,8 кг/м2, выполнено гастрошунтирование на Ру петле. В период с 2018 до 2020 г похудела на 40 кг, чувствовала себя хорошо, работала, придерживалась диеты, питалась дробно, мелкими порциями до 5-6 раз в день. С 2021 года стала отмечать слабость после приема пищи, диарею. Неоднократно обследовалась и лечилась у гастроэнтерологов с временным положительным эффектом. Однако, учитывая нарастание слабости и прогрессирующее снижение массы тела, обратилась 17.01.2022 г в ФГБУ Национальный медицинский исследовательский центр хирургии им. А.В. Вишневского МЗ РФ (далее – НМИЦ). Лабораторные исследования представлены в таблице 1.
Таблица 1
после реконструкции
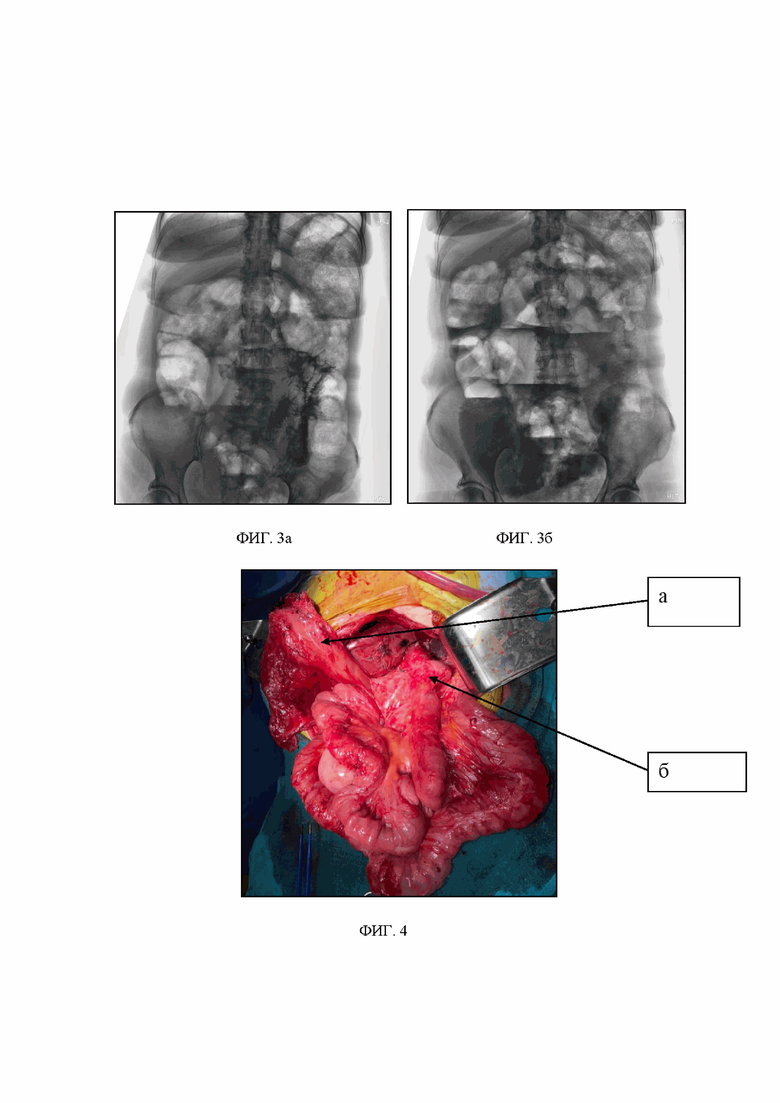
При рентгенографии брюшной полости с контрастом выявлено, что сульфат бария при пероральном приеме через 30 минут весь находился в дистальных отделах тонкой кишки и правых отделах ободочной. Таким образом, у больной зафиксирован ускоренный пассаж по кишечнику (фиг. 3). Выставлен диагноз: Тяжелый демпинг-синдром. Прогрессирующая нутритивная недостаточность. Состояние после гастрошунтирования по Ру от 12.12.2018 г. Принято решение о реконструктивной операции, проведена предоперационная подготовка, которая включала переливание крови, свежезамороженной плазмы, альбумина, питательных смесей.
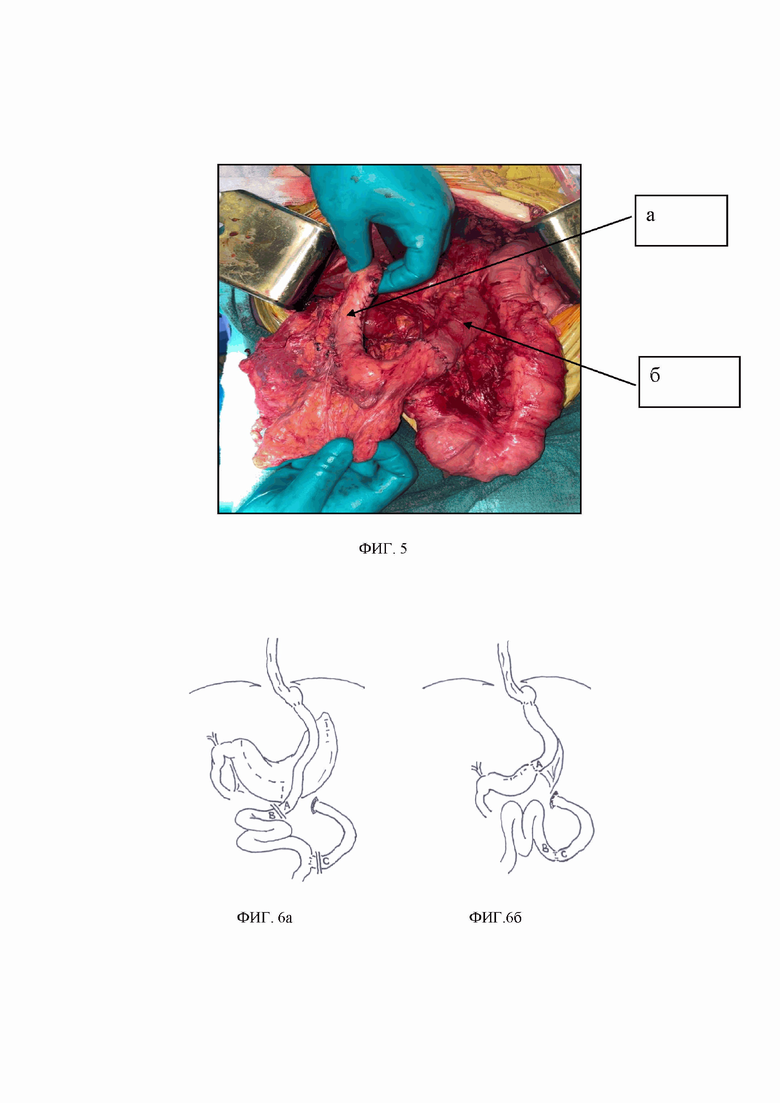
В НМИЦ 26.01.2022 выполнена лапаротомия, транспозиция отводящей петли гастроэнтероанастомоза в культю желудка заявленным способом (фиг. 4-6). Послеоперационный период протекал без осложнений. Больная выписана на 8-е сутки после операции.
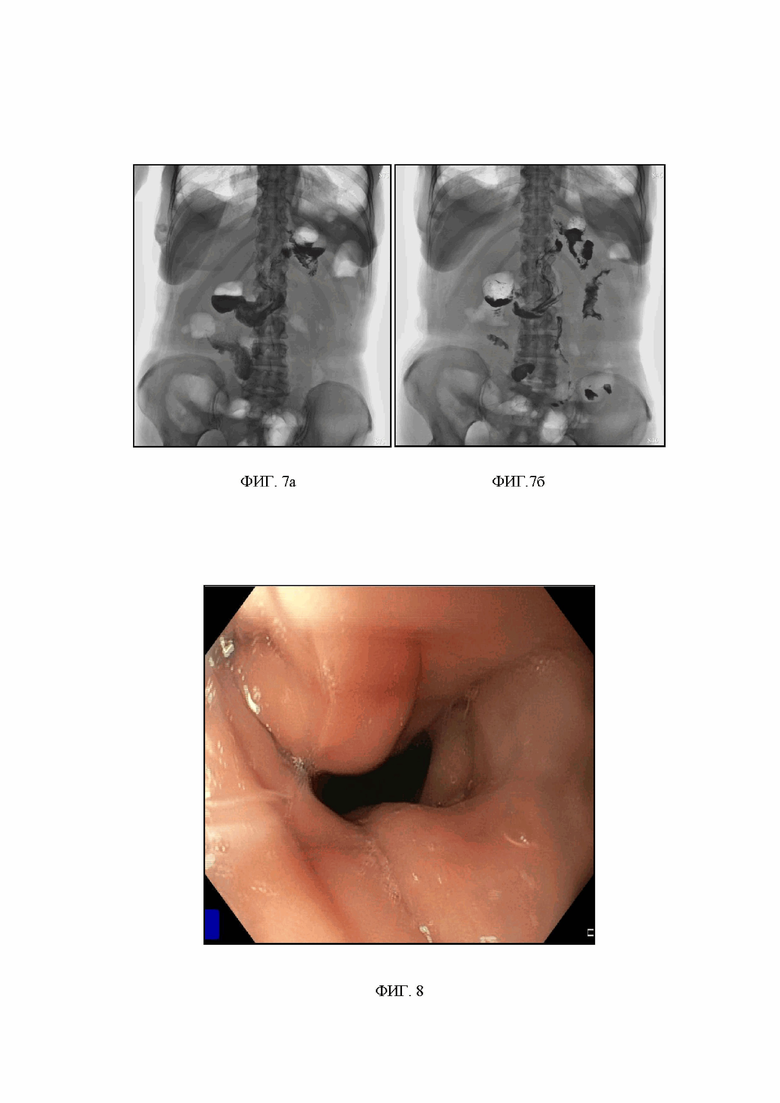
При контрастной рентгеноскопии через 6 месяцев анастомозы проходимы, пассаж контрастного вещества порционный, своевременный. Барий через 2 часа в петлях тонкой кишки, эвакуация порционная (фиг. 7). По данным ФГДС через 1 год после операции признаков рефлюкса-эзофагита нет. Больная вернулась к прежнему образу жизни, работает, диеты не придерживается, питается 4-5 раз в день. Жалоб нет. Стул регулярный 1 раз в сутки. После реконструктивной операции прибавила в весе на 24 кг за 6 месяцев, после вес сохранился в тех же значениях и спустя год после операции (фиг. 8-10). ИМТ составляет 22,7 кг/м2.
Таким образом, предложенный вариант реконструкции позволяет восстановить естественный пассаж пищи, устранить болезни оперированного желудка и предотвратить повторный набор веса.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ЛАПАРОСКОПИЧЕСКОГО ВЫПОЛНЕНИЯ МИНИ-ГАСТРОШУНТИРОВАНИЯ ДЛЯ ЛЕЧЕНИЯ ОЖИРЕНИЯ | 2015 |
|
RU2600925C1 |
| СПОСОБ РЕДУОДЕНИЗАЦИИ С СОЗДАНИЕМ КИШЕЧНОГО РЕЗЕРВУАРА ПРИ БОЛЕЗНЯХ ОПЕРИРОВАННОГО ЖЕЛУДКА ПОСЛЕ ГАСТРЭКТОМИИ В ПЕТЛЕВОЙ РЕКОНСТРУКЦИИ ПО БРАУНУ | 2023 |
|
RU2801773C1 |
| Способ модифицированного минижелудочного шунтирования с ручным гастроэнтероанастомозом | 2022 |
|
RU2800963C1 |
| КОМБИНИРОВАННЫЙ СПОСОБ ЛЕЧЕНИЯ ОЖИРЕНИЯ БИЛИОПАНКРЕАТИЧЕСКИМ ШУНТИРОВАНИЕМ НА КОРОТКОЙ ПЕТЛЕ ПО РУ | 2007 |
|
RU2341209C1 |
| Способ одномоментной профилактики билиарного рефлюкса и протекции гастроэнтероанастомоза при выполнении минижелудочного шунтирования | 2016 |
|
RU2629045C1 |
| Способ хирургического лечения морбидного ожирения | 2016 |
|
RU2640783C1 |
| СПОСОБ РЕДУОДЕНИЗАЦИИ С ФОРМИРОВАНИЕМ АНТИРЕФЛЮКСНОГО КЛАПАНА ПРИ БОЛЕЗНЯХ ОПЕРИРОВАННОГО ЖЕЛУДКА ПОСЛЕ ГАСТРЭКТОМИИ В ПЕТЛЕВОЙ РЕКОНСТРУКЦИИ ПО БРАУНУ | 2023 |
|
RU2801772C1 |
| Способ лапароскопического бесстеплерного бариатрического шунтирования желудка | 2017 |
|
RU2669460C1 |
| СПОСОБ НАЛОЖЕНИЯ ГАСТРОЭНТЕРОАНАСТОМОЗА ПРИ ЛАПАРОСКОПИЧЕСКОМ ГАСТРОШУНТИРОВАНИИ У ПАЦИЕНТОВ С МОРБИДНЫМ ОЖИРЕНИЕМ | 2020 |
|
RU2739467C1 |
| Способ хирургического лечения ожирения в сочетании с грыжей пищеводного отверстия диафрагмы и гастроэзофагеальной рефлюксной болезнью | 2022 |
|
RU2794406C1 |
Изобретение относится к медицине, а именно к хирургии, и может быть использовано в лечении прогрессирующей нутритивной недостаточности у больных после гастрошунтирования по Ру. Способ хирургического лечения прогрессирующей нутритивной недостаточности после гастрошунтирования по Ру включает транспозицию отводящей петли гастроэнтероанастомоза в культю желудка, при этом отводящую петлю пересекают на 20 см дистальнее гастроэнтероанастомоза, затем выполняют мобилизацию и резекцию желудка, формируя из него трубку длиной 12 см и шириной 4 см с питанием на правых желудочно-сальниковых сосудах, далее дистальный конец отводящей петли соединяют с культей желудка «конец в конец», разобщают межкишечный анастомоз и восстанавливают непрерывность тонкой кишки, после чего формируют анастомоз между бывшей приводящей и отводящей кишкой «конец в конец». Изобретение направлено на восстановление естественного пассажа пищи. Способ позволяет надежно предотвратить заброс желудочного и кишечного содержимого в пищевод и обеспечить порционную эвакуацию пищи в нижележащие отделы ЖКТ. 1 табл., 1 пр., 10 ил.
Способ хирургического лечения прогрессирующей нутритивной недостаточности после гастрошунтирования по Ру, включающий транспозицию отводящей петли гастроэнтероанастомоза в культю желудка, при этом отводящую петлю пересекают на 20 см дистальнее гастроэнтероанастомоза, затем выполняют мобилизацию и резекцию желудка, формируя из него трубку длиной 12 см и шириной 4 см с питанием на правых желудочно-сальниковых сосудах, далее дистальный конец отводящей петли соединяют с культей желудка «конец в конец», разобщают межкишечный анастомоз и восстанавливают непрерывность тонкой кишки, после чего формируют анастомоз между бывшей приводящей и отводящей кишкой «конец в конец».
| Sampaio-Neto J., Branco-Filho A.J., Nassif L.S., Nassif A.T., Masi F.D., Gasperin G | |||
| Proposal of a revisional surgery to treat severe nutritional deficiency post-gastric bypass | |||
| Arq Bras Cir Dig | |||
| Токарный резец | 1924 |
|
SU2016A1 |
| Солесос | 1922 |
|
SU29A1 |
| Дорожная спиртовая кухня | 1918 |
|
SU98A1 |
| Способ профилактики нутритивной недостаточности у детей с болезнью Гиршпрунга | 2018 |
|
RU2694839C1 |
| Дегтерев Д.А | |||
| и др., РЕДКОЕ ОСЛОЖНЕНИЕ БАРИАТРИЧЕСКИХ ОПЕРАЦИЙ: ПОЛИРАДИКУЛОНЕВРОПАТИЯ ПО | |||
Авторы
Даты
2023-08-08—Публикация
2023-04-25—Подача