Изобретение относится к экспериментальной медицине и фармакологии, а именно, средствам лечения головного мозга от патологий, вызванных воздействием острой гипоксии с гиперкапнией.
Патологические состояния головного мозга, инициируемые гипоксией, являются важнейшими социальной и медицинской проблемами в связи с высокой их распространенностью и тяжелыми последствиями для состояния здоровья населения. В связи с чем повышение эффективности терапии, а также профилактика этих заболеваний является одной из важных задач неврологии [Смирнова И.Н., Федорова Т.Н., Танашян М.М., Суслина З.А. Клиническая эффективность и антиоксидантная активность Мексидола при хронических цереброваскулярных заболеваниях // Нервные болезни. 2006. №1. С. 33-36].
Основной стратегией лечения постгипоксических состояний мозга является фармакологическая коррекция, направленная на устранение ключевых патологических звеньев данного заболевания. Одним из таких звеньев при развитии гипоксических состояний является окислительный стресс. Перепроизводство активных форм кислорода (АФК) и азота, а также нарушение баланса антиоксидантных ферментных систем организма приводит к разрушению клеточных структур, липидов, белков, ДНК и РНК [Islam М.Т. Oxidative stress and mitochondrial dysfunction-linked neurodegenerative disorders // Neurol. Res. 2017. Vol. 39(1). P. 73-82]. В головном мозге есть необходимые предпосылки для развития свободнорадикальных процессов, особенно при гипоксических условиях. Это наличие высокого содержания полиненасыщенных жирных кислот, очень низкая активность катал азы и глутатионпероксидазы, высокое содержание ионов двухвалентного железа и малое количество витамина А. Гиперпродукция активных форм кислорода и азота, а также развитие процессов перекисного окисления липидов приводят к нарушению гематоэнцефалического барьера, развитию воспалительного процесса, апоптотической и некротической гибели нейронов. Поэтому для снижения последствий инсульта была предложена антиоксидантная терапия. Антиоксиданты подразделяются на прямые и косвенные. Первые осуществляют захват радикалов за счет особенностей структурного строения: наличие ненасыщенных связей и доноров протонов в структуре молекулы, способностью образовывать хелатные соединения с металлами переменной валентностью, участвующих в реакции Фентона. Косвенный эффект достигается повышением собственного антиоксидантного потенциала организма за счет активации стресс лимитирующих систем организма. В мозге к таким системам относят ГАМК-, опиоид- и NO-ергичексие системы.
В соответствии с этим для предотвращения распространения повреждений тканей головного мозга человека, вызванных развитием гипоксических состояний, рассматривается необходимость поиска и применения биологически активных веществ, способных препятствовать чрезмерному накоплению свободных радикалов и поддерживать собственную антиоксидантную систему организма. А значит защищать ткань мозга от повреждения и сохранять функциональную активность ЦНС.
Известен способ применения лекарственного средства Милдронат (химическое название - 2-(2-карбоксиэтил)-1,1,1-триметилгидразиний (мельдоний)), применяемого в условиях ишемии миокарда и головного мозга. В условиях ишемии мельдоний восстанавливает равновесие между процессами доставки кислорода и его потребления в клетках, предупреждает нарушение транспорта аденозинтрифосфата (АТФ); одновременно с этим активирует гликолиз, который протекает без дополнительного потребления кислорода. В результате снижения концентрации карнитина усиленно синтезируется гамма-бутиробетаин, обладающий вазодилатирующими свойствами. Показаниями к применению являются: ишемической болезни сердца - стенокардия, инфаркт миокарда (в составе комплексной терапии); хроническая сердечная недостаточность; подострые и хронические нарушения кровоснабжения мозга (после инсульта, цереброваскулярная недостаточность) в составе комплексной терапии. Сниженная работоспособность, умственные и физические перегрузки (в том числе у спортсменов), деменции [Электронный ресурс] Режим доступа: hrtps://www.rlsnet.ru/drugs/mildronat-775 = Дата обращения: 10.06.2022 г.]. Недостатком данного способа является слабая эффективность, положительный результат на допинг контроле и ряд побочных действий: тахикардия, повышение и понижение артериального давления, повышенная возбудимость.
Антигипоксантом, применяемым в клинике для лечения острого инсульта, является препарат 2-этил-6-метил-3-гидроксипиридина сукцинат - Мексидол (Регистр лекарственных средств России. Энциклопедия лекарств. М: «РЛС2006», вып. 14, с. 489-490). Данный препарат оказывает мембранопротекторное, антиоксидантное и анксиолитическое действие. Показаниями для применения препарата являются: последствия острых нарушений мозгового кровообращения, в т.ч. после транзиторных ишемических атак, в фазе субкомпенсации (в качестве профилактических курсов); легкая черепно-мозговая травма, последствия черепно-мозговых травм; энцефалопатии различного генеза (дисциркуляторные, дисметаболические, посттравматические, смешанные); синдром вегетативной дистонии; легкие когнитивные расстройства атеросклеротического генеза; тревожные расстройства при невротических и неврозоподобных состояниях; ишемическая болезнь сердца (в составе комплексной терапии); купирование абстинентного синдрома при алкоголизме с преобладанием неврозоподобных и вегетативно-сосудистых расстройств, постабстинентные расстройства; состояния после острой интоксикации антипсихотическими средствами; астенические состояния, а также для профилактики развития соматических заболеваний под воздействием экстремальных факторов и нагрузок; воздействие экстремальных (стрессорных) факторов.
Недостатком данного препарата для лечения гипоксического воздействия является набор побочных эффектов, а также быстрое выведение из организма. [Мексидол® / Государственный реестр лекарственных средств [Электронный ресурс] Режим доступа: https://grls.rosminzdrav.ra/Grls_View_v2.aspx?routingGuid=708700b3-7590-48be-86ba-2442e525bb88&t=Дата обращения: 10.06.2022 г.].
Известен лекарственный препарат нимодипин - 3-(метоксиэтил) 5-пропан-2-ил 2,6-диметил-4-(3-нитрофенил)-1,4-дигидропиридин-3,5-дикарбоновая кислота. Обладает нейропротекторным, ноотропным и вазотропным действием. Нимодипин по своей химической структуре относится к производным дигидропиридина, а по своему механизму действия - к блокаторам потенциалзависимых кальциевых каналов L-типа. Применяется при ишемическом нарушении мозгового кровообращения, субарахиноидальных кровоизлияниях, в нейрореабилитационный период. Недостатком данного препарата для лечения гипоксического воздействия является: гиперчувствительность, выраженная гипотензия, отек мозга, повышенное внутричерепное давление, тяжелые нарушения функции печени, оказывает побочные действия: гипотензия, спазм периферических сосудов, гипертензия, анемия и тромбоцитопения и другие. Не рекомендуется применять во время работы водителям транспортных средств и людям, профессия которых связана с повышенной концентрацией внимания [http://www.rlsnet.ru/mnn_index_id_1024.htm#protivopokazaniya дата обращения 06.05.2019].
Наиболее близким аналогом является способ профилактики и коррекции метаболических и функциональных нарушений центральной нервной системы в условиях стресса [Патент РФ на изобретение RU 2717107 С1]. Способ заключается в пероральном введении обедненной дейтерием воды для профилактики и коррекции нарушений метаболического и функционального состояния нервной системы в условиях стресса (в том числе гипоксии) в течение 42 дней.
Недостатком данного способа является низкая эффективность ввиду продолжительного приема (не менее 42 дней) описываемого средства.
Задачей предлагаемого изобретения является усовершенствование способа лечения головного мозга при острой гипоксии с гиперкапнией, характеризующегося высокой эффективностью за меньшее количество времени.
Техническим результатом является предотвращение окислительного повреждения тканей головного мозга, вызванных острой гипоксией с гиперкапнией, при помощи повышения уровня восстановленного глутатиона (GSH) в головном мозге.
Технический результат достигается тем, что способ лечения головного мозга при острой гипоксии с гиперкапнией включает пероральное введение защитного средства, при этом в качестве защитного средства вводят меконовую кислоту в количестве от 2 до 4 мг/кг массы тела в течение 3-4 суток. Лечение окислительного повреждения нервной ткани, вызванных гипоксическим воздействием за короткое время (в течение 3-4 суток) достигается за счет перорального введения меконовой кислоты в количестве от 2 до 4 мг/кг массы тела, которое способствует повышению уровня GSH - трипептида, являющегося одним из ключевых звеньев в антиоксидантной защите нервных клеток при окислительном стрессе [Калинина Е.В., Чернов Н.Н., Новичкова М.Д. Роль глутатиона, глутатионтрансферазы и глутаредоксина в регуляции редокс-зависимых процессов // Успехи биологической химии, Т. 54, 2014, С. 299-348.; Зозуля Ю.А., Барабой В.А., Сутковой Д.А. Свободнорадикальное окисление и антиоксидантная защита при патологии головного мозга М.: Знание-М. 2000. 344 с.]. Тиоловые группы в составе GSH вступают в реакцию с свободнорадикальными частицами азота и кислорода, что приводит к ингибированию процессов перекисного окисления липидов и предотвращению повреждения клеточных мембран нейронов, выражающееся уменьшением первичных и вторичных продуктов окисления - диеновых конъюгатов (ДК) и малонового диальдегида (МДА).
Изменение количественных параметров меконовой кислоты не позволяет достичь технического результата, так как экспериментально установлено, что введение меконовой кислоты в количестве менее 2 мг/кг массы тела в течение 2-5 суток не приводит к необходимой выработке GSH, связанное с недостаточной активацией экспрессии генов, кодирующих ферменты - глутатионсинтазу и γ-глутамилцистеинлигазу, которые участвуют в синтезе GSH de novo. В результате чего воздействие гипоксии инициирует окислительный стресс, проявляющийся в повышении уровня ДК и МДА.
Экспериментальным путем установлено, что введение меконовой кислоты в дозе свыше 4 мг/кг позволяет достигнуть сопоставимый технический результат, что и при введении меконовой кислоты в дозе 4 мг/кг. Однако, при введении меконовой кислоты в дозе свыше 4 мг/кг развивается умеренный седативный эффект, связанный с накоплением достаточного количества меконовой кислоты в клетках головного мозга для активации ГАМКа-рецепторов [Khrapov А.А., Chepkova A.N., Shurygin A.Y., Skrebitskii V.G. Balysum-2 inhibits evoked activity of the pyramidal neurons in hippocampus // Bulletin of Experimental Biology and Medicine. 1998. Vol. 125, №1. P. 53-55.], а введение меконовой кислоты в дозе 5 мг/кг и более способствует развитию выраженного седативного действия [US 2003/0181516 A1 Substance with sedative effect. Pub. Date: Sep. 25, 2003]. Развитие умеренного седативного действия может привести к снижению скорости реакции, вниманию и концентрации, а также может повышать травматизм [Предотвращение падений и снижение травматизма при падениях / Ж.Б. Бекбергенова, К. Аймолдина, Б. Ниязова, А. Баймульдина - Нур-Султан: 2019. - 44 с.], что делает нецелесообразным введение меконовой кислоты в дозе свыше 4 мг/кг для достижения технического результата.
Результаты исследования представлены в таблице 1.

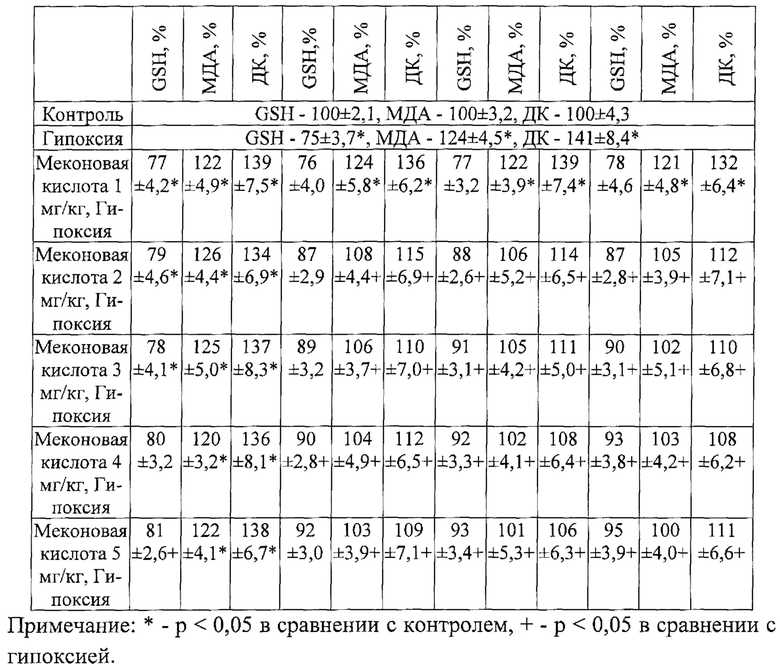
Пример 1.
Исследование выполнено на крысах-самцах Wistar в возрасте 2 месяца и массой 200±21 г. Крысы были разделены на группы:
1. Контрольные, получавшие воду;
2. Получавшие меконовую кислоту в количестве 1 мг/кг в течение 4 суток;
3. Получавшие меконовую кислоту в количестве 2 мг/кг в течение 4 суток;
4. Гипоксированные, получавшие воду;
5. Гипоксированные, получавшие меконовую кислоту в количестве 1 мг/кг в течение 4 суток;
6. Гипоксированные, получавшие меконовую кислоту в количестве 2 мг/кг в течение 4 суток;
Острую гипоксию с гиперкапнией моделировали у крыс, помещая их в герметичные сосуды, емкостью 1 л. Животные находились в таких условиях до появления первого атонального вздоха. После этого крыс извлекали и помещали в стандартные клетки. На следующий день после моделирования острой гипоксии с гиперкапнией крыс декапитировали, а головной мозг помещали в жидкий азот для последующего анализа.
Интенсивность окислительных процессов в тканях головного мозга оценивали содержанием первичных и вторичных продуктов перекисного окисления липидов - ДК и МДА в условиях нормоксии (без воздействия гипоксии) и через 1 сутки после воздействия острой гипоксии с гиперкапнией. ДК, образующиеся в результате миграции двойной связи в полиненасыщенных жирных кислотах, определяли по В.Б. Гаврилову. После экстракции в смеси гептан-изопропанол (2:1) и последующего наслаивания HCI (рН 2,0), диеновые конъюгаты выявляли в гептановой фазе при 233 нм. Содержание МДА определяли по концентрации окрашенного комплекса, образующегося при взаимодействии МДА с тиобарбитуровой кислотой по методу [Гаврилов В.Б., Гаврилова А.Р., Мажуль Л.М. Анализ методов определения продуктов перекисного окисления липидов в сыворотке крови по тесту с тиобарбитуровой кислотой // Вопр. мед. химии. 1987. Т. 33, №1. С. 118-122]. Содержание восстановленного глутатиона определяли с помощью реактива Эллмана (5,5'-дитиобис-(2-нитробензойной кислоты)), данные предстваляли в мкмоль на 1 г белка [The in vitro and in vivo neuroprotective activity of sodium comenate in stress / L.V. Shurygina, A.A. Kravtsov, E.I. Zlishcheva, L.G. Khaspekov // Neurochemical Journal. - 2017. - Vol. 11. - No 3. - P. 250-254. - DOI 10.1134/S1819712417020118.]. Статистическую обработку полученных данных проводили с использованием STATISTIC А 10. Для оценки достоверности различий выборок в биохимических тестах применяли t-критерий Стью-дента.
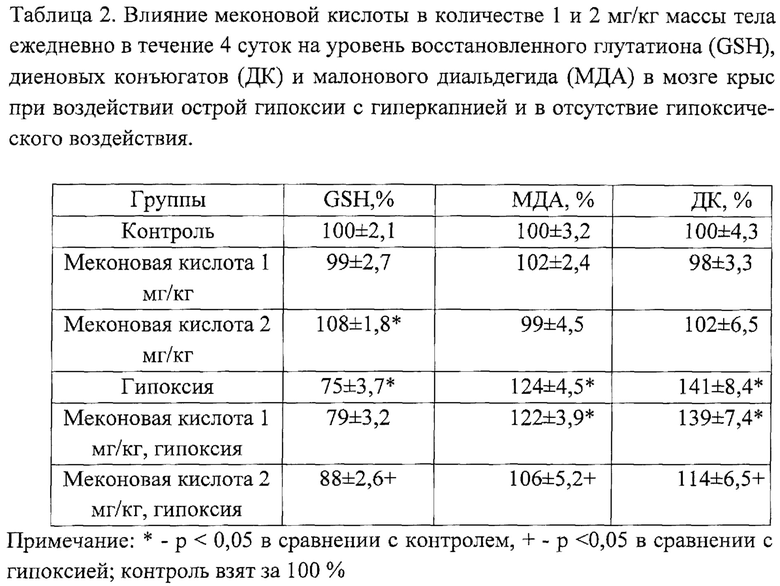
Как показал анализ результатов, гипоксическое воздействие привело к окислительному повреждению тканей головного мозга, выражающееся достоверным повышением первичных продуктов окисления - диеновых конъюгатов (ДК) на 41% и вторичных продуктов окисления - малонового диальдегида (МДА) на 24% относительно контроля, и снижению уровня GSH на 25% соответственно (Табл. 2). Применение меконовой кислоты до воздействия острой гипоксии с гиперкапнией в количестве 2 мг/кг массы тела перорально один раз ежедневно в течение 4 суток способствовало снижению окислительного повреждения нервной ткани, выражающееся меньшим накоплением продуктов перекисного окисления липидов на 6 и 14% (р>0,05 в сравнении с контролем, р<0,05 в сравнении с гипоксией) по сравнению с группой - гипоксия. Выраженное понижение повреждения нервной ткани окислительным стрессом связано с тем, что меконовая кислота способствует повышению антиоксидантного потенциала тканей головного мозга за счет дополнительного образования GSH на 8% по сравнению с контрольной группой. Это создает возможность поддерживать достаточно высокий уровень тиоловых групп, обеспечивающих защиту нейронов при гипоксическом воздействии. В отсутствие гипоксии меконовая кислота не оказала достоверного влияния на показатели окислительного стресса: уровень ДК и МДА измелились на 1-2%, что говорит об отсутствии токсического действия исследуемого вещества. Применение меконовой кислоты до воздействия острой гипоксии с гиперкапнией в количестве 1 мг/кг массы тела ежедневно в течение 4 суток не способствовало достоверному снижению интенсивности окислительных процессов и повышению уровня GSH в тканях головного мозга и, следовательно, не оказало защитного действия.
Пример 2.
Исследование выполнено на крысах-самцах Wistar в возрасте 2 месяца и массой 200±21 г. Крысы были разделены на группы:
1. Контрольные, получавшие воду;
2. Получавшие меконовую кислоту в количестве 3 мг/кг в течение 3 суток;
3. Получавшие меконовую кислоту в количестве 4 мг/кг в течение 3 суток;
4. Гипоксированные, получавшие воду;
5. Гипоксированные, получавшие меконовую кислоту в количестве 3 мг/кг в течение 3 суток;
6. Гипоксированные, получавшие меконовую кислоту в количестве 4 мг/кг в течение 3 суток;
Острую гипоксию с гиперкапнией моделировали у крыс, помещая их в герметичные сосуды, емкостью 1 л. Животные находились в таких условиях до появления первого атонального вздоха. После этого крыс извлекали и помещали в стандартные клетки. На следующий день после моделирования острой гипоксии с гиперкапнией крыс декапитировали, а головной мозг помещали в жидкий азот для последующего анализа.
Интенсивность окислительных процессов в тканях головного мозга оценивали содержанием первичных и вторичных продуктов перекисного окисления липидов - ДК и МДА в условиях нормоксии (без воздействия гипоксии) и через 1 сутки после воздействия острой гипоксии с гиперкапнией. ДК, образующиеся в результате миграции двойной связи в полиненасыщенных жирных кислотах, определяли по В.Б. Гаврилову. После экстракции в смеси гептан-изопропанол (2:1) и последующего наслаивания HCI (рН 2,0), диеновые конъюгаты выявляли в гептановой фазе при 233 нм. Содержание МДА определяли по концентрации окрашенного комплекса, образующегося при взаимодействии МДА с тиобарбитуровой кислотой по методу Гаврилов В.Б. и соавт. Содержание восстановленного глутатиона определяли с помощью реактива Эллмана (5,5'-дитиобис-(2-нитробензойной кислоты)), данные представляли в мкмоль на 1 г белка. Статистическую обработку полученных данных проводили с использованием STATISTIC А 10. Для оценки достоверности различий выборок в биохимических тестах применяли t-критерий Стьюдента.
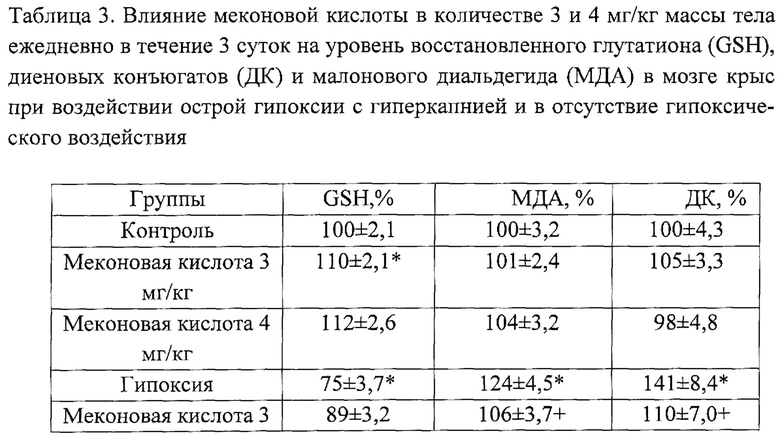

Из таблицы 3 видно, что гипоксичсское воздействие привело к смещению прооксидантного/антиоксидантного равновесия в сторону развития окислительного стресса, выражающиеся повреждением мембран нервных клеток, и как следствие возрастанию ДК на 41% и МДА на 24% по сравнению с контрольной группой. Чрезмерное образование свободных радикалов оказало нагрузку на глутатионовую систему и привело к окислительному повреждению тиоловых групп GSH на 25% (Табл. 3). Применение меконовой кислоты в количестве 3 мг/кг массы тела пероралыю один раз ежедневно в течение 3 суток до воздействия острой гипоксии с гиперкапнией способствовало активации синтезу GSH и повышению его запасов на 10% по сравнению с контрольной группой, что способствовало снижению интенсивности окислительных процессов, вызванных гипоксией, сопровождающиеся сохранению данных параметров на уровне физиологической нормы (р>0,05 в сравнении с контролем, р<0,05 в сравнении с гипоксией). Применение меконовой кислоты в количестве 4 мг/кг массы тела ежедневно в течение 3 суток до воздействия острой гипоксии с гиперкапнией показало схожий технический результат, что при введении 3 мг/кг в течение 3 суток. А именно, способствовало повышению содержания GSH в тканях головного мозга на 12% по сравнению контролем, и снижению продуктов окислительного стресса. Уровень ДК составил 13%, а для МДА 6%. В отсутствие гипоксии меконовая кислота в количестве 3 и 4 мг/кг в течение 3 суток применения не оказала достоверного влияния на показатели окислительного стресса. Уровень ДК и МДА в этих группах животных сопоставим с контрольной группой.
Таким образом, введение меконовой кислоты в количестве 3 и 4 мг/кг массы тела ежедневно в течение 3 суток оказывала защитный эффект на ткани головного мозга после воздействия острой гипоксии с гиперкапнией.
Пример 3.
Исследование выполнено на крысах-самцах Wistar в возрасте 2 месяца и массой 200±21 г. Крысы были разделены на группы:
1. Контрольные, получавшие воду;
2. Получавшие меконовую кислоту в количестве 4 мг/кг в течение 4 суток;
3. Получавшие меконовую кислоту в количестве 5 мг/кг в течение 4 суток;
4. Гипоксированные, получавшие воду;
5. Гипоксированные, получавшие меконовую кислоту в количестве 4 мг/кг в течение 4 суток;
6. Гипоксированные, получавшие меконовую кислоту в количестве 5 мг/кг в течение 4 суток;
Острую гипоксию с гиперкапнией моделировали у крыс, помещая их в герметичные сосуды, емкостью 1 л. Животные находились в таких условиях до появления первого атонального вздоха. После этого крыс извлекали и помещали в стандартные клетки. На следующий день после моделирования острой гипоксии с гиперкапнией крыс декапитировали, а головной мозг помещали в жидкий азот для последующего анализа.
Интенсивность окислительных процессов в тканях головного мозга оценивали содержанием первичных и вторичных продуктов перекисного окисления липидов - ДК и МДА в условиях нормоксии (без воздействия гипоксии) и через 1 сутки после воздействия острой гипоксии с гиперкапнией. ДК, образующиеся в результате миграции двойной связи в полиненасыщенных жирных кислотах, определяли по В.Б. Гаврилову. После экстракции в смеси гентан-изопропанол (2:1) и последующего наслаивания HCI (рН 2,0), диеновые конъюгаты выявляли в гептановой фазе при 233 нм. Содержание МДА определяли по концентрации окрашенного комплекса, образующегося при взаимодействии МДА с тиобарбитуровой кислотой по методу Гаврилов В.Б. и соавт. Содержание восстановленного глутатиона определяли с помощью реактива Эллмана (5,5'-дитиобис-(2-нитробензойной кислоты)), данные представляли в мкмоль на 1 г белка. Статистическую обработку полученных данных проводили с использованием STATISTICA 10. Для оценки достоверности различий выборок в биохимических тестах применяли t-критерий Стьюдента.
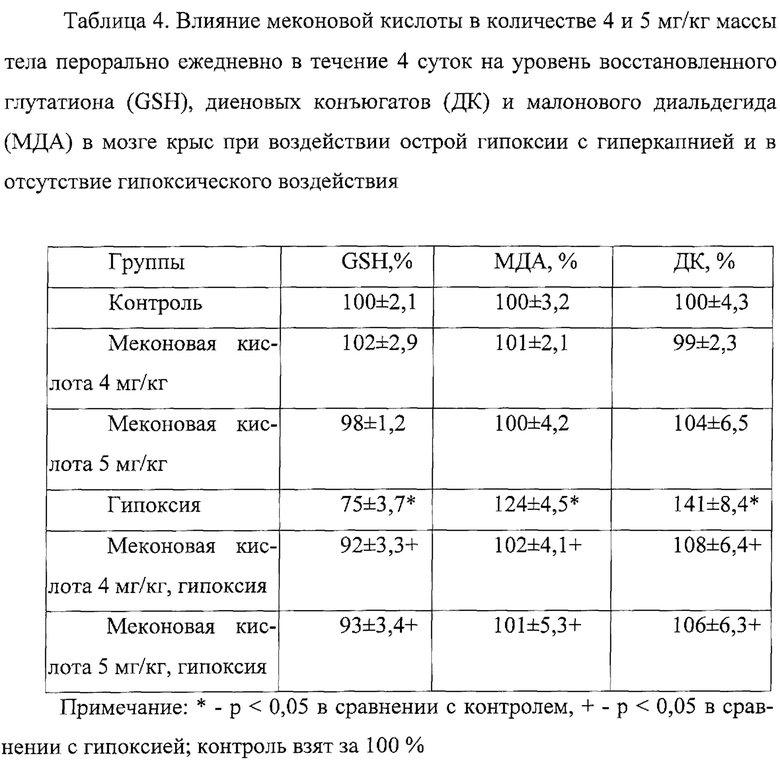
Из результатов экспериментов, представленных в таблице 4, видно, что гипоксическое воздействие привело к окислительному повреждению тканей головного мозга, выражающееся достоверным повышением первичных (ДК) на 41% и вторичных продуктов (МДА) 24% окислительного стресса и снижению уровня GSH на 25% соответственно. Применение меконовой кислоты в количестве 4 мг/кг массы тела ежедневно в течение 4 суток до воздействия острой гипоксии с гиперкапнией привело к повышению уровня GSH относительно гипоксии (р<0,05), что привело к снижению окислительных процессов в тканях головного мозга по отношению к гипоксии - уровни ДК и МДА остались на уровне физиологической нормы (р>0,05 в сравнении с контролем). Аналогичная картина наблюдалась при применении меконовой кислоты в количестве 5 мг/кг массы тела ежедневно в течение 4 суток - уровни GSH, ДК и МДА остались на уровне контрольной группы и достоверно отличались от гипоксии, однако при применении меконовой кислоты в количестве 5 мг/кг массы тела ежедневно в течение 4 суток до воздействия острой гипоксии с гиперкапнией наблюдалось снижение двигательной активности животных, что является одним из признаков седативного действия. Из научно-технических источников известно, что применение меконовой кислоты в количестве свыше 4 мг/кг, например, 5 мг/кг, проявляется сильное седативное действие, что является неприемлемым побочным эффектом в случае лечения последствий гипоксии.
Использование предлагаемого способа лечения головного мозга при острой гипоксии с гиперкапнией позволило предотвратить развитие окислительного повреждения тканей головного мозга за счет повышения уровня восстановленного глутатиона в них, обеспечивая тем самым высокую эффективность за меньшее время.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПРОФИЛАКТИКИ И КОРРЕКЦИИ МЕТАБОЛИЧЕСКИХ И ФУНКЦИОНАЛЬНЫХ НАРУШЕНИЙ ЦЕНТРАЛЬНОЙ НЕРВНОЙ СИСТЕМЫ В УСЛОВИЯХ СТРЕССА | 2019 |
|
RU2717107C1 |
| АНТИОКСИДАНТНОЕ, СТРЕСС-И НЕЙРОПРОТЕКТОРНОЕ ФАРМАКОЛОГИЧЕСКОЕ СРЕДСТВО-КОМЕНАТ КАЛИЯ | 2012 |
|
RU2514632C1 |
| СРЕДСТВО НА ОСНОВЕ ПРИРОДНЫХ ФОСФОЛИПИДОВ | 2008 |
|
RU2367443C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ АНТИРАДИКАЛЬНЫМИ, ЦЕРЕБРОПРОТЕКТОРНЫМИ И ПРОТИВОИШЕМИЧЕСКИМИ СВОЙСТВАМИ | 2010 |
|
RU2445090C1 |
| АНТИОКСИДАНТНОЕ, СТРЕСС- И НЕЙРОПРОТЕКТОРНОЕ ФАРМАКОЛОГИЧЕСКОЕ СРЕДСТВО - КОМЕНАТ НАТРИЯ | 2012 |
|
RU2506078C1 |
| НЕЙРОПРОТЕКТОРНОЕ ФАРМАКОЛОГИЧЕСКОЕ СРЕДСТВО | 2013 |
|
RU2528914C1 |
| НЕЙРОПРОТЕКТОРНОЕ ФАРМАКОЛОГИЧЕСКОЕ СРЕДСТВО | 2014 |
|
RU2561045C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЛИТИЕВОЙ СОЛИ КОМЕНОВОЙ КИСЛОТЫ И ПРИМЕНЕНИЕ ЕЕ КАК АНТИОКСИДАНТНОГО СТРЕСС- И НЕЙРОПРОТЕКТОРНОГО СРЕДСТВА | 2011 |
|
RU2477722C1 |
| ПРИМЕНЕНИЕ L-КАРНОЗИНА ДЛЯ ПРИГОТОВЛЕНИЯ НАНОПРЕПАРАТА, ОБЛАДАЮЩЕГО АНТИГИПОКСИЧЕСКОЙ И АНТИОКСИДАНТНОЙ АКТИВНОСТЬЮ | 2012 |
|
RU2482867C1 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ СВЯЗАННЫХ СО СТРЕССОВЫМИ УСЛОВИЯМИ ЗАБОЛЕВАНИЙ И РАССТРОЙСТВ У ЧЕЛОВЕКА И ЖИВОТНЫХ, А ТАКЖЕ СПОСОБ ЛЕЧЕНИЯ И/ИЛИ ПРОФИЛАКТИКИ С ИСПОЛЬЗОВАНИЕМ ЭТОГО СРЕДСТВА | 2009 |
|
RU2450823C2 |
Изобретение относится к медицине, а именно к экспериментальной медицине и неврологии, и может быть использовано при лечении головного мозга при острой гипоксии с гиперкапнией. Способ включает пероральное введение защитного средства. В качестве защитного средства применяют меконовую кислоту в количестве от 2 до 4 мг/кг массы тела ежедневно в течение 3-4 суток. Использование изобретения позволяет предотвратить окислительное повреждение тканей головного мозга, вызванное острой гипоксией с гиперкапнией, за счет повышения уровня восстановленного глутатиона (GSH) в головном мозге. 4 табл., 3 пр.
Способ лечения головного мозга при острой гипоксии с гиперкапнией, включающий пероральное введение защитного средства, отличающийся тем, что в качестве защитного средства применяют меконовую кислоту в количестве от 2 до 4 мг/кг массы тела ежедневно в течение 3-4 суток.
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ПРОТИВОГИПОКСИЧЕСКОЙ, АНТИАМНЕСТИЧЕСКОЙ И НЕЙРОПРОТЕКТОРНОЙ АКТИВНОСТЬЮ | 2020 |
|
RU2750418C1 |
| СПОСОБ ПОВЫШЕНИЯ УСТОЙЧИВОСТИ ОРГАНИЗМА К ОСТРОЙ ГИПОКСИИ В ЭКСПЕРИМЕНТЕ | 2013 |
|
RU2517032C1 |
| СИНТЕТИЧЕСКОЕ АНАЛЬГЕТИЧЕСКОЕ СРЕДСТВО И СПОСОБ ЛЕЧЕНИЯ НА ОСНОВЕ ЭТОГО СРЕДСТВА | 2006 |
|
RU2322977C1 |
| ЕВСЕЕВА М | |||
| А | |||
| и др | |||
| Механизмы развития острой гипоксии и пути ее фармакологической коррекции//Обзоры по клинической фармакологии и лекарственной терапии | |||
| Станок для изготовления деревянных ниточных катушек из цилиндрических, снабженных осевым отверстием, заготовок | 1923 |
|
SU2008A1 |
| Приспособление для точного наложения листов бумаги при снятии оттисков | 1922 |
|
SU6A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| KOZIN S.V | |||
| et al | |||
| Cytoprotective and Antioxidant Effects of Meconic Acid in Model | |||
Авторы
Даты
2023-09-12—Публикация
2022-10-21—Подача