Изобретение относится к экспериментальной медицине и фармакологии, а именно средствам для профилактики и лечения нейродегенеративных заболеваний, вызываемых оксидативным повреждением мозга.
Многие патологии ЦНС, при которых наблюдаются деструктивные процессы нейронов головного мозга, связаны с активацией перекисного окисления липидов (ПОЛ) [Попова М.С., Степаничев М.Ю. Индукция клеточного цикла, амилоид-бетта и свободные радикалы в механизме развития нейродегенеративных процессов в мозге. // Нейрохимия. 2008. Т.25. №3. С.170-178; Зозуля Ю.А., Барабой В.А., Сутковой Д.А. Свободнорадикальное окисление и антиоксидантная защита при патологии головного мозга. М.: Знание. 2000. С.226-221]. Окислительный стресс, ведущий к гиперпродукции свободных радикалов (СР) и деструкции мембран, связанной с активацией фосфолипазного гидролиза, играет главную роль в патогенетических механизмах ишемии мозга. Ишемия головного мозга инициирует каскад биохимических реакций, лежащих в основе тканевого повреждения. Основные механизмы нейронального повреждения включают истощение энергетических ресурсов в условиях ацидоза ткани мозга, нарушение ионного гомеостаза, деполяризацию клеточных мембран, накопление возбуждающих аминокислот и гиперпродукцию активных форм кислорода (АФК). Хронический окислительный стресс приводит к повреждению всех классов биомолекул, включая липиды, белки, и нуклеиновые кислоты. Избыток свободных радикалов, отрицательно воздействующий на ДНК нейронов мозга, может вызвать изменение в генетическом коде и гибель клетки [Смирнова И.Н., Федорова Т.Н., Танашян М.М., Суслина З.А. Клиническая эффективность и антиоксидантная активность мексидола при хронических цереброваскулярных заболеваниях. // Нервные болезни. 2006. №1. С 33-36; Федорова Т.Н. Окислительный стресс и защита головного мозга от ишемического повреждения: Дисс. д-ра биол. наук: 03.00.04: Москва. 2004. 298 с. РГБ ОД. 71:05-3/6; Завалишин И.А., Захарова М.Н. Рассеянный склероз: современные аспекты этиологии и патогенеза. // Журнал неврологии и психиатрии им. С.С.Корсакова (прил. «Рассеянный склероз»). 2003. №1. С.72-75].
Другим важнейшим фактором, вызывающим гибель нейронов, является продолжительная стимуляция нейронов ЦНС нейромедиатором глутаматом. Являясь возбуждющим нейромедиатором, глутамат содержится в большинстве нейронов мозга. В условиях ишемии глутамат высвобождается из окончаний ишемизированных нейронов в межклеточное пространство. В нормальных условиях нейроны и клетки глии поглощают избыточный глутамат из межклеточного пространства. Однако ишемические клетки лишены необходимой для этого энергии. В результате накопления большого количества глутамата происходит насыщение рецепторов соседних нейронов и зона повреждения расширяется Перевозбуждение глутаматных рецепторов, сопровождающее гипоксию, ишемию, оказывает поражающее действие на нейроны, приводит к нарушениям кальциевого гомеостаза. Отсроченная кальциевая дизрегуляция является одним из ключевых сигналов, приводящих к усилению генерации АФК и ПОЛ после токсического действия глутамата, снижению уровня эндогенных антиоксидантов, повреждению и гибели клеток мозга при ишемических состояниях [Суслина З.А., Максимова М.Ю. Концепция нейропротекции: новые возможности ургентной терапии ишемического инсульта. Симпозиум НИИ неврологии РАМН «Лечение ОНМК: состояние проблемы». // Нервные болезни. 2004. №3. С 4-7; Vergun О., Keelan J., Khodorov B.I., Duchen M.R. Glutamate-induced mitochondrial depolarisation and perturbation of calcium homeostasis in cultured rat hippocampal neurons. // J. Physiol. 1999. Vol.519. P.451-466; Пинелис В.Г., Быкова Л.П., Богачев А.П., Исаев Н.К., Викторов И.В., Ходоров Б.И. Токсическое действие глутамата на культивируемые зернистые клетки мозжечка снижает внутриклеточное содержание АТФ. Роль ионов Са2+. // Бюл. эксперим. биол. и мед. 1997. Т.123. №2. С.162-164; Nishizawa Y. Glutamate release and neuronal damage in ischemia. // Life Sciences. 2001. Vol.69. P.369-381].
Антиоксидантная защита организма при оксидативном стрессе неспособна полностью нейтрализовать образующийся избыток АФК. В этих условиях очевидна целесообразность использования антиоксидантных препаратов, способных защитить мозговую ткань от повреждения [Nonaka Sh., Katsube N. and Chuang D. -M. Lithium Protects Rat Cerebellar Granule Cells against Apoptosis Induced by Anticonvulsants, Phenytoin and Carbamazepine. // JPET. 1998. V.286. P.539-547].
В настоящее время для профилактики и лечения дегенеративных заболеваний с ишемическим повреждением применяют антиоксиданты, которые по своему происхождению подразделяют на две основные группы: природные и синтетические.
Природные антиоксиданты: ферменты, белки, низкомолекулярные соединения (витамины Е и С, каротиноиды, убихинон и др.).
Группу синтетических антиоксидантов представляют синтетические аналоги витамина Е, ароматические фенолы и полифенолы (ионол, пробукол), эмоксипин и мексидол, некоторые производные барбитуровой кислоты и фенотиазина, препараты железа и цинка, органические кислоты и их производные, некоторые аминокислоты и производные аминостероидов [Карнеев А.Н., Соловьева Э.Ю. и др. Использование препаратов альфа-липоевой кислоты в качестве нейропротективной терапии хронической ишемии мозга. Справочник поликлинического врача. http://old.consilium-medicum.com/media/refer/06_08/76.shtml]. При этом интоксикация некоторыми лекарственными препаратами, в том числе барбитуратами может вызвать обратимые когнитивные расстройства - дисметаболические деменции [Чухловина М.Л. Деменция. Диагностика и лечение. Санкт-Петербург. 2010. С.60].
Известно применение натрия оксибутирата (натриевая соль g-оксимасляной кислоты). Натрия оксибутират обладает выраженным антигипоксическим действием. Он повышает устойчивость организма, в том числе тканей мозга, сердца, также сетчатки глаза, к кислородной недостаточности. Препарат оказывает седативное и центральное миорелаксантное действие, в больших дозах вызывает сон и состояние наркоза. Препарат противопоказан при гипокалиемии, миастении. Осторожность требуется при токсикозах беременных с гипертензивным синдромом. В связи с седативным эффектом не надлежит назначать продукт (при неврозах, глаукоме и т.д.) в дневные часы лицам, работа которых требует быстрой физической и психической реакции [http://ru.wikipedia.org/wiki; Крыжановский Г.Н. Возможности применения оксибутирата лития в патологии. // Новые данные по фармакологии и клиническому применению солей лития: сборник трудов НИИ фармакологии АМН ССР. Под ред. д-ра мед. наук, проф. Любимова. М. 1984. С.49-57].
Известно антиоксидантное нейропротекторное средство пикамилон - натриевая соль N-никотинол-γ-аминомасляной кислоты. Наличие в химической структуре пикамилона гаммааминомасляной кислоты (ГАМК) и никотиновой кислоты обусловливает его ноотропное и вазоактивное действие. Он улучшает мозговое кровообращение и позитивно влияет на метаболизм ткани головного мозга. Препарат оказывает также антигипоксическое, антиоксидантное и антиагрегантное действие, обладает транквилизирующим эффектом. Механизм действия пикамилона обусловлен его взаимодействием с ГАМК-рецепторами. Имеет побочные эффекты: аллергические реакции, головная боль, головокружение, чувство тревоги [Фармакология спорта. / Горчакова Н.А., Гудивок Я.С., Гунина Л.М. и др.; под общ. ред. С.А. Олейкина, Л.М. Гуниной, Р.Д. Сейфуллы. К.: Олимп. л-ра. 2010. 640 с].
Наиболее близким к заявляемомому антиоксидантному нейропротекторному средству является коменовая кислота (5-гидрокси-γ-пирон-2-карбоновая).
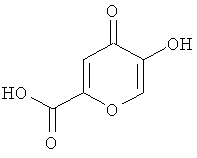
Коменовая кислота обладает антиоксидантным и нейротропным свойствами [Шурыгин А.Я., Колендо С.В., Югай Г.А. Антиоксидантное действие коменовой кислоты. Известия ВУЗов. Северо-Кавказский регион. Естественные науки. 2000. №1. С.100-101; Гусарук Л.Р. Влияние перенесенного стресса на морфофункциональные особенности культивируемых нейронов крыс. Автореф. дисс. канд. биол. наук. М. 1998; Шурыгин А.Я. Препарат бализ. 2002. 416 с.].
Коменовая кислота обладает мягким седативным действием, не вызывающим привыкания [патент РФ на изобретение №2209062, МПК7 А61К 31/351, А61Р 25/20], является высокоэффективным ненаркотическим анальгетическим средством, не имеющим негативных побочных эффектов, не вызывающих зависимости и привыкания, приводящим к долговременному снятию болевого синдрома [патент РФ №2322977, А61К 31/351 (2006.01), А61Р 29/02 (2006.01)]. Обладает антиабстинентным, анксиолитическим и антидепресантными свойствами [Панова Т.И. Механизмы влияния коменовой кислоты на интегративную деятельность мозга. / Теоретическая экспериментальная медицина. Медицина сегодня и завтра. 2005. №1. С.28-33].
Техническим результатом является создание лекарственного средства, способствующего снижению гибели нейронов при различных нейродегенеративных заболеваниях, связанных с оксидативным повреждением мозга.
Для достижения технического результата предлагается использовать в качестве фармакологического средства для профилактики и лечения нейродегенеративных заболеваний, вызываемых оксидативным повреждением мозга, натриевую соль коменовой кислоты (коменат натрия), полученную при смешении раствора коменовой кислоты, подогретого до температуры не более 80±2°С, с раствором карбоната или гидроксида натрия при объемах, взятых из расчета, произведенного стехиометрически, до значения рН, равного 4,6. Коменат натрия применяют в количестве от 1 до 4-х мг на 1 кг массы тела в качестве антиоксидантного, стресс- и нейропротекторного средства ежедневно один раз натощак, в течение 3-х суток.
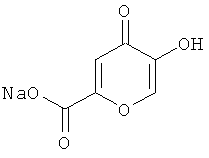
Для получения натриевой соли коменовой кислоты с карбонатом натрия берем 25 мл 0,12 н. горячего раствора коменовой кислоты (80±2°С) и добавляем 15 мл 0,2 н. раствора карбоната натрия, помешивая.
Для получения натриевой соли коменовой кислоты с гидроксидом натрия берем 25 мл 0,12 н. горячего раствора коменовой кислоты (80±2°С) и добавляем 30 мл 0,1 н. раствора гидроксида натрия, помешивая.
Реакции протекают быстро, раствор окрашивается в желтый цвет. Натриевую соль коменовой кислоты выделяют из раствора отгонкой воды под вакуумом или выпариванием воды из раствора соли на водяной бане. Выход натриевой соли коменовой кислоты составляет 85-90%.
Известно, что натрий важен для нервной и мышечной деятельности, поскольку образует электролитическую среду (электролитическую среду создают в основном 3 элемента - натрий, хлор и калий), необходимую для нормальной работы нервных окончаний и мышечных клеток [http://www.lishnemuvesu.ru/natrii.html]. Натрий участвует в поддержании осмотического давления и кислотно-щелочного равновесия, в проведении нервных импульсов [http://vitameal.ru/ibod.php?h=mna].
Установлено также, что помимо регуляции осмоса, генерации потенциала действия натрий играет ряд важных функций в ЦНС.
Антиоксидантные, стресс- и нейропротекторные свойства натриевой соли коменовой кислоты изучали с использованием модельной системы, генерирующей свободные радикалы (система ЦФЛ), культуры нейронов мозга, а также модели стресса на экспериментальных животных.
Действие комената натрия на генерацию АФК в модельной системе изучали в среде ЦФЛ следующего состава: 4 мл цитратного-фосфатного буфера (105 мМ KCl, 20 мМ KH2PO4, 4 мМ цитрата натрия; рН 7,45) с добавлением люминола (10 мМ). Образование АФК инициировали введением при постоянном перемешивании 30 мкл 35 мМ раствора сернокислого железа. В данной модели окисление ионов железа в присутствии ортофосфата и цитрата сопровождается образованием АФК и при этом возникает ХЛ, избирательно усиливающаяся люминолом, которая подавляется в присутствии антиоксидантов. Регистрацию ХЛ осуществляли прибором SmartLum 5773 в течение 5 минут. Оценивали светосумму хемилюминесценции. Антиокислительную активность натриевой соли коменовой кислоты оценивали по угнетению ХЛ модельной системы при добавлении водных растворов препарата в сравнении с раствором коменовой кислоты. Конечная концентрация вещества в кювете составляла 0,1 мг/мл и 0,01 мг/мл. Хемилюминесценсия свободных радикалов модельной системы ЦФЛ (контроль) принимается за 100% [Фархутдинов P.P., Лиховских В.А. Хемилюминесцентные методы исследования свободно-радикального окисления в биологии и медицине. 1995. Уфа. 90 с.]. Результаты экспериментов определяли по интенсивности хемилюминесценции (в у.е.) и рассчитывали в процентах от контроля. Обработку полученных данных осуществляли с помощью программного обеспечения PowerGraph версия 3.3. Достоверность отличий оценивали с помощью критерия Стьюдента. Результаты исследования представлены в таблице 1.
1 * р<0,001 в сравнении с контролем;
2 ** р<0,001 в сравнении с 0,01 мг/кг.
Анализ данных, представленных в таблице 1, показывает, что 0,1 мг/мл раствора натриевой соль коменовой кислоты значительно снижает содержание свободных радикалов в сравнении с контролем в модельной системе ЦФЛ. При этом уровень снижения свободных радикалов коменатом натрия практически не отличается от уровня гашения свободных радикалов коменовой кислотой. Антиокислительные свойства комената натрия и коменовой кислоты зависят от концентрации вещества. Так, повышение концентрации в испытуемом растворе с 0,01 мг/мл до 0,1 мг/мл способствует значительному, более чем на 30%, повышению уровня гашения свободных радикалов.
Таким образом, натриевая соль коменовой кислоты обладает выраженным антиоксидантным действием, при этом ее антиокислительные свойства практически не отличаются от таковых коменовой кислоты.
Влияние натриевой соли коменовой кислоты на антиоксидантную систему в мозге стрессированных животных
Известно, что в состав антиоксидантной системы, необходимой для контроля за продукцией активных форм кислорода и предотвращения свободнорадикальных реакций, входят как ферменты, так и многочисленные низкомолекулярные антиоксиданты или соединения, препятствующие образованию свободных радикалов. Различные антиоксиданты играют в тканях разную роль. Супероксиддисмутаза (СОД) контролирует клеточный уровень супероксид-аниона, дисмутируя его избыток в перекись водорода. Каталаза и глутатионовые ферменты превращают в воду гидропероксид, если он не покидает внутриклеточное пространство. В мозге антиоксидантная ферментная система представлена в основном суперокисддисмутазой и глутатион-зависимыми ферментами. [Федорова Т.Н. Окислительный стресс и защита головного мозга от ишемического повреждения: Дисс. д-ра биол. наук: 03.00.04: М. 2004. 298 с. РГБ ОД, 71:05-3/6]. СОД определяли по методу Е.Е. Дубининой [Дубинина Е.Е. и др. Сравнительный анализ активности супероксиддисмутазы и каталазы эритроцитов и цельной крови у новорожденных детей при хронической гипоксии. Лабораторное дело 1988. №8. С.16-19].
Активность каталазы определяли по методу, описанному М.А. Королюк и др. [Метод определения активности каталазы. // Лабораторное дело. 1988. №1. С.16-19].
Важным звеном защиты клеток от токсического действия первичных продуктов перекисного окисления липидов (ПОЛ) является антиоксидантная глутатионовая система [Барабой В.А., Сутковой Д.А. Окислительно-антиоксидантный гомеостаз в норме и патологии. / Под. ред. акад. АМН Украины Ю.А. Зозули. К. 1997. 413 с]. Влияние натриевой соли коменовой кислоты на антиоксидантную глутатионовую систему оценивали по активности ферментов глутатионпероксидазы, глутатионредуктазы и содержанию восстановленного глутатиона в мозге стрессированных животных.
Глутатион выполняет функцию донора водорода и кофактора ряда антиоксидантных ферментных систем. Снижение внутриклеточного содержания восстановленного глутатиона существенно снижает устойчивость клеток и организма к интоксикации. Определение свободных сульфгидрильных групп (восстановленного глутатиона (GSH)) в кислоторастворимом надосадке) проводили по методу J.Sedlak [Sedlak J., Lindsay R.H. Estimation of total, proteinbound and nonprotein sulthydryl groups in tissue with Ellman's reagent. Anal Biochem 1968. Vol.25. P.192-205].
Фермент глутатионпероксидаза (ГП) является одним из основных ферментов антиокислительной защиты организма от эндогенно или экзогенно индуцированного образования перекисей, в том числе перекисей липидов. С помощью глутатиона ГП восстанавливает основной продукт перекисного окисления липидов - гидроперекиси липидов, обезвреживает их токсическое действие на мембраны и предотвращает инициацию вторичных реакций окисления липидов [Гаврилова А.Р., Хмара Н.Ф. Определение активности глутатионпероксидазы эритроцитов при насыщающих концентрациях субстрата. // Лабораторное дело. 1986. №12. С.721-724].
Глутатионпероксидазу определяли по скорости окисления глутатиона восстановленного в присутствии гидроперекиси третичного бутила [Моин В.М. Простой и специфический метод определения активности глутатионпероксидазы в эритроцитах. // Лабораторное дело. 1986. №12. С.724-727]. Сущность метода заключается в том, что во время инкубации пробы глутатионпероксидаза из супернатанта окисляет насыщающие концентрации глутатиона восстановленного - субстрата. По количеству оставшегося не окисленным глутатиона восстановленного судят об активности глутатионпероксидазы.
Функциональная роль высокоспецифичной цитоплазматической глутатионредуктазы заключается в генерации восстановленного глутатиона из его дисульфидной формы.
Активность глутатионредуктазы (ГР) определяется по методу Л.Б. Юсупова [Юсупов Л.Б. О повышении точности определения активности глутатионпероксидазы эритроцитов. // Лабораторное дело. 1989. №4. С.100-101].
Эксперимент проводили на белых беспородных мышах-самцах, массой 18-20 г.
Коменат натрия вводили мышам per os, натощак, в дозах 1, 2 и 4 мг/кг массы тела в течение 3-х суток, до стрессирования животных, один раз в сутки. Стресс вызывали методом иммобилизации, путем подвешивания мышей за шейную складку в течение пяти часов. Через 5 часов мышей декапитировали, головной мозг помещали в жидкий азот и затем определяли содержание восстановленного глутатиона, активность ферментов глутатионпероксидазы и глутатионредуктазы, СОД и каталазы. Дозы комената натрия были определены по результатам предварительных исследований. Анализ данных экспериментов показал, что коменат натрия, применяемый нами в более низких количествах, менее 1 мг/кг массы тела, практически не оказывает влияния на антиокислительные процессы в мозге стрессированных животных. При применении комената натрия в количествах, более высоких чем 4 мг/кг массы тела, эффективность существенно не отличается от данных при применении в количестве 4 мг/кг массы тела.
Были сформированы следующие группы животных:
1. интактные;
2. интактные + коменат натрия 1 мг/кг массы тела;
3. интактные + коменат натрия 2 мг/кг массы тела;
4. интактные + коменат натрия 4 мг/кг массы тела;
5. стрессированные;
6. стрессированные + коменат натрия 1 мг/кг массы тела;
7. стрессированные + коменат натрия 2 мг/кг массы тела;
8. стрессированные + коменат натрия 4 мг/кг массы тела.
Результаты исследования представлены в таблице 2.
*р≤0,05; **р≤0,05; ***р≤0,01 - достоверность статистически значимых различий по сравнению с интактным контролем
▪ р≤0,05; ▪▪ р≤0,01; ▪▪▪ р≤0,001 - достоверность по сравнению со стрессированными животными (стресс-контроль).
Анализ данных, представленных в таблице 2, показал, что при введении интактным мышам per os натриевой соли коменовой кислоты в количествах 1 и 2 мг/кг массы тела (группы 2, 3) активность ферментов глутатионпероксидазы, глутатионредуктазы и содержание восстановленного глутатиона оставались на уровне интактного контроля. Не выявлено изменений в этих группах и в активности ферментов СОД и каталазы. При применении комената натрия в количестве 4 мг/кг массы тела (группа 4) уровень восстановленного глутатиона снизился до уровня стрессированных животных (р>0,05), несколько повысилась ферментативная активность глутатионредуктазы, практически не отличалась от интактного контроля активность глутатионпероксидазы. Не выявлено существенных изменений при применении комената натрия в количестве 4 мг/кг массы тела (группа 4) в активности ферментов СОД и каталазы.
Стрессовое воздействие на организм мышей (группа 5) сопровождается выраженными изменениями в антиоксидантной глутатионовой защите. Так, увеличивается в сравнении с интактными животными в головном мозге активность глутатионпероксидазы (р≤0,05), повышается ферментативная активность глутатионредуктазы (р≤0,01), отмечается значительное снижение концентрации восстановленного глутатиона (р≤0,001).
При введении комената натрия per os в количествах 1 и 2 и 4 мг/кг массы тела (группы 6, 7, 8) в течение трех дней до стрессирования в головном мозге указанных групп животных отмечается восстановление антиоксидантной глутатионовой защиты до ее уровня у интактных животных.
Под влиянием стресса у мышей отмечается выраженное снижение ферментативной активности СОД и повышение активности каталазы (группа 5). При применении комената натрия в количествах 1, 2 и 4 мг/кг массы тела активность СОД и каталазы в головном мозге стрессированных мышей практически восстанавливается до уровня у интактных животных (группы 6, 7, 8).
Таким образом, установлено, что иммобилизационное стрессовое воздействие на организм мышей приводит к мобилизации глутатионовой АОС (статистически значимое повышение активности ферментов глутатионпероксидазы и глутатионредуктазы), снижению активности СОД и увеличению активности каталазы в головном мозге.
Применение натриевой соли коменовой кислоты в количествах от 1 до 4-х мг/кг массы тела один раз в сутки в течение трех дней до стрессирования животных способствует нормализации антиоксидантной защиты головного мозга. Это проявляется в снижении активности ферментов глутатионпероксидазы и глутатионредуктазы, повышении концентрации восстановленного глутатиона. Установлено также, что применение комената натрия в количествах от 1 до 4-х мг/кг массы тела способствует восстановлению после стрессового воздействия ферментативной активности СОД и каталазы. При этом уровень антиоксидантной защиты при применении комената натрия практически не отличается от такового в мозге интактных животных (группа 1).
Влияние натриевой соли коменовой кислоты на глутаматную цитотоксичность в культуре зернистых клеток мозжечка крысят.
Разработка методов профилактики и лечения базируется на предположении о том, что значительное число клеток мозга можно спасти, блокируя инициацию или ход внутринейрональных патохимических деструктивных процессов, имеющих определенные временные и пространственные характеристики.
Влияние натриевой соли коменовой кислоты на глутаматную цитотоксичность в культуре нейронов мозжечка крысят изучали в сравнении с коменовой кислотой.
Исследования выполнены на крысятах линии Wistar. Культуры зернистых клеток мозжечка получали из мозга 7-9-дневных крысят методом ферментно-механической диссоциации [Викторов И.В., Хаспеков Л.Г., Шашкова Н.А. // Руководство по культивированию нервной ткани: методы, техника, проблемы. 1986. М. 266 с]. Культуры клеток после 7 дней культивирования подвергали действию глутамата и/или комената натрия, коменовой кислоты.
Коменат натрия и коменовую кислоту вносили в группы культур нейронов без воздействия глутамата и после 10-минутного воздействия (100 мкМ) глутамата в сбалансированном солевом растворе (ССР), предварительно поместив их в исходную питательную среду. После чего культуры инкубировали в СО2-инкубаторе еще 4,5-5 часов. Исследовано влияние комената натрия в концентрациях 10-2 М, 10-3 М, 10-4 М, 10-5 М, 10-6 М и коменовой кислоты в концентрациях 10-3 М, 10-4 М. Контролем служили культуры, помещенные на 10 мин в ССР, а также культуры, обработанные глутаматом в ССР. После фиксации культур учитывали число живых и погибших нейронов на инвертированном микроскопе Invertoscopes ID 03. Достоверность отличий оценивали с помощью критерия Стьюдента в МО Excel 2003.
Культуры нейронов мозжечка, полученные от интактных крысят, делили на следующие группы соответственно:
1.1 контроль ССР;
1.2 ССР + коменат натрия 10-2 М;
1.3 ССР + коменат натрия 10-3 М;
1.4 ССР + коменат натрия 10-4 М;
1.5 ССР + коменат натрия 10-5 М;
1.6 ССР + коменат натрия 10-6 М;
1.7 ССР + коменовая кислота 10-3 М;
1.8 ССР + коменовая кислота 10-4 М;
1.9 контроль ССР с глутаматом (Glu) 100 мкМ;
2.0 ССР с глутаматом (Glu) 100 мкМ + коменат натрия 10-2 М;
2.1 ССР с глутаматом (Glu) 100 мкМ + коменат натрия 10-3 М;
2.2 ССР с глутаматом (Glu) 100 мкМ + коменат натрия 10-4 М;
2.3 ССР с глутаматом (Glu) 100 мкМ + коменат натрия 10-5 М.
2.4 ССР с глутаматом (Glu) 100 мкМ + коменат натрия 10-6 М;
2.5 ССР с глутаматом (Glu) 100 мкМ + коменовая кислота 10-3 М;
2.6 ССР с глутаматом (Glu) 100 мкМ + коменовая кислота 10-4 М.
Результаты исследования представлены в таблице 3.
1 # р<0,001 - в сравнении с контролем ССР;
2 *р<0,05 - в сравнении с группой контроль глутамат;
3 **р<0,001- в сравнении с группой контроль глутамат.
Анализ результатов исследований, отраженных в таблице 3, показал, что число выживших нейронов после воздействия коменатов натрия (группы 1.2-1.6) и коменовой кислоты (группы 1.7, 1.8) на интактные зернистые клетки мозжечка независимо от концентрации вещества, практически не отличается от контроля (группа 1.1). После воздействия глутамата выживаемость зернистых клеток мозжечка значительно (на 66,08%) снижается (группа 2.1), р<0,001. Практически на этом же уровне остается и выживаемость нейронов при добавлении в культуры с глутаматом комената натрия в концентрации 10-2 М и 10-6 М (группы 2.2 и 2.6). Повышение устойчивости нейронов мозжечка к глутаматной цитотоксичности отмечается при внесении в культуру обработанную глутаматом комената натрия в концентрациях 10-3 М-10-5 М (группы 2.3 и 2.4). При применении коменовой кислоты выживаемость нейронов в группах культур, обработанных глутаматом (2.7 и 2.8), была достоверно выше, чем в группе контроль-глутамат, однако ее максимум был значительно ниже, чем при добавлении в культуры натриевой соли коменовой кислоты.
Таким образом, установлено, что применение натриевой соли коменовой кислоты на фоне глутаматной цитотоксичности способствует значительному увеличению выживаемости нейронов мозжечка в культуре. При этом устойчивость нейронов к токсическому воздействию глутамата в культурах с добавлением натриевой соли коменовой кислоты превышает таковую при применении коменовой кислоты.
Токсичность натриевой соли коменовой кислоты мы оценивали по показателям антиоксидантной защиты в головном мозге экспериментальных животных (табл.2), а также по контрольным культурам нейронов мозжечка с добавлением исследуемых доз вышеназванной соли. Результаты исследований показали, что натриевая соль коменовой кислоты в количествах 1-4 мг/кг массы тела не токсична.
Известно, что основой для проведения клинических испытаний антиоксидантов при лечении заболеваний с дегенеративными расстройствами служат исследования, проведенные на культивируемых клетках и модельных животных [Andersen Julie К. Oxidative stress in neurodegene ration: cause or consequence? // Nature Reviews Neuroscience 2004. Vol.5. S18-S25].
Нами исследовано влияние различных доз натриевой соли коменовой кислоты на свободнорадикальное окисление in vitro в модельной системе ЦФЛ (табл.1), антиоксидантную систему в головном мозге стрессированных животных (табл.2), а также ее влияние на выживаемость культивируемых нейронов мозжечка на фоне глутаматной цитотоксичности.
Результаты исследований влияния комената натрия на свободнорадикальное окисление in vitro (модельная система ЦФЛ) и антиоксидантную систему головного мозга in vivo свидетельствуют о том, что натриевая соль коменовой кислоты обладает выраженными антиоксидантными свойствами. Применение комената натрия в количествах 1-4 мг/кг массы тела, один раз в день в течение 3-х суток до стрессирования мышей способствует восстановлению антиоксидантной системы головного мозга. При этом наиболее выраженное антиоксидантное, стресспротекторное действие при пероральном введении натриевая соль коменовой кислоты оказывает в количестве 2 мг/кг массы тела.
Установлено также, что применение натриевой соли коменовой кислоты в культуре нейронов мозжечка на фоне глутаматной цитотоксичности значительно повышает устойчивость нейронов мозжечка к глутаматной цитотоксичности. Максимальная выживаемость нейронов на фоне глутаматной цитотоксичности отмечается в группе культур после воздействии комената натрия в концентрации 10-4 М, 10-5 М (группа 2.4, 2.5).
Известно, что ионный гомеостаз является ключевым биохимическим показателем организма в норме и патологии, а также одной из наиболее значимых и привлекательных мишеней для дифференцированных фармакологических вмешательств. В ряду макро- и микроэлементов определяющих уровень здоровья человека и целый ряд важных физиологических реакций, в том числе со стороны нервной системы, весьма важное значение принадлежит натрию.
Ранее уже указывалось, что натрий важен для нервной и мышечной деятельности, поскольку образует электролитическую среду, он необходим для поддержания осмотического давления и кислотно-щелочного равновесия, для нормальной работы нервных окончаний и мышечных клеток в проведении нервных импульсов [Скальный А.В., Рудаков И.А. Биоэлементы в медицине. М. 2004. 272 с.]. Натрий играет ряд важных функций в ЦНС. Так работа транспортеров глутамата основана на градиенте ионов натрия, калия и самой аминокислоты [Семьянов А.В., Казанцев В.Б. Нейрон-глиальное взаимодействие в мозге. Нижний Новгород. 2007. 107 с]. От натрия зависит транспорт аминокислот, сахаров, различных неорганических и органических анионов через мембраны клеток. Для человека натрий нетоксичен.
Получение комената натрия и изучение авторами изобретения элементов тонкого механизма его воздействия на активированные окислительные процессы в головном мозге стрессированных животных и развитие глутаматной эксайтотоксичности, позволяют сделать вывод о перспективности его использования в качестве антиоксидантного, стресс- и нейропротекторного средства при нейродегенеративных заболеваниях, в том числе связанных с нарушениями ионного гомеостаза. Анализ известного уровня техники подтверждает новизну полученного соединения как антиоксидантного, стресс- и нейропротекторного средства.
Тем самым расширяется спектр высокоэффективных лекарственных средств с антиоксидантными, стресс- и нейропротекторными свойствами для профилактики и лечения нейродегенеративных заболеваний, вызываемых оксидативным повреждением мозга.
Следовательно, заявляемое техническое решение удовлетворяет критериям: новизна, изобретательский уровень и промышленная применимость.
| название | год | авторы | номер документа |
|---|---|---|---|
| АНТИОКСИДАНТНОЕ, СТРЕСС-И НЕЙРОПРОТЕКТОРНОЕ ФАРМАКОЛОГИЧЕСКОЕ СРЕДСТВО-КОМЕНАТ КАЛИЯ | 2012 |
|
RU2514632C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЛИТИЕВОЙ СОЛИ КОМЕНОВОЙ КИСЛОТЫ И ПРИМЕНЕНИЕ ЕЕ КАК АНТИОКСИДАНТНОГО СТРЕСС- И НЕЙРОПРОТЕКТОРНОГО СРЕДСТВА | 2011 |
|
RU2477722C1 |
| НЕЙРОПРОТЕКТОРНОЕ ФАРМАКОЛОГИЧЕСКОЕ СРЕДСТВО | 2014 |
|
RU2561045C1 |
| НЕЙРОПРОТЕКТОРНОЕ ФАРМАКОЛОГИЧЕСКОЕ СРЕДСТВО | 2013 |
|
RU2528914C1 |
| СПОСОБ ПРОФИЛАКТИКИ И КОРРЕКЦИИ НАРУШЕНИЙ ОСНОВНЫХ ФУНКЦИЙ ЦЕНТРАЛЬНОЙ НЕРВНОЙ СИСТЕМЫ ПРИ СВИНЦОВОЙ ИНТОКСИКАЦИИ В ПРЕНАТАЛЬНЫЙ И РАННИЙ ПОСЛЕРОДОВОЙ ПЕРИОД | 2009 |
|
RU2410107C1 |
| НЕЙРОПРОТЕКТОРНОЕ СРЕДСТВО | 2016 |
|
RU2614697C1 |
| СПОСОБ ПРОФИЛАКТИКИ И КОРРЕКЦИИ МЕТАБОЛИЧЕСКИХ И ФУНКЦИОНАЛЬНЫХ НАРУШЕНИЙ ЦЕНТРАЛЬНОЙ НЕРВНОЙ СИСТЕМЫ В УСЛОВИЯХ СТРЕССА | 2019 |
|
RU2717107C1 |
| КОМБИНИРОВАННОЕ ЛЕКАРСТВЕННОЕ СРЕДСТВО ДЛЯ ПЕРВИЧНОЙ НЕЙРОПРОТЕКЦИИ | 2017 |
|
RU2636616C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ПРЕДНАЗНАЧЕННАЯ ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ ЦЕНТРАЛЬНОЙ И ПЕРИФЕРИЧЕСКОЙ НЕРВНОЙ СИСТЕМЫ СОСУДИСТОГО, ТРАВМАТИЧЕСКОГО, ТОКСИЧЕСКОГО, ГИПОКСИЧЕСКОГО И АУТОИММУННОГО ГЕНЕЗА | 2010 |
|
RU2445106C1 |
| СПОСОБ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ НЕЙРОДЕГЕНЕРАТИВНОЙ ПАТОЛОГИИ И СОСУДИСТОЙ ДЕМЕНЦИИ | 2014 |
|
RU2587617C1 |
Изобретение относится к области медицины и фармакологии и касается применения натриевой соли коменовой кислоты в качестве профилактического и лечебного антиоксидантного, стресс- и нейропротекторного средства в количестве от 1 до 4-х мг на 1 кг массы тела ежедневно натощак, в течение 3-х суток. Изобретение обеспечивает высокую эффективность лечения. 3 табл.
Применение натриевой соли коменовой кислоты в качестве профилактического и лечебного антиоксидантного, стресс- и нейропротекторного средства в количестве от 1 до 4 мг на 1 кг массы тела, натощак один раз, в течение 3 суток.
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| - М., 2009, с.268-269 | |||
| US 3654316 А, 04.04.1972 | |||
| ВЕЩЕСТВО, ОБЛАДАЮЩЕЕ СЕДАТИВНЫМ ДЕЙСТВИЕМ | 2002 |
|
RU2209062C1 |
Авторы
Даты
2014-02-10—Публикация
2012-08-16—Подача