Область техники
Настоящее изобретение относится к самогерметизирующей инъекционной игле для предотвращения образования фистулы на глазном яблоке и к способу ее подготовки, а более конкретно, к самогерметизирующей инъекционной игле для предотвращения образования фистулы на глазном яблоке, причем поверхность инъекционной иглы покрыта гиалуроновой кислотой, а также к способу ее подготовки.
Уровень техники
Благодаря увеличению средней продолжительности жизни и численности пожилого населения, зрение приходится использовать в течение более длительного времени, при этом растет процент пациентов с глаукомой, диабетической ретинопатией и макулярной дегенерацией, которые являются хроническими заболеваниями, поражающими кровеносные сосуды глаза, широко известными как три основных заболевания, приводящие к слепоте.
Число пациентов с глаукомой увеличилось на 49% за четыре года, с 515 000 в 2011 году до 767 000 в 2015 году. За тот же период число пациентов с диабетической ретинопатией увеличилось примерно на 24%, а число пациентов с макулярной дегенерацией примерно на 48%. По состоянию на 2015 год общее число пациентов, страдающих от трех основных заболеваний, вызывающих слепоту, превысило около 1,2 миллиона человек. Если эта тенденция сохранится, то ожидается, что к 2020 году число подобных пациентов увеличится до 200 миллионов во всем мире.
Вышеупомянутые офтальмологические заболевания лечатся посредством интравитреальной инъекции, при которой антитела или противовоспалительный препарат вводят непосредственно в полость стекловидного тела.
Интравитреальная инъекция представляет собой процедуру, широко используемую в лекарственной терапии различных заболеваний, поражающих задний сегмент глаза. В частности, после освоения практики интравитреальной инъекции триамцинолона ацетонида для лечения диабетической ретинопатии, макулярного отека и увеита, в последнее время были предприняты попытки интравитреальной инъекции, различными способами, фактора роста эндотелия сосудов (анти-VEGF, от англ. anti-vascular endothelial growth factor) для лечения возрастной макулярной дегенерации и других заболеваний, что привело к хорошим результатам, поэтому популярность глазных инъекций быстро возросла (Гупта О.П. и др., Офтальмология. 2010 Ноябрь; 117 (11): 2134-40; Скэнлон П.Х. и др., Технология здравоохранения. Анализ. 2015 Сентябрь; 19(74): 1-116; Расмуссен А. и др., Acta. Офтальмология. 2017 Март; 95(2): 128-132).
Соответственно, увеличилось внимание к осложнениям, возникающим при интравитреальной инъекции. В частности, несмотря на относительно низкую частоту инфекционного эндофтальмита по сравнению с другими осложнениями, инфекционный эндофтальмит является осложнением, которое может привести к критическим последствиям, таким как слепота, поэтому ему необходимо уделять особое внимание (Соуед Е.Х. и др., Ретроспективный анализ базы данных претензий. Офтальмологическая эпидемиология. 2016; 23(2):71-9; Райес Н. и др., Британский журнал Офтальмология. 2016 Август; 100 (8):1058-61; Вандербик Б.Л. и др., журнал Американской медицинской ассоциации Офтальмология. 2015 Октябрь; 133 (10):1159-64). Однако интравитреальная инъекция требует повторного введения препарата через определенные промежутки времени, а не однократной инъекции, поскольку эффективность препарата непродолжительна. При увеличении частоты введения препарата внутриглазную инъекцию повторяют, поэтому в глазное яблоко могут попасть бактерии по ходу прокола инъекционной иглы, что повышает риск глазной инфекции. В результате анализа бактерий, вызывающих внутриглазные инфекции из-за глазной инъекции, стало известно, что большинство из них представляют собой Золотистый стафилококк, обитающий на поверхности глазного яблока, а также, что бактерии проникают через прокол, образованный во время и после глазной инъекции, вызывая, таким образом, внутриглазную инфекцию.
Хотя внутриглазная инфекция является самым страшным осложнением в офтальмологии, которое может привести к слепоте, существующие меры предотвращения такого инфекционного эндофтальмита предусматривают лишь использование стерильной среды, раствора повидон-иода и стерильного катетера. Это значит, что существует острая необходимость в способе, позволяющем гарантированно препятствовать возникновению инфекционного эндофтальмита, сопровождающего выполнение глазных инъекций.
Сдерживать кровотечение, возникающее при инъекции, способна гемостатическая игла по корейскому патенту №10-1576503, выданному авторам настоящего изобретения, которая покрыта сшитым хитозаном, функционализированным катехоловой группой и окисленным катехолом. Однако применение этой иглы в отношении ткани глаза характеризуется сильным прилипанием к ткани и высоким трением о ткань, из-за чего пациент будет испытывать ощущение жесткости, а глазное яблоко во время инъекции будет подвергаться давлению. Кроме того, при многократном введении лекарства в белую часть глазного яблока во время клинического применения, как это показано на фиг. 1, хитозан с введенной в него катехоловой группой остается в белой области, а место инъекции приобретает характерный цвет из-за изменения цвета полимера в результате окисления стечением времени, что нежелательно.
Соответственно, авторы настоящего изобретения приложили большие усилия для решения вышеуказанных проблем и установили, что если поверхность инъекционной иглы покрыть биосовместимым полимером, таким как желатин, коллаген, гиалуроновая кислота или т.п., то вытекание лекарства можно предотвратить за счет немедленного закрытия отверстия, которое неизбежно образуется в результате извлечения инъекционной иглы из глазного яблока по завершении глазной инъекции, и можно избежать внутриглазной инфекции путем недопущения проникновения бактерий. Указанные обстоятельства нашли свое отражение в настоящем изобретении.
Сущность изобретения
Цель изобретения заключается в создании самогерметизирующей инъекционной иглы для предотвращения образования фистулы на глазном яблоке после инъекции, что исключает возможность вытекания внутриглазной жидкости, вытекания лекарства и проникновения бактерий. Кроме того, цель изобретения заключается в создании способа подготовки такой иглы.
Для достижения вышеуказанной цели изобретение предлагает инъекционную иглу для предотвращения образования фистулы на глазном яблоке, причем поверхность этой иглы покрыта по меньшей мере одним биосовместимым полимером, выбранным из группы, состоящей из гиалуроновой кислоты и коллагена.
Кроме того, настоящее изобретение предлагает способ подготовки инъекционной иглы для предотвращения образования фистулы на глазном яблоке, содержащий этапы, на которых (а) подвергают инъекционную иглу кислородно-плазменной обработке и (б) покрывают инъекционную иглу раствором по меньшей мере одного биосовместимого полимера, выбранного из группы, состоящей из гиалуроновой кислоты и коллагена.
Краткое описание чертежей
Фиг. 1 изображает фотографию, на которой показана предложенная инъекционная игла, покрытая хитозаном с введенной в него катехоловой группой и применяемая в отношении ткани глаза.
Фиг. 2 изображает фотографию, на которой сравниваются возможность обеспечения герметизации предложенной самогерметизирующей инъекционной иглой, покрытой гиалуроновой кислотой (в зависимости от значения молекулярной массы гиалуроновой кислоты), и возможность обеспечения герметизации обычной инъекционной иглой;
Фиг. 3 изображает предложенную инъекционную иглу 30G, покрытую гиалуроновой кислотой в два этапа;
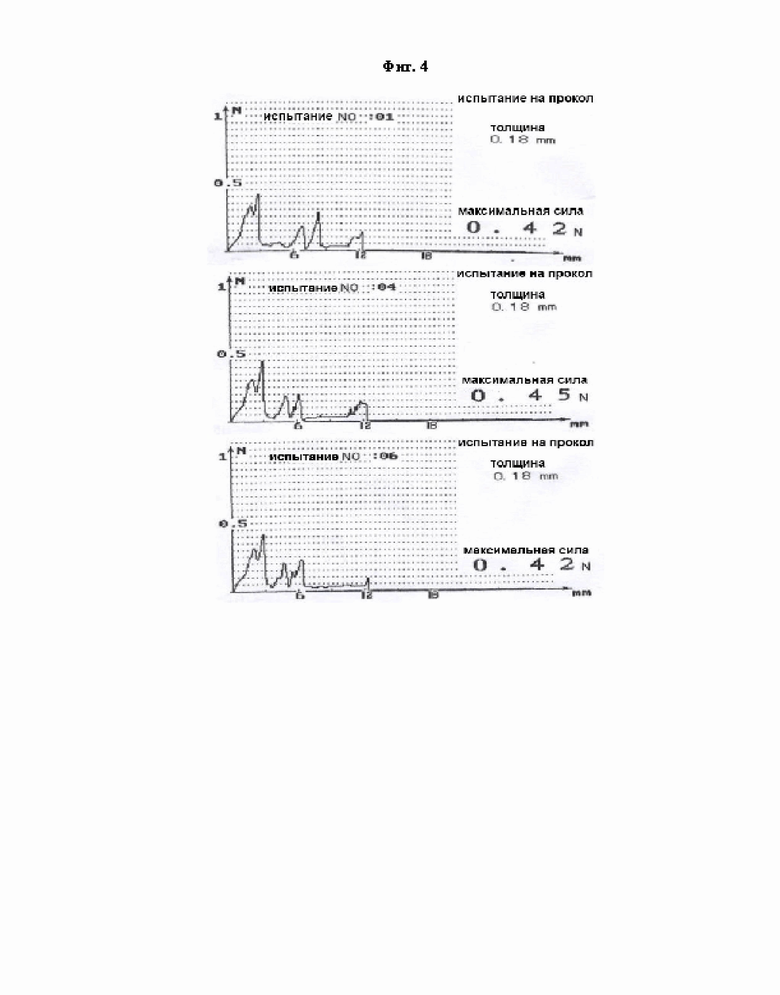
Фиг. 4 изображает графические результаты анализа предложенной самогерметизирующей инъекционной иглы, покрытой гиалуроновой кислотой, проведенного с использованием измерителя силы проникновения иглы;
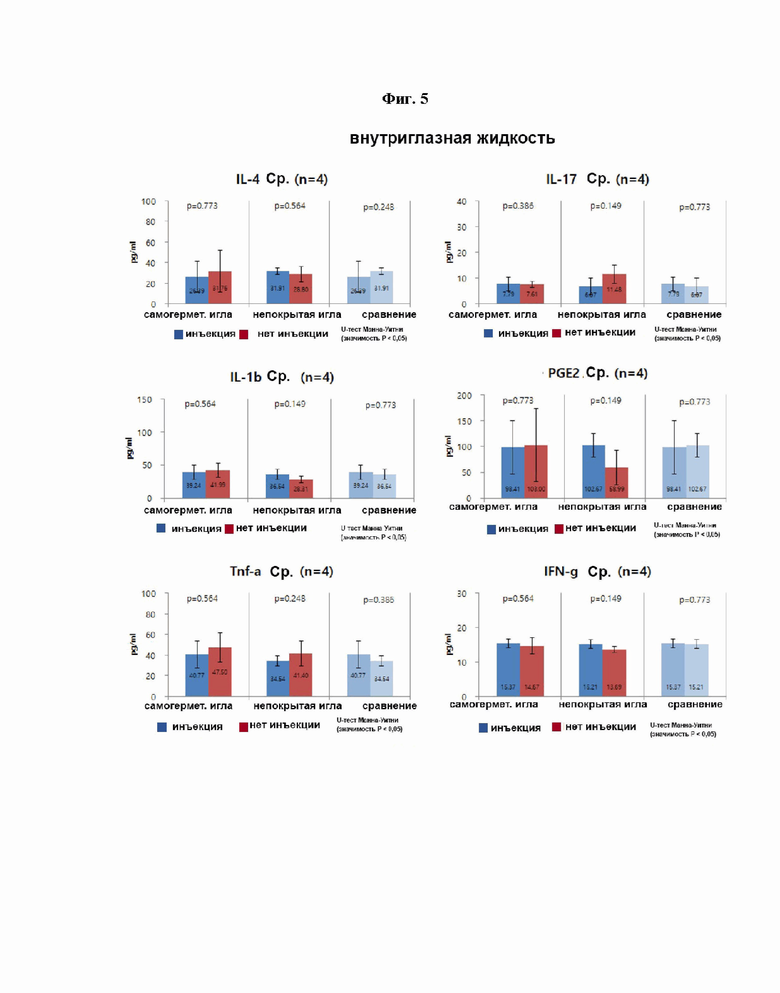
Фиг. 5 изображает графические результаты, подтверждающие значения концентрации шести цитокинов во внутриглазной жидкости глазного яблока кролика, введенных посредством предложенной самогерметизирующей инъекционной иглы, покрытой гиалуроновой кислотой.
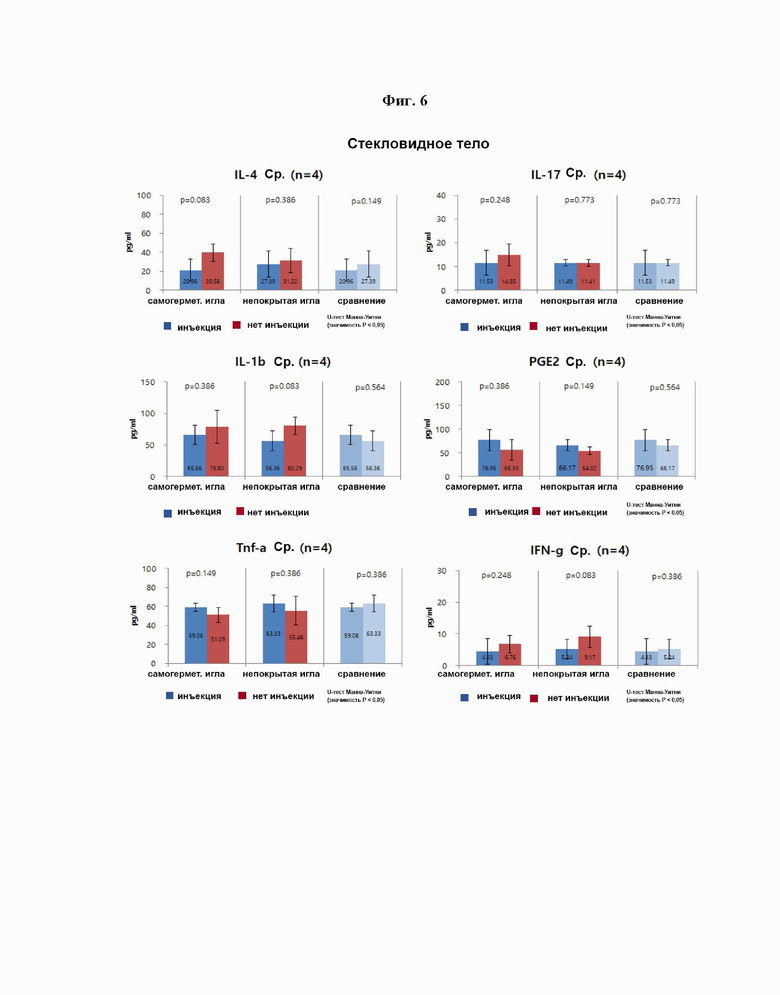
И фиг. 6 изображает графические результаты, подтверждающие значения концентрации шести цитокинов в жидкости стекловидного тела глазного яблока кролика, введенных посредством предложенной самогерметизирующей инъекционной иглы, покрытой гиалуроновой кислотой.
Осуществление изобретения
Если не указано иное, все технические и научные термины, используемые в данной заявке, имеют те же значения, которые обычно понимаются специалистами в области, к которой относится настоящее изобретение. В целом, используемая в заявке терминология хорошо известна в данной области и является типичной.
В настоящем изобретении подтверждено, что в случае изготовления инъекционной иглы путем покрытия ее поверхности гиалуроновой кислотой, она способна немедленно закрыть отверстие, которое неизбежно образуется при извлечении иглы из глазного яблока по завершению глазной инъекции, тем самым предотвращая вытекание внутриглазной жидкости, внеглазное выделение лекарства и проникновение бактерий, в конечном итоге предотвращая внутриглазную инфекцию.
Соответственно, один из аспектов изобретения относится к инъекционной игле для предотвращения образования фистулы на глазном яблоке, причем поверхность инъекционной иглы покрыта по меньшей мере одним биосовместимым полимером, выбранным из группы, состоящей из гиалуроновой кислоты и коллагена.
Другой аспект изобретения относится к способу подготовки инъекционной иглы для предотвращения образования фистулы на глазном яблоке, включающему этапы, на которых: (а) подвергают инъекционную иглу плазменной обработке и (б) покрывают инъекционную иглу раствором по меньшей мере одного биосовместимого полимера, выбранного из группы, состоящей из гиалуроновой кислоты и коллагена.
Далее дается подробное описание предложенной инъекционной иглы для предотвращения образования фистулы на глазном яблоке, а также способа ее подготовки.
Предложенная инъекционная игла для предотвращения образования фистулы на глазном яблоке характеризуется тем, что ее поверхность покрыта по меньшей мере одним биосовместимым полимером, выбранным из группы, состоящей из гиалуроновой кислоты и коллагена.
В соответствии с настоящим изобретением, биосовместимым полимером, нанесенным на инъекционную иглу для предотвращения образования фистулы на глазном яблоке, может быть анионный полимер, катионный полимер, нейтральный полимер или синтетический полимер. В предпочтительном случае это анионный полимер, такой как гиалуроновая кислота, альгинат, карбоксиметилцеллюлоза и т.д., катионный полимер, такой как хитозан и т.д., нейтральный полимер, такой как желатин, коллаген, декстран и т.д., или синтетический полимер, такой как полиэтиленгликоль и т.д. В частности, биосовместимым полимером предпочтительно является гиалуроновая кислота, коллаген или смесь гиалуроновой кислоты и коллагена.
Предложенная офтальмологическая инъекционная игла, покрытая гиалуроновой кислотой, обладает хорошей биосовместимостью с тканью глаза и обеспечивает герметизирующий эффект, позволяющий предотвращать не только вытекание лекарства, но и внутриглазное воспаление из-за попадания в инъекционный прокол бактерий, которые могут находиться на веках. Другое преимущество заключается в том, что от ее использования нет ощущения жесткости по сравнению с обычным шприцем, поскольку сила трения с тканью во время инъекции уменьшается.
В настоящем изобретении молекулярная масса гиалуроновой кислоты может составлять от 20 до 1000 кДа, предпочтительно от 66 до 850 кДа и более предпочтительно от 151 до 749 кДа.
Если молекулярная масса гиалуроновой кислоты составляет менее 20 кДа, то степень поглощения воды низкая из-за ее низкой молекулярной массы, поэтому степень расширения низкая, а также она легко всасывается в ткань из-за слабых физических свойств, что делает невозможной закупорку фистулы в достаточной степени. С другой стороны, если она превышает 1000 кДа, то из-за высокой молекулярной массы могут возникнуть жесткие физические свойства, так что при использовании могут возникать ощущения жесткости во время инъекции; или полимерная пленка, нанесенная на инъекционную иглу, может не фиксироваться на ткани, а отслаиваться и выдавливаться из фистулы, образовавшейся после инъекции, что делает невозможной закупорку фистулы.
В настоящем изобретении количество наносимой гиалуроновой кислоты может составлять от 12,6 до 276 мкг, предпочтительно от 12,6 до 138 мкг.
Если количество гиалуроновой кислоты составляет менее 12,6 мкг, то количество полимера невелико и его набухание из-за влагосодержания ткани будет незначительным, поэтому фистула не может быть в достаточной степени закупорена из-за низких физических свойств. С другой стороны, если оно превышает 276 мкг, то полимерная пленка может стать толстой, поэтому при использовании могут возникать ощущения жесткости, а глазное яблоко может быть сильно сдавлено во время инъекции.
В настоящем изобретении толщина покрытия инъекционной иглы может составлять от 0,1 до 40 мкм, и предпочтительно, толщина покрытия передней части иглы, которая первой касается глазного яблока, составляет от 0,1 до 10 мкм, а толщина покрытия ее задней части составляет от 20 до 40 мкм. В данном случае, если толщина покрытия превышает 40 мкм, то полимерная пленка может стать толстой, и могут возникать ощущения жесткости при использовании, а глазное яблоко может быть сильно сдавлено во время инъекции.
В настоящем изобретении глазное яблоко может представлять собой глазное яблоко пациента, страдающего офтальмологическим заболеванием, выбранным из группы, состоящей из диабетической ретинопатии, макулярной дегенерации, увеита, ретинопатии недоношенных, отторжения роговичного трансплантата, неоваскулярной глаукомы и пролиферативной ретинопатии и предпочтительно диабетической ретинопатии, макулярной дегенерации или увеита. Объектом лечения может быть любое офтальмологическое заболевание, если оно поддается лечению с помощью глазных инъекций.
Предложенный способ подготовки инъекционной иглы для предотвращения образования фистулы на глазном яблоке может включать этапы, на которых (а) подвергают инъекционную иглу плазменной обработке и (б) покрывают инъекционную иглу раствором по меньшей мере одного биосовместимого полимера, выбранного из группы, состоящей из гиалуроновой кислоты и коллагена.
В соответствии с настоящим изобретением, покрытие на этапе (b) можно наносить при температуре от 15 до 25°С в течение времени от 0,5 до 18 часов.
В соответствии с настоящим изобретением, кислородно-плазменную обработку можно проводить при температуре от 15 до 25°С от 5 минут до 20 минут, предпочтительно от 8 минут до 12 минут, и наиболее предпочтительно 10 минут.
В соответствии с настоящим изобретением, молекулярная масса гиалуроновой кислоты может составлять от 20 до 1000 кДа, а концентрация раствора гиалуроновой кислоты может составлять от 0,1 до 2,0% масс.
Настоящее изобретение также предусматривает способ немедленного закрытия отверстия, образовавшегося после операции, за счет применения самогерметизирующей инъекционной иглы для предотвращения образования фистулы на глазном яблоке к отверстию, оставшемуся после извлечения инструмента в случае операции, проводимой путем образования отверстия в глазном яблоке и введения инструмента в глазное яблоко, как при первичной витрэктомии.
Далее приведены примеры, способствующие пониманию настоящего изобретения. Эти примеры приведены только для иллюстрации изобретения и не должны рассматриваться как ограничение объема его правовой охраны, что очевидно специалистам в данной области техники.
Пример 1: Выбор полимера, подходящего для ткани глаза
Были изготовлены офтальмологические шприцы, соответственно покрытые гиалуроновой кислотой (ГК), альгинатом,
карбоксиметилцеллюлозой (КМЦ), хитозаном, желатином, коллагеном, декстраном и хитозаном с введенной в него катехоловой группой в качестве полимера.
Хитозан с введенной в него катехоловой группой представляет собой полимер, раскрытый в более раннем патенте (Корейский патент №10-1576503, название изобретения: Гемостатическая игла, покрытая сшитым хитозаном, который функционализирован катехоловой группой и окисленным катехолом).
Способность к герметизации и ощущения от использования в ткани глаза свиней сравнивались и подтверждались с помощью офтальмологических шприцов, покрытых различными биосовместимыми полимерами, причем было проведено пять независимых испытаний.
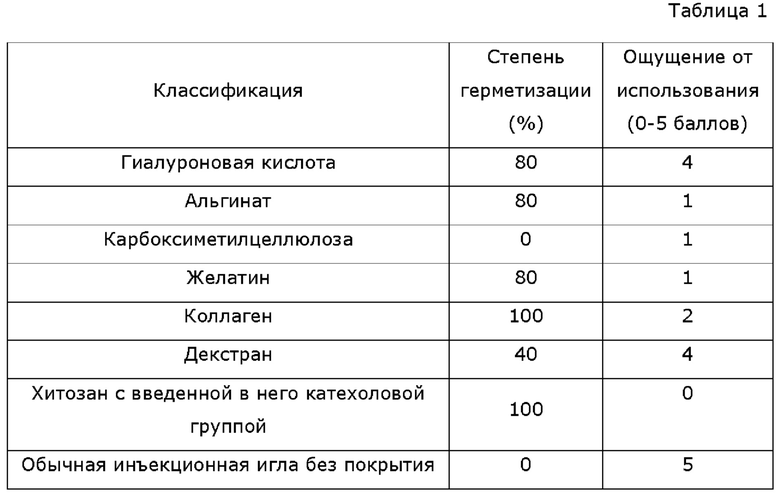
В нижеприведенной таблице 1 представлены результаты сравнения способности к герметизации и ощущений от использования офтальмологических шприцов, покрытых различными биосовместимыми полимерами. Установлено, что офтальмологический шприц, покрытый гиалуроновой кислотой, характеризуется превосходными способностью к герметизации и ощущением от использования в отличие от применения других биосовместимых полимеров. В данном случае способность к герметизации определялась на основе вытекания раствора после инъекции в глазное яблоко свиньи, а ощущения от использования оценивались по ощущениям, испытываемым пользователем, когда полимерное покрытие инъекционной иглы прокалывает глазное яблоко во время глазной инъекции, и по явлению сдавливания глазного яблока. Высокая оценка присваивалась, когда ощущения от использования были хорошими.
Хитозан с введенной в него катехоловой группой способен сам по себе сдерживать кровотечение во время инъекции, но когда он использовался для ткани глаза, пользователь испытывал ощущение жесткости из-за его сильного прилипания к ткани и высокого трения от ткань, и в момент инъекции наблюдалось сдавливание глазного яблока. Кроме того, при многократном введении препарата в белую часть глазного яблока во время клинического применения, существует вероятность обесцвечивания места инъекции в результате окисления с течением времени, поскольку хитозан с введенной в него катехоловой группой остается в белой области, в которой проводится инъекция, как это показано на фиг. 1.
Однако офтальмологический шприц, покрытый гиалуроновой кислотой, обладает хорошей биосовместимостью с тканью глаза и демонстрирует герметизирующий эффект, сдерживающий не только вытекание лекарства, но и внутриглазное воспаление из-за попадания в инъекционный прокол бактерий, которые могут находиться на веках. Таким образом, гиалуроновая кислота и коллаген были выбраны в качестве полимеров, подходящих для глазных инъекций, поскольку не возникали ощущения жесткости от их использования по сравнению с обычным шприцем из-за уменьшения силы трения с тканью в момент инъекции.
Пример 2: Изготовление самогерметизирующей инъекционной иглы
Для изготовления самогерметизирующей инъекционной иглы, в 1 мл дистиллированной воды растворили 15 мг гиалуроновой кислоты (НА, от англ. hyaluronic acid) с молекулярной массой от 10 до 1190 кДа.
Обычную инъекционную иглу (30G) подвергли кислородно-плазменной обработке в течение 10 минут; нанесли на инъекционную иглу раствор гиалуроновой кислоты с молекулярной массой от 10 до 1190 кДа; и покрывали им инъекционную иглу при вращении при комнатной температуре в течение 1 часа. Вышеописанную процедуру повторили дважды с получением самогерметизирующей инъекционной иглы.
Экспериментальный пример 1: Сравнение герметизирующих свойств в ткани глаза свиньи в зависимости от молекулярной массы гиалуроновой кислоты
В этом экспериментальном примере предметом наблюдения было вытекание раствора красителя (после того как раствор красителя был введен в ткань глаза свиньи, а затем инъекционная игла была извлечена из нее), а цель заключалась в сравнении и оценке герметизирующего эффекта самогерметизирующих инъекционных игл (30G), покрытых гиалуроновой кислотой с различными молекулярными массами, как в примере 2.
На фиг. 2 и в нижеприведенной таблице 2 показаны результаты сравнения способности к герметизации в зависимости от молекулярной массы гиалуроновой кислоты. Обычная инъекционная игла (30G) не обладала способностью к герметизации из-за вытекания раствора красителя через инъекционный прокол, тогда как самогерметизирующая инъекционная игла, покрытая гиалуроновой кислотой с молекулярной массой 176-350 кДа, и самогерметизирующая инъекционная игла, покрытая гиалуроновой кислотой с молекулярной массой 601-850 кДа, продемонстрировали наилучший герметизирующий эффект в ткани глаза.

Экспериментальный пример 2: Контроль и проверка толщины покрытия из гиалуроновой кислоты на инъекционной игле
В этом экспериментальном примере инъекционная игла изготовлена путем регулирования толщины пленки гиалуроновой кислоты на ней таким образом, при котором передняя часть и задняя часть инъекционной иглы покрыты гиалуроновой кислотой различной толщины с молекулярной массой 601-850 кДа, которая имела наилучший герметизирующий эффект в ткани глаза в экспериментальном примере 1, чтобы проявить герметизирующий эффект и одновременно обеспечить возможность инъекции без жесткости за счет уменьшения трения с тканью во время использования.
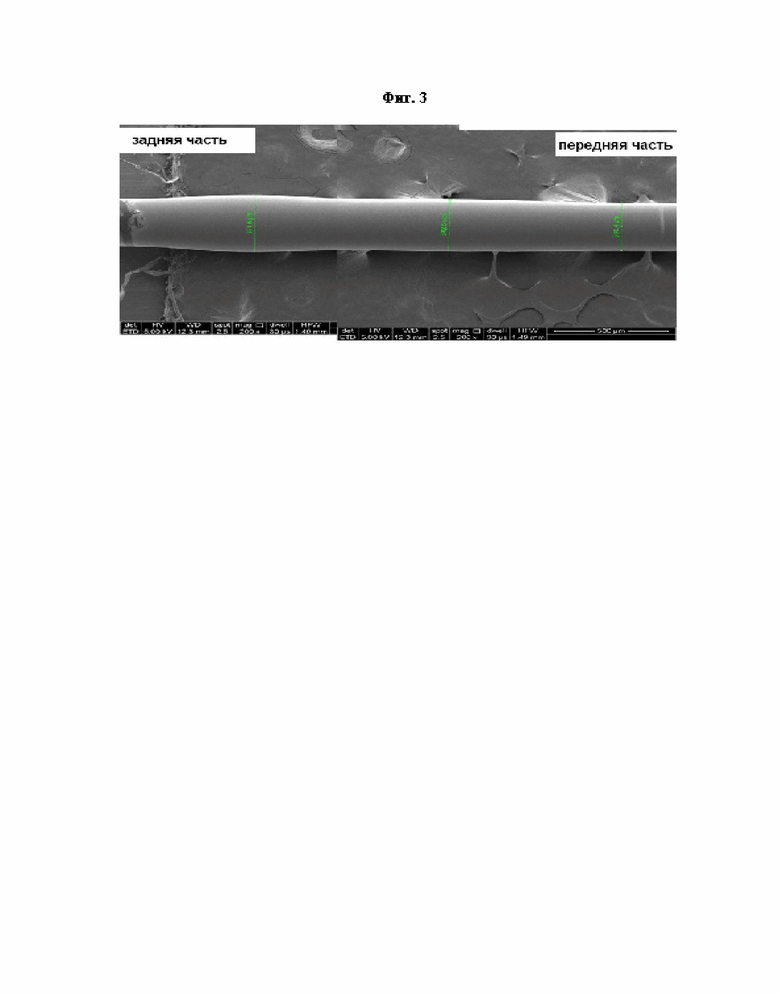
Увеличенное изображение инъекционной иглы, передняя часть и задняя часть которой покрыты гиалуроновой кислотой различной толщины, получали посредством сканирующего электронного микроскопа (СЭМ), с помощью которого анализировали форму пленки на инъекционной игле. На фиг. 3 показано изображение инъекционной иглы 30G, покрытой гиалуроновой кислотой, у которой толщина передней части, покрытой гиалуроновой кислотой, составляет около 310,4 мкм, а толщина задней части - 371,6 мкм.
Инъекционная игла 30G имела следующие характеристики.

Было подтверждено, что передняя часть инъекционной иглы, используемой для инъекций, покрыта тонким слоем для уменьшения трения с тканью, а ее задняя часть покрыта более толстым слоем, чем передняя часть, для придания герметизирующих свойств.
Экспериментальный пример 2-1: Проверка силы проникновения самогерметизирующей инъекционной иглы
В этом экспериментальном примере, чтобы оценить способность пленки из гиалуроновой кислоты на изготовленной самогерметизирующей инъекционной игле (30G) проникать в ткань при введении в биоткань, был проведен анализ с использованием измерителя силы проникновения иглы. Было проведено три независимых испытания.
На фиг. 4 показаны результаты анализа с использованием измерителя силы проникновения иглы. В момент проникновения иглы в искусственную ткань, была измерена наибольшая сила, равная 0,42-0,45 Н, а сила проникновения в месте нанесения пленки из гиалуроновой кислоты составила 0,20-0,30 Н, что меньше, чем указанная наибольшая сила.
Экспериментальный пример 2-2: Сравнительная оценка герметизирующих свойств и ощущений от использования в ткани глаза свиньи
В этом экспериментальном примере для сравнения и оценки герметизирующих свойств и ощущений от использования инъекционной иглы, передняя часть и задняя часть которой покрыты гиалуроновой кислотой разной толщины, и инъекционной иглы, передняя часть и задняя часть которой покрыты гиалуроновой кислотой одинаковой толщины, при введении раствора красителя в ткань глаза свиньи, а затем извлечении инъекционной иглы из нее, наблюдали, вытекает ли раствор красителя, и в то же время сравнивали и оценивали ощущения, испытываемые пользователем, когда покрытие гиалуроновой кислоты прокалывает ткань глаза во время инъекции, а также явления сдавливания глазного яблока.
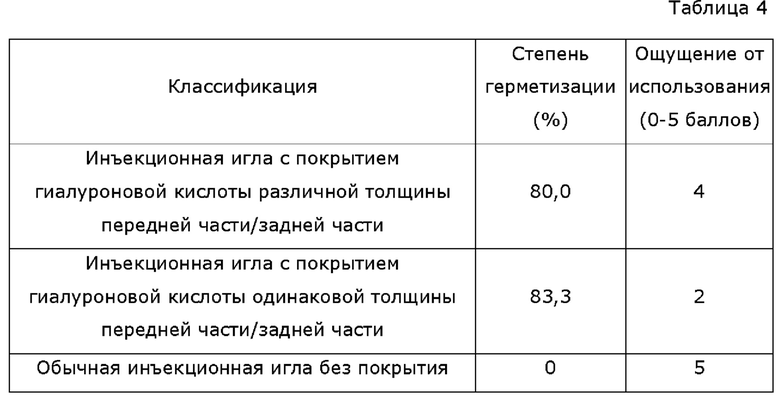
В нижеприведенной таблице 4 показаны результаты сравнения герметизирующих свойств и ощущений от использования инъекционной иглы в зависимости от толщины покрытия ее передней части и задней части. По сравнению с инъекционной иглой, передняя часть и задняя часть которой покрыты гиалуроновой кислотой с одинаковой толщиной, было подтверждено, что инъекционная игла, передняя часть и задняя часть которой покрыты гиалуроновой кислотой с разной толщиной, сохраняет герметизирующий эффект и демонстрирует улучшенные ощущения от использования.
Экспериментальный пример 2-3: Проверка герметизирующих свойств в модели глазной инъекции кролику
В данном экспериментальном примере герметизирующие свойства сравнивали и оценивали путем применения изготовленной самогерметизирующей инъекционной иглы (30G) и обычной инъекционной иглы (30G) к модели глазной инъекции кролику. В качестве подопытного животного использовали новозеландского белого кролика. Группы испытуемых были разделены на "контрольную группу", к которой применяли обычную инъекционную иглу, и "экспериментальную группу", к которой применяли самогерметизирующую инъекционную иглу, изготовленную как в примере 2. Было проведено три независимых испытания.
После того как кролик был полностью анестезирован, в глазное яблоко кролика вводили раствор красителя с помощью обычной инъекционной иглы или самогерметизирующей инъекционной иглы, а затем визуально наблюдали за вытеканием раствора красителя через инъекционный прокол.
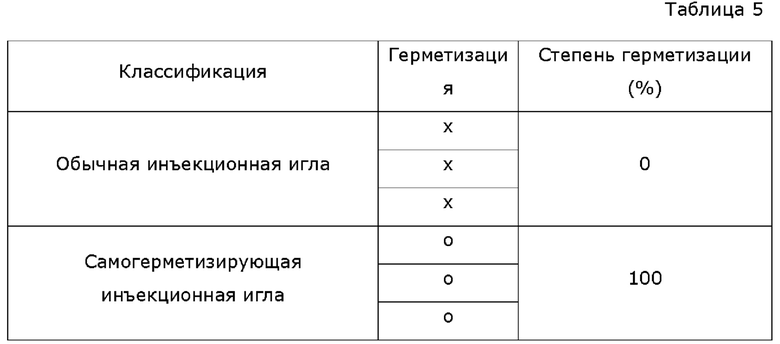
В нижеприведенной таблице 5 показаны результаты визуального наблюдения за вытеканием введенного раствора красителя через инъекционный прокол после введения раствора красителя с помощью обычной инъекционной иглы или самогерметизирующей инъекционной иглы. Было подтверждено, что раствор красителя вытекал через инъекционный прокол при использовании обычной инъекционной иглы, но не вытекал при использовании самогерметизирующей инъекционной иглы.
Экспериментальный пример 2-4: Выявление воспалительных цитокинов во внутриглазной жидкости и стекловидном теле глазного яблока после проведения глазной инъекции кролику
Согласно данному примеру, был проведен эксперимент, направленный на то, чтобы оценить, вызывает ли материал покрытия воспалительную реакцию после проведения глазной инъекции с использованием изготовленной самогерметизирующей инъекционной иглы (30G) по сравнению с обычной инъекционной иглой (30G).
Кролик был полностью анестезирован, а затем четыре раза подвергался глазной инъекции. Вышеописанная процедура была выполнена таким же образом на 3-й и 7-й дни. После завершения глазной инъекции на 7-й день глазное яблоко животного извлекли и хранили в замороженном виде, после чего внутриглазная жидкость и жидкость стекловидного тела в глазном яблоке были отделены друг от друга. Концентрация шести родственных с воспалением цитокинов, а именно IL-4, IL-17, IL-1b, PEG2, TNG-a и IFN-g, в каждой из внутриглазной жидкости и жидкости стекловидного тела была проанализирована с помощью иммуноферментного анализа (ИФА).
На фиг. 5 показаны результаты, подтверждающие значения концентрации шести цитокинов в внутриглазной жидкости, а на фиг. 6 показаны результаты, подтверждающие значения концентрации шести цитокинов в жидкости стекловидного тела. Здесь было подтверждено отсутствие разницы в воспалительной реакции при сравнении значений концентрации воспалительных цитокинов в момент глазной инъекции с использованием обычной инъекционной иглы и самогерметизирующей инъекционной иглы.
Промышленная применимость
Заявляемая инъекционная игла, покрытая гиалуроновой кислотой для предотвращения образования фистулы на глазном яблоке, выполнена таким образом, что поверхность инъекционной иглы для использования в глазном яблоке покрыта очень тонким слоем офтальмологического самогерметизирующего материала, позволяющим немедленно закрывать отверстие, которое неизбежно образуется при извлечении инъекционной иглы из глазного яблока по завершении глазной инъекции, тем самым предотвращая вытекание внутриглазной жидкости и проникновение бактерий, в конечном итоге предотвращая внутриглазную инфекцию.
Кроме того, можно предотвратить внеглазное выделение лекарств, которое часто происходит при введении дорогостоящих лекарств, таких как Lucentis или Eylea, используемых при различных глазных заболеваниях, таких как макулярная дегенерация и т.п. (стоимость одной инъекции Lucentis составляет, например, около 1 миллиона вон), что позволяет с высокой степенью точности ввести необходимую дозу, установленную фармацевтической компанией, и тем самым значительно снизить нагрузку на пациента.
Хотя выше раскрыты лишь некоторые варианты настоящего изобретения, специалистам в данной области техники должно быть очевидно, что описание призвано иллюстрировать только предпочтительные варианты изобретения и его не следует толковать как ограничение объема правовой охраны изобретения. Объем правовой охраны настоящего изобретения определяется признаками прилагаемой формулы и их эквивалентами.
| название | год | авторы | номер документа |
|---|---|---|---|
| СНИЖЕНИЕ ВНУТРИГЛАЗНОГО ДАВЛЕНИЯ ПРИ ПОМОЩИ ВНУТРИКАМЕРНЫХ ИМПЛАНТАТОВ БИМАТОПРОСТА | 2011 |
|
RU2586298C2 |
| ВНУТРИГЛАЗНЫЕ СИСТЕМЫ ДОСТАВКИ ЛЕКАРСТВЕННОГО СРЕДСТВА С ЗАМЕДЛЕННЫМ ВЫСВОБОЖДЕНИЕМ И СПОСОБЫ ЛЕЧЕНИЯ ГЛАЗНЫХ ЗАБОЛЕВАНИЙ | 2010 |
|
RU2532333C2 |
| ВНУТРИКАМЕРНЫЕ ИМПЛАНТАТЫ С ПРОЛОНГИРОВАННЫМ ВЫСВОБОЖДЕНИЕМ ТЕРАПЕВТИЧЕСКОГО АГЕНТА | 2011 |
|
RU2565445C2 |
| Способ лечения атрофической возрастной макулярной дегенерации | 2009 |
|
RU2668371C2 |
| СПОСОБ ЛЕЧЕНИЯ АТРОФИЧЕСКОЙ ВОЗРАСТНОЙ МАКУЛЯРНОЙ ДЕГЕНЕРАЦИИ | 2009 |
|
RU2521338C9 |
| СПОСОБ ЛЕЧЕНИЯ ПОВЫШЕННОГО ВНУТРИГЛАЗНОГО ДАВЛЕНИЯ С ПОМОЩЬЮ ВНУТРИГЛАЗНОЙ СИСТЕМЫ ДОСТАВКИ ЛЕКАРСТВЕННОГО СРЕДСТВА С ЗАМЕДЛЕННЫМ ВЫСВОБОЖДЕНИЕМ | 2014 |
|
RU2664686C2 |
| Способ комбинированного лечения неоваскулярной закрытоугольной глаукомы на фоне диабетического или посттромботического макулярного отека у пациентов с остаточным зрением | 2023 |
|
RU2815812C1 |
| СПОСОБ ВВЕДЕНИЯ ЛЕКАРСТВЕННОГО ПРЕПАРАТА В СУПРАХОРИОДАЛЬНОЕ ПРОСТРАНСТВО ГЛАЗНОГО ЯБЛОКА | 2024 |
|
RU2835865C1 |
| ДРЕНАЖ ДЛЯ ЛЕЧЕНИЯ ГЛАУКОМЫ | 2015 |
|
RU2610368C1 |
| СПОСОБ ЛЕЧЕНИЯ ДЕГЕНЕРАТИВНОЙ МИОПИИ | 2006 |
|
RU2308952C1 |

Группа изобретений относится к самогерметизирующим инъекционным иглам для предотвращения образования фистулы на глазном яблоке. Самогерметизирующая инъекционная игла для предотвращения образования фистулы на глазном яблоке поверхность которой покрыта по меньшей мере одним биосовместимым полимером, выбранным из группы, состоящей из гиалуроновой кислоты и коллагена. При этом передняя часть и задняя часть инъекционной иглы имеют разную толщину покрытия, и толщина покрытия задней части инъекционной иглы больше, чем толщина покрытия передней части инъекционной иглы. Также раскрывается способ подготовки самогерметизирующей инъекционной иглы. Группа изобретений обеспечивает исключение возможности вытекания внутриглазной жидкости, вытекания лекарства и проникновения бактерий. 2 н. и 14 з.п. ф-лы, 6 ил., 5 табл., 2 пр.
1. Самогерметизирующая инъекционная игла для предотвращения образования фистулы на глазном яблоке, причем поверхность инъекционной иглы покрыта по меньшей мере одним биосовместимым полимером, выбранным из группы, состоящей из гиалуроновой кислоты и коллагена, при этом передняя часть и задняя часть инъекционной иглы имеют разную толщину покрытия, и толщина покрытия задней части инъекционной иглы больше, чем толщина покрытия передней части инъекционной иглы.
2. Самогерметизирующая инъекционная игла по п. 1, в которой биосовместимым полимером является гиалуроновая кислота.
3. Самогерметизирующая инъекционная игла по п. 1, в которой биосовместимым полимером является коллаген.
4. Самогерметизирующая инъекционная игла по п. 1, в которой биосовместимым полимером является смесь гиалуроновой кислоты и коллагена.
5. Самогерметизирующая инъекционная игла по п. 2, в которой молекулярная масса гиалуроновой кислоты составляет от 20 до 1000 кДа.
6. Самогерметизирующая инъекционная игла по п. 1, в которой толщина покрытия инъекционной иглы составляет 0,1-40 мкм.
7. Самогерметизирующая инъекционная игла по п. 1, в которой толщина покрытия передней части инъекционной иглы составляет от 0,1 до 10 мкм, а толщина покрытия ее задней части составляет от 20 до 40 мкм.
8. Самогерметизирующая инъекционная игла по п. 1, в которой глазное яблоко представляет собой глазное яблоко субъекта, страдающего офтальмологическим заболеванием, выбранным из группы, состоящей из диабетической ретинопатии, макулярной дегенерации, увеита, ретинопатии недоношенных, отторжения роговичного трансплантата, неоваскулярной глаукомы и пролиферативной ретинопатии.
9. Способ подготовки самогерметизирующей инъекционной иглы по п. 1, включающий следующие этапы:
(a) подвергают инъекционную иглу плазменной обработке; и
(b) покрывают инъекционную иглу раствором по меньшей мере одного биосовместимого полимера, выбранного из группы, состоящей из гиалуроновой кислоты и коллагена, при этом передняя часть и задняя часть инъекционной иглы имеют разную толщину покрытия, и толщина покрытия задней части инъекционной иглы больше, чем толщина покрытия передней части инъекционной иглы.
10. Способ подготовки самогерметизирующей инъекционной иглы по п. 9, в котором биосовместимым полимером является гиалуроновая кислота.
11. Способ подготовки самогерметизирующей инъекционной иглы по п. 9, в котором биосовместимым полимером является коллаген.
12. Способ подготовки самогерметизирующей инъекционной иглы по п. 9, в котором биосовместимым полимером является смесь гиалуроновой кислоты и коллагена.
13. Способ подготовки самогерметизирующей инъекционной иглы по п. 9, в котором этап (b) покрытия осуществляют при температуре от 15 до 25°C в течение от 0,5 до 18 ч.
14. Способ подготовки самогерметизирующей инъекционной иглы по п. 9, в котором плазменную обработку осуществляют при температуре от 15 до 25°C в течение 5-20 мин.
15. Способ подготовки самогерметизирующей инъекционной иглы по п. 10, в котором молекулярная масса гиалуроновой кислоты составляет от 20 до 1000 кДа.
16. Способ подготовки самогерметизирующей инъекционной иглы по п. 10, в котором концентрация раствора гиалуроновой кислоты составляет от 0,1 до 2,0 масс.%.
| EP 2059272 A1, 20.05.2009 | |||
| WO 2018056737 A1, 29.03.2018 | |||
| KR 20100058778 A, 04.06.2010 | |||
| Способ дистанционной безотходно-самоконтрольной запайки стеклянных ампул | 1959 |
|
SU122577A1 |
| ГАЗО-ГИДРАВЛИЧЕСКИЙ ДВИГАТЕЛЬ | 1927 |
|
SU9092A1 |
Авторы
Даты
2023-09-12—Публикация
2020-11-18—Подача