1. ПРАВА ПРАВИТЕЛЬСТВА США
Настоящее изобретение было создано при государственной поддержке в рамках гранта DA018151, присужденного Национальными институтами здравоохранения. Правительство имеет определенные права на данное изобретение.
2. ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение в целом относится к применению налфурафина (NalF) для предотвращения и лечения демиелинизирующих заболеваний, в частности, рассеянного склероза.
3. УРОВЕНЬ ТЕХНИКИ
Миелиновая оболочка покрывает важные нервные волокна в центральной и периферической нервной системе млекопитающих, облегчая передачу нервных импульсов. Заболевания, поражающие миелин, прерывают такие процессы передачи нервных импульсов. На развивающуюся миелиновую оболочку могут негативно влиять врожденные метаболические нарушения, такие как фенилкетонурия, болезнь Тея-Сакса, болезнь Ниманна-Пика, синдром Гурлера и болезнь Краббе. Демиелинизация также может возникать у взрослых людей в результате травмы, метаболических нарушений, иммунной атаки, ишемии и воздействия токсичных веществ.
Демиелинизация нарушает передачу сигналов пораженным нервам, что приводит к недостаточности ощущения, движений, когнитивной недостаточности и недостаточности других функций. Демиелинизация центральной нервной системы связана с рассеянным склерозом (РС), болезнью Девика, острым рассеянным энцефаломиелитом, адренолейкодистрофией, лейкоэнцефалопатией и атрофией зрительного нерва Лебера. Демиелинизация симптома периферической нервной системы приводит к развитию таких заболеваний, как синдром Гийена-Барре, хроническая воспалительная демиелинизирующая полинейропатия, болезнь Шарко-Мари-Тута (CMT) и прогрессирующая воспалительная нейропатия.
Рассеянный склероз (РС) представляет собой наиболее известное демиелинизирующее заболевание, от которого страдают примерно 2,5 миллионов человек во всем мире. Больные страдают от целого ряда симптомов, в том числе от усталости, проблем со зрением, онемения, когнитивного нарушения, недержания мочи, нарушения равновесия и мышечной слабости, что в конечном итоге приводит к параличу. РС может протекать согласно четырем основным типам развития заболевания, каждое из которых может быть легким, средним или тяжелым:
1. Рецидивирующе-ремиттирующий РС (RRMS) - четко выраженные приступы (обострения), приводящие к ухудшению неврологической функции, за которыми следует частичная или полная ремиссия.
2. Первично-прогрессирующий РС (PPMS) - медленное ухудшение неврологической функции с переменной скоростью, без отчетливой ремиссии.
3. Вторично-прогрессирующий РС (SPMS) - после начального периода RRMS следует устойчивое ухудшение, с обострениями и ремиссиями или без них.
4. Прогрессивно-рецидивирующий РС (PRMS) - постоянное ухудшение неврологической функции с явными обострениями и частичной ремиссией или без нее.
Хотя не существует лечения от РС, многие одобренные FDA (Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США) препараты, такие как бета-интерферон и глатирамера ацетат, используют для снижения частоты рецидивов и уменьшения образования новых очагов поражения. К сожалению, современные методы лечения не очень успешны с точки зрения предотвращения инвалидизации, связанной с РС, и являются более успешными при лечении RRMS, чем других типов заболевания. Например, современные лекарственные препараты неспособны остановить или обратить вспять прогрессирование заболевания и инвалидизацию. Очевидно, что необходимы альтернативные способы лечения РС.
Соответственно, задача настоящего изобретения состоит в по меньшей мере некотором продвижении в сторону удовлетворения такой потребности в данной области техники, обеспечении продуктов и способов, подходящих для лечения инвалидизации, связанной с РС, и/или способных остановить и/или обратить вспять прогрессирование заболевания и инвалидизацию при РС, и/или в по меньшей мере предоставлении общественности подходящего выбора.
4. РАСКРЫТИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
Согласно одному из аспектов в настоящем изобретении предложена фармацевтическая композиция, содержащая налфурафин и фармацевтически приемлемые наполнители, для лечения демиелинизирующего заболевания у субъекта, нуждающегося в этом.
Согласно одному из аспектов в настоящем изобретении предложена фармацевтическая композиция, содержащая налфурафин и по меньшей мере один фармацевтически приемлемый наполнитель, для применения для лечения демиелинизирующего заболевания у субъекта, нуждающегося в этом.
Согласно другому аспекту в настоящем изобретении предложены стандартные лекарственные формы, содержащие от примерно 0,01 до примерно 5 мг налфурафина и по меньшей мере один фармацевтически приемлемый носитель или наполнитель. Согласно одному из вариантов реализации стандартная лекарственная форма содержит от 0,05 до примерно 2,0 мг налфурафина и по меньшей мере один фармацевтически приемлемый носитель или наполнитель. Согласно одному из вариантов реализации стандартная лекарственная форма содержит от примерно 0,15 до примерно 0,6 мг налфурафина и по меньшей мере один фармацевтически приемлемый носитель или наполнитель.
Согласно другому аспекту в настоящем изобретении предложен способ лечения демиелинизирующего заболевания у субъекта, нуждающегося в этом, включающий введение указанному субъекту терапевтически эффективного количества налфурафина.
Согласно другому аспекту в настоящем изобретении предложен способ лечения демиелинизирующего заболевания у субъекта, включающий выявление субъекта, который получит пользу от пониженного уровня демиелинизации, и введение указанному субъекту терапевтически эффективного количества агента, снижающего уровень демиелинизации у субъекта по сравнению с уровнем демиелинизации до введения указанного агента, при этом указанный агент содержит налфурафин.
Согласно другому аспекту в настоящем изобретении предложен способ лечения демиелинизирующего заболевания у субъекта, нуждающегося в этом, включающий введение указанному субъекту терапевтически эффективного количества агента, снижающего уровень демиелинизации у субъекта по сравнению с уровнем демиелинизации до введения указанного агента, при этом указанный агент содержит налфурафин.
Согласно другому аспекту в настоящем изобретении предложен способ увеличения ремиелинизации у субъекта, нуждающегося в этом, включающий введение указанному субъекту терапевтически эффективного количества налфурафина.
Согласно другому аспекту в настоящем изобретении предложен способ увеличения ремиелинизации у субъекта, включающий выявление субъекта, который получит пользу от повышенного уровня ремиелинизации, и введение указанному субъекту терапевтически эффективного количества агента, повышающего уровень ремиелинизации у субъекта по сравнению с уровнем ремиелинизации до введения указанного агента, при этом указанный агент содержит налфурафин.
Согласно другому аспекту в настоящем изобретении предложен способ увеличения ремиелинизации у субъекта, нуждающегося в этом, включающий введение указанному субъекту терапевтически эффективного количества агента, повышающего уровень ремиелинизации у субъекта по сравнению с уровнем ремиелинизации до введения указанного агента, при этом указанный агент содержит налфурафин.
В настоящем изобретении также предложено применение налфурафина при производстве лекарственного средства для лечения демиелинизирующего заболевания у субъекта, нуждающегося в этом.
В настоящем изобретении также предложено применение налфурафина при производстве лекарственного средства для увеличения ремиелинизации у субъекта, нуждающегося в этом.
Кроме того, в настоящем изобретении предложен налфурафин для применения для лечения демиелинизирующего заболевания.
В настоящем изобретении также предложен налфурафин для применения для увеличения ремиелинизации.
Согласно одному из вариантов реализации заболевание представляет собой демиелинизирующее миелинокластическое заболевание.
Согласно одному из вариантов реализации заболевание представляет собой демиелинизирующее лейкодистрофическое заболевание.
Согласно одному из вариантов реализации демиелинизирующее заболевание представляет собой демиелинизирующее заболевание центральной нервной системы. Согласно одному из вариантов реализации демиелинизирующее заболевание центральной нервной системы выбрано из группы, включающей РС (в том числе клинически изолированный синдром; CIS), неврит зрительного нерва, болезнь Девика, воспалительные демиелинизирующие заболевания, нейропатии центральной нервной системы, миелопатии, такие как сухотка спинного мозга, лейкоэнцефалопатии, лейкодистрофии или их комбинацию.
Согласно одному из вариантов реализации демиелинизирующее заболевание представляет собой РС.
Согласно другому варианту реализации демиелинизирующее заболевание представляет собой демиелинизирующее заболевание периферической нервной системы. Согласно одному из вариантов реализации демиелинизирующее заболевание периферической нервной системы выбрано из группы, включающей синдром Гийена-Барре и его хронический аналог, хроническую воспалительную демиелинизирующую полинейропатию, периферическую нейропатию с антимиелин-ассоциированным гликопротеином (MAG), болезнь Шарко-Мари-Тута (CMT), дефицит меди и прогрессирующую воспалительную нейропатию.
Согласно другому аспекту в настоящем изобретении предложен способ ослабления демиелинизации у субъекта, нуждающегося в этом, включающий введение указанному субъекту терапевтически эффективного количества налфурафина и, тем самым, снижение уровня демиелинизации у субъекта по сравнению с уровнем демиелинизации в отсутствие введения налфурафина.
В настоящем изобретении также предложено применение налфурафина при производстве лекарственного средства для ослабления демиелинизации у субъекта, нуждающегося в этом. Согласно одному из вариантов реализации субъект представляет собой человека с РС.
В настоящем изобретении также предложен налфурафин для применения для ослабления демиелинизации у субъекта, нуждающегося в этом.
Согласно другому аспекту в настоящем изобретении предложен способ лечения РС у субъекта, нуждающегося в этом, включающий введение указанному субъекту терапевтически эффективного количества налфурафина.
Согласно другому аспекту в настоящем изобретении предложен способ лечения РС у субъекта, нуждающегося в этом, включающий введение указанному субъекту терапевтически эффективного количества агента, снижающего уровень демиелинизации у субъекта по сравнению с уровнем до введения указанного агента и/или повышающего уровень ремиелинизации у субъекта по сравнению с уровнем до введения указанного агента, при этом указанный агент содержит налфурафин.
В настоящем изобретении также предложено применение налфурафина при производстве лекарственного средства для лечения РС у субъекта, нуждающегося в этом.
Кроме того, в настоящем изобретении предложен налфурафин для применения для лечения РС у субъекта, нуждающегося в этом.
Согласно одному из вариантов реализации субъект страдает от RRMS. Согласно одному из вариантов реализации субъект страдает от PPMS. Согласно одному из вариантов реализации субъект страдает от SPMS или у него диагностирован SPMS. Согласно одному из вариантов реализации субъект страдает от PRMS или у него диагностирован PRMS. Согласно одному из вариантов реализации субъект страдает от клинически изолированного синдрома (CIS) или у него диагностирован клинически изолированный синдром (CIS).
Согласно одному из вариантов реализации лечение РС приводит к одному или более клиническим результатам по сравнению с субъектами, не подвергавшимися лечению с помощью налфурафина, выбранным из группы, состоящей из:
(а) уменьшения прогрессирования заболевания РС;
(b) снижения тяжести заболевания РС;
(c) уменьшения демиелинизации нервных клеток;
(d) уменьшения частоты или тяжести приступов рецидивирующего РС;
(e) уменьшения клинических симптомов РС;
(е) заживления поврежденной нервной ткани (восстановления функции нервной ткани);
(g) увеличения ремиелинизации демиелинизированных нервов в центральной нервной системе (восстановления функции нервной ткани/нейропротекции);
(h) защиты поврежденной нервной ткани от дальнейшей активности заболевания (нейропротекции);
(i) стимулирования удлинения нейронов (нейрорегенерации) в центральной нервной системе;
(j) уменьшения проявления инвалидизации, вызванной РС;
(k) улучшения функции нервной системы; и
(k) повышенной скорости ремиссии.
Согласно другому варианту реализации лечение РС приводит к уменьшению одного или более клинических симптомов РС, включающих, но не ограниченных ими, потерю чувствительности или изменения ощущения, такие как звон в ушах, покалывание булавками и иглами или онемение, мышечную слабость или паралич различной степени тяжести, сильно выраженные рефлексы, мышечные спазмы или затруднение при движении; трудности с координацией и равновесием (атаксия); спастичность; проблемы с речью или глотанием, проблемы со зрением (нистагм, неврит зрительного нерва или двоение в глазах), усталость, острую или хроническую боль, нейропатическую боль, лицевую боль (невралгию тройничного нерва), проблемы с мочевым пузырем и кишечником, недержание мочи, снижение когнитивных способностей, депрессию, беспокойство и другие эмоциональные отклонения, сексуальную дисфункцию, феномен Утхоффа (ухудшение симптомов вследствие воздействия более высоких, чем обычно, температур) и симптом Лермитта (ощущение воздействия электрического тока, которое проходит по спине при сгибании шеи).
Согласно одному из аспектов в настоящем изобретении предложен способ ускорения ремиссии при РС у субъекта, нуждающегося в этом, включающий введение указанному субъекту терапевтически эффективного количества налфурафина.
Согласно одному из аспектов в настоящем изобретении предложен способ ускорения ремиссии при РС у субъекта, нуждающегося в этом, включающий введение терапевтически эффективного количества агента, снижающего уровень демиелинизации у субъекта по сравнению с уровнем демиелинизации до введения указанного агента, при этом указанный агент содержит налфурафин.
Согласно одному из аспектов в настоящем изобретении предложен способ ускорения ремиссии при РС у субъекта, нуждающегося в этом, включающий введение указанному субъекту терапевтически эффективного количества агента, повышающего уровень ремиелинизации у субъекта по сравнению с уровнем ремиелинизации до введения указанного агента, при этом указанный агент содержит налфурафин.
В настоящем изобретении также предложено применение налфурафина при производстве лекарственного средства для ускорения ремиссии при РС у субъекта, нуждающегося в этом.
В настоящем изобретении также предложен налфурафин для применения для ускорения ремиссии при РС у субъекта, нуждающегося в этом.
Согласно другому аспекту в настоящем изобретении предложен способ лечения демиелинизирующего заболевания у субъекта, включающий выявление субъекта, который получит пользу от пониженного уровня демиелинизации, и введение указанному субъекту терапевтически эффективного количества агента, снижающего уровень демиелинизации по сравнению с уровнем демиелинизации до введения указанного агента, при этом указанный агент содержит налфурафин.
Согласно другому аспекту в настоящем изобретении предложен способ увеличения ремиелинизации у субъекта, включающий выявление субъекта, который получит пользу от повышенного уровня ремиелинизации, и введение указанному субъекту терапевтически эффективного количества агента, повышающего уровень ремиелинизации по сравнению с уровнем ремиелинизации до введения указанного агента, при этом указанный агент содержит налфурафин.
В описанных выше способах настоящего изобретения:
Согласно одному из вариантов реализации терапевтически эффективное количество для субъекта эквивалентно дозе от примерно 0,003 до примерно 0,3 мг/кг/сутки при введении мышам.
Согласно одному из вариантов реализации субъект представляет собой человека. Согласно одному из вариантов реализации предложенный способ включает введение от примерно 0,01 до примерно 5 мкг налфурафина в сутки, от примерно 0,01 до примерно 4 мкг, от примерно 0,01 до примерно 3 мкг, от примерно 0,01 до примерно 2,5 мкг, от примерно 0,01 до примерно 2 мкг, от примерно 0,01 до примерно 1,5 мкг, от примерно 0,01 до примерно 1 мкг, от примерно 0,01 до примерно 0,75 мкг, от примерно 0,01 до примерно 0,5 мкг или примерно 0,25 мкг налфурафина в сутки.
Согласно некоторым вариантам реализации предложенный способ включает введение менее примерно 1 мкг налфурафина, предпочтительно менее 1 мкг налфурафина в сутки.
Согласно некоторым вариантам реализации предложенный способ включает длительную терапию.
Согласно некоторым вариантам реализации длительная терапия включает введение терапевтически эффективной дозы налфурафина субъекту, нуждающемуся в этом, в течение по меньшей мере 5 дней, по меньшей мере 6 дней или по меньшей мере 7 дней.
Согласно некоторым вариантам реализации длительная терапия включает введение терапевтически эффективной дозы налфурафина субъекту, нуждающемуся в этом, в течение по меньшей мере недели, по меньшей мере 2 недель, по меньшей мере 3 недель, по меньшей мере 4 недель, по меньшей мере 6 недель или по меньшей мере 8 недель.
Согласно некоторым вариантам реализации длительная терапия включает введение в течение по меньшей мере 5 дней, по меньшей мере 6 дней, по меньшей мере 7 дней, по меньшей мере 14 дней, по меньшей мере 21 дня, по меньшей мере 28 дней, по меньшей мере 35 дней, по меньшей мере 42 дней, по меньшей мере 45 дней, по меньшей мере 60 дней, по меньшей мере 120 дней, по меньшей мере 240 дней или по меньшей мере 360 дней.
Согласно некоторым вариантам реализации длительная терапия включает определенный интервал дозирования, составляющий по меньшей мере 1 день.
Другие аспекты настоящего изобретения могут стать понятными из следующего описания, которое приведено только в качестве примера и со ссылкой на прилагаемые фигуры.
В настоящем описании изобретения, в котором были даны ссылки на описания патентов, другие внешние документы или другие источники информации, такое цитирование в общем случае сделано с целью обеспечения контекста для обсуждения особенностей настоящего изобретения. Если специально не указано иное, ссылку на такие внешние документы не следует толковать как признание того, что указанные документы или указанные источники информации, в любой юрисдикции, являются предшествующим уровнем техники или составляют часть общих знаний в данной области техники. Однако все такие внешние документы и ссылки приведены в настоящем документе посредством ссылки в полном объеме или по меньшей мере в той степени, в которой они описаны в настоящем документе.
Подразумевают, что ссылка на диапазон чисел, приведенный в настоящем документе (например, от 1 до 10), также включает ссылку на все рациональные числа в таком диапазоне (например, 1, 1,1, 2, 3, 3,9, 4, 5, 6, 6,5, 7, 8, 9 и 10), а также любой диапазон рациональных чисел внутри данного диапазона (например, от 2 до 8, от 1,5 до 5,5 и от 3,1 до 4,7) и, следовательно, все поддиапазоны внутри всех диапазонов, явно описанных в настоящем документе, тем самым, тоже описаны явным образом. Выше приведены только примеры того, что конкретно подразумевается, при этом все возможные комбинации числовых значений между перечисленными наименьшим и наибольшим значениями следует рассматривать как явно указанные в настоящей заявке аналогичным образом.
Всякий раз, когда в настоящем описании указан диапазон, например диапазон температур, диапазон времени или диапазон состава, подразумевается, что все промежуточные диапазоны и поддиапазоны, а также все отдельные значения, включенные в приведенные диапазоны, включены в описание настоящего изобретения. В описании и формуле изобретения «и/или» означает дополнительно или альтернативно. Кроме того, любое применение термина в единственном числе также включает формы множественного числа.
5. КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
Далее настоящее изобретение будет описано только в качестве примера и со ссылкой на чертежи, на которых:
Фигура 1 представляет собой график, на котором показано прогрессирование заболевания у мышей с экспериментальным аутоиммунным энцефаломиелитом (ЭАЭ) на протяжении 45 дней, при этом в примере 1 такие мыши получали 0,01, 0,03, 0,1 или 0,3 мг/кг налфурафина в сутки с начала заболевания (день 17).
Фигура 2 представляет собой два графика, на которых показана полная инвалидизация мышей с ЭАЭ в течение (A) 45 дней и (B) 18 дней, при этом в примере 2 такие мыши получали 0,03, 0,1 или 0,3 мг/кг налфурафина в сутки с начала заболевания (день 17).
Фигура 3 представляет собой график, на котором показано % изменение массы мышей с ЭАЭ в примере 3 в течение 45 дней, при этом такие мыши получали 0,03, 0,1 или 0,3 мг/кг налфурафина в сутки с начала заболевания (день 17).
Фигура 4 представляет собой три графика, на которых показана инфильтрация иммунных клеток в головной мозг мышей с ЭАЭ в примере 4 через 45 дней, при этом такие мыши получали 0,03, 0,1 или 0,3 мг/кг налфурафина в сутки с начала заболевания (день 17).
Фигура 5 представляет собой график, на котором показано прогрессирование заболевания у мышей с ЭАЭ в примере 5 в течение 45 дней, при этом указанные мыши, у которых еще не развился ЭАЭ, получали 0,03, 0,1 или 0,3 мг/кг налфурафина в сутки с начала заболевания (день 17).
Фигура 6 представляет собой серию полученных с помощью просвечивающей электронной микроскопии (TEM) изображений срезов спинного мозга мышей с ЭАЭ в примере 6 через 45 дней, при этом такие мыши получали 0,03 мг/кг налфурафина в сутки с начала заболевания (день 17).
Фигура 7 представляет собой график, на котором показано увеличение массы в течение 65 дней у мышей в примере 7, получавших 0,3% купризона в течение 5 недель, при этом таких мышей лечили с применением 0,1 мг/кг налфурафина в сутки, начиная с 4 недели.
Фигура 8 представляет собой график, на котором показаны результаты оценки способности мышей удерживаться на вращающемся стержне в примере 8 через 9 недель, получавших купризон в течение 5 недель, при этом таких мышей лечили с применением 0,1 мг/кг налфурафина в сутки, начиная с 4 недели.
Фигура 9 представляет собой серию TEM изображений мозолистого тела мышей в примере 9 через 9 недель, получавших купризон в течение 5 недель, при этом таких мышей лечили с применением 0,1 мг/кг налфурафина в сутки, начиная с 4 недели.
На фигуре 10 показано, что налфурафин способствует функциональному восстановлению от паралича при терапевтическом введении (в начале заболевания) в модели РС на основе экспериментального аутоиммунного энцефаломиелита (ЭАЭ).
На фигуре 11 показано, что налфурафин не является эффективным при терапевтическом введении в течение короткого 4-дневного курса с момента начала заболевания в модели РС на основе ЭАЭ.
На фигуре 12 показано, что налфурафин не изменяет пик заболевания при терапевтическом введении в модели РС на основе ЭАЭ.
На фигуре 13 показано, что налфурафин способствует полному восстановлению от паралича, вызванного ЭАЭ, при терапевтическом введении.
На фигуре 14 показано, что налфурафин способствует полному восстановлению от паралича, вызванного ЭАЭ, при терапевтическом введении с ЕС50 для восстановления (%), составляющей <0,001 мг/кг.
На фигуре 15 показано, что налфурафин способствует устойчивому восстановлению от паралича, вызванного ЭАЭ, при терапевтическом введении.
На фигуре 16 показано, что налфурафин также способствует функциональному восстановлению самцов мышей от паралича при терапевтическом введении в модели РС на основе ЭАЭ.
На фигуре 17 показано, что налфурафин также способствует полному восстановлению самцов мышей при терапевтическом введении в модели РС на основе ЭАЭ.
На фигуре 18 показано, что налфурафин способствует устойчивому восстановлению самцов мышей от паралича, вызванного ЭАЭ, при терапевтическом введении.
На фигуре 19 показано, что налфурафин уменьшает инфильтрацию иммунных клеток в головной мозг при терапевтическом введении в модели РС на основе ЭАЭ (A), тогда как U 50488 не уменьшает (B).
На фигуре 20 показано улучшение миелинизаци у мышей, получавших налфурафин после начала паралича, в модели РС на основе ЭАЭ.
На фигуре 21 показано, что налфурафин не изменяет долю основных популяций лимфоцитов в селезенке во время хронической фазы ЭАЭ.
На фигуре 22 показано, что налфурафин не изменяет общее количество CD4 Т-клеток-хелперов в селезенке, но переключает CD4 Т-клетки от фенотипа эффекторных клеток к фенотипу клеток памяти, что указывает на разрешение иммунного ответа во время хронической фазы ЭАЭ.
На фигуре 23 показано, что налфурафин уменьшает проявление заболевания, но не может привести к полному восстановлению при блокировке опиоидного каппа-рецептора (KOR).
На фигуре 24 показано, что активация KOR необходима для полного восстановления от паралича, опосредованного налфурафином.
На фигуре 25 показано улучшение миелинизаци у мышей, получавших налфурафин после начала паралича, в модели РС на основе ЭАЭ.
На фигуре 26 показано, что лечение с помощью налфурафина уменьшает клеточную инфильтрацию в спинной мозг при терапевтическом введении в модели РС на основе ЭАЭ.
На фигуре 27 показано, что лечение с помощью налфурафина снижает уровень активированных астроцитов в спинном мозге при терапевтическом введении в модели РС на основе ЭАЭ.
На фигуре 28 показано, что лечение с помощью налфурафина усиливает восстановление от потери массы при терапевтическом введении в купризоновой модели РС.
На фигуре 29 показано, что лечение с помощью налфурафина усиливает ремиелинизацию головного мозга при введении после демиелинизации в купризоновой модели демиелинизирующего заболевания РС.
На фигуре 30 показано, что налфурафин является более эффективным при стимулировании функционального восстановления, чем клемастина фумарат, известный ремиелинизирующий препарат.
На фигуре 31 показано, что налфурафин способствует большему и более устойчивому восстановлению, чем клемастина фумарат, известный ремиелинизирующий препарат.
На фигуре 32 показано, что налфурафин способствует восстановлению болевого порога при введении после демиелинизации в купризоновой модели демиелинизирующего заболевания РС.
6. ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
6. 1 Налфурафин
Налфурафин представляет собой лекарственный препарат, обычно назначаемый для лечения уремического зуда у людей с хроническим заболеванием почек. Такой препарат представляет собой ненаркотический опиоид с активностью селективного агониста κ-опиоидных рецепторов (KOR). В ходе работы авторы изобретения обнаружили, что налфурафин является неожиданно эффективным средством лечения демиелинизирующих заболеваний.
Общее название «налфурафин» относится к соединению:
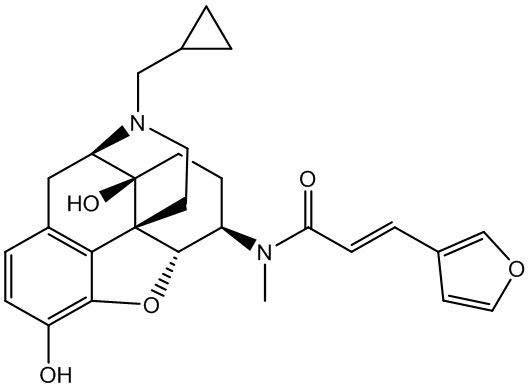
Названием налфурафина в номенклатуре IUPAC является (E)-N-[(4R,4aS,7R,7aR,12bS)-3-(циклопропилметил)-4a,9-дигидрокси-1,2,4,5,6,7,7a,13-октагидро-4,12-метанобензофуро[3,2-e]изохинолин-7-ил]-3-(фуран-3-ил)-N-метилпроп-2-енамид. Его номер в реестре Chemical Abstracts Service (CAS) соответствует 152657-84-6. Налфурафин HCl также можно назвать 17-циклопропилметил-3,14-бета-дигидрокси-4,5-альфа-эпокси-6бета-(N-метил-транс-3-(3-фурил)акриламидо)морфинан гидрохлоридом, TRK 820, AC-820 и MT-9938.
В настоящем документе термин «налфурафин» относится к соединению, определенному выше, а также к его фармацевтически приемлемым солям и сольватам.
Термин «фармацевтически приемлемые соли» относится к солям, полученным из фармацевтически приемлемых нетоксичных оснований или кислот, в том числе неорганических или органических оснований и неорганических или органических кислот. Соли, полученные из неорганических оснований, включают соли алюминия, аммония, кальция, меди, трехвалентного железа, двухвалентного железа, лития, магния, марганца, двухвалентный марганец, калий, натрий, цинк и тому подобное. Особенно предпочтительными являются соли аммония, кальция, магния, калия и натрия. Соли в твердой форме могут существовать в более чем одной кристаллической структуре, а также могут быть в форме гидратов. Соли, полученные из фармацевтически приемлемых органических нетоксичных оснований, включают соли первичных, вторичных и третичных аминов, замещенных аминов, в том числе встречающихся в природе замещенных аминов, циклических аминов и основных ионообменных смол, таких как аргинин, бетаин, кофеин, холин, N,N'-дибензилэтилендиамин, диэтиламин, 2-диэтиламиноэтанол, 2-диметиламиноэтанол, этаноламин, этилендиамин, N-этилморфолин, N-этилпиперидин, глюкамин, глюкозамин, гистидин, гидрабамин, изопропиламин, лизин, метилглюкамин, морфолин, пиперазин, пиперидин, полиаминовые смолы, прокаин, пурины, теобромин, триэтиламин, триметиламин, трипропиламин, трометамин и т.п. Когда налфурафин является основным, соли можно получить из фармацевтически приемлемых нетоксичных кислот, в том числе неорганических и органических кислот. Такие кислоты включают уксусную, бензолсульфоновую, бензойную, камфорсульфоновую, лимонную, этансульфоновую, фумаровую, глюконовую, глутаминовую, бромистоводородную, хлористоводородную, изетионовую, молочную, малеиновую, яблочную, миндальную, этансульфоновую, муциновую, азотную, памовую, пантотеновую, фосфорную, янтарную, серную, винную, п-толуолсульфоновую кислоту и т.п. Особенно предпочтительными являются лимонная, бромистоводородная, хлористоводородная, малеиновая, фосфорная, серная, фумаровая и винная кислоты.
Термин «сольват» относится к агрегату, который состоит из иона или молекулы растворенного вещества с одной или более молекулами растворителя. «Сольваты» включают гидраты, то есть агрегаты исследуемого соединения с водой.
Налфурафин можно приобрести у поставщиков малых молекул, таких как Med Chem Express, Монмут Джанкшен и Нью-Джерси, США; AdooQ BioScience, Ирвин, Калифорния, США.
6. 2. Фармацевтические композиции налфурафина
Эффективные способы лечения демиелинизирующих заболеваний, в том числе РС, отсутствуют, и, в частности, имеется мало эффективных агентов, действие которых направлено на снижение демиелинизации и/или увеличение ремиелинизации. Авторы изобретения неожиданно обнаружили, что фармацевтические композиции, содержащие налфурафин, можно применять для лечения демиелинизующих заболеваний, в том числе, но не ограничиваясь ими, РС, путем действия, направленного на увеличение ремиелинизации и/или снижение демиелинизации.
Соответственно, согласно одному из аспектов в настоящем изобретении предложена фармацевтическая композиция, содержащая налфурафин и фармацевтически приемлемые наполнители, для лечения демиелинизирующего заболевания у субъекта, нуждающегося в этом.
Согласно другому аспекту в настоящем изобретении предложена фармацевтическая композиция, содержащая налфурафин и по меньшей мере один фармацевтически приемлемый наполнитель, для применения для лечения демиелинизирующего заболевания у субъекта, нуждающегося в этом.
В настоящем документе термин «фармацевтическая композиция» включает продукт, содержащий один или более активных агентов и фармацевтически приемлемые наполнители, содержащие инертные ингредиенты, а также любой продукт, который получают, прямо или косвенно, в результате объединения, комплексообразования или агрегации любых двух или более ингредиентов, или в результате диссоциации одного или более ингредиентов, или в результате других типов реакций или взаимодействий одного или более ингредиентов. В общем случае, фармацевтические композиции получают путем объединения активного агента с жидким носителем, мелкоизмельченным твердым носителем или с обоими, а затем, при необходимости, путем придания продукту формы с получением требуемого состава. Указанные композиции получают в соответствии с общепринятыми способами смешивания, гранулирования или нанесения покрытия, соответственно, и имеют определенное процентное содержание (%) активного ингредиента и могут быть определены квалифицированным специалистом, исходя из уровня техники.
В настоящем документе термин «содержащий» означает «состоящий по меньшей мере частично из». В настоящем описании при интерпретации каждого утверждения, включающего термин «содержащий», могут также присутствовать признаки, отличные от признака или признаков, которым предшествует данный термин. Связанные термины, такие как «содержат» и «содержит», следует интерпретировать аналогичным образом.
В настоящем документе термин «состоящий по существу из» означает указанные материалы или стадии, а также такие материалы или стадии, которые существенно не влияют на основную и новую характеристику(и) заявленного изобретения.
В настоящем документе термин «состоящий из» означает указанные материалы или стадии заявленного изобретения, за исключением любого элемента, стадии или ингредиента, не указанного в пункте формулы изобретения.
Под «фармацевтически приемлемым наполнителем» или «фармацевтически приемлемым носителем» подразумевают, что наполнитель или носитель должен быть совместим с другими ингредиентами состава и не причинять вред субъекту, которому вводят такую композицию.
Описанные в настоящем документе фармацевтические композиции можно вводить местно, перорально или парентерально.
Например, фармацевтические композиции можно вводить перорально, в том числе сублингвально, в форме капсул, таблеток, эликсиров, растворов, суспензий или болюсов, приготовленных таким образом, чтобы они растворялись, например, в толстой или двенадцатиперстной кишке. Указанные составы могут содержать наполнители, такие как крахмал или лактоза, или ароматизаторы, консерванты или красители.
Фармацевтические композиции можно инъецировать парентерально, например, внутривенно, внутримышечно или подкожно. Для парентерального введения композиции могут быть приготовлены в виде стерильного водного раствора или суспензии, которая необязательно содержит другие вещества, такие как соль или глюкоза.
Композиции можно вводить местно в форме стерильных кремов, гелей, составов для поливания или точечного нанесения, суспензий, лосьонов, мазей, присыпок, повязок, содержащих лекарственный препарат, шампуней, воротников или трансдермальных пластырей. Например, описанные в настоящем документе композиции могут быть включены в крем, содержащий водную или масляную эмульсию полиэтиленгликолей или жидкого парафина; мазь, содержащую мягкую парафиновую основу в виде белого воска; гидрогель с производными целлюлозы или полиакрилата или другими подходящими модификаторами вязкости; сухой порошок; аэрозоль с пропеллентами в виде бутана, пропана, HFA (гидрофторалкана) или CFC (хлорфторуглерода); повязку, такую как сетчатый перевязочный материал, с марлевыми повязками, пропитанными белым мягким парафином или полиэтиленгликолем, или гидрогелевыми повязками, гидроколлоидными повязками или повязками в виде альгинатной пленки. Композиции также можно вводить внутриглазным способом в виде глазных капель с соответствующими буферными растворами, модификаторами вязкости (например, производными целлюлозы) и консервантами (например, хлоридом бензалкония).
Описанные в настоящем документе фармацевтические композиции также могут быть включены в трансдермальный пластырь, содержащий налфурафин. Подробную информацию о таких пластырях можно найти, например, в WO2015/025766, WO2015/025767, WO2016/208729, WO2017/094337 и WO2017/170933, подробное описание которых включено в настоящий документ посредством ссылки.
В случае перорального введения капсулы, болюсы или таблетки можно приготовить путем смешивания фармацевтических композиций, описанных в настоящем документе, с подходящим мелкоизмельченным разбавителем или носителем, дополнительно содержащим вещество для улучшения распадаемости таблеток и/или связующее вещество, такое как крахмал, лактоза, тальк или стеарат магния.
В случае парентерального введения составы для инъекций можно приготовить в форме стерильного раствора или эмульсии.
Описанные в настоящем документе композиции могут быть представлены в виде стандартной лекарственной формы и могут быть приготовлены любым из способов, хорошо известных в области фармацевтики. Термин «стандартная лекарственная форма» означает однократную дозу, в которой все активные и неактивные ингредиенты объединены в подходящей системе, так что пациент или человек, вводящий лекарственный препарат, может открыть один контейнер или упаковку с содержащейся в ней всей дозой и не должен смешивать вместе какие-либо компоненты из двух или более контейнеров или упаковок. Типичными примерами стандартных лекарственных форм являются таблетки или капсулы для перорального введения или трансдермальные пластыри, содержащие однократную дозировку. Приведенные примеры стандартных лекарственных форм никоим образом не предназначены для ограничения, а просто представляют собой типичные примеры стандартных лекарственных форм в области фармацевтики.
Согласно другому аспекту в настоящем изобретении предложены стандартные лекарственные формы, содержащие от примерно 0,01 до примерно 5 мг налфурафина и по меньшей мере один фармацевтически приемлемый носитель или наполнитель. Согласно одному из вариантов реализации стандартная лекарственная форма содержит от 0,05 до примерно 2,0 мг налфурафина и по меньшей мере один фармацевтически приемлемый носитель или наполнитель. Согласно одному из вариантов реализации стандартная лекарственная форма содержит от примерно 0,15 до примерно 0,6 мг налфурафина и по меньшей мере один фармацевтически приемлемый носитель или наполнитель.
Согласно одному из аспектов в настоящем изобретении предложена стандартная лекарственная форма, содержащая от примерно 0,1 до примерно 10 мкг налфурафина и по меньшей мере один фармацевтически приемлемый носитель или наполнитель. Согласно одному из вариантов реализации стандартная лекарственная форма содержит от примерно 0,5 до примерно 7,5 мкг налфурафина, от примерно 0,75 до примерно 5 мкг налфурафина, примерно от 1 до 4 мкг налфурафина, примерно от 2 до 3 мкг налфурафина, примерно 2 мкг налфурафина, примерно 3 мкг налфурафина, примерно 4 мкг налфурафина или примерно 5 мкг налфурафина.
Согласно одному из вариантов реализации стандартная лекарственная форма содержит менее примерно 2 мкг, 1,5 мкг, 1,0 мкг, 0,5 мкг, 0,25 мкг или 0,1 мкг, предпочтительно менее 2 мкг, 1,5 мкг, 1,0 мкг, 0,5 мкг, 0,25 мкг или 0,1 мкг.
Согласно другому варианту реализации стандартная лекарственная форма предназначена для лечения демиелинизирующего заболевания у субъекта, нуждающегося в этом, при этом указанный субъект предпочтительно болен РС. Согласно другому варианту реализации однократную дозировку приготавливают для лечения демиелинизирующего заболевания у субъекта, нуждающегося в этом. Согласно одному из вариантов реализации демиелинизирующее заболевание представляет собой РС.
Согласно другому варианту реализации однократную дозу приготавливают для увеличения ремиелинизации у субъекта, нуждающегося в этом, при этом указанный субъект предпочтительно болен РС.
Согласно одному из вариантов реализации стандартная лекарственная форма предназначена для перорального введения, стандартную лекарственную форму предпочтительно приготавливают для перорального введения. Согласно другому варианту реализации стандартная лекарственная форма представляет собой трансдермальный пластырь.
В настоящем документе термин «примерно» означает разумную величину отклонения модифицированного термина, так что конечный результат существенно не изменяется. Например, при применении к определенному значению указанный термин следует толковать как включающий отклонение +/- 5% относительно данного значения.
Фармацевтические композиции налфурафина можно использовать в комбинации с другими терапевтическими средствами для лечения демиелинизирующих заболеваний.
6. 3. Терапевтическое применение налфурафина
Авторы изобретения неожиданно обнаружили, что налфурафин вызывает множество положительных эффектов при демиелинизации в мышиных моделях РС. Например, авторы изобретения обнаружили, что налфурафин является эффективным при лечении демиелинизации в мышиных моделях ЭАЭ и купризон-индуцированной демиелинизации, результаты, которые можно использовать для лечения демиелинизирующих заболеваний, таких как РС, у людей. Авторы изобретения также обнаружили, что налфурафин неожиданно является эффективным в отношении увеличения ремиелинизации у субъектов, нуждающихся в этом. Соответственно, такой препарат, имеющий доказанные показатели безопасности, может быть очень полезным при лечении демиелинизирующих заболеваний и/или для увеличения ремиелинизации.
Как показано в примерах 1, 10 и 12-18, налфурафин способствует функциональному (в том числе полному и устойчивому) восстановлению от паралича, вызванного ЭАЭ, у самцов и самок мышей. Налфурафин также приводит к уменьшению полной инвалидизации, вызванной ЭАЭ (см. пример 2), и способствует восстановлению от потери массы, вызванной ЭАЭ (см. пример 3). Важно отметить, что в описанных в настоящем документе примерах индекс заболевания полностью уменьшается до <0,5, что, как считается в данной области техники, соответствует «полному восстановлению» от паралича, за одним исключением. Короткий 4-дневный курс, начатый в начале заболевания, не был эффективен в отношении стимулирования восстановления (пример 11), что демонстрирует эффективность длительной терапии, как описано в настоящем документе.
Налфурафин уменьшает инфильтрацию иммунных клеток в головной мозг в модели РС на основе ЭАЭ (см. пример 4) и является более эффективным, чем препарат сравнения U-50488, который не уменьшает инфильтрацию (пример 19). При введении до начала заболевания налфурафин способствует функциональному восстановлению от паралича в модели РС на основе ЭАЭ (см. пример 5). Миелинизация также улучшается у мышей, получавших налфурафин после начала паралича, в модели РС на основе ЭАЭ (примеры 6, 20 и 25).
С помощью описанных в настоящем документе примеров авторы изобретения ясно показывают, что налфурафин вызывает и/или увеличивает ремиелинизацию в модели ЭАЭ. В примере 6 TEM изображения спинного мозга мышей с ЭАЭ, получавших налфурафин, напоминают изображения здорового животного контрольной группы.
Результаты ЭАЭ были подтверждены исследованиями с применением купризона, описанными в примерах 7-9 и 11. В примерах 7 и 28 налфурафин улучшал увеличение массы при введении после демиелинизации, вызванной купризоном. В примере 8 налфурафин усиливал функциональное восстановление координации и равновесия у демиелинизированных мышей. При введении налфурафина мышам, получавшим купризон, происходила ремиелинизация мозолистого тела (см. примеры 9 и 29).
В примере 15 демонстрация устойчивого восстановления заслуживает особого внимания и показывает совершенно неожиданную способность налфурафина устойчиво обращать вспять симптомы демиелинизации. Такой неожиданный результат указывает на то, что налфурафин может опосредовать устойчивое восстановление при демиелинизирующих заболеваниях, в том числе РС.
В примере 21 налфурафин не приводит к истощению основных популяций иммунных клеток на периферии, несмотря на снижение инфильтрации иммунных клеток в головной мозг. В примере 22 налфурафин способствует переключению Т-клеток-хелперов от эффекторных клеток к клеткам памяти, что указывает на разрешение иммунного ответа.
В примерах 23 и 24 для обеспечения полного эффекта налфурафина требуется KOR, но налфурафин является эффективным в отношении уменьшения проявления заболевания независимо от KOR, что позволяет предположить, что полный механизм, посредством которого налфурафин обеспечивает свои эффекты, является более сложным, чем активация KOR.
Положительное воздействие налфурафина на мышей было особенно неожиданным при дозировках от 0,003 мг/кг до 0,3 мг/кг, которые можно преобразовать в эквивалентную дозу для человека с помощью уравнения Рейгана-Шоу (Reagan-Shaw S; Nihal M; Ahmad N: Dose translation from animal to human studies revisited, FASEB J. 2007, Oct 17).
Альтернативно, дозы от 0,003 до 0,3 мг/кг можно преобразовать в эквивалентную дозу для человека, используя описанный в настоящем документе способ межвидового сравнения.
Квалифицированный специалист в данной области техники понимает, что существуют альтернативные алгоритмы, которые можно использовать для преобразования наблюдаемой терапевтической дозы, полученной при применении мышиной модели, в эквивалентную дозу для человека после демонстрации эффективной дозировки для мыши. Такие алгоритмы могут эффективно использоваться специалистом в данной области техники для определения подходящей дозы для человека.
Например, используя способ межвидового сравнения, квалифицированный специалист применяет отношение эффективной дозы для лечения зуда к эффективной дозе для лечения РС у одного и того же вида. Такое отношение может быть применимо к дозе для человека для преобразования дозы для лечения зуда в дозу для лечения РС. В этом случае имеются данные о дозах для лечения зуда, как в мышиной модели, так и модели человека, и это позволяет проводить расчеты, описанные ниже.
Данные, описывающие дозу лекарственного препарата, обеспечивающую 50% от максимального эффекта (ED50).
(мкг/кг)
(мкг/кг)
Для модели зуда средняя эффективная доза ED50 in vivo составляет ~ 2,71 мкг/кг (округлено до 3 мкг/кг) при подкожном или внутривенном введении (в данном расчете использовали только данные в двух верхних строках приведенной выше таблицы). Обоснованием этого является:
• Введение в проведенном исследовании ЭАЭ было внутрибрюшинным (i.p.)
• Биодоступность налфурафина (описанная в Winfuran - Assessment report European Medicines Agency, Committee for Medicinal Products for Human Use (EMA/CHMP/138212/2014):
o при пероральном (PO) введении составляет ~ 32%
o при подкожном (s. c.) введении составляет 96%
o при внутривенном (IV) введении составляет 100%
• Следовательно, подкожное и внутривенное введение будут характеризоваться биодоступностью, аналогичной внутрибрюшинному введению, тогда как пероральное введение не будет вследствие эффекта первого прохождения печеночного метаболизма, и поэтому оно было исключено из расчетов. Кроме того, модель расчесывания, вызванного морфином, работает посредством механизма действия, не связанного с механизмом действия зуда, вызванного веществом P, и поэтому была исключена.
Преобразование дозировки для лечения зуда в сравнении с ЭАЭ
При таком расчете предполагают, что реакция в виде зуда является биомаркером (суррогатом) для ЭАЭ.
1. Доза для мышей для лечения зуда составляет 3 мкг/кг/сутки.
2. Доза для мышей для лечения ЭАЭ составляет 3 мкг/кг/сутки (эффективная доза, показанная на фигуре 10).
3. Следовательно, отношение дозы для лечения зуда к дозе для лечения ЭАЭ у мыши = 1.
4. Применение показателя эффективности для лечения зуда в сравнении с ЭАЭ у одного и того же вида (мыши), составляющего 1.
5. Эффективная доза для людей для лечения зуда составляет 2,5 мкг/тело/сутки.
6. Расчет для преобразования дозы для мыши с ЭАЭ в прогнозируемую дозу для человека:
Доза для мыши с ЭАЭ /(3 мкг/кг/сутки для лечения зуда у мыши × 2,5 мкг/тело/сутки для лечения зуда у человека) = доза для лечения РС у человека.
7. Преобразование дозы для мыши с ЭАЭ в прогнозируемую дозу для лечения РС у человека:
1. 3 мкг/кг/сутки для мыши = 2,5 мкг/тело/сутки для человека (фигура 10).
2. 10 мкг/кг/сутки для мыши = 8,33 мкг/тело/сутки для человека (фигура 1).
3. 30 мкг/кг/сутки для мыши = 25 мкг/тело/сутки для человека (фигура 1).
4. 100 мкг/кг/сутки для мыши = 83,33 мкг/тело/сутки для человека (фигура 1).
5. 300 мкг/кг/сутки для мыши = 250 мкг/тело/сутки для человека (фигура 1).
Поскольку многие демиелинизирующие заболевания вызывают ужасно изнуряющие симптомы, любое улучшение результатов лечения является важным достижением. Авторы изобретения обнаружили, что налфурафин представляет собой эффективное средство лечения демиелинизирующих заболеваний, и в частности РС. В одном из примеров авторы изобретения полагают, что лечение с помощью налфурафина будет эффективным в отношении облегчения изнуряющих симптомов, связанных с клинически изолированным синдромом (CIS). Будучи одним из течений заболевания РС, CIS в общем случае относится к первому эпизоду неврологических симптомов, связанных с РС. Как правило, такой начальный эпизод вызван воспалением или демиелинизацией в центральной нервной системе (ЦНС) и будет продолжаться 24 часа или более.
Следовательно, согласно одному из аспектов в настоящем изобретении предложен способ лечения демиелинизирующего заболевания у субъекта, нуждающегося в этом, включающий введение указанному субъекту терапевтически эффективного количества налфурафина.
Согласно другому аспекту в настоящем изобретении предложен способ лечения демиелинизирующего заболевания у субъекта, включающий выявление субъекта, который получит пользу от пониженного уровня демиелинизации, и введение указанному субъекту терапевтически эффективного количества агента, снижающего уровень демиелинизации у субъекта по сравнению с уровнем демиелинизации до введения указанного агента, при этом указанный агент содержит налфурафин.
Согласно другому аспекту в настоящем изобретении предложен способ лечения демиелинизирующего заболевания у субъекта, нуждающегося в этом, включающий введение указанному субъекту терапевтически эффективного количества агента, снижающего уровень демиелинизации у субъекта по сравнению с уровнем демиелинизации до введения указанного агента, при этом указанный агент содержит налфурафин.
Термин «лечение», используемый в настоящем документе применительно к заболеванию или состоянию, относится к следующему: (а) ослаблению заболевания или состояния, например, путем устранения или инициирования регресса или уменьшения тяжести заболевания или медицинского состояния субъекта, подвергаемого лечению, по сравнению с субъектом, не получавшим лечение, согласно принятым в данной области техники критериям мониторинга заболевания или состояния (Wattjes et al. (2015). Evidence-based guidelines: MAGNIMS consensus guidelines on the use of MRI in multiple sclerosis--establishing disease prognosis and monitoring patients. Nat. Rev. Neurol. 11, 597–606; Traboulsee et al. (2016). Revised Recommendations of the Consortium of MS Centers Task Force for a Standardized MRI Protocol and Clinical Guidelines for the Diagnosis and Follow-Up of Multiple Sclerosis. AJNR Am. J. Neuroradiol. 37, 394–401; Toosy et al. (2014). Optic neuritis. Lancet Neurol. 13, 83–99; Ontaneda et al. (2017). Clinical outcome measures for progressive MS trials. Mult. Scler. 23, 1627–1635; Naismith et al. (2012). Diffusion tensor imaging in acute optic neuropathies: predictor of clinical outcomes. Arch. Neurol. 69, 65–71); (б) подавлению заболевания или состояния, например, путем замедления или прекращения развития заболевания или состояния по сравнению с субъектом, не получавшим лечение, согласно принятым в данной области техники критериям мониторинга заболевания или состояния (Oh et al. (2019). Imaging outcome measures of neuroprotection and repair in MS: A consensus statement from NAIMS. Neurology; Sormani et al. (2017). Assessing Repair in Multiple Sclerosis: Outcomes for Phase II Clinical Trials. Neurother. J. Am. Soc. Exp. Neurother. 14, 924–933; Zhang et al. (2018). Clinical trials in multiple sclerosis: milestones. Ther. Adv. Neurol. Disord. 11; Bjartmar et al. (2003). Axonal loss in the pathology of MS: consequences for understanding the progressive phase of the disease. J. Neurol. Sci. 206, 165–171; Toosy et al. (2014). Optic neuritis. Lancet Neurol. 13, 83–99), или (c) облегчению симптома заболевания или состояния у субъекта по сравнению с субъектом, не получавшим лечение, согласно принятым в данной области техники критериям мониторинга заболевания или состояния (van Munster et al. (2017). Outcome Measures in Clinical Trials for Multiple Sclerosis. CNS Drugs 31, 217–236; Uitdehaag (2018). Disability Outcome Measures in Phase III Clinical Trials in Multiple Sclerosis. CNS Drugs 32, 543–558; Toosy et al. (2014). Optic neuritis. Lancet Neurol. 13, 83–99). Согласно некоторым предпочтительным вариантам реализации «лечение» относится к статистически значимому ослаблению, как в (a), подавлению, как в (b), и/или облегчению, как в (c), по сравнению с соответствующим не получавшим лечение контрольным субъектом согласно принятым в данной области техники критериям мониторинга заболевания или состояния.
В определении «лечения» принятые в данной области техники критерии представляют собой один или более критериев измерения инвалидизации, которые могут включать расширенную шкалу инвалидизации, функциональную комплексную Z-оценку рассеянного склероза и шкалу влияния рассеянного склероза и краткий опросник на основании исследования течения заболевания, визуализацию головного мозга, спинного мозга или зрительного нерва, комплексную функциональную шкалу оценки рассеянного склероза и новые комплексные показатели инвалидизации, наряду с исследованиями, в которых оценивают ловкость руки, способность передвигаться, зрение (в том числе показатели осевой диффузивности, остроты зрения, контрастной чувствительности, вызванных зрительных потенциалов (VEP), толщину слоя нервных волокон сетчатки (RNFL)) и когнитивные способности.
Субъект может демонстрировать наблюдаемое или измеримое уменьшение одного или более симптомов, ассоциированных или связанных с заболеванием или состоянием, как известно специалистам в данной области техники, что указывает на улучшение. Согласно некоторым вариантам реализации заболевание или состояние представляет собой демиелинизирующее заболевание, предпочтительно РС, при этом у субъекта проявляется наблюдаемое и измеримое уменьшение одного или более симптомов, ассоциированных или связанных с РС, предпочтительно уменьшение демиелинизации, как известно специалистам в данной области техники, что указывает на улучшение. Согласно предпочтительным вариантам реализации улучшение представляет собой статистически значимое улучшение по сравнению с соответствующим не получавшим лечение контрольным субъектом согласно принятым в данной области техники критериям мониторинга заболевания или состояния.
Термины «уменьшение» и «уменьшенный» (и их грамматические варианты), используемые в настоящем документе применительно к демиелинизации, означают любое измеримое или наблюдаемое снижение степени или уровня демиелинизации или любого симптома демиелинизирующего заболевания, связанного с демиелинизацией, у подвергавшегося лечению субъекта по сравнению с уровнем демиелинизации у соответствующего (например, не получавшего лечение) контрольного субъекта. Согласно предпочтительным вариантам реализации измеримое или выявляемое уменьшение или снижение представляет собой статистически значимое уменьшение или снижение по сравнению с соответствующим контролем.
Термин «увеличение» (и его грамматические варианты), используемый в настоящем документе применительно к демиелинизации, означает любое измеримое или наблюдаемое увеличение степени или уровня ремиелинизации или улучшение любого симптома демиелинизирующего заболевания, связанного с ремиелинизацией, у подвергавшегося лечению субъекта по сравнению с уровнем ремиелинизации у соответствующего (например, не получавшего лечение) субъекта контрольной группы; например, получавшего плацебо или неактивный агент. Пример количественной оценки ремиелинизации продемонстрирован при лечении с помощью клемастина фумарата с применением показателей VEP для оценки ремиелинизации и восстановления (Green et al. (2017) Clemastine fumarate as a remyelinating therapy for multiple sclerosis (ReBUILD): a randomised, controlled, double-blind, crossover trial. Lancet. 390, 2481–2489; Jankowska-Lech et al. (2019). Peripapillary retinal nerve fiber layer thickness measured by optical coherence tomography in different clinical subtypes of multiple sclerosis. Mult. Scler. Relat. Disord. 27, 260–268; Naismith et al. (2012). Diffusion tensor imaging in acute optic neuropathies: predictor of clinical outcomes. Arch. Neurol. 69, 65–71; Oh et al. (2019). Imaging outcome measures of neuroprotection and repair in MS: A consensus statement from NAIMS. Neurology; Sormani et al. (2017). Assessing Repair in Multiple Sclerosis: Outcomes for Phase II Clinical Trials. Neurother. J. Am. Soc. Exp. Neurother. 14, 924–933). Согласно предпочтительным вариантам реализации измеримое или выявляемое снижение представляет собой статистически значимое снижение по сравнению с соответствующим контролем.
Под терминами «введение» или «прием» следует понимать предоставление налфурафина или фармацевтической композиции, содержащей, состоящей по существу из или состоящей из налфурафина, субъекту, нуждающемуся в лечении, в терапевтически полезной форме для определенного способа введения. Налфурафин можно вводить любым подходящим путем. Возможные пути введения включают, без ограничения, пероральный, парентеральный (в том числе внутримышечный, подкожный, внутрикожный, внутривенный, внутриартериальный, интрамедуллярный и интратекальный), внутрибрюшинный и местный (в том числе кожный/накожный, трансдермальный, мукозальный, трансмукозальный, интраназальный (например, с помощью назального спрея или капель), внутриглазной (например, с помощью глазных капель), пульмональный (например, путем ингаляции), буккальный, сублингвальный, ректальный и вагинальный.
В настоящем документе термин «терапевтически» означает «в начале заболевания».
Согласно определенным вариантам реализации налфурафин вводят с помощью лекарственных форм для перорального применения, таких как таблетки, капсулы, сиропы, суспензии и т. п. Согласно другому варианту реализации налфурафин вводят с помощью трансдермального пластыря.
Термин «терапевтически эффективное количество» относится к достаточному количеству активного агента в подходящей композиции и в подходящей лекарственной форме для лечения указанных болезненных состояний или для получения измеримого или наблюдаемого результата, такого как уменьшение демиелинизации или увеличение ремиелинизации. «Терапевтически эффективное количество» будет меняться в зависимости от соединения, тяжести демиелинизирующего заболевания и вида, возраста, массы и т. д. субъекта, подвергаемого лечению.
Согласно одному из вариантов реализации терапевтически эффективное количество налфурафина представляет собой количество, эквивалентное от примерно 0,003 до примерно 0,3 мг/кг при введении мыши, которое можно преобразовать в соответствии с принятой практикой в дозу для субъекта, представляющего собой животное или человека. Например, при применении уравнения Рейгана-Шоу терапевтически эффективное количество налфурафина для собаки будет составлять от примерно 0,67 до примерно 2 мг/кг.
Согласно одному из вариантов реализации терапевтически эффективное количество налфурафина представляет собой количество, эквивалентное от примерно 0,003 до примерно 0,3 мг/кг при введении мыши, преобразованное согласно способу межвидового сравнения, описанному в настоящем документе. Согласно одному из вариантов реализации терапевтически эффективное количество налфурафина для человека составляет от примерно 0,01 до примерно 5 мкг налфурафина в сутки, предпочтительно от примерно 0,01 до примерно 2,5 мкг налфурафина в сутки.
Согласно одному из вариантов реализации субъект представляет собой человека. Согласно одному из вариантов реализации предложенный способ включает введение от примерно 0,01 до примерно 5 мкг налфурафина в сутки, от примерно 0,01 до примерно 4 мкг, от примерно 0,01 до примерно 3 мкг, от примерно 0,01 до примерно 2,5 мкг, от примерно 0,01 до примерно 2 мкг, от примерно 0,01 до примерно 1,5 мкг, от примерно 0,01 до примерно 1 мкг, от примерно 0,01 до примерно 0,75 мкг, от примерно 0,01 до примерно 0,5 мкг или примерно 0,25 мкг налфурафина в сутки.
Согласно одному из вариантов реализации предложенный способ включает введение от примерно 0,01 до примерно 2,5 мкг налфурафина в сутки, от примерно 0,025 до примерно 2 мкг, от примерно 0,05 до примерно 1 мкг, от примерно 0,075 до примерно 0,75 мкг, от примерно 0,1 до примерно 0,5 мкг или от примерно 0,225 до примерно 0,325 мкг налфурафина в сутки.
Согласно некоторым вариантам реализации предложенный способ включает введение менее примерно 1 мкг налфурафина в сутки, предпочтительно менее 1 мкг налфурафина в сутки.
Согласно одному из вариантов реализации предложенный способ включает введение от примерно 0,01 до примерно 0,1 мкг налфурафина в сутки, от примерно 0,025 до примерно 0,075 мкг, от примерно 0,06 до примерно 0,04 мкг или примерно 0,05 мкг налфурафина в сутки.
Согласно одному из вариантов реализации предложенный способ включает длительную терапию.
Согласно некоторым вариантам реализации длительная терапия включает введение терапевтически эффективной дозы налфурафина субъекту, нуждающемуся в этом, в течение по меньшей мере 5 дней, по меньшей мере 6 дней или по меньшей мере 7 дней.
Согласно некоторым вариантам реализации длительная терапия включает введение терапевтически эффективной дозы налфурафина субъекту, нуждающемуся в этом, в течение по меньшей мере 5, предпочтительно по меньшей мере 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, предпочтительно по меньшей мере 90 дней.
Согласно некоторым вариантам реализации длительная терапия включает введение терапевтически эффективной дозы налфурафина субъекту, нуждающемуся в этом, в течение по меньшей мере недели, по меньшей мере 2 недель, по меньшей мере 3 недель, по меньшей мере 4 недель, по меньшей мере 6 недель или по меньшей мере 8 недель.
Согласно некоторым вариантам реализации длительная терапия включает введение в течение по меньшей мере 5 дней, по меньшей мере 6 дней, по меньшей мере 7 дней, по меньшей мере 14 дней, по меньшей мере 21 дня, по меньшей мере 28 дней, по меньшей мере 35 дней, по меньшей мере по меньшей мере 42 дней, по меньшей мере 45 дней, по меньшей мере 60 дней, по меньшей мере 120 дней, по меньшей мере 240 дней или по меньшей мере 360 дней.
Согласно некоторым вариантам реализации длительная терапия включает введение терапевтически эффективной дозы налфурафина субъекту, нуждающемуся в этом, в течение по меньшей мере 1 недели, по меньшей мере 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51 или по меньшей мере 52 недель.
Согласно некоторым вариантам реализации длительная терапия включает введение терапевтически эффективной дозы налфурафина субъекту, нуждающемуся в этом, в течение по меньшей мере 1 месяца, по меньшей мере 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35 или по меньшей мере 36 месяцев.
Согласно некоторым вариантам реализации длительная терапия включает определенный интервал дозирования, при этом указанный интервал дозирования предпочтительно составляет по меньшей мере 1 день.
Согласно некоторым вариантам реализации интервал дозирования составляет по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13 или 14 дней.
Согласно некоторым вариантам реализации интервал дозирования составляет по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11 или 12 недель.
Согласно некоторым вариантам реализации интервал дозирования составляет по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или 11 месяцев.
Термин «демиелинизирующее заболевание» относится к заболеванию нервной системы, при котором повреждается миелиновая оболочка нейронов. Демиелинизирующие заболевания включают демиелинизирующие миелинокластические заболевания и демиелинизирующие лейкодистрофические заболевания. Лечение демиелинизирующего заболевания может включать лечение с помощью агента, уменьшающего демиелинизацию, и/или агента, усиливающего ремиелинизацию.
Демиелинизирующие заболевания могут влиять на центральную нервную систему и периферическую нервную систему. Демиелинизирующие заболевания центральной нервной системы включают рассеянный склероз, в том числе клинически изолированный синдром (CIS), неврит зрительного нерва, болезнь Девика, воспалительные демиелинизирующие заболевания, нейропатии центральной нервной системы, такие как нейропатии, вызванные дефицитом витамина B12, миелопатии, такие как сухотка спинного мозга, лейкоэнцефалопатии, такие как прогрессирующая мультифокальная лейкоэнцефалопатия, лейкодистрофии или их комбинацию. Демиелинизирующие заболевания периферической нервной системы включают синдром Гийена-Барре и его хронический аналог, хроническую воспалительную демиелинизирующую полинейропатию, анти-MAG периферическую нейропатию, болезнь Шарко-Мари-Тута (CMT), дефицит меди, прогрессирующую воспалительную нейропатию или их комбинацию. Термин «субъект» относится к млекопитающему, более предпочтительно к человеку или домашнему животному. Предпочтительные домашние животные включают кошек, собак и лошадей. Другие субъекты, представляющие собой млекопитающих, включают сельскохозяйственных животных, в том числе лошадей, свиней, овец, коз, коров, оленей или домашнюю птицу, и лабораторных животных, в том числе обезьян, крыс, мышей, кроликов и морских свинок.
В настоящем изобретении также предложено применение налфурафина при производстве лекарственного средства для лечения демиелинизирующего заболевания у субъекта, нуждающегося в этом.
В настоящем изобретении также предложено применение налфурафина при производстве лекарственного средства для увеличения ремиелинизации у субъекта, нуждающегося в этом.
Кроме того, в настоящем изобретении предложен налфурафин для применения для лечения демиелинизирующего заболевания.
В настоящем изобретении также предложен налфурафин для применения для увеличения ремиелинизации.
Согласно одному из вариантов реализации заболевание представляет собой демиелинизирующее миелинокластическое заболевание.
Согласно одному из вариантов реализации заболевание представляет собой демиелинизирующее лейкодистрофическое заболевание.
Согласно одному из вариантов реализации демиелинизирующее заболевание представляет собой демиелинизирующее заболевание центральной нервной системы. Согласно одному из вариантов реализации демиелинизирующее заболевание центральной нервной системы выбрано из группы, включающей РС (в том числе клинически изолированный синдром; CIS), неврит зрительного нерва, болезнь Девика, воспалительные демиелинизирующие заболевания, нейропатии центральной нервной системы, миелопатии, такие как сухотка спинного мозга, лейкоэнцефалопатии, лейкодистрофии или их комбинацию.
Согласно одному из вариантов реализации демиелинизирующее заболевание представляет собой РС.
Согласно другому варианту реализации демиелинизирующее заболевание представляет собой демиелинизирующее заболевание периферической нервной системы. Согласно одному из вариантов реализации демиелинизирующее заболевание периферической нервной системы выбрано из группы, включающей синдром Гийена-Барре и его хронический аналог, хроническую воспалительную демиелинизирующую полинейропатию, периферическую нейропатию с антимиелин-ассоциированным гликопротеином (MAG), болезнь Шарко-Мари-Тута (CMT), дефицит меди и прогрессирующую воспалительную нейропатию.
Согласно другому аспекту в настоящем изобретении предложен способ увеличения ремиелинизации у субъекта, нуждающегося в этом, включающий введение указанному субъекту терапевтически эффективного количества налфурафина.
Согласно другому аспекту в настоящем изобретении предложен способ увеличения ремиелинизации у субъекта, включающий выявление субъекта, который получит пользу от повышенного уровня ремиелинизации, и введение указанному субъекту терапевтически эффективного количества агента, повышающего уровень ремиелинизации у субъекта по сравнению с уровнем ремиелинизации до введения указанного агента, при этом указанный агент содержит налфурафин.
Согласно другому аспекту в настоящем изобретении предложен способ увеличения ремиелинизации у субъекта, нуждающегося в этом, включающий введение указанному субъекту терапевтически эффективного количества агента, повышающего уровень ремиелинизации у субъекта по сравнению с уровнем ремиелинизации до введения указанного агента, при этом указанный агент содержит налфурафин.
В качестве вариантов реализации описанного в настоящем документе изобретения, относящегося к способу увеличения ремиелинизации у субъекта, специально рассмотрены все варианты реализации изобретения, изложенные в настоящем документе, относящиеся к аспектам изобретения, представляющим собой способы уменьшения демиелинизации, способы лечения РС, способы ослабления демиелинизации, способы ускорения ремиссии РС и способы лечения демиелинизирующего заболевания.
Согласно другому аспекту в настоящем изобретении предложен способ ослабления демиелинизации у субъекта, нуждающегося в этом, включающий введение указанному субъекту терапевтически эффективного количества налфурафина и, тем самым, снижение уровня демиелинизации у субъекта по сравнению с уровнем демиелинизации в отсутствие введения налфурафина.
Согласно другому аспекту в настоящем изобретении предложен способ ослабления демиелинизации у субъекта, нуждающегося в этом, включающий введение терапевтически эффективного количества агента, снижающего уровень демиелинизации у субъекта по сравнению с уровнем демиелинизации до введения указанного агента и/или увеличивающего уровень ремиелинизации у субъекта по сравнению с уровнем ремиелинизации до введения указанного агента, при этом указанный агент содержит налфурафин.
Согласно одному из вариантов реализации субъект представляет собой человека. Согласно одному из вариантов реализации предложенный способ включает введение от примерно 0,01 до примерно 5 мкг налфурафина в сутки, от примерно 0,01 до примерно 4 мкг, от примерно 0,01 до примерно 3 мкг, от примерно 0,01 до примерно 2,5 мкг, от примерно 0,01 до примерно 2 мкг, от примерно 0,01 до примерно 1,5 мкг, от примерно 0,01 до примерно 1 мкг, от примерно 0,01 до примерно 0,75 мкг, от примерно 0,01 до примерно 0,5 мкг или примерно 0,25 мкг налфурафина в сутки.
Согласно одному из вариантов реализации предложенный способ включает введение от примерно 0,01 до примерно 2,5 мкг налфурафина в сутки, от примерно 0,025 до примерно 2 мкг, от примерно 0,05 до примерно 1 мкг, от примерно 0,075 до примерно 0,75 мкг, от примерно 0,1 до примерно 0,5 мкг или от примерно 0,225 до примерно 0,325 мкг налфурафина в сутки.
Согласно некоторым вариантам реализации предложенный способ включает введение менее примерно 1 мкг налфурафина в сутки, предпочтительно менее 1 мкг налфурафина в сутки.
Согласно одному из вариантов реализации предложенный способ включает введение от примерно 0,01 до примерно 0,1 мкг налфурафина в сутки, от примерно 0,025 до примерно 0,075 мкг, от примерно 0,06 до примерно 0,04 мкг или примерно 0,05 мкг налфурафина в сутки.
Термин «ослабление демиелинизации» означает, что согласно определенным вариантам реализации степень или уровень демиелинизации у субъекта в качестве результата заболевания или в качестве симптома заболевания уменьшается по сравнению с другими идентичными состояниями у соответствующего контрольного субъекта или в соответствующий контрольный заданный момент времени, и/или что согласно определенным вариантам реализации степень или уровень ремиелинизации у субъекта увеличивается по сравнению с идентичными в других аспектах состояниями у соответствующего контрольного субъекта или в соответствующий контрольный заданный момент времени. Согласно некоторым предпочтительным вариантам реализации уменьшение или увеличение по сравнению с соответствующим контролем представляет собой статистически значимое уменьшение или увеличение.
Таким образом, согласно некоторым предпочтительным вариантам реализации термин «ослабление демиелинизации» означает, что степень или уровень демиелинизации у субъекта в качестве результата заболевания или в качестве симптома заболевания статистически значимо снижается или уменьшается по сравнению с подходящим контролем, как будет понятно специалисту в данной области техники с учетом описания настоящего изобретения, и/или степень или уровень ремиелинизации у субъекта статистически значимо увеличивается по сравнению с подходящим контролем, как будет понятно специалисту в данной области техники с учетом описания настоящего изобретения.
Аналогичным образом, термин «улучшение нервной функции» относится к определяемому количественно улучшению функции, характеризующемуся статистически разным изменением измеряемого параметра по сравнению с соответствующим контролем, как признано специалистом в данной области техники. Согласно некоторым вариантам реализации улучшение функции характеризуется статистически значимым изменением измеряемого параметра. Согласно одному из вариантов реализации измеряемый параметр представляет собой индекс заболевания, описанный в примере 1.
Симптомы, относящиеся к демиелинизации, будут меняться в зависимости от заболевания, но могут включать, например, но не ограничиваться ими, неврологические расстройства, такие как хроническая боль, когнитивное нарушение (в том числе нарушение памяти, внимания, концептуализации и способности к решению проблем) и обработка информации; парестезию одной или более конечностей, туловища или одной стороны лица; слабость или неуклюжесть ноги или руки; или нарушения зрения, например частичную слепоту и боль в одном глазу (ретробульбарный неврит зрительного нерва), слабость зрения или скотомы.
В настоящем изобретении также предложено применение налфурафина при производстве лекарственного средства для ослабления демиелинизации у субъекта, нуждающегося в этом.
В настоящем изобретении также предложен налфурафин для применения для ослабления демиелинизации у субъекта, нуждающегося в этом.
Согласно другому аспекту в настоящем изобретении предложен способ лечения РС у субъекта, нуждающегося в этом, включающий введение указанному субъекту терапевтически эффективного количества налфурафина. Субъект может страдать от любого типа РС, в том числе CIS, RRMS, PRMS, SPMS, PRMS или РС, сопровождаемого другим и/или неопределенным течением болезни.
В настоящем изобретении также предложено применение налфурафина при производстве лекарственного средства для лечения РС у субъекта, нуждающегося в этом.
Кроме того, в настоящем изобретении предложен налфурафин для применения для лечения РС у субъекта, нуждающегося в этом.
Согласно одному из вариантов реализации субъект страдает от RRMS. Согласно одному из вариантов реализации субъект страдает от PPMS. Согласно одному из вариантов реализации субъект страдает от SPMS или у него диагностирован SPMS. Согласно одному из вариантов реализации субъект страдает от PRMS или у него диагностирован PRMS. Согласно одному из вариантов реализации субъект страдает от клинически изолированного синдрома (CIS) или у него диагностирован клинически изолированный синдром (CIS).
Согласно другому аспекту в настоящем изобретении предложен способ лечения РС у субъекта, нуждающегося в этом, включающий введение указанному субъекту терапевтически эффективного количества агента, снижающего уровень демиелинизации у субъекта по сравнению с уровнем до введения указанного агента и/или повышающего уровень ремиелинизации у субъекта по сравнению с уровнем до введения указанного агента, при этом указанный агент содержит налфурафин.
Согласно некоторым вариантам реализации способы лечения РС, описанные в настоящем документе, могут включать одну или более из следующих стадий, выбранных из группы, состоящей из диагностирования РС у субъекта, тестирования на наличие демиелинизации у субъекта, тестирования на уменьшение или реверсирование демиелинизации у субъекта, тестирования на ремиелинизацию у субъекта, тестирования на степень паралича или уменьшение или реверсирование степени паралича у субъекта и тестирования на ухудшение или улучшение координации и/или равновесия у субъекта.
Согласно одному из вариантов реализации предложенный способ лечения РС, и/или лечения демиелинизирующего заболевания, и/или ослабления демиелинизации, и/или увеличения ремиелинизации включает выявление субъекта, который получит пользу от пониженного уровня демиелинизации.
Согласно некоторым вариантам реализации субъекта, который получит пользу от пониженного уровня демиелинизации и/или повышенного уровня ремиелинизации, выявляют на основании проявления одного или более клинических симптомов РС, включающих, но не ограниченных ими: потерю чувствительности или изменения ощущения, такие как звон в ушах, покалывание булавками и иглами или онемение, мышечная слабость различной степени тяжести, сильно выраженные рефлексы, мышечные спазмы или затруднение при движении; трудности с координацией и равновесием (атаксию); спастичность; проблемы с речью или глотанием, проблемы со зрением (нистагм, неврит зрительного нерва или двоение в глазах), усталость, острую или хроническую боль, лицевую боль (невралгию тройничного нерва), проблемы с мочевым пузырем и кишечником, недержание мочи, снижение когнитивных способностей, депрессию, беспокойство и другие эмоциональные отклонения, сексуальную дисфункцию, феномен Утхоффа (ухудшение симптомов вследствие воздействия более высоких, чем обычно, температур) и симптом Лермитта (ощущение воздействия электрического тока, которое проходит по спине при сгибании шеи).
Согласно некоторым вариантам реализации терапевтически эффективное количество налфурафина, применяемое для введения субъекту, представляющему собой человека, составляет от примерно 0,01 до примерно 5 мг налфурафина в сутки, от примерно 0,01 до примерно 4 мкг, от примерно 0,01 до примерно 3 мкг, от примерно 0,01 до примерно 2,5 мкг, от примерно 0,01 до примерно 2 мкг, от примерно 0,01 до примерно 1,5 мкг, от примерно 0,01 до примерно 1 мкг, от примерно 0,01 до примерно 0,75 мкг, от примерно 0,01 до примерно 0,5 мкг или примерно 0,25 мкг налфурафина в сутки.
Согласно некоторым вариантам реализации терапевтически эффективное количество налфурафина, применяемое для введения субъекту, представляющему собой человека, составляет от примерно 0,01 до примерно 2,5 мкг налфурафина в сутки, от примерно 0,025 до примерно 2 мкг, от примерно 0,05 до примерно 1 мкг, от примерно 0,075 до примерно 0,75 мкг, от примерно 0,1 до примерно 0,5 мкг или от примерно 0,225 до примерно 0,325 мкг налфурафина в сутки.
Согласно некоторым вариантам реализации предложенный способ включает введение менее примерно 1 мкг налфурафина в сутки, предпочтительно менее 1 мкг налфурафина в сутки.
Согласно некоторым вариантам реализации терапевтически эффективное количество налфурафина, применяемое для введения субъекту, представляющему собой человека, составляет от примерно 0,01 до примерно 0,1 мкг налфурафина в сутки, от примерно 0,025 до примерно 0,075 мкг, от примерно 0,06 до примерно 0,04 мкг или примерно 0,05 мкг налфурафина в сутки.
Согласно одному из вариантов реализации лечение приводит к одному или более клиническим результатам по сравнению с субъектами, не подвергавшимися лечению с помощью налфурафина, выбранным из группы, состоящей из:
(а) уменьшения прогрессирования заболевания РС;
(b) снижения тяжести заболевания РС;
(c) уменьшения демиелинизации нервных клеток;
(d) уменьшения частоты или тяжести приступов рецидивирующего РС;
(e) уменьшения клинических симптомов РС;
(е) заживления поврежденной нервной ткани (восстановления функции нервной ткани);
(g) увеличения ремиелинизации демиелинизированных нервов в центральной нервной системе (восстановления функции нервной ткани/нейропротекции);
(h) защиты поврежденной нервной ткани от дальнейшей активности заболевания (нейропротекции);
(i) стимулирования удлинения нейронов (нейрорегенерации) в центральной нервной системе;
(j) уменьшения проявления инвалидизации, вызванной РС;
(k) улучшения функции нервной системы; и
(k) повышенной скорости ремиссии.
Согласно другому варианту реализации такое лечение приводит к уменьшению одного или более клинических симптомов РС, включающих, но не ограниченных ими, потерю чувствительности или изменения ощущения, такие как звон в ушах, покалывание булавками и иглами или онемение, мышечную слабость различной степени тяжести, сильно выраженные рефлексы, мышечные спазмы или затруднение при движении; трудности с координацией и равновесием (атаксию); спастичность; проблемы с речью или глотанием, проблемы со зрением (нистагм, неврит зрительного нерва или двоение в глазах), усталость, острую или хроническую боль, лицевую боль (невралгию тройничного нерва), проблемы с мочевым пузырем и кишечником, недержание мочи, снижение когнитивных способностей, депрессию, беспокойство и другие эмоциональные отклонения, сексуальную дисфункцию, феномен Утхоффа (ухудшение симптомов вследствие воздействия более высоких, чем обычно, температур) и симптом Лермитта (ощущение воздействия электрического тока, которое проходит по спине при сгибании шеи).
Согласно одному из аспектов в настоящем изобретении предложен способ ускорения ремиссии РС у субъекта, нуждающегося в этом, включающий введение указанному субъекту терапевтически эффективного количества налфурафина.
Согласно одному из аспектов в настоящем изобретении предложен способ ускорения ремиссии при РС у субъекта, нуждающегося в этом, включающий введение указанному субъекту терапевтически эффективного количества агента, снижающего уровень демиелинизации у субъекта по сравнению с уровнем демиелинизации до введения указанного агента, при этом указанный агент содержит налфурафин.
Согласно одному из аспектов в настоящем изобретении предложен способ ускорения ремиссии при РС у субъекта, нуждающегося в этом, включающий введение указанному субъекту терапевтически эффективного количества агента, повышающего уровень ремиелинизации у субъекта по сравнению с уровнем ремиелинизации до введения указанного агента, при этом указанный агент содержит налфурафин.
В настоящем изобретении также предложено применение налфурафина при производстве лекарственного средства для ускорения ремиссии при РС у субъекта, нуждающегося в этом.
В настоящем изобретении также предложен налфурафин для применения для ускорения ремиссии при РС у субъекта, нуждающегося в этом.
Согласно некоторым вариантам реализации терапевтически эффективное количество налфурафина, применяемое для введения субъекту, представляющему собой человека, составляет от примерно 0,01 до примерно 5 мкг налфурафина в сутки, от примерно 0,01 до примерно 4 мкг, от примерно 0,01 до примерно 3 мкг, от примерно 0,01 до примерно 2,5 мкг, от примерно 0,01 до примерно 2 мкг, от примерно 0,01 до примерно 1,5 мкг, от примерно 0,01 до примерно 1 мкг, от примерно 0,01 до примерно 0,75 мкг, от примерно 0,01 до примерно 0,5 мкг или примерно 0,25 мкг налфурафина в сутки.
Согласно некоторым вариантам реализации терапевтически эффективное количество налфурафина, применяемое для введения субъекту, представляющему собой человека, составляет от примерно 0,01 до примерно 2,5 мкг налфурафина в сутки, от примерно 0,025 до примерно 2 мкг, от примерно 0,05 до примерно 1 мкг, от примерно 0,075 до примерно 0,75 мкг, от примерно 0,1 до примерно 0,5 мкг или от примерно 0,225 до примерно 0,325 мкг налфурафина в сутки.
Согласно некоторым вариантам реализации предложенный способ включает введение менее примерно 1 мкг налфурафина в сутки, предпочтительно менее 1 мкг налфурафина в сутки.
Согласно некоторым вариантам реализации терапевтически эффективное количество налфурафина, применяемое для введения субъекту, представляющему собой человека, составляет от примерно 0,01 до примерно 0,1 мкг налфурафина в сутки, от примерно 0,025 до примерно 0,075 мкг, от примерно 0,06 до примерно 0,04 мкг или примерно 0,05 мкг налфурафина в сутки.
В настоящем документе термин «усиленная ремиссия РС» означает, что начало процесса ремиссии достигается быстрее и/или скорость, с которой достигается ремиссия, является более высокой (по сравнению с субъектами, не подвергавшимися лечению с помощью налфурафина).
Ремиссию при рассеянном склерозе можно измерить с применением любого способа, известного в данной области техники, в том числе, но не ограничиваясь ими, статуса физической инвалидизации, биологических маркеров и сканирования головного мозга посредством МРТ.
Согласно одному из аспектов в настоящем изобретении предложен способ лечения РС у субъекта, представляющего собой человека, нуждающегося в этом, включающий введение субъекту от примерно 0,01 до примерно 5 мг налфурафина в сутки, от примерно 0,05 до примерно 2,0 мг, примерно от 0,15 до 0,6 мг налфурафина в сутки, при этом такое лечение приводит к одному или более клиническим результатам по сравнению с субъектами, не подвергавшимися лечению с помощью налфурафина, выбранным из группы, состоящей из:
(а) уменьшения прогрессирования заболевания РС;
(b) снижения тяжести заболевания РС;
(c) уменьшения демиелинизации нервных клеток;
(d) уменьшения частоты или тяжести приступов рецидивирующего РС;
(e) уменьшения клинических симптомов РС;
(е) заживления поврежденной нервной ткани (восстановления функции нервной ткани);
(g) увеличения ремиелинизации демиелинизированных нервов в центральной нервной системе (восстановления функции нервной ткани/нейропротекции);
(h) защиты поврежденной нервной ткани от дальнейшей активности заболевания (нейропротекции);
(i) стимулирования удлинения нейронов (нейрорегенерации) в центральной нервной системе;
(j) уменьшения проявления инвалидизации, вызванной РС;
(k) улучшения функции нервной системы; и
(k) повышенной скорости ремиссии.
Согласно одному из аспектов в настоящем изобретении предложен способ лечения РС у субъекта, представляющего собой человека, нуждающегося в этом, включающий введение субъекту от примерно 0,01 до примерно 5 мкг налфурафина в день, от примерно 0,01 до примерно 4 мкг, от примерно 0,01 до примерно 3 мкг, от примерно 0,01 до примерно 2,5 мкг, от примерно 0,01 до примерно 2 мкг, от примерно 0,01 до примерно 1,5 мкг, от примерно 0,01 до примерно 1 мкг, от примерно 0,01 до примерно 0,75 мкг, от примерно 0,01 до примерно 0,5 мкг или примерно 0,25 мкг налфурафина в день, при этом такое лечение приводит к одному или более клиническим результатам по сравнению с субъектами, не подвергавшимися лечению с помощью налфурафина, выбранным из группы, состоящей из:
(а) уменьшения прогрессирования заболевания РС;
(b) снижения тяжести заболевания РС;
(c) уменьшения демиелинизации нервных клеток;
(d) уменьшения частоты или тяжести приступов рецидивирующего РС;
(e) уменьшения клинических симптомов РС;
(е) заживления поврежденной нервной ткани (восстановления функции нервной ткани);
(g) увеличения ремиелинизации демиелинизированных нервов в центральной нервной системе (восстановления функции нервной ткани/нейропротекции);
(h) защиты поврежденной нервной ткани от дальнейшей активности заболевания (нейропротекции);
(i) стимулирования удлинения нейронов (нейрорегенерации) в центральной нервной системе;
(j) уменьшения проявления инвалидизации, вызванной РС;
(k) улучшения функции нервной системы; и
(k) повышенной скорости ремиссии.
Согласно некоторым вариантам реализации терапевтически эффективное количество налфурафина, применяемое для введения субъекту, представляющему собой человека, составляет от примерно 0,01 до примерно 2,5 мкг налфурафина в сутки, от примерно 0,025 до примерно 2 мкг, от примерно 0,05 до примерно 1 мкг, от примерно 0,075 до примерно 0,75 мкг, от примерно 0,1 до примерно 0,5 мкг или от примерно 0,225 до примерно 0,325 мкг налфурафина в сутки.
Согласно некоторым вариантам реализации предложенный способ включает введение менее примерно 1 мкг налфурафина в сутки, предпочтительно менее 1 мкг налфурафина в сутки.
Согласно некоторым вариантам реализации терапевтически эффективное количество налфурафина, применяемое для введения субъекту, представляющему собой человека, составляет от примерно 0,01 до примерно 0,1 мкг налфурафина в сутки, от примерно 0,025 до примерно 0,075 мкг, от примерно 0,06 до примерно 0,04 мкг или примерно 0,05 мкг налфурафина в сутки.
Согласно другому аспекту в настоящем изобретении предложен способ лечения демиелинизирующего заболевания у субъекта, включающий выявление субъекта, который получит пользу от пониженного уровня демиелинизации, и введение указанному субъекту терапевтически эффективного количества агента, снижающего уровень демиелинизации по сравнению с уровнем демиелинизации до введения указанного агента, при этом указанный агент содержит налфурафин.
Согласно другому аспекту в настоящем изобретении предложен способ увеличения ремиелинизации у субъекта, включающий выявление субъекта, который получит пользу от повышенного уровня ремиелинизации, и введение указанному субъекту терапевтически эффективного количества агента, повышающего уровень ремиелинизации по сравнению с уровнем ремиелинизации до введения указанного агента, при этом указанный агент содержит налфурафин.
В качестве вариантов реализации описанного в настоящем документе изобретения, относящегося к налфурафину для применения для уменьшения демиелинизации, ослабления демиелинизации, ускорения ремиссии при РС, лечения РС, лечения демиелинизирующего заболевания и увеличения ремиелинизации, специально подразумеваются все варианты реализации изобретения, изложенные в настоящем документе, относящиеся к аспектам изобретения, представляющим собой способы уменьшения демиелинизации, ослабления демиелинизации, ускорения ремиссии при РС, лечения РС, лечения демиелинизирующего заболевания и увеличения ремиелинизации.
Кроме того, в качестве вариантов реализации описанного в настоящем документе изобретения, относящегося к применению налфурафина при производстве лекарственного средства для уменьшения демиелинизации, ослабления демиелинизации, ускорения ремиссии при РС, лечения РС или для увеличения ремиелинизации, специально подразумеваются все варианты реализации изобретения, изложенные в настоящем документе, относящиеся к аспектам изобретения, представляющим собой способы уменьшения демиелинизации, ослабления демиелинизации, ускорения ремиссии при РС, лечения РС, лечения демиелинизирующего заболевания и увеличения ремиелинизации.
Кроме того, в настоящем документе для всех перечисленных аспектов настоящего изобретения, включающих способ, применение и налфурафин для применения, специально подразумеваются все варианты реализации, изложенные в настоящем документе, относящиеся к длительной терапии и интервалам дозирования при длительной терапии.
Настоящее изобретение состоит из описания, приведенного выше, а также предусматривает конструкции, примеры которых приведены ниже и которые никоим образом не ограничивают объем изобретения.
6.4. Примеры
Пример 1. Налфурафин способствует функциональному восстановлению от паралича при терапевтическом введении в модели РС на основе экспериментального аутоиммунного энцефаломиелита (ЭАЭ).
Подробный план эксперимента: Для индуцирования ЭАЭ самок мышей C57BL/6 иммунизировали подкожно (s.c.) в задний пах с применением пептида миелин-олигодендроцитарного гликопротеина (MOG) 35-55 (50 мг/мышь) в полном адъюванте Фрейнда, содержащем убитые нагреванием Mycobacterium tuberculosis (500 мкг/мышь). Кроме того, в дни 0 и 2 внутрибрюшинно (i.p.) вводили коклюшный токсин (200 нг/мышь). Мышей взвешивали и записывали полученные данные ежедневно. На 17 день (вертикальная пунктирная линия на фигуре 1) мыши начали ежедневно получать только носитель (носит.; 10% твин и 10% ДМСО в солевом растворе) или налфурафин в количестве 0,3, 0,1, 0,03 или 0,01 мг/кг путем внутрибрюшинной инъекции. Налфурафин был получен из Канзасского университета, Центральной лаборатории химико-синтетической биологии (University of Kansas, Synthetic Chemical Biology Core Laboratory) (чистота 97,6% согласно ВЭЖХ). Распределение в группы лечения было слепым. Индекс заболевания оценивали в баллах от 0 до 5: 0 (соответствует норме), 1 (частичный паралич хвоста), 2 (полный паралич хвоста), 3 (парализована одна задняя конечность или тяжелая инвалидизация обеих задних конечностей), 4 (полный паралич обеих задних конечностей) и 5 (смерть). Такая модель является стандартной моделью заболевания для рассеянного склероза и описана в публикации White et al. 2018. Scientific Reports. 8:259, которая в полном объеме включена в настоящий документ посредством ссылки. На фигуре 1 показаны объединенные результаты двух независимых экспериментов. Согласно однофакторному дисперсионному анализу с применением критерия множественного сравнения Даннетта, ****p<0,0001 и *p<0,05.
Объяснение и воздействие: Полученные результаты продемонстрировали, что налфурафин способен лечить текущее заболевание. Уменьшение проявления заболевания во всех группах, получавших налфурафин, указывает на восстановление от паралича, которое является полным при некоторых дозах (0,1 и 0,03 мг/кг) и является необычным в такой модели. В конечном счете, доза, при которой налфурафин демонстрировал наиболее быстрое восстановление в данном примере, составляла 0,1 мг/кг, при этом дозы выше и ниже указанного уровня оказались менее эффективными.
Пример 2: Налфурафин уменьшает уровень полной инвалидизации при терапевтическом введении в модели РС на основе ЭАЭ.
Подробный план эксперимента: ЭАЭ индуцировали у самок мышей C57BL/6, как описано в примере 1. На 17 день мыши начали ежедневно получать только носитель (носит.) или налфурафин в количестве 0,3, 0,1 или 0,03 мг/кг путем внутрибрюшинной инъекции. Площадь под кривой (AUC) рассчитывалась для каждой мыши на основании ежедневной оценки индекса заболевания и представляет собой полную инвалидизацию, определенную опытным путем. На фигуре 2 показаны результаты из 1 репрезентативного эксперимента. Согласно однофакторному дисперсионному анализу с применением критерия множественного сравнения Даннетта *p<0,05.
Объяснение и воздействие: Несмотря на то, что все группы лечения имели похожие индексы заболевания в начале лечения (нижний график), мыши, ежедневно получавшие налфурафин, имели значительно более низкий уровень полной инвалидизации к 45 дню после иммунизации, выполненной для индуцирования ЭАЭ (верхний график). Дозы 0,03 и 0,1 мг/кг налфурафина оказали наибольшее влияние на уменьшение инвалидизации. Доза налфурафина 0,1 мг/кг приводила к уменьшению проявления заболевания на 60%.
Не желая ограничиваться теорией, авторы изобретения полагают, что результаты, полученные в примере 2, свидетельствуют о преимуществах лечения с помощью налфурафина в течение периода, составляющего по меньшей мере неделю. Соответственно, согласно некоторым вариантам реализации введение включает введение в течение по меньшей мере 7 дней, по меньшей мере 14 дней, по меньшей мере 30 дней, по меньшей мере 45 дней, по меньшей мере 60 дней, по меньшей мере 120 дней, по меньшей мере 240 дней или по меньшей мере 360 дней.
Пример 3: Налфурафин способствует восстановлению от потери массы, вызванной ЭАЭ, при терапевтическом введении.
Подробный план эксперимента: ЭАЭ индуцировали у самок мышей C57BL/6, как описано в примере 1. Мышей ежедневно взвешивали и рассчитывали % изменение массы тела. На 17 день (вертикальная пунктирная линия на фигуре 3) мыши начали ежедневно получать только носитель (носит.) или налфурафин в количестве 0,3, 0,1 или 0,03 мг/кг путем внутрибрюшинной инъекции.
Объяснение и воздействие: Как показано на фигуре 3, в начале заболевания мыши быстро теряли массу. После начала лечения с помощью налфурафина (вертикальная пунктирная линия) мыши восстанавливались от потери массы, вызванной ЭАЭ.
Пример 4. Налфурафин уменьшает инфильтрацию иммунных клеток в головной мозг при терапевтическом введении в низких дозах в модели РС на основе ЭАЭ.
Подробный план эксперимента: ЭАЭ индуцировали у самок мышей C57BL/6, как описано в примере 1. На 17 день мыши начали ежедневно получать только носитель (носит.) или налфурафин в количестве 0,3, 0,1 или 0,03 мг/кг путем внутрибрюшинной инъекции. На 45 день после иммунизации, выполненной для индуцирования ЭАЭ, мышей выбраковывали и выделяли из головного мозга иммунные клетки. Выделение осуществляли посредством градиента плотности перколла, как описано в White et al. 2018. Scientific Reports. 8:259. После выделения клетки окрашивали с помощью флуоресцентно-меченных антител для распознавания специфических типов иммунных клеток и анализировали посредством проточной цитометрии. Все инфильтрирующие иммунные клетки были идентифицированы по экспрессии CD45high; CD4 Т-клетки были идентифицированы как CD45highCD4+, а макрофаги как CD45highCD11b+Gr-1-. Относительное количество клеток выражено как отношение к микроглии (MG), резидентные иммунные клетки головного мозга идентифицированы как CD45mediumCD11b+. Согласно однофакторному дисперсионному анализу с применением критерия множественного сравнения Даннетта *p<0,05.
Объяснение и воздействие: Как показано на фигуре 4, на 45 день наблюдалось значительное увеличение количества иммунных клеток в головном мозге мышей с ЭАЭ, получавших носитель, по сравнению со здоровыми животными. Лечение с применением 0,03 мг/кг налфурафина значительно уменьшало количество инфильтрирующих иммунных клеток, что позволяет предположить, что при такой дозе налфурафин может обладать иммуномодулирующими свойствами. Интересно, что хотя мыши, получавшие 0,1 мг налфурафина, имели аналогичные уровни инфильтрирующих клеток, что и животные, получавшие носитель, такие мыши не проявляли выраженных признаков заболевания и полностью восстановились от паралича (фигура 1).
Пример 5: Налфурафин способствует функциональному восстановлению от паралича при введении до начала паралича в модели РС на основе ЭАЭ.
Подробный план эксперимента: ЭАЭ индуцировали у самок мышей C57BL/6, как описано в примере 1. На 17 день (вертикальная пунктирная линия на фигуре 5) мыши начали ежедневно получать только носитель (носит.) или налфурафин в количестве 0,3, 0,1 или 0,03 мг/кг путем внутрибрюшинной инъекции. На фигуре 5 показаны результаты для мышей, которые не были больны во время лечения, но заболевание развилось позже. Согласно двухфакторному дисперсионному анализу с применением критерия множественного сравнения Холма-Сидака *p<0,05.
Объяснение и воздействие: Лечение с помощью налфурафина до начала заболевания не изменяло начало заболевания. Однако лечение с помощью налфурафина привело к быстрому восстановлению от паралича по сравнению с мышами, получавшими носитель. Такие данные позволяют предположить, что лечение с помощью налфурафина также будет эффективным в отношении снижения проявления общей инвалидизации при его введении до начала заболевания, но оно не может предотвратить начало заболевания.
Пример 6: Миелинизация у мышей, получавших налфурафин после начала паралича, улучшается в модели РС на основе ЭАЭ.
Подробный план эксперимента: ЭАЭ индуцировали у самок мышей C57BL/6, как описано в примере 1. На 17 день мыши начали ежедневно получать только носитель или налфурафин в количестве 0,03 мг/кг путем внутрибрюшинной инъекции. На 45 день после иммунизации, выполненной для индуцирования ЭАЭ, мышей выбраковывали и обрабатывали спинной мозг для анализа методом просвечивающей электронной микроскопии (TEM). На фигуре 6 показаны репрезентативные TEM изображения срезов спинного мозга, взятого у здоровых мышей (A), мышей с ЭАЭ, получавших носитель (B), или мышей с ЭАЭ, получавших налфурафин (C), окрашенных для демонстрации темных миелиновых колец вокруг аксонов нервных клеток.
Объяснение и воздействие: На 45 день наблюдалось значительное уменьшение количества темно-окрашенного миелина в спинном мозге мышей с ЭАЭ, получавших носитель, что свидетельствует о протекании демиелинизации. Кроме того, аксоны нервных клеток выглядели раздутыми, а цитоплазма дезорганизованной, что свидетельствует о клеточном стрессе. Напротив, у мышей, получавших налфурафин, аксоны нервных клеток выглядели здоровыми и хорошо миелинизированными, что соответствует полному функциональному восстановлению.
Пример 7: Налфурафин улучшал увеличение массы при введении после демиелинизации в купризоновой модели демиелинизации.
Подробный план эксперимента: Для индуцирования демиелинизации самок мышей C57BL/6 в течение 5 недель кормили 0,3% купризоном, введенным в рацион. В начале 4 недели (вертикальная пунктирная линия на фигуре 7) мыши начали ежедневно получать только носитель или налфурафин в количестве 0,1 мг/кг путем внутрибрюшинной инъекции. В начале 5 недели (вертикальная пунктирная линия на фигуре 7) купризон был исключен из рациона для обеспечения спонтанной ремиелинизации. Мышей ежедневно взвешивали и рассчитывали % изменение массы.
Объяснение и воздействие. Как показано на фигуре 7, купризон вызвал значительную потерю массы у мышей, как сообщалось ранее. Такую потерю массы гораздо более эффективно реверсировали путем введения налфурафина, чем при применении одного носителя.
Пример 8: Налфурафин усиливает функциональное восстановление координации и равновесия при введении после демиелинизации в купризоновой модели демиелинизации.
Подробный план эксперимента: Для индуцирования демиелинизации самок мышей C57BL/6 в течение 5 недель кормили 0,3% купризоном, введенным в рацион, и подвергали лечению с помощью налфурафина, как описано в примере 7. Еженедельно выполняли поведенческие тесты, в том числе тест для оценки способности удерживаться на вращающемся стержне, позволяющий измерить координацию. Мышей обучали на ускорительном приборе для оценки способности удерживаться на вращающемся стержне (Panlab, Harvard Apparatus) в течение периода от 4 до 5 дней перед регистрацией исходных показателей латентности на день 0 с последующими еженедельными измерениями на протяжении всего периода приема купризона и восстановления. Вращающийся стержень был установлен на 4 оборота в минуту (об/мин) и скорость ускорения 40 об/мин при максимальном времени отключения 5 минут. Регистрировали время и скорость, с которой животное падает с вращающегося стержня, и фиксировали среднее значение из 3 параллельных экспериментов. Полученные данные демонстрируют способность удерживаться на 9 неделе после приема носителя или налфурафина (0,1 мг/кг) по сравнению со способностью удерживаться на 5 неделе. Согласно t-критерию Стьюдента *p<0,05.
Объяснение и воздействие: Как показано на фигуре 8, купризон нарушал координацию у мышей, о чем сообщалось ранее. Вызванную купризоном инвалидизацию реверсировали путем введения налфурафина. Такие данные позволяют предположить, что налфурафин является эффективным в отношении уменьшения инвалидизации в модели демиелинизации, опосредованной неиммунной системой, например, демиелинизации, обнаруживаемой у некоторых пациентов с прогрессирующим РС.
Пример 9: Налфурафин усиливает миелинизацию при введении после демиелинизации в купризоновой модели демиелинизации.
Подробный план эксперимента. Для индуцирования демиелинизации самок мышей C57BL/6 в течение 5 недель кормили 0,3% купризоном, введенным в рацион, как описано в примере 7. На 65 день мышей выбраковывали и обрабатывали головной мозг для анализа методом просвечивающей электронной микроскопии (ТЕМ). Приведены репрезентативные ТЕМ-изображения срезов мозолистого тела здоровой мыши (без купризона), мыши, получавшей носитель и купризон, или мыши, получавшей налфурафин и купризон, окрашенных для демонстрации темных миелиновых колец вокруг аксонов нервных клеток. Миелин количественно определяли с помощью g-соотношения, представляющего собой внутренний диаметр аксона, деленный на общий внешний диаметр.
Объяснение и воздействие: Как показано на фигуре 9, купризон вызывал потерю миелина и сопутствующее нарушение регулярных аксональных структур в мозолистом теле по сравнению со здоровыми животными контрольной группы. Напротив, у животных, получавших купризон и налфурафин, было обнаружено больше миелина, при этом структура мозолистого тела была менее дезорганизованной. Такие данные указывают, что лечение с помощью налфурафина способствует ремиелинизации и восстановлению после вызванной купризоном демиелинизации, опосредованной неиммунной системой. Подобная демиелинизация, ассоциированная с неиммунной системой, наблюдается у некоторых пациентов с прогрессирующим РС.
Пример 10: Налфурафин способствует функциональному восстановлению от паралича при терапевтическом введении в модели РС на основе экспериментального аутоиммунного энцефаломиелита (ЭАЭ).
Подробный план эксперимента: ЭАЭ индуцировали у самок мышей C57BL/6, как описано в примере 1. Результаты показаны на фигуре 10. В день начала заболевания (индекс >1, пунктирная линия) мыши начали ежедневно получать только носитель (носит.) или налфурафин в количестве 0,3, 0,1, 0,03, 0,01 или 0,003 мг/кг путем внутрибрюшинной инъекции. Распределение в группы лечения было слепым. Приведены выровненные индексы для мышей (n = 33 в группе, получавшей носитель, 3 в группе, получавшей 0,3 мг/кг, 4 в группе, получавшей 0,1 мг/кг, 5 в группе, получавшей 0,03 мг/кг, 20 в группе, получавшей 0,01 мг/кг и 4 в группе, получавшей 0,003 мг/кг) с момента начала заболевания/начала лечения. Одно животное в группе, получавшей 0,3 мг/кг налфурафина, и 2 животных из группы, получавшей носитель, были умерщвлены на 17-18 день. Согласно двухфакторному дисперсионному анализу ****p<0,0001 для всех доз (кроме 0,3 мг/кг) по сравнению с носителем.
Объяснение и воздействие: При проведении лечения после начала заболевания (паралича) авторы изобретения показали, что налфурафин способен лечить текущее заболевание. Уменьшение проявления заболевания во всех группах, получавших налфурафин, указывает на восстановление от паралича, которое было полным при некоторых дозах (0,01 и 0,03 мг/кг); полное восстановление от заболевания необычно в такой модели, и эффективность лечения с помощью налфурафина является неожиданным. В конечном счете, доза, при которой налфурафин демонстрировал наиболее быстрое восстановление в этом примере, составляла 0,01 мг/кг, причем такой результат был воспроизведен в 6 независимых экспериментах.
Пример 11: Налфурафин не является эффективным при введении в течение короткого 4-дневного курса с момента начала заболевания в модели РС на основе ЭАЭ.
Подробный план эксперимента: ЭАЭ индуцировали у самок мышей C57BL/6, как описано в примере 1. Результаты показаны на фигуре 11. В день начала заболевания (индекс >1, пунктирная линия) мыши начали ежедневно получать только носитель или налфурафин в количестве 0,01 мг/кг в сутки путем внутрибрюшинной инъекции в течение всего экспериментального курса или только в течение четырех дней (заштрихованная область). Приведены выровненные индексы для мышей (n = 5/группа) с момента начала заболевания/начала лечения. **p<0,01 согласно двухфакторному дисперсионному анализу NalF (полноценное лечение) по сравнению с налфурафином (4 дня) или носителем.
Объяснение и воздействие: Лечение с помощью налфурафина не усиливало восстановление при введении в течение только четырех дней с момента начала заболевания, тогда как более продолжительное лечение действительно эффективно усиливало восстановление.
Пример 12. Налфурафин не изменяет пик заболевания при терапевтическом введении в модели РС на основе ЭАЭ.
Подробный план эксперимента: ЭАЭ индуцировали у самок мышей C57BL/6, как описано в примере 1. Результаты показаны на фигуре 12. В день начала заболевания (индекс >1) мыши начали ежедневно получать только носитель или налфурафин в количестве 0,3, 0,1, 0,03, 0,01 или 0,003 мг/кг путем внутрибрюшинной инъекции. Был измерен индекс на пике заболевания во время первого эпизода ЭАЭ и приведены среднее значение и стандартная ошибка для отдельных мышей (n = 33 в группе, получавшей носитель, 3 в группе, получавшей 0,3 мг/кг, 4 в группе, получавшей 0,1 мг/кг, 5 в группе, получавшей 0,03 мг/кг, 20 в группе, получавшей 0,01 мг/кг и 4 в группе, получавшей 0,003 мг/кг). Согласно тесту Крускала-Уоллиса с применением критерия множественного сравнения Дьюнна не было обнаружено значимых различий между любой дозой налфурафина и носителем. Приведенные данные получены на основе тех же экспериментов, что и в примере 10.
Объяснение и воздействие. Поскольку при любой дозе налфурафина не было обнаружено различия в индексе на пике заболевания по сравнению с носителем, налфурафин, по-видимому, не влиял на первичное иммунно-опосредованное нейровоспалительное событие, приводящее к демиелинизации и параличу. Такое обнаружение позволяет предположить, что наблюдаемое функциональное улучшение (то есть восстановление от паралича) происходит потому, что произошло заживление первичного повреждения, а, возможно, не потому, что первичное повреждение само было прекращено.
Пример 13: Налфурафин способствует полному восстановлению от паралича, вызванного ЭАЭ, при терапевтическом введении.
Подробный план эксперимента: ЭАЭ индуцировали у самок мышей C57BL/6, как описано в примере 1. Результаты показаны на фигуре 13. В день начала заболевания (индекс >1) мыши начали ежедневно получать только носитель или налфурафин в количестве 0,3, 0,1, 0,03, 0,01 или 0,003 мг/кг путем внутрибрюшинной инъекции. Мышей считали выздоровевшими, если они получали индекс <0,5 к 23 дню после начала лечения. Приведены проценты выздоровевших мышей в каждой группе (n = 33 в группе, получавшей носитель, 3 в группе, получавшей 0,3 мг/кг, 4 в группе, получавшей 0,1 мг/кг, 5 в группе, получавшей 0,03 мг/кг, 20 в группе, получавшей 0,01 мг/кг и 4 в группе, получавшей 0,003 мг/кг). Согласно точному критерию Фишера ****p<0,0001, **p<0,01 и *p<0,05. Приведенные данные получены на основе тех же экспериментов, что и в примере 10.
Объяснение и воздействие: Лечение с помощью налфурафина обеспечило полное функциональное восстановление (то есть отсутствие паралича) при терапевтическом введении и в широком диапазоне доз (все дозы от 0,003 до 0,1 мг/кг продемонстрировали значительный эффект). Полное восстановление в такой модели заболевания является необычным. Эффективность, достигаемая при лечении с применением налфурафина, является экстраординарной.
Пример 14: Налфурафин способствует полному восстановлению от паралича, вызванного ЭАЭ, при терапевтическом введении с EC50 <0,001 мг/кг.
Подробный план эксперимента: ЭАЭ индуцировали у самок мышей C57BL/6, как описано в примере 1. Результаты показаны на фигуре 14. В день начала заболевания (индекс >1) мыши начали ежедневно получать только носитель или налфурафин в количестве 0,1, 0,03, 0,01 или 0,003 мг/кг путем внутрибрюшинной инъекции. Мышей считали выздоровевшими, если они получали индекс <0,5 к 23 дню после начала лечения. Приведены проценты выздоровевших мышей в каждой группе (n = 33 в группе, получавшей носитель, 4 в группе, получавшей 0,1 мг/кг, 5 в группе, получавшей 0,03 мг/кг, 20 в группе, получавшей 0,01 мг/кг и 4 в группе, получавшей 0,003 мг/кг). Кривая доза-ответ была построена в диапазоне от дозы 0,1 мг/кг, при которой выздоровело 100%, до одного носителя, при приеме которого выздоровело 12,1%. На основе такой кривой рассчитали ЕС50, составляющую <0,001 мг/кг. Приведенные данные получены на основе тех же экспериментов, что и в примере 13.
Объяснение и воздействие: Лечение с помощью налфурафина обеспечило полное функциональное восстановление (то есть отсутствие паралича) при терапевтическом введении и в широком диапазоне доз (все дозы от 0,003 до 0,1 мг/кг продемонстрировали значительный эффект). Полное восстановление в такой модели болезни является неожиданным. Эффективность, достигаемая при лечении с применением налфурафина, является экстраординарной. Для достижения 50% от такого эффекта (то есть EC50) требуется расчетная доза <0,001 мг/кг.
Пример 15: Налфурафин способствует устойчивому функциональному восстановлению от паралича, вызванного ЭАЭ, при терапевтическом введении.
Подробный план эксперимента: ЭАЭ индуцировали у самок мышей C57BL/6, как описано в примере 1. Результаты показаны на фигуре 15. В день начала заболевания (индекс >1) мыши начали ежедневно получать только носитель или налфурафин в количестве 0,3, 0,1, 0,03, 0,01 или 0,003 мг/кг путем внутрибрюшинной инъекции. Мышей считали выздоровевшими, если они получали индекс <0,5 к 23 дню после начала лечения. Приведено количество дней, в течение которых мыши в каждой группе находились на стадии выздоровления (n = 33 в группе, получавшей носитель, 3 в группе, получавшей 0,3 мг/кг, 4 в группе, получавшей 0,1 мг/кг, 5 в группе, получавшей 0,03 мг/кг, 20 в группе, получавшей 0,01 мг/кг и 4 в группе, получавшей 0,003 мг/кг). Согласно однофакторному дисперсионному анализу с применением критерия множественного сравнения Холма-Сидака ****p<0,0001, **p<0,01 и *p<0,05. Приведенные данные получены на основе тех же экспериментов, что и в примере 10.
Объяснение и воздействие: Лечение с помощью налфурафина обеспечивает устойчивое функциональное восстановление (то есть отсутствие паралича) при терапевтическом введении и в широком диапазоне доз (все дозы от 0,003 до 0,1 мг/кг продемонстрировали значительный эффект).
Пример 16. Налфурафин способствует функциональному восстановлению от паралича у мышей-самцов при терапевтическом введении в модели РС на основе ЭАЭ.
Подробный план эксперимента: ЭАЭ индуцировали у мышей-самцов C57BL/6, как описано в примере 1. Результаты показаны на фигуре 16. В день начала заболевания (индекс >1, пунктирная линия) мыши начали ежедневно получать только носитель или налфурафин в количестве 0,01 мг/кг путем внутрибрюшинной инъекции. Распределение в группы лечения было слепым. Приведены выровненные индексы для мышей (n = 5/группа) с момента начала заболевания/начала лечения. Согласно двухфакторному дисперсионному анализу ****p<0,0001 по сравнению с носителем.
Объяснение и воздействие: Налфурафин является эффективным при обеспечении функционального восстановления от паралича, как у самок, так и у самцов.
Пример 17: Налфурафин способствует полному восстановлению мышей-самцов при терапевтическом введении в модели РС на основе ЭАЭ.
Подробный план эксперимента: ЭАЭ индуцировали у мышей-самцов C57BL/6, как описано в примере 1. Результаты показаны на фигуре 17. В день начала заболевания (индекс >1) мыши начали ежедневно получать только носитель или налфурафин в количестве 0,01 мг/кг путем внутрибрюшинной инъекции. Мышей считали выздоровевшими, если они получали индекс <0,5 к 23 дню после начала лечения. Приведены проценты выздоровевших мышей в каждой группе (n = 5/группа). Согласно точному критерию Фишера **p<0,01. Приведенные данные получены на основе тех же экспериментов, что и в примере 16.
Объяснение и воздействие: При терапевтическом введении лечение с помощью налфурафина способствует полному восстановлению (то есть отсутствию паралича) как у самок, так и у самцов.
Пример 18: Налфурафин способствует устойчивому восстановлению мышей-самцов от паралича, вызванного ЭАЭ, при терапевтическом введении.
Подробный план эксперимента: ЭАЭ индуцировали у мышей-самцов C57BL/6, как описано в примере 1. Результаты показаны на фигуре 18. В день начала заболевания (индекс >1) мыши начали ежедневно получать только носитель или налфурафин в количестве 0,01 мг/кг путем внутрибрюшинной инъекции. Мышей считали выздоровевшими, если они получали индекс <0,5 к 23 дню после начала лечения. Приведено количество дней, в течение которых мыши в каждой группе находились на стадии выздоровления (n = 5/группа). Согласно t-критерию Стьюдента ****p<0,0001. Приведенные данные получены на основе тех же экспериментов, что и в примере 16.
Объяснение и воздействие: При терапевтическом введении лечение с помощью налфурафина обеспечивает устойчивое функциональное восстановление (то есть отсутствие паралича) как у самок, так и у самцов.
Пример 19: Лечение с помощью налфурафина уменьшает инфильтрацию иммунных клеток в головной мозг при терапевтическом введении в модели РС на основе ЭАЭ (A), тогда как U-50488 не уменьшает (B).
Подробный план эксперимента: ЭАЭ индуцировали у самок мышей C57BL/6, как описано в примере 1. Результаты показаны на фигурах 19A и 19B. В день начала заболевания (индекс >1) мыши начали ежедневно получать только носитель или налфурафин в количестве 0,3, 0,1, 0,03, 0,01 или 0,003 мг/кг путем внутрибрюшинной инъекции (А). В отдельном эксперименте мышей аналогичным образом подвергали лечению с помощью только носителя или U-50488, агониста KOR, в количестве 1,6 и 5 мг/кг (B). Во время хронической фазы (> 24 дней после начала лечения) мышей выбраковывали и выделяли из головного мозга иммунные клетки. Выделение осуществляли посредством градиента плотности перколла, как описано в White et al. 2018. Scientific Reports. 8:259. После выделения клетки окрашивали с помощью флуоресцентно-меченных антител для распознавания специфических типов иммунных клеток и анализировали посредством проточной цитометрии. Все инфильтрирующие иммунные клетки были идентифицированы по экспрессии CD45high. Относительное количество клеток выражено как отношение к микроглии (MG), резидентные иммунные клетки головного мозга идентифицированы как CD45mediumCD11b+. Согласно однофакторному дисперсионному анализу с применением критерия множественного сравнения Холма-Сидака *p<0,05 по сравнению с носителем. NS, незначимый.
Объяснение и воздействие: На хронической стадии ЭАЭ наблюдалось значительное увеличение количества иммунных клеток в головном мозге мышей с ЭАЭ, получавших носитель, по сравнению со здоровыми животными (A). Лечение с применением 0,03 и 0,01 мг/кг налфурафина значительно уменьшало количество инфильтрирующих иммунных клеток, что позволяет предположить, что при указанных дозах налфурафин может обладать иммуномодулирующими свойствами. Интересно, что хотя мыши, получавшие 0,1 и 0,003 мг/кг налфурафина, имели аналогичные уровни инфильтрирующих клеток, что и животные, получавшие носитель, такие мыши не проявляли выраженных признаков заболевания и полностью выздоровели от паралича (фигура 13). Кроме того, налфурафин, а не U-50488, уменьшал нейровоспаление в такой модели, что указывает на то, что не все агонисты KOR обладают указанной активностью (B).
Пример 20. Миелинизация улучшилась у мышей, получавших налфурафин после начала паралича, в модели РС на основе ЭАЭ.
Подробный план эксперимента: ЭАЭ индуцировали у самок мышей C57BL/6, как описано в примере 1. Результаты показаны на фигуре 20. В день начала заболевания (индекс >1) мыши начали ежедневно получать только носитель или налфурафин в количестве 0,03 или 0,01 мг/кг путем внутрибрюшинной инъекции. Во время хронической фазы (> 24 дней после начала лечения) мышей выбраковывали, подвергали перфузии с применением 4% параформальдегида и обрабатывали спинной мозг для гистологического исследования. Срезы окрашивали люксолом прочным синим для оценки % площади спинного мозга, которая была демиелинизирована (то есть не окрашена люксолом прочным синим). % демиелинизации оценивали с помощью ImageJ. Приведены средние значения и стандартная ошибка отдельных значений для мышей с ЭАЭ, получавших носитель (n = 7) или 0,01 мг/кг (n = 6) и 0,03 мг/кг (n = 4) налфурафина. Согласно однофакторному дисперсионному анализу с применением критерия множественного сравнения Холма-Сидака **p<0,01.
Объяснение и воздействие: Во время хронической фазы, когда налфурафин обеспечивал полное функциональное восстановление у мышей, наблюдалось значительное снижение процента демиелинизации в спинном мозге мышей с ЭАЭ, получавших налфурафин, что предполагает возможность протекания ремиелинизации.
Пример 21: Налфурафин не изменяет долю основных популяций лимфоцитов в селезенке во время хронической фазы ЭАЭ.
Подробный план эксперимента: ЭАЭ индуцировали у самок мышей C57BL/6, как описано в примере 1. Результаты показаны на фигуре 21. В день начала заболевания (индекс >1) мыши начали ежедневно получать только носитель или налфурафин в количестве 0,01 мг/кг путем внутрибрюшинной инъекции. Во время хронической фазы (27 дней после начала лечения) мышей выбраковывали и оценивали их спленоциты с помощью проточной цитометрии. Процент основных популяций лимфоцитов определяли с применением CD4 (CD4 Т-клеток-хелперов), CD8 (CD8 цитотоксических Т-клеток) и B220 (В-клеток) и выражали в виде % живых лейкоцитов (то есть CD45 + клеток). Приведены средние значения и стандартная ошибка для отдельных мышей при n = 3 (здоровые животные), 4 (носитель) и 8. Согласно однофакторному дисперсионному анализу с применением критерия множественного сравнения Холма-Сидака не было обнаружено значимых различий между мышами, принимавшими носитель, и здоровыми мышами или мышами, принимавшими налфурафин.
Объяснение и воздействие: Налфурафин не изменял долю основных популяций лимфоцитов в селезенке, несмотря на снижение количества инфильтрирующих иммунных клеток, проникающих в центральную нервную систему. Сохранение количества нормальных лимфоцитов в селезенке у мышей, получавших налфурафин, указывает на то, что налфурафин не уменьшает инфильтрацию иммунных клеток в головной мозг путем уничтожения иммунных клеток.
Пример 22: Налфурафин не изменяет общее количество CD4 Т-клеток-хелперов в селезенке, но переключает CD4 Т-клетки из эффекторного состояния в состояние памяти, что указывает на разрешение иммунного ответа во время хронической фазы ЭАЭ.
Подробный план эксперимента: ЭАЭ индуцировали у самок мышей C57BL/6, как описано в примере 1. Результаты показаны на фигуре 22. В день начала заболевания (индекс >1) мыши начали ежедневно получать только носитель или налфурафин в количестве 0,01 мг/кг путем внутрибрюшинной инъекции. Во время хронической фазы (27 дней после начала лечения) мышей выбраковывали и оценивали их спленоциты с применением проточной цитометрии. Наивные CD4 Т-клетки (CD4+CD44-CD62Lhigh), эффекторные CD4 Т-клетки (CD4+CD44+CD62L-) и центральные Т-клетки памяти CD4 (CD4+CD44+CD62Lhigh) выражены в виде % CD4 Т-клеток. «Соотношение Teff:cm» представляет собой отношение эффекторных Т-клеток к центральным Т-клеткам памяти. Приведены средние значения и стандартная ошибка для отдельных мышей при n = 3 (здоровые животные), 4 (носитель) и 8. Согласно однофакторному дисперсионному анализу с применением критерия множественного сравнения Холма-Сидака **p<0,01 и *p<0,05.
Объяснение и воздействие: Повышенное отношение эффекторных клеток к центральным клеткам памяти у мышей с ЭАЭ, получавших носитель, по сравнению со здоровыми мышами указывает на продолжающийся и активный иммунный ответ, опосредованный CD4 Т-клетками. Общее количество CD4 Т-клеток было одинаковым у мышей, получавших налфурафин, и мышей, получавших носитель. Уменьшенное отношение у мышей, получавших налфурафин, по сравнению с мышами, получавшими носитель, указывает на смещение в направлении фенотипа клеток памяти, которое происходит во время фазы разрешения иммунного ответа. Переход в состояние памяти указывает на то, что разрешение иммунного ответа происходит у получавших налфурафин мышей в модели рассеянного склероза при инициировании заболевания посредством активного иммунного ответа.
Пример 23: Налфурафин уменьшает проявление заболевания, но не может привести к полному восстановлению при блокировке опиоидного каппа-рецептора (KOR).
Подробный план эксперимента: ЭАЭ индуцировали у самок мышей C57BL/6, как описано в примере 1. Результаты показаны на фигуре 23. В день начала заболевания (индекс >1, пунктирная линия) мышей подвергали лечению с применением только носителя (ежедневно), налфурафина (0,01 мг/кг в сутки путем внутрибрюшинной инъекции), антагониста KOR norBNI (10 мг/кг в неделю путем внутрибрюшинной инъекции) или одновременно налфурафина и norBNI. Приведены выровненные индексы для мышей (n = 8-9/группа) с момента начала заболевания/начала лечения. ****p<0,0001 согласно двухфакторному дисперсионному анализу NalF по сравнению с носителем или NalF + noBNI.
Объяснение и воздействие: Введение антагониста KOR, norBNI, устраняло способность налфурафина обеспечивать полное восстановление от паралича (то есть индекс <0,5), и такое обнаружение указывает на то, что для обеспечения полного эффекта налфурафина необходим KOR. Обнаружение того, что налфурафин является эффективным в отношении уменьшения проявления заболевания независимо от KOR (то есть в присутствии norBNI), указывает на то, что полный механизм, посредством которого налфурафин вызывает свои эффекты, является более сложным, чем активация KOR.
Пример 24: Активация KOR необходима для полного восстановления от паралича, опосредованного налфурафином.
Подробный план эксперимента: ЭАЭ индуцировали у самок мышей C57BL/6, как описано в примере 1. Результаты показаны на фигуре 24. В день начала заболевания (индекс >1, пунктирная линия) мышей подвергали лечению с применением только носителя (ежедневно), налфурафина (0,01 мг/кг в сутки путем внутрибрюшинной инъекции), антагониста KOR norBNI (10 мг/кг в неделю путем внутрибрюшинной инъекции) или одновременно налфурафина и norBNI. Регистрировали индекс на пике заболевания во время первого эпизода ЭАЭ, и считали мышей выздоровевшими, если они получали индекс <0,5 к 23 дню после начала лечения. Приведены индексы на пике заболевания, процент выздоровевших мышей в каждой группе и количество дней на стадии восстановления (n = 8–9/группа). **p<0,01 и ****p<0,0001 согласно точному критерию Фишера (% выздоровевших) или однофакторному дисперсионному анализу с применением критерия множественного сравнения Холма-Сидака (количество дней на стадии восстановления). Приведенные данные получены на основе тех же экспериментов, что и в примере 23.
Объяснение и воздействие: Введение антагониста KOR, norBNI, устраняло способность налфурафина обеспечивать и поддерживать восстановление от паралича (то есть индекс <0,5), и такое обнаружение указывает на то, что KOR необходим для обеспечения полного эффекта налфурафина в отношении содействия полному восстановлению, но не уменьшения проявления заболевания.
Пример 25: Миелинизация улучшается у мышей, получавших налфурафин после начала паралича, в модели РС на основе ЭАЭ.
Подробный план эксперимента: ЭАЭ индуцировали у самок мышей C57BL/6, как описано в примере 1. Результаты показаны на фигуре 25. В день начала заболевания (индекс >1) мыши начали ежедневно получать только носитель или налфурафин в количестве 0,01 мг/кг путем внутрибрюшинной инъекции. Во время хронической фазы (>24 дней после начала лечения) мышей выбраковывали, подвергали перфузии с применением 4% параформальдегида и обрабатывали спинной мозг для гистологического исследования. Для оценки демиелинизации срезы окрашивали люксолом прочным синим. Исследуемый участок, взятый для анализа, показан на фигуре 25А. Следует отметить присутствие демиелинизированных областей (очагов поражения) с меньшим окрашиванием люксолом прочным синим (LFB) (миелин) в переднем роге у мышей с ЭАЭ, получавших носитель (круг – фигура 25B), и отсутствие демиелинизированных очагов поражения у мышей, получавших налфурафин (фигура 25C). Количественные данные показаны на фигуре 25D. Для каждого изображения 5 рандомизированных участков переднего рога спинного мозга были проанализированы в ImageJ с применением средней насыщенности серого цвета и интегрированной плотности пикселей в качестве показателя плотности миелина. Данные получены на основе двух отдельных экспериментов с применением n = 4 (носитель), n = 8 (налфурафин) мышей с ЭАЭ, соответственно. Масштабная метка = 50 мкм. Согласно t-критерию Стьюдента *p<0,05.
Объяснение и воздействие: Заболевание ЭАЭ вызывало объемные поражения спинного мозга (см. только носитель (фигура 25B)), характеризующиеся потерей миелина и нейродегенерацией, что свидетельствует о том, что ЭАЭ является деструктивным заболеванием ЦНС. Лечение указанного болезненного состояния с помощью налфурафина уменьшало тяжесть такого поражения и демиелинизацию, что позволяет предположить, что предложенное лечение восстанавливает ткань спинного мозга до почти нормального состояния путем ремиелинизации.
Пример 26: Лечение с помощью налфурафина уменьшает клеточную инфильтрацию в спинной мозг при терапевтическом введении в модели РС на основе ЭАЭ.
Подробный план эксперимента: ЭАЭ индуцировали у самок мышей C57BL/6, как описано в примере 1. Результаты показаны на фигуре 26. В день начала заболевания (индекс >1) мыши начали ежедневно получать только носитель или налфурафин в количестве 0,01 мг/кг путем внутрибрюшинной инъекции. Во время хронической фазы (>24 дней после начала лечения) мышей выбраковывали, подвергали перфузии с применением 4% параформальдегида и погружали спинной мозг в парафин для гистологического исследования. Коронарные срезы 10 мкм окрашивали гематоксилином и эозином (H&E) для оценки инфильтрации лейкоцитов, маркера воспаления в очагах поражения, вызванных заболеванием ЭАЭ. Следует отметить большее количество лейкоцитов, присутствующих в переднем роге мышей с ЭАЭ, получавшим носитель, чем у мышей с ЭАЭ, которым вводили налфурафин. Изображения оценивали с помощью наблюдателя в слепом режиме (т.е. при маскировании данных) по уровню инфильтрации по шкале в диапазоне от 0 (отсутствие инфильтрации) до 3 (максимальная инфильтрация). Данные получены на основе двух отдельных экспериментов: n = 7 мышей (11 срезов) для мышей с ЭАЭ, получавших носитель; и n = 9 мышей (13 срезов) для мышей с ЭАЭ, получавших налфурафин. Масштабная метка = 50 мкм. t-критерий Стьюдента, * p<0,05.
Объяснение и воздействие: Заболевание ЭАЭ вызывало значительную гистопатологию спинного мозга. Окрашивание лейкоцитов с помощью H&E является показателем тяжести поражения, при этом чем больше количество инфильтрирующих клеток, тем серьезнее поражение, в том числе демиелинизация, как показано на панели «только носитель» и при количественной оценке. Лечение с помощью налфурафина продемонстрировало неожиданное уменьшение инфильтрирующих лейкоцитов при почти полном отсутствии очагов поражения и демиелинизации, что указывает на то, что такое лечение может устранить очаги поражения и/или вызвать ремиелинизацию.
Пример 27: Лечение с помощью налфурафина снижает уровень активированных астроцитов в спинном мозге при терапевтическом введении в модели РС на основе ЭАЭ.
Подробный план эксперимента: ЭАЭ индуцировали у самок мышей C57BL/6, как описано в примере 1. Результаты показаны на фигуре 27A-B. На 17 день мыши начали ежедневно получать только носитель или налфурафин в количестве 0,01 мг/кг путем внутрибрюшинной инъекции. На 45 день после иммунизации, выполненной для индуцирования ЭАЭ, мышей выбраковывали и обрабатывали спинной мозг для иммуногистохимического анализа (IHC). На фигуре 27А показаны репрезентативные клетки, иммуномеченые глиальным фибриллярным кислым белком (GFAP) (черное окрашивание), из коронарных срезов переднего рога спинного мозга, взятого у мышей с ЭАЭ. Изображения получены с применением 10 мкм погруженных в парафин срезов, окрашенных кроличьими антителами к GFAP при (1:1000, компания DAKO) перед фотографированием при 20-кратном увеличении, масштабная метка = 50 мкм. Количество астроцитов на срез в стандартной области интереса подсчитывали с применением подключаемого модуля устройства для подсчета клеток в ImageJ. Оценивали две секции на животное. Секции оценивали при n = 7 (10-13 секций), на основе 2 отдельных экспериментов. ***p = 0,0003 (фигура 27B).
Объяснение и воздействие: Как показано и количественно выражено на фигуре 27A, на 45 день наблюдалось значительное повышение количества активированных GFAP+ астроцитов в спинном мозге мышей с ЭАЭ, получавших носитель. Известно, что астроциты являются ранними и высокоактивными игроками в процессе образования очага поражения и представляют собой ключевой фактор обеспечения доступа периферических иммунных клеток к центральной нервной системе (Ponath et al. The Role of Astrocytes in Multiple Sclerosis. Front Immunol. 2018; 9: 217). Лечение путем внутрибрюшинного введения 0,01 мг/кг налфурафина значительно снижает количество активированных астроцитов, что позволяет предположить, что лечение с применением налфурафина может оказывать нейропротективное и противовоспалительное действие на ткань спинного мозга в указанном болезненном состоянии (фигура 27B).
Пример 28: Лечение с помощью налфурафина усиливает восстановление от потери массы при терапевтическом введении в купризоновой модели демиелинизирующего заболевания РС.
На фигуре 28А показана временная динамика вызванной купризоном демиелинизации и режим лечения.
Подробный план эксперимента: У самок мышей C57BL/6 индуцировали состояние демиелинизирующего заболевания (возраст от 8 до 14 недель и масса от 17 до 23 грамм). Как показано на временной шкале на фигуре 28А, мыши получали корм, содержащий купризон (0,3% (масс./масс.) купризона), или только корм (здоровые животные контрольной группы) в течение 35 дней, после чего их снова переводили на стандартный корм. На 28 день мыши начали ежедневно получать только носитель (ДМСО:Твин 80:солевой раствор) или налфурафин в количестве 0,1 мг/кг путем внутрибрюшинной инъекции или U-50488 в количестве 1,6 мг/кг путем внутрибрюшинной инъекции. На 70 день мышей выбраковывали и обрабатывали ткань головного мозга для анализа методом просвечивающей электронной микроскопии (ТЕМ). Мышей ежедневно взвешивали и рассчитывали % изменение массы.
Объяснение и воздействие: Такая модель является общепризнанной в качестве инструмента для изучения демиелинизации, вызванной неиммунной системой. Указанная модель позволяет оценить предполагаемые терапевтические средства, способствующие ремиелинизации (Matsushima and Morell, 2001. The neurotoxicant, cuprizone, as amodel to study demyelination and remyelination in the central nervous system. Brain Pathol. 11, 107–116).
На фигуре 28В показано вызванное купризоном изменение массы на протяжении всего периода исследования.
Подробный план эксперимента. Состояние демиелинизирующего заболевания индуцировали у самок мышей C57BL/6, как описано в примере 28 и проиллюстрировано на фигуре 28.
Объяснение и воздействие: Мыши, получавшие 0,3% купризона (CPZ), теряли массу при индуцировании заболевания по сравнению с мышами с обычным рационом в соответствии с индуцированием и тяжестью заболевания.
На фигуре 28C показано, что лечение с помощью налфурафина способствовало увеличению массы в фазе восстановления купризоновой модели демиелинизирующего заболевания РС, тогда как U-50488 не способствовал этому.
Подробный план эксперимента: Состояние демиелинизирующего заболевания индуцировали у самок мышей C57BL/6, как показано на фигуре 28C. Заболевших животных подвергали лечению с применением только носителя, налфурафина (0,1 мг/кг), U-50488 (1,6 мг/кг), как показано на фигуре 28A. Мышей ежедневно взвешивали и рассчитывали % изменение массы. *p<0,05 = мыши, получавшие налфурафин; #p<0,05 = мыши, получавшие U-50488. Двухфакторный дисперсионный анализ с повторными измерениями с последующим применением критериев множественного сравнения Тьюки. n = 15 мышей/группа из 3 параллельных экспериментов. С помощью дисперсионного анализа было обнаружено значимое взаимодействие F (40, 600) = 2,212 (p<0,0001) со значимым временем F (8, 600) = 101,2 (p<0,0001) и эффектами лечения F (5,75) = 5,52 (P<0,0002).
Объяснение и воздействие. Мыши, получавшие 0,3% купризона (CPZ), теряли массу при индуцировании заболевания. Мыши выздоравливали при возврате к обычному корму (удаление купризона) (фигура 28C). Лечение с помощью налфурафина усиливало восстановление потерянной массы быстрее по сравнению с мышами, получавшими только носитель или подвергаемыми лечению с применением U-50488.
Фигура 29: Лечение с помощью налфурафина усиливает ремиелинизацию при введении после демиелинизации в купризоновой модели демиелинизирующего заболевания РС.
Подробный план эксперимента: Состояние демиелинизирующего заболевания индуцировали у самок мышей C57BL/6, как показано на фигуре 28A. Результаты показаны на фигуре 29A-G. На панелях A-D на фигуре 29 показаны полученные посредством просвечивающей электронной микроскопии (TEM) репрезентативные изображения мозолистого тела мышей (A), получавших обычный рацион, и мышей (B-D), получавших 0,3% купризона для индуцирования демиелинизации. В соответствии с временной динамикой, показанной на фигуре 28A, мышам, получавшим купризон, вводили (B) только носитель, (C) U-50488 (1,6 мг/кг/внутрибрюшинно) и (D) налфурафин (0,1 мг/кг/внутрибрюшинно), а затем умерщвляли на 70 день эксперимента. Масштабные метки соответствуют 2000 нм.
На фигуре 29 (E) приведены результаты количественной оценки и анализа g-соотношений, демонстрирующие значимое различие между группами лечения F (3953) = 21,18 (p<0,0001). У мышей, получавших обычный рацион, среднее g-соотношение составляет 0,78 ± 0,09, в отличие от мышей, получавших 0,3% купризона, у которых наблюдалось значительное увеличение g-соотношения до 0,84 ± 0,1, соответствующее уменьшению толщины миелина (####p<0,0001). Мыши, получавшие рацион с купризоном, подвергаемые лечению с применением налфурафина (0,1 мг/кг/внутрибрюшинно) (0,75 ± 0,15), демонстрировали значительное снижение g-соотношения по сравнению с животными контрольной группы, получавшими наполнитель (****p<0,0001), соответствующее увеличению толщины миелина. Мыши, получавшие рацион с купризоном, подвергаемые лечению с применением U-50488, демонстрировали некоторое увеличение толщины миелина по сравнению с животными контрольной группы, получавшими носитель, при среднем g-соотношении (0,80) (**p<0,01), но, что неожиданно, при лечении с помощью налфурафина наблюдалось значительное увеличение толщины миелина (уменьшение g-соотношения) по сравнению с мышами, получавшими U-50488 (1,6 мг/кг/внутрибрюшинно) (^^^p<0,001), что указывает на то, что налфурафин является значительно более эффективным в отношении увеличения толщины миелина, чем U-50488. Приведенные данные представляют измерения 5 TEM изображений мозолистого тела, взятого от двух-трех мышей на группу лечения, и g-соотношения, рассчитанные (мера толщины миелина) с применением программного обеспечения Image J. Анализ проводили эксперты при маскировании данных в отношении групп лечения. (n = 204-267 аксонов на группу лечения).
На фигуре 29 (F) приведены результаты количественной оценки и анализа ряда миелинизированных аксонов в сравнении с немиелинизированными аксонами в исследуемой области (390 мкм2). n = 20 изображений на группу лечения (из n = 2-3 мышей).
На фигуре 29 (G) приведены результаты количественной оценки и анализа области окрашивания миелина на каждое TEM изображение, выполненное с применением программного обеспечения Image J (20 изображений на группу лечения из n = 2-3 мышей, умерщвленных на 70 день). TEM изображения были инвертированы по цвету (миелин белый), при этом для обнаружения миелина использовали порог. Площадь такого миелинового порога измеряли для каждой группы лечения.
Все данные анализировали с помощью однофакторного дисперсионного анализа с последующим применением критерия множественных сравнений Тьюки. Значимые различия по сравнению с введением только носителя обозначены как *; между здоровыми мышами и мышами, получавшими купризон/носитель #; и между налфурафином и U-50488 как ^. (*p<0,05; **p<0,01; ***p<0,001; ****p<0,0001).
Объяснение и воздействие: Как показано на фигурах 29A-G, демиелинизация в мозолистом теле головного мозга индуцированных купризоном животных, получавших только носитель (панель B), была достаточно очевидной. Соотношение между окружностью аксона и окружностью миелина (g-соотношение) уменьшалось при нормальной миелинизации. Индуцированные купризоном животные, получавшие налфурафин, демонстрировали более нормальную миелиновую структуру аксонов, миелинизированные аксоны были плотно упакованы внутри белого вещества, а миелиновые оболочки соседних волокон часто непосредственно соприкасались. Окрашивание миелиновых оболочек (черный) было более выраженным, что указывает на усиленную ремиелинизацию. Ультраструктура такой ткани животных, получавших налфурафин, была удивительно похожа на структуру ткани животных, не получавших лечение (здоровых). Согласно количественной оценке ткань животных, получавших налфурафин, имела значительно более низкое g-соотношение по сравнению с тканью животных, получавших только носитель, что свидетельствует об усиленной ремиелинизации, при этом g-соотношение было ближе к g-соотношению ткани животных, не получавших лечение (здоровых). Такой результата был дополнительно подтвержден анализом процентного увеличения количества миелинизированных аксонов и процентного увеличения площади миелинизации у животных, получавших налфурафин. Напротив, лечение с применением соединения U-50488 не привело к восстановлению или возврату к почти нормальному состоянию. Согласно качественной оценке миелиновая структура аксонов была дезорганизована, наблюдалась потеря аксонов и явно увеличенные миелиновые структуры аксонов. Согласно количественной оценке лечение с помощью U-50488 дало результаты, аналогичные результатам для образцов животных, получавших только носитель (то есть без явно выраженной ремиелинизации), тогда как лечение с помощью налфурафина привело к результатам, аналогичным результатам для ткани животных, не получавших лечение. Согласно качественной и количественной оценке лечение с помощью налфурафина усиливает ремиелинизацию, что свидетельствует о почти полном восстановлении после повреждения при демиелинизации, вызванной купризоном.
Пример 30: Налфурафин является более эффективным в отношении функционального восстановления, чем клемастина фумарат, известный ремиелинизирующий лекарственный препарат.
Подробный план эксперимента: ЭАЭ индуцировали у самок мышей C57BL/6, как описано в примере 1. Результаты показаны на фигуре 30. В день начала заболевания (индекс >1, пунктирная линия) мышей подвергали лечению с применением только носителя (ежедневно, n = 9) или налфурафина (0,01 мг/кг в сутки путем внутрибрюшинной инъекции; n = 8). В отдельном аналогичном эксперименте мышей подвергали лечению с применением только носителя (n = 5) или клемастина фумарата (10 мг/кг путем внутрибрюшинной инъекции; n = 7). Приведены выровненные индексы для мышей с момента начала заболевания/начала лечения. ****p<0,0001 согласно двухфакторному дисперсионному анализу NalF или клемастина по сравнению с носителем.
Объяснение и воздействие: Было показано, что клемастина фумарат, антигистамин, который также является антагонистом мускаринового рецептора, уменьшает проявление хронической инвалидизации в модели ЭАЭ при применении в количестве 10 мг/кг, начиная с момента иммунизации. Кроме того, было показано, что он усиливает ремиелинизацию у мышей и людей (Li et al. 2015, Clemastine rescues behavioral changes and enhances remyelination in the cuprizone mouse model of demyelination. Neurosci Bull. ; 31: 617-625; Green, A. J et al, 2017 Clemastine fumarate as a remyelinating therapy for multiple sclerosis (ReBUILD): a randomised, controlled, double-blind, crossover trial. Lancet Lond. Engl. 390, 2481–2489). В предложенной авторами изобретения модели ЭАЭ клемастин так же эффективен, как и в ранее опубликованных отчетах, но гораздо менее эффективен, чем налфурафин, в отношении обеспечения полного функционального восстановления (Mei, F. et al. 2016, Accelerated remyelination during inflammatory demyelination prevents axonal loss and improves functional recovery. ELife 5). Такой пример показывает, что в указанной модели налфурафин превосходит клемастина фумарат.
Пример 31: Налфурафин способствует большему и более устойчивому восстановлению, чем клемастина фумарат, известный ремиелинизирующий препарат.
Подробный план эксперимента: ЭАЭ индуцировали у самок мышей C57BL/6, как описано в примере 1. Результаты показаны на фигуре 31A-B. В день начала заболевания (индекс >1, пунктирная линия) мышей подвергали лечению с применением только носителя (ежедневно, n = 9) или налфурафина (0,01 мг/кг в сутки путем внутрибрюшинной инъекции; n = 8) (A). В отдельном аналогичном эксперименте мышей подвергали лечению с применением только носителя (n = 5) или клемастина фумарата (10 мг/кг путем внутрибрюшинной инъекции; n = 7) (B). Мышей считали выздоровевшими, если они получали индекс <0,5 к 23 дню после начала лечения. Приведены процент выздоровевших мышей в каждой группе (A) и количество дней на стадии восстановления (B). ****p<0,0001 согласно точному критерию Фишера (% выздоровевших; A) или однофакторному дисперсионному анализу с применением критерия множественного сравнения Холма-Сидака (количество дней на стадии восстановления; B). Приведенные данные получены на основе тех же экспериментов, что и в примере 30.
Объяснение и воздействие: Было показано, что клемастина фумарат, антигистамин, который также является антагонистом мускаринового рецептора, уменьшает проявление хронической инвалидизации в модели ЭАЭ при применении в количестве 10 мг/кг, начиная с момента иммунизации. Кроме того, было показано, что он усиливает ремиелинизацию у мышей и людей. В предложенной авторами изобретения модели ЭАЭ лечение с помощью клемастина фумарата способствовало восстановлению чуть более 50% мышей, но такое восстановление не было устойчивым. Напротив, все мыши выздоравливали после лечения с помощью налфурафина и демонстрировали устойчивое восстановление. Такое обнаружение указывает на то, что налфурафин превосходит клемастина фумарат в указанной модели и обеспечивает более устойчивое улучшение у каждого животного, подвергавшегося лечению.
Пример 32: Налфурафин способствует восстановлению болевого порога при введении после демиелинизации в купризоновой модели демиелинизирующего заболевания РС.
Подробный план эксперимента: У самок мышей C57BL/6 индуцировали состояние демиелинизирующего заболевания (старше 8-14 недель и массой от 17 до 23 грамм). Мыши получали корм, содержащий купризон (0,3% (масс./масс.) купризона), или только корм (здоровые животные контрольной группы) в течение 35 дней, после чего их снова переводили на стандартный корм. На 28 день мыши начали ежедневно получать только носитель (ДМСО:Твин 80:солевой раствор) или налфурафин в количестве 0,1 мг/кг путем внутрибрюшинной инъекции. Во втором эксперименте мыши получали корм, содержащий купризон (0,3% (масс./масс.) купризона), или только корм (здоровые животные контрольной группы) в течение 42 дней, после чего их снова переводили на стандартный корм. На 35 день мыши начали ежедневно получать только носитель (ДМСО:Твин 80:солевой раствор) или налфурафин в количестве 0,1 мг/кг путем внутрибрюшинной инъекции. В обоих исследованиях на 70 день мышей выбраковывали. См. фигуру 32А, на которой схематично показано индуцирование заболевания и временная динамика лечения.
Чувствительность к механическому воздействию вызывала у мышей отдергивание лапы. Порог отдергивания измеряли с применением калиброванных нитей фон Фрея посредством способа «вверх-вниз» (Bonin et al. A simplified up-down method (SUDO) for measuring mechanical nociception in rodents using von Frey filaments. Molecular Pain. 2014; 10:1-11) при максимальном проявлении заболевания, до лечения с помощью налфурафина. Купризон вызывал повышенную чувствительность к механическому воздействию по сравнению с мышами, получавшими обычный рацион (^p<0,05) (фигура 32В), при этом такое увеличение порога отдергивания при механическом воздействии уменьшалось до исходных уровней после лечения с помощью налфурафина (0,1 мг/кг/внутрибрюшино). *p<0,05 при максимальном проявлении заболевания (28 или 35 день) и после ежедневного лечения с помощью налфурафина (средний порог, 45-70 дни). У мышей, получавших налфурафин, улучшились показатели порога при механическом воздействии по сравнению с мышами, получавшими носитель (# p<0,05). t-критерий Стьюдента, n = 10-11 мышей/группа из 2 независимых экспериментов. ^ по сравнению с мышами на обычном рационе; * порог до и после лечения; # различия при восстановлении между группами лечения. Были проанализированы объединенные данные из 2 экспериментальных когорт (максимальное проявление заболевания наступает за неделю до начала лечения и при максимальном восстановлении (63-70 дни).
Объяснение и воздействие: Хроническая боль часто связана с рассеянным склерозом. Аллодиния представляет собой усиление болевых ощущений при воздействии обычно безболезненного раздражителя. В таком тесте нити фон Фрея используют для измерения порога отдергивания лапы после приложения определенного механического воздействия. После демиелинизации, вызванной купризоном, болевой порог является функциональным биомаркером восстановления, свидетельствующим о ремиелинизации нервных волокон. Примечательно, что заболевшие животные, получавшие налфурафин, имели болевую чувствительность, аналогичную исходной, что указывает на то, что предложенное лечение улучшает функциональное восстановление.
| название | год | авторы | номер документа |
|---|---|---|---|
| НОВЫЕ СПОСОБЫ ЛЕЧЕНИЯ РАССЕЯННОГО СКЛЕРОЗА | 2018 |
|
RU2765820C2 |
| ЖИВОТНАЯ МОДЕЛЬ, ЭКСПРЕССИРУЮЩАЯ ЛЮЦИФЕРАЗУ ПОД КОНТРОЛЕМ ПРОМОТОРА ОСНОВНОГО БЕЛКА МИЕЛИНА (MBP-LUCI), И ПРИМЕНЕНИЕ МОДЕЛИ ДЛЯ ВИЗУАЛИЗАЦИИ БИОЛЮМИНЕСЦЕНЦИИ IN VIVO | 2010 |
|
RU2601128C2 |
| КОМПОЗИЦИЯ И СПОСОБ ЛЕЧЕНИЯ АУТОИММУННОГО ЗАБОЛЕВАНИЯ | 2012 |
|
RU2621129C2 |
| СПОСОБЫ И ЛЕЧЕНИЕ ОПРЕДЕЛЕННЫХ НАРУШЕНИЙ НА ОСНОВЕ ДЕМИЕЛИНИЗАЦИИ И ДИСМИЕЛИНИЗАЦИИ И/ИЛИ СТИМУЛЯЦИИ РЕМИЕЛИНИЗАЦИИ | 2014 |
|
RU2686677C2 |
| НОВОЕ ЛЕЧЕНИЕ РАССЕЯННОГО СКЛЕРОЗА ( РС ) | 2011 |
|
RU2595861C2 |
| ЛЕЧЕНИЕ РАССЕЯННОГО СКЛЕРОЗА | 2010 |
|
RU2539034C2 |
| Генно-клеточный везикулярный терапевтический препарат и способ терапии рассеянного склероза посредством трансплантации генно-клеточного везикулярного терапевтического препарата | 2021 |
|
RU2762855C1 |
| ЛИПОСОМЫ, СОДЕРЖАЩИЕ ОЛИГОПЕПТИДНЫЕ ФРАГМЕНТЫ ОСНОВНОГО БЕЛКА МИЕЛИНА, ФАРМАЦЕВТИЧЕСКИЙ СОСТАВ И СПОСОБ ЛЕЧЕНИЯ РАССЕЯННОГО СКЛЕРОЗА | 2013 |
|
RU2639497C2 |
| ПРОИЗВОДНЫЕ СОБЕТИРОМА | 2017 |
|
RU2776372C2 |
| Лекарственная комбинация для лечения рассеянного склероза | 2024 |
|
RU2828047C1 |
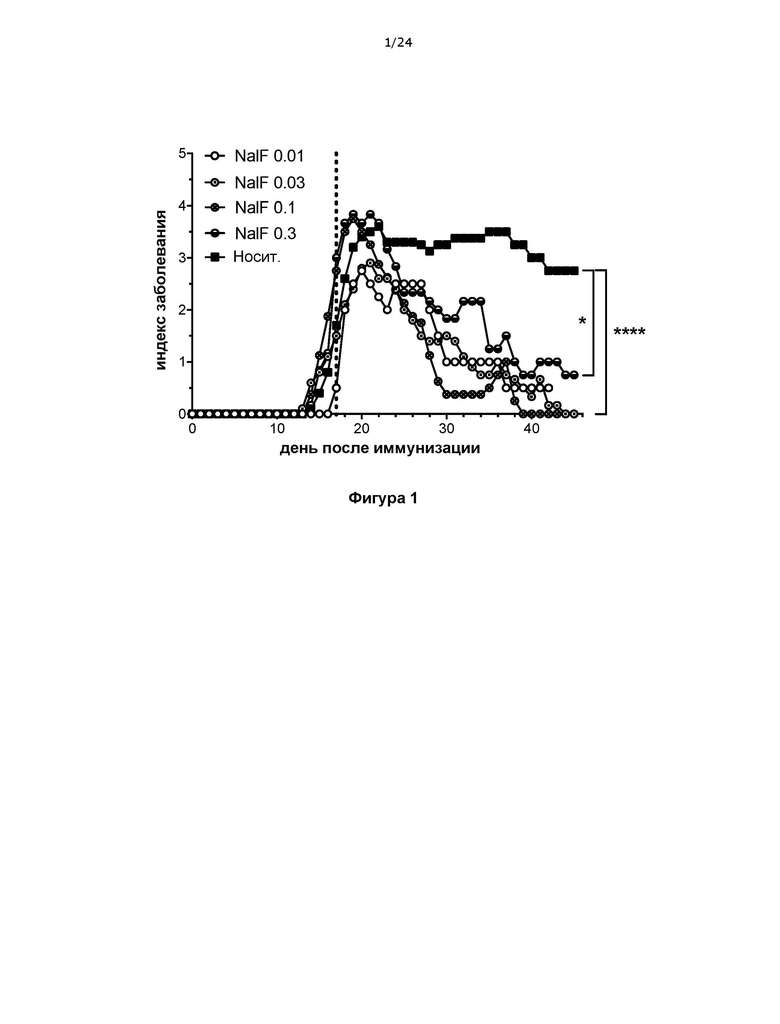
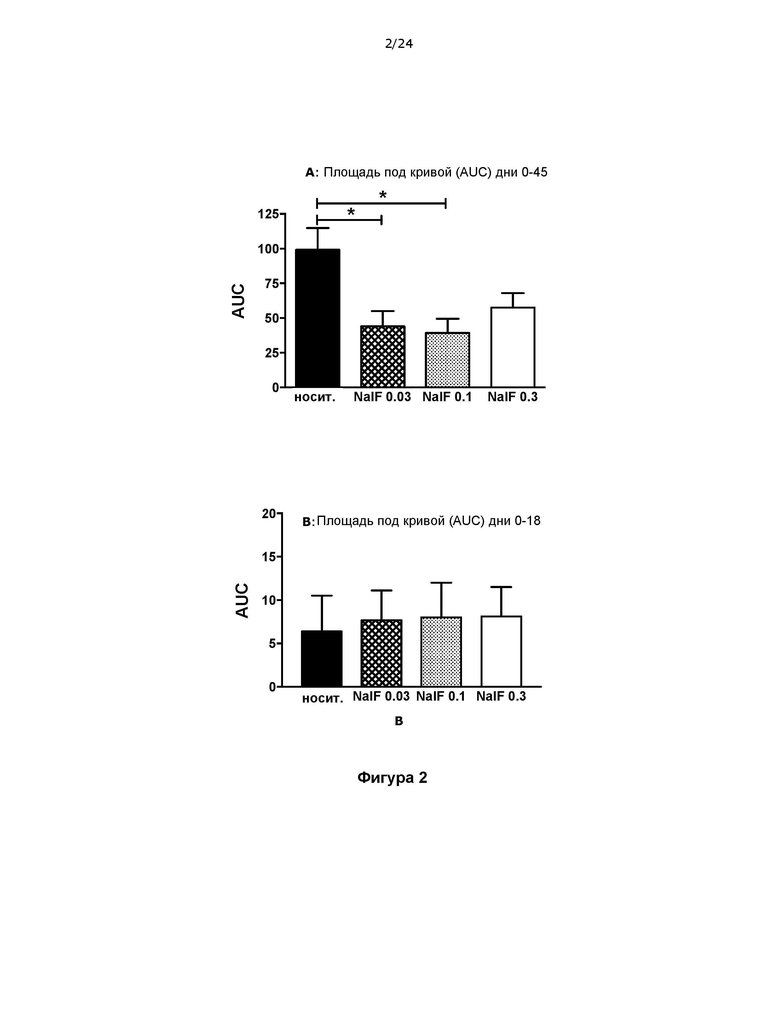
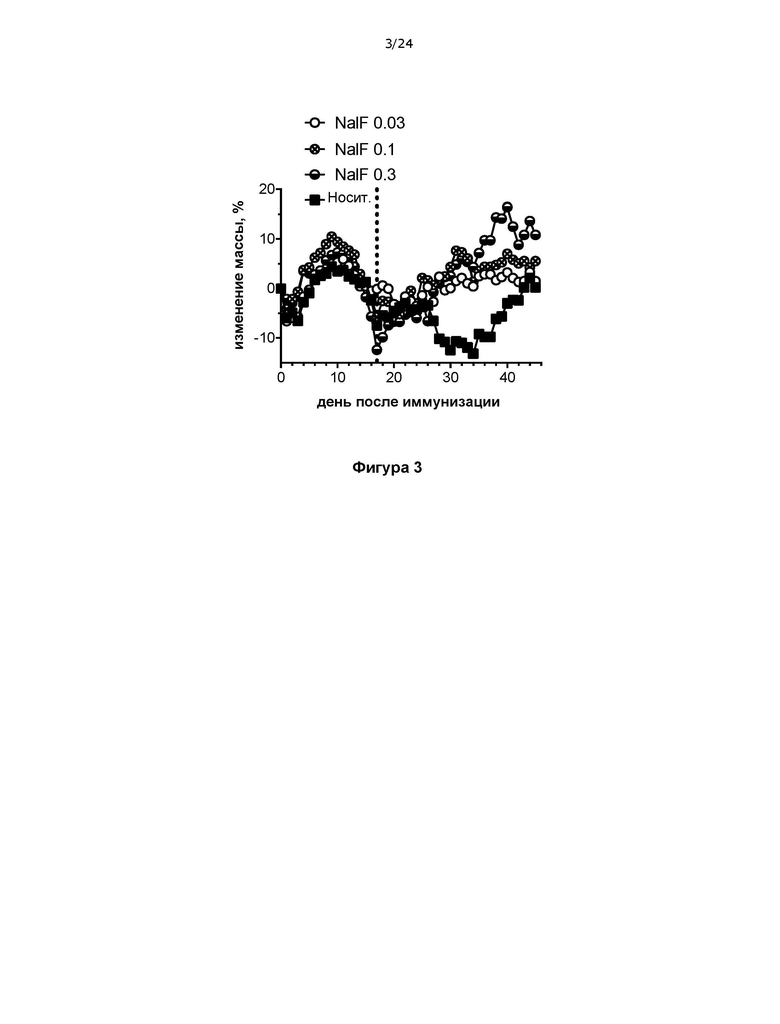
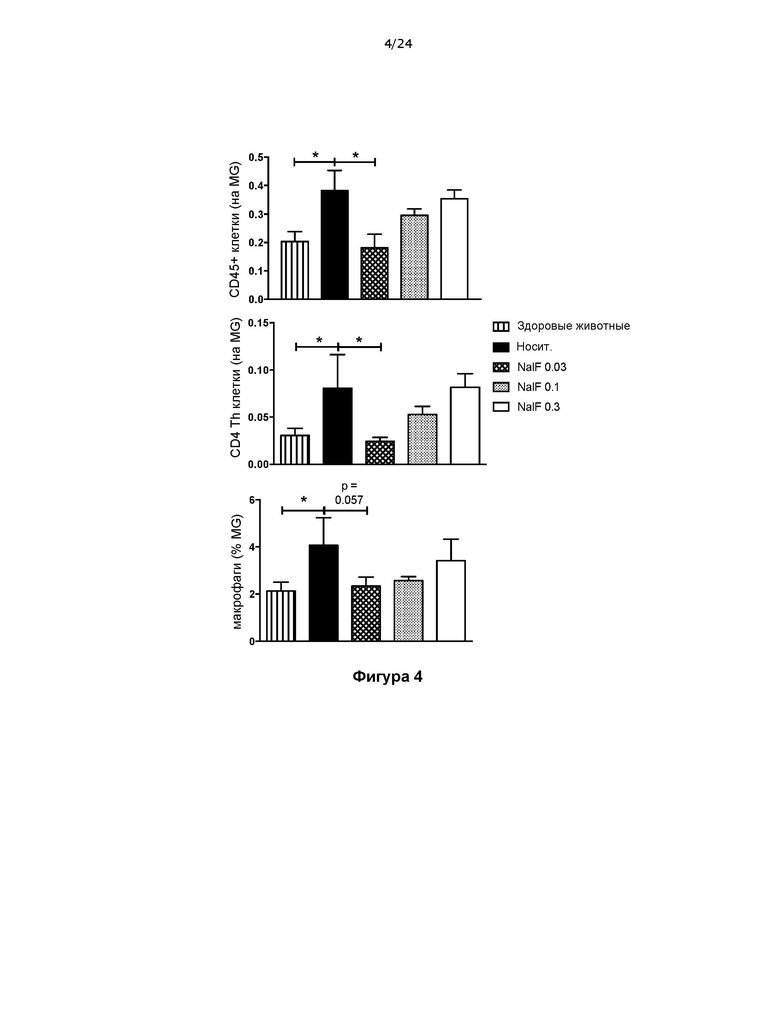

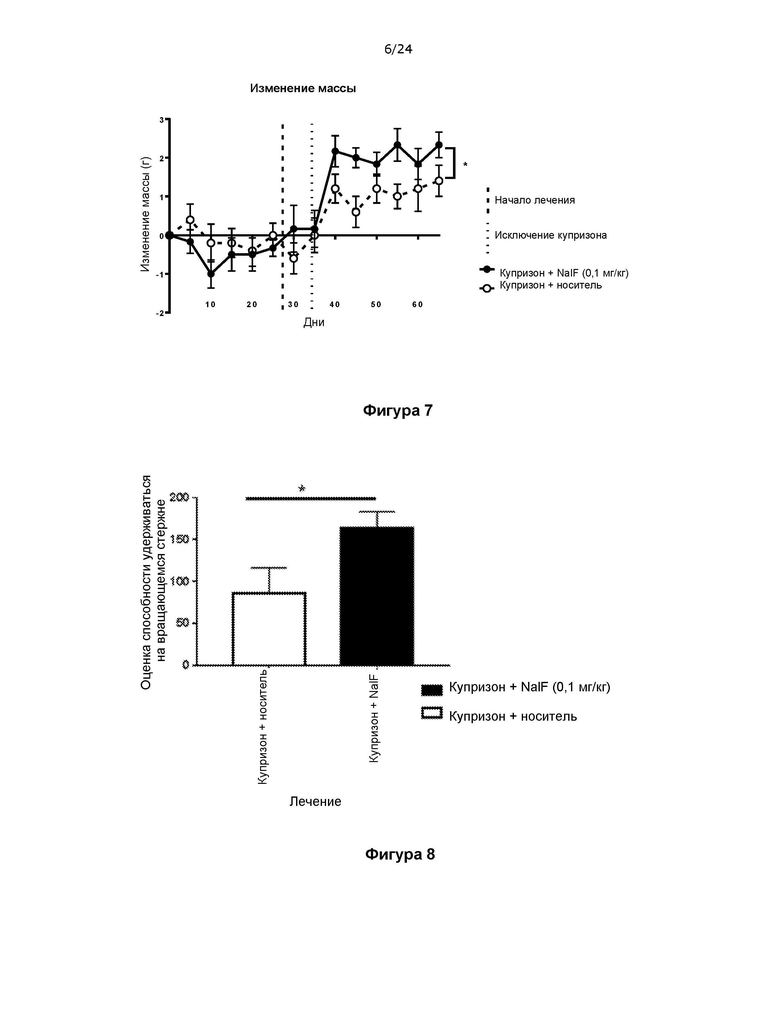
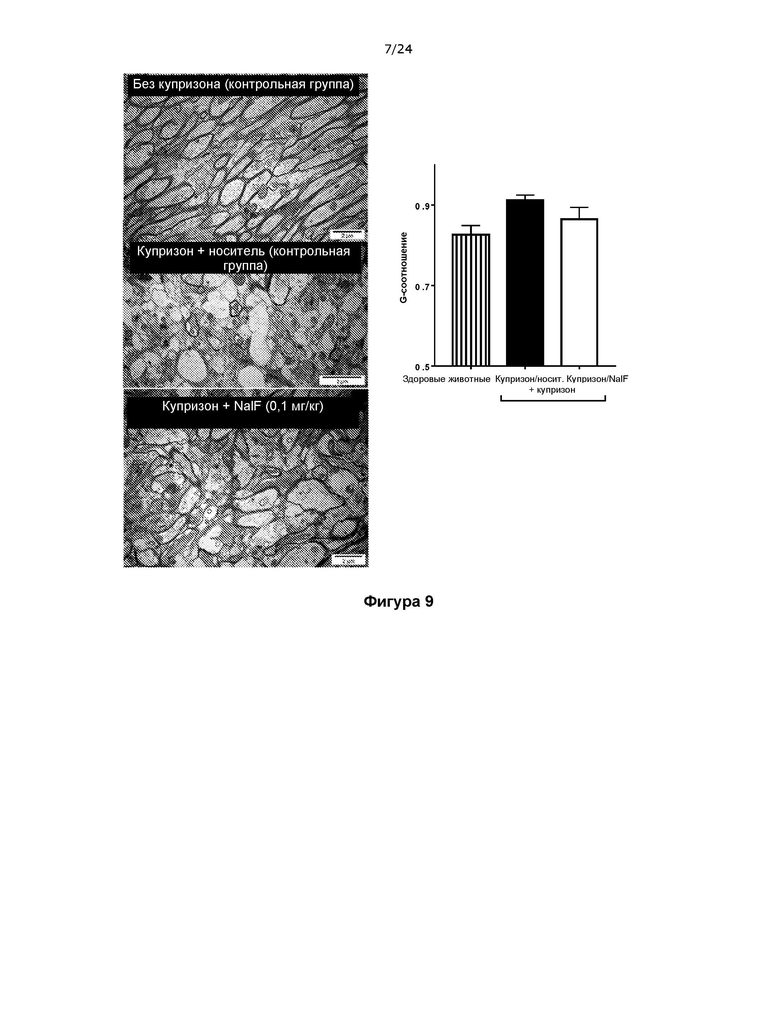
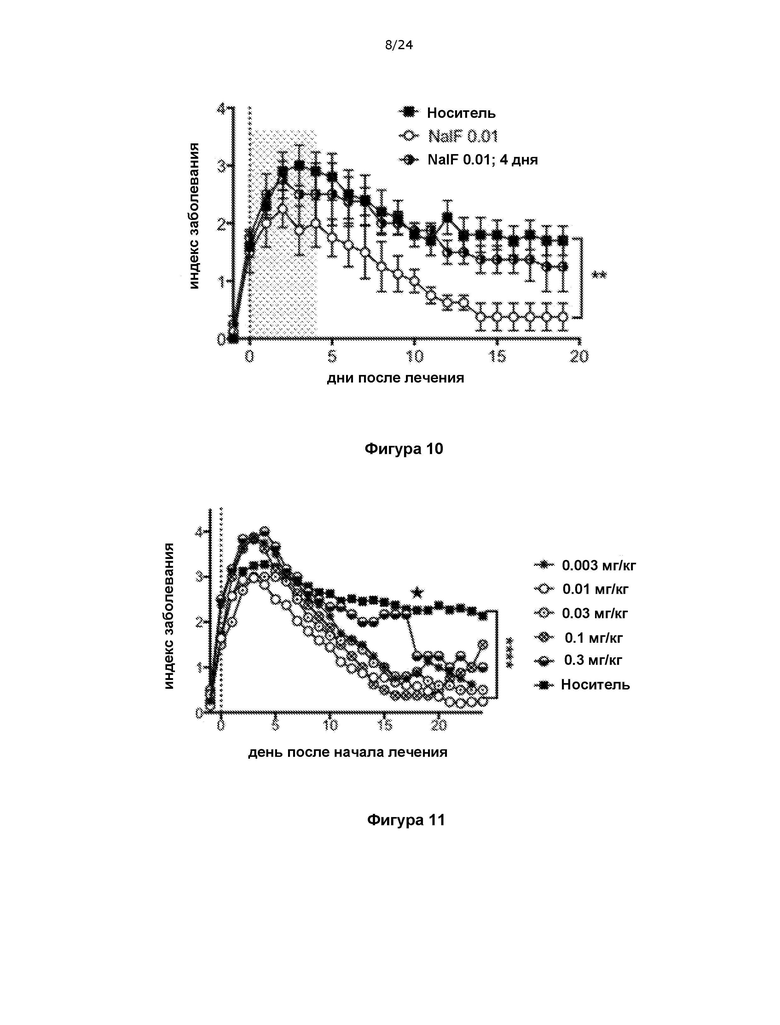
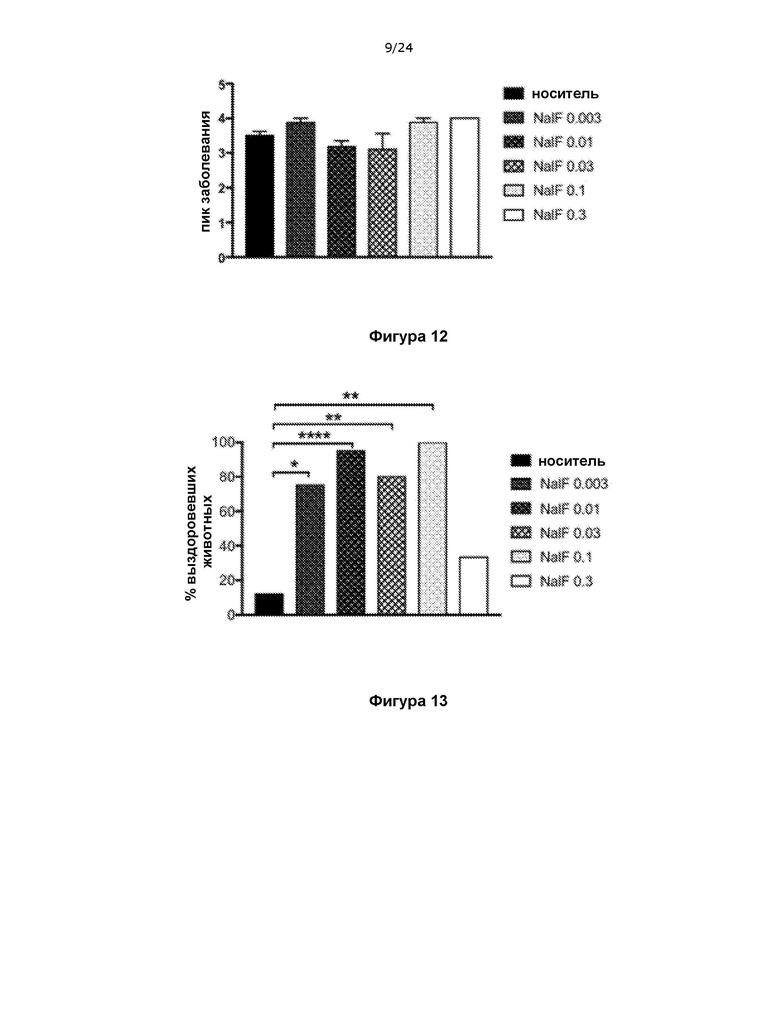
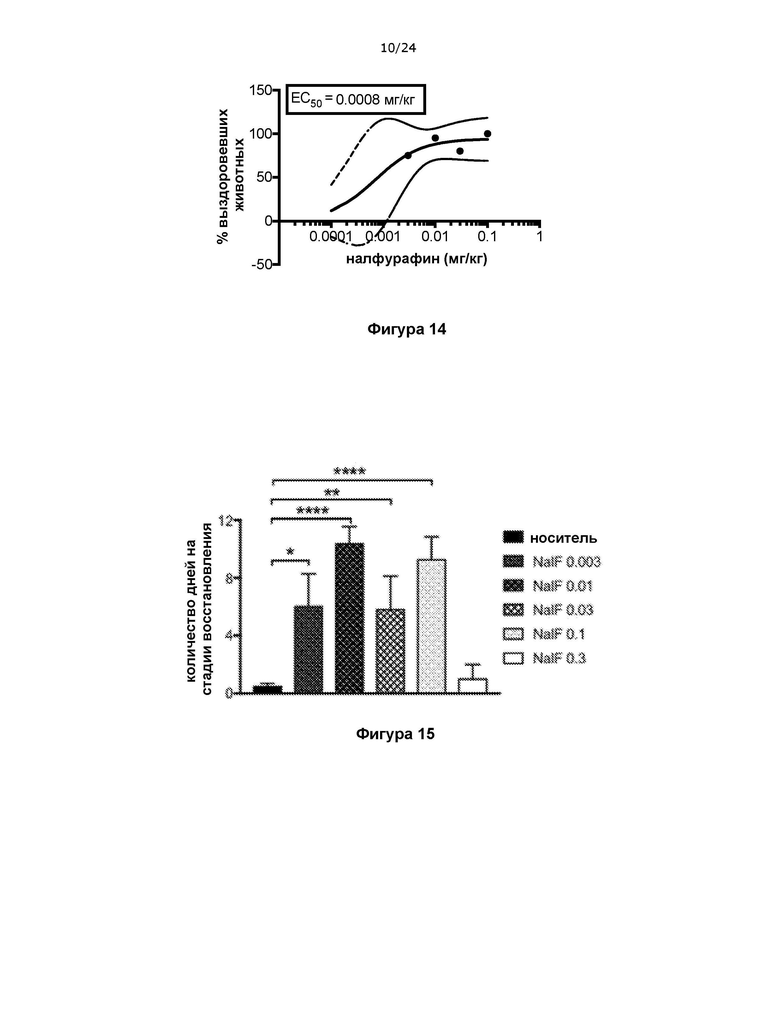
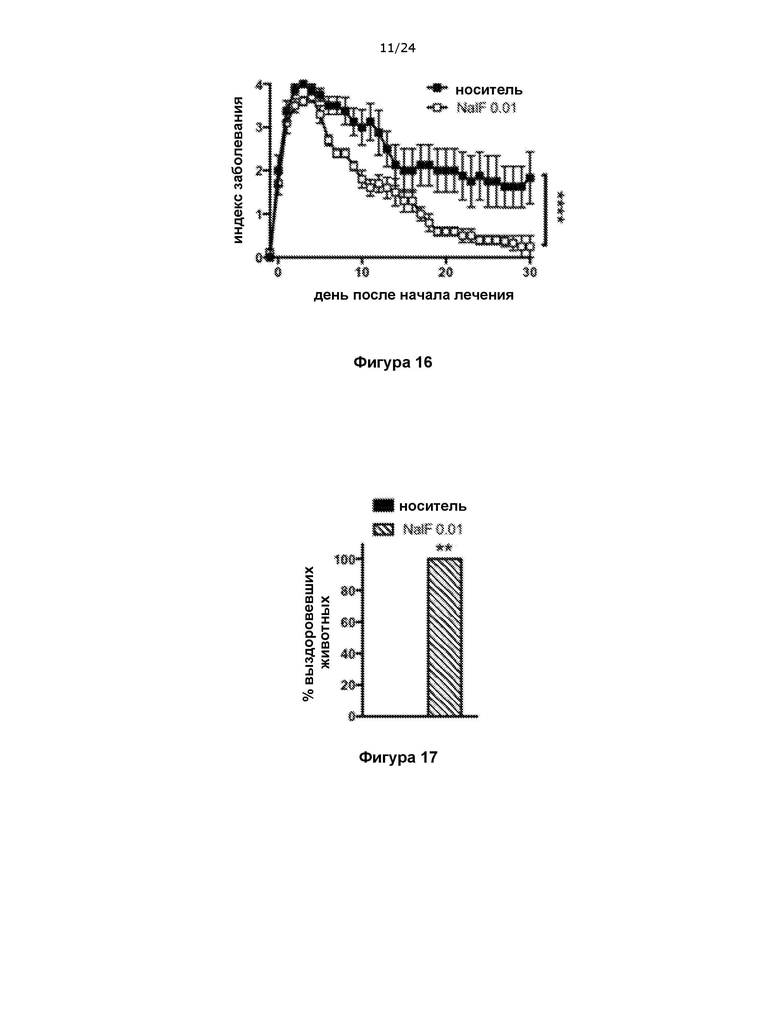

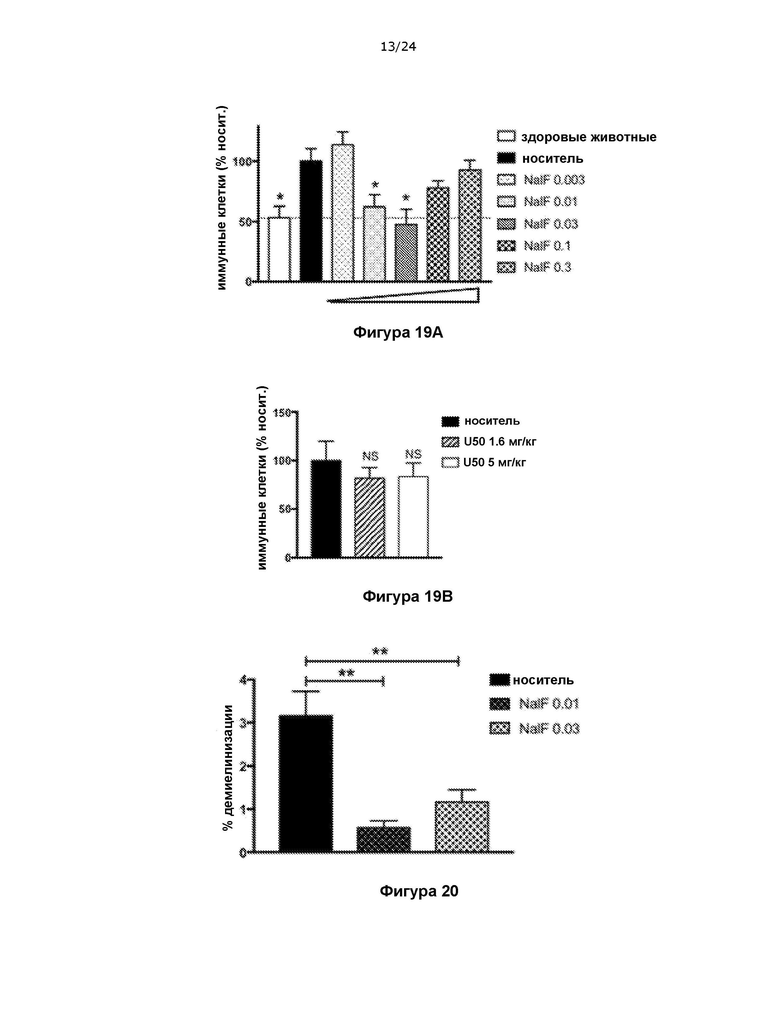
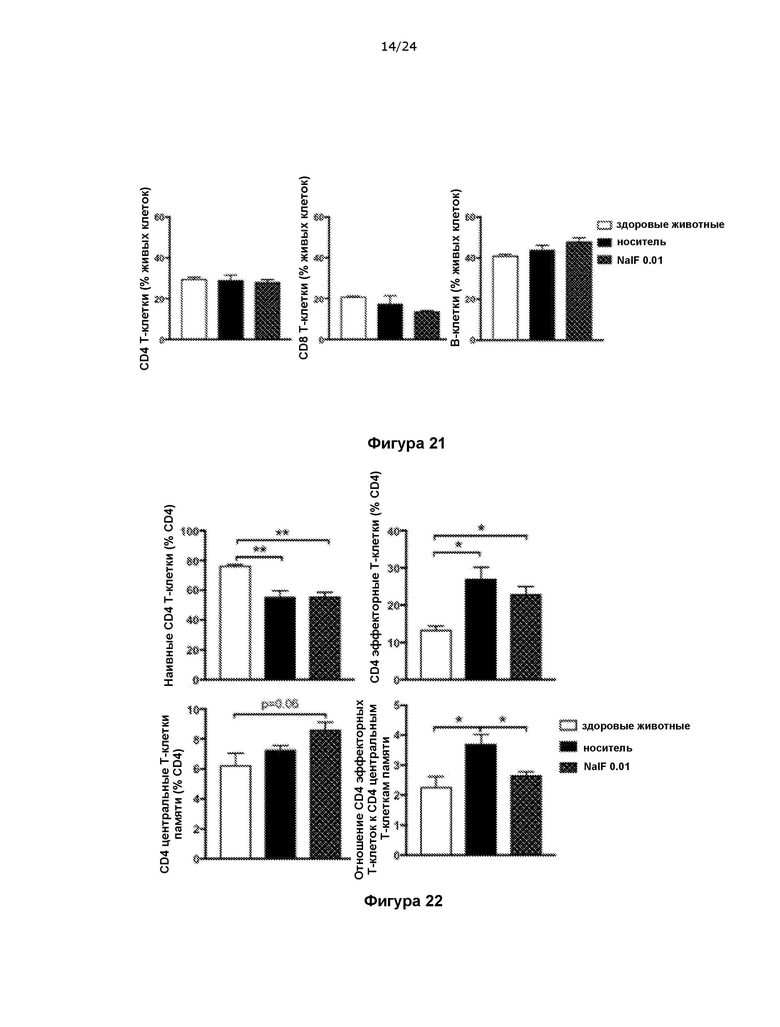
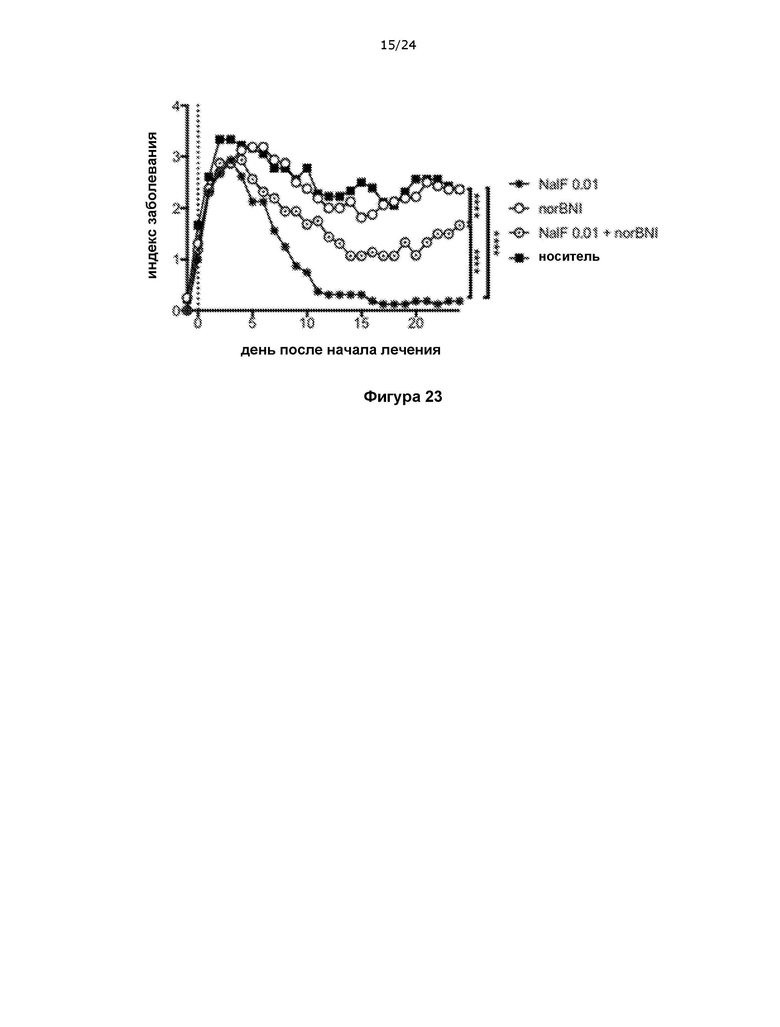
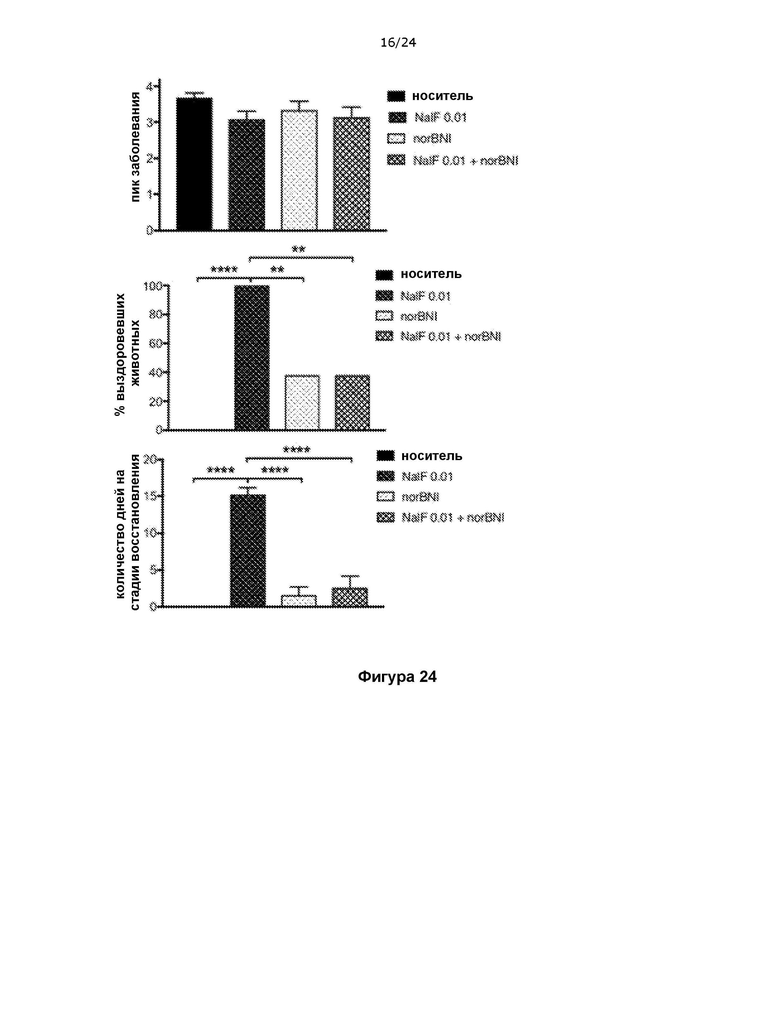

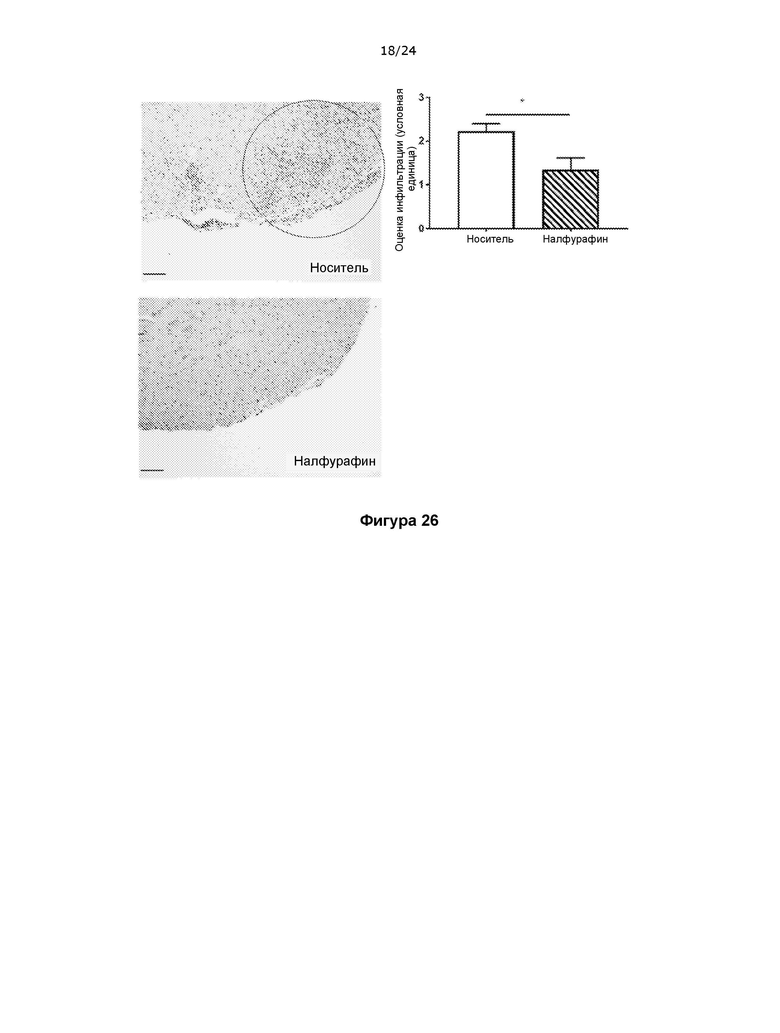
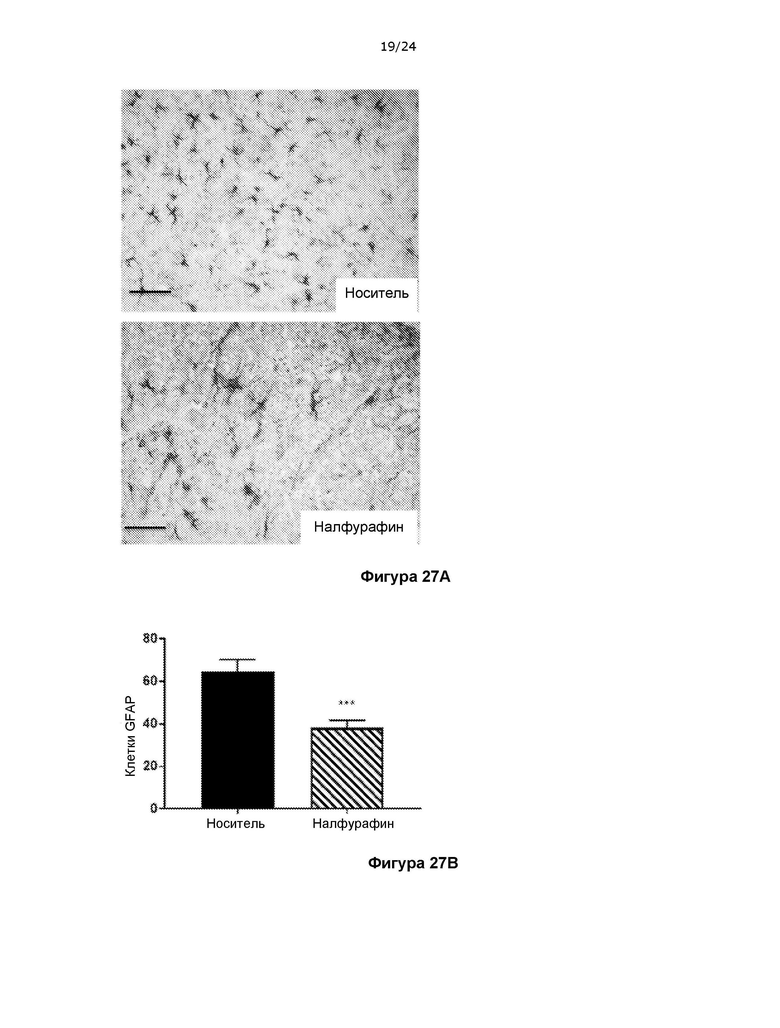
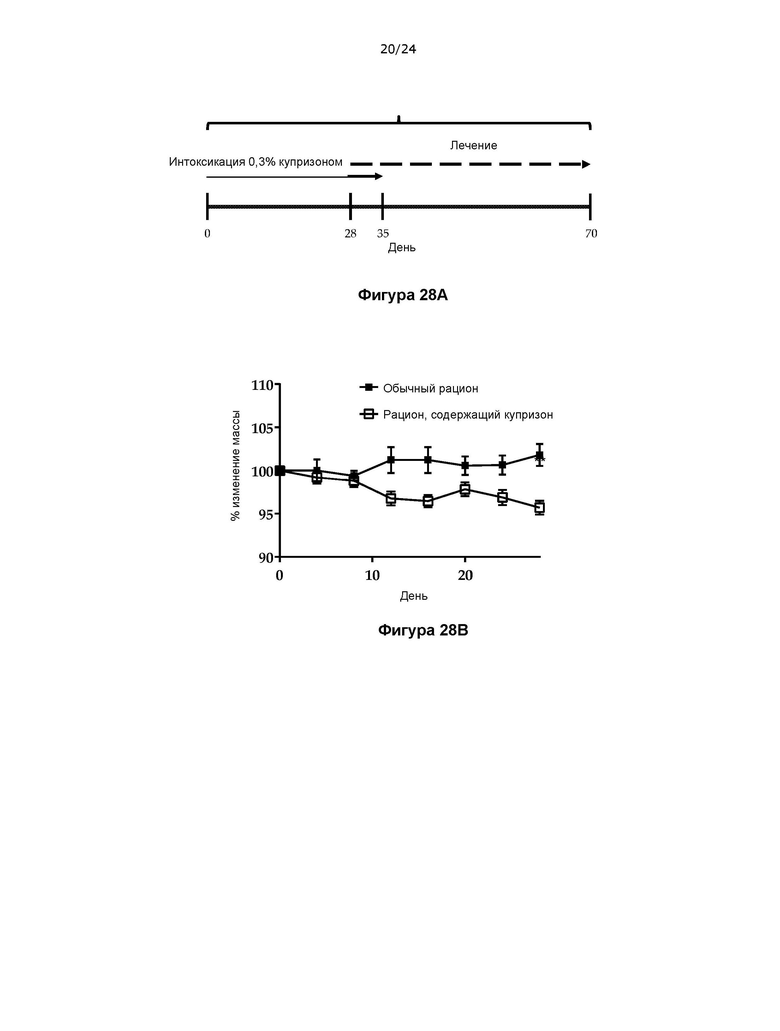
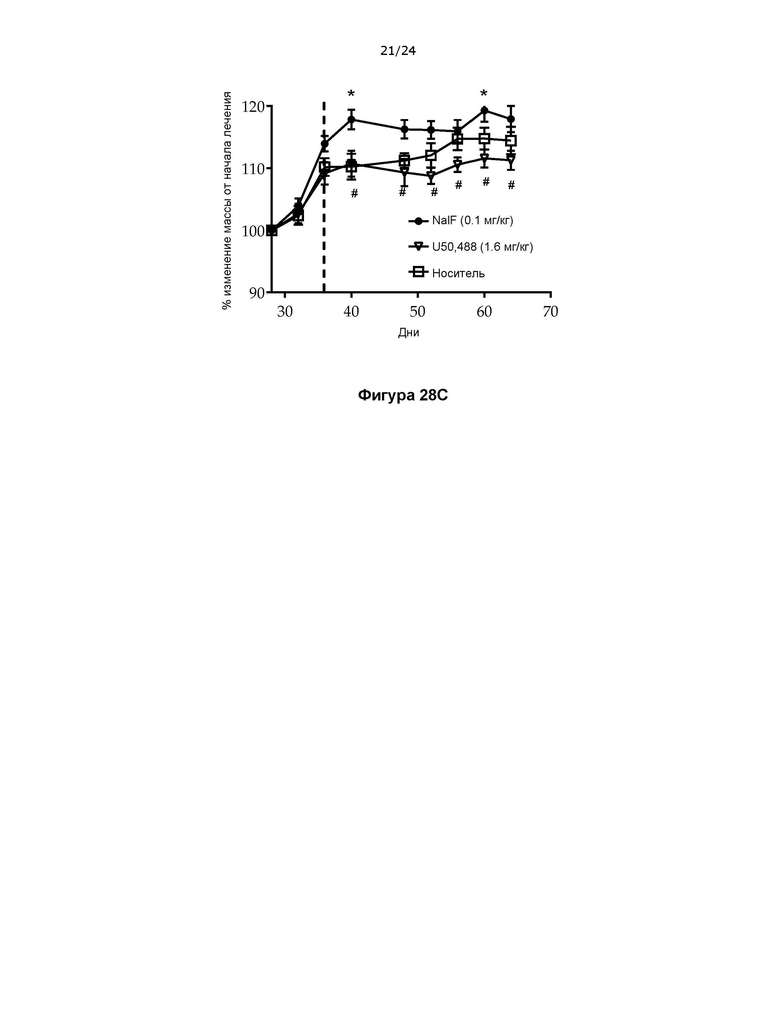

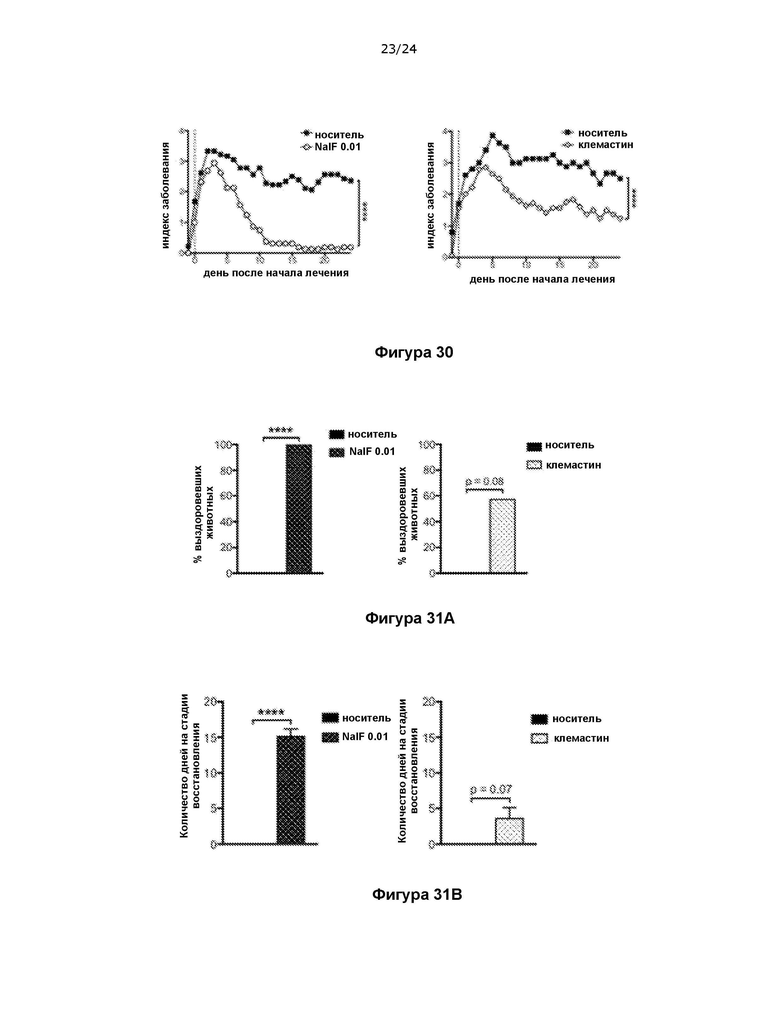
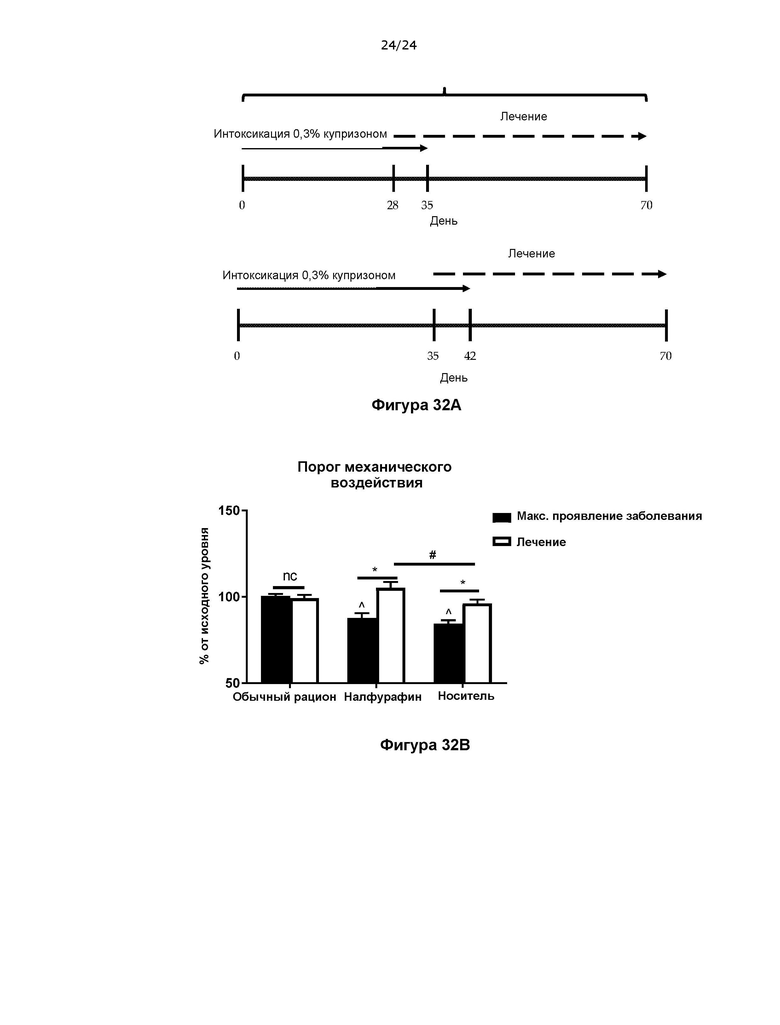
Группа изобретений относится к области медицины, а именно к терапии и неврологии, и предназначена для лечения и/или предотвращения демиелинизирующего заболевания у субъекта. Применяют фармацевтическую композицию, содержащую налфурафин, для (i) лечения демиелинизирующего заболевания у субъекта, (ii) увеличения ремиелинизации нервов у субъекта или (iii) ослабления демиелинизации нервов у субъекта. Также представлен способ (i) лечения демиелинизирующего заболевания у субъекта, (ii) увеличения ремиелинизации нервов у субъекта или (iii) ослабления демиелинизации нервов у субъекта, включающий введение субъекту фармацевтической композиции, содержащей налфурафин. В другом воплощении раскрывается применение налфурафина для приготовления фармацевтической композиции для (i) лечения демиелинизирующего заболевания у субъекта, (ii) увеличения ремиелинизации нервов у субъекта или (iii) ослабления демиелинизации нервов у субъекта. Использование группы изобретений обеспечивает эффективное лечение демиелинизирующего заболевания у субъекта, а также позволяет увеличить ремиелинизацию нервов у субъекта или ослабить демиелинизацию нервов у субъекта. 3 н. и 15 з.п. ф-лы, 32 ил., 1 табл., 32 пр.
1. Применение фармацевтической композиции, содержащей налфурафин, для (i) лечения демиелинизирующего заболевания у субъекта, (ii) увеличения ремиелинизации нервов у субъекта или (iii) ослабления демиелинизации нервов у субъекта.
2. Применение по п. 1, отличающееся тем, что указанную фармацевтическую композицию вводят субъекту в течение периода (i) по меньшей мере 7 дней, (ii) по меньшей мере 14 дней или (iii) по меньшей мере одного месяца.
3. Применение по п. 1, отличающееся тем, что указанную фармацевтическую композицию вводят субъекту для обеспечения дозы налфурафина от примерно 0,1 до примерно 10,0 мкг в сутки.
4. Применение по п. 1, отличающееся тем, что указанную фармацевтическую композицию вводят субъекту для обеспечения дозы налфурафина, эквивалентной дозе налфурафина от примерно 0,003 до примерно 0,3 мг/кг при введении мышам.
5. Применение по любому из пп. 1-4, отличающееся тем, что субъект имеет один или более симптомов демиелинизирующего заболевания, выбранного из группы, состоящей из рассеянного склероза (РС), неврита зрительного нерва, болезни Девика, воспалительных демиелинизирующих заболеваний, нейропатий центральной нервной системы, миелопатий, сухотки спинного мозга, лейкоэнцефалопатий, лейкодистрофий, синдрома Гийена-Барре и его хронического аналога, хронической воспалительной демиелинизирующей полинейропатии, анти-MAG (миелин-ассоциированный гликопротеин) периферической нейропатии, болезни Шарко-Мари-Тута (CMT), дефицита меди, прогрессирующей воспалительной нейропатии и любой их комбинации.
6. Применение по п. 5, отличающееся тем, что введение субъекту указанной фармацевтической композиции приводит к
(i) одному или более клиническим результатам, выбранным из группы, состоящей из:
уменьшения или замедления демиелинизации нервных клеток;
заживления поврежденной нервной ткани;
увеличения ремиелинизации демиелинизированных нервов в центральной нервной системе субъекта;
нейропротекции;
защиты поврежденной нервной ткани от дальнейшей активности заболевания;
стимулирования удлинения нейронов в центральной нервной системе субъекта;
и/или
(ii) одному или более клиническим результатам, выбранным из группы, состоящей из:
улучшения функции нервной системы;
уменьшения прогрессирования демиелинизирующего заболевания;
уменьшения тяжести демиелинизирующего заболевания;
уменьшения частоты или тяжести приступов рецидивирующего демиелинизирующего заболевания;
уменьшения проявления инвалидизации, вызванной демиелинизирующим заболеванием;
уменьшения клинических симптомов демиелинизирующего заболевания;
уменьшения паралича;
улучшения равновесия или координации;
повышенной скорости ремиссии;
и/или
(iii) уменьшению одного или более клинических симптомов, выбранных из группы, состоящей из:
потери чувствительности, мышечной слабости, нарушения ходьбы, нарушения функции рук, выраженных рефлексов, мышечных спазмов, затруднения при движении, атаксии, спастичности, проблем с речью или глотанием, проблем со зрением, утомляемости, острой или хронической боли, лицевой боли, недержания мочи, снижения когнитивных способностей, депрессии, тревоги, сексуальной дисфункции, феномена Утхоффа и симптома Лермитта.
7. Способ (i) лечения демиелинизирующего заболевания у субъекта, (ii) увеличения ремиелинизации нервов у субъекта или (iii) ослабления демиелинизации нервов у субъекта, включающий введение субъекту фармацевтической композиции, содержащей налфурафин.
8. Способ по п. 7, в котором указанную фармацевтическую композицию вводят субъекту в течение периода (i) по меньшей мере 7 дней, (ii) по меньшей мере 14 дней или (iii) по меньшей мере одного месяца.
9. Способ по п. 7, в котором указанную фармацевтическую композицию вводят субъекту для обеспечения дозы налфурафина от примерно 0,1 до примерно 10,0 мкг в сутки.
10. Способ по п. 7, в котором указанную фармацевтическую композицию вводят субъекту для обеспечения дозы налфурафина, эквивалентной дозе налфурафина от примерно 0,003 до примерно 0,3 мг/кг при введении мышам.
11. Способ по любому из пп. 7-10, в котором субъект имеет один или более симптомов демиелинизирующего заболевания, выбранного из группы, состоящей из рассеянного склероза (РС), неврита зрительного нерва, болезни Девика, воспалительных демиелинизирующих заболеваний, нейропатий центральной нервной системы, миелопатий, сухотки спинного мозга, лейкоэнцефалопатий, лейкодистрофий, синдрома Гийена-Барре и его хронического аналога, хронической воспалительной демиелинизирующей полинейропатии, анти-MAG (миелин-ассоциированный гликопротеин) периферической нейропатии, болезни Шарко-Мари-Тута (CMT), дефицита меди, прогрессирующей воспалительной нейропатии и любой их комбинации.
12. Способ по п. 11, в котором введение субъекту указанной фармацевтической композиции приводит к
(i) одному или более клиническим результатам, выбранным из группы, состоящей из:
уменьшения или замедления демиелинизации нервных клеток;
заживления поврежденной нервной ткани;
увеличения ремиелинизации демиелинизированных нервов в центральной нервной системе субъекта;
нейропротекции;
защиты поврежденной нервной ткани от дальнейшей активности заболевания;
стимулирования удлинения нейронов в центральной нервной системе субъекта;
улучшения функции нервной системы;
и/или
(ii) одному или более клиническим результатам, выбранным из группы, состоящей из:
уменьшения прогрессирования демиелинизирующего заболевания;
уменьшения тяжести демиелинизирующего заболевания;
уменьшения частоты или тяжести приступов рецидивирующего демиелинизирующего заболевания;
уменьшения проявления инвалидизации, вызванной демиелинизирующим заболеванием;
уменьшения клинических симптомов демиелинизирующего заболевания;
уменьшения паралича;
улучшения равновесия или координации; и
повышенной скорости ремиссии;
и/или
(iii) уменьшению одного или более клинических симптомов, выбранных из группы, состоящей из:
потери чувствительности, мышечной слабости, нарушения ходьбы, нарушения функции рук, выраженных рефлексов, мышечных спазмов, затруднения при движении, атаксии, спастичности, проблем с речью или глотанием, проблем со зрением, утомляемости, острой или хронической боли, лицевой боли, недержания мочи, снижения когнитивных способностей, депрессии, тревоги, сексуальной дисфункции, феномена Утхоффа и симптома Лермитта.
13. Применение налфурафина для приготовления фармацевтической композиции для (i) лечения демиелинизирующего заболевания у субъекта, (ii) увеличения ремиелинизации нервов у субъекта или (iii) ослабления демиелинизации нервов у субъекта.
14. Применение по п. 13, отличающееся тем, что указанную фармацевтическую композицию вводят субъекту в течение периода (i) по меньшей мере 7 дней, (ii) по меньшей мере 14 дней или (iii) по меньшей мере одного месяца.
15. Применение по п. 13, отличающееся тем, что указанную фармацевтическую композицию вводят субъекту для обеспечения дозы налфурафина от примерно 0,1 до примерно 10,0 мкг в сутки.
16. Применение по п. 13, отличающееся тем, что указанную фармацевтическую композицию вводят субъекту для обеспечения дозы налфурафина, эквивалентной дозе налфурафина от примерно 0,003 до примерно 0,3 мг/кг при введении мышам.
17. Применение по любому из пп. 13-16, отличающееся тем, что субъект имеет один или более симптомов демиелинизирующего заболевания, выбранного из группы, состоящей из рассеянного склероза (РС), неврита зрительного нерва, болезни Девика, воспалительных демиелинизирующих заболеваний, нейропатий центральной нервной системы, миелопатий, сухотки спинного мозга, лейкоэнцефалопатий, лейкодистрофий, синдрома Гийена-Барре и его хронического аналога, хронической воспалительной демиелинизирующей полинейропатии, анти-MAG (миелин-ассоциированный гликопротеин) периферической нейропатии, болезни Шарко-Мари-Тута (CMT), дефицита меди, прогрессирующей воспалительной нейропатии и любой их комбинации.
18. Применение по п. 17, отличающееся тем, что введение субъекту указанной фармацевтической композиции приводит к
(i) одному или более клиническим результатам, выбранным из группы, состоящей из:
уменьшения или замедления демиелинизации нервных клеток;
заживления поврежденной нервной ткани;
увеличения ремиелинизации демиелинизированных нервов в центральной нервной системе субъекта;
нейропротекции;
защиты поврежденной нервной ткани от дальнейшей активности заболевания;
стимулирования удлинения нейронов в центральной нервной системе субъекта;
улучшения функции нервной системы;
и/или
(ii) одному или более клиническим результатам, выбранным из группы, состоящей из:
уменьшения прогрессирования демиелинизирующего заболевания;
уменьшения тяжести демиелинизирующего заболевания;
уменьшения частоты или тяжести приступов рецидивирующего демиелинизирующего заболевания;
уменьшения проявления инвалидизации, вызванной демиелинизирующим заболеванием;
уменьшения клинических симптомов демиелинизирующего заболевания;
уменьшения паралича;
улучшения равновесия или координации; и
повышенной скорости ремиссии;
и/или
(iii) уменьшению одного или более клинических симптомов, выбранных из группы, состоящей из:
потери чувствительности, мышечной слабости, нарушения ходьбы, нарушения функции рук, выраженных рефлексов, мышечных спазмов, затруднения при движении, атаксии, спастичности, проблем с речью или глотанием, проблем со зрением, утомляемости, острой или хронической боли, лицевой боли, недержания мочи, снижения когнитивных способностей, депрессии, тревоги, сексуальной дисфункции, феномена Утхоффа и симптома Лермитта.
| JP 2015168630 A, 28.09.2015 | |||
| WO 2013112859 A1, 01.08.2013 | |||
| WO 2017049252 A1, 23.03.2017 | |||
| WO 2017220431 A1, 28.12.2017 | |||
| BORNIGER JC et al | |||
| Enhancing Remyelination through a Novel Opioid-Receptor Pathway | |||
| J Neurosci., 2016, 36(47): 11831-11833 | |||
| MEI F et al | |||
| Identification of the Kappa-Opioid Receptor as a Therapeutic Target for Oligodendrocyte |
Авторы
Даты
2023-10-11—Публикация
2019-03-07—Подача