ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
Настоящая заявка испрашивает приоритет по предварительной заявке на патент США № 62/450017, поданной 24 января 2017 г., и предварительной заявке на патент США № 62/583736, поданной 9 ноября 2017 г., содержание которых включено в данный документ посредством ссылки в полном объеме.
УРОВЕНЬ ТЕХНИКИ
Некоторые беспозвоночные, такие как нематоды и членистоногие (например, насекомые, например, европейские медоносные пчелы (Apis mellifera) или шелкопряды (Bombyx mori)), используются в сельском хозяйстве в программах опыления и для контроля вредителей, а также в коммерческих целях для производства коммерческих продуктов, таких как мед или шелк. Для культивирования полезных нематод и членистоногих с целью применения в сельскохозяйственной или коммерческой промышленности в данной области техники существует потребность в способах содействия росту и приспособленности полезных беспозвоночных.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В данном документе раскрыты композиции и способы для модулирования приспособленности беспозвоночных для целей сельского хозяйства или коммерческой деятельности. Композиция содержит средство, которое изменяет уровень, активность или метаболизм одного или нескольких микроорганизмов, обитающих в организме хозяина, при этом изменение приводит к модулированию приспособленности хозяина.
В одном аспекте в данном документе раскрыт способ повышения приспособленности медоносной пчелы, при этом способ включает введение медоносной пчеле композиции, содержащей эффективное количество бактерий, метаболизирующих фосфорорганические инсектициды, составленных с носителем, съедобным для насекомых.
В некоторых вариантах осуществления введение предусматривает доставку композиции в улей с медоносными пчелами или в по меньшей мере одну среду обитания, где медоносная пчела растет, живет, размножается или питается.
В некоторых вариантах осуществления композиция может быть жидкой, твердой, аэрозольной, пастообразной, гелеобразной или газообразной.
В некоторых вариантах осуществления фосфорорганический инсектицид может представлять собой фенитротион.
В определенных вариантах осуществления носитель может представлять собой средство для нанесения покрытия на семена.
В некоторых вариантах осуществления медоносная пчела может находиться в колонии медоносных пчел.
В другом аспекте в данном документе предусмотрена композиция, содержащая эффективное количество бактерий, метаболизирующих фосфорорганические инсектициды, составленных с носителем, съедобным для насекомых, в виде жидкости, твердого вещества, аэрозоля, пасты, геля или газа.
В некоторых вариантах осуществления второго аспекта бактерии, метаболизирующие фосфорорганические инсектициды, метаболизируют фенитротион.
В некоторых вариантах осуществления второго аспекта носитель представляет собой средство для нанесения покрытия на семена.
В некоторых вариантах осуществления второго аспекта бактерии, метаболизирующие фосфорорганические инсектициды, присутствуют в концентрации по меньшей мере 100000 клеток/мл (например, по меньшей мере приблизительно 100000 клеток/мл, по меньшей мере приблизительно 150000 клеток/мл, по меньшей мере приблизительно 200000 клеток/мл, по меньшей мере приблизительно 250000 клеток/мл, по меньшей мере приблизительно 300000 клеток/мл, по меньшей мере приблизительно 350000 клеток/мл, по меньшей мере приблизительно 400000 клеток/мл, по меньшей мере приблизительно 450000 клеток/мл или по меньшей мере приблизительно 500000 клеток/мл).
В еще одном аспекте композиция содержит средство, которое изменяет уровень, активность или метаболизм одного или нескольких микроорганизмов, обитающих в организме насекомого-хозяина, при этом изменение приводит к повышению приспособленности насекомого-хозяина.
В другом случае композиция содержит средство, которое изменяет уровень, активность или метаболизм одного или нескольких микроорганизмов, обитающих в организме нематоды-хозяина, при этом изменение приводит к повышению приспособленности нематоды-хозяина.
В некоторых вариантах осуществления любой из вышеуказанных композиций один или несколько микроорганизмов могут представлять собой бактерию или гриб, обитающие в организме хозяина. В некоторых вариантах осуществления бактерия, обитающая в организме хозяина, представляет собой по меньшей мере одну бактерию, выбранную из группы, состоящей из Candidatus spp, Buchenera spp, Blattabacterium spp, Baumania spp, Wigglesworthia spp, Wolbachia spp, Rickettsia spp, Orientia spp, Sodalis spp, Burkholderia spp, Cupriavidus spp, Frankia spp, Snirhizobium spp, Streptococcus spp, Wolinella spp, Xylella spp, Erwinia spp, Agrobacterium spp, Bacillus spp, Paenibacillus spp, Streptomyces spp, Micrococcus spp, Corynebacterium spp, Acetobacter spp, Cyanobacteria spp, Salmonella spp, Rhodococcus spp, Pseudomonas spp, Lactobacillus spp, Enterococcus spp, Alcaligenes spp, Klebsiella spp, Paenibacillus spp, Arthrobacter spp, Corynebacterium spp, Brevibacterium spp, Thermus spp, Pseudomonas spp, Clostridium spp и Escherichia spp. В некоторых вариантах осуществления гриб, обитающий в организме хозяина, представляет собой по меньшей мере один гриб, выбранный из группы, состоящей из Candida, Metschnikowia, Debaromyces, Starmerella, Pichia, Cryptococcus, Pseudozyma, Symbiotaphrina bucneri, Symbiotaphrina kochii, Scheffersomyces shehatae, Scheffersomyces stipites, Cryptococcus, Trichosporon, Amylostereum areolatum, Epichloe spp, Pichia pinus, Hansenula capsulate, Daldinia decipien, Ceratocytis spp, Ophiostoma spp и Attamyces bromatificus.
В любой из вышеуказанных композиций средство, которое далее в данном документе также может называться модулирующим средством, может изменять рост, деление, жизнеспособность, метаболизм и/или продолжительность жизни микроорганизма, обитающего в организме хозяина. В любом из вышеуказанных вариантов осуществления модулирующее средство может снижать жизнеспособность одного или нескольких микроорганизмов, обитающих в организме хозяина. В некоторых вариантах осуществления модулирующее средство повышает темпы роста или жизнеспособность одного или нескольких микроорганизмов, обитающих в организме хозяина.
В любом из вышеуказанных вариантов осуществления модулирующее средство представляет собой фаг, полипептид, малую молекулу, антибиотик, бактерию или любую их комбинацию.
В некоторых вариантах осуществления фаг связывается с белком клеточной поверхности в бактерии, обитающей в организме хозяина. В некоторых вариантах осуществления фаг является вирулентным по отношению к бактерии, обитающей в организме хозяина. В некоторых вариантах осуществления фаг представляет собой по меньшей мере один фаг, выбранный из группы, состоящей из Myoviridae, Siphoviridae, Podoviridae, Lipothrixviridae, Rudiviridae, Ampullaviridae, Bicaudaviridae, Clavaviridae, Corticoviridae, Cystoviridae, Fuselloviridae, Gluboloviridae, Guttaviridae, Inoviridae, Leviviridae, Microviridae, Plasmaviridae и Tectiviridae.
В некоторых вариантах осуществления полипептид представляет собой по меньшей мере одно из бактериоцина, бактериоцина R-типа, C-богатого пептида клубеньков, противомикробного пептида, лизина или регуляторного пептида бактериоцитов.
В некоторых вариантах осуществления малая молекула представляет собой метаболит.
В некоторых вариантах осуществления антибиотик представляет собой антибиотик широкого спектра действия.
В некоторых вариантах осуществления модулирующее средство представляет собой встречающуюся в природе бактерию. В некоторых вариантах осуществления бактерия представляет собой по меньшей мере одну бактерию, выбранную из группы, состоящей из Bartonella apis, Parasaccharibacter apium, Frischella perrara, Snodgrassella alvi, Gilliamela apicola, Bifidobacterium spp и Lactobacillus spp. В некоторых вариантах осуществления бактерия представляет собой по меньшей мере одну бактерию, выбранную из группы, состоящей из Candidatus spp, Buchenera spp, Blattabacterium spp, Baumania spp, Wigglesworthia spp, Wolbachia spp, Rickettsia spp, Orientia spp, Sodalis spp, Burkholderia spp, Cupriavidus spp, Frankia spp, Snirhizobium spp, Streptococcus spp, Wolinella spp, Xylella spp, Erwinia spp, Agrobacterium spp, Bacillus spp, Paenibacillus spp, Streptomyces spp, Micrococcus spp, Corynebacterium spp, Acetobacter spp, Cyanobacteria spp, Salmonella spp, Rhodococcus spp, Pseudomonas spp, Lactobacillus spp, Enterococcus spp, Alcaligenes spp, Klebsiella spp, Paenibacillus spp, Arthrobacter spp, Corynebacterium spp, Brevibacterium spp, Thermus spp, Pseudomonas spp, Clostridium spp и Escherichia spp. В определенных случаях бактерия представляет собой встречающуюся в природе бактерию, которая способна расщеплять пестициды, такие как фосфорорганические инсектициды (например, тиофосфатные инсектициды, например, фенитротион).
В любой из вышеуказанных композиций приспособленность хозяина может быть измерена по выживаемости, размножению или метаболизму хозяина. В некоторых вариантах осуществления модулирующее средство модулирует приспособленность хозяина путем снижения восприимчивости хозяина к пестицидам (например, восприимчивости к пестициду, приведенному в таблице 12). В некоторых вариантах осуществления восприимчивость к пестицидам представляет собой восприимчивость к бактерицидам или фунгицидам. В некоторых вариантах осуществления восприимчивость к пестицидам представляет собой восприимчивость к инсектицидам или нематоцидам.
В любой из вышеуказанных композиций композиция может содержать множество различных модулирующих средств. В некоторых вариантах осуществления композиция содержит модулирующее средство и пестицидное средство (например, пестицид, приведенный в таблице 12). В некоторых вариантах осуществления пестицидное средство представляет собой бактерицидное или фунгицидное средство. В некоторых вариантах осуществления пестицидное средство представляет собой инсектицидное или нематоцидное средство.
В любой из вышеуказанных композиций композиция может содержать модулирующее средство и средство, повышающее темпы роста сельскохозяйственной культуры.
В любой из вышеуказанных композиций модулирующее средство может быть связано со вторым фрагментом. В некоторых вариантах осуществления второй фрагмент представляет собой модулирующее средство.
В любой из вышеуказанных композиций модулирующее средство может быть связано с нацеливающим доменом. В некоторых вариантах осуществления нацеливающий домен нацеливает модулирующее средство на участок-мишень в организме хозяина. В некоторых вариантах осуществления нацеливающий домен нацеливает модулирующее средство на один или несколько микроорганизмов, обитающих в организме хозяина.
В любой из вышеуказанных композиций модулирующее средство может содержать инактивирующую пре- или пропоследовательность с образованием тем самым модулирующего средства-предшественника. В некоторых вариантах осуществления модулирующее средство-предшественник превращается в активную форму в организме хозяина.
В любой из вышеуказанных композиций модулирующее средство может содержать линкер. В некоторых вариантах осуществления линкер представляет собой расщепляемый линкер.
В любой из вышеуказанных композиций композиция может дополнительно содержать носитель. В некоторых случаях носитель может представлять собой приемлемый с точки зрения сельского хозяйства носитель.
В любой из вышеуказанных композиций композиция может дополнительно содержать приманку для хозяина, липкое средство или их комбинацию. В некоторых вариантах осуществления приманка для хозяина представляет собой съедобное средство и/или хемоаттрактант.
В любой из вышеуказанных композиций композиция может содержаться в дозе, эффективной для модулирования приспособленности хозяина.
В любой из вышеуказанных композиций композиция может быть составлена для доставки в микроорганизм, обитающий в кишке хозяина.
В любой из вышеуказанных композиций композиция может быть составлена для доставки в микроорганизм, обитающий в бактериоците хозяина и/или кишке хозяина. В некоторых вариантах осуществления композиция может быть составлена для доставки в растение. В некоторых вариантах осуществления композиция может быть составлена для применения в кормушке для хозяина.
В любой из вышеуказанных композиций композиция может быть составлена в виде жидкости, порошка, гранул или наночастиц. В некоторых вариантах осуществления композицию составляют в виде композиции, выбранной из группы, состоящей из липосомы, полимера, бактерии, секретирующей пептид, и синтетической нанокапсулы. В некоторых вариантах осуществления синтетическая нанокапсула доставляет композицию в участок-мишень в организме хозяина. В некоторых вариантах осуществления участок-мишень представляет собой кишку хозяина. В некоторых вариантах осуществления участок-мишень представляет собой бактериоцит в организме хозяина.
В дополнительном аспекте в данном документе также предусмотрены хозяева, которые содержат любую из вышеуказанных композиций. В некоторых вариантах осуществления хозяин представляет собой насекомое. В некоторых вариантах осуществления насекомое способствует контролю вредителей, опылению, созданию коммерческого продукта или их комбинации. В некоторых вариантах осуществления насекомое представляет собой вид, принадлежащий к Coccinellidae, Carabidae, Mantidae, Syrphidae, Lampyridae, Myrmeleontidae, Chrysopidae, Hemerobiidae, Braconidae, Ichneumonidae или Odonata. В некоторых вариантах осуществления насекомое представляет собой вид, принадлежащий к Andrenidae, Apidae, Colletidae, Halictidae или Megachilidae. В некоторых вариантах осуществления насекомое представляет собой вид, принадлежащий к Bombycidae или Saturniidae. В определенных вариантах осуществления насекомое представляет собой медоносную пчелу или шелкопряда.
В некоторых вариантах осуществления хозяин представляет собой нематоду. В некоторых вариантах осуществления нематода представляет собой вид, принадлежащий к Heterorhabditis или Steinernema.
В еще одном дополнительном аспекте в данном документе также предусмотрена система для модулирования приспособленности хозяина, содержащая модулирующее средство, которое целенаправленно воздействует на микроорганизм, требуемый для приспособленности хозяина, при этом система является эффективной для модулирования приспособленности хозяина, и при этом хозяин представляет собой насекомое или нематоду. Модулирующее средство может включать в себя любую из композиций, описанных в данном документе. В некоторых вариантах осуществления модулирующее средство составляют в виде порошка. В некоторых вариантах осуществления модулирующее средство составляют в виде растворителя. В некоторых вариантах осуществления модулирующее средство составляют в виде концентрата. В некоторых вариантах осуществления модулирующее средство составляют в виде разбавителя. В некоторых вариантах осуществления модулирующее средство готовят для доставки посредством объединения любой из предыдущих композиций с носителем.
В другом аспекте также предусмотрены способы модулирования приспособленности насекомого или нематоды с помощью любой из композиций, описанных в данном документе. В одном случае способ модулирования приспособленности насекомого-хозяина или нематоды-хозяина предусматривает доставку композиции по любому из предыдущих пунктов хозяину, при этом модулирующее средство целенаправленно воздействует на один или несколько микроорганизмов, обитающих в организме хозяина, и тем самым модулирует приспособленность хозяина. В другом случае способ модулирования разнообразия микроорганизмов в организме насекомого-хозяина или нематоды-хозяина предусматривает доставку композиции по любому из предыдущих пунктов хозяину, при этом модулирующее средство целенаправленно воздействует на один или несколько микроорганизмов, обитающих в организме хозяина, и тем самым модулирует разнообразие микроорганизмов в организме хозяина.
В некоторых вариантах осуществления любого из вышеуказанных способов модулирующее средство может изменять уровни одного или нескольких микроорганизмов, обитающих в организме хозяина. В некоторых вариантах осуществления любого из вышеуказанных способов модулирующее средство может изменять функцию одного или нескольких микроорганизмов, обитающих в организме хозяина. В некоторых вариантах осуществления один или несколько микроорганизмов может представлять собой бактерию и/или гриб. В некоторых вариантах осуществления один или несколько микроорганизмов требуются для приспособленности хозяина. В некоторых вариантах осуществления один или несколько микроорганизмов требуются для выживаемости хозяина.
В некоторых вариантах осуществления любого из вышеуказанных способов этап доставки может включать предоставление модулирующего средства в дозе и в течение времени, достаточных для воздействия на один или несколько микроорганизмов с модулированием тем самым разнообразия микроорганизмов в организме хозяина. В некоторых вариантах осуществления этап доставки включает местное применение любой из предыдущих композиций в отношении растения. В некоторых вариантах осуществления этап доставки включает предоставление модулирующего средства через генетически модифицированное растение. В некоторых вариантах осуществления этап доставки включает предоставление модулирующего средства хозяину в виде съедобного средства. В некоторых вариантах осуществления этап доставки включает получение хозяина, несущего модулирующее средство. В некоторых вариантах осуществления хозяин, несущий модулирующее средство, может переносить модулирующее средство одному или нескольким дополнительным хозяевам.
В некоторых вариантах осуществления любого из вышеуказанных способов композиция является эффективной для повышения уровня здоровья и/или выживаемости хозяина. В некоторых вариантах осуществления композиция является эффективной для повышения приспособленности хозяина, увеличения продолжительности жизни хозяина, увеличения интенсивности эффективного опыления, увеличения образования продукта хозяина, увеличения интенсивности размножения хозяина или их комбинации. В некоторых вариантах осуществления композиция является эффективной для снижения восприимчивости хозяина к пестицидному средству (например, пестициду, приведенному в таблице 12). В определенных вариантах осуществления пестицидное средство представляет собой неоникотиноид (например, имидаклоприд). В определенных вариантах осуществления пестицидное средство представляет собой фосфорорганический инсектицид (например, тиофосфатный инсектицид, например, фенитротион). В некоторых вариантах осуществления композиция является эффективной для повышения устойчивости хозяина к аллелохимическому средству, продуцируемому растением. В некоторых вариантах осуществления аллелохимическое средство является токсичным для хозяина до доставки композиции. В некоторых вариантах осуществления аллелохимическое средство представляет собой кофеин, цистатин N сои, монотерпены, дитерпеновые кислоты или фенольные соединения.
В некоторых вариантах осуществления любого из вышеуказанных способов хозяин представляет собой насекомое. В некоторых вариантах осуществления насекомое способствует контролю вредителей, опылению, созданию коммерческого продукта, разложению отходов или их комбинации. В некоторых вариантах осуществления насекомое представляет собой вид, принадлежащий к Coccinellidae, Carabidae, Mantidae, Syrphidae, Lampyridae, Myrmeleontidae, Chrysopidae, Hemerobiidae, Braconidae, Ichneumonidae или Odonata. В некоторых вариантах осуществления насекомое представляет собой вид, принадлежащий к Andrenidae, Apidae, Colletidae, Halictidae или Megachilidae. В некоторых вариантах осуществления насекомое представляет собой вид, принадлежащий к Bombycidae или Saturniidae. В определенных вариантах осуществления насекомое представляет собой медоносную пчелу или шелкопряда.
В некоторых вариантах осуществления хозяин представляет собой нематоду. В некоторых вариантах осуществления нематода представляет собой вид, принадлежащий к Heterorhabditis или Steinernema.
В некоторых вариантах осуществления любого из вышеуказанных способов этап доставки включает доставку любой из предыдущих композиций в растение. В некоторых вариантах осуществления растение представляет собой сельскохозяйственную культуру. В некоторых вариантах осуществления сельскохозяйственная культура представляет собой несобранную сельскохозяйственную культуру на момент доставки. В некоторых вариантах осуществления сельскохозяйственная культура представляет собой собранную сельскохозяйственную культуру на момент доставки. В некоторых вариантах осуществления сельскохозяйственная культура включает собранные фрукты или овощи. В некоторых вариантах осуществления композицию доставляют в количестве и в течение периода времени, эффективных для повышения темпов роста сельскохозяйственной культуры. В некоторых вариантах осуществления сельскохозяйственная культура включает растения кукурузы, сои или пшеницы.
В другом аспекте в данном документе также предусмотрены скрининговые анализы для идентификации модулирующего средства, которое модулирует приспособленность хозяина. В одном случае скрининговый анализ для идентификации модулирующего средства, которое модулирует приспособленность хозяина, включает этапы (a) воздействия на микроорганизм, который может обитать в организме хозяина, одного или нескольких кандидатных модулирующих средств и (b) идентификации модулирующего средства, которое повышает приспособленность хозяина.
В некоторых вариантах осуществления скринингового анализа модулирующее средство представляет собой микроорганизм, обитающий в организме хозяина. В некоторых вариантах осуществления микроорганизм представляет собой бактерию. В некоторых вариантах осуществления бактерия, обитая в организме хозяина, повышает приспособленность хозяина. В некоторых вариантах осуществления бактерия расщепляет пестицид (например, пестицид, приведенный в таблице 12). В определенных вариантах осуществления пестицид представляет собой неоникотиноид (например, имидаклоприд) или фосфорорганический инсектицид (например, тиофосфатный инсектицид, например, фенитротион). В некоторых вариантах осуществления бактерия секретирует аминокислоту. В определенных вариантах осуществления аминокислота представляет собой метионин.
В некоторых вариантах осуществления скринингового анализа модулирующее средство отрицательно влияет на микроорганизм, расщепляющий аллелохимикат. В некоторых вариантах осуществления модулирующее средство представляет собой фаг, антибиотик или исследуемое соединение. В некоторых вариантах осуществления антибиотик представляет собой тиментин или азитромицин.
В некоторых вариантах осуществления скринингового анализа хозяин может представлять собой беспозвоночное. В некоторых вариантах осуществления беспозвоночное представляет собой насекомое или нематоду. В определенных вариантах осуществления насекомое представляет собой медоносную пчелу. В других конкретных вариантах осуществления насекомое представляет собой шелкопряда.
В любом из вышеуказанных вариантов осуществления скринингового анализа приспособленность хозяина может быть модулирована путем изменения микробиоты хозяина.
Определения
Используемый в данном документе термин "бактериоцин" относится к пептиду или полипептиду, который обладает противомикробными свойствами. Встречающиеся в природе бактериоцины продуцируются определенными прокариотами и действуют против организмов, родственных штамму-продуценту, но не против самого штамма-продуцента. Бактериоцины, предусмотренные в данном документе, включают в себя без ограничения встречающиеся в природе бактериоцины, такие как бактериоцины, продуцируемые бактериями, или их производные, такие как сконструированные бактериоцины, рекомбинантно экспрессируемые бактериоцины или химически синтезируемые бактериоцины. В некоторых случаях бактериоцин представляет собой функционально активный вариант бактериоцинов, описанных в данном документе. В некоторых случаях вариант бактериоцина является на по меньшей мере 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичным, например, в определенной области или во всей последовательности, последовательности бактериоцина, описанного в данном документе, или встречающегося в природе бактериоцина.
Используемый в данном документе термин "бактериоцит" относится к специализированной клетке, встречающейся в определенных насекомых, в которых обитают внутриклеточные бактерии со свойствами симбиотических бактерий.
Используемый в данном документе термин "эффективное количество" относится к количеству модулирующего средства (например, фага, лизина, бактериоцина, малой молекулы или антибиотика) или композиции, содержащей указанное средство, достаточному для получения указанного результата, например, для повышения или содействия приспособленности организма-хозяина (например, насекомого); для достижения целевого уровня (например, предварительно определенного или порогового уровня) концентрации модулирующего средства в организме хозяина-мишени; для достижения целевого уровня (например, предварительно определенного или порогового уровня) концентрации модулирующего средства в кишке хозяина-мишени; для достижения целевого уровня (например, предварительно определенного или порогового уровня) концентрации модулирующего средства в бактериоците хозяина-мишени; для модулирования уровня или активности одного или нескольких микроорганизмов (например, эндосимбионтов) в организме хозяина-мишени.
Используемый в данном документе термин "приспособленность" относится к способности организма-хозяина выживать, расти и/или давать жизнеспособное потомство. Приспособленность организма может быть измерена с помощью одного или нескольких параметров, в том числе без ограничения продолжительности жизни, скорости размножения, подвижности, массы тела и/или скорости метаболизма. Приспособленность, кроме того, может быть измерена на основании показателей активности (например, опыления) или выхода продукта (например, меда или шелка).
Используемый в данном документе термин "кишка" относится к любой части кишки хозяина, в том числе передней кишке, средней кишке или задней кишке хозяина.
Используемый в данном документе термин "хозяин" относится к организму (например, насекомому), несущему обитающие в нем микроорганизмы (например, эндогенные микроорганизмы, эндосимбиотические микроорганизмы (например, первичные или вторичные эндосимбионты), организмы-комменсалы и/или патогенные микроорганизмы).
Используемый в данном документе термин "повышение приспособленности хозяина" или "содействие приспособленности хозяина" относится к любому благоприятному изменению физиологических процессов хозяина или любой активности, осуществляемой указанным хозяином, вследствие введения модулирующего средства, в том числе без ограничения любому одному или нескольким из следующих необходимых эффектов: (1) увеличению популяции хозяина на приблизительно 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 95%, 99%, 100% или больше; (2) увеличению скорости размножения хозяина (например, насекомого, например, пчелы или шелкопряда) на приблизительно 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 95%, 99%, 100% или больше; (3) увеличению подвижности хозяина (например, насекомого, например, пчелы или шелкопряда) на приблизительно 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 95%, 99%, 100% или больше; (4) увеличению массы тела хозяина (например, насекомого, например, пчелы или шелкопряда) на приблизительно 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 95%, 99%, 100% или больше; (5) увеличению скорости метаболизма или активности хозяина (например, насекомого, например, пчелы или шелкопряда) на приблизительно 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 95%, 99%, 100% или больше; (6) увеличению интенсивности опыления (например, увеличению количества опыленных растений за указанное количество времени) хозяином (например, насекомым, например, пчелой или шелкопрядом) на приблизительно 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 95%, 99%, 100% или больше; (7) увеличению продуцирования у хозяина (например, насекомого, например, пчелы или шелкопряда) продуктов жизнедеятельности (например, меда у медоносной пчелы или шелка у шелкопряда) на приблизительно 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 95%, 99%, 100% или больше; (8) увеличению содержания питательных веществ у хозяина (например, насекомого) (например, белка, жирных кислот или аминокислот) на приблизительно 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 95%, 99%, 100% или больше; или (9) повышению устойчивости хозяина к пестицидам (например, неоникотиноиду (например, имидаклоприду) или фосфорорганическому инсектициду (например, тиофосфатному инсектициду, например, фенитротиону)) на приблизительно 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 95%, 99%, 100% или больше. Повышение приспособленности хозяина может быть определено по сравнению с организмом-хозяином, которому модулирующее средство не было введено.
Термин "насекомое" включает любой организм, принадлежащий к типу Arthropoda и классу Insecta или классу Arachnida, на любой стадии развития, т. е. неполовозрелых или взрослых насекомых.
Используемый в данном документе термин "лизин", также известный как эндолизин, аутолизин, муреингидролаза, пептидогликангидролаза или гидролаза клеточной стенки, относится к гидролитическому ферменту, который может лизировать бактерию посредством расщепления пептидогликана в клеточной стенке бактерии. Лизины, предусмотренные в данном документе, включают в себя без ограничения встречающиеся в природе лизины, такие как лизины, продуцируемые фагами, лизины, продуцируемые бактериями, или их производные, такие как сконструированные лизины, рекомбинантно экспрессируемые лизины или химически синтезируемые лизины. Функционально активный вариант бактериоцина может являться на по меньшей мере 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичным, например, в определенной области или во всей последовательности, последовательности синтетического, рекомбинантного или встречающегося в природе бактериоцина, в том числе любого описанного в данном документе.
Используемый в данном документе термин "микроорганизм" относится к бактериям или грибам. Микроорганизмы могут относиться к микроорганизмам, обитающим в организме-хозяине (например, эндогенным микроорганизмам, эндосимбиотическим микроорганизмам (например, первичным или вторичным эндосимбионтам)), или микроорганизмам, экзогенным для хозяина, в том числе микроорганизмам, которые могут выступать в качестве модулирующих средств. Используемый в данном документе термин "микроорганизм-мишень" относится к микроорганизму, который обитает в организме хозяина и подвергается воздействию модулирующего средства, прямо или косвенно.
Используемый в данном документе термин "средство" или "модулирующее средство" относится к средству, которое способно изменять уровни и/или функционирование микроорганизмов, обитающих в организме-хозяине (например, насекомом), и тем самым модулировать (например, повышать) приспособленность организма-хозяина (например, насекомого).
Используемый в данном документе термин "пестицид" или "пестицидное средство" относится к веществу, которое можно применять для контроля вредителей, значимых для сельского хозяйства, окружающей среды и домашнего хозяйства/быта, таких как насекомые, грибы, бактерии или вирусы. Термин "пестицид" понимают как охватывающий встречающиеся в природе или синтетические инсектициды (ларвициды или адультициды), регуляторы роста насекомых, акарициды (майтициды), нематоциды, эктопаразитициды, бактерициды, фунгициды или гербициды (вещества, которые можно применять в сельском хозяйстве для контроля или модификации роста растений). Дополнительные примеры пестицидов или пестицидных средств приведены в таблице 12. В некоторых случаях пестицид представляет собой аллелохимикат. Используемый в данном документе термин "аллелохимикат" или "аллелохимическое средство" означает вещество, продуцируемое организмом, которое может воздействовать на физиологическую функцию (например, зарождение, рост, выживаемость или размножение) другого организма (например, насекомого-хозяина или нематоды-хозяина).
Используемый в данном документе термин "пептид", "белок" или "полипептид" охватывает любую цепь из встречающихся в природе или не встречающихся в природе аминокислот (как D-, так и L-аминокислот), независимо от длины (например, по меньшей мере 2, 3, 4, 5, 6, 7, 10, 12, 14, 16, 18, 20, 25, 30, 40, 50, 100 или больше аминокислот), наличия или отсутствия посттрансляционных модификаций (например, гликозилирования или фосфорилирования) или наличия, например, одной или нескольких не являющихся аминоацильными групп (например, углеводных, липидных и т. д.), ковалентно связанных с пептидом, и включает, например, природные белки, синтетические или рекомбинантные полипептиды и пептиды, гибридные молекулы, пептоиды или пептидомиметики.
Как используется в данном документе, "процент идентичности" между двумя последовательностями определяют с помощью алгоритма BLAST 2.0, который описан в Altschul et al. (J. Mol. Biol. 215:403-410, 1990). Программное обеспечение для проведения анализов BLAST общедоступно благодаря Национальному центру биотехнологической информации.
Используемый в данном документе термин "фаг" или "бактериофаг" относится к вирусу, который инфицирует бактерии и реплицируется в них. Бактериофаги реплицируются в бактериях после введения их генома в цитоплазму и осуществляют это с помощью литического цикла, который приводит к лизису бактериальной клетки, или лизогенного (не являющегося литическим) цикла, при котором бактериальная клетка остается интактной. Фаг может представлять собой изолят встречающегося в природе фага или сконструированный фаг, в том числе векторы или нуклеиновые кислоты, которые кодируют частичный геном фага (например, в том числе по меньшей мере все важнейшие гены, необходимые для осуществления жизненного цикла фага в бактерии-хозяине) или полный геном фага.
Используемый в данном документе термин "растение" относится к целым растениям, органам растений, растительным тканям, растительным клеткам, семенам и их потомству. Растительные клетки включают в себя без ограничения клетки из семян, суспензионных культур, зародышей, участков меристемы, каллюсной ткани, листьев, корней, побегов, гаметофитов, спорофитов, пыльцы или микроспор. Части растений включают в себя дифференцированные или недифференцированные ткани, в том числе без ограничения: корни, стебли, побеги, листья, пыльцу, семена, опухолевую ткань и различные формы клеток и культуры (например, отдельные клетки, протопласты, зародыши или каллюсную ткань). Растительная ткань может находиться в растении или в органе, ткани или культуре клеток растения. Кроме того, растение может быть генетически модифицированным таким образом, что в нем продуцируется гетерологичный белок или РНК, например, любого из модулирующих средств в способах и композициях, описанных в данном документе.
Термины "получаемый", "производимый" или т. п. используются для указания того, что пункт формулы изобретения или вариант осуществления относится к соединению, композиции, продукту и т. д. как таковым, т. е. что соединение, композиция, продукт и т. д. могут быть получены или произведены способом, который описан для изготовления соединения, композиции, продукта и т. д., но при этом соединение, композиция, продукт и т. д. также могут быть получены или произведены способами, отличными от описанного. Термины "полученный", "произведенный" или т. п. указывают на то, что соединение, композиция, продукт получены или произведены указанным конкретным способом. Следует понимать, что термины "получаемый", "производимый" или т. п. также раскрывают термины "полученный", "произведенный" и т. п. в качестве предпочтительного варианта осуществления "получаемого", "производимого" и т. п.
Другие характеристики и преимущества настоящего изобретения будут очевидны из следующего подробного описания и формулы изобретения.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
Фигуры предусмотрены для иллюстрации одной или нескольких характеристик, аспектов или вариантов осуществления настоящего изобретения и не предполагаются как ограничивающие.
На фиг. 1 представлен график, демонстрирующий время достижения эмбрионами зрелого возраста у Drosophila melanogaster. Эмбрионы Drosophila melanogaster выращивали на рационе, засеянном Corynebacterium glutamicum (штаммом, продуцирующим глутамат - C. glutamicum Glu), либо на рационе в аксенических условиях без каких-либо бактерий. Процентное содержание взрослых особей, появляющихся из куколок, измеряли каждые 12 часов с момента появления первой взрослой особи. Организмы, выращиваемые на рационе с добавлением бактерий, достигают зрелого возраста быстрее, чем аналогичные особи в условиях без добавления бактерий.
На фиг. 2А представлен график, демонстрирующий влияние мужского пола на различия в скорости развития у Drosophila melanogaster. Определяли пол взрослых особей, появление которых отображено на фиг. 1, и скорость их появления откладывали на графике.
На фиг. 2В представлен график, демонстрирующий влияние женского пола на различия в скорости развития у Drosophila melanogaster. Определяли пол взрослых особей, появление которых отображено на фиг. 1, и скорость их появления откладывали на графике. Увеличение скорости развития у самок за счет присутствия бактерий в рационе является значительно большим, чем у аналогичных особей мужского пола. Благоприятные эффекты присутствия бактерий в рационе мух являются более выраженными у самок по сравнению с самцами.
На фиг. 3 представлен график, демонстрирующий, что штаммы C. glutamicum содействовали образованию биомассы личинок. Личинки, выращиваемые на рационе, дополненном штаммами C. glutamicum, продуцирующими глутамат либо метионин, являются более крупными, чем личинки, выращиваемые на стерильном рационе или рационе, дополненном Escherichia coli. Площади тела личинок измерены в виде количества пикселей на изображениях личинок. Медианы и 95% доверительные интервалы показаны в виде линий на графике.
На фиг. 4 представлена панель графиков, демонстрирующих результаты анализа внеклеточного потока Seahorse в отношении дыхания бактерий. Бактерии выращивали до логарифмической фазы и загружали в планшеты Seahorse XFe96 для временных измерений скорости потребления кислорода (OCR) и скорости закисления внеклеточной среды (ECAR), как описано в способах. Средства обработки вводили в лунки примерно через 20 минут, и бактерии отслеживали для выявления изменений роста. Рифампицин=100 мкг/мл; хлорамфеникол=25 мкг/мл; фаги (T7 в случае E. coli и ΦSmVL-C1 в случае Serratia marcescens) представляли собой лизаты, разведенные 1:2 либо 1:100 в буфере SM. Отметки на каждой линии предусмотрены исключительно в качестве индикаторов состояния, которым каждая линия соответствует, и не указывают на точки данных.
На фиг. 5 представлен график, демонстрирующий, что фаг, противодействующий S. marcescens, приводил к снижению смертности мух. Все мухи, которым вводили путем прокола S. marcescens, погибали в течение дня, в том время как значительная часть мух, которым вводили путем прокола как S. marcescens, так и фаг, выживали в течение пяти дней после обработки. Почти все из контрольных мух, которых никак не обрабатывали, выживали до конца эксперимента. Логарифмический ранговый критерий использовали для сравнения кривых для определения статистической значимости, звездочка обозначает p<0,0001.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В данном документе предусмотрены способы и композиции для применения в сельском хозяйстве, например, для изменения уровня, активности или метаболизма одного или нескольких микроорганизмов, обитающих в организме нематоды-хозяина или членистоногого-хозяина (например, медоносной пчелы или шелкопряда), при этом данное изменение приводит к повышению приспособленности хозяина. В настоящем изобретении описана композиция, которая содержит модулирующее средство (например, фаг, пептид, малую молекулу, антибиотик или их комбинации), которое может изменять микробиоту хозяина таким образом, что это является благоприятным для хозяина. Модулирующее средство, описанное в данном документе, можно применять для повышения приспособленности ряда полезных нематод или членистоногих, таких как медоносные пчелы и шелкопряды, используемые в сельском хозяйстве и коммерческой деятельности, посредством содействия достижению благоприятных уровней микроорганизмов, активности микроорганизмов, метаболизма микроорганизмов и/или разнообразия микроорганизмов.
Способы и композиции, описанные в данном документе, частично основаны на примерах, которые иллюстрируют, как различные средства, например, микроорганизмы, расщепляющие имидаклоприд, микроорганизмы, расщепляющие фенитротион, и различные фаги, можно применять в отношении насекомых-хозяев, таких как медоносные пчелы или Drosophila, для опосредованного улучшения состояния здоровья этих хозяев путем изменения уровня, активности или метаболизма микроорганизмов в организмах этих хозяев. Микроорганизмы, расщепляющие имидаклоприд, являются иллюстративным примером микроорганизмов, расщепляющих неоникотиноиды, и в более общем смысле иллюстрируют микроорганизмы, расщепляющие инсектициды или пестициды. Аналогично, микроорганизмы, расщепляющие фенитротион, являются иллюстративным примером микроорганизмов, расщепляющих фосфорорганические инсектициды, и в более общем смысле иллюстрируют микроорганизмы, расщепляющие инсектициды или пестициды. На основании этого в настоящем изобретении описан ряд различных подходов к применению средств, которые изменяют уровень, активность или метаболизм одного или нескольких микроорганизмов, обитающих в организме хозяина, при этом изменение приводит к модулированию приспособленности хозяина.
I. Хозяева
i. Хозяева
Хозяином в отношении любой из композиций или способов, описанных в данном документе, может являться любой организм, принадлежащий к типу Nematoda (например, нематоды, например, полезные нематоды) или Arthropoda (например, насекомые, например, полезные насекомые), включая любых членистоногих, описанных в данном документе. В некоторых случаях хозяином являются полезные насекомое или нематода (например, опылитель, естественный конкурент вредителя или продуцент полезных для человека веществ). Используемый в данном документе термин "полезное насекомое" или "полезная нематода" относится к насекомому или нематоде, которые приносят пользу (например, экономическую и/или экологическую) людям, животным, экосистеме и/или окружающей среде. Например, хозяином может являться насекомое, которое участвует в получении коммерческого продукта, в том числе без ограничения насекомые, культивируемые для получения продуктов питания (например, меда от медоносных пчел, например, Apis mellifera), материалов (таких как шелк от Bombyx mori) и/или веществ (например, лака от Laccifer lacca или красителей от Dactylopius coccus и Cynipidae). Кроме того, хозяин может включать в себя насекомых или нематод, которых используют в сельскохозяйственных путях применения, в том числе насекомых, которые способствуют опылению сельскохозяйственных культур, распространению семян или контролю вредителей. Кроме того, в некоторых случаях хозяином может являться насекомое, пригодное для утилизации и/или органической переработки отходов (например, дождевые черви, термиты или личинки Diptera).
В некоторых случаях хозяин продуцирует применимый продукт (например, мед, шелк, пчелиный воск или шеллак). В некоторых случаях хозяином является пчела. Иллюстративные роды пчел включают в себя без ограничения Apis, Bombus, Trigona и Osmia. В некоторых случаях пчела представляет собой медоносную пчелу (например, насекомое, принадлежащее к роду Apis). В некоторых случаях медоносная пчела представляет собой виды Apis mellifera (европейская или западная медоносная пчела), Apis cerana (азиатская, восточная или гималайская медоносная пчела), Apis dorsata ("гигантская" медоносная пчела), Apis florea ("красная карликовая" медоносная пчела), Apis andreniformis ("черная карликовая" медоносная пчела) или Apis nigrocincta. В некоторых случаях хозяином является шелкопряд. Шелкопряд может представлять собой вид из семейства Bombycidae или Saturniidae. В некоторых случаях шелкопряд представляет собой Bombyx mori. В некоторых случаях хозяином является лаковый червец. Лаковый червец может представлять собой вид из семейства Kerriidae. В некоторых случаях лаковый червец представляет собой Kerria lacca.
В некоторых случаях хозяин способствует опылению растения (например, пчелы, жуки, осы, мухи, бабочки или моли). В некоторых примерах хозяином, способствующим опылению растения, является жук. В некоторых случаях жук представляет собой вид из семейства Buprestidae, Cantharidae, Cerambycidae, Chrysomelidae, Cleridae, Coccinellidae, Elateridae, Melandryidae, Meloidae, Melyridae, Mordellidae, Nitidulidae, Oedemeridae, Scarabaeidae или Staphylinidae. В некоторых случаях хозяином, способствующим опылению растения, является бабочка или моль (например, Lepidoptera). В некоторых случаях бабочка или моль представляет собой вид из семейства Geometridae, Hesperiidae, Lycaenidae, Noctuidae, Nymphalidae, Papilionidae, Pieridae или Sphingidae. В некоторых случаях хозяином, способствующим опылению растения, является муха (например, Diptera). В некоторых случаях муха принадлежит к семейству Anthomyiidae, Bibionidae, Bombyliidae, Calliphoridae, Cecidomiidae, Ceratopogonidae, Chironomidae, Conopidae, Culicidae, Dolichopodidae, Empididae, Ephydridae, Lonchopteridae, Muscidae, Mycetophilidae, Phoridae, Simuliidae, Stratiomyidae или Syrphidae. В некоторых случаях хозяином, способствующим опылению растения, является муравей (например, Formicidae), пилильщик (например, Tenthredinidae) или оса (например, Sphecidae или Vespidae). В некоторых случаях хозяином, способствующим опылению растения, является пчела. В некоторых случаях пчела принадлежит к семейству Andrenidae, Apidae, Colletidae, Halictidae или Megachilidae.
В некоторых случаях хозяин способствует контролю вредителей. В некоторых случаях хозяином, способствующим контролю вредителей, является хищная нематода. В конкретных примерах нематода представляет собой вид Heterorhabditis или Steinernema. В некоторых случаях хозяином, способствующим контролю вредителей, является насекомое. Например, хозяин, способствующий контролю вредителей, может представлять собой вид, принадлежащий к семейству Braconidae (например, паразитоидные осы), Carabidae (например, жужелицы), Chrysopidae (например, златоглазки), Coccinellidae (например, божьи коровки), Hemerobiidae (например, гемеробы), Ichneumonidae (например, наездники-ихневмониды), Lampyridae (например, светляки), Mantidae (например, богомолы), Myrmeleontidae (например, муравьиные львы), Odonata (например, разнокрылые стрекозы и равнокрылые стрекозы) или Syrphidae (например, журчалка). В других случаях хозяином, способствующим контролю вредителей, является насекомое, которое конкурирует с насекомым, считающимся вредителем (например, сельскохозяйственным вредителем). Например, средиземноморская плодовая мушка Ceratitis capitata является распространенным вредителем фруктов и овощей во всем мире. Одним из способов контроля C. capitata является выпускание стерилизованных самцов этих насекомых в окружающую среду с целью конкуренции с дикими самцами за спаривание с самками. В этих случаях хозяином может являться стерилизованный самец, принадлежащий к виду, который обычно считается вредителем.
В некоторых случаях хозяин способствует разложению отходов или органического материала. В некоторых примерах хозяин, способствующий разложению отходов или органического материала, принадлежит к Coleoptera или Diptera. В некоторых случаях хозяин, принадлежащий к Diptera, принадлежит к семейству Calliphoridae, Curtonotidae, Drosophilidae, Fanniidae, Heleomyzidae, Milichiidae, Muscidae, Phoridae, Psychodidae, Scatopsidae, Sepsidae, Sphaeroceridae, Stratiomyidae, Syrphidae, Tephritidae или Ulidiidae. В некоторых случаях хозяин, принадлежащий к Coleoptera, принадлежит к семейству Carabidae, Hydrophilidae, Phalacaridae, Ptiliidae или Staphylinidae.
В конкретных случаях модулирующие средства, раскрытые в данном документе, можно применять для повышения приспособленности медоносных пчел-хозяев или шелкопрядов-хозяев.
ii. Приспособленность хозяев
Способы и композиции, предусмотренные в данном документе, можно применять для повышения приспособленности любого из хозяев, описанных в данном документе. Повышение приспособленности может возникать в результате любых изменений в микроорганизмах, обитающих в организме хозяина, при этом изменения представляют собой следствие введения модулирующего средства и оказывают благоприятные или полезные воздействия на хозяина.
В некоторых случаях повышение приспособленности хозяина может проявляться в виде улучшения физиологических процессов хозяина (например, улучшения состояния здоровья или выживаемости) вследствие введения модулирующего средства. В некоторых случаях приспособленность организма может быть измерена с помощью одного или нескольких параметров, в том числе без ограничения скорости размножения, продолжительности жизни, подвижности, плодовитости, массы тела, скорости метаболизма или активности или выживаемости по сравнению с организмом-хозяином, которому модулирующее средство не было введено. Например, способы или композиции, предусмотренные в данном документе, могут быть эффективными для улучшения общего состояния здоровья хозяина или для улучшения общей выживаемости хозяина по сравнению с организмом-хозяином, которому модулирующее средство не было введено. В некоторых случаях улучшение выживаемости хозяина составляет приблизительно 2%, 5%, 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 100% или более чем 100% по сравнению с эталонным уровнем (например, уровнем, обнаруживаемым у хозяина, который не получает модулирующее средство). В некоторых случаях способы и композиции являются эффективными для повышения интенсивности размножения хозяина (например, скорости размножения) по сравнению с организмом-хозяином, которому модулирующее средство не было введено. В некоторых случаях способы и композиции являются эффективными для увеличения других физиологических параметров, таких как подвижность, масса тела, продолжительность жизни, плодовитость или скорость метаболизма, на приблизительно 2%, 5%, 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 100% или более чем на 100% по сравнению с эталонным уровнем (например, уровнем, обнаруживаемым у хозяина, который не получает модулирующее средство).
В некоторых случаях повышение приспособленности хозяина может проявляться в виде увеличения продуцирования продукта, образуемого указанным хозяином, по сравнению с организмом-хозяином, которому модулирующее средство не было введено. В некоторых случаях способы или композиции, предусмотренные в данном документе, могут быть эффективными для увеличения продуцирования продукта, образуемого хозяином, описанным в данном документе (например, меда, пчелиного воска, перги, прополиса, шелка или лака), на приблизительно 2%, 5%, 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 100% или более чем на 100% по сравнению с эталонным уровнем (например, уровнем, обнаруживаемым у хозяина, который не получает модулирующее средство).
В некоторых случаях повышение приспособленности хозяина может проявляться в виде увеличения частоты или эффективности желаемой активности, осуществляемой хозяином (например, опыления, истребления вредителей, распространения семян или разрушения отходов или органического материала), по сравнению с организмом-хозяином, которому модулирующее средство не было введено. В некоторых случаях способы или композиции, предусмотренные в данном документе, могут быть эффективными для увеличения частоты или эффективности желаемой активности, осуществляемой хозяином (например, опыления, истребления вредителей, распространения семян или разрушения отходов или органического материала), на приблизительно 2%, 5%, 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 100% или более чем на 100% по сравнению с эталонным уровнем (например, уровнем, обнаруживаемым у хозяина, который не получает модулирующее средство).
В некоторых случаях повышение приспособленности хозяина может проявляться в виде увеличения продуцирования одного или нескольких питательных веществ в организме хозяина (например, витаминов, углеводов, аминокислот или полипептидов) по сравнению с организмом-хозяином, которому модулирующее средство не было введено. В некоторых случаях способы или композиции, предусмотренные в данном документе, могут быть эффективными для увеличения продуцирования питательных веществ в организме хозяина (например, витаминов, углеводов, аминокислот или полипептидов) на приблизительно 2%, 5%, 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 100% или более чем на 100% по сравнению с эталонным уровнем (например, уровнем, обнаруживаемым у хозяина, который не получает модулирующее средство). В некоторых случаях способы или композиции, предусмотренные в данном документе, могут обеспечивать увеличение содержания питательных веществ в организме хозяина путем увеличения продуцирования питательных веществ одним или несколькими микроорганизмами (например, эндосимбионтами) в организме хозяина.
В некоторых случаях повышение приспособленности хозяина может проявляться в виде снижения восприимчивости хозяина к пестицидному средству (например, пестициду, приведенному в таблице 12) и/или повышения устойчивости хозяина к пестицидному средству (например, пестициду, приведенному в таблице 12) по сравнению с организмом-хозяином, которому модулирующее средство не было введено. В некоторых случаях способы или композиции, предусмотренные в данном документе, могут быть эффективными для снижения восприимчивости хозяина к пестицидному средству (например, пестициду, приведенному в таблице 12) на приблизительно 2%, 5%, 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 100% или более чем на 100% по сравнению с эталонным уровнем (например, уровнем, обнаруживаемым у хозяина, который не получает модулирующее средство). В некоторых случаях восприимчивость хозяина к пестицидному средству изменяют путем введения модулирующего средства, которое расщепляет пестицидное средство (например, бактерий, расщепляющих пестициды, например, бактерий, расщепляющих неоникотиноиды, или бактерий, расщепляющих фосфорорганические инсектициды). Пестицидное средство может представлять собой любое пестицидное средство, известное в данной области техники, в том числе инсектицидные средства. В некоторых случаях пестицидное средство представляет собой неоникотиноид (например, имидаклоприд) или фосфорорганический инсектицид (например, тиофосфатный инсектицид, например, фенитротион). В некоторых случаях способы или композиции, предусмотренные в данном документе, могут снижать восприимчивость хозяина к пестицидному средству (например, пестициду, приведенному в таблице 12) посредством повышения способности хозяина метаболизировать пестицидное средство или расщеплять его на пригодные к использованию субстраты.
В некоторых случаях восприимчивость хозяина к пестицидному средству изменяют путем введения модулирующего средства, которое детоксифицирует ксенобиотик.
В некоторых случаях повышение приспособленности хозяина может проявляться в виде снижения восприимчивости хозяина к аллелохимическому средству и/или повышения устойчивости хозяина к аллелохимическому средству по сравнению с организмом-хозяином, которому модулирующее средство не было введено. В некоторых случаях способы и композиции, предусмотренные в данном документе, могут быть эффективными для повышения устойчивости хозяина к аллелохимическому средству на приблизительно 2%, 5%, 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 100% или более чем на 100% по сравнению с эталонным уровнем (например, уровнем, обнаруживаемым у хозяина, который не получает модулирующее средство). В некоторых случаях аллелохимическое средство представляет собой кофеин, цистатин N сои, монотерпены, дитерпеновые кислоты или фенольные соединения. В некоторых случаях способы или композиции, предусмотренные в данном документе, могут снижать восприимчивость хозяина к аллелохимическому средству посредством повышения способности хозяина метаболизировать аллелохимическое средство или расщеплять его на пригодные к использованию субстраты.
В некоторых случаях способы или композиции, предусмотренные в данном документе, могут быть эффективными для повышения устойчивости хозяина к паразитам или патогенам (например, грибным, бактериальным или вирусным патогенам или паразитическим микроскопическим клещам (например, к микроскопическому клещу Varroa destructor у медоносных пчел)) по сравнению с организмом-хозяином, которому модулирующее средство не было введено. В некоторых случаях способы или композиции, предусмотренные в данном документе, могут быть эффективными для повышения устойчивости хозяина к патогенам или паразитам (например, грибным, бактериальным или вирусным патогенам или паразитическим микроскопическим клещам (например, к микроскопическому клещу Varroa destructor у медоносных пчел)) на приблизительно 2%, 5%, 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 100% или более чем на 100% по сравнению с эталонным уровнем (например, уровнем, обнаруживаемым у хозяина, который не получает модулирующее средство).
В некоторых случаях повышение приспособленности хозяина может проявляться в виде других преимуществ приспособленности, таких как улучшенная переносимость определенных факторов окружающей среды (например, переносимость высокой или низкой температуры), улучшенная способность к выживанию в определенных средах обитания или улучшенная способность к поддержанию определенного рациона (например, улучшенная способность метаболизировать сою по сравнению с кукурузой), по сравнению с организмом-хозяином, которому модулирующее средство не было введено. В некоторых случаях способы или композиции, предусмотренные в данном документе, могут быть эффективными для повышения приспособленности хозяина множеством способов, описанных в данном документе. Кроме того, модулирующее средство может повышать приспособленность хозяина в любом количестве классов, отрядов, семейств, родов или видов хозяев (например, у 1 вида хозяев, 2, 3, 4, 5, 6, 7, 8, 9, 10, 15, 20, 30, 40, 50, 60, 70, 80, 90, 100, 150, 200, 200, 250, 500 или больше видов хозяев). В некоторых случаях модулирующее средство действует на один класс, отряд, семейство, род или вид хозяев.
Приспособленность хозяина может быть оценена с помощью любых стандартных способов в данной области техники. В некоторых случаях приспособленность хозяина может быть оценена посредством оценки отдельного хозяина. В качестве альтернативы, приспособленность хозяина может быть оценена посредством оценки популяции хозяев. Например, повышение приспособленности хозяина может проявляться в виде повышения степени успешного конкурирования по сравнению с другими насекомыми, что тем самым приводит к увеличению размера популяции хозяев.
iii. Беспозвоночные-хозяева в сельском хозяйстве
Благодаря повышению приспособленности полезных нематод или насекомых модулирующие средства, предусмотренные в данном документе, могут быть эффективными для содействия росту растений, на которые указанные хозяева производят благоприятный эффект. Модулирующее средство может быть доставлено с использованием любых составов и способов доставки, описанных в данном документе, в количестве и в течение периода времени, эффективных для повышения приспособленности хозяев, представляющих интерес, что тем самым производит благоприятный эффект на растение (например, в виде повышения темпов роста сельскохозяйственной культуры, повышения урожайности сельскохозяйственной культуры, снижения заражения вредителями и/или уменьшения вреда, причиняемого растениям). Это может предусматривать или не предусматривать непосредственное применение модулирующего средства в отношении растения. Например, в случаях, когда первоначальная среда обитания хозяина отличается от региона, в котором растет растение, модулирующее средство может применяться в отношении одного из первоначальной среды обитания хозяина либо растений, представляющих интерес, или комбинации того и другого.
В некоторых случаях растение может представлять собой сельскохозяйственную культуру, такую как злаковая, зерновая, бобовая, фруктовая или овощная культура. Композиции, описанные в данном документе, могут быть доставлены в сельскохозяйственную культуру в любое время до или после сбора урожая злаковой, зерновой, бобовой, фруктовой или овощной сельскохозяйственной культуры. Урожайность сельскохозяйственной культуры является показателем, часто используемым, например, в отношении злаковых, зерновых или бобовых культур, который обычно измеряется в метрических тоннах с гектара (или килограммах с гектара). Урожайность сельскохозяйственной культуры также может относиться к фактическому образованию семян растением. В некоторых случаях модулирующее средство может быть эффективным для повышения урожайности сельскохозяйственной культуры (например, увеличения количества метрических тонн злаковой, зерновой, бобовой, фруктовой или овощной культуры, собираемых с гектара, и/или увеличения образования семян) на приблизительно 2%, 5%, 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 100% или больше по сравнению с эталонным уровнем (например, у сельскохозяйственной культуры, в которую модулирующее средство не было введено).
В некоторых случаях растение (например, сельскохозяйственная культура) может иметь риск развития заражения вредителем (например, насекомым), или у него уже может развиться заражение вредителем. Способы и композиции, описанные в данном документе, можно применять для снижения или предупреждения заражения вредителями таких сельскохозяйственных культур путем содействия приспособленности полезных насекомых, которые охотятся на сельскохозяйственных вредителей. В некоторых случаях модулирующее средство может быть эффективным для снижения заражения сельскохозяйственной культуры (например, уменьшения количества зараженных растений, уменьшения размера популяции вредителя или уменьшения вреда, причиняемого растениям) на приблизительно 2%, 5%, 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 100% или больше по сравнению с эталонным уровнем (например, у сельскохозяйственной культуры, в которую модулирующее средство не было введено). В других случаях модулирующее средство может быть эффективным для предупреждения или снижения вероятности заражения сельскохозяйственной культуры на приблизительно 2%, 5%, 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 100% или больше по сравнению с эталонным уровнем (например, у сельскохозяйственной культуры, в которую модулирующее средство не было введено).
Композиции и способы, описанные в данном документе, могут производить благоприятный эффект на любые подходящие растительные ткани, в том числе без ограничения на соматические зародыши, пыльцу, листья, стебли, каллюсы, столоны, микроклубни и побеги. Способы, описанные в данном документе, могут включать обработку покрытосеменных и голосеменных растений, таких как акация, люцерна, яблоня, абрикос, артишок, ясень, спаржа, авокадо, банан, ячмень, разновидности фасоли, свекла, береза, бук, ежевика, черника, брокколи, разновидности брюссельской капусты, кочанная капуста, канола, дыня мускусная, морковь, маниок съедобный, цветная капуста, кедр, злаковое растение, сельдерей, каштан, вишня, пекинская капуста, цитрусовое растение, клементин, клевер, кофейное дерево, кукуруза, хлопчатник, вигна китайская, огурец, кипарис, баклажан, вяз, цикорий салатный, эвкалипт, разновидности конских бобов, фенхель, разновидности инжира, пихта, герань, виноград, грейпфрут, разновидности земляного ореха, физалис, тсуга канадская, гикори, кудрявая капуста, актинидия, кольраби, лиственница, латук, лук-порей, лимон, лайм, робиния, сосна, курчавый папоротник, маис, манго, клен, дыня обыкновенная, просо, шампиньон, горчица, орехоплодные растения, дуб, разновидности овса, абельмош съедобный, лук репчатый, апельсин, декоративное растение или цветочное растение или дерево, папайя, пальма, петрушка, пастернак посевной, горох, персик, арахис, груша, торфообразующее растение, перец, хурма, голубиный горох, сосна, ананас, плантан, слива, гранат, картофель, тыква, итальянский цикорий, редька, рапс, малина, рис, рожь посевная, сорго, ива, соя, шпинат, ель, кабачок, земляника, сахарная свекла, сахарный тростник, подсолнечник, сладкий картофель, сахарная кукуруза, танжерин, чайный куст, табак, томат, древесные растения, тритикале, дернообразующие травянистые растения, разновидности турнепса, виноград культурный, грецкий орех, жеруха лекарственная, арбуз обыкновенный, пшеница, разновидности ямса, тис и цукини.
II. Микроорганизмы-мишени
Микроорганизмы, на которые целенаправленно воздействует модулирующее средство, описанное в данном документе, могут включать в себя любой микроорганизм, обитающий в организме хозяина или на нем, в том числе без ограничения любые бактерии и/или грибы, описанные в данном документе. Микроорганизмы, обитающие в организме хозяина, могут включать в себя, например, симбиотические микроорганизмы (например, эндосимбиотические микроорганизмы, которые предоставляют полезные питательные вещества или ферменты хозяину), микроорганизмы-комменсалы, патогенные или паразитические микроорганизмы. Симбиотический микроорганизм (например, бактерия или гриб) может являться облигатным симбионтом хозяина или факультативным симбионтом хозяина. Микроорганизмы, обитающие в организме хозяина, могут быть приобретены с помощью любого пути переноса, в том числе вертикального, горизонтального переноса или переноса множественного происхождения.
i. Бактерии
Иллюстративные бактерии, на которые можно целенаправленно воздействовать в соответствии со способами и композициями, предусмотренными в данном документе, включают в себя без ограничения Xenorhabdus spp, Photorhabdus spp, Candidatus spp, Buchnera spp, Blattabacterium spp, Baumania spp, Wigglesworthia spp, Wolbachia spp, Rickettsia spp, Orientia spp, Sodalis spp, Burkholderia spp, Cupriavidus spp, Frankia spp, Snirhizobium spp, Streptococcus spp, Wolinella spp, Xylella spp, Erwinia spp, Agrobacterium spp, Bacillus spp, Paenibacillus spp, Streptomyces spp, Micrococcus spp, Corynebacterium spp, Acetobacter spp, Cyanobacteria spp, Salmonella spp, Rhodococcus spp, Pseudomonas spp, Lactobacillus spp, Enterococcus spp, Alcaligenes spp, Klebsiella spp, Paenibacillus spp, Arthrobacter spp, Corynebacterium spp, Brevibacterium spp, Thermus spp, Pseudomonas spp, Clostridium spp и Escherichia spp. Неограничивающие примеры бактерий, на которые можно целенаправленно воздействовать с помощью способов и композиций, предусмотренных в данном документе, показаны в таблице 1.
Таблица 1. Примеры бактерий-мишеней и насекомых-хозяев
На любое количество видов бактерий можно целенаправленно воздействовать с помощью композиций или способов, описанных в данном документе. Например, в некоторых случаях модулирующее средство может целенаправленно воздействовать на один вид бактерий. В некоторых случаях модулирующее средство может целенаправленно воздействовать на по меньшей мере приблизительно любой из 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 15, 20, 30, 40, 50, 60, 70, 80, 90, 100, 150, 200, 250, 500 или больше различных видов бактерий. В некоторых случаях модулирующее средство может целенаправленно воздействовать на любой из от приблизительно 1 до приблизительно 5, от приблизительно 5 до приблизительно 10, от приблизительно 10 до приблизительно 20, от приблизительно 20 до приблизительно 50, от приблизительно 50 до приблизительно 100, от приблизительно 100 до приблизительно 200, от приблизительно 200 до приблизительно 500, от приблизительно 10 до приблизительно 50, от приблизительно 5 до приблизительно 20 или от приблизительно 10 до приблизительно 100 различных видов бактерий. В некоторых случаях модулирующее средство может целенаправленно воздействовать на по меньшей мере приблизительно любые из 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 15, 20, 30, 40, 50, 60, 70, 80, 90, 100 или больше типов, классов, порядков, семейств или родов бактерий.
В некоторых случаях модулирующее средство может увеличивать популяцию одной или нескольких бактерий (например, симбиотических бактерий) на по меньшей мере приблизительно любое значение из 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90% или больше в организме хозяина по сравнению с организмом-хозяином, которому модулирующее средство не было введено. В некоторых случаях модулирующее средство может уменьшать популяцию одной или нескольких бактерий (например, патогенных или паразитических бактерий) на по меньшей мере приблизительно любое значение из 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90% или больше в организме хозяина по сравнению с организмом-хозяином, которому модулирующее средство не было введено. В некоторых случаях модулирующее средство может уничтожать популяцию бактерии (например, патогенных или паразитических бактерий) в организме хозяина. В некоторых случаях модулирующее средство может повышать уровень одной или нескольких симбиотических бактерий на по меньшей мере приблизительно любое значение из 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90% или больше в организме хозяина и/или может снижать уровень одной или нескольких патогенных бактерий на по меньшей мере приблизительно любое значение из 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90% или больше в организме хозяина по сравнению с организмом-хозяином, которому модулирующее средство не было введено.
В некоторых случаях модулирующее средство может изменять разнообразие бактерий и/или состав бактерий хозяина. В некоторых случаях модулирующее средство может увеличивать разнообразие бактерий в организме хозяина относительно исходного разнообразия на по меньшей мере приблизительно любое значение из 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90% или больше по сравнению с организмом-хозяином, которому модулирующее средство не было введено. В некоторых случаях модулирующее средство может уменьшать разнообразие бактерий в организме хозяина относительно исходного разнообразия на по меньшей мере приблизительно любое значение из 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90% или больше по сравнению с организмом-хозяином, которому модулирующее средство не было введено.
В некоторых случаях модулирующее средство может изменять функцию, активность, рост и/или деление одной или нескольких бактериальных клеток. Например, модулирующее средство может изменять экспрессию одного или нескольких генов в бактерии. В некоторых случаях модулирующее средство может изменять функцию одного или нескольких белков в бактерии. В некоторых случаях модулирующее средство может изменять функцию одной или нескольких клеточных структур (например, клеточной стенки, внешней или внутренней мембраны) в бактерии. В некоторых случаях модулирующее средство может уничтожать (например, лизировать) бактерию.
Бактерия-мишень может обитать в одной или нескольких частях организма насекомого. Кроме того, бактерия-мишень может быть внутриклеточной или внеклеточной. В некоторых случаях бактерии обитают в одной или нескольких частях кишки хозяина, в том числе, например, в передней кишке, средней кишке и/или задней кишке. Например, у медоносных пчел (например, Apis mellifera) бактериальные симбионты, приуроченные к задней кишке взрослых особей, приобретаются в первые несколько дней после выхода взрослых особей из стадии куколки посредством социальных взаимодействий с другими взрослыми рабочими пчелами в колонии. Обитатели кишки медоносной пчелы принадлежат к небольшому количеству характерных линий, встречающихся только у медоносных пчел, а также у других видов Apis и у видов Bombus (шмели). В некоторых случаях бактерии-мишени обитают в организме медоносной пчелы. В некоторых случаях одна или несколько бактерий-мишеней в организме медоносной пчелы представляют собой Snodgrassella spp. (например, Snodgrassella alvi), Gilliamella spp. (например, Gilliamella apicola), Bartonella spp. (например, Bartonella apis), Parasaccharibacter spp. (например, Parasaccharibacter apium) или Lactobacillus spp. (например, Lactobacillus kunkeei, Lactobacillus Firm-4).
В некоторых случаях бактерии обитают в виде внутриклеточных бактерий в клетке насекомого-хозяина. В некоторых случаях бактерии обитают в бактериоците насекомого-хозяина.
Изменения в отношении популяций бактерий в организме хозяина могут быть определены с помощью любых способов, известных в данной области техники, таких как микроматричный анализ, полимеразная цепная реакция (ПЦР), ПЦР в реальном времени, проточная цитометрия, флуоресцентная микроскопия, трансмиссионная электронная микроскопия, флуоресцентная гибридизация in situ (например, FISH), спектрофотометрия, масс-спектрометрия с матрично-активированной лазерной десорбцией/ионизацией (MALDI-MS) и секвенирование ДНК. В некоторых случаях образец от хозяина, обработанного модулирующим средством, секвенируют (например, с помощью метагеномного секвенирования 16S рРНК или рДНК) для определения микробиоты хозяина после доставки или введения модулирующего средства. В некоторых случаях образец от хозяина, который не получал модулирующее средство, также секвенируют для получения эталона.
ii. Грибы
Иллюстративные грибы, на которые можно целенаправленно воздействовать в соответствии со способами и композициями, предусмотренными в данном документе, включают в себя без ограничения Amylostereum areolatum, Epichloe spp, Pichia pinus, Hansenula capsulate, Daldinia decipien, Ceratocytis spp, Ophiostoma spp и Attamyces bromatificus. Неограничивающие примеры дрожжевых и дрожжеподобных симбионтов, обнаруживаемых в организмах насекомых, включают в себя Candida, Metschnikowia, Debaryomyces, Scheffersomyces shehatae и Scheffersomyces stipites, Starmerella, Pichia, Trichosporon, Cryptococcus, Pseudozyma, а также дрожжеподобные симбионты из подтипа Pezizomycotina (например, Symbiotaphrina bucneri и Symbiotaphrina kochii). Неограничивающие примеры дрожжевых грибов, на которые можно целенаправленно воздействовать с помощью способов и композиций согласно данному документу, приведены в таблице 2.
Таблица 2. Примеры дрожжевых грибов у насекомых
H. sycophanta
На любое количество видов грибов можно целенаправленно воздействовать с помощью композиций или способов, описанных в данном документе. Например, в некоторых случаях модулирующее средство может целенаправленно воздействовать на один вид грибов. В некоторых случаях модулирующее средство может целенаправленно воздействовать на по меньшей мере приблизительно любой из 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 15, 20, 30, 40, 50, 60, 70, 80, 90, 100, 150, 200, 250, 500 или больше различных видов грибов. В некоторых случаях модулирующее средство может целенаправленно воздействовать на любой из от приблизительно 1 до приблизительно 5, от приблизительно 5 до приблизительно 10, от приблизительно 10 до приблизительно 20, от приблизительно 20 до приблизительно 50, от приблизительно 50 до приблизительно 100, от приблизительно 100 до приблизительно 200, от приблизительно 200 до приблизительно 500, от приблизительно 10 до приблизительно 50, от приблизительно 5 до приблизительно 20 или от приблизительно 10 до приблизительно 100 различных видов грибов. В некоторых случаях модулирующее средство может целенаправленно воздействовать на по меньшей мере приблизительно любые из 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 15, 20, 30, 40, 50, 60, 70, 80, 90, 100 или больше типов, классов, порядков, семейств или родов грибов.
В некоторых случаях модулирующее средство может увеличивать популяцию одного или нескольких грибов (например, симбиотических грибов) на по меньшей мере приблизительно любое значение из 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90% или больше в организме хозяина по сравнению с организмом-хозяином, которому модулирующее средство не было введено. В некоторых случаях модулирующее средство может уменьшать популяцию одного или нескольких грибов (например, патогенных или паразитических грибов) на по меньшей мере приблизительно любое значение из 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90% или больше в организме хозяина по сравнению с организмом-хозяином, которому модулирующее средство не было введено. В некоторых случаях модулирующее средство может уничтожать популяцию грибов (например, патогенных или паразитических грибов) в организме хозяина. В некоторых случаях модулирующее средство может повышать уровень одного или нескольких симбиотических грибов на по меньшей мере приблизительно любое значение из 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90% или больше в организме хозяина и/или может снижать уровень одного или нескольких патогенных грибов на по меньшей мере приблизительно любое значение из 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90% или больше в организме хозяина по сравнению с организмом-хозяином, которому модулирующее средство не было введено.
В некоторых случаях модулирующее средство может изменять разнообразие грибов и/или состав грибов хозяина. В некоторых случаях модулирующее средство может повышать разнообразие грибов в организме хозяина относительно исходного разнообразия на по меньшей мере приблизительно любое значение из 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90% или больше по сравнению с организмом-хозяином, которому модулирующее средство не было введено. В некоторых случаях модулирующее средство может снижать разнообразие грибов в организме хозяина относительно исходного разнообразия на по меньшей мере приблизительно любое значение из 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90% или больше по сравнению с организмом-хозяином, которому модулирующее средство не было введено.
В некоторых случаях модулирующее средство может изменять функцию, активность, рост и/или деление одного или нескольких грибов. Например, модулирующее средство может изменять экспрессию одного или нескольких генов в грибе. В некоторых случаях модулирующее средство может изменять функцию одного или нескольких белков в грибе. В некоторых случаях модулирующее средство может изменять функцию одного или нескольких клеточных компонентов в грибе. В некоторых случаях модулирующее средство может уничтожать гриб.
Кроме того, гриб-мишень может обитать в одной или нескольких частях организма насекомого. В некоторых случаях гриб обитает в одной или нескольких частях кишки насекомого или на них, в том числе, например, в передней кишке, средней кишке и/или задней кишке. В некоторых случаях гриб живет внеклеточно в гемолимфе, жировых телах или в специализированных структурах в организме хозяина.
Изменения в отношении популяции грибов в организме хозяина могут быть определены с помощью любых способов, известных в данной области техники, таких как микроматричный анализ, полимеразная цепная реакция (ПЦР), ПЦР в реальном времени, проточная цитометрия, флуоресцентная микроскопия, трансмиссионная электронная микроскопия, флуоресцентная гибридизация in situ (например, FISH), спектрофотометрия, масс-спектрометрия с матрично-активированной лазерной десорбцией/ионизацией (MALDI-MS) и секвенирование ДНК. В некоторых случаях образец от хозяина, обработанного модулирующим средством, секвенируют (например, с помощью метагеномного секвенирования) для определения микробиоты хозяина после доставки или введения модулирующего средства. В некоторых случаях образец от хозяина, который не получал модулирующее средство, также секвенируют для получения эталона.
III. Модулирующие средства
Модулирующее средство из способов и композиций, предусмотренных в данном документе, может включать в себя фаг, полипептид, малую молекулу, антибиотик, вторичный метаболит, бактерию или любую их комбинацию.
i. Фаг
Модулирующее средство, описанное в данном документе, может включать в себя фаг (например, литический фаг или нелитический фаг). В некоторых случаях эффективная концентрация любого фага, описанного в данном документе, может изменять уровень, активность или метаболизм одного или нескольких микроорганизмов (описанных в данном документе), обитающих в организме хозяина, описанного в данном документе, при этом изменение приводит к повышению приспособленности хозяина. В некоторых случаях модулирующее средство включает в себя по меньшей мере один фаг, выбранный из порядков Tectiviridae, Myoviridae, Siphoviridae, Podoviridae, Caudovirales, Lipothrixviridae, Rudiviridae или Ligamenvirales. В некоторых случаях композиция содержит по меньшей мере один фаг, выбранный из семейства Myoviridae, Siphoviridae, Podoviridae, Lipothrixviridae, Rudiviridae, Ampullaviridae, Bicaudaviridae, Clavaviridae, Corticoviridae, Cystoviridae, Fuselloviridae, Gluboloviridae, Guttaviridae, Inoviridae, Leviviridae, Microviridae, Plasmaviridae и Tectiviridae. Дополнительные неограничивающие примеры фагов, пригодных в способах и композициях, приведены в таблице 3.
Таблица 3. Примеры фагов и бактерий-мишеней
ΦRSB1 (NC_011201), ΦRSL1 (NC_010811), RSM1 (NC_008574)
В некоторых случаях модулирующее средство включает в себя литический фаг. Таким образом, после доставки литического фага в бактериальную клетку, обитающую в организме хозяина, фаг вызывает лизис в бактериальной клетке-мишени. В некоторых случаях литический фаг целенаправленно воздействует на бактерию, обитающую в организме насекомого-хозяина, и уничтожает ее с повышением приспособленности хозяина. В качестве альтернативы или дополнительно, фаг модулирующего средства может представлять собой нелитический фаг (также называемый лизогенным или умеренным фагом). Таким образом, после доставки нелитического фага в бактериальную клетку, обитающую в организме хозяина, бактериальная клетка может оставаться жизнеспособной и способной стабильно поддерживать экспрессию генов, кодируемых в геноме фага. В некоторых случаях нелитический фаг применяют для изменения экспрессии генов в бактерии, обитающей в организме насекомого-хозяина, с повышением приспособленности хозяина. В некоторых случаях модулирующее средство включает в себя смесь литического и нелитического фага.
Модулирующее средство, описанное в данном документе, может включать в себя фаг с узким или широким спектром бактерий-мишеней. В некоторых случаях фаг имеет узкий спектр бактерий-мишеней. В некоторых случаях фаг представляет собой промискуитетный фаг с широким спектром бактерий-мишеней. Например, промискуитетный фаг может целенаправленно воздействовать на по меньшей мере приблизительно любую из 5, 10, 20, 30, 40, 50 или больше бактерий, обитающих в организме хозяина. Фаг с узким спектром бактерий-мишеней может целенаправленно воздействовать на конкретный штамм бактерий в организме хозяина без отрицательного влияния на другую, например, не являющуюся мишенью, бактерию в организме хозяина. Например, фаг может целенаправленно воздействовать на не более чем приблизительно любую из 50, 40, 30, 20, 10, 8, 6, 4, 2 или 1 бактерии, обитающей в организме хозяина. Например, композиции, описанные в данном документе, могут целенаправленно воздействовать на бактериального патогена Paenibacillus larvae в организме медоносных пчел, но не могут целенаправленно воздействовать на другие бактерии (например, симбиотические бактерии), в том числе Lactobacillus Firm4, Lactobacillus Firm5, Bifidobacterium sp, Snodgrassella alvi, Gilliamella apicola, Bartonella apis, Parasaccharibacter apium или Lactobacillus kunkeei. В некоторых случаях фаг инфицирует одну или несколько конкретных бактерий путем связывания с белком клеточной поверхности (например, OmpF, LamB, BtuB, TolC и т. д.) или с другой распознающей молекулой (например, гликолипидами, LPS, липотейхоевой кислотой и т. д.).
Композиции, описанные в данном документе, могут содержать любое количество фагов, как, например, по меньшей мере приблизительно любое количество из 1, 2, 3, 4, 5, 10, 15, 20, 30, 40, 50, 100 или больше фагов. В некоторых случаях композиция содержит фаг из одного или нескольких семейств (например, 2, 3, 4, 5, 6, 7, 8, 9, 10 или больше фагов), одного или нескольких порядков (например, 2, 3, 4, 5, 6, 7, 8, 9, 10 или больше фагов) или одного или нескольких видов (например, 1, 2, 3, 4, 5, 10, 15, 20, 30, 40, 50, 100 или больше фагов). Композиции, содержащие один или несколько фагов, также называются в данном документе "коктейлями фагов". Коктейли фагов являются пригодными, поскольку они обеспечивают целенаправленное воздействие на более широкий спектр хозяев бактерий. Кроме того, они обеспечивают целенаправленное воздействие на каждый штамм (т. е. подвид) бактерий многочисленных ортогональных фагов, тем самым предупреждая или значительно задерживая появление устойчивости. В некоторых случаях коктейль содержит несколько фагов, целенаправленно воздействующих на один вид бактерий. В некоторых случаях коктейль содержит несколько фагов, целенаправленно воздействующих на несколько видов бактерий. В некоторых случаях в однофаговом "коктейле" содержится один промискуитетный фаг (т. е. фаг с широким спектром хозяев), целенаправленно воздействующий на многие штаммы в пределах вида.
Подходящие концентрации фага в модулирующем средстве, описанном в данном документе, зависят от таких факторов, как эффективность, показатель выживаемости, переносимость фага, количество различных фагов и/или типы лизина в композициях, состав и способы применения композиции. В некоторых случаях фаг находится в жидком или твердом составе. В некоторых случаях концентрация каждого фага в любой из композиций, описанных в данном документе, имеет по меньшей мере приблизительно любое значение из 102, 103, 104, 105, 106, 107, 108, 109, 1010 или больше БОЕ/мл. В некоторых случаях концентрация каждого фага в любой из композиций, описанных в данном документе, имеет не более чем приблизительно любое значение из 102, 103, 104, 105, 106, 107, 108, 109 БОЕ/мл. В некоторых случаях концентрация каждого фага в композиции имеет любое значение из от приблизительно 102 до приблизительно 103, от приблизительно 103 до приблизительно 104, от приблизительно 104 до приблизительно 105, от приблизительно 105 до приблизительно 106, от приблизительно 107 до приблизительно 108, от приблизительно 108 до приблизительно 109, от приблизительно 102 до приблизительно 104, от приблизительно 104 до приблизительно 106, от приблизительно 106 до приблизительно 109 или от приблизительно 103 до приблизительно 108 БОЕ/мл. В некоторых случаях, если композиция содержит по меньшей мере два типа фагов, то концентрация каждого типа фагов может быть одной и той же или разной. Например, в некоторых случаях концентрация одного фага в коктейле составляет приблизительно 108 БОЕ/мл, и концентрация второго фага в коктейле составляет приблизительно 106 БОЕ/мл.
Модулирующее средство, включающее в себя фаг, описанный в данном документе, может быть приведено в контакт с хозяином-мишенью в количестве и в течение времени, достаточных для: (a) достижения целевого уровня (например, предварительно определенного или порогового уровня) концентрации фага внутри хозяина-мишени; (b) достижения целевого уровня (например, предварительно определенного или порогового уровня) концентрации фага внутри кишки хозяина-мишени; (c) достижения целевого уровня (например, предварительно определенного или порогового уровня) концентрации фага внутри бактериоцита хозяина-мишени; (d) модулирования уровня или активности одного или нескольких микроорганизмов (например, эндосимбионтов) в организме хозяина-мишени или/и (e) модулирования приспособленности хозяина-мишени.
Как проиллюстрировано в примерах 7 и 11, фаги можно применять в качестве модулирующих средств при устранении бактериальных патогенов, таких как Serratia marcescens, Erwinia carotovora и Pseudomonas entomophila, из организмов насекомых-хозяев, таких как медоносные пчелы или шелкопряды.
ii. Полипептиды
Многочисленные полипептиды (например, бактериоцин, бактериоцин R-типа, C-богатый пептид клубеньков, противомикробный пептид, лизин или регуляторный пептид бактериоцитов) можно применять в композициях и способах, описанных в данном документе. В некоторых случаях эффективная концентрация любого пептида или полипептида, описанного в данном документе, может изменять уровень, активность или метаболизм одного или нескольких микроорганизмов (описанных выше), обитающих в организме хозяина, при этом изменение приводит к повышению приспособленности хозяина. Полипептиды, включенные в данный документ, могут включать в себя встречающиеся в природе полипептиды или рекомбинантно получаемые варианты. Например, полипептид может представлять собой функционально активный вариант любого из полипептидов, описанных в данном документе, на по меньшей мере 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичный, например, в определенной области или во всей последовательности, последовательности полипептида, описанного в данном документе, или встречающегося в природе полипептида.
Модулирующее средство, включающее в себя полипептид, описанный в данном документе, может быть приведено в контакт с хозяином-мишенью в количестве и в течение времени, достаточных для: (a) достижения целевого уровня (например, предварительно определенного или порогового уровня) концентрации внутри хозяина-мишени; (b) достижения целевого уровня (например, предварительно определенного или порогового уровня) концентрации внутри кишки хозяина-мишени; (c) достижения целевого уровня (например, предварительно определенного или порогового уровня) концентрации внутри бактериоцита хозяина-мишени; (d) модулирования уровня или активности одного или нескольких микроорганизмов (например, эндосимбионтов) в организме хозяина-мишени или/и (e) модулирования приспособленности хозяина-мишени.
Полипептидные модулирующие средства, обсуждаемые далее в данном документе, а именно бактериоцины, лизины, противомикробные пептиды, C-богатые пептиды клубеньков и регуляторные пептиды бактериоцитов, можно применять для изменения уровня, активности или метаболизма микроорганизмов-мишеней, как указано в разделе касательно повышения приспособленности насекомых, таких как медоносные пчелы и шелкопряды.
(a) Бактериоцины
Модулирующее средство, описанное в данном документе, может включать в себя бактериоцин. В некоторых случаях бактериоцин продуцируется естественным образом грамположительными бактериями, такими как Pseudomonas, Streptomyces, Bacillus, Staphylococcus или молочнокислые бактерии (LAB, такие как Lactococcus lactis). В некоторых случаях бактериоцин продуцируется естественным образом грамотрицательными бактериями, такими как Hafnia alvei, Citrobacter freundii, Klebsiella oxytoca, Klebsiella pneumonia, Enterobacter cloacae, Serratia plymithicum, Xanthomonas campestris, Erwinia carotovora, Ralstonia solanacearum или Escherichia coli. Иллюстративные бактериоцины включают в себя без ограничения антибиотики LAB I-IV класса (такие как лантибиотики), колицины, микроцины и пиоцины. Неограничивающие примеры бактериоцинов приведены в таблице 4.
Таблица 4. Примеры бактериоцинов
В некоторых случаях бактериоцин представляет собой колицин, пиоцин или микроцин, продуцируемые грамотрицательными бактериями. В некоторых случаях бактериоцин представляет собой колицин. Колицин может представлять собой колицин группы A (например, использует систему Tol для проникновения через внешнюю мембрану бактерии-мишени) или колицин группы B (например, использует систему Ton для проникновения через внешнюю мембрану бактерии-мишени). В некоторых случаях бактериоцин представляет собой микроцин. Микроцин может представлять собой микроцин класса I (например, < 5 кДа, имеет посттрансляционные модификации) или микроцин класса II (например, 5-10 кДа, с посттрансляционными модификациями или без них). В некоторых случаях микроцин класса II представляет собой микроцин класса IIa (например, требует более одного гена для синтеза и сборки функциональных пептидов) или микроцин класса IIb (например, линейные пептиды с посттрансляционными модификациями на С-конце или без них). В некоторых случаях бактериоцин представляет собой пиоцин. В некоторых случаях пиоцин представляет собой R-пиоцин, F-пиоцин или S-пиоцин.
В некоторых случаях бактериоцин представляет собой бактериоцин класса I, класса II, класса III или класса IV, продуцируемый грамположительными бактериями. В некоторых случаях модулирующее средство включает в себя бактериоцин класса I (например, антибиотики, содержащие лантионин (лантибиотики), продуцируемые грамположительными бактериями). Бактериоцины класса I или лантибиотики могут представлять собой пептид с низкой молекулярной массой (например, менее чем приблизительно 5 кДа) и могут иметь аминокислотные остатки с посттрансляционными модификациями (например, лантионин, β-метиллантионин или дегидрированные аминокислоты).
В некоторых случаях бактериоцин представляет собой бактериоцин класса II (например, соединения, не являющиеся лантибиотиками, продуцируемые грамположительными бактериями). Многие из них являются положительно заряженными не содержащими лантионина пептидами, которые, в отличие от лантибиотиков, не подвергаются обширной посттрансляционной модификации. Бактериоцин класса II может принадлежать к одному из следующих подклассов: "педиоциноподобные" бактериоцины (например, педиоцин PA-1 и карнобактериоцин X (класс IIa)); двухпептидные бактериоцины (например, лактацин F и ABP-118 (класс IIb)); круговые бактериоцины (например, карноциклин А и энтероцин AS-48 (класс IIc)) или немодифицированные линейные непедиоциноподобные бактериоцины (например, эпидермицин NI01 и лактококцин A (класс IId)).
В некоторых случаях бактериоцин представляет собой бактериоцин класса III (например, продуцируемый грамположительными бактериями). Бактериоцины класса III могут иметь молекулярную массу более 10 кДа и могут представлять собой термонестабильные белки. Бактериоцины класса III могут быть дополнительно подразделены на бактериоцины группы IIIA и группы IIIB. Бактериоцины группы IIIA включают в себя бактериолитические ферменты, которые уничтожают восприимчивые штаммы посредством лизиса клеточной стенки, такие как энтеролизин А. Бактериоцины группы IIIB включают в себя нелитические белки, такие как казеицин 80, гельветицин J и лактацин B.
В некоторых случаях бактериоцин представляет собой бактериоцин класса IV (например, продуцируемый грамположительными бактериями). Бактериоцины класса IV представляют собой группу сложных белков, ассоциированных с другими липидными или углеводными фрагментами, которые, по-видимому, требуются для активности. Они являются относительно гидрофобными и термостабильными. Примерами бактериоцинов класса IV являются лейконоцин S, лактоцин 27 и лактоцин S.
В некоторых случаях бактериоцин представляет собой бактериоцин R-типа. Бактериоцины R-типа представляют собой сократительные бактериоцидные белковые комплексы. Некоторые бактериоцины R-типа имеют сократительную структуру, подобную отростку фага. C-концевая область белка нити отростка фага определяет специфичность связывания с мишенью. Они могут прикрепляться к клеткам-мишеням посредством белка, связывающегося с рецептором, например, нити отростка. За прикреплением следует сокращение наружного чехла и введение сердцевины через оболочку бактерии-мишени. Проникновение сердцевины приводит к быстрой деполяризации потенциала клеточной мембраны и мгновенной гибели клетки. Контакт с одной частицей бактериоцина R-типа может приводить к гибели клетки. Бактериоцин R-типа, например, может быть термолабильным, умеренно кислотостойким, устойчивым к трипсину, способным осаждаться в результате центрифугирования, быть различимым при использовании электронной микроскопии или обладать комбинацией этих свойств. Другие бактериоцины R-типа могут представлять собой сложные молекулы, включающие в себя многочисленные белки, полипептиды или субъединицы, и могут напоминать структуру отростка бактериофагов семейства Myoviridae. У встречающихся в природе бактериоцинов R-типа структуры субъединиц могут кодироваться бактериальным геномом, таким как геном C. difficile или P. aeruginosa, и образовывать бактериоцины R-типа, которые выступают в качестве природной защиты против других бактерий. В некоторых случаях бактериоцин R-типа представляет собой пиоцин. В некоторых случаях пиоцин представляет собой R-пиоцин, F-пиоцин или S-пиоцин.
В некоторых случаях бактериоцин представляет собой функционально активный вариант бактериоцинов, описанных в данном документе. В некоторых случаях вариант бактериоцина является на по меньшей мере 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичным, например, в определенной области или во всей последовательности, последовательности бактериоцина, описанного в данном документе, или встречающегося в природе бактериоцина.
В некоторых случаях бактериоцин можно создавать с помощью биоинженерии в соответствии со стандартными способами для модулирования его биологической активности, например, повышения, или снижения, или регулирования, или для определения его микроорганизмов-мишеней. В других случаях бактериоцин продуцируется трансляционным аппаратом (например, рибосомой и т. д.) микробной клетки. В некоторых случаях бактериоцин синтезируют химическим путем. Некоторые бактериоцины могут образовываться из полипептидного предшественника. Полипептидный предшественник может подвергаться расщеплению (например, процессингу под действием протеазы) с образованием самого полипептида бактериоцина. Таким образом, в некоторых случаях бактериоцин продуцируется из полипептида-предшественника. В некоторых других случаях бактериоцин включает в себя полипептид, который подвергся посттрансляционным модификациям, например, расщеплению или добавлению одной или нескольких функциональных групп.
Бактериоцины, описанные в данном документе, могут быть составлены в виде композиции для любого из путей применения, описанных в данном документе. Композиции, раскрытые в данном документе, могут содержать любые количество или тип (например, классы) бактериоцинов, как, например, по меньшей мере приблизительно любое количество из 1 бактериоцина, 2, 3, 4, 5, 10, 15, 20, 30, 40, 50, 100 или больше бактериоцинов. Подходящие концентрации каждого бактериоцина в композициях, описанных в данном документе, зависят от таких факторов, как эффективность, стабильность бактериоцина, количество различных типов бактериоцина в композициях, состав и способы применения композиции. В некоторых случаях концентрация каждого бактериоцина в жидкой композиции составляет от приблизительно 0,01 нг/мл до приблизительно 100 мг/мл. В некоторых случаях концентрация каждого бактериоцина в твердой композиции составляет от приблизительно 0,01 нг/г до приблизительно 100 мг/г. В некоторых случаях, если композиция содержит по меньшей мере два типа бактериоцинов, то концентрация каждого типа бактериоцинов может быть одной и той же или разной. В некоторых случаях бактериоцин предусмотрен в композиции, содержащей бактериальную клетку, которая секретирует бактериоцин. В некоторых случаях бактериоцин предусмотрен в композиции, содержащей полипептид (например, полипептид, выделенный из бактериальной клетки).
Бактериоцины могут нейтрализовать (например, уничтожать) по меньшей мере один микроорганизм, отличный от отдельной бактериальной клетки, в которой полипептид образуется, в том числе клетки, клонально родственные бактериальной клетке, и другие микробные клетки. Таким образом, бактериальная клетка может проявлять цитотоксические или ингибирующие рост эффекты в отношении множества микроорганизмов посредством секреции бактериоцинов. В некоторых случаях бактериоцин целенаправленно воздействует на один или несколько видов бактерий, обитающих в организме хозяина, и уничтожает их посредством образования пор в цитоплазматической мембране, разрушения клеточной стенки (например, активности пептидогликаназы) или активности нуклеазы (например, активности ДНКазы, активности 16S рРНКазы или активности тРНКазы).
В некоторых случаях бактериоцин характеризуется нейтрализующей активностью. Нейтрализующая активность бактериоцинов может включать в себя без ограничения остановку размножения микроорганизмов или цитотоксичность. Некоторые бактериоцины характеризуются цитотоксической активностью, и, таким образом, могут уничтожать микроорганизмы, например, бактерии, дрожжевые грибы, водоросли и т. п. Некоторые бактериоцины могут ингибировать размножение микроорганизмов, например, бактерий, дрожжевых грибов, водорослей и т. п., например, посредством остановки клеточного цикла.
В некоторых случаях бактериоцин характеризуется уничтожающей активностью. Механизм уничтожения у бактериоцинов является специфичным для каждой группы бактериоцинов. В некоторых случаях бактериоцин характеризуется биологической активностью узкого спектра. Бактериоцины известны своей очень высокой активностью в отношении своих штаммов-мишеней. Активность некоторых бактериоцинов ограничена штаммами, которые являются близкородственными по отношению к штамму-продуценту бактериоцина (биологическая активность узкого спектра). В некоторых случаях бактериоцин характеризуется биологической активностью широкого спектра в отношении широкого круга родов.
В некоторых случаях бактериоцины взаимодействуют с рецепторной молекулой или стыковочной молекулой на клеточной мембране бактерии-мишени. Например, низин является крайне активным в отношении своих штаммов бактерий-мишеней, демонстрируя противомикробную активность даже в одноразрядной наномолярной концентрации. Было показано, что молекула низина связывается с липидом II, который является основным переносчиком субъединиц пептидогликанов из цитоплазмы в клеточную стенку.
В некоторых случаях бактериоцин характеризуется противогрибковой активностью. Был идентифицирован ряд бактериоцинов с противодрожжевой или противогрибковой активностью. Например, было показано, что бактериоцины из Bacillus характеризуются нейтрализующей активностью в отношении некоторых штаммов дрожжевых грибов (см., например, Adetunji and Olaoye, Malaysian Journal of Microbiology 9:130-13, 2013). В другом примере было показано, что пептид Enterococcus faecalis характеризуется нейтрализующей активностью в отношении видов Candida (см., например, Shekh and Roy, BMC Microbiology 12:132, 2012). В другом примере было показано, что бактериоцины из Pseudomonas характеризуются нейтрализующей активностью в отношении грибов, таких как Curvularia lunata, виды Fusarium, виды Helminthosporium и виды Biopolaris (см., например, Shalani and Srivastava, The Internet Journal of Microbiology Volume 5 Number 2, 2008). В другом примере было показано, что ботрицидин AJ1316 и алирин B1 из B. subtilis характеризуются противогрибковой активностью.
Модулирующее средство, включающее в себя бактериоцин, описанный в данном документе, может быть приведено в контакт с хозяином-мишенью в количестве и в течение времени, достаточных для: (a) достижения целевого уровня (например, предварительно определенного или порогового уровня) концентрации бактериоцина внутри хозяина-мишени; (b) достижения целевого уровня (например, предварительно определенного или порогового уровня) концентрации бактериоцина внутри кишки хозяина-мишени; (c) достижения целевого уровня (например, предварительно определенного или порогового уровня) концентрации бактериоцина внутри бактериоцита хозяина-мишени; (d) модулирования уровня или активности одного или нескольких микроорганизмов (например, эндосимбионтов) в организме хозяина-мишени или/и (e) модулирования приспособленности хозяина-мишени.
(b) Лизины
Модулирующее средство, описанное в данном документе, может включать в себя лизин (например, также известный как муреингидролаза или аутолизин пептидогликанов). Можно применять любой лизин, подходящий для ингибирования бактерии, обитающей в организме хозяина. В некоторых случаях лизин представляет собой лизин, который может продуцироваться естественным путем бактериальной клеткой. В некоторых случаях лизин представляет собой лизин, который может продуцироваться естественным путем бактериофагом. В некоторых случаях лизин получают из фага, который ингибирует бактерию, обитающую в организме хозяина. В некоторых случаях лизин конструируют на основе встречающегося в природе лизина. В некоторых случаях лизин конструируют для секреции бактерией-хозяином, например, посредством введения сигнального пептида в лизин. В некоторых случаях лизин применяют в комбинации с холином фага. В некоторых случаях лизин экспрессируется рекомбинантным бактериальным хозяином, который не является восприимчивым к лизину. В некоторых случаях лизин применяют для ингибирования грамположительной или грамотрицательной бактерии, обитающей в организме хозяина.
Лизин может представлять собой лизин любого класса и может иметь один или несколько видов субстратной специфичности. Например, лизин может представлять собой гликозидазу, эндопептидазу, карбопептидазу или их комбинацию. В некоторых случаях лизин расщепляет β-1-4-гликозидную связь в сахарном фрагменте клеточной стенки, амидную связь, соединяющую сахарные и пептидные фрагменты бактериальной клеточной стенки, и/или пептидные связи между пептидными фрагментами клеточной стенки. Лизин может принадлежать к одной или нескольким специфическим группам лизина в зависимости от участка расщепления в пептидогликане. В некоторых случаях лизин представляет собой N-ацетил-β-D-мурамидазу (например, лизоцим), литическую трансгликозилазу, N-ацетил-β-D-глюкозаминидазу, N-ацетилмурамил-L-аланинамидазу, L,D-эндопептидазу, D,D-эндопептидазу, D,D-карбоксипептидазу, L,D-карбоксипептидазу или L,D-транспептидазу. Неограничивающие примеры лизинов и форм их активности приведены в таблице 5.
Таблица 5. Примеры лизинов
В некоторых случаях лизин представляет собой функционально активный вариант лизинов, описанных в данном документе. В некоторых случаях вариант лизина является на по меньшей мере 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичным, например, в определенной области или во всей последовательности, последовательности лизина, описанного в данном документе, или встречающегося в природе лизина.
В некоторых случаях лизин можно создавать с помощью биоинженерии для модулирования его биологической активности, например, повышения, или снижения, или регулирования, или для определения его микроорганизма-мишени. В некоторых случаях лизин продуцируется трансляционным аппаратом (например, рибосомой и т. д.) микробной клетки. В некоторых случаях лизин синтезируют химическим путем. В некоторых случаях лизин образуется из полипептидного предшественника. Полипептидный предшественник может подвергаться расщеплению (например, процессингу под действием протеазы) с образованием самого полипептида лизина. Таким образом, в некоторых случаях лизин продуцируется из полипептида-предшественника. В некоторых случаях лизин включает в себя полипептид, который подвергся посттрансляционным модификациям, например, расщеплению или добавлению одной или нескольких функциональных групп.
Лизины, описанные в данном документе, могут быть составлены в виде композиции для любого из путей применения, описанных в данном документе. Композиции, раскрытые в данном документе, могут содержать любые количество или тип (например, классы) лизинов, как, например, по меньшей мере приблизительно любое количество из 1 лизина, 2, 3, 4, 5, 10, 15, 20 или больше лизинов. Подходящая концентрация каждого лизина в композиции зависит от таких факторов, как эффективность, стабильность лизина, количество различных лизинов, состав и способы применения композиции. В некоторых случаях концентрация каждого лизина в жидкой композиции составляет от приблизительно 0,1 нг/мл до приблизительно 100 мг/мл. В некоторых случаях концентрация каждого лизина в твердой композиции составляет от приблизительно 0,1 нг/г до приблизительно 100 мг/г. В некоторых случаях, если композиция содержит по меньшей мере два типа лизинов, то концентрация каждого типа лизинов может быть одной и той же или разной.
Модулирующее средство, включающее в себя лизин, описанный в данном документе, может быть приведено в контакт с хозяином-мишенью в количестве и в течение времени, достаточных для: (a) достижения целевого уровня (например, предварительно определенного или порогового уровня) концентрации лизина внутри хозяина-мишени; (b) достижения целевого уровня (например, предварительно определенного или порогового уровня) концентрации лизина внутри кишки хозяина-мишени; (c) достижения целевого уровня (например, предварительно определенного или порогового уровня) концентрации лизина внутри бактериоцита хозяина-мишени; (d) модулирования уровня или активности одного или нескольких микроорганизмов (например, эндосимбионтов) в организме хозяина-мишени или/и (e) модулирования приспособленности хозяина-мишени.
(c) Противомикробные пептиды
Модулирующее средство, описанное в данном документе, может включать в себя противомикробный пептид (AMP). Можно применять любой AMP, подходящий для ингибирования микроорганизма, обитающего в организме хозяина. AMP представляют собой разнообразную группу молекул, которые разделяются на подгруппы на основании их аминокислотного состава и структуры. AMP могут быть получены из любого организма или продуцироваться в любом организме, который естественным образом продуцирует AMP, в том числе AMP, получаемые из растений (например, копсин), насекомых (например, дрозоцин, пептид скорпиона (например, Uy192, UyCT3, D3, D10, Uy17, Uy192), мастопаран, понератоксин, цекропин, морицин, меллитин), лягушек (например, магаинин, дермасептин, ауреин) и млекопитающих (например, кателицидины, дефензины и протегрины). Например, AMP может представлять собой пептид скорпиона, такой как Uy192 (5'-FLSTIWNGIKGLL-3'; SEQ ID NO: 193), UyCT3 (5'-LSAIWSGIKSLF-3'; SEQ ID NO: 194), D3 (5'-LWGKLWEGVKSLI-3'; SEQ ID NO: 195) и D10 (5'-FPFLKLSLKIPKSAIKSAIKRL-3'; SEQ ID NO: 196), Uy17 (5'-ILSAIWSGIKGLL-3'; SEQ ID NO: 197). Другие неограничивающие примеры AMP приведены в таблице 6.
Таблица 6. Примеры противомикробных пептидов
AMP может быть активным в отношении любого количества микроорганизмов-мишеней. В некоторых случаях AMP может характеризоваться формами антибактериальной и/или противогрибковой активности. В некоторых случаях AMP может характеризоваться биологической активностью узкого спектра или биологической активностью широкого спектра. Например, некоторые AMP целенаправленно воздействуют только на несколько видов бактерий или грибов и уничтожают их, тогда как другие являются активными в отношении как грамотрицательных, так и грамположительных бактерий, а также грибов.
Кроме того, AMP может функционировать посредством ряда известных механизмов действия. Например, цитоплазматическая мембрана представляет собой частую мишень для AMP, однако AMP могут также нарушать синтез ДНК и белка, сворачивание белка и синтез клеточной стенки. В некоторых случаях AMP с суммарным катионным зарядом и амфипатической природой разрушают мембраны бактерий, приводя к лизису клеток. В некоторых случаях AMP могут проникать в клетки и взаимодействовать с внутриклеточной мишенью с нарушением синтеза ДНК, РНК, белка или клеточной стенки. Помимо уничтожения микроорганизмов, AMP продемонстрировали ряд иммуномодулирующих функций, которые вовлечены в устранение инфекции, в том числе способность изменять экспрессию генов хозяев, выступать в роли хемокинов и/или индуцировать продуцирование хемокинов, ингибировать продуцирование провоспалительных цитокинов, индуцированное липополисахаридами, способствовать заживлению ран и модулировать ответы дендритных клеток и клеток, участвующих в адаптивном иммунном ответе.
В некоторых случаях AMP представляет собой функционально активный вариант AMP, описанных в данном документе. В некоторых случаях вариант AMP является на по меньшей мере 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичным, например, в определенной области или во всей последовательности, последовательности AMP, описанного в данном документе, или AMP природного происхождения.
В некоторых случаях AMP можно создавать с помощью биоинженерии для модулирования его биологической активности, например, повышения, или снижения, или регулирования, или для определения его микроорганизма-мишени. В некоторых случаях AMP продуцируется трансляционным аппаратом (например, рибосомой и т. д.) клетки. В некоторых случаях AMP синтезируют химическим путем. В некоторых случаях AMP образуется из полипептидного предшественника. Полипептидный предшественник может подвергаться расщеплению (например, процессингу под действием протеазы) с образованием самого полипептида AMP. Таким образом, в некоторых случаях AMP продуцируется из полипептида-предшественника. В некоторых случаях AMP включает в себя полипептид, который подвергся посттрансляционным модификациям, например, расщеплению или добавлению одной или нескольких функциональных групп.
AMP, описанные в данном документе, могут быть составлены в виде композиции для любого из путей применения, описанных в данном документе. Композиции, раскрытые в данном документе, могут содержать любые количество или тип (например, классы) AMP, как, например, по меньшей мере приблизительно любое количество из 1 AMP, 2, 3, 4, 5, 10, 15, 20 или больше AMP. Подходящая концентрация каждого AMP в композиции зависит от таких факторов, как эффективность, стабильность AMP, количество различных AMP в композиции, состав и способы применения композиции. В некоторых случаях концентрация каждого AMP в жидкой композиции составляет от приблизительно 0,1 нг/мл до приблизительно 100 мг/мл. В некоторых случаях концентрация каждого AMP в твердой композиции составляет от приблизительно 0,1 нг/г до приблизительно 100 мг/г. В некоторых случаях, если композиция содержит по меньшей мере два типа AMP, то концентрация каждого типа AMP может быть одной и той же или разной.
Модулирующее средство, включающее в себя AMP, описанный в данном документе, может быть приведено в контакт с хозяином-мишенью в количестве и в течение времени, достаточных для: (a) достижения целевого уровня (например, предварительно определенного или порогового уровня) концентрации AMP внутри хозяина-мишени; (b) достижения целевого уровня (например, предварительно определенного или порогового уровня) концентрации AMP внутри кишки хозяина-мишени; (c) достижения целевого уровня (например, предварительно определенного или порогового уровня) концентрации AMP внутри бактериоцита хозяина-мишени; (d) модулирования уровня или активности одного или нескольких микроорганизмов (например, эндосимбионтов) в организме хозяина-мишени или/и (e) модулирования приспособленности хозяина-мишени.
(d) C-богатые пептиды клубеньков
Модулирующее средство, описанное в данном документе, может включать в себя C-богатый пептид клубеньков (пептид NCR). Пептиды NCR продуцируются в определенных видах бобовых растений и играют важную роль в мутуалистическом азотфиксирующем симбиозе растений с бактериями из семейства Rhizobiaceae (клубеньковыми бактериями), который приводит к образованию корневых клубеньков, в которых растительные клетки содержат тысячи внутриклеточных эндосимбионтов. Пептиды NCR обладают противомикробными свойствами, управляя необратимым процессом терминальной дифференцировки бактерий, например, с пермеабилизацией мембраны бактерий, нарушением клеточного деления или ингибированием синтеза белка. Например, в клетках клубеньков Medicago truncatula, инфицированных Sinorhizobium meliloti, продуцируются сотни пептидов NCR, которые управляют необратимым процессом дифференцировки бактерий в крупные полиплоидные азотфиксирующие бактероиды. Неограничивающие примеры пептидов NCR приведены в таблице 7.
Таблица 7. Примеры пептидов NCR
Любой пептид NCR, известный в данной области техники, является подходящим для применения в способах или композициях, описанных в данном документе. Растения, продуцирующие пептиды NCR, включают в себя без ограничения Pisum sativum (горох), Astragalus sinicus (бобовые IRLC), Phaseolus vulgaris (фасоль), Vigna unguiculata (коровий горох), Medicago truncatula (люцерну усеченную) и Lotus japonicus. Например, на основании геномной последовательности M. truncatula прогнозируют свыше 600 потенциальных пептидов NCR, и почти 150 различных пептидов NCR были выявлены в клетках, выделенных из корневых клубеньков, с помощью масс-спектрометрии.
Пептиды NCR, описанные в данном документе, могут быть зрелыми или незрелыми пептидами NCR. Незрелые пептиды NCR имеют C-концевой сигнальный пептид, который требуется для транслокации в эндоплазматический ретикулум и отщепляется после транслокации. N-конец пептида NCR содержит сигнальный пептид, который может быть отщепляемым, для нацеливания на секреторный путь. Пептиды NCR, как правило, представляют собой малые пептиды с дисульфидными мостиками, которые стабилизируют их структуры. Зрелые пептиды NCR имеют длину в диапазоне от приблизительно 20 до приблизительно 60 аминокислот, от приблизительно 25 до приблизительно 55 аминокислот, от приблизительно 30 до приблизительно 50 аминокислот, от приблизительно 35 до приблизительно 45 аминокислот или в любом диапазоне в промежутке между этими значениями. Пептиды NCR могут содержать консервативную последовательность из цистеиновых остатков, при этом остальная часть пептидной последовательности является высоковариабельной. Пептиды NCR, как правило, имеют приблизительно четыре или восемь цистеиновых остатков.
Пептиды NCR могут быть анионными, нейтральными или катионными. В некоторых случаях синтетические катионные пептиды NCR, имеющие pI, превышающую приблизительно восемь, обладают формами противомикробной активности. Например, как NCR247 (pI=10,15, RNGCIVDPRCPYQQCRRPLYCRRR; SEQ ID NO: 164), так и NCR335 (pI=11,22) являются эффективными в отношении грамотрицательных и грамположительных бактерий, а также грибов. В некоторых случаях нейтральные и/или анионные пептиды NCR, такие как NCR001 (MAQFLLFVYSLIIFLSLFFGEAAFERTETRMLTIPCTSDDNCPKVISPCHTKCFDGFCGWYIEGSYEGP; SEQ ID NO: 165), не обладают формами противомикробной активности при pI, превышающей приблизительно 8.
В некоторых случаях пептид NCR является эффективным в уничтожении бактерий. В некоторых случаях пептид NCR является эффективным в уничтожении S. meliloti, Xenorhabdus spp, Photorhabdus spp, Candidatus spp, Buchnera spp, Blattabacterium spp, Baumania spp, Wigglesworthia spp, Wolbachia spp, Rickettsia spp, Orientia spp, Sodalis spp, Burkholderia spp, Cupriavidus spp, Frankia spp, Snirhizobium spp, Streptococcus spp, Wolinella spp, Xylella spp, Erwinia spp, Agrobacterium spp, Bacillus spp, Paenibacillus spp, Streptomyces spp, Micrococcus spp, Corynebacterium spp, Acetobacter spp, Cyanobacteria spp, Salmonella spp, Rhodococcus spp, Pseudomonas spp, Lactobacillus spp, Enterococcus spp, Alcaligenes spp, Klebsiella spp, Paenibacillus spp, Arthrobacter spp, Corynebacterium spp, Brevibacterium spp, Thermus spp, Pseudomonas spp, Clostridium spp или Escherichia spp.
В некоторых случаях пептид NCR представляет собой функционально активный вариант пептида NCR, описанного в данном документе. В некоторых случаях вариант пептида NCR является на по меньшей мере 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичным, например, в определенной области или во всей последовательности, последовательности пептида NCR, описанного в данном документе, или пептида NCR природного происхождения.
В некоторых случаях пептид NCR можно создавать с помощью биоинженерии для модулирования его биологической активности, например, повышения, или снижения, или регулирования, или для определения его микроорганизма-мишени. В некоторых случаях пептид NCR продуцируется трансляционным аппаратом (например, рибосомой и т. д.) клетки. В некоторых случаях пептид NCR синтезируют химическим путем. В некоторых случаях пептид NCR образуется из полипептидного предшественника. Полипептидный предшественник может подвергаться расщеплению (например, процессингу под действием протеазы) с образованием самого пептида NCR. Таким образом, в некоторых случаях пептид NCR продуцируется из полипептида-предшественника. В некоторых случаях пептид NCR включает в себя полипептид, который подвергся посттрансляционным модификациям, например, расщеплению или добавлению одной или нескольких функциональных групп.
Пептид NCR, описанный в данном документе, может быть составлен в виде композиции для любого из путей применения, описанных в данном документе. Композиции, раскрытые в данном документе, могут содержать любые количество или тип пептидов NCR, как, например, по меньшей мере приблизительно любое количество из 1 пептида NCR, 2, 3, 4, 5, 10, 15, 20, 30, 40, 50, 100 или больше пептидов NCR. Подходящая концентрация каждого пептида NCR в композиции зависит от таких факторов, как эффективность, стабильность пептида NCR, количество различных пептидов NCR, состав и способы применения композиции. В некоторых случаях концентрация каждого пептида NCR в жидкой композиции составляет от приблизительно 0,1 нг/мл до приблизительно 100 мг/мл. В некоторых случаях концентрация каждого пептида NCR в твердой композиции составляет от приблизительно 0,1 нг/г до приблизительно 100 мг/г. В некоторых случаях, если композиция содержит по меньшей мере два типа пептидов NCR, то концентрация каждого типа пептида NCR может быть одной и той же или разной.
Модулирующее средство, включающее в себя пептид NCR, описанный в данном документе, может быть приведено в контакт с хозяином-мишенью в количестве и в течение времени, достаточных для: (a) достижения целевого уровня (например, предварительно определенного или порогового уровня) концентрации пептида NCR внутри хозяина-мишени; (b) достижения целевого уровня (например, предварительно определенного или порогового уровня) концентрации пептида NCR внутри кишки хозяина-мишени; (c) достижения целевого уровня (например, предварительно определенного или порогового уровня) концентрации пептида NCR внутри бактериоцита хозяина-мишени; (d) модулирования уровня или активности одного или нескольких микроорганизмов (например, эндосимбионтов) в организме хозяина-мишени или/и (e) модулирования приспособленности хозяина-мишени.
(e) Регуляторные пептиды бактериоцитов
Модулирующее средство, описанное в данном документе, может включать в себя регуляторный пептид бактериоцитов (BRP). BRP представляют собой пептиды, экспрессируемые в бактериоцитах насекомых. Эти гены впервые экспрессируются в момент времени развития, совпадающий с включением симбионтов, а их специфичная для бактериоцитов экспрессия поддерживается в течение всей жизни насекомого. В некоторых случаях BRP имеет гидрофобный аминоконцевой домен, который, как предполагается, представляет собой сигнальный пептид. Помимо этого, некоторые BRP имеют домен, богатый цистеином. В некоторых случаях регуляторный пептид бактериоцитов представляет собой специфичный для бактериоцитов белок, богатый цистеином (BCR). Регуляторные пептиды бактериоцитов имеют длину от приблизительно 40 до 150 аминокислот. В некоторых случаях регуляторный пептид бактериоцитов имеет длину в диапазоне от приблизительно 45 до приблизительно 145, от приблизительно 50 до приблизительно 140, от приблизительно 55 до приблизительно 135, от приблизительно 60 до приблизительно 130, от приблизительно 65 до приблизительно 125, от приблизительно 70 до приблизительно 120, от приблизительно 75 до приблизительно 115, от приблизительно 80 до приблизительно 110, от приблизительно 85 до приблизительно 105 или в любом диапазоне в промежутке между этими значениями. Неограничивающие примеры BRP и форм их активности приведены в таблице 8.
Таблица 8. Примеры регуляторных пептидов бактериоцитов
В некоторых случаях BRP изменяет рост и/или активность одной или нескольких бактерий, обитающих в бактериоците хозяина. В некоторых случаях BRP можно создавать с помощью биоинженерии для модулирования его биологической активности (например, повышения, снижения или регулирования) или для определения его микроорганизма-мишени. В некоторых случаях BRP продуцируется трансляционным аппаратом (например, рибосомой и т. д.) клетки. В некоторых случаях BRP синтезируют химическим путем. В некоторых случаях BRP образуется из полипептидного предшественника. Полипептидный предшественник может подвергаться расщеплению (например, процессингу под действием протеазы) с образованием самого полипептида BRP. Таким образом, в некоторых случаях BRP продуцируется из полипептида-предшественника. В некоторых случаях BRP включает в себя полипептид, который подвергся посттрансляционным модификациям, например, расщеплению или добавлению одной или нескольких функциональных групп.
Функционально активные варианты BRP, описанные в данном документе, также пригодны в композициях и способах, описанных в данном документе. В некоторых случаях вариант BRP является на по меньшей мере 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичным, например, в определенной области или во всей последовательности, последовательности BRP, описанного в данном документе, или BRP природного происхождения.
BRP, описанный в данном документе, может быть составлен в виде композиции для любого из путей применения, описанных в данном документе. Композиции, раскрытые в данном документе, могут содержать любые количество или тип (например, классы) BRP, как, например, по меньшей мере приблизительно любое количество из 1 BRP, 2, 3, 4, 5, 10, 15, 20 или больше BRP. Подходящая концентрация каждого BRP в композиции зависит от таких факторов, как эффективность, стабильность BRP, количество различных BRP, состав и способы применения композиции. В некоторых случаях концентрация каждого BRP в жидкой композиции составляет от приблизительно 0,1 нг/мл до приблизительно 100 мг/мл. В некоторых случаях концентрация каждого BRP в твердой композиции составляет от приблизительно 0,1 нг/г до приблизительно 100 мг/г. В некоторых случаях, если композиция содержит по меньшей мере два типа BRP, то концентрация каждого типа BRP может быть одной и той же или разной.
Модулирующее средство, включающее в себя BRP, описанный в данном документе, может быть приведено в контакт с хозяином-мишенью в количестве и в течение времени, достаточных для: (a) достижения целевого уровня (например, предварительно определенного или порогового уровня) концентрации BRP внутри хозяина-мишени; (b) достижения целевого уровня (например, предварительно определенного или порогового уровня) концентрации BRP внутри кишки хозяина-мишени; (c) достижения целевого уровня (например, предварительно определенного или порогового уровня) концентрации BRP внутри бактериоцита хозяина-мишени; (d) модулирования уровня или активности одного или нескольких микроорганизмов (например, эндосимбионтов) в организме хозяина-мишени или/и (e) модулирования приспособленности хозяина-мишени.
iii. Малые молекулы
Многочисленные малые молекулы (например, антибиотик или метаболит) можно применять в композициях и способах, описанных в данном документе. В некоторых случаях эффективная концентрация любой малой молекулы, описанной в данном документе, может изменять уровень, активность или метаболизм одного или нескольких микроорганизмов (описанных выше), обитающих в организме хозяина, при этом изменение приводит к повышению приспособленности хозяина.
Модулирующее средство, включающее в себя малую молекулу, описанную в данном документе, может быть приведено в контакт с хозяином-мишенью в количестве и в течение времени, достаточных для: (a) достижения целевого уровня (например, предварительно определенного или порогового уровня) концентрации малой молекулы внутри хозяина-мишени; (b) достижения целевого уровня (например, предварительно определенного или порогового уровня) концентрации малой молекулы внутри кишки хозяина-мишени; (c) достижения целевого уровня (например, предварительно определенного или порогового уровня) концентрации малой молекулы внутри бактериоцита хозяина-мишени; (d) модулирования уровня или активности одного или нескольких микроорганизмов (например, эндосимбионтов) в организме хозяина-мишени или/и (e) модулирования приспособленности хозяина-мишени.
Малые молекулы, обсуждаемые далее в данном документе, а именно антибиотики и вторичные метаболиты, можно применять для изменения уровня, активности или метаболизма микроорганизмов-мишеней, как указано в разделах касательно повышения приспособленности насекомых, таких как медоносные пчелы и шелкопряды.
(a) Антибиотики
Модулирующее средство, описанное в данном документе, может включать в себя антибиотик. Можно применять любой антибиотик, известный в данной области техники. Антибиотики обычно классифицируются на основании их механизма действия, химической структуры или спектра активности.
Антибиотик, описанный в данном документе, может целенаправленно воздействовать на любую функцию или процессы роста бактерий и может быть как бактериостатическим (например, замедлять или предупреждать рост бактерий), так и бактерицидным (например, уничтожать бактерии). В некоторых случаях антибиотик представляет собой бактерицидный антибиотик. В некоторых случаях бактерицидный антибиотик представляет собой антибиотик, который целенаправленно воздействует на клеточную стенку бактерий (например, пенициллины и цефалоспорины); антибиотик, который целенаправленно воздействует на клеточную мембрану (например, полимиксины); или антибиотик, который ингибирует важнейшие ферменты бактерий (например, рифамицины, липиармицины, хинолоны и сульфонамиды). В некоторых случаях бактерицидный антибиотик представляет собой аминогликозид. В некоторых случаях антибиотик представляет собой бактериостатический антибиотик. В некоторых случаях бактериостатический антибиотик целенаправленно воздействует на синтез белка (например, макролиды, линкозамиды и тетрациклины). Дополнительные классы антибиотиков, которые можно применять в данном документе, включают в себя циклические липопептиды (такие как даптомицин), глицилциклины (такие как тигециклин), оксазолидиноны (такие как линезолид) или липиармицины (такие как фидаксомицин). Примеры антибиотиков включают в себя рифампицин, ципрофлоксацин, доксициклин, ампициллин и полимиксин B. Неограничивающие примеры антибиотиков находятся в таблице 9.
Таблица 9. Примеры антибиотиков
Антибиотик, описанный в данном документе, может характеризоваться любым уровнем специфичности к мишеням (например, узким или широким спектром действия). В некоторых случаях антибиотик представляет собой антибиотик узкого спектра действия и, таким образом, целенаправленно воздействует на конкретные типы бактерий, такие как грамотрицательные или грамположительные бактерии. В качестве альтернативы, антибиотик может представлять собой антибиотик широкого спектра действия, который целенаправленно воздействует на широкий круг бактерий.
Антибиотики, описанные в данном документе, могут быть составлены в виде композиции для любого из путей применения, описанных в данном документе. Композиции, раскрытые в данном документе, могут содержать любые количество или тип (например, классы) антибиотиков, как, например, по меньшей мере приблизительно любое количество из 1 антибиотика, 2, 3, 4, 5, 10, 15, 20 или больше антибиотиков (например, комбинацию рифампицина и доксициклина или комбинацию ампициллина и рифампицина). Подходящая концентрация каждого антибиотика в композиции зависит от таких факторов, как эффективность, стабильность антибиотика, количество различных антибиотиков, состав и способы применения композиции. В некоторых случаях, если композиция содержит по меньшей мере два типа антибиотиков, то концентрация каждого типа антибиотика может быть одной и той же или разной.
Модулирующее средство, включающее в себя антибиотик, описанный в данном документе, может быть приведено в контакт с хозяином-мишенью в количестве и в течение времени, достаточных для: (a) достижения целевого уровня (например, предварительно определенного или порогового уровня) концентрации антибиотика внутри хозяина-мишени; (b) достижения целевого уровня (например, предварительно определенного или порогового уровня) концентрации антибиотика внутри кишки хозяина-мишени; (c) достижения целевого уровня (например, предварительно определенного или порогового уровня) концентрации антибиотика внутри бактериоцита хозяина-мишени; (d) модулирования уровня или активности одного или нескольких микроорганизмов (например, эндосимбионтов) в организме хозяина-мишени или/и (e) модулирования приспособленности хозяина-мишени.
(b) Вторичные метаболиты
В некоторых случаях модулирующее средство в композициях и способах, описанных в данном документе, включает в себя вторичный метаболит. Вторичные метаболиты образуются из органических молекул, продуцируемых организмом. Вторичные метаболиты могут выступать (i) в качестве конкурентных средств, применяемых в отношении бактерий, грибов, амеб, растений, насекомых и крупных животных; (ii) в качестве средств, транспортирующих металлы; (iii) в качестве средств симбиоза между микроорганизмами и растениями, нематодами, насекомыми и более крупными животными; (iv) в качестве половых гормонов и (v) в качестве эффекторов дифференцировки. Неограничивающие примеры вторичных метаболитов находятся в таблице 10.
Таблица 10. Примеры вторичных метаболитов
Вторичный метаболит, применяемый в данном документе, может включать в себя метаболит из любой известной группы вторичных метаболитов. Например, вторичные метаболиты можно классифицировать на следующие группы: алкалоиды, терпеноиды, флавоноиды, гликозиды, природные фенолы (например, госсиполуксусная кислота), енали (например, транс-коричный альдегид), феназины, бифенолы и дибензофураны, поликетиды, пептиды синтазы жирных кислот, нерибосомальные пептиды, пептиды, синтезируемые в рибосомах и подвергающиеся посттрансляционным модификациям, полифенолы, полисахариды (например, хитозан) и биополимеры. Углубленный обзор вторичных метаболитов см., например, в Vining, Annu. Rev. Microbiol. 44:395-427, 1990.
Вторичные метаболиты, пригодные для композиций и способов, описанных в данном документе, включают в себя метаболиты, которые изменяют природную функцию эндосимбионта (например, первичного или вторичного эндосимбионта), бактериоцита или внеклеточного симбионта. В некоторых случаях один или несколько вторичных метаболитов, описанных в данном документе, выделяют в результате высокопроизводительного скрининга (HTS) противомикробных соединений. Например, скрининг HTS выявил 49 антибактериальных экстрактов, которые характеризуются специфичностью в отношении грамположительных и грамотрицательных бактерий, из свыше 39000 неочищенных экстрактов из организмов, растущих в различных экосистемах одного конкретного региона. В некоторых случаях вторичный метаболит транспортируется внутрь бактериоцита.
В некоторых случаях малая молекула представляет собой ингибитор синтеза витаминов. В некоторых случаях ингибитор синтеза витаминов представляет собой аналог предшественника витамина. В определенных случаях аналог предшественника витамина представляет собой пантотенол.
В некоторых случаях малая молекула представляет собой аналог аминокислоты. В определенных случаях аналог аминокислоты представляет собой L-канаванин, D-аргинин, D-валин, D-метионин, D-фенилаланин, D-гистидин, D-триптофан, D-треонин, D-лейцин, L-NG-нитроаргинин или их комбинацию.
В некоторых случаях малая молекула представляет собой природное противомикробное соединение, такое как пропионовая кислота, левулиновая кислота, транс-коричный альдегид, низин или низкомолекулярный хитозан. Вторичный метаболит, описанный в данном документе, может быть составлен в виде композиции для любого из путей применения, описанных в данном документе. Композиции, раскрытые в данном документе, могут содержать любые количество или тип (например, классы) вторичных метаболитов, как, например, по меньшей мере приблизительно любое количество из 1 вторичного метаболита, 2, 3, 4, 5, 10, 15, 20 или больше вторичных метаболитов. Подходящая концентрация каждого вторичного метаболита в композиции зависит от таких факторов, как эффективность, стабильность вторичного метаболита, количество различных вторичных метаболитов, состав и способы применения композиции. В некоторых случаях, если композиция содержит по меньшей мере два типа вторичных метаболитов, то концентрация каждого типа вторичного метаболита может быть одной и той же или разной.
Модулирующее средство, включающее в себя вторичный метаболит, описанный в данном документе, может быть приведено в контакт с хозяином-мишенью в количестве и в течение времени, достаточных для: (a) достижения целевого уровня (например, предварительно определенного или порогового уровня) концентрации вторичного метаболита внутри хозяина-мишени; (b) достижения целевого уровня (например, предварительно определенного или порогового уровня) концентрации вторичного метаболита внутри кишки хозяина-мишени; (c) достижения целевого уровня (например, предварительно определенного или порогового уровня) концентрации вторичного метаболита внутри бактериоцита хозяина-мишени; (d) модулирования уровня или активности одного или нескольких микроорганизмов (например, эндосимбионтов) в организме хозяина-мишени или/и (e) модулирования приспособленности хозяина-мишени.
iv. Бактерии в качестве модулирующих средств
В некоторых случаях модулирующее средство, описанное в данном документе, включает в себя одну или несколько бактерий. Многочисленные бактерии являются пригодными в композициях и способах, описанных в данном документе. В некоторых случаях средство представляет собой вид бактерий, обнаруживаемый эндогенно в организме хозяина. В некоторых случаях бактериальное модулирующее средство представляет собой вид эндосимбиотических бактерий. Неограничивающие примеры бактерий, которые можно применять в качестве модулирующих средств, включают в себя все виды бактерий, описанные в данном документе в разделе II подробного описания, и виды бактерий, приведенные в таблице 1, начиная со страницы 15. Например, модулирующее средство может представлять собой вид бактерий из любого типа бактерий, присутствующего в кишках насекомых, в том числе Gammaproteobacteria, Alphaproteobacteria, Betaproteobacteria, Bacteroidetes, Firmicutes (например, Lactobacillus и Bacillus spp.), Clostridia, Actinomycetes, Spirochetes, Verrucomicrobia и Actinobacteria.
В некоторых случаях модулирующее средство представляет собой бактерию, которая содействует разнообразию микроорганизмов или в других отношениях изменяет микробиоту хозяина благоприятным образом. В одном случае могут быть предусмотрены бактерии, содействующие развитию микробиома у медоносных пчел. Например, модулирующее средство может включать в себя, например, Bartonella apis, Parasaccharibacter apium, Frischella perrara, Snodgrassella alvi, Gilliamela apicola, Bifidobacterium spp или Lactobacillus spp.
Бактериальные модулирующие средства, обсуждаемые в данном документе, можно применять для изменения уровня, активности или метаболизма микроорганизмов-мишеней, как указано в разделах касательно повышения приспособленности насекомых, таких как медоносные пчелы и шелкопряды.
В некоторых случаях такие бактериальные модулирующие средства представляют собой бактерии, способные расщеплять пестициды, изложенные в таблице 12, в том числе инсектициды. Такие инсектициды включают в себя неоникотиноиды, такие как имидаклоприд, или фосфорорганические инсектициды, такие как фенитротион. В некоторых случаях бактерии, метаболизирующие пестициды, присутствуют в концентрации по меньшей мере 100000 клеток/мл (например, по меньшей мере приблизительно 100000 клеток/мл, по меньшей мере приблизительно 150000 клеток/мл, по меньшей мере приблизительно 200000 клеток/мл, по меньшей мере приблизительно 250000 клеток/мл, по меньшей мере приблизительно 300000 клеток/мл, по меньшей мере приблизительно 350000 клеток/мл, по меньшей мере приблизительно 400000 клеток/мл, по меньшей мере приблизительно 450000 клеток/мл или по меньшей мере приблизительно 500000 клеток/мл).
В примерах 1-3, 5 и 6 описывается, как могут быть идентифицированы микроорганизмы, расщепляющие имидаклоприд и фенитротион, которые затем могут применяться в качестве модулирующих средств в организмах насекомых-хозяев, таких как медоносные пчелы, что дает обработанным насекомым-хозяевам конкурентное преимущество. Следует понимать, что изменение уровня, активности или метаболизма одного или нескольких микроорганизмов, обитающих в организме хозяина, охватывает введение таких микроорганизмов, расщепляющих пестициды, например, микроорганизмов, расщепляющих имидаклоприд или фенитротион, насекомым-хозяевам, таким как медоносные пчелы.
В некоторых случаях такие бактериальные модулирующие средства представляют собой бактерии, способные продуцировать питательные вещества, в том числе аминокислоты (например, метионин или глутамат). Бактерии, продуцирующие питательные вещества, могут являться встречающимися в природе бактериями, например, встречающимися в природе бактериями, экзогенными для насекомых-хозяев. Такие бактерии могут быть выделены из популяции бактерий, такой как популяция, обнаруживаемая в образце окружающей среды. Могут быть выделены бактерии, которые продуцируют одну или несколько аминокислот таким образом, при котором у хозяина увеличивается продуцирование аминокислот по сравнению с хозяином, которому не были введены бактерии, продуцирующие аминокислоты. Аминокислоты, которые могут продуцироваться бактериями в организме хозяина, включают в себя метионин, аланин, аргинин, аспарагин, аспарагиновую кислоту, цистеин, глутамин, глутаминовую кислоту, глутамат, глицин, гистидин, изолейцин, лейцин, лизин, метионин, фенилаланин, пролин, серин, треонин, триптофан, тирозин или валин. В некоторых случаях бактерии, продуцирующие аминокислоты, представляют собой бактерии, продуцирующие метионин.
В некоторых случаях бактерии, продуцирующие питательные вещества (например, бактерии, продуцирующие аминокислоты, например, бактерии, продуцирующие метионин) присутствуют в концентрации по меньшей мере 100000 клеток/мл (например, по меньшей мере приблизительно 100000 клеток/мл, по меньшей мере приблизительно 150000 клеток/мл, по меньшей мере приблизительно 200000 клеток/мл, по меньшей мере приблизительно 250000 клеток/мл, по меньшей мере приблизительно 300000 клеток/мл, по меньшей мере приблизительно 350000 клеток/мл, по меньшей мере приблизительно 400000 клеток/мл, по меньшей мере приблизительно 450000 клеток/мл или по меньшей мере приблизительно 500000 клеток/мл).
В примерах 8, 9 и 10 описывается, как могут быть идентифицированы микроорганизмы, продуцирующие метионин, которые затем могут применяться в качестве модулирующих средств в организмах насекомых-хозяев, таких как медоносные пчелы, или в модельном организме Drosophila для повышения приспособленности хозяев (например, для повышения содержания аминокислот (например, содержания метионина или содержания глутамата)).
v. Модификации в отношении модулирующих средств
(a) Продукты слияния
Любое из модулирующих средств, описанных в данном документе, может быть слито или связано с дополнительным фрагментом. В некоторых случаях модулирующее средство включает в себя продукт слияния одного или нескольких дополнительных фрагментов (например, 1 дополнительного фрагмента, 2, 3, 4, 5, 6, 7, 8, 9, 10 или больше дополнительных фрагментов). В некоторых случаях дополнительный фрагмент представляет собой любое из модулирующих средств, описанных в данном документе (например, пептид, полипептид, малую молекулу или антибиотик). В качестве альтернативы, дополнительный фрагмент может сам по себе не выступать в качестве модулирующего средства, однако вместо этого может выполнять вторичную функцию. Например, дополнительный фрагмент может облегчать доступ, связывание или активирование модулирующего средства в участке-мишени в организме хозяина (например, в кишке хозяина или бактериоците хозяина) или в микроорганизме-мишени, обитающем в организме хозяина (например, медоносной пчелы или шелкопряда).
В некоторых случаях дополнительный фрагмент может облегчать проникновение модулирующего средства в клетку хозяина-мишени или микроорганизм-мишень, обитающий в организме хозяина. Например, дополнительный фрагмент может включать в себя пептид, проникающий в клетку. Пептиды, проникающие в клетку (CPP), могут представлять собой природные последовательности, полученные из белков; химерные пептиды, которые образуются в результате слияния двух природных последовательностей; или синтетические CPP, которые представляют собой последовательности, сконструированные синтетическим путем на основании исследований взаимосвязи структуры и активности. В некоторых случаях CPP характеризуются способностью повсеместно проникать через клеточные мембраны (например, клеточные мембраны прокариот и эукариот) с ограниченной токсичностью. Кроме того, CPP могут характеризоваться способностью проникать через клеточные мембраны посредством энергозависимых и/или энергонезависимых механизмов без необходимости хирального распознавания специфическими рецепторами. CPP могут связываться с любыми из модулирующих средств, описанных в данном документе. Например, CPP может связываться с противомикробным пептидом (AMP), например, пептидом скорпиона, например, UY192, слитым с пептидом, проникающим в клетку (например, YGRKKRRQRRRFLSTIWNGIKGLLFAM; SEQ ID NO: 198). Неограничивающие примеры CPP приведены в таблице 11.
Таблица 11. Примеры пептидов, проникающих в клетку (CPP)
В других случаях дополнительный фрагмент облегчает связывание модулирующего средства с микроорганизмом-мишенью (например, грибом или бактерией), обитающим в организме хозяина. Дополнительный фрагмент может включать в себя один или несколько нацеливающих доменов. В некоторых случаях нацеливающий домен может нацеливать модулирующее средство на один или несколько микроорганизмов (например, бактерию или гриб), обитающих в кишке хозяина. В некоторых случаях нацеливающий домен может нацеливать модулирующее средство на конкретную область в организме хозяина (например, кишку или бактериоцит хозяина) для доступа к микроорганизмам, которые обычно присутствуют в указанной области организма хозяина. Например, нацеливающий домен может нацеливать модулирующее средство на переднюю кишку, среднюю кишку или заднюю кишку хозяина. В других случаях нацеливающий домен может нацеливать модулирующее средство на бактериоцит в организме хозяина и/или одну или несколько конкретных бактерий, обитающих в бактериоците хозяина. Например, нацеливающий домен может представлять собой лектин или агглютинин Galanthus nivalis (GNA), связанный с модулирующим средством, описанным в данном документе, например, AMP, например, пептидом скорпиона, например, Uy192.
(b) Пре- или продомены
В некоторых случаях модулирующее средство может включать в себя аминокислотную пре- или пропоследовательность. Например, модулирующее средство может представлять собой неактивный белок или пептид, которые могут быть активированы посредством расщепления или посттрансляционной модификации пре- или пропоследовательности. В некоторых случаях модулирующее средство конструируют с инактивирующей пре- или пропоследовательностью. Например, пре- или пропоследовательность может закрывать сайт активации на модулирующем средстве, например, сайт связывания с рецептором, или может индуцировать конформационное изменение в модулирующем средстве. Таким образом, при отщеплении пре- или пропоследовательности модулирующее средство активируется.
В качестве альтернативы, модулирующее средство может включать в себя малую пре- или промолекулу, например, антибиотик. Модулирующее средство может представлять собой неактивную малую молекулу, описанную в данном документе, которая может быть активирована в среде-мишени внутри хозяина. Например, малая молекула может быть активирована при достижении определенного значения pH в кишке хозяина.
(c) Линкеры
В случаях, если модулирующее средство связано с дополнительным фрагментом, модулирующее средство может дополнительно содержать линкер. Например, линкер может представлять собой химическую связь, например, одну или несколько ковалентных связей или нековалентных связей. В некоторых случаях линкер может представлять собой пептидный линкер (например, длиной 2, 3, 4, 5, 6, 8, 10, 12, 14, 16, 20, 25, 30, 35, 40 или больше аминокислот). Линкер может включать в себя любые гибкие, жесткие или расщепляемые линкеры, описанные в данном документе.
Гибкий пептидный линкер может включать в себя любой из линкеров, широко применяемых в данной области техники, в том числе линкеры, имеющие последовательности, содержащие главным образом остатки Gly и Ser (линкер "GS"). Гибкие линкеры могут быть пригодны для соединения доменов, которые требуют определенной степени подвижности или взаимодействия, и могут содержать небольшие, неполярные (например, Gly) или полярные (например, Ser или Thr) аминокислоты.
В качестве альтернативы, пептидный линкер может представлять собой жесткий линкер. Жесткие линкеры пригодны для сохранения фиксированного расстояния между фрагментами и поддержания их независимых функций. Жесткие линкеры также могут быть пригодны, если пространственное разделение доменов является важным для сохранения стабильности или биологической активности одного или нескольких компонентов в продукте слияния. Жесткие линкеры, например, могут иметь альфа-спиральную структуру или Pro-богатую последовательность, (XP)n, при этом X обозначает любую аминокислоту, предпочтительно Ala, Lys или Glu.
В еще нескольких случаях пептидный линкер может представлять собой расщепляемый линкер. В некоторых случаях линкеры могут расщепляться в специфических условиях, таких как присутствие восстанавливающих реагентов или протеаз. Расщепляемые in vivo линкеры могут использовать обратимую природу дисульфидной связи. Один пример включает в себя чувствительную к тромбину последовательность (например, PRS) между двумя остатками Cys. Обработка тромбином CPRSC in vitro приводит к расщеплению чувствительной к тромбину последовательности, тогда как обратимая дисульфидная связь остается интактной. Такие линкеры известны и описаны, например, в Chen et al., Adv. Drug Deliv. Rev. 65(10):1357-1369, 2013. Расщепление линкеров в продуктах слияния также может осуществляться протеазами, которые экспрессируются в условиях in vivo в конкретных клетках или тканях хозяина или микроорганизмах, обитающих в организме хозяина. В некоторых случаях при достижении участка- или клетки-мишени в результате расщепления линкера может высвобождаться свободное функциональное модулирующее средство.
Продукты слияния, описанные в данном документе, в качестве альтернативы могут быть связаны со связывающей молекулой, в том числе гидрофобным линкером, таким как отрицательно заряженная сульфонатная группа; липидами, такими как поли(--CH2--)углеводородные цепи, такие как полиэтиленгликолевая (PEG) группа, их ненасыщенными вариантами, их гидроксилированными вариантами, их амидированными или в других отношениях N-содержащими вариантами, неуглеродными линкерами; углеводными линкерами; фосфодиэфирными линкерами или другими молекулами, способными ковалентно связывать две или более молекул, например, два модулирующих средства. Можно применять нековалентные линкеры, такие как гидрофобные липидные глобулы, с которыми связывается модулирующее средство, например, посредством гидрофобной области модулирующего средства или гидрофобного удлинения модулирующего средства, такого как ряд остатков, богатый лейцином, изолейцином, валином или, возможно, также аланином, фенилаланином или даже тирозином, метионином, глицином или другим гидрофобным остатком. Модулирующее средство может быть связано с помощью химического взаимодействия зарядов таким образом, что положительно заряженный фрагмент модулирующего средства связывается с отрицательно заряженным другим модулирующим средством или дополнительным фрагментом.
IV. Составы и композиции
Композиции, описанные в данном документе, могут быть составлены в чистой форме (например, композиция содержит только модулирующее средство) либо совместно с одним или несколькими дополнительными средствами (такими как наполнитель, средство доставки, носитель, разбавитель, стабилизатор и т. д.) для облегчения применения или доставки композиций. Примеры подходящих наполнителей и разбавителей включают в себя без ограничения лактозу, декстрозу, сахарозу, сорбит, маннит, крахмалы, аравийскую камедь, фосфат кальция, альгинаты, трагакант, желатин, силикат кальция, микрокристаллическую целлюлозу, поливинилпирролидон, целлюлозу, воду, солевой раствор, сироп, метилцеллюлозу, метил- и пропилгидроксибензоаты, тальк, стеарат магния и минеральное масло.
В некоторых случаях композиция содержит средство доставки или носитель. В некоторых случаях средство доставки включает в себя наполнитель. Иллюстративные наполнители включают в себя без ограничения твердые или жидкие материалы-носители, растворители, стабилизаторы, наполнители для составов с замедленным высвобождением, красители и поверхностно-активные вещества (поверхностно-активные средства). В некоторых случаях средство доставки представляет собой стабилизирующее средство доставки. В некоторых случаях стабилизирующее средство доставки включает в себя стабилизирующий наполнитель. Иллюстративные стабилизирующие наполнители включают в себя без ограничения эпоксидированные растительные масла, противовспенивающие средства, например, силиконовое масло, консерванты, регуляторы вязкости, связующие средства и средства, придающие липкость. В некоторых случаях стабилизирующее средство доставки представляет собой буфер, подходящий для модулирующего средства. В некоторых случаях композиция является микроинкапсулированной в средство доставки на основе полимерных гранул. В некоторых случаях стабилизирующее средство доставки защищает модулирующее средство от УФ и/или кислых условий. В некоторых случаях средство доставки содержит pH-буфер. В некоторых случаях композиция составлена таким образом, что она имеет pH в диапазоне от приблизительно 4,5 до приблизительно 9,0, включая, например, любой из диапазонов pH от приблизительно 5,0 до приблизительно 8,0, от приблизительно 6,5 до приблизительно 7,5 или от приблизительно 6,5 до приблизительно 7,0.
В зависимости от предполагаемых целей и преобладающих обстоятельств композиция может быть составлена в виде концентратов эмульсий, концентратов суспензий, непосредственно распыляемых или разбавляемых растворов, паст, наносимых в виде покрытия, разбавленных эмульсий, распыляемых порошков, растворимых порошков, диспергируемых порошков, смачиваемых порошков, пылевидных препаратов, гранул, форм, инкапсулированных в полимерные вещества, микрокапсул, пен, аэрозолей, препаратов на основе газообразного диоксида углерода, таблеток, препаратов на основе смол, препаратов на основе бумаги, препаратов на основе нетканого полотна или препаратов на основе трикотажного или тканого полотна. В некоторых случаях композиция представляет собой жидкость. В некоторых случаях композиция представляет собой твердое вещество. В некоторых случаях композиция представляет собой аэрозоль, как, например, в находящемся под давлением аэрозольном баллончике. В некоторых случаях композиция присутствует в отходах (таких как экскременты) вредителя. В некоторых случаях композиция присутствует внутри или на поверхности тела живого вредителя.
В некоторых случаях средство доставки представляет собой пищу или воду для хозяина. В других случаях средство доставки представляет собой источник пищи для хозяина. В некоторых случаях средство доставки представляет собой пищевую приманку для хозяина. В некоторых случаях композиция представляет собой съедобное средство, поглощаемое хозяином. В некоторых случаях композиция доставляется хозяином второму хозяину и поглощается вторым хозяином. В некоторых случаях композиция поглощается хозяином или вторым хозяином, и композиция высвобождается в окружение хозяина или второго хозяина с отходами (такими как экскременты) хозяина или второго хозяина. В некоторых случаях модулирующее средство включено в пищевую приманку, предназначенную для поглощения хозяином или переноса назад в его колонию.
В некоторых случаях модулирующее средство может составлять от приблизительно 0,1% до приблизительно 100% композиции, как, например, любое количество из от приблизительно 0,01% до приблизительно 100%, от приблизительно 1% до приблизительно 99,9%, от приблизительно 0,1% до приблизительно 10%, от приблизительно 1% до приблизительно 25%, от приблизительно 10% до приблизительно 50%, от приблизительно 50% до приблизительно 99% или от приблизительно 0,1% до приблизительно 90% активных ингредиентов (таких как фаг, лизин или бактериоцин). В некоторых случаях композиция содержит по меньшей мере любое количество из 0,1%, 0,5%, 1%, 5%, 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 95% или больше активных ингредиентов (таких как фаг, лизин и бактериоцин). В некоторых случаях концентрированные средства являются предпочтительными в качестве коммерческих продуктов, а конечный потребитель, как правило, использует разведенные средства, которые имеют значительно более низкую концентрацию активного ингредиента.
Любой из составов, описанных в данном документе, можно применять в форме приманки, спирали, электрического коврика, дымящегося препарата, фумиганта или листа.
i. Жидкие составы
Композиции, предусмотренные в данном документе, могут находиться в форме жидкого состава. Жидкие составы, как правило, смешивают с водой, однако в некоторых случаях их можно применять с растительным маслом, дизельным топливом, керосином или другим легким маслом в качестве носителя. Количество активного ингредиента часто находится в диапазоне от приблизительно 0,5 до приблизительно 80 процентов по весу.
Состав в виде концентрата эмульсии может содержать жидкий активный ингредиент, один или несколько растворителей на нефтяной основе и средство, которое способствует смешиванию состава с водой с образованием эмульсии. Такие концентраты можно применять в составах для сельского хозяйства, декоративных и газонных растений, лесного хозяйства, обработки зданий, обработки пищевых продуктов, сельскохозяйственных животных и вредителей, значимых для общественного здравоохранения. Их можно адаптировать для эксплуатационного оборудования от небольших переносных опрыскивателей до гидравлических опрыскивателей, малообъемных наземных опрыскивателей, вентиляторных туманообразователей и малообъемных авиационных опрыскивателей. Некоторые активные ингредиенты легко растворяются в жидком носителе. При смешивании с носителем они образуют раствор, в котором не происходит осаждение или разделение, например, гомогенный раствор. Составы этого типа могут содержать активный ингредиент, носитель и один или несколько других ингредиентов. Растворы можно применять в любом типе распылителя, в закрытом помещении и на свежем воздухе.
В некоторых случаях композиция может быть составлена в виде обратной эмульсии. Обратная эмульсия представляет собой водорастворимый активный ингредиент, диспергированный в масляном носителе. Обратные эмульсии требуют эмульгатора, который способствует смешиванию активного ингредиента с большим объемом носителя на нефтяной основе, обычно топливного масла. Обратные эмульсии способствуют снижению сноса. В случае других составов некоторый снос при распылении происходит, когда капли воды начинают испаряться до достижения целевых поверхностей; в результате этого капли могут стать очень маленькими и легковесными. Поскольку масло испаряется более медленно, чем вода, капли обратной эмульсии сжимаются меньше, и большее количество активного ингредиента достигает цели. Масло дополнительно способствует снижению поверхностного стока и повышает устойчивость к дождю. Оно дополнительно выступает в качестве адгезивного средства, улучшая степень покрытия поверхности и всасывание. Поскольку капли являются сравнительно большими и тяжелыми, то им сложно пройти насквозь покрытие нижней стороны листьев. Обратные эмульсии наиболее широко применяются в полосах отчуждения, где снос на восприимчивые нецелевые площади может быть проблемой.
Текучий или жидкий состав объединяет многие из характеристик концентратов эмульсий и смачиваемых порошков. Изготовители используют эти составы, если активный ингредиент представляет собой твердое вещество, которое не растворяется ни в воде, ни в масле. Активный ингредиент, пропитанный веществом, таким как глина, измельчают до очень мелкого порошка. Затем порошок суспендируют в небольшом количестве жидкости. Образующийся в результате жидкий продукт является достаточно плотным. Текучие и жидкие составы имеют многие из характеристик концентратов эмульсий, а также они имеют аналогичные недостатки. Они требуют умеренного взбалтывания для поддержания их в виде суспензии и оставляют видимые остатки, аналогичные таковым у смачиваемых порошков.
Текучие/жидкие составы являются легкими в обращении и применении. Поскольку они представляют собой жидкости, то они подлежат разбрызгиванию и расплескиванию. Они содержат твердые частицы, поэтому они способствуют абразивному износу насадок и насосов. Текучие и жидкие суспензии осаждаются в своих контейнерах. Поскольку текучие и жидкие составы склонны к осаждению, упаковка в контейнеры по пять галлонов или меньше облегчает повторное смешивание.
Аэрозольные составы содержат один или несколько активных ингредиентов и растворитель. Большинство аэрозолей имеют низкое процентное содержание активных ингредиентов. Существует два типа аэрозольных составов - готовый к применению тип, широко доступный в находящихся под давлением запечатанных контейнерах, и продукты, используемые в электрических или работающих на бензине аэрозольных генераторах, которые высвобождают состав в виде дыма или тумана.
Готовые к применению аэрозольные составы обычно представляют собой небольшие автономные блоки, которые высвобождают состав, когда клапан насадки приводится в движение. Состав пропускается через тонкое отверстие с помощью инертного газа под давлением с образованием мелкодисперсных капель. Эти продукты используются в теплицах, на небольших площадях внутри зданий или на ограниченных площадях на открытом воздухе. Коммерческие модели, которые удерживают до 5 фунтов активного ингредиента, обычно являются многоразовыми.
Дымообразующие или туманообразующие аэрозольные составы не находятся под давлением. Они используются в машинах, которые разбивают жидкий состав на мелкодисперсный туман или густой туман (аэрозоль) с помощью быстро вращающегося диска или нагреваемой поверхности.
ii. Сухие или твердые составы
Сухие составы могут быть разделены на два типа: готовые к применению и концентраты, которые должны быть смешаны с водой для применения в качестве спрея. Большинство пылевидных составов являются готовыми к применению и имеют низкое процентное содержание активных ингредиентов (меньше чем приблизительно 10 процентов по весу) наряду с очень тонкодисперсным сухим инертным носителем, изготовленным из талька, мела, глины, ореховой скорлупы или вулканического пепла. Размер отдельных пылевидных частиц варьируется. Некоторые пылевидные составы представляют собой концентраты и имеют высокое процентное содержание активных ингредиентов. Перед применением их смешивают с сухими инертными носителями. Порошки всегда используются сухими и могут легко сноситься на нецелевые участки.
iii. Гранулированные или пеллетированные составы
В некоторых случаях композиция составлена в виде гранул. Гранулированные составы аналогичны пылевидным составам, за исключением того, что гранулированные частицы являются более крупными и тяжелыми. Крупнодисперсные частицы могут быть получены из таких материалов, как глина, кукурузные початки или скорлупа грецких орехов. Активный ингредиент покрывает наружную поверхность гранул или всасывается в них. Количество активного ингредиента может быть относительно малым, обычно находясь в диапазоне от приблизительно 0,5 до приблизительно 15 процентов по весу. Гранулированные составы наиболее часто используются для применения в отношении почвы, насекомых или нематод, живущих в почве, или всасывания растениями через корни. Гранулированные составы иногда применяют с использованием самолета или вертолета с целью сведения к минимуму сноса или проникновения в густые заросли. После применения гранулы могут медленно высвобождать активный ингредиент. Некоторые гранулы требуют почвенной влаги для высвобождения активного ингредиента. Гранулированные составы также используются для контроля личинок комаров и других водных вредителей. Гранулы используются в операциях контроля вредителей в сельском хозяйстве, при обработке зданий, на декоративных и газонных растениях, в водной среде, в полосах отчуждения, а также в общественном здравоохранении (в отношении жалящих насекомых).
В некоторых случаях композиция составлена в виде пеллет. Большинство пеллетированных составов являются весьма сходными с гранулированными составами; эти термины используются взаимозаменяемо. Однако в пеллетированном составе все частицы имеют одну и ту же массу и форму. Однородность частиц облегчает применение с использованием точного эксплуатационного оборудования.
iv. Порошки
В некоторых случаях композиция составлена в виде порошка. В некоторых случаях композиция составлена в виде смачиваемого порошка. Смачиваемые порошки представляют собой сухие тонкоизмельченные составы, которые выглядят как пылевидные препараты. Обычно они должны смешиваться с водой для применения в качестве спрея. Однако, немного продуктов можно применять в качестве пылевидного препарата или в качестве смачиваемого порошка - выбор остается за потребителем. Смачиваемые порошки имеют от приблизительно 1 до приблизительно 95 процентов по весу активного ингредиента; в некоторых случаях более чем приблизительно 50 процентов. Частицы не растворяются в воде. Они быстро осаждаются, если их постоянно не взбалтывать для поддержания в суспендированном состоянии. Их можно применять для решения большинства проблем, связанных с вредителями, и в большинстве типов распылительного оборудования, в которых возможно взбалтывание. Смачиваемые порошки обладают превосходной остаточной активностью. В связи с их физическими свойствами большинство состава остается на поверхности обработанных пористых материалов, таких как бетон, штукатурка и необработанная древесина. В таких случаях только вода проникает в материал.
В некоторых случаях композиция составлена в виде растворимого порошка. Растворимые порошковые составы выглядят как смачиваемые порошки. В то же время при смешивании с водой растворимые порошки легко растворяются и образуют истинный раствор. После их тщательного смешивания дополнительное взбалтывание не требуется. Количество активного ингредиента в растворимых порошках находится в диапазоне от приблизительно 15 до приблизительно 95 процентов по весу; в некоторых случаях более чем приблизительно 50 процентов. Растворимые порошки имеют все преимущества смачиваемых порошков и ни одного из недостатков, за исключением опасности вдыхания во время смешивания.
В некоторых случаях композиция составлена в виде гранул, диспергируемых в воде. Гранулы, диспергируемые в воде, также известные как сухие текучие составы, подобны смачиваемым порошкам за исключением того, что являются пылевидными, и их составляют в виде небольших легко определяемых гранул. Гранулы, диспергируемые в воде, должны быть смешаны с водой перед применением. Оказавшись в воде, гранулы распадаются на мелкодисперсные частицы, аналогичные смачиваемым порошкам. Состав требует непрерывного взбалтывания для поддержания его в суспендированном состоянии в воде. Процентное содержание активного ингредиента является высоким, часто не менее 90 процентов по весу. Гранулы, диспергируемые в воде, имеют многие из тех же самых преимуществ и недостатков смачиваемых порошков, за исключением того, что они являются более легко определяемыми и смешиваемыми. В связи с низким содержанием пылевидных частиц они обуславливают меньшую опасность вдыхания для потребителя во время использования.
v. Приманка
В некоторых случаях композиция включает в себя приманку. Приманка может находиться в любой подходящей форме, такой как твердое вещество, паста, пеллетированная или порошкообразная форма. Приманка также может переноситься хозяином назад в популяцию указанного хозяина (например, колонию или улей). Приманка может затем выступать в качестве источника пищи для других членов колонии, тем самым предоставляя эффективное модулирующее средство большому числу хозяев и потенциально всей колонии хозяина.
Приманки могут быть предоставлены в подходящем "домике" или "ловушке". Такие домики и ловушки являются коммерчески доступными, и существующие ловушки могут быть адаптированы для включения композиций, описанных в данном документе. Домик или ловушка могут быть предусмотрены, например, в форме коробки, и могут быть предусмотрены в готовом виде или могут быть изготовлены, например, из складывающегося картона. Подходящие материалы для домика или ловушки включают в себя пластмассу и картон, в частности, гофрированный картон. Внутренние поверхности ловушек могут быть выстланы липким веществом с целью ограничения движения хозяина при попадании в ловушку. Домик или ловушка могут содержать подходящую бороздку внутри, которая может удерживать приманку на месте. Ловушка отличается от домика, поскольку хозяин не может легко покинуть ловушку после попадания, тогда как домик выступает в качестве "кормушки", которая обеспечивает хозяина предпочтительной средой, в которой они могут кормиться и чувствовать себя в безопасности от хищников.
vi. Аттрактанты
В некоторых случаях композиция содержит аттрактант (например, хемоаттрактант). Аттрактант может привлекать взрослого хозяина или неполовозрелого хозяина (например, личинку) к месту поблизости композиции. Аттрактанты включают в себя феромоны - химические вещества, которые секретируются животным, в частности насекомым, которые влияют на поведение или развитие других особей этого же вида. Другие аттрактанты включают в себя сахарные сиропы и сиропы на основе гидролизатов белков, дрожжевые грибы и гниющее мясо. Аттрактанты также можно объединять с активным ингредиентом и распылять на листья или другие предметы в обрабатываемой области.
Известны различные аттрактанты, которые влияют на поведение хозяина, например, поиск хозяином пищи, мест для откладывания яиц или спаривания или партнеров для спаривания. Аттрактанты, пригодные в способах и композициях, описанных в данном документе, включают в себя, например, эвгенол, фенэтилпропионат, этилдиметилизобутилциклопропанкарбоксилат, пропилбензодиоксанкарбоксилат, цис-7,8-эпокси-2-метилоктадекан, транс-8,транс-0-додекадиенол, цис-9-тетрадеценаль (и цис-11-гексадеценаль), транс-11-тетрадеценаль, цис-11-гексадеценаль, (Z)-11,12-гексадекадиеналь, цис-7-додеценилацетат, цис-8-додеценилацетат, цис-9-додеценилацетат, цис-9-тетрадеценилацетат, цис-11-тетрадеценилацетат, транс-11-тетрадеценилацетат (и цис-11), цис-9,транс-11-тетрадекадиенилацетат (и цис-9,транс-12), цис-9,транс-12-тетрадекадиенилацетат, цис-7,цис-11-гексадекадиенилацетат (и цис-7,транс-11), цис-3,цис-13-октадекадиенилацетат, транс-3,цис-13-октадекадиенилацетат, анетол и изоамилсалицилат.
Для привлечения насекомых также можно применять средства, отличные от хемоаттрактантов, в том числе осветительные устройства с различными длинами волн или цветами излучения.
vii. Нанокапсулы/микроинкапсулирование/липосомы
В некоторых случаях композиция предусмотрена в виде микроинкапсулированного состава. Микроинкапсулированные составы смешивают с водой и распыляют таким же образом, как и другие распыляемые составы. После распыления пластмассовые покрытия разрушаются и медленно высвобождают активный ингредиент.
viii. Носители
Любая из композиций, описанных в данном документе, может быть составлена с включением модулирующего средства, описанного в данном документе, и инертного носителя. Такой носитель может представлять собой твердый носитель, жидкий носитель, гелеобразный носитель и/или газообразный носитель. В определенных вариантах осуществления носитель может представлять собой средство для нанесения покрытия на семена. Средство для нанесения покрытия на семена представляет собой любой не встречающийся в природе состав, который прилипает, целиком или частично, к поверхности семени. Состав может дополнительно содержать вспомогательное вещество или поверхностно-активное вещество. Состав может также содержать одно или несколько модулирующих средств для расширения спектра действия.
Твердый носитель, используемый для состава, включает в себя мелкодисперсный порошок или гранулы глины (например, каолиновой глины, диатомовой земли, бентонитовой глины, глины Фубасами, кислой глины и т. д.), синтетический гидратированный диоксид кремния, тальк, керамические материалы, другие неорганические материалы (например, серицит, кварц, серу, активированный уголь, карбонат кальция, гидратированный диоксид кремния и т. д.), вещество, которое может быть сублимировано и находится в твердой форме при комнатной температуре (например, 2,4,6-триизопропил-1,3,5-триоксан, нафталин, п-дихлорбензол, камфору, адамантан и т. д.); шерсть; шелк; хлопок; пеньку; жом; синтетические смолы (например, полиэтиленовые смолы, такие как полиэтилен низкой плотности, немодифицированный полиэтилен низкой плотности и полиэтилен высокой плотности; сополимеры этилена и винилового сложного эфира, такие как сополимеры этилена и винилацетата; сополимеры этилена и сложного эфира метакриловой кислоты, такие как сополимеры этилена и метилметакрилата и сополимеры этилена и этилметакрилата; сополимеры этилена и сложного эфира акриловой кислоты, такие как сополимеры этилена и метилакрилата и сополимеры этилена и этилакрилата; сополимеры этилена и винилкарбоновой кислоты, такие как сополимеры этилена и акриловой кислоты; сополимеры этилена и тетрациклододецена; полипропиленовые смолы, такие как гомополимеры пропилена и сополимеры пропилена и этилена; поли-4-метилпентен-1, полибутен-1, полибутадиен, полистирол; смолы на основе сополимера акрилонитрила и стирола; стирольные эластомеры, такие как смолы на основе сополимера акрилонитрила, бутадиена и стирола, блок-сополимеры диенов с сопряженными двойными связями и стирола и гидриды блок-сополимеров диенов с сопряженными двойными связями и стирола; фторкаучуки; акриловые смолы, такие как поли(метилметакрилат); полиамидные смолы, такие как нейлон 6 и нейлон 66; полиэфирные смолы, такие как полиэтилентерефталат, полиэтиленнафталат, полибутилентерефталат и полициклогексилендиметилентерефталат, поликарбонаты, полиацетали, полиакрилсульфоны, полиарилаты, полиэфиры гидроксибензойной кислоты, полиэфиримиды, полиэфиркарбонаты, полифениленэфирные смолы, поливинилхлорид, поливинилиденхлорид, полиуретан и пористые смолы, такие как пенополиуретан, пенополипропилен или пеноэтилен и т. д.), стекла, металлы, керамические материалы, волокнистые материалы, ткани, трикотажные полотна, листы, бумагу, пряжу, пену, пористые вещества и мультифиламенты.
Жидкий носитель может включать в себя, например, ароматические или алифатические углеводороды (например, ксилол, толуол, алкилнафталин, фенилксилилэтан, керосин, газойль, гексан, циклогексан и т. д.), галогензамещенные углеводороды (например, хлорбензол, дихлорметан, дихлорэтан, трихлорэтан и т. д.), спирты (например, метанол, этанол, изопропиловый спирт, бутанол, гексанол, бензиловый спирт, этиленгликоль и т. д.), эфиры (например, диэтиловый эфир, диметиловый эфир этиленгликоля, монометиловый эфир диэтиленгликоля, моноэтиловый эфир диэтиленгликоля, монометиловый эфир пропиленгликоля, тетрагидрофуран, диоксан и т. д.), сложные эфиры (например, этилацетат, бутилацетат и т. д.), кетоны (например, ацетон, метилэтилкетон, метилизобутилкетон, циклогексанон и т. д.), нитрилы (например, ацетонитрил, изобутиронитрил и т. д.), сульфоксиды (например, диметилсульфоксид и т. д.), амиды (например, N,N-диметилформамид, N,N-диметилацетамид, циклические имиды (например, N-метилпирролидон), алкилиденкарбонаты (например, пропиленкарбонат и т. д.), растительное масло (например, соевое масло, хлопковое масло и т. д.), растительные эфирные масла (например, апельсиновое масло, масло иссопа, лимонное масло и т. д.) или воду.
Газообразный носитель может включать в себя, например, газообразный бутан, газообразный политетрафторэтилен, сжиженный нефтяной газ (LPG), диметиловый эфир и газообразный диоксид углерода.
ix. Вспомогательные вещества
В некоторых случаях композиция, предусмотренная в данном документе, может содержать вспомогательное вещество. Вспомогательные вещества представляют собой химические вещества, которые не обладают активностью. Вспомогательные вещества предварительно смешивают в составе или добавляют в распылительный резервуар для улучшения смешивания или применения или для усиления функциональных характеристик. Они широко используются в продуктах, предназначенных для применения в отношении листьев. Вспомогательные вещества можно использовать для придания индивидуальных свойств составу в соответствии с конкретными нуждами и введения поправки на местные условия. Вспомогательные вещества могут быть предназначены для осуществления конкретных функций, в том числе смачивания, распределения, прилипания, снижения испарения, снижения улетучивания, буферизации, эмульгирования, диспергирования, снижения сноса при распылении и снижения пенообразования. Ни одно вспомогательное вещество не может осуществлять все эти функции само по себе, однако совместимые вспомогательные вещества часто можно объединять для осуществления нескольких функций одновременно.
Среди неограничивающих примеров вспомогательных веществ, включенных в состав, присутствуют связующие вещества, диспергирующие вещества и стабилизаторы, в частности, например, казеин, желатин, полисахариды (например, крахмал, аравийская камедь, производные целлюлозы, альгиновая кислота и т. д.), производные лигнина, бентонит, сахара, синтетические водорастворимые полимеры (например, поливиниловый спирт, поливинилпирролидон, полиакриловая кислота и т. д.), PAP (кислый изопропилфосфат), BHT (2,6-ди-трет-бутил-4-метилфенол), BHA (смесь 2-трет-бутил-4-метоксифенола и 3-трет-бутил-4-метоксифенола), растительные масла, минеральные масла, жирные кислоты и сложные эфиры жирных кислот.
x. Поверхностно-активные вещества
В некоторых случаях композиция, предусмотренная в данном документе, содержит поверхностно-активное вещество. Поверхностно-активные вещества, также называемые смачивающими средствами и распределителями, физически изменяют поверхностное натяжение капли спрея. Для того, чтобы состав надлежащим образом выполнял свою функцию, капля спрея должна быть способной смачивать листья и распределяться равномерно по листу. Поверхностно-активные вещества увеличивают площадь, покрываемую составом, тем самым усиливая воздействие химического вещества на вредителя. Поверхностно-активные вещества особенно важны при применении состава в отношении листьев, покрытых воском, или волосистых листьев. Без надлежащего смачивания и распределения капли спрея часто стекают или не могут покрыть поверхности листьев надлежащим образом. В то же время слишком большое количество поверхностно-активного вещества может вызвать избыточный поверхностный сток и снизить эффективность.
Поверхностно-активные вещества классифицируются на основе способа их ионизации или расщепления на электрически заряженные атомы или молекулы, называемые ионами. Поверхностно-активное вещество с отрицательным зарядом является анионным. Поверхностно-активное вещество с положительным зарядом является катионным, и поверхностно-активное вещество без электрического заряда является неионогенным. Активность состава в присутствии неионогенного поверхностно-активного вещества может значительно отличаться от активности в присутствии катионного или анионного поверхностно-активного вещества. Выбор неправильного поверхностно-активного вещества может снижать эффективность пестицидного продукта и наносить вред растению-мишени. Анионные поверхностно-активные вещества являются наиболее эффективными при использовании с контактными пестицидами (пестициды, которые контролируют вредителя путем непосредственного контакта, а не системного всасывания). Катионные поверхностно-активные вещества никогда не должны применяться в качестве самостоятельных поверхностно-активных веществ, поскольку они обычно являются фитотоксичными.
Неионогенные поверхностно-активные вещества, часто применяемые с системными пестицидами, облегчают проникновение пестицидных спреев через кутикулы растений. Неионогенные поверхностно-активные вещества совместимы с большинством пестицидов, и для большинства пестицидов, зарегистрированных EPA, которым необходимо поверхностно-активное вещество, рекомендуется неионогенный тип. Вспомогательные вещества включают в себя без ограничения клеящие вещества, сухие разбавители, вещества, обеспечивающие проникновение в растения, факторы совместимости, буферы или модификаторы pH, дополнительные компоненты для контроля сноса, противовспенивающие средства и загустители.
Среди неограничивающих примеров поверхностно-активных веществ, включенных в композиции, описанные в данном документе, присутствуют соли алкилсульфатных сложных эфиров, алкилсульфонаты, аклиларилсульфонаты, алкилариловые эфиры и их полиоксиэтиленированные продукты, простые эфиры полиэтиленгликоля, сложные эфиры многоатомных спиртов и производные сахарных спиртов.
xi. Комбинации
В составах и в применяемых формах, полученных из этих составов, модулирующее средство может находиться в смеси с другими активными соединениями, такими как пестицидные средства (например, инсектициды, стерилизаторы, акарициды, нематоциды, моллюскоциды или фунгициды; см., например, пестициды, приведенные в таблице 12), аттрактанты, вещества, регулирующие рост, или гербициды. Используемый в данном документе термин "пестицидное средство" относится к любому веществу или смеси веществ, предусмотренных для предупреждения воздействия, нарушения воздействия, отпугивания или ослабления воздействия любого вредителя. Пестицид может представлять собой химическое вещество или биологическое средство, применяемое против вредителей, в том числе насекомых, моллюсков, патогенов, сорняков, нематод и микроорганизмов, которые конкурируют с человеком за пищу, разрушают имущество, распространяют заболевания или представляют собой негативный раздражитель. Термин "пестицидное средство" может дополнительно охватывать другие биологически активные молекулы, такие как антибиотики, противовирусные пестициды, противогрибковые средства, антигельминтные средства, питательные вещества, пыльцу, сахарозу и/или средства, которые останавливают или замедляют движение насекомых.
В случаях, когда модулирующее средство применяют в отношении растений, смесь с другими известными соединениями, такими как гербициды, удобрения, регуляторы роста, антидоты, химические сигнальные вещества или другие средства для улучшения свойств растения, также является возможной.
V. Доставка
Хозяин, описанный в данном документе, может подвергаться воздействию любой из композиций, описанных в данном документе, любым подходящим образом, который обеспечивает доставку или введение композиции насекомому. Модулирующее средство может быть доставлено в отдельности или в комбинации с другими активными или неактивными веществами и может применяться, например, посредством распыления, микроинъекции, через растения, посредством полива, погружения, в форме концентрированных жидкостей, гелей, растворов, суспензий, спреев, порошков, пеллет, брикетов, плиток и т. п., составленных для доставки эффективной концентрации модулирующего средства.
Количества и места для применения композиций, описанных в данном документе, как правило, определяются условиями обитания хозяина, стадией жизненного цикла, на которой на микроорганизмы хозяина можно целенаправленно воздействовать с помощью модулирующего средства, участком, в котором применение должно выполняться, а также физическими и функциональными характеристиками модулирующего средства. Модулирующие средства, описанные в данном документе, можно вводить насекомому путем перорального заглатывания, однако также можно вводить с помощью средств, которые обеспечивают проникновение через кутикулу или проникновение в дыхательную систему насекомого.
В некоторых случаях насекомое может быть просто "намочено" или "опрыскано" раствором, содержащим модулирующее средство. В качестве альтернативы, модулирующее средство может быть связано с пищевым компонентом (например, съедобным) для насекомого для облегчения доставки и/или в целях повышения поглощения модулирующего средства насекомым. Способы перорального введения включают в себя, например, непосредственное смешивание модулирующего средства с пищей для насекомого, распыление модулирующего средства в среде обитания насекомого или поле, а также подходы на основе конструирования, в которых вид, который применяется в качестве пищи, конструируется с целью экспрессии модулирующего средства, после чего скармливается насекомому, подлежащему отрицательному влиянию. В некоторых случаях, например, композиция на основе модулирующего средства может быть включена в состав рациона насекомого или покрывать его сверху. Например, композицию на основе модулирующего средства можно распылять на поле с сельскохозяйственными культурами, на которых насекомое обитает.
В некоторых случаях композицию распыляют непосредственно на растение, например, сельскохозяйственные культуры, например, путем распыления из рюкзака, распыления с воздуха, опрыскивания/опыления растительных культур и т. д. В случаях, когда модулирующее средство доставляют в растение, растение, получающее модулирующее средство, может находиться на любой стадии роста растения. Например, составленные модулирующие средства можно применять в виде покрытия для семян или средства для обработки корней на ранних стадиях роста растения или в виде средства для полной обработки растения на более поздних стадиях цикла урожая. В некоторых случаях модулирующее средство можно применять в отношении растения в качестве местного средства, так чтобы насекомое-хозяин заглатывало или иным образом приходило в контакт с растением при взаимодействии с растением.
Кроме того, модулирующее средство можно применять (например, в отношении почвы, в которой растение растет, или в отношении воды, которую используют для полива растения) в качестве системного средства, которое поглощается и распределяется по тканям (например, стеблям или листьям) растения-хозяина или животного-хозяина таким образом, что насекомое, питающееся на нем, будет получать эффективную дозу модулирующего средства. В некоторых случаях растения или организмы, используемые в качестве пищи, могут быть генетически трансформированы для экспрессии модулирующего средства, так чтобы хозяин, питающийся на растении или организме, используемом в качестве пищи, заглатывал модулирующее средство.
Замедленное или непрерывное высвобождение также может достигаться посредством покрытия модулирующего средства или композиции с модулирующим(модулирующими) средством(средствами) растворимым или биоразрушаемым слоем покрытия, таким так желатин, при этом данное покрытие растворяется или разрушается в среде применения, что затем делает модулирующее средство доступным, или посредством диспергирования средства в растворимой или разрушаемой матрице. Такое непрерывное высвобождение и/или распределение означает, что устройства могут быть предпочтительно использованы для устойчивого поддержания эффективной концентрации одного или нескольких модулирующих средств, описанных в данном документе, в конкретной среде обитания хозяина.
Модулирующее средство также может быть включено в среду, в которой насекомое растет, живет, размножается, питается или осуществляет заражение. Например, модулирующее средство может быть включено в контейнер для пищи, кормушку, защитную обертку или улей. В некоторых путях применения модулирующее средство может быть связано с твердой подложкой для применения в порошкообразной форме или в "ловушке" или "кормушке". В качестве примера, в путях применения, в которых композиция подлежит применению в ловушке или в виде приманки для определенного насекомого-хозяина, композиции также могут быть связаны с твердой подложкой или инкапсулированы в материал с медленным высвобождением. Например, в случаях, когда хозяином является медоносная пчела, композиции, описанные в данном документе, можно вводить посредством доставки композиции в улей с медоносными пчелами или в по меньшей мере одну среду обитания, где медоносная пчела растет, живет, размножается или питается.
VI. Скрининг
В данный документ включены скрининговые анализы для идентификации модулирующего средства, где модулирующее средство является эффективным для изменения микробиоты хозяина и повышения тем самым приспособленности хозяина (например, приспособленности насекомого или нематоды). Например, скрининговый анализ можно применять для идентификации одного или нескольких модулирующих средств, которые целенаправленно воздействуют на конкретные микроорганизмы и/или конкретных хозяев. Кроме того, скрининговые анализы можно применять для идентификации одного или нескольких микроорганизмов с улучшенными функциональными способностями. Например, скрининговый анализ может быть эффективным для выделения одного или нескольких микроорганизмов с улучшенной способностью метаболизировать (например, расщеплять) пестицид (например, пестицид, приведенный в таблице 12, или инсектицид, известный из уровня техники, например, неоникотиноид (например, имидаклоприд) или фосфорорганический инсектицид (например, тиофосфатный инсектицид, например, фенитротион)) или растительный аллелохимикат (например, кофеин, цистатин N сои, монотерпены, дитерпеновые кислоты или фенольные соединения). Доставка и колонизация выделенного микроорганизма в организме хозяина может повышать устойчивость хозяина к пестициду (например, пестициду, приведенному в таблице 12) или растительному аллелохимикату, повышая тем самым приспособленность хозяина. Способы также могут быть пригодны для выделения микроорганизмов с улучшенной способностью колонизировать организм любого из хозяев, описанных в данном документе.
Например, для скрининга микроорганизмов, которые повышают устойчивость хозяина к пестициду (например, пестициду, приведенному в таблице 12), можно применять стартовую культуру, которая содержит микроорганизмы (например, бактерии) и высокие концентрации пестицида (например, пестицида, приведенного в таблице 12, или инсектицида, известного из уровня техники, например, неоникотиноида (например, имидаклоприда) или фосфорорганического инсектицида (например, тиофосфатного инсектицида, например, фенитротиона)). В некоторых случаях пестицид может быть предусмотрен в форме образца окружающей среды, обогащенного пестицидом (например, образец почвы). В качестве альтернативы, пестицид (например, пестицид, приведенный в таблице 12) может быть предусмотрен в чистой форме или в комбинации с другими носителями. Кроме того, один или несколько изолятов микроорганизмов могут быть инокулированы непосредственно в среду (например, из лабораторного штамма) или могут представлять собой образец окружающей среды, содержащий один или несколько видов микроорганизмов. Среда для роста может быть жидкой либо твердой. В некоторых случаях пестицид, представляющий интерес, является единственным источником углерода или азота для микроорганизмов в среде. Культура может быть субкультивирована (например, инокулирована в свежую среду с высокими уровнями пестицида) любое количество раз для обогащения штаммами микроорганизмов (например, штаммами бактерий), способными метаболизировать пестицид, и/или их выделения. Исходная культура или субкультуры могут быть оценены с использованием любых способов, известных из уровня техники, для исследования изменений (например, снижения) уровней пестицида в образце (например, с помощью HPLC). Изоляты, которые снижают концентрацию пестицида (например, пестицида, приведенного в таблице 12, или пестицида, известного из уровня техники, например, неоникотиноида (например, имидаклоприда) или фосфорорганического инсектицида (например, тиофосфатного инсектицида, например, фенитротиона)), могут быть выделены для применения в качестве модулирующего средства в любых способах или композициях, описанных в данном документе.
Способы можно применять для дальнейшего отбора микроорганизмов, описанных в данном документе, в том числе выделенных на основании скринингового анализа, с улучшенной способностью колонизировать организм хозяина (например, насекомого, например, пчелы) и выживать в нем. Например, в организм хозяина можно инокулировать бактериальный изолят (например, изолят, обладающий способностью расщеплять пестицид). Затем хозяина можно исследовать через регулярные промежутки времени на наличие бактериального изолята (например, посредством культивирования или выделения 16s РНК из кишок хозяина (например, медоносной пчелы)). Бактериальные изоляты, которые выживают в организме хозяина (например, в средней кишке медоносной пчелы), могут быть выделены для применения в качестве модулирующего средства в любых способах или композициях, описанных в данном документе.
ПРИМЕРЫ
Далее представлен пример способов по настоящему изобретению. Следует понимать, что на практике могут осуществляться различные другие варианты осуществления c учетом общего описания, приведенного выше.
Пример 1. Выделение микроорганизмов, которые расщепляют никотиноид имидаклоприд
Данный пример демонстрирует получение библиотеки микроорганизмов, способных расщеплять неоникотиноид имидаклоприд.
Схема эксперимента
Собирали четыре образца почвы с повышенными концентрациями имидаклоприда, как описано в Bonmatin et al. (Environ. Sci. Pollut. Res. Int. 22:35-67, 2015) и разбавляли в среде Кауфмана-Керни с минимальным содержанием солей (MSM) для обогащения микроорганизмами, расщепляющими имидаклоприд. Три варианта культур для каждого образца почвы включали следующее: 50 мл MSM с ограниченным содержанием углерода с 83 мг/л имидаклоприда в качестве единственного источника углерода; 50 мл MSM с ограниченным содержанием азота с имидаклопридом в качестве единственного источника азота, а также цитратом натрия и сахарозой, добавленными в качестве дополнительных источников углерода; и 50 мл бульона MSM со всеми компонентами с добавлением цитрата натрия, сахарозы и имидаклоприда. В каждую культуру инокулировали 2 г собранной почвы.
Культуры выдерживали на шейкере при 100 об/мин и 27°С. Субкультуры (1 мл культивируемого раствора, разбавленного в 25 мл новой среды) готовили ежемесячно, чтобы получить обогащенные образцы без использования почвы. Аликвоты культур периодически отбирали из колб шейкера для HPLC-анализа, как описано в Tago et al. (Microbes Environ. 21:58-64, 2006). Для HPLC-анализа ≈7,0 × 107 микроорганизмов инкубировали в 1,0 мл 20 мM натрий-калий-фосфатного буфера (pH 7,0) с 1,0 мM имидаклоприда. После 20-минутного инкубирования при 30°C добавляли 1,0 мл метанола. Имидаклоприд и продукты его частичного разложения анализировали количественно в системе HPLC (насос 600E и детектор поглощения на двух длинах волн 2487; Waters). Время удерживания и площади пиков в HPLC-профилях сравнивали с таковыми у известных стандартов из Bonmatin et al. (Environ. Sci. Pollut. Res. Int. 22:35-67, 2015).
Смешанные обогатительные культуры из почвы, которые демонстрировали уменьшение количества имидаклоприда в HPLC-анализе при инкубировании, высевали поверхностным методом с использованием разведений от 10-1 до 10-6 на чашки с агаром с ограниченным содержанием азота и 36 мг/кг имидаклоприда и стрептомицином.
После инкубирования при 27°C в течение одной недели чашки подвергали скринингу в отношении колоний, кажущихся морфологически отличающимися друг от друга (с различиями в размерах). Отдельные колонии высевали на новые чашки с агаром с имидаклопридом в качестве единственного источника азота. Через три недели отдельные колонии помещали в 25 мл триптического соевого бульона (TSB) с 25 мг/л имидаклоприда.
После трехдневного роста каждый из изолятов центрифугировали в конических пробирках Falcon в течение 10 минут при 6700 x g. Надосадочную жидкость удаляли, а изоляты повторно суспендировали в стерильном фосфатном буфере до общего объема 10 мл. Образец каждого изолята объемом 2 мл инокулировали в культуры в MSM с ограниченным содержанием азота и MSM с ограниченным содержанием углерода; при этом обе культуры содержали 30 мг/л имидаклоприда в общем объеме 25 мл. Также получали неинокулированные контроли путем инокуляции 2 мл фосфатного буфера в каждый тип среды. Все образцы оборачивали алюминиевой фольгой и помещали на шейкер, работающий при 27°C и 100 об/мин. Затем образцы анализировали в отношении концентрации имидаклоприда с помощью HPLC.
Спустя семь дней инкубирования в колбы добавляли 25 мл метанола. Затем каждый образец обрабатывали ультразвуком в течение шести минут при 50% коэффициенте заполнения и центрифугировали при 6700 x g. Затем анализировали надосадочную жидкость и количественно измеряли имидаклоприд с помощью HPLC, как описано в данном документе.
Изоляты, которые снижали концентрацию имидаклоприда, хранили при -80°C в растворе 50% глицерина.
Пример 2. Отбор изолятов, расщепляющих имидаклоприд, которые выживают в средней кишке пчел
Данный пример демонстрирует возможность отбора микроорганизма, расщепляющего имидаклоприд, из изолятов, описанных в примере 1, которые способны выживать в средней кишке пчелы.
Схема терапии Десять изолятов, описанных в примере 1, составляли при 0 (отрицательный контроль), 102, 105 или 108 КОЕ/мл в 10 мл 50% сахарного сиропа.
Схема эксперимента
Приблизительно пятьдесят пчел на бактериальный изолят собирали и держали в деревянном садке. Штаммы бактерий, выделенные в предыдущем примере, культивировали и готовили для скармливания следующим образом. Клетки из каждого изолята промывали и разбавляли до OD600 0,1 с помощью MSM, дополненной 50% (вес/об.) сахарным сиропом, и инкубировали при 30°C для роста клеток. Четыре концентрации свежих культур бактерий вводили пчелам в виде корма (0-108 КОЕ/мл) следующим образом. Разные концентрации изолятов помещали в пробирку объемом 15 мл с шестью небольшими узкими отверстиями, в которые пчелы запускали свои хоботки и поедали растворы, содержащие изолят. Свежие культуры, содержащие изолят, готовили ежедневно для использования в качестве корма, и смертность пчел оценивали каждый день в течение всей продолжительности (7 дней) эксперимента путем подсчета и удаления мертвых пчел. Через 7 дней раствор, содержащий изолят, заменяли на 15% (вес/об.) сахарозу на 48 часов.
Десять пчел удаляли из каждой повторности каждые 24 часа для анализа бактерий; первый образец отбирали до начала эксперимента, и за этим следовал отбор образцов в семь дополнительных моментов. После каждого отбора образцов пчел анестезировали на льду, и удаляли среднюю кишку. Повторности для каждого момента времени объединяли и гомогенизировали в 150 мкл 1 × PBS, затем подвергали серийному разведению и высевали на чашки с агаром с ограниченным содержанием азота с 36 мг/кг имидаклоприда для выращивания бактерий в избирательных условиях роста при 30°C в течение 2 дней.
Бактериальные изоляты, которые выживали в средней кишке пчел, отбирали для введения для повышения устойчивости пчел к неоникотиноидам.
Пример 3. Повышение устойчивости пчел к неоникотиноидам посредством введения бактерий, расщепляющих имидаклоприд
Данный пример демонстрирует возможность повышения устойчивости пчел к инсектицидам, и более конкретно, к неоникотиноидам. Пчелы играют важную роль в опылении цветковых растений и являются основным типом опылителей во многих экосистемах, содержащих цветковые растения. Согласно оценкам одна треть пищевых ресурсов человека зависит от опыления насекомыми, птицами и летучими мышами, большая часть которого обеспечивается пчелами, в частности домашней европейской медоносной пчелой. Число колоний, содержащихся пчеловодами, уменьшилось в результате урбанизации, систематического использования пестицидов, а также воздействия трахейных клещей и микроскопических клещей из рода Varroa. Из-за непосредственного потребления загрязненных нектара и пыльцы с растений, обработанных инсектицидами, неоникотиноиды в инсектицидах отрицательно влияют на добывание пищи, обучаемость и память у рабочих пчел. Ожидается, что благодаря введению в их микробиом бактерий, расщепляющих имидаклоприд, у пчел повысится устойчивость к неоникотиноидам в виде улучшения поведения, как, например, увеличения интенсивности добывания пищи, интенсивности гигиенического поведения и выживаемости.
Схема терапии Бактериальный изолят, отобранный в примере 2 и идентифицированный как выживающий в средней кишке пчел, составляли при 108 организмов в 10 мл 50% сахарного сиропа.
Схема эксперимента
Изолят, отобранный в примере 2, готовили при концентрации 108 клеток/мл (см. пример 2) и помещали в пробирку объемом 15 мл с шестью небольшими узкими отверстиями, в которые пчелы запускали свои хоботки и поедали раствор, содержащий изолят. Свежие культуры, содержащие изолят, готовили ежедневно для использования в качестве корма. Предварительная обработка длилась в общей сложности семь дней.
Примерно 1500, 3000 или 7000 рабочих пчел из ульев, оцененных по массе рабочих пчел Apis mellifera (соответственно 0,5, 1 и 2 фунта или 0,23, 0,45 и 0,1 кг), предварительно обрабатывали изолятом, отобранным в примере 2, приготовленным при концентрации 108 клеток/мл и помещенным в пробирку объемом 15 мл с шестью небольшими узкими отверстиями, в которые пчелы запускали свои хоботки и поедали раствор, содержащий изолят. Свежие культуры, содержащие изолят, готовили ежедневно для использования в качестве корма. Предварительная обработка длилась в общей сложности семь дней.
После 7-дневной предварительной обработки каждую рабочую пчелу из улья кормили 2-4 граммами пыльцевой добавки и сахарного сиропа (1:1) в течение 1-2 дней перед обработкой имидаклопридом. Более мелкие колонии (1500 и 3000 пчел) помещали в наблюдательные ульи со стеклянными стенками. Более крупные колонии (7000 пчел) помещали в наблюдательные ульи Ulster (Brushy Mountain Bee Supply, Северная Каролина), в которых находился нижний ящик с 4 стандартными рамками и кормушка с разделительной доской, где предоставлялся сироп для обработки. Все наблюдательные ульи размещали под навесами и поддерживали при постоянной температуре и относительной влажности (23-25°C и 70%). Кроме того, во всех ульях имелся леток, ведущий во внешний мир, что позволяло пчелам самостоятельно добывать пищу на окружающих сельскохозяйственных полях и в городских жилых кварталах.
Когда откладывание яиц подтверждалось визуально, каждой колонии случайным образом назначали обработку имидаклопридом (0, 10, 20, 50 и 100 частей на миллион), предоставляемым в 50% сахарном сиропе. Колониям через дозирующую систему, аналогичную описанной в примере 2, давали пропорциональные количества раствора сахарозы с имидаклопридом: 80, 160 и 320 мл для колоний из 1500, 3000 и 7000 пчел соответственно. Запасы сиропа пополняли через день в течение 3 недель. Количество сиропа было предназначено для дополнения, но не поддержания колоний, поэтому пчелы должны были самостоятельно добывать пищу из других источников. Исходные растворы имидаклоприда (100 частей на миллион) готовили с использованием 99,5 ± 0,5% имидаклоприда технической чистоты, приобретенного у Chem Service, Inc (PS-2086), растворенного при взбалтывании в 50% сахарозе в течение ночи. Исходные растворы готовили каждые две недели, а растворы для обработки готовили каждую неделю. Образцы растворов для обработки (3-6 на дозу) отбирали случайным образом и исследовали в отношении остаточных концентраций для подтверждения точности дозировки.
Измерения поведенческих фенотипов
Пищедобывающую активность измеряли путем регистрации количества рабочих пчел, входящих в пчелиную колонию и выходящих из нее через леток во время одноминутных наблюдений два раза в день. Гигиеническое поведение использовали в качестве меры для оценивания активности рабочих пчел в улье и определяли как способность рабочих пчел выявлять и удалять больной и зараженный микроскопическими клещами расплод, тем самым ограничивая передачу патогенов и паразитов в пределах колонии. Гигиеническое поведение определяли с помощью анализа с убитым замораживанием расплодом, в котором 3-дюймовую (7,6 см) трубку из поливинилхлорида осторожно помещали в секцию сот, содержащую большую площадь запечатанных ячеек с куколками (взятых из неэкспериментальных полевых колоний). Количество пустых ячеек подсчитывали и регистрировали перед тем, как вылить 400 мл жидкого азота для убивания замораживанием примерно 160 куколок. Затем рамку временно помещали в пчелиную колонию, и через 24 часа количественно определяли долю куколок, полностью или частично удаленных из ячеек, для оценки гигиенического поведения. Удаление убитого замораживанием расплода коррелировало с удалением больного и зараженного паразитами расплода.
Пчелы, предварительно обработанные бактериальным изолятом, отобранным в примере 2, демонстрировали более высокую активность, чем пчелы, обработанные контролем.
Пример 4. Обработка микроскопических клещей из рода Varroa, которые инфицируют пчел, растворами окситетрациклина
Данный пример демонстрирует возможность уничтожения или снижения приспособленности микроскопических клещей из рода Varroa посредством их обработки раствором антибиотика. Данный пример демонстрирует, что влияние окситетрациклина на микроскопических клещей из рода Varroa опосредовано изменением популяций бактерий, таких как Bacillus, эндогенных по отношению к микроскопическим клещам из рода Varroa, которые являются восприимчивыми к окситетрациклину.
Микроскопические клещи из рода Varroa считаются основной причиной широко распространенного синдрома разрушения колоний (CCD), который приводит к массовому снижению численности колоний домашних медоносных пчел Apis mellifera во всем мире. Они прикрепляются к брюшку пчел и высасывают их кровь, лишая их питательных веществ и в конечном счете уничтожая их. Хотя микроскопических клещей из рода Varroa можно уничтожить с помощью химически синтезируемых майтицидов, эти типы химических веществ следует держать в отдалении от съедобного меда.
Схема терапии. Раствор окситетрациклина составляли при 0 (отрицательный контроль), 1, 10 или 50 мкг/мл в 10 мл стерильной воды с 0,5% сахарозой и незаменимыми аминокислотами.
Схема эксперимента
Для определения того, имеют ли взрослые микроскопические клещи из рода Varroa на стадии размножения другую восприимчивость по сравнению с форетическими микроскопическими клещами или их потомством, поскольку их кутикула не является завтердевшей, собирали микроскопических клещей из рода Varroa, живущих на взрослых пчелах Apis mellifera, и микроскопических клещей, ассоциированных с личинками и куколками. В этом анализе исследовали влияние растворов антибиотика на различные типы микроскопических клещей и определяли, как их приспособленность изменяется в результате целенаправленного воздействия на эндогенные микроорганизмы, такие как Bacillus.
Микроскопических клещей, поражающих расплод, собирали из сот (или кусочков сот) в колониях пчел, зараженных микроскопическими клещами из рода Varroa. Микроскопических клещей собирали из ячеек, в которых развиваются личинки пчел.
Микроскопических клещей из рода Varroa разделяли на группы по возрасту их хозяев в расплоде и анализировали по отдельности. Возраст расплода определяли на основании морфологических характеристик и пигментации личинок или куколок следующим образом: микроскопических клещей из рода Varroa, собранных из закрученных личинок, которые были достаточно маленькими для того, чтобы передвигаться по своей ячейке, помещали в группу 1; микроскопических клещей из рода Varroa, собранных из выпрямленных личинок, которые были слишком большими, чтобы лежать в ячейке, и начинали вытягиваться прямо с помощью своего ротового аппарата в направлении отверстия ячейки, помещали в группу 2; и микроскопических клещей из рода Varroa, собранных из куколок, помещали в группу 3. Микроскопических клещей хранили на личинках или куколках их хозяев в стеклянных чашках Петри до тех пор, пока не собирали 50 единиц. Это обеспечивало сохранение неизменным их стандартных условий питания и физиологического состояния. Чтобы предупредить отделение микроскопических клещей от личинок или куколок их хозяев или заползание друг на друга, в одной и той же чашке содержали только хозяев на одной и той же стадии развития.
Устройство - кольцо из нержавеющей стали (внутренний диаметр 56 мм, высота 2-3 мм) и 2 стеклянных круга (диаметр 62 мм) -очищали ацетоном и гексаном или пентаном с образованием испытательной арены. Растворы окситетрациклина и контрольный раствор наносили на устройство путем однородного распыления на стеклянные диски и кольцо арены. Для этого в резервуар загружали 1 мл растворов; устанавливали расстояние от опрыскиваемой поверхности до дна пробирки на 11 мм, и использовали форсунку на 0,0275 дюйма. Давление регулировали (обычно в диапазоне 350-500 гПа) до тех пор, пока количество отложенного раствора не составляло 1 ± 0,05 мг/см2. Растворы антибиотика выливали в соответствующие чашки, покрывая все дно чашек, а остаточную жидкость выпаривали под вытяжным устройством. Кольцо помещали между стеклянными кругами, образуя камеру. Камеры использовали в течение 60 часов после приготовления не более чем для трех анализов в целях контроля воздействия растворов антибиотика на микроскопических клещей. В эту камеру вводили от 10 до 15 микроскопических клещей из рода Varroa, и части устройства соединяли вместе каплями расплавленного воска. Использовали микроскопических клещей, собранных из закрученных личинок, выпрямленных личинок, белоглазых куколок и темноглазых куколок с белыми и бледными тельцами.
Через 4 часа микроскопических клещей переносили на чистую стеклянную чашку Петри (диаметр 60 мм) с двумя или тремя белоглазыми куколками (через 4 5 дней после покрытия оболочкой) для вскармливания. Микроскопических клещей наблюдали под препаровальной лупой через 4 часа, 24 часа и 48 часов после обработки антибиотиком или контрольными растворами и классифицировали в соответствии со следующими категориями:
• Подвижные: они передвигались на своих конечностях, вне зависимости от того, тыкали ли в них иглой.
• Парализованные: они двигали одним или несколькими придатками, без стимуляции или после стимуляции, однако они не могли передвигаться.
• Мертвые: неподвижные и не реагировали на 3 последовательные стимуляции.
Стерильную зубочистку или иглу использовали для стимуляции микроскопических клещей путем прикасания к их конечностям. Новые зубочистки или стерильные иглы использовали для стимуляции каждой группы для избежания контаминации между группами микроскопических клещей.
Анализы проводили при 32,5°C и относительной влажности 60 70%. Если смертность контрольных особей превышала 30%, то повторность исключали. Каждый эксперимент повторяли с использованием четырех серий камер.
Статус Bacillus в группах микроскопических клещей из рода Varroa оценивали с помощью ПЦР. Общую ДНК выделяли из контрольных (не обработанных окситетрациклином) и обработанных окситетрациклином особей (целого тела) с помощью набора для выделения ДНК (OMEGA, Bio-tek) в соответствии с протоколом производителя. Праймеры для Bacillus, прямой праймер 5'-GAGGTAGACGAAGCGACCTG-3' (SEQ ID NO: 186) и обратный праймер 5'-TTCCCTCACGGTACTGGTTC-3' (SEQ ID NO: 187), разрабатывали на основе последовательностей 23S-5S рРНК, полученных из генома Bacillus (номер доступа: AP007209.1) (Takeno et al., J. Bacteriol. 194(17):4767-4768, 2012) с использованием программного обеспечения Primer 5.0 (Primer-E Ltd., Плимут, Великобритания). Циклы ПЦР-амплификации включали в себя начальный этап денатурации при 95°C в течение 5 минут, 35 циклов при 95°C в течение 1 минуты, при 59°C в течение 1 минуты и при 72°C в течение 2 минут и конечный этап элонгации в течение 5 минут при 72°C. Продукты амплификации из обработанных окситетрациклином и контрольных образцов анализировали на 1% агарозных гелях, окрашивали с помощью SYBR Safe и визуализировали с использованием системы визуализации.
Показатели выживаемости микроскопических клещей из рода Varroa, обработанных раствором окситетрациклина, сравнивали с микроскопическими клещами из рода Varroa, обработанными отрицательным контролем.
Показатели выживаемости и подвижность микроскопических клещей из рода Varroa, обработанных раствором окситетрациклина, снижались по сравнению с контролем.
Пример 5. Выделение микроорганизмов, которые расщепляют фосфорорганический инсектицид фенитротион
Данный пример демонстрирует получение библиотеки микроорганизмов, способных расщеплять фосфорорганический инсектицид фенитротион.
Схема эксперимента
Образцы почвы получали из различных участков, где ранее использовали фенитротион для контроля насекомых. Бактерии, расщепляющие фенитротион, выделяли из образцов почвы, как описано (Microbes Environ. Vol. 21, No. 1, 58-64, 2006). Вкратце, 1 г образца почвы тщательно смешивали с 9 мл стерильной дистиллированной воды. Затем частицы почвы центрифугировали при RCF 1000 g в течение 5 минут, а затем 100 мкл надосадочной жидкости высевали в среду с фенитротионом и минеральными солями (0,4 г/л дрожжевого экстракта, 0,4 г/л фенитротиона, 15 г/л бактериологического агара). Чашки были мутными при приготовлении, поскольку фенитротион представлял собой эмульсию.
Колонии, которые образовывали вокруг себя прозрачные зоны и, вероятно, могли расщеплять или метаболизировать фенитротион, выделяли и повторно выращивали на агаре LB, питательном агаре, глюкозо-дрожжевом агаре, агаре TSA, агаре BHI или агаре MRS. После идентификации уникальных бактериальных колоний их геномы экстрагировали с помощью набора для экстракции геномной ДНК (Qiagen, набор для выделения ДНК из крови и тканей DNeasy) в соответствии с протоколом производителя.
Ген 16S рРНК амплифицировали с помощью универсальных праймеров для бактерий 27F (5'-AGAGTTTGATCMTGGCTCAG-3'; SEQ ID NO: 188) и 1492R (5'-TACCTTGTTACGACTT-3'; SEQ ID NO: 189) и с применением следующих условий ПЦР: 94°C в течение 2 минут, 30 циклов при 94°C в течение 1 минуты, при 56°C в течение 1 минуты и при 72°C в течение 2 минут и конечная элонгация при 72°C в течение 5 минут. Гель-электрофорез применяли для подтверждения того, что ампликоны имеют правильный размер (~ 1500 п. н.), и продукты вырезали из геля и очищали с помощью набора для извлечения из геля (Qiagen, QIAquick) в соответствии с протоколом производителя. Ампликоны правильного размера секвенировали по Сэнгеру, и применяли BLAST для сопоставления последовательности с различными репозиториями последовательностей генов 16s rRNA для идентификации бактерий.
Чтобы определить, расщепляет ли выделенная бактерия фенитротион, ~107 бактериальных клеток инкубировали в 1 мл 20 мM натрий-калий-фосфатного буфера (pH 7) с 1 мM фенитротиона, как описано в PNAS, Vol. 109, No. 22, 8618-8622, 2012. После 30 минут инкубирования при 30°C реакцию останавливали, добавляя равный объем метанола. Затем фенитротион и его метаболит 3-метил-4-нитрофенол анализировали с помощью HPLC. Время удерживания и площади пиков в HPLC-профилях сравнивали с таковыми у известных стандартов.
Уникальные бактериальные изоляты, которые обладали способностью расщеплять фенитротион, затем хранили замороженными в глицерине при -80°C.
Пример 6. Повышение устойчивости Drosophila melanogaster к фенитротиону путем введения бактерий, расщепляющих фенитротион
Данный пример демонстрирует возможность защиты насекомых Drosophila melanogaster в модели от одного или нескольких отрицательных эффектов инсектицидов в их рационе, более конкретно фенитротиона. Следующий подход является имитационным для других насекомых, таких как пчелы или другие насекомые, раскрытые в данном документе, например, насекомых, которые являются важными опылителями многих культурных цветковых растений и овощных растений. Было показано, что многие инсектициды, в том числе фенитротион, токсичны для пчел.
Схема эксперимента
Схема терапии Бактериальные изоляты, отобранные в примере 5, составляли при 109 организмов в 100 мкл кормовой среды для мух с фенитротионом и без него.
Среда, используемая для выкармливания мух, представляла собой среду, содержащую кукурузную муку, мелассу и дрожжи (11 г/л дрожжей, 54 г/л желтой кукурузной муки, 5 г/л агара, 66 мл/л мелассы и 4,8 мл/л пропионовой кислоты). Для экспериментальных процедур фенитротион при 0, 10 и 100 частей на миллион или фосфатно-солевой буферный раствор в качестве отрицательного контроля вливали в стерильную кормовую среду для мух.
Анализ скорости развития
В первый день в стерильную кормовую среду для мух с фенитротионом или без него добавляли 109 бактерий, расщепляющих фенитротион, описанных в примере 5, суспендированных в 100 мкл фосфатно-солевого буферного раствора, или равный объем солевого раствора (отрицательный контроль). Все образцы оставляли высушиваться в течение дня при 25°С, как описано в Appl. Environ. Microbiol. Vol. 82, No. 20, 6204-6213, 2016.
Во второй день оплодотворенные эмбрионы, собранные от мух, обрабатывали 2% раствором гипохлорита в течение 5 минут, а затем промывали стерильной водой для удаления любых внеклеточных микроорганизмов из эмбрионов. 10 мкл суспензии эмбрионов в воде (суспензии эмбрионы:вода 1:3) добавляли в засеянную бактериями или отрицательную контрольную кормовую среду для мух с фенитротионом или без него. Когорты с эмбрионами на кормовой среде для мух выдерживали при 25°С с циклом чередования 12 часов света и 12 часов темноты до конца эксперимента.
Время до образования пупария и количество образующихся куколок измеряли в каждой когорте. Время до появления взрослых особей и скорость появления измеряли в каждом образце. С момента появления первой взрослой особи из куколки каждые 12 часов подсчитывали число появляющихся взрослых мух, и вычисляли скорость появления.
Ожидалось, что эмбрионы на кормовой среде для мух, в которую был влит фенитротион, засеянной бактериями, расщепляющими фенитротион, будут развиваться быстрее, чем эмбрионы на кормовой среде, в которую был влит фенитротион, без бактерий, расщепляющих фенитротион.
Анализ выживаемости
Приблизительно за 12 дней до первого дня стерильные эмбрионы получали, как описано ранее, и выращивали на стерильной кормовой среде для мух. Взрослые особи начинали появляться из своих куколок через 11 дней после сбора эмбрионов при выращивании на стерильной кормовой среде для мух без фенитротиона при 25°C с циклом чередования 12 часов света и 12 часов темноты.
В первый день 109 бактерий, расщепляющих фенитротион, в фосфатно-солевом буферном растворе добавляли в стерильную кормовую среду для мух, как описано в предыдущем примере.
Во второй день 10 вновь появившихся стерильных взрослых самцов и самок помещали на засеянную бактериями или отрицательную контрольную кормовую среду для мух с фенитротионом или без него. Кормовую среду для мух с мухами выдерживали при 25°С с циклом чередования 12 часов света и 12 часов темноты до конца эксперимента. Число выживших самцов и самок мух подсчитывали каждый день, пока все мухи не погибли. Анализы выживаемости проводили для оценки благоприятного эффекта приспособленности, производимого бактериями, расщепляющими фенитротион, в отношении выживаемости мух.
Ожидалось, что мухи, выращиваемые на кормовой среде для мух, в которую был влит фенитротион, засеянной бактериями, расщепляющими фенитротион, будут выживать дольше, чем мухи, выращиваемые на кормовой среде, в которую был влит фенитротион, без бактерий, расщепляющих фенитротион.
Пример 7. Устранение энтомопатогенных бактерий из Drosophila melanogaster с помощью встречающихся в природе фагов
Данный пример демонстрирует возможность устранения бактериальных патогенов насекомых (таких как Serratia marcescens, Erwinia carotovora и Pseudomonas entomophila) у Drosophila melanogaster с помощью встречающихся в природе фагов. Эта процедура может быть пригодна в качестве имитационного анализа для устранения бактерий у других видов насекомых, таких как пчелы.
Схема эксперимента
Схема терапии. Использовали коллекции библиотек фагов, содержащие следующие семейства фагов: Myoviridae, Siphoviridae, Podoviridae, Lipothrixviridae, Rudiviridae, Ampullaviridae, Bicaudaviridae, Clavaviridae, Corticoviridae, Cystoviridae, Fuselloviridae, Gluboloviridae, Guttaviridae, Inoviridae, Leviviridae, Microviridae, Plasmaviridae, Tectiviridae.
Несколько образцов окружающей среды (почва, прудовые донные отложения и сточная вода) собирали в стерильные колбы на 1 л в течение периода 2 недель и незамедлительно обрабатывали после сбора и затем хранили при 4°C. Твердые образцы гомогенизировали в стерильном бульоне Лурия (LB) или триптическом соевом бульоне (TSB) двойной концентрации от Difco с добавлением 2 мM CaCl2 до конечного объема 100 мл. Значения pH и уровни фосфата измеряли с помощью индикаторных полос для фосфата. Для очистки все образцы центрифугировали при 3000-6000 g в течение 10-15 минут при 4°C и фильтровали через фильтры с размером пор 0,2 мкм с низким связыванием белка для удаления всех оставшихся бактериальных клеток. Надосадочную жидкость, содержащую библиотеку фагов, затем хранили при 4°C в присутствии хлороформа в стеклянном флаконе.
20-30 мл библиотеки фагов разбавляли до объема 30-40 мл бульоном LB. Штамм бактерий-мишеней (например, Serratia marcescens, Erwinia carotovora и Pseudomonas entomophila) добавляли (50-200 мкл культуры, выращенной в течение ночи в бульоне LB) для обогащения популяции фагов, которые целенаправленно воздействуют на этот конкретный штамм бактерий в культуре. Эту культуру инкубировали в течение ночи при 37°C со встряхиванием при 230 об/мин. Бактерии из этой обогатительной культуры удаляли центрифугированием (3000-6000 g, 15-20 минут, 4°C) и фильтровали (фильтр с размером пор 0,2 или 0,45 мкм). 2,5 мл культуры, не содержащей бактерий, добавляли к 2,5 мл бульона LB, и 50-100 мкл бактерий-мишеней добавляли обратно в культуру для дополнительного обогащения фагами. Обогатительную культуру выращивали в течение ночи, как описано выше. Образец из этой обогатительной культуры центрифугировали при 13000 g в течение 15 минут при комнатной температуре, и 10 мкл надосадочной жидкости помещали на чашку Петри с агаром LB совместно с 100-300 мкл бактерий-мишеней и 3 мл расплавленного 0,7% мягкого агара. Чашки инкубировали в течение ночи при 37°C.
Каждую из бляшек, наблюдаемых на бактериальном газоне, собирали и переносили в 500 мкл бульона LB. Образец из этой исходной культуры бляшек дополнительно высевали на бактерии-мишени. Очистку бляшек выполняли три раза для всех обнаруженных фагов с целью выделения одного однородного фага из неоднородной смеси фагов.
Лизаты из чашек с фагами с высокими титрами (> 1x 10^10 БОЕ/мл) получали путем сбора верхних слоев с планшетов, содержащих штамм бактерий-хозяев, демонстрирующий сливной лизис. После добавления 5 мл буфера верхний мягкий слой агара мацерировали, очищали центрифугированием и стерилизовали фильтрацией. Полученные лизаты хранили при 4°C. Фаговые лизаты с высоким титром дополнительно очищали с помощью изопикнического центрифугирования с использованием CsCl, как описано в Summer et al., J. Bacteriol. 192:179-190, 2010.
ДНК выделяли из очищенных с помощью CsCl фаговых суспензий, как описано в Summer, Methods Mol. Biol. 502:27-46, 2009. Отдельный выделенный фаг секвенировали в виде части двух пулов геномов фагов с помощью способа пиросеквенирования 454. Вкратце, геномную ДНК фагов смешивали в эквимолярных количествах до конечной концентрации приблизительно 100 нг/л. Объединенную ДНК фрагментировали, лигировали с помощью мультиплексной идентификационной метки (MID), специфичной для каждого из пулов, и секвенировали с помощью пиросеквенирования с использованием полнопланшетной реакции на секвенаторе (Roche) в соответствии с протоколами производителя. Объединенная ДНК фагов присутствовала в двух реакциях секвенирования. Выходные данные, соответствующие каждому из пулов, собирали отдельно с использованием программного обеспечения (454 Life Sciences), регулируя настройки таким образом, чтобы были включены только риды с одной MID на сборку. Идентичность отдельных контигов определяли с помощью ПЦР с использованием праймеров, образованных для последовательностей контигов и отдельных препаратов геномной ДНК фагов, в качестве матрицы. Программное обеспечение для секвенирования (Gene Codes Corporation) использовали для сборки и редактирования последовательностей.
Хромосомные концевые структуры фагов определяли экспериментально. Липкие концы (cos) для фагов определяли посредством секвенирования концов фагового генома и секвенирования продуктов ПЦР, полученных путем амплификации посредством лигирующего соединения циркуляризованной геномной ДНК, как описано в Summer, Methods Mol. Biol. 502:27-46, 2009. Области, кодирующие белки, изначально прогнозировали с использованием программного обеспечения для прогнозирования генов (Lukashin et al. Nucleic Acids Res. 26:1107-1115, 1998), очищали посредством ручного анализа в Artemis (Rutherford et al., Bioinformatics 16:944-945, 2000) и анализировали путем применения BLAST (пороговое E-значение 0,005) (Camacho et al., BMC Bioinformatics 10:421, 2009). Белки, представляющие особый интерес, дополнительно анализировали с помощью программного обеспечения для поиска последовательностей (Hunter et al., Nucleic Acids Res. 40:D306-D312, 2012).
Электронную микроскопию очищенного с помощью CsCl фага (> 1×10^11 БОЕ/мл), который лизировал патогенные для Drosophila виды бактерий, выполняли путем разведения исходного раствора фага буфером на основе триптического соевого бульона. Фаги наносили на тонкие сетки на 400 меш с углеродным покрытием, окрашивали 2% (вес/об.) уранилацетатом и сушили на воздухе. Образцы наблюдали в трансмиссионном электронном микроскопе, функционирующем при ускоряющем напряжении 100 кВ. Пять вирионов каждого фага измеряли для расчета средних значений и стандартных отклонений размеров капсида и отростка при необходимости.
Включение фагов в пищу
Среда, используемая для выкармливания мух, представляла собой среду, содержащую кукурузную муку, мелассу и дрожжи (11 г/л дрожжей, 54 г/л желтой кукурузной муки, 5 г/л агара, 66 мл/л мелассы и 4,8 мл/л пропионовой кислоты). Растворы фагов вливали в кормовую среду для мух с получением конечных концентраций фагов 0-108 БОЕ/мл.
Бактерии S. marcescens, Erwinia carotovora и Pseudomonas entomophila выращивали при 30°C в питательном бульоне или в бульоне LB.
Стерильные эмбрионы мух получали путем обработки оплодотворенных эмбрионов, собранных от мух, 2% раствором гипохлорита в течение 5 минут, а затем промывали стерильной водой для удаления любых внеклеточных микроорганизмов. Личинки мух с бактериями-мишенями получали путем посева 109 КОЕ бактерий на стерильную кормовую среду для мух и добавления стерильных эмбрионов мух в эту кормовую среду. Через 2 дня в кормовую среду для мух добавляли десять инфицированных S. marcescens личинок мух на стадии первого возраста с диапазоном концентраций фагов (0-108 БОЕ/мл). Личинок оставляли расти на кормовой среде вместе с фагами в течение 3 дней, пока они не достигали стадии третьего возраста. Затем личинок собирали и по отдельности гомогенизировали в питательном бульоне или бульоне LB, высевали на чашки с питательным агаром или агаром LB и инкубировали при 30°C. Регистрировали число КОЕ S. marcescens, полученных от личинок в кормовой среде для мух с различными концентрациями фагов. Это показывало количество живых бактерий, которые присутствовали в организмах мух.
Ожидалось, что количество живых бактерий будет уменьшено у личинок, выращенных на кормовой среде для мух с фагами, противодействующими бактериям.
Пример 8. Создание библиотеки природных микроорганизмов
Данный пример демонстрирует выделение из почвы бактерий, которые естественным образом продуцируют аминокислоту метионин.
Среда, используемая для выделения микроорганизмов, представляет собой агар с крахмалом, казеином и нитратом (10,0 г крахмала; 0,003 г казеина; 0,02 г KNO3; 0,02 г NaCl; 0,5 мг MgSO4; 0,2 мг CaCO3; 0,1 мг FeSO4; 12,0 г агара; 1 л H2O; pH 7,0) (Kuster and Williams, 1964). Каждый образец почвы из окружающей среды (1,0 г) суспендировали в 9 мл стерильной воды, и 1 мл суспензии подвергали десятикратному серийному разведению стерильной дистиллированной водой. Один миллилитр разведения 10-5 инокулировали в агаровую среду и инкубировали в течение 7 дней при 30°C. В конце этого периода чашки осматривали на наличие роста. Отдельные белые и плотные колонии собирали и выращивали в новых чашках с агаром с крахмалом, казеином и нитратом для создания библиотеки изолятов. После 7 дней роста при 30°С чашки выдерживали при 4°С.
Пример 9. Скрининг изолятов, которые продуцируют метионин
Данный пример демонстрирует скрининговый анализ изолятов из примера 8, которые естественным образом продуцируют аминокислоту метионин.
Скрининг в отношении продуцирования метионина
Для ферментации использовали модифицированную базальную среду (0,3 г K2HPO4; 0,7 г KH2PO4; 1,0 г Na2CO3; 5,0 мг CaCl2; 0,3 г MgSO4; 1,0 мг FeSO4; 1 л H2O) с сахарозой (20,0 г) и NH4Cl (10,0 г) (Chay, B.P., Galvez, F.C.F., and Padolina, W.G.P.U.L.B.P. (1992). Methionine production by batch fermentation from various carbohydrates. ASEAN Food Journal (Malaysia)). Значение pH среды составляло 7,2.
Условия культивирования. Две петли 7-дневной культуры изолята из примера 8 инокулировали в колбу Эрленмейера объемом 250 мл с 30 мл ферментационной среды. Продуцирование метионина анализировали после инкубирования колбы в течение 5 дней на ротационном шейкере (160 об/мин) при 30°C. Готовили колбы в двух повторностях, а неинокулированные колбы служили в качестве контроля во всех экспериментах.
Присутствие метионина в бульонных культурах изолятов изучали с помощью хроматографии на бумаге согласно модифицированному способу Khanna и Nag (Khanna et al., "Production of amino acids in vitro tissue culture", Indian Journal of Experimental Biology (1973)). Бульонную культуру центрифугировали при 5000 × g в течение 20 минут, и 2 мкл надосадочной жидкости наносили на 1,5 см выше одного края фильтровальной бумаги Whatman № 1 размером 18 см × 22 см. 1 мкл объема стандартного раствора метионина (0,1 мг/мл) наносили вместе с надосадочной жидкостью, и хроматограмму проявляли в смеси растворителей н-бутанола, уксусной кислоты и воды (4:1:1) в течение 18 часов. Хроматограмму высушивали на воздухе при комнатной температуре, опрыскивали 0,15% раствором нингидрина в бутаноле и снова высушивали перед нагреванием при 60°С в течение 5 минут в печи. Значение показателя цвета нингидрин-положительного пятна (голубовато-фиолетового) надосадочной жидкости, которое соответствует значению стандартного раствора метионина, указывает на присутствие метионина в бульонной культуре. Концентрацию метионина, продуцируемого в бульонной культуре изолята, оценивали следующим образом. Нингидрин-положительное пятно надосадочной жидкости изолята на хроматограмме элюировали 10% этанолом, и регистрировали спектрофотометрические показания элюата при 520 нм. Концентрацию метионина в надосадочной жидкости определяли по калибровочной кривой. График значений оптических плотностей в зависимости от различных концентраций (0,1-0,9 мг/мл) раствора метионина служил калибровочной кривой для метионина.
Изоляты, которые продуцировали метионин, выдерживали в чашках со свежим агаром, и готовили исходный раствор путем суспендирования двух петель для посева микроорганизма в аликвоте 50% раствора глицерина.
Пример 10. Введение штамма бактерий, продуцирующих аминокислоту, в Drosophila melanogaster с рационом для увеличения скорости их развития
Данный пример демонстрирует возможность обработки Drosophila melanogaster бактериями, продуцирующими аминокислоту, для увеличения скорости их развития при выращивании на рационах, лишенных питательных веществ. Эта схема эксперимента может быть расширена для способствования развитию других насекомых, таких как медоносные пчелы, которым может не хватать питательных веществ в их рационе.
Схема терапии
Выделенные бактерии Corynebacterium glutamicum, являющиеся продуцентами глутамата или метионина, составляли в растворе 109 колониеобразующих единиц (CFU), смешанном с питательным субстратом для мух Drosophila.
Схема эксперимента
Штаммы Corynebacterium glutamicum, которые продуцируют глутамат или метионин, выращивали в питательном бульоне при 30°C.
Среда, используемая для выкармливания мух, представляла собой среду, содержащую кукурузную муку, мелассу и дрожжи (11 г/л дрожжей, 54 г/л желтой кукурузной муки, 5 г/л агара, 66 мл/л мелассы и 4,8 мл/л пропионовой кислоты). Все компоненты этого рациона, за исключением пропионовой кислоты, нагревали совместно до 80°C в деионизированной воде при постоянном перемешивании в течение 30 минут, и им давали охладиться до 60°C. Затем примешивали пропионовую кислоту, и 50 мл рациона разделяли на аликвоты в отдельные флаконы и оставляли охлаждаться и затвердевать. Мух выращивали при 26°C, цикле свет:темнота 16:8 часов, при влажности около 60%.
Для постановки эксперимента с целью измерения скорости роста личинок использовали рацион определенного состава (Piper et al., 2014, Nature Methods). В рационе определенного состава устранялось влияние варьирования ингредиентов, используемых для рациона на основе кукурузной муки, между партиями. Кроме того, рацион определенного состава позволял исключить отдельные компоненты для исследования их влияния на развитие мух.
Анализ скорости развития
В первый день 100 мкл суспензии Corynebacterium glutamicum в питательном бульоне, состоящем из 109 колониеобразующих единиц (КОЕ), добавляли в кормовую среду для мух в пяти повторностях. В качестве контроля питательный бульон без бактерий добавляли еще в пять флаконов с кормовой средой для мух. Оплодотворенные эмбрионы, собранные от плодовых мушек, обрабатывали 2% раствором гипохлорита в течение пяти минут, а затем промывали стерильной водой для удаления любых внеклеточных микроорганизмов из эмбрионов. 10 мкл суспензии эмбрионов в воде (суспензия эмбрионы:вода один к трем) добавляли во все флаконы с засеянной бактериями и контрольной кормовой средой. Кормовую среду для мух с эмбрионами выдерживали при температуре 26°C, цикле свет:темнота 16:8 часов, при влажности около 60% до конца эксперимента. Время до появления взрослых особей и скорость появления измеряли в каждой повторности. С момента появления первой взрослой особи из куколки каждые 12 часов подсчитывали число появляющихся взрослых мух и вычисляли скорость появления.
Анализ массы личинок
Для исследования того, может ли присутствие бактерий, продуцирующих аминокислоты, обеспечивать увеличение массы тела развивающихся личинок при выращивании на рационе определенного состава, авторы настоящего изобретения получали личинок, которые являются аксеническими и моноассоциированными с одним штаммом бактерии. В этих анализах использовали три различные бактерии: Corynebacterium glutamicum - штамм, продуцирующий глутамат, Corynebacterium glutamicum - штамм, продуцирующий метионин, и E. coli.
Сначала получали аксенические эмбрионы. Оплодотворенные эмбрионы собирали от плодовых мушек в течение периода 6 часов на чашках с агаром с виноградным соком и дрожжами. Для устранения любой бактериальной контаминации эмбрионы обрабатывали 2% раствором гипохлорита в течение пяти минут, а затем трижды промывали стерильной водой. Один объем эмбрионов затем суспендировали в 3 объемах воды.
Рацион определенного состава разделяли на аликвоты в пузырьки, и для каждого исследуемого условия использовали девять повторностей. Условия представляли собой следующее:
1. Кормовая среда без добавления бактерий
2. Кормовая среда содержит штамм C. glutamicum, который продуцирует глутамат (C.glu-Glu)
3. Кормовая среда содержит штамм C. glutamicum, который продуцирует метионин (C.glu-Met)
4. Кормовая среда содержит E. coli
В каждый пузырек с кормовой средой, которая соответствовала условиям 2, 3 и 4, добавляли 100 мкл ночных культур в стационарной фазе.
В каждую из девяти повторностей каждого условия добавляли 10 мкл стерильной суспензии эмбрионов и воды. Пузырьки затем инкубировали при 26°С, влажности 60%, цикле свет:темнота 16:8.
Через 13 дней отбирали образцы 10-15 случайно выбранных личинок из каждой повторности и измеряли их площади тела в качестве приблизительного показателя их биомассы и веса. Личинки выскабливали из кормовой среды стерильным шпателем, промывали в воде для очистки их тел от кормовой среды, и получали изображение каждой отобранной личинки отдельно для каждой повторности каждого условия. Скрипт ImageJ использовали для идентификации, обрисовки и измерения площади тела личинки на каждом изображении.
При обработке бактериями, продуцирующими аминокислоту, увеличивается скорость развития насекомых
Эмбрионы, которые развивались на рационе, засеянном штаммом бактерии, продуцирующим аминокислоту, достигали зрелого возраста значительно быстрее, чем эмбрионы, выращиваемые на стерильном рационе (фиг. 1). Кроме того, этот эффект был несколько сильнее у самок мух, чем у самцов мух (фиг. 2А и 2В).
При обработке бактериями, продуцирующими аминокислоту, увеличивается масса тела личинок
Личинки на рационе, дополненном C. glu-Met, имели в среднем наибольший размер тела, за ними следовали личинки на рационе с C.glu-Glu, E. coli и без бактерий (фиг. 3). Это показывает, что дополнение рациона насекомых бактериями, которые продуцируют аминокислоту, обеспечивало более быстрый прирост биомассы насекомых, чем рацион без добавок.
В совокупности эти данные демонстрируют, что дополнение рациона насекомых бактериями, способными продуцировать аминокислоты, обеспечивало более быстрый прирост биомассы насекомых, чем рацион без добавок. При распространении этого на других насекомых, таких как пчелы, добавление в их рацион бактерий, способных продуцировать метионин, может обеспечивать повышение их приспособленности.
Пример 11. Насекомые, обработанные раствором очищенных фагов
Данный пример демонстрирует выделение и очистку из образцов окружающей среды фагов, которые целенаправленно воздействовали на специфические бактерии насекомых. Данный пример также демонстрирует эффективность выделенных фагов в отношении бактерий-мишеней в анализах бляшкообразования in vitro, измеренную по их скорости потребления кислорода и скорости закисления внеклеточной среды. Наконец, данный пример демонстрирует эффективность фагов in vivo, измеренную по способности фага целенаправленно воздействовать на бактерии мух посредством их обработки выделенным фагом, противодействующим бактериям. Данный пример демонстрирует, что патогенная бактерия, которая снижала приспособленность насекомого, могла быть устранена с помощью фага, целенаправленно воздействующего на бактерию. В частности, Serratia marcescens, которая представляет собой патогенную бактерию мух, может быть устранена с помощью фага, который был выделен из садового компоста.
Существует несколько полезных и коммерчески пригодных насекомых, на которых отрицательно влияют встречающиеся в природе бактериальные патогены. Одним из таких примеров является бактерия Paenibacillus larvae, которая является причиной гнильца у медоносных пчел. Применение фага для лечения гнильца имело бы большое значение для уменьшения огромных потерь из-за гнильца.
Схема эксперимента
Выделение специфических бактериофагов из природных источников
Бактериофаги, противодействующие бактериям-мишеням, выделяли из исходного материала окружающей среды. Вкратце, насыщенную культуру Serratia marcescens разбавляли в свежем триптическом соевом бульоне двойной концентрации (TSB) и выращивали в течение ~120 минут до ранней лог-фазы при 24-26°C или в бульоне Лурия-Бертани двойной концентрации (LB) и выращивали в течение ~90 минут при 37°C. Садовый компост готовили путем гомогенизации в PBS и стерилизовали путем фильтрации через фильтр с размером пор 0,2 мкм. Неочищенные сточные воды стерилизовали путем фильтрации через фильтр с размером пор 0,2 мкм. Один объем фильтрованного исходного материала добавляли к культурам бактерий в лог-фазе, и инкубирование продолжали в течение 24 ч. Обогащенный исходный материал готовили путем осаждения культур центрифугированием и фильтрования надосадочной жидкости через мембраны с размером пор 0,45 мкм.
Фаги выделяли путем высевания образцов на бактериальные газоны в двойном слое агара. Стационарные культуры бактерий объединяли с LB или TSB c расплавленным 0,6% агаром и наливали в чашки c LB или TSB с 1,5% агаром. После затвердения 2,5 мкл разведенных образцов фагов наносили на чашки с двойным слоем агара и оставляли для поглощения. Затем чашки заворачивали в обертку и инкубировали в течение ночи при 25°C (TSA) или 37°C (LB), после этого оценивали в отношении образования видимых бляшек. Свежевыделенные бляшки очищали посредством последовательного пассирования отдельных бляшек на штамме-мишени путем отбора бляшек в буфере SM (50 мM Tris-HCl [pH 7,4], 10 мM MgSO4, 100 мM NaCl) и инкубирования в течение 15 минут при 55°C, затем повторения способа нанесения на двойной слой агара, как указано выше, с использованием суспензии бляшек.
Бактериофаги успешно выделяли как из сточных вод, так и из компоста, как подробно описано выше. Образование бляшек было отчетливо заметно после нанесения образцов на газоны из бактерий S. marcescens, используемые для обогащений.
Пассирование, количественная оценка и размножение бактериофагов
Размножение и образование фаговых лизатов для применения в последующих экспериментах осуществляли с помощью бактериофагов, выделенных и очищенных, как описано выше. Вкратце, насыщенные культуры бактерий разбавляли в 100 раз в свежей среде и выращивали в течение 60-120 минут для достижения состояния ранней логарифмической фазы роста с целью эффективного инфицирования фагами. Суспензии фагов или фаговые лизаты добавляли к культурам в ранней логарифмической фазе роста, и инкубирование продолжали до тех пор, пока не наблюдали очищение бульона, что указывало на размножение фагов и лизис бактерий, или до прохождения 24 ч. после инфицирования. Лизаты собирали путем осаждения клеток центрифугированием при 7197 x g в течение 20 мин. с последующим фильтрованием надосадочной жидкости через мембраны с размером пор 0,45 или 0,2 мкм. Отфильтрованные лизаты хранили при 4°C.
Подсчет инфекционных фаговых частиц осуществляли с помощью способа нанесения на двойной слой агара. Вкратце, в PBS выполняли серийное разведение образцов 1:10, и разведения наносили на чашки с затвердевшим двойным слоем агара, полученными с бактериями хозяина, как описано выше. Бляшкообразующие единицы (БОЕ) подсчитывали после инкубирования в течение ночи с определением примерного титра образцов.
Анализ выделенных фагов in vitro путем измерения дыхания бактерий
Анализатор Seahorse XFe96 (Agilent) использовали для измерения влияния фагов на бактерии путем отслеживания скорости потребления кислорода (OCR) и скорости закисления внеклеточной среды (ECAR) в ходе инфицирования. Планшеты XFe96 покрывали за день до экспериментов с помощью 15 мкл 1 мг/мл исходного раствора поли-L-лизина на лунку и высушивали в течение ночи при 28°C, и зонды XFe96 уравновешивали путем помещения в лунки, содержащие 200 мкл калибрующего вещества XF, и инкубирования в темноте при комнатной температуре. На следующий день планшеты, покрытые поли-L-лизином, промывали дважды с помощью ddH2O. Насыщенные ночные культуры E. coli BL21 (LB, 37°C) или S. marcescens (TSB, 25°C) субкультивировали при 1:100 в той же самой среде и выращивали при вентиляции в течение ~2,5 ч. при 30°C. Затем культуры разбавляли до O.D. 600 нм ~ 0,02 с помощью той же самой среды. Средства обработки получали путем разведения исходных растворов в буфере SM при 10x конечной концентрации и загрузки 20 мкл 10x растворов в подходящие отверстия для ввода проб планшета с зондами. Хотя зонды уравновешивали в анализаторе XFe96 Flux, планшеты с бактериями готовили путем добавления 90 мкл бактериальных суспензий или контролей со средой и центрифугировали при 3000 об./мин. в течение 10 минут. После центрифугирования дополнительные 90 мкл соответствующей среды осторожно добавляли в лунки так, чтобы не нарушить прилипание бактерий, доводя общий объем до 180 мкл на лунку.
Анализатор XFe96 прогоняли при ~30°C в соответствии с циклами смешивания, ожидания, считывания продолжительностью 1:00, 0:30, 3:00. Выполняли четыре цикла, чтобы обеспечить уравновешивание/нормализацию бактерий, затем вводили 20 мкл средств обработки, и циклы продолжали, как описано выше, в течение общего времени примерно 6 ч. Данные анализировали с помощью пакета компьютерных программ Seahorse XFe96 Wave.
Влияние выделенных бактериофагов анализировали путем измерения скорости потребления кислорода (OCR) и скорости закисления внеклеточной среды (ECAR) у бактерий в анализаторе Seahorse XFe96. Когда E. coli инфицировали фагом T7, а S. marcescens инфицировали свежевыделенным фагом ΦSmVL-C1, наблюдались существенные снижения OCR после кратковременных пиков этой скорости (фиг. 4). Для обоих фагов с обоими организмами-хозяевами анализ Seahorse способствовал выявлению успешного инфицирования фагами без необходимости в анализах бляшкообразования. Таким образом, данный способ применим для выявления инфицирования фагами организма-хозяина, не поддающегося традиционным способам выявления фагов.
Анализ трансдукции с использованием SYBR Gold для идентификации инфекции
Препараты бактериофагов готовили для окрашивания путем предварительной обработки нуклеазами для удаления вневирусных нуклеиновых кислот, которые могли нарушать интерпретацию флуоресцентного сигнала. Вкратце, MgCl2 добавляли к 10 мл фагового лизата при конечной концентрации 10 мM, и как РНКазу A (Qiagen), так и ДНКазу I (Sigma) добавляли до конечных концентраций 10 мкг/мл. Образцы инкубировали в течение 1 ч. при комнатной температуре. После обработки нуклеазами 5 мл лизатов объединяли с 1 мкл SYBR Gold (Thermo, 10000x) и инкубировали при комнатной температуре в течение ~1,5 ч. Избыточный краситель затем удаляли из образцов с помощью ультрафильтрационных колонок Amicon. Вкратце, колонки Amicon (15 мл, MWCO 10 кДа) промывали путем добавления 10 мл буфера SM и центрифугировали при 5000 x g, 4°C в течение 5 минут. Меченые образцы фагов затем центрифугировали в колонках при 5000 x g, 4°C до тех пор, пока объем не снижался примерно в 10 раз (15-30 мин.). Для промывания образцов 5 мл буфера SM добавляли в каждый резервуар, и центрифугирование повторяли с последующими двумя дополнительными промывками. После третьей промывки оставшиеся образцы отбирали пипеткой из резервуаров Amicon и доводили до примерно 1 мл с помощью буфера SM. Для удаления более крупных контаминантов промытые и меченые образцы фагов центрифугировали при 10000 x g в течение 2 минут, и образцы надосадочной жидкости затем фильтровали через мембраны с размером пор 0,2 мкм в черные микропробирки и хранили при 4°C.
Насыщенные культуры бактерий (E. coli MG1655, выращенная в LB при 37°C, S. marcescens и S. symbiotica, выращенные в TSB при 26°C) получали путем центрифугирования 1 мл аликвот и однократного промывания с помощью 1 мл PBS перед заключительным ресуспендированием с помощью 1 мл PBS. Меченые положительным контролем бактерии окрашивали путем объединения 500 мкл промытых бактерий и 1 мкл SYBR Gold и инкубирования в течение 1 ч. в темноте при комнатной температуре. Бактерии осаждали путем центрифугирования при 8000 x g в течение 5 мин. и промывали дважды равным объемом PBS с последующим ресуспендированием в конечном объеме 500 мкл PBS. Объем 25 мкл окрашенных бактерий объединяли с 25 мкл буфера SM в черной микропробирке, к которой добавляли 50 мкл 10% формалина (5% конечный объем, ~2% формальдегид) и смешивали путем пощелкивания. Образцы фиксировали при комнатной температуре в течение ~3 ч. и затем промывали с помощью ультрафильтрационных колонок Amicon. Вкратце, 500 мкл воды РicoРure добавляли в колонки Amicon (0,5 мл, MWCO 100 кДа) и центрифугировали при 14000 x g в течение 5 мин. для промывания мембран. Фиксированные образцы разбавляли путем добавления 400 мкл PBS и затем переносили в предварительно промытые микроцентрифужные колонки и центрифугировали при 14000 x g в течение 10 мин. Колонки переносили в свежие пробирки для сбора образцов, и 500 мкл PBS добавляли для разбавления фиксатора, остающегося в ретентате. Затем проводили два дополнительных разбавления с помощью PBS, в общей сложности в количестве трех промывок. Конечные ретентаты разбавляли до около 100 мкл, затем колонки помещали вверх дном в свежие пробирки для сбора образцов и центрифугировали при 1000 x g в течение 2 мин. для сбора образцов. Промытые образцы переносили в черные микропробирки и хранили при 4°C.
Для экспериментов по трансдукции и контролей 25 мкл бактерий (или PBS) и 25 мкл меченого SYBR Gold фага (или буфера SM) объединяли в черных микропробирках и инкубировали в неподвижном состоянии в течение 15-20 мин. при комнатной температуре для обеспечения адсорбции фагов и впрыскивания в получающие их бактерии. Сразу после инкубирования 50 мкл 10% формалина добавляли к образцам, и фиксацию осуществляли при комнатной температуре в течение ~4 ч. Образцы промывали с помощью PBS с использованием колонок Amicon, как указано выше.
Для успешного инфицирования фагом бактериальной клетки-хозяина требовалось впрыскивание нуклеиновой кислоты бактериофагов. Колифаг P1kc, меченный SYBR Gold и инкубированный совместно с S. marcescens, выявил присутствие флуоресцирующих бактерий с помощью микроскопии, подтверждая применение данного анализа в процессе выделения фагов. Как и в случае анализа Seahorse, данный подход предусматривал альтернативу традиционным способам анализа фагов для обеспечения распространения на организмы, не поддающиеся анализу бляшкообразования. Кроме того, анализ трансдукции с использованием SYBR Gold не требовал роста бактерий, поэтому был применим для анализа фагов, целенаправленно воздействующих на сложные в культивировании или даже не поддающиеся культивированию организмы, в том числе эндосимбионты, такие как Buchnera.
Исследование эффективности фагов in vivo в отношении S. marcescens у мух Drosophila melanogaster
Культуры S. marcescens выращивали в триптическом соевом бульоне (TSB) при 30°C при постоянном встряхивании при 200 об./мин.
Среда, используемая для выкармливания исходных популяций мух, представляла собой среду, содержащую кукурузную муку, мелассу и дрожжи (11 г/л дрожжей, 54 г/л желтой кукурузной муки, 5 г/л агара, 66 мл/л мелассы и 4,8 мл/л пропионовой кислоты). Все компоненты этого рациона, за исключением пропионовой кислоты, нагревали совместно до 80°C в деионизированной воде при постоянном перемешивании в течение 30 минут, и им давали охладиться до 60°C. Затем примешивали пропионовую кислоту, и 50 мл рациона разделяли на аликвоты в отдельные флаконы и оставляли охлаждаться и затвердевать. Мух выращивали при 26°C, цикле свет:темнота 16:8 часов, при влажности около 60%.
Для инфицирования мух S. marcescens тонкую иглу (с кончиком шириной приблизительно 10 мкм) погружали в плотную ночную культуру в стационарной фазе, и грудь мух прокалывали. Для этого эксперимента четыре повторности по 10 самцов и 10 самок в каждой инфицировали S. marcescens с помощью способа прокалывания иглой в качестве положительного контроля в отношении смертности мух. В группах обработки четырем повторностям по 10 самцов и 10 самок в каждой вводили путем прокалывания S. marcescens и раствор фага, содержащий приблизительно 108 фаговых частиц/мл. Наконец, две повторности по 10 самцов и 10 самок в каждой, которых не прокалывали и не обрабатывали каким-либо другим образом, использовали в качестве отрицательного контроля в отношении смертности.
Мух во всех состояниях помещали во флаконы с кормовой средой и инкубировали при 26°C, цикле свет:темнота 16:8 часов, при влажности 60%. Число живых и мертвых мух подсчитывали ежедневно в течение четырех дней после прокалывания. Все мухи, которым вводили путем прокалывания только S. marcescens, были мертвыми через 24 часа после обработки. Для сравнения, более чем 60% мух в группе обработки фагами и все мухи в группе контроля без обработки были живыми в этот момент времени (фиг. 5). Кроме того, большинство мух в группе обработки фагами и группе отрицательного контроля продолжали выживать в течение еще четырех дней после того, как эксперимент завершали.
Для определения причины гибели мух мертвых мух из мух, которым вводили путем прокалывания как S. marcescens, так и S. marcescens+фаги, гомогенизировали и высевали. Четыре мертвые мухи из каждой из четырех повторностей обработки как с помощью S. marcescens, так и с помощью S. marcescens+фагов гомогенизировали в 100 мкл TSB. Разведение 1:100 также получали путем разведения гомогената в TSB. 10 мкл концентрированного гомогената, а также разведение 1:100 высевали на чашки с TSA и инкубировали в течение ночи при 30°C. При исследовании чашек в отношении роста бактерий во всех чашках с мертвыми мухами, которым вводили путем прокалывания S. marcescens, был газон из бактерий, растущих на них, тогда как в чашках с мертвыми мухами, которым вводили путем прокалывания S. marcescens+фаги, не было бактерий. Это указывало на то, что в отсутствие фага S. marcescens, вероятно, индуцировала септический шок у мух, приводя к их смерти. В то же время в присутствии фага смертность могла быть обусловлена повреждением, вызванным прокалыванием иглой.
ДРУГИЕ ВАРИАНТЫ ОСУЩЕСТВЛЕНИЯ
Несмотря на то, что вышеизложенное изобретение было достаточно подробно описано с помощью иллюстраций и примеров в целях ясности понимания, описания и примеры не следует истолковывать как ограничивающие объем настоящего изобретения. Раскрытия всех источников патентной и научной литературы, цитируемых в данном документе, явным образом включено в их полном объеме посредством ссылки.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> Flagship Pioneering, Inc.
<120> КОМПОЗИЦИИ И СООТВЕТСТВУЮЩИЕ СПОСОБЫ ДЛЯ СЕЛЬСКОГО ХОЗЯЙСТВА
<130> 51215-002WO3
<150> US 62/583,736
<151> 2017-11-09
<150> US 62/450,017
<151> 2017-01-24
<160> 198
<170> PatentIn версия 3.5
<210> 1
<211> 1505
<212> ДНК
<213> Snodgrassella alvi
<400> 1
gagagtttga tcctggctca gattgaacgc tggcggcatg ccttacacat gcaagtcgaa
60
cggcagcacg gagagcttgc tctctggtgg cgagtggcga acgggtgagt aatgcatcgg
120
aacgtaccga gtaatggggg ataactgtcc gaaaggatgg ctaataccgc atacgccctg
180
agggggaaag cgggggatcg aaagacctcg cgttatttga gcggccgatg ttggattagc
240
tagttggtgg ggtaaaggcc taccaaggcg acgatccata gcgggtctga gaggatgatc
300
cgccacattg ggactgagac acggcccaaa ctcctacggg aggcagcagt ggggaatttt
360
ggacaatggg gggaaccctg atccagccat gccgcgtgtc tgaagaaggc cttcgggttg
420
taaaggactt ttgttaggga agaaaagccg ggtgttaata ccatctggtg ctgacggtac
480
ctaaagaata agcaccggct aactacgtgc cagcagccgc ggtaatacgt agggtgcgag
540
cgttaatcgg aattactggg cgtaaagcga gcgcagacgg ttaattaagt cagatgtgaa
600
atccccgagc tcaacttggg acgtgcattt gaaactggtt aactagagtg tgtcagaggg
660
aggtagaatt ccacgtgtag cagtgaaatg cgtagagatg tggaggaata ccgatggcga
720
aggcagcctc ctgggataac actgacgttc atgctcgaaa gcgtgggtag caaacaggat
780
tagataccct ggtagtccac gccctaaacg atgacaatta gctgttggga cactagatgt
840
cttagtagcg aagctaacgc gtgaaattgt ccgcctgggg agtacggtcg caagattaaa
900
actcaaagga attgacgggg acccgcacaa gcggtggatg atgtggatta attcgatgca
960
acgcgaagaa ccttacctgg tcttgacatg tacggaatct cttagagata ggagagtgcc
1020
ttcgggaacc gtaacacagg tgctgcatgg ctgtcgtcag ctcgtgtcgt gagatgttgg
1080
gttaagtccc gcaacgagcg caacccttgt cattagttgc catcattaag ttgggcactc
1140
taatgagact gccggtgaca aaccggagga aggtggggat gacgtcaagt cctcatggcc
1200
cttatgacca gggcttcaca cgtcatacaa tggtcggtac agagggtagc gaagccgcga
1260
ggtgaagcca atctcagaaa gccgatcgta gtccggattg cactctgcaa ctcgagtgca
1320
tgaagtcgga atcgctagta atcgcaggtc agcatactgc ggtgaatacg ttcccgggtc
1380
ttgtacacac cgcccgtcac accatgggag tgggggatac cagaattggg tagactaacc
1440
gcaaggaggt cgcttaacac ggtatgcttc atgactgggg tgaagtcgta acaaggtagc
1500
cgtag
1505
<210> 2
<211> 1541
<212> ДНК
<213> Gilliamella apicola
<400> 2
ttaaattgaa gagtttgatc atggctcaga ttgaacgctg gcggcaggct taacacatgc
60
aagtcgaacg gtaacatgag tgcttgcact tgatgacgag tggcggacgg gtgagtaaag
120
tatggggatc tgccgaatgg agggggacaa cagttggaaa cgactgctaa taccgcataa
180
agttgagaga ccaaagcatg ggaccttcgg gccatgcgcc atttgatgaa cccatatggg
240
attagctagt tggtagggta atggcttacc aaggcgacga tctctagctg gtctgagagg
300
atgaccagcc acactggaac tgagacacgg tccagactcc tacgggaggc agcagtgggg
360
aatattgcac aatgggggaa accctgatgc agccatgccg cgtgtatgaa gaaggccttc
420
gggttgtaaa gtactttcgg tgatgaggaa ggtggtgtat ctaataggtg catcaattga
480
cgttaattac agaagaagca ccggctaact ccgtgccagc agccgcggta atacggaggg
540
tgcgagcgtt aatcggaatg actgggcgta aagggcatgt aggcggataa ttaagttagg
600
tgtgaaagcc ctgggctcaa cctaggaatt gcacttaaaa ctggttaact agagtattgt
660
agaggaaggt agaattccac gtgtagcggt gaaatgcgta gagatgtgga ggaataccgg
720
tggcgaaggc ggccttctgg acagatactg acgctgagat gcgaaagcgt ggggagcaaa
780
caggattaga taccctggta gtccacgctg taaacgatgt cgatttggag tttgttgcct
840
agagtgatgg gctccgaagc taacgcgata aatcgaccgc ctggggagta cggccgcaag
900
gttaaaactc aaatgaattg acgggggccc gcacaagcgg tggagcatgt ggtttaattc
960
gatgcaacgc gaagaacctt acctggtctt gacatccaca gaatcttgca gagatgcggg
1020
agtgccttcg ggaactgtga gacaggtgct gcatggctgt cgtcagctcg tgttgtgaaa
1080
tgttgggtta agtcccgcaa cgagcgcaac ccttatcctt tgttgccatc ggttaggccg
1140
ggaactcaaa ggagactgcc gttgataaag cggaggaagg tggggacgac gtcaagtcat
1200
catggccctt acgaccaggg ctacacacgt gctacaatgg cgtatacaaa gggaggcgac
1260
ctcgcgagag caagcggacc tcataaagta cgtctaagtc cggattggag tctgcaactc
1320
gactccatga agtcggaatc gctagtaatc gtgaatcaga atgtcacggt gaatacgttc
1380
ccgggccttg tacacaccgc ccgtcacacc atgggagtgg gttgcaccag aagtagatag
1440
cttaaccttc gggagggcgt ttaccacggt gtggtccatg actggggtga agtcgtaaca
1500
aggtaaccgt aggggaacct gcggttggat cacctcctta c
1541
<210> 3
<211> 1528
<212> ДНК
<213> Bartonella apis
<400> 3
aagccaaaat caaattttca acttgagagt ttgatcctgg ctcagaacga acgctggcgg
60
caggcttaac acatgcaagt cgaacgcact tttcggagtg agtggcagac gggtgagtaa
120
cgcgtgggaa tctacctatt tctacggaat aacgcagaga aatttgtgct aataccgtat
180
acgtccttcg ggagaaagat ttatcggaga tagatgagcc cgcgttggat tagctagttg
240
gtgaggtaat ggcccaccaa ggcgacgatc catagctggt ctgagaggat gaccagccac
300
attgggactg agacacggcc cagactccta cgggaggcag cagtggggaa tattggacaa
360
tgggcgcaag cctgatccag ccatgccgcg tgagtgatga aggccctagg gttgtaaagc
420
tctttcaccg gtgaagataa tgacggtaac cggagaagaa gccccggcta acttcgtgcc
480
agcagccgcg gtaatacgaa gggggctagc gttgttcgga tttactgggc gtaaagcgca
540
cgtaggcgga tatttaagtc aggggtgaaa tcccggggct caaccccgga actgcctttg
600
atactggata tcttgagtat ggaagaggta agtggaattc cgagtgtaga ggtgaaattc
660
gtagatattc ggaggaacac cagtggcgaa ggcggcttac tggtccatta ctgacgctga
720
ggtgcgaaag cgtggggagc aaacaggatt agataccctg gtagtccacg ctgtaaacga
780
tgaatgttag ccgttggaca gtttactgtt cggtggcgca gctaacgcat taaacattcc
840
gcctggggag tacggtcgca agattaaaac tcaaaggaat tgacgggggc ccgcacaagc
900
ggtggagcat gtggtttaat tcgaagcaac gcgcagaacc ttaccagccc ttgacatccc
960
gatcgcggat ggtggagaca ccgtctttca gttcggctgg atcggtgaca ggtgctgcat
1020
ggctgtcgtc agctcgtgtc gtgagatgtt gggttaagtc ccgcaacgag cgcaaccctc
1080
gcccttagtt gccatcattt agttgggcac tctaagggga ctgccggtga taagccgaga
1140
ggaaggtggg gatgacgtca agtcctcatg gcccttacgg gctgggctac acacgtgcta
1200
caatggtggt gacagtgggc agcgagaccg cgaggtcgag ctaatctcca aaagccatct
1260
cagttcggat tgcactctgc aactcgagtg catgaagttg gaatcgctag taatcgtgga
1320
tcagcatgcc acggtgaata cgttcccggg ccttgtacac accgcccgtc acaccatggg
1380
agttggtttt acccgaaggt gctgtgctaa ccgcaaggag gcaggcaacc acggtagggt
1440
cagcgactgg ggtgaagtcg taacaaggta gccgtagggg aacctgcggc tggatcacct
1500
cctttctaag gaagatgaag aattggaa
1528
<210> 4
<211> 1390
<212> ДНК
<213> Parasaccharibacter apium
<220>
<221> другой_признак
<222> (643)..(756)
<223> n представляет собой a, g, c или t
<400> 4
ctaccatgca agtcgcacga aacctttcgg ggttagtggc ggacgggtga gtaacgcgtt
60
aggaacctat ctggaggtgg gggataacat cgggaaactg gtgctaatac cgcatgatgc
120
ctgagggcca aaggagagat ccgccattgg aggggcctgc gttcgattag ctagttggtt
180
gggtaaaggc tgaccaaggc gatgatcgat agctggtttg agaggatgat cagccacact
240
gggactgaga cacggcccag actcctacgg gaggcagcag tggggaatat tggacaatgg
300
gggcaaccct gatccagcaa tgccgcgtgt gtgaagaagg tcttcggatt gtaaagcact
360
ttcactaggg aagatgatga cggtacctag agaagaagcc ccggctaact tcgtgccagc
420
agccgcggta atacgaaggg ggctagcgtt gctcggaatg actgggcgta aagggcgcgt
480
aggctgtttg tacagtcaga tgtgaaatcc ccgggcttaa cctgggaact gcatttgata
540
cgtgcagact agagtccgag agagggttgt ggaattccca gtgtagaggt gaaattcgta
600
gatattggga agaacaccgg ttgcgaaggc ggcaacctgg ctnnnnnnnn nnnnnnnnnn
660
nnnnnnnnnn nnnnnnnnnn nnnnnnnnnn nnnnnnnnnn nnnnnnnnnn nnnnnnnnnn
720
nnnnnnnnnn nnnnnnnnnn nnnnnnnnnn nnnnnngagc taacgcgtta agcacaccgc
780
ctggggagta cggccgcaag gttgaaactc aaaggaattg acgggggccc gcacaagcgg
840
tggagcatgt ggtttaattc gaagcaacgc gcagaacctt accagggctt gcatggggag
900
gctgtattca gagatggata tttcttcgga cctcccgcac aggtgctgca tggctgtcgt
960
cagctcgtgt cgtgagatgt tgggttaagt cccgcaacga gcgcaaccct tgtctttagt
1020
tgccatcacg tctgggtggg cactctagag agactgccgg tgacaagccg gaggaaggtg
1080
gggatgacgt caagtcctca tggcccttat gtcctgggct acacacgtgc tacaatggcg
1140
gtgacagagg gatgctacat ggtgacatgg tgctgatctc aaaaaaccgt ctcagttcgg
1200
attgtactct gcaactcgag tgcatgaagg tggaatcgct agtaatcgcg gatcagcatg
1260
ccgcggtgaa tacgttcccg ggccttgtac acaccgcccg tcacaccatg ggagttggtt
1320
tgaccttaag ccggtgagcg aaccgcaagg aacgcagccg accaccggtt cgggttcagc
1380
gactggggga
1390
<210> 5
<211> 1549
<212> ДНК
<213> Enterococcus
<400> 5
aggtgatcca gccgcacctt ccgatacggc taccttgtta cgacttcacc ccaatcatct
60
atcccacctt aggcggctgg ctccaaaaag gttacctcac cgacttcggg tgttacaaac
120
tctcgtggtg tgacgggcgg tgtgtacaag gcccgggaac gtattcaccg cggcgtgctg
180
atccgcgatt actagcgatt ccggcttcat gcaggcgagt tgcagcctgc aatccgaact
240
gagagaagct ttaagagatt tgcatgacct cgcggtctag cgactcgttg tacttcccat
300
tgtagcacgt gtgtagccca ggtcataagg ggcatgatga tttgacgtca tccccacctt
360
cctccggttt gtcaccggca gtctcgctag agtgcccaac taaatgatgg caactaacaa
420
taagggttgc gctcgttgcg ggacttaacc caacatctca cgacacgagc tgacgacaac
480
catgcaccac ctgtcacttt gtccccgaag ggaaagctct atctctagag tggtcaaagg
540
atgtcaagac ctggtaaggt tcttcgcgtt gcttcgaatt aaaccacatg ctccaccgct
600
tgtgcgggcc cccgtcaatt cctttgagtt tcaaccttgc ggtcgtactc cccaggcgga
660
gtgcttaatg cgtttgctgc agcactgaag ggcggaaacc ctccaacact tagcactcat
720
cgtttacggc gtggactacc agggtatcta atcctgtttg ctccccacgc tttcgagcct
780
cagcgtcagt tacagaccag agagccgcct tcgccactgg tgttcctcca tatatctacg
840
catttcaccg ctacacatgg aattccactc tcctcttctg cactcaagtc tcccagtttc
900
caatgaccct ccccggttga gccgggggct ttcacatcag acttaagaaa ccgcctgcgc
960
tcgctttacg cccaataaat ccggacaacg cttgccacct acgtattacc gcggctgctg
1020
gcacgtagtt agccgtggct ttctggttag ataccgtcag gggacgttca gttactaacg
1080
tccttgttct tctctaacaa cagagtttta cgatccgaaa accttcttca ctcacgcggc
1140
gttgctcggt cagactttcg tccattgccg aagattccct actgctgcct cccgtaggag
1200
tctgggccgt gtctcagtcc cagtgtggcc gatcaccctc tcaggtcggc tatgcatcgt
1260
ggccttggtg agccgttacc tcaccaacta gctaatgcac cgcgggtcca tccatcagcg
1320
acacccgaaa gcgcctttca ctcttatgcc atgcggcata aactgttatg cggtattagc
1380
acctgtttcc aagtgttatc cccctctgat gggtaggtta cccacgtgtt actcacccgt
1440
ccgccactcc tctttccaat tgagtgcaag cactcgggag gaaagaagcg ttcgacttgc
1500
atgtattagg cacgccgcca gcgttcgtcc tgagccagga tcaaactct
1549
<210> 6
<211> 1541
<212> ДНК
<213> Delftia
<400> 6
cagaaaggag gtgatccagc cgcaccttcc gatacggcta ccttgttacg acttcacccc
60
agtcacgaac cccgccgtgg taagcgccct ccttgcggtt aggctaccta cttctggcga
120
gacccgctcc catggtgtga cgggcggtgt gtacaagacc cgggaacgta ttcaccgcgg
180
catgctgatc cgcgattact agcgattccg acttcacgca gtcgagttgc agactgcgat
240
ccggactacg actggtttta tgggattagc tccccctcgc gggttggcaa ccctctgtac
300
cagccattgt atgacgtgtg tagccccacc tataagggcc atgaggactt gacgtcatcc
360
ccaccttcct ccggtttgtc accggcagtc tcattagagt gctcaactga atgtagcaac
420
taatgacaag ggttgcgctc gttgcgggac ttaacccaac atctcacgac acgagctgac
480
gacagccatg cagcacctgt gtgcaggttc tctttcgagc acgaatccat ctctggaaac
540
ttcctgccat gtcaaaggtg ggtaaggttt ttcgcgttgc atcgaattaa accacatcat
600
ccaccgcttg tgcgggtccc cgtcaattcc tttgagtttc aaccttgcgg ccgtactccc
660
caggcggtca acttcacgcg ttagcttcgt tactgagaaa actaattccc aacaaccagt
720
tgacatcgtt tagggcgtgg actaccaggg tatctaatcc tgtttgctcc ccacgctttc
780
gtgcatgagc gtcagtacag gtccagggga ttgccttcgc catcggtgtt cctccgcata
840
tctacgcatt tcactgctac acgcggaatt ccatccccct ctaccgtact ctagccatgc
900
agtcacaaat gcagttccca ggttgagccc ggggatttca catctgtctt acataaccgc
960
ctgcgcacgc tttacgccca gtaattccga ttaacgctcg caccctacgt attaccgcgg
1020
ctgctggcac gtagttagcc ggtgcttatt cttacggtac cgtcatgggc cccctgtatt
1080
agaaggagct ttttcgttcc gtacaaaagc agtttacaac ccgaaggcct tcatcctgca
1140
cgcggcattg ctggatcagg ctttcgccca ttgtccaaaa ttccccactg ctgcctcccg
1200
taggagtctg ggccgtgtct cagtcccagt gtggctggtc gtcctctcag accagctaca
1260
gatcgtcggc ttggtaagct tttatcccac caactaccta atctgccatc ggccgctcca
1320
atcgcgcgag gcccgaaggg cccccgcttt catcctcaga tcgtatgcgg tattagctac
1380
tctttcgagt agttatcccc cacgactggg cacgttccga tgtattactc acccgttcgc
1440
cactcgtcag cgtccgaaga cctgttaccg ttcgacttgc atgtgtaagg catgccgcca
1500
gcgttcaatc tgagccagga tcaaactcta cagttcgatc t
1541
<210> 7
<211> 1502
<212> ДНК
<213> Pelomonas
<220>
<221> другой_признак
<222> (192)..(193)
<223> n представляет собой a, c, g или t
<220>
<221> другой_признак
<222> (832)..(833)
<223> n представляет собой a, c, g или t
<400> 7
atcctggctc agattgaacg ctggcggcat gccttacaca tgcaagtcga acggtaacag
60
gttaagctga cgagtggcga acgggtgagt aatatatcgg aacgtgccca gtcgtggggg
120
ataactgctc gaaagagcag ctaataccgc atacgacctg agggtgaaag cgggggatcg
180
caagacctcg cnngattgga gcggccgata tcagattagg tagttggtgg ggtaaaggcc
240
caccaagcca acgatctgta gctggtctga gaggacgacc agccacactg ggactgagac
300
acggcccaga ctcctacggg aggcagcagt ggggaatttt ggacaatggg cgcaagcctg
360
atccagccat gccgcgtgcg ggaagaaggc cttcgggttg taaaccgctt ttgtcaggga
420
agaaaaggtt ctggttaata cctgggactc atgacggtac ctgaagaata agcaccggct
480
aactacgtgc cagcagccgc ggtaatacgt agggtgcaag cgttaatcgg aattactggg
540
cgtaaagcgt gcgcaggcgg ttatgcaaga cagaggtgaa atccccgggc tcaacctggg
600
aactgccttt gtgactgcat agctagagta cggtagaggg ggatggaatt ccgcgtgtag
660
cagtgaaatg cgtagatatg cggaggaaca ccgatggcga aggcaatccc ctggacctgt
720
actgacgctc atgcacgaaa gcgtggggag caaacaggat tagataccct ggtagtccac
780
gccctaaacg atgtcaactg gttgttggga gggtttcttc tcagtaacgt anntaacgcg
840
tgaagttgac cgcctgggga gtacggccgc aaggttgaaa ctcaaaggaa ttgacgggga
900
cccgcacaag cggtggatga tgtggtttaa ttcgatgcaa cgcgaaaaac cttacctacc
960
cttgacatgc caggaatcct gaagagattt gggagtgctc gaaagagaac ctggacacag
1020
gtgctgcatg gccgtcgtca gctcgtgtcg tgagatgttg ggttaagtcc cgcaacgagc
1080
gcaacccttg tcattagttg ctacgaaagg gcactctaat gagactgccg gtgacaaacc
1140
ggaggaaggt ggggatgacg tcaggtcatc atggccctta tgggtagggc tacacacgtc
1200
atacaatggc cgggacagag ggctgccaac ccgcgagggg gagctaatcc cagaaacccg
1260
gtcgtagtcc ggatcgtagt ctgcaactcg actgcgtgaa gtcggaatcg ctagtaatcg
1320
cggatcagct tgccgcggtg aatacgttcc cgggtcttgt acacaccgcc cgtcacacca
1380
tgggagcggg ttctgccaga agtagttagc ctaaccgcaa ggagggcgat taccacggca
1440
gggttcgtga ctggggtgaa gtcgtaacaa ggtagccgta tcggaaggtg cggctggatc
1500
ac
1502
<210> 8
<211> 34
<212> БЕЛОК
<213> Lactococcus lactis
<400> 8
Ile Thr Ser Ile Ser Leu Cys Thr Pro Gly Cys Lys Thr Gly Ala Leu
1 5 10 15
Met Gly Cys Asn Met Lys Thr Ala Thr Cys His Cys Ser Ile His Val
20 25 30
Ser Lys
<210> 9
<211> 22
<212> БЕЛОК
<213> Staphylococcus epidermis
<400> 9
Ile Ala Ser Lys Phe Ile Cys Thr Pro Gly Cys Ala Lys Thr Gly Ser
1 5 10 15
Phe Asn Ser Tyr Cys Cys
20
<210> 10
<211> 44
<212> БЕЛОК
<213> Pediococcus acidilactici
<400> 10
Lys Tyr Tyr Gly Asn Gly Val Thr Cys Gly Lys His Ser Cys Ser Val
1 5 10 15
Asp Trp Gly Lys Ala Thr Thr Cys Ile Ile Asn Asn Gly Ala Met Ala
20 25 30
Trp Ala Thr Gly Gly His Gln Gly Asn His Lys Cys
35 40
<210> 11
<211> 44
<212> БЕЛОК
<213> Enterococcus faecium
<400> 11
Ala Thr Arg Ser Tyr Gly Asn Gly Val Tyr Cys Asn Asn Ser Lys Cys
1 5 10 15
Trp Val Asn Trp Gly Glu Ala Lys Glu Asn Ile Ala Gly Ile Val Ile
20 25 30
Ser Gly Trp Ala Ser Gly Leu Ala Gly Met Gly His
35 40
<210> 12
<211> 39
<212> БЕЛОК
<213> Streptococcus lactis
<400> 12
Gly Thr Trp Asp Asp Ile Gly Gln Gly Ile Gly Arg Val Ala Tyr Trp
1 5 10 15
Val Gly Lys Ala Met Gly Asn Met Ser Asp Val Asn Gln Ala Ser Arg
20 25 30
Ile Asn Arg Lys Lys Lys His
35
<210> 13
<211> 48
<212> БЕЛОК
<213> Lactobacillus johnsonii
<400> 13
Asn Arg Trp Gly Asp Thr Val Leu Ser Ala Ala Ser Gly Ala Gly Thr
1 5 10 15
Gly Ile Lys Ala Cys Lys Ser Phe Gly Pro Trp Gly Met Ala Ile Cys
20 25 30
Gly Val Gly Gly Ala Ala Ile Gly Gly Tyr Phe Gly Tyr Thr His Asn
35 40 45
<210> 14
<211> 70
<212> БЕЛОК
<213> Enterococcus faecalis
<400> 14
Met Ala Lys Glu Phe Gly Ile Pro Ala Ala Val Ala Gly Thr Val Leu
1 5 10 15
Asn Val Val Glu Ala Gly Gly Trp Val Thr Thr Ile Val Ser Ile Leu
20 25 30
Thr Ala Val Gly Ser Gly Gly Leu Ser Leu Leu Ala Ala Ala Gly Arg
35 40 45
Glu Ser Ile Lys Ala Tyr Leu Lys Lys Glu Ile Lys Lys Lys Gly Lys
50 55 60
Arg Ala Val Ile Ala Trp
65 70
<210> 15
<211> 51
<212> БЕЛОК
<213> Staphylococcus aureus
<400> 15
Met Ser Trp Leu Asn Phe Leu Lys Tyr Ile Ala Lys Tyr Gly Lys Lys
1 5 10 15
Ala Val Ser Ala Ala Trp Lys Tyr Lys Gly Lys Val Leu Glu Trp Leu
20 25 30
Asn Val Gly Pro Thr Leu Glu Trp Val Trp Gln Lys Leu Lys Lys Ile
35 40 45
Ala Gly Leu
50
<210> 16
<211> 43
<212> БЕЛОК
<213> Lactococcus garvieae
<400> 16
Ile Gly Gly Ala Leu Gly Asn Ala Leu Asn Gly Leu Gly Thr Trp Ala
1 5 10 15
Asn Met Met Asn Gly Gly Gly Phe Val Asn Gln Trp Gln Val Tyr Ala
20 25 30
Asn Lys Gly Lys Ile Asn Gln Tyr Arg Pro Tyr
35 40
<210> 17
<211> 103
<212> БЕЛОК
<213> Escherichia coli
<400> 17
Met Arg Thr Leu Thr Leu Asn Glu Leu Asp Ser Val Ser Gly Gly Ala
1 5 10 15
Ser Gly Arg Asp Ile Ala Met Ala Ile Gly Thr Leu Ser Gly Gln Phe
20 25 30
Val Ala Gly Gly Ile Gly Ala Ala Ala Gly Gly Val Ala Gly Gly Ala
35 40 45
Ile Tyr Asp Tyr Ala Ser Thr His Lys Pro Asn Pro Ala Met Ser Pro
50 55 60
Ser Gly Leu Gly Gly Thr Ile Lys Gln Lys Pro Glu Gly Ile Pro Ser
65 70 75 80
Glu Ala Trp Asn Tyr Ala Ala Gly Arg Leu Cys Asn Trp Ser Pro Asn
85 90 95
Asn Leu Ser Asp Val Cys Leu
100
<210> 18
<211> 339
<212> БЕЛОК
<213> Cp1
<400> 18
Met Val Lys Lys Asn Asp Leu Phe Val Asp Val Ser Ser His Asn Gly
1 5 10 15
Tyr Asp Ile Thr Gly Ile Leu Glu Gln Met Gly Thr Thr Asn Thr Ile
20 25 30
Ile Lys Ile Ser Glu Ser Thr Thr Tyr Leu Asn Pro Cys Leu Ser Ala
35 40 45
Gln Val Glu Gln Ser Asn Pro Ile Gly Phe Tyr His Phe Ala Arg Phe
50 55 60
Gly Gly Asp Val Ala Glu Ala Glu Arg Glu Ala Gln Phe Phe Leu Asp
65 70 75 80
Asn Val Pro Met Gln Val Lys Tyr Leu Val Leu Asp Tyr Glu Asp Asp
85 90 95
Pro Ser Gly Asp Ala Gln Ala Asn Thr Asn Ala Cys Leu Arg Phe Met
100 105 110
Gln Met Ile Ala Asp Ala Gly Tyr Lys Pro Ile Tyr Tyr Ser Tyr Lys
115 120 125
Pro Phe Thr His Asp Asn Val Asp Tyr Gln Gln Ile Leu Ala Gln Phe
130 135 140
Pro Asn Ser Leu Trp Ile Ala Gly Tyr Gly Leu Asn Asp Gly Thr Ala
145 150 155 160
Asn Phe Glu Tyr Phe Pro Ser Met Asp Gly Ile Arg Trp Trp Gln Tyr
165 170 175
Ser Ser Asn Pro Phe Asp Lys Asn Ile Val Leu Leu Asp Asp Glu Glu
180 185 190
Asp Asp Lys Pro Lys Thr Ala Gly Thr Trp Lys Gln Asp Ser Lys Gly
195 200 205
Trp Trp Phe Arg Arg Asn Asn Gly Ser Phe Pro Tyr Asn Lys Trp Glu
210 215 220
Lys Ile Gly Gly Val Trp Tyr Tyr Phe Asp Ser Lys Gly Tyr Cys Leu
225 230 235 240
Thr Ser Glu Trp Leu Lys Asp Asn Glu Lys Trp Tyr Tyr Leu Lys Asp
245 250 255
Asn Gly Ala Met Ala Thr Gly Trp Val Leu Val Gly Ser Glu Trp Tyr
260 265 270
Tyr Met Asp Asp Ser Gly Ala Met Val Thr Gly Trp Val Lys Tyr Lys
275 280 285
Asn Asn Trp Tyr Tyr Met Thr Asn Glu Arg Gly Asn Met Val Ser Asn
290 295 300
Glu Phe Ile Lys Ser Gly Lys Gly Trp Tyr Phe Met Asn Thr Asn Gly
305 310 315 320
Glu Leu Ala Asp Asn Pro Ser Phe Thr Lys Glu Pro Asp Gly Leu Ile
325 330 335
Thr Val Ala
<210> 19
<211> 296
<212> БЕЛОК
<213> Dp-1
<400> 19
Met Gly Val Asp Ile Glu Lys Gly Val Ala Trp Met Gln Ala Arg Lys
1 5 10 15
Gly Arg Val Ser Tyr Ser Met Asp Phe Arg Asp Gly Pro Asp Ser Tyr
20 25 30
Asp Cys Ser Ser Ser Met Tyr Tyr Ala Leu Arg Ser Ala Gly Ala Ser
35 40 45
Ser Ala Gly Trp Ala Val Asn Thr Glu Tyr Met His Ala Trp Leu Ile
50 55 60
Glu Asn Gly Tyr Glu Leu Ile Ser Glu Asn Ala Pro Trp Asp Ala Lys
65 70 75 80
Arg Gly Asp Ile Phe Ile Trp Gly Arg Lys Gly Ala Ser Ala Gly Ala
85 90 95
Gly Gly His Thr Gly Met Phe Ile Asp Ser Asp Asn Ile Ile His Cys
100 105 110
Asn Tyr Ala Tyr Asp Gly Ile Ser Val Asn Asp His Asp Glu Arg Trp
115 120 125
Tyr Tyr Ala Gly Gln Pro Tyr Tyr Tyr Val Tyr Arg Leu Thr Asn Ala
130 135 140
Asn Ala Gln Pro Ala Glu Lys Lys Leu Gly Trp Gln Lys Asp Ala Thr
145 150 155 160
Gly Phe Trp Tyr Ala Arg Ala Asn Gly Thr Tyr Pro Lys Asp Glu Phe
165 170 175
Glu Tyr Ile Glu Glu Asn Lys Ser Trp Phe Tyr Phe Asp Asp Gln Gly
180 185 190
Tyr Met Leu Ala Glu Lys Trp Leu Lys His Thr Asp Gly Asn Trp Tyr
195 200 205
Trp Phe Asp Arg Asp Gly Tyr Met Ala Thr Ser Trp Lys Arg Ile Gly
210 215 220
Glu Ser Trp Tyr Tyr Phe Asn Arg Asp Gly Ser Met Val Thr Gly Trp
225 230 235 240
Ile Lys Tyr Tyr Asp Asn Trp Tyr Tyr Cys Asp Ala Thr Asn Gly Asp
245 250 255
Met Lys Ser Asn Ala Phe Ile Arg Tyr Asn Asp Gly Trp Tyr Leu Leu
260 265 270
Leu Pro Asp Gly Arg Leu Ala Asp Lys Pro Gln Phe Thr Val Glu Pro
275 280 285
Asp Gly Leu Ile Thr Ala Lys Val
290 295
<210> 20
<211> 233
<212> БЕЛОК
<213> гамма
<400> 20
Met Glu Ile Gln Lys Lys Leu Val Asp Pro Ser Lys Tyr Gly Thr Lys
1 5 10 15
Cys Pro Tyr Thr Met Lys Pro Lys Tyr Ile Thr Val His Asn Thr Tyr
20 25 30
Asn Asp Ala Pro Ala Glu Asn Glu Val Ser Tyr Met Ile Ser Asn Asn
35 40 45
Asn Glu Val Ser Phe His Ile Ala Val Asp Asp Lys Lys Ala Ile Gln
50 55 60
Gly Ile Pro Leu Glu Arg Asn Ala Trp Ala Cys Gly Asp Gly Asn Gly
65 70 75 80
Ser Gly Asn Arg Gln Ser Ile Ser Val Glu Ile Cys Tyr Ser Lys Ser
85 90 95
Gly Gly Asp Arg Tyr Tyr Lys Ala Glu Asp Asn Ala Val Asp Val Val
100 105 110
Arg Gln Leu Met Ser Met Tyr Asn Ile Pro Ile Glu Asn Val Arg Thr
115 120 125
His Gln Ser Trp Ser Gly Lys Tyr Cys Pro His Arg Met Leu Ala Glu
130 135 140
Gly Arg Trp Gly Ala Phe Ile Gln Lys Val Lys Asn Gly Asn Val Ala
145 150 155 160
Thr Thr Ser Pro Thr Lys Gln Asn Ile Ile Gln Ser Gly Ala Phe Ser
165 170 175
Pro Tyr Glu Thr Pro Asp Val Met Gly Ala Leu Thr Ser Leu Lys Met
180 185 190
Thr Ala Asp Phe Ile Leu Gln Ser Asp Gly Leu Thr Tyr Phe Ile Ser
195 200 205
Lys Pro Thr Ser Asp Ala Gln Leu Lys Ala Met Lys Glu Tyr Leu Asp
210 215 220
Arg Lys Gly Trp Trp Tyr Glu Val Lys
225 230
<210> 21
<211> 481
<212> БЕЛОК
<213> MR11
<400> 21
Met Gln Ala Lys Leu Thr Lys Lys Glu Phe Ile Glu Trp Leu Lys Thr
1 5 10 15
Ser Glu Gly Lys Gln Phe Asn Val Asp Leu Trp Tyr Gly Phe Gln Cys
20 25 30
Phe Asp Tyr Ala Asn Ala Gly Trp Lys Val Leu Phe Gly Leu Leu Leu
35 40 45
Lys Gly Leu Gly Ala Lys Asp Ile Pro Phe Ala Asn Asn Phe Asp Gly
50 55 60
Leu Ala Thr Val Tyr Gln Asn Thr Pro Asp Phe Leu Ala Gln Pro Gly
65 70 75 80
Asp Met Val Val Phe Gly Ser Asn Tyr Gly Ala Gly Tyr Gly His Val
85 90 95
Ala Trp Val Ile Glu Ala Thr Leu Asp Tyr Ile Ile Val Tyr Glu Gln
100 105 110
Asn Trp Leu Gly Gly Gly Trp Thr Asp Arg Ile Glu Gln Pro Gly Trp
115 120 125
Gly Trp Glu Lys Val Thr Arg Arg Gln His Ala Tyr Asp Phe Pro Met
130 135 140
Trp Phe Ile Arg Pro Asn Phe Lys Ser Glu Thr Ala Pro Arg Ser Ile
145 150 155 160
Gln Ser Pro Thr Gln Ala Ser Lys Lys Glu Thr Ala Lys Pro Gln Pro
165 170 175
Lys Ala Val Glu Leu Lys Ile Ile Lys Asp Val Val Lys Gly Tyr Asp
180 185 190
Leu Pro Lys Arg Gly Gly Asn Pro Lys Gly Ile Val Ile His Asn Asp
195 200 205
Ala Gly Ser Lys Gly Ala Thr Ala Glu Ala Tyr Arg Asn Gly Leu Val
210 215 220
Asn Ala Pro Leu Ser Arg Leu Glu Ala Gly Ile Ala His Ser Tyr Val
225 230 235 240
Ser Gly Asn Thr Val Trp Gln Ala Leu Asp Glu Ser Gln Val Gly Trp
245 250 255
His Thr Ala Asn Gln Leu Gly Asn Lys Tyr Tyr Tyr Gly Ile Glu Val
260 265 270
Cys Gln Ser Met Gly Ala Asp Asn Ala Thr Phe Leu Lys Asn Glu Gln
275 280 285
Ala Thr Phe Gln Glu Cys Ala Arg Leu Leu Lys Lys Trp Gly Leu Pro
290 295 300
Ala Asn Arg Asn Thr Ile Arg Leu His Asn Glu Phe Thr Ser Thr Ser
305 310 315 320
Cys Pro His Arg Ser Ser Val Leu His Thr Gly Phe Asp Pro Val Thr
325 330 335
Arg Gly Leu Leu Pro Glu Asp Lys Gln Leu Gln Leu Lys Asp Tyr Phe
340 345 350
Ile Lys Gln Ile Arg Val Tyr Met Asp Gly Lys Ile Pro Val Ala Thr
355 360 365
Val Ser Asn Glu Ser Ser Ala Ser Ser Asn Thr Val Lys Pro Val Ala
370 375 380
Ser Ala Trp Lys Arg Asn Lys Tyr Gly Thr Tyr Tyr Met Glu Glu Asn
385 390 395 400
Ala Arg Phe Thr Asn Gly Asn Gln Pro Ile Thr Val Arg Lys Ile Gly
405 410 415
Pro Phe Leu Ser Cys Pro Val Ala Tyr Gln Phe Gln Pro Gly Gly Tyr
420 425 430
Cys Asp Tyr Thr Glu Val Met Leu Gln Asp Gly His Val Trp Val Gly
435 440 445
Tyr Thr Trp Glu Gly Gln Arg Tyr Tyr Leu Pro Ile Arg Thr Trp Asn
450 455 460
Gly Ser Ala Pro Pro Asn Gln Ile Leu Gly Asp Leu Trp Gly Glu Ile
465 470 475 480
Ser
<210> 22
<211> 239
<212> БЕЛОК
<213> B30
<400> 22
Met Val Ile Asn Ile Glu Gln Ala Ile Ala Trp Met Ala Ser Arg Lys
1 5 10 15
Gly Lys Val Thr Tyr Ser Met Asp Tyr Arg Asn Gly Pro Ser Ser Tyr
20 25 30
Asp Cys Ser Ser Ser Val Tyr Phe Ala Leu Arg Ser Ala Gly Ala Ser
35 40 45
Asp Asn Gly Trp Ala Val Asn Thr Glu Tyr Glu His Asp Trp Leu Ile
50 55 60
Lys Asn Gly Tyr Val Leu Ile Ala Glu Asn Thr Asn Trp Asn Ala Gln
65 70 75 80
Arg Gly Asp Ile Phe Ile Trp Gly Lys Arg Gly Ala Ser Ala Gly Ala
85 90 95
Phe Gly His Thr Gly Met Phe Val Asp Pro Asp Asn Ile Ile His Cys
100 105 110
Asn Tyr Gly Tyr Asn Ser Ile Thr Val Asn Asn His Asp Glu Ile Trp
115 120 125
Gly Tyr Asn Gly Gln Pro Tyr Val Tyr Ala Tyr Arg Tyr Ser Gly Lys
130 135 140
Gln Ser Asn Ala Lys Val Asp Asn Lys Ser Val Val Ser Lys Phe Glu
145 150 155 160
Lys Glu Leu Asp Val Asn Thr Pro Leu Ser Asn Ser Asn Met Pro Tyr
165 170 175
Tyr Glu Ala Thr Ile Ser Glu Asp Tyr Tyr Val Glu Ser Lys Pro Asp
180 185 190
Val Asn Ser Thr Asp Lys Glu Leu Leu Val Ala Gly Thr Arg Val Arg
195 200 205
Val Tyr Glu Lys Val Lys Gly Trp Ala Arg Ile Gly Ala Pro Gln Ser
210 215 220
Asn Gln Trp Val Glu Asp Ala Tyr Leu Ile Asp Ala Thr Asp Met
225 230 235
<210> 23
<211> 495
<212> БЕЛОК
<213> K
<400> 23
Met Ala Lys Thr Gln Ala Glu Ile Asn Lys Arg Leu Asp Ala Tyr Ala
1 5 10 15
Lys Gly Thr Val Asp Ser Pro Tyr Arg Val Lys Lys Ala Thr Ser Tyr
20 25 30
Asp Pro Ser Phe Gly Val Met Glu Ala Gly Ala Ile Asp Ala Asp Gly
35 40 45
Tyr Tyr His Ala Gln Cys Gln Asp Leu Ile Thr Asp Tyr Val Leu Trp
50 55 60
Leu Thr Asp Asn Lys Val Arg Thr Trp Gly Asn Ala Lys Asp Gln Ile
65 70 75 80
Lys Gln Ser Tyr Gly Thr Gly Phe Lys Ile His Glu Asn Lys Pro Ser
85 90 95
Thr Val Pro Lys Lys Gly Trp Ile Ala Val Phe Thr Ser Gly Ser Tyr
100 105 110
Glu Gln Trp Gly His Ile Gly Ile Val Tyr Asp Gly Gly Asn Thr Ser
115 120 125
Thr Phe Thr Ile Leu Glu Gln Asn Trp Asn Gly Tyr Ala Asn Lys Lys
130 135 140
Pro Thr Lys Arg Val Asp Asn Tyr Tyr Gly Leu Thr His Phe Ile Glu
145 150 155 160
Ile Pro Val Lys Ala Gly Thr Thr Val Lys Lys Glu Thr Ala Lys Lys
165 170 175
Ser Ala Ser Lys Thr Pro Ala Pro Lys Lys Lys Ala Thr Leu Lys Val
180 185 190
Ser Lys Asn His Ile Asn Tyr Thr Met Asp Lys Arg Gly Lys Lys Pro
195 200 205
Glu Gly Met Val Ile His Asn Asp Ala Gly Arg Ser Ser Gly Gln Gln
210 215 220
Tyr Glu Asn Ser Leu Ala Asn Ala Gly Tyr Ala Arg Tyr Ala Asn Gly
225 230 235 240
Ile Ala His Tyr Tyr Gly Ser Glu Gly Tyr Val Trp Glu Ala Ile Asp
245 250 255
Ala Lys Asn Gln Ile Ala Trp His Thr Gly Asp Gly Thr Gly Ala Asn
260 265 270
Ser Gly Asn Phe Arg Phe Ala Gly Ile Glu Val Cys Gln Ser Met Ser
275 280 285
Ala Ser Asp Ala Gln Phe Leu Lys Asn Glu Gln Ala Val Phe Gln Phe
290 295 300
Thr Ala Glu Lys Phe Lys Glu Trp Gly Leu Thr Pro Asn Arg Lys Thr
305 310 315 320
Val Arg Leu His Met Glu Phe Val Pro Thr Ala Cys Pro His Arg Ser
325 330 335
Met Val Leu His Thr Gly Phe Asn Pro Val Thr Gln Gly Arg Pro Ser
340 345 350
Gln Ala Ile Met Asn Lys Leu Lys Asp Tyr Phe Ile Lys Gln Ile Lys
355 360 365
Asn Tyr Met Asp Lys Gly Thr Ser Ser Ser Thr Val Val Lys Asp Gly
370 375 380
Lys Thr Ser Ser Ala Ser Thr Pro Ala Thr Arg Pro Val Thr Gly Ser
385 390 395 400
Trp Lys Lys Asn Gln Tyr Gly Thr Trp Tyr Lys Pro Glu Asn Ala Thr
405 410 415
Phe Val Asn Gly Asn Gln Pro Ile Val Thr Arg Ile Gly Ser Pro Phe
420 425 430
Leu Asn Ala Pro Val Gly Gly Asn Leu Pro Ala Gly Ala Thr Ile Val
435 440 445
Tyr Asp Glu Val Cys Ile Gln Ala Gly His Ile Trp Ile Gly Tyr Asn
450 455 460
Ala Tyr Asn Gly Asn Arg Val Tyr Cys Pro Val Arg Thr Cys Gln Gly
465 470 475 480
Val Pro Pro Asn Gln Ile Pro Gly Val Ala Trp Gly Val Phe Lys
485 490 495
<210> 24
<211> 281
<212> БЕЛОК
<213> A118
<400> 24
Met Thr Ser Tyr Tyr Tyr Ser Arg Ser Leu Ala Asn Val Asn Lys Leu
1 5 10 15
Ala Asp Asn Thr Lys Ala Ala Ala Arg Lys Leu Leu Asp Trp Ser Glu
20 25 30
Ser Asn Gly Ile Glu Val Leu Ile Tyr Glu Thr Ile Arg Thr Lys Glu
35 40 45
Gln Gln Ala Ala Asn Val Asn Ser Gly Ala Ser Gln Thr Met Arg Ser
50 55 60
Tyr His Leu Val Gly Gln Ala Leu Asp Phe Val Met Ala Lys Gly Lys
65 70 75 80
Thr Val Asp Trp Gly Ala Tyr Arg Ser Asp Lys Gly Lys Lys Phe Val
85 90 95
Ala Lys Ala Lys Ser Leu Gly Phe Glu Trp Gly Gly Asp Trp Ser Gly
100 105 110
Phe Val Asp Asn Pro His Leu Gln Phe Asn Tyr Lys Gly Tyr Gly Thr
115 120 125
Asp Thr Phe Gly Lys Gly Ala Ser Thr Ser Asn Ser Ser Lys Pro Ser
130 135 140
Ala Asp Thr Asn Thr Asn Ser Leu Gly Leu Val Asp Tyr Met Asn Leu
145 150 155 160
Asn Lys Leu Asp Ser Ser Phe Ala Asn Arg Lys Lys Leu Ala Thr Ser
165 170 175
Tyr Gly Ile Lys Asn Tyr Ser Gly Thr Ala Thr Gln Asn Thr Thr Leu
180 185 190
Leu Ala Lys Leu Lys Ala Gly Lys Pro His Thr Pro Ala Ser Lys Asn
195 200 205
Thr Tyr Tyr Thr Glu Asn Pro Arg Lys Val Lys Thr Leu Val Gln Cys
210 215 220
Asp Leu Tyr Lys Ser Val Asp Phe Thr Thr Lys Asn Gln Thr Gly Gly
225 230 235 240
Thr Phe Pro Pro Gly Thr Val Phe Thr Ile Ser Gly Met Gly Lys Thr
245 250 255
Lys Gly Gly Thr Pro Arg Leu Lys Thr Lys Ser Gly Tyr Tyr Leu Thr
260 265 270
Ala Asn Thr Lys Phe Val Lys Lys Ile
275 280
<210> 25
<211> 341
<212> БЕЛОК
<213> A511
<400> 25
Met Val Lys Tyr Thr Val Glu Asn Lys Ile Ile Ala Gly Leu Pro Lys
1 5 10 15
Gly Lys Leu Lys Gly Ala Asn Phe Val Ile Ala His Glu Thr Ala Asn
20 25 30
Ser Lys Ser Thr Ile Asp Asn Glu Val Ser Tyr Met Thr Arg Asn Trp
35 40 45
Lys Asn Ala Phe Val Thr His Phe Val Gly Gly Gly Gly Arg Val Val
50 55 60
Gln Val Ala Asn Val Asn Tyr Val Ser Trp Gly Ala Gly Gln Tyr Ala
65 70 75 80
Asn Ser Tyr Ser Tyr Ala Gln Val Glu Leu Cys Arg Thr Ser Asn Ala
85 90 95
Thr Thr Phe Lys Lys Asp Tyr Glu Val Tyr Cys Gln Leu Leu Val Asp
100 105 110
Leu Ala Lys Lys Ala Gly Ile Pro Ile Thr Leu Asp Ser Gly Ser Lys
115 120 125
Thr Ser Asp Lys Gly Ile Lys Ser His Lys Trp Val Ala Asp Lys Leu
130 135 140
Gly Gly Thr Thr His Gln Asp Pro Tyr Ala Tyr Leu Ser Ser Trp Gly
145 150 155 160
Ile Ser Lys Ala Gln Phe Ala Ser Asp Leu Ala Lys Val Ser Gly Gly
165 170 175
Gly Asn Thr Gly Thr Ala Pro Ala Lys Pro Ser Thr Pro Ala Pro Lys
180 185 190
Pro Ser Thr Pro Ser Thr Asn Leu Asp Lys Leu Gly Leu Val Asp Tyr
195 200 205
Met Asn Ala Lys Lys Met Asp Ser Ser Tyr Ser Asn Arg Asp Lys Leu
210 215 220
Ala Lys Gln Tyr Gly Ile Ala Asn Tyr Ser Gly Thr Ala Ser Gln Asn
225 230 235 240
Thr Thr Leu Leu Ser Lys Ile Lys Gly Gly Ala Pro Lys Pro Ser Thr
245 250 255
Pro Ala Pro Lys Pro Ser Thr Ser Thr Ala Lys Lys Ile Tyr Phe Pro
260 265 270
Pro Asn Lys Gly Asn Trp Ser Val Tyr Pro Thr Asn Lys Ala Pro Val
275 280 285
Lys Ala Asn Ala Ile Gly Ala Ile Asn Pro Thr Lys Phe Gly Gly Leu
290 295 300
Thr Tyr Thr Ile Gln Lys Asp Arg Gly Asn Gly Val Tyr Glu Ile Gln
305 310 315 320
Thr Asp Gln Phe Gly Arg Val Gln Val Tyr Gly Ala Pro Ser Thr Gly
325 330 335
Ala Val Ile Lys Lys
340
<210> 26
<211> 289
<212> БЕЛОК
<213> A500
<400> 26
Met Ala Leu Thr Glu Ala Trp Leu Ile Glu Lys Ala Asn Arg Lys Leu
1 5 10 15
Asn Ala Gly Gly Met Tyr Lys Ile Thr Ser Asp Lys Thr Arg Asn Val
20 25 30
Ile Lys Lys Met Ala Lys Glu Gly Ile Tyr Leu Cys Val Ala Gln Gly
35 40 45
Tyr Arg Ser Thr Ala Glu Gln Asn Ala Leu Tyr Ala Gln Gly Arg Thr
50 55 60
Lys Pro Gly Ala Ile Val Thr Asn Ala Lys Gly Gly Gln Ser Asn His
65 70 75 80
Asn Tyr Gly Val Ala Val Asp Leu Cys Leu Tyr Thr Asn Asp Gly Lys
85 90 95
Asp Val Ile Trp Glu Ser Thr Thr Ser Arg Trp Lys Lys Val Val Ala
100 105 110
Ala Met Lys Ala Glu Gly Phe Lys Trp Gly Gly Asp Trp Lys Ser Phe
115 120 125
Lys Asp Tyr Pro His Phe Glu Leu Cys Asp Ala Val Ser Gly Glu Lys
130 135 140
Ile Pro Ala Ala Thr Gln Asn Thr Asn Thr Asn Ser Asn Arg Tyr Glu
145 150 155 160
Gly Lys Val Ile Asp Ser Ala Pro Leu Leu Pro Lys Met Asp Phe Lys
165 170 175
Ser Ser Pro Phe Arg Met Tyr Lys Val Gly Thr Glu Phe Leu Val Tyr
180 185 190
Asp His Asn Gln Tyr Trp Tyr Lys Thr Tyr Ile Asp Asp Lys Leu Tyr
195 200 205
Tyr Met Tyr Lys Ser Phe Cys Asp Val Val Ala Lys Lys Asp Ala Lys
210 215 220
Gly Arg Ile Lys Val Arg Ile Lys Ser Ala Lys Asp Leu Arg Ile Pro
225 230 235 240
Val Trp Asn Asn Ile Lys Leu Asn Ser Gly Lys Ile Lys Trp Tyr Ala
245 250 255
Pro Asn Val Lys Leu Ala Trp Tyr Asn Tyr Arg Arg Gly Tyr Leu Glu
260 265 270
Leu Trp Tyr Pro Asn Asp Gly Trp Tyr Tyr Thr Ala Glu Tyr Phe Leu
275 280 285
Lys
<210> 27
<211> 239
<212> БЕЛОК
<213> Профаг LambdaSa1
<400> 27
Met Val Ile Asn Ile Glu Gln Ala Ile Ala Trp Met Ala Ser Arg Lys
1 5 10 15
Gly Lys Val Thr Tyr Ser Met Asp Tyr Arg Asn Gly Pro Ser Ser Tyr
20 25 30
Asp Cys Ser Ser Ser Val Tyr Phe Ala Leu Arg Ser Ala Gly Ala Ser
35 40 45
Asp Asn Gly Trp Ala Val Asn Thr Glu Tyr Glu His Asp Trp Leu Ile
50 55 60
Lys Asn Gly Tyr Val Leu Ile Ala Glu Asn Thr Asn Trp Asn Ala Gln
65 70 75 80
Arg Gly Asp Ile Phe Ile Trp Gly Lys Arg Gly Ala Ser Ala Gly Ala
85 90 95
Phe Gly His Thr Gly Met Phe Val Asp Pro Asp Asn Ile Ile His Cys
100 105 110
Asn Tyr Gly Tyr Asn Ser Ile Thr Val Asn Asn His Asp Glu Ile Trp
115 120 125
Gly Tyr Asn Gly Gln Pro Tyr Val Tyr Ala Tyr Arg Tyr Ala Arg Lys
130 135 140
Gln Ser Asn Ala Lys Val Asp Asn Gln Ser Val Val Ser Lys Phe Glu
145 150 155 160
Lys Glu Leu Asp Val Asn Thr Pro Leu Ser Asn Ser Asn Met Pro Tyr
165 170 175
Tyr Glu Ala Thr Ile Ser Glu Asp Tyr Tyr Val Glu Ser Lys Pro Asp
180 185 190
Val Asn Ser Thr Asp Lys Glu Leu Leu Val Ala Gly Thr Arg Val Arg
195 200 205
Val Tyr Glu Lys Val Lys Gly Trp Ala Arg Ile Gly Ala Pro Gln Ser
210 215 220
Asn Gln Trp Val Glu Asp Ala Tyr Leu Ile Asp Ala Thr Asp Met
225 230 235
<210> 28
<211> 468
<212> БЕЛОК
<213> Профаг LambdaSa2
<400> 28
Met Glu Ile Asn Thr Glu Ile Ala Ile Ala Trp Met Ser Ala Arg Gln
1 5 10 15
Gly Lys Val Ser Tyr Ser Met Asp Tyr Arg Asp Gly Pro Asn Ser Tyr
20 25 30
Asp Cys Ser Ser Ser Val Tyr Tyr Ala Leu Arg Ser Ala Gly Ala Ser
35 40 45
Ser Ala Gly Trp Ala Val Asn Thr Glu Tyr Met His Asp Trp Leu Ile
50 55 60
Lys Asn Gly Tyr Glu Leu Ile Ala Glu Asn Val Asp Trp Asn Ala Val
65 70 75 80
Arg Gly Asp Ile Ala Ile Trp Gly Met Arg Gly His Ser Ser Gly Ala
85 90 95
Gly Gly His Val Val Met Phe Ile Asp Pro Glu Asn Ile Ile His Cys
100 105 110
Asn Trp Ala Asn Asn Gly Ile Thr Val Asn Asn Tyr Asn Gln Thr Ala
115 120 125
Ala Ala Ser Gly Trp Met Tyr Cys Tyr Val Tyr Arg Leu Lys Ser Gly
130 135 140
Ala Ser Thr Gln Gly Lys Ser Leu Asp Thr Leu Val Lys Glu Thr Leu
145 150 155 160
Ala Gly Asn Tyr Gly Asn Gly Glu Ala Arg Lys Ala Val Leu Gly Asn
165 170 175
Gln Tyr Glu Ala Val Met Ser Val Ile Asn Gly Lys Thr Thr Thr Asn
180 185 190
Gln Lys Thr Val Asp Gln Leu Val Gln Glu Val Ile Ala Gly Lys His
195 200 205
Gly Asn Gly Glu Ala Arg Lys Lys Ser Leu Gly Ser Gln Tyr Asp Ala
210 215 220
Val Gln Lys Arg Val Thr Glu Leu Leu Lys Lys Gln Pro Ser Glu Pro
225 230 235 240
Phe Lys Ala Gln Glu Val Asn Lys Pro Thr Glu Thr Lys Thr Ser Gln
245 250 255
Thr Glu Leu Thr Gly Gln Ala Thr Ala Thr Lys Glu Glu Gly Asp Leu
260 265 270
Ser Phe Asn Gly Thr Ile Leu Lys Lys Ala Val Leu Asp Lys Ile Leu
275 280 285
Gly Asn Cys Lys Lys His Asp Ile Leu Pro Ser Tyr Ala Leu Thr Ile
290 295 300
Leu His Tyr Glu Gly Leu Trp Gly Thr Ser Ala Val Gly Lys Ala Asp
305 310 315 320
Asn Asn Trp Gly Gly Met Thr Trp Thr Gly Gln Gly Asn Arg Pro Ser
325 330 335
Gly Val Thr Val Thr Gln Gly Ser Ala Arg Pro Ser Asn Glu Gly Gly
340 345 350
His Tyr Met His Tyr Ala Ser Val Asp Asp Phe Leu Thr Asp Trp Phe
355 360 365
Tyr Leu Leu Arg Ala Gly Gly Ser Tyr Lys Val Ser Gly Ala Lys Thr
370 375 380
Phe Ser Glu Ala Ile Lys Gly Met Phe Lys Val Gly Gly Ala Val Tyr
385 390 395 400
Asp Tyr Ala Ala Ser Gly Phe Asp Ser Tyr Ile Val Gly Ala Ser Ser
405 410 415
Arg Leu Lys Ala Ile Glu Ala Glu Asn Gly Ser Leu Asp Lys Phe Asp
420 425 430
Lys Ala Thr Asp Ile Gly Asp Gly Ser Lys Asp Lys Ile Asp Ile Thr
435 440 445
Ile Glu Gly Ile Glu Val Thr Ile Asn Gly Ile Thr Tyr Glu Leu Thr
450 455 460
Lys Lys Pro Val
465
<210> 29
<211> 236
<212> БЕЛОК
<213> Профаг (ATCC700407)
<400> 29
Met Thr Asp Ser Ile Gln Glu Met Arg Lys Leu Gln Ser Ile Pro Val
1 5 10 15
Arg Tyr Asp Met Gly Asp Arg Tyr Gly Asn Asp Ala Asp Arg Asp Gly
20 25 30
Arg Ile Glu Met Asp Cys Ser Ser Ala Val Ser Lys Ala Leu Gly Ile
35 40 45
Ser Met Thr Asn Asn Thr Glu Thr Leu Gln Gln Ala Leu Pro Ala Ile
50 55 60
Gly Tyr Gly Lys Ile His Asp Ala Val Asp Gly Thr Phe Asp Met Gln
65 70 75 80
Ala Tyr Asp Val Ile Ile Trp Ala Pro Arg Asp Gly Ser Ser Ser Leu
85 90 95
Gly Ala Phe Gly His Val Leu Ile Ala Thr Ser Pro Thr Thr Ala Ile
100 105 110
His Cys Asn Tyr Gly Ser Asp Gly Ile Thr Glu Asn Asp Tyr Asn Tyr
115 120 125
Ile Trp Glu Ile Asn Gly Arg Pro Arg Glu Ile Val Phe Arg Lys Gly
130 135 140
Val Thr Gln Thr Gln Ala Thr Val Thr Ser Gln Phe Glu Arg Glu Leu
145 150 155 160
Asp Val Asn Ala Arg Leu Thr Val Ser Asp Lys Pro Tyr Tyr Glu Ala
165 170 175
Thr Leu Ser Glu Asp Tyr Tyr Val Glu Ala Gly Pro Arg Ile Asp Ser
180 185 190
Gln Asp Lys Glu Leu Ile Lys Ala Gly Thr Arg Val Arg Val Tyr Glu
195 200 205
Lys Leu Asn Gly Trp Ser Arg Ile Asn His Pro Glu Ser Ala Gln Trp
210 215 220
Val Glu Asp Ser Tyr Leu Val Asp Ala Thr Glu Met
225 230 235
<210> 30
<211> 481
<212> БЕЛОК
<213> Phi11 и Phi12
<400> 30
Met Gln Ala Lys Leu Thr Lys Asn Glu Phe Ile Glu Trp Leu Lys Thr
1 5 10 15
Ser Glu Gly Lys Gln Phe Asn Val Asp Leu Trp Tyr Gly Phe Gln Cys
20 25 30
Phe Asp Tyr Ala Asn Ala Gly Trp Lys Val Leu Phe Gly Leu Leu Leu
35 40 45
Lys Gly Leu Gly Ala Lys Asp Ile Pro Phe Ala Asn Asn Phe Asp Gly
50 55 60
Leu Ala Thr Val Tyr Gln Asn Thr Pro Asp Phe Leu Ala Gln Pro Gly
65 70 75 80
Asp Met Val Val Phe Gly Ser Asn Tyr Gly Ala Gly Tyr Gly His Val
85 90 95
Ala Trp Val Ile Glu Ala Thr Leu Asp Tyr Ile Ile Val Tyr Glu Gln
100 105 110
Asn Trp Leu Gly Gly Gly Trp Thr Asp Gly Ile Glu Gln Pro Gly Trp
115 120 125
Gly Trp Glu Lys Val Thr Arg Arg Gln His Ala Tyr Asp Phe Pro Met
130 135 140
Trp Phe Ile Arg Pro Asn Phe Lys Ser Glu Thr Ala Pro Arg Ser Val
145 150 155 160
Gln Ser Pro Thr Gln Ala Pro Lys Lys Glu Thr Ala Lys Pro Gln Pro
165 170 175
Lys Ala Val Glu Leu Lys Ile Ile Lys Asp Val Val Lys Gly Tyr Asp
180 185 190
Leu Pro Lys Arg Gly Ser Asn Pro Lys Gly Ile Val Ile His Asn Asp
195 200 205
Ala Gly Ser Lys Gly Ala Thr Ala Glu Ala Tyr Arg Asn Gly Leu Val
210 215 220
Asn Ala Pro Leu Ser Arg Leu Glu Ala Gly Ile Ala His Ser Tyr Val
225 230 235 240
Ser Gly Asn Thr Val Trp Gln Ala Leu Asp Glu Ser Gln Val Gly Trp
245 250 255
His Thr Ala Asn Gln Ile Gly Asn Lys Tyr Tyr Tyr Gly Ile Glu Val
260 265 270
Cys Gln Ser Met Gly Ala Asp Asn Ala Thr Phe Leu Lys Asn Glu Gln
275 280 285
Ala Thr Phe Gln Glu Cys Ala Arg Leu Leu Lys Lys Trp Gly Leu Pro
290 295 300
Ala Asn Arg Asn Thr Ile Arg Leu His Asn Glu Phe Thr Ser Thr Ser
305 310 315 320
Cys Pro His Arg Ser Ser Val Leu His Thr Gly Phe Asp Pro Val Thr
325 330 335
Arg Gly Leu Leu Pro Glu Asp Lys Arg Leu Gln Leu Lys Asp Tyr Phe
340 345 350
Ile Lys Gln Ile Arg Ala Tyr Met Asp Gly Lys Ile Pro Val Ala Thr
355 360 365
Val Ser Asn Glu Ser Ser Ala Ser Ser Asn Thr Val Lys Pro Val Ala
370 375 380
Ser Ala Trp Lys Arg Asn Lys Tyr Gly Thr Tyr Tyr Met Glu Glu Ser
385 390 395 400
Ala Arg Phe Thr Asn Gly Asn Gln Pro Ile Thr Val Arg Lys Val Gly
405 410 415
Pro Phe Leu Ser Cys Pro Val Gly Tyr Gln Phe Gln Pro Gly Gly Tyr
420 425 430
Cys Asp Tyr Thr Glu Val Met Leu Gln Asp Gly His Val Trp Val Gly
435 440 445
Tyr Thr Trp Glu Gly Gln Arg Tyr Tyr Leu Pro Ile Arg Thr Trp Asn
450 455 460
Gly Ser Ala Pro Pro Asn Gln Ile Leu Gly Asp Leu Trp Gly Glu Ile
465 470 475 480
Ser
<210> 31
<211> 481
<212> БЕЛОК
<213> (Phi)H5
<400> 31
Met Gln Ala Lys Leu Thr Lys Lys Glu Phe Ile Glu Trp Leu Lys Thr
1 5 10 15
Ser Glu Gly Lys Gln Tyr Asn Ala Asp Gly Trp Tyr Gly Phe Gln Cys
20 25 30
Phe Asp Tyr Ala Asn Ala Gly Trp Lys Ala Leu Phe Gly Leu Leu Leu
35 40 45
Lys Gly Val Gly Ala Lys Asp Ile Pro Phe Ala Asn Asn Phe Asp Gly
50 55 60
Leu Ala Thr Val Tyr Gln Asn Thr Pro Asp Phe Leu Ala Gln Pro Gly
65 70 75 80
Asp Met Val Val Phe Gly Ser Asn Tyr Gly Ala Gly Tyr Gly His Val
85 90 95
Ala Trp Val Ile Glu Ala Thr Leu Asp Tyr Ile Ile Val Tyr Glu Gln
100 105 110
Asn Trp Leu Gly Gly Gly Trp Thr Asp Gly Val Gln Gln Pro Gly Ser
115 120 125
Gly Trp Glu Lys Val Thr Arg Arg Gln His Ala Tyr Asp Phe Pro Met
130 135 140
Trp Phe Ile Arg Pro Asn Phe Lys Ser Glu Thr Ala Pro Arg Ser Val
145 150 155 160
Gln Ser Pro Thr Gln Ala Ser Lys Lys Glu Thr Ala Lys Pro Gln Pro
165 170 175
Lys Ala Val Glu Leu Lys Ile Ile Lys Asp Val Val Lys Gly Tyr Asp
180 185 190
Leu Pro Lys Arg Gly Ser Asn Pro Asn Phe Ile Val Ile His Asn Asp
195 200 205
Ala Gly Ser Lys Gly Ala Thr Ala Glu Ala Tyr Arg Asn Gly Leu Val
210 215 220
Asn Ala Pro Leu Ser Arg Leu Glu Ala Gly Ile Ala His Ser Tyr Val
225 230 235 240
Ser Gly Asn Thr Val Trp Gln Ala Leu Asp Glu Ser Gln Val Gly Trp
245 250 255
His Thr Ala Asn Gln Ile Gly Asn Lys Tyr Gly Tyr Gly Ile Glu Val
260 265 270
Cys Gln Ser Met Gly Ala Asp Asn Ala Thr Phe Leu Lys Asn Glu Gln
275 280 285
Ala Thr Phe Gln Glu Cys Ala Arg Leu Leu Lys Lys Trp Gly Leu Pro
290 295 300
Ala Asn Arg Asn Thr Ile Arg Leu His Asn Glu Phe Thr Ser Thr Ser
305 310 315 320
Cys Pro His Arg Ser Ser Val Leu His Thr Gly Phe Asp Pro Val Thr
325 330 335
Arg Gly Leu Leu Pro Glu Asp Lys Arg Leu Gln Leu Lys Asp Tyr Phe
340 345 350
Ile Lys Gln Ile Arg Ala Tyr Met Asp Gly Lys Ile Pro Val Ala Thr
355 360 365
Val Ser Asn Asp Ser Ser Ala Ser Ser Asn Thr Val Lys Pro Val Ala
370 375 380
Ser Ala Trp Lys Arg Asn Lys Tyr Gly Thr Tyr Tyr Met Glu Glu Ser
385 390 395 400
Ala Arg Phe Thr Asn Gly Asn Gln Pro Ile Thr Val Arg Lys Val Gly
405 410 415
Pro Phe Leu Ser Cys Pro Val Gly Tyr Gln Phe Gln Pro Gly Gly Tyr
420 425 430
Cys Asp Tyr Thr Glu Val Met Leu Gln Asp Gly His Val Trp Val Gly
435 440 445
Tyr Thr Trp Glu Gly Gln Arg Tyr Tyr Leu Pro Ile Arg Thr Trp Asn
450 455 460
Gly Ser Ala Pro Pro Asn Gln Ile Leu Gly Asp Leu Trp Gly Glu Ile
465 470 475 480
Ser
<210> 32
<211> 477
<212> БЕЛОК
<213> (Phi)WMY
<400> 32
Met Lys Thr Lys Ala Gln Ala Lys Ser Trp Ile Asn Ser Lys Ile Gly
1 5 10 15
Lys Gly Ile Asp Trp Asp Gly Met Tyr Gly Tyr Gln Cys Met Asp Glu
20 25 30
Ala Val Asp Tyr Ile His His Val Thr Asp Gly Lys Val Thr Met Trp
35 40 45
Gly Asn Ala Ile Asp Ala Pro Lys Asn Asn Phe Gln Gly Leu Cys Thr
50 55 60
Val Tyr Thr Asn Thr Pro Glu Phe Arg Pro Ala Tyr Gly Asp Val Ile
65 70 75 80
Val Trp Ser Tyr Gly Thr Phe Ala Thr Tyr Gly His Ile Ala Ile Val
85 90 95
Val Asn Pro Asp Pro Tyr Gly Asp Leu Gln Tyr Ile Thr Val Leu Glu
100 105 110
Gln Asn Trp Asn Gly Asn Gly Ile Tyr Lys Thr Glu Phe Ala Thr Ile
115 120 125
Arg Thr His Asp Tyr Thr Gly Val Ser His Phe Ile Arg Pro Lys Phe
130 135 140
Ala Asp Glu Val Lys Glu Thr Ala Lys Thr Val Asn Lys Leu Ser Val
145 150 155 160
Gln Lys Lys Ile Val Thr Pro Lys Asn Ser Val Glu Arg Ile Lys Asn
165 170 175
Tyr Val Lys Thr Ser Gly Tyr Ile Asn Gly Glu His Tyr Glu Leu Tyr
180 185 190
Asn Arg Gly His Lys Pro Lys Gly Val Val Ile His Asn Thr Ala Gly
195 200 205
Thr Ala Ser Ala Thr Gln Glu Gly Gln Arg Leu Thr Asn Met Thr Phe
210 215 220
Gln Gln Leu Ala Asn Gly Val Ala His Val Tyr Ile Asp Lys Asn Thr
225 230 235 240
Ile Tyr Glu Thr Leu Pro Glu Asp Arg Ile Ala Trp His Val Ala Gln
245 250 255
Gln Tyr Gly Asn Thr Glu Phe Tyr Gly Ile Glu Val Cys Gly Ser Arg
260 265 270
Asn Thr Asp Lys Glu Gln Phe Leu Ala Asn Glu Gln Val Ala Phe Gln
275 280 285
Glu Ala Ala Arg Arg Leu Lys Ser Trp Gly Met Arg Ala Asn Arg Asn
290 295 300
Thr Val Arg Leu His His Thr Phe Ser Ser Thr Glu Cys Pro Asp Met
305 310 315 320
Ser Met Leu Leu His Thr Gly Tyr Ser Met Lys Asn Gly Lys Pro Thr
325 330 335
Gln Asp Ile Thr Asn Lys Cys Ala Asp Tyr Phe Met Lys Gln Ile Asn
340 345 350
Ala Tyr Ile Asp Gly Lys Gln Pro Thr Ser Thr Val Val Gly Ser Ser
355 360 365
Ser Ser Asn Lys Leu Lys Ala Lys Asn Lys Asp Lys Ser Thr Gly Trp
370 375 380
Asn Thr Asn Glu Tyr Gly Thr Leu Trp Lys Lys Glu His Ala Thr Phe
385 390 395 400
Thr Cys Gly Val Arg Gln Gly Ile Val Thr Arg Thr Thr Gly Pro Phe
405 410 415
Thr Ser Cys Pro Gln Ala Gly Val Leu Tyr Tyr Gly Gln Ser Val Asn
420 425 430
Tyr Asp Thr Val Cys Lys Gln Asp Gly Tyr Val Trp Ile Ser Trp Thr
435 440 445
Thr Ser Asp Gly Tyr Asp Val Trp Met Pro Ile Arg Thr Trp Asp Arg
450 455 460
Ser Thr Asp Lys Val Ser Glu Ile Trp Gly Thr Ile Ser
465 470 475
<210> 33
<211> 443
<212> БЕЛОК
<213> (Phi)NCTC 11261
<400> 33
Met Ala Thr Tyr Gln Glu Tyr Lys Ser Arg Ser Asn Gly Asn Ala Tyr
1 5 10 15
Asp Ile Asp Gly Ser Phe Gly Ala Gln Cys Trp Asp Gly Tyr Ala Asp
20 25 30
Tyr Cys Lys Tyr Leu Gly Leu Pro Tyr Ala Asn Cys Thr Asn Thr Gly
35 40 45
Tyr Ala Arg Asp Ile Trp Glu Gln Arg His Glu Asn Gly Ile Leu Asn
50 55 60
Tyr Phe Asp Glu Val Glu Val Met Gln Ala Gly Asp Val Ala Ile Phe
65 70 75 80
Met Val Val Asp Gly Val Thr Pro Tyr Ser His Val Ala Ile Phe Asp
85 90 95
Ser Asp Ala Gly Gly Gly Tyr Gly Trp Phe Leu Gly Gln Asn Gln Gly
100 105 110
Gly Ala Asn Gly Ala Tyr Asn Ile Val Lys Ile Pro Tyr Ser Ala Thr
115 120 125
Tyr Pro Thr Ala Phe Arg Pro Lys Val Phe Lys Asn Ala Val Thr Val
130 135 140
Thr Gly Asn Ile Gly Leu Asn Lys Gly Asp Tyr Phe Ile Asp Val Ser
145 150 155 160
Ala Tyr Gln Gln Ala Asp Leu Thr Thr Thr Cys Gln Gln Ala Gly Thr
165 170 175
Thr Lys Thr Ile Ile Lys Val Ser Glu Ser Ile Ala Trp Leu Ser Asp
180 185 190
Arg His Gln Gln Gln Ala Asn Thr Ser Asp Pro Ile Gly Tyr Tyr His
195 200 205
Phe Gly Arg Phe Gly Gly Asp Ser Ala Leu Ala Gln Arg Glu Ala Asp
210 215 220
Leu Phe Leu Ser Asn Leu Pro Ser Lys Lys Val Ser Tyr Leu Val Ile
225 230 235 240
Asp Tyr Glu Asp Ser Ala Ser Ala Asp Lys Gln Ala Asn Thr Asn Ala
245 250 255
Val Ile Ala Phe Met Asp Lys Ile Ala Ser Ala Gly Tyr Lys Pro Ile
260 265 270
Tyr Tyr Ser Tyr Lys Pro Phe Thr Leu Asn Asn Ile Asp Tyr Gln Lys
275 280 285
Ile Ile Ala Lys Tyr Pro Asn Ser Ile Trp Ile Ala Gly Tyr Pro Asp
290 295 300
Tyr Glu Val Arg Thr Glu Pro Leu Trp Glu Phe Phe Pro Ser Met Asp
305 310 315 320
Gly Val Arg Trp Trp Gln Phe Thr Ser Val Gly Val Ala Gly Gly Leu
325 330 335
Asp Lys Asn Ile Val Leu Leu Ala Asp Asp Ser Ser Lys Met Asp Ile
340 345 350
Pro Lys Val Asp Lys Pro Gln Glu Leu Thr Phe Tyr Gln Lys Leu Ala
355 360 365
Thr Asn Thr Lys Leu Asp Asn Ser Asn Val Pro Tyr Tyr Glu Ala Thr
370 375 380
Leu Ser Thr Asp Tyr Tyr Val Glu Ser Lys Pro Asn Ala Ser Ser Ala
385 390 395 400
Asp Lys Glu Phe Ile Lys Ala Gly Thr Arg Val Arg Val Tyr Glu Lys
405 410 415
Val Asn Gly Trp Ser Arg Ile Asn His Pro Glu Ser Ala Gln Trp Val
420 425 430
Glu Asp Ser Tyr Leu Val Asn Ala Thr Asp Met
435 440
<210> 34
<211> 334
<212> БЕЛОК
<213> (Phi)FWLLm3
<400> 34
Met Val Lys Tyr Thr Val Glu Asn Lys Ile Ile Ala Gly Leu Pro Lys
1 5 10 15
Gly Lys Leu Lys Gly Ala Asn Phe Val Ile Ala His Glu Thr Ala Asn
20 25 30
Ser Lys Ser Thr Ile Asp Asn Glu Val Ser Tyr Met Thr Arg Asn Trp
35 40 45
Gln Asn Ala Phe Val Thr His Phe Val Gly Gly Gly Gly Arg Val Val
50 55 60
Gln Val Ala Asn Val Asn Tyr Val Ser Trp Gly Ala Gly Gln Tyr Ala
65 70 75 80
Asn Ser Tyr Ser Tyr Ala Gln Val Glu Leu Cys Arg Thr Ser Asn Ala
85 90 95
Thr Thr Phe Lys Lys Asp Tyr Glu Val Tyr Cys Gln Leu Leu Val Asp
100 105 110
Leu Ala Lys Lys Ala Gly Ile Pro Ile Thr Leu Asp Ser Gly Ser Lys
115 120 125
Thr Ser Asp Lys Gly Ile Lys Ser His Lys Trp Val Ala Asp Lys Leu
130 135 140
Gly Gly Thr Thr His Gln Asp Pro Tyr Ala Tyr Leu Ser Ser Trp Gly
145 150 155 160
Ile Ser Lys Ala Gln Phe Ala Ser Asp Leu Ala Lys Val Ser Gly Gly
165 170 175
Gly Asn Thr Gly Thr Ala Pro Ala Lys Pro Ser Thr Pro Ser Thr Asn
180 185 190
Leu Asp Lys Leu Gly Leu Val Asp Tyr Met Asn Ala Lys Lys Met Asp
195 200 205
Ser Ser Tyr Ser Asn Arg Ala Lys Leu Ala Lys Gln Tyr Gly Ile Ala
210 215 220
Asn Tyr Ser Gly Thr Ala Ser Gln Asn Thr Thr Leu Leu Ser Lys Ile
225 230 235 240
Lys Gly Gly Ala Pro Lys Pro Ser Thr Pro Ala Pro Lys Pro Ser Thr
245 250 255
Ser Thr Ala Lys Lys Ile Tyr Phe Pro Pro Asn Lys Gly Asn Trp Ser
260 265 270
Val Tyr Pro Thr Asn Lys Ala Pro Val Lys Ala Asn Ala Ile Gly Ala
275 280 285
Ile Asn Pro Thr Lys Phe Gly Gly Leu Thr Tyr Thr Ile Gln Lys Asp
290 295 300
Arg Gly Asn Gly Val Tyr Glu Ile Gln Thr Asp Gln Phe Gly Arg Val
305 310 315 320
Gln Val Tyr Gly Ala Pro Ser Thr Gly Ala Val Ile Lys Lys
325 330
<210> 35
<211> 1278
<212> БЕЛОК
<213> (Phi)BPS13
<400> 35
Met Ala Lys Arg Glu Lys Tyr Ile Phe Asp Val Glu Ala Glu Val Gly
1 5 10 15
Lys Ala Ala Lys Ser Ile Lys Ser Leu Glu Ala Glu Leu Ser Lys Leu
20 25 30
Gln Lys Leu Asn Lys Glu Ile Asp Ala Thr Gly Gly Asp Arg Thr Glu
35 40 45
Lys Glu Met Leu Ala Thr Leu Lys Ala Ala Lys Glu Val Asn Ala Glu
50 55 60
Tyr Gln Lys Met Gln Arg Ile Leu Lys Asp Leu Ser Lys Tyr Ser Gly
65 70 75 80
Lys Val Ser Arg Lys Glu Phe Asn Asp Ser Lys Val Ile Asn Asn Ala
85 90 95
Lys Thr Ser Val Gln Gly Gly Lys Val Thr Asp Ser Phe Gly Gln Met
100 105 110
Leu Lys Asn Met Glu Arg Gln Ile Asn Ser Val Asn Lys Gln Phe Asp
115 120 125
Asn His Arg Lys Ala Met Val Asp Arg Gly Gln Gln Tyr Thr Pro His
130 135 140
Leu Lys Thr Asn Arg Lys Asp Ser Gln Gly Asn Ser Asn Pro Ser Met
145 150 155 160
Met Gly Arg Asn Lys Ser Thr Thr Gln Asp Met Glu Lys Ala Val Asp
165 170 175
Lys Phe Leu Asn Gly Gln Asn Glu Ala Thr Thr Gly Leu Asn Gln Ala
180 185 190
Leu Tyr Gln Leu Lys Glu Ile Ser Lys Leu Asn Arg Arg Ser Glu Ser
195 200 205
Leu Ser Arg Arg Ala Ser Ala Ser Gly Tyr Met Ser Phe Gln Gln Tyr
210 215 220
Ser Asn Phe Thr Gly Asp Arg Arg Thr Val Gln Gln Thr Tyr Gly Gly
225 230 235 240
Leu Lys Thr Ala Asn Arg Glu Arg Val Leu Glu Leu Ser Gly Gln Ala
245 250 255
Thr Gly Ile Ser Lys Glu Leu Asp Arg Leu Asn Ser Lys Lys Gly Leu
260 265 270
Thr Ala Arg Glu Gly Glu Glu Arg Lys Lys Leu Met Arg Gln Leu Glu
275 280 285
Gly Ile Asp Ala Glu Leu Thr Ala Arg Lys Lys Leu Asn Ser Ser Leu
290 295 300
Asp Glu Thr Thr Ser Asn Met Glu Lys Phe Asn Gln Ser Leu Val Asp
305 310 315 320
Ala Gln Val Ser Val Lys Pro Glu Arg Gly Thr Met Arg Gly Met Met
325 330 335
Tyr Glu Arg Ala Pro Ala Ile Ala Leu Ala Ile Gly Gly Ala Ile Thr
340 345 350
Ala Thr Ile Gly Lys Leu Tyr Ser Glu Gly Gly Asn His Ser Lys Ala
355 360 365
Met Arg Pro Asp Glu Met Tyr Val Gly Gln Gln Thr Gly Ala Val Gly
370 375 380
Ala Asn Trp Arg Pro Asn Arg Thr Ala Thr Met Arg Ser Gly Leu Gly
385 390 395 400
Asn His Leu Gly Phe Thr Gly Gln Glu Met Met Glu Phe Gln Ser Asn
405 410 415
Tyr Leu Ser Ala Asn Gly Tyr His Gly Ala Glu Asp Met Lys Ala Ala
420 425 430
Thr Thr Gly Gln Ala Thr Phe Ala Arg Ala Thr Gly Leu Gly Ser Asp
435 440 445
Glu Val Lys Asp Phe Phe Asn Thr Ala Tyr Arg Ser Gly Gly Ile Asp
450 455 460
Gly Asn Gln Thr Lys Gln Phe Gln Asn Ala Phe Leu Gly Ala Met Lys
465 470 475 480
Gln Ser Gly Ala Val Gly Arg Glu Lys Asp Gln Leu Lys Ala Leu Asn
485 490 495
Gly Ile Leu Ser Ser Met Ser Gln Asn Arg Thr Val Ser Asn Gln Asp
500 505 510
Met Met Arg Thr Val Gly Leu Gln Ser Ala Ile Ser Ser Ser Gly Val
515 520 525
Ala Ser Leu Gln Gly Thr Lys Gly Gly Ala Leu Met Glu Gln Leu Asp
530 535 540
Asn Gly Ile Arg Glu Gly Phe Asn Asp Pro Gln Met Arg Val Leu Phe
545 550 555 560
Gly Gln Gly Thr Lys Tyr Gln Gly Met Gly Gly Arg Ala Ala Leu Arg
565 570 575
Lys Gln Met Glu Lys Gly Ile Ser Asp Pro Asp Asn Leu Asn Thr Leu
580 585 590
Ile Asp Ala Ser Lys Ala Ser Ala Gly Gln Asp Pro Ala Glu Gln Ala
595 600 605
Glu Val Leu Ala Thr Leu Ala Ser Lys Met Gly Val Asn Met Ser Ser
610 615 620
Asp Gln Ala Arg Gly Leu Ile Asp Leu Gln Pro Ser Gly Lys Leu Thr
625 630 635 640
Lys Glu Asn Ile Asp Lys Val Met Lys Glu Gly Leu Lys Glu Gly Ser
645 650 655
Ile Glu Ser Ala Lys Arg Asp Lys Ala Tyr Ser Glu Ser Lys Ala Ser
660 665 670
Ile Asp Asn Ser Ser Glu Ala Ala Thr Ala Lys Gln Ala Thr Glu Leu
675 680 685
Asn Asp Met Gly Ser Lys Leu Arg Gln Ala Asn Ala Ala Leu Gly Gly
690 695 700
Leu Pro Ala Pro Leu Tyr Thr Ala Ile Ala Ala Val Val Ala Phe Thr
705 710 715 720
Ala Ala Val Ala Gly Ser Ala Leu Met Phe Lys Gly Ala Ser Trp Leu
725 730 735
Lys Gly Gly Met Ala Ser Lys Tyr Gly Gly Lys Gly Gly Lys Gly Gly
740 745 750
Lys Gly Gly Gly Thr Gly Gly Gly Gly Gly Ala Gly Gly Ala Ala Ala
755 760 765
Thr Gly Ala Gly Ala Ala Ala Gly Ala Gly Gly Val Gly Ala Ala Ala
770 775 780
Ala Gly Glu Val Gly Ala Gly Val Ala Ala Gly Gly Ala Ala Ala Gly
785 790 795 800
Ala Ala Ala Gly Gly Ser Lys Leu Ala Gly Val Gly Lys Gly Phe Met
805 810 815
Lys Gly Ala Gly Lys Leu Met Leu Pro Leu Gly Ile Leu Met Gly Ala
820 825 830
Ser Glu Ile Met Gln Ala Pro Glu Glu Ala Lys Gly Ser Ala Ile Gly
835 840 845
Ser Ala Val Gly Gly Ile Gly Gly Gly Ile Ala Gly Gly Ala Ala Thr
850 855 860
Gly Ala Ile Ala Gly Ser Phe Leu Gly Pro Ile Gly Thr Ala Val Gly
865 870 875 880
Gly Ile Ala Gly Gly Ile Ala Gly Gly Phe Ala Gly Ser Ser Leu Gly
885 890 895
Glu Thr Ile Gly Gly Trp Phe Asp Ser Gly Pro Lys Glu Asp Ala Ser
900 905 910
Ala Ala Asp Lys Ala Lys Ala Asp Ala Ser Ala Ala Ala Leu Ala Ala
915 920 925
Ala Ala Gly Thr Ser Gly Ala Val Gly Ser Ser Ala Leu Gln Ser Gln
930 935 940
Met Ala Gln Gly Ile Thr Gly Ala Pro Asn Met Ser Gln Val Gly Ser
945 950 955 960
Met Ala Ser Ala Leu Gly Ile Ser Ser Gly Ala Met Ala Ser Ala Leu
965 970 975
Gly Ile Ser Ser Gly Gln Glu Asn Gln Ile Gln Thr Met Thr Asp Lys
980 985 990
Glu Asn Thr Asn Thr Lys Lys Ala Asn Glu Ala Lys Lys Gly Asp Asn
995 1000 1005
Leu Ser Tyr Glu Arg Glu Asn Ile Ser Met Tyr Glu Arg Val Leu
1010 1015 1020
Thr Arg Ala Glu Gln Ile Leu Ala Gln Ala Arg Ala Gln Asn Gly
1025 1030 1035
Ile Met Gly Val Gly Gly Gly Gly Thr Ala Gly Ala Gly Gly Gly
1040 1045 1050
Ile Asn Gly Phe Thr Gly Gly Gly Lys Leu Gln Phe Leu Ala Ala
1055 1060 1065
Gly Gln Lys Trp Ser Ser Ser Asn Leu Gln Gln His Asp Leu Gly
1070 1075 1080
Phe Thr Asp Gln Asn Leu Thr Ala Glu Asp Leu Asp Lys Trp Ile
1085 1090 1095
Asp Ser Lys Ala Pro Gln Gly Ser Met Met Arg Gly Met Gly Ala
1100 1105 1110
Thr Phe Leu Lys Ala Gly Gln Glu Tyr Gly Leu Asp Pro Arg Tyr
1115 1120 1125
Leu Ile Ala His Ala Ala Glu Glu Ser Gly Trp Gly Thr Ser Lys
1130 1135 1140
Ile Ala Arg Asp Lys Gly Asn Phe Phe Gly Ile Gly Ala Phe Asp
1145 1150 1155
Asp Ser Pro Tyr Ser Ser Ala Tyr Glu Phe Lys Asp Gly Thr Gly
1160 1165 1170
Ser Ala Ala Glu Arg Gly Ile Met Gly Gly Ala Lys Trp Ile Ser
1175 1180 1185
Glu Lys Tyr Tyr Gly Lys Gly Asn Thr Thr Leu Asp Lys Met Lys
1190 1195 1200
Ala Ala Gly Tyr Ala Thr Asn Ala Ser Trp Ala Pro Asn Ile Ala
1205 1210 1215
Ser Ile Met Ala Gly Ala Pro Thr Gly Ser Gly Ser Gly Asn Val
1220 1225 1230
Thr Ala Thr Ile Asn Val Asn Val Lys Gly Asp Glu Lys Val Ser
1235 1240 1245
Asp Lys Leu Lys Asn Ser Ser Asp Met Lys Lys Ala Gly Lys Asp
1250 1255 1260
Ile Gly Ser Leu Leu Gly Phe Tyr Ser Arg Glu Met Thr Ile Ala
1265 1270 1275
<210> 36
<211> 495
<212> БЕЛОК
<213> (Phi)GH15
<400> 36
Met Ala Lys Thr Gln Ala Glu Ile Asn Lys Arg Leu Asp Ala Tyr Ala
1 5 10 15
Lys Gly Thr Val Asp Ser Pro Tyr Arg Ile Lys Lys Ala Thr Ser Tyr
20 25 30
Asp Pro Ser Phe Gly Val Met Glu Ala Gly Ala Ile Asp Ala Asp Gly
35 40 45
Tyr Tyr His Ala Gln Cys Gln Asp Leu Ile Thr Asp Tyr Val Leu Trp
50 55 60
Leu Thr Asp Asn Lys Val Arg Thr Trp Gly Asn Ala Lys Asp Gln Ile
65 70 75 80
Lys Gln Ser Tyr Gly Thr Gly Phe Lys Ile His Glu Asn Lys Pro Ser
85 90 95
Thr Val Pro Lys Lys Gly Trp Ile Ala Val Phe Thr Ser Gly Ser Tyr
100 105 110
Gln Gln Trp Gly His Ile Gly Ile Val Tyr Asp Gly Gly Asn Thr Ser
115 120 125
Thr Phe Thr Ile Leu Glu Gln Asn Trp Asn Gly Tyr Ala Asn Lys Lys
130 135 140
Pro Thr Lys Arg Val Asp Asn Tyr Tyr Gly Leu Thr His Phe Ile Glu
145 150 155 160
Ile Pro Val Lys Ala Gly Thr Thr Val Lys Lys Glu Thr Ala Lys Lys
165 170 175
Ser Ala Ser Lys Thr Pro Ala Pro Lys Lys Lys Ala Thr Leu Lys Val
180 185 190
Ser Lys Asn His Ile Asn Tyr Thr Met Asp Lys Arg Gly Lys Lys Pro
195 200 205
Glu Gly Met Val Ile His Asn Asp Ala Gly Arg Ser Ser Gly Gln Gln
210 215 220
Tyr Glu Asn Ser Leu Ala Asn Ala Gly Tyr Ala Arg Tyr Ala Asn Gly
225 230 235 240
Ile Ala His Tyr Tyr Gly Ser Glu Gly Tyr Val Trp Glu Ala Ile Asp
245 250 255
Ala Lys Asn Gln Ile Ala Trp His Thr Gly Asp Gly Thr Gly Ala Asn
260 265 270
Ser Gly Asn Phe Arg Phe Ala Gly Ile Glu Val Cys Gln Ser Met Ser
275 280 285
Ala Ser Asp Ala Gln Phe Leu Lys Asn Glu Gln Ala Val Phe Gln Phe
290 295 300
Thr Ala Glu Lys Phe Lys Glu Trp Gly Leu Thr Pro Asn Arg Lys Thr
305 310 315 320
Val Arg Leu His Met Glu Phe Val Pro Thr Ala Cys Pro His Arg Ser
325 330 335
Met Val Leu His Thr Gly Phe Asn Pro Val Thr Gln Gly Arg Pro Ser
340 345 350
Gln Ala Ile Met Asn Lys Leu Lys Asp Tyr Phe Ile Lys Gln Ile Lys
355 360 365
Asn Tyr Met Asp Lys Gly Thr Ser Ser Ser Thr Val Val Lys Asp Gly
370 375 380
Lys Thr Ser Ser Ala Ser Thr Pro Ala Thr Arg Pro Val Thr Gly Ser
385 390 395 400
Trp Lys Lys Asn Gln Tyr Gly Thr Trp Tyr Lys Pro Glu Asn Ala Thr
405 410 415
Phe Val Asn Gly Asn Gln Pro Ile Val Thr Arg Ile Gly Ser Pro Phe
420 425 430
Leu Asn Ala Pro Val Gly Gly Asn Leu Pro Ala Gly Ala Thr Ile Val
435 440 445
Tyr Asp Glu Val Cys Ile Gln Ala Gly His Ile Trp Ile Gly Tyr Asn
450 455 460
Ala Tyr Asn Gly Asp Arg Val Tyr Cys Pro Val Arg Thr Cys Gln Gly
465 470 475 480
Val Pro Pro Asn His Ile Pro Gly Val Ala Trp Gly Val Phe Lys
485 490 495
<210> 37
<211> 264
<212> БЕЛОК
<213> (Phi)8074-B1
<400> 37
Met Lys Ile Gly Ile Asp Met Gly His Thr Leu Ser Gly Ala Asp Tyr
1 5 10 15
Gly Val Val Gly Leu Arg Pro Glu Ser Val Leu Thr Arg Glu Val Gly
20 25 30
Thr Lys Val Ile Tyr Lys Leu Gln Lys Leu Gly His Val Val Val Asn
35 40 45
Cys Thr Val Asp Lys Ala Ser Ser Val Ser Glu Ser Leu Tyr Thr Arg
50 55 60
Tyr Tyr Arg Ala Asn Gln Ala Asn Val Asp Leu Phe Ile Ser Ile His
65 70 75 80
Phe Asn Ala Thr Pro Gly Gly Thr Gly Thr Glu Val Tyr Thr Tyr Ala
85 90 95
Gly Arg Gln Leu Gly Glu Ala Thr Arg Ile Arg Gln Glu Phe Lys Ser
100 105 110
Leu Gly Leu Arg Asp Arg Gly Thr Lys Asp Gly Ser Gly Leu Ala Val
115 120 125
Ile Arg Asn Thr Lys Ala Lys Ala Met Leu Val Glu Cys Cys Phe Cys
130 135 140
Asp Asn Pro Asn Asp Met Lys Leu Tyr Asn Ser Glu Ser Phe Ser Asn
145 150 155 160
Ala Ile Val Lys Gly Ile Thr Gly Lys Leu Pro Asn Gly Glu Ser Gly
165 170 175
Asn Asn Asn Gln Gly Gly Asn Lys Val Lys Ala Val Val Ile Tyr Asn
180 185 190
Glu Gly Ala Asp Arg Arg Gly Ala Glu Tyr Leu Ala Asp Tyr Leu Asn
195 200 205
Cys Pro Thr Ile Ser Asn Ser Arg Thr Phe Asp Tyr Ser Cys Val Glu
210 215 220
His Val Tyr Ala Val Gly Gly Lys Lys Glu Gln Tyr Thr Lys Tyr Leu
225 230 235 240
Lys Thr Leu Leu Ser Gly Ala Asn Arg Tyr Asp Thr Met Gln Gln Ile
245 250 255
Leu Asn Phe Ile Asn Gly Gly Lys
260
<210> 38
<211> 209
<212> БЕЛОК
<213> (Phi)SPN1S
<400> 38
Met Asp Ile Asn Gln Phe Arg Arg Ala Ser Gly Ile Asn Glu Gln Leu
1 5 10 15
Ala Ala Arg Trp Phe Pro His Ile Thr Thr Ala Met Asn Glu Phe Gly
20 25 30
Ile Thr Lys Pro Asp Asp Gln Ala Met Phe Ile Ala Gln Val Gly His
35 40 45
Glu Ser Gly Gly Phe Thr Arg Leu Gln Glu Asn Phe Asn Tyr Ser Val
50 55 60
Asn Gly Leu Ser Gly Phe Ile Arg Ala Gly Arg Ile Thr Pro Asp Gln
65 70 75 80
Ala Asn Ala Leu Gly Arg Lys Thr Tyr Glu Lys Ser Leu Pro Leu Glu
85 90 95
Arg Gln Arg Ala Ile Ala Asn Leu Val Tyr Ser Lys Arg Met Gly Asn
100 105 110
Asn Gly Pro Gly Asp Gly Trp Asn Tyr Arg Gly Arg Gly Leu Ile Gln
115 120 125
Ile Thr Gly Leu Asn Asn Tyr Arg Asp Cys Gly Asn Gly Leu Lys Val
130 135 140
Asp Leu Val Ala Gln Pro Glu Leu Leu Ala Gln Asp Glu Tyr Ala Ala
145 150 155 160
Arg Ser Ala Ala Trp Phe Phe Ser Ser Lys Gly Cys Met Lys Tyr Thr
165 170 175
Gly Asp Leu Val Arg Val Thr Gln Ile Ile Asn Gly Gly Gln Asn Gly
180 185 190
Ile Asp Asp Arg Arg Thr Arg Tyr Ala Ala Ala Arg Lys Val Leu Ala
195 200 205
Leu
<210> 39
<211> 290
<212> БЕЛОК
<213> (Phi)CN77
<400> 39
Met Gly Tyr Trp Gly Tyr Pro Asn Gly Gln Ile Pro Asn Asp Lys Met
1 5 10 15
Ala Leu Tyr Arg Gly Cys Leu Leu Arg Ala Asp Ala Ala Ala Gln Ala
20 25 30
Tyr Ala Leu Gln Asp Ala Tyr Thr Arg Ala Thr Gly Lys Pro Leu Val
35 40 45
Ile Leu Glu Gly Tyr Arg Asp Leu Thr Arg Gln Lys Tyr Leu Arg Asn
50 55 60
Leu Tyr Leu Ser Gly Arg Gly Asn Ile Ala Ala Val Pro Gly Leu Ser
65 70 75 80
Asn His Gly Trp Gly Leu Ala Cys Asp Phe Ala Ala Pro Leu Asn Ser
85 90 95
Ser Gly Ser Glu Glu His Arg Trp Met Arg Gln Asn Ala Pro Leu Phe
100 105 110
Gly Phe Asp Trp Ala Arg Gly Lys Ala Asp Asn Glu Pro Trp His Trp
115 120 125
Glu Tyr Gly Asn Val Pro Val Ser Arg Trp Ala Ser Leu Asp Val Thr
130 135 140
Pro Ile Asp Arg Asn Asp Met Ala Asp Ile Thr Glu Gly Gln Met Gln
145 150 155 160
Arg Ile Ala Val Ile Leu Leu Asp Thr Glu Ile Gln Thr Pro Leu Gly
165 170 175
Pro Arg Leu Val Lys His Ala Leu Gly Asp Ala Leu Leu Leu Gly Gln
180 185 190
Ala Asn Ala Asn Ser Ile Ala Glu Val Pro Asp Lys Thr Trp Asp Val
195 200 205
Leu Val Asp His Pro Leu Ala Lys Asn Glu Asp Gly Thr Pro Leu Lys
210 215 220
Val Arg Leu Gly Asp Val Ala Lys Tyr Glu Pro Leu Glu His Gln Asn
225 230 235 240
Thr Arg Asp Ala Ile Ala Lys Leu Gly Thr Leu Gln Phe Thr Asp Lys
245 250 255
Gln Leu Ala Thr Ile Gly Ala Gly Val Lys Pro Ile Asp Glu Ala Ser
260 265 270
Leu Val Lys Lys Ile Val Asp Gly Val Arg Ala Leu Phe Gly Arg Ala
275 280 285
Ala Ala
290
<210> 40
<211> 185
<212> БЕЛОК
<213> (Phi)AB2
<400> 40
Met Ile Leu Thr Lys Asp Gly Phe Ser Ile Ile Arg Asn Glu Leu Phe
1 5 10 15
Gly Gly Lys Leu Asp Gln Thr Gln Val Asp Ala Ile Asn Phe Ile Val
20 25 30
Ala Lys Ala Thr Glu Ser Gly Leu Thr Tyr Pro Glu Ala Ala Tyr Leu
35 40 45
Leu Ala Thr Ile Tyr His Glu Thr Gly Leu Pro Ser Gly Tyr Arg Thr
50 55 60
Met Gln Pro Ile Lys Glu Ala Gly Ser Asp Ser Tyr Leu Arg Ser Lys
65 70 75 80
Lys Tyr Tyr Pro Tyr Ile Gly Tyr Gly Tyr Val Gln Leu Thr Trp Lys
85 90 95
Glu Asn Tyr Glu Arg Ile Gly Lys Leu Ile Gly Val Asp Leu Ile Lys
100 105 110
Asn Pro Glu Lys Ala Leu Glu Pro Leu Ile Ala Ile Gln Ile Ala Ile
115 120 125
Lys Gly Met Leu Asn Gly Trp Phe Thr Gly Val Gly Phe Arg Arg Lys
130 135 140
Arg Pro Val Ser Lys Tyr Asn Lys Gln Gln Tyr Val Ala Ala Arg Asn
145 150 155 160
Ile Ile Asn Gly Lys Asp Lys Ala Glu Leu Ile Ala Lys Tyr Ala Ile
165 170 175
Ile Phe Glu Arg Ala Leu Arg Ser Leu
180 185
<210> 41
<211> 262
<212> БЕЛОК
<213> (Phi)B4
<400> 41
Met Ala Met Ala Leu Gln Thr Leu Ile Asp Lys Ala Asn Arg Lys Leu
1 5 10 15
Asn Val Ser Gly Met Arg Lys Asp Val Ala Asp Arg Thr Arg Ala Val
20 25 30
Ile Thr Gln Met His Ala Gln Gly Ile Tyr Ile Cys Val Ala Gln Gly
35 40 45
Phe Arg Ser Phe Ala Glu Gln Asn Ala Leu Tyr Ala Gln Gly Arg Thr
50 55 60
Lys Pro Gly Ser Ile Val Thr Asn Ala Arg Gly Gly Gln Ser Asn His
65 70 75 80
Asn Tyr Gly Val Ala Val Asp Leu Cys Leu Tyr Thr Gln Asp Gly Ser
85 90 95
Asp Val Ile Trp Thr Val Glu Gly Asn Phe Arg Lys Val Ile Ala Ala
100 105 110
Met Lys Ala Gln Gly Phe Lys Trp Gly Gly Asp Trp Val Ser Phe Lys
115 120 125
Asp Tyr Pro His Phe Glu Leu Tyr Asp Val Val Gly Gly Gln Lys Pro
130 135 140
Pro Ala Asp Asn Gly Gly Ala Val Asp Asn Gly Gly Gly Ser Gly Ser
145 150 155 160
Thr Gly Gly Ser Gly Gly Gly Ser Thr Gly Gly Gly Ser Thr Gly Gly
165 170 175
Gly Tyr Asp Ser Ser Trp Phe Thr Lys Glu Thr Gly Thr Phe Val Thr
180 185 190
Asn Thr Ser Ile Lys Leu Arg Thr Ala Pro Phe Thr Ser Ala Asp Val
195 200 205
Ile Ala Thr Leu Pro Ala Gly Ser Pro Val Asn Tyr Asn Gly Phe Gly
210 215 220
Ile Glu Tyr Asp Gly Tyr Val Trp Ile Arg Gln Pro Arg Ser Asn Gly
225 230 235 240
Tyr Gly Tyr Leu Ala Thr Gly Glu Ser Lys Gly Gly Lys Arg Gln Asn
245 250 255
Tyr Trp Gly Thr Phe Lys
260
<210> 42
<211> 274
<212> БЕЛОК
<213> (Phi)CTP1
<400> 42
Met Lys Lys Ile Ala Asp Ile Ser Asn Leu Asn Gly Asn Val Asp Val
1 5 10 15
Lys Leu Leu Phe Asn Leu Gly Tyr Ile Gly Ile Ile Ala Lys Ala Ser
20 25 30
Glu Gly Gly Thr Phe Val Asp Lys Tyr Tyr Lys Gln Asn Tyr Thr Asn
35 40 45
Thr Lys Ala Gln Gly Lys Ile Thr Gly Ala Tyr His Phe Ala Asn Phe
50 55 60
Ser Thr Ile Ala Lys Ala Gln Gln Glu Ala Asn Phe Phe Leu Asn Cys
65 70 75 80
Ile Ala Gly Thr Thr Pro Asp Phe Val Val Leu Asp Leu Glu Gln Gln
85 90 95
Cys Thr Gly Asp Ile Thr Asp Ala Cys Leu Ala Phe Leu Asn Ile Val
100 105 110
Ala Lys Lys Phe Lys Cys Val Val Tyr Cys Asn Ser Ser Phe Ile Lys
115 120 125
Glu His Leu Asn Ser Lys Ile Cys Ala Tyr Pro Leu Trp Ile Ala Asn
130 135 140
Tyr Gly Val Ala Thr Pro Ala Phe Thr Leu Trp Thr Lys Tyr Ala Met
145 150 155 160
Trp Gln Phe Thr Glu Lys Gly Gln Val Ser Gly Ile Ser Gly Tyr Ile
165 170 175
Asp Phe Ser Tyr Ile Thr Asp Glu Phe Ile Lys Tyr Ile Lys Gly Glu
180 185 190
Asp Glu Val Glu Asn Leu Val Val Tyr Asn Asp Gly Ala Asp Gln Arg
195 200 205
Ala Ala Glu Tyr Leu Ala Asp Arg Leu Ala Cys Pro Thr Ile Asn Asn
210 215 220
Ala Arg Lys Phe Asp Tyr Ser Asn Val Lys Asn Val Tyr Ala Val Gly
225 230 235 240
Gly Asn Lys Glu Gln Tyr Thr Ser Tyr Leu Thr Thr Leu Ile Ala Gly
245 250 255
Ser Thr Arg Tyr Thr Thr Met Gln Ala Val Leu Asp Tyr Ile Lys Asn
260 265 270
Leu Lys
<210> 43
<211> 628
<212> БЕЛОК
<213> Вирус стафилококка 187
<400> 43
Met Ala Leu Pro Lys Thr Gly Lys Pro Thr Ala Lys Gln Val Val Asp
1 5 10 15
Trp Ala Ile Asn Leu Ile Gly Ser Gly Val Asp Val Asp Gly Tyr Tyr
20 25 30
Gly Arg Gln Cys Trp Asp Leu Pro Asn Tyr Ile Phe Asn Arg Tyr Trp
35 40 45
Asn Phe Lys Thr Pro Gly Asn Ala Arg Asp Met Ala Trp Tyr Arg Tyr
50 55 60
Pro Glu Gly Phe Lys Val Phe Arg Asn Thr Ser Asp Phe Val Pro Lys
65 70 75 80
Pro Gly Asp Ile Ala Val Trp Thr Gly Gly Asn Tyr Asn Trp Asn Thr
85 90 95
Trp Gly His Thr Gly Ile Val Val Gly Pro Ser Thr Lys Ser Tyr Phe
100 105 110
Tyr Ser Val Asp Gln Asn Trp Asn Asn Ser Asn Ser Tyr Val Gly Ser
115 120 125
Pro Ala Ala Lys Ile Lys His Ser Tyr Phe Gly Val Thr His Phe Val
130 135 140
Arg Pro Ala Tyr Lys Ala Glu Pro Lys Pro Thr Pro Pro Ala Gln Asn
145 150 155 160
Asn Pro Ala Pro Lys Asp Pro Glu Pro Ser Lys Lys Pro Glu Ser Asn
165 170 175
Lys Pro Ile Tyr Lys Val Val Thr Lys Ile Leu Phe Thr Thr Ala His
180 185 190
Ile Glu His Val Lys Ala Asn Arg Phe Val His Tyr Ile Thr Lys Ser
195 200 205
Asp Asn His Asn Asn Lys Pro Asn Lys Ile Val Ile Lys Asn Thr Asn
210 215 220
Thr Ala Leu Ser Thr Ile Asp Val Tyr Arg Tyr Arg Asp Glu Leu Asp
225 230 235 240
Lys Asp Glu Ile Pro His Phe Phe Val Asp Arg Leu Asn Val Trp Ala
245 250 255
Cys Arg Pro Ile Glu Asp Ser Ile Asn Gly Tyr His Asp Ser Val Val
260 265 270
Leu Ser Ile Thr Glu Thr Arg Thr Ala Leu Ser Asp Asn Phe Lys Met
275 280 285
Asn Glu Ile Glu Cys Leu Ser Leu Ala Glu Ser Ile Leu Lys Ala Asn
290 295 300
Asn Lys Lys Met Ser Ala Ser Asn Ile Ile Val Asp Asn Lys Ala Trp
305 310 315 320
Arg Thr Phe Lys Leu His Thr Gly Lys Asp Ser Leu Lys Ser Ser Ser
325 330 335
Phe Thr Ser Lys Asp Tyr Gln Lys Ala Val Asn Glu Leu Ile Lys Leu
340 345 350
Phe Asn Asp Lys Asp Lys Leu Leu Asn Asn Lys Pro Lys Asp Val Val
355 360 365
Glu Arg Ile Arg Ile Arg Thr Ile Val Lys Glu Asn Thr Lys Phe Val
370 375 380
Pro Ser Glu Leu Lys Pro Arg Asn Asn Ile Arg Asp Lys Gln Asp Ser
385 390 395 400
Lys Ile Asp Arg Val Ile Asn Asn Tyr Thr Leu Lys Gln Ala Leu Asn
405 410 415
Ile Gln Tyr Lys Leu Asn Pro Lys Pro Gln Thr Ser Asn Gly Val Ser
420 425 430
Trp Tyr Asn Ala Ser Val Asn Gln Ile Lys Ser Ala Met Asp Thr Thr
435 440 445
Lys Ile Phe Asn Asn Asn Val Gln Val Tyr Gln Phe Leu Lys Leu Asn
450 455 460
Gln Tyr Gln Gly Ile Pro Val Asp Lys Leu Asn Lys Leu Leu Val Gly
465 470 475 480
Lys Gly Thr Leu Ala Asn Gln Gly His Ala Phe Ala Asp Gly Cys Lys
485 490 495
Lys Tyr Asn Ile Asn Glu Ile Tyr Leu Ile Ala His Arg Phe Leu Glu
500 505 510
Ser Ala Asn Gly Thr Ser Phe Phe Ala Ser Gly Lys Thr Gly Val Tyr
515 520 525
Asn Tyr Phe Gly Ile Gly Ala Phe Asp Asn Asn Pro Asn Asn Ala Met
530 535 540
Ala Phe Ala Arg Ser His Gly Trp Thr Ser Pro Thr Lys Ala Ile Ile
545 550 555 560
Gly Gly Ala Glu Phe Val Gly Lys Gly Tyr Phe Asn Val Gly Gln Asn
565 570 575
Thr Leu Tyr Arg Met Arg Trp Asn Pro Gln Lys Pro Gly Thr His Gln
580 585 590
Tyr Ala Thr Asp Ile Ser Trp Ala Lys Val Gln Ala Gln Met Ile Ser
595 600 605
Ala Met Tyr Lys Glu Ile Gly Leu Thr Gly Asp Tyr Phe Ile Tyr Asp
610 615 620
Gln Tyr Lys Lys
625
<210> 44
<211> 291
<212> БЕЛОК
<213> (Phi)P35
<400> 44
Met Ala Arg Lys Phe Thr Lys Ala Glu Leu Val Ala Lys Ala Glu Lys
1 5 10 15
Lys Val Gly Gly Leu Lys Pro Asp Val Lys Lys Ala Val Leu Ser Ala
20 25 30
Val Lys Glu Ala Tyr Asp Arg Tyr Gly Ile Gly Ile Ile Val Ser Gln
35 40 45
Gly Tyr Arg Ser Ile Ala Glu Gln Asn Gly Leu Tyr Ala Gln Gly Arg
50 55 60
Thr Lys Pro Gly Asn Ile Val Thr Asn Ala Lys Gly Gly Gln Ser Asn
65 70 75 80
His Asn Phe Gly Val Ala Val Asp Phe Ala Ile Asp Leu Ile Asp Asp
85 90 95
Gly Lys Ile Asp Ser Trp Gln Pro Ser Ala Thr Ile Val Asn Met Met
100 105 110
Lys Arg Arg Gly Phe Lys Trp Gly Gly Asp Trp Lys Ser Phe Thr Asp
115 120 125
Leu Pro His Phe Glu Ala Cys Asp Trp Tyr Arg Gly Glu Arg Lys Tyr
130 135 140
Lys Val Asp Thr Ser Glu Trp Lys Lys Lys Glu Asn Ile Asn Ile Val
145 150 155 160
Ile Lys Asp Val Gly Tyr Phe Gln Asp Lys Pro Gln Phe Leu Asn Ser
165 170 175
Lys Ser Val Arg Gln Trp Lys His Gly Thr Lys Val Lys Leu Thr Lys
180 185 190
His Asn Ser His Trp Tyr Thr Gly Val Val Lys Asp Gly Asn Lys Ser
195 200 205
Val Arg Gly Tyr Ile Tyr His Ser Met Ala Lys Val Thr Ser Lys Asn
210 215 220
Ser Asp Gly Ser Val Asn Ala Thr Ile Asn Ala His Ala Phe Cys Trp
225 230 235 240
Asp Asn Lys Lys Leu Asn Gly Gly Asp Phe Ile Asn Leu Lys Arg Gly
245 250 255
Phe Lys Gly Ile Thr His Pro Ala Ser Asp Gly Phe Tyr Pro Leu Tyr
260 265 270
Phe Ala Ser Arg Lys Lys Thr Phe Tyr Ile Pro Arg Tyr Met Phe Asp
275 280 285
Ile Lys Lys
290
<210> 45
<211> 342
<212> БЕЛОК
<213> (Phi)CP-7
<400> 45
Met Val Lys Lys Asn Asp Leu Phe Val Asp Val Ala Ser His Gln Gly
1 5 10 15
Tyr Asp Ile Ser Gly Ile Leu Glu Glu Ala Gly Thr Thr Asn Thr Ile
20 25 30
Ile Lys Val Ser Glu Ser Thr Ser Tyr Leu Asn Pro Cys Leu Ser Ala
35 40 45
Gln Val Ser Gln Ser Asn Pro Ile Gly Phe Tyr His Phe Ala Trp Phe
50 55 60
Gly Gly Asn Glu Glu Glu Ala Glu Ala Glu Ala Arg Tyr Phe Leu Asp
65 70 75 80
Asn Val Pro Thr Gln Val Lys Tyr Leu Val Leu Asp Tyr Glu Asp His
85 90 95
Ala Ser Ala Ser Val Gln Arg Asn Thr Thr Ala Cys Leu Arg Phe Met
100 105 110
Gln Ile Ile Ala Glu Ala Gly Tyr Thr Pro Ile Tyr Tyr Ser Tyr Lys
115 120 125
Pro Phe Thr Leu Asp Asn Val Asp Tyr Gln Gln Ile Leu Ala Gln Phe
130 135 140
Pro Asn Ser Leu Trp Ile Ala Gly Tyr Gly Leu Asn Asp Gly Thr Ala
145 150 155 160
Asn Phe Glu Tyr Phe Pro Ser Met Asp Gly Ile Arg Trp Trp Gln Tyr
165 170 175
Ser Ser Asn Pro Phe Asp Lys Asn Ile Val Leu Leu Asp Asp Glu Lys
180 185 190
Glu Asp Asn Ile Asn Asn Glu Asn Thr Leu Lys Ser Leu Thr Thr Val
195 200 205
Ala Asn Glu Val Ile Gln Gly Leu Trp Gly Asn Gly Gln Glu Arg Tyr
210 215 220
Asp Ser Leu Ala Asn Ala Gly Tyr Asp Pro Gln Ala Val Gln Asp Lys
225 230 235 240
Val Asn Glu Ile Leu Asn Ala Arg Glu Ile Ala Asp Leu Thr Thr Val
245 250 255
Ala Asn Glu Val Ile Gln Gly Leu Trp Gly Asn Gly Gln Glu Arg Tyr
260 265 270
Asp Ser Leu Ala Asn Ala Gly Tyr Asp Pro Gln Ala Val Gln Asp Lys
275 280 285
Val Asn Glu Ile Leu Asn Ala Arg Glu Ile Ala Asp Leu Thr Thr Val
290 295 300
Ala Asn Glu Val Ile Gln Gly Leu Trp Gly Asn Gly Gln Glu Arg Tyr
305 310 315 320
Asp Ser Leu Ala Asn Ala Gly Tyr Asp Pro Gln Ala Val Gln Asp Lys
325 330 335
Val Asn Glu Leu Leu Ser
340
<210> 46
<211> 328
<212> БЕЛОК
<213> (Phi)EFAP-1
<400> 46
Met Lys Leu Lys Gly Ile Leu Leu Ser Val Val Thr Thr Phe Gly Leu
1 5 10 15
Leu Phe Gly Ala Thr Asn Val Gln Ala Tyr Glu Val Asn Asn Glu Phe
20 25 30
Asn Leu Gln Pro Trp Glu Gly Ser Gln Gln Leu Ala Tyr Pro Asn Lys
35 40 45
Ile Ile Leu His Glu Thr Ala Asn Pro Arg Ala Thr Gly Arg Asn Glu
50 55 60
Ala Thr Tyr Met Lys Asn Asn Trp Phe Asn Ala His Thr Thr Ala Ile
65 70 75 80
Val Gly Asp Gly Gly Ile Val Tyr Lys Val Ala Pro Glu Gly Asn Val
85 90 95
Ser Trp Gly Ala Gly Asn Ala Asn Pro Tyr Ala Pro Val Gln Ile Glu
100 105 110
Leu Gln His Thr Asn Asp Pro Glu Leu Phe Lys Ala Asn Tyr Lys Ala
115 120 125
Tyr Val Asp Tyr Thr Arg Asp Met Gly Lys Lys Phe Gly Ile Pro Met
130 135 140
Thr Leu Asp Gln Gly Gly Ser Leu Trp Glu Lys Gly Val Val Ser His
145 150 155 160
Gln Trp Val Thr Asp Phe Val Trp Gly Asp His Thr Asp Pro Tyr Gly
165 170 175
Tyr Leu Ala Lys Met Gly Ile Ser Lys Ala Gln Leu Ala His Asp Leu
180 185 190
Ala Asn Gly Val Ser Gly Asn Thr Ala Thr Pro Thr Pro Lys Pro Asp
195 200 205
Lys Pro Lys Pro Thr Gln Pro Ser Lys Pro Ser Asn Lys Lys Arg Phe
210 215 220
Asn Tyr Arg Val Asp Gly Leu Glu Tyr Val Asn Gly Met Trp Gln Ile
225 230 235 240
Tyr Asn Glu His Leu Gly Lys Ile Asp Phe Asn Trp Thr Glu Asn Gly
245 250 255
Ile Pro Val Glu Val Val Asp Lys Val Asn Pro Ala Thr Gly Gln Pro
260 265 270
Thr Lys Asp Gln Val Leu Lys Val Gly Asp Tyr Phe Asn Phe Gln Glu
275 280 285
Asn Ser Thr Gly Val Val Gln Glu Gln Thr Pro Tyr Met Gly Tyr Thr
290 295 300
Leu Ser His Val Gln Leu Pro Asn Glu Phe Ile Trp Leu Phe Thr Asp
305 310 315 320
Ser Lys Gln Ala Leu Met Tyr Gln
325
<210> 47
<211> 48
<212> БЕЛОК
<213> Homo sapiens
<400> 47
Ser Ser Leu Leu Glu Lys Gly Leu Asp Gly Ala Lys Lys Ala Val Gly
1 5 10 15
Gly Leu Gly Lys Leu Gly Lys Asp Ala Val Glu Asp Leu Glu Ser Val
20 25 30
Gly Lys Gly Ala Val His Asp Val Lys Asp Val Leu Asp Ser Val Leu
35 40 45
<210> 48
<211> 37
<212> БЕЛОК
<213> Hyalophora cecropia
<400> 48
Lys Trp Lys Leu Phe Lys Lys Ile Glu Lys Val Gly Gln Asn Ile Arg
1 5 10 15
Asp Gly Ile Ile Lys Ala Gly Pro Ala Val Ala Val Val Gly Gln Ala
20 25 30
Thr Gln Ile Ala Lys
35
<210> 49
<211> 62
<212> БЕЛОК
<213> Drosophila teissieri
<400> 49
Met Lys Tyr Phe Ser Val Leu Val Val Leu Thr Leu Ile Leu Ala Ile
1 5 10 15
Val Asp Gln Ser Asp Ala Phe Ile Asn Leu Leu Asp Lys Val Glu Asp
20 25 30
Ala Leu His Thr Gly Ala Gln Ala Gly Phe Lys Leu Ile Arg Pro Val
35 40 45
Glu Arg Gly Ala Thr Pro Lys Lys Ser Glu Lys Pro Glu Lys
50 55 60
<210> 50
<211> 66
<212> БЕЛОК
<213> Bombyx mori
<400> 50
Met Asn Ile Leu Lys Phe Phe Phe Val Phe Ile Val Ala Met Ser Leu
1 5 10 15
Val Ser Cys Ser Thr Ala Ala Pro Ala Lys Ile Pro Ile Lys Ala Ile
20 25 30
Lys Thr Val Gly Lys Ala Val Gly Lys Gly Leu Arg Ala Ile Asn Ile
35 40 45
Ala Ser Thr Ala Asn Asp Val Phe Asn Phe Leu Lys Pro Lys Lys Arg
50 55 60
Lys His
65
<210> 51
<211> 71
<212> БЕЛОК
<213> Ceratitis capitata
<400> 51
Met Ala Asn Leu Lys Ala Val Phe Leu Ile Cys Ile Val Ala Phe Ile
1 5 10 15
Ala Leu Gln Cys Val Val Ala Glu Pro Ala Ala Glu Asp Ser Val Val
20 25 30
Val Lys Arg Ser Ile Gly Ser Ala Leu Lys Lys Ala Leu Pro Val Ala
35 40 45
Lys Lys Ile Gly Lys Ile Ala Leu Pro Ile Ala Lys Ala Ala Leu Pro
50 55 60
Val Ala Ala Gly Leu Val Gly
65 70
<210> 52
<211> 53
<212> БЕЛОК
<213> Apis mellifera
<400> 52
Met Lys Val Val Ile Phe Ile Phe Ala Leu Leu Ala Thr Ile Cys Ala
1 5 10 15
Ala Phe Ala Tyr Val Pro Leu Pro Asn Val Pro Gln Pro Gly Arg Arg
20 25 30
Pro Phe Pro Thr Phe Pro Gly Gln Gly Pro Phe Asn Pro Lys Ile Lys
35 40 45
Trp Pro Gln Gly Tyr
50
<210> 53
<211> 283
<212> БЕЛОК
<213> Apis mellifera
<400> 53
Lys Asn Phe Ala Leu Ala Ile Leu Val Val Thr Phe Val Val Ala Val
1 5 10 15
Phe Gly Asn Thr Asn Leu Asp Pro Pro Thr Arg Pro Thr Arg Leu Arg
20 25 30
Arg Glu Ala Lys Pro Glu Ala Glu Pro Gly Asn Asn Arg Pro Val Tyr
35 40 45
Ile Pro Gln Pro Arg Pro Pro His Pro Arg Leu Arg Arg Glu Ala Glu
50 55 60
Pro Glu Ala Glu Pro Gly Asn Asn Arg Pro Val Tyr Ile Pro Gln Pro
65 70 75 80
Arg Pro Pro His Pro Arg Leu Arg Arg Glu Ala Glu Leu Glu Ala Glu
85 90 95
Pro Gly Asn Asn Arg Pro Val Tyr Ile Ser Gln Pro Arg Pro Pro His
100 105 110
Pro Arg Leu Arg Arg Glu Ala Glu Pro Glu Ala Glu Pro Gly Asn Asn
115 120 125
Arg Pro Val Tyr Ile Pro Gln Pro Arg Pro Pro His Pro Arg Leu Arg
130 135 140
Arg Glu Ala Glu Leu Glu Ala Glu Pro Gly Asn Asn Arg Pro Val Tyr
145 150 155 160
Ile Ser Gln Pro Arg Pro Pro His Pro Arg Leu Arg Arg Glu Ala Glu
165 170 175
Pro Glu Ala Glu Pro Gly Asn Asn Arg Pro Val Tyr Ile Pro Gln Pro
180 185 190
Arg Pro Pro His Pro Arg Leu Arg Arg Glu Ala Glu Pro Glu Ala Glu
195 200 205
Pro Gly Asn Asn Arg Pro Val Tyr Ile Pro Gln Pro Arg Pro Pro His
210 215 220
Pro Arg Leu Arg Arg Glu Ala Glu Pro Glu Ala Glu Pro Gly Asn Asn
225 230 235 240
Arg Pro Val Tyr Ile Pro Gln Pro Arg Pro Pro His Pro Arg Leu Arg
245 250 255
Arg Glu Ala Lys Pro Glu Ala Lys Pro Gly Asn Asn Arg Pro Val Tyr
260 265 270
Ile Pro Gln Pro Arg Pro Pro His Pro Arg Ile
275 280
<210> 54
<211> 228
<212> БЕЛОК
<213> Sus scrofa
<400> 54
Met Glu Thr Gln Arg Ala Ser Leu Cys Leu Gly Arg Trp Ser Leu Trp
1 5 10 15
Leu Leu Leu Leu Ala Leu Val Val Pro Ser Ala Ser Ala Gln Ala Leu
20 25 30
Ser Tyr Arg Glu Ala Val Leu Arg Ala Val Asp Arg Leu Asn Glu Gln
35 40 45
Ser Ser Glu Ala Asn Leu Tyr Arg Leu Leu Glu Leu Asp Gln Pro Pro
50 55 60
Lys Ala Asp Glu Asp Pro Gly Thr Pro Lys Pro Val Ser Phe Thr Val
65 70 75 80
Lys Glu Thr Val Cys Pro Arg Pro Thr Arg Arg Pro Pro Glu Leu Cys
85 90 95
Asp Phe Lys Glu Asn Gly Arg Val Lys Gln Cys Val Gly Thr Val Thr
100 105 110
Leu Asp Gln Ile Lys Asp Pro Leu Asp Ile Thr Cys Asn Glu Gly Val
115 120 125
Arg Arg Phe Pro Trp Trp Trp Pro Phe Leu Arg Arg Pro Arg Leu Arg
130 135 140
Arg Gln Ala Phe Pro Pro Pro Asn Val Pro Gly Pro Arg Phe Pro Pro
145 150 155 160
Pro Asn Val Pro Gly Pro Arg Phe Pro Pro Pro Asn Phe Pro Gly Pro
165 170 175
Arg Phe Pro Pro Pro Asn Phe Pro Gly Pro Arg Phe Pro Pro Pro Asn
180 185 190
Phe Pro Gly Pro Pro Phe Pro Pro Pro Ile Phe Pro Gly Pro Trp Phe
195 200 205
Pro Pro Pro Pro Pro Phe Arg Pro Pro Pro Phe Gly Pro Pro Arg Phe
210 215 220
Pro Gly Arg Arg
225
<210> 55
<211> 144
<212> БЕЛОК
<213> Bos taurus
<400> 55
Met Gln Thr Gln Arg Ala Ser Leu Ser Leu Gly Arg Trp Ser Leu Trp
1 5 10 15
Leu Leu Leu Leu Gly Leu Val Val Pro Ser Ala Ser Ala Gln Ala Leu
20 25 30
Ser Tyr Arg Glu Ala Val Leu Arg Ala Val Asp Gln Leu Asn Glu Leu
35 40 45
Ser Ser Glu Ala Asn Leu Tyr Arg Leu Leu Glu Leu Asp Pro Pro Pro
50 55 60
Lys Asp Asn Glu Asp Leu Gly Thr Arg Lys Pro Val Ser Phe Thr Val
65 70 75 80
Lys Glu Thr Val Cys Pro Arg Thr Ile Gln Gln Pro Ala Glu Gln Cys
85 90 95
Asp Phe Lys Glu Lys Gly Arg Val Lys Gln Cys Val Gly Thr Val Thr
100 105 110
Leu Asp Pro Ser Asn Asp Gln Phe Asp Leu Asn Cys Asn Glu Leu Gln
115 120 125
Ser Val Ile Leu Pro Trp Lys Trp Pro Trp Trp Pro Trp Arg Arg Gly
130 135 140
<210> 56
<211> 149
<212> БЕЛОК
<213> Sus scrofa
<400> 56
Met Glu Thr Gln Arg Ala Ser Leu Cys Leu Gly Arg Trp Ser Leu Trp
1 5 10 15
Leu Leu Leu Leu Ala Leu Val Val Pro Ser Ala Ser Ala Gln Ala Leu
20 25 30
Ser Tyr Arg Glu Ala Val Leu Arg Ala Val Asp Arg Leu Asn Glu Gln
35 40 45
Ser Ser Glu Ala Asn Leu Tyr Arg Leu Leu Glu Leu Asp Gln Pro Pro
50 55 60
Lys Ala Asp Glu Asp Pro Gly Thr Pro Lys Pro Val Ser Phe Thr Val
65 70 75 80
Lys Glu Thr Val Cys Pro Arg Pro Thr Arg Gln Pro Pro Glu Leu Cys
85 90 95
Asp Phe Lys Glu Asn Gly Arg Val Lys Gln Cys Val Gly Thr Val Thr
100 105 110
Leu Asp Gln Ile Lys Asp Pro Leu Asp Ile Thr Cys Asn Glu Val Gln
115 120 125
Gly Val Arg Gly Gly Arg Leu Cys Tyr Cys Arg Arg Arg Phe Cys Val
130 135 140
Cys Val Gly Arg Gly
145
<210> 57
<211> 17
<212> БЕЛОК
<213> Tachypleus gigas
<400> 57
Lys Trp Cys Phe Arg Val Cys Tyr Arg Gly Ile Cys Tyr Arg Arg Cys
1 5 10 15
Arg
<210> 58
<211> 102
<212> БЕЛОК
<213> Anopheles gambiae
<400> 58
Met Lys Cys Ala Thr Ile Val Cys Thr Ile Ala Val Val Leu Ala Ala
1 5 10 15
Thr Leu Leu Asn Gly Ser Val Gln Ala Ala Pro Gln Glu Glu Ala Ala
20 25 30
Leu Ser Gly Gly Ala Asn Leu Asn Thr Leu Leu Asp Glu Leu Pro Glu
35 40 45
Glu Thr His His Ala Ala Leu Glu Asn Tyr Arg Ala Lys Arg Ala Thr
50 55 60
Cys Asp Leu Ala Ser Gly Phe Gly Val Gly Ser Ser Leu Cys Ala Ala
65 70 75 80
His Cys Ile Ala Arg Arg Tyr Arg Gly Gly Tyr Cys Asn Ser Lys Ala
85 90 95
Val Cys Val Cys Arg Asn
100
<210> 59
<211> 70
<212> БЕЛОК
<213> Drosophila melanogaster
<400> 59
Met Met Gln Ile Lys Tyr Leu Phe Ala Leu Phe Ala Val Leu Met Leu
1 5 10 15
Val Val Leu Gly Ala Asn Glu Ala Asp Ala Asp Cys Leu Ser Gly Arg
20 25 30
Tyr Lys Gly Pro Cys Ala Val Trp Asp Asn Glu Thr Cys Arg Arg Val
35 40 45
Cys Lys Glu Glu Gly Arg Ser Ser Gly His Cys Ser Pro Ser Leu Lys
50 55 60
Cys Trp Cys Glu Gly Cys
65 70
<210> 60
<211> 63
<212> БЕЛОК
<213> Medicago truncatula
<400> 60
Met Thr Lys Ile Val Val Phe Ile Tyr Val Val Ile Leu Leu Leu Thr
1 5 10 15
Ile Phe His Val Ser Ala Lys Lys Lys Arg Tyr Ile Glu Cys Glu Thr
20 25 30
His Glu Asp Cys Ser Gln Val Phe Met Pro Pro Phe Val Met Arg Cys
35 40 45
Val Ile His Glu Cys Lys Ile Phe Asn Gly Glu His Leu Arg Tyr
50 55 60
<210> 61
<211> 76
<212> БЕЛОК
<213> Medicago truncatula
<400> 61
Met Ala Lys Ile Met Lys Phe Val Tyr Asn Met Ile Pro Phe Leu Ser
1 5 10 15
Ile Phe Ile Ile Thr Leu Gln Val Asn Val Val Val Cys Glu Ile Asp
20 25 30
Ala Asp Cys Pro Gln Ile Cys Met Pro Pro Tyr Glu Val Arg Cys Val
35 40 45
Asn His Arg Cys Gly Trp Val Asn Thr Asp Asp Ser Leu Phe Leu Thr
50 55 60
Gln Glu Phe Thr Arg Ser Lys Gln Tyr Ile Ile Ser
65 70 75
<210> 62
<211> 76
<212> БЕЛОК
<213> Medicago truncatula
<400> 62
Met Tyr Lys Val Val Glu Ser Ile Phe Ile Arg Tyr Met His Arg Lys
1 5 10 15
Pro Asn Met Thr Lys Phe Phe Lys Phe Val Tyr Thr Met Phe Ile Leu
20 25 30
Ile Ser Leu Phe Leu Val Val Thr Asn Ala Asn Ala His Asn Cys Thr
35 40 45
Asp Ile Ser Asp Cys Ser Ser Asn His Cys Ser Tyr Glu Gly Val Ser
50 55 60
Leu Cys Met Asn Gly Gln Cys Ile Cys Ile Tyr Glu
65 70 75
<210> 63
<211> 64
<212> БЕЛОК
<213> Medicago truncatula
<400> 63
Met Val Glu Thr Leu Arg Leu Phe Tyr Ile Met Ile Leu Phe Val Ser
1 5 10 15
Leu Cys Leu Val Val Val Asp Gly Glu Ser Lys Leu Glu Gln Thr Cys
20 25 30
Ser Glu Asp Phe Glu Cys Tyr Ile Lys Asn Pro His Val Pro Phe Gly
35 40 45
His Leu Arg Cys Phe Glu Gly Phe Cys Gln Gln Leu Asn Gly Pro Ala
50 55 60
<210> 64
<211> 67
<212> БЕЛОК
<213> Medicago truncatula
<400> 64
Met Ala Lys Ile Val Asn Phe Val Tyr Ser Met Ile Val Phe Leu Phe
1 5 10 15
Leu Phe Leu Val Ala Thr Lys Ala Ala Arg Gly Tyr Leu Cys Val Thr
20 25 30
Asp Ser His Cys Pro Pro His Met Cys Pro Pro Gly Met Glu Pro Arg
35 40 45
Cys Val Arg Arg Met Cys Lys Cys Leu Pro Ile Gly Trp Arg Lys Tyr
50 55 60
Phe Val Pro
65
<210> 65
<211> 96
<212> БЕЛОК
<213> Medicago truncatula
<400> 65
Met Gln Ile Gly Lys Asn Met Val Glu Thr Pro Lys Leu Asp Tyr Val
1 5 10 15
Ile Ile Phe Phe Phe Leu Tyr Phe Phe Phe Arg Gln Met Ile Ile Leu
20 25 30
Arg Leu Asn Thr Thr Phe Arg Pro Leu Asn Phe Lys Met Leu Arg Phe
35 40 45
Trp Gly Gln Asn Arg Asn Ile Met Lys His Arg Gly Gln Lys Val His
50 55 60
Phe Ser Leu Ile Leu Ser Asp Cys Lys Thr Asn Lys Asp Cys Pro Lys
65 70 75 80
Leu Arg Arg Ala Asn Val Arg Cys Arg Lys Ser Tyr Cys Val Pro Ile
85 90 95
<210> 66
<211> 65
<212> БЕЛОК
<213> Medicago truncatula
<400> 66
Met Leu Arg Leu Tyr Leu Val Ser Tyr Phe Leu Leu Lys Arg Thr Leu
1 5 10 15
Leu Val Ser Tyr Phe Ser Tyr Phe Ser Thr Tyr Ile Ile Glu Cys Lys
20 25 30
Thr Asp Asn Asp Cys Pro Ile Ser Gln Leu Lys Ile Tyr Ala Trp Lys
35 40 45
Cys Val Lys Asn Gly Cys His Leu Phe Asp Val Ile Pro Met Met Tyr
50 55 60
Glu
65
<210> 67
<211> 79
<212> БЕЛОК
<213> Medicago truncatula
<400> 67
Met Ala Glu Ile Leu Lys Phe Val Tyr Ile Val Ile Leu Phe Val Ser
1 5 10 15
Leu Leu Leu Ile Val Val Ala Ser Glu Arg Glu Cys Val Thr Asp Asp
20 25 30
Asp Cys Glu Lys Leu Tyr Pro Thr Asn Glu Tyr Arg Met Met Cys Asp
35 40 45
Ser Gly Tyr Cys Met Asn Leu Leu Asn Gly Lys Ile Ile Tyr Leu Leu
50 55 60
Cys Leu Lys Lys Lys Lys Phe Leu Ile Ile Ile Ser Val Leu Leu
65 70 75
<210> 68
<211> 95
<212> БЕЛОК
<213> Medicago truncatula
<400> 68
Met Ala Glu Ile Ile Lys Phe Val Tyr Ile Met Ile Leu Cys Val Ser
1 5 10 15
Leu Leu Leu Ile Glu Val Ala Gly Glu Glu Cys Val Thr Asp Ala Asp
20 25 30
Cys Asp Lys Leu Tyr Pro Asp Ile Arg Lys Pro Leu Met Cys Ser Ile
35 40 45
Gly Glu Cys Tyr Ser Leu Tyr Lys Gly Lys Phe Ser Leu Ser Ile Ile
50 55 60
Ser Lys Thr Ser Phe Ser Leu Met Val Tyr Asn Val Val Thr Leu Val
65 70 75 80
Ile Cys Leu Arg Leu Ala Tyr Ile Ser Leu Leu Leu Lys Phe Leu
85 90 95
<210> 69
<211> 100
<212> БЕЛОК
<213> Medicago truncatula
<400> 69
Met Ala Glu Ile Leu Lys Asp Phe Tyr Ala Met Asn Leu Phe Ile Phe
1 5 10 15
Leu Ile Ile Leu Pro Ala Lys Ile Arg Gly Glu Thr Leu Ser Leu Thr
20 25 30
His Pro Lys Cys His His Ile Met Leu Pro Ser Leu Phe Ile Thr Glu
35 40 45
Val Phe Gln Arg Val Thr Asp Asp Gly Cys Pro Lys Pro Val Asn His
50 55 60
Leu Arg Val Val Lys Cys Ile Glu His Ile Cys Glu Tyr Gly Tyr Asn
65 70 75 80
Tyr Arg Pro Asp Phe Ala Ser Gln Ile Pro Glu Ser Thr Lys Met Pro
85 90 95
Arg Lys Arg Glu
100
<210> 70
<211> 78
<212> БЕЛОК
<213> Medicago truncatula
<400> 70
Met Val Glu Ile Leu Lys Asn Phe Tyr Ala Met Asn Leu Phe Ile Phe
1 5 10 15
Leu Ile Ile Leu Ala Val Lys Ile Arg Gly Ala His Phe Pro Cys Val
20 25 30
Thr Asp Asp Asp Cys Pro Lys Pro Val Asn Lys Leu Arg Val Ile Lys
35 40 45
Cys Ile Asp His Ile Cys Gln Tyr Ala Arg Asn Leu Pro Asp Phe Ala
50 55 60
Ser Glu Ile Ser Glu Ser Thr Lys Met Pro Cys Lys Gly Glu
65 70 75
<210> 71
<211> 72
<212> БЕЛОК
<213> Medicago truncatula
<400> 71
Met Phe His Ala Gln Ala Glu Asn Met Ala Lys Val Ser Asn Phe Val
1 5 10 15
Cys Ile Met Ile Leu Phe Leu Ala Leu Phe Phe Ile Thr Met Asn Asp
20 25 30
Ala Ala Arg Phe Glu Cys Arg Glu Asp Ser His Cys Val Thr Arg Ile
35 40 45
Lys Cys Val Leu Pro Arg Lys Pro Glu Cys Arg Asn Tyr Ala Cys Gly
50 55 60
Cys Tyr Asp Ser Asn Lys Tyr Arg
65 70
<210> 72
<211> 78
<212> БЕЛОК
<213> Medicago truncatula
<400> 72
Met Gln Met Arg Gln Asn Met Ala Thr Ile Leu Asn Phe Val Phe Val
1 5 10 15
Ile Ile Leu Phe Ile Ser Leu Leu Leu Val Val Thr Lys Gly Tyr Arg
20 25 30
Glu Pro Phe Ser Ser Phe Thr Glu Gly Pro Thr Cys Lys Glu Asp Ile
35 40 45
Asp Cys Pro Ser Ile Ser Cys Val Asn Pro Gln Val Pro Lys Cys Ile
50 55 60
Met Phe Glu Cys His Cys Lys Tyr Ile Pro Thr Thr Leu Lys
65 70 75
<210> 73
<211> 71
<212> БЕЛОК
<213> Medicago truncatula
<400> 73
Met Ala Thr Ile Leu Met Tyr Val Tyr Ile Thr Ile Leu Phe Ile Ser
1 5 10 15
Ile Leu Thr Val Leu Thr Glu Gly Leu Tyr Glu Pro Leu Tyr Asn Phe
20 25 30
Arg Arg Asp Pro Asp Cys Arg Arg Asn Ile Asp Cys Pro Ser Tyr Leu
35 40 45
Cys Val Ala Pro Lys Val Pro Arg Cys Ile Met Phe Glu Cys His Cys
50 55 60
Lys Asp Ile Pro Ser Asp His
65 70
<210> 74
<211> 57
<212> БЕЛОК
<213> Medicago truncatula
<400> 74
Met Thr Thr Ser Leu Lys Phe Val Tyr Val Ala Ile Leu Phe Leu Ser
1 5 10 15
Leu Leu Leu Val Val Met Gly Gly Ile Arg Arg Phe Glu Cys Arg Gln
20 25 30
Asp Ser Asp Cys Pro Ser Tyr Phe Cys Glu Lys Leu Thr Val Pro Lys
35 40 45
Cys Phe Trp Ser Lys Cys Tyr Cys Lys
50 55
<210> 75
<211> 57
<212> БЕЛОК
<213> Medicago truncatula
<400> 75
Met Thr Thr Ser Leu Lys Phe Val Tyr Val Ala Ile Leu Phe Leu Ser
1 5 10 15
Leu Leu Leu Val Val Met Gly Gly Ile Arg Lys Lys Glu Cys Arg Gln
20 25 30
Asp Ser Asp Cys Pro Ser Tyr Phe Cys Glu Lys Leu Thr Ile Ala Lys
35 40 45
Cys Ile His Ser Thr Cys Leu Cys Lys
50 55
<210> 76
<211> 66
<212> БЕЛОК
<213> Medicago truncatula
<400> 76
Met Gln Ile Gly Lys Asn Met Val Glu Thr Pro Lys Leu Val Tyr Phe
1 5 10 15
Ile Ile Leu Phe Leu Ser Ile Phe Leu Cys Ile Thr Val Ser Asn Ser
20 25 30
Ser Phe Ser Gln Ile Phe Asn Ser Ala Cys Lys Thr Asp Lys Asp Cys
35 40 45
Pro Lys Phe Gly Arg Val Asn Val Arg Cys Arg Lys Gly Asn Cys Val
50 55 60
Pro Ile
65
<210> 77
<211> 57
<212> БЕЛОК
<213> Medicago truncatula
<400> 77
Met Thr Ala Ile Leu Lys Lys Phe Ile Asn Ala Val Phe Leu Phe Ile
1 5 10 15
Val Leu Phe Leu Ala Thr Thr Asn Val Glu Asp Phe Val Gly Gly Ser
20 25 30
Asn Asp Glu Cys Val Tyr Pro Asp Val Phe Gln Cys Ile Asn Asn Ile
35 40 45
Cys Lys Cys Val Ser His His Arg Thr
50 55
<210> 78
<211> 74
<212> БЕЛОК
<213> Medicago truncatula
<400> 78
Met Gln Lys Arg Lys Asn Met Ala Gln Ile Ile Phe Tyr Val Tyr Ala
1 5 10 15
Leu Ile Ile Leu Phe Ser Pro Phe Leu Ala Ala Arg Leu Val Phe Val
20 25 30
Asn Pro Glu Lys Pro Cys Val Thr Asp Ala Asp Cys Asp Arg Tyr Arg
35 40 45
His Glu Ser Ala Ile Tyr Ser Asp Met Phe Cys Lys Asp Gly Tyr Cys
50 55 60
Phe Ile Asp Tyr His His Asp Pro Tyr Pro
65 70
<210> 79
<211> 76
<212> БЕЛОК
<213> Medicago truncatula
<400> 79
Met Gln Met Arg Lys Asn Met Ala Gln Ile Leu Phe Tyr Val Tyr Ala
1 5 10 15
Leu Leu Ile Leu Phe Thr Pro Phe Leu Val Ala Arg Ile Met Val Val
20 25 30
Asn Pro Asn Asn Pro Cys Val Thr Asp Ala Asp Cys Gln Arg Tyr Arg
35 40 45
His Lys Leu Ala Thr Arg Met Ile Cys Asn Gln Gly Phe Cys Leu Met
50 55 60
Asp Phe Thr His Asp Pro Tyr Ala Pro Ser Leu Pro
65 70 75
<210> 80
<211> 64
<212> БЕЛОК
<213> Medicago truncatula
<400> 80
Met Asn His Ile Ser Lys Phe Val Tyr Ala Leu Ile Ile Phe Leu Ser
1 5 10 15
Ile Tyr Leu Val Val Leu Asp Gly Leu Pro Ile Ser Cys Lys Asp His
20 25 30
Phe Glu Cys Arg Arg Lys Ile Asn Ile Leu Arg Cys Ile Tyr Arg Gln
35 40 45
Glu Lys Pro Met Cys Ile Asn Ser Ile Cys Thr Cys Val Lys Leu Leu
50 55 60
<210> 81
<211> 67
<212> БЕЛОК
<213> Medicago truncatula
<400> 81
Met Gln Arg Glu Lys Asn Met Ala Lys Ile Phe Glu Phe Val Tyr Ala
1 5 10 15
Met Ile Ile Phe Ile Leu Leu Phe Leu Val Glu Lys Asn Val Val Ala
20 25 30
Tyr Leu Lys Phe Glu Cys Lys Thr Asp Asp Asp Cys Gln Lys Ser Leu
35 40 45
Leu Lys Thr Tyr Val Trp Lys Cys Val Lys Asn Glu Cys Tyr Phe Phe
50 55 60
Ala Lys Lys
65
<210> 82
<211> 61
<212> БЕЛОК
<213> Medicago truncatula
<400> 82
Met Ala Gly Ile Ile Lys Phe Val His Val Leu Ile Ile Phe Leu Ser
1 5 10 15
Leu Phe His Val Val Lys Asn Asp Asp Gly Ser Phe Cys Phe Lys Asp
20 25 30
Ser Asp Cys Pro Asp Glu Met Cys Pro Ser Pro Leu Lys Glu Met Cys
35 40 45
Tyr Phe Leu Gln Cys Lys Cys Gly Val Asp Thr Ile Ala
50 55 60
<210> 83
<211> 59
<212> БЕЛОК
<213> Medicago truncatula
<400> 83
Met Ala Asn Thr His Lys Leu Val Ser Met Ile Leu Phe Ile Phe Leu
1 5 10 15
Phe Leu Ala Ser Asn Asn Val Glu Gly Tyr Val Asn Cys Glu Thr Asp
20 25 30
Ala Asp Cys Pro Pro Ser Thr Arg Val Lys Arg Phe Lys Cys Val Lys
35 40 45
Gly Glu Cys Arg Trp Thr Arg Met Ser Tyr Ala
50 55
<210> 84
<211> 63
<212> БЕЛОК
<213> Medicago truncatula
<400> 84
Met Gln Arg Arg Lys Lys Lys Ala Gln Val Val Met Phe Val His Asp
1 5 10 15
Leu Ile Ile Cys Ile Tyr Leu Phe Ile Val Ile Thr Thr Arg Lys Thr
20 25 30
Asp Ile Arg Cys Arg Phe Tyr Tyr Asp Cys Pro Arg Leu Glu Tyr His
35 40 45
Phe Cys Glu Cys Ile Glu Asp Phe Cys Ala Tyr Ile Arg Leu Asn
50 55 60
<210> 85
<211> 57
<212> БЕЛОК
<213> Medicago truncatula
<400> 85
Met Ala Lys Val Tyr Met Phe Val Tyr Ala Leu Ile Ile Phe Val Ser
1 5 10 15
Pro Phe Leu Leu Ala Thr Phe Arg Thr Arg Leu Pro Cys Glu Lys Asp
20 25 30
Asp Asp Cys Pro Glu Ala Phe Leu Pro Pro Val Met Lys Cys Val Asn
35 40 45
Arg Phe Cys Gln Tyr Glu Ile Leu Glu
50 55
<210> 86
<211> 77
<212> БЕЛОК
<213> Medicago truncatula
<400> 86
Met Ile Lys Gln Phe Ser Val Cys Tyr Ile Gln Met Arg Arg Asn Met
1 5 10 15
Thr Thr Ile Leu Lys Phe Pro Tyr Ile Met Val Ile Cys Leu Leu Leu
20 25 30
Leu His Val Ala Ala Tyr Glu Asp Phe Glu Lys Glu Ile Phe Asp Cys
35 40 45
Lys Lys Asp Gly Asp Cys Asp His Met Cys Val Thr Pro Gly Ile Pro
50 55 60
Lys Cys Thr Gly Tyr Val Cys Phe Cys Phe Glu Asn Leu
65 70 75
<210> 87
<211> 73
<212> БЕЛОК
<213> Medicago truncatula
<400> 87
Met Gln Arg Ser Arg Asn Met Thr Thr Ile Phe Lys Phe Ala Tyr Ile
1 5 10 15
Met Ile Ile Cys Val Phe Leu Leu Asn Ile Ala Ala Gln Glu Ile Glu
20 25 30
Asn Gly Ile His Pro Cys Lys Lys Asn Glu Asp Cys Asn His Met Cys
35 40 45
Val Met Pro Gly Leu Pro Trp Cys His Glu Asn Asn Leu Cys Phe Cys
50 55 60
Tyr Glu Asn Ala Tyr Gly Asn Thr Arg
65 70
<210> 88
<211> 85
<212> БЕЛОК
<213> Medicago truncatula
<400> 88
Met Thr Ile Ile Ile Lys Phe Val Asn Val Leu Ile Ile Phe Leu Ser
1 5 10 15
Leu Phe His Val Ala Lys Asn Asp Asp Asn Lys Leu Leu Leu Ser Phe
20 25 30
Ile Glu Glu Gly Phe Leu Cys Phe Lys Asp Ser Asp Cys Pro Tyr Asn
35 40 45
Met Cys Pro Ser Pro Leu Lys Glu Met Cys Tyr Phe Ile Lys Cys Val
50 55 60
Cys Gly Val Tyr Gly Pro Ile Arg Glu Arg Arg Leu Tyr Gln Ser His
65 70 75 80
Asn Pro Met Ile Gln
85
<210> 89
<211> 69
<212> БЕЛОК
<213> Medicago truncatula
<400> 89
Met Arg Lys Asn Met Thr Lys Ile Leu Met Ile Gly Tyr Ala Leu Met
1 5 10 15
Ile Phe Ile Phe Leu Ser Ile Ala Val Ser Ile Thr Gly Asn Leu Ala
20 25 30
Arg Ala Ser Arg Lys Lys Pro Val Asp Val Ile Pro Cys Ile Tyr Asp
35 40 45
His Asp Cys Pro Arg Lys Leu Tyr Phe Leu Glu Arg Cys Val Gly Arg
50 55 60
Val Cys Lys Tyr Leu
65
<210> 90
<211> 58
<212> БЕЛОК
<213> Medicago truncatula
<400> 90
Met Ala His Lys Leu Val Tyr Ala Ile Thr Leu Phe Ile Phe Leu Phe
1 5 10 15
Leu Ile Ala Asn Asn Ile Glu Asp Asp Ile Phe Cys Ile Thr Asp Asn
20 25 30
Asp Cys Pro Pro Asn Thr Leu Val Gln Arg Tyr Arg Cys Ile Asn Gly
35 40 45
Lys Cys Asn Leu Ser Phe Val Ser Tyr Gly
50 55
<210> 91
<211> 61
<212> БЕЛОК
<213> Medicago truncatula
<400> 91
Met Asp Glu Thr Leu Lys Phe Val Tyr Ile Leu Ile Leu Phe Val Ser
1 5 10 15
Leu Cys Leu Val Val Ala Asp Gly Val Lys Asn Ile Asn Arg Glu Cys
20 25 30
Thr Gln Thr Ser Asp Cys Tyr Lys Lys Tyr Pro Phe Ile Pro Trp Gly
35 40 45
Lys Val Arg Cys Val Lys Gly Arg Cys Arg Leu Asp Met
50 55 60
<210> 92
<211> 62
<212> БЕЛОК
<213> Medicago truncatula
<400> 92
Met Ala Lys Ile Ile Lys Phe Val Tyr Val Leu Ala Ile Phe Phe Ser
1 5 10 15
Leu Phe Leu Val Ala Lys Asn Val Asn Gly Trp Thr Cys Val Glu Asp
20 25 30
Ser Asp Cys Pro Ala Asn Ile Cys Gln Pro Pro Met Gln Arg Met Cys
35 40 45
Phe Tyr Gly Glu Cys Ala Cys Val Arg Ser Lys Phe Cys Thr
50 55 60
<210> 93
<211> 61
<212> БЕЛОК
<213> Medicago truncatula
<400> 93
Met Val Lys Ile Ile Lys Phe Val Tyr Phe Met Thr Leu Phe Leu Ser
1 5 10 15
Met Leu Leu Val Thr Thr Lys Glu Asp Gly Ser Val Glu Cys Ile Ala
20 25 30
Asn Ile Asp Cys Pro Gln Ile Phe Met Leu Pro Phe Val Met Arg Cys
35 40 45
Ile Asn Phe Arg Cys Gln Ile Val Asn Ser Glu Asp Thr
50 55 60
<210> 94
<211> 67
<212> БЕЛОК
<213> Medicago truncatula
<400> 94
Met Asp Glu Ile Leu Lys Phe Val Tyr Thr Leu Ile Ile Phe Phe Ser
1 5 10 15
Leu Phe Phe Ala Ala Asn Asn Val Asp Ala Asn Ile Met Asn Cys Gln
20 25 30
Ser Thr Phe Asp Cys Pro Arg Asp Met Cys Ser His Ile Arg Asp Val
35 40 45
Ile Cys Ile Phe Lys Lys Cys Lys Cys Ala Gly Gly Arg Tyr Met Pro
50 55 60
Gln Val Pro
65
<210> 95
<211> 62
<212> БЕЛОК
<213> Medicago truncatula
<400> 95
Met Gln Arg Arg Lys Asn Met Ala Asn Asn His Met Leu Ile Tyr Ala
1 5 10 15
Met Ile Ile Cys Leu Phe Pro Tyr Leu Val Val Thr Phe Lys Thr Ala
20 25 30
Ile Thr Cys Asp Cys Asn Glu Asp Cys Leu Asn Phe Phe Thr Pro Leu
35 40 45
Asp Asn Leu Lys Cys Ile Asp Asn Val Cys Glu Val Phe Met
50 55 60
<210> 96
<211> 65
<212> БЕЛОК
<213> Medicago truncatula
<400> 96
Met Val Asn Ile Leu Lys Phe Ile Tyr Val Ile Ile Phe Phe Ile Leu
1 5 10 15
Met Phe Phe Val Leu Ile Asp Val Asp Gly His Val Leu Val Glu Cys
20 25 30
Ile Glu Asn Arg Asp Cys Glu Lys Gly Met Cys Lys Phe Pro Phe Ile
35 40 45
Val Arg Cys Leu Met Asp Gln Cys Lys Cys Val Arg Ile His Asn Leu
50 55 60
Ile
65
<210> 97
<211> 74
<212> БЕЛОК
<213> Medicago truncatula
<400> 97
Met Ile Ile Gln Phe Ser Ile Tyr Tyr Met Gln Arg Arg Lys Leu Asn
1 5 10 15
Met Val Glu Ile Leu Lys Phe Ser His Ala Leu Ile Ile Phe Leu Phe
20 25 30
Leu Ser Ala Leu Val Thr Asn Ala Asn Ile Phe Phe Cys Ser Thr Asp
35 40 45
Glu Asp Cys Thr Trp Asn Leu Cys Arg Gln Pro Trp Val Gln Lys Cys
50 55 60
Arg Leu His Met Cys Ser Cys Glu Lys Asn
65 70
<210> 98
<211> 58
<212> БЕЛОК
<213> Medicago truncatula
<400> 98
Met Asp Glu Val Phe Lys Phe Val Tyr Val Met Ile Ile Phe Pro Phe
1 5 10 15
Leu Ile Leu Asp Val Ala Thr Asn Ala Glu Lys Ile Arg Arg Cys Phe
20 25 30
Asn Asp Ala His Cys Pro Pro Asp Met Cys Thr Leu Gly Val Ile Pro
35 40 45
Lys Cys Ser Arg Phe Thr Ile Cys Ile Cys
50 55
<210> 99
<211> 64
<212> БЕЛОК
<213> Medicago truncatula
<400> 99
Met His Arg Lys Pro Asn Met Thr Lys Phe Phe Lys Phe Val Tyr Thr
1 5 10 15
Met Phe Ile Leu Ile Ser Leu Phe Leu Val Val Thr Asn Ala Asn Ala
20 25 30
Asn Asn Cys Thr Asp Thr Ser Asp Cys Ser Ser Asn His Cys Ser Tyr
35 40 45
Glu Gly Val Ser Leu Cys Met Asn Gly Gln Cys Ile Cys Ile Tyr Glu
50 55 60
<210> 100
<211> 69
<212> БЕЛОК
<213> Medicago truncatula
<400> 100
Met Gln Met Lys Lys Met Ala Thr Ile Leu Lys Phe Val Tyr Leu Ile
1 5 10 15
Ile Leu Leu Ile Tyr Pro Leu Leu Val Val Thr Glu Glu Ser His Tyr
20 25 30
Met Lys Phe Ser Ile Cys Lys Asp Asp Thr Asp Cys Pro Thr Leu Phe
35 40 45
Cys Val Leu Pro Asn Val Pro Lys Cys Ile Gly Ser Lys Cys His Cys
50 55 60
Lys Leu Met Val Asn
65
<210> 101
<211> 64
<212> БЕЛОК
<213> Medicago truncatula
<400> 101
Met Val Glu Thr Leu Arg Leu Phe Tyr Ile Met Ile Leu Phe Val Ser
1 5 10 15
Leu Tyr Leu Val Val Val Asp Gly Val Ser Lys Leu Ala Gln Ser Cys
20 25 30
Ser Glu Asp Phe Glu Cys Tyr Ile Lys Asn Pro His Ala Pro Phe Gly
35 40 45
Gln Leu Arg Cys Phe Glu Gly Tyr Cys Gln Arg Leu Asp Lys Pro Thr
50 55 60
<210> 102
<211> 63
<212> БЕЛОК
<213> Medicago truncatula
<400> 102
Met Thr Thr Phe Leu Lys Val Ala Tyr Ile Met Ile Ile Cys Val Phe
1 5 10 15
Val Leu His Leu Ala Ala Gln Val Asp Ser Gln Lys Arg Leu His Gly
20 25 30
Cys Lys Glu Asp Arg Asp Cys Asp Asn Ile Cys Ser Val His Ala Val
35 40 45
Thr Lys Cys Ile Gly Asn Met Cys Arg Cys Leu Ala Asn Val Lys
50 55 60
<210> 103
<211> 61
<212> БЕЛОК
<213> Medicago truncatula
<400> 103
Met Arg Ile Asn Arg Thr Pro Ala Ile Phe Lys Phe Val Tyr Thr Ile
1 5 10 15
Ile Ile Tyr Leu Phe Leu Leu Arg Val Val Ala Lys Asp Leu Pro Phe
20 25 30
Asn Ile Cys Glu Lys Asp Glu Asp Cys Leu Glu Phe Cys Ala His Asp
35 40 45
Lys Val Ala Lys Cys Met Leu Asn Ile Cys Phe Cys Phe
50 55 60
<210> 104
<211> 54
<212> БЕЛОК
<213> Medicago truncatula
<400> 104
Met Ala Glu Ile Leu Lys Ile Leu Tyr Val Phe Ile Ile Phe Leu Ser
1 5 10 15
Leu Ile Leu Ala Val Ile Ser Gln His Pro Phe Thr Pro Cys Glu Thr
20 25 30
Asn Ala Asp Cys Lys Cys Arg Asn His Lys Arg Pro Asp Cys Leu Trp
35 40 45
His Lys Cys Tyr Cys Tyr
50
<210> 105
<211> 65
<212> БЕЛОК
<213> Medicago truncatula
<400> 105
Met Arg Lys Ser Met Ala Thr Ile Leu Lys Phe Val Tyr Val Ile Met
1 5 10 15
Leu Phe Ile Tyr Ser Leu Phe Val Ile Glu Ser Phe Gly His Arg Phe
20 25 30
Leu Ile Tyr Asn Asn Cys Lys Asn Asp Thr Glu Cys Pro Asn Asp Cys
35 40 45
Gly Pro His Glu Gln Ala Lys Cys Ile Leu Tyr Ala Cys Tyr Cys Val
50 55 60
Glu
65
<210> 106
<211> 58
<212> БЕЛОК
<213> Medicago truncatula
<400> 106
Met Asn Thr Ile Leu Lys Phe Ile Phe Val Val Phe Leu Phe Leu Ser
1 5 10 15
Ile Phe Leu Ser Ala Gly Asn Ser Lys Ser Tyr Gly Pro Cys Thr Thr
20 25 30
Leu Gln Asp Cys Glu Thr His Asn Trp Phe Glu Val Cys Ser Cys Ile
35 40 45
Asp Phe Glu Cys Lys Cys Trp Ser Leu Leu
50 55
<210> 107
<211> 64
<212> БЕЛОК
<213> Medicago truncatula
<400> 107
Met Ala Glu Ile Ile Lys Phe Val Tyr Ile Met Ile Leu Cys Val Ser
1 5 10 15
Leu Leu Leu Ile Ala Glu Ala Ser Gly Lys Glu Cys Val Thr Asp Ala
20 25 30
Asp Cys Glu Asn Leu Tyr Pro Gly Asn Lys Lys Pro Met Phe Cys Asn
35 40 45
Asn Thr Gly Tyr Cys Met Ser Leu Tyr Lys Glu Pro Ser Arg Tyr Met
50 55 60
<210> 108
<211> 64
<212> БЕЛОК
<213> Medicago truncatula
<400> 108
Met Ala Lys Ile Ile Lys Phe Val Tyr Ile Met Ile Leu Cys Val Ser
1 5 10 15
Leu Leu Leu Ile Val Glu Ala Gly Gly Lys Glu Cys Val Thr Asp Val
20 25 30
Asp Cys Glu Lys Ile Tyr Pro Gly Asn Lys Lys Pro Leu Ile Cys Ser
35 40 45
Thr Gly Tyr Cys Tyr Ser Leu Tyr Glu Glu Pro Pro Arg Tyr His Lys
50 55 60
<210> 109
<211> 64
<212> БЕЛОК
<213> Medicago truncatula
<400> 109
Met Ala Lys Val Thr Lys Phe Gly Tyr Ile Ile Ile His Phe Leu Ser
1 5 10 15
Leu Phe Phe Leu Ala Met Asn Val Ala Gly Gly Arg Glu Cys His Ala
20 25 30
Asn Ser His Cys Val Gly Lys Ile Thr Cys Val Leu Pro Gln Lys Pro
35 40 45
Glu Cys Trp Asn Tyr Ala Cys Val Cys Tyr Asp Ser Asn Lys Tyr Arg
50 55 60
<210> 110
<211> 55
<212> БЕЛОК
<213> Medicago truncatula
<400> 110
Met Ala Lys Ile Phe Asn Tyr Val Tyr Ala Leu Ile Met Phe Leu Ser
1 5 10 15
Leu Phe Leu Met Gly Thr Ser Gly Met Lys Asn Gly Cys Lys His Thr
20 25 30
Gly His Cys Pro Arg Lys Met Cys Gly Ala Lys Thr Thr Lys Cys Arg
35 40 45
Asn Asn Lys Cys Gln Cys Val
50 55
<210> 111
<211> 69
<212> БЕЛОК
<213> Medicago truncatula
<400> 111
Met Thr Glu Ile Leu Lys Phe Val Cys Val Met Ile Ile Phe Ile Ser
1 5 10 15
Ser Phe Ile Val Ser Lys Ser Leu Asn Gly Gly Gly Lys Asp Lys Cys
20 25 30
Phe Arg Asp Ser Asp Cys Pro Lys His Met Cys Pro Ser Ser Leu Val
35 40 45
Ala Lys Cys Ile Asn Arg Leu Cys Arg Cys Arg Arg Pro Glu Leu Gln
50 55 60
Val Gln Leu Asn Pro
65
<210> 112
<211> 69
<212> БЕЛОК
<213> Medicago truncatula
<400> 112
Met Ala His Ile Ile Met Phe Val Tyr Ala Leu Ile Tyr Ala Leu Ile
1 5 10 15
Ile Phe Ser Ser Leu Phe Val Arg Asp Gly Ile Pro Cys Leu Ser Asp
20 25 30
Asp Glu Cys Pro Glu Met Ser His Tyr Ser Phe Lys Cys Asn Asn Lys
35 40 45
Ile Cys Glu Tyr Asp Leu Gly Glu Met Ser Asp Asp Asp Tyr Tyr Leu
50 55 60
Glu Met Ser Arg Glu
65
<210> 113
<211> 77
<212> БЕЛОК
<213> Medicago truncatula
<400> 113
Met Tyr Arg Glu Lys Asn Met Ala Lys Thr Leu Lys Phe Val Tyr Val
1 5 10 15
Ile Val Leu Phe Leu Ser Leu Phe Leu Ala Ala Lys Asn Ile Asp Gly
20 25 30
Arg Val Ser Tyr Asn Ser Phe Ile Ala Leu Pro Val Cys Gln Thr Ala
35 40 45
Ala Asp Cys Pro Glu Gly Thr Arg Gly Arg Thr Tyr Lys Cys Ile Asn
50 55 60
Asn Lys Cys Arg Tyr Pro Lys Leu Leu Lys Pro Ile Gln
65 70 75
<210> 114
<211> 56
<212> БЕЛОК
<213> Medicago truncatula
<400> 114
Met Ala His Ile Phe Asn Tyr Val Tyr Ala Leu Leu Val Phe Leu Ser
1 5 10 15
Leu Phe Leu Met Val Thr Asn Gly Ile His Ile Gly Cys Asp Lys Asp
20 25 30
Arg Asp Cys Pro Lys Gln Met Cys His Leu Asn Gln Thr Pro Lys Cys
35 40 45
Leu Lys Asn Ile Cys Lys Cys Val
50 55
<210> 115
<211> 77
<212> БЕЛОК
<213> Medicago truncatula
<400> 115
Met Ala Glu Ile Leu Lys Cys Phe Tyr Thr Met Asn Leu Phe Ile Phe
1 5 10 15
Leu Ile Ile Leu Pro Ala Lys Ile Arg Glu His Ile Gln Cys Val Ile
20 25 30
Asp Asp Asp Cys Pro Lys Ser Leu Asn Lys Leu Leu Ile Ile Lys Cys
35 40 45
Ile Asn His Val Cys Gln Tyr Val Gly Asn Leu Pro Asp Phe Ala Ser
50 55 60
Gln Ile Pro Lys Ser Thr Lys Met Pro Tyr Lys Gly Glu
65 70 75
<210> 116
<211> 70
<212> БЕЛОК
<213> Medicago truncatula
<400> 116
Met Ala Tyr Ile Ser Arg Ile Phe Tyr Val Leu Ile Ile Phe Leu Ser
1 5 10 15
Leu Phe Phe Val Val Ile Asn Gly Val Lys Ser Leu Leu Leu Ile Lys
20 25 30
Val Arg Ser Phe Ile Pro Cys Gln Arg Ser Asp Asp Cys Pro Arg Asn
35 40 45
Leu Cys Val Asp Gln Ile Ile Pro Thr Cys Val Trp Ala Lys Cys Lys
50 55 60
Cys Lys Asn Tyr Asn Asp
65 70
<210> 117
<211> 64
<212> БЕЛОК
<213> Medicago truncatula
<400> 117
Met Ala Asn Val Thr Lys Phe Val Tyr Ile Ala Ile Tyr Phe Leu Ser
1 5 10 15
Leu Phe Phe Ile Ala Lys Asn Asp Ala Thr Ala Thr Phe Cys His Asp
20 25 30
Asp Ser His Cys Val Thr Lys Ile Lys Cys Val Leu Pro Arg Thr Pro
35 40 45
Gln Cys Arg Asn Glu Ala Cys Gly Cys Tyr His Ser Asn Lys Phe Arg
50 55 60
<210> 118
<211> 62
<212> БЕЛОК
<213> Medicago truncatula
<400> 118
Met Gly Glu Ile Met Lys Phe Val Tyr Val Met Ile Ile Tyr Leu Phe
1 5 10 15
Met Phe Asn Val Ala Thr Gly Ser Glu Phe Ile Phe Thr Lys Lys Leu
20 25 30
Thr Ser Cys Asp Ser Ser Lys Asp Cys Arg Ser Phe Leu Cys Tyr Ser
35 40 45
Pro Lys Phe Pro Val Cys Lys Arg Gly Ile Cys Glu Cys Ile
50 55 60
<210> 119
<211> 61
<212> БЕЛОК
<213> Medicago truncatula
<400> 119
Met Gly Glu Met Phe Lys Phe Ile Tyr Thr Phe Ile Leu Phe Val His
1 5 10 15
Leu Phe Leu Val Val Ile Phe Glu Asp Ile Gly His Ile Lys Tyr Cys
20 25 30
Gly Ile Val Asp Asp Cys Tyr Lys Ser Lys Lys Pro Leu Phe Lys Ile
35 40 45
Trp Lys Cys Val Glu Asn Val Cys Val Leu Trp Tyr Lys
50 55 60
<210> 120
<211> 63
<212> БЕЛОК
<213> Medicago truncatula
<400> 120
Met Ala Arg Thr Leu Lys Phe Val Tyr Ser Met Ile Leu Phe Leu Ser
1 5 10 15
Leu Phe Leu Val Ala Asn Gly Leu Lys Ile Phe Cys Ile Asp Val Ala
20 25 30
Asp Cys Pro Lys Asp Leu Tyr Pro Leu Leu Tyr Lys Cys Ile Tyr Asn
35 40 45
Lys Cys Ile Val Phe Thr Arg Ile Pro Phe Pro Phe Asp Trp Ile
50 55 60
<210> 121
<211> 66
<212> БЕЛОК
<213> Medicago truncatula
<400> 121
Met Ala Asn Ile Thr Lys Phe Val Tyr Ile Ala Ile Leu Phe Leu Ser
1 5 10 15
Leu Phe Phe Ile Gly Met Asn Asp Ala Ala Ile Leu Glu Cys Arg Glu
20 25 30
Asp Ser His Cys Val Thr Lys Ile Lys Cys Val Leu Pro Arg Lys Pro
35 40 45
Glu Cys Arg Asn Asn Ala Cys Thr Cys Tyr Lys Gly Gly Phe Ser Phe
50 55 60
His His
65
<210> 122
<211> 68
<212> БЕЛОК
<213> Medicago truncatula
<400> 122
Met Gln Arg Val Lys Lys Met Ser Glu Thr Leu Lys Phe Val Tyr Val
1 5 10 15
Leu Ile Leu Phe Ile Ser Ile Phe His Val Val Ile Val Cys Asp Ser
20 25 30
Ile Tyr Phe Pro Val Ser Arg Pro Cys Ile Thr Asp Lys Asp Cys Pro
35 40 45
Asn Met Lys His Tyr Lys Ala Lys Cys Arg Lys Gly Phe Cys Ile Ser
50 55 60
Ser Arg Val Arg
65
<210> 123
<211> 72
<212> БЕЛОК
<213> Medicago truncatula
<400> 123
Met Gln Ile Arg Lys Ile Met Ser Gly Val Leu Lys Phe Val Tyr Ala
1 5 10 15
Ile Ile Leu Phe Leu Phe Leu Phe Leu Val Ala Arg Glu Val Gly Gly
20 25 30
Leu Glu Thr Ile Glu Cys Glu Thr Asp Gly Asp Cys Pro Arg Ser Met
35 40 45
Ile Lys Met Trp Asn Lys Asn Tyr Arg His Lys Cys Ile Asp Gly Lys
50 55 60
Cys Glu Trp Ile Lys Lys Leu Pro
65 70
<210> 124
<211> 54
<212> БЕЛОК
<213> Medicago truncatula
<400> 124
Met Phe Val Tyr Asp Leu Ile Leu Phe Ile Ser Leu Ile Leu Val Val
1 5 10 15
Thr Gly Ile Asn Ala Glu Ala Asp Thr Ser Cys His Ser Phe Asp Asp
20 25 30
Cys Pro Trp Val Ala His His Tyr Arg Glu Cys Ile Glu Gly Leu Cys
35 40 45
Ala Tyr Arg Ile Leu Tyr
50
<210> 125
<211> 69
<212> БЕЛОК
<213> Medicago truncatula
<400> 125
Met Gln Arg Arg Lys Lys Ser Met Ala Lys Met Leu Lys Phe Phe Phe
1 5 10 15
Ala Ile Ile Leu Leu Leu Ser Leu Phe Leu Val Ala Thr Glu Val Gly
20 25 30
Gly Ala Tyr Ile Glu Cys Glu Val Asp Asp Asp Cys Pro Lys Pro Met
35 40 45
Lys Asn Ser His Pro Asp Thr Tyr Tyr Lys Cys Val Lys His Arg Cys
50 55 60
Gln Trp Ala Trp Lys
65
<210> 126
<211> 140
<212> БЕЛОК
<213> Medicago truncatula
<400> 126
Met Phe Val Tyr Thr Leu Ile Ile Phe Leu Phe Pro Ser His Val Ile
1 5 10 15
Thr Asn Lys Ile Ala Ile Tyr Cys Val Ser Asp Asp Asp Cys Leu Lys
20 25 30
Thr Phe Thr Pro Leu Asp Leu Lys Cys Val Asp Asn Val Cys Glu Phe
35 40 45
Asn Leu Arg Cys Lys Gly Lys Cys Gly Glu Arg Asp Glu Lys Phe Val
50 55 60
Phe Leu Lys Ala Leu Lys Lys Met Asp Gln Lys Leu Val Leu Glu Glu
65 70 75 80
Gln Gly Asn Ala Arg Glu Val Lys Ile Pro Lys Lys Leu Leu Phe Asp
85 90 95
Arg Ile Gln Val Pro Thr Pro Ala Thr Lys Asp Gln Val Glu Glu Asp
100 105 110
Asp Tyr Asp Asp Asp Asp Glu Glu Glu Glu Glu Glu Glu Asp Asp Val
115 120 125
Asp Met Trp Phe His Leu Pro Asp Val Val Cys His
130 135 140
<210> 127
<211> 60
<212> БЕЛОК
<213> Medicago truncatula
<400> 127
Met Ala Lys Phe Ser Met Phe Val Tyr Ala Leu Ile Asn Phe Leu Ser
1 5 10 15
Leu Phe Leu Val Glu Thr Ala Ile Thr Asn Ile Arg Cys Val Ser Asp
20 25 30
Asp Asp Cys Pro Lys Val Ile Lys Pro Leu Val Met Lys Cys Ile Gly
35 40 45
Asn Tyr Cys Tyr Phe Phe Met Ile Tyr Glu Gly Pro
50 55 60
<210> 128
<211> 58
<212> БЕЛОК
<213> Medicago truncatula
<400> 128
Met Ala His Lys Phe Val Tyr Ala Ile Ile Leu Phe Ile Phe Leu Phe
1 5 10 15
Leu Val Ala Lys Asn Val Lys Gly Tyr Val Val Cys Arg Thr Val Asp
20 25 30
Asp Cys Pro Pro Asp Thr Arg Asp Leu Arg Tyr Arg Cys Leu Asn Gly
35 40 45
Lys Cys Lys Ser Tyr Arg Leu Ser Tyr Gly
50 55
<210> 129
<211> 61
<212> БЕЛОК
<213> Medicago truncatula
<400> 129
Met Gln Arg Lys Lys Asn Met Gly Gln Ile Leu Ile Phe Val Phe Ala
1 5 10 15
Leu Ile Asn Phe Leu Ser Pro Ile Leu Val Glu Met Thr Thr Thr Thr
20 25 30
Ile Pro Cys Thr Phe Ile Asp Asp Cys Pro Lys Met Pro Leu Val Val
35 40 45
Lys Cys Ile Asp Asn Phe Cys Asn Tyr Phe Glu Ile Lys
50 55 60
<210> 130
<211> 57
<212> БЕЛОК
<213> Medicago truncatula
<400> 130
Met Ala Gln Thr Leu Met Leu Val Tyr Ala Leu Ile Ile Phe Thr Ser
1 5 10 15
Leu Phe Leu Val Val Ile Ser Arg Gln Thr Asp Ile Pro Cys Lys Ser
20 25 30
Asp Asp Ala Cys Pro Arg Val Ser Ser His His Ile Glu Cys Val Lys
35 40 45
Gly Phe Cys Thr Tyr Trp Lys Leu Asp
50 55
<210> 131
<211> 77
<212> БЕЛОК
<213> Medicago truncatula
<400> 131
Met Leu Arg Arg Lys Asn Thr Val Gln Ile Leu Met Phe Val Ser Ala
1 5 10 15
Leu Leu Ile Tyr Ile Phe Leu Phe Leu Val Ile Thr Ser Ser Ala Asn
20 25 30
Ile Pro Cys Asn Ser Asp Ser Asp Cys Pro Trp Lys Ile Tyr Tyr Thr
35 40 45
Tyr Arg Cys Asn Asp Gly Phe Cys Val Tyr Lys Ser Ile Asp Pro Ser
50 55 60
Thr Ile Pro Gln Tyr Met Thr Asp Leu Ile Phe Pro Arg
65 70 75
<210> 132
<211> 59
<212> БЕЛОК
<213> Medicago truncatula
<400> 132
Met Ala Val Ile Leu Lys Phe Val Tyr Ile Met Ile Ile Phe Leu Phe
1 5 10 15
Leu Leu Tyr Val Val Asn Gly Thr Arg Cys Asn Arg Asp Glu Asp Cys
20 25 30
Pro Phe Ile Cys Thr Gly Pro Gln Ile Pro Lys Cys Val Ser His Ile
35 40 45
Cys Phe Cys Leu Ser Ser Gly Lys Glu Ala Tyr
50 55
<210> 133
<211> 62
<212> БЕЛОК
<213> Medicago truncatula
<400> 133
Met Asp Ala Ile Leu Lys Phe Ile Tyr Ala Met Phe Leu Phe Leu Phe
1 5 10 15
Leu Phe Val Thr Thr Arg Asn Val Glu Ala Leu Phe Glu Cys Asn Arg
20 25 30
Asp Phe Val Cys Gly Asn Asp Asp Glu Cys Val Tyr Pro Tyr Ala Val
35 40 45
Gln Cys Ile His Arg Tyr Cys Lys Cys Leu Lys Ser Arg Asn
50 55 60
<210> 134
<211> 67
<212> БЕЛОК
<213> Medicago truncatula
<400> 134
Met Gln Ile Gly Arg Lys Lys Met Gly Glu Thr Pro Lys Leu Val Tyr
1 5 10 15
Val Ile Ile Leu Phe Leu Ser Ile Phe Leu Cys Thr Asn Ser Ser Phe
20 25 30
Ser Gln Met Ile Asn Phe Arg Gly Cys Lys Arg Asp Lys Asp Cys Pro
35 40 45
Gln Phe Arg Gly Val Asn Ile Arg Cys Arg Ser Gly Phe Cys Thr Pro
50 55 60
Ile Asp Ser
65
<210> 135
<211> 76
<212> БЕЛОК
<213> Medicago truncatula
<400> 135
Met Gln Met Arg Lys Asn Met Ala Gln Ile Leu Phe Tyr Val Tyr Ala
1 5 10 15
Leu Leu Ile Leu Phe Ser Pro Phe Leu Val Ala Arg Ile Met Val Val
20 25 30
Asn Pro Asn Asn Pro Cys Val Thr Asp Ala Asp Cys Gln Arg Tyr Arg
35 40 45
His Lys Leu Ala Thr Arg Met Val Cys Asn Ile Gly Phe Cys Leu Met
50 55 60
Asp Phe Thr His Asp Pro Tyr Ala Pro Ser Leu Pro
65 70 75
<210> 136
<211> 77
<212> БЕЛОК
<213> Medicago truncatula
<400> 136
Met Tyr Val Tyr Tyr Ile Gln Met Gly Lys Asn Met Ala Gln Arg Phe
1 5 10 15
Met Phe Ile Tyr Ala Leu Ile Ile Phe Leu Ser Gln Phe Phe Val Val
20 25 30
Ile Asn Thr Ser Asp Ile Pro Asn Asn Ser Asn Arg Asn Ser Pro Lys
35 40 45
Glu Asp Val Phe Cys Asn Ser Asn Asp Asp Cys Pro Thr Ile Leu Tyr
50 55 60
Tyr Val Ser Lys Cys Val Tyr Asn Phe Cys Glu Tyr Trp
65 70 75
<210> 137
<211> 67
<212> БЕЛОК
<213> Medicago truncatula
<400> 137
Met Ala Lys Ile Val Asn Phe Val Tyr Ser Met Ile Ile Phe Val Ser
1 5 10 15
Leu Phe Leu Val Ala Thr Lys Gly Gly Ser Lys Pro Phe Leu Thr Arg
20 25 30
Pro Tyr Pro Cys Asn Thr Gly Ser Asp Cys Pro Gln Asn Met Cys Pro
35 40 45
Pro Gly Tyr Lys Pro Gly Cys Glu Asp Gly Tyr Cys Asn His Cys Tyr
50 55 60
Lys Arg Trp
65
<210> 138
<211> 62
<212> БЕЛОК
<213> Medicago truncatula
<400> 138
Met Val Arg Thr Leu Lys Phe Val Tyr Val Ile Ile Leu Ile Leu Ser
1 5 10 15
Leu Phe Leu Val Ala Lys Gly Gly Gly Lys Lys Ile Tyr Cys Glu Asn
20 25 30
Ala Ala Ser Cys Pro Arg Leu Met Tyr Pro Leu Val Tyr Lys Cys Leu
35 40 45
Asp Asn Lys Cys Val Lys Phe Met Met Lys Ser Arg Phe Val
50 55 60
<210> 139
<211> 62
<212> БЕЛОК
<213> Medicago truncatula
<400> 139
Met Ala Arg Thr Leu Lys Phe Val Tyr Ala Val Ile Leu Phe Leu Ser
1 5 10 15
Leu Phe Leu Val Ala Lys Gly Asp Asp Val Lys Ile Lys Cys Val Val
20 25 30
Ala Ala Asn Cys Pro Asp Leu Met Tyr Pro Leu Val Tyr Lys Cys Leu
35 40 45
Asn Gly Ile Cys Val Gln Phe Thr Leu Thr Phe Pro Phe Val
50 55 60
<210> 140
<211> 65
<212> БЕЛОК
<213> Medicago truncatula
<400> 140
Met Ser Asn Thr Leu Met Phe Val Ile Thr Phe Ile Val Leu Val Thr
1 5 10 15
Leu Phe Leu Gly Pro Lys Asn Val Tyr Ala Phe Gln Pro Cys Val Thr
20 25 30
Thr Ala Asp Cys Met Lys Thr Leu Lys Thr Asp Glu Asn Ile Trp Tyr
35 40 45
Glu Cys Ile Asn Asp Phe Cys Ile Pro Phe Pro Ile Pro Lys Gly Arg
50 55 60
Lys
65
<210> 141
<211> 76
<212> БЕЛОК
<213> Medicago truncatula
<400> 141
Met Lys Arg Val Val Asn Met Ala Lys Ile Val Lys Tyr Val Tyr Val
1 5 10 15
Ile Ile Ile Phe Leu Ser Leu Phe Leu Val Ala Thr Lys Ile Glu Gly
20 25 30
Tyr Tyr Tyr Lys Cys Phe Lys Asp Ser Asp Cys Val Lys Leu Leu Cys
35 40 45
Arg Ile Pro Leu Arg Pro Lys Cys Met Tyr Arg His Ile Cys Lys Cys
50 55 60
Lys Val Val Leu Thr Gln Asn Asn Tyr Val Leu Thr
65 70 75
<210> 142
<211> 66
<212> БЕЛОК
<213> Medicago truncatula
<400> 142
Met Lys Arg Gly Lys Asn Met Ser Lys Ile Leu Lys Phe Ile Tyr Ala
1 5 10 15
Thr Leu Val Leu Tyr Leu Phe Leu Val Val Thr Lys Ala Ser Asp Asp
20 25 30
Glu Cys Lys Ile Asp Gly Asp Cys Pro Ile Ser Trp Gln Lys Phe His
35 40 45
Thr Tyr Lys Cys Ile Asn Gln Lys Cys Lys Trp Val Leu Arg Phe His
50 55 60
Glu Tyr
65
<210> 143
<211> 64
<212> БЕЛОК
<213> Medicago truncatula
<400> 143
Met Ala Lys Thr Leu Asn Phe Met Phe Ala Leu Ile Leu Phe Ile Ser
1 5 10 15
Leu Phe Leu Val Ser Lys Asn Val Ala Ile Asp Ile Phe Val Cys Gln
20 25 30
Thr Asp Ala Asp Cys Pro Lys Ser Glu Leu Ser Met Tyr Thr Trp Lys
35 40 45
Cys Ile Asp Asn Glu Cys Asn Leu Phe Lys Val Met Gln Gln Met Val
50 55 60
<210> 144
<211> 59
<212> БЕЛОК
<213> Medicago truncatula
<400> 144
Met Ala Asn Thr His Lys Leu Val Ser Met Ile Leu Phe Ile Phe Leu
1 5 10 15
Phe Leu Val Ala Asn Asn Val Glu Gly Tyr Val Asn Cys Glu Thr Asp
20 25 30
Ala Asp Cys Pro Pro Ser Thr Arg Val Lys Arg Phe Lys Cys Val Lys
35 40 45
Gly Glu Cys Arg Trp Thr Arg Met Ser Tyr Ala
50 55
<210> 145
<211> 59
<212> БЕЛОК
<213> Medicago truncatula
<400> 145
Met Ala His Phe Leu Met Phe Val Tyr Ala Leu Ile Thr Cys Leu Ser
1 5 10 15
Leu Phe Leu Val Glu Met Gly His Leu Ser Ile His Cys Val Ser Val
20 25 30
Asp Asp Cys Pro Lys Val Glu Lys Pro Ile Thr Met Lys Cys Ile Asn
35 40 45
Asn Tyr Cys Lys Tyr Phe Val Asp His Lys Leu
50 55
<210> 146
<211> 66
<212> БЕЛОК
<213> Medicago truncatula
<400> 146
Met Asn Gln Ile Pro Met Phe Gly Tyr Thr Leu Ile Ile Phe Phe Ser
1 5 10 15
Leu Phe Pro Val Ile Thr Asn Gly Asp Arg Ile Pro Cys Val Thr Asn
20 25 30
Gly Asp Cys Pro Val Met Arg Leu Pro Leu Tyr Met Arg Cys Ile Thr
35 40 45
Tyr Ser Cys Glu Leu Phe Phe Asp Gly Pro Asn Leu Cys Ala Val Glu
50 55 60
Arg Ile
65
<210> 147
<211> 61
<212> БЕЛОК
<213> Medicago truncatula
<400> 147
Met Arg Lys Asp Met Ala Arg Ile Ser Leu Phe Val Tyr Ala Leu Ile
1 5 10 15
Ile Phe Phe Ser Leu Phe Phe Val Leu Thr Asn Gly Glu Leu Glu Ile
20 25 30
Arg Cys Val Ser Asp Ala Asp Cys Pro Leu Phe Pro Leu Pro Leu His
35 40 45
Asn Arg Cys Ile Asp Asp Val Cys His Leu Phe Thr Ser
50 55 60
<210> 148
<211> 60
<212> БЕЛОК
<213> Medicago truncatula
<400> 148
Met Ala Gln Ile Leu Met Phe Val Tyr Phe Leu Ile Ile Phe Leu Ser
1 5 10 15
Leu Phe Leu Val Glu Ser Ile Lys Ile Phe Thr Glu His Arg Cys Arg
20 25 30
Thr Asp Ala Asp Cys Pro Ala Arg Glu Leu Pro Glu Tyr Leu Lys Cys
35 40 45
Gln Gly Gly Met Cys Arg Leu Leu Ile Lys Lys Asp
50 55 60
<210> 149
<211> 56
<212> БЕЛОК
<213> Medicago truncatula
<400> 149
Met Ala Arg Val Ile Ser Leu Phe Tyr Ala Leu Ile Ile Phe Leu Phe
1 5 10 15
Leu Phe Leu Val Ala Thr Asn Gly Asp Leu Ser Pro Cys Leu Arg Ser
20 25 30
Gly Asp Cys Ser Lys Asp Glu Cys Pro Ser His Leu Val Pro Lys Cys
35 40 45
Ile Gly Leu Thr Cys Tyr Cys Ile
50 55
<210> 150
<211> 62
<212> БЕЛОК
<213> Medicago truncatula
<400> 150
Met Gln Arg Arg Lys Asn Met Ala Gln Ile Leu Leu Phe Ala Tyr Val
1 5 10 15
Phe Ile Ile Ser Ile Ser Leu Phe Leu Val Val Thr Asn Gly Val Lys
20 25 30
Ile Pro Cys Val Lys Asp Thr Asp Cys Pro Thr Leu Pro Cys Pro Leu
35 40 45
Tyr Ser Lys Cys Val Asp Gly Phe Cys Lys Met Leu Ser Ile
50 55 60
<210> 151
<211> 66
<212> БЕЛОК
<213> Medicago truncatula
<400> 151
Met Asn His Ile Ser Lys Phe Val Tyr Ala Leu Ile Ile Phe Leu Ser
1 5 10 15
Val Tyr Leu Val Val Leu Asp Gly Arg Pro Val Ser Cys Lys Asp His
20 25 30
Tyr Asp Cys Arg Arg Lys Val Lys Ile Val Gly Cys Ile Phe Pro Gln
35 40 45
Glu Lys Pro Met Cys Ile Asn Ser Met Cys Thr Cys Ile Arg Glu Ile
50 55 60
Val Pro
65
<210> 152
<211> 86
<212> БЕЛОК
<213> Medicago truncatula
<400> 152
Met Lys Ser Gln Asn His Ala Lys Phe Ile Ser Phe Tyr Lys Asn Asp
1 5 10 15
Leu Phe Lys Ile Phe Gln Asn Asn Asp Ser His Phe Lys Val Phe Phe
20 25 30
Ala Leu Ile Ile Phe Leu Tyr Thr Tyr Leu His Val Thr Asn Gly Val
35 40 45
Phe Val Ser Cys Asn Ser His Ile His Cys Arg Val Asn Asn His Lys
50 55 60
Ile Gly Cys Asn Ile Pro Glu Gln Tyr Leu Leu Cys Val Asn Leu Phe
65 70 75 80
Cys Leu Trp Leu Asp Tyr
85
<210> 153
<211> 62
<212> БЕЛОК
<213> Medicago truncatula
<400> 153
Met Thr Tyr Ile Ser Lys Val Val Tyr Ala Leu Ile Ile Phe Leu Ser
1 5 10 15
Ile Tyr Val Gly Val Asn Asp Cys Met Leu Val Thr Cys Glu Asp His
20 25 30
Phe Asp Cys Arg Gln Asn Val Gln Gln Val Gly Cys Ser Phe Arg Glu
35 40 45
Ile Pro Gln Cys Ile Asn Ser Ile Cys Lys Cys Met Lys Gly
50 55 60
<210> 154
<211> 63
<212> БЕЛОК
<213> Medicago truncatula
<400> 154
Met Thr His Ile Ser Lys Phe Val Phe Ala Leu Ile Ile Phe Leu Ser
1 5 10 15
Ile Tyr Val Gly Val Asn Asp Cys Lys Arg Ile Pro Cys Lys Asp Asn
20 25 30
Asn Asp Cys Asn Asn Asn Trp Gln Leu Leu Ala Cys Arg Phe Glu Arg
35 40 45
Glu Val Pro Arg Cys Ile Asn Ser Ile Cys Lys Cys Met Pro Met
50 55 60
<210> 155
<211> 60
<212> БЕЛОК
<213> Medicago truncatula
<400> 155
Met Val Gln Thr Pro Lys Leu Val Tyr Val Ile Val Leu Leu Leu Ser
1 5 10 15
Ile Phe Leu Gly Met Thr Ile Cys Asn Ser Ser Phe Ser His Phe Phe
20 25 30
Glu Gly Ala Cys Lys Ser Asp Lys Asp Cys Pro Lys Leu His Arg Ser
35 40 45
Asn Val Arg Cys Arg Lys Gly Gln Cys Val Gln Ile
50 55 60
<210> 156
<211> 77
<212> БЕЛОК
<213> Medicago truncatula
<400> 156
Met Thr Lys Ile Leu Met Leu Phe Tyr Ala Met Ile Val Phe His Ser
1 5 10 15
Ile Phe Leu Val Ala Ser Tyr Thr Asp Glu Cys Ser Thr Asp Ala Asp
20 25 30
Cys Glu Tyr Ile Leu Cys Leu Phe Pro Ile Ile Lys Arg Cys Ile His
35 40 45
Asn His Cys Lys Cys Val Pro Met Gly Ser Ile Glu Pro Met Ser Thr
50 55 60
Ile Pro Asn Gly Val His Lys Phe His Ile Ile Asn Asn
65 70 75
<210> 157
<211> 64
<212> БЕЛОК
<213> Medicago truncatula
<400> 157
Met Ala Lys Thr Leu Asn Phe Val Cys Ala Met Ile Leu Phe Ile Ser
1 5 10 15
Leu Phe Leu Val Ser Lys Asn Val Ala Leu Tyr Ile Ile Glu Cys Lys
20 25 30
Thr Asp Ala Asp Cys Pro Ile Ser Lys Leu Asn Met Tyr Asn Trp Arg
35 40 45
Cys Ile Lys Ser Ser Cys His Leu Tyr Lys Val Ile Gln Phe Met Val
50 55 60
<210> 158
<211> 72
<212> БЕЛОК
<213> Medicago truncatula
<400> 158
Met Gln Lys Glu Lys Asn Met Ala Lys Thr Phe Glu Phe Val Tyr Ala
1 5 10 15
Met Ile Ile Phe Ile Leu Leu Phe Leu Val Glu Asn Asn Phe Ala Ala
20 25 30
Tyr Ile Ile Glu Cys Gln Thr Asp Asp Asp Cys Pro Lys Ser Gln Leu
35 40 45
Glu Met Phe Ala Trp Lys Cys Val Lys Asn Gly Cys His Leu Phe Gly
50 55 60
Met Tyr Glu Asp Asp Asp Asp Pro
65 70
<210> 159
<211> 57
<212> БЕЛОК
<213> Medicago truncatula
<400> 159
Met Ala Ala Thr Arg Lys Phe Ile Tyr Val Leu Ser His Phe Leu Phe
1 5 10 15
Leu Phe Leu Val Thr Lys Ile Thr Asp Ala Arg Val Cys Lys Ser Asp
20 25 30
Lys Asp Cys Lys Asp Ile Ile Ile Tyr Arg Tyr Ile Leu Lys Cys Arg
35 40 45
Asn Gly Glu Cys Val Lys Ile Lys Ile
50 55
<210> 160
<211> 75
<212> БЕЛОК
<213> Medicago truncatula
<400> 160
Met Gln Arg Leu Asp Asn Met Ala Lys Asn Val Lys Phe Ile Tyr Val
1 5 10 15
Ile Ile Leu Leu Leu Phe Ile Phe Leu Val Ile Ile Val Cys Asp Ser
20 25 30
Ala Phe Val Pro Asn Ser Gly Pro Cys Thr Thr Asp Lys Asp Cys Lys
35 40 45
Gln Val Lys Gly Tyr Ile Ala Arg Cys Arg Lys Gly Tyr Cys Met Gln
50 55 60
Ser Val Lys Arg Thr Trp Ser Ser Tyr Ser Arg
65 70 75
<210> 161
<211> 102
<212> БЕЛОК
<213> Medicago truncatula
<400> 161
Met Lys Phe Ile Tyr Ile Met Ile Leu Phe Leu Ser Leu Phe Leu Val
1 5 10 15
Gln Phe Leu Thr Cys Lys Gly Leu Thr Val Pro Cys Glu Asn Pro Thr
20 25 30
Thr Cys Pro Glu Asp Phe Cys Thr Pro Pro Met Ile Thr Arg Cys Ile
35 40 45
Asn Phe Ile Cys Leu Cys Asp Gly Pro Glu Tyr Ala Glu Pro Glu Tyr
50 55 60
Asp Gly Pro Glu Pro Glu Tyr Asp His Lys Gly Asp Phe Leu Ser Val
65 70 75 80
Lys Pro Lys Ile Ile Asn Glu Asn Met Met Met Arg Glu Arg His Met
85 90 95
Met Lys Glu Ile Glu Val
100
<210> 162
<211> 59
<212> БЕЛОК
<213> Medicago truncatula
<400> 162
Met Ala Gln Phe Leu Met Phe Ile Tyr Val Leu Ile Ile Phe Leu Tyr
1 5 10 15
Leu Phe Tyr Val Glu Ala Ala Met Phe Glu Leu Thr Lys Ser Thr Ile
20 25 30
Arg Cys Val Thr Asp Ala Asp Cys Pro Asn Val Val Lys Pro Leu Lys
35 40 45
Pro Lys Cys Val Asp Gly Phe Cys Glu Tyr Thr
50 55
<210> 163
<211> 70
<212> БЕЛОК
<213> Medicago truncatula
<400> 163
Met Lys Met Arg Ile His Met Ala Gln Ile Ile Met Phe Phe Tyr Ala
1 5 10 15
Leu Ile Ile Phe Leu Ser Pro Phe Leu Val Asp Arg Arg Ser Phe Pro
20 25 30
Ser Ser Phe Val Ser Pro Lys Ser Tyr Thr Ser Glu Ile Pro Cys Lys
35 40 45
Ala Thr Arg Asp Cys Pro Tyr Glu Leu Tyr Tyr Glu Thr Lys Cys Val
50 55 60
Asp Ser Leu Cys Thr Tyr
65 70
<210> 164
<211> 41
<212> БЕЛОК
<213> Medicago truncatula
<400> 164
Thr Arg Met Leu Thr Ile Pro Cys Thr Ser Asp Asp Asn Cys Pro Lys
1 5 10 15
Val Ile Ser Pro Cys His Thr Lys Cys Phe Asp Gly Phe Cys Gly Trp
20 25 30
Tyr Ile Glu Gly Ser Tyr Glu Gly Pro
35 40
<210> 165
<211> 69
<212> БЕЛОК
<213> Medicago truncatula
<400> 165
Met Ala Gln Phe Leu Leu Phe Val Tyr Ser Leu Ile Ile Phe Leu Ser
1 5 10 15
Leu Phe Phe Gly Glu Ala Ala Phe Glu Arg Thr Glu Thr Arg Met Leu
20 25 30
Thr Ile Pro Cys Thr Ser Asp Asp Asn Cys Pro Lys Val Ile Ser Pro
35 40 45
Cys His Thr Lys Cys Phe Asp Gly Phe Cys Gly Trp Tyr Ile Glu Gly
50 55 60
Ser Tyr Glu Gly Pro
65
<210> 166
<211> 78
<212> БЕЛОК
<213> Buchnera aphidicola
<400> 166
Met Lys Leu Leu His Gly Phe Leu Ile Ile Met Leu Thr Met His Leu
1 5 10 15
Ser Ile Gln Tyr Ala Tyr Gly Gly Pro Phe Leu Thr Lys Tyr Leu Cys
20 25 30
Asp Arg Val Cys His Lys Leu Cys Gly Asp Glu Phe Val Cys Ser Cys
35 40 45
Ile Gln Tyr Lys Ser Leu Lys Gly Leu Trp Phe Pro His Cys Pro Thr
50 55 60
Gly Lys Ala Ser Val Val Leu His Asn Phe Leu Thr Ser Pro
65 70 75
<210> 167
<211> 77
<212> БЕЛОК
<213> Buchnera aphidicola
<400> 167
Met Lys Leu Leu Tyr Gly Phe Leu Ile Ile Met Leu Thr Ile His Leu
1 5 10 15
Ser Val Gln Tyr Phe Glu Ser Pro Phe Glu Thr Lys Tyr Asn Cys Asp
20 25 30
Thr His Cys Asn Lys Leu Cys Gly Lys Ile Asp His Cys Ser Cys Ile
35 40 45
Gln Tyr His Ser Met Glu Gly Leu Trp Phe Pro His Cys Arg Thr Gly
50 55 60
Ser Ala Ala Gln Met Leu His Asp Phe Leu Ser Asn Pro
65 70 75
<210> 168
<211> 86
<212> БЕЛОК
<213> Buchnera aphidicola
<400> 168
Met Ser Val Arg Lys Asn Val Leu Pro Thr Met Phe Val Val Leu Leu
1 5 10 15
Ile Met Ser Pro Val Thr Pro Thr Ser Val Phe Ile Ser Ala Val Cys
20 25 30
Tyr Ser Gly Cys Gly Ser Leu Ala Leu Val Cys Phe Val Ser Asn Gly
35 40 45
Ile Thr Asn Gly Leu Asp Tyr Phe Lys Ser Ser Ala Pro Leu Ser Thr
50 55 60
Ser Glu Thr Ser Cys Gly Glu Ala Phe Asp Thr Cys Thr Asp His Cys
65 70 75 80
Leu Ala Asn Phe Lys Phe
85
<210> 169
<211> 69
<212> БЕЛОК
<213> Buchnera aphidicola
<400> 169
Met Arg Leu Leu Tyr Gly Phe Leu Ile Ile Met Leu Thr Ile Tyr Leu
1 5 10 15
Ser Val Gln Asp Phe Asp Pro Thr Glu Phe Lys Gly Pro Phe Pro Thr
20 25 30
Ile Glu Ile Cys Ser Lys Tyr Cys Ala Val Val Cys Asn Tyr Thr Ser
35 40 45
Arg Pro Cys Tyr Cys Val Glu Ala Ala Lys Glu Arg Asp Gln Trp Phe
50 55 60
Pro Tyr Cys Tyr Asp
65
<210> 170
<211> 77
<212> БЕЛОК
<213> Buchnera aphidicola
<400> 170
Met Arg Leu Leu Tyr Gly Phe Leu Ile Ile Met Leu Thr Ile His Leu
1 5 10 15
Ser Val Gln Asp Ile Asp Pro Asn Thr Leu Arg Gly Pro Tyr Pro Thr
20 25 30
Lys Glu Ile Cys Ser Lys Tyr Cys Glu Tyr Asn Val Val Cys Gly Ala
35 40 45
Ser Leu Pro Cys Ile Cys Val Gln Asp Ala Arg Gln Leu Asp His Trp
50 55 60
Phe Ala Cys Cys Tyr Asp Gly Gly Pro Glu Met Leu Met
65 70 75
<210> 171
<211> 108
<212> БЕЛОК
<213> Buchnera aphidicola
<400> 171
Met Lys Leu Phe Val Val Val Val Leu Val Ala Val Gly Ile Met Phe
1 5 10 15
Val Phe Ala Ser Asp Thr Ala Ala Ala Pro Thr Asp Tyr Glu Asp Thr
20 25 30
Asn Asp Met Ile Ser Leu Ser Ser Leu Val Gly Asp Asn Ser Pro Tyr
35 40 45
Val Arg Val Ser Ser Ala Asp Ser Gly Gly Ser Ser Lys Thr Ser Ser
50 55 60
Lys Asn Pro Ile Leu Gly Leu Leu Lys Ser Val Ile Lys Leu Leu Thr
65 70 75 80
Lys Ile Phe Gly Thr Tyr Ser Asp Ala Ala Pro Ala Met Pro Pro Ile
85 90 95
Pro Pro Ala Leu Arg Lys Asn Arg Gly Met Leu Ala
100 105
<210> 172
<211> 178
<212> БЕЛОК
<213> Buchnera aphidicola
<400> 172
Met Val Ala Cys Lys Val Ile Leu Ala Val Ala Val Val Phe Val Ala
1 5 10 15
Ala Val Gln Gly Arg Pro Gly Gly Glu Pro Glu Trp Ala Ala Pro Ile
20 25 30
Phe Ala Glu Leu Lys Ser Val Ser Asp Asn Ile Thr Asn Leu Val Gly
35 40 45
Leu Asp Asn Ala Gly Glu Tyr Ala Thr Ala Ala Lys Asn Asn Leu Asn
50 55 60
Ala Phe Ala Glu Ser Leu Lys Thr Glu Ala Ala Val Phe Ser Lys Ser
65 70 75 80
Phe Glu Gly Lys Ala Ser Ala Ser Asp Val Phe Lys Glu Ser Thr Lys
85 90 95
Asn Phe Gln Ala Val Val Asp Thr Tyr Ile Lys Asn Leu Pro Lys Asp
100 105 110
Leu Thr Leu Lys Asp Phe Thr Glu Lys Ser Glu Gln Ala Leu Lys Tyr
115 120 125
Met Val Glu His Gly Thr Glu Ile Thr Lys Lys Ala Gln Gly Asn Thr
130 135 140
Glu Thr Glu Lys Glu Ile Lys Glu Phe Phe Lys Lys Gln Ile Glu Asn
145 150 155 160
Leu Ile Gly Gln Gly Lys Ala Leu Gln Ala Lys Ile Ala Glu Ala Lys
165 170 175
Lys Ala
<210> 173
<211> 311
<212> БЕЛОК
<213> Buchnera aphidicola
<400> 173
Met Lys Thr Ser Ser Ser Lys Val Phe Ala Ser Cys Val Ala Ile Val
1 5 10 15
Cys Leu Ala Ser Val Ala Asn Ala Leu Pro Val Gln Lys Ser Val Ala
20 25 30
Ala Thr Thr Glu Asn Pro Ile Val Glu Lys His Gly Cys Arg Ala His
35 40 45
Lys Asn Leu Val Arg Gln Asn Val Val Asp Leu Lys Thr Tyr Asp Ser
50 55 60
Met Leu Ile Thr Asn Glu Val Val Gln Lys Gln Ser Asn Glu Val Gln
65 70 75 80
Ser Ser Glu Gln Ser Asn Glu Gly Gln Asn Ser Glu Gln Ser Asn Glu
85 90 95
Gly Gln Asn Ser Glu Gln Ser Asn Glu Val Gln Ser Ser Glu His Ser
100 105 110
Asn Glu Gly Gln Asn Ser Lys Gln Ser Asn Glu Gly Gln Asn Ser Glu
115 120 125
Gln Ser Asn Glu Val Gln Ser Ser Glu His Ser Asn Glu Gly Gln Asn
130 135 140
Ser Glu Gln Ser Asn Glu Val Gln Ser Ser Glu His Ser Asn Glu Gly
145 150 155 160
Gln Asn Ser Lys Gln Ser Asn Glu Gly Gln Asn Ser Lys Gln Ser Asn
165 170 175
Glu Val Gln Ser Ser Glu His Trp Asn Glu Gly Gln Asn Ser Lys Gln
180 185 190
Ser Asn Glu Asp Gln Asn Ser Glu Gln Ser Asn Glu Gly Gln Asn Ser
195 200 205
Lys Gln Ser Asn Glu Gly Gln Asn Ser Lys Gln Ser Asn Glu Asp Gln
210 215 220
Asn Ser Glu Gln Ser Asn Glu Gly Gln Asn Ser Lys Gln Ser Asn Glu
225 230 235 240
Val Gln Ser Ser Glu Gln Ser Asn Glu Gly Gln Asn Ser Lys Gln Ser
245 250 255
Asn Glu Gly Gln Ser Ser Glu Gln Ser Asn Glu Gly Gln Asn Ser Lys
260 265 270
Gln Ser Asn Glu Val Gln Ser Pro Glu Glu His Tyr Asp Leu Pro Asp
275 280 285
Pro Glu Ser Ser Tyr Glu Ser Glu Glu Thr Lys Gly Ser His Glu Ser
290 295 300
Gly Asp Asp Ser Glu His Arg
305 310
<210> 174
<211> 431
<212> БЕЛОК
<213> Buchnera aphidicola
<400> 174
Met Lys Thr Ile Ile Leu Gly Leu Cys Leu Phe Gly Ala Leu Phe Trp
1 5 10 15
Ser Thr Gln Ser Met Pro Val Gly Glu Val Ala Pro Ala Val Pro Ala
20 25 30
Val Pro Ser Glu Ala Val Pro Gln Lys Gln Val Glu Ala Lys Pro Glu
35 40 45
Thr Asn Ala Ala Ser Pro Val Ser Asp Ala Lys Pro Glu Ser Asp Ser
50 55 60
Lys Pro Val Asp Ala Glu Val Lys Pro Thr Val Ser Glu Val Lys Ala
65 70 75 80
Glu Ser Glu Gln Lys Pro Ser Gly Glu Pro Lys Pro Glu Ser Asp Ala
85 90 95
Lys Pro Val Val Ala Ser Glu Ser Lys Pro Glu Ser Asp Pro Lys Pro
100 105 110
Ala Ala Val Val Glu Ser Lys Pro Glu Asn Asp Ala Val Ala Pro Glu
115 120 125
Thr Asn Asn Asp Ala Lys Pro Glu Asn Ala Ala Ala Pro Val Ser Glu
130 135 140
Asn Lys Pro Ala Thr Asp Ala Lys Ala Glu Thr Glu Leu Ile Ala Gln
145 150 155 160
Ala Lys Pro Glu Ser Lys Pro Ala Ser Asp Leu Lys Ala Glu Pro Glu
165 170 175
Ala Ala Lys Pro Asn Ser Glu Val Pro Val Ala Leu Pro Leu Asn Pro
180 185 190
Thr Glu Thr Lys Ala Thr Gln Gln Ser Val Glu Thr Asn Gln Val Glu
195 200 205
Gln Ala Ala Pro Ala Ala Ala Gln Ala Asp Pro Ala Ala Ala Pro Ala
210 215 220
Ala Asp Pro Ala Pro Ala Pro Ala Ala Ala Pro Val Ala Ala Glu Glu
225 230 235 240
Ala Lys Leu Ser Glu Ser Ala Pro Ser Thr Glu Asn Lys Ala Ala Glu
245 250 255
Glu Pro Ser Lys Pro Ala Glu Gln Gln Ser Ala Lys Pro Val Glu Asp
260 265 270
Ala Val Pro Ala Ala Ser Glu Ile Ser Glu Thr Lys Val Ser Pro Ala
275 280 285
Val Pro Ala Val Pro Glu Val Pro Ala Ser Pro Ser Ala Pro Ala Val
290 295 300
Ala Asp Pro Val Ser Ala Pro Glu Ala Glu Lys Asn Ala Glu Pro Ala
305 310 315 320
Lys Ala Ala Asn Ser Ala Glu Pro Ala Val Gln Ser Glu Ala Lys Pro
325 330 335
Ala Glu Asp Ile Gln Lys Ser Gly Ala Val Val Ser Ala Glu Asn Pro
340 345 350
Lys Pro Val Glu Glu Gln Lys Pro Ala Glu Val Ala Lys Pro Ala Glu
355 360 365
Gln Ser Lys Ser Glu Ala Pro Ala Glu Ala Pro Lys Pro Thr Glu Gln
370 375 380
Ser Ala Ala Glu Glu Pro Lys Lys Pro Glu Ser Ala Asn Asp Glu Lys
385 390 395 400
Lys Glu Gln His Ser Val Asn Lys Arg Asp Ala Thr Lys Glu Lys Lys
405 410 415
Pro Thr Asp Ser Ile Met Lys Lys Gln Lys Gln Lys Lys Ala Asn
420 425 430
<210> 175
<211> 160
<212> БЕЛОК
<213> Buchnera aphidicola
<400> 175
Met Asn Gly Lys Ile Val Leu Cys Phe Ala Val Val Phe Ile Gly Gln
1 5 10 15
Ala Met Ser Ala Ala Thr Gly Thr Thr Pro Glu Val Glu Asp Ile Lys
20 25 30
Lys Val Ala Glu Gln Met Ser Gln Thr Phe Met Ser Val Ala Asn His
35 40 45
Leu Val Gly Ile Thr Pro Asn Ser Ala Asp Ala Gln Lys Ser Ile Glu
50 55 60
Lys Ile Arg Thr Ile Met Asn Lys Gly Phe Thr Asp Met Glu Thr Glu
65 70 75 80
Ala Asn Lys Met Lys Asp Ile Val Arg Lys Asn Ala Asp Pro Lys Leu
85 90 95
Val Glu Lys Tyr Asp Glu Leu Glu Lys Glu Leu Lys Lys His Leu Ser
100 105 110
Thr Ala Lys Asp Met Phe Glu Asp Lys Val Val Lys Pro Ile Gly Glu
115 120 125
Lys Val Glu Leu Lys Lys Ile Thr Glu Asn Val Ile Lys Thr Thr Lys
130 135 140
Asp Met Glu Ala Thr Met Asn Lys Ala Ile Asp Gly Phe Lys Lys Gln
145 150 155 160
<210> 176
<211> 415
<212> БЕЛОК
<213> Buchnera aphidicola
<400> 176
Met His Leu Phe Leu Ala Leu Gly Leu Phe Ile Val Cys Gly Met Val
1 5 10 15
Asp Ala Thr Phe Tyr Asn Pro Arg Ser Gln Thr Phe Asn Gln Leu Met
20 25 30
Glu Arg Arg Gln Arg Ser Ile Pro Ile Pro Tyr Ser Tyr Gly Tyr His
35 40 45
Tyr Asn Pro Ile Glu Pro Ser Ile Asn Val Leu Asp Ser Leu Ser Glu
50 55 60
Gly Leu Asp Ser Arg Ile Asn Thr Phe Lys Pro Ile Tyr Gln Asn Val
65 70 75 80
Lys Met Ser Thr Gln Asp Val Asn Ser Val Pro Arg Thr Gln Tyr Gln
85 90 95
Pro Lys Asn Ser Leu Tyr Asp Ser Glu Tyr Ile Ser Ala Lys Asp Ile
100 105 110
Pro Ser Leu Phe Pro Glu Glu Asp Ser Tyr Asp Tyr Lys Tyr Leu Gly
115 120 125
Ser Pro Leu Asn Lys Tyr Leu Thr Arg Pro Ser Thr Gln Glu Ser Gly
130 135 140
Ile Ala Ile Asn Leu Val Ala Ile Lys Glu Thr Ser Val Phe Asp Tyr
145 150 155 160
Gly Phe Pro Thr Tyr Lys Ser Pro Tyr Ser Ser Asp Ser Val Trp Asn
165 170 175
Phe Gly Ser Lys Ile Pro Asn Thr Val Phe Glu Asp Pro Gln Ser Val
180 185 190
Glu Ser Asp Pro Asn Thr Phe Lys Val Ser Ser Pro Thr Ile Lys Ile
195 200 205
Val Lys Leu Leu Pro Glu Thr Pro Glu Gln Glu Ser Ile Ile Thr Thr
210 215 220
Thr Lys Asn Tyr Glu Leu Asn Tyr Lys Thr Thr Gln Glu Thr Pro Thr
225 230 235 240
Glu Ala Glu Leu Tyr Pro Ile Thr Ser Glu Glu Phe Gln Thr Glu Asp
245 250 255
Glu Trp His Pro Met Val Pro Lys Glu Asn Thr Thr Lys Asp Glu Ser
260 265 270
Ser Phe Ile Thr Thr Glu Glu Pro Leu Thr Glu Asp Lys Ser Asn Ser
275 280 285
Ile Thr Ile Glu Lys Thr Gln Thr Glu Asp Glu Ser Asn Ser Ile Glu
290 295 300
Phe Asn Ser Ile Arg Thr Glu Glu Lys Ser Asn Ser Ile Thr Thr Glu
305 310 315 320
Glu Asn Gln Lys Glu Asp Asp Glu Ser Met Ser Thr Thr Ser Gln Glu
325 330 335
Thr Thr Thr Ala Phe Asn Leu Asn Asp Thr Phe Asp Thr Asn Arg Tyr
340 345 350
Ser Ser Ser His Glu Ser Leu Met Leu Arg Ile Arg Glu Leu Met Lys
355 360 365
Asn Ile Ala Asp Gln Gln Asn Lys Ser Gln Phe Arg Thr Val Asp Asn
370 375 380
Ile Pro Ala Lys Ser Gln Ser Asn Leu Ser Ser Asp Glu Ser Thr Asn
385 390 395 400
Gln Gln Phe Glu Pro Gln Leu Val Asn Gly Ala Asp Thr Tyr Lys
405 410 415
<210> 177
<211> 126
<212> БЕЛОК
<213> Sitophilus zeamais
<400> 177
Met Thr Arg Thr Met Leu Phe Leu Ala Cys Val Ala Ala Leu Tyr Val
1 5 10 15
Cys Ile Ser Ala Thr Ala Gly Lys Pro Glu Glu Phe Ala Lys Leu Ser
20 25 30
Asp Glu Ala Pro Ser Asn Asp Gln Ala Met Tyr Glu Ser Ile Gln Arg
35 40 45
Tyr Arg Arg Phe Val Asp Gly Asn Arg Tyr Asn Gly Gly Gln Gln Gln
50 55 60
Gln Gln Gln Pro Lys Gln Trp Glu Val Arg Pro Asp Leu Ser Arg Asp
65 70 75 80
Gln Arg Gly Asn Thr Lys Ala Gln Val Glu Ile Asn Lys Lys Gly Asp
85 90 95
Asn His Asp Ile Asn Ala Gly Trp Gly Lys Asn Ile Asn Gly Pro Asp
100 105 110
Ser His Lys Asp Thr Trp His Val Gly Gly Ser Val Arg Trp
115 120 125
<210> 178
<211> 16
<212> БЕЛОК
<213> Acyrthosiphon pisum
<400> 178
Arg Gln Ile Lys Ile Trp Phe Gln Asn Arg Arg Met Lys Trp Lys Lys
1 5 10 15
<210> 179
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Пептид Tat
<400> 179
Gly Arg Lys Lys Arg Arg Gln Arg Arg Arg Pro Pro Gln
1 5 10
<210> 180
<211> 18
<212> БЕЛОК
<213> Вирус иммунодефицита человека 1
<400> 180
Leu Leu Ile Ile Leu Arg Arg Arg Ile Arg Lys Gln Ala His Ala His
1 5 10 15
Ser Lys
<210> 181
<211> 27
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Транспортан
<400> 181
Gly Trp Thr Leu Asn Ser Ala Gly Tyr Leu Leu Gly Lys Ile Asn Leu
1 5 10 15
Lys Ala Leu Ala Ala Leu Ala Lys Lys Ile Leu
20 25
<210> 182
<211> 27
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> MPG
<400> 182
Gly Ala Leu Phe Leu Gly Phe Leu Gly Ala Ala Gly Ser Thr Met Gly
1 5 10 15
Ala Trp Ser Gln Pro Lys Lys Lys Arg Lys Val
20 25
<210> 183
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Pep-1
<400> 183
Lys Glu Thr Trp Trp Glu Thr Trp Trp Thr Glu Trp Ser Gln Pro Lys
1 5 10 15
Lys Lys Arg Lys Val
20
<210> 184
<211> 18
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> MAP
<400> 184
Lys Leu Ala Leu Lys Leu Ala Leu Lys Ala Leu Lys Ala Ala Leu Lys
1 5 10 15
Leu Ala
<210> 185
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> R6W3
<400> 185
Arg Arg Trp Trp Arg Arg Trp Arg Arg
1 5
<210> 186
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Прямой праймер для Bacillus
<400> 186
gaggtagacg aagcgacctg
20
<210> 187
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Обратный праймер для Bacillus
<400> 187
ttccctcacg gtactggttc
20
<210> 188
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Универсальный праймер для бактерий 27F
<400> 188
agagtttgat cmtggctcag
20
<210> 189
<211> 16
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Универсальный праймер для бактерий 1492R
<400> 189
taccttgtta cgactt
16
<210> 190
<211> 1583
<212> ДНК
<213> Lactobacillus kunkeei
<400> 190
ttccttagaa aggaggtgat ccagccgcag gttctcctac ggctaccttg ttacgacttc
60
accctaatca tctgtcccac cttagacgac tagctcctaa aaggttaccc catcgtcttt
120
gggtgttaca aactctcatg gtgtgacggg cggtgtgtac aaggcccggg aacgtattca
180
ccgtggcatg ctgatccacg attactagtg attccaactt catgcaggcg agttgcagcc
240
tgcaatccga actgagaatg gctttaagag attagcttga cctcgcggtt tcgcgactcg
300
ttgtaccatc cattgtagca cgtgtgtagc ccagctcata aggggcatga tgatttgacg
360
tcgtccccac cttcctccgg tttatcaccg gcagtctcac tagagtgccc aactaaatgc
420
tggcaactaa taataagggt tgcgctcgtt gcgggactta acccaacatc tcacgacacg
480
agctgacgac aaccatgcac cacctgtcat tctgtccccg aagggaacgc ccaatctctt
540
gggttggcag aagatgtcaa gagctggtaa ggttcttcgc gtagcatcga attaaaccac
600
atgctccacc acttgtgcgg gcccccgtca attcctttga gtttcaacct tgcggtcgta
660
ctccccaggc ggaatactta atgcgttagc tgcggcactg aagggcggaa accctccaac
720
acctagtatt catcgtttac ggcatggact accagggtat ctaatcctgt tcgctaccca
780
tgctttcgag cctcagcgtc agtaacagac cagaaagccg ccttcgccac tggtgttctt
840
ccatatatct acgcatttca ccgctacaca tggagttcca ctttcctctt ctgtactcaa
900
gttttgtagt ttccactgca cttcctcagt tgagctgagg gctttcacag cagacttaca
960
aaaccgcctg cgctcgcttt acgcccaata aatccggaca acgcttgcca cctacgtatt
1020
accgcggctg ctggcacgta gttagccgtg gctttctggt taaataccgt caaagtgtta
1080
acagttactc taacacttgt tcttctttaa caacagagtt ttacgatccg aaaaccttca
1140
tcactcacgc ggcgttgctc catcagactt tcgtccattg tggaagattc cctactgctg
1200
cctcccgtag gagtctgggc cgtgtctcag tcccaatgtg gccgattacc ctctcaggtc
1260
ggctacgtat catcgtcttg gtgggctttt atctcaccaa ctaactaata cggcgcgggt
1320
ccatcccaaa gtgatagcaa agccatcttt caagttggaa ccatgcggtt ccaactaatt
1380
atgcggtatt agcacttgtt tccaaatgtt atcccccgct tcggggcagg ttacccacgt
1440
gttactcacc agttcgccac tcgctccgaa tccaaaaatc atttatgcaa gcataaaatc
1500
aatttgggag aactcgttcg acttgcatgt attaggcacg ccgccagcgt tcgtcctgag
1560
ccaggatcaa actctcatct taa
1583
<210> 191
<211> 1395
<212> ДНК
<213> Lactobacillus Firm-4
<400> 191
acgaacgctg gcggcgtgcc taatacatgc aagtcgagcg cgggaagtca gggaagcctt
60
cgggtggaac tggtggaacg agcggcggat gggtgagtaa cacgtaggta acctgcccta
120
aagcggggga taccatctgg aaacaggtgc taataccgca taaacccagc agtcacatga
180
gtgctggttg aaagacggct tcggctgtca ctttaggatg gacctgcggc gtattagcta
240
gttggtggag taacggttca ccaaggcaat gatacgtagc cgacctgaga gggtaatcgg
300
ccacattggg actgagacac ggcccaaact cctacgggag gcagcagtag ggaatcttcc
360
acaatggacg caagtctgat ggagcaacgc cgcgtggatg aagaaggtct tcggatcgta
420
aaatcctgtt gttgaagaag aacggttgtg agagtaactg ctcataacgt gacggtaatc
480
aaccagaaag tcacggctaa ctacgtgcca gcagccgcgg taatacgtag gtggcaagcg
540
ttgtccggat ttattgggcg taaagggagc gcaggcggtc ttttaagtct gaatgtgaaa
600
gccctcagct taactgagga agagcatcgg aaactgagag acttgagtgc agaagaggag
660
agtggaactc catgtgtagc ggtgaaatgc gtagatatat ggaagaacac cagtggcgaa
720
ggcggctctc tggtctgtta ctgacgctga ggctcgaaag catgggtagc gaacaggatt
780
agataccctg gtagtccatg ccgtaaacga tgagtgctaa gtgttgggag gtttccgcct
840
ctcagtgctg cagctaacgc attaagcact ccgcctgggg agtacgaccg caaggttgaa
900
actcaaagga attgacgggg gcccgcacaa gcggtggagc atgtggttta attcgaagca
960
acgcgaagaa ccttaccagg tcttgacatc tcctgcaagc ctaagagatt aggggttccc
1020
ttcggggaca ggaagacagg tggtgcatgg ttgtcgtcag ctcgtgtcgt gagatgttgg
1080
gttaagtccc gcaacgagcg caacccttgt tactagttgc cagcattaag ttgggcactc
1140
tagtgagact gccggtgaca aaccggagga aggtggggac gacgtcaaat catcatgccc
1200
cttatgacct gggctacaca cgtgctacaa tggatggtac aatgagaagc gaactcgcga
1260
ggggaagctg atctctgaaa accattctca gttcggattg caggctgcaa ctcgcctgca
1320
tgaagctgga atcgctagta atcgcggatc agcatgccgc ggtgaatacg ttcccgggcc
1380
ttgtacacac cgccc
1395
<210> 192
<211> 220
<212> БЕЛОК
<213> Sitophilus zeamais
<400> 192
Met Lys Glu Thr Thr Val Val Trp Ala Lys Leu Phe Leu Ile Leu Ile
1 5 10 15
Ile Leu Ala Lys Pro Leu Gly Leu Lys Ala Val Asn Glu Cys Lys Arg
20 25 30
Leu Gly Asn Asn Ser Cys Arg Ser His Gly Glu Cys Cys Ser Gly Phe
35 40 45
Cys Phe Ile Glu Pro Gly Trp Ala Leu Gly Val Cys Lys Arg Leu Gly
50 55 60
Thr Pro Lys Lys Ser Asp Asp Ser Asn Asn Gly Lys Asn Ile Glu Lys
65 70 75 80
Asn Asn Gly Val His Glu Arg Ile Asp Asp Val Phe Glu Arg Gly Val
85 90 95
Cys Ser Tyr Tyr Lys Gly Pro Ser Ile Thr Ala Asn Gly Asp Val Phe
100 105 110
Asp Glu Asn Glu Met Thr Ala Ala His Arg Thr Leu Pro Phe Asn Thr
115 120 125
Met Val Lys Val Glu Gly Met Gly Thr Ser Val Val Val Lys Ile Asn
130 135 140
Asp Arg Lys Thr Ala Ala Asp Gly Lys Val Met Leu Leu Ser Arg Ala
145 150 155 160
Ala Ala Glu Ser Leu Asn Ile Asp Glu Asn Thr Gly Pro Val Gln Cys
165 170 175
Gln Leu Lys Phe Val Leu Asp Gly Ser Gly Cys Thr Pro Asp Tyr Gly
180 185 190
Asp Thr Cys Val Leu His His Glu Cys Cys Ser Gln Asn Cys Phe Arg
195 200 205
Glu Met Phe Ser Asp Lys Gly Phe Cys Leu Pro Lys
210 215 220
<210> 193
<211> 13
<212> БЕЛОК
<213> Pandinus imperator
<400> 193
Phe Leu Ser Thr Ile Trp Asn Gly Ile Lys Gly Leu Leu
1 5 10
<210> 194
<211> 13
<212> БЕЛОК
<213> Urodacus yaschenkoi
<400> 194
Ile Leu Ser Ala Ile Trp Ser Gly Ile Lys Ser Leu Phe
1 5 10
<210> 195
<211> 13
<212> БЕЛОК
<213> Scorpiops tibetanus
<400> 195
Leu Trp Gly Lys Leu Trp Glu Gly Val Lys Ser Leu Ile
1 5 10
<210> 196
<211> 22
<212> БЕЛОК
<213> Apostichopus japonicus
<400> 196
Phe Pro Phe Leu Lys Leu Ser Leu Lys Ile Pro Lys Ser Ala Ile Lys
1 5 10 15
Ser Ala Ile Lys Arg Leu
20
<210> 197
<211> 13
<212> БЕЛОК
<213> Urodacus yaschenkoi
<400> 197
Ile Leu Ser Ala Ile Trp Ser Gly Ile Lys Gly Leu Leu
1 5 10
<210> 198
<211> 27
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Uy192 + пептид, проникающий в клетку
<400> 198
Tyr Gly Arg Lys Lys Arg Arg Gln Arg Arg Arg Phe Leu Ser Thr Ile
1 5 10 15
Trp Asn Gly Ile Lys Gly Leu Leu Phe Ala Met
20 25
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБЫ И СООТВЕТСТВУЮЩИЕ КОМПОЗИЦИИ ДЛЯ ИЗГОТОВЛЕНИЯ ПРОДУКТОВ ПИТАНИЯ И КОРМОВ | 2018 |
|
RU2780586C2 |
| КОМПОЗИЦИИ И СООТВЕТСТВУЮЩИЕ СПОСОБЫ ДЛЯ СЕЛЬСКОГО ХОЗЯЙСТВА | 2018 |
|
RU2783258C2 |
| КОМПОЗИЦИИ И СООТВЕТСТВУЮЩИЕ СПОСОБЫ КОНТРОЛЯ ЗАБОЛЕВАНИЙ, ПЕРЕДАВАЕМЫХ ПЕРЕНОСЧИКАМИ | 2018 |
|
RU2777518C2 |
| КОМПОЗИЦИИ И СООТВЕТСТВУЮЩИЕ СПОСОБЫ КОНТРОЛЯ ЗАБОЛЕВАНИЙ, ПЕРЕДАВАЕМЫХ ПЕРЕНОСЧИКАМИ | 2018 |
|
RU2804136C2 |
| ИНСЕКТИЦИДНЫЕ БЕЛКИ | 2018 |
|
RU2761666C2 |
| АBC-ТРАНСПОРТЕРЫ ДЛЯ ВЫСОКОЭФФЕКТИВНОГО ПРОИЗВОДСТВА РЕБАУДИОЗИДОВ | 2020 |
|
RU2795855C2 |
| СКОНСТРУИРОВАННЫЕ ПЕСТИЦИДНЫЕ БЕЛКИ И СПОСОБЫ КОНТРОЛЯ ВРЕДИТЕЛЕЙ РАСТЕНИЙ | 2017 |
|
RU2817591C2 |
| СКОНСТРУИРОВАННЫЕ ПЕСТИЦИДНЫЕ БЕЛКИ И СПОСОБЫ КОНТРОЛЯ ВРЕДИТЕЛЕЙ РАСТЕНИЙ | 2017 |
|
RU2816526C2 |
| ВИРУСОПОДОБНЫЕ ЧАСТИЦЫ С ВЫСОКОПЛОТНЫМ ПОКРЫТИЕМ ДЛЯ ИНДУКЦИИ ЭКСПРЕССИИ АНТИТЕЛ | 2017 |
|
RU2813282C2 |
| Ферменты лактазы с улучшенными свойствами при кислом pH | 2019 |
|
RU2814542C2 |
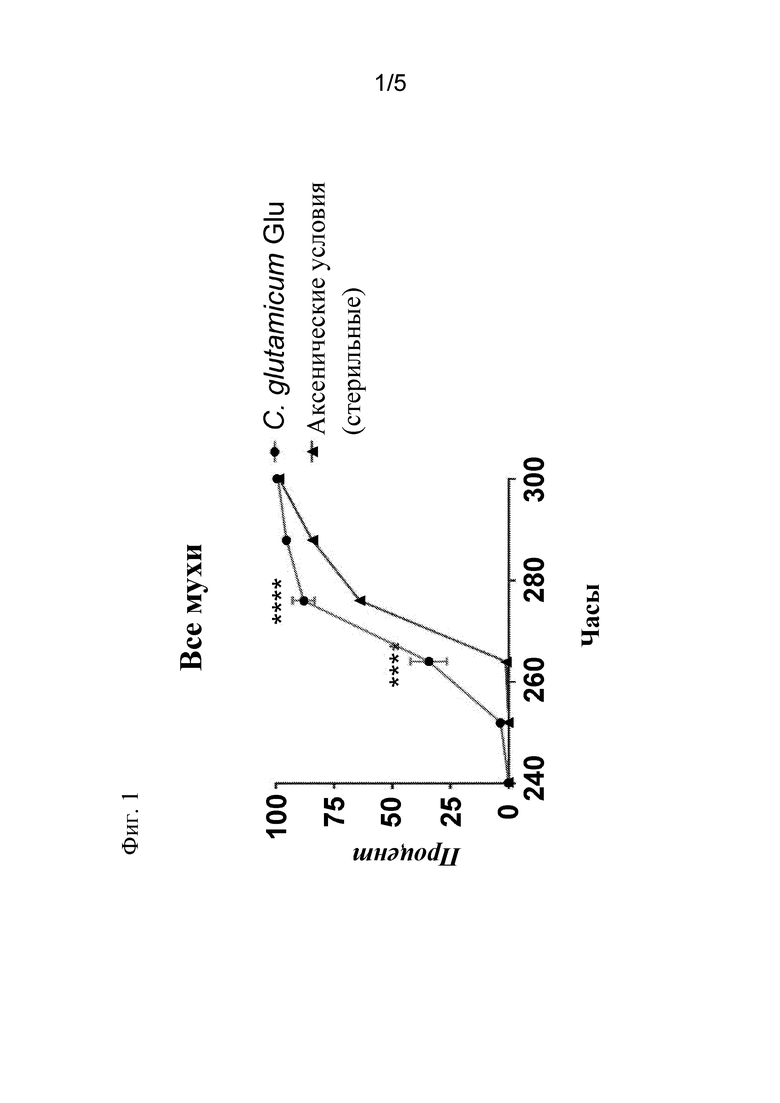
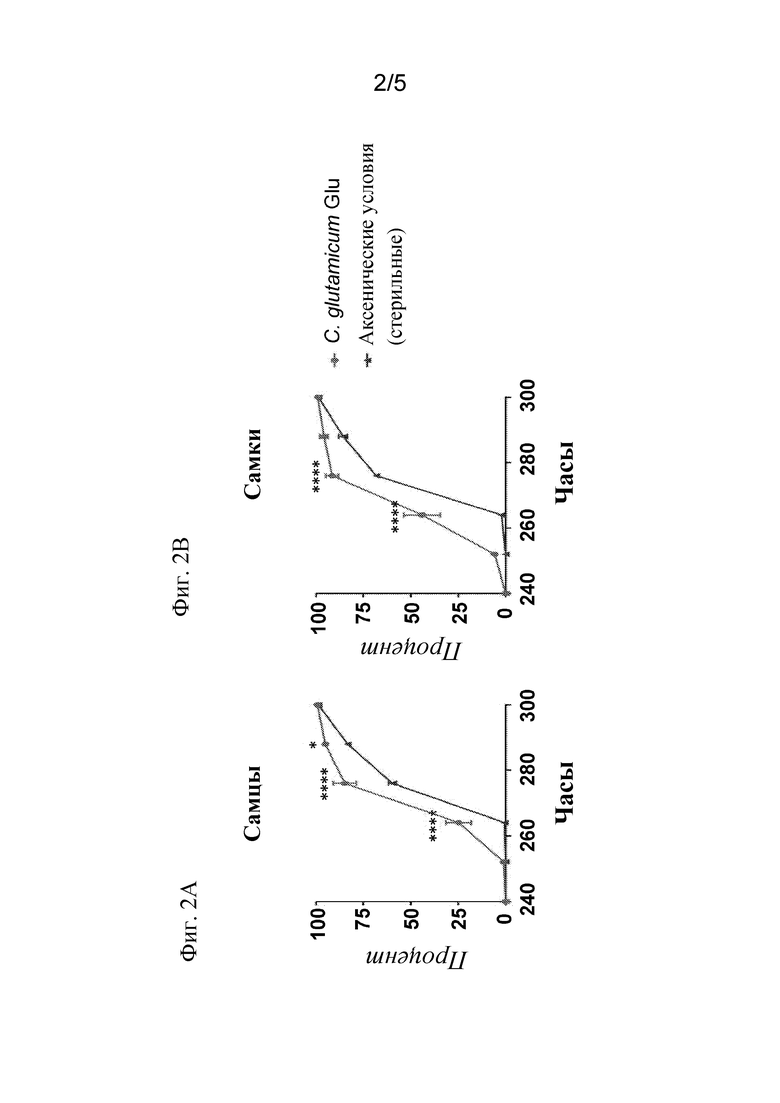
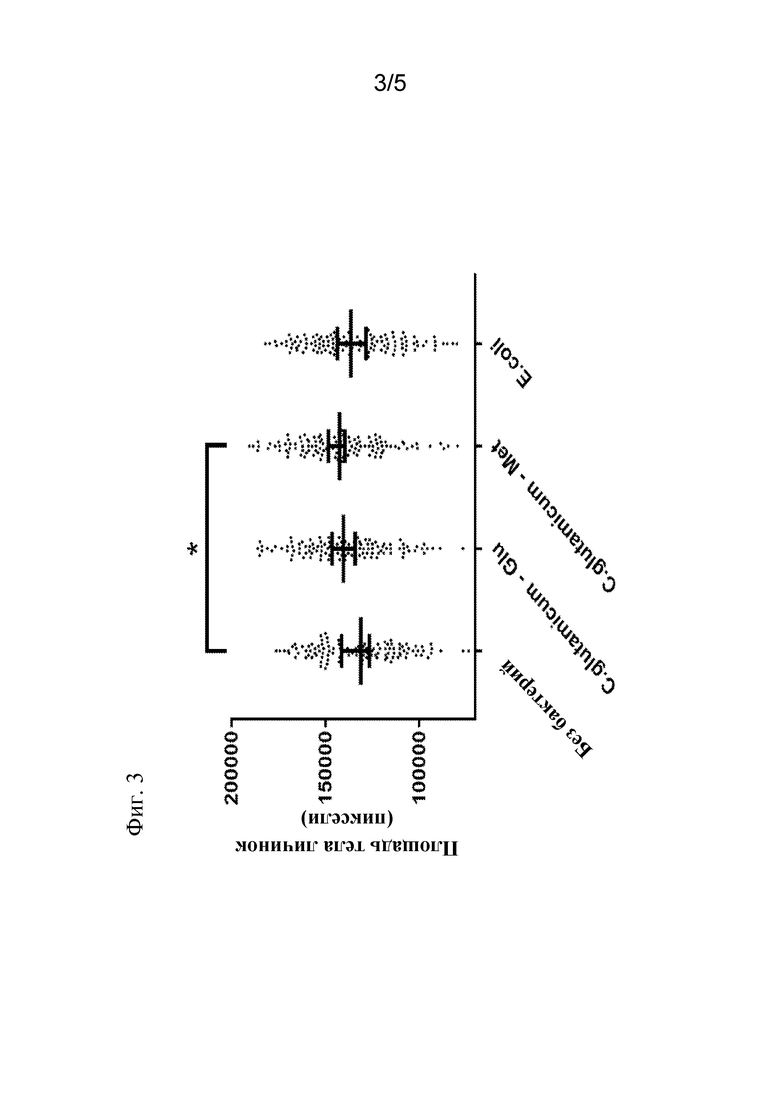
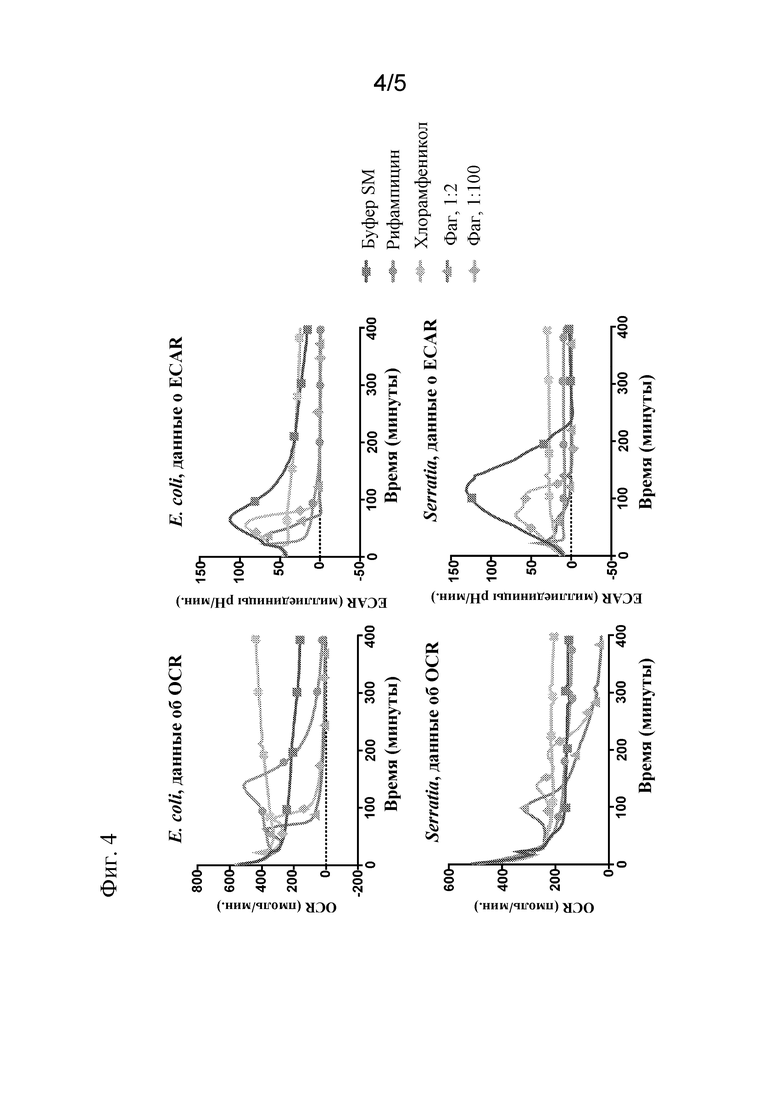
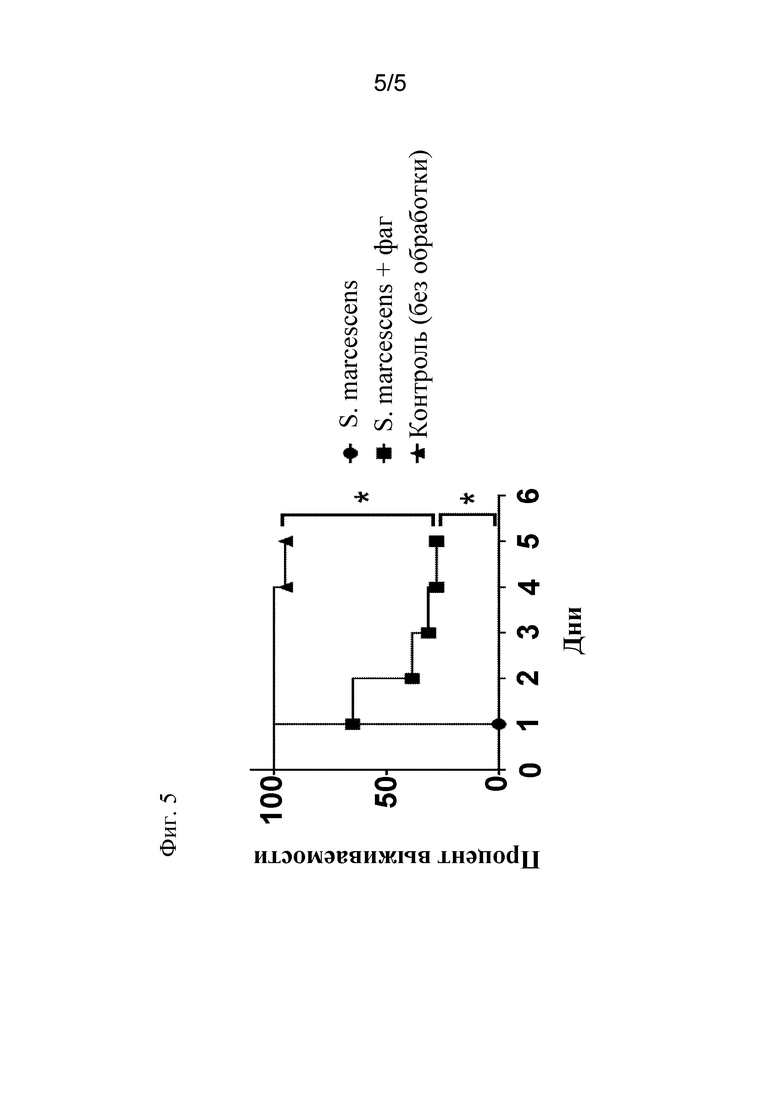
Изобретение относится к композиции и способу для применения в сельском хозяйстве. Способ повышения приспособленности медоносной пчелы к фосфорорганическим инсектицидам включает введение медоносной пчеле композиции, содержащей эффективное количество бактерий, метаболизирующих фосфорорганические инсектициды, составленных с носителем, съедобным для насекомых. Бактерии, метаболизирующие фосфорорганические инсектициды, выбраны из группы, состоящей из Snodgrassella spp., Bartonella spp., Parasaccharibacter spp. и Lactobacillus spp., и способны колонизировать кишечник пчелы, тем самым повышая ее приспособленность. Изобретение касается также композиции для повышения приспособленности медоносной пчелы к фосфорорганическим инсектицидам, содержащей эффективное количество бактерий, метаболизирующих фосфорорганические инсектициды, составленных с носителем, съедобным для насекомых. Техническим результатом является изменение уровня, активности или метаболизма одного или нескольких микроорганизмов, обитающих в организме хозяина, например медоносной пчелы, тем самым повышая приспособленность медоносной пчелы к фосфорорганическим инсектицидам. 2 н. и 8 з.п. ф-лы, 12 табл., 10 пр., 5 ил.
1. Способ повышения приспособленности медоносной пчелы к фосфорорганическим инсектицидам, при этом способ включает: введение медоносной пчеле композиции, содержащей эффективное количество бактерий, метаболизирующих фосфорорганические инсектициды, составленных с носителем, съедобным для насекомых, где бактерии, метаболизирующие фосфорорганические инсектициды, выбраны из группы, состоящей из Snodgrassella spp., Bartonella spp., Parasaccharibacter spp. и Lactobacillus spp., и способны колонизировать кишечник пчелы, тем самым повышая ее приспособленность.
2. Способ по п. 1, где введение включает доставку композиции в улей с медоносными пчелами или в по меньшей мере одну среду обитания, где медоносная пчела растет, живет, размножается или питается.
3. Способ по любому из пп. 1, 2, где композиция представляет собой жидкость, твердое вещество, аэрозоль, пасту, гель или газ.
4. Способ по любому из пп. 1-3, где фосфорорганический инсектицид представляет собой фенитротион.
5. Способ по любому из пп. 1-4, где носитель представляет собой средство для нанесения покрытия на семена.
6. Способ по любому из пп. 1-5, где медоносная пчела находится в колонии медоносных пчел.
7. Композиция для повышения приспособленности медоносной пчелы к фосфорорганическим инсектицидам, содержащая эффективное количество бактерий, метаболизирующих фосфорорганические инсектициды, составленных с носителем, съедобным для насекомых, в виде жидкости, твердого вещества, аэрозоля, пасты, геля или газа, где носитель представляет собой покрытие семян и где бактерии, метаболизирующие фосфорорганические инсектициды, выбраны из группы, состоящей из Snodgrassella spp., Bartonella spp., Parasaccharibacter spp. и Lactobacillus spp., и способны колонизировать кишечник пчелы.
8. Композиция по п. 7, где бактерии, метаболизирующие фосфорорганические инсектициды, метаболизируют фенитротион.
9. Композиция по п. 7 или 8, где бактерии, метаболизирующие фосфорорганические инсектициды, присутствуют в концентрации по меньшей мере 100000 клеток/мл.
10. Способ по любому из пп. 1-6, в котором бактерии, метаболизирующие фосфорорганические инсектициды, присутствуют в концентрации по меньшей мере 100000 клеток/мл.
| HEATHER AMOS "UBC students give bees a chance", The University of British Columbia, 18.09.2015, найдено в Интернет: https://news.ubc.ca/2015/09/18/ubc-students-give-bees-a-chance/ | |||
| US 5631024 A1, 20.05.1997 | |||
| СОСТАВ ДЛЯ СТИМУЛЯЦИИ РАЗВИТИЯ ПЧЕЛИНЫХ СЕМЕЙ, ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ АСКОСФЕРОЗА | 2014 |
|
RU2552672C1 |
| БИОТРИЛАКТ - БИОПРЕПАРАТ ДЛЯ ПОВЫШЕНИЯ ЖИЗНЕДЕЯТЕЛЬНОСТИ И АКТИВНОСТИ ПЧЕЛ В ЗАКРЫТОМ ГРУНТЕ | 2015 |
|
RU2579266C1 |
| СПОСОБ ПОВЫШЕНИЯ АДАПТИВНОГО СТАТУСА ПЧЕЛИНОЙ СЕМЬИ | 2012 |
|
RU2511304C2 |
| ПРЕПАРАТ ДЛЯ ПОВЫШЕНИЯ РЕЗИСТЕНТНОСТИ ПЧЕЛ, ПРОФИЛАКТИКИ ОТРАВЛЕНИЙ И СПОСОБ ПРОФИЛАКТИКИ ОТРАВЛЕНИЙ ПЧЕЛ ЯДОХИМИКАТАМИ | 2005 |
|
RU2305935C1 |
Авторы
Даты
2023-10-11—Публикация
2018-01-24—Подача