Изобретение относится к фармацевтической химии и онкологии, а именно к органическим соединениям для фотодинамического разрушения злокачественных опухолевых клеток.
Известен сенсибилизатор для фотодинамического разрушения клеток злокачественных новообразований [RU 2071320 C1, МПК A61K 31/40 (1995.01), C09B 47/00 (1995.01), опубл. 10.01.1997], который представляет собой сульфированный тетрафенилтетрабензопорфин общей формулы С60H38N4O12S4, оказывающий терапевтический эффект при облучении криптоновым лазером с длиной волны 675 нм в течение 15 минут.
Известен фотосенсибилизатор для фотодинамической терапии злокачественных новообразований [RU 2164136 C2, МПК A61K 31/409 (2000.01), А61Р 35/00 (2000.01), опубл. 20.03.2001], который представляет собой водорастворимое производное тетраазапорфириновых комплексов титанила общей формулы
RnLТiO,
где L - лиганд, представляющий собой производное тетраазапорфирина, выбранное из группы, включающей фталоцианин, нафталоцианин, тетрапиразинопорфиразин;
R - придающий растворимость в воде гидрофильный заместитель;
n = 3 - 10, число заместителей.
Этот фотосенсибилизатор оказывает воздействие на глубокие опухолевые ткани и другие патологические образования в условиях гипоксии при облучении патологического участка оптическим излучением в спектральном диапазоне 635-728 нм.
Известен фотосенсибилизатор для фотодинамической терапии рака [RU 2411943 C2, МПК (2006.01) A61K 31/409, A61K 9/10, A61N 5/067, A61P 35/00, C07D 487/22, B82B1/00, опубл. 20.10.2010], представляющий собой наноструктурированную водную дисперсию на основе производного бактериохлорина p, который представляет собой метиловый эфир O-этилоксима N-этоксициклоимида бактериохлорина p C38H46N6O6. Наноструктурированная водная дисперсия представляет собой липосомальную дисперсию на основе лецитина и холестерина, а метиловый эфир O-этилоксима N-этоксициклоимида бактериохлорина р включен в липидный бислой липосом.
Терапевтический эффект реализуется при облучении патологического участка оптическим излучением в спектральном диапазоне 790-810 нм.
Известен сенсибилизатор для фотодинамического разрушения опухолевых клеток [RU 2771237 C1, МПК (2006.01) С07В 257/08, A61K 31/395, А61К 41/00, A61P 35/00, опубл. 28.04.2022], выбранный в качестве прототипа, который представляет собой 1-(1-(4-нитрофенил)этил)-2,4,6-трифенил-1,4-дигидро-1,2,4,5-тетразин-3(2H)-он со структурной формулой:
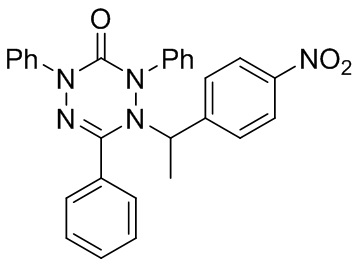
Фотосенсибилизирующие свойства данного соединения проявляются при световом воздействии с длиной волны 395-410 нм. Однако, данный сенсибилизатор обладает низкой растворимостью, что ограничивает его потенциальную биологическую эффективность.
Техническим результатом заявленного изобретения является расширение арсенала средств для фотодинамического разрушения опухолевых клеток.
В качестве фотосенсибилизатора предлагается 1-(1-(4-нитрофенил)этил)-2,4-дифенил-6-(4-(1-(2-(((2R,3R,4S,5S,6R)-3,4,5-тригидрокси-6-(гидроксиметил)тетрагидро-2H-пиран-2-ил)окси)этил)-1H-1,2,3-триазол-4-ил)фенил)-1,4-дигидро-1,2,4,5-тетразин-3(2H)-он со структурной формулой:

При световом воздействии с длиной волны 395 – 410 нм в течение 20 минут фотосенсибилизатор проявляет цитотоксическую активность.
Растворимость заявленного фотосенсибилизатора в водном растворе составляет 400 мкМ, что значительно превышает данный параметр у прототипа, растворимость которого составляет 25 мкМ.
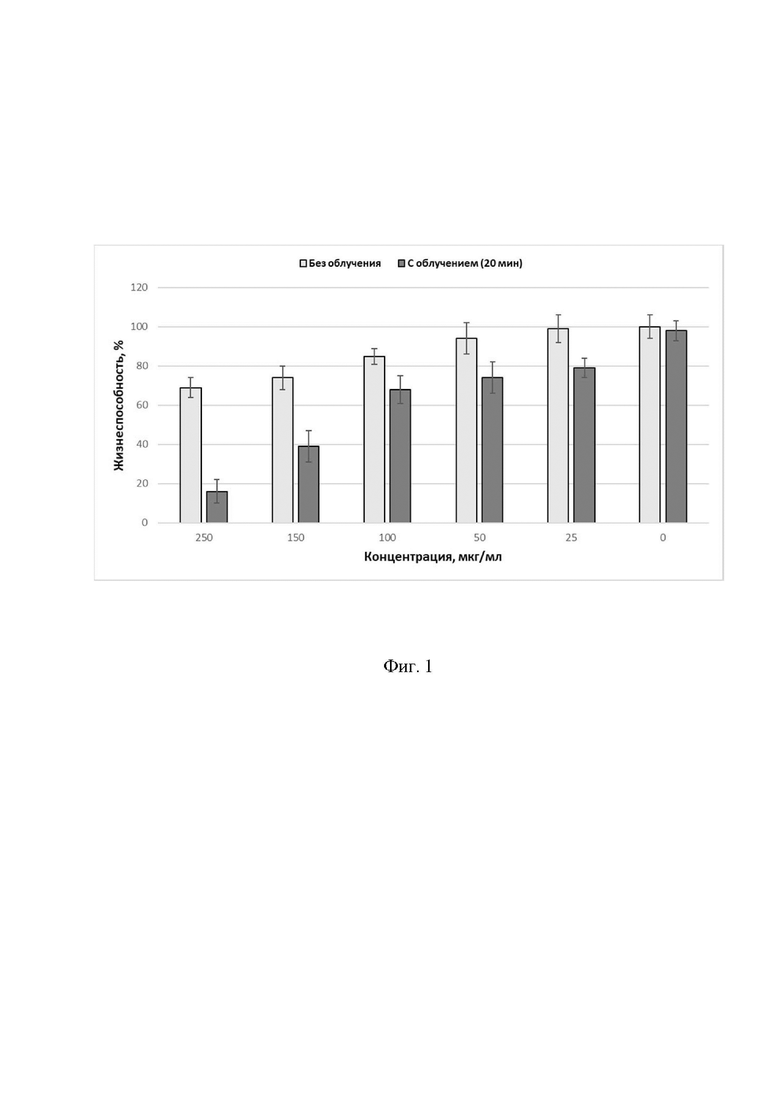
На фиг. 1 показана жизнеспособность опухолевых клеток после фотодинамического воздействия в присутствии фотосенсибилизатора.
Для получения фотосенсибилизатора в колбу внесли 501 мг (2R,3R,4S,5R,6R)-2-(ацетоксиметил)-6-(2-азидоэтокси)тетрагидро-2H-пиран-3,4,5-триил триацетат (417 мг) и 6-(4-этинилфенил)-1-(1-(4-нитрофенил)этил)-2,4-дифенил-1,4-дигидро-1,2,4,5-тетразин-3(2H)-он и вакуумировали в течение 1 часа при давлении 1 мбар, а затем заполнили аргоном с использованием линии Шленка. В колбу через септу шприцом добавили предварительно обескислороженные барботированием аргона 6 мл тетрагидрофурана и 3 мл воды, затем при перемешивании добавили 159 мг аскорбата натрия и 100 мг сульфата меди (II), полученную реакционную массу выдержали при температуре 70°С при постоянном перемешивании в атмосфере аргона в течение 2 часов. После этого реакционную массу охладили до комнатной температуры, растворитель удалили в вакууме на ротационном испарителе, остаток растворили в воде и экстрагировали этилацетатом 4 раза по 100 мл, органический слой отделили, осушили с использованием безводного сульфата магния, а затем упарили на ротационном испарителе в вакууме до объема 5 мл. Продукт реакции выделяли с использованием колоночной хроматографии на силикагеле в градиенте растворителей от гексан/этилацетат = 2/1 до гексан/этилацетат = 1/5. После упаривания и вакуумирования был получен серый порошок массой 573 мг, что составляет 62% от теоретического выхода тетраацетата 1-(1-(4-нитрофенил)этил)-2,4-дифенил-6-(4-(1-(2-(((2R,3R,4S,5S,6R)-3,4,5-тригидрокси-6-(гидроксиметил)тетрагидро-2H-пиран-2-ил)окси)этил)-1H-1,2,3-триазол-4-ил)фенил)-1,4-дигидро-1,2,4,5-тетразин-3(2H)-она.
Далее полученный порошок массой 460 мг растворили в 50 мл безводного метанола и добавили 40 мг метилата натрия, полученный раствор перемешивали при комнатной температуре в течение 2 часов. После этого pH раствора довели до значения 7 с использованием ионообменной смолы Amberlist® H15, после чего раствор отфильтровали на фильтре Шотта от ионообменной смолы, смолу на фильтре промыли метанолом 3 раза по 20 мл, после чего комбинированный раствор метанола упарили досуха в вакууме на ротационном испарителе.
Выделение целевого продукта осуществляли с использованием колоночной хроматографии на силикагеле в градиенте растворителей от дихлорметан/метанол 10/1 до дихлорметан/метанол 5/1, которая после упаривания и вакуумирования дала серый порошок массой 377 мг, что составляет 86% от теоретического выхода 1-(1-(4-нитрофенил)этил)-2,4-дифенил-6-(4-(1-(2-(((2R,3R,4S,5S,6R)-3,4,5-тригидрокси-6-(гидроксиметил)тетрагидро-2H-пиран-2-ил)окси)этил)-1H-1,2,3-триазол-4-ил)фенил)-1,4-дигидро-1,2,4,5-тетразин-3(2H)-она с общей формулой C44H44N8O12.
Фотосенсибилизирующие свойства заявленного соединения оценивали по уровню цитотоксического воздействия на культуру опухолевых клеток рака предстательной железы человека (линия РС-3) при воздействии светом с длиной волны 395-410 нм. Для этого клетки засевали в 96-луночный планшет в концентрации 5000 клеток в лунку в бесфенольной питательной среде RPMI 1640, с добавлением 10% эмбриональной телячьей сыворотки и антибиотиков. Далее клетки инкубировали в течение 24 часов при 37°С в среде 5% углекислого газа. После чего вносили заявленное соединение. Предварительно готовили серийные разведения заявленного соединения в питательной среде RPMI 1640 для культивирования клеточных культур в диапазоне концентраций 250-25 мкг/мл. Далее питательную среду в планшете с клетками заменяли на аналогичную, но содержащую заявленное соединение в концентрациях 250, 150, 100, 50, 25 мкг/мл в 6 повторах. В качестве контрольной группы использовали лунки с клетками, в которых меняли среду на свежую без добавления соединения. Среду без клеток использовали в качестве положительного контроля.
Далее планшет с клетками и внесенным соединением подвергали световому воздействию в течение 20 мин. Источник излучения: светодиодная матрица, состоящая из 5 столбцов по 7 светодиодов в столбце с междиодными расстояниями 18 мм в рядах и столбцах, диапазон излучения 395-410 нм (Thorlabs LED395L). Расстояние от светодиода до лунки с опухолевыми клетками составляло 2 см. Мощность излучения на уровне клеток - 5,5 мВт/см2, максимум излучения 395 нм.
Второй аналогичный планшет с клетками не подвергался световому воздействию, но подвергался всем остальным процедурам культивирования для оценки собственной токсичности соединения.
После светового воздействия клетки снова помещали в СО2 инкубатор при 37°С в среде 5% углекислого газа на 24 часа.
После завершения инкубации клеток проводили оценку жизнеспособности культуры с помощью МТТ-теста. Для этого из каждой лунки удаляли питательную среду и вносили 100 мкл раствора MTT-реагента (бромида 3-(4,5-диметилтиазол-2-ил)-2,5-дифенилтетразолия) в питательной среде RPMI 1640, далее планшеты помещали в СО2 инкубатор при 37°С на 4 часа. Затем из планшетов полностью удаляли среду и добавляли по 100 мкл диметилсульфоксида в каждую лунку для растворения образовавшихся кристаллов формазана. После этого измеряли оптическую плотность образцов с помощью микропланшетного фотоколориметра (MULTISCAN FC) при длине волны 570 нм. Жизнеспособность клеток рассчитывали по формуле:
жизнеспособность%= (ОПобр-ОПпуст)/(ОПконтр-ОПпуст)*100,
где, ОПобр-средняя оптическая плотность образцов клеток с внесенным фотосенсибилизатором;
ОПпуст – средняя оптическая плотность среды без клеток;
ОПконтр– средняя оптическая плотность контроля (клетки, не подвергавшиеся воздействию сенсибилизатора).
Результаты определения уровня жизнеспособности культуры клеток PC-3 после фотодинамического облучения с использованием заявляемого соединения и контрольной группы без облучения представлены на фиг. 1. Процент жизнеспособных клеток после фотодинамического воздействия в присутствии заявленного соединения в концентрациях 250-25 мкг/мл статистически ниже уровня контроля без препарата, и соответствующих контрольных точек с добавлением препарата, но без воздействия света (p<0,001).
Растворимость заявленного фотосенсибилизатора и сенсибилизатора-прототипа определяли следующим образом: навеску 20 мг соединения помещали в мерную колбу объемом 50 мл, колбу наполняли дистиллированной водой до метки, после чего помещали на ультразвуковую баню на 20 минут. После этого дисперсию переливали в пробирку для центрифугирования и осаждали нерастворившийся фотосенсибилизатор или сенсибилизатор-прототип на центрифуге при 10000 оборотах в минуту. Супернатант аккуратно переливали в мерную колбу для того, чтобы удалить из колбы весь не растворившийся осадок, после чего центрифугирование повторяли. После удаления супернатанта осадок высушивали сначала на воздухе, а затем при давлении 0,5 мбар, после чего взвешивали осадок и определяли концентрацию растворившегося вещества. Растворимость заявленного фотосенсибилизатора в водном растворе составила 400 мкМ, а растворимость сенсибилизатора - 25 мкМ.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ФОТОСЕНСИБИЛИЗАТОРА ДЛЯ ФОТОДИНАМИЧЕСКОГО РАЗРУШЕНИЯ ОПУХОЛЕВЫХ КЛЕТОК | 2023 |
|
RU2807293C1 |
| СЕНСИБИЛИЗАТОР ДЛЯ ФОТОДИНАМИЧЕСКОГО РАЗРУШЕНИЯ ОПУХОЛЕВЫХ КЛЕТОК | 2021 |
|
RU2771237C1 |
| ПРОИЗВОДНЫЕ МАННОЗЫ ДЛЯ ЛЕЧЕНИЯ БАКТЕРИАЛЬНЫХ ИНФЕКЦИЙ | 2013 |
|
RU2667060C2 |
| ПРОИЗВОДНЫЕ МАННОЗЫ ДЛЯ ЛЕЧЕНИЯ БАКТЕРИАЛЬНЫХ ИНФЕКЦИЙ | 2014 |
|
RU2678327C2 |
| Метод и реактивы для детекции активности люциферазы | 2020 |
|
RU2826202C2 |
| Иммуномодулирующие азалиды на основе мочевины | 2021 |
|
RU2811591C1 |
| БЕТА-ЛАКТАМЫ, СПОСОБ ПОЛУЧЕНИЯ УКАЗАННЫХ СОЕДИНЕНИЙ И СЫВОРОТОЧНЫЕ ГИПОХОЛЕСТЕРИНЕМИЧЕСКИЕ СРЕДСТВА, СОДЕРЖАЩИЕ ТАКИЕ СОЕДИНЕНИЯ | 2002 |
|
RU2301799C2 |
| С-ГЛИКОЗИДНЫЕ ПРОИЗВОДНЫЕ, СОДЕРЖАЩИЕ КОНДЕНСИРОВАННОЕ ФЕНИЛЬНОЕ КОЛЬЦО, ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ, СПОСОБ ПОЛУЧЕНИЯ ТАКОВЫХ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ТАКОВЫЕ | 2017 |
|
RU2739024C2 |
| ПРОИЗВОДНЫЕ ЦИКЛОГЕКСАНА ИЛИ ТЕТРАГИДРОПИРАНА, ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ, ИЛИ ГИДРАТЫ, ИЛИ СОЛЬВАТЫ ЭТИХ СОЕДИНЕНИЙ, ИЛИ ИХ СОЛЕЙ, ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ ДЛЯ ИХ ПОЛУЧЕНИЯ И ФУНГИЦИДНОЕ СРЕДСТВО | 1992 |
|
RU2084439C1 |
| КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ИНГИБИТОРЫ КОТРАНСПОРТЕРОВ НАТРИЯ-ГЛЮКОЗЫ 1 И 2, И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2012 |
|
RU2669921C2 |
Изобретение относится к фармацевтической химии и онкологии, а именно к органическим соединениям для фотодинамического разрушения злокачественных опухолевых клеток. Раскрывается фотосенсибилизатор для фотодинамического разрушения опухолевых клеток, который представляет собой 1-(1-(4-нитрофенил)этил)-2,4-дифенил-6-(4-(1-(2-(((2R,3R,4S,5S,6R)-3,4,5-тригидрокси-6-(гидроксиметил)тетрагидро-2H-пиран-2-ил)окси)этил)-1H-1,2,3-триазол-4-ил)фенил)-1,4-дигидро-1,2,4,5-тетразин-3(2H)-он со следующей структурной формулой (см.ниже). Изобретение обеспечивает эффективное фотодинамическое разрушение злокачественных опухолевых клеток. 1 ил.

Фотосенсибилизатор для фотодинамического разрушения опухолевых клеток, отличающийся тем, что он представляет собой 1-(1-(4-нитрофенил)этил)-2,4-дифенил-6-(4-(1-(2-(((2R,3R,4S,5S,6R)-3,4,5-тригидрокси-6-(гидроксиметил)тетрагидро-2H-пиран-2-ил)окси)этил)-1H-1,2,3-триазол-4-ил)фенил)-1,4-дигидро-1,2,4,5-тетразин-3(2H)-он со структурной формулой:
 .
.
| СЕНСИБИЛИЗАТОР ДЛЯ ФОТОДИНАМИЧЕСКОГО РАЗРУШЕНИЯ ОПУХОЛЕВЫХ КЛЕТОК | 2021 |
|
RU2771237C1 |
| D | |||
| E | |||
| VOTKINA et al | |||
| Kinetic investigation of thermal and photoinduced homolysis of alkylated verdazyls | |||
| Phys | |||
| Chem., 2020, vol.22, pp.21881-21887 | |||
| D | |||
| E | |||
| VOTKINA et al | |||
| Alkylverdazyls as a Source of Alkyl Radicals for Light-Triggered Cancer Cell Death | |||
| Molecular Pharmaceutics, 2022, vol.19 (1), pp.354-357 | |||
| Е | |||
| С | |||
Авторы
Даты
2023-10-11—Публикация
2023-03-17—Подача