Изобретение относится к области фармацевтической химии и онкологии, а именно к способам получения органических соединений для фотодинамического разрушения опухолевых клеток.
Фотосенсибилизаторы - это соединения, которые при поглощении света подвергаются химическому и физическому изменению состояния, что приводит к появлению активных молекул или фрагментов, оказывающих повреждающее биологическое действие. Фотосенсибилизирующими свойствами обладают вещества из разных химических групп, поэтому существуют различные способы их получения.
Известен способ получения фотосенсибилизатора [RU 2416614 C2 МПК (2006.01) C07D 487/22, A61P 35/00, A61K 31/409, опубл.: 20.04.2011], который заключается в обработке суспензии лиофильно высушенной спирулины в метаноле или абсолютном спирте до получения алкилфеофорбида и с взаимодействием последнего, например, с этилендиамином, предпочтительно, в органическом растворителе, выделении соответствующего эфира моноамида хлорина е 6, его растворении в спирте и добавлении адипиновой кислоты в мольном соотношении 2:1.
Известен способ получения сенсибилизатора для фотодинамического разрушения опухолевых клеток [RU 2771237 C1, МПК (2006.01) С07В 257/08, A61K 31/395, А61К 41/00, A61P 35/00, опубл. 28.04.2022], который представляет собой 1-(1-(4-нитрофенил)этил)-2,4,6-трифенил-1,4-дигидро-1,2,4,5-тетразин-3(2H)-он со структурной формулой:
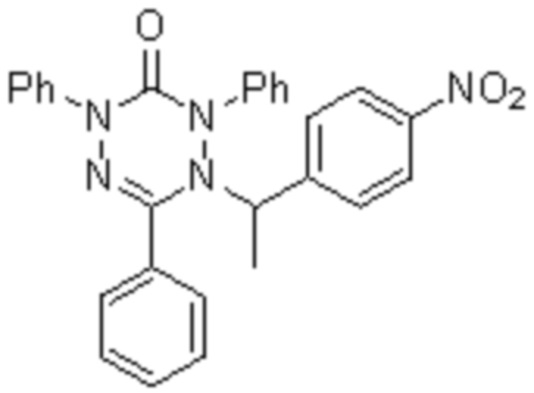
Для получения такого сенсибилизатора в двугорлую круглодонную колбу объемом 100 мл вносят 76 мг обескислороженной суспензии порошка меди и 86 мг бромида меди (I) в 30 мл бензола, а затем добавляют 125 мкл N,N,N′,N′′,N′′-пентаметилдиэтилентриамина. К полученной смеси добавляют обескислороженный раствор, полученный растворением 327 мг 1,3,5-трифенилвердазильного радикала и 276 мг 1-(1-бромоэтил)-4-нитробензола в 20 мл бензола. Полученную реакционную массу кипятят 8 часов с обратным холодильником Димрота в атмосфере аргона, который подают из линии Шленка. После охлаждения на воздухе до комнатной температуры полученную реакционную массу пропускают через 3 см слоя силикагеля, а затем силикагель дополнительно промывают 15 мл бензола для полного переноса продукта в маточник. Полученный маточный раствор упаривают в вакууме в круглодонной колбе с помощью ротационного испарителя до 3-4 мл итогового раствора. После этого в колбу с концентрированным раствором добавляют 50 мл гексана для осаждения продукта. Выпавший продукт отфильтровывают на фильтре Шотта, присоединенного к колбе Бунзена под абсолютным давлением 800 мбар, промывают гексаном 100 мл и сушат на воздухе в темноте.
В результате получают кристаллическое вещество бледно-желтого цвета с формулой C28H23N5O3.
Фотосенсибилизирующие свойства этого соединения проявляются при световом воздействии с длиной волны 395-410 нм.
Однако, данный сенсибилизатор обладает низкой растворимостью, что ограничивает его потенциальную биологическую эффективность.
Техническим результатом заявленного изобретения является расширения арсенала средств для фотодинамического разрушения опухолевых клеток
Способ получения фотосенсибилизатора для фотодинамического разрушения опухолевых клеток со структурной формулой:
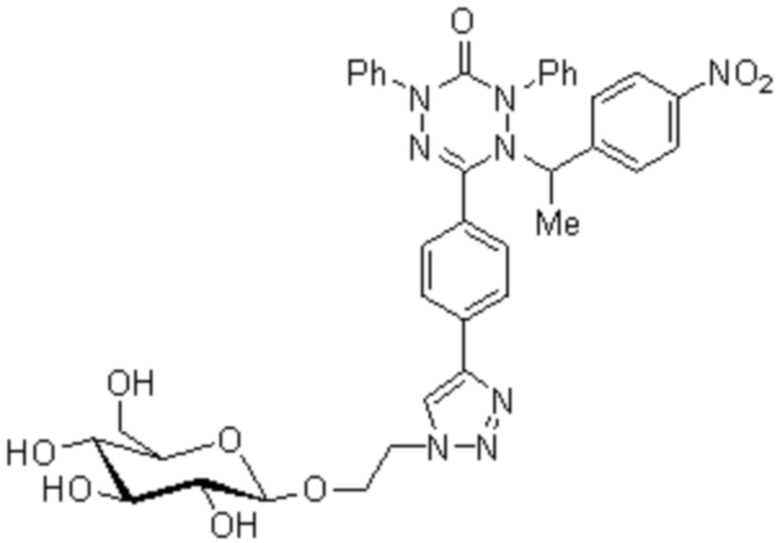 ,
,
включает взаимодействие 1 мольного эквивалента (2R,3R,4S,5R,6R)-2-(ацетоксиметил)-6-(2-азидоэтокси)тетрагидро-2H-пиран-3,4,5-триил триацетата с 1 мольным эквивалентом 6-(4-этинилфенил)-1-(1-(4-нитрофенил)этил)-2,4-дифенил-1,4-дигидро-1,2,4,5-тетразин-3(2H)-она в обескислороженной смеси тетрагидрофурана и воды, полученной при их соотношении 6:3 мл на 1 ммоль (2R,3R,4S,5R,6R)-2-(ацетоксиметил)-6-(2-азидоэтокси)тетрагидро-2H-пиран-3,4,5-триил триацетата) в присутствии 0,8 мольных эквивалентов аскорбата натрия и 0,4 мольных эквивалентов сульфата меди (II) при температуре 70°С при постоянном перемешивании в атмосфере аргона в течение 2 часов. После этого реакционную массу охлаждают до комнатной температуры, растворитель удаляют в вакууме, остаток растворяют в воде и экстрагируют этилацетатом. Органический слой отделяют, сушат с использованием безводного сульфата магния, а затем упаривают. Продукт реакции выделяют колоночной хроматографией на силикагеле с использованием гексана и этилацетата. Далее 1 мольный эквивалент полученного продукта растворяют в 100 мл безводного метанола на 1 ммоль тетраацетата 1-(1-(4-нитрофенил)этил)-2,4-дифенил-6-(4-(1-(2-(((2R,3R,4S,5S,6R)-3,4,5-тригидрокси-6-(гидроксиметил)тетрагидро-2H-пиран-2-ил)окси)этил)-1H-1,2,3-триазол-4-ил)фенил)-1,4-дигидро-1,2,4,5-тетразин-3(2H)-она и добавляют 1,5 мольных эквивалента метилата натрия, перемешивают при комнатной температуре в течение 2 часов, pH раствора доводят до 7, используя ионообменную смолу. Затем раствор отфильтровывают от ионообменной смолы, смолу на фильтре промывают метанолом 3 раза и комбинированный раствор метанола упаривают досуха в вакууме на ротационном испарителе. Целевой продукт выделяют колоночной хроматографией на силикагеле с использованием дихлорметана и метанола. В результате получают 1-(1-(4-нитрофенил)этил)-2,4-дифенил-6-(4-(1-(2-(((2R,3R,4S,5S,6R)-3,4,5-тригидрокси-6-(гидроксиметил)тетрагидро-2H-пиран-2-ил)окси)этил)-1H-1,2,3-триазол-4-ил)фенил)-1,4-дигидро-1,2,4,5-тетразин-3(2H)-она с общей формулой C44H44N8O12.
Полученный фотосенсибилизатор проявляет цитотоксическую активность при световом воздействии с длиной волны 395 - 410 нм в течение 20 минут.
Растворимость полученного фотосенсибилизатора в водном растворе составляет 400 мкМ, что значительно превышает данный параметр сенсибилизатора, полученного способом-прототипом, растворимость которого составляет 25 мкМ.
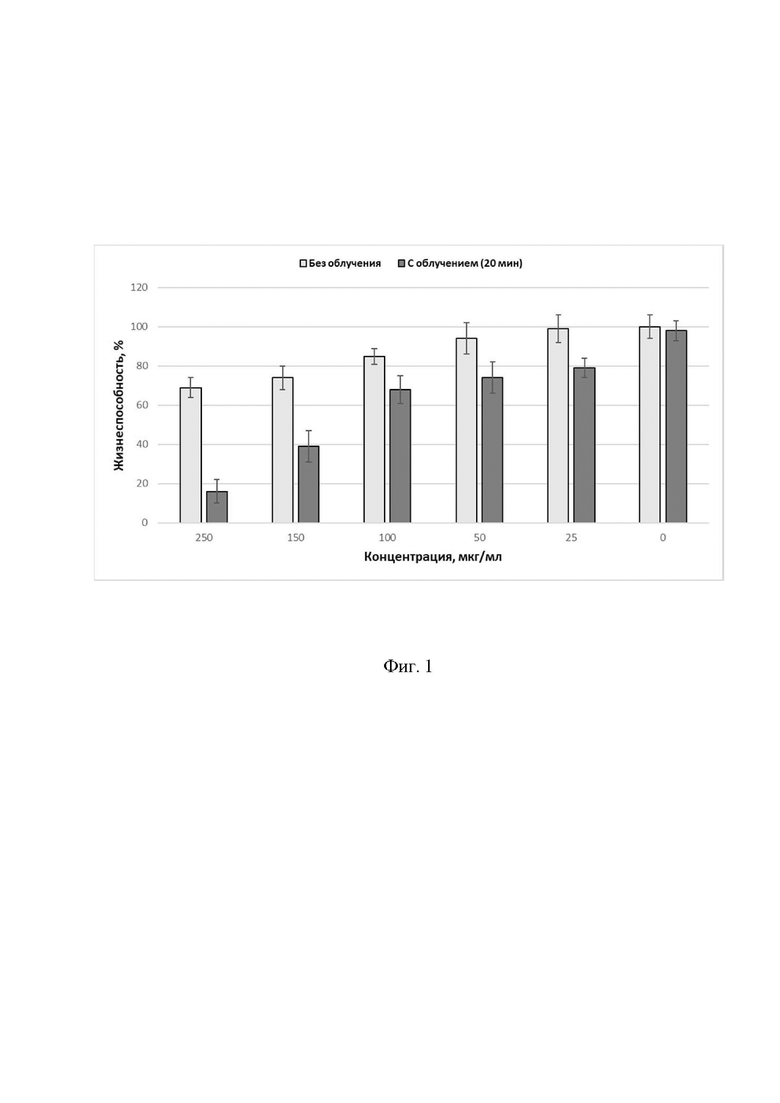
На фиг. 1 показана жизнеспособность опухолевых клеток после фотодинамического воздействия в присутствии фотосенсибилизатора.
Для получения фотосенсибилизатора в колбу внесли 501 мг (2R,3R,4S,5R,6R)-2-(ацетоксиметил)-6-(2-азидоэтокси)тетрагидро-2H-пиран-3,4,5-триил триацетат (417 мг) и 6-(4-этинилфенил)-1-(1-(4-нитрофенил)этил)-2,4-дифенил-1,4-дигидро-1,2,4,5-тетразин-3(2H)-он и вакуумировали в течение 1 часа при давлении 1 мбар, а затем заполнили аргоном с использованием линии Шленка. В колбу через септу шприцом добавили предварительно обескислороженные барботированием аргона 6 мл тетрагидрофурана и 3 мл воды, затем при перемешивании добавили 159 мг аскорбата натрия и 100 мг сульфата меди (II), полученную реакционную массу выдержали при температуре 70°С при постоянном перемешивании в атмосфере аргона в течение 2 часов. После этого реакционную массу охладили до комнатной температуры, растворитель удалили в вакууме на ротационном испарителе, остаток растворили в воде и экстрагировали этилацетатом 4 раза по 100 мл, органический слой отделили, осушили с использованием безводного сульфата магния, а затем упарили на ротационном испарителе в вакууме до объема 5 мл. Продукт реакции выделяли с использованием колоночной хроматографии на силикагеле в градиенте растворителей от гексан/этилацетат = 2/1 до гексан/этилацетат = 1/5. После упаривания и вакуумирования был получен серый порошок массой 573 мг, что составляет 62% от теоретического выхода тетраацетата 1-(1-(4-нитрофенил)этил)-2,4-дифенил-6-(4-(1-(2-(((2R,3R,4S,5S,6R)-3,4,5-тригидрокси-6-(гидроксиметил)тетрагидро-2H-пиран-2-ил)окси)этил)-1H-1,2,3-триазол-4-ил)фенил)-1,4-дигидро-1,2,4,5-тетразин-3(2H)-она.
Далее полученный порошок массой 460 мг растворили в 50 мл безводного метанола и добавили 40 мг метилата натрия, полученный раствор перемешивали при комнатной температуре в течение 2 часов. После этого pH раствора довели до значения 7 с использованием ионообменной смолы Amberlist® H15, после чего раствор отфильтровали на фильтре Шотта от ионообменной смолы, смолу на фильтре промыли метанолом 3 раза по 20 мл, после чего комбинированный раствор метанола упарили досуха в вакууме на ротационном испарителе.
Выделение целевого продукта осуществляли с использованием колоночной хроматографии на силикагеле в градиенте растворителей от дихлорметан/метанол 10/1 до дихлорметан/метанол 5/1, которая после упаривания и вакуумирования дала серый порошок массой 377 мг, что составляет 86% от теоретического выхода 1-(1-(4-нитрофенил)этил)-2,4-дифенил-6-(4-(1-(2-(((2R,3R,4S,5S,6R)-3,4,5-тригидрокси-6-(гидроксиметил)тетрагидро-2H-пиран-2-ил)окси)этил)-1H-1,2,3-триазол-4-ил)фенил)-1,4-дигидро-1,2,4,5-тетразин-3(2H)-она с общей формулой C44H44N8O12.
Фотосенсибилизирующие свойства полученного продукта оценивали по уровню цитотоксического воздействия на культуру опухолевых клеток рака предстательной железы человека (линия РС-3) при воздействии светом с длиной волны 395-410 нм. Для этого клетки засевали в 96-луночный планшет в концентрации 5000 клеток в лунку в бесфенольной питательной среде RPMI 1640, с добавлением 10% эмбриональной телячьей сыворотки и антибиотиков. Далее клетки инкубировали в течение 24 часов при 37°С в среде 5% углекислого газа. После чего вносили полученный продукт. Предварительно готовили серийные разведения полученного продукта в питательной среде RPMI 1640 для культивирования клеточных культур в диапазоне концентраций 250-25 мкг/мл. Далее питательную среду в планшете с клетками заменяли на аналогичную, но содержащую полученный продукт в концентрациях 250, 150, 100, 50, 25 мкг/мл в 6 повторах. В качестве контрольной группы использовали лунки с клетками, в которых меняли среду на свежую без добавления соединения. Среду без клеток использовали в качестве положительного контроля.
Далее планшет с клетками и внесенным продуктом подвергали световому воздействию в течение 20 мин. Источник излучения: светодиодная матрица, состоящая из 5 столбцов по 7 светодиодов в столбце с междиодными расстояниями 18 мм в рядах и столбцах, диапазон излучения 395-410 нм (Thorlabs LED395L). Расстояние от светодиода до лунки с опухолевыми клетками составляло 2 см. Мощность излучения на уровне клеток - 5,5 мВт/см2, максимум излучения 395 нм.
Второй аналогичный планшет с клетками не подвергали световому воздействию, но подвергали всем остальным процедурам культивирования для оценки собственной токсичности полученного продукта.
После светового воздействия клетки снова помещали в СО2 инкубатор при 37°С в среде 5% углекислого газа на 24 часа.
После завершения инкубации клеток проводили оценку жизнеспособности культуры с помощью МТТ-теста. Для этого из каждой лунки удаляли питательную среду и вносили 100 мкл раствора MTT-реагента (бромида 3-(4,5-диметилтиазол-2-ил)-2,5-дифенилтетразолия) в питательной среде RPMI 1640, далее планшеты помещали в СО2 инкубатор при 37°С на 4 часа. Затем из планшетов полностью удаляли среду и добавляли по 100 мкл диметилсульфоксида в каждую лунку для растворения образовавшихся кристаллов формазана. После этого измеряли оптическую плотность образцов с помощью микропланшетного фотоколориметра (MULTISCAN FC) при длине волны 570 нм. Жизнеспособность клеток рассчитывали по формуле:
жизнеспособность%= (ОПобр-ОПпуст)/(ОПконтр-ОПпуст)*100,
где, ОПобр - средняя оптическая плотность образцов клеток с внесенным фотосенсибилизатором;
ОПпуст - средняя оптическая плотность среды без клеток;
ОПконтр - средняя оптическая плотность контроля (клетки, не подвергавшиеся воздействию сенсибилизатора).
Результаты определения уровня жизнеспособности культуры клеток PC-3 после фотодинамического облучения с использованием полученного продукта и контрольной группы без облучения представлены на фиг. 1. Процент жизнеспособных клеток после фотодинамического воздействия в присутствии полученного фотосенсибилизатора в концентрациях 250-25 мкг/мл статистически ниже уровня контроля без фотосенсибилизатора, и соответствующих контрольных точек с добавлением, фотосенсибилизатора, но без воздействия света (p<0,001).
Растворимость полученного предложенным способом фотосенсибилизатора и сенсибилизатора, полученного способом-прототипом, определяли следующим образом: навеску 20 мг соединения помещали в мерную колбу объемом 50 мл, колбу наполняли дистиллированной водой до метки, после чего помещали на ультразвуковую баню на 20 минут. После этого дисперсию переливали в пробирку для центрифугирования и осаждали не растворившийся фотосенсибилизатор или сенсибилизатор-прототип на центрифуге при 10000 оборотах в минуту. Супернатант аккуратно переливали в мерную колбу для того, чтобы удалить из колбы весь не растворившийся осадок, после чего центрифугирование повторяли. После удаления супернатанта осадок высушивали сначала на воздухе, а затем при давлении 0,5 мбар, после чего взвешивали осадок и определяли концентрацию растворившегося вещества. Растворимость полученного предложенным способом фотосенсибилизатора в водном растворе составила 400 мкМ, а растворимость сенсибилизатора, полученного способом-протипом - 25 мкМ.
| название | год | авторы | номер документа |
|---|---|---|---|
| ФОТОСЕНСИБИЛИЗАТОР ДЛЯ ФОТОДИНАМИЧЕСКОГО РАЗРУШЕНИЯ ОПУХОЛЕВЫХ КЛЕТОК | 2023 |
|
RU2805148C1 |
| Метод и реактивы для детекции активности люциферазы | 2020 |
|
RU2826202C2 |
| ПРОИЗВОДНЫЕ МАННОЗЫ ДЛЯ ЛЕЧЕНИЯ БАКТЕРИАЛЬНЫХ ИНФЕКЦИЙ | 2013 |
|
RU2667060C2 |
| ПРОИЗВОДНЫЕ МАННОЗЫ ДЛЯ ЛЕЧЕНИЯ БАКТЕРИАЛЬНЫХ ИНФЕКЦИЙ | 2014 |
|
RU2678327C2 |
| БЕТА-ЛАКТАМЫ, СПОСОБ ПОЛУЧЕНИЯ УКАЗАННЫХ СОЕДИНЕНИЙ И СЫВОРОТОЧНЫЕ ГИПОХОЛЕСТЕРИНЕМИЧЕСКИЕ СРЕДСТВА, СОДЕРЖАЩИЕ ТАКИЕ СОЕДИНЕНИЯ | 2002 |
|
RU2301799C2 |
| СЕНСИБИЛИЗАТОР ДЛЯ ФОТОДИНАМИЧЕСКОГО РАЗРУШЕНИЯ ОПУХОЛЕВЫХ КЛЕТОК | 2021 |
|
RU2771237C1 |
| Иммуномодулирующие азалиды на основе мочевины | 2021 |
|
RU2811591C1 |
| ПРОИЗВОДНЫЕ ЦИКЛОГЕКСАНА ИЛИ ТЕТРАГИДРОПИРАНА, ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ, ИЛИ ГИДРАТЫ, ИЛИ СОЛЬВАТЫ ЭТИХ СОЕДИНЕНИЙ, ИЛИ ИХ СОЛЕЙ, ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ ДЛЯ ИХ ПОЛУЧЕНИЯ И ФУНГИЦИДНОЕ СРЕДСТВО | 1992 |
|
RU2084439C1 |
| СИНТЕЗ АНТИБАКТЕРИАЛЬНЫХ АМИНОГЛИКОЗИДНЫХ АНАЛОГОВ | 2018 |
|
RU2798844C2 |
| С-ГЛИКОЗИДНЫЕ ПРОИЗВОДНЫЕ, СОДЕРЖАЩИЕ КОНДЕНСИРОВАННОЕ ФЕНИЛЬНОЕ КОЛЬЦО, ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ, СПОСОБ ПОЛУЧЕНИЯ ТАКОВЫХ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ТАКОВЫЕ | 2017 |
|
RU2739024C2 |
Изобретение относится к области органической и фармацевтической химии, а именно к способу получения органического соединения для фотодинамического разрушения опухолевых клеток. Раскрывается способ получения фотосенсибилизатора для фотодинамического разрушения опухолевых клеток с указанной структурной формулой, включающий взаимодействие 1 мольного эквивалента (2R,3R,4S,5R,6R)-2-(ацетоксиметил)-6-(2-азидоэтокси)тетрагидро-2H-пиран-3,4,5-триил триацетата с 1 мольным эквивалентом 6-(4-этинилфенил)-1-(1-(4-нитрофенил)этил)-2,4-дифенил-1,4-дигидро-1,2,4,5-тетразин-3(2H)-она в обескислороженной смеси тетрагидрофурана и воды, полученной при их соотношении 6:3 мл на 1 ммоль (2R,3R,4S,5R,6R)-2-(ацетоксиметил)-6-(2-азидоэтокси)тетрагидро-2H-пиран-3,4,5-триил триацетата в присутствии 0,8 мольных эквивалентов аскорбата натрия и 0,4 мольных эквивалентов сульфата меди (II) при температуре 70°С при постоянном перемешивании в атмосфере аргона в течение 2 часов, после этого реакционную массу охлаждают до комнатной температуры, растворитель удаляют в вакууме, остаток растворяют в воде и экстрагируют этилацетатом, органический слой отделяют, сушат с использованием безводного сульфата магния, а затем упаривают, продукт реакции выделяют колоночной хроматографией на силикагеле с использованием гексана и этилацетата, далее 1 мольный эквивалент полученного продукта растворяют в 100 мл безводного метанола на 1 ммоль тетраацетата 1-(1-(4-нитрофенил)этил)-2,4-дифенил-6-(4-(1-(2-(((2R,3R,4S,5S,6R)-3,4,5-тригидрокси-6-(гидроксиметил)тетрагидро-2H-пиран-2-ил)окси)этил)-1H-1,2,3-триазол-4-ил)фенил)-1,4-дигидро-1,2,4,5-тетразин-3(2H)-она и добавляют 1,5 мольных эквивалента метилата натрия, перемешивают при комнатной температуре в течение 2 часов, pH раствора доводят до 7, используя ионообменную смолу, затем раствор отфильтровывают от ионообменной смолы, смолу на фильтре промывают метанолом 3 раза и комбинированный раствор метанола упаривают досуха в вакууме на ротационном испарителе, целевой продукт выделяют колоночной хроматографией на силикагеле с использованием дихлорметана и метанола, в результате чего получают 1-(1-(4-нитрофенил)этил)-2,4-дифенил-6-(4-(1-(2-(((2R,3R,4S,5S,6R)-3,4,5-тригидрокси-6-(гидроксиметил)тетрагидро-2H-пиран-2-ил)окси)этил)-1H-1,2,3-триазол-4-ил)фенил)-1,4-дигидро-1,2,4,5-тетразин-3(2H)-она с общей формулой C44H44N8O12. Изобретение обеспечивает получение нового фотосенсибилизатора, который проявляет цитотоксическую активность при световом воздействии с длиной волны 395-410 нм в течение 20 минут, а его растворимость в водном растворе составляет 400 мкМ. 1 ил., 1 пр.
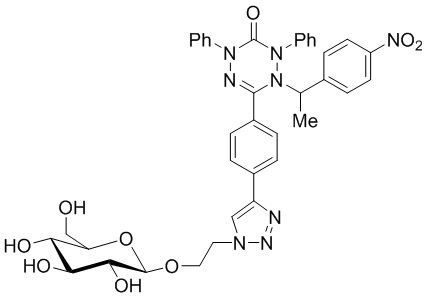
Способ получения фотосенсибилизатора для фотодинамического разрушения опухолевых клеток со структурной формулой
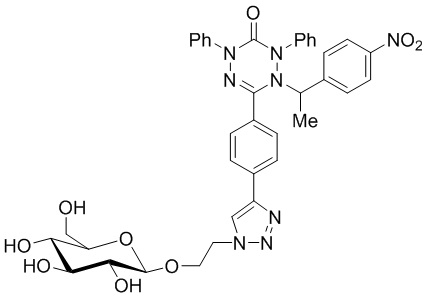 ,
,
включающий взаимодействие 1 мольного эквивалента (2R,3R,4S,5R,6R)-2-(ацетоксиметил)-6-(2-азидоэтокси)тетрагидро-2H-пиран-3,4,5-триил триацетата с 1 мольным эквивалентом 6-(4-этинилфенил)-1-(1-(4-нитрофенил)этил)-2,4-дифенил-1,4-дигидро-1,2,4,5-тетразин-3(2H)-она в обескислороженной смеси тетрагидрофурана и воды, полученной при их соотношении 6:3 мл на 1 ммоль (2R,3R,4S,5R,6R)-2-(ацетоксиметил)-6-(2-азидоэтокси)тетрагидро-2H-пиран-3,4,5-триил триацетата) в присутствии 0,8 мольных эквивалентов аскорбата натрия и 0,4 мольных эквивалентов сульфата меди (II) при температуре 70°С при постоянном перемешивании в атмосфере аргона в течение 2 часов, после этого реакционную массу охлаждают до комнатной температуры, растворитель удаляют в вакууме, остаток растворяют в воде и экстрагируют этилацетатом, органический слой отделяют, сушат с использованием безводного сульфата магния, а затем упаривают, продукт реакции выделяют колоночной хроматографией на силикагеле с использованием гексана и этилацетата, далее 1 мольный эквивалент полученного продукта растворяют в 100 мл безводного метанола на 1 ммоль тетраацетата 1-(1-(4-нитрофенил)этил)-2,4-дифенил-6-(4-(1-(2-(((2R,3R,4S,5S,6R)-3,4,5-тригидрокси-6-(гидроксиметил)тетрагидро-2H-пиран-2-ил)окси)этил)-1H-1,2,3-триазол-4-ил)фенил)-1,4-дигидро-1,2,4,5-тетразин-3(2H)-она и добавляют 1,5 мольных эквивалента метилата натрия, перемешивают при комнатной температуре в течение 2 часов, pH раствора доводят до 7, используя ионообменную смолу, затем раствор отфильтровывают от ионообменной смолы, смолу на фильтре промывают метанолом 3 раза и комбинированный раствор метанола упаривают досуха в вакууме на ротационном испарителе, целевой продукт выделяют колоночной хроматографией на силикагеле с использованием дихлорметана и метанола, в результате чего получают 1-(1-(4-нитрофенил)этил)-2,4-дифенил-6-(4-(1-(2-(((2R,3R,4S,5S,6R)-3,4,5-тригидрокси-6-(гидроксиметил)тетрагидро-2H-пиран-2-ил)окси)этил)-1H-1,2,3-триазол-4-ил)фенил)-1,4-дигидро-1,2,4,5-тетразин-3(2H)-она с общей формулой C44H44N8O12.
| СЕНСИБИЛИЗАТОР ДЛЯ ФОТОДИНАМИЧЕСКОГО РАЗРУШЕНИЯ ОПУХОЛЕВЫХ КЛЕТОК | 2021 |
|
RU2771237C1 |
| D | |||
| E | |||
| VOTKINA et al | |||
| Kinetic investigation of thermal and photoinduced homolysis of alkylated verdazyls | |||
| Phys | |||
| Chem., 2020, vol.22, pp.21881-21887 | |||
| D | |||
| E | |||
| VOTKINA et al | |||
| Alkylverdazyls as a Source of Alkyl Radicals for Light-Triggered Cancer Cell Death | |||
| Molecular Pharmaceutics, 2022, vol.19 (1), pp.354-357 | |||
| Е | |||
| С | |||
Авторы
Даты
2023-11-13—Публикация
2023-03-17—Подача