Изобретение относится к медицине, а именно к радиационной онкологии, и может быть использовано для снижения лучевой нагрузки на прямую кишку при лечении рака предстательной железы (РПЖ).
Топография органов малого таза определяет виды лучевой токсичности, регистрируемых после облучения предстательной железы (ПЖ). Наибольшее значение имеют ранние и поздние осложнения со стороны прямой кишки. Длительное время в клинической практике использовались два способа повышения безопасности лучевой терапии, которые заключались в выборе оптимального режима фракционирования, основанного на особенностях радиобиологии опухолевой и нормальных тканей, а также и применении радиомодификаторов. В последние годы приобретает популярность новый путь снижения лучевой токсичности, связанный с механическим увеличением расстояния от облучаемого объема до критических органов. Эта идея реализуется за счет введения в ткани биодеградирующих субстанций (БДС) или спейсеров (англ. - space), вызывающих временное изменение пространственного взаимоотношения между органами. Анатомия ПЖ позволяют максимально продемонстрировать преимущества такого подхода:
1. прилежание передней стенки прямой кишки к облучаемой мишени (ПЖ), что гарантирует ее попадание в зону высокой дозы;
2. наличие клетчатки между апоневрозом Денонвилье, покрывающим ПЖ и прямую кишку;
3. возможность относительно простого введения БДС через кожные покровы промежности.
Известен способ снижения лучевой нагрузки при лечении РПЖ путем промежностного введения гиалуроновой кислоты при РПЖ (Prada P.J., Fernandez J., Martinez A.A. et al. Transperineal injection of hyaluronic acid in anterior perirectal fat to decrease rectal toxicity from radiation delivered with intensity modulated brachytherapy or EBRT for prostate cancer patients. Int J Radiat Oncol Biol Phys. 2007 Sep 1;69(1):95-102. DOI: 10.1016/j.ijrobp.2007.02.034).
Наибольший опыт применения в качестве БДС имеет препарат «SpaceOAR®» (Boston Scientific (США)), состоящим из полиэтиленгликолевого гидрогеля (ПЭГ). В конце 2020 г. в странах Западной Европы зарегистрирован и внедрен в клиническую практику первый спейсер на основе гиалуроновой кислоты - «Barrigel®» (Palette Life Sciences (США)).
В настоящее время в Российской Федерации (РФ) ни один из перечисленных препаратов не разрешен для клинического применения. Кроме того, высокая стоимость этих БДС (2 500-3 000 $) будет существенным ограничением для их широкого применения в радиотерапевтической практике даже при условии их регистрации на территории РФ. Отечественные аналоги, которые бы могли успешно заменить зарубежные БДС, также отсутствуют.
Единственный на данный момент опыт использования при лучевом лечении РПЖ в качестве спейсера другого распространенного биополимера - коллагена, опубликован в 2012 году. (Noyes W.R., Hosford С.С., Schultz S.E. Human collagen injections to reduce rectal dose during radiotherapy. Int J Radiat Oncol Biol Phys 2012; 82(5): 1918-22. DOI: 10.1016/j.ijrobp.2011.02.034). В данной работе авторы описали методику введения и фармакокинетику препарата «Cymetra®» (измельченная форма «AlloDerm®») у 11 пациентов РПЖ, получивших лечение в виде дистанционной лучевой терапии (суммарная очаговая доза 75,6 Гр). «Cymetra®» - инъекционный материал, изготовленный из кожи трупа человека, полученный посредством специальной технологии обработки, обеспечивающей антигенную и аллергическую безопасность. Основной сферой применения этого препарата является оториноларингология, где он выполняет объем-образующую функцию, помогая восстановить закрытие голосовых связок (старческие атрофические изменения, болезнь Паркинсона, парез и паралич голосовых связок). В исследовании Noyes W.R. и соавт. среднее значение созданного между предстательной железой и передней стенкой прямой кишки расстояния составило 12,7 мм (8-19 мм), а снижение дозной нагрузки на последнюю - около 50%. Стабильность препарата была умеренный, что потребовало его введения в объеме 20 мл на одну процедуру (стандартный рекомендованный объем «SpaceOAR®» - 10 мл, «Barrigel®» - 10 мл). Высокая стоимость человеческого коллагена, а также субоптимальные показатели пространственной стабильности в тканях, привели к тому, что его клиническое применение в качестве спейсера не получило признания, уступив эту нишу более подходящим аналогам на основе ПЭГ и гиалуроновой кислоты.
В настоящее время процедура промежностного введения спейсеров на основе ПЭГ и коллагена при лучевом лечении РПЖ достаточно стандартизована и преследует своей целью создание пространства между предстательной железой и передней стенкой прямой кишки ≥1 см.
Техническим результатом изобретения является расширение арсенала отечественных средств для снижения лучевой нагрузки при лечении РПЖ, увеличение расстояния от передней стенки прямой кишки до простаты до 10 мм и более, снижение лучевой нагрузки на переднюю стенку прямой кишки на 40%-60%.
Указанный технический результат достигается в способе снижения лучевой нагрузки на прямую кишку при лечении РПЖ путем введения биодеградирующих субстанций (БДС) в жировую клетчатку, расположенную между стенкой прямой кишки и предстательной железой, в котором в качестве БДС используют «Сферо®ГЕЛЬ» с диаметром частиц 200-360 мкм, который в объеме 10 мл вводят до начала процедуры облучения под контролем трансректального УЗИ трансперинеально.
Способ иллюстрируется фиг. 1-5, где:
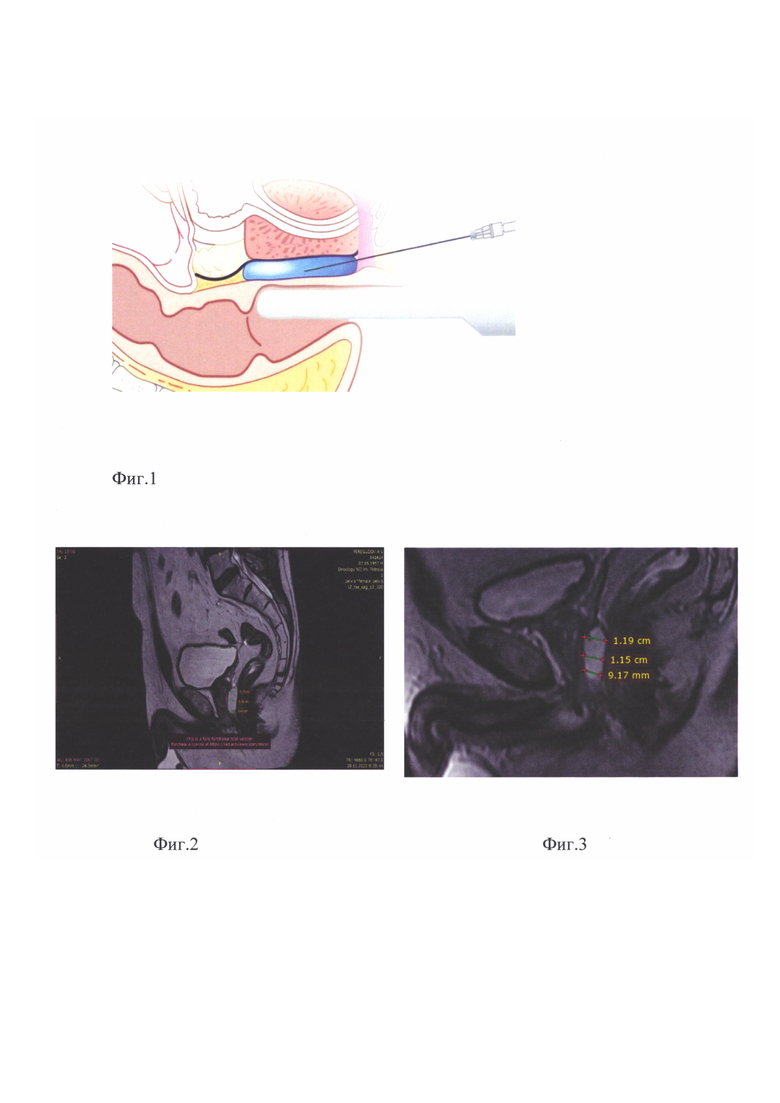
На фиг. 1 - схема введения БДС (спейсера) на основе препарата «Сферо®ГЕЛЬ»;
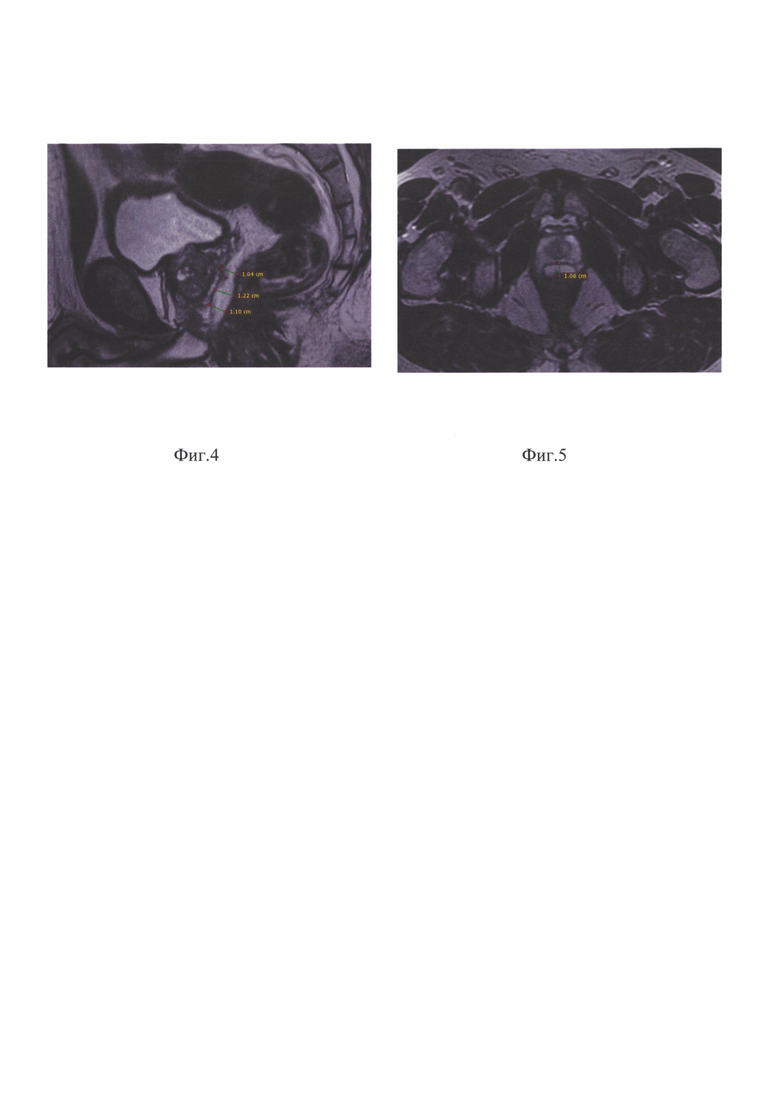
На фиг. 2 - топометрическая MP-томография пациента У. с введенным парапростатическим спейсером (сагиттальный скан);
На фиг. 3 - контрольная MP-томография пациента У., выполненная через две недели после введения спейсера и окончания лучевого лечения (сагиттальный скан);
На фиг. 4 - топометрическая MP-томография пациента Б. с введенным парапростатическим спейсером (сагиттальный скан);
На фиг. 5 - контрольная MP-томография пациента Б., выполненная через две недели после введения спейсера и окончания лучевого лечения (аксиальный скан).
Как показали проведенные нами исследования, биодеградирующий гель («Сферо®ГЕЛЬ», ЗАО Биомир сервис, г. Москва; per. удостоверение РУ № ФСР 2012/13033 от 15.07.2015) с диаметром частиц 200-360 мкм позволяет увеличить расстояние от передней стенки прямой кишки до простаты до 10 мм и более и при проведении облучения предстательной железы снизить радиационную нагрузку на переднюю стенку прямой кишки на 40%-60%.
Заявляемый способ основан на проведенном с 2019 года исследовании по апробации различных биополимеров отечественного производства в качестве радиотерапевтических спейсеров.
Первый опыт связан с использованием препарата «Мезогель®» (НПО Линтекс, г. Санкт-Петербург). Основа этого гидрогеля, разрешенного для введения в полости и клетчаточные пространства человека (рег. удостоверение от 27.04.2018 г. №ФСР 2010/08895), представлена карбоксиметилцеллюлезой. В парапростатическое пространство по стандартной методике вводилось около 10 мл препарата. Процедура введения «Мезогель®» (7 пациентов) не сопровождалась какими-либо осложнениями. Однако проведение МРТ органов малого таза уже на следующий после имплантации день демонстрировало практически полную миграцию карбоксиметилцеллюлезы по параректальной клетчатке без создания рекомендованного (около 1 см) пространства между структурами интереса во всех 7 наблюдениях, что делало невозможным использование данного препарата в качестве БДС при облучении ПЖ.
Опыт использования второго отечественного препарата «Bellarti Lift®» (ООО Гротекс, г. Санкт-Петербург) (рег. удостоверение РЗН 2020/12181 от 07.10.2020) на основе 1,8% раствор гиалуроновой кислоты в группе из 10 пациентов также не позволил получить удовлетворительные результаты. Контрольные MP-исследования выявили существенное снижение объема введенного препарата (10 мл) на 3-4 сутки. Низкая локальная стабильность «Bellarti Lift®» не позволяет обеспечивать необходимую пространственную топографическую анатомию простаты и критических структур на протяжении всего курса лучевой терапии.
Оптимальные результаты были получены при использовании отечественного препарата «Сферо®ГЕЛЬ» (ЗАО Биомир сервис, г. Москва) (рег. удостоверение РУ № ФСР 2012/13033 от 15.07.2015). «Сферо®ГЕЛЬ» - гетерогенная композиция, состоящая из микрочастиц «сшитого» коллагена животного происхождения, помещенных в гель, идентичный природному внеклеточному матриксу. До настоящего времени накоплен длительный опыт клинического применения этого препарата в области травматологии, нейрохирургии, хирургии, урологии, офтальмологии, гинекологии и косметологии.
В зависимости от размера сшитой фракции «Сферо®ГЕЛЬ» выделяют три основные варианта исполнения этого препарата (табл. 1).

Опыт применения «Сферо®ГЕЛЬ» в вариантах LIGHT и MEDIUM в группе из 12 пациентов продемонстрировал недостаточную стабильность в тканях, что проявлялось в быстрой миграции введенного коллагена по всему объему парапростатической клетчатки уже на 1-3 сутки после его введения. Использование в качестве спейсера наиболее «тяжелой» фракции (10 пациентов) - LONG с размерами сшитых частиц 200-360 мкм позволил добиться необходимого расстояния, равного или превышающего 1 см, сохраняющегося на протяжении всего срока лучевого лечения (не менее 14 суток). Во всех наблюдениях, независимо от используемой формы препарата, не отмечалось негативных местных (общих) реакций и осложнений, обусловленных имплантацией БДС.
Способ осуществляют, например, следующим образом:
за два часа до процедуры выполняют очистительную клизму и подготовку операционного поля (бритье кожных покровов промежности);
- за 30 минут до процедуры осуществляют антибактериальную профилактику однократным парентеральным введением антибиотика широкого спектра действия;
- пациента укладывают в литотомическую позицию для промежностных манипуляций;
- после введения эндоректального датчика в прямую кишку, закрепленного на степпере, производят обработку кожных покровов операционного поля раствором антисептика;
- осуществляют стандартную установку трех рентгеноконстрастных маркеров в разные доли предстательной железы;
- посредством местной инфильтрационной анестезии 1% раствором лидокаина производят обезболивание кожной точки введения иглы-интродьюсера и парапростатических тканей;
- для введения достаточно плотной субстанции используют иглы-интродьюсеры диаметром 14-16 СН;
- введение иглы-интродьюсера осуществляют строго по срединной линии на 1-1,5 см выше анального края;
- продвижение иглы-интродьюсера осуществляют под УЗИ-контролем в сагиттальной плоскости сканирования в пространство между апоневрозом; Денонвилье и простатой (сверху) и передней стенкой прямой кишки (мезоректальной фасции) снизу (фиг. 1);
- при достижении иглой-интродьюсера уровня, соответствующего середине предстательной железы, осуществляют гидродиссекцию 1% раствором лидокаина в объеме 2-3 мл, для создания первичного пространства и ориентировки в слоях тканей для предотвращения повреждения иглой передней стенки прямой кишки;
- производят введение имплантируемого препарата в объеме 10 мл с последующим извлечением иглы-интродьюсера;
- накладывают асептическую повязку на кожу промежности.
Способ иллюстрируется клиническими примерами.
Пример 1 (Фиг. 2, 3). Пациент У., 1969 г.р. Клинический диагноз: рак предстательной железы cT2aN0M0G2. Уровень ПСА - 8,7 нг/мл (группа промежуточного риска по NCCN). Сформулированы показания для проведения стереотаксической лучевой терапии (5 фракций по 7,25 Гр до суммарной очаговой дозы 36,25 Гр, изоэффективная доза, эквивалентная дозе при режиме фракционирования 2 Гр (EQD2) (α/β - 1,5 Гр) - 90, 6 Гр). Перед проведением топометрических исследований (КТ и МРТ) по стандартной методике введено 10 мл сферогеля (спейсера) - «Сферо®ГЕЛЬ» LONG с размерами сшитых частиц 200-360 мкм (фиг. 2).
Предварительный (до введения спейсера) расчет дозиметрического плана продемонстрировал высокую дозную нагрузку на область прямой кишки: значение D2cc (доза, подводимая к 2 см3 прямой кишки) составила 35 Гр (EQD2 (α/β 3 Гр)=70 Гр экв.), что достаточно близко к рекомендованному лимиту по этому показателю - 75 Гр экв. Введение спейсера позволило на 40% снизить расчетное значение D2cc - 42 Гр экв.
Пример 2 (Фиг. 4, 5). Пациент Б., 1970 г.р. Клинический диагноз: рак предстательной железы cT2cN0M0G2. Уровень ПСА - 7,3 нг/мл (группа промежуточного риска по NCCN). Запланировано лучевое лечение в виде стереотаксической лучевой терапии (5 фракций по 7,25 Гр). Перед началом планирования лучевой терапии введен сферогель (спейсер) -«Сферо®ГЕЛЬ» LONG с размерами сшитых частиц 200-360 мкм в объеме 10 мл (фиг. 3).
Дозиметрический выигрыш от использования спейсера относительно нагрузки на прямую кишку составил 57%.
Во всех десяти клинических случаях достигнуто снижение лучевой нагрузки на переднюю стенку прямой кишки на 40%-60%.
Таким образом, заявляемый способ расширяет арсенал отечественных средств для снижения лучевой нагрузки при лечении РПЖ, позволяет увеличить расстояние от передней стенки прямой кишки до простаты до 10 мм и более, снизить лучевую нагрузки на переднюю стенку прямой кишки на 40%-60%.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ИМПЛАНТАЦИИ ПАРАПРОСТАТИЧЕСКОГО СПЕЙСЕРА | 2023 |
|
RU2836674C1 |
| СПОСОБ ПЛАНИРОВАНИЯ ВЫСОКОДОЗНОЙ ВНУТРИТКАНЕВОЙ ЛУЧЕВОЙ ТЕРАПИИ РАКА ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ | 2014 |
|
RU2576875C1 |
| СПОСОБ ЛУЧЕВОГО ЛЕЧЕНИЯ РАКА ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ ГРУПП ВЫСОКОГО И КРАЙНЕ ВЫСОКОГО РИСКА РЕЦИДИВА | 2021 |
|
RU2752709C1 |
| СПОСОБ ЛЕЧЕНИЯ РАКА ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ | 2004 |
|
RU2258503C1 |
| СПОСОБ СОСУДОСБЕРЕГАЮЩЕЙ ВЫСОКОМОЩНОСТНОЙ БРАХИТЕРАПИИ РАКА ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ | 2022 |
|
RU2808154C1 |
| СПОСОБ ОТБОРА ПАЦИЕНТОВ С РЕЦИДИВОМ РАКА ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ ПОСЛЕ ПРОВЕДЕНИЯ НИЗКОДОЗНОЙ БРАХИТЕРАПИИ ДЛЯ ЛЕЧЕНИЯ ТРАНСРЕКТАЛЬНЫМ ВЫСОКОИНТЕНСИВНЫМ ФОКУСИРОВАННЫМ УЛЬТРАЗВУКОМ | 2019 |
|
RU2735656C1 |
| Способ лучевой терапии больных раком предстательной железы с метастазами в регионарных лимфатических узлах таза | 2021 |
|
RU2757641C1 |
| Способ лечения больных локальным раком простаты, относящихся к группе высокого риска прогрессирования заболевания | 2015 |
|
RU2625598C2 |
| Способ профилактики развития эректильной дисфункции при внутритканевой лучевой терапии рака предстательной железы источником высокой мощности дозы Ir192 | 2021 |
|
RU2765404C1 |
| СПОСОБ ВИЗУАЛИЗАЦИИ ВНУТРЕННЕЙ ПОЛОВОЙ АРТЕРИИ ПРИ ЛУЧЕВОМ ЛЕЧЕНИИ РАКА ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ | 2021 |
|
RU2756251C1 |
Изобретение относится к медицине, а именно к онкологии, и может быть использовано для снижения лучевой нагрузки на прямую кишку при лечении рака предстательной железы (РПЖ). Способ включает введение биодеградирующих субстанций (БДС) в жировую клетчатку, расположенную между стенкой прямой кишки и предстательной железой. В качестве БДС используют сферогель с диаметром частиц 200-360 мкм, который в объеме 10 мл вводят до начала процедуры облучения под контролем трансректального УЗИ трансперинеально. Использование изобретения позволяет увеличить расстояние от передней стенки прямой кишки до простаты до 10 мм и более, снизить лучевую нагрузки на переднюю стенку прямой кишки на 40%-60%. 1 табл., 2 пр., 5 ил.
Способ снижения лучевой нагрузки на прямую кишку при лечении рака предстательной железы (РПЖ) путем введения биодеградирующих субстанций (БДС) в жировую клетчатку, расположенную между стенкой прямой кишки и предстательной железой, отличающийся тем, что в качестве БДС используют сферогель с диаметром частиц 200-360 мкм, который в объеме 10 мл вводят до начала процедуры облучения под контролем трансректального УЗИ трансперинеально.
| СПОСОБ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ ЛУЧЕВЫХ ПОВРЕЖДЕНИЙ НИЖНИХ ОТДЕЛОВ ТОЛСТОЙ КИШКИ | 2003 |
|
RU2242988C1 |
| СПОСОБ ЛЕЧЕНИЯ И/ИЛИ ПРОФИЛАКТИКИ РЕКТИТОВ | 1992 |
|
RU2034541C1 |
| НОВИКОВ Р.В | |||
| и др | |||
| Технологии снижения лучевой токсичности у больных раком предстательной железы: спейсеры - простое и эффективное решение//Онкоурология | |||
| Способ регенерирования сульфо-кислот, употребленных при гидролизе жиров | 1924 |
|
SU2021A1 |
| Нефтяной конвертер | 1922 |
|
SU64A1 |
| КЛИМЕНКО К.А | |||
| и др | |||
| Лучевые ректиты при комплексном лечении рака органов малого таза (обзор литературы)//Вестник | |||
Авторы
Даты
2023-10-23—Публикация
2022-11-16—Подача