Настоящее изобретение относится к метаболитам триптофана, используемым для лечения и предотвращения заболеваний, связанных с мышечной атрофией.
Область техники, к которой относится настоящее изобретение
С функциональной точки зрения важно отделить мышечную силу, участвующую во многих основных видах деятельности (перехода от сидения к стоянию, подъема по лестнице, ходьбы), от постоянной силы (способности поддерживать максимальный уровень сокращения во время длительных усилий) и от качества мышц (показателя силы на единицу мышечной массы), которое может ухудшаться в зависимости от ситуации, например, при некоторых заболеваниях, связанных с непрочностью или атрофией мышц (кахексия, саркопения, саркопеническое ожирение, рак, мышечная дистрофия Дюшенна (DMD), боковой амиотрофический склероз (ALS), миотоническая дистрофия (MDA), сердечная недостаточность и т.д.) или во время мышечных травм после чрезмерно интенсивных физических усилий. Коэффициент изокинетической выносливости (отношение силы между тремя последними концентрическими сокращениями мышц относительно первых трех) и изменение потери мышечной силы, как правило, являются адекватными показателями независимо от ситуации.
Старение мышечной функции или ухудшение работы мышц вследствие постепенного уменьшения мышечной массы и производительности и/или силы, также называемой саркопенией, является причиной значительных осложнений, таких как увеличение количества падений, уменьшение физической самостоятельности, нарушения иммунной системы. Вовлечены множественные сложные механизмы, такие как гиподинамия, снижение физической активности, слабый алиментарный статус, лежащее в основе воспалительное состояние, а также гормональные и нейрогенные факторы, такие как дисбаланс между деградацией и синтезом мышечного белка, которые в итоге приводят к атрофии мышечных волокон и снижению способности производить силу. Эти же механизмы, вклад которых варьирует в зависимости от ситуации, также обнаруживаются в случае длительной иммобилизации при раке, сердечной или почечной недостаточности или других серьезных хронических или острых заболеваниях (кахексии, саркопеническом ожирении, мышечной дистрофии Дюшенна (DMD), боковом амиотрофическом склерозе (ALS), миотонической дистрофии (MDA), а также после мышечной травмы или слишком интенсивных физических нагрузок.
Например, у пожилых людей, когда аминокислоты не попадают в мышцы, резистентность к инсулину, распространенность которой увеличивается с возрастом, играет неблагоприятную роль за счет увеличения протеолиза мышечного белка, что приводит к потере мышечной массы и силы (Bauer et al., 2013; Biolo et al., 2014). Аналогично, снижение уровня анаболических гормонов (тестостерона, GH-IGF1, DHEA), подобно повышению уровня провоспалительных цитокинов (в частности, IL-6 и TNF-α), усиливают протеолитический процесс (Bosutti et al., 2008; Biolo et al., 2008; Guillet et al., 2009). Более того, уменьшение активации сателлитных клеток, ответственных за регенерацию мышц, увеличение уровня миостатина (или GDF-8), который, как известно, экспрессируется в скелетных мышцах и играет тормозящую роль в росте и развитии мышц (Lee, 2010), атрогина-1 (или MAFbx) и MURF-1, старение митохондрий и апоптоз (приводящий к запрограммированной гибели клеток) также способствуют этому феномену, который также может усугубляться при увеличении внутримышечного жира в случае саркопенического ожирения (Beyer et al., 2012). И наоборот, генетические мутации в гене миостатина, например, увеличивают массу скелетных мышц у животных как вследствие гиперпластического, так и гипертрофического роста миофибрилл (McPherron and Lee, 2002 and 2003; Bass et al., 1999).
Хотя укрепление мышц можно по меньшей мере частично компенсировать посредством увеличения физической активности и дополнительного потребления пищевых белков (Deutz et al., 2014), предотвращение или лечение саркопении в настоящее время основывается исключительно на программе регулярной физической активности, адаптированной к каждому индивидууму, и мониторинге потребления белков и калорий. В существующих на сегодня рекомендациях рекомендуются физические (аэробные) упражнения на выносливость, а также силовые упражнения (с сопротивлением), и еще упражнения, которые специально требуют баланса. С терапевтической точки зрения, тестостерон и гормон роста (GH) улучшают работу мышц только у индивидуумов с гипогонадизмом или с дефицитом GH; к сожалению, DHEA не дает никаких преимуществ с точки зрения мышечной производительности; витамин D снижает риск падения без непосредственного улучшения мышечной силы или мощности. Таким образом, в настоящее время с целью определения новых терапевтических и профилактических подходов проводят другие направления исследований. Некоторые селективные модуляторы андрогенных рецепторов, или SARM, а также ингибиторы миостатина, которые в настоящее время изучаются, могут оказаться полезными, подобно определенным аминокислотам, предоставляемым в форме пищевых добавок, особенно для пожилых индивидуумов с недостаточностью питания.
Триптофан (TRP) является незаменимой аминокислотой, необходимой для биосинтеза белка, а также является предшественником нескольких биологических молекул. Метаболизируемый, по существу, по кинурениновому пути (KP), триптофан образует многочисленные метаболиты (по меньшей мере около ста), такие как кинуренин (KYN), кинурениновая кислота (KA), антраниловая кислота (АА), ксантуреновая кислота, хинолиновая кислота (QUIN), пиколиновая кислота (PICO), хинальдиновая кислота (QL-Dic) или, в частности, 3ОН-кинуренин (Widner В et al., 1997), а также является важным источником синтеза de novo NAD+, или никотинамид-адениндинуклеотида.
Было показано, что добавление TRP мышам, находящимся на диете с низким содержанием белка, способно уменьшить потерю мышечной массы посредством увеличения содержания IGF-1 в мышцах и изменения экспрессии генов, которые играют важную роль в синтезе белка, развитии мышц или размере волокон (Dukes A. et al., 2015), тогда как эффект L-кинуренина варьирует в зависимости от тестируемой дозы (благотворной или отрицательной). Предыдущие исследования уже продемонстрировали положительное влияние TRP на мышцы, их морфологию и синтез белка (Sanfilippo et al., 1995; Linetal., 1988).
Однако ни один документ не описывает и не предполагает, что метаболиты триптофана, выбранные из кинуреновой кислоты, антраниловой кислоты, хинолиновой кислоты, пиколиновой кислоты и хинальдиновой кислоты, могут оказывать положительное влияние на мышечную массу. Даже, напротив, в примере 1 было доказано, что согласно данному изобретению, что один из метаболитов триптофана, 3ОН-кинуэренин, не влияет на синтез белка в клетках С2С12.
При отсутствии эффективных способов лечения на сегодняшний день следует учитывать, что индивидуумы и, в более широком смысле, млекопитающие, у которых наблюдается снижение мышечной производительности и/или мышечной силы/мощности, могут получить большую пользу от медикаментозной терапии, обогащенных пищевых продуктов или пищевых добавок, предназначенных для максимального увеличения анаболизма мышечной ткани и уменьшения катаболизма мышечной ткани.
При том, что миостатин является понижающим регулятором развития мышц у нескольких видов, таких как человек, ингибирование активности фермента и его экспрессии фактически представляет собой терапевтический подход или вмешательство, представляющее интерес для лечения и предотвращения мышечной дисфункции.
Подробное раскрытие настоящего изобретения
Таким образом, настоящее изобретение относится к одному или более метаболитам триптофана (TRP) (также называемым продуктом согласно настоящему изобретению), выбранным из кинуреновой кислоты (KA), антраниловой кислоты (АА), хинолиновой кислоты (QUIN), пиколиновой кислоты (PICO) и хинальдиновой кислоты (QL-Dic) и их смесей или энантиомеров, диастереоизомеров, гидратов, сольватов, таутомеров, рацемических смесей или их фармацевтически приемлемых солей, для использования в качестве лекарственного средства, предназначенного для увеличения и/или поддержания мышечной массы и/или силы у млекопитающего.
Наиболее предпочтительным метаболитом в контексте настоящего изобретения является кинуреновая кислота (КА), которую можно использовать отдельно или в комбинации с одной или несколькими из антраниловой кислоты (АА), хинолиновой кислоты (QUIN), пиколиновой кислоты (PICO) и хинальдиновой кислоты (QL-DIC).
В частности, настоящее изобретение относится к кинуреновой кислоте (КА) или ее энантиомеру, диастереоизомеру, гидрату, сольвату, таутомеру, рацемической смеси или фармацевтически приемлемой соли для использования в качестве лекарственного средства, предназначенного для увеличения и/или поддержания мышечной массы и/или силы у млекопитающего.
Оно также относится к антраниловой кислоте (АА) или ее энантиомеру, диастереоизомеру, гидрату, сольвату, таутомеру, рацемической смеси или фармацевтически приемлемой соли для использования в качестве лекарственного средства, предназначенного для увеличения и/или поддержания мышечной массы и/или силы у млекопитающего.
Кроме того, оно относится к хинолиновой кислоте (QUIN), или ее энантиомеру, диастереоизомеру, гидрату, сольвату, таутомеру, рацемической смеси или фармацевтически приемлемой соли для использования в качестве лекарственного средства, предназначенного для увеличения и/или поддержания мышечной массы и/или силы у млекопитающего.
Более того, оно относится к пиколиновой кислоте (PICO) или ее энантиомеру, диастереоизомеру, гидрату, сольвату, таутомеру, рацемической смеси или фармацевтически приемлемой соли для использования в качестве лекарственного средства, предназначенного для увеличения и/или поддержания мышечной массы и/или силы у млекопитающего.
Кроме того, оно относится к хинальдиновой кислоте (QL-Dic) или ее энантиомеру, диастереоизомеру, гидрату, сольвату, таутомеру, рацемической смеси или фармацевтически приемлемой соли для использования в качестве лекарственного средства, предназначенного для увеличения и/или поддержания мышечной массы и/или силы у млекопитающего.
В заключение, оно относится к смеси по меньшей мере двух продуктов, выбранных из группы, состоящей из кинуреновой кислоты (KA), антраниловой кислоты (АА), хинолиновой кислоты (QUIN), пиколиновой кислоты (PICO) и хинальдиновой кислоты (QL-Dic), преимущественно, по меньшей мере трех продуктов, конкретно, по меньшей мере четырех продуктов, более преимущественно, всех этих продуктов или энантиомеров, диастереоизомеров, гидратов, сольватов, таутомеров, рацемических смесей или их фармацевтически приемлемых солей для использования в качестве лекарственного средства, предназначенного для увеличения и/или поддержания мышечной массы и/или силы у млекопитающего.
Преимущественно, метаболит (метаболиты)/продукт (продукты) согласно настоящему изобретению предназначены для лечения и/или предотвращения мышечной атрофии у млекопитающих и/или для ограничения мышечной атрофии у млекопитающих и/или для стимуляции мышечного роста у млекопитающих, выполняющих упражнения и направленных на увеличение мышечной массы и/или качества и/или силы, для предотвращения появления симптомов саркопении или для реабилитации после потери мышечной массы и/или для улучшения времени восстановления после интенсивных физических усилий.
Конкретно, мышечная атрофия связана с возрастом и/или с последствиями медикаментозного лечения и/или с заболеванием в связи с аномалиями дистрофина и/или с иммобилизацией и/или с кахексией и/или с нервной анорексией и/или с состоянием пониженного питания и/или с дисфагией вследствие патологических состояний.
Преимущественно, мышечная атрофия представляет собой пресаркопению, саркопению или тяжелую саркопению. Преимущественно, пресаркопения, саркопения или тяжелая саркопения связаны со старением, ожирением или хроническими заболеваниями, такими как диабет или сердечная недостаточность.
В одном конкретном варианте осуществления мышечная атрофия связана с заболеванием, ассоциированным с аномалиями дистрофина, конкретно выбранным из мышечной дистрофии Дюшенна, мышечной дистрофии Беккера, бокового амиотрофического склероза и миотонической дистрофии Штейнерта.
В еще одном конкретном варианте осуществления мышечная атрофия связана с иммобилизацией независимо от причины, например, вследствие слабости, связанной со старением, мышечных травм или госпитализации (например, восстановление после перелома, происходящей до/после бариатрического хирургического вмешательства, ожогов), в результате несчастного случая или хирургического вмешательства, например, вставления протеза коленного или тазобедренного сустава.
В другом конкретном варианте осуществления мышечная атрофия связана с кахексией, а именно с кахексией, ассоциированной с хроническим заболеванием, выбранным из рака, синдрома приобретенного иммунодефицита (AIDS, СПИД), хронической обструктивной болезни легких (COPD, ХОБЛ), сердечной недостаточности, печеночной недостаточности, туберкулеза, терминальной стадии хронической болезни почек (ESRD) и хронических воспалительных заболеваний кишечника (IBD).
В другом конкретном варианте осуществления мышечная атрофия связана с расстройствами пищевого поведения, такими как нервная анорексия.
В другом конкретном варианте осуществления мышечная атрофия связана с дисфагией вследствие патологических состояний (например, постинсультный период, болезнь Паркинсона, окулофарингеальная мышечная дистрофия (OPMD)).
Конкретно, млекопитающее, которому вводят метаболит/продукт согласно настоящему изобретению, также страдает метаболическими заболеваниями, такими как диабет, ожирение, неалкогольная жировая болезнь печени (NAFLD) или неалкогольный стеатогепатит (NASH), хроническими воспалительными заболеваниями кишечника (IBD), раком, почечной или сердечной недостаточностью, нейродегенеративными патологическими состояниями или психическими расстройствами, такими как депрессия.
Действительно, в случае, когда млекопитающее страдает такими метаболическими заболеваниями, как диабет, ожирение, неалкогольная жировая болезнь печени (NAFLD) или неалкогольный стеатогепатит (NASH), хронические воспалительные заболевания кишечника (IBD), рак, почечная или сердечная недостаточность, нейродегенеративные патологические состояния или психические расстройства, такие как депрессия, метаболит согласно настоящему изобретению также будет благоприятно влиять на это заболевание, помимо эффектов, описанных выше.
Метаболит/продукт согласно настоящему изобретению также используют для стимуляции роста мышц у млекопитающих, выполняющих упражнения и направленных на увеличение мышечной массы и/или качества и/или силы, для предотвращения, например, появления возрастных симптомов саркопении или для реабилитации после потери мышечной ткани и/или для улучшения времени восстановления после интенсивных физических усилий.
Млекопитающее может представлять собой животное (домашнее животное, такое как собака или кошка) или другое животное (крупный рогатый скот, члены семейства свиней, члены семейства овец, члены семейства коз, члены семейства лошадиных) или человек; преимущественно это человек.
Авторы изобретения обнаружили, что метаболиты/продукты согласно настоящему изобретению позволяют увеличивать синтез белка в мышечных клетках С2С12, уменьшать экспрессию гена миостатина в мышечных клетках С2С12 и/или увеличить диаметр миотрубочек клеток С2С12 и, следовательно, размер эти мышечных волокон.
Кроме того, настоящее изобретение связано с использованием метаболита/продукта триптофана согласно настоящему изобретению, как определено выше, для получения лекарственного средства, предназначенного для увеличения и/или поддержания мышечной массы и/или силы у млекопитающего и/или лечения и/или предотвращения мышечной атрофии у млекопитающих и/или ограничения мышечной атрофии у млекопитающих и/или для стимуляции мышечного роста у млекопитающих, выполняющих упражнения и направленных на увеличение мышечной массы и/или качества и/или силы, для предотвращения появления возрастных симптомов саркопении или для реабилитации после потери мышечной ткани и/или для улучшения времени восстановления после интенсивных физических усилий.
Наконец, оно относится к способу сохранения и/или увеличения мышечной массы и/или силы у млекопитающего, для лечения и/или профилактического лечения и/или для отсрочки появления мышечной атрофии у млекопитающих и/или для ограничения мышечной атрофии у млекопитающих и/или для стимуляции мышечного роста у млекопитающих, выполняющих упражнения и направленных на увеличение мышечной массы и/или качества и/или силы, для предотвращения возникновения симптомов саркопении или для реабилитации после потери мышечной ткани и/или для улучшения времени восстановления после интенсивных физических усилий, включая введение эффективного количества метаболита/продукта триптофана согласно настоящему изобретению нуждающемуся в этом субъекту.
Эффективное количество будет корректироваться в зависимости от природы и серьезности подлежащего лечению симптома, пути введения, а также от массы и возраста субъекта. В целом, средняя доза будет варьировать между дозой от 50 до 300 мг метаболита/продукта, в частности, кинуреновой кислоты (КА), в день на один или более приемов, когда субъектом является человек.
Таким образом, изобретение можно преимущественно использовать при различных состояниях пониженного питания или при состояниях, ассоциированных с непрочностью или атрофией мышц: саркопенией (связанной со старением, ожирением или хроническими заболеваниями, такими как диабет или сердечная недостаточность), кахексией, ассоциированной с некоторыми заболеваниями (такими как, в частности, рак, синдром приобретенного иммунодефицита (AIDS, СПИД), хроническая обструктивная болезнь легких (COPD, ХОБЛ), терминальная стадия хронической почечной недостаточности (ESRD)), дисфагией вследствие патологических состояний (например, постинсультный период, болезнь Паркинсона, окулофарингеальная мышечная дистрофия (OPMD), мышечными травмами или госпитализацией (например, восстановление после перелома, происходящей до/после бариатрического хирургического вмешательства, ожогов), нервной анорексией, редкими заболеваниями (такими как мышечная дистрофия Дюшенна (DMD), боковой амиотрофический склероз (ALS), миотоническая дистрофия (MD) и т.д.). Изобретение также можно использовать в спортивной медицине для улучшения, например, времени восстановления после интенсивных физических усилий или в качестве части композиции ветеринарных препаратов для увеличения мышечной массы и/или качества у определенных животных.
В одном предпочтительном варианте осуществления метаболит/продукт согласно настоящему изобретению находится в очищенной форме, например, полученной посредством химического синтеза, или в форме (неочищенного или частично очищенного) растительного экстракта, полученного способами, хорошо известными специалистам в данной области (мацерация, перколяция и т.д.) в полярном или органическом растворителе или их смеси.
Действительно, триптофан и его метаболиты, такие как, например, кинуреновая кислота, относительно распространены в обычной пище или некоторых растениях, таких как клубни картофеля, мед, брокколи, лекарственные травы (Turski MP et al., 2011; Turski MP et al., 2012; Donarski et al., 2010).
Таким образом, можно обеспечить полезную дозу активных метаболитов TRP/продукта согласно настоящему изобретению посредством потребления пищевой добавки или путем приема пищевых продуктов (например, молочного продукта или напитка), обогащенных экстрактом или натуральными или синтетическими очищенными активными веществами.
Преимущественно, метаболит/продукт согласно настоящему изобретению находится в форме фармацевтической или ветеринарной композиции, содержащей фармацевтически приемлемое вспомогательное вещество. Он также может быть в форме нутрицевтической композиции или пищевой добавки, предназначенной для перорального приема.
В одном предпочтительном варианте осуществления фармацевтическая, ветеринарная или нутрицевтическая композиция или пищевая добавка согласно настоящему изобретению также содержит другое активное вещество, обладающее дополнительным или синергетическим эффектом.
Это второе активное вещество можно вводить в той же фармацевтической или нутрицевтической или ветеринарной композиции или в той же пищевой добавке, что и метаболит согласно настоящему изобретению. Его также можно вводить отдельно, одновременно или последовательно с течением времени.
Это активное вещество может представлять собой одно или более лекарственных средств или пищевых добавок, или пищевых продуктов, или ветеринарных продуктов, или антител, обычно используемых для профилактики или лечения мышечной дисфункции или уменьшения мышечной массы, которые могут создавать полезный фармакологические синергизм с метаболитами согласно настоящему изобретению, в зависимости от состояния (саркопении, саркопенического ожирения, сердечной или почечной недостаточности, анорексии, кахексии, связанной с раком или другими хроническими заболеваниями, мышечной дистрофии Дюшенна (DMD), бокового амиотрофического склероза (ALS), миотонической дистрофии (MD), дисфагии, связанной с некоторыми патологическими состояниями, мышечными травмами или госпитализацией, бариатрическими хирургическими вмешательствами, интенсивными физическими усилиями и т.д.).
Это активное вещество может соответствовать пищевым продуктам, таким как смеси белков (таких как креатин) или аминокислот (таких как, например, лизин, аргинин, лейцин, бета-гидрокси-бета-метилбутират, цитруллин), витаминам (таким как витамин D, витамины группы В и т.д.), минеральным веществам (таким как магний, кальций и т.д.) или другим нутрицевтическим веществам, известным своими противовоспалительными свойствами (таким как полиненасыщенные жирные кислоты омега-3 (DHA, ЕРА)) или другим активные питательным веществам, которые способствуют его действию на клетки, такие как фосфолипиды, например фосфатидилхолин, фосфатидилсерин).
Это активное вещество может также соответствовать определенным гормонам (таким как гормон роста (GH), инсулиноподобный фактор роста (IGF-1)) для оптимизации их эффектов и потенциального уменьшения их побочных эффектов.
Это активное вещество может также соответствовать медикаментозной терапии (такой как терапия антагонистами рецепторов ангиотензина II, или селективными модуляторами андрогенных рецепторов (SARM), или ингибиторами миостатина, или антителами).
Кроме того, это активное вещество может также соответствовать хондропротекторам (таким как глюкозамин, хондроитинсульфат, гиалуроновая кислота или гидролизаты коллагена) с целью усиления мышечной массы, нарушенной вследствие неподвижности у индивидуумов, страдающих остеоартритом.
ОПРЕДЕЛЕНИЯ
В контексте настоящего изобретения термин «фармацевтически приемлемый» предназначен для обозначения того, что является полезным при получении фармацевтической или ветеринарной композиции, которая в целом безопасна, нетоксична и не является ни биологически нежелательной, ни нежелательной в ином отношении, и которая является приемлемой для использования в ветеринарии, а также для фармацевтического применения у человека.
В контексте настоящего изобретения выражение «фармацевтически приемлемые соли метаболита или продукта» предназначено для обозначения солей, которые являются фармацевтически приемлемыми, как определено в данном документе, и которые обладают желаемой фармакологической активностью исходного метаболита. Таким образом, они представляют собой органические и неорганические соли присоединения кислоты и соли присоединения оснований), которые являются физиологически переносимыми и не вызывают аллергических или подобных нежелательных реакций, таких как головокружение, когда их вводят человеку или животному. Примеры солей включают в себя, без ограничения: ацетат, адипат, альгинат, аспартат, бензоат, бензолсульфонат, бисульфат, бутират, цитрат, камфорат, камфорсульфонат, циклопентилпропионат, диглюконат, додецилсульфат, этансульфонат, фумарат, флукогептаноат, глицерофосфат, гемисульфат, гептаноат, гексаноат, гидрохлорид, гидробромид, гидриодид, 2-гидроксиэтил метансульфонат, лактат, малеат, метансульфонат, 2-нафталинсульфонат, никотинат, оксалат, пальмоат, пектинат, персульфат, фенилпропионат, пикрат, пивалат, пропионат, пропионат, сукцинат, тартрат, тиоцианат, тозилат, ундеканоат и тому подобное. Другие примеры солей включают анионы соединений настоящего изобретения, смешанные с соответствующим катионом, таким как Na+, NH4+, NWV4+(где W представляет собой С1-С4 алкильную группу), и т.д.
В контексте настоящего изобретения выражение «сольват метаболита или продукта» предназначено для обозначения любого соединения, полученного путем добавления молекулы инертного растворителя к метаболиту/продукту согласно настоящему изобретению, при этом сольват образуется в результате их силы взаимного притяжения. Сольваты представляют собой, например, алкоксиды соединения. Гидрат представляет собой сольват, в котором в качестве инертного растворителя используют воду. Он может быть моно-, ди- или тригидратированным.
В контексте настоящего изобретения термин «таутомер» предназначен для обозначения любого структурного изомера метаболитов согласно настоящему изобретению, которые взаимозаменяемы в результате обратимой химической реакции, известной как таутомеризация. В большинстве случаев реакция происходит за счет миграции атома водорода, сопровождаемой изменением положения двойной связи. В растворе соединения, способного к таутомеризации, создается равновесие между двумя таутомерами. Соотношение между таутомерами зависит от растворителя, температуры и рН. Таким образом, таутомерия представляет собой превращение одной функциональной группы в другую, обычно путем сопутствующего сдвига атома водорода и π-связи (двойной или тройной связи). Обычными таутомерами являются, например, следующие пары: альдегиды/кетоны - спирты или более конкретно енол; амиды - имидные кислоты; лактамы - лактимы; имины - енамины; енамины - енамины. Конкретно, она может включать кольчато-цепную таутомерию, которая имеет место, когда перемещение протона сопровождается преобразованием открытой структуры в кольцо.
Выражение «вспомогательное вещество» означает нетоксичное вещество, используемое в составах фармацевтических, нутрицевтических или ветеринарных композиций или пищевой добавки для предоставления среды, и/или формы, которую можно использовать для фармацевтической, нутрицевтической или ветеринарной композиции или пищевой добавки. Носитель может содержать одно или более из этих веществ, таких как стабилизатор, или водный раствор при забуференном рН. Примеры вспомогательных веществ, которые являются фармацевтически приемлемыми или которые можно использовать в нутрицевтической композиции или пищевой добавке, включают водные или твердые буферные ингредиенты, включая фосфат, цитрат и другие органические кислоты; антиоксиданты, включая аскорбиновую кислоту; низкомолекулярные полипептиды (менее чем приблизительно 10 остатков); белки, такие как сывороточный альбумин, желатин или иммуноглобулины; гидрофильные полимеры, такие как поливинилпирролидон; аминокислоты, такие как глицин, глутамин, аспарагин, аргинин или лизин; моносахариды, дисахариды и другие углеводы, включая глюкозу, маннозу или декстрины; хелатообразующие агенты, такие как EDTA; сахарные спирты, такие как маннит или сорбит; солеобразующие противоионы, такие как натрий; и/или неионогенные поверхностно-активные вещества, такие как Tween®, полиэтиленгликоль (PEG) и Pluronics®.
Фармацевтическую, нутрицевтическую или ветеринарную композицию или пищевую добавку получают так, чтобы она подходила для способа введения. Приемлемые фармацевтические или нутрицевтические вспомогательные вещества частично определяются вводимой композицией, а также конкретным процессом, применяемым для введения композиции. Следовательно, существует большое разнообразие подходящих составов фармацевтических, нутрицевтических или ветеринарных композиций или пищевых добавок, которые могут содержать метаболиты/продукты, которые описаны в данном документе. Дозировка этих подлежащих введению метаболитов/продуктов зависит от конкретного случая и, как обычно, должна быть адаптирована к индивидуальным обстоятельствам, чтобы получить эффективное терапевтическое количество и оптимальный эффект. Таким образом, она зависит от характера и степени тяжести заболевания, подлежащего лечению, а также от прогрессирования заболевания, а также от возраста и общего состояния здоровья пациента и от индивидуального ответа человека или животного, подлежащего лечению. Суточную дозу можно вводить в виде одной дозы или, в частности, когда вводятся большие количества, можно разделить на несколько отдельных доз.
Композиции могут быть в твердой, жидкой или полутвердой форме, подходящей для различных путей введения (перорального, ректального, назального, интраокулярного, местного - например, топического, трансдермального, буккального, вагинального или сублингвального или парентерального, например, подкожного, внутримышечного, внутривенного или внутрикожного). Пероральное введение является предпочтительным; этот путь наиболее подходит для длительного лечения. Тем не менее, возможно введение другими путями, например, внутривенно и трансдермально. Внутривенные лекарственные формы содержат активное вещество, растворенное в суспензии или эмульгированное в стерильном носителе, необязательно в присутствии эмульгирующих веществ, стабилизаторов, буферных веществ и других стандартных добавок; обычно их распределяют по небольшим бутылям или флаконам для инфузий, и их можно хранить в виде сухих продуктов, подлежащих восстановлению водой или подходящим носителем перед использованием. Твердые фармацевтические композиции могут представлять собой таблетки, гелевые капсулы, порошки, гранулы, пилюли, порошки для восстановления и т.д.; они могут содержать обычные вспомогательные вещества, такие как связующие вещества, наполнители, разбавители, вещества для прессования, смазывающие вещества, моющие средства, красители, ароматизаторы и смачивающие вещества. Таблетки могут быть покрыты оболочкой в соответствии со способами, хорошо известными в данной области техники. Подходящие наполнители включают целлюлозу, маннит, лактозу и другие подобные вещества. Жидкие композиции для перорального введения могут быть в форме водных или масляных суспензий, растворов, эмульсий, сиропов или эликсиров или могут быть представлены в форме сухих продуктов для восстановления водой или подходящим носителем перед использованием; они могут содержать обычные добавки, например, суспендирующие вещества, такие как сорбит, сироп, метилцеллюлоза, желатин, гидроксиэтилцеллюлоза, карбоксиметилцеллюлоза, гель стеарата алюминия или гидрогенизированные пищевые жиры, эмульгаторы, такие как лецитин, сорбитан моноолеат или аравийская камедь; неводные транспортеры (которые могут содержать пищевые масла), такие как миндальное масло, фракционированное кокосовое масло, масляные сложные эфиры, такие как сложные эфиры глицерина, пропиленгликоля или этилового спирта; консерванты, такие как метил или пропил р-гидроксибензоат или сорбиновая кислота и, при необходимости, обычные ароматизаторы или красители.
Термин «предотвращение» относится к снижению риска возникновения или развития заболевания или расстройства (например, при полной уверенности, что по меньшей мере один из клинических симптомов заболевания не может развиться) у субъекта, который может подвергаться воздействию патогенного агента или предрасположенного к заболеванию до его появления.
Термин «лечение» заболевания или расстройства в одном варианте осуществления обозначает улучшение заболевания или расстройства (например, путем остановки заболевания или уменьшения проявления, степени или серьезности по меньшей мере одного из его клинических симптомов).
Натуральные или синтетические молекулы можно использовать в комбинации с подходящим фармацевтическим носителем. Такие композиции содержат эффективное количество метаболитов TRP или продукта согласно настоящему изобретению и фармацевтически приемлемый носитель или вспомогательное вещество.
Изобретение будет более понятным при прочтении описания последующих фигур и примеров, которые даны исключительно в качестве неограничивающего указания.
На фигуре 1 представлено действие кинуреновой кислоты (KA) на синтез белка в мышечных клетках С2С12 в зависимости от используемой дозы.
На фигуре 2 представлено действие антраниловой кислоты на синтез белка в мышечных клетках С2С12.
На фигуре 3 представлено действие хинолиновой кислоты на синтез белка в мышечных клетках С2С12.
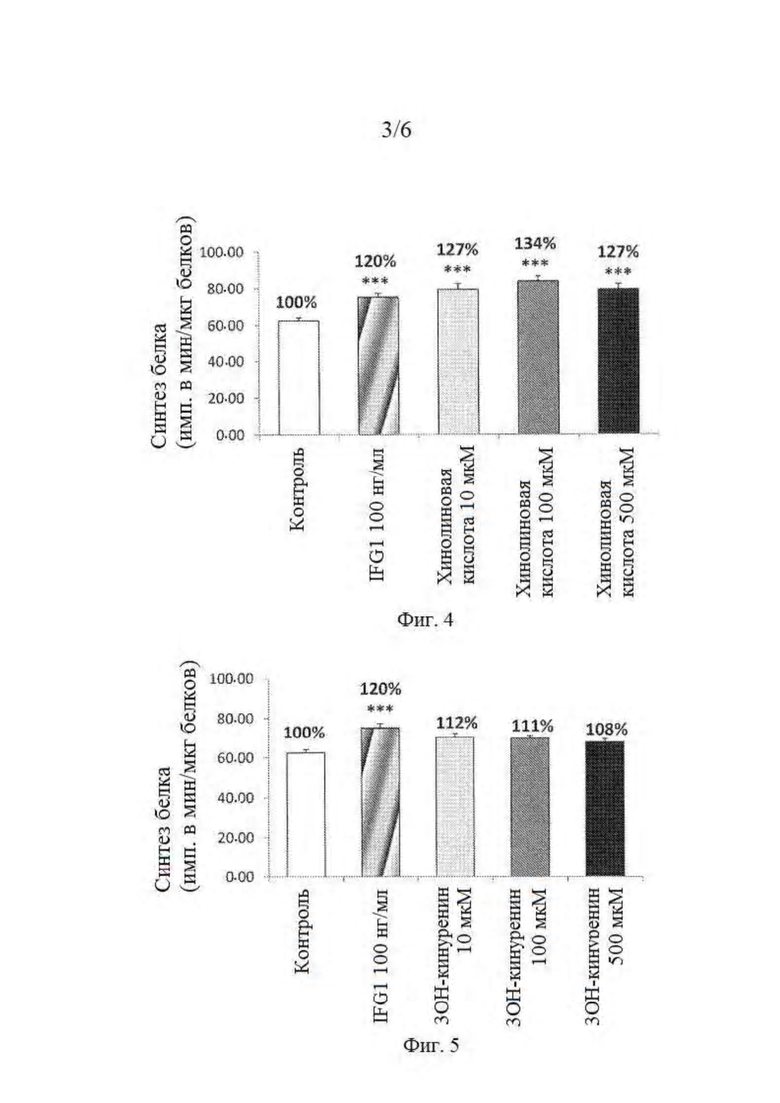
На фигуре 4 представлено действие пиколиновой кислоты на синтез белка в мышечных клетках С2С12.
На фигуре 5 представлено действие 3ОН-кинуренина на синтез белка в мышечных клетках С2С12.
На фигуре 6 представлено действие кинуреновой кислоты на экспрессию гена миостатина в мышечных клетках С2С12.
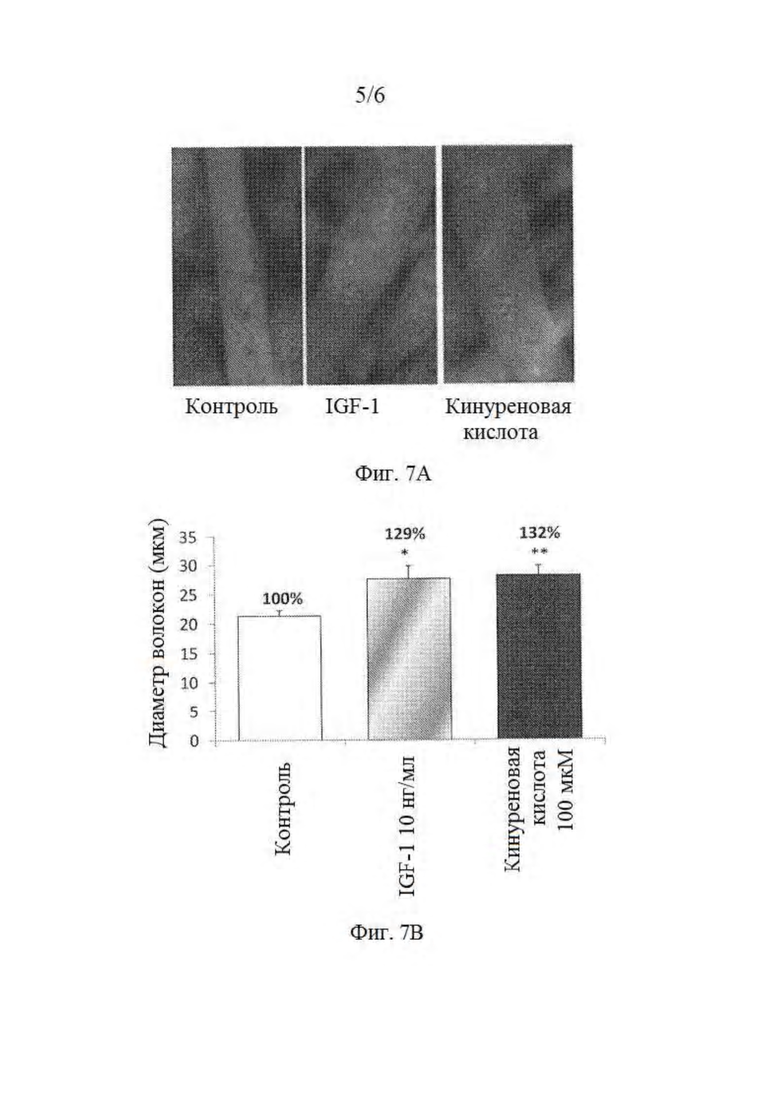
На фигуре 7 представлено действие кинуреновой кислоты на морфометрические параметры мышечных волокон С2С12 (Фигуры 7А-В).
На фигуре 8 представлено действие кинуреновой кислоты на мышечную атрофию, индуцированную иммобилизацией в течение 7 дней у здоровых мышей.
Пример 1. Измерение синтеза белка в клетках С2С12.
Клетки подсчитывают и высевают при плотности 20000 клеток на лунку в 24-луночный планшет в среде DMEM, содержащей глюкозу в пропорции 4,5 г/л и дополненной фетальной телячьей сывороткой (10%) и антибиотиками (пенициллином и стрептомицином). Через сорок восемь часов индуцируют дифференцировку миобластов посредством частичного обеднения сыворотки (2% вместо 10%) в течение 5 дней. Затем клетки помещают в среду без глюкозы или лейцина (среда Кребса) на 1 ч при 37°С, затем инкубируют в течение 150 мин в присутствии тестируемых продуктов (DMSO (контроль), кинуреновой кислоты, или антраниловой кислоты, или хинолиновой кислоты, или пиколиновой кислоты, или 3ОН-кинуренина) или эталона (IGF-1, 100 нг/мл) в бессывороточной среде DMEM, содержащей 2,5 мкКи/мл меченного изотопом лейцина. В конце инкубации супернатанты удаляют и клетки лизируют в 0,1N растворе NaOH в течение 30 мин. Радиоактивность измеряют в клеточной фракции, а общее количество белков определяют путем анализа по методу Лоури. Каждое состояние оценивают по меньшей мере с n=6; согласно авторам изобретения, IGF-1, 100 нг/мл, является контролем стимуляции синтеза белка. Результаты выражены в имп. в мин/мкг белков после 150 мин инкубации или в процентах относительно контрольного состояния. Результаты выражают в % от контроля и проводится статистический тест: тест Даннетта или Dun (*р<0,05, **р<0,01, ***р<0,001 по сравнению с контролем). Результаты, полученные с кинуреновой кислотой, антраниловой кислотой, хинолиновой кислотой, пиколиновой кислотой и 3ОН-кинуренином, представлены на фигурах 1-5. Они демонстрируют, что кинуреновая кислота, антраниловая кислота, хинолиновая кислота и пиколиновая кислота в значительной степени индуцируют синтез белка. Дозозависимая стимуляция синтеза белка наблюдается через 150 мин инкубации в присутствии кинуреновой кислоты. С другой стороны, 3ОН-кинуренинин, другой метаболит триптофана, не влияет на синтез белка.
Пример 2. Измерение экспрессии гена миостатина в клетках С2С12.
Клетки миобластов С2С12 (АТСС CRL-1772) высевают в 24-луночные планшеты с плотностью 30000 клеток на лунку и культивируют в среде DMEM, содержащей глюкозу в пропорции 4,5 г/л и дополненной фетальной сывороткой теленка (10%) и антибиотиками (пенициллином и стрептомицином). Через сорок восемь часов индуцируют дифференцировку миобластов посредством частичного обеднения сыворотки (2% вместо 10%) в течение 5 дней. Затем клетки помещают в бессывороточную, обедненную глюкозой среду (DMEM, содержащую 1 г/л глюкозы) в присутствии тестируемых молекул (DMSO (контроль) или IGF-1 (100 нг/мл) или кинуреновой кислоты) или эталонов (IGF-1 в концентрации 100 нг/мл) в течение 6 часов. В конце эксперимента матричные РНК (мРНК) экстрагируют, используя традиционную методологию на основе фенола и хлороформа. Кратко, клетки лизируют в растворе тризола (Sigma Т9424), содержащем сильную кислоту и фенол. мРНК отделяют от белков путем добавления хлороформа с последующим центрифугированием. Затем ее осаждают из изопропанола, чтобы затем суспендировать в концентрации 1 мкг/мкл в ультрачистой воде, не содержащей РНКазы и ДНКазы. Затем 1 мкг мРНК превращают путем обратной транскрипции в комплементарную ДНК с использованием фермента AMV в присутствии праймера и смеси нуклеотидов в соответствии с протоколом, предоставленным поставщиком (Applied Biosystems 4368814). Экспрессию гена исследуют с помощью полимеразной цепной реакции, обычно называемой ПЦР, в количественных условиях, отсюда и специфическое название кПЦР. кПЦР выполняют в ПЦР-анализаторе реального времени 7900НТ Fast (Applied Biosystems). Условия программирования являются стандартными и состоят из 1 цикла при 95°С в течение 15 минут, за которым следуют 40 циклов при 95°С в течение 15 с и при 60°С в течение 1 мин и заканчивающиеся стадией кривой плавления между 60°С и 95°С. Все анализируемые образцы содержат 100 мг кДНК, буфер кПЦР, включающий фермент, смесь олигонуклеотидов и интеркалирующий агент (sybergreen) и пару праймеров, специфичных для изучаемого гена, стратегически выбранных между двумя последовательностями экзонов и в конечной концентрации 200 нМ. Флуоресцентные зонды связываются с двухцепочечной ДНК и флуоресцируют только один раз, когда связываются с ДНК. Порог флуоресценции устанавливается программой машины. Когда количество ДНК позволяет флуоресцентному зонду превысить этот порог, получают номер цикла ПЦР, называемый «Ct» для «Cycle Threshold» («Порогового цикла»). Именно это значение составляет основу для расчетов для сравнительного количественного определения ДНК. Соотношение R устанавливается между количеством исходной ДНК образца и количеством исходной ДНК контроля, который не подвергали обработке (т.е. R=2-(Ct образца - Ct контроля)), и это измерение, которое связано с измерением генов домашнего хозяйства, которые, как известно, не модулируются обработкой (т.е. R=2-ΔΔCt).
Используемые праймеры приведены в таблице 1 ниже:

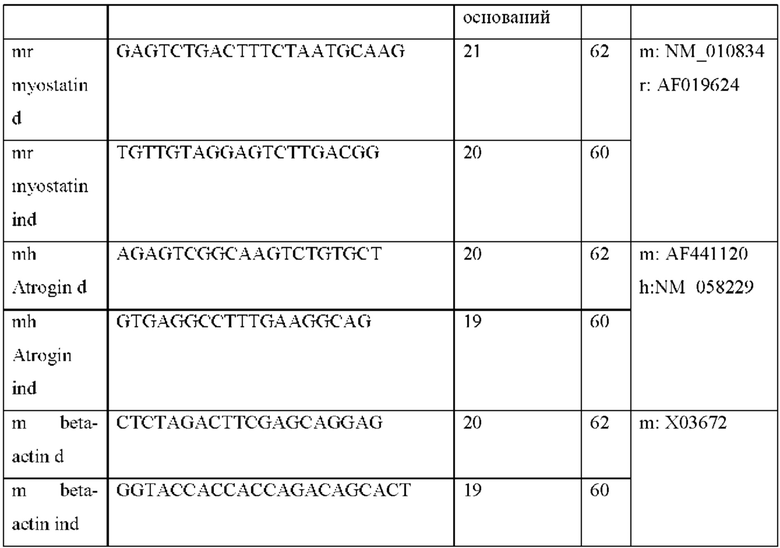
В конце инкубации экспрессию гена миостатина измеряют с помощью кПЦР в реальном времени и стандартизируют, используя ген домашнего хозяйства бета-актина. Проводят статистический тест: тест Даннетта или Dun (*р<0,05, **р<0,01, ***р<0,001 по сравнению с контролем). Результаты, полученные с кинуреновой кислотой, представлены на фигуре 6. Значительное дозозависимое ингибирование экспрессии гена миостатина наблюдается после 6 часов инкубации с кинуреновой кислотой.
Пример 3: Оценка диаметра мышечных волокон С2С12
Клетки миобластов С2С12 (АТСС CRL-1772) высевают в 8-луночные планшеты, обработанные глицерином, при плотности 10000 клеток на лунку и культивируют в среде DMEM, содержащей глюкозу в пропорции 4,5 г/л и дополненной фетальной сывороткой теленка (10%) и антибиотиками (пенициллином и стрептомицином). Через сорок восемь часов индуцируют дифференцировку миобластов посредством частичного обеднения сыворотки (2% вместо 10%) в течение 3 дней. Затем клетки помещают в бессывороточную, обедненную глюкозой среду (DMEM, содержащую 1 г/л глюкозы) в присутствии тестируемых молекул (DMSO (контроль) или IGF-1 (100 нг/мл) или кинуреновой кислоты) или эталонов (IGF-1 в концентрации 10 нг/мл или дексаметазона (10 мкМ) в течение 3 дней. В конце культивирования клетки промывают и фиксируют с использованием 2,5% раствора глутаральдегида/0,1% тритона в течение 1 ч при температуре окружающей среды. Клеточный слой покрывают DAPI (флуоресцентная маркировка клеточного ядра). После хранения в темноте в течение 16 ч на холоде предметные стекла исследуют под флуоресцентным микроскопом (Carl Zeiss, AxioVert 200), и изображения анализируют с использованием программного обеспечения Axiovision 4.1 для измерения диаметра волокон.
Демонстрируют типовое изображение каждого состояния. Проводят статистический тест: тест Даннетта или Dun (*р<0,05, **р<0,01, ***р<0,001 по сравнению с контролем). Результаты, полученные с кинуреновой кислотой, представлены на фигуре 7. После инкубации в течение 3 дней в присутствии кинуреновой кислоты (100 мкМ) наблюдается увеличение размера мышечных волокон С2С12.
Пример 4: Действие кинуреновой кислоты на мышечную атрофию, индуцированную иммобилизацией у мышей
Известно, что иммобилизация конечностей вызывает атрофию скелетных мышц с участием механизмов, связанных с деградацией белка, изменением типов мышечных волокон, окислительным стрессом или воспалительными механизмами. Кратко, в этом исследовании использовали самцов мышей CD1 в возрасте 8-9 недель. Лапу левой задней конечности иммобилизовали на 7 дней в соответствии с процедурой, описанной Caron et al. (2009), в положении дорзо-тибиального сгибания, с помощью хирургической скобки. Другую лапу (правую заднюю конечность) используют в качестве контроля. На время иммобилизации одна группа животных (n=12) получала обработку кинуреновой кислотой (3 мг/кг в день) в питьевой воде. Другая группа животных служила контролем (n=16 животных). В конце 7 суток исследования животных умерщвляли, чтобы извлечь переднюю большеберцовую мышцу из двух задних конечностей. Для каждого животного вычисляют разницу между массой мышц иммобилизованной конечности и свободной конечности, которую затем соотносят с массой тела. Результаты выражают в виде потери массы иммобилизованной конечности относительно контрольной конечности (в мг на г массы тела), и проводят статистический тест: критерий Стьюдента (*р<0,05, **р<0,01, ***р<0,001 по сравнению с контрольной группой). Полученные результаты показывают, что кинуреновая кислота значительно снижает потерю массы мышцы (Tibialis anterior), вызванную иммобилизацией, по сравнению с контрольной группой без обработки (фигура 8).
ЛИТЕРАТУРА
Bass J et al., Domest Anim Endocrinol, 1999, 17(2-3): 191-197
Bauer J et al., J Am Med Dir Assoc, 2013, 14: 542-559
Beyer et al., Curr. Opin. Clin. Nutr. Metab. Care, 2012, 15: 12-22
Biolo G et al., Am J Clin Nutr, 2008, 88: 950-958
Biolo et al., Clinical Nutrition, 2014, 33: 737-748
Bosutti A et al., J Clin Endocrinol Metab, 2008, 93: 3226-3229
Caron AZ et al. J Appl Physiol. 2009; 106: 2049-2059
Deutz NE et al., Clin Nutr, 2014, 33(6): 929-36
Donarski J.A. et al. Food Chemistry, 2010, 118: 987-994
Dukes A. et al., Nutrition, 2015, 31: 1018-1024
Guillet С et al., Obes Rev, 2012, 13 (Suppl. 2): 51-57
Guillet С et al., J Clin Endocrinol Metab, 2009, 94: 3044-3050
Lee SJ. Immunol Endocr Metab Agents Med Chem., 2010, 10: 183-194
Lin FD, et al., J Nutr., 1988, 118: 445-449
McPherron AC et al., J Clin Invest. 2002, 109: 595-601
McPherron AC and Lee, Proc. Natl. Acad. Sci. USA 2003, 100 (260): 15842-15846
Sanfilippo et al., Ital J Anat Embryol, 1995, 100: 131-141
Turski M.P., et al. Planta Med., 2011, 77: 858-864
Turski M.P. et al. Plant Foods Hum Nutr, 2012, 67:17-23
Widner В et al., Clinical Chemistry, 1997, 43: 2424-26.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> Metabrain Research
<120> ИСПОЛЬЗОВАНИЕ МЕТАБОЛИТОВ ТРИПТОФАНА ДЛЯ ЛЕЧЕНИЯ МЫШЕЧНОЙ АТРОФИИ
<130> 1H308550 0005
<160> 6
<170> PatentIn version 3.5
<210> 1
<211> 22
<212> ДНК
<213> Искусственная последовательность
<220>
<223> mr myostatin d
<400> 1
gagtctgact ttctaatgca ag 22
<210> 2
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<223> mr myostatin ind
<400> 2
tgttgtagga gtcttgacgg 20
<210> 3
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<223> mh Atrogin d
<400> 3
agagtcggca agtctgtgct 20
<210> 4
<211> 19
<212> ДНК
<213> Искусственная последовательность
<220>
<223> mh Atrogin ind
<400> 4
gtgaggcctt tgaaggcag 19
<210> 5
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<223> m beta-actin d
<400> 5
ctctagactt cgagcaggag 20
<210> 6
<211> 19
<212> ДНК
<213> Искусственная последовательность
<220>
<223> m beta-actin ind
<400> 6
ggtaccacca gacagcact 19
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ, ПРИМЕНЯЕМЫЕ ДЛЯ ЛЕЧЕНИЯ МЫШЕЧНОЙ АТРОФИИ | 2016 |
|
RU2715553C2 |
| ПРИМЕНЕНИЕ АНГИОГЕНИНА ИЛИ АГОНИСТОВ АНГИОГЕНИНА ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ И НАРУШЕНИЙ | 2009 |
|
RU2519645C2 |
| ХИМИЧЕСКИЕ СОЕДИНЕНИЯ И ИХ ПРИМЕНЕНИЕ ДЛЯ УЛУЧШЕНИЯ КАЧЕСТВА МЫШЦ | 2015 |
|
RU2724329C2 |
| ПРИМЕНЕНИЕ АНТАГОНИСТОВ МИОСТАТИНА, СОДЕРЖАЩИЕ ИХ КОМБИНАЦИИ И ИХ ПРИМЕНЕНИЕ | 2016 |
|
RU2781401C2 |
| Генетическая конструкция и способ экспрессии ERVW-1 и MYMK | 2025 |
|
RU2839754C1 |
| УЛУЧШЕННЫЕ АНТИТЕЛА-АНТАГОНИСТЫ ПРОТИВ GDF-8 И ИХ ПРИМЕНЕНИЯ | 2013 |
|
RU2630634C2 |
| Новые гибридные ActRIIB белки-ловушки лигандов для лечения заболеваний, связанных с мышечной атрофией | 2016 |
|
RU2733492C2 |
| КОМПОЗИЦИИ И СПОСОБЫ ДЛЯ УЛУЧШЕННОГО МЫШЕЧНОГО МЕТАБОЛИЗМА | 2016 |
|
RU2730853C2 |
| КОМПОЗИЦИИ, СОДЕРЖАЩИЕ НИКОТИНАМИДРИБОЗИД И УРОЛИТИН | 2016 |
|
RU2751638C2 |
| ИНГИБИТОР СИГНАЛА МИОСТАТИНА | 2019 |
|
RU2820270C2 |




Изобретение относится к области медицина и фармацевтики, а именно к лечению мышечной атрофии. Раскрывается применение кинуреновой кислоты для лечения мышечной атрофии, представляющей собой пресаркопению, саркопению или тяжелую саркопению. Изобретение обеспечивает эффективное лечение мышечной атрофии. 4 з.п. ф-лы, 8 ил., 1 табл., 4 пр.
1. Применение кинуреновой кислоты для лечения мышечной атрофии у млекопитающего, причем мышечная атрофия представляет собой пресаркопению, саркопению или тяжелую саркопению.
2. Применение по п. 1, отличающееся тем, что пресаркопения, саркопения или тяжелая саркопения связаны со старением, ожирением или хроническими заболеваниями, такими как диабет или сердечная недостаточность.
3. Применение по любому из пп. 1 или 2, отличающееся тем, что млекопитающее также страдает метаболическими заболеваниями, такими как диабет, ожирение, неалкогольная жировая болезнь печени (NAFLD) или неалкогольный стеатогепатит (NASH), хроническими воспалительными заболеваниями кишечника (IBD), раком, почечной или сердечной недостаточностью, нейродегенеративными патологическими состояниями или психическими расстройствами, такими как депрессия, в частности диабетом.
4. Применение по любому из пп. 1-3, отличающееся тем, что млекопитающее является человеком.
5. Применение по любому из пп. 1-4, отличающееся тем, что кинуреновая кислота находится в очищенном виде или в виде растительного экстракта.
| WO 2016114655 A1, 21.07.2016 | |||
| MICHAEL D | |||
| LOVELACE et al | |||
| Current Evidence for a Role of the Kynurenine Pathway of Tryptophan Metabolism in Multiple Sclerosis, Frontiers Immunology, 2016, vol | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| WO 2010007085 A1, 21.01.2010 | |||
| WALKER LANCE S et al | |||
| Chromium picolinate effects on body composition and muscular performance in | |||
Авторы
Даты
2023-10-31—Публикация
2017-09-05—Подача