ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННУЮ ЗАЯВКУ
[0001] В данной заявке заявляется приоритет по предварительной заявке на патент США №14612973, поданной 3 февраля 2015, включенной в данный документ в полном объеме посредством ссылки.
ОБЛАСТЬ ТЕХНИКИ
[0002] Данное описание предлагает композиции и способы для повышения уровня синтеза мышечного протеина, уменьшения мышечного протеолиза, увеличения мышечной массы и/или силы, и улучшения спортивной аэробной/анаэробной характеристики. Полезные композиции включают, но не ограничиваются ими, экстракты Rhaponticum и Rhodiola, и их комбинации.
КРАТКОЕ ОПИСАНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
[0003] В одном аспекте изобретение включает композицию, содержащую экстракт Rhaponticum. В некоторых вариантах реализации изобретения экстракт Rhaponticum содержит по меньшей мере 0,01%, 0,05%, 0,1%, 0,2%, 0,3%, 0,4%, 0,5%, 0,75%, 1%, 2%, 3%, 4%, 5%, 6%, 7%, 8%, 9% или 10% экдистероидов, включая, например, около 0,1 до 10% экдистероидов или около 0,4%-5% экдистероидов. В некоторых вариантах реализации изобретения композиция на основе экстракта Rhaponticum содержит по меньшей мере 0,01%, 0,05%, 0,1%, 0,2%, 0,3%, 0,4%, 0,5%, 0,75%, 1%, 2%, 3%, 4%, 5%, 6%, 7%, 8%, 9% или 10% 20-гидроксиэкдизона, включая, например, около 0,1-5,0% 20-гидроксиэкдизона.
[0004] В другом аспекте изобретение включает композицию, содержащую экстракт Rhodiola. В некоторых вариантах реализации изобретения экстракт Rhodiola содержит по меньшей мере 0,5%, 0,75%, 1%, 2%, 3%, 4%, 5%, 6%, 7%, 8%, 9% или 10% салидрозидов, включая, например, около 1-4%. В некоторых вариантах реализации изобретения композиция на основе экстракта Rhodiola содержит по меньшей мере 0,1%, 0,2%, 0,3%, 0,4%, 0,5%, 0,75%, 1%, 2%, 3%, 4%, 5%, 6%, 7%, 8%, 9% или 10% розавинов, включая, например, около 0,5-10% или около 3%-6% розавинов. В некоторых вариантах реализации изобретения композиция содержит по меньшей мере 0,1%, 0,2%, 0,3%, 0,4%, 0,5%, 0,75%, 1%, 2%, 3%, 4%, 5%, 6%, 7%, 8%, 9% или 10% розавина, включая, например, около 0,5-10% розавина или около 1%-5% розавина. В некоторых вариантах реализации изобретения, композиция на основе экстракта Rhodiola содержит по меньшей мере 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% или 99% экстракта Rhodiola, включая, например, около 50%-99%, около 60%-95%, около 70%-95% экстракта Rhodiola.
[0005] В одном аспекте изобретение включает композицию, содержащую экстракт Rhaponticum и экстракт Rhodiola. В некоторых вариантах реализации изобретения экстракт Rhaponticum содержит по меньшей мере 0,01%, 0,05%, 0,1%, 0,2%, 0,3%, 0,4%, 0,5%, 0,75%, 1%, 2%, 3%, 4%, 5%, 6%, 7%, 8%, 9% или 10% экдистероидов, включая, например, около 0,1-10% экдистероидов или около 0,4%-5% экдистероидов. В некоторых вариантах реализации изобретения композиция содержит по меньшей мере 0,01%, 0,05%, 0,1%, 0,2%, 0,3%, 0,4%, 0,5%, 0,75%, 1%, 2%, 3%, 4%, 5%, 6%, 7%, 8%, 9% или 10% 20-гидроксиэкдизона, включая, например, около 0,1-5,0% 20-гидроксиэкдизона.
[0006] В некоторых вариантах реализации изобретения экстракт Rhodiola содержит по меньшей мере 0,5%, 0,75%, 1%, 2%, 3%, 4%, 5%, 6%, 7%, 8%, 9% или 10% салидрозидов, включая, например, около 1-4%. В некоторых вариантах реализации изобретения композиция содержит по меньшей мере 0,1%, 0,2%, 0,3%, 0,4%, 0,5%, 0,75%, 1%, 2%, 3%, 4%, 5%, 6%, 7%, 8%, 9% или 10% розавинов, включая, например, около 3-6% розавинов. В некоторых вариантах реализации изобретения, композиция содержит по меньшей мере 0,1%, 0,2%, 0,3%, 0,4%, 0,5%, 0,75%, 1%, 2%, 3%, 4%, 5%, 6%, 7%, 8%, 9% или 10% розавина, включая, например, около 2-5% розавина.
[0007] В некоторых вариантах реализации изобретения, композиция содержит по меньшей мере 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% или 99% экстракта Rhodiola, включая, например, около 50%-99%, около 60%-95%, около 70%-95% экстракта Rhodiola.
[0008] В другом аспекте изобретение включает композиции содержащие (i) по меньшей мере 0,1%, 0,2%, 0,3%, 0,4%, 0,5%, 0,75%, 1%, 2%, 3%, 4%, 5%, 6%, 7%, 8%, 9% или 10% экдистероидов, включая, например, около 0,1-10% экдистероидов или около 0,4%-5% экдистероидов, и (ii) по меньшей мере 0,5%, 0,75%, 1%, 2%, 3%, 4%, 5%, 6%, 7%, 8%, 9% или 10% салидрозидов, включая, например, около 1-4%. В некоторых вариантах реализации изобретения композиция содержит по меньшей мере 0,1%, 0,2%, 0,3%, 0,4%, 0,5%, 0,75%, 1%, 2%, 3%, 4%, 5%, 6%, 7%, 8%, 9% или 10% 20-гидроксиэкдизона, включая, например, около 0,1-5,0% 20-гидроксиэкдизона. В некоторых вариантах реализации изобретения композиция содержит по меньшей мере 0,1%, 0,2%, 0,3%, 0,4%, 0,5%, 0,75%, 1%, 2%, 3%, 4%, 5%, 6%, 7%, 8%, 9% или 10% розавинов, включая, например, около 3-6% розавинов. В некоторых вариантах реализации изобретения, композиция содержит по меньшей мере 0,1%, 0,2%, 0,3%, 0,4%, 0,5%, 0,75%, 1%, 2%, 3%, 4%, 5%, 6%, 7%, 8%, 9% или 10% розавина, включая, например, около 2-5% розавина.
[0009] В других вариантах реализации изобретения, любые вышеупомянутые композиции могут быть включены в фармацевтический лекарственный состав. Композиция может быть приготовлена в любой удобной и подходящей лекарственной форме в зависимости от пути предполагаемого введения. Подходящие лекарственные формы для перорального введения включают, например, таблетку, капсулу, порошок, раствор, суспензию, сироп, или эликсир. Необязательно, композиция дополнительно содержит фармацевтически приемлемое вспомогательное вещество или носитель, или другой фармацевтически активный или не активный ингредиент.
[0010] Другие аспекты изобретения включают способы повышения уровня синтеза протеина, увеличения мышечной силы и/или уменьшения протеолиза протеина у субъекта путем введения субъекту любой из композиций или фармацевтических лекарственных составов, описанных выше. Дополнительные аспекты изобретения включают способы лечения состояний, связанных с или характеризующихся мышечной атрофией у субъекта, путем введения субъекту любой из композиций или фармацевтических лекарственных составов, описанных выше. Композиция или лекарственный состав могут быть введены субъекту с помощью любого подходящего способа введения. В одном варианте реализации изобретения, композицию вводят перорально. В некоторых вариантах реализации изобретения, субъекту вводят дневную дозу по меньшей мере 1 мг/кг/день, 5 мг/кг/день, 10 мг/кг/день, 20 мг/кг/день, 30 мг/кг/день, 40 мг/кг/день, 50 мг/кг/день, 75 мг/кг/день, 100 мг/кг/день, 200 мг/кг/день, 400 мг/кг/день, 600 мг/кг/день, 800 мг/кг/день, 1000 мг/кг/день, 2000 мг/кг/день, 3000 мг/кг/день, 5000 мг/кг/день или более в день. В одном варианте реализации изобретения, лекарственный состав для перорального введения является около 30-1000 мг/кг/день. В другом варианте реализации изобретения, лекарственная форма для перорального введения составляет около 50-100 мг/кг/день, около 5-50 мг/кг/день, или менее, чем 200 мг/кг/день. В дополнительном варианте реализации изобретения, лекарственная форма для перорального введения может составлять около 200-500 мг/день, или около 50-2000 мг/день. Общая суточная доза может вводиться в виде единичной дозы или разделяться на несколько доз, вводимых в разное время (например, два, три, четыре или более раз в день).
[0011] В различных вариантах реализации изобретения, дозировка может быть модифицирована на основе типа субъекта и/или массы субъекта. Например, в некоторых вариантах реализации изобретения подходящая дозировка субъекта-человека может быть 50-2000 мг/день или 200-500 мг/день. Например, в некоторых вариантах реализации изобретения желаемая дозировка субъекта-человека или субъекта-жвачного может быть 5-50 мг/кг/день или менее чем 200 мг/кг/день.
[0012] В некоторых вариантах реализации изобретения, субъекта могут лечить от состояний включающих, саркопению, саркопенное ожирение, рак, рассеянный склероз, мышечную дистрофию, перелом кости, требующий иммобилизации (например, шина или гипсовая повязка), амиотрофический боковой склероз (ALS), периферическую невропатию, инсульт или кахексию. Субъекты могут иметь или быть диагностированными, как имеющие такое состояние, и такое состояние может быть идиопатическим или вторичным по отношению к другому состоянию. В некоторых вариантах реализации изобретения, субъект является млекопитающим включая, например, человека или животное (например, животное из семейства собачьих, кошачьих, или овец, быков, или жвачных животных, и т.п.). Соответственно, в различных вариантах реализации изобретения, описанных в данном документе, композиции могут быть использованы в пищевых продуктах, кормовых продуктах или пищевых добавках для людей или животных.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
[0013] Фиг. 1а представляет собой графическое изображение суммы всех фенолов, идентифицированных в экстракте Примера 11;
[0014] Фиг. 1b представляет собой графическое изображение суммы всех органических кислот, идентифицированных в экстракте Примера 11;
[0015] Фиг. 2 представляет собой графическое изображение суммы всех углеводов, идентифицированных в экстракте Примера 11;
[0016] Фигуры 3а, 3b, 4а, 4b, 5а, 5b, 6а, 6b, 7а, и 7b представляют собой гистограммы, изображающие определение уровня фосфорилирования S6K1 треонина 389 в миотрубочках С2С12 после инкубации с 5 различными лекарственными составами экстракта Rhaponticum при трех концентрациях, и с высоким и низким содержанием аминокислот;
[0017] Фигуры 8а, 8b, 9а, 9b, 10а, 10b, 11а, 11b, 12а, и 12b представляют собой гистограммы, изображающие определение уровня фосфорилирования Akt треонина 308 в миотрубочках С2С12 после инкубации с 5 различными лекарственными составами экстракта Rhaponticum при трех концентрациях, и с высоким и низким содержанием аминокислот;
[0018] Фигуры 13а, 13b, 14а, 14b, 15а, 15b, 16а, 16b, 17а и 17b представляют собой гистограммы, изображающие определение уровня синтеза протеина в миотрубочках С2С12 после инкубации с 5 различными лекарственными составами экстракта Rhaponticum при трех концентрациях, и с высоким и низким содержанием аминокислот;
[0019] Фигуры 18а и 18b представляют собой гистограммы, изображающие определение уровня синтеза протеина в миотрубочках С2С12 после инкубации с экстрактами Rhaponticum F0 и Rhodiola при трех концентрациях;
[0020] Фигуры 19а, 19b, 20а, 20b и 21 представляют собой гистограммы, изображающие определение уровня синтеза протеина в миотрубочках С2С12 после инкубации с экстрактами Rhaponticum F0 и Rhodiola отдельно, или в комбинации при двух концентрациях;
[0021] Фигуры 22а и 22b представляют собой гистограммы, изображающие эффект экстрактов Rhaponticum F0 и Rhodiola на уровень экспрессии генов миостатина и атрогина в С2С12 миотрубочках;
[0022] Фигуры 23а, 23b, 24а и 24b представляют собой гистограммы, изображающие эффект ко-инкубации экстрактов Rhaponticum F0 и Rhodiola на уровень экспрессии гена миостатина в С2С12 миотрубочках;
[0023] Фигуры 25а, 25b, 26а и 26b представляют собой гистограммы изображающие эффект ко-инкубации экстрактов Rhaponticum F0 и Rhodiola на уровень экспрессии гена атрогина в С2С12 миотрубочках;
[0024] Фигуры 27а, 27b и 28 представляют собой гистограммы изображающие определение уровня синтеза протеина в миотрубочках С2С12 после инкубации с различными лекарственными формами экстрактов Rhaponticum при двух концентрациях;
[0025] Фиг. 29а изображает блок-схему представляющую способ извлечения из экстрактов из корня Rhaponticum; и
[0026] Фиг. 29b изображает блок-схему, представляющую фракции, полученные с использованием разных растворителей.
[0027] Фиг. 30а представляет собой гистограмму, изображающую увеличение в силе захвата (в кг-силе) у крыс породы Вистар в контрольной группе и в экспериментальной группе после 42 дней лечения, с использованием композиции Rhaponticum и Rhodiola.
[0028] Фиг. 30b представляет собой гистограмму, изображающую увеличение в силе захвата (в кг-силе / г веса тела) у крыс породы Вистар в контрольной группе и в экспериментальной группе после 42 дней лечения с использованием композиции Rhaponticum и Rhodiola.
[0029] Фиг. 31а представляет собой гистограмму, изображающую вес длинного разгибателя пальцев (EDL) (в граммах) у крыс породы Вистар в контрольной группе и в экспериментальной группе после 42 дней лечения с использованием композиции Rhaponticum и Rhodiola.
[0030] Фиг. 31b представляет собой гистограмму, изображающую вес (EDL) (в виде процента от общей массы тела) у крыс породы Вистар в контрольной группе и в экспериментальной группе после 42 дней лечения с использованием композиции Rhaponticum и Rhodiola.
[0031] Фиг. 32а представляет собой гистограмму, изображающую вес камбаловидной мышцы (в граммах) у крыс породы Вистар в контрольной группе и в экспериментальной группе после 42 дней лечения с использованием композиции Rhaponticum и Rhodiola.
[0032] Фиг. 32b представляет собой гистограмму, изображающую вес камбаловидной мышцы (в виде процента от общей массы тела) у крыс породы Вистар в контрольной группе и в экспериментальной группе после 42 дней лечения с использованием композиции Rhaponticum и Rhodiola.
[0033] Фиг. 33а представляет собой гистограмму, изображающую содержание протеина в длинном разгибателе пальца (EDL) у крыс породы Вистар в контрольной группе и в экспериментальной группе после 42 дней лечения с использованием композиции Rhaponticum и Rhodiola.
[0034] Фиг. 33b представляет собой гистограмму, изображающую содержание протеина в EDL у крыс породы Вистар в контрольной группе и в экспериментальной группе после 42 дней лечения с использованием композиции Rhaponticum и Rhodiola.
[0035] Фиг. 34а представляет собой гистограмму, изображающую содержание протеина в камбаловидной мышце у крыс породы Вистар в контрольной группе и в экспериментальной группе после 42 дней лечения с использованием композиции Rhaponticum и Rhodiola.
[0036] Фиг. 34b представляет собой гистограмму, изображающую содержание протеина в камбаловидной мышце у крыс породы Вистар в контрольной группе и в экспериментальной группе после 42 дней лечения с использованием композиции Rhaponticum и Rhodiola.
[0037] Фиг. 35а изображает вестерн блот протеина, извлеченного из образца ПДФ мышцы с помощью анти-пуромицина.
[0038] Фиг. 35b представляет собой график, изображающий относительные единицы уровней пуромицина, нормированные на количество введения и отрицательный контроль. * Значительно отличается р<0,05. * * Значительно отличается р<0,001,
[0039] Фиг. 35с представляет собой график, изображающий относительные единицы уровней пуромицина, нормированные на количество введения и сывороточные протеины. * Значительно отличается р<0,05. * * Значительно отличается р<0,001,
[0040] Фиг. 35d представляет собой график, изображающий относительные единицы уровней пуромицина, нормированные на количество введения и лечение Rhodiola rosea. * Значительно отличается р<0,05. * * Значительно отличается р<0,001,
[0041] Фиг. 35е представляет собой график, изображающий относительные единицы уровней пуромицина, нормированные на количество введения и лечение Rhaponticum carthamoides. * Значительно отличается р<0,05. * * Значительно отличается р<0,001,
[0042] Фиг. 36а изображает вестерн блот протеина извлеченного из образца дельтовидной мышцы с помощью анти пуромицина. * Значительно отличается р<0,05. * * Значительно отличается р<0,001,
[0043] Фиг. 36b представляет собой график, изображающий относительные единицы уровней пуромицина, нормированные на количество введения и отрицательный контроль. * Значительно отличается р<0,05. * * Значительно отличается р<0,001,
[0044] Фиг. 36с представляет собой график, изображающий относительные единицы уровней пуромицина, нормированные на количество введения и сывороточные протеины. * Значительно отличается р<0,05. * * Значительно отличается р<0,001,
[0045] Фиг. 36d представляет собой график, изображающий относительные единицы уровней пуромицина, нормированные на количество введения и лечение Rhodiola rosea. * Значительно отличается р<0,05. * * Значительно отличается р<0,001,
[0046] Фиг. 36е представляет собой график, изображающий относительные единицы уровней пуромицина, нормированные на количество введения и лечение Rhaponticum carthamoides. * Значительно отличается р<0,05. * * Значительно отличается р<0,001,
[0047] Фиг. 37а изображает вестерн блот протеина извлеченного из образца бицепса с помощью анти пуромицина. В:
[0048] Фиг. 37b представляет собой график, изображающий относительные единицы уровней пуромицина, нормированные на количество введения и отрицательный контроль. * Значительно отличается р<0,05. * * Значительно отличается р<0,001,
[0049] Фиг. 37с представляет собой график, изображающий относительные единицы уровней пуромицина, нормированные на количество введения и сывороточные протеины. * Значительно отличается р<0,05. * * Значительно отличается р<0,001,
[0050] Фиг. 37d представляет собой график, изображающий относительные единицы уровней пуромицина, нормированные на количество введения и лечение Rhodiola rosea. * Значительно отличается р<0,05. * * Значительно отличается р<0,001,
[0051] Фиг. 37е представляет собой график, изображающий относительные единицы уровней пуромицина, нормированные на количество введения и лечение Rhaponticum carthamoides. * Значительно отличается p<0,05. * * Значительно отличается p<0,001,
[0052] Фиг. 38 представляет собой график уровней синтеза протеина во всех мышцах крысы (ПДФ, дельтовидной мышце и бицепсе вместе взятых) после интенсивного упражнения на сопротивление, данный график изображает относительные единицы уровней пуромицина нормированные на количество введения и негативный контроль. Значительно отличается от негативного контроля р<0,001,  Значительно отличается от сывороточных протеинов р<0,05.
Значительно отличается от сывороточных протеинов р<0,05.  Значительно отличается от лечения Rhodiola Rosea р<0,05.
Значительно отличается от лечения Rhodiola Rosea р<0,05.  : Значительно отличается от лечения Rhaponticum carthamoides р<0,001,
: Значительно отличается от лечения Rhaponticum carthamoides р<0,001,
[0053] Следует также отметить, что эти фигуры предназначены только для облегчения описания предпочтительных вариантов реализации изобретения. Фигуры не иллюстрируют каждый аспект описанных вариантов реализации изобретения и не ограничивают объем данного описания.
ПОДРОБНОЕ ОПИСАНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
[0054] Настоящее описание представляет примерные варианты реализации изобретения с использованием новых композиций для фармацевтического или пищевого применения у млекопитающих, предпочтительно у человека, для повышения уровня синтеза протеина, увеличения мышечной массы и/или мышечной силы. Действующие образцы демонстрируют, что комбинация экстрактов Rhodiola и Rhaponticum, и родственные синтетические композиции могут увеличивать уровень синтеза протеина, уменьшать протеолиз (ингибировать экспрессию атрогина-1 и миостатина), увеличивать мышечную массу и мышечную силу. В различных вариантах реализации изобретения, предложены композиции, содержащие экстракт Rhodiola rosea и/или экстракт Rhaponticum carthamoides. Синтетические композиции (то есть, композиции в которых один или более ингредиентов не получены из растений) также описаны в данном документе.
ЭКСТРАКТЫ RHAPONTICUM
[0055] Экстракты Rhaponticum могут быть получены из любого вида Rhaponticum включая (но не ограничиваясь ими) Rhaponticum acaule (L.) DC, Rhaponticum aulieatense Iljin, Rhaponticum australe (Gaudich.), Rhaponticum berardioides (Batt.), Rhaponticum canariense DC., Rhaponticum carthamoides (Willd.), Rhaponticum coniferum (L.) Greuter, Rhaponticum cossonianum (Ball) Greuter, Rhaponticum cynaroides Less., Rhaponticum exaltatum (Willk.) Greuter, Rhaponticum fontqueri, Rhaponticoides hajastana (Tzvelev) M.V.Agab. & Greuter, Rhaponticum heleniifolium Godr. & Gren., Rhaponticoides iconiensis (Hub.-Mor.) M.V.Agab. & Greuter, Rhaponticum insigne (Boiss.) Wagenitz, Rhaponticum integrifolium C.Winkl., Rhapontikum karatavicum Iljin, Rhaponticum longifolium (Hoffmanns. & Link) Dittrich, Rhaponticum lyratum C.Winkl. ex Iljin, Rhaponticum namanganicum Iljin, Rhaponticum nanum Lipsky, Rhaponticum nitidum Fisch, Rhaponticum pulchrum Fisch. & C.A. Mey. Rhaponticum repens (L.) Hidalgo, Rhaponticum scariosum Lam., Rhaponticum serratuloides (Georgi) Bobrov, Rhaponticum uniflorum (L.) DC. В некоторых вариантах реализации изобретения, экстракты Rhaponticum получены из растения выбраного из семейства Asteraceae, рода Rhaponticum и более конкретно вида Rhaponticum Carthamoides.
[0056] Экстракт может быть получен из любой части(ей) растения Rhaponticum, тем не менее, корень является особенно подходящим. Корень Rhaponticum может экстрагироваться растворителем из группы включающей этанол, метанол, воду, водный этанол, этилацетат, ацетон, гексан или любой стандартный для экстракции растворитель, предпочтительно водный этанол или воду, более предпочтительно раствор этанола в воде с от 10 до 90% об./об., и даже более предпочтительно раствор этанола в воде с от 30 до 70% (об./об.). В одном варианте реализации изобретения, экстракция состоит из смешивания перемолотого корня Rhaponticum с растворителем при соотношении растворитель: растение между 1:1 и 30:1 и растение может подвергаться единичной, или, как альтернативный вариант, двойной экстракции (или более экстракциям). Предпочтительная длительность экстракции составляет >1 ч, более предпочтительно 1,5 ч. В предпочтительном варианте изобретения, корень Rhaponticum смешивают с раствором этанола в воде (50% об./об.) в соотношении 10:1 и подвергают 3 последовательным экстракциям. После экстракции, комбинированная смесь может быть профильтрована и/или отцентрифугирована, и супернатант сконцентрирован до от 30 до 70% на сухое вещество, более предпочтительно до 50% на сухое вещество, и окончательно до твердой формы с <10% влаги, в виде порошка. Специалист в данной области техники признает, что существует множество способов получения экстрактов растений, и что они могут быть использованы в данном описании, в дополнение к конкретному способу описанному в данном документе.
[0057] Интересующими компонентами в Rhaponticum являются экдистероиды, в частности 20-гидроксиэкдизон ((2β, 3β, 5β, 22R)-2, 3, 14, 20, 22, 25-Гексагидроксихолест-7-ен-6-он). Это соединение может использоваться в качестве сравнения для определения качества лекарственных форм, несмотря на то, что это соединение может быть не единственным приводящим к эффектам, и смесь соединений вероятно сделает экстракт более эффективным по сравнению с чистым 20НЕ.
[0058] В некоторых вариантах реализации изобретения, экстракт Rhaponticum содержит по меньшей мере 0,01% суммы общего количества экдистероидов, около 0,05% до 99%, 98%, 97%, 96%, 95%, 90%, 80%, 70%, 60%, 50%, 40%, 30%, 20% или 10% суммы общего количества экдистероидов на основании общей массы экстракта (в весовом соотношении), более предпочтительно по меньшей мере около 0,1%-10% суммы общего количества экдистероидов, наиболее предпочтительно около 0,4%-5%, суммы общего количества экдистероидов на основании общей массы экстракта (в весовом соотношении).
[0059] В некоторых вариантах реализации изобретения, экстракт Rhaponticum содержит по меньшей мере 0,01%) 20-гидроксиэкдизона (20НЕ) на основании общей массы экстракта (в весовом соотношении), около 0,05%) до 99%, 98%, 97%, 96%, 95%, 90%, 80%, 70%, 60%, 50%, 40%, 30%, 20%, или 10% 20НЕ, более предпочтительно по меньшей мере около 0,1%-5,0% 20НЕ на основании общей массы экстракта (в весовом соотношении).
[0060] Дополнительно, экстракт Rhaponticum может также содержать экдистероиды отличные от экдистерона, такие как, в качестве не ограничивающего Примера, следующие экдистероиды: полиподин В, макистерон А, 2-деоксиэкдистерон, интегристерон А, интегристерон В, таксистерон, ажугастерон С, α-экдизон, лестерон, рапистерон D, инокостерон, рапистерон, 20-гидроксиэкдизон 2,3;20,22-диацетонид, 20-гидроксиэкдизон 2,3-моноацетонид; 20-гидроксиэкдизон 20,22-моноацетонид; 22-оксо-20-гидроксиэкдизон, 24(28)-дегидромакистерон А; (24z)-29-гидрокси-24(28)дегидромакистерон С; картамостерон; рубростерон, дигидрорубростерон; ростерон, изовитексирон, лейзеастерон, макистерон С, полиподин В 20,22-ацетонид; рапистерон В, рапистерон С, рапистерон D 20-ацетат, 24(24')(z)-дегидроамарастерон В, полиподин В-22-бензоат; картамостерон А, картамостерон В; амарастерон А; картамолейстерон; 24(28)-дегидроамарастерон В, 22-деокси-28-гидроксимакистерон С; 3-эпи-20-гидроксиэкдизон; 24-эпи-макистерон А, 14-эпи-понастерон А 22-глюкозид; 5-α-20-гидроксиэкдизон; 20-гидроксиэкдизон 2-ацетат, 20-гидроксиэкдизон 3-ацетат; 1β-гидроксимакистерон С; 26-гидроксимакистерон С; 15-гидроксипонастерон А; инокостерон 20,22-ацетонид, туркестон.
[0061] Экстракт Rhaponticum может также содержать экдистероиды: абутастерон 25-ацетокси-20-гидроксиэкдизон 3-о-; бета; -d-глюкопиранозид; ацетилпиннастерол; ахирантестерон; ажугакетальстерон а; ажугацетальстерон b; ажугалид е; ажугастерон b; ажугастерон b; ажугастерон с 3; 22-диацетонид; ажугастерон с 22-этилиден; ацеталь; ажугастерон с 22-моноацетонид; ажугастерон d; амарастерон а; амарастерон b; астерастер b; атротостерон а; атротостерон b; атротостерон с; блехнозид а; блехнозид b; бомбикостерол; бомбикостерол 3-фосфат; брахуистерон; калонистерон; кальвастер а; кальвастер b; канесценстерон; капитастерон; карпестерол; кастастерон; хеилантон а; хеилантон b; коронатастерон; цианостерон а; циастерон; циастерон 3-ацетат; циастерон 22-ацетат; циастерон 3-моноацетонид; циатистерон; дакрихаинанстерон; декумбестерон а; дегидроажугалактон; дегидроажугалактон; дегидроамарастерон b; дегидроциастерон 2-глюкозид; 3-дегидроэкдизон; 2-дегидро-3-эпи-20-гидроксиэкдизон; и/или 22-дегидро-12-гидроксисуастерон, дегидро-20-гидроксиэкдизон; 3-дегидро-20-гидроксиэкдизон; дегидро-242-гидроксимакистерон с дегидро-12-гидрокси-29-нор-циастероном; дегидро-12-гидрокси-29-нор-сенгостерон; дегидро-12-гидрокси-сенгостерон; (28)-дегидромакистерон а; 2-дегидропостстерон; 24-дегидропрециастерон; 2-деоксикастастерон; 22-деокси-21-дигидроксиэкдизон; 22-деокси-26-дигидроксиэкдизон; 2-деокси-26-дигидроксиэкдизон; 3-деокси-1(альфа) 20-дигидроксиэкдизон; 2-деокси-20-дигидроксиэкдизон 2-деокси-полиподин b; 2-деоксиэкдизон; деоксиэкдизон; 2-деоксиэкдизон 3-ацетат; 2-деоксиэкдизон 22-ацетат; 2-деоксиэкдизон 22-аденозин-монофосфат; 2-деоксиэкдизон 22-бензоат; 2-деоксиэкдизон 3-4-(1-(бета)-d-глюкопиранозил)-ферулат; 2-деоксиэкдизон 22-(бета)-d-глюкозид; 25-деоксиэкдизон 22-о-(бета)-d-глюкопиранозид; 2-деоксиэкдизон 22-фосфат; 2-деоксиэкдизон 25-рамнозид; (5(альфа))-2-деокси-21-гидроксиэкдизон; 2-деокси-20-гидроксиэкдизон; 22-деокси-26-гидроксиэкдизон; 14-деокси-20-гидроксиэкдизон; 2-деокси-21-гидроксиэкдизон; 2-деокси-20-гидроксиэкдизон 25-ацетат; 2-деокси-20-гидроксиэкдизон 22-ацетат; (5(альфа))-2-деокси-20-гидроксиэкдизон 3-ацетат; 2-деокси-20-гидроксиэкдизон 3-ацетат; 2-деокси-20-гидроксиэкдизон 22-бензоат; и/или 2-деокси-20-гидроксиэкдизон 3-кротонат.
[0062] Экстракт Rhaponticum может содержать полифенолы (в частности галловую кислоту и полимер процианидин В1).
[0063] Экстракт Rhaponticum может содержать фенольные соединения (в частности цинарин и холорогеновую кислоту).
[0064] Экстракт Rhaponticum может содержать флавоноиды, такие как патулетин, 6-гидроксикаемпферол-7-глюкозид, кверцетагитрин, кверцетин, кверцетагетин, лутеолин, каемпферол, изогамнетин, кверцетин-3-метиловый эфир, кверцетин-5-o-β-D-галактозид, изорамнетин 5-о-α-L-рамнозид, кверцетагетин-7-о-β-глюкопиранозид; апигенин, ариодиктиол, эриодиктиол-7-β-глюкопиранозид, гесперин, хризантемин, цианин.
[0065] Экстракт Rhaponticum может содержать лигнаны (картамогенин, картамозид, трахелогенин, трахелозид).
[0066] Экстракт Rhaponticum может содержать танины (элаговая кислота).
[0067] Экстракт Rhaponticum может содержать серотонин фенилпропаноиды.
[0068] Экстракт Rhaponticum может содержать полиацетилены.
[0069] Экстракт Rhaponticum может содержать сексвитерпеновые лактоны.
[0070] Экстракт Rhaponticum может содержать тритерпеновые гликозиды (рапонтикозиды от А до Н).
[0071] Экстракт Rhaponticum может содержать тритерпеноиды (паркеол, паркеил ацетат).
ЭКСТРАКТЫ RHODIOLA
[0072] Данное описание также включает экстракт Rhodiola, растущее в высокогорных районах растение имеющее около 200 видов, включая R. rosea и R. crenulata (Kelly, Altern. Med. Rev. 6:293-302, (2001); Ming et al., Phytother. Res. 19:740-743, (2005)). Rhodiola rosea является адаптогеном, который помогает телу адаптироваться к и сопротивляться разнообразным физическим, химическим и окружающим стрессам.
[0073] Экстракт Rhodiola, использованный в композиции настоящего описания, может быть приготовлен из любой части растения из группы Rhodiola rosea, Rhodiola crenulata, Rhodiola sachalinensis Rhodiola sacra, Rhodiola algida, Rhodiola dumulosa, Rhodiola kirilowii, Rhodiola henryi, Rhodiola yunannensis. Экстракт может быть приготовлен из любой части растения Rhodiola, тем не менее, экстракты полученные из корня и корневища, являются особенно полезными.
[0074] Виды Rhodiola могут содержать фенилпропаноиды, такие как розавин ((2Е)-3-фенилпроп-2-ен-1-ил 6-О-α-L-арабинопиранозил-α-D-глюкопиранозид), розин ((2R,3S,4S,5R,6R)-2-(гидроксиметил)-6-[(E)-3-фенилпроп-2-енокси]оксан-3,4,5-триол) и розарин ((2Е)-3-фенил-2-пропенил 6-O-альфа-L-арабинофуранозил-(9CI); [(Е)-3-Фенил-2-пропенил]6-O-α-L-арабинофуранозил-β-D-глюкопиранозид; [(Е)-3-Фенил-2-пропенил1]6-O-(α-L-арабинофуранозил)-β-D-глюкопиранозид). Виды Rhodiola могут также содержать производные фенилэтанола, такие как салидрозид/родиолозид (2-(4-гидроксифенил1)этил β-D-глюкопиранозид) и тирозол (4-(2-гидроксиэтил)фенол). Виды Rhodiola могут дополнительно содержать флавоноиды (например, родиолин, родионин, родиозин, ацетилродальгин и трицин); монотерпены (например, розиридол и розаридин); тритерпены (например, даукостерол и бета-ситостерол); фенольные кислоты (например, хлорогеновую, гидроксикоричную и галловую кислоты); танины, незаменымые аминокислоты и минералы. Активные ингредиенты, такие как п-триозол, салидрозид, розавин, пиридрид, родиозин и родионин, найдены в большинстве видов Rhodiola, но количества их могут варьировать. Одним интересующим биоактивным ингредиентом в Rhodiola rosea является салидрозид. Розавины (например, общая сумма розарина, розина и розавина) являются другими биоактивным составляющими идентифицированными в растении. Салидрозид и/или розавины могут использоваться в качестве стандартов для определения качества лекарственных форм.
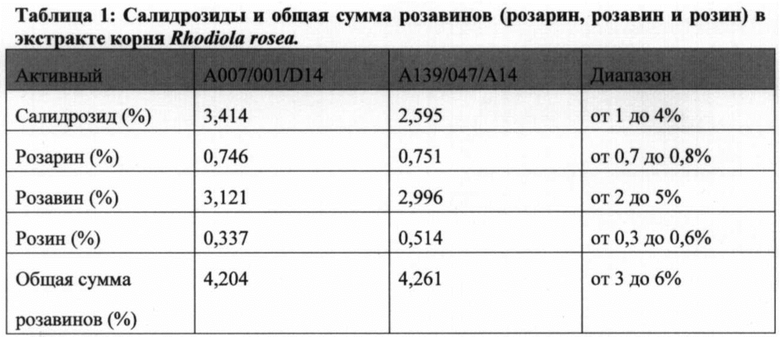
[0075] В некоторых вариантах реализации изобретения, экстракт Rhodiola содержит по меньшей мере около 0,10% до 90%, 80%, 70%, 60%, 50%, 40%, 30%, 20% или 10% салидрозидов на основании общей массы сухого экстракта; более предпочтительно по меньшей мере около 1%-4% салидрозидов. В некоторых вариантах реализации изобретения, экстракт Rhodiola содержит по меньшей мере около 0,10%-90%, 80%, 70%, 60%, 50%, 40%, 30%, 20% или 10% розавина, более предпочтительно по меньшей мере около 2,0%-5% розавина на основании общей массы экстракта. В некоторых вариантах реализации изобретения, экстракт Rhodiola содержит по меньшей мере около 0,10%-90%, 80%, 70%, 60%, 50%, 40%, 30%, 20% или 10% розавинов (например, общей суммы розарина, розавина и розина), более предпочтительно по меньшей мере около 3%-6% или около 1-6% розавинов на основании общей массы растительного экстракта.
КОМБИНАЦИИ ЭКСТРАКТОВ
[0076] В некоторых вариантах реализации изобретения, экстракт Rhodiola составляет около 1 до 99%, 98%, 97%, 96%, 95%, 90%, 80%, 70%, 60%, 50%, 40%, 30%, 20% или 10% мас./мас. (например, около 1%-10%, около 20%, около 30%, около 40%, около 50%, около 60%, около 70%, около 80%, около 90% или около 99% в весовом соотношении) на основании общей массы композиции и экстракт Rhaponticum составляет около 99%-1% мас./мас. (например, около 1%, около 10%, около 20%, около 30%, около 40%, около 50%, около 60%, около 70%, около 80%, или около 90%, или около 99% в весовом соотношении) на основании общей массы композиции.
[0077] Экстракт Rhodiola может составлять около 50-99% мас./мас. и экстракт Rhaponticum составляет около 1-50% мас./мас. от общей массы композиции. Экстракт Rhodiola может составлять около 1-50% мас./мас. и экстракт Rhaponticum составляет около 50-99% мас./мас. от общей массы композиции. Разнообразные подходящие Примеры пропорционирования Rhodiola и Rhaponticum являются следующими.
[0078] Экстракт Rhodiola составляет около 90% мас./мас. и экстракт Rhaponticum составляет около 10% мас./мас. от общей массы композиции. Экстракт Rhodiola составляет около 10% мас./мас. и экстракт Rhaponticum составляет около 90% мас./мас.. от общей массы композиции. Экстракт Rhodiola составляет около 60% мас./мас. и экстракт Rhaponticum составляет около 40% мас./мас. от общей массы композиции. Экстракт Rhodiola составляет около 40% мас./мас. и экстракт Rhaponticum составляет около 60% мас./мас. от общей массы композиции. Экстракт Rhodiola составляет около 50% мас./мас. и экстракт Rhaponticum составляет около 50% мас./мас. от общей массы композиции. В некоторых вариантах реализации изобретения, массовое отношение Rhaponticum и Rhodiola может быть около между 60:40 и 80:20, В одном варианте реализации изобретения, массовое отношение Rhaponticum и Rhodiola может быть около 75:25.
[0079] В одном варианте реализации изобретения, предложенные композиции, которые содержат экстракт корня Rhodiola rosea около 50% мас./мас. и экстракт корня Rhaponticum carthamoides около 50% мас./мас. от общей массы компонентов экстракта композиции. Экстракт Rhodiola содержит 1-4% салидрозидов, 2-5% розавина и 3-6% розавинов и экстракт Rhaponticum содержит 0,37% 20НЕ и 0,78% экдистеронов в целом. В некоторых вариантах реализации изобретения, комопзиция содержит около 0,1%-10% экдистеронов или около 0,5%-3% экдистеронов.
[0080] Любая подходящая комбинация пропорций травяных экстрактов Rhodiola rosea и Rhaponticum carthamoides предполагаемо охватывается композициями, описанными в данном документе. Процентное содержание предложенное в данном документе относится к весовому соотношению сухой массы порции экстракта к общему весу композиции.
ФАРМАЦЕВТИЧЕСКИЕ ЛЕКАРСТВЕННЫЕ СОСТАВЫ
[0081] Как описывается в данном документе, разнообразные виды растений, трав или их частей могут выбираться как часть композиций и способов для лечения заболевания и стимуляции улучшенного мышечного метаболизма. Экстракты таких видов могут быть приготовлены с помощью разнообразных подходящих способов. В одном варианте реализации изобретения, экстракт растений, трав или их частей может получаться обработкой водой и/или спиртом, или обоими растворителями, и последующим высушиванием до получения порошка. В другом варианте реализации изобретения, экстракция может проводиться с помощью суперкритической CO2 экстракции.
[0082] Композиции настоящего описания могут быть, например, в твердой, жидкой, или аэрозольной лекарственной форме, содержащей по меньшей мере два экстракта в любых пропорциях (один или более экстрактов), как раскрыто в данном документе. Композиции описания могут дополнительно содержать другие компоненты, например, но не ограничиваясь ими, витамины, лекарственные средства, или вспомогательные вещества для приготовления лекарственных составов в количестве от 0,1 до 99%, 98%, 97%, 96%, 95%, 90%, 80%, 70%, 60%, 50%, 40%, 30%, 20% или 10% мас./мас. конечного продукта, и отношения экстрактов могут соответственно варьироваться. Некоторые составы могут производиться в разнообразных лекарственных формах, которые вводяться млекопитающим для стимуляции роста и мышечной силы.
[0083] В одном варианте реализации изобретения, композиция изобретения содержится в капсулах. Капсулы, подходящие для перорального введения включают плотно входящие капсулы, сделанные из желатина, а также мягкие, герметичные капсулы, сделанные из желатина и пластификатора, такого как глицерин или сорбит. Плотно входящие капсулы могут содержать активные ингредиенты в смеси с наполнителем, таким как лактоза, связующимими веществами, такими как крахмалы, и/или смазывающими веществами, такими как тальк или стеарат магния и, необязательно, стабилизаторы.
[0084] Жидкости для введения могут представлять собой растворы или суспензии. В одном примере, композиция изобретения предложена в виде сухого порошка. Субъект растворяет или суспендирует порошок в любом выбраном напитке (например, вода, безалкогольный напиток, фруктовый сок, и т.п.) и затем потребляет, этот напиток. Альтернативно, композиции изобретения предложены в виде жидких форм. В случае таблеток, пресованных субстанций, или капсул, лекарственные формы должны быть приспособлены к колеблющемуся дозированию. Единицы имеющие разные уровни доз могут быть предварительно расфасованы, например, в блистерные упаковки, и маркированы для времени проглатывания. Интервалы могут быть дважды в день, трижды в день, четырежды в день или более частыми. В случае капсул, одна или более пеллет с отложенным действием, могут быть включены вместе с гранулами длительного действия. Несомненно существуют другие альтернативные пути приготовления лекарственных форм. В качестве примера, долго действующие микрочастицы и подходящие количества одного или более количеств микрочастиц с более отстроченным действием могут смешиваться и инкапсулироваться. Матричные субстраты могут использоваться для формирования 2,3, или 4 мультислойных таблеток или пресованных таблеток с покрытием. Пресованные таблетки с покрытием могут иметь ядра с отстроченным действием. Могут использоваться различно приготовленные многослойные и пресованные таблетки с покрытием, которые могут включать покрытые и непокрытые таблетки, упакованные для уточнения времени применения. Долгодействующие микрочастицы и частицы с отстроченным действием могут быть аналогично суспендированны в парентеральных жидкостях для получения неравномерного дозирования.
[0085] В некоторых вариантах реализации изобретения, может быть получен экстракт выбранных видов, высушенный и измельченный. В дополнительных вариантах реализации изобретения, экстракт может концентрироваться перед высушиванием, что может быть желательно для уменьшения объема экстракта. Такие концентрации могут уменьшить объем экстракта, при этом сохраняя весь спектр характеристик и уровней маркерных соединений исходного растения, травы, или ее частей.
[0086] В дополнительных вариантах реализации изобретения, может использоваться методика низкотемпературной водной обработки. Такая обработка можеть быть желательной, поскольку, она может задержать большую часть сопутствующих веществ, таких как полисахариды, флавоноиды, терпены и важные летучие вещества, масла и резины (часть которых типично является уловленными с помощью спирта или гексана, и оба растворителя оставляют нежелательные остаточные количества). Экстрагированный растительный материал может быть затем сконцентрирован, и сконцентрированная жидкость может быть высушена с использованием ультраскоростной спрэй сушилки, которая производит тонкий порошок, или тому подобное. В некоторых вариантах реализации изобретения, концентрирование растительных субстратов для высушивания в порошок может уменьшить объем растительного порошка без практического изменения в составе составляющих растение частей. Такой способ может быть желателен для уменьшения нежелательных следов химических соединений, которые могут быть внесены в растительный материал, и таким образом получается более чистый, полносоставный травяной порошок. Например, могут быть получены отношения концентраций от 10-к-1 до 20-к-1, что может значительно уменьшить объем материала и предложить подходящее дозирование в капсулах.
[0087] "Фармацевтически приемлемый носитель" представляет собой субстанцию, которая может добавляться к активным ингредиентам для того, чтобы помочь приготовить лекарственную форму или стабилизировать лекарственную форму, и не вызывает значительных побочных токсикологических эффектов у пациента. Примеры таких носителей хорошо известны специалисту в данной области техники и включают воду, сахара, такие как мальтоза или сахароза, альбумин, соли, такие как хлорид натрия, и т.п. Другие носители описаны, например, в Remington's Pharmaceutical Sciences ред. Е.W. Martin, включенной в данный документ посредством ссылки во всей своей полноте. Такие композиции будут содержать терапевтически эффективное количество экстрактов Rhodiola и Rhaponticum.
[0088] Фармацевтически приемлемые носители включают стерильные водные растворы или дисперсии и стерильные порошки для лекарственных форм немедленного приема, стерильных инъекционных растворов или дисперсий. Использование таких сред и агентов для фармацевтически активных субстанций известно в данной области техники. Композиция предпочтительно приготовлена для перорального приема. Композиция может быть приготовлена в виде раствора, микроэмульсии, липосомы, или другой упорядоченной структуры, подходящей для высокой концентрации лекарства. Носитель может являться растворителем или дисперсионной средой содержащей, например, воду, полиол (например, глицерин, пропиленгликоль, и жидкий полиэтиленгликоль, и тому подобное), и подходящей их смесью. В некоторых случаях, носитель будет включать изотонические агенты, например, сахара, полиспирты, такие как маннитол, сорбитол, или хлорид натрия в композиции.
[0089] Как используется в данном документе, «носители» включают фармацевтически приемлемые носители, вспомогательные вещества, или стабилизаторы, которые не токсичны для клетки или млекопитающего поддающегося их действию при используемых дозировках и концентрациях. Часто физиологически приемлемый носитель является водным рН буферным раствором. Примеры физиологически приемлемых носителей включают буфферы, такие как фосфатный, цитратный, и другие органические кислоты; антиоксиданты, включая аскорбиновую кислоту; полипептиды с малой молекулярной массой (менее чем около 10 остатков); протеины, такие как сыровоточный альбумин, желатин или иммуноглобулины; гидрофильные полимеры, такие как поливинилпирролидон; аминокислоты, такие как глицин, глютамин, аспарагин, аргинин или лизин; моносахариды, дисахариды и другие углеводы, включая глюкозу, маннозу или декстрины; хелатирующие агенты, такие как ЭДТА; сахарные спирты, такие как миннитол или сорбитол; солеобразующие противоионы, такие как натрий; и/или неионные поверхностно-активные вещества, такие как TWEEN, полиэтиленгликоль (ПЭГ) и PLURONIC.
[0090] Фармацевтически приемлемые носители также включают природные и синтетические носители, такие как мальтодекстрин, гумиарабик (Е414), силиций диоксид (Е551), декстрин тапиоки, декстрины, камедь акации и тому подобное.
[0091] Изобретение также включает синтетические лекарственные составы, имеющие такие же активные ингредиенты, в такой же пропорции, как указано выше. Эти ингредиенты могут быть очищены или синтезированы, и включены в композиции и лекарственные формы, без включения любого другого природного растительного материала, который обычно присутствует в экстракте.
ИСПОЛЬЗОВАННЫЕ СПОСОБЫ
[0092] Экстракт Rhodiola может быть использован для увеличения уровня синтеза протеина и уменьшения уровня экспрессии генов миостатина и/или атрогина в клетках скелетных мышщ. Экстракт Rhaponticum может быть использован для увеличения уровня синтеза протеина, увеличения уровня фосфорилирования членов пути Akt, увеличения уровня фосфорилирования S6K1, и/или уменьшения экспрессии генов миостатина и/или атрогина в клетках скелетных мышц.
[0093] В дополнительном варианте реализации изобретения, комбинация экстрактов Rhodiola и Rhaponticum может вводиться в количествах, которые увеличивают их функции, по сравнению со случаем, когда каждый из них вводили отдельно.
[0094] В еще одном аспекте изобретения, предложен способ увеличения мышечной массы и мышечной силы у млекопитающего, включающий введение млекопитающему эффективного количества описанной в данном документе композиции. Предпочтительно, млекопитающее представляет собой человека, более предпочтительно атлета. В еще одном аспекте описания, предложен способ улучшения аэробных и анаэробных спортивных/физических характеристик у млекопитающего, включающий введение млекопитающему эффективного количества описанной в данном документе композиции. В еще одном аспекте изобретения, предложен способ лечения состояний связанных с или характеризующихся мышечной атрофией у млекопитающего, включающий введение млекопитающему эффективного количества описанной в данном документе композиции.
[0095] В некоторых вариантах реализации изобретения, композицию млекопитающему вводили перорально, предпочтительно человеку, при дневной дозе около 1-5000 мг/день, предпочтительно около 30-1000 мг/день, более предпочтительно около 50-1000 мг/день, и даже более предпочтительно около 100-600 мг/день или 200-500 мг/день. Меньшие дозы около 0,5 мг/день или дозы больше чем 5000 мг/день также могут быть предложены. В некоторых вариантах реализации изобретения, предложены множественные дневные дозы в 10, 50, 100, 200, 300, 400, 500, 600, 700, 800 или более мг за один прием.
[0096] Интервалы дозирования условны QD (один раз в день), BID (дважды в день), TID (трижды в день), QID (четырежды в день) или более частые включая 5, 6, 7, 8, 9, 10, или более доз в день. Время введения может основываться на времени полужизни, использованной лекарственной формы, систематической реактивности, удобства, будь то самовведение или введение по режиму, и будь то терапевтическая, пищевая, стероидная или противоинфекционная субстанция.
[0097] Если композиция не высвобождается контролируемо, или не имеет длительного периода полураспада, позволяющего введение один раз в день, временной интервал между приемом доз может быть неравномерным. Например, если субстанция принимается во внутрь во время пробуждения и во время отхода ко сну, интервалы представляют собой 16 и 8 часов. Если принимается во время пробуждения, посередине дня, и во время отхода ко сну, интервалы могут быть 5, 11 и 8 часов. Если принимается равномерно во время часов пробуждения, интервалы могут быть 5,33, 5,33, 5,33 и 8 часов. В таких случаях, рациональное дозирование следует равномерно с равными временными интервалами.
[0098] Пищевые и определенные лекарства, и стероиды, антибиотики, и подобные субстанции следует принимать на полный желудок. Такие дневные интервалы могут быть равномерно распределены и время между последней дневной дозой и следующей утренней дозой отличается.
[0099] Для предупреждения или лечения болезни или стимулирования улучшенных физических функций, подходящая дозировка активного агента, будет зависеть от типа болезни, которую лечат, или функции на которую нацелены, как определено выше, тяжести и течения заболевания, вне зависимости от того, вводили ли препарат в качестве профилакти или терапии, предыдущей терапии, клинической истории субъекта, и ответа на препарат, и усмотрения лечащего врача. Препарат подходит для введения субъекту в один прием или в серии процедур. Дозировки и концентрация требуемого лекарственного средства композиции могут сильно зависеть от конкретного предполагаемого использования. Определение подходящей дозировки или пути введения находяться в области деятельности специалиста в данной области техники. Эксперименты на животных обеспечивают надежное руководство в определении эффективных доз для терапии человека. Соответственно, «эффективное количество» любой конкретной композиции или лекарственного состава, согласно с данным описанием будет варьироваться в зависимости от конкретных обстоятельств, и подходящее эффективное количество может быть определено в каждом случае применения специалистом в данной области техники с использованием рутинного экспериментирования, для достижения желаемого эффекта.
[00100] Как используется в данном документе, термины «лечение», «терапия» и тому подобное, относятся к лечащей терапии, профилактической терапии, и превентивной терапии, включая терапию здоровых субъектов. Примером «превентивной терапии» является профилактика или уменьшение целевого патологического состояния или расстройства. Нуждающиеся в лечении включают субъектов уже имеющих расстройство, а также субъектов склонных к расстройству или таковых у которых расстройство следует предотвратить. «Хроническое» введение относится к введению препарата(ов) в непрерывном режиме, что является противоположным, единичному режиму, чтобы поддерживать первоначальный терапевтический эффект (активность) в течение длительного периода времени. «Прерывистое» введение является лечением, которое не является последовательным без перерывов, но скорее, является цикличным по своей природе. Введение «в комбинации с» одним или более дополнительных терапевтических препаратов включает одновременное (конкурентное) и последовательное введение в любом порядке. В некоторых вариантах реализации изобретения, композиции и способы, описанные в данном документе, могут быть использованы для лечения состояний ассоциированных с или характеризующихся мышечной атрофией включающих, саркопению, саркопенное ожирение, рак, рассеянный склероз, мышечную дистрофию, перелом кости, требующий иммобилизации (например, шина или гипсовая повязка), амиотрофический боковой склероз (ALS), периферическую невропатию, инсульт, кахексию, или тому подобное. Такие состояния могут быть идиопатическими, вторичными по отношению к диагностируемому состоянию, и тому подобное.
[00101] Как используется в данном документе, «терапевтически эффективное количество» является минимальным количеством активного препарата (например, композиции содержащей экстракты Rhodiola и Rhaponticum), которое необходимо субъекту для получения терапевтической выгоды. Например, «терапевтически эффективное количество» для страдающего субъекта или предотвращения его страданий, является таким количеством, которое индуцирует, улучшает, или в противном случае вызывает улучшение в патологических симптомах, прогрессировании болезни, физиологических состояний связанных с или устойчивость к описанным расстройствам.
[00102] Следующие примеры включены для иллюстрации предпочтительных вариантов реализации изобретения. Специалисту в данной области техники следует принять во внимание, что техники, раскрытые в следующих примерах, представляют хорошо функционирующие техники, и таким образом, можно считать, что они представляют собой предпочтительные способы для практики. Специалист в данной области техники, тем не менее, должен, в свете данного расскрытия, оценить, что многие изменения могут быть сделаны в раскрытых конкретных вариантах реализации изобретения, и тем не менее привести к получению того же или подобного результата, не отступая от сущности и объема вариантов реализации изобретения.
ПОЛУЧЕНИЕ ЭКСТРАКТА
[00103] Экстракты могут быть получены с использованием методики экстракции органическим растворителем. Например, корни Rhaponticum carthamoides следует перемолоть (например, до размера в 4 мм меш) и молотый материал смешать с растворителем включающим, но не ограничивающимся, 100% воду, этанол от 1% до 99% в воде (об./об.), метанол от 1% до 99% в воде (об./об.), этилацетат, ацетон, гексан или любой другой органический растворитель традиционно используемый для экстракции (например, EtOH 50%) в реакторе или любом контейнере имеющем функцию экстракции. Подходящее соотношение растворитель: растение составляет между около 1:1 до 30:1, более предпочтительно между 5:1 и 15:1 (например 10:1 (об./мас.)). Сырой материал экстрагировали, к примеру в условиях кипячения с перемешиванием, но это также может быть мацерация, с или без кипячения с перемешиванием, с или без перемешивания, и с или без дополнительного давления. Температура экстракции будет обычно зависеть от используемого растворителя. Время экстракции предпочтительно является по меньшей мере 1 ч (например 1 ч 30).
[00104] После экстракции, смесь может быть профильтрована или отцентрифугирована для отделения жидкости от твердой фазы (осадка на фильтре). На стадии фильтрования, могут быть использованы фильтры 25 микрон.
[00105] Стадия экстракции может быть повторена несколько раз, для достижения более чем одного цикла (например, повторить 2 раза для достижения 3 циклов в общем), и фильтраты скомбинированы. Твердую фазу отбрасывают.
[00106] Скомбинированные фильтраты могут быть сконцентрированы в вакууме (например, при 0,8 Па) до между от 30% до 70% на сухое вещество (предпочтительно 50% на сухое вещество). Может быть использован любой тип системы для испарения растворителя. Полученная часть после экстракции называется «нативный экстракт».
[00107] Нативный экстракт затем высушивали до % содержания на сухое вещество около 90% до 99% (например, 97%), но экстракт может быть высушен и до меньших значений % на сухое вещество. Эта стадия может быть проведена с использованием любого способа сушки, включающего, но не ограничивающегося, атомизацию, высушивание на воздухе, высушивание в сушильном шкафу, высушивание на солнце, и т.п. с или без носителя.
Пример 1: Экстракция Rhaponticum этанолом 50% (об./об.) (F0).
[00108] Схематическая версия последующей экстракции изображена на Фиг. 29а. Сырую траву Rhaponticum (корень, 65 кг в перерасчете на сухое вещество) взвешивали и измельчали в крупный порошок. Порошок помещали в экстракционную камеру/ реактор и добавляли 700 л смеси этанол вода (50% спирта, об./об.), что составляло приблизительно соотношение 10:1 (об./мас.)). Смесь кипятили с перемешиванием в течение 1,5 часов, при температуре 80-90°C. После 1,5 часов, жидкость отфильтровывали и хранили отдельно. Остаток (твердая фаза) собирали отдельно и стадию экстракции повторяли еще два раза (для достижения в общем трех циклов).
[00109] Фильтраты комбинировали перед концентрированием в вакууме (0,8 Па) до 30-60%) содержания на сухое вещество (например, 39% на сухое вещество). Полученную сконцентрированную пасту, в общем 25 кг, (называемую «F0-нативный экстракт») анализировали на биоактивные ингредиенты.
[00110] В данном способе, этанол может быть собран из фильтрата и использован повторно на стадии экстракции, при этом необходимо проконтролировать, чтобы растворитель всегда содержит 50% спирта.
[00111] Сконцентрированную экстракционную пасту сушили с помощью атомизации, получая сухой порошок (меньше чем 10% влаги) (F0-EtOH 50% сухой порошок). Полученный образец сухого порошка использовали для анализа биоактивных ингредиентов, микробиологического анализа, анализа на тяжелые металы, пестициды, и пищевого анализа.
Пример 2: Стадии центрифугирования и фильтрования (F0 как изображено на Фиг. 29а)
[00112] 12 кг нативного экстракта Rhaponticum (при 39% содержания на сухое вещество), полученного согласно Примеру 1, разбавляли водой до 10% содержания на сухое вещество, и затем центрифугировали. Выход составлял 43 кг разбавленого нативного экстракта при приблизительно 10% содержания на сухое вещество (F0-нативный экстракт разбавленный и центрифугированный).
[00113] Ультрафильтрование (UF) при 5 кДа, затем при 1 кДа проводили на 42 кг разбавленного нативного экстракта (при 10% содержания на сухое вещество), получая 3 фракции: >5 кДа, 1-5 кДа и <1 кДа. Фракции сушили в вакууме или путем атомизации (выход составлял 1,55 кг, 0,90 кг и 1,15 кг, соответственно) (F0-нативный экстракт UF). Образец посылали на анализ биоактивных веществ.
Пример 3: Стадия очистки (F5' как изображено на Фиг. 29а)
[00114] 1 кг разбавленого нативного экстракта Rhaponticum (при приблизительно 10% содержания на сухое вещество), полученного согласно Примеру 2 (F0-нативный экстракт разбавленный и центрифугированный) очищали на адсорбирующей колонке со смолой D-101 (объем смолы 1 л). Элюат концентрировали, и сушили получая тонкий порошок ((получили 14,5 г порошка очищенного экстракта) (F5'-Очищенный EtOH 50% экстракт).
Пример 4: Экстракция Rhaponticum этанолом 70% (об./об.) (F5 и F7).
[00115] Известное количество корня Rhaponticum, измельченного в крупный порошок, смешивали с водой в соотношении растворитель: растение 10:1 (об./мас.) и экстрагировали без кипячения с обратным холодильником, и перемешивания при 80°C в течение 2 ч. Была выполнена одна экстракция. Твердую фазу отбрасывали, а жидкую фазу собирали и фильтровали через 25 мкм.
[00116] Часть фильтрата концентрировали, с использованием роторного испарителя, для удаления большей части растворителя и окончательно высушивали в вакууме до <10% влажности. Экстракт представлял собой порошок (F7: EtOH 70% экстракт).
[00117] Другую часть фильтрата очищали на колонке с сорбционной смолой, как описано в Примере 3, концентрировали и высушивали в вакууме до <10% влажности. Экстракт представлял собой порошок (F5-Очищенный EtOH 70% экстракт).
[00118]
Пример 5: Способ экстракции Rhaponticum водой (F1 & F3)
[00119] Повторяли аналогичный Примеру 4 способ, за исключением того, что использовали воду вместо EtOH 70%:
[00120] Известное количество корня Rhaponticum, измельченного в крупный порошок, смешивали с водой в виде растворителя в соотношении растворитель: растение 10:1 (об./мас.) и экстрагировали без кипячения с обратным холодильником, и перемешивания при 80°C в течение 2 ч. Была выполнена одна экстракция. Твердую фазу отбрасывали, а жидкую фазу собирали и фильтровали через 25 мкм.
[00121] Часть фильтрата концентрировали, с использованием роторного испарителя, для удаления большей части растворителя и окончательно высушивали в вакууме до <10% влажности. Экстракт представлял собой порошок (F1: Водный экстракт).
[00122] Другую часть фильтрата очищали на колонке с сорбционной смолой, как описано в Примере 3, концентрировали и высушивали в вакууме до <10% влажности. Экстракт представлял собой порошок. (F3-Очищенный водный экстракт).
Пример 6: Способ экстракции Rhaponticum ацетоном (F2 и F4)
[00123] Повторяли аналогичный Примеру 4 способ, за исключением того, что использовали ацетон вместо EtOH 70%:
[00124] Известное количество корня Rhaponticum, измельченного в крупный порошок, смешивали с ацетоном в виде растворителя в соотношении растворитель: растение 10:1 (об./мас.), и экстрагировали без кипячения с обратным холодильником и перемешивания при 80°C в течение 2 ч. Была выполнена одна экстракция. Твердую фазу отбрасывали, а жидкую фазу собирали и фильтровали через 25 мкм.
[00125] Часть фильтрата концентрировали, с использованием роторного испарителя, для удаления большей части растворителя, и окончательно высушивали в вакууме до <10% влажности. Экстракт представлял собой порошок. (F2: Ацетоновый экстракт).
[00126] Другую часть фильтрата очищали на колонке с сорбционной смолой, концентрировали и высушивали в вакууме до <10% влажности. Экстракт представлял собой порошок. (F4-Очищенный ацетоновый экстракт).
Пример 7: Получение травяного экстракта Rhodiola rosea
[00127] Высушенный материал Rhodiola rosea экстрагировали водным спиртом. Например, в некоторых лекарственных формах, предпочтительными являлись 50% или 70% этанол. Полученный экстракт затем фильтровали и супернатант концентрировали. Отфильтрованный экстракт центрифугировали и прозрачный супернатант очищали с помощью колоночной хроматографии. В качестве элюента использовали этанол. Полученный этанольный элюат затем концентрировали. Некоторые лекарственные формы включали необязательную стадию сушки.
Пример 8. Дозировка салидрозидов и общей суммы розавинов в травяном экстракте Rhodiola rosea
[00128] Количество разнообразных соединений, включая салидрозиды, и общую сумму розавинов (розарии, розавин и розин), определяли в экстракте корня Rhodiola rosea с использованием способа ВЭЖХ разработанного: М. Ganzera et al., "Analysis of the marker compounds of Rhodiola rosea L. (Golden root) by reversed phase high performance liquid chromatography" Chem. Pharm. Bull. 49(4) 465-467 (2001). Вкратце, квантифицирование целевых соединений выполняли на системе ВЭЖХ Agilent 1100 HPLC system оснащенной УФ детектором. Разделение соединений проводили на колонке для ВЭЖХ АСЕ С18 (250×4,6 мм, 5 мкм) при температуре 45°C. Подвижная фаза состояла из ацетонитрила (элюент А) и фосфатного буфера рН 7 (элюент В). Градиент был следующим: 11% изократический А (10 мин), 11-30% А (20 мин), 30-80%) А (5 мин), 80% изократический А (10 мин), 80-11% А (5 мин). Общее время анализа составляло 50 мин. Объем введения составлял 5 мкл и скорость потока равнялась 1 мл/мин. УФ контроль осуществлялся при 225 нм для детектирования салидрозидов и 250 нм для детектирования розавинов. Количество целевых соединений квантифицировали с помощью сравнения площади пика образца с площадью пика стандартного соединения известной концентрации.
Пример 9: Анализ 20НЕ в разных экстрактах корня Rhaponticum
[00129] Количество бета-экдизона (20НЕ) в разных экстрактах Rhaponticum, полученных как в Примерах от 1 до 6, определяли с использованием Agilent 1100 HPLC system оснащенной УФ-видимый свет детектором. Разделение соединений проводили на ВЭЖХ колонке Zorbax Eclipse Plus C18 (2,1×50 мм-1,8 мкм) с температурой колонки 35°C. Подвижная фаза состояла из метанола (элюент А) и 0,1% муравьиной кислоты в воде (элюент В). Скорость потока составляла 0,4 мл/мин. Градиент был линейным с уклоном от 10 до 100% А за 15 мин. Объем введения составлял 2 мкл. УФ детектирование производили на длине волны 250 нм, ширина полосы 8 нм. Количество целевых соединений квантифицировали с помощью сравнения площади пика образца с площадью пика стандартного соединения известной концентрации.
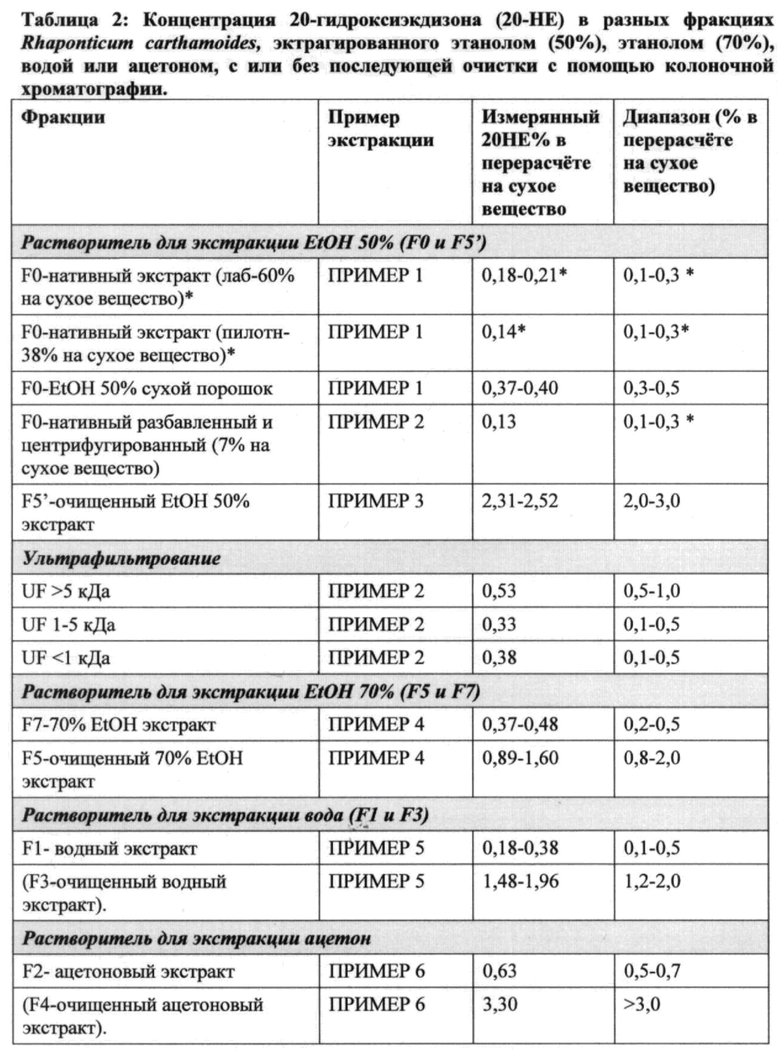
значения выражены исходя из анализируемого образца и не на основании сухого веса
Пример 10: Анализ экдистероидов в этанольном экстракте корня Rhaponticum
[00130] Сухой экстракт корня Rhaponticum carthamoides (F0-EtOH 50% сухой порошок) получали экстракцией смесью этанол-вода 50% (об./об.), как описано в Примере 1. Идентификацию экдистероидов выполняли на системе ВЭЖХ, оснащенной фотодиодным детектором. Разделение соединений проводили на ВЭЖХ колонке Atlantis С18 (150×3 мм-3 мкм) с температурой колонки 40°C. Подвижная фаза состояла из метанола с 0,1% уксусной кислоты (об./об., элюент А) и 0,1% (об./об.) уксусной кислоты в воде (элюент В). Скорость потока составляла 0,6 мл/мин. Программа градиента была следующей: 20% изократический А (5 мин), 20-40% А (25 мин), 40-70% А (15 мин), 70-85% (15 мин). Общее время анализа составляет 60 мин. Детектирование производили на длине волны 242 нм.
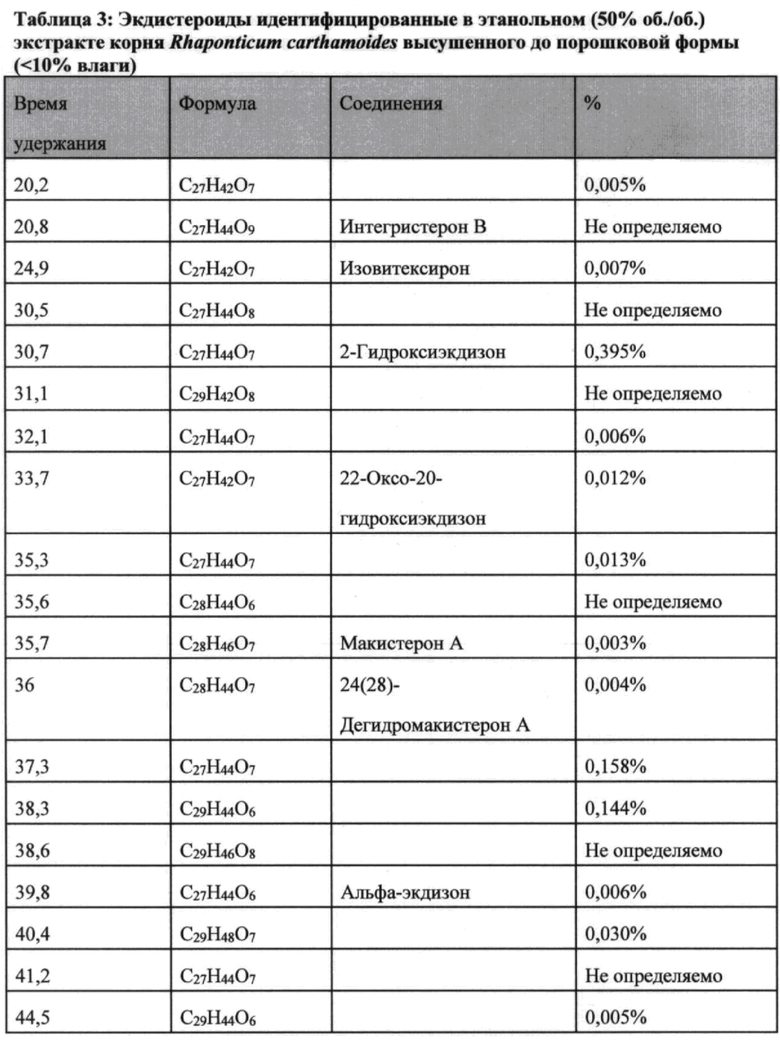
Общая сумма экдизонов (в виде 20-Гидроксиэкдизона)=0,788%.
[00131] Всего идентифицировано 19 экдизонов в экстракте корня Rhaponticum. Некоторые были определяемы только по их химических структурах.
Пример 11: Фитохимический и физико-химический анализ этанольного экстракта корня Rhaponticum (за исключением экдистероидов)
[00132] Сухой экстракт корня Rhaponticum carthamoides (F0-EtOH 50% сухой порошок) получали экстракцией смесью этанол-вода 50% (об./об.), как описано в Примере 1, и анализировали на содержание фито-соединений отличных от экдистероидов, и проводили физические анализы. Кривые суммы фенолов, суммы органических кислот и суммы свободных углеводов идентифицированных в композиции изображены на Фигурах 1a, 1b и 2.
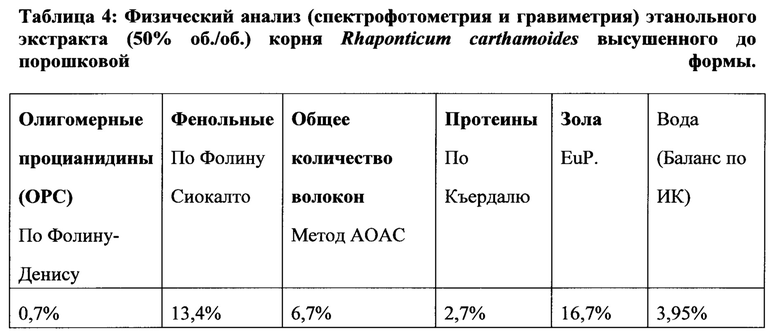
Общее количество золы, волокон, протеина, воды и ВЭЖХ/ГХ результаты показали 70,6% от массы экстракта, соединения, такие как ацетилентиофены и стирол найдены в малых количествах (идентифицированы, но не квантифицированы).
Способы использования экстрактов Rhaponticum и Rhodiola
[00133] Следующие Примеры оценивают влияние экстракта Rhaponticum и экстракта Rhodiola, отдельно и в комбинации, на уровень синтеза протеина и метаболические сигнальные пути.
Пример 12: Влияние разных лекарственных составов экстрактов Rhaponticum carthamoides (Стадия 1, изображенная на Фиг. 29а) на фосфорилирование S6K1 треонина 389 и Akt треонина 308.
[00134] Исследование было направлено на оценку способности экстракта Rhaponticum стимулировать синтез протеина и метаболические пути на уровне Akt. Серин/треонин киназа Akt (протеин киназа В) активируется с помощью разнообразных стимулов через фосфорилирование по Thr308 и Ser473. Как только Akt фосфорилирована, она мигрирует в ядро, где учавствует в разнообразных клеточных процессах, таких как транспорт глюкозы, синтез протеина или липидов, и хранение триглицеридов.
[00135] Также была оценена способность экстракта Rhaponticum стимулировать синтез протеина на уровне S6 киназы 1, sp70 S6 киназа является широкораспространненым протеином, который активируется в ответ на цитокины. Она находится ниже в пути mTOR/PI3K и фосфорилируется по множествам остатков, включая треонин 389. Фосфорилирование Thr389, тем не менее, очень сильно коррелирует с активностью р70 киназы in vivo. Будучи активированной, р70 S6 киназа фосфорилирует S6 протеин в 40S рибосомальном протеине (rpS6), что приводит к процессу синтеза протеина.
[00136] С2С12 клетки превоначально полученные Yaffe и Saxel (1977) путем селективного последовательного прохождения миобластов, культивируемых из мышцы бедра мышей СЗН через 70 часов после травмы (Yaffe D, 1977). Эти клетки показали способность к дифференциации. Клетки С2С12 являются полезной моделью для изучения дифференциации миогенных клеток в клетки скелетных мышц (например, через механизмы фосфорилирования миозина) и экспрессируют мышечные протеины и андрогенные рецепторы.
[00137] Было получено пять разных лекарственных составов экстрактов Rhaponticum. 50% этанольный экстракт, 70% этанольный экстракт, 100% водный экстракт, а также экстракты, очищенные с помощью колоночной хроматографии (за исключением 50% EtOH экстракта), как описано в Примерах с 1 до 5 настоящего описания.
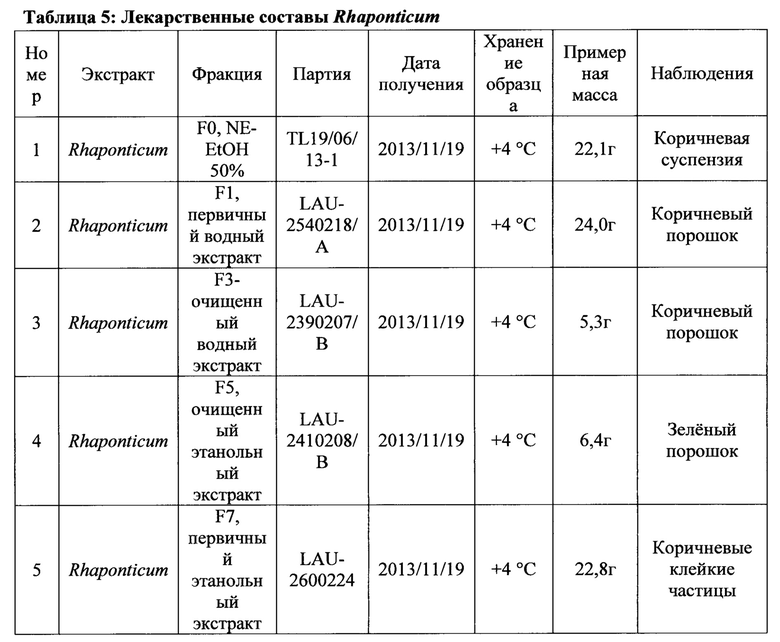
[00138] Концентрации тестируемых образцов экстракта Rhaponticum приготовили таким образом, чтобы финальная концентрация гидрокси-экдизона составляла 0,1 мкМ, 1 мкМ и 10 мкМ. Основываясь на измеряных концентрациях гидрокси-экдизона в каждом экстракте, концентрации, используемые в каждой лекарственном составе Rhaponticum были следующими:

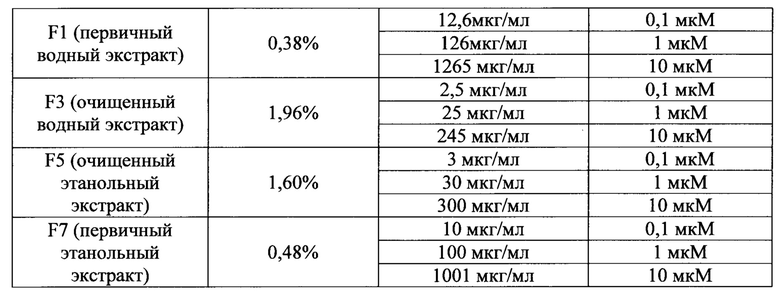
[00139] После начала исследования величину % гидроксиэкдизона в F0 экстракте не определяли, и конечная тестируемая концентрация основывалась на концентрации гидроксиэкдизона в экстракте F7. Тем не менее, концентрация данного экдизона в F0 была преувеличена. Это причина того, почему конечная концентрация гидроксиэкдизона, тестируемая для экстракта F0, была отличной от других фракций.
[00140] Растущие клетки собирали и помещали в 6 луночный планшет с плотностью 170000 клеток на лунку. Клетки выращивались в течение 48 ч в 5% CO2 при 37°C. После того как клетки достигли 80% слияния, среду заменяли на дифференциирующую среду (DMEM + 2% FBS). После 5 дней, миобласты сливались в мультинуклеарные миотрубочки. За 1 ч до начала эксперимента, клетки инкубировали со средой Кребса для лишения клеток аминокислот.
[00141] Клетки обрабатывали пятью лекарственными составами растительного экстракта Rhaponticum, при 3 концентрациях, в присутствии нормальной (0,8 мМ) или низкой (0,08 мМ) концентраций аминокислот и ДМСО (0,002%) в течение 2 ч.
[00142] В конце эксперимента, клетки лизировали в клеточном лизисном буфере (100 мкл на лунку) и центрифугировали, для изолирования растворенного в супернатанте протеина. Протеины из этого клеточного анализа квантифицировали с помощью колориметрического анализа, производного способа LOWRY. Для этого, 50 мкг общего протеина в 100 мкл лизисного буфера переносили в микролуночные полоски покрытые антителом pS6Kl или pAkt и инкубировали 2 ч при 37°C. После нескольких промывок добавляли детектирующее антитело и инкубировали 1 ч при 37°C. После нескольких промывок добавляли HRP-связанное вторичное антитело. В конце 30 мин инкубации при 37°C, добавляли субстрат ТМВ (3,3',5,5'-тетраметилбензидин), и наблюдали за голубым окрашиванием в положительных лунках. Для избежания насыщения сигнала добавляли стоп раствор, который индуцировал желтый цвет. Интенсивность желтого цвета могла быть считана на спектрометре на 450 нм, и была напрямую пропорциональна детектируемому количеству pS6K1 или Akt.
[00143] Каждое состояние тестировали в n=5 или n=6. IGF1 100 нг/мл использовали в качестве положительного контроля.
[00144] Результаты фосфорилированной Akt выражены в поглощении на мкг протеина (поглощение/мкг протеина) после 2 ч инкубации, и в % от необработанного контроля (100%).
[00145] Результаты фосфорилированной Т389 S6 киназы 1 выражены в поглощении на мкг протеина (поглощение/мкг протеина) после 2 ч инкубации и в % от необработанного контроля (100%).
[00146] Все результаты выражены в % от необработанного контроля. Разницы между полученными значениями оценивались с помощью ANOVA для повторяющихся измерений, с последовательным тестом Дюннета, если ANOVA показывала существенные отличия, с помощью теста Ю-Ман-Уитни по сравнению с необработанными контролями по отношению к IGF1 или растительным экстрактам; р<0,05, **р<0,01, ***р<0,001, по сравнению с необработанным контролем.
[00147] Все результаты даны в виде значение ± стандартная ошибка среднего значения. Для всех оцененных параметров статистические анализы проводили с использованием не параметрического теста Крускал-Валлис с последующим пост тестом Дюнна (GraphPad PRISM®4). Сравнение между двумя состояниями проводили с использованием теста Манна-Уитни. Значение р 0,05 рассматривалось как значительное.
[00148] Инсулиноподобный фактор роста (IGF-1) является установленным анаболическим фактором, который может индуцировать рост скелетных мышц с помощью активации фосфоинозитидин 3-киназ (PI3K)/Akt/цель рапамицин у млекопитающих (mTOR) пути. Стимулирование фосфорилировния обоих S6K1 и Akt было ранее сообщено Miyazaki et al. (Miyazaki M, 2010). M. В следствии этого, IGF-1 выбрали в качестве положительного контроля в эксперименте. Базальное фосфорилирование S6K1 было в четыре раза выше в присутствии нормальной концентрации аминокислот, чем в присутствии низкой концентрации аминокислот (0,8 мМ по сравнению с 0,08 мМ).
[00149] В присутствии низкой концентрации аминокислот, все тестируемые фракции, за исключением F7, при всех тестированных концентрациях увеличивали уровень фосфорилирования S6K1 (См Фигуры 3а, 3b, 4а, 4b, 5а, 5b, 6а, 6b, 7а, и 7b). Эффекты не зависели от тестируемых доз.
[00150] В присутствии нормальной концентрации аминокислот, наименьшая доза каждой фракции, за исключением F3, и промежуточные концентрации F0, F3 и F5 стимулировали фосфорилирование S6K1 (См. Фигуры 3а, 3b, 4а, 4b, 5а, 5b, 6а, 6b, 7а, и 7b). Наблюдаемые эффекты были ниже, чем таковые наблюдаемые с IGF-1, и были значительными лишь для фракций F0, F1 и F3 (наименьшая и средняя дозы). Следует отметить, что в условии частичной растворимости экстракта F7 при средней и высокой тестируемых концентрациях, наблюдалось снижение фосфорилирования S6K1, Фигуры 3а, 3b, 4а, 4b, 5а, 5b, 6а, 6b, 7а, и 7b: Определение S6K1 фосфорилирования треонина 389 в С2С12 миотрубочках после инкубации с 5 разными лекарственными составами экстракта Rhaponticum при трех концентрациях.
[00151] Пять разных лекарственных составов экстракта Rhaponticum, при трех концентрациях, инкубировали в течение 2 ч в присутствии дифференциированных С2С12 миотрубочек. В конце инкубации клетки лизировали, сумму растворимых протеинов квантифицировали, и измеряли уровень S6K1 фосфорилирования остатка треонина 389, и нормализованного бета-актин протеина. Значение ± стандартная ошибка среднего значения. *р<0,05; **р<0,01; ***р<0,001 по сравнению с контрольным значением.
[00152] IGF-1 был ранее указан как стимулирующий Akt стимулирование, и был в этом контексте выбран в качестве положительного контроля в анализе (Miyazaki М, 2010). После IGF-1 (100 нг/мл, 2 ч) инкубации, Akt фосфорилирование было активировано на фактор 1,6. Аналогичные результаты были ранее опубликованы для Akt фосфорилирования Latres или Miyazaki (Latres Е, 2005) (Miyazaki М, 2010).
[00153] В присутствии низкой или нормальной концентрации аминокислот, наблюдалась незначительная стимуляция Akt фосфорилирования для всех тестируемых фракций при наименьшей дозе, за исключением фракции F0, инкубированной с низкой концентрацией аминокислот, и F3, инкубированной с нормальной концентрацией аминокислот, где незначительное увеличение наблюдалось при средней дозе.
[00154] Было отмечено, что базальный уровень Akt фосфорилирования был в два раза выше в присутствии нормальных аминокислотных условий по сравнению с низко аминосодержащим условием. В конечном счете, в условии частичной растворимости экстракта F1 (высокая концентрация) или F7 (средняя и высокие концентрации), было отмечено снижение фосфорилирования Akt, независимо от концентраций используемых аминокислот.
[00155] Фигуры 8а, 8b, 9а, 9b, 10а, 10b, 11а, 11b, 12а и 12b: Определение Akt фосфорилирования треонина 308 в С2С12 миотрубочках после инкубации с 5 разными лекарственными составами экстракта Rhaponticum при трех концентрациях.
[00156] Пять разных лекарственных составов экстракта Rhaponticum, при трех концентрациях, инкубировали в течение 2 ч в присутствии дифференциированных С2С12 миотрубочек. В конце инкубации клетки лизировали, сумму растворимых протеинов квантифицировали, и измеряли уровень Akt фосфорилирования остатка треонина 308 и нормализованного бета-актин протеина. Значение ± стандартная ошибка среднего значения. *р<0,05; **р<0,01; ***р<0,001 по сравнению с контрольным значением.
Пример 13: Влияние 5 разных лекарственных составов экстрактов Rhaponticum carthamoides на синтез протеина (встраивание тритий-меченого лейцина) в С2С12 миотрубочках (Стадия 1, как изображено на Фиг. 29а).
[00157] Исследование было направлено на оценку способности экстрактов растения стимулировать синтез протеина, путем измерения встраивания тритий-меченого лейцина. С2С12 клетки и пять разных лекарственных составов экстрактов Rhaponticum были получены как в Примере 12.
[00158] Для анализа синтеза протеина, растущие клетки собирали и помещали в 24 луночный планшет с плотностью 30000 клеток на лунку. Клетки выращивались в течение 48 ч в 5% СО2 при 37°С. После того как клетки достигали 80% слияния, среду заменяли на дифференциирующую среду (DMEM + 2% FBS). После 5 дней, миобласты сливались в мультинуклеарные миотрубочки. Синтез протеина определяли измерением встраивания тритий-меченной аминокислоты - лейцина. Кратко, 1 ч перед встраиванием лейцина, клетки инкубировали в свободной от аминокислот среде. Затем клетки инкубировали в течение 2 ч 30 в присутствии: радиомеченого лейцина мкКи/мл и IGF1 100 нг/мл, или растительного экстракта в присутствии нормальной (0,8 мМ) или низкой (0,08 мМ) концентраций аминокислот и ДМСО (0,002%).
[00159] Все результаты выражены в % от необработанного контроля. Разницы между полученными значениями оценивались с помощью ANOVA для повторяющихся измерений, с последовательным тестом Дюннета, если ANOVA показывала существенные отличия, с помощью теста Ю-Ман-Уитни по сравнению с необработанными контролями по отношению к IGF1 или растительным экстрактам; р<0,05, **р<0,01, ***р<0,001, по сравнению с необработанным контролем.
[00160] Все результаты даны в виде значение ± стандартная ошибка среднего значения. Для всех оцененных параметров статистические анализы проводили с использованием не параметрического теста Крускал-Валлис с последующим пост тестом Дюнна (GraphPad PRISM®4). Сравнение между двумя состояниями проводили с использованием теста Манна-Уитни. Значение р 0,05 рассматривалось как значительное.
[00161] IGF1 индуцирует синтез протеина в присутствии низкой (+45%, р<0,001) или нормальной концентрации (+21%, р<0,001) аминокислот. Тест был подтвержден, так как данные с IGF-1 влияния на протеиновый синтез являются аналогичным указанным в литературе, которые описывают увеличение уровня синтеза протеина при 20-50% содержания IGF1 с низкой или нормальной концентрацией аминокислот (Kazi АА, 2010) (Broussard SR, 2004). Было отмечено, что введение радиоактивности было выше при низкой концентрации аминокислот, указывая на то, что конкурирование между радиоактивным и обычным лейцином было слабее, чем в присутствии нормальной концентрации аминокислот, как ожидалось.
[00162] Среди разных лекарственных составов R. Carthamoides, фракции F0 (нативный EtOH 50%), F5 (очищенный EtOH70% экстракт) и F7 (EtOH70% экстракт) были способны существенно стимулировать синтез протеина. Эта стимуляция была эквивалентной или сильнее, чем в контрольном анализе: IGF1 (IGF-1 100нг/мл +21% р<0,001 по сравнению с F0 10 мкг/мл +43% р<0,001 или F5 300 мкг/мл +23% р<0,01 или F7 10 мкг/мл +29% р<0,001). Фракция F5 стимулирует синтез протеина в дозозависимой манере, и значительный эффект 30 мкг/мл соответствует концентрации 20НЕ 1 мкМ. Дополнительно, фракции F0 и F7 показали эффект при наименьшей дозе (соответственно эквивалент 0,04 мкМ и 0,1 мкМ 20НЕ). Стимулирование синтеза протеина, индуцированное фракцией F0 10 мкг/мл было значительно выше, чем это наблюдалось для IGF-1,
[00163] Фракции F1 (водный экстракт) и F3 имели очень слабый, незначительный эффект, в присутствии низких концентраций аминокислот, и это также наблюдалось для F3 при высоких концентрациях аминокислот.
[00164] Фигуры 13а, 13b, 14а, 14b, 15а, 15b, 16а, 16b, 17а и 17b: Определение синтеза протеина в миотрубочках С2С12 после инкубации с 5 разными лекарственными составами экстракта Rhaponticum при трех концентрациях.
[00165] Пять разных лекарственных составов экстракта Rhaponticum, при трех концентрациях, инкубировали в течение 2 ч 30, в присутствии дифференциированных С2С12 миотрубочек и тритий меченого лейцина (5 мкКи). В конце инкубации клетки лизировали, сумму растворимых протеинов квантифицировали, и измеряли уровень тритий меченого лейцина встроеного в клетки. Значение ± стандартная ошибка среднего значения. *р<0,05; **р<0,01; ***р<0,001 по сравнению с контрольным значением.
[00166] Суммируя результаты этих экспериментов, присутствие нормальной концентрации аминокислот, F0, F5 и F7 фракций значительно стимулирует синтез протеина. Эта стимуляция была аналогичной или более сильной, по сравнению с контрольным анализом, IGF1 (IGF-1 100нг/мл +20% р<0,001 по сравнению с F0 10 мкг/мл +43% р<0,001 или F5 300 мкг/мл +23% р<0,01 или F7 10 мкг/мл +29% р<0,001). Эти фракции также стимулировали сигнальный путь (Akt и S6K1 фосфорилирования) при тестируемых низких дозах. Были отмечены проблемы в растворимости для F1 1300 мкг/мл и F7 1000 мкг/мл в анализах.
[00167] С другой стороны, фракции F1 и F3 не стимулировали синтез протеина. Тем не менее, для этих фракций, F1 и F3, наблюдалась некоторая стимуляция.
[00168] В заключение, фракция F0, и в меньшей степени фракция F7, обе, при низких концентрациях (эквивалентных 0,04-0,1 мкМ 20НЕ), увеличивали Akt и S6K1 фосфорилирование, что коррелирует со значительным увеличением в синтезе протеина.
Пример 14: Влияние одного выбранного лекарственного состава экстракта Rhaponticum carthamoides с Rhodiola на синтез протеина (встраивание тритий-меченого лейцина) в С2С12 миотрубочках (Стадия 2а и b, как изображено на Фиг. 29а).
[00169] В наших экспериментальных условиях, наилучшие результаты получены с меньшими дозами фракции F0 в присутствии нормальной концентрации аминокислот, показывая стимулирование синтеза протеина и активирование сигнального пути (индуцирование S6K1 и akt фосфорилирований) (См. Пример 13). Таким образом, эта фракция была выбрана для тестирования в эксперименте по ко-инкубации с лекарственным составом другого растения, производного вида Rhodiola, который содержит салидрозид в виде активного компонента.
[00170] Использованный экстракт Rhodiola содержал:

[00171] В первой части исследования, наилучший эффект растительного экстракта Rhaponticum был отмечен для фракции F0 при низкой дозе, новая оценка доза-ответ 0,1-10 мкг/мл для синтеза протеина проводилась паралельно для анализа доза-ответ для экстракта Rhodiola. Выбранные концентрации Rhodiola составляли: 10-104-417 мкг/мл, соответствующие конечные концентрации салидрозида 1-10-40 мкМ
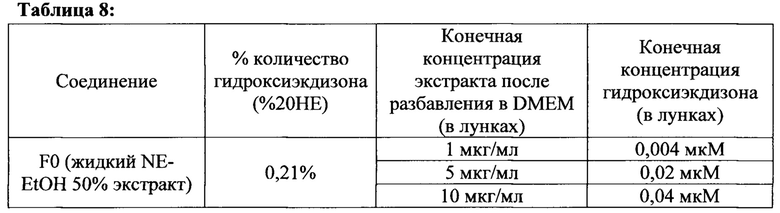
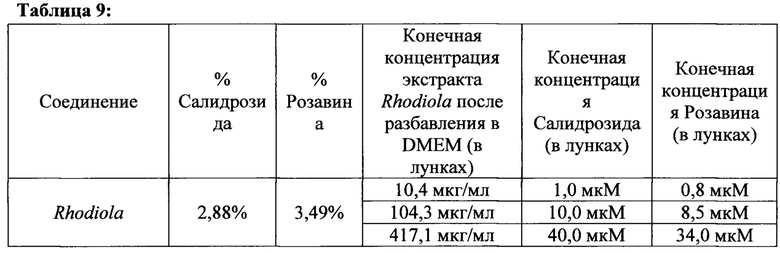
[00172] Для этого исследования, С2С12 клетки получали, как описано в Примере 12. Анализ синтеза протеина проводили, как описано в Примере 13, за исключением того, что были использованы радиоактивно меченный лейцин 5 мкКи/мл и IGF1 100нг/мл, F0 экстракт при 1, 5 и 10 мкг/мл или экстракт Rhodiola при 10, 104 и 417 мкг/мл в присутствии нормальной (0,8 мМ) концентрации аминокислот и с 0,005% ДМСО.
[00173] Фигуры 18а и 18b: Определение синтеза протеина в С2С12 миотрубочках после инкубации с экстрактами Rhaponticum F0 и Rhodiola при трех концентрациях;
[00174] Экстракты Rhaponticum F0 и Rhodiola, при трех концентрациях, инкубировали в течение 2 ч 30 в присутствии дифференциированных С2С12 миотрубочек и тритий меченого лейцина (5 мкКи). В конце инкубации клетки лизировали, сумму растворимых протеинов квантифицировали, и измеряли уровень тритий меченого лейцина встроеного в клетки. Значение ± стандартная ошибка среднего значения. *р<0,05; **р<0,01; ***р<0,001 по сравнению с контрольным значением.
[00175] Все результаты даны в виде значение ± стандартная ошибка среднего значения. Для всех оцененных параметров статистические анализы проводили с использованием не параметрического теста Крускал-Валлис с последующим пост тестом Дюнна (GraphPad PRISM®4). Сравнение между двумя состояниями проводили с использованием теста Манна Уитни. Значение р 0,05 рассматривалось как значительное.
[00176] IGF1 индуцирует синтез протеина в присутствии нормальной концентрации аминокислот, как сообщалось ранее (Kazi АА, 2010) (Broussard SR, 2004). Этот результат подтвержден нашими предыдущими данными, полученными на стадии 1 (IGF-1 стадия 1 +21%, р<0,001 по сравнению IGF-1 стадия 2 +27%, р<0,01).
[00177] F0 фракция была способна к значительной стимуляции синтеза протеина при 1 мкг/мл (См. Фигуры 18а и 18b). Эта стимуляция была эквивалентной стимуляции в контрольном анализе: IGF-1 (IGF-1 100нг/мл или F0 1 мкг/мл +27% р<0,01). Стимуляция синтеза протеина наблюдалася с F0 10 мкг/мл, тем не менее, она не достигла статистической значимости и была слабее, чем на первой стадии (+16% по сравнению с +43%). Эта разница может быть объяснима более высокой концентрацией ДМСО, использованной в эксперименте, из-за растворимости экстракта Rhodiola и ожидания последующего эксперимента по ко-инкубации. Эти результаты указывают на то, что активное вещество (а) в фракции F0 при анализе синтеза протеина является(ются) чувствительным к концентрации ДМСО.
[00178] Экстракт Rhodiola индуцирует синтез протеина при низшей концентрации (+23%, р<0,01). Эта активность аналогична активности IGF-1, в противоположность этому, при 417 мкг/мл, экстракт Rhodiola ингибирует синтез протеина (См. Фигуры 18а и 18b). Тем не менее, эта высокая доза была, возможно, вызвана ограниченной растворимостью экстракта и могла привести к негативному эффекту на синтез протеина.
[00179] Таким образом, для последующих экспериментов, было решено тестировать экстракт Rhaponticum F0 и экстракт Rhodiola при 1 и 10 мг/мл, отдельно и в комбинации, с конечной концентрацией ДМСО 0,005%. Каждую лекарственную форму обрабатывали ультразвуком для повышения растворимости.
[00180] На второй стадии, отдельные комбинации обоих растительных экстрактов изучались на определение регистрируемого потенциального влияния на синтез протеина.
[00181] Для этого исследования, С2С12 клетки получали, как описано в Примере 12. Анализ синтеза протеина проводили, как описано в Примере 13, за исключением того, что были использованы радиоактивно меченый лейцин 5 мкКи/мл и IGF1 100нг/мл, F0 экстракт при 1 и 10 мкг/мл, или экстракт Rhodiola при 1 и 10 мкг/мл, или комбинации F0 с Rhodiola при разных концентрациях в присутствии нормальной (0,8 мМ) концентрации аминокислот и с 0,005% ДМСО.
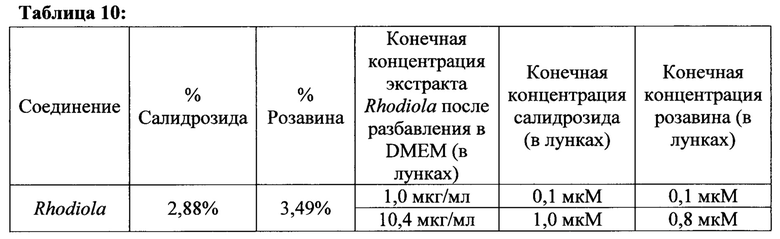

[00182] Фигуры 19а, 19b, 20а, 20b, и 21: Определение синтеза протеина в С2С12 миотрубочках после инкубации с экстрактами Rhaponticum F0 и Rhodiola, отдельно или в комбинации при двух концентрациях.
[00183] Две концентрации экстрактов Rhaponticum F0 и Rhodiola инкубировали в течение 2 ч 30, в присутствии дифференциированных С2С12 миотрубочек и тритий меченого лейцина (5 мкКи). Дополнительно, комбинацию экстрактов Rhaponticum F0 и Rhodiola, при двух разных концентрациях каждого, инкубировали в течение 2 ч 30 в присутствии дифференциированных С2С12 миотрубочек и тритий меченого лейцина (5 мкКи). В конце инкубации клетки лизировали, сумму растворимых протеинов квантифицировали и измеряли уровень тритий меченого лейцина встроеного в клетки. Значение ± стандартная ошибка среднего значения. *р<0,05; **р<0,01; ***р<0,001 по сравнению с контрольным значением.
[00184] IGF1 значительно индуцировал синтез протеина в присутствии нормальной концентрации аминокислот, как сообщалось ранее (+22%, р<0,05 относительно +27%, р<0,01 и +21%, р<0,001 в предыдущих исследованиях).
[00185] Экстракты Rhodiola сильно и значительно индуцировали синтез протеина при 10 мкг/мл, как сообщалось ранее (+30%, р<0,001 относительно +23%, р<0,01 в предыдущей стадии) (См. Фигуры 19а, 19b, 20а, 20b и 21).
[00186] F0 значительно индуцирует синтез при 1 и 10 мкг/мл, как сообщалось ранее. Аналогично стадии 1, индуцирование синтеза протеина F0 (10 мкг/мл) было значительным и более сильным по сравнению с эффектом IGF-1. Разница по сравнению со стадией 2а эксперимента могла возникнуть из-за стадии обработки ультразвуком во время растворения экстракта. Влияния F0 и Rhodiola на синтез протеина были аналогичны, когда были рассмотрены эквивалентные дозы (См. Фигуры 19а, 19b, 20а, 20b, и 21).
[00187] Усиление действия наблюдали при низких дозах обоих экстрактов (F0 и Rhodiola 1:1 +19% р<0,05 относительно F0 1 мкг/мл +14% NS и Rhodiola/мл +10% NS). Увеличение синтеза протеина комбинацией было выше, чем в случае употребления отдельно экстрактов Rhaponticum и Rhodiola, вследствии чего наблюдался стимулирующий эффект.
[00188] F0 отдельно (10 мкг/мл), Rhodiola отдельно (10 мкг/мл) и их комбинация, все существенно увеличивают синтез протеина по сравнению с контрольной группой. Тем не менее, усиления синтеза протеина не наблюдалось с комбинацией высоких доз Rhodiola и F0, по сравнению с каждым экстрактом отдельно (F0 и Rhodiola 10:10 +28% р<0,001 относительно F0 10 мкг/мл +29% р<0,001 и Rhodiola 10 мкг/мл +30% р<0,001).
[00189] Меньший эффект, чем эффект каждого экстракта в отдельности при высокой дозе (10 мкг/мл), но более сильный эффект, чем каждого экстракта отдельно при низкой дозе (1 мкг/мл), наблюдали при комбинации высокой дозы одного экстракта и низкой дозы другого (F0 и Rhodiola 1:10 +16% NS относительно F0 1 мкг/мл +14% NS и Rhodiola 10 мкг/мл +30% р<0,001 или F0 и Rhodiola 10:1 +19% р<0,05 относительно F0 10 мкг/мл +29% р<0,001 и Rhodiola 1 мкг/мл +10% NS).
Пример 15: Оценка влияния двух концентраций экстракта Rhaponticum F0 и двух концентраций экстракта Rhodiola на экспрессию генов миостатина и атрогина и их комбинации (Стадия 2с изображена на Фиг. 29а)
[00190] Исследование проводили для определения существования усиления других физиологических процессов и эффектов, вызванных экстрактами в отдельности и в комбинации на мышечный протеолиз, с помощью измерения эффекта экстрактов и их комбинации на экспрессию генов миостатина и атрогина 1. Экстракт Rhaponticum F0 и экстракт Rhodiola использовали, как описано в Примере 14.
[00191] Для анализа экспресии генов, растущие клетки собирали и помещали в 24 луночный планшет с плотностью 30000 клеток на лунку. Клетки выращивались в течение 48 ч в 5% СО2 при 37°С. После того как клетки достигли 80% слияния, среду заменяли на дифференциирующую среду (DMEM + 2% FBS). После 5 дней, миобласты сливались в мультинуклеарные миотрубочки.
[00192] Клетки обрабатывали экстрактом F0 при 1 и 10 мкг/мл, или экстрактом Rhodiola при 1 и 10 мкг/мл, или комбинацией F0 и Rhodiola при разных концентрациях, в течение 6 ч. В конце эксперимента, С2С12 клетки лизировали в тризольном растворе и РНК экстрагировали и очищали с использованием фенол/хлороформенного способа. Количество РНК после экстракции квантифицировали с помощью спектрофотометра (260 нм, 280 нм / 320 нм) и суспендировали при конечной концентрации 1 мкг/мкл. Последовательно, 1 мкг РНК использовали в качестве темплата для синтеза первой цепи цДНК с использованием олиго(dT) праймеров и обратной транскрипазной системы ВМЛ, как описано производителем (Applied Biosystems 4368814). Затем проводили количественные ПЦР с использованием 7900НТ Fast real-Time PCR detection system (Applied Biosystems) и стандартной программы для количественной ПЦР (1 цикл 95°С 15 мин, 40 циклов 95°С 15 сек и 60°С 1 мин, кривая плавления от 60 до 95°С для syber green пробы). Термоциклические эксперименты проводили в SYBR green PCR master mix (Applied Biosystems) для бета актина, образцы генов миостатина и атрогина, содержащие 100 нг цДНК, и набор праймеров с конечной концентрацией 200 нМ определяли в два разных экзона.
[00193] Все результаты даны в виде значение ± стандартная ошибка среднего значения. Для всех оцененных параметров статистические анализы проводили с использованием не параметрического теста Крускал-Валлис с последующим пост тестом Дюнна (GraphPad PRISM®4). Сравнение между двумя состояниями проводили с использованием теста Манна-Уитни. Значение р 0,05 рассматривалось как значительное.
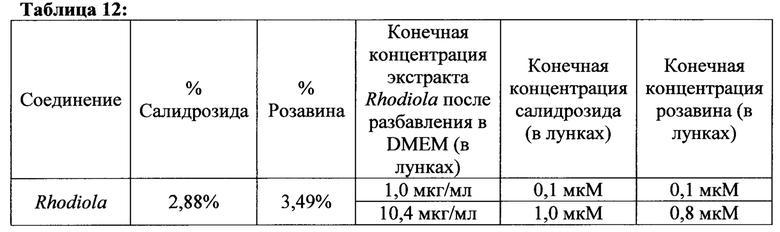

[00194] В литературе, некоторые статьи сообщают о ингибировании экспрессии гена атрогина около 40% после 24 ч инкубации с IGF-1 при 10 нг/мл (Latres Е, 2005) (Stitt TN, 2004). Никаких данных по ингибированию экспрессии гена миостатина IGF-1 не опубликовано, потому как большинство исследований фокусировались на антагонизме IGF-1 к отрицательному эффекту миостатина (Trendelenburg AU, 2009). Тем не менее, внутренне, мы отметили 20-40% ингибирующий эффект IGF-1 на экспрессию гена миостатина. Основываясь на литературе и внутренних данных, мы выбрали IGF-1 в качестве нашего положительного контроля в данном анализе. В данном эксперименте IGF1 значительно ингибировал экспрессию генов миостатина и атрогина (соответственно -25%, р<0,001 и -59%, р<0,001).
[00195] Фигуры 23а, 23b, 24а и 24b: Эффект ко-инкубации экстрактов Rhaponticum F0 и Rhodiola на экспрессию генов в С2С12 миотрубочках. Комбинацию экстрактов Rhaponticum F0 и Rhodiola, при двух разных концентрациях каждого, инкубировали в течение 6 ч в присутствии дифференциированных С2С12 миотрубочек. В конце инкубации клетки лизировали и экстрагировали РНК, превращая его в цДНК для проведения количественной ПЦР. Значение ± стандартная ошибка среднего значения. *р<0,05; **р<0,01; ***р<0,001 относительно контрольного значения; ### р<0,001 относительно контрольного значения (Манн-Уитни тест).
[00196] Rhodiola значительно и дозозависимо ингибирует ген экспрессии миостатина (-15% NS и -54% р<0,001 при низкой и высокой дозе, соответственно), в то время как, экстракт имел лишь небольшой, не значительный эффект на экспрессию гена атрогина при высокой дозе (-13% NS) (См. Фигуры 22а и 22b).
[00197] F0 индуцировал небольшое, еле заметное уменьшение в экспрессии гена миостатина (-10% NS и -21% NS при низкой и высокой дозировке, соответственно), но не оказывал никакого эффекта на экспрессию гена атрогина (+12% NS и -4% NS при низкой и высокой дозировке, соответственно).
[00198] Фигуры 22а и 22b: Эффект экстрактов Rhaponticum F0 и Rhodiola на экспрессию генов миостатина и атрогина в С2С12 миотрубочках.
[00199] Экстракты Rhaponticum F0 и Rhodiola, при двух разных концентрациях каждого, инкубировали в течение 6 ч в присутствии дифференциированных С2С12 миотрубочек. В конце инкубации клетки лизировали и экстрагировали РНК, превращая его в цДНК для проведения количественной ПЦР. Значение ± стандартная ошибка среднего значения. *р<0,05; **р<0,01; ***р<0,001 относительно контрольного значения; ### р<0,001 относительно контрольного значения (Манн-Уитни тест).
[00200] Результаты экспрессии генов миостатина представлены на фигурах 23а, 23b, 24а и 24b.
[00201] Комбинация F0 10 мкг/мл и Rhodiola 1 мкг/мл индуцирует значительное уменьшение экспрессии гена миостатина (-23%; р<0,05 относительно контрольного значения), в то время как F0 10 мкг/мл отдельно индуцирует только -21% (NS относительно контрольного значения) и Rhodiola 1 мкг/мл только -15% (NS относительно контрольного значения). Таким образом уменьшение с использованием комбинации было большим, чем в случае употребления отдельно экстрактов, вследствии чего наблюдался стимулирующий эффект.
[00202] F0 и Rhodiola 1 мкг/мл отдельно или в комбинации индуцируют небольшое, не значительное уменьшение в экспрессии гена миостатина. Магнитуда эффекта была сильнее в случае комбинации (-19% NS) по сравнению с F0 отдельно (-10%) или Rhodiola отдельно (-15% NS) (См. фигуры 23а, 23b, 24а, и 24b).
[00203] Rhodiola 10 мкг/мл сильно и значительно ингибирует экспрессию гена миостатина; тем не менее в присутствии F0 1 мкг/мл или 10 мкг/мл, не наблюдалось усиление эффекта ингибирования комбинации, и эффект был систематически ниже, чем в случае с Rhodiola (10 мкг/мл) отдельно.
[00204] Фигуры 25а, 25b, 26а и 26b: Эффект ко-инкубации экстрактов Rhaponticum F0 и Rhodiola на экспрессию гена атрогина в С2С12 миотрубочках.
[00205] Комбинацию экстрактов Rhaponticum F0 и Rhodiola, при двух разных концентрациях каждого, инкубировали в течение 6 ч в присутствии дифференциированных С2С12 миотрубочек. В конце инкубации клетки лизировали и экстрагировали РНК, превращая его в цДНК для проведения количественной ПЦР. Значение ± стандартная ошибка среднего значения. *р<0,05; **р<0,01; ***р<0,001 относительно контрольного значения; ### р<0,001 относительно контрольного значения (Манн-Уитни тест).
[00206] Комбинация F0 1 мкг/мл или Rhodiola 10 мкг/мл индуцировала сильное и значительное уменьшение экспрессии гена атрогина (-31%; р<0,05 относительно контрольного значения), в то время как каждая фракция в отдельности не оказывала никакого влияния: F0 1 мк/мл отдельно индуцировал увеличение на 21% (NS относительно контрольного значения) и Rhodiola 10 мкг/мл уменьшал на -13% (NS относительно контрольного значения). Таким образом, уменьшение с использованием комбинации было большим, чем в случае употребления отдельно экстрактов, вследствии чего наблюдался стимулирующий эффект.
[00207] Комбинация F0 10 мкг/мл и Rhodiola 1 мкг/мл уменьшала экспрессию гена атрогина в незначительной мере (-10% NS), и это уменьшение было большим по сравнению с F0 отдельно (-4% NS) или Rhodiola отдельно (+25% NS).
[00208] F0 и Rhodiola не имели значительного эффекта на экспрессию гена атрогина отдельно или в комбинации. Следует отметить, что магнитуда эффекта была сильнее в случае комбинации (-3% NS) по сравнению с F0 отдельно (+21% NS) или Rhodiola отдельно (+25% NS) как изображено на фигурах 25а, 25b, 26а, и 26b.
[00209] F0 и Rhodiola 10 мкг/мл имели небольшой, но не значительный эффект на экспрессию гена атрогина отдельно или в комбинации, и эффекта усиления не наблюдалось.
[00210] В заключение, комбинация F0 1 мкг/мл и Rhodiola 10 мкг/мл показала стимулирующий эффект на ингибирование экспрессии гена атрогина. Уменьшение с использованием комбинации было большим, чем в случае употребления отдельно экстрактов, вследствии чего наблюдался стимулирующий эффект.
Пример 16. Оценка 4 новых лекарственых составов фракции F0 из экстракта Rhaponticum при 2 концентрациях (стадия 3 изображена на Фиг. 29а)
[00211] Для улучшения результатов полученных в увеличении уровня синтеза протеина и для увеличения шансов на получение лучшего и более чистого продукта для тестирования в животных моделях, фракцию F0 по-разному обрабатывали и дополнительно очищали, получая новые фракции. F0 Ne-EtOH относится к начальной F0, ранее тестируемой в Примерах 12, 13, 14 и 15. F1 фракция соответствует фракции F1 из Примеров 12 и 13. После атомизации фракции F0 была получена сухая F0 фракция. После разбавления фракции F0 в водном растворе и очистки на колонке была получена фракция F5'.
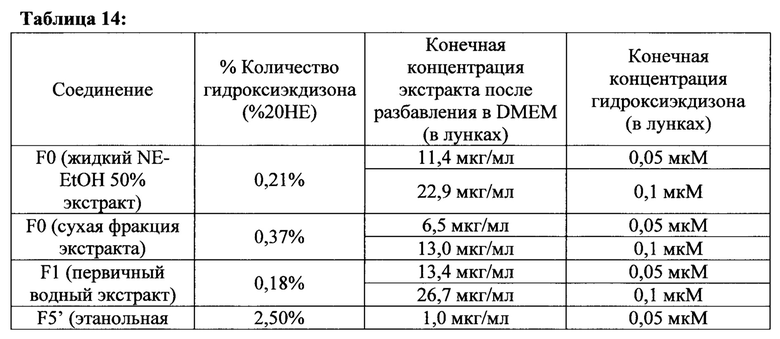

[00212] Для этого исследования, С2С12 клетки получали, как описано в Примере 12. Анализ синтеза протеина проводили, как описано в Примерах 13 и 14, за исключением того, что были использованы радиоактивно меченый лейцин 5 мкКи/мл и IGF1 100 нг/мл, F0 экстракт при 11,4 и 22,9 мкг/мл, или сухой экстракт F0 при 6,5 и 13 мкг/мл, или экстракт F1 при 13,4 и 26,7 мкг/мл, или экстракт F5' при 1 и 1,9 мкг/мл в присутствии нормальной (0,8 мМ) концентрации аминокислот и с 0,005% ДМСО. В конце эксперимента супернатанты отбрасывали и клетки лизировали 0,1н раствором гидроксида натрия в течение 30 мин. Растворимые клеточные фракции, имеющие радиоактивность, затем считывали и протеин квантифицировали с использованием колориметрического метода Лоури.
[00213] Каждое состояние тестировали в n=6. IGF1 100 нг/мл использовали в качестве положительного контроля для стимуляции синтеза протеина и сигнальной активности. Результаты синтеза протеина выражали в к.ф.в. мин/мкл/2,5 ч и в % от необработанного контрольного состояния (100%).
[00214] Результаты представлены на Фигурах 27а, 27b и 28.
[00215] IGF1 значительно индуцирует синтез протеина в присутствии нормальной концентрации аминокислот (+25%, р<0,001), как ранее сообщалось в стадиях 1-2а-2b (стадия 1 +21%, р<0,001; стадия 2а +27%, р<0,01; стадия 2b +21%, р<0,05 относительно стадии 3 +25%, р<0,001). Аналогичные результаты сообщались в литературе в присутствии нормальной концентрации аминокислот (Kazi АА, 2010) (Broussard SR, 2004).
[00216] Экстракт Rhaponticum F0 NE-EtOH 50% (нативный EtOH 50% экстракт) значительно индуцирует синтез протеина при 0,05 мкМ 20НЕ и 0,1 мкМ 20 НЕ (соответственно +20%, р<0,01 и +18%, р<0,05). Стимуляция синтеза протеина фракцией F0 была ранее отмечена при 0,04 мкМ 20НЕ (+29%, р<0,001 в стадии 2В). При 0,05 мкМ и 0,1 мкМ влияние на синтез протеина значительно, но слабее, чем при 0,04 мкМ.
[00217] Экстракт Rhaponticum F0 EtOH 50% (форма сухого порошк) индуцировал синтез протеина при обеих концентрациях, но стимуляция была сильной и значительной только при меньшей дозе (+33%, р<0,00 при 6,5 мкг/мл соответствуя 0,05 мкМ НЕ). Этот эффект был сильнее, чем эффект наблюдаемый с фракцией F0 NE-EtOH 50%.
[00218] Никакого эффекта на синтез протеина фракции F5' (очищеный EtOH 50% экстракт) не наблюдалось, ни при одной из конечных тестируемых концентраций 20НЕ.
[00219] Неочищенная водная фракция F1 показала большую активность в увеличении синтеза протеина, чем форма NE-EtOH 50% и ее производные фракции. При конечной концентрации 0,05 мкМ 20НЕ, F1 фракция показала аналогичный процент стимулирования синтеза протеина, что и сухая фракция F0 (+30%, р<0,001 и +33% соответственно, р<0,001). Не зависимо от конечной концентрации 20НЕ, эффект фракции F1 на синтез протеина был аналогичным.
[00220] Среди разных протестированных фракций Rhaponticum фракции F1 (водный экстракт), F0 NE-EtOH 50% (нативный EtOH 50% экстракт) и сухой F0 (атомизированный порошок F0 50% EtOH) показали значительный эффект стимуляции синтеза протеина. Для каждой положительной фракции лучший эффект наблюдался при меньшей дозе 20НЕ (0,05 мкМ). Самый сильный эффект на синтез протеина получен с использованием атомизированного порошка F0 50% EtOH.
[00221] С другой стороны, фракция F5', полученная из фракции F0 NE-ETOH 50% и обогащенная 20НЕ не стимулирует синтез протеина. Все результаты позволяют предположить, что эффект экстрактов Rhaponticum на протеиновый синтез не зависит лишь от концентрации 20НЕ, и что другой(ие) активный(ые) компонент(ы) способные стимулировать синтез протеина присутствует(ют) в активных экстрактах. Фигуры 27а, 27b, и 28: Определение синтеза протеина в С2С12 миотрубочках после инкубации с разными формами экстрактов Rhaponticum при двух концентрациях.
[00222] Четыре разных лекарственных состава экстракта Rhaponticum при двух концентрациях инкубировали в присутствии дифференциированных С2С12 миотрубочек и тритий меченого лейцина (5 мкКи) в течение 2 ч 30. В конце инкубации клетки лизировали, сумму растворимых протеинов квантифицировали и измеряли уровень тритий меченого лейцина встроеного в клетки считыванием. Значение ± стандартная ошибка среднего значения. *р<0,05; **р<0,01; ***р<0,001 относительно контрольного значения.
[00223] Мы наблюдали усиление синтеза протеина в анализе с комбинацией Rhodiola (1 мкг/мл) и Rhaponticum (1 мкг/мл).
[00224] Синтез протеина может стимулироваться через ингибирование миостатиновой мишени. Welle et al. продемонстрировали, что в зрелых мышах миостатин оказывает тонизирующее ингибирующее влияние на скорость синтеза миофибрилярного белка, даже после полного развития мышц (Welle S, 2008). Блокирование миостатина или его естественное отсутствие приводит к значительному увеличению мышечной массы (Lee SJ, 2005). В нашем эксперименте мы отметили уменьшение экспрессии гена миостатина после обработки С2С12 экстрактом растения Rhodiola при 10 мкг/мл (эквивалент 10 м.д.) в два раза выше, чем в случает контроля IGF-1. Интересно, Zubeldia et al сообщили, что миотрубочки обработанные в течение 6 ч экстрактом Ajuga turkestanica при 20 м.д. (растительный экстракт, содержащий экдизон, включая 20НЕ и туркестерон) значительно ингибирует экспрессию гена миостатина, и ингибирование было в два раза сильнее, чем ингибирование, индуцированное анаболическим стероидом метандростенолоном (1 мкМ) (Zubeldia JM, 2012).
[00225] Фракция Rhaponticum F0 не показала значительного эффекта на экспрессию гена миостатина, в то время как экстракт Rhodiola (10 мкг/мл) отдельно значительно уменьшал экспрессию. Насколько нам известо, до сих пор не сообщалось в литературе о прямом эффекте Rhodiola на экспрессию гена миостатина. Дополнительно, усиление эффекта ингибирования экспрессии гена миостатина наблюдалось при применении комбинации Rhodiola и Rhaponticum в нашем исследовании. Как отмечается, для синтеза белка, ранее не задокументировано эффекта усиления при применении обоих экстрактов (Rhaponticum и Rhodiola).
[00226] Увеличение мышечной массы является балансом между синтезом протеина, его протеолизом и дифференциацией сателитных клеток. Атрогин-1 или F-box мышечной атрофии (MAFbx) является главной связанной с атрофией Е3 убиквитин лигазой высоко экспрессированной в скелетной мышце во время мышечной атрофии и других болезненных состояниях, таких как сепсис, раковая кахексия, и голодание (Cong Н, 2011). Мы исследовали убиквитин протеазомную систему. Ни один из экстрактов отдельно не показал значительного эффекта на экпрессию гена атрогина. Напротив, интересно что, эффект усиления ингибирования экпрессии гена атрогина наблюдался (-31%, р<0,05), когда фракцию F0 экстракта Rhaponticum инкубировали с экстрактом Rhodiola в соотношении 1:10. Cong et al. показали, что уменьшение количества атрогина с применением SiMAFbx аденовирусов приводило к 55% ингибированию генной экспрессии, 60% ингибированию уровня протеина и 20% увеличению мышечной массы. Продемонстрировано, что атрогин нацелен на MyoD деградацию в скелетной мышечной атрофии (Lagirand-Cantaloube J, 2009).
[00227] Результаты при низком содержании аминокислот:
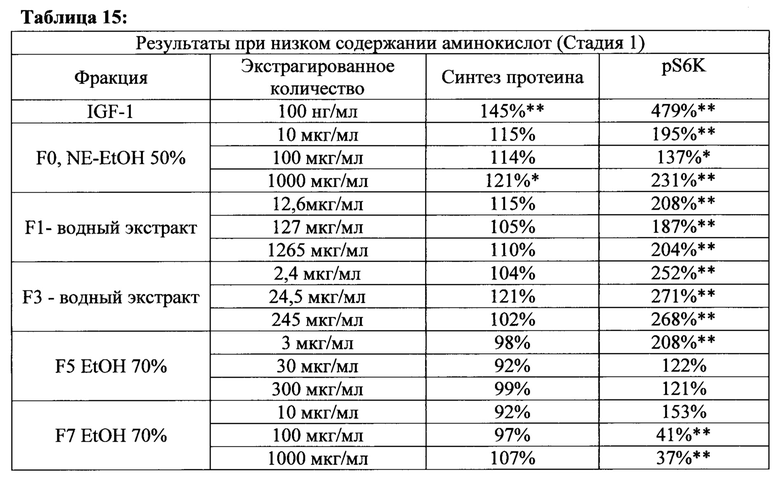
[00228] В присутствии низкого содержания аминокислот, не наблюдалось значительной индукции синтеза протеина, за исключением, как в присутствии фракции F0 EtOH 50%; тем не менее, стимулирование синтеза протеина или pS6K1 фосфорилирования было в два раза ниже, чем таковое индуцированное IGF-1. Отмечено, что практически во всех случаях сигнальный путь pS6K1 был активирован, но возможно, не достигал необходимого порога для индуцирования физиологического ответа. Более того, при низком содержании аминокислот уровень pS6K1 был ниже, чем таковой наблюдаемый в контрольных условиях в присутствии нормальной концентрации аминокислот (максимум 1,2 для лучшей фракции относительно 2,1 для контроля в присутствии нормальной концентрации аминокислот). Таким образом, предпочтительно использовать экстракт растения в присутствии нормальной концентрации аминокислот.
[00229] F3, F5 и F5' являются очищенными фракциями из водных (отмечены голубым) или этанольных (отмечены оранжевым) экстрактов. Во всех этих очищенных фракциях, не наблюдалось никакой стимулирующей протеиновый синтез активности, или она была меньшей по сравнению с наблюдаемой активностью для маточного раствора. Эти данные указывают, что во время стадии очистки активное соединение(я) теряется(ются) в течение очистки.
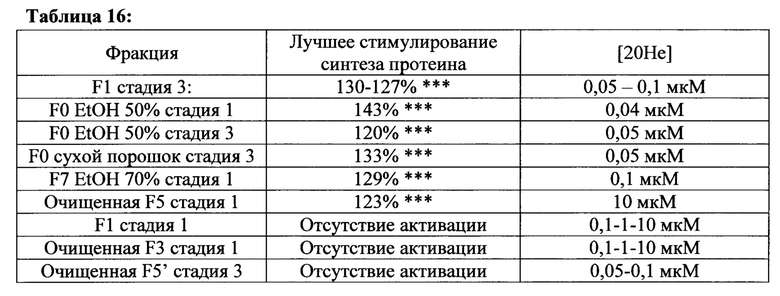
[00230] Никакой реальной корреляции не было найдено между концентрацией 20НЕ и стимулированием синтеза протеина. Тем не менее, в неочищенной фракции, показавшей самый сильный эффект стимуляции синтеза протеина, концентрация 20НЕ является наилучшей и является между 0,05 и 0,1 мкМ. Эти результаты позволяют предположить, что 20НЕ не является единственным активным веществом, вовлеченным в активацию протеинового синтеза. Таким образом, было бы особенно интересно получить информацию о составе разных фракций для определения, какая смесь соединений вносит вклад в стимуляцию синтеза протеина.
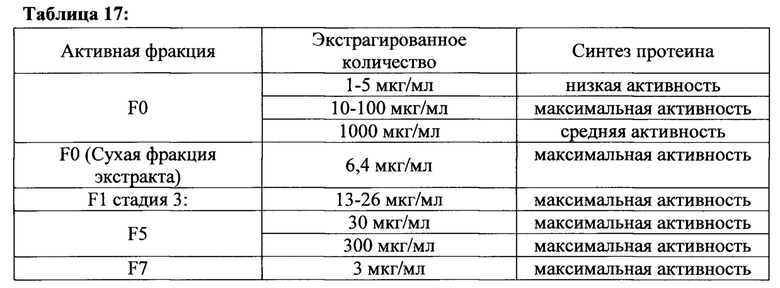
[00231] Максимальная активность экстракта растения Rhaponticum наблюдалась при концентрации между 10 мкг/мл и 100 мкг/мл. Когда фракция теряла часть своей активности из-за стадии очистки, наблюдалось, то, что экстракт должен был быть тестирован при более высокой концентрации для наблюдения аналогичного эффекта на синтез протеина. Таким образом, лучшие концентрации в оценке in vitro экстрактов растения Rhaponticum являются 10-100 мкг/мл.

[00232] Экстракты Rhaponticum и Rhodiola были оба активны в синтезе протеина; каждый экстракт по отдельности увеличивал синтез протеина на 20-30%, достигая наивысшего уровня, который может быть получен в анализе. Эффект усиления синтеза протеина должен лучше оцениваться на уровне сигнального пути, так как максимальный лимит стимуляции является более 100%, когда измеряются уровни pAkt или pS6K.
[00233] Экстракт Rhodiola индуцирует ингибирование экспрессии гена миостатина, но с меньшим эффектом, по сравнению со случаем, когда ко-инкубируют Rhodiola и F0 фракцию Rhaponticum. Результаты позволяют полагать, что соединение(ния) во фракции F0 было способно антагонизировать полезные эффекты экстракта Rhodiola. Идентификация и предварительная очистка этого вещества (веществ) может улучшить эффект ко-инкубации.
[00234] Ни один из данных экстрактов отдельно не имеет ингибирующего эффекта на экпрессию гена атрогина, в то же время при определенных условиях ко-инкубации (F0 1 мкг/мл и Rhodiola 10 мкг/мл) наблюдался эффект усиления ингибирования экспрессии гена атрогина. Наблюдался синергический и полезный эффект экстрактов Rhodiola и Rhaponticum на протеолиз.
[00235] В заключеие, данное исследование продемонстрировало, что экстракт Rhaponticum EtOH 50% был наиболее активной фракцией среди оцененных фракций при стимуляции синтеза протеина. Экстракты Rhodiola также сильно увеличивают синтез протеина. Когда ко-инкубируют с фракцией F0 Rhaponticum, может наблюдаться более сильный эффект на этот параметр, в сравнении с каждым экстрактом отдельно (когда каждый экстракт смешивали при концентрации 1 мкг/мл).
[00236] Паралельно, экстракт Rhodiola сильно уменьшает экспрессию гена миостатина при 10 мкг/мл, но лучшего эффкта не наблюдалось при ко-инкубировании фракции F0 Rhaponticum. Следует отметить, что эффект усиления наблюдался при экспрессии гена миостатина, при комбинировании Rhodiola (1 мкг/мл) и Rhaponticum (1 мкг/мл), вследствии чего экспрессия гена миостатина была ниже (но не значительно) по сравнению с каждым экстрактом по отдельности.
[00237] Наблюдаемый синергичный ингибирующий эффект смеси экстрактов на экспрессию гена атрогина, позволяет предположить полезное влияние смеси экстрактов Rhaponticum и Rhodiola на протеолиз в дополнении к ее эффекту на синтез протеина.
Пример 17: Тестирование влияния комбинирования экстракта Rhodiola и экстракта Rhaponticum на синтез протеина в мышце, и на ассоциированные пути, на мышечную массу, и мышечную силу в животной модели.
[00238] Комбинацию экстрактов Rhodiola и Rhaponticum тестировали на ее влияние на физическую силу, мышечный вес, Akt фосфорилирование в мышце и содержание протеина, содержание глюкозы и лактата в плазме.
[00239] Сухой экстракт корня Rhaponticum carthamoides (F0-EtOH 50% сухой порошок) получали экстракцией смесью этанол-вода 50% (об./об.), как описано в Примере 1. Экстракт может предпочтительно содержать (% мас./мас.) 0,395% 20НЕ, 0,79% общей суммы экдистероидов и 13,4% общей суммы полифенолов (по Фолину Сиокалто) на основе общего сухого веса травяного экстракта.
[00240] Этанольный экстракт корня Rhodiola rosea может быть получен таким образом, чтобы предпочтительно содержать приблизительно (%мас./мас.) 3,41% салидрозидов, 3,12% розавина и 4,20% розавинов (в виде общей суммы розарина, розавина и розина) на основе общего сухого веса травяного экстракта.
[00241] Оба экстракта представляли собой порошок с <5% влажности. Экстракты смешивали в соотношении 50:50 (мас./мас.) на основании общей массы композиции. В некоторых тестах не добавлялись ни носитель, ни дополнительные вспомогательные вещества.
[00242] Эту комбинацию двух экстрактов корня Rhodiola rosea и корня Rhaponticum carthamoides анализировали на целевые вещества.
[00243] Самцы крыс породы Вистар получали комбинацию экстракта при дозе 50 мг/кг живого веса (n=10) или носитель (n=10) в течение периода 6 недель. Комбинацию вводили кормлением через желудочный зонд один раз в день.
[00244] Силу захвата передней лапы крыс Вистар оценивали до лечения (день 0) и через 42 дня лечения (день 43), и изменение силы захвата передней конечности от дня 0 до дня 43 расчитывали как разницу (сила захвата на день 43 - сила захвата на день 0). Как хорошо известно в данной области техники, этот тест силы захвата нацелен на измерение силы передней лапы и задней лапы у крыс, и был ранее использован другими, например, для измерения силы после введения 20НЕ (Feldman-Gorelick et al, 2008, JAFC).
[00245] Как проиллюстрировано на Фиг. 30а, увеличение в разнице силы захвата в смешаной группе было на 45% выше, чем увеличение, наблюдаемое в контрольной группе, не получавшей лечение. Дополнительно, как проиллюстрировано на Фиг. 30b, когда разница в силе захвата является альтернативно представленной на основании веса тела (то есть, кг сила / г веса тела), смешанная группа, получавшая лечение, имела на 40% выше увеличение в силе, чем увеличение, наблюдаемое в контрольной группе, не получавшей лечение.
[00246] Вес крыс измеряли дважды в неделю, каждую неделю во время периода кормления. Уровень глюкозы и лактата в плазме измеряли до начала лечения и после 6 недель лечения (до и после упражнения).
[00247] После окончания 43 дневного лечения (день 44), после теста на силу захвата передней конечности и забора проб крови, животных убивали. Мышцы передней и задней конечнойстей крыс породы Вистар изымали (длинный разгибатель пальцев (EDL), камбаловидная мышца, квадрицепс, большеберцовая мышца и трицепс) и взвешивали. Как проиллюстрировано на Фигурах 31а и 31b, наблюдали увеличение веса EDL на 5% и соотношение вес EDL к весу тела (р<0,05 Манн-Уитни для обоих). Дополнительно, как проиллюстрировано на Фигурах 32а и 32b, также найдено увеличение в весе камбаловидной мышцы и отношении вес камбаловидной мышцы к весу тела. Никаких существенных изменений в весе остальных мышц не отмечено.
[00248] Содержание протеина и Akt фосфорилирование измеряли в образцах мышц. Вводимая в течение 6 недель комбинация Rhaponticum и Rhodiola при дозировке 50 мг/кг не изменяла значительно количество протеина в EDL мышце (в мкг протеина на мг ткани; Фиг. 33а) и общего количества протеина в EDL (мг на мышцу; Фиг. 33b). Тем не менее, увеличение в содержании протеина (в мкг протеина на мг ткани; +10%, р=0,08, Фиг. 34а) и общем количестве протеина в EDL (мг на мышцу; +14%, Фиг. 34b) наблюдали в камбаловидной мышце крыс породы Вистар.
Пример 18: Тестирование влияния 8 недельного приема добавки комбинации экстрактов Rhodiola и Rhaponticum на конституцию тела, мышечную массу, мышечную силу и устойчивость к упражнениям у физически активных мужчин во время программы тренировки устойчивости.
[00249] Имея результаты in vitro и исследований на животных, предположено, что прием в качестве добавки описанной смеси физически активными мужчинами во время тренировки устойчивости может принести пользу в увеличении силы и мышечного размера. Целью этого исследования является определение влияния описанного лекарственного состава в качестве пищевой добавки на физически активных мужчин в течение 8 недельной программы динамического постоянного внешнего сопротивления (DCER) на силу и толщину мыщц в поперечном сечении.
[00250] Первичной целью исследования является оценить эффекты 8-недельного приема пищевой добавки комбинации экстрактов Rhaponticum/Rhodiola (см., например, Пример 17 для описания смеси) на мышечную силу (1-максимальное повторение в тренажере-платформе для ног и в жиме лежа). Испытание может оценить максимальную и минимальную мышечную силу тела, с использованием 1-максимального повторения в жиме лежа, и в тренажере-платформе для ног, тестированием на 4 и 8 неделях.
[00251] Вторичными целями являются оценить влияние 8-недельного приема пищевой добавки комбинации экстрактов Rhaponticum/Rhodiola на состав тела и мышечную массу (DXA), содержание мышечного протеина, уровень глюкозы в крови и устойчивость / время к утомлению во время тренировки на устойчивость.
[00252] Исследование может быть рандомизированным, дважды-слепым, плацебо контролированным, и исследованием в паралельных группах. Согласно с рандомизацией, участники могут принимать низкую (100 мг) или высокую (400 мг) дозу в виде пищевой добавки или плацебо каждый день в течении 8 недель. Изменения в мышечной силе (мышечная сила верхней и нижней части тела) могут быть оценены на неделе 0 (базовая линия), неделе 4 и неделе 8 с применением 1-максимального повторения в жиме лежа, и в тренажере-платформе для ног. Изменения в конституции тела и мышечной массе могут быть оценены на неделе 0 и неделе 8 с применением DEXA. Мышечная биопсия и анализы могут проводиться на неделе 0 и неделе 8. Устойчивость/время к утомлению может быть измерена путем увеличения количества повторений в 1-максимальном повторении на неделе 0 (перед приемом; базовая линия), и неделе 8. Ментальная утомляемость может быть оценена с использованием опросника Рейтинга воспринимаемого напряжения (RPE) на неделе 0 (перед приемом; базовая линия), и на неделе 8.
[00253] В порядке проверки точечных метаболических ответов на прием пищевой добавки (в начале и в конце фазы приема), может быть проведен точечный прием пищевой добавки, рандомизированный, дважды-слепой, перекрестный, плацебо контролированный. Точечный прием низкой (200 мг) и высокой (400 мг) дозы пищевой добавки или плацебо может следовать оценке мышечной силы (мышечной силе верхней и нижней частей тела), как описано выше. Биологические параметры, такие как уровень глюкозы в крови и уровень лактата в крови могут быть также измеряны.
[00254] Для исследования, могут быть отобраны здоровые, физически активные мужчины возвраста колледжа (18-35 лет, например), которые могут брать участие в исследовании. Участники могут быть допущены к исследованию, если они удовлетворяют всем критерия включения и не имеют критериев исключения (определенным по опросникам). Этическое подтверждение может быть получено от этического комитета соответственого университета.
[00255] Участники могут быть включены в исследование, если они:
- Не курят;
- В возврасте от 18 до 35 лет;
- С ИМТ 19-29,9 кг/м2;
- Имеют стабильный вес (то есть не набирали или не теряли более чем 3 кг/м2 за последние 3 месяца);
- Являются физически активными, то есть, ходят в спортивный зал приблизительно дважды в неделю, но не следуют интенсивным тренировкам или соревновательной программе (определить виды спорта, которым они занимаются и частоту/интенсивность);
- Имели по меньшей мере 2 раза в неделю в течение 3 последних месяцев до начала исследования тренировки с весам;
- Не принимают какие-либо лекарства (установить ограниченную длительность перед началом исследования) и/или не принимали в течение последнего месяца какие-либо пищевые добавки, которые как известно исследователю влияют на метаболизм, вес тела и/или аппетит; и
- Не принимали эргогенических пищевых добавок, которые могут влиять на мышечную массу (например, креатин, НМВ и т.п.) и/или добавки, которые могут влиять на уровень анаболических/катаболических гормонов (например, андростенедион, DHEA и т.п.) в течение 1 месяца (определить) до начала исследования.
[00256] Участники будут исключены если они:
- Курят;
- Ходят в спортивный зал больше двух раз в неделю и/или следуют интенсивным тренировкам или соревновательной программе (нежелательные виды спорта и частоту/интенсивность следует определить);
- Имеют поставленный диагноз существенного медицинского состояния;
- Имеют в анамнезе, или имеют симптомы метаболических, эндокринных или кардио расстройств;
- Принимают любые медицинские или пищевые добавки и/или принимали в течение последнего месяца пищевые добавки, которые, как известно исследователю влияют на метаболизм, вес тела и/или апетит; или
- Принимали эргогенические уровни пищевых добавок, которые могут влиять на мышечную массу (например, креатин, НМВ и т.п.) и/или добавки, которые могут влиять на уровень анаболических/катаболических гормонов (например, андростенедион, DHEA и т.п.) в течение 1 месяца (определить) до начала исследования.
[00257] Участники могут быть распределены в две группы: принимающие добавку или плацебо (20 участников в каждой группе). Группы могут быть подобранными как можно ближе по физическим характеристикам.
[00258] Продуктом исследования может быть комбинация экстрактов Rhodiola и Rhaonticum, как описано в Примере 17. Две дозы тестируемого продукта могут тестироваться в исследовании: низкая доза (100 мг) и высокая доза (400 мг). Инертное плацебо может быть применено и состоять из целлюлозы.
[00259] Все участники могут выполнить силовой тест до начала приема добавки (неделя 0) и на 4 неделе и на 8 неделе. Одно максимальное повторение (1RM; самый тяжелый вес, которые может быть поднят в конкретном упражнении с правильной формой) может оцениваться для верхней и нижней частей тела с помощью жима лежа (с применением машины Смита) и тренажера-платформы для ног, соответственно.
[00260] Перед и после 8 недель приема пищевой добавки, вес и рост участников будет записан, а также их обхваты конечностей и обхваты талии. Конституция тела и мышечный вес могут оцениваться с помощью DEXA на базовой линии (неделя 0) и после 8 недель, на день перед 1RM упражнением.
[00261] Биопсии мышц до и после приема добавки могут выполняться для измерения количества фосфорилированного протеина по сравнению с общим протеином, анализа протеина, анализа путей Akt/pS6K1, и измерения диаметра мышечных волокон. Также уровень глюкозы в крови может быть измерен.
[00262] Устойчивость/время до утомления, эти параметры могут быть измерены путем увеличения количества повторений в 1-RM. Ментальная утомляемость может быть оценена с использованием опросника Рейтинга воспринимаемого напряжения (RPE).
[00263] Все участники могут пройти 8 недельную контролируемую тренировочную программу с двумя сессиями в неделю для проверки гомогенности в упражнениях между участниками. Тренировочная нагрузка может быть представлена как процент измерений базовой линии 1RM и тренировочная программа может прогрессировать в интенсивности каждые 2 недели. Участники могут тренироваться 2-3 раза в неделю под руководством квалифицированного по силе и обучению тренера. Все тренировочные сессии проводятся с утра и каждая сессия длится приблизительно 90 мин. Каждая сессия может состоять из стандартизированного разогрева, 4x6 повторений каждого упражнения (с 4 мин отдыха между сетами) и заминкой. Могут выполняться упражнения нацелены на мускулатуру верхней части тела (например, жим лежа, тренажер для дельтовидных мышц и отжимания на трицепс) и нижней части тела (например, тренажер-платформа, и разгибание ног, сгибание ног на бицепс бедра). Оценка воспринимаемого напряжения может регистрироваться с интервалами во время тренировок. Всем участникам может быть преподана правильная техника выполнения каждого упражнения до начала исследования.
[00264] Для контроля приема протеина участниками, диетолог посоветует диеты способствующие набору протеина и диетические записи в форме 24-часового диетического отзыва, которые могут использоваться и проанализированы на недели 0, 4 и 8.
[00265] Средние значения на 0, 4, и 8 недели могут быть вычислены. Изменение от уровня базовой линии может быть оценено на каждой временной точке, и в любой группе, с применением повторяющегося измерения ANOVA (или одно направленное ANOVA, если в наличие лишь только две точки).
[00266] Также, изменение от уровня базовой линии (ΔТх-Т0) может быть расчитано для каждой переменой и значения может сравниваться между группами с применением кратного ANOVA.
[00267] Ожидается, что результаты покажут увеличение в мышечной массе, и мышечной силе (1-RM), размере мышечного волокна и содержания протеина. Ожидается, что добавка увеличит время утомление/сопротивление в упражнении и улучшит порог ментальной уставаемости.
[00268] Пример 19: Тестирование влияния экстракта Rhodiola и экстракта Rhaponticum или комбинации обоих на синтез протеина в мышце, после тренировки устойчивости в животной модели.
[00269] Экстракт Rhodiola или экстракт Rhaponticum, отдельно или в комбинации обоих экстрактов, тестировались на их влияние на стимулирование синтеза протеина в мышце после интенсивной тренировки сопротивления.
[00270] 11-недельные крысы породы Вистар Хан приобретали у Charles River (Charles River Laboratories, L'Arbresle,  , France) и размещали при постоянной комнатной температуре и влажности, и поддерживали 12/12 ч день/ночь цикл. Крысы получали 30 г/день специальной низко протеиновой диеты для крыс, бедной на протеин, антиоксиданты и витамины (см. таблицы ниже, указывающие лист ингредиентов и пищевую ценность диеты) для максимально точного моделирования диеты физически активного человека, полученной от SAFE (Scientific Animal Food & Engineering, Augy, France), и количество воды при этом не ограничивалось. Крысы были 12-недельного возвраста на начало эксперимента и считались полностью взрослыми.
, France) и размещали при постоянной комнатной температуре и влажности, и поддерживали 12/12 ч день/ночь цикл. Крысы получали 30 г/день специальной низко протеиновой диеты для крыс, бедной на протеин, антиоксиданты и витамины (см. таблицы ниже, указывающие лист ингредиентов и пищевую ценность диеты) для максимально точного моделирования диеты физически активного человека, полученной от SAFE (Scientific Animal Food & Engineering, Augy, France), и количество воды при этом не ограничивалось. Крысы были 12-недельного возвраста на начало эксперимента и считались полностью взрослыми.

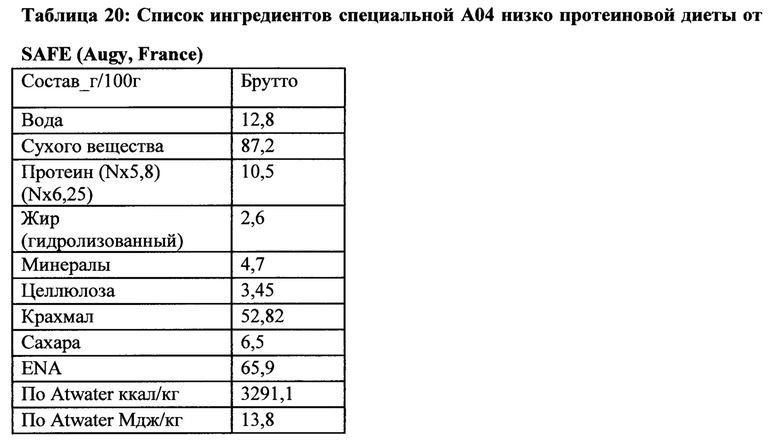
[00271] Эксперимент проводили на 8 группах состоящих из 8 крыс каждая, которые получали лечение указанное ниже:
[00272] Группа 1 (контрольная группа): 0,5% КМЦ (карбоксиметилцеллюлозы) в качестве носителя и негативного контроля.
[00273] Группа 2: 0,24 мг/мл протеина Whey Milical
[00274] Группа 3: 10 мг/мл экстракта корня Rhodiola rosea
[00275] Группа 4: 10 мг/мл экстракта корня Rhaponticum carthamoides
[00276] Группа 5: 20 мг/мл Rhodiola / Rhaponthicum, отношение 50:50 (мас./мас.)
[00277] Группа 6: 10 мг/мл Rhodiola / Rhaponthicum, отношение 50:50 (мас./мас.)
[00278] Группа 7: 5 мг/мл Rhodiola / Rhaponthicum, отношение 50:50 (мас./мас.)
[00279] Группа 8: 2 мг/мл Rhodiola / Rhaponthicum, отношение 50:50 (мас./мас.)
[00280] Соответственная эквивалентная доза для человека (в мг/кг веса тела и мг/день), а также соответственная дозировка в мг/кг веса тела крысы указаны в Таблице 21 ниже.
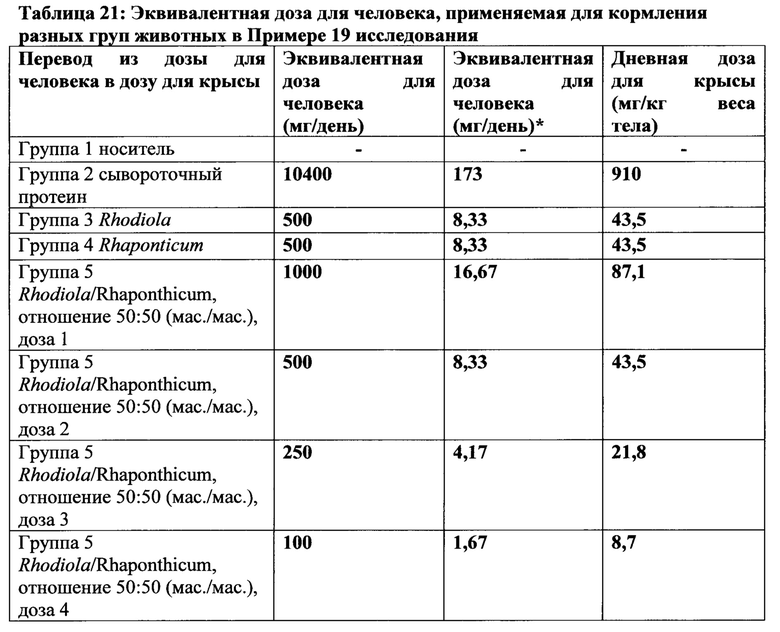
*Формула из FDA, 2005; Эквивалентна доза для человека HED (мг/кг)=животная доза в мг/кг х (вес животного в кг/вес человека в кг)0,33
[00281] Сухой экстракт корня Rhaponticum carthamoides (F0-EtOH 50% сухой порошок) получали экстракцией смесью этанол-вода 50% (об./об.), как описано в Примере 1. Экстракт может предпочтительно содержать (% мас./мас.) 0,395% 20НЕ, 0,79% общей суммы экдистероидов и 13,4% общей суммы полифенолов (по Фолину Сиокалто) на основе общего сухого веса травяного экстракта.
[00282] Этанольный экстракт корня Rhodiola rosea может быть получен таким образом, чтобы предпочтительно содержать приблизительно (%мас./мас.) 2,45% салидрозидов, 1,14% розавина и 2,43% розавинов (в виде общей суммы розарина, розавина и розина) на основе общего сухого веса травяного экстракта.
[00283] Оба экстракта представляли собой порошок с <5% влажности. Экстракты смешивали в соотношении 50:50 (мас./мас.) на основании общей массы композиции. В некоторых тестах не добавлялись ни носитель, ни дополнительные вспомогательные вещества.
[00284] Эту комбинацию двух экстрактов корня Rhodiola rosea и корня Rhaponticum carthamoides анализировали на целевые вещества.
Тренировка
[00285] После одной недели адаптации 16 крыс случайно разделили на 2 группы по 8 крыс. За 72 час до тренировки, крысы проходили урок-обучение для того чтобы быть знакомыми с лестницей и их не кормили 24 часа перед началом эксперимента.
[00286] В день эксперимента, 4 крысы из одной и той же группы тренировали во временной манере на 1 м высокой лестнице. Каждые 4 крысы группы делали 10 вскарабкиваний с нагрузкой, которая составляла 0% от веса тела, 50% и 75% от их веса тела. Между каждым вскарабкиванием, крысам позволяли отдохнуть 2 мин, и 5 мин между каждым подходом.
[00287] Мешочки, содержащие веса прикреплялись к основанию хвоста клейкой лентой.
[00288] После обучения, крысы продолжали голодать и не получали новой еды.
Введение лекарства
[00289] Лекарства вводили незамедлительно после каждой тренировочной сессии с помощью кормления с зондом.
[00290] Растворы готовили для немедленного применения в 0,5% CMC.
Вскрытие и изъятие мышц
[00291] Два часа после тренировки, крысам внутрибрюшино вводили 10 мМ пиромицина 100 мкл/25 г (Sigma Aldrich, Catalog Number P8833), и им вводили анестезию путем внутрибрюшинной инъекции пентобарбитала 150 мг/кг (PENTOBARBITAL ®).
[00292] Менее чем через 30 мин после инъекции пиромицина, правый глубокий сгибатель пальцев кисти (FDP), дельтовидную мышцу и бицепс изымали и помещали в раствор с изопентаном, быстро замораживали жидким азотом и хранили при -80°С для последующих биохимических анализов.
Эктракция протеина и дозировка
[00293] 20 мг каждого образца гомогенизировали в 10 объемах лизисного буфера (Tris 20 мМ рН 6.8, NaCl 150 мМ, ЭДТА 2 мМ, Triton Х-100 1%) с ингибирующим протеазы коктейлем (Р8340, Sigma Aldrich). Сумму протеинов мышцы экстрагировали IKA ULTRA TURRAX Т25 digital. Гомогенат вращали 10 мин при 4°С и собирали супернатант.
Квантифицирование синтеза протеина
[00294] Общий синтез протеина анализировали с помощью Вестерн Блота анти-пиромицина.
[00295] 50 мкг образцов протеина денатурировали, разделяли на 10% ДСН-ПААГ-электрофорезе и переносили на нитроцеллюлозную мембрану. Первичное антитело анти пиромицин (Анти- пиромицин антитело, клон 12D10 от EMD Millipore (1/3000) применяли в течение ночи при 4°С, и последовательно инкубировали с вторичным антитело конъюгатом с пероксидазой (анти-мышиный IgG ECL от GE Healthcare UK Limited).
[00296] Квантифицирование внедрения пиромицина в цепи протеина (через образование пептидной связт) с помощью количественного анализа Вестерн Блота представляет собой de novo синтезированный протеин (индукция синтеза протеина) в мышцах in vivo и представляет собой стимулирование синтеза протеина после тренировочной сессии в зависимости от введения лекарства (Goodman and Hornberger, 2013). Синтез протеина, таким образом, выражен как относительное отношение синтезированного протеина в виде % от контрольных условий (группы животных получавших носитель) или других условий.
[00297] Все результаты даны в виде значение ± стандартная ошибка среднего значения. Для сравнения данных использовался Fishers LSD ANOVA. Значимость была установлена при р<0,05.
[00298] Как проилюстрировано на Фиг. 35а, показанный вестерн блот правого глубокого сгибателяь пальцев кисти (FDP) восьми животных для каждого лечения и на Фиг. 35b, показано относительные единицы уровней пиромицина нормализованные к количественной загрузке общего протеина и негативномой контрольной группе, экстракты корня Rhaponticum carthamoides отдельно, но не экстракты корня Rhodiola rosea были способны значительно стимулировать синтез протеина, но в меньшей степени, чем любые концентрации (с уменьшением дозы) комбинации обоих экстрактов.
[00299] Комбинация экстрактов (для четырех уменьшающихся тестированных доз: от эквивалентной дозы для человека = 1000 мг/день до 100 мг/день) была очевидно более активной относительно экстракта корня Rhodiola rosea или корня Rhaponticum carthamoides отдельно, как показано на Фигурах 35d и 35е соответственно (показано относительные единицы уровней пиромицина нормализованные к количественной загрузке всего протеина, в Rhodiola группе или в Rhaponticum группе соответственно). Более того, эффект комбинации экстрактов (для четырех уменьшающихся тестированных доз: от эквивалентной дозы для человека = 1000 мг/день до 100 мг/день) была также существенно выше для сыроваточных протеинов, как показано на Фиг. 35с (показано относительные единицы уровней пиромицина нормализованные к количественной загрузке всего протеина, и группе сывороточных протеинов). Таблица 22 иллюстрирует разницу межу результатами, полученными применением различных доз комбинации относительно, с тем, что могло ожидаться из результатов экстракта корня Rhodiola rosea и экстракта корня Rhaponticum carthamoides по отдельности. Неожиданно, эффект стимулирования синтеза протеина в FDP комбинации половинных концентраций корня Rhodiola rosea и корня Rhaponticum carthamoides показал эффект лучше, чем полные концентрации Rhodiola oru Rhaponticum отдельно. Что является синергией. Дополнительно, эффект комбинации половины концентрации Rhodiola и половины концентрации Rhaponticum был выше (1,9 раз больше), чем ожидалось. Дополнительно, эффект комбинации четверти концентрации Rhodiola и четверти концентрации Rhaponticum был выше (в 3,0 раза больше), чем ожидалось. В результате, эффект комбинации в 10 раз меньшей концентрации Rhodiola и 10 раз меньшей Rhaponticum был выше (в 5,8 раз больше), чем ожидалось. Эти результаты четко демонстрируют синергию комбинации экстрактов на стимуляцию синтеза протеина в мышце FDP с последующим точечным упражнением на сопротивление при 500 мг/день, 250 мг/день и 100 мг/день комбинации с сотношением 50:50 (мас./мас).
[00300]
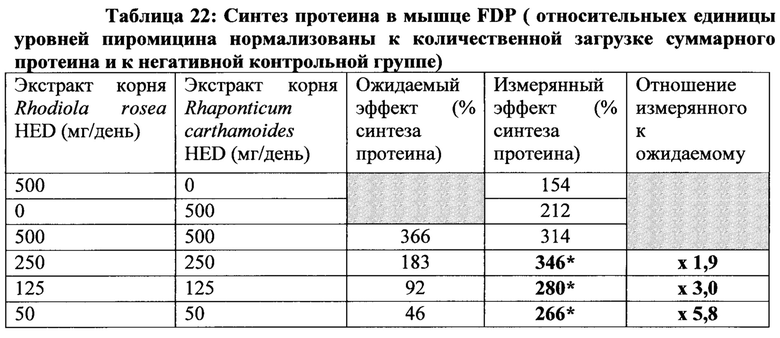
*: сильные неожиданные результаты с комбинацией экстракта корня Rhodiola rosea и экстракта корня Rhaponticum carthamoides, отношение 50:50 (мас./мас.)
[00301] Как проилюстрировано на Фиг. 36а, показанный вестерн блот дельтовидной мышцы восьми животных каждого лечения, и на Фиг. 36b, показано относительные единицы уровней пиромицина нормализованного к количественной загрузке общего протеина и негативной контрольной группе, ни экстракт корня Rhaponticum carthamoides отдельно, ни экстракт корня Rhodiola rosea не были способны значительно стимулировать синтез протеина, но комбинация обоих экстрактов значительно стимулирует синтез протеина при уменьшающихся HED 1000 мг/день, 500 мг/день и 250 мг/день.
[00302] Комбинация экстрактов (для трех уменьшающихся HED: 500 мг/день до 100 мг/день) была, очевидно, более активной относительно экстракта корня Rhodiola rosea отдельно, как показано на Фигуре 36d (показано относительные единицы уровней пиромицина нормализованные к количественной загрузке всего протеина, и Rhodiola группе). Комбинация экстрактов (от HED: 1000 мг/день до 100 мг/день) была, очевидно, более активной относительно экстракта корня Rhaponticum carthamoides отдельно, как показано на Фигуре 36е (показано относительные единицы уровней пиромицина нормализованные к количественной загрузке всего протеина, и Rhaponticum группе). Кроме того, эффект комбинации экстрактов (для HED=1000 мг/день и 500 мг/день) также был существенно выше относительно сывороточных протеинов, как показано на Фиг. 36с (показано относительные единицы уровней пиромицина нормализованные к количественной загрузке всего протеина, и группе с сывороточным протеином). Таблица 23 (ниже) иллюстрирует разницу между результатами, полученными с применением разных доз комбинации по сранению с таковыми, которые можно было бы ожидать от экстракта корня Rhodiola rosea и экстракта корня Rhaponticum carthamoides по отдельности. Неожиданно, эффект стимулирования синтеза протеина в дельтовидной мышце комбинацией половинных концентраций корня Rhodiola rosea и корня Rhaponticum carthamoides показал эффект лучше, чем полные концентрации Rhodiola oru Rhaponticum отдельно. Что является синергией. Дополнительно, эффект комбинации половинной концентрации Rhodiola и половинной концентрации Rhaponticum был выше (1,6 раз больше), чем ожидалось. Дополнительно, эффект комбинации четверти концентрации Rhodiola и четверти концентрации Rhaponticum был выше (в 3,4 раза больше), чем ожидалось. В результате, эффект комбинации в 10 раз меньшей концентрации Rhodiola и 10 раз меньшей Rhaponticum был выше (в 5,4 раз больше), чем ожидалось. Эти результаты четко демонстрируют синергию комбинации экстрактов на стимуляцию синтеза протеина в дельтовидной мышце с последующим интенсивным упражнением на сопротивление при 500 мг/день, 250 мг/день и 100 мг/день комбинации с сотношением 50:50 (мас./мас).
[00303]
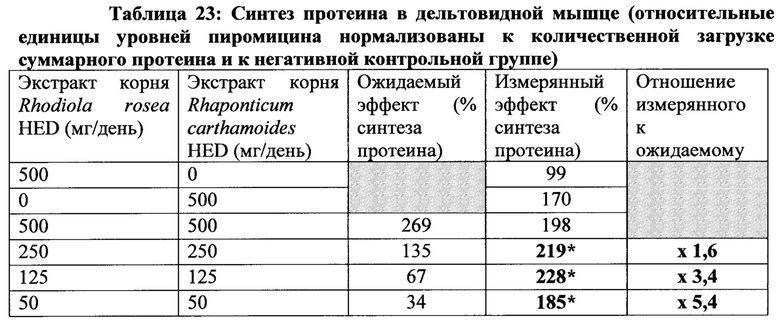
*: сильные неожиданные результаты с комбинацией экстракта корня Rhodiola rosea и экстракта корня Rhaponticum carthamoides, отношение 50:50 (мас./мас.)
[00304] Как проилюстрировано на Фиг. 37а, показанный вестерн блот бицепса восьми животных каждого лечения, и на Фиг. 37b, показано относительные единицы уровней пиромицина нормализованного к количественной загрузке общего протеина и негативномой контрольной группе, ни экстракт корня Rhaponticum carthamoides отдельно, ни экстракт корня Rhodiola rosea не были способны значительно стимулировать синтез протеина, но комбинация обоих экстрактов значительно стимулирует синтез протеина при уменьшающихся HED 1000 мг/день, 500 мг/день и 250 мг/день.
[00305] Комбинация экстрактов (HED: 1000 мг/день и 500 мг/день) была, очевидно, более активной относительно экстракта корня Rhodiola rosea отдельно, как показано на Фигуре 37d (показано относительные единицы уровней пиромицина нормализованные к количественной загрузке всего протеина, и Rhodiola группе). Комбинация экстрактов (HED: 1000 мг/день и 500 мг/день) была, очевидно, более активной относительно экстракта корня Rhaponticum carthamoides отдельно, как показано на Фигуре 37е (показано относительные единицы уровней пиромицина нормализованные к количественной загрузке всего протеина, и Rhaponticum группе). Кроме того, эффект комбинации экстрактов (для HED=1000 мг/день и 500 мг/день) также был существенно выше относительно сывороточных протеинов, как показано на Фиг. 37с (показано относительные единицы уровней пиромицина нормализованные к количественной загрузке всего протеина, и группе с сывороточным протеином). Таблица 24 (ниже) иллюстрирует разницу между результатами, полученными с применением разных доз комбинации по сранению с таковыми, которые можно было бы ожидать от экстракта корня Rhodiola rosea и экстракта корня Rhaponticum carthamoides по отдельности. Неожиданно, эффект стимулирования синтеза протеина в бицепсе комбинацией половинных концентраций корня Rhodiola rosea и корня Rhaponticum carthamoides показал эффект лучше, чем полные концентрации Rhodiola или Rhaponticum отдельно. Что является синергией. Дополнительно, эффект комбинации половины концентрации Rhodiola и половины концентрации Rhaponticum был выше (2,0 раз больше), чем ожидалось. Дополнительно, эффект комбинации четверти концентрации Rhodiola и четверти концентрации Rhaponticum был выше (в 2,5 раза больше), чем ожидалось. В результате, эффект комбинации в 10 раз меньшей концентрации Rhodiola и 10 раз меньшей Rhaponticum был выше (в 5,0 раз больше), чем ожидалось. Эти результаты четко демонстрируют синергию комбинации экстрактов на стимуляцию синтеза протеина в дельтовидной мышце с последующим интенсивным упражнением на сопротивление при 500 мг/день, 250 мг/день и 100 мг/день комбинации с сотношением 50:50 (мас./мас).
[00306]
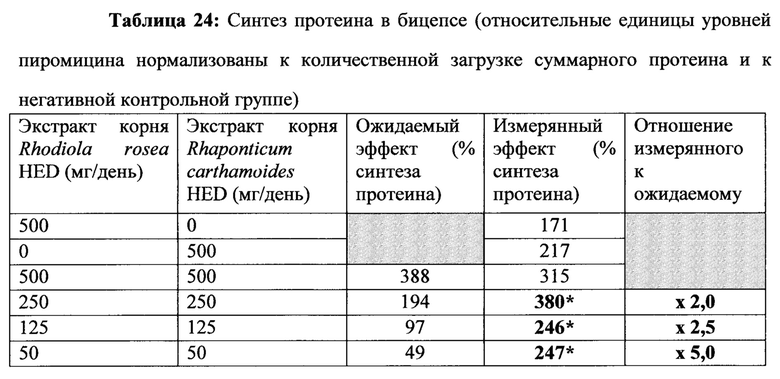
*: сильные неожиданные результаты с комбинацией экстракта корня Rhodiola rosea и экстракта корня Rhaponticum carthamoides, отношение 50:50 (мас./мас.)
[00307] Как проилюстрировано на Фиг. 38, показано относительные единицы уровней пиромицина нормализованные к количественной загрузке общего протеина и негативной контрольной группе для всех мышц в общем (FDP + дельтовидная мышца + бицепс) экстракты корня Rhaponticum carthamoides отдельно, но не экстракты корня Rhodiola rosea были способны значительно стимулировать синтез протеина, но в меньшей степени, чем любые концентрации (с уменьшением дозы) комбинации обоих экстрактов. Комбинация экстрактов была, очевидно, более активной относительно экстракта корня Rhodiola rosea отдельно, для четырех уменьшающихся тестируемых концентраций (от HED=1000 мг/день до 100 мг/день) и была значительно активнее, чем экстракт корня Rhaponticum carthamoides отдельно при HED=1000 мг/день и 500 мг/день. Более того, все тестированные дозы комбинации экстрактов (от HED=1000 мг/день до 100 мг/день) были значительно активнее по отношению к сыроваточным протеинам.
[00308] Таблица 25 (ниже) иллюстрирует разницу между результатами, полученными с применением разных доз комбинации по сранению с таковыми, которые можно было бы ожидать от экстракта корня Rhodiola rosea и экстракта корня Rhaponticum carthamoides по отдельности. Неожиданно, эффект стимулирования синтеза протеина во всех мышцах комбинацией половинных концентраций корня Rhodiola rosea и корня Rhaponticum carthamoides показал эффект лучше, чем полные концентрации Rhodiola oru Rhaponticum отдельно. Что является синергией. Дополнительно, эффект комбинации половины концентрации Rhodiola и половины концентрации Rhaponticum был выше (1,8 раз больше), чем ожидалось. Дополнительно, эффект комбинации четверти концентрации Rhodiola и четверти концентрации Rhaponticum был выше (в 3,0 раза больше), чем ожидалось. В результате, эффект комбинации в 10 раз меньшей концентрации Rhodiola и 10 раз меньшей Rhaponticum был выше (в 5,4 раз больше), чем ожидалось. Эти результаты четко демонстрируют синергию комбинации экстрактов на стимуляцию синтеза протеина во всех мышцах (FDP + дельтовидной мышце + бицепсе) с последующим точечным упражнением на сопротивление при 500 мг/день, 250 мг/день и 100 мг/день комбинации с сотношением 50:50 (мас./мас).
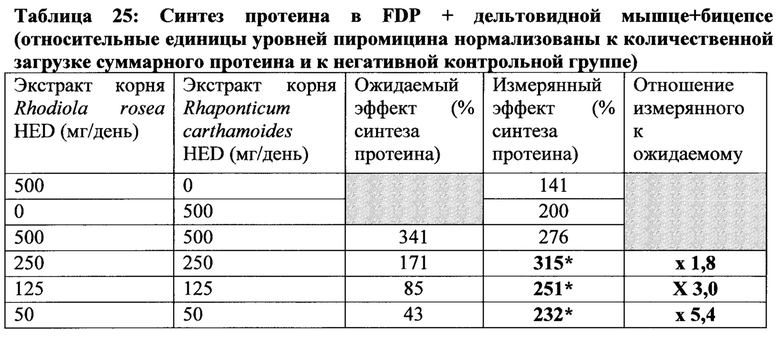
*: сильные неожидаемые результаты с комбинацией экстракта корня Rhodiola rosea и экстракта корня Rhaponticum carthamoides, отношение 50:50 (мас./мас.)
[00309] Описанные варианты реализации изобретения восприимчивы к различным модификациям и альтернативным формам, и их конкретные примеры продемонстрированы в качестве примера на графических материалах и подробно описаны в данном документе. Однако следует понимать, что описанные варианты реализации изобретения не должны ограничиваться конкретными раскрытыми формами или способами, но, наоборот, настоящее раскрытие охватывает все модификации, эквиваленты и альтернативы.
Ссылки
Goodman СА, Hornberger ТА. Measuring protein synthesis with SUnSET: a valid alternative to traditional techniques? Exercise and sport sciences reviews. 2013; 41(2): 107-115. doi: 10,1097/JES, 0b013e3182798a95, включена путем ссылки во всей своей полноте в данный документ.
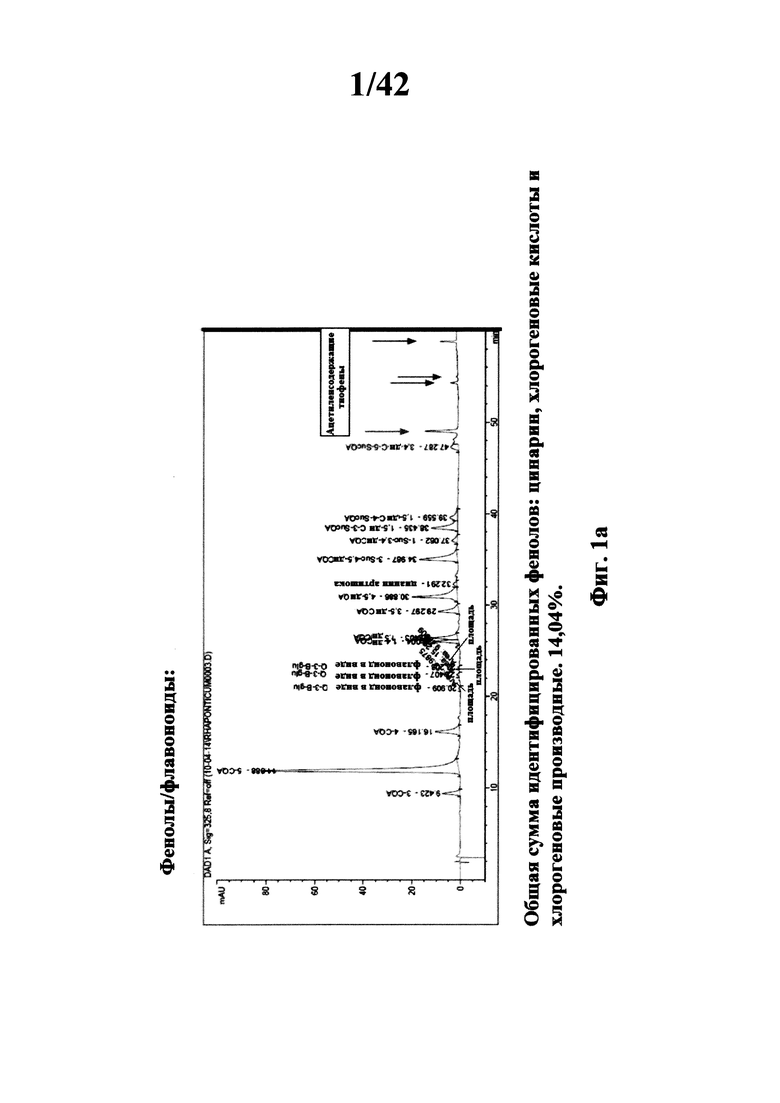
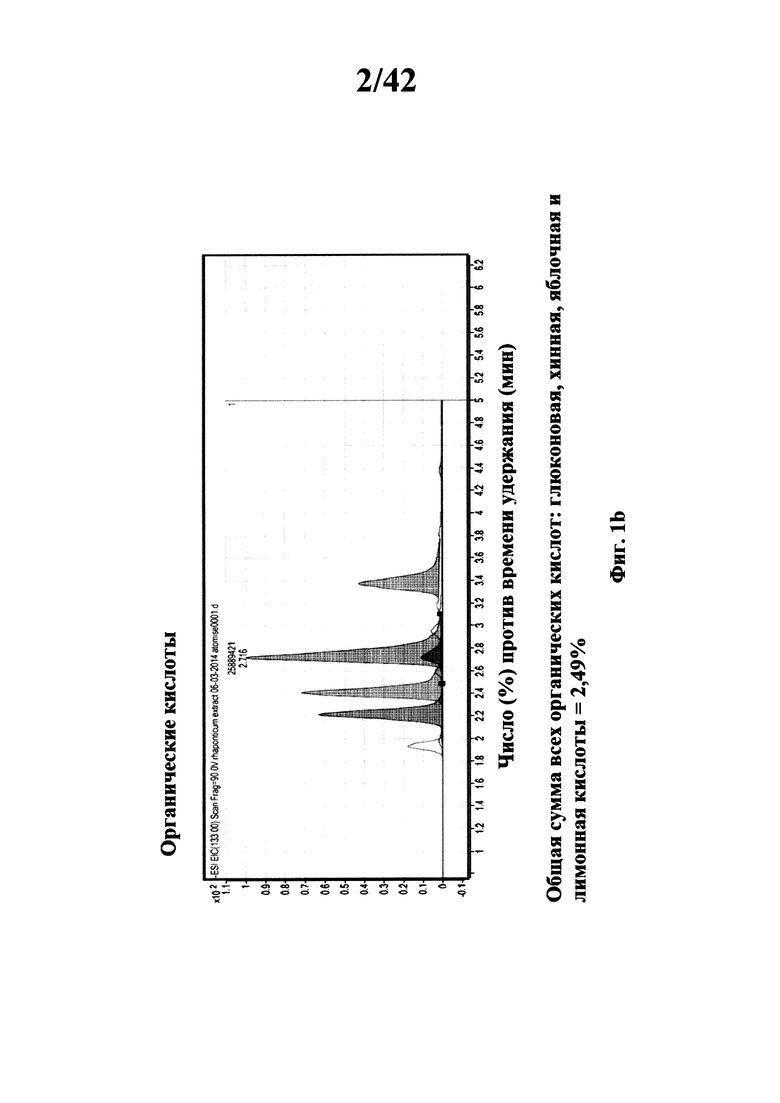
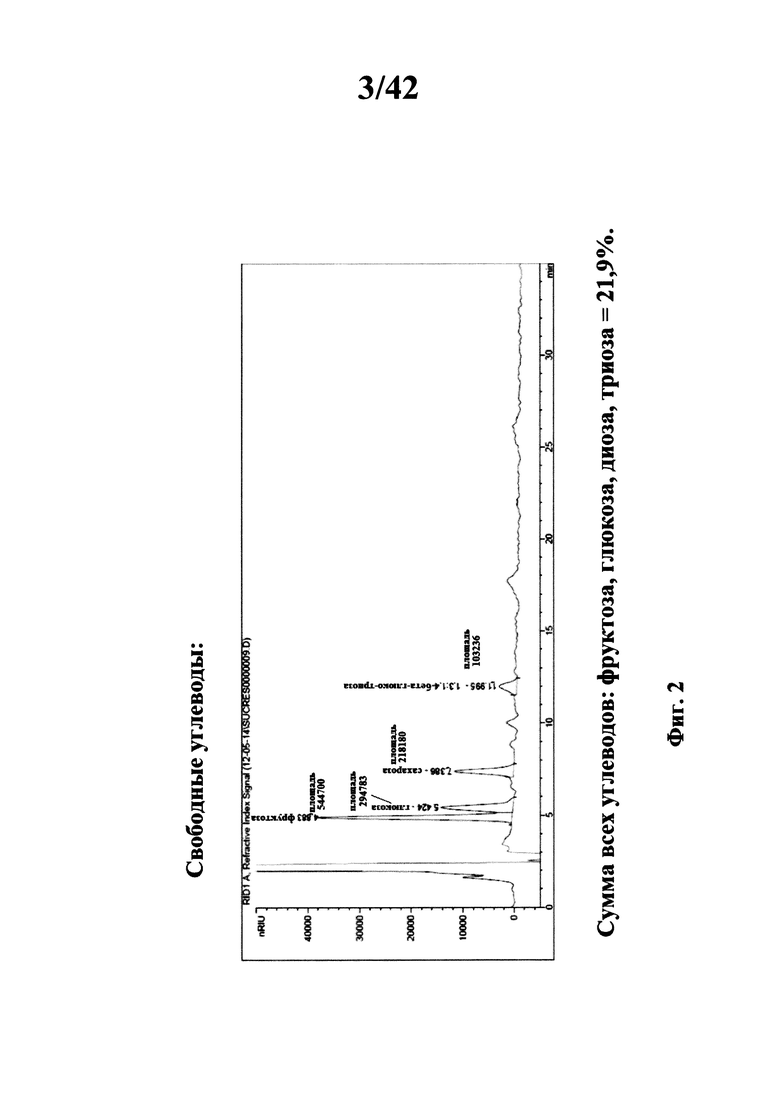
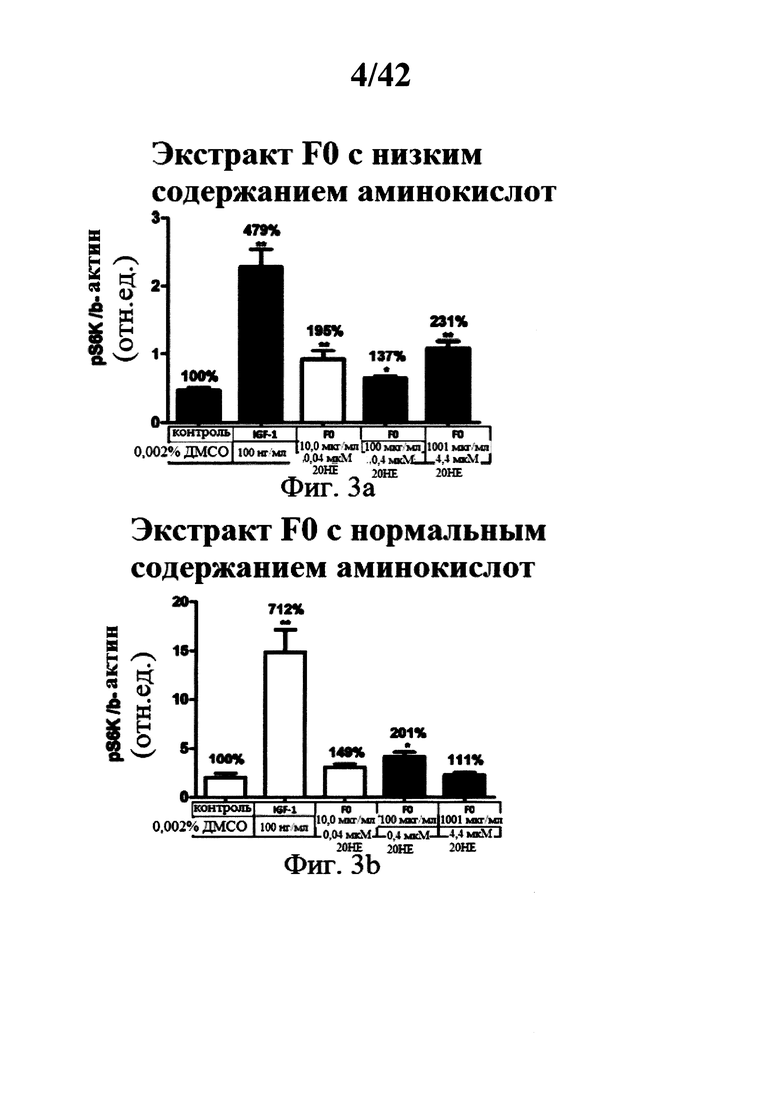
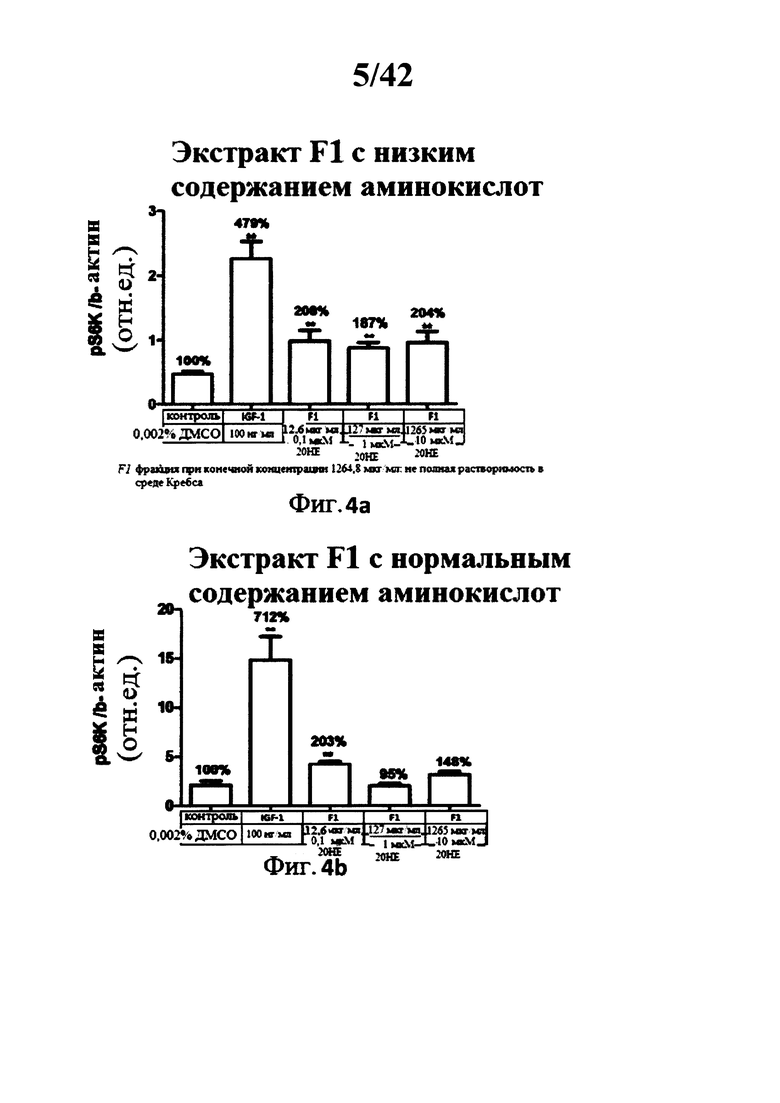
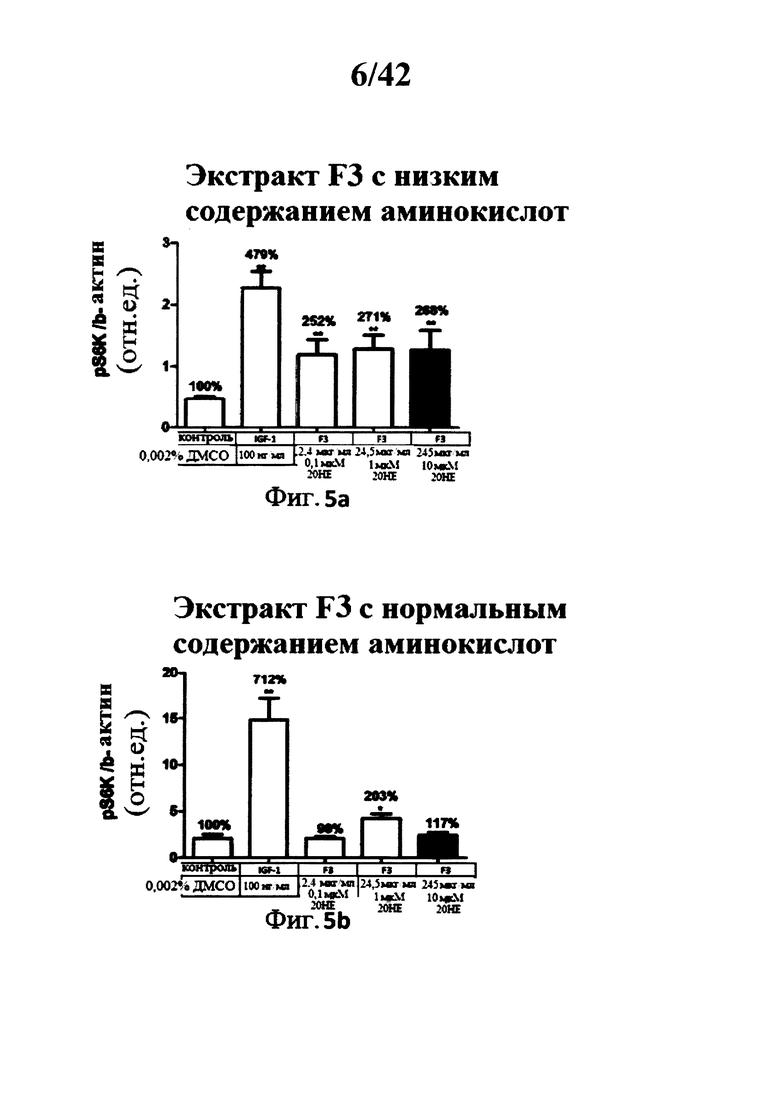
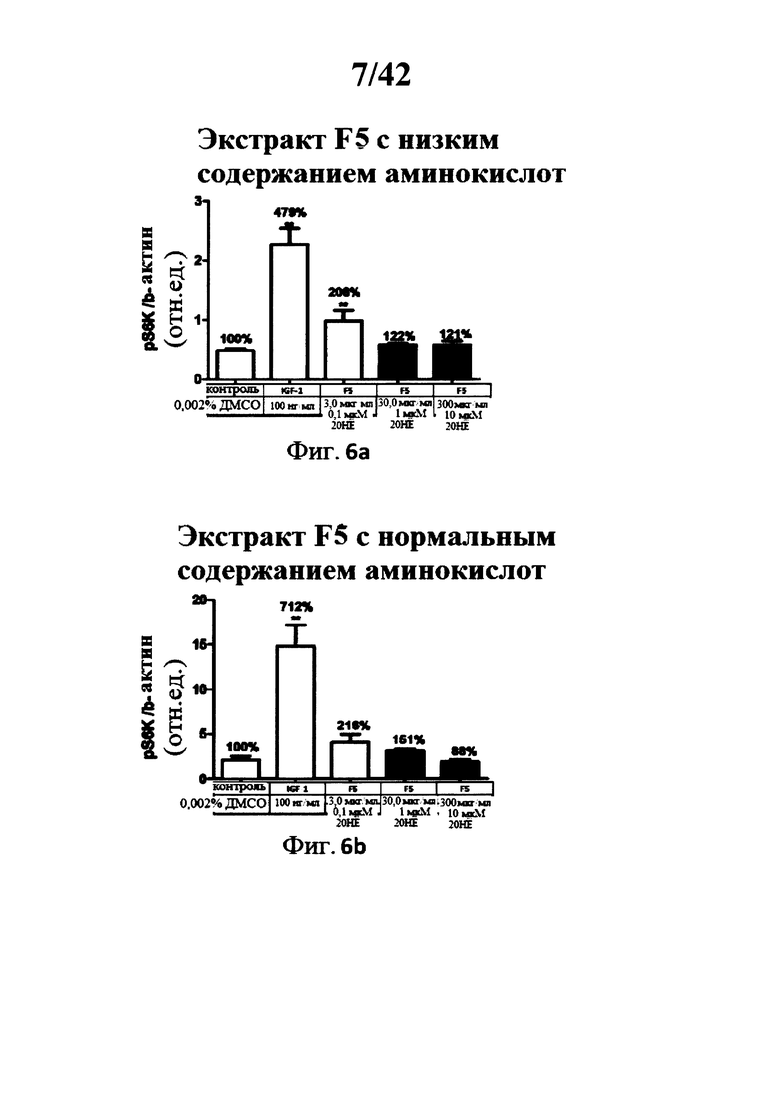
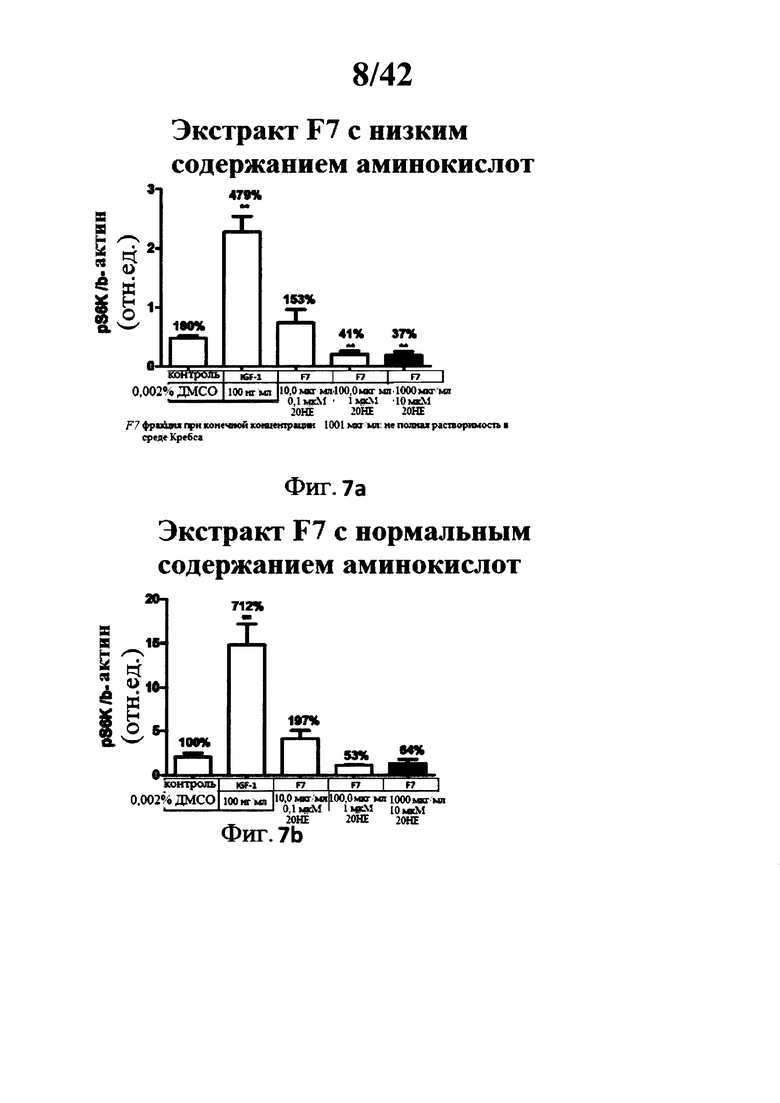
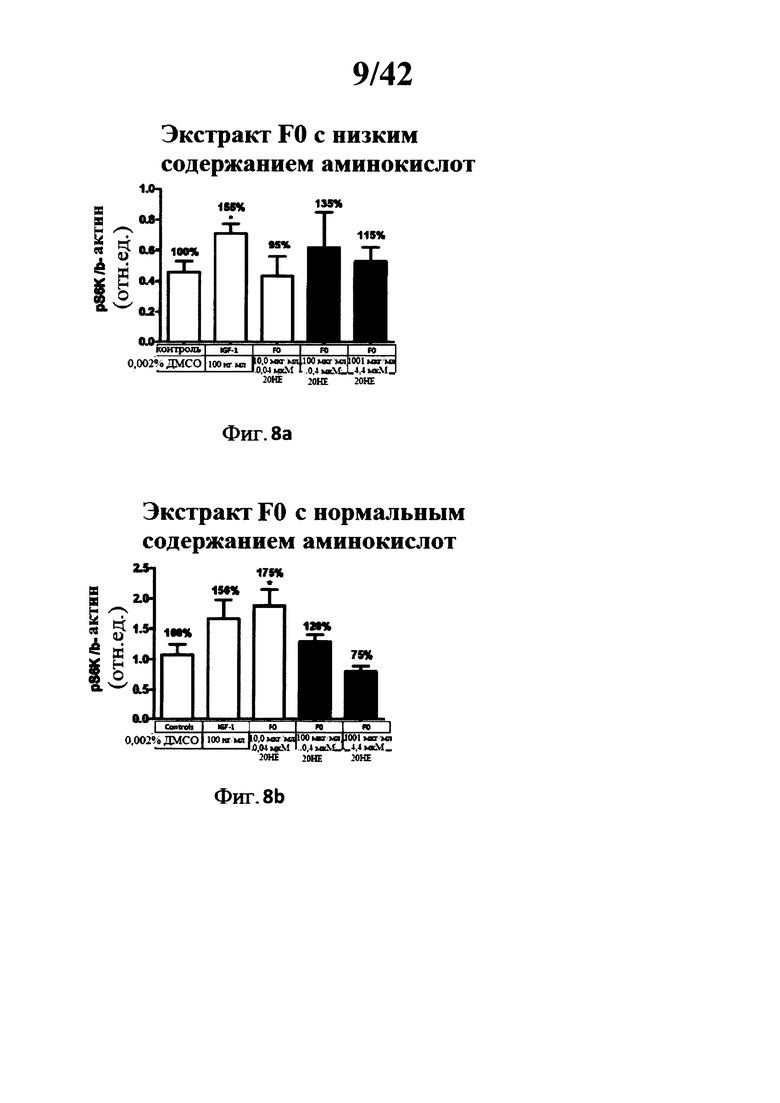
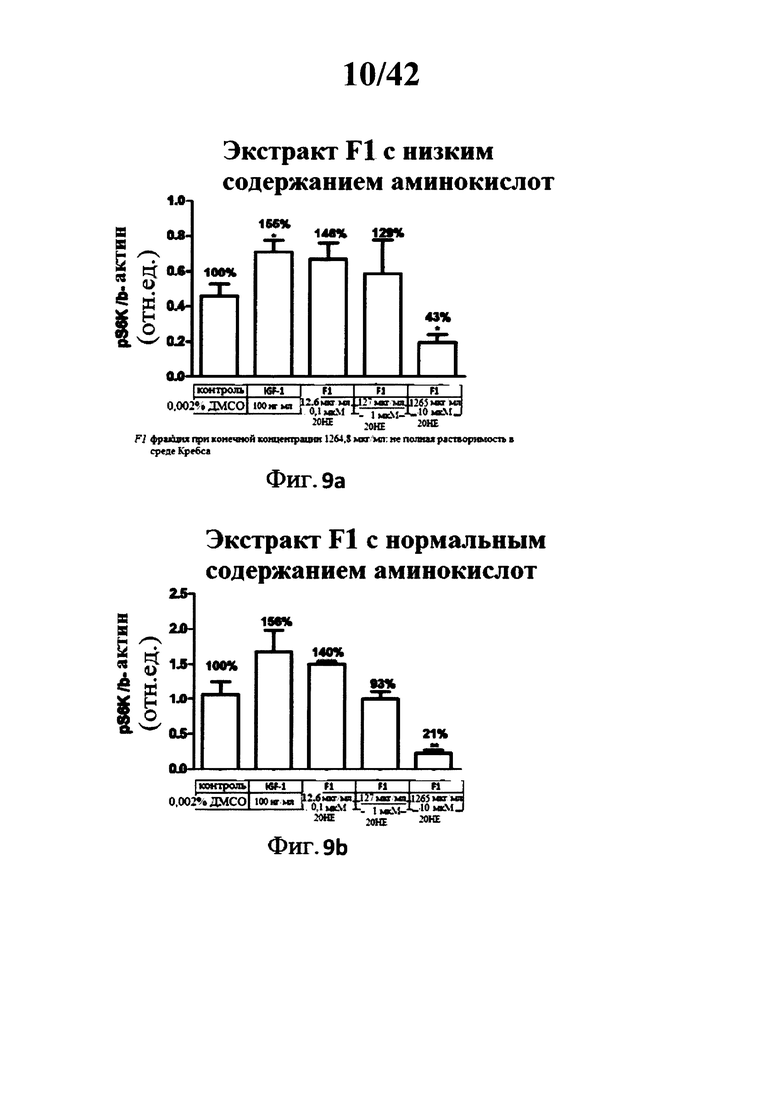
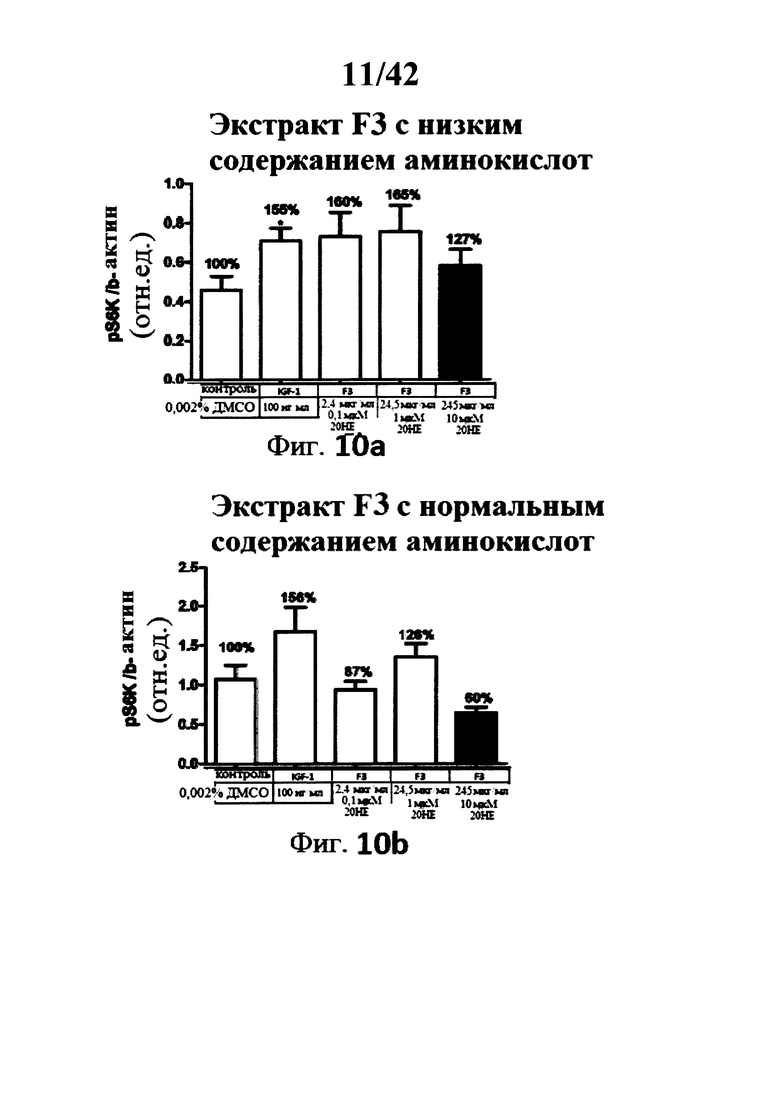
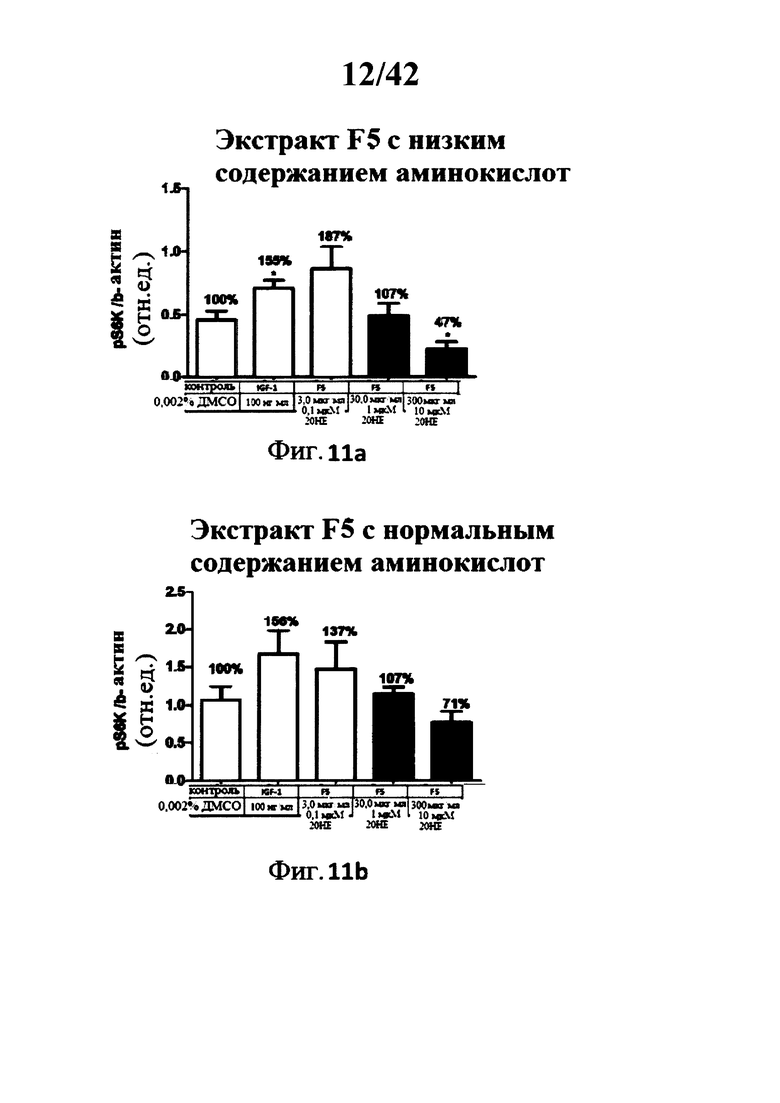
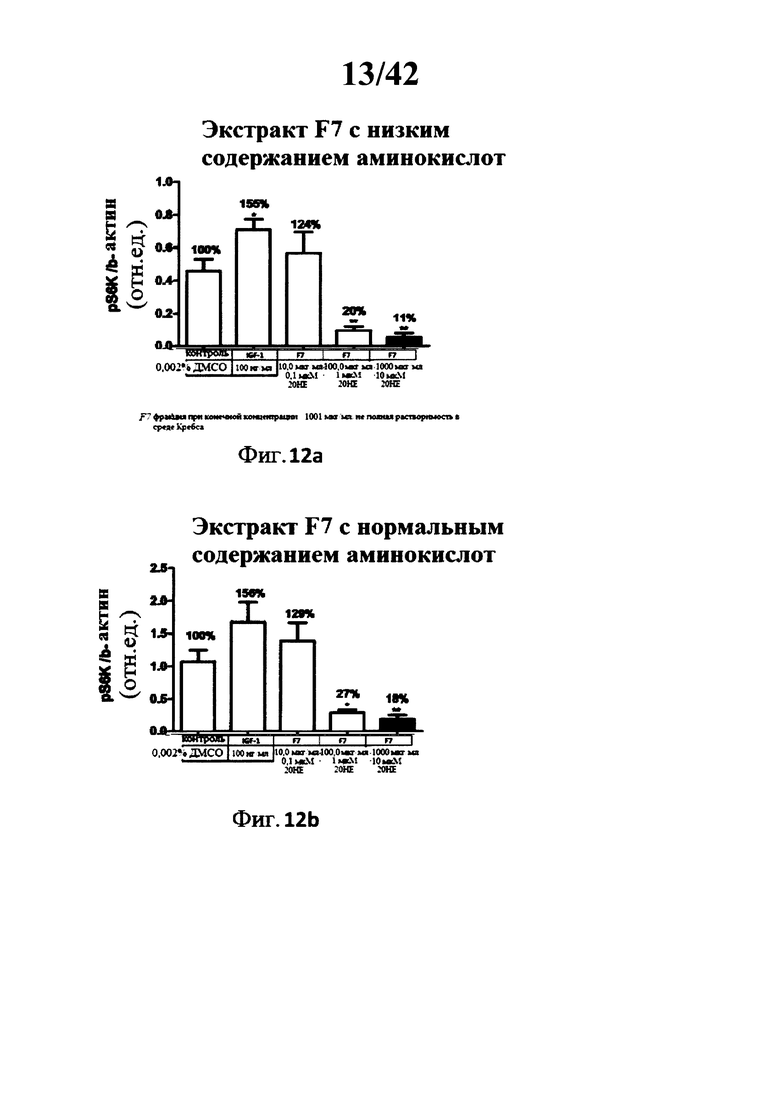

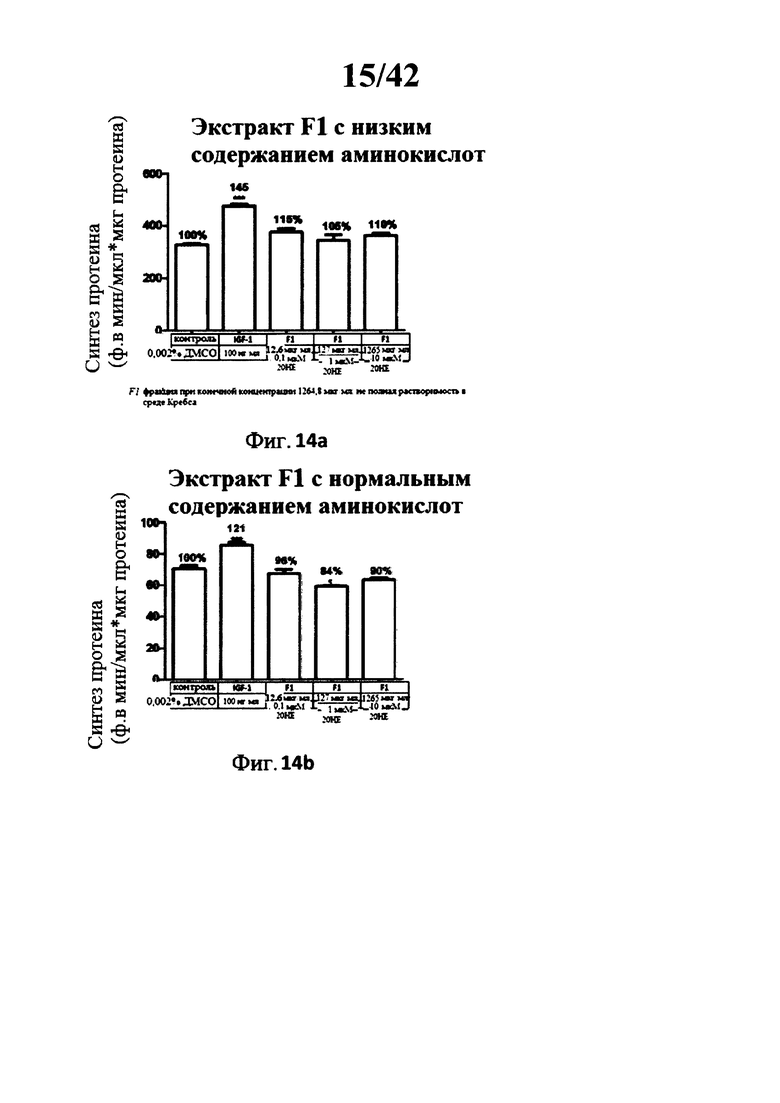
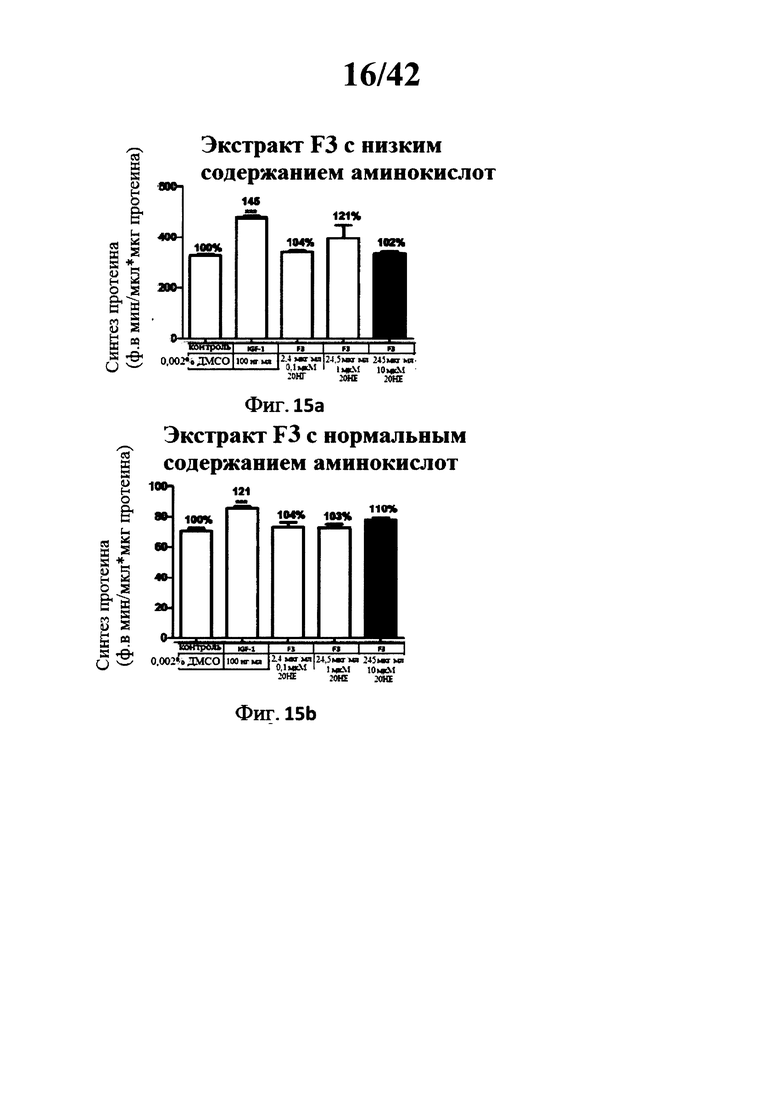
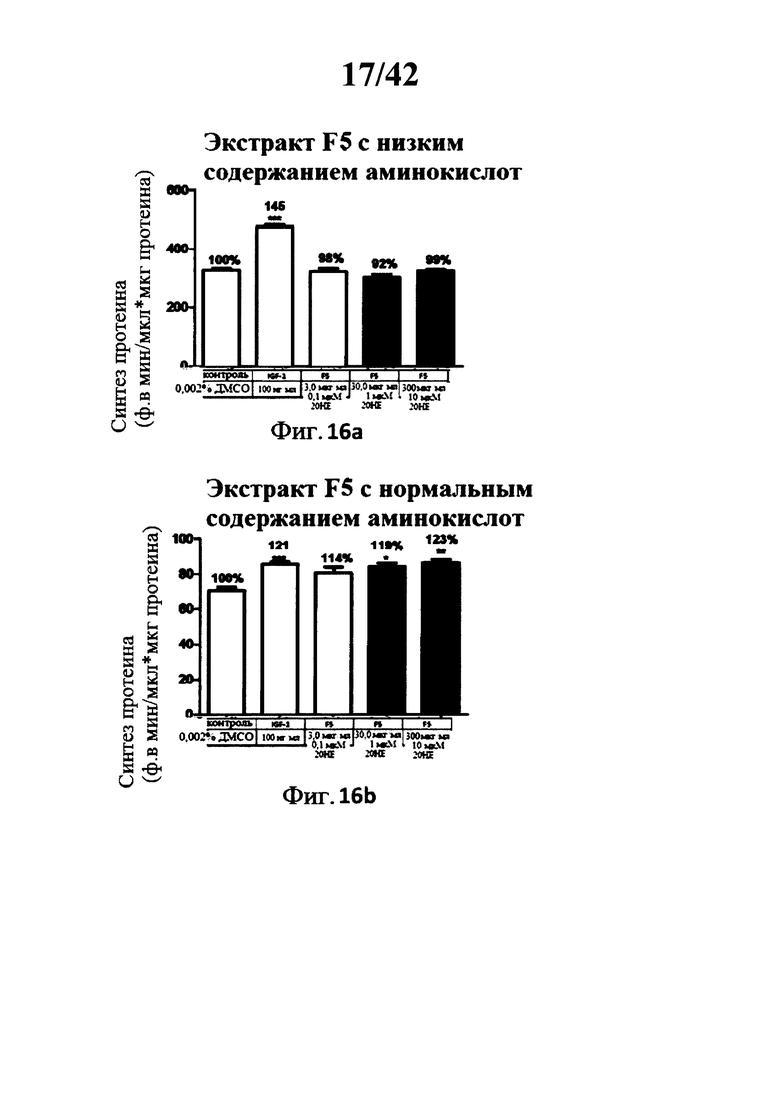
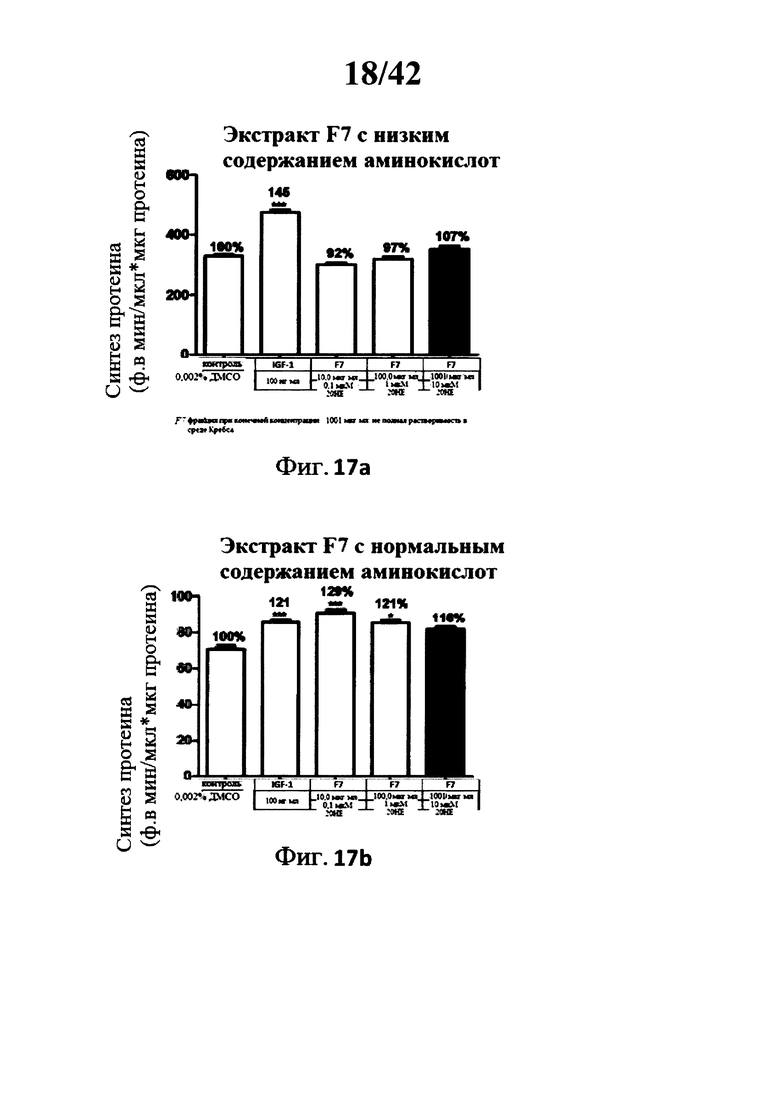
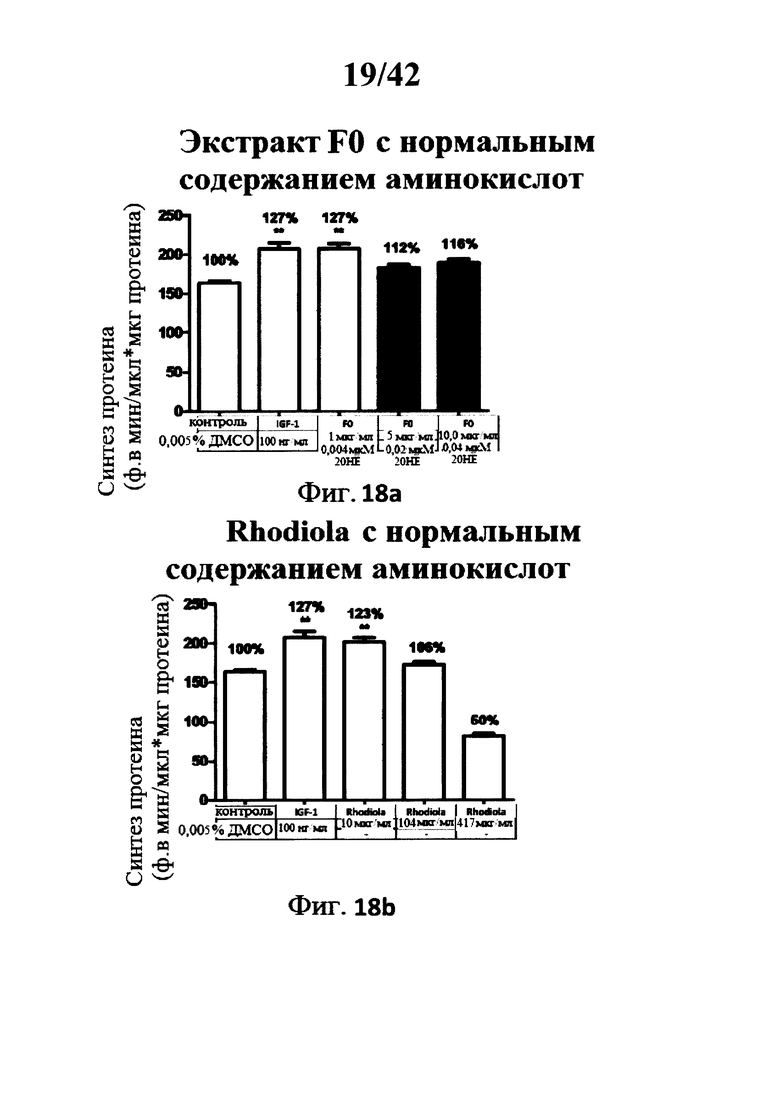
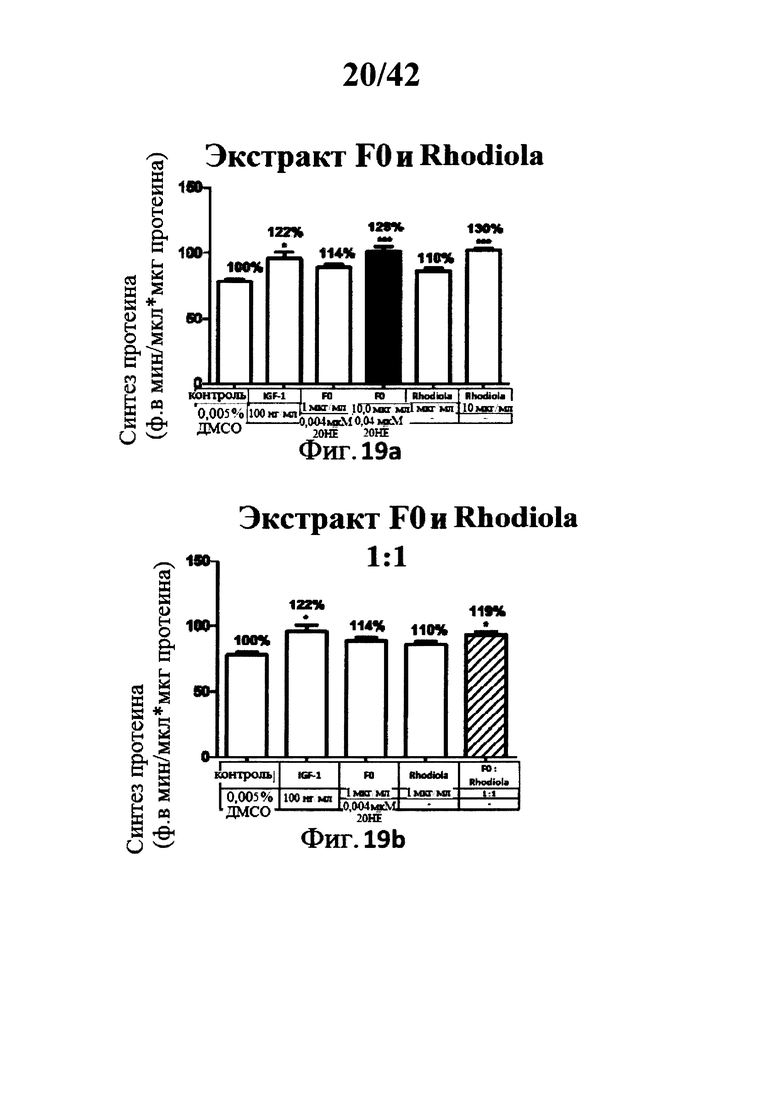

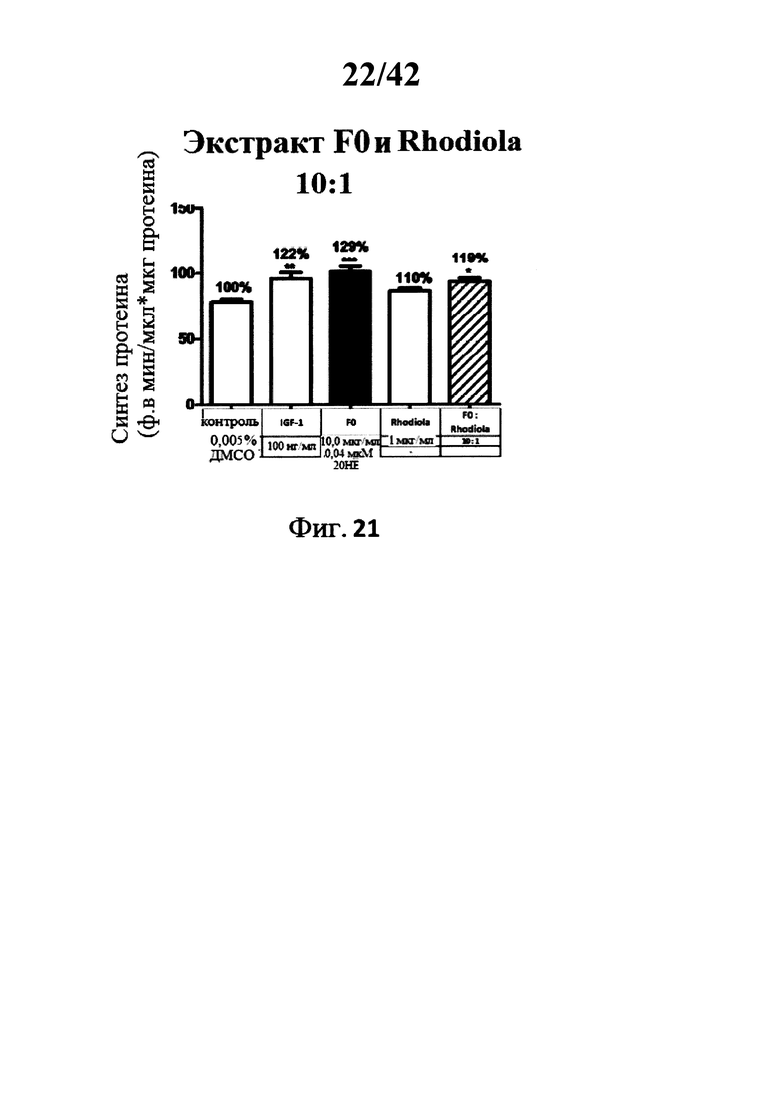
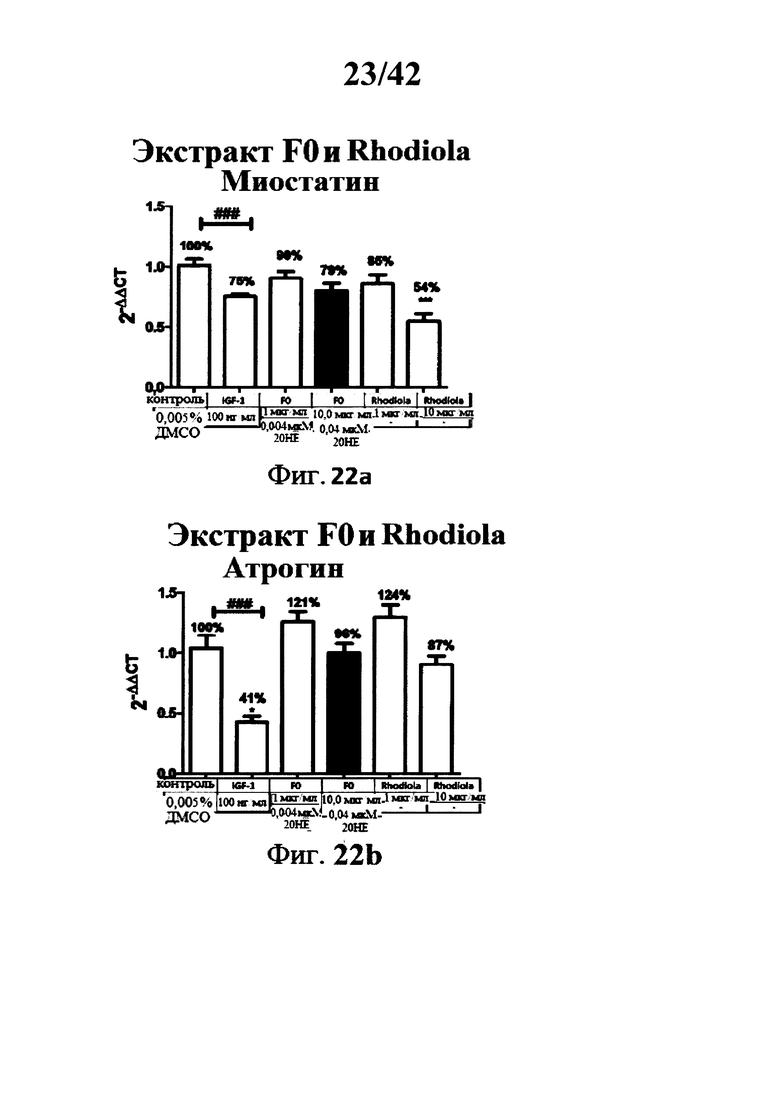
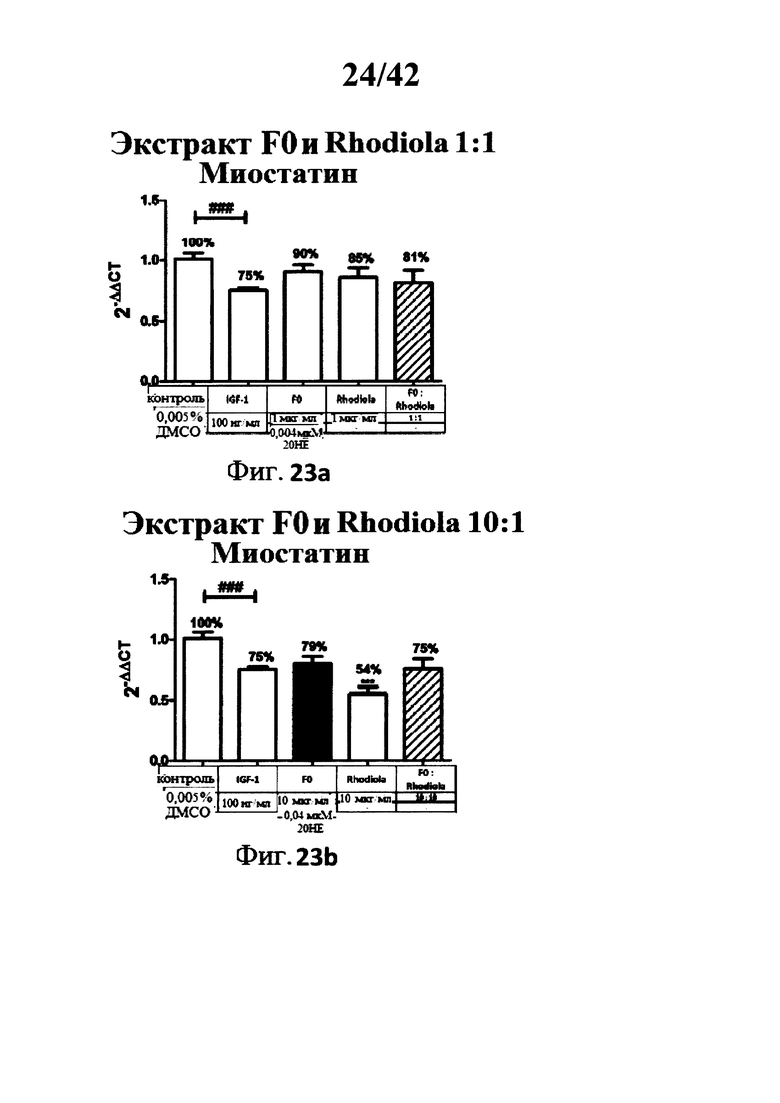
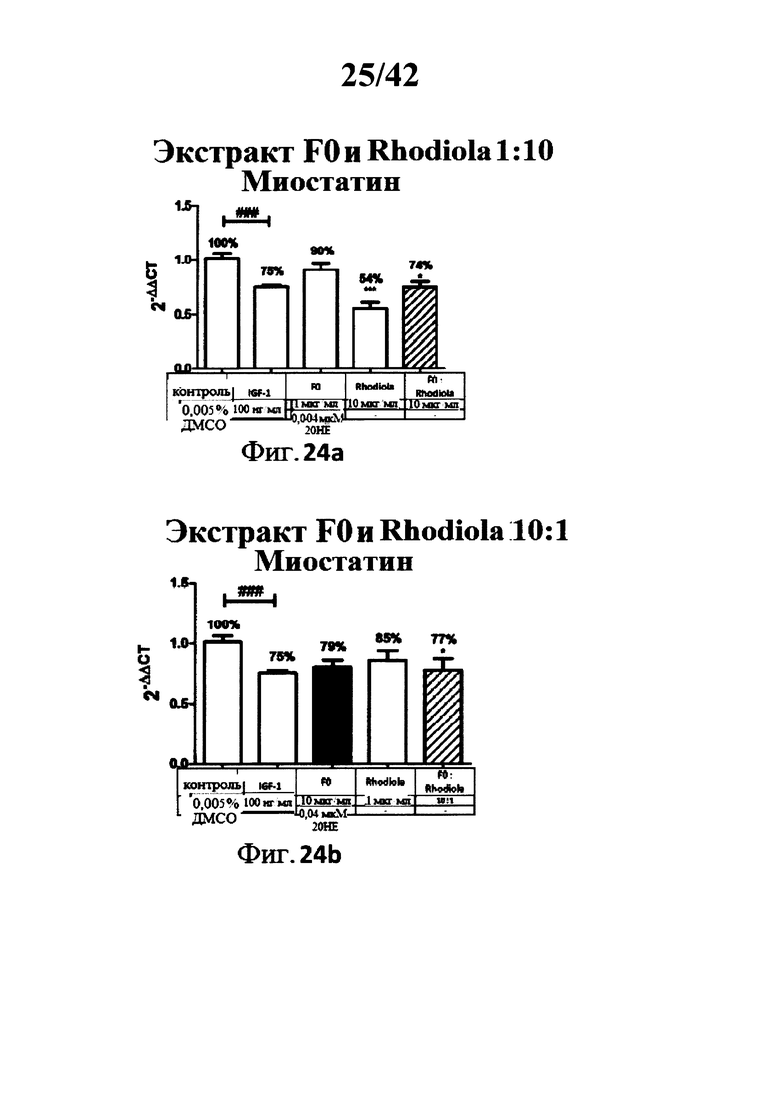
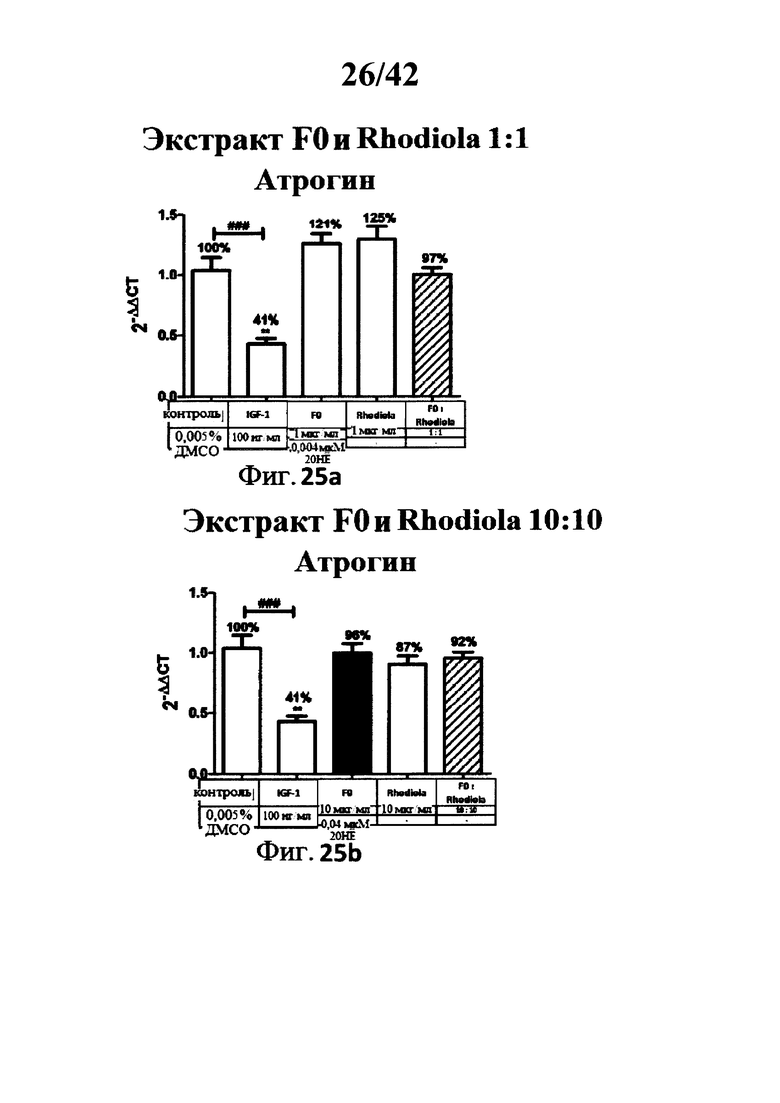
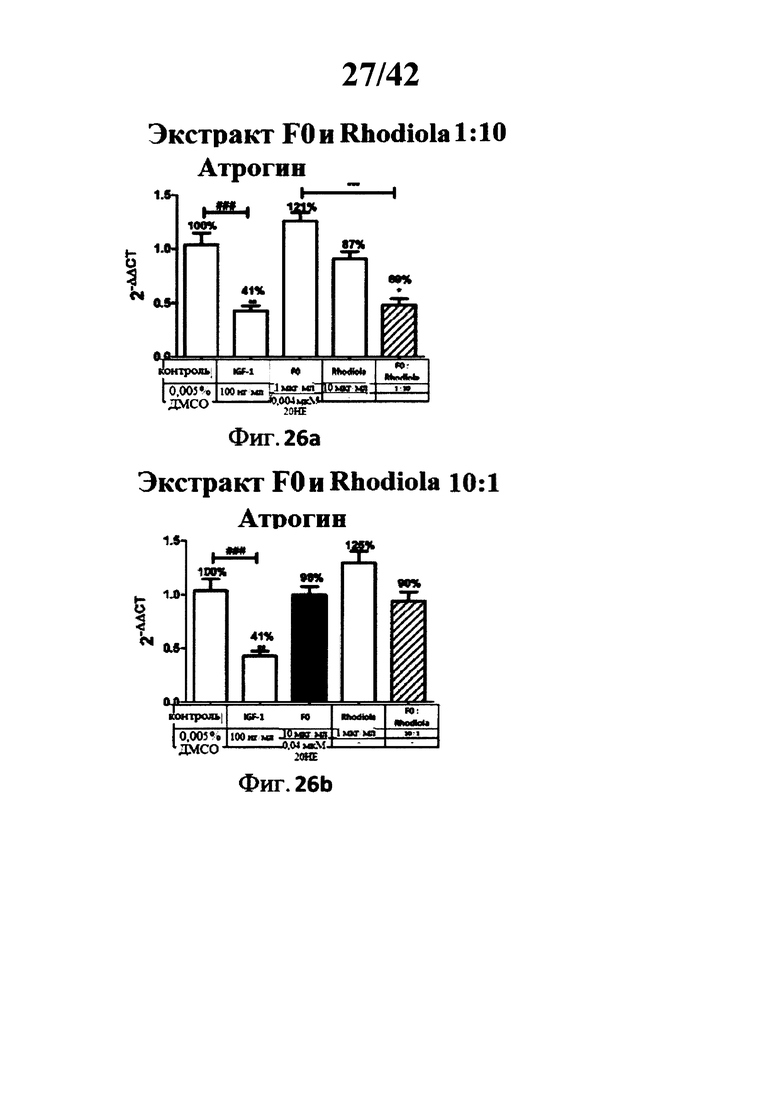
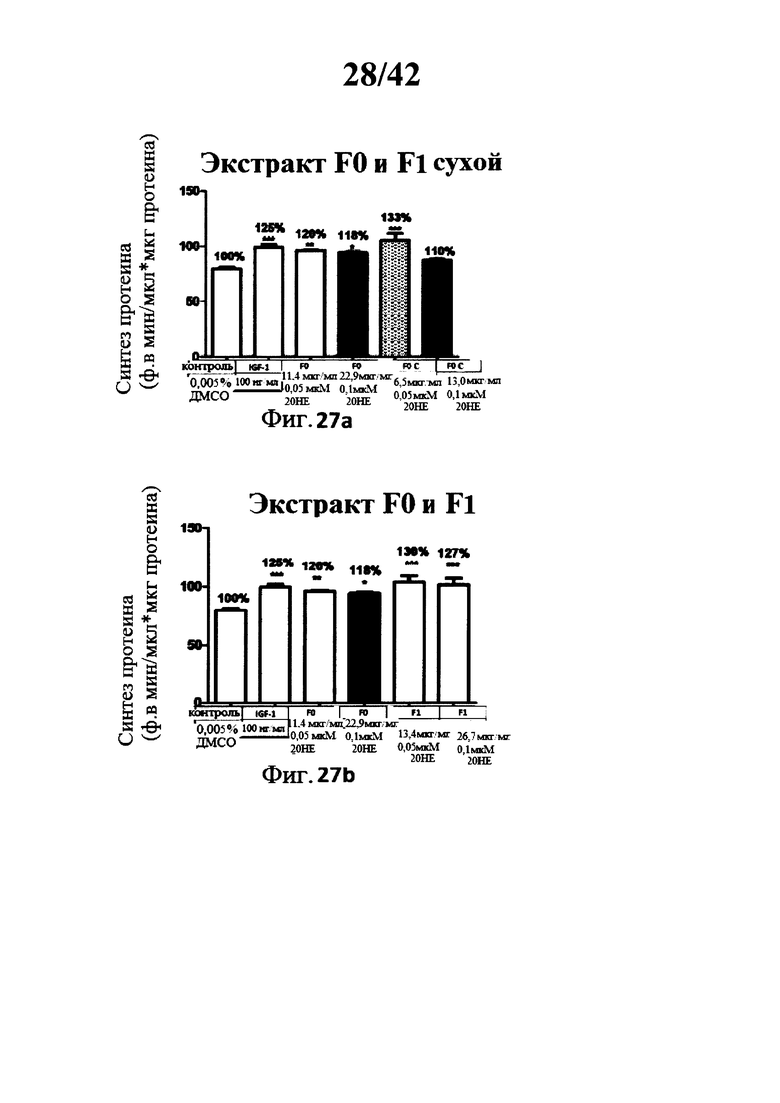
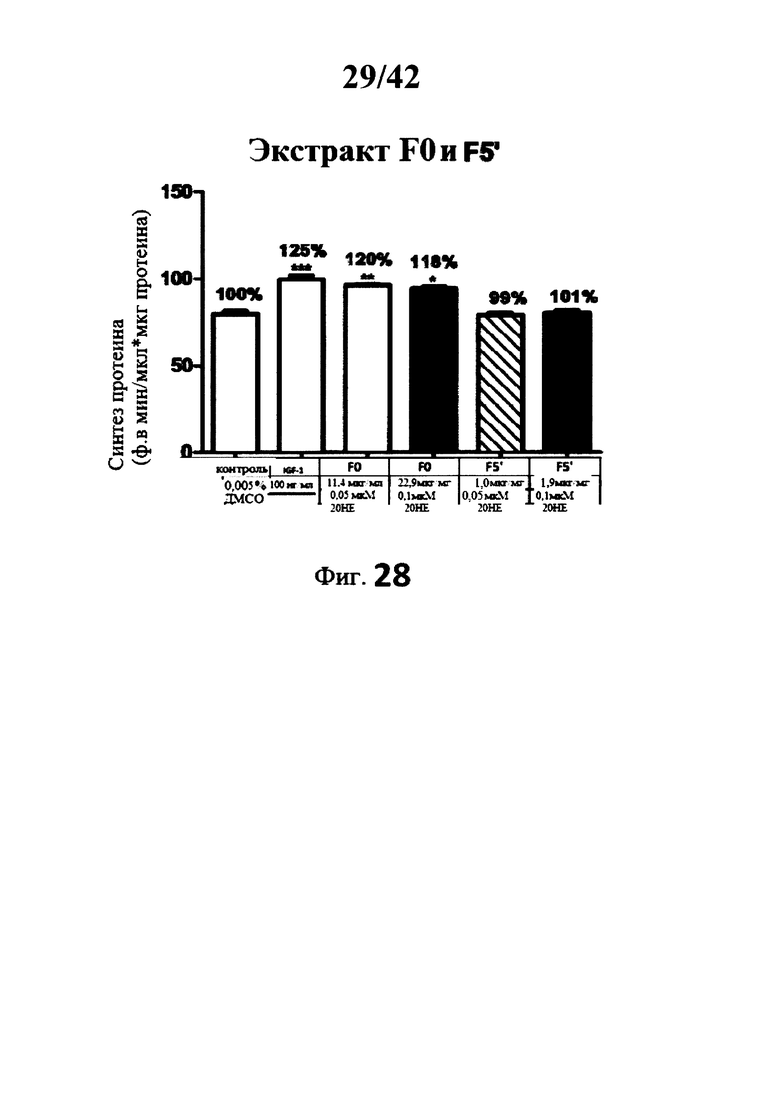

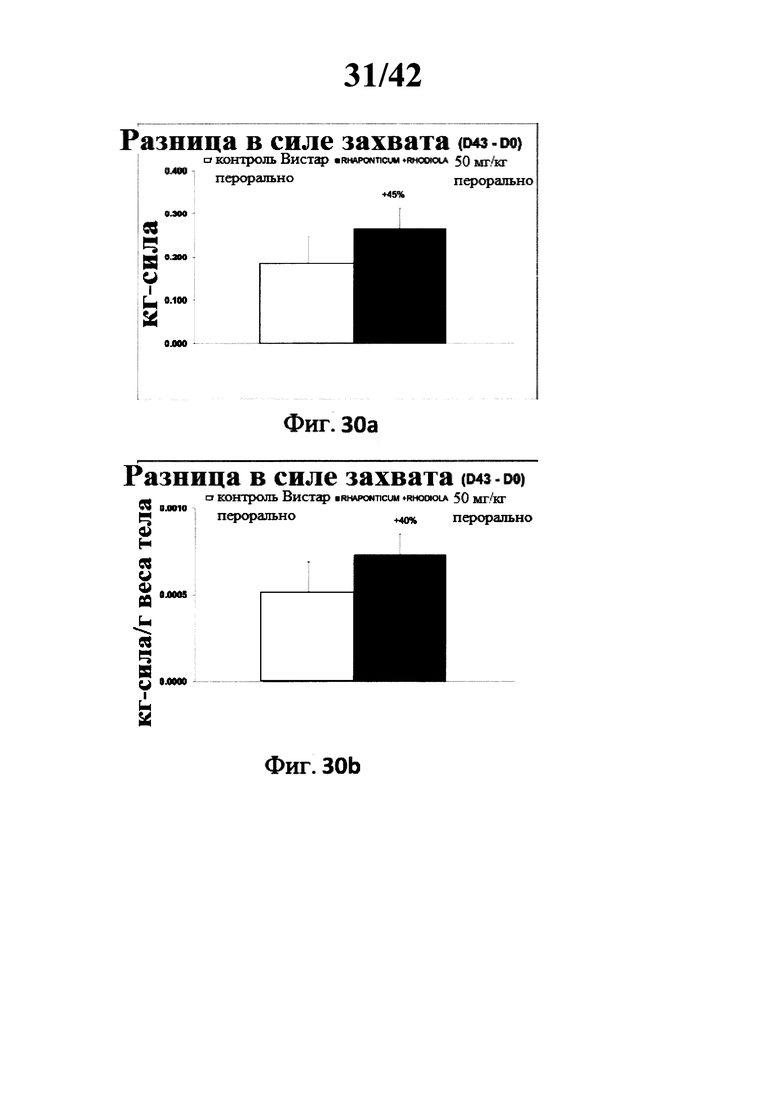
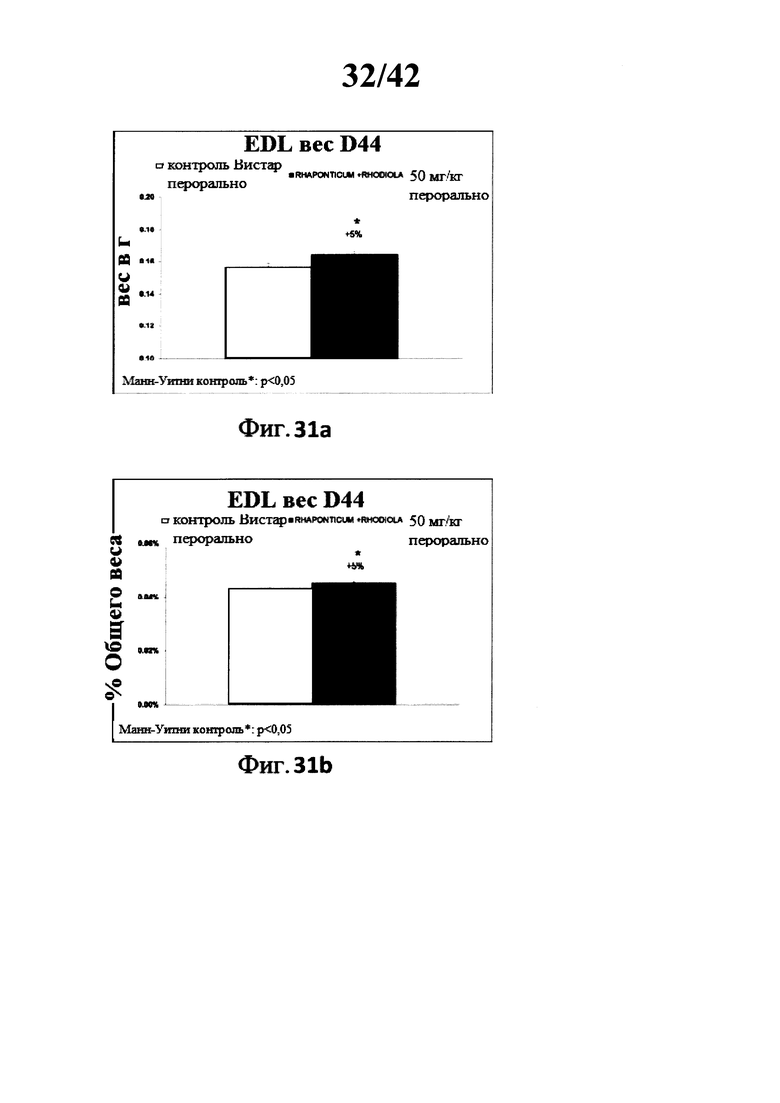
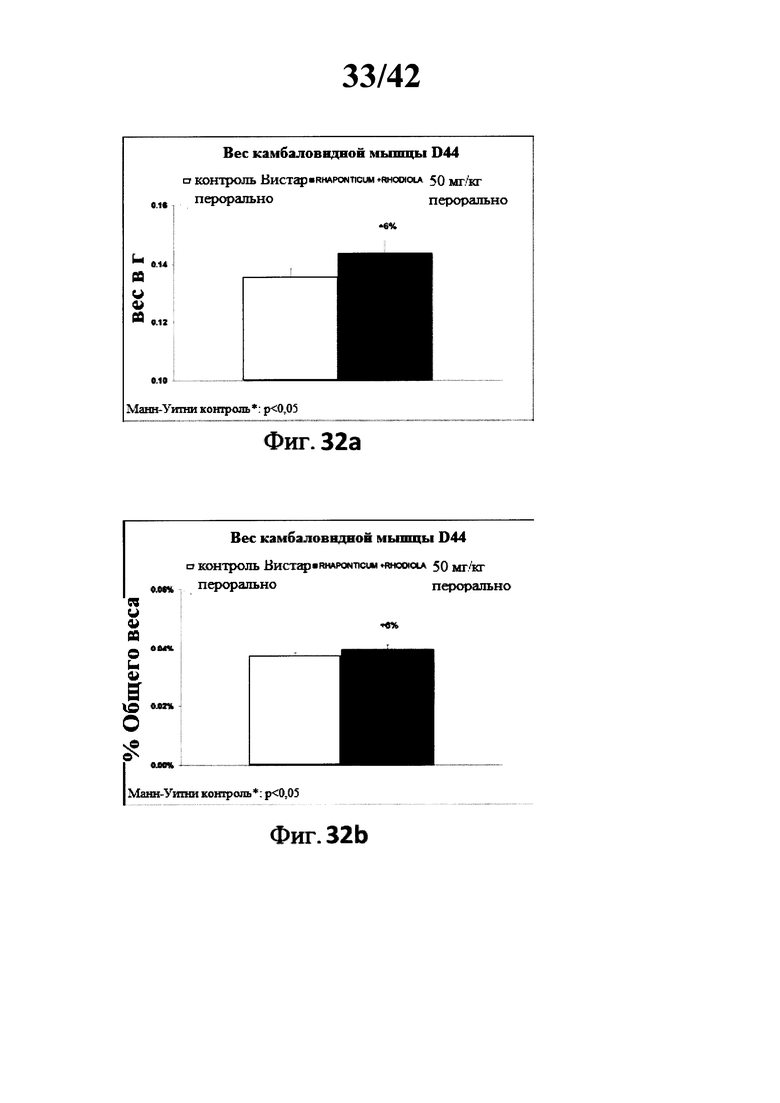
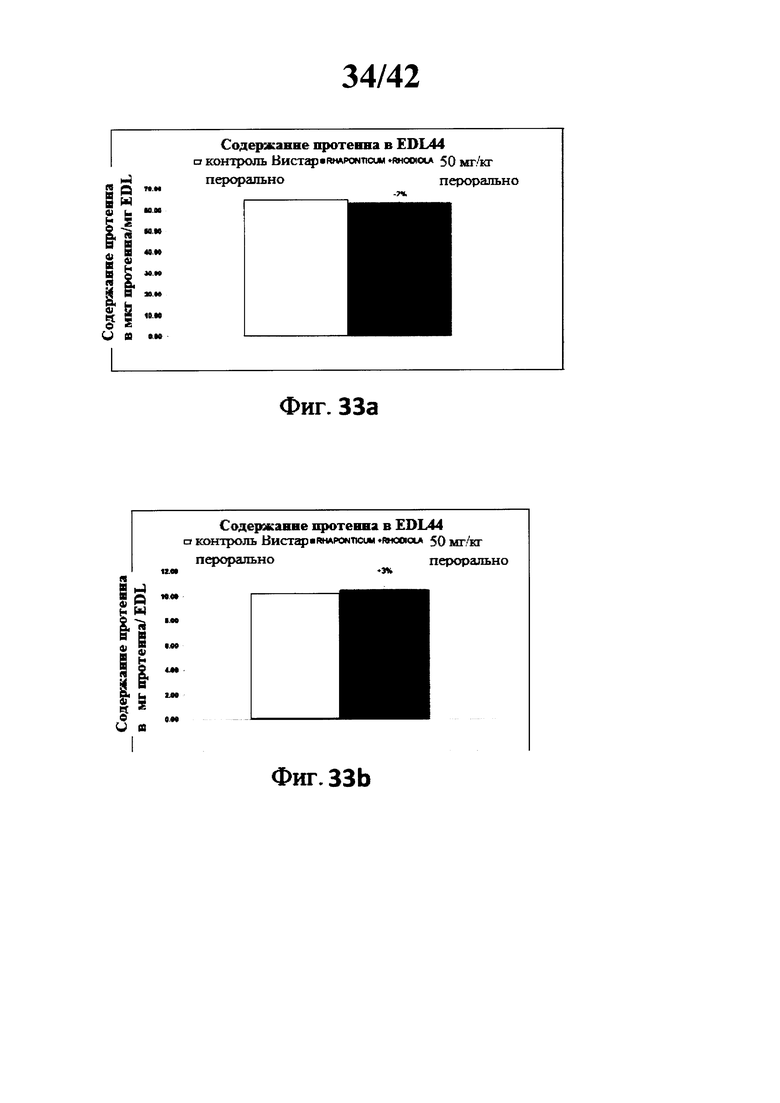
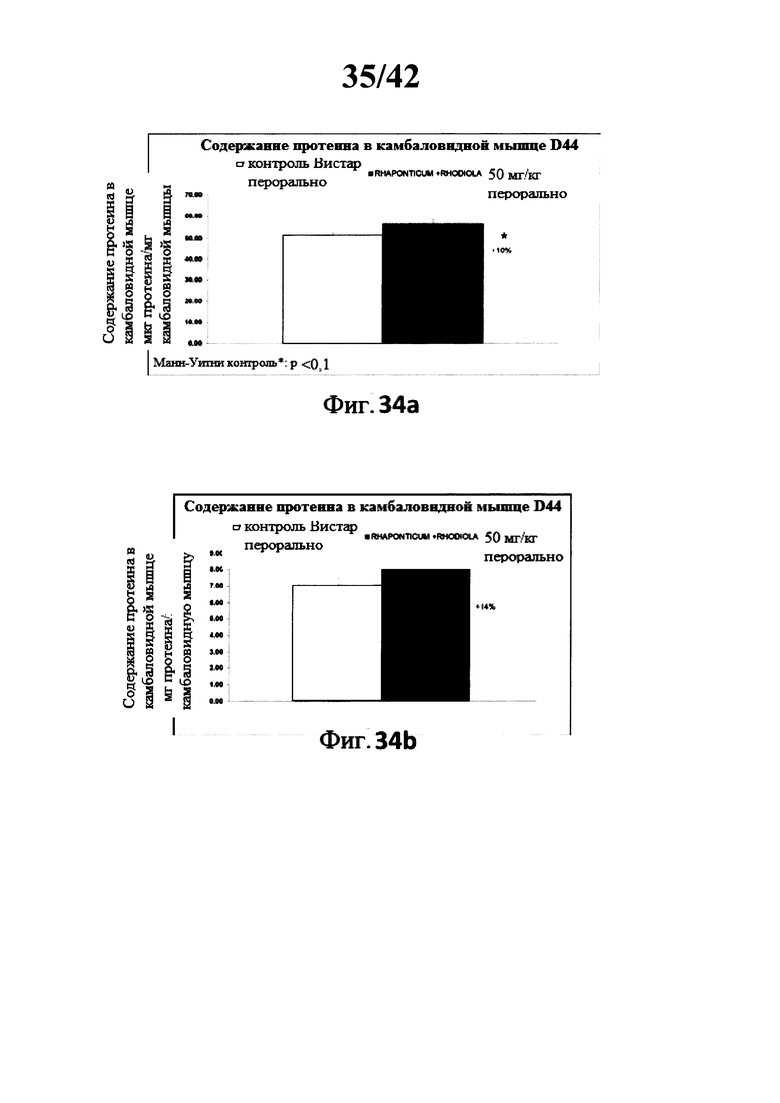
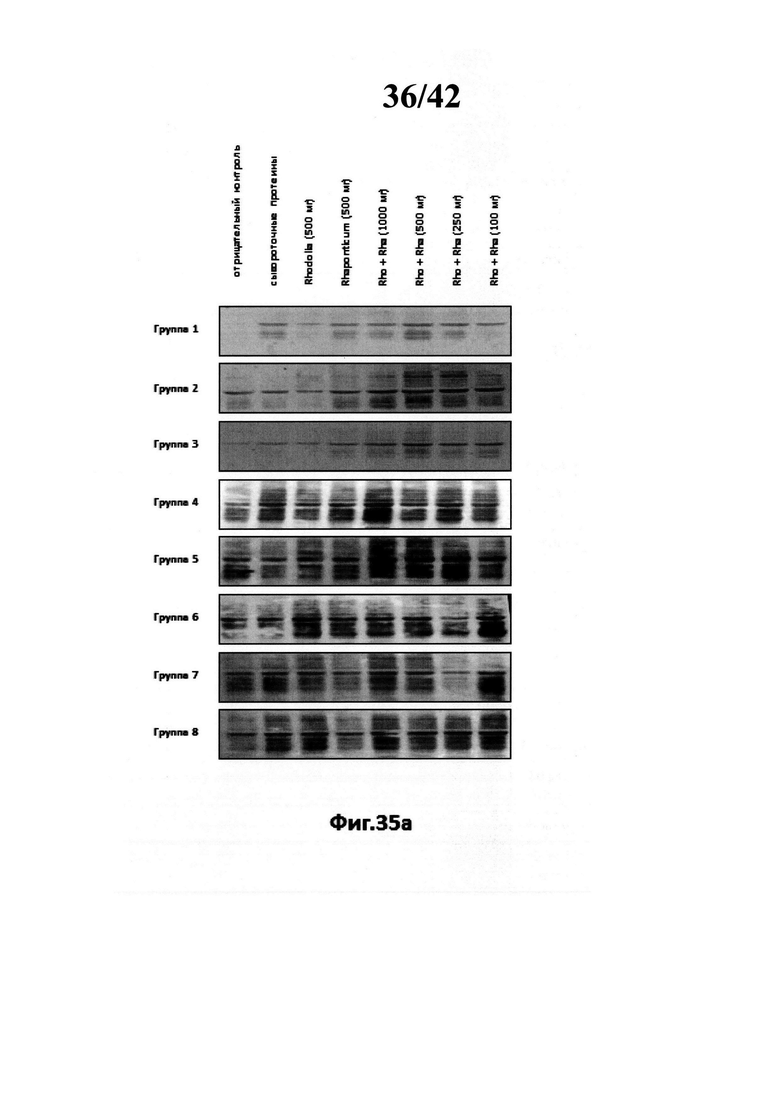
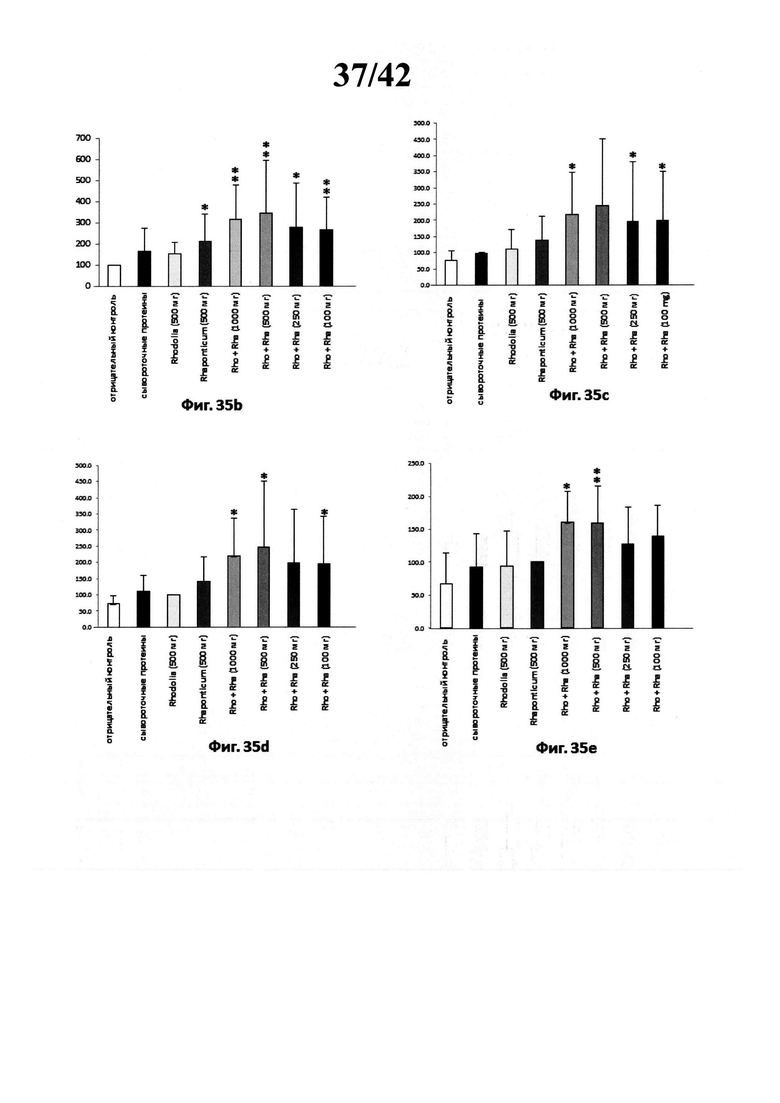
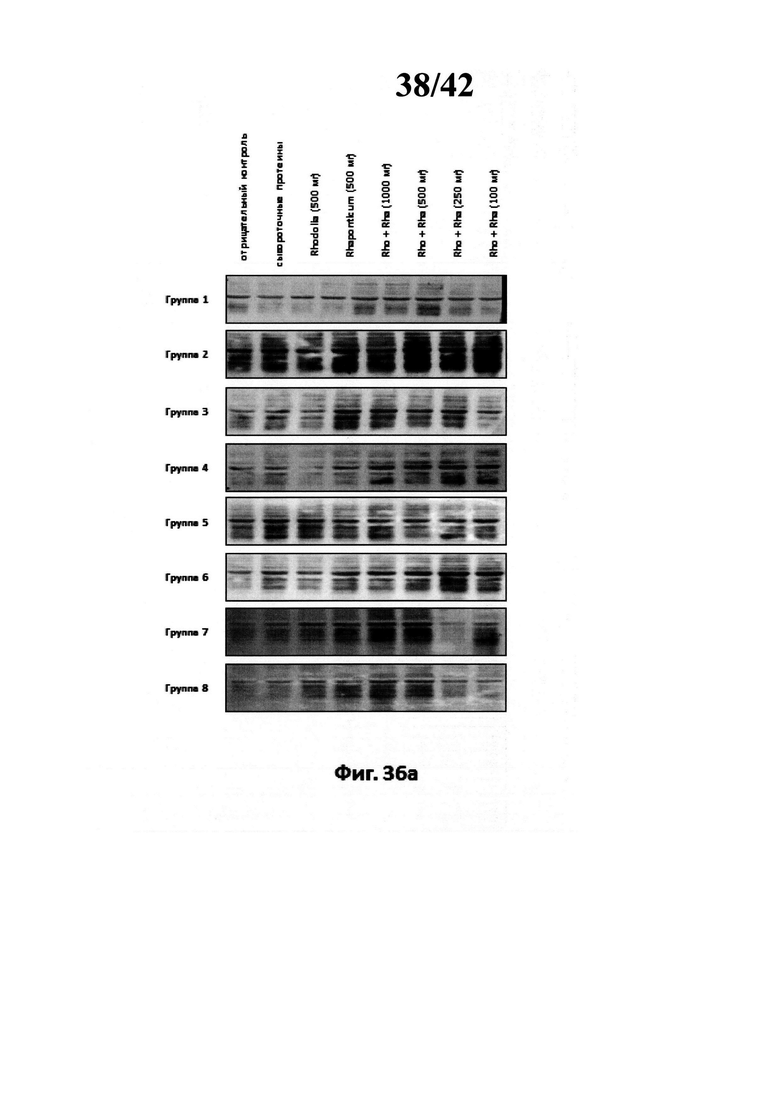
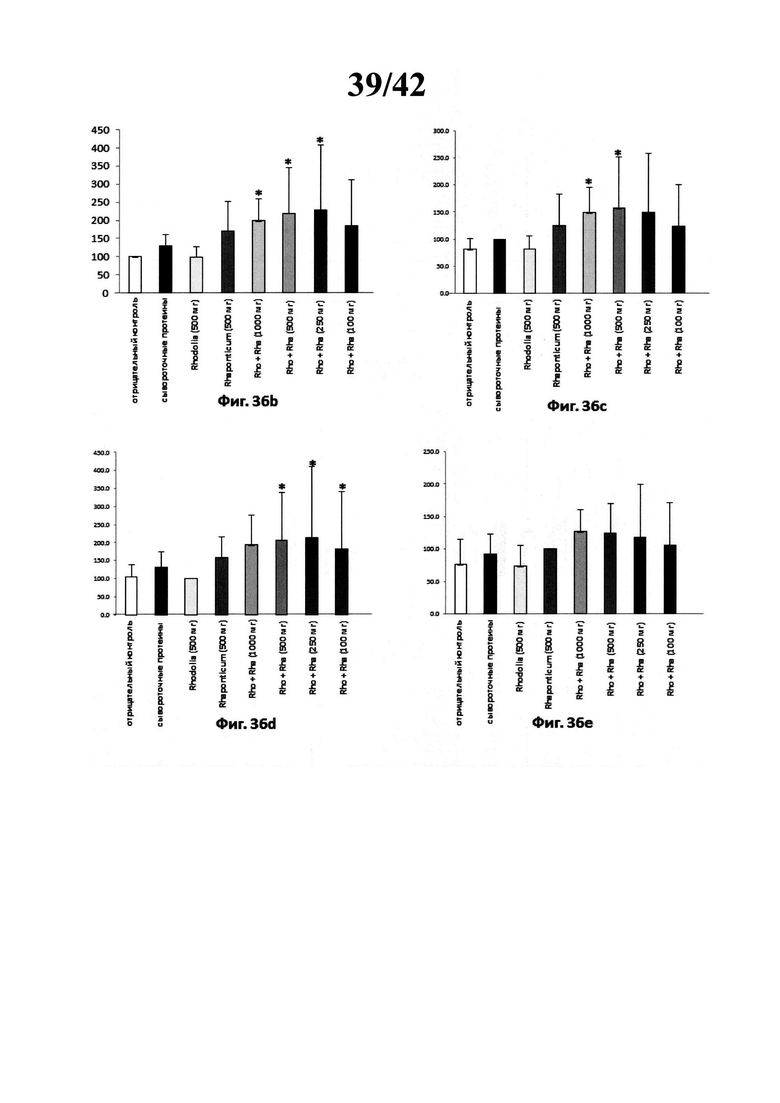
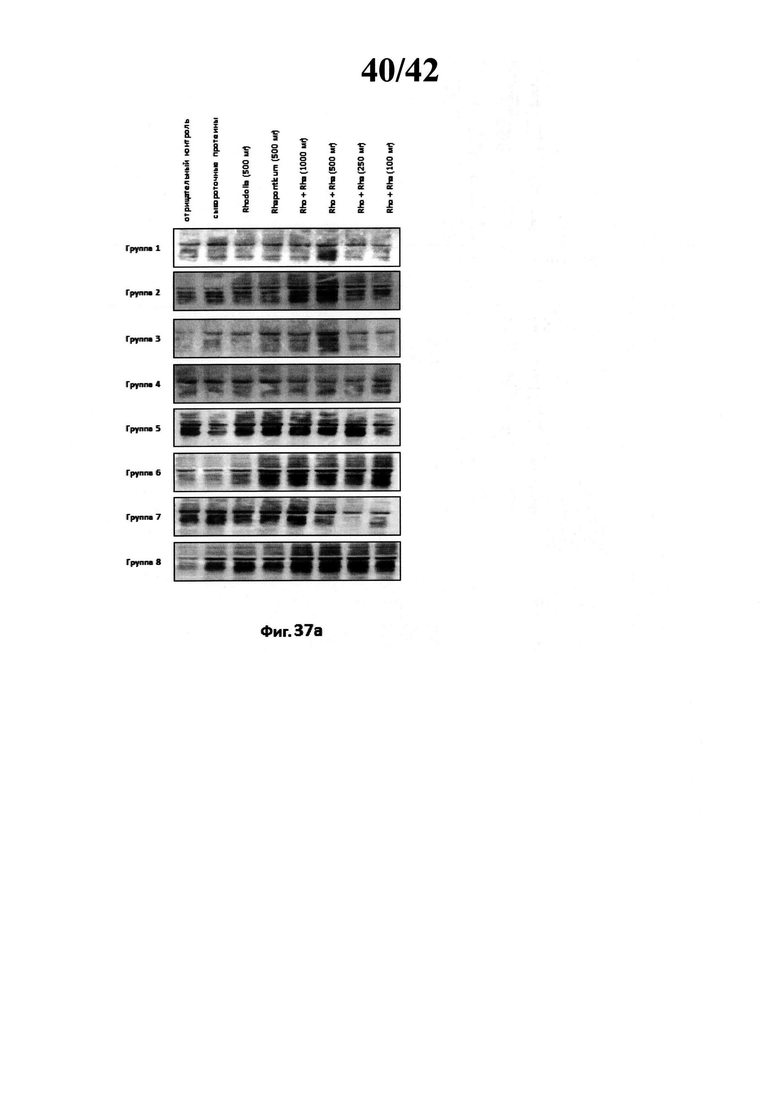
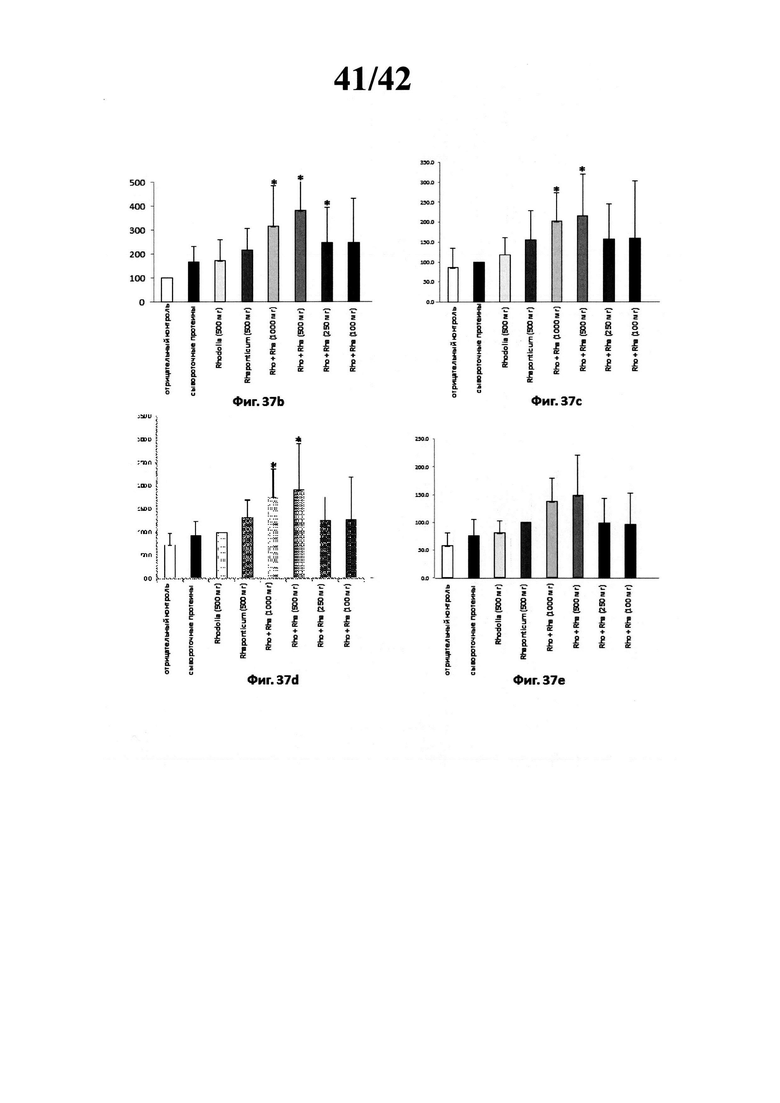
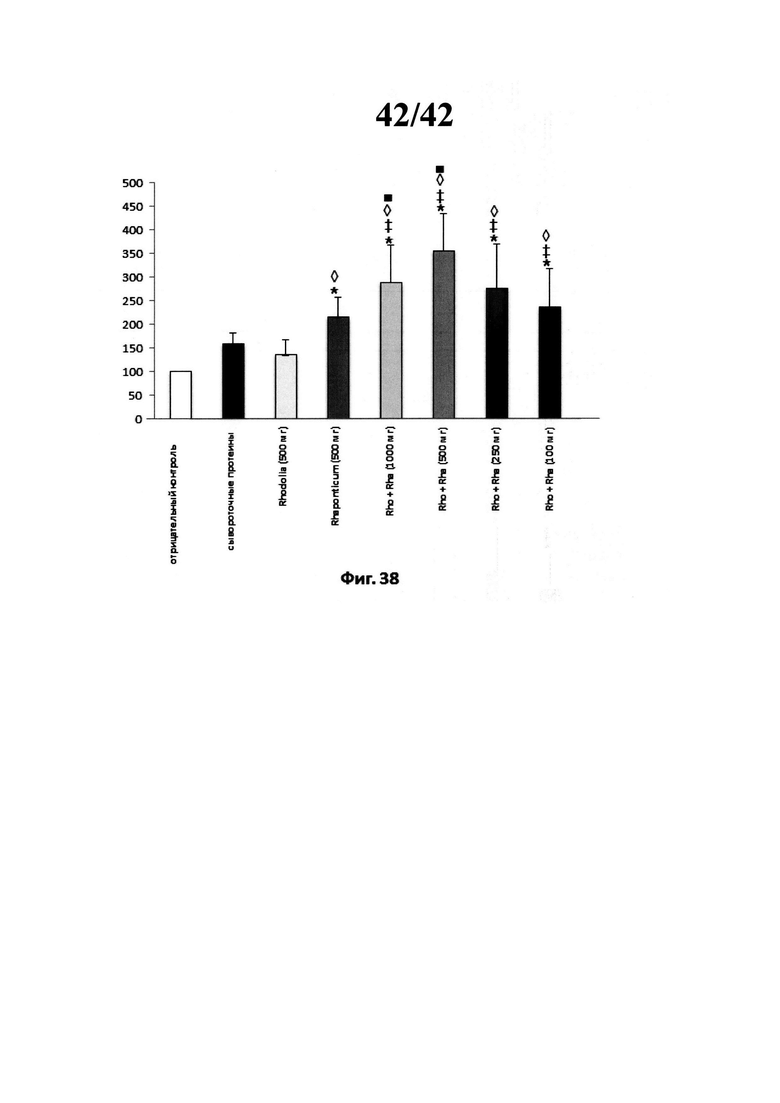
Группа изобретений относится к фармацевтической промышленности, а именно к композиции для улучшения мышечного метаболизма. Композиция для улучшения мышечного метаболизма содержит экстракт корня Rhaponticum и экстракт корня Rhodiola, причем экстракт корня Rhaponticum и экстракт корня Rhodiola получен экстракцией смесью этанол-вода и композиция содержит экстракт корня Rhodiola в количестве от 1 до 50% от массы композиции и экстракт корня Rhaponticum в количестве от 50 до 99% от массы композиции или композиция содержит экстракт корня Rhodiola в количестве от 50 до 99% от массы композиции и экстракт корня Rhaponticum в количестве от 1 до 50% от массы композиции. Способ увеличения уровня синтеза протеина у субъекта, включающий пероральное введение субъекту лекарственного состава, содержащего композицию. Способ уменьшения протеолиза протеина у субъекта включает пероральное введение субъекту лекарственного состава, содержащего композицию. Способ уменьшения саркопении у субъекта включает пероральное введение композиции. Способ ингибирования уменьшения мышечной массы у субъекта включает пероральное введение субъекту состава, содержащего композицию. Способ уменьшения мышечной атрофии или дисфункциональной атрофии, или детренированости у субъекта включает пероральное введение субъекту состава, содержащего композицию. Вышеописанная композиция эффективно улучшает мышечный метаболизм, проявляет синергетический эффект в отношении синтеза протеина, мышечной массы и мышечной силы и уменьшает протеиновый протеолиз. 6 н. и 23 з.п. ф-лы, 38 ил., 25 табл., 19 пр.
1. Композиция для улучшения мышечного метаболизма, содержащая экстракт корня Rhaponticum и экстракт корня Rhodiola, причем экстракт корня Rhaponticum и экстракт корня Rhodiola получен экстракцией смесью этанол-вода и композиция содержит экстракт корня Rhodiola в количестве от 1 до 50% от массы композиции и экстракт корня Rhaponticum в количестве от 50 до 99% от массы композиции или композиция содержит экстракт корня Rhodiola в количестве от 50 до 99% от массы композиции и экстракт корня Rhaponticum в количестве от 1 до 50% от массы композиции.
2. Композиция по п. 1, отличающаяся тем, что содержит 0,1-10% экдистеронов.
3. Композиция по п. 1, отличающаяся тем, что содержит 0,5-3% экдистеронов.
4. Композиция по п. 1, отличающаяся тем, что экстракт корня Rhaponticum содержит 0,1-10% экдистеронов.
5. Композиция по п. 1, отличающаяся тем, что экстракт корня Rhaponticum содержит 0,4-5% экдистеронов.
6. Композиция по п. 1, отличающаяся тем, что содержит 0,1-5,0% 20-гидроксиэкдизона.
7. Композиция по п. 1, отличающаяся тем, что экстракт корня Rhodiola содержит 1-4% салидрозидов.
8. Композиция по п. 1, отличающаяся тем, что экстракт корня Rhodiola содержит 1-10% розавинов.
9. Композиция по п. 1, отличающаяся тем, что экстракт корня Rhodiola содержит 1-10% розавина.
10. Композиция по п. 1, отличающаяся тем, что экстракт корня Rhodiola содержит:
1-4% салидрозидов,
0,5-10% розавина, и
0,5-10% общей суммы розавинов; и
причем экстракт корня Rhaponticum содержит:
0,1-5,0% 20-гидроксиэкдизона, и
0,1-10% общей суммы экдистеронов.
11. Способ увеличения уровня синтеза протеина у субъекта, включающий пероральное введение субъекту лекарственного состава, содержащего композицию по п. 1.
12. Способ по п. 11, отличающийся тем, что субъекту вводят 0,5-100 мг/кг/день композиции.
13. Способ по п. 11, отличающийся тем, что субъекту вводят 50-500 мг/день композиции.
14. Способ по п. 11, отличающийся тем, что субъекту вводят 50-2000 мг/день композиции.
15. Способ по п. 11, отличающийся тем, что лекарственный состав дополнительно содержит фармацевтически приемлемый носитель.
16. Способ уменьшения протеолиза протеина у субъекта, включающий пероральное введение субъекту лекарственного состава, содержащего композицию по п. 1.
17. Способ по п. 16, отличающийся тем, что субъекту вводят 0,5-100 мг/кг/день композиции.
18. Способ по п. 16, отличающийся тем, что субъекту вводят 50-500 мг/день композиции.
19. Способ по п. 16, отличающийся тем, что субъекту вводят 50-2000 мг/день композиции.
20. Способ по п. 16, отличающийся тем, что субъект является человеком.
21. Способ по п. 16, отличающийся тем, что лекарственный состав дополнительно содержит фармацевтически приемлемый носитель.
22. Способ уменьшения саркопении у субъекта, включающий пероральное введение композиции по п. 1.
23. Способ ингибирования уменьшения мышечной массы у субъекта, включающий пероральное введение субъекту состава, содержащего композицию по п. 1, причем композиция необязательно содержит подходящий фармацевтический носитель.
24. Способ уменьшения мышечной атрофии или дисфункциональной атрофии, или детренированости у субъекта, включающий пероральное введение субъекту состава, содержащего композицию по п. 1, причем композиция необязательно содержит подходящий фармацевтический носитель.
25. Способ по любому из пп. 22-24, отличающийся тем, что субъекту вводят 0,5-50 мг/кг/день композиции.
26. Способ по любому из пп. 22-24, отличающийся тем, что субъекту вводят 50-500 мг/день композиции.
27. Способ по любому из пп. 22-24, отличающийся тем, что субъекту вводят 50-2000 мг/день композиции.
28. Способ по любому из пп. 22-24, отличающийся тем, что субъект является человеком.
29. Способ по любому из пп. 22-24, отличающийся тем, что субъект является животным.
| WO 2012054993 A1, 03.05.2012 | |||
| ANTOSHECHKIN A | |||
| et al | |||
| Influence of the plant extract complex "AdMax" on global gene expression levels in cultured human fiibroblasts //J Diet Suppl | |||
| Станок для изготовления деревянных ниточных катушек из цилиндрических, снабженных осевым отверстием, заготовок | 1923 |
|
SU2008A1 |
| US 20140314870 A1, 23.10.2014 | |||
| CHENG D M et al | |||
| Прибор для промывания газов | 1922 |
|
SU20A1 |
Авторы
Даты
2020-08-26—Публикация
2016-02-03—Подача