Область техники
Настоящее изобретение относится к применению эффектов экзосом растений на иммунную систему в качестве стимуляторов, супрессоров и модуляторов иммунной системы при заболеваниях.
Уровень техники
Везикулы представляют собой небольшие пузырьки, которые участвуют в транспорте и хранении веществ внутри клетки, и отделены по меньшей мере одним липидным бислоем от цитоплазматической жидкости. Экзосомы представляют собой везикулы, которые высвобождаются многими организмами от прокариот до высших эукариот и растений, и которые содержат липидные бислойные везикулы разного размера [1]. Значение этих пузырьков не ограничивается способностью передавать информацию другим клеткам, чтобы оказать влияние на функцию клетки. Передача сигнала через экзосомы осуществляется с помощью биологических молекул многих различных групп, включающих белки, липиды, нуклеиновые кислоты и сахара [2].
Функциональные взаимодействия внеклеточных везикул с клетками были впервые обнаружены в 1982 г. после экспериментального определения того, что везикулы, выделенные из семенной плазмы, повышают подвижность сперматозоидов [3]. С этого момента и до сегодняшнего дня проводились исследования со многими различными тканями, связанные с молекулярным механизмом функционирования везикул и выяснением вопросов, которые оставались неясными.
Иммунная система представляет собой защитный механизм организма, который защищает его от инфекций и болезней. Иммунная система защищает людей от многих микроорганизмов, таких как вирусы, бактерии, грибки, простейшие и паразиты, которые определяются как микроорганизмы, и их вредных воздействий. Основная функция иммунной системы заключается в предупреждении попадания этих микроорганизмов в организм, уничтожении тех, которые проникли, и предупреждении или задержке их распространения. Основным элементом иммунной системы являются лейкоциты. Лейкоциты, которые также называют белыми кровяными тельцами или лейкоцитами, продуцируются в костном мозге, лимфатических узлах, селезенке и вилочковой железе. Лейкоциты диаметром 20 мкм составляют важный компонент иммунной системы, защищая организм от инфекционных заболеваний и чужеродных веществ. Лейкоциты делятся на две группы. Многоядерные определяются как гранулоциты, и одноядерные определяются как лимфоциты и моноциты. У каждого лейкоцита имеется своя функция в защитном механизме. Нейтрофилы разрушают болезнетворные клетки, моноциты разрушают клетки, оставшиеся от мертвых тканей, эозинофилы разрушают токсичные вещества, вызывающие аллергию клетки и паразиты, лимфоциты формируют полноценную иммунную систему организма и защищают ее. В крови здорового взрослого человека, содержащей один миллион клеток, находится 4×103-11×103 лейкоцитов, другими словами, одна капля крови содержит примерно от 4000 до 11000 лейкоцитов.
Т-клетки представляют собой тип лейкоцитов, которые контролируют клеточные аномалии и инфекции и играют важную роль в защите иммунной системы. Деструктивные эффекты небольшой субпопуляции Т-клеток в организме очень важны при таких заболеваниях, как ВИЧ/СПИД. Имеет место несколько разных субпопуляций Т-клеток. В общем, их можно разделить на два разных типа. Во-первых, «Т-клетки-киллеры, положительные на поверхностный маркер CD8» «охотятся» и разрушают инфицированные или опухолевые клетки. Во-вторых, «Т-хелперы, положительные на поверхностный маркер CD4» модулируют ответ иммунной системы и играют важную роль во всех звеньях иммунной системы.
Для пояснения функции Т-клеток в организме человека, они:
- контролируют внутриклеточную среду на предмет чужеродных «пришельцев»,
- выполняют команду к прямой индукции гибели инфицированных вирусом или бактериями клеток,
- сражаются за разрушение опухолевых клеток,
- помогают активировать структуру, называемую антителом, которая продуцируется организмом для нейтрализации патогенных факторов и
- сохраняют память о микроорганизмах, обнаруженных в организме в течение многих лет тому назад, и принимают соответствующие предупреждающие меры.
Т-клетки также ответственны за отторжение трансплантированного органа, болезни иммунной системы, такие как диабет и рассеянный склероз, и реакции иммунной системы, такие как аллергические реакции, такие как непереносимость глютена. Низкое количество Т-клеток встречается чаще, чем высокое количество Т-клеток. Низкое количество Т-клеток обычно указывает на проблемы в иммунной системе или лимфатических узлах. Низкое количество Т-клеток можно встретить при вирусных инфекциях, таких как грипп, а также в случае иммунной недостаточности, радиационного воздействия, ВИЧ и СПИДа и при заболеваниях, поражающих кровь или лимфатические узлы, таких как лейкоз. Химиотерапевтические препараты, лучевая терапия, иммуносупрессоры могут отрицательно влиять на количество Т-клеток.
В-клетки представляют собой лимфоциты, которые играют важную роль в гуморальном иммунном ответе. В организме человека ежедневно продуцируются миллионы различных типов В-клеток, и каждый из них имеет специфический рецепторный белок, который может связываться с определенным антигеном на его мембране. CD19 присутствует в качестве маркера на всей мембране B-клеток. В организме человека миллионы В-клеток циркулируют в крови и лимфе, не продуцируя антител. Когда какая-либо В-клетка встречается с антигеном и получает дополнительный сигнал от хелперной Т-клетки; то она дифференцируется в один из двух различных типов В-клеток, описанных ниже. Несмотря на то, что В-клетки могут непосредственно трансформироваться в один из этих типов клеток, они также могут трансформироваться после промежуточной стадии.
Естественные клетки-киллеры представляют неспециализированные защитные клетки иммунной системы. Естественные клетки-киллеры составляют примерно 10% лимфоцитов в крови. В них отсутствует реаранжировка гена, кодирующего рецепторы антигена, обнаруженные в Т- и В-лимфоцитах. Естественные клетки-киллеры не атакуют клетки, в которых имеются нормальные уровни молекул MHC класса 1, но подвергают киллингу клетки с чужеродными MHC, они также убивают клетки, в которых экспрессия MHC I снижена или отсутствует. Это часто наблюдается при вирусных инфекциях и раке. Естественные клетки-киллеры можно обнаружить в периферической крови в виде крупных лимфоцитов, содержащих красные гранулы. Молекула адгезии CD56 является маркером типичных естественных клеток-киллеров.
Общие цели использования адъювантов являются следующими:
- повышение иммуногенности антигенов, рекомбинантных или полученных посредством тщательной очистки,
- индукция более сильного и более продолжительного иммунного ответа в короткий период времени,
- снижение количества антигенов или количества вакцинаций, необходимых для достижения первичного иммунного ответа, и тем самым снижения стоимости вакцинации,
- повышение активности вакцины у новорожденных, пожилых людей и людей с иммунодефицитом,
- усиление поступления антигенов на слизистую оболочку (стимуляция мукозального иммунитета),
- стимуляция клеточного иммунитета,
- предупреждение конкуренции антигенов в комбинированных вакцинах.
Клеточный иммунный ответ необходим для защиты от внутриклеточных патогенных микроорганизмов, и гуморальный иммунный ответ необходим для защиты от внеклеточных микроорганизмов. Соли алюминия являются слабыми адъювантами, потому что они повышают ответную выработку антител, только стимулируя гуморальный иммунный ответ. Их имеется достаточный ассортимент для заболеваний, при которых требуется гуморальный иммунный ответ (например, гепатит В и коклюш). Однако они не обладают активностью в стимуляции цитотоксических Т-лимфоцитов (клеточный иммунитет). Например, в вакцинах против ВИЧ целью является не продукция антител, а стимуляция цитотоксических лимфоцитов. Кроме того, соединения алюминия не подходят для перорального или интраназального введения. Они не могут индуцировать мукозальный IgA ответ. Напротив, у некоторых людей они могут вызывать аллергические реакции за счет усиления IgE ответа. Следовательно, многие химические вещества, биохимические продукты и белки, образующиеся в результате активности иммунной системы (например, цитокины), в последние годы начали исследовать в качестве потенциальных адъювантов. Однако местная и системная токсичность, наблюдаемая для большинства таких веществ, в настоящее время не позволяет использовать многие из них в качестве адъювантов в вакцинах для человека. Чем выше адъювантная активность, тем выше частота проявления побочных эффектов. Могут встречаться местные побочные эффекты, такие как воспаление, отек, некроз в месте инъекции, гранулемы, стерильные абсцессы и лимфаденопатии, а также системные побочные эффекты, такие как тошнота, лихорадка, артрит, увеит, эозинофилия, аллергия, анафилаксия, подавление иммунитета и аутоиммунные заболевания, вызванные адъювантами. В исследованиях, связанных с адъювантами, минимизация токсичности рассматривается в качестве наиболее трудной стадии. По этой причине только алюминиевые адъюванты продолжали использоваться в качестве адъювантов для человеческих вакцин в течение почти столетия.
Независимо от того, какой тип защиты требуется, клеточный или гуморальный, идеальный адъювант должен обеспечивать желаемый иммунитет; должен обеспечивать иммунную память, т.е. длительный иммунитет; должен быть безопасным и иметь минимум побочных эффектов; не должен обладать никаким эффектом стимуляции аутоиммунитета; не должен быть мутагенным, канцерогенным, тератогенным; должен быть биодеградируемым; и должен быть недорогим и иметь длительный срок хранения.
Сапонины представляют собой стероидные или тритерпеноидные гликозиды, обнаруженные в растениях, некоторых примитивных морских организмах и бактериях. Они изобилуют в природе. Тритерпеноидные сапонины обнаружены в соевых бобах, бобах, горохе, чае, шпинате, сахарной свекле, лакрице, подсолнечнике, конском каштане и женьшене, тогда как стероидные сапонины обнаружены в овсе, болгарском перце, баклажанах, семенах томатов, луке, спарже, сладком картофеле и женьшене. Тритерпеноидные сапонины содержат гидрофобное ядро и связанные с ним углеводные цепи. Адъюванты, содержащие сапонины, стимулируют как клеточный, так и гуморальный иммунитет. Для проявления адъювантной активности достаточно их введения в низкой дозе. Сапонины также усиливают ответ цитотоксических CD8(+) лимфоцитов и усиливают иммунный ответ на антигены на слизистой оболочке. Однако, поскольку они являются поверхностно-активными веществами, то в исследованиях in vitro было установлено, что они вызывают гемолиз. Существует множество адъювантов, содержащих сапонин.
Использование иммуномодулирующих химических соединений имеет большое значение в проведении и поддержании непрерывности в трансплантации клеток или органов, которая сегодня часто выполняется в качестве очень важного метода лечения. Болезнь «трансплантат против хозяина» (GVHD), которая возникает, особенно при трансплантации солидных органов и трансплантации гемопоэтических стволовых клеток, и которая характеризуется тяжелой иммунологической реакцией, опосредованной здоровыми Т-лимфоцитами, является одним из заболеваний, при котором широко используются иммуномодуляторы. Самая важная причина состоит в том, что это основной фактор смертности и заболеваемости в посттрансплантационном процессе. Данное заболевание, которое может возникнуть в течение первых трех месяцев после трансплантации, оказывает значительное влияние в основном на кожу, печень и кишечник. Несмотря на то, что в прошлом и в настоящее время достигнут значительный прогресс в профилактике данного заболевания с помощью иммуносупрессоров, таких как циклоспорин и метотрексат, к сожалению, прогресс в лечении этого заболевания является ограниченным. В общем, заболевание подразделяется на две формы, а именно острую и хроническую GVHD, в зависимости от времени начала после трансплантации гемопоэтических стволовых клеток. Соответственно, важно подтвердить диагноз биопсией, поскольку лечение хронической GVHD, возникающей через 3 месяца, включает высокие дозы иммуносупрессоров и сохраняется в течение длительного времени. Кроме того, инфекции, возникающие в процессе лечения, являются одной из наиболее частых причин смерти пациентов с хронической GVHD. Следовательно, введение противомикробных препаратов в профилактических целях этим пациентам во время иммуносупрессорной терапии стало жизненно необходимым условием. Исследования по разработке различных профилактических и терапевтических методов продолжаются в последние годы в соответствии с данными о патогенезе как острой, так и хронической GVHD.
Чрезмерная или неадекватная реакция иммунной системы на антиген называется гиперчувствительностью. В то время как иммунная система здоровых субъектов может бороться с патогенами, не нанося значительного ущерба их клеткам, иммунный ответ у людей с гиперчувствительностью вызывает повреждение здоровых тканей. Аллергия, то есть ответная реакция иммунной системы на безвредный антиген, относится к проявлению гиперчувствительности. Экзема, аллергическая астма и сенная лихорадка представляют собой одни из самых распространенных типов хронической аллергии.
При лечении заболеваний, связанных с гиперчувствительностью, используются противовоспалительные препараты широкого спектра действия, антицитокиновая терапия и, в частности, в более серьезных случаях, методы лечения, которые уменьшают количество лимфоцитов в организме. Десенсибилизирующая терапия может использоваться для снижения чувствительности субъектов к антигену, на который у них имеется аллергия. Десенсибилизация достигается введением антигена, на который у субъекта имеется аллергия, в контролируемых дозах в течение периода лечения, тем самым повышая толерантность к антигену.
Проблемы, определенные в патентах на способ применения, можно обобщить следующим образом:
- важной проблемой для алюминиевых адъювантов является то, что их применение ограничивается бактериальными и вирусными вакцинами, которые индуцируют продукцию нейтрализующих антител,
- алюминиевые адъюванты могут вызывать аллергию и потенциальную нейротоксичность за счет повышенной выработки IgE,
- интоксикация алюминием также ассоциирована с боковым амиотрофическим склерозом и болезнью Альцгеймера,
- адъюванты, содержащие сапонины растительного происхождения, вызывают гемолиз в исследованиях in vitro, поскольку являются поверхностно-активными веществами,
- иммуносупрессоры, такие как циклоспорин и метотрексат, делают пациентов уязвимыми к инфекционным заболеваниям при длительном применении,
- циклоспорин, который активно применяется в лечении GVHD, вызывает тяжелую нефротоксичность и артериальную гипертензию [4],
- подкожная инъекция интерферона бета (IFNβ), который вводят пациентам с рассеянным склерозом (РС), сопровождается сначала панникулитом, а затем локальной липодистрофией в месте инъекции,
- препараты азатиоприн и 6-меркаптопурин, используемые для иммуносупрессорных целей, вызывают у субъектов гепатит, панкреатит и многие другие инфекции в зависимости от продолжительности применения,
- различные экстракты растений, содержащие фитохимические вещества, такие как флавоноиды, полисахариды, лактоны, алкалоиды, дитерпеноиды и гликозиды, оказывают модулирующее действие на иммунную систему; однако за счет высокого содержания химических примесей, присутствующих в дополнение к активным ингредиентам, имеются сомнения относительно их эффективного использования и потенциальных побочных эффектов.
В заявке на патент Южной Кореи № KR20120002942, известной в данной области техники, раскрыты микровезикулы, полученные из протопластов клеток, и их применение. Эти клетки могут представлять собой бактериальные клетки, клетки архей, клетки плесеней, растительные клетки или L-формы бактерий. Композиция для доставки материала для диагностики или лечения заболеваний или вакцинирования содержит микровезикулы. Способ получения микровезикул включает стадии удаления клеточных стенок из клеток для получения протопласта, приготовления микровезикул в жидкой суспензии, содержащей протопласт, и выделения микровезикул из суспензионной жидкости.
В международной заявке на патент WO2016166716, известной в данной области, раскрыта противоопухолевая активность нановезикул, выделенных из Citrus limon. Способ получения нановезикул из цитрусовых растений включает стадии: а) центрифугирование и фильтрование сока в одном или более последовательных циклах; b) ультрацентрифугирование сока, полученного на стадии (а), с получением тем самым супернатанта и осадка после центрифугирования, содержащего нановезикулы, и выделение везикул. Способ может дополнительно включать стадии c) подвергание выделенного осадка ультрацентрифугированию в градиенте сахарозы; d) выделение фракции с плотностью от 1,12 до 1,19 г/мл; e) необязательное ультрацентрифугирование фракции; и f) необязательно промывание осадка физиологическим раствором.
В заявке на патент Китая № CN102697812, известной в данной области, раскрыт способ экстракции экзосом из куриной желчи и применение указанных экзосом в иммунологии. Экзосомы можно использовать в качестве адъюванта для иммунной реакции в целях иммуномодуляции.
В международной заявке на патент WO2016168680, известной в данной области техники, раскрыт способ разработки вакцин на основе экзосом. Варианты осуществления изобретения относятся к способам создания иммуногенных композиций и способам применения таких иммуногенных композиций для лечения различных заболеваний.
В заявке на патент Турции № TR 2012/05117 (EP1267924B1), заявке из предшествующего уровня техники, раскрыты иммунотерапевтические способы и композиции. Это изобретение относится к способам и композициям для введения химических соединений в антигенпрезентирующие клетки. Полученная презентация указанных антигенов на поверхности антигенпрезентирующих клеток оказывает положительное влияние на иммунную систему. Изобретение также относится к полученным модифицированным антигенпредставляющим клеткам и фармацевтическим композициям, содержащим эти клетки. Изобретение раскрывает новое понимание феномена адъювантности и адъювантных препаратов, включая ряд родственных пептидов и фосфолипидных везикул, включающих указанные пептиды.
В заявке на патент Турции № TR 2016/08391 (EP2591802B1), заявке из предшествующего уровня техники, раскрыты вакцинные композиции на основе стихолизина, инкапсулированного в липосомы. Указанное изобретение относится к области биотехнологии, используемой в здравоохранении. В заявке описывается носитель для вакцины, в котором токсины эукариотических микроорганизмов инкапсулированы в многослойные везикулы, полученные процедурой дегидратации-регидратации, липидный состав которых представляет собой дипальмитоилфосфатидилхолин:холестерин в молярном соотношении 1:1, для подкожного или внутримышечного введения. Для этих композиций не требуется использование других адъювантов. Раскрытые композиции позволяют модулировать CTL-специфический иммунный ответ против одного или более антигенов, совместно инкапсулированных в токсинсодержащих липосомах. Носитель для вакцины по указанному изобретению демонстрирует преимущества по сравнению с другими, раскрытыми на предшествующем уровне техники, за счет устойчивости и функциональности индуцированного иммунного ответа, а также его иммуномодулирующих свойств.
Патентные заявки с номерами US9717733, WO2006007529, WO1999003499, WO2017004526 и US20100092524 также являются заявками, соответствующими предшествующему уровню техники.
Сущность изобретения
Целью настоящего изобретения является применение экзосом растений, выделенных из лизатов растений, в качестве стимуляторов, супрессоров и модуляторов иммунной системы, при заболеваниях, вызванных нарушениями иммунной системы.
Другой целью настоящего изобретения является обеспечение более высокой супрессии по сравнению с супрессией, полученной с помощью веществ, полученных из аналогичных стимуляторов и химических соединений, используемых в настоящее время для подавления активации клеток крови.
Еще одной целью настоящего изобретения является обеспечение более высокой стимуляции по сравнению со стимуляцией, полученной с помощью веществ, полученных из аналогичных стимуляторов и химических соединений, используемых в настоящее время для усиления активации клеток крови.
Еще одной целью настоящего изобретения является получение иммуномодулирующего средства, которое не оказывает токсического влияния на печень и другие органы, в отличие от других лекарственных средств, поскольку оно имеет полностью растительное происхождение.
Подробное описание изобретения
«Применение экзосом растений для демонстрации модулирующих эффектов на клетки иммунной системы», разработанное для достижения целей настоящего изобретения, показано на прилагаемых фигурах, где:
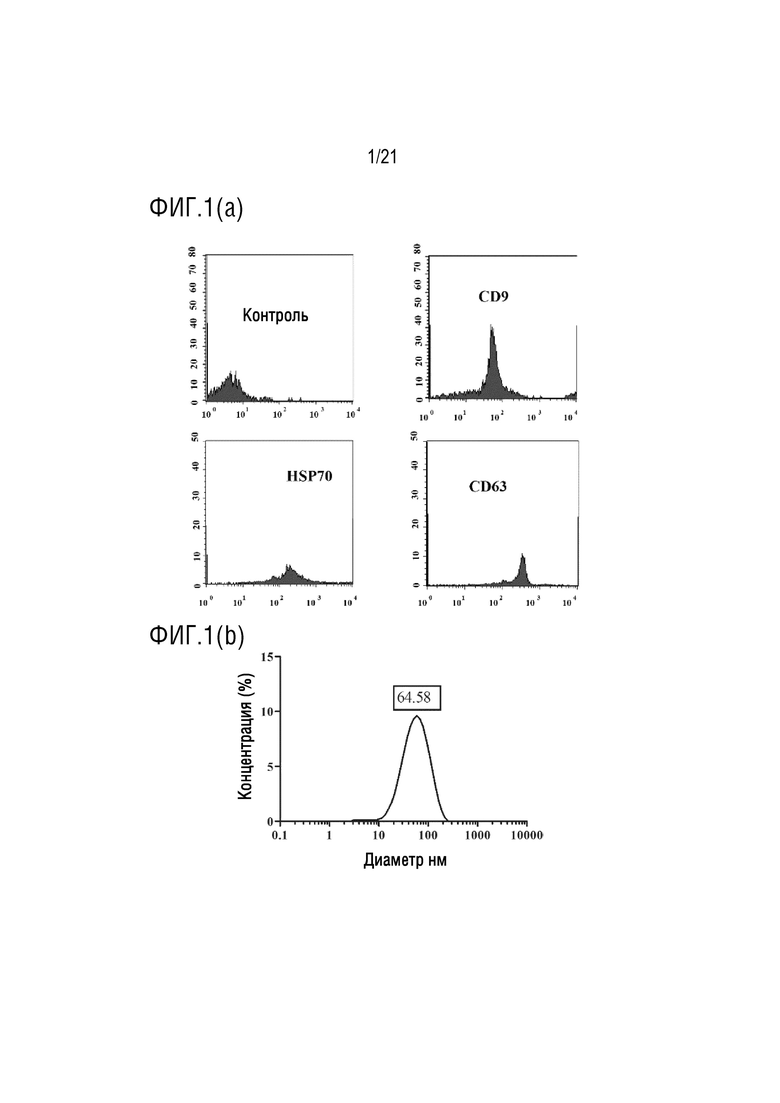
На фиг.1 приведено графическое представление характеристики экзосомы, выделенной из растения ревеня с бородавчатыми листьями по настоящему изобретению (график проточной цитометрии, полученный с антителами к CD9, CD63 и HSP70, которые являются маркерами характеристики экзосом, с помощью устройства для проточной цитометрии (а); и график определения диаметра экзосом (b)).
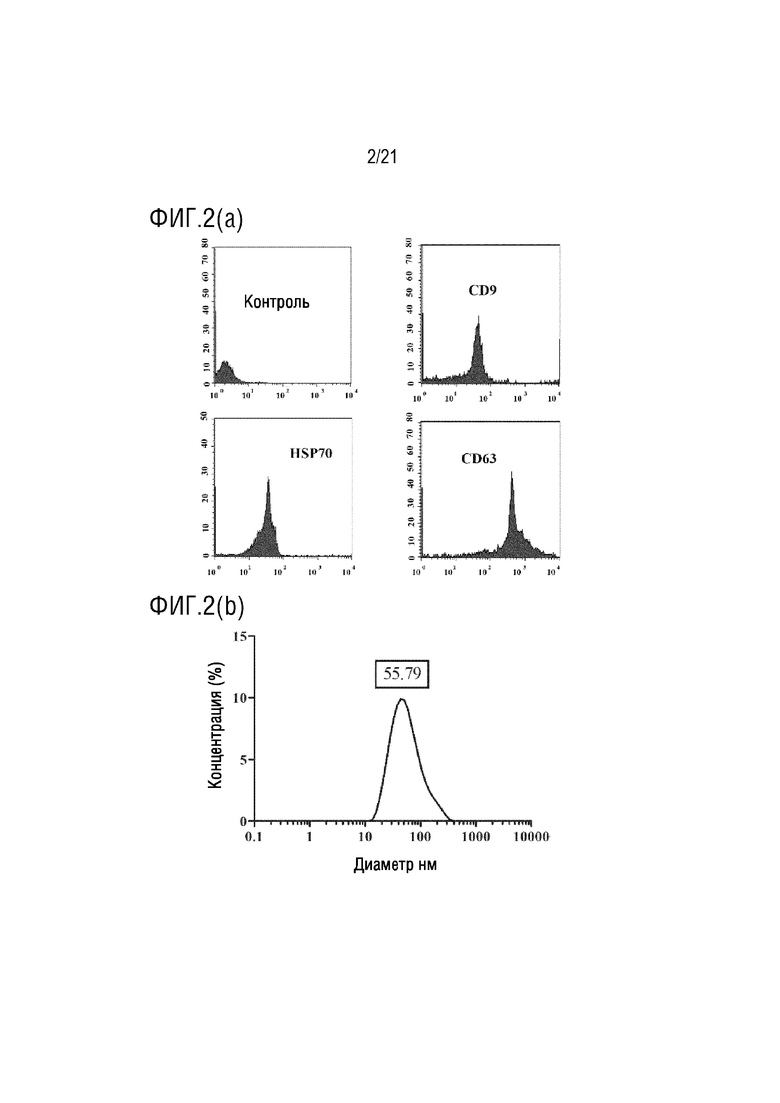
На фиг. 2 приведено графическое представление характеристики экзосомы, выделенной из сельдерея по настоящему изобретению (график проточной цитометрии, полученный с антителами к CD9, CD63 и HSP70, которые являются маркерами характеристики экзосом, с помощью устройства проточной цитометрии (а); и график определения диаметра экзосом (b)).
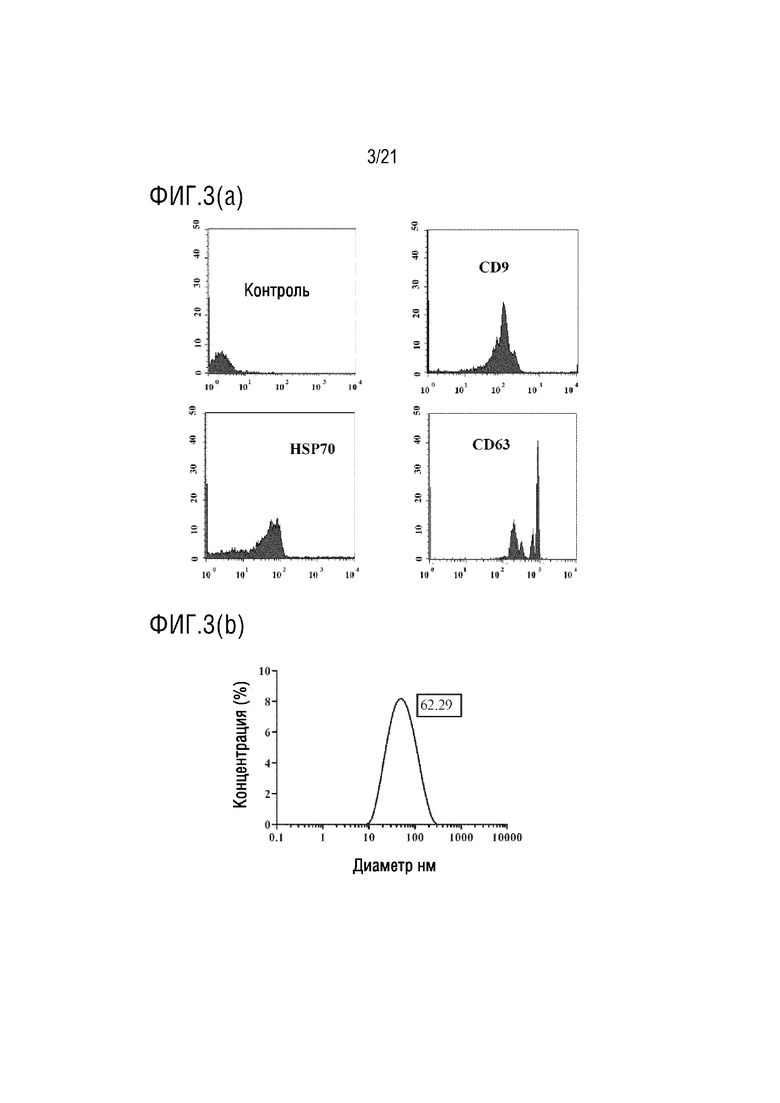
На фиг.3 приведено графическое представление характеристики экзосомы, выделенной из граната по настоящему изобретению (график проточной цитометрии, полученный с антителами к CD9, CD63 и HSP70, которые являются маркерами характеристики экзосом, с помощью устройства для проточной цитометрии (а); и график измерения диаметра экзосом (b)).
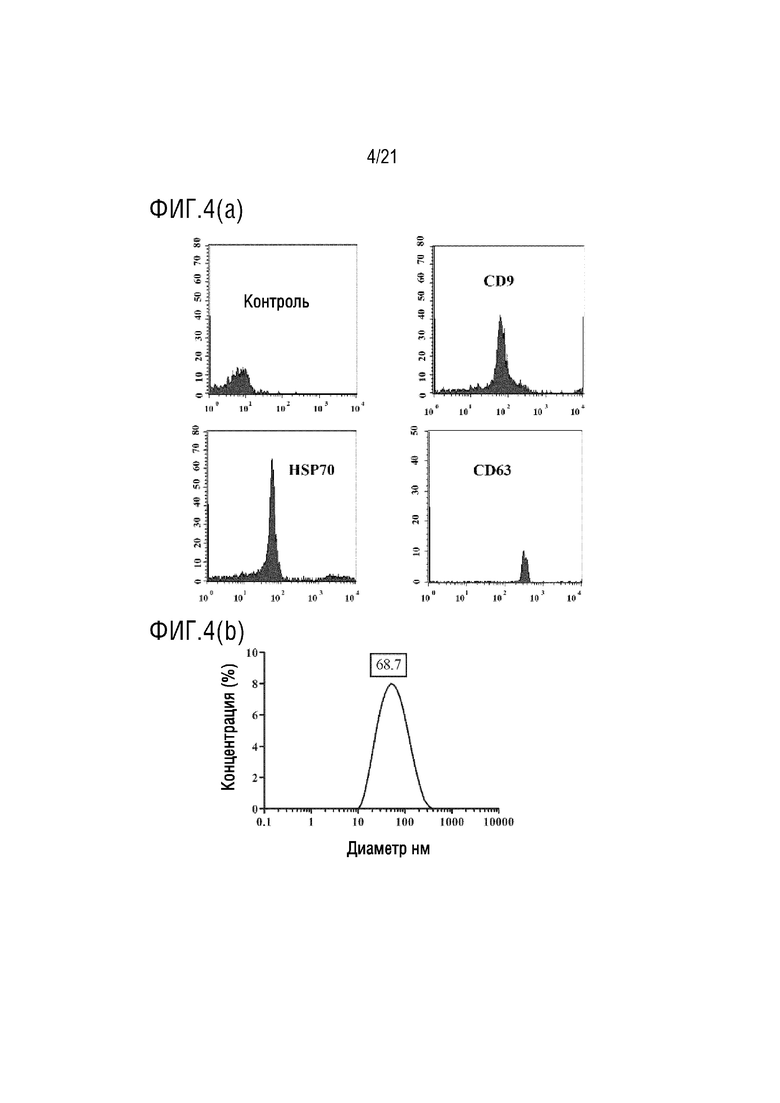
На фиг.4 приведено графическое представление характеристики экзосомы, выделенной из лука-порея по настоящему изобретению (график проточной цитометрии, полученный с антителами к CD9, CD63 и HSP70, которые являются маркерами характеристики экзосом, с помощью устройства для проточной цитометрии (а); и график измерения диаметра экзосом (b)).
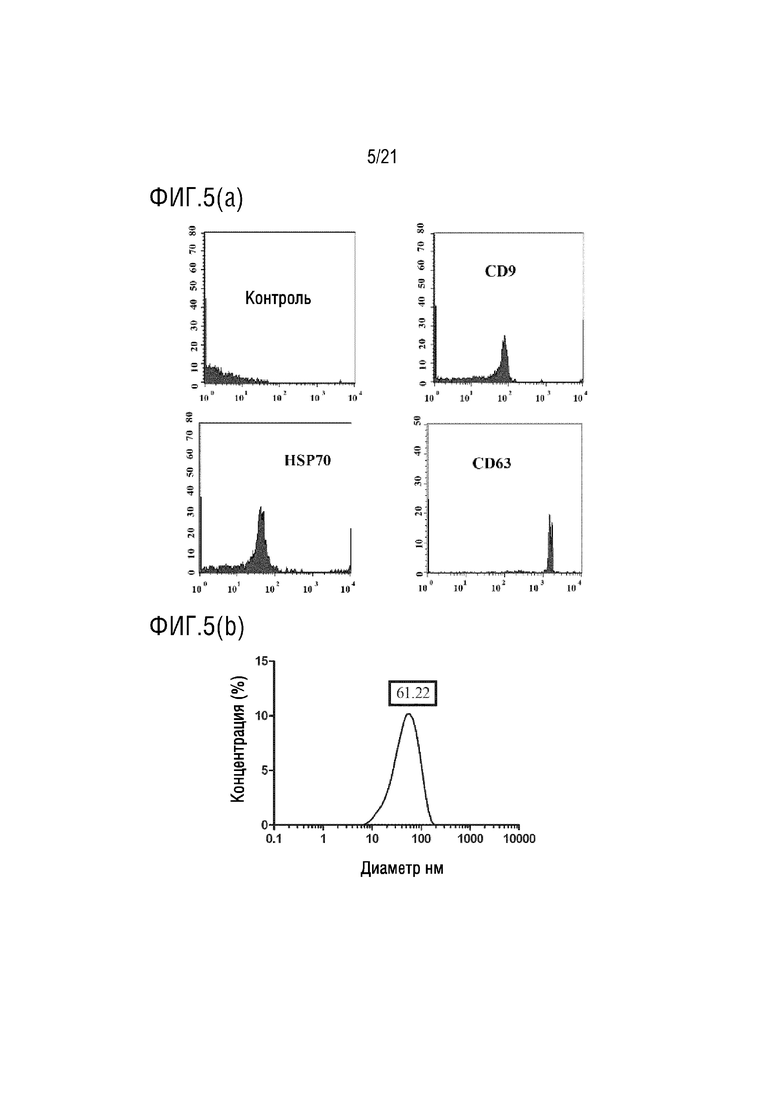
На фиг.5 приведено графическое представление характеристики экзосомы, выделенной из хрена по настоящему изобретению (график проточной цитометрии, полученный с антителами к CD9, CD63 и HSP70, которые являются маркерами характеристики экзосом, с помощью устройства для проточной цитометрии (а); и график измерения диаметра экзосом (b)).
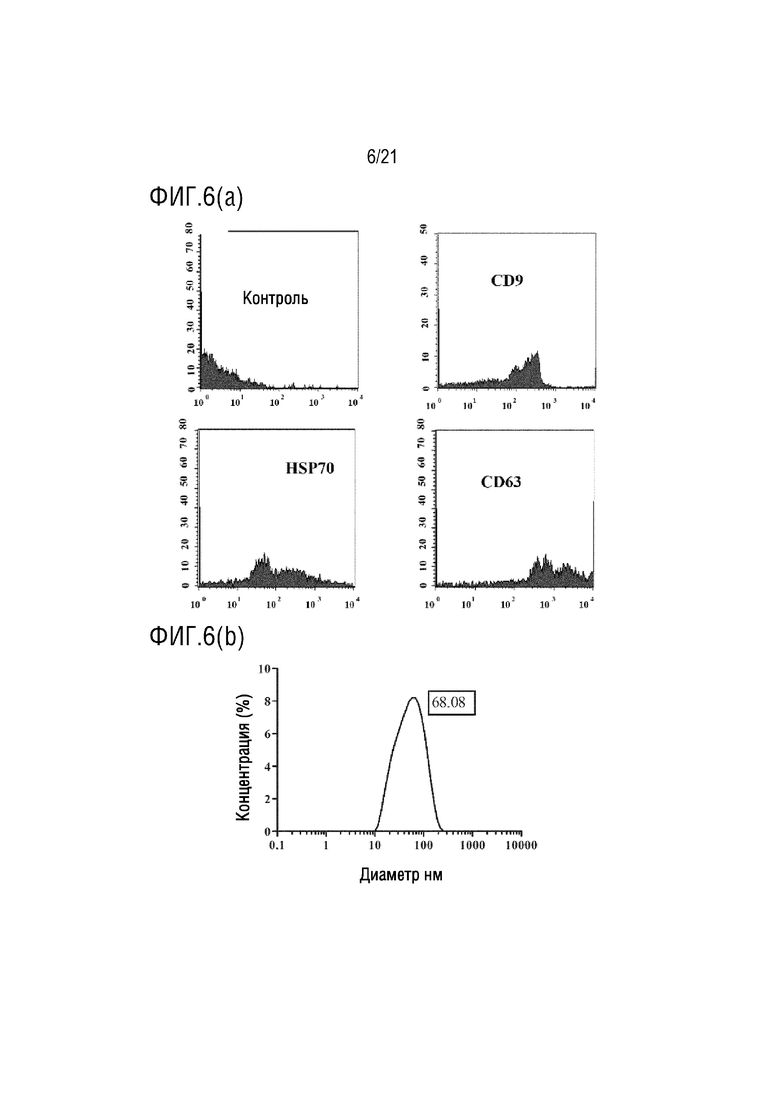
На фиг.6 приведено графическое представление характеристики экзосомы, выделенной из имбиря по настоящему изобретению (график проточной цитометрии, полученный с антителами к CD9, CD63 и HSP70, которые являются маркерами характеристики экзосом, с помощью устройства для проточной цитометрии (а); и график измерения диаметра экзосом (b)).
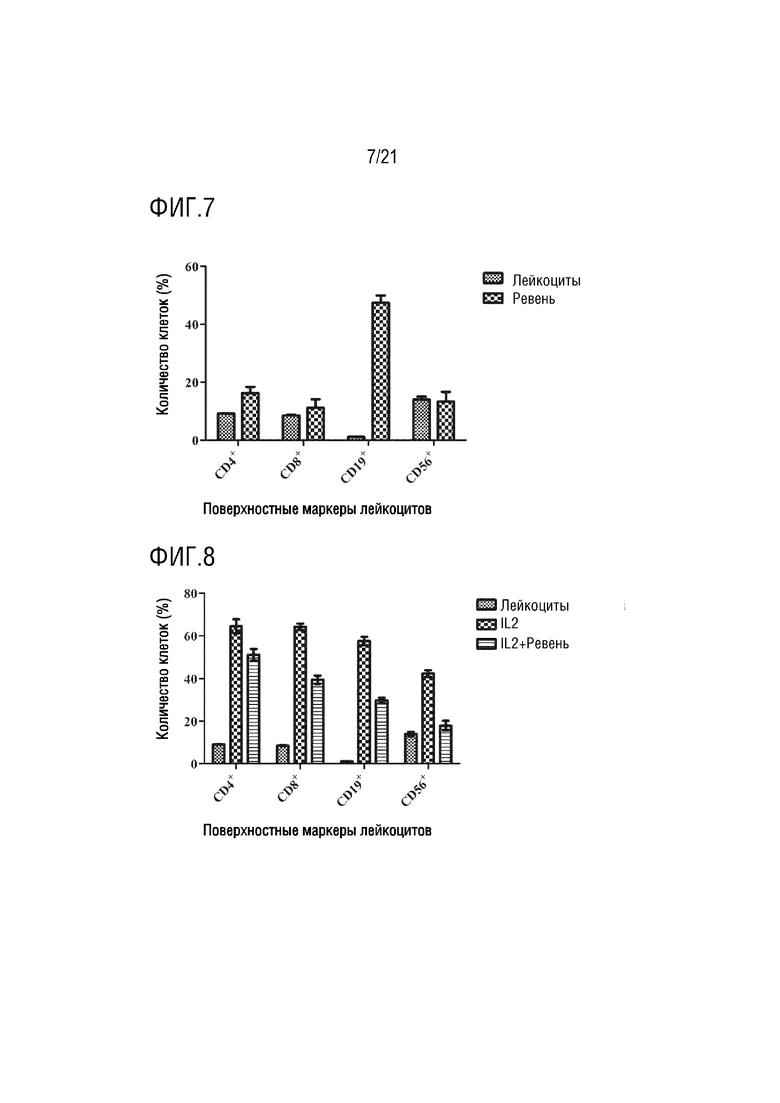
На фиг.7 показано графическое представление влияния экзосомы ревеня с бородавчатыми листьями на лейкоциты по настоящему изобретению (график определения CD4 хелперных T-лимфоцитов, CD8 цитотоксических T-лимфоцитов, CD19 B-лимфоцитов и CD56 естественных клеток-киллеров с антителами, которые являются поверхностными маркерами, с помощью устройства для проточной цитометрии).
На фиг. 8 показано графическое представление влияния экзосомы ревеня с бородавчатыми листьями на лейкоциты, активированные IL2, по настоящему изобретению (график определения CD4 хелперных T-лимфоцитов, CD8 цитотоксических T-лимфоцитов, CD19 B-лимфоцитов и CD56 естественных клеток-киллеров с антителами, которые являются поверхностными маркерами, с помощью устройства для проточной цитометрии)
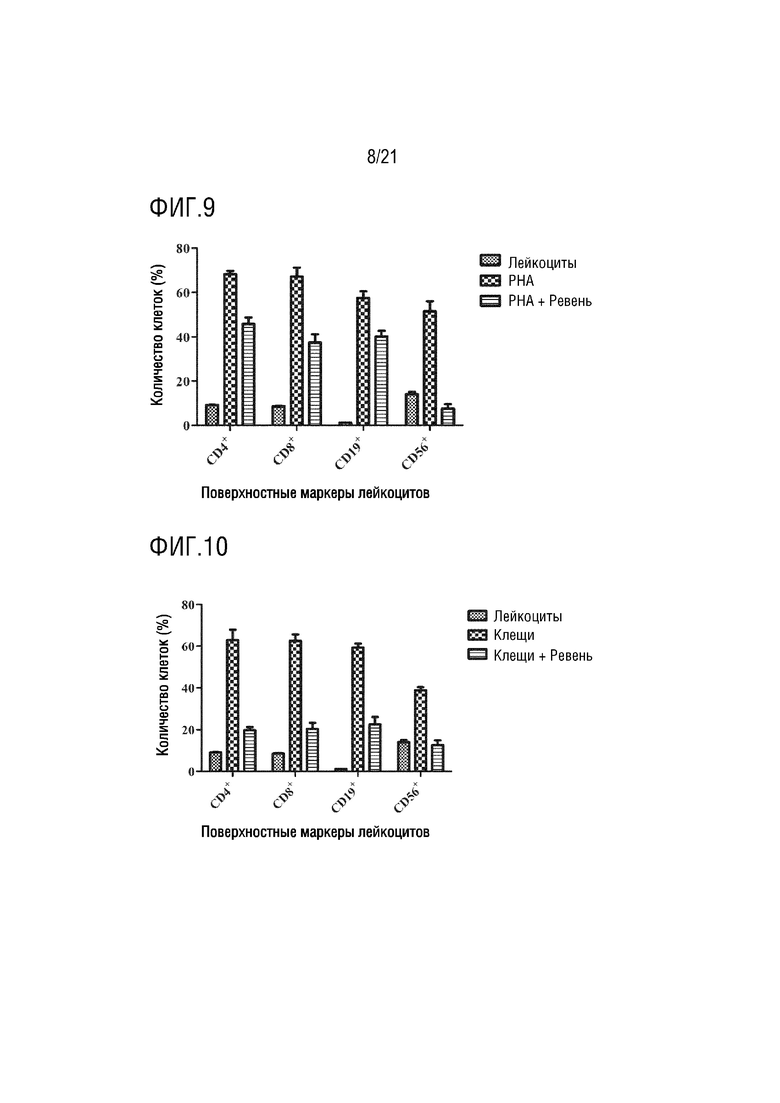
На фиг.9 показано графическое представление влияния экзосомы ревеня с бородавчатыми листьями на лейкоциты, активированные PHA, по настоящему изобретению (график определения CD4 хелперных T-лимфоцитов, CD8 цитотоксических T-лимфоцитов, CD19 B-лимфоцитов и CD56 естественных клеток-киллеров с антителами, которые являются поверхностными маркерами, с помощью устройства для проточной цитометрии).
На фиг.10 показано графическое представление влияния экзосомы ревеня с бородавчатыми листьями на лейкоциты, активированные аллергеном клещей, по настоящему изобретению (график определения CD4 хелперных T-лимфоцитов, CD8 цитотоксических T-лимфоцитов, CD19 B-лимфоцитов и CD56 естественных клеток-киллеров с антителами, которые являются поверхностными маркерами, с помощью устройства для проточной цитометрии).
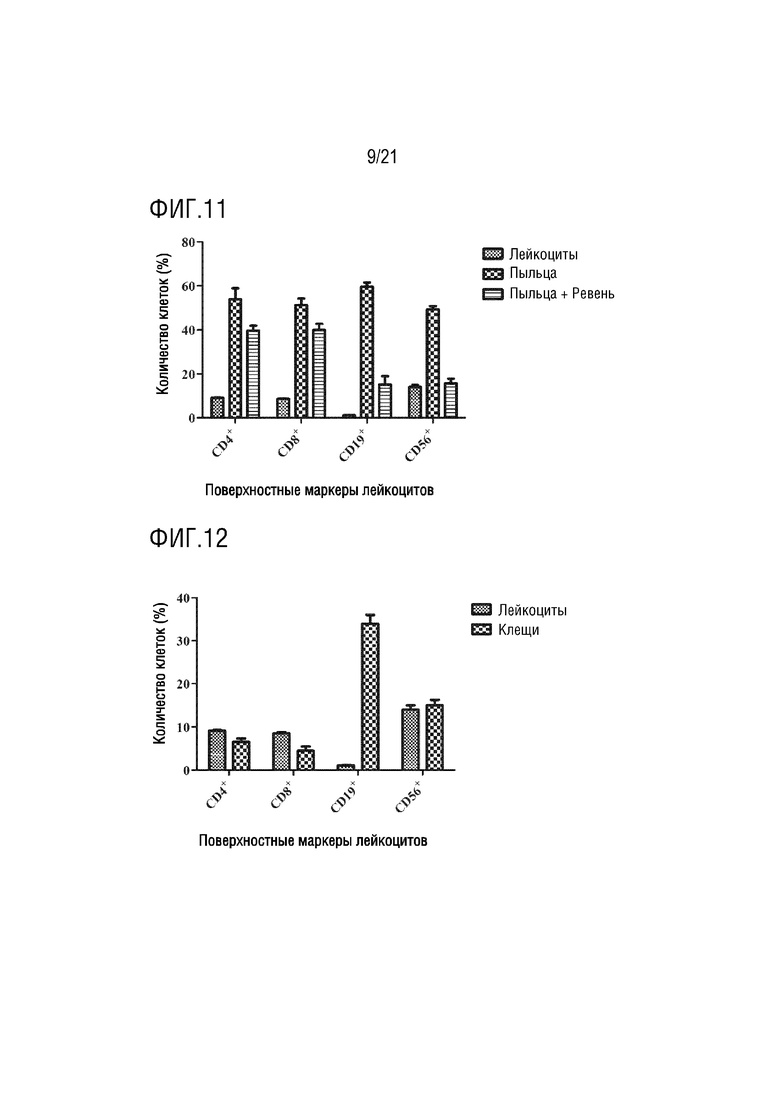
На фиг. 11 показано графическое представление влияния экзосомы ревеня с бородавчатыми листьями на лейкоциты, активированные аллергеном пыльцы, по настоящему изобретению (график определения CD4 хелперных T-лимфоцитов, CD8 цитотоксических T-лимфоцитов, CD19 B-лимфоцитов и CD56 естественных клеток-киллеров с антителами, которые являются поверхностными маркерами, с помощью устройства для проточной цитометрии).
На фиг. 12 показано графическое представление влияния экзосомы сельдерея на лейкоциты по настоящему изобретению (график определения CD4 хелперных T-лимфоцитов, CD8 цитотоксических T-лимфоцитов, CD19 B-лимфоцитов и CD56 естественных клеток-киллеров с антителами, которые являются поверхностными маркерами, с помощью устройства для проточной цитометрии).
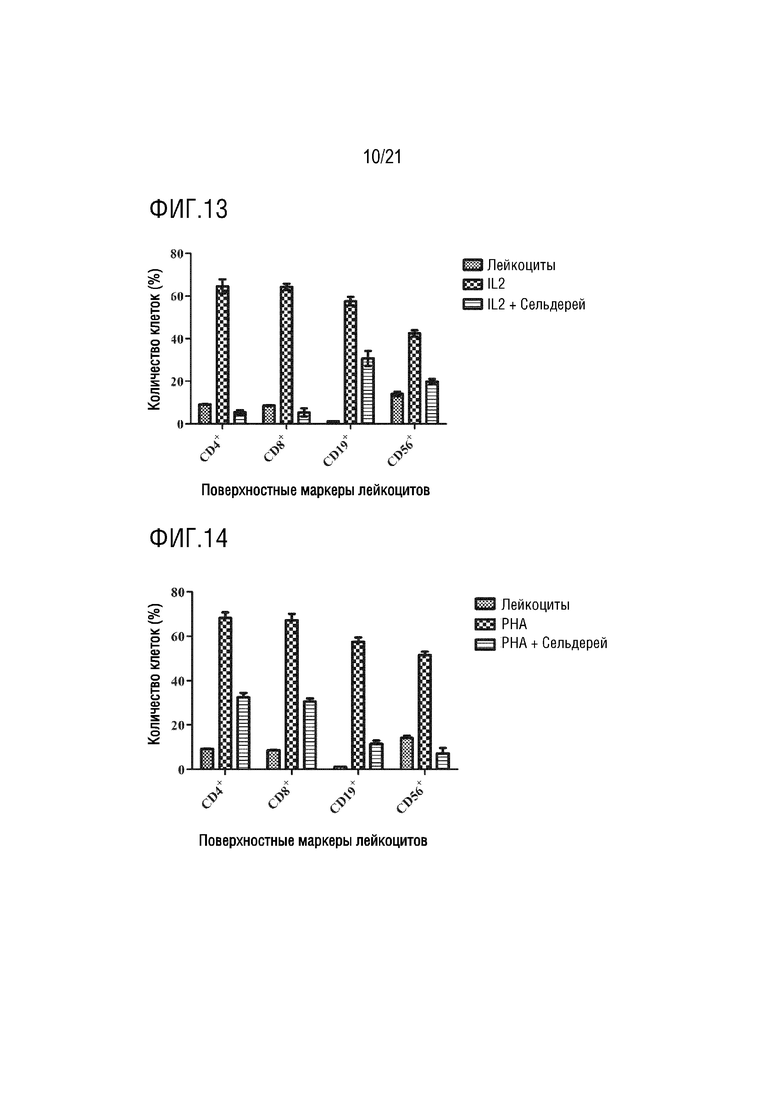
На фиг. 13 показано графическое представление влияния экзосомы сельдерея на лейкоциты, активированные IL2, по настоящему изобретению (график определения CD4 хелперных T-лимфоцитов, CD8 цитотоксических T-лимфоцитов, CD19 B-лимфоцитов и CD56 естественных клеток-киллеров с антителами, которые являются поверхностными маркерами, с помощью устройства для проточной цитометрии).
На фиг. 14 показано графическое представление влияния экзосомы сельдерея на лейкоциты, активированные PHA, по настоящему изобретению (график определения CD4 хелперных T- лимфоцитов, CD8 цитотоксических T-лимфоцитов, CD19 B-лимфоцитов и CD56 естественных клеток-киллеров с антителами, которые являются поверхностными маркерами, с помощью устройства для проточной цитометрии).
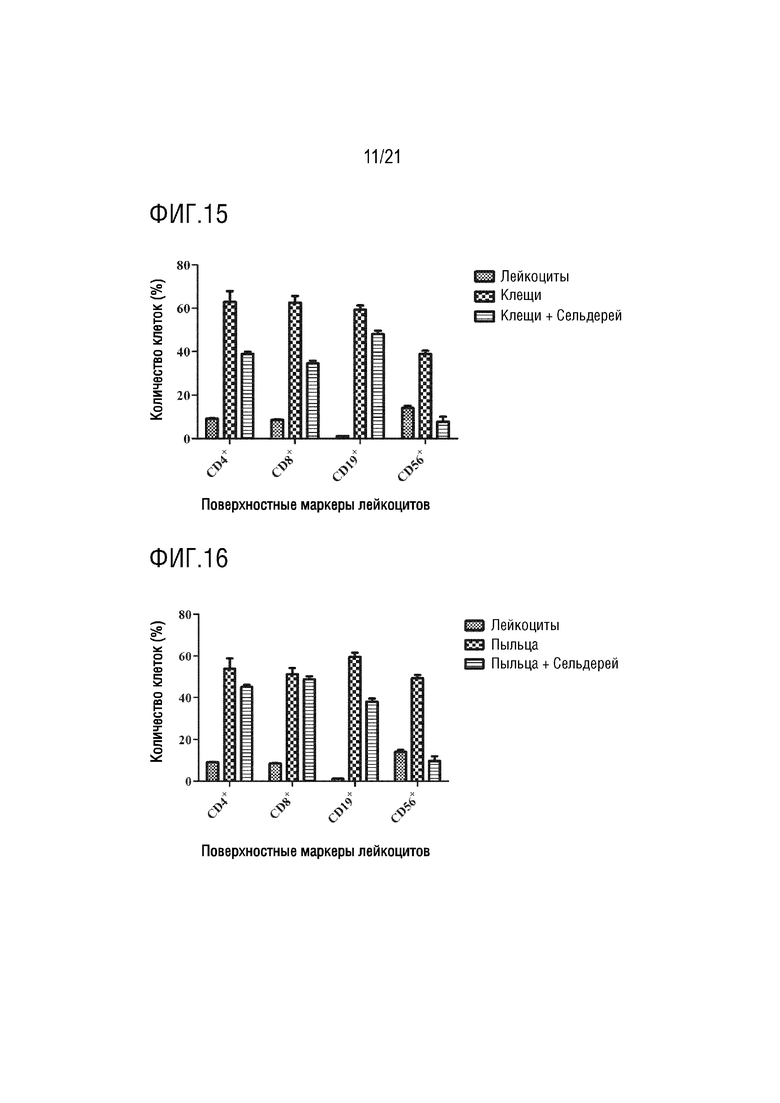
На фиг. 15 показано графическое представление влияния экзосомы сельдерея на лейкоциты, активированные аллергеном клещей, по настоящему изобретению (график определения CD4 хелперных T-лимфоцитов, CD8 цитотоксических T-лимфоцитов, CD19 B-лимфоцитов и CD56 естественных клеток-киллеров с антителами, которые являются поверхностными маркерами, с помощью устройства для проточной цитометрии).
На фиг. 16 показано графическое представление влияния экзосомы сельдерея на лейкоциты, активированные аллергеном пыльцы, по настоящему изобретению (график определения CD4 хелперных T-лимфоцитов, CD8 цитотоксических T-лимфоцитов, CD19 B-лимфоцитов и CD56 естественных клеток-киллеров с антителами, которые являются поверхностными маркерами, с помощью устройства для проточной цитометрии).
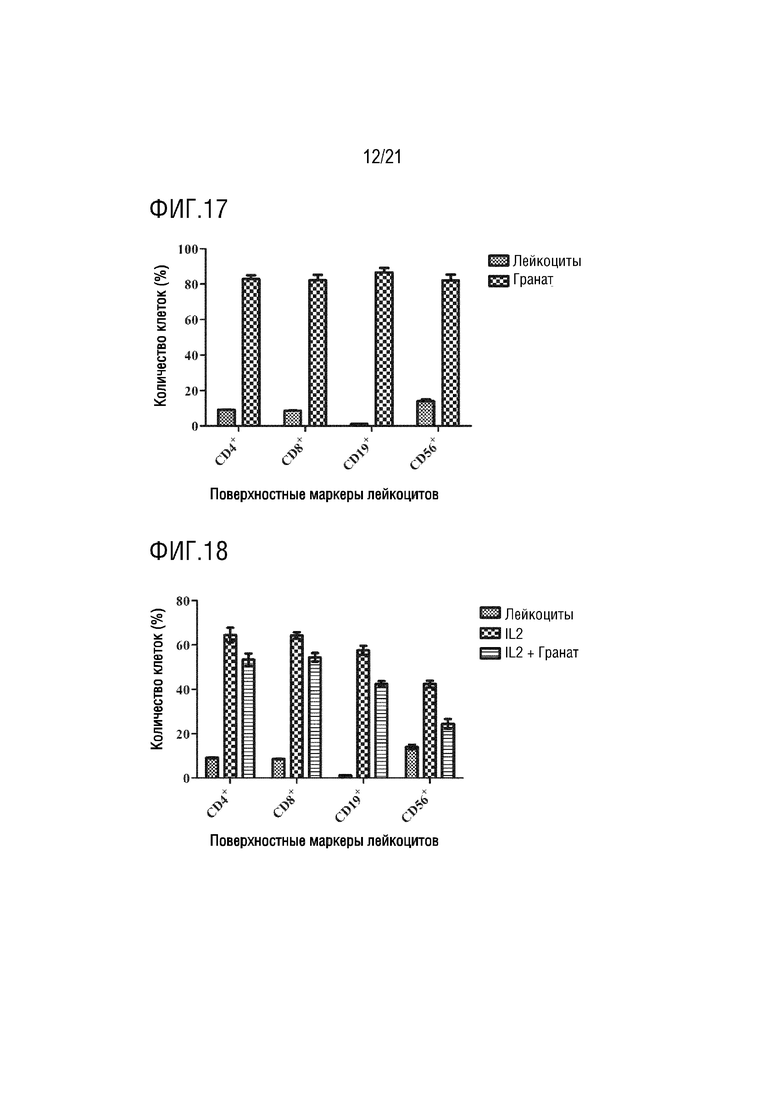
На фиг. 17 показано графическое представление влияния экзосомы граната на лейкоциты по настоящему изобретению (график определения CD4 хелперных T-лимфоцитов, CD8 цитотоксических T-лимфоцитов, CD19 B-лимфоцитов и CD56 естественных клеток-киллеров с антителами, которые являются поверхностными маркерами, с помощью устройства для проточной цитометрии).
На фиг. 18 показано графическое представление влияния экзосомы граната на лейкоциты, активированные IL2, по настоящему изобретению (график определения CD4 хелперных T-лимфоцитов, CD8 цитотоксических T-лимфоцитов, CD19 B-лимфоцитов и CD56 естественных клеток-киллеров с антителами, которые являются поверхностными маркерами, с помощью устройства для проточной цитометрии).
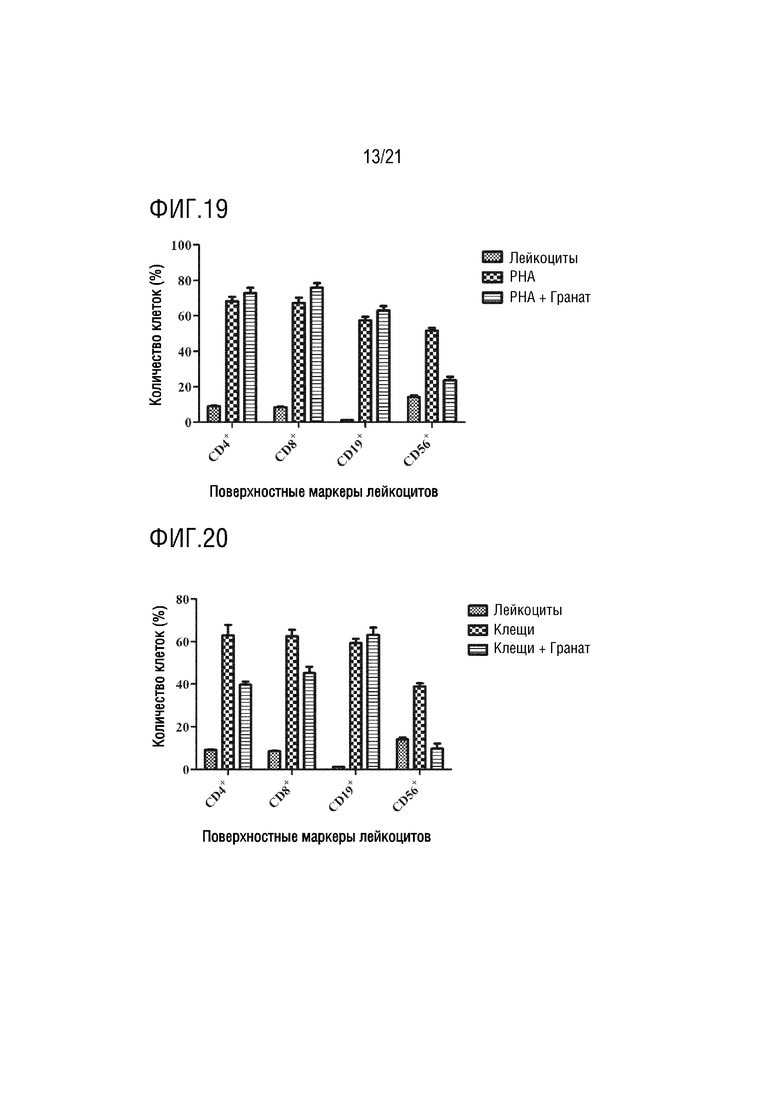
На фиг. 19 показано графическое представление влияния экзосомы граната на лейкоциты, активированные PHA, по настоящему изобретению (график определения CD4 хелперных T-лимфоцитов, CD8 цитотоксических T-лимфоцитов, CD19 B-лимфоцитов и CD56 естественных клеток-киллеров с антителами, которые являются поверхностными маркерами, с помощью устройства для проточной цитометрии).
На фиг. 20 показано графическое представление влияния экзосомы граната на лейкоциты, активированные аллергеном клещей, по настоящему изобретению (график определения CD4 хелперных T- лимфоцитов, CD8 цитотоксических T-лимфоцитов, CD19 B-лимфоцитов и CD56 естественных клеток-киллеров с антителами, которые являются поверхностными маркерами, с помощью устройства для проточной цитометрии).
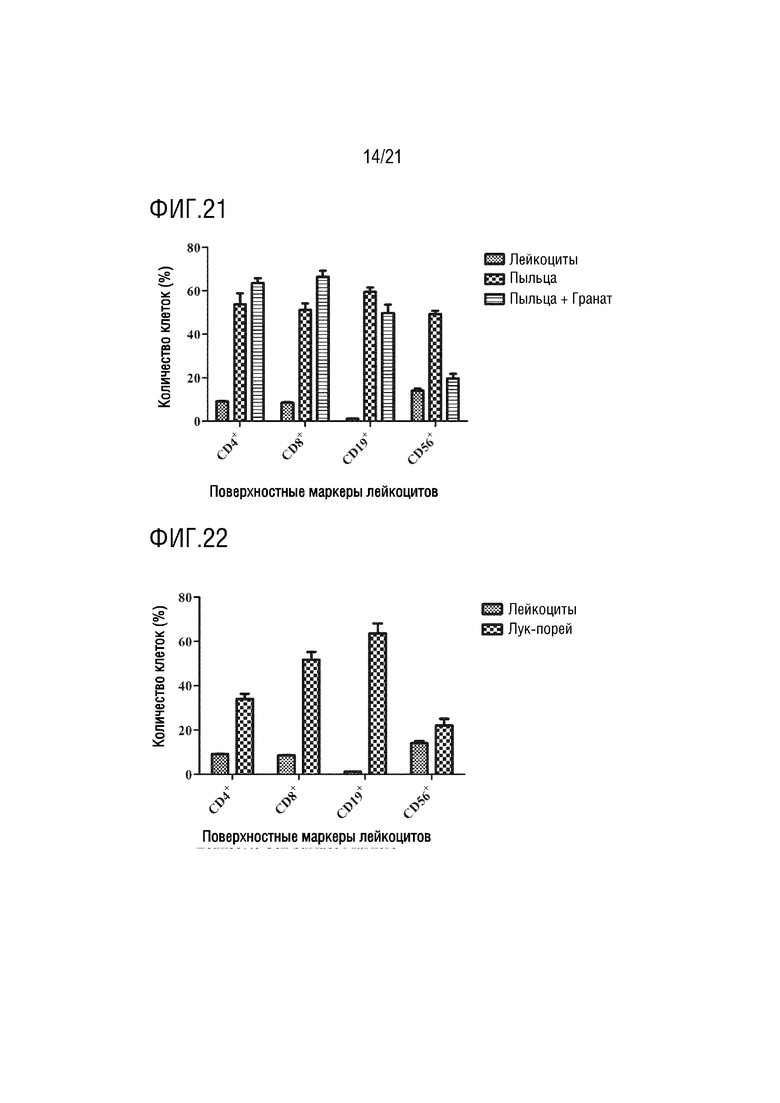
На фиг. 21 показано графическое представление влияния экзосомы граната на лейкоциты, активированные аллергеном пыльцы, по настоящему изобретению (график определения CD4 хелперных T- лимфоцитов, CD8 цитотоксических T-лимфоцитов, CD19 B-лимфоцитов и CD56 естественных клеток-киллеров с антителами, которые являются поверхностными маркерами, с помощью устройства для проточной цитометрии).
На фиг. 22 показано графическое представление влияния экзосомы лука-порея на лейкоциты по настоящему изобретению (график определения CD4 хелперных T-лимфоцитов, CD8 цитотоксических T-лимфоцитов, CD19 B-лимфоцитов и CD56 естественных клеток-киллеров с антителами, которые являются поверхностными маркерами, с помощью устройства для проточной цитометрии).
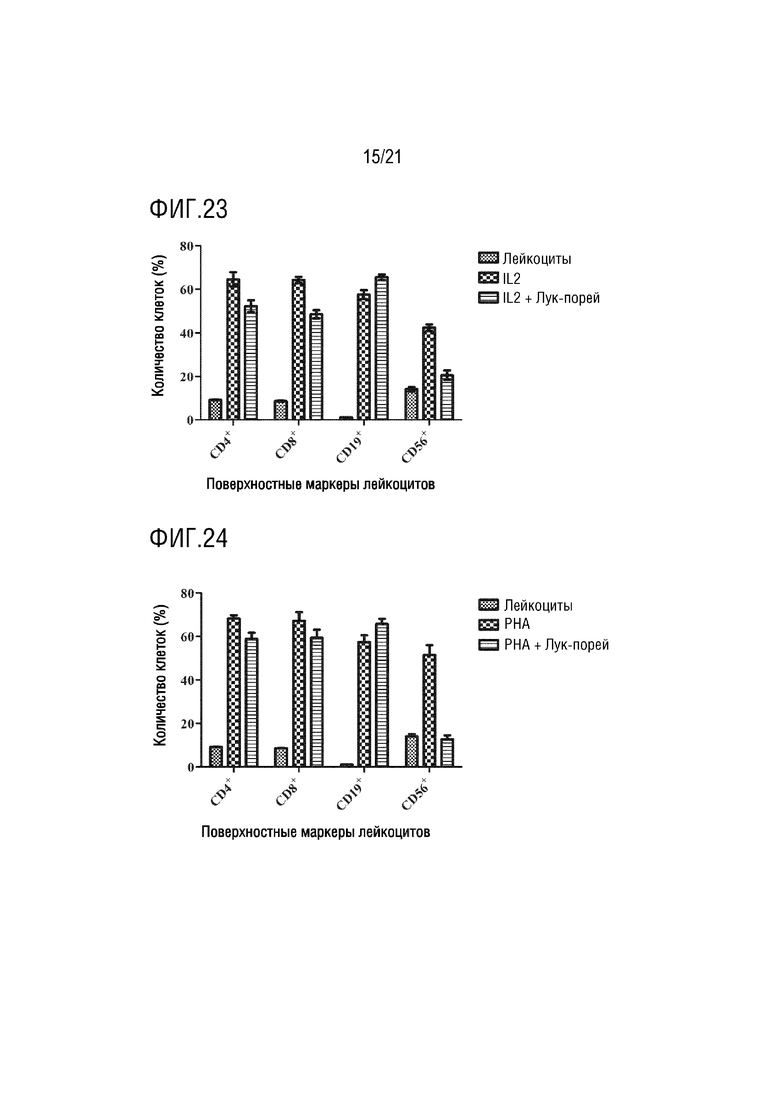
На фиг. 23 показано графическое представление влияния экзосомы лука-порея на лейкоциты, активированные IL2, по настоящему изобретению (график определения CD4 хелперных T- лимфоцитов, CD8 цитотоксических T-лимфоцитов, CD19 B-лимфоцитов и CD56 естественных клеток-киллеров с антителами, которые являются поверхностными маркерами, с помощью устройства для проточной цитометрии).
На фиг. 24 показано графическое представление влияния экзосомы лука-порея на лейкоциты, активированные PHA, по настоящему изобретению (график определения CD4 хелперных T- лимфоцитов, CD8 цитотоксических T-лимфоцитов, CD19 B-лимфоцитов и CD56 естественных клеток-киллеров с антителами, которые являются поверхностными маркерами, с помощью устройства для проточной цитометрии).
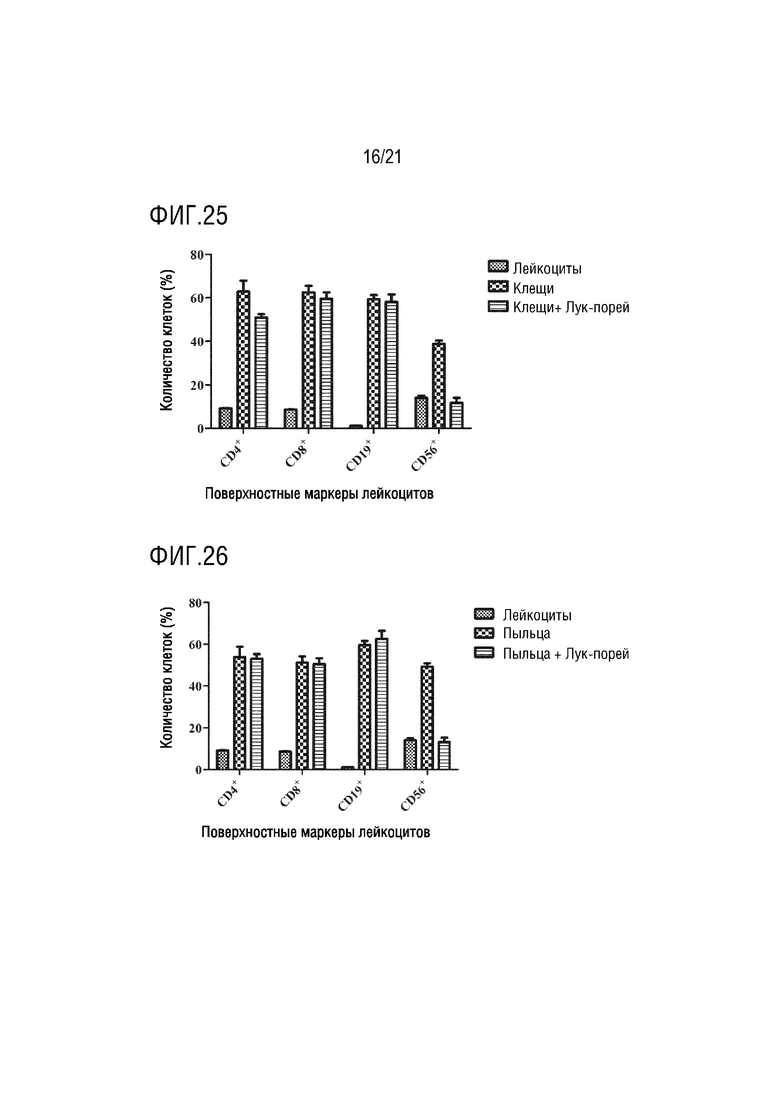
На фиг. 25 показано графическое представление влияния экзосомы лука-порея на лейкоциты, активированные аллергеном клещей, по настоящему изобретению (график определения CD4 хелперных T- лимфоцитов, CD8 цитотоксических T-лимфоцитов, CD19 B-лимфоцитов и CD56 естественных клеток-киллеров с антителами, которые являются поверхностными маркерами, с помощью устройства для проточной цитометрии).
На фиг. 26 показано графическое представление влияния экзосомы лука-порея на лейкоциты, активированные аллергеном пыльцы по настоящему изобретению (график определения CD4 хелперных T- лимфоцитов, CD8 цитотоксических T-лимфоцитов, CD19 B-лимфоцитов и CD56 естественных клеток-киллеров с антителами, которые являются поверхностными маркерами, с помощью устройства для проточной цитометрии).
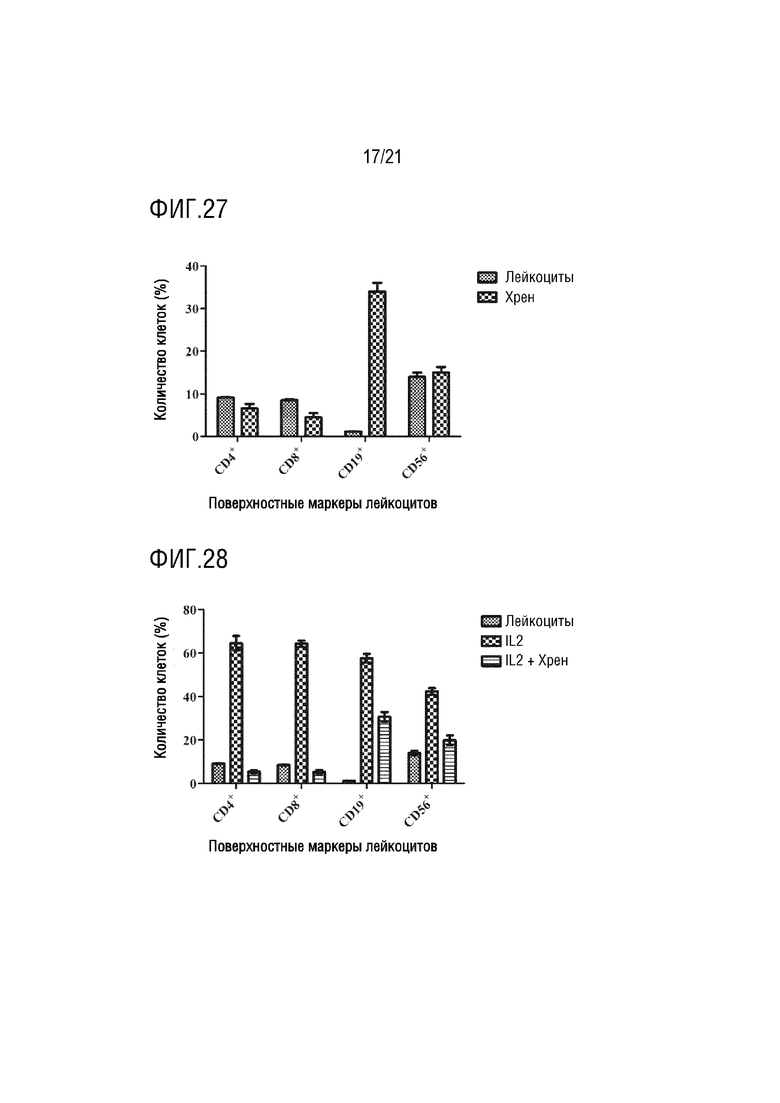
На фиг. 27 показано графическое представление влияния экзосомы хрена на лейкоциты по настоящему изобретению (график определения CD4 хелперных T-лимфоцитов, CD8 цитотоксических T-лимфоцитов, CD19 B-лимфоцитов и CD56 естественных клеток-киллеров с антителами, которые являются поверхностными маркерами, с помощью устройства для проточной цитометрии).
На фиг. 28 показано графическое представление влияние экзосомы хрена на лейкоциты, активированные IL2, по настоящему изобретению (график определения CD4 хелперных T-лимфоцитов, CD8 цитотоксических T-лимфоцитов, CD19 B-лимфоцитов и CD56 естественных клеток-киллеров с антителами, которые являются поверхностными маркерами, с помощью устройства для проточной цитометрии).
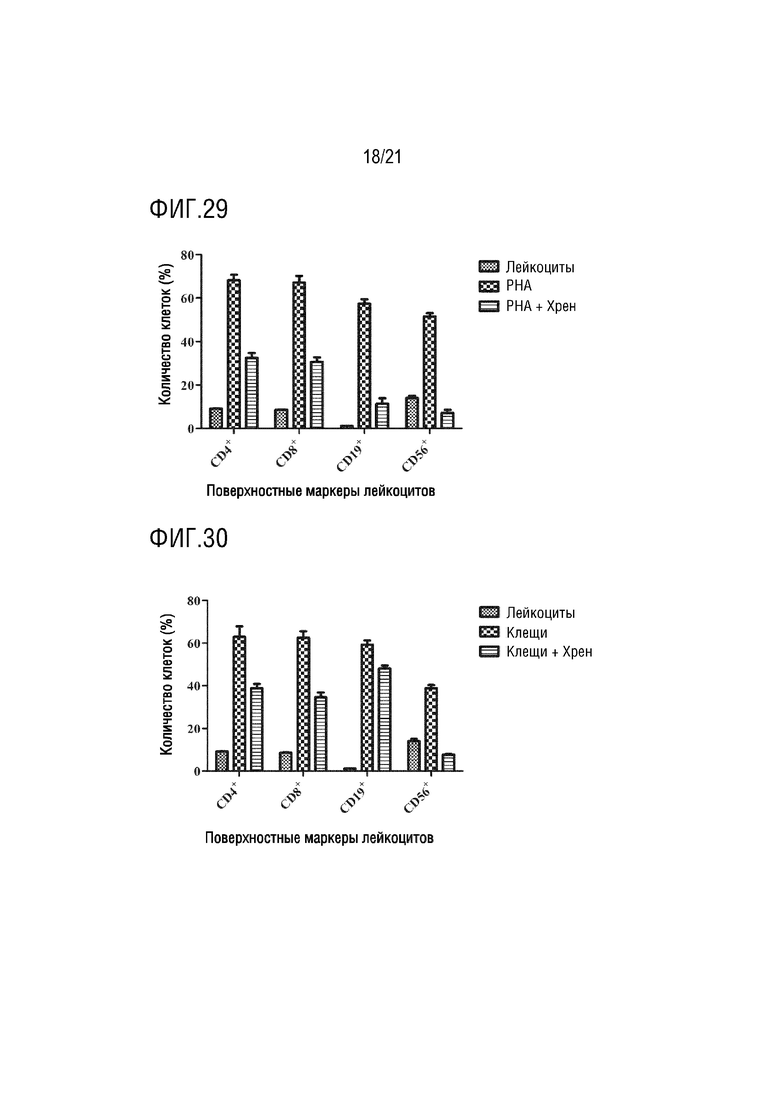
На фиг. 29 показано графическое представление влияния экзосомы хрена на лейкоциты, активированные PHA по настоящему изобретению (график определения CD4 хелперных T-лимфоцитов, CD8 цитотоксических T-лимфоцитов, CD19 B-лимфоцитов и CD56 естественных клеток-киллеров с антителами, которые являются поверхностными маркерами, с помощью устройства для проточной цитометрии).
На фиг. 30 показано графическое представление влияния экзосомы хрена на лейкоциты, активированные аллергеном клеща, по настоящему изобретению (график определения CD4 хелперных T- лимфоцитов, CD8 цитотоксических T-лимфоцитов, CD19 B-лимфоцитов и CD56 естественных клеток-киллеров с антителами, которые являются поверхностными маркерами, с помощью устройства для проточной цитометрии).
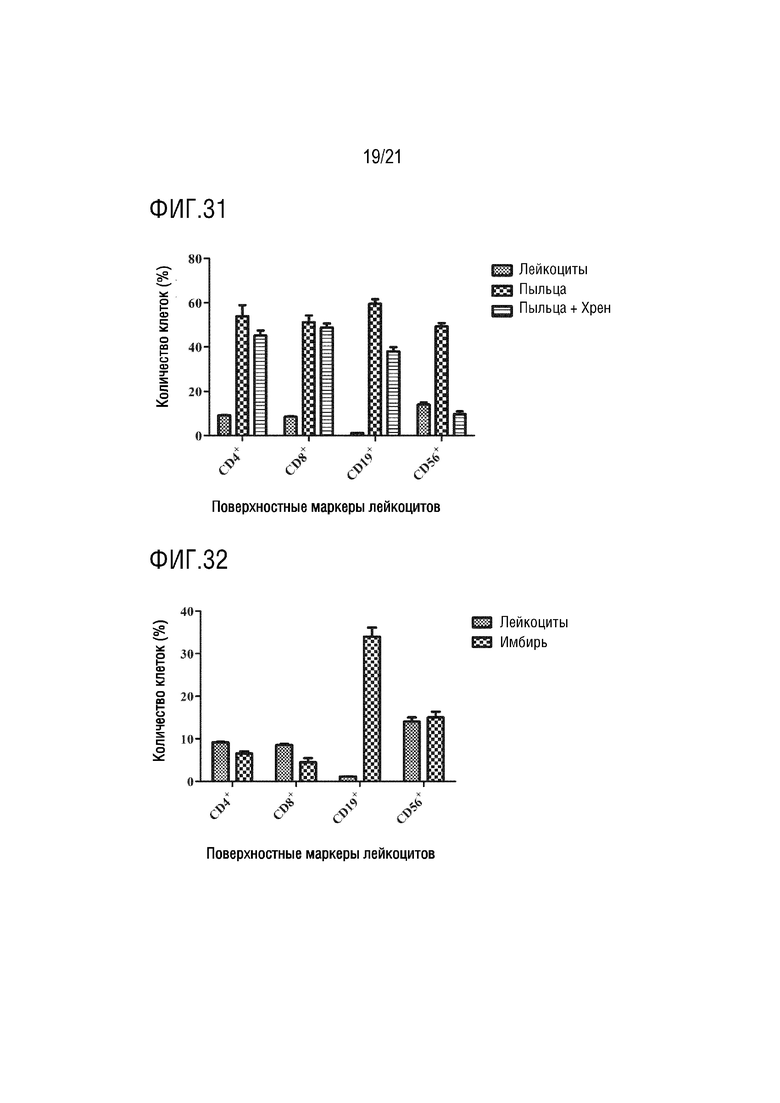
На фиг. 31 показано графическое представление влияния экзосомы хрена на лейкоциты, активированные аллергеном пыльцы, по настоящему изобретению (график определения CD4 хелперных T- лимфоцитов, CD8 цитотоксических T-лимфоцитов, CD19 B-лимфоцитов и CD56 естественных клеток-киллеров с антителами, которые являются поверхностными маркерами, с помощью устройства для проточной цитометрии).
На фиг. 32 показано графическое представление влияния экзосомы имбиря на лейкоциты по настоящему изобретению (график определения CD4 хелперных T-лимфоцитов, CD8 цитотоксических T-лимфоцитов, CD19 B-лимфоцитов и CD56 естественных клеток-киллеров с антителами, которые являются поверхностными маркерами, с помощью устройства для проточной цитометрии.
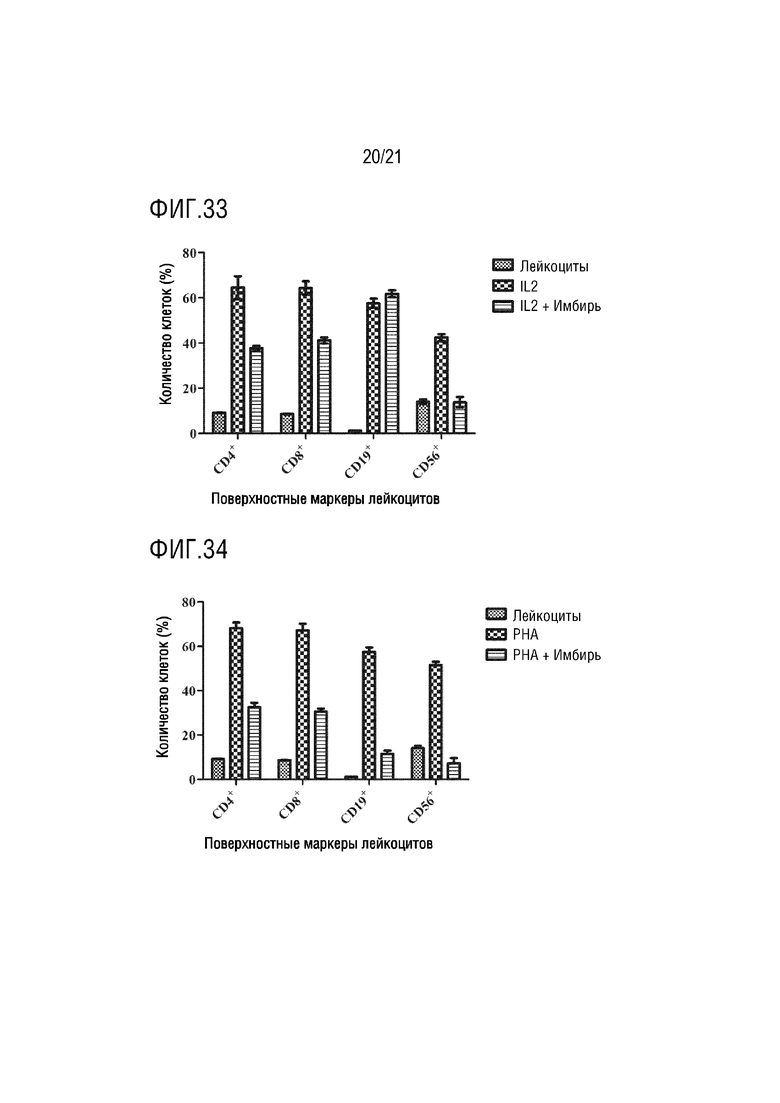
На фиг. 33 показано графическое представление влияния экзосомы имбиря на лейкоциты, активированные IL2, по настоящему изобретению (график определения CD4 хелперных T-лимфоцитов, CD8 цитотоксических T-лимфоцитов, CD19 B-лимфоцитов и CD56 естественных клеток-киллеров с антителами, которые являются поверхностными маркерами, с помощью устройства для проточной цитометрии).
На фиг. 34 показано графическое представление влияния экзосомы имбиря на лейкоциты, активированные PHA, по настоящему изобретению (график определения CD4 хелперных T-лимфоцитов, CD8 цитотоксических T-лимфоцитов, CD19 B-лимфоцитов и CD56 естественных клеток-киллеров с антителами, которые являются поверхностными маркерами, с помощью устройства для проточной цитометрии).
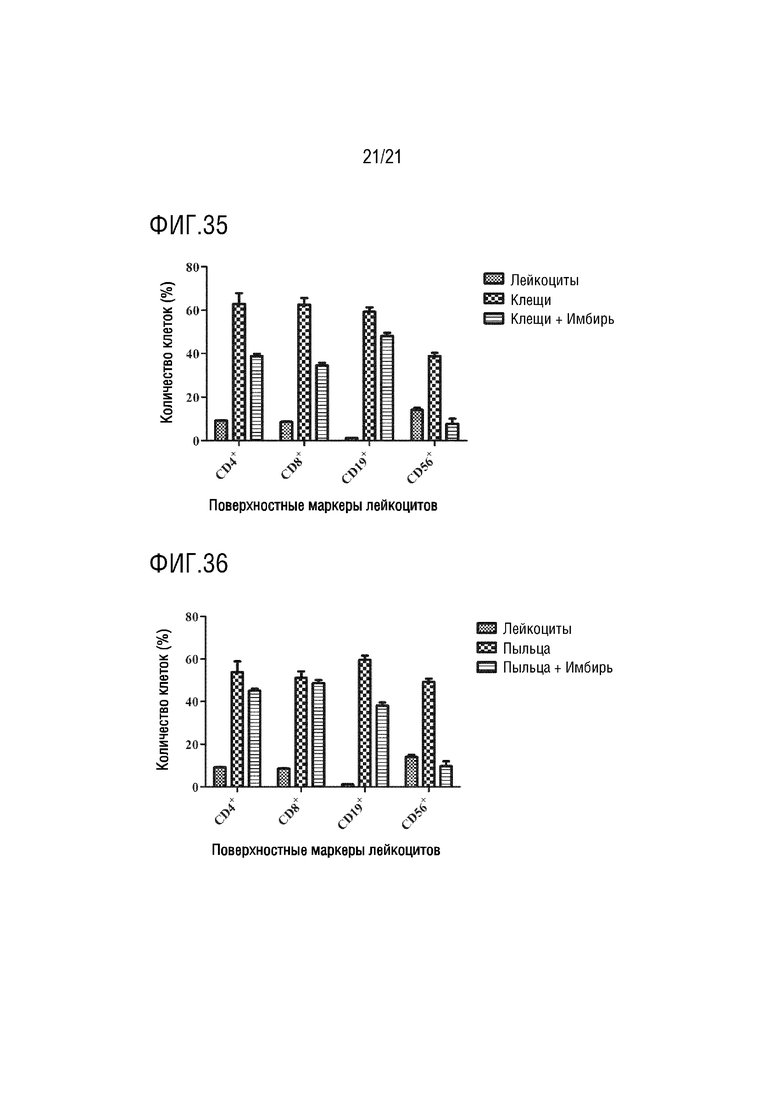
На фиг. 35 показано графическое представление влияния экзосомы имбиря на лейкоциты, активированные аллергеном клещей, по настоящему изобретению (график измерения CD4 хелперных T- лимфоцитов, CD8 цитотоксических T-лимфоцитов, CD19 B-лимфоцитов и CD56 естественных клеток-киллеров с антителами, которые являются поверхностными маркерами, с помощью устройства для проточной цитометрии).
На фиг. 36 показано графическое представление влияния экзосомы имбиря на лейкоциты, активированные аллергеном пыльцы по настоящему изобретению (график определения CD4 хелперных T- лимфоцитов, CD8 цитотоксических T-лимфоцитов, CD19 B-лимфоцитов и CD56 естественных клеток-киллеров с антителами, которые являются поверхностными маркерами, с помощью устройства для проточной цитометрии).
Предметом настоящего изобретения является применение экзосом растений, выделенных из растительных лизатов, в качестве стимуляторов, супрессоров и модуляторов иммунной системы при заболеваниях, оказывающих отрицательное влияние на иммунную систему. Экзосомы растений по настоящему изобретению представляют собой экзосомы растительного происхождения, которые позволяют профилактировать и лечить заболевания посредством стимуляции, супрессии и модуляции клеток иммунной системы.
Действие экзосом растений по настоящему изобретению на иммунную систему основано на их влиянии на деление клеток иммунной системы. Экзосомы растений, которые активируют иммунную систему, стимулируют клетки иммунной системы, способствуя их пролиферации, тем самым усиливая иммунный ответ. С другой стороны, экзосомы растений, оказывающие супрессивное действие, делают клетки иммунной системы нечувствительными к делению, тем самым подавляя ответ иммунной системы. Такие эффекты экзосом, обсуждаемых в изобретении, показаны в данных, представленных изменениями в поверхностных белках клеток иммунной системы, к которым они применяются (CD 8, CD 19 и CD 56).
В рамках настоящего изобретения, экзосомы растений применяются в основном при аутоиммунных заболеваниях, а также при трансплантации клеток, тканей, органов и при болезни «трансплантат против хозяина» в качестве стимуляторов, супрессоров или, при необходимости, в качестве модуляторов иммунной системы, выполняющих обе первые две функции.
В рамках настоящего изобретения, экзосомы растений получают, по меньшей мере, из одной части растения, выбранной из группы, состоящей из цельного растения, плода, листа, семени, корня или дифференцированных тканей, таких как среда для культивирования растения, стволовые клетки, отходные вещества, скорлупа или флоэма. Культура тканей растений является предпочтительным источником, из которого получают экзосомы растений, с получением экзосом в концентрации в 5 раз выше, чем концентрация экзосом, полученных из аналогичных растений, и для поддержания содержания и свойств полученных экзосом в течение длительного времени, тем самым предотвращая их воздействие на выращивание растений, сбор урожая, транспортировку и т. д.
Экзосомы растений по настоящему изобретению трансфектируют, чтобы дать возможность клеткам в культуре ткани растений продуцировать белки, стимулирующие, супрессирующие или модулирующие иммунную систему. Трансфекция представляет собой перенос чужеродного гена в клетку. Трансфекция клеток в культуре растений может позволить им продуцировать целевые белки, и экзосомы, секретируемые этими клетками, могут, таким образом, содержать эти белки.
В рамках настоящего изобретения, экзосомы растений выделяют способом выделения, выбранным из группы, состоящей из выделения с помощью двухфазной жидкой системы, градиентного центрифугирования, ультрафильтрации, хроматографических методов, выделения на основе полимера и выделения с помощью микрогранул. Среди них наиболее чистое выделение экзосом достигается выделением с помощью двухфазной жидкой системы, и, следовательно, этот способ выделения является предпочтительным в рамках настоящей заявки.
Экзосомы растительного происхождения по настоящему изобретению используются в основном при аутоиммунных заболеваниях и при трансплантации клеток, тканей, органов, при болезни «трансплантат против хозяина» и заболеваниях, при которых поражается иммунная система, таких как ревматоидный артрит, ювенильный ревматоидный артрит, системная красная волчанка, склероз, синдром Шегрена, диабет 1 типа, аллергическая астма, гранулематоз Вегенера, рассеянный склероз, болезнь Крона, псориаз, болезнь Грейвса, целиакия, очаговая алопеция (пелада), васкулит центральной нервной системы, тиреоидит Хашимото, миастения гравис, синдром Гудпасчера, аутоиммунная гемолитическая анемия, синдром Гийена-Барре, узелковый полиартериит, идиопатическая тромбоцитарная пурпура, височный артериит, первичный билиарный цирроз, болезнь Аддисона, анкилозирующий спондилит, синдром Рейтера, артериит Такаясу и витилиго, в качестве супрессоров, при необходимости, в качестве модуляторов иммунной системы, выполняющих обе первые две функции. Экзосомы растительного происхождения вводят перорально, интраназально, внутривенно, внутримышечно, внутрикожно, местно, внутрибрюшинно и инъекцией для введения пациенту эффективной дозы выбранных экзосом растений для лечения заболеваний, опосредованных иммунной системой. Они также используются для переноса иммуномодулирующих препаратов, в качестве адъюванта при вакцинации и в качестве пищевой добавки с целью модуляции иммунной системы.
Способ выделения с помощью двухфазной жидкой системы, используемый для выделения экзосом растений по настоящему изобретению, включает следующие стадии:
- разрушение растения, экзосому которого требуется выделить, с помощью гомогенизатора для получения его лизата,
- центрифугирование со скоростью перемешивания от 2000 g до 10000 g в течение 5-20 мин для выделения экзосом из растительного лизата,
- удаление частиц размером 220 нм и выше фильтрованием после центрифугирования,
- перенос смеси экзосома-белок, полученной центрифугированием, в двухфазную жидкую систему, содержащую фазу PEG и фазу DEX, для их разделения,
- удаление неэкзосомальных белков, клеточного жира и других примесей из экзосом за счет использования химического сродства фазы PEG к белкам и фазы DEX к фосфолипидным структурированным мембранам,
- получение выделенных экзосом.
Настоящее изобретение предназначено для применения эффектов экзосом растений на иммунную систему в качестве стимуляторов, супрессоров и модуляторов иммунной системы при заболеваниях. В рамках настоящего изобретения, иммуномодулирующие эффекты экзосом растений используются в основном при аутоиммунных заболеваниях, а также при трансплантации клеток, тканей, органов и при таких заболеваниях, как болезнь «трансплантат против хозяина», в качестве стимуляторов, супрессоров иммунной системы или, при необходимости, в качестве модуляторов, выполняющих обе первые две функции. Эффекты экзосом растений могут варьироваться в зависимости от растения, из которого экзосома выделена. Несмотря на то, что это может быть цельное растение, плод, лист, семя и корень, они также могут быть дифференцированными тканями, такими как среда для культивирования растения, стволовые клетки, отходные вещества, скорлупа или флоэма. Экзосомы растений можно выделить многими методами, такими как выделение с помощью двухфазной жидкой системы, градиентное центрифугирование, ультрафильтрация, хроматографические методы, выделение на основе полимера и выделение с помощью микрогранул. Экзосомы, использованные в исследовании, проведенном в рамках настоящего изобретения, выделены из растений, приведенных в таблице 1.
Растения, используемые для выделения экзосом по изобретению
Частицы большого размера, образующиеся в результате дезинтеграции растений в результате центрифугирования, выполняемого со скоростью 2000 g и 10000 g в течение 5-20 мин для выделения экзосом из растительного лизата, не приводят к появлению каких-либо примесей в фазе декстрана при осаждении при центрифугировании, применяемого во время двухфазного процесса разделения и их массы. Кроме того, гарантируется, что фильтр, который используется в процессе фильтрации для удаления частиц размером 220 нм и выше, не засоряется. Экзосомы отделяют от неэксосомальных белков, клеточных жиров и других примесей за счет использования химического сродства фазы PEG к белкам и фазы DEX к фосфолипидным структурированным мембранам в двухфазной жидкой системе. Фаза DEX, образованная за счет концентраций полимеров, используемых в растворе, разделяет экзосомы.
Экспериментальные исследования
Выделенные экзосомы метятся антителами к поверхностным маркерам CD9, CD63 и HSP70, которые переносятся экзосомами, и экзосомы, несущие эти маркеры, определяются на устройстве для проточной цитометрии. В то же время, размеры экзосом, выделенных с помощью устройства Zeta Sizer, также измеряются (фиг. 1-6).
Выделение лейкоцитов проводится для определения влияния экзосом растений на клетки крови. Кровь, внесенную в пробирку, содержащую ЭДТА, или раствор, обеспечивающий свертывание крови, смешивают с PBS в соотношении 1:1 по объему. Смесь осторожно выливают на раствор фиколла в другой пробирке, не перемешивая фазы. Пробирку, содержащую кровь, PBS и фиколл, центрифугируют в течение 15 мин примерно при 3000 об/мин. После центрифугирования белый промежуточный слой, содержащий лейкоциты, между верхней плазмой и фиколлом, отбирают и переносят в чистую пробирку, и ее промывают, добавляя к ней примерно 10 мл PBS. Клетки снова центрифугируют при 1500 об/мин в течение 5 мин. Клеточный осадок удаляют, и лейкоциты культивируют в среде. Эти выделенные лейкоциты включают клетки, которые играют роль в иммунной системе, такие как Т-клетки, В-клетки, естественные клетки-киллеры и дендритные клетки.
Клетки, культивированные в среде, инкубируют с IL2, PHA, аллергенами клещей и аллергенами пыльцы, тем самым активируя клетки иммунной системы. Выделенные экзосомы растений доставляют в активированные и неактивированные клетки крови. Для демонстрации эффектов экзосом растений на лейкоциты, определяют процент клеток крови, меченных антителами к CD4, CD8, CD19 и CD56, на устройстве для проточной цитометрии. Эффект экзосом ревеня с бородавчатыми листьями на клетки крови показан на фиг. 7, их влияние на клетки крови, активированные IL2, показано на фиг. 8, их влияние на клетки крови, активированные PHA, показано на фиг. 9, их влияние на клетки крови, активированные аллергеном клещей, показаны на фиг. 10, и их влияние на клетки крови, активированные аллергеном пыльцы, показано на фиг.11. Эффект экзосом сельдерея на клетки крови показан на фиг. 12, их влияние на клетки крови, активированные IL2, показано на фиг. 13, их влияние на клетки крови, активированные PHA, показано на фиг. 14, их влияние на клетки крови, активированные аллергеном клещей, показано на фиг. 15, и их влияние на клетки крови, активированные аллергеном пыльцы, показано на фиг. 16. Эффект экзосом граната на клетки крови показан на фиг. 17, их влияние на клетки крови, активированные IL2, показано на фиг. 18, их влияние на клетки крови, активированные PHA, показано на фиг. 19, их влияние на клетки крови, активированные аллергеном клещей, показано на фиг. 20, и их влияние на клетки крови, активированные аллергеном пыльцы, показано на фиг. 21. Эффект экзосом лука-порея на клетки крови показано на фиг. 22, их влияние на клетки крови, активированные IL2, показано на фиг. 23, их влияние на клетки крови, активированные PHA, показано на фиг. 24, их влияние на клетки крови, активированные аллергеном клещей, показано на фиг. 25, и их влияние на клетки крови, активированные аллергеном пыльцы, показано на фиг. 26. Эффект экзосом хрена на клетки крови показан на фиг. 27, их влияние на клетки крови, активированные IL2, показано на фиг. 28, их влияние на клетки крови, активированные PHA, показано на фиг. 29, их влияние на клетки крови, активированные аллергеном клещей, показано на фиг. 30, и их влияние на клетки крови, активированные аллергеном пыльцы показано на фиг. 31. Эффект экзосом имбиря на клетки крови показан на фиг. 32, их влияние на клетки крови, активированные IL2, показано на фиг. 33, их влияние на клетки крови, активированные PHA, показано на фиг. 34, их влияние на клетки крови, активированные аллергеном клещей, показано на фиг. 35, и их влияние на клетки крови, активированные аллергеном пыльцы, показано на фиг. 36.
В рамках настоящего изобретения, преимущества применения эффектов экзосом растений на иммунную систему в качестве стимуляторов, супрессоров и модуляторов иммунной системы при заболеваниях можно перечислить следующим образом:
- экзосомы имеют полностью растительное происхождение,
- стимуляция выше, чем с аналогичными активаторами (IL2), и более успешна, чем в веществами, полученными в виде аналогичных химических соединений,
- их можно недорого получить в больших количествах,
- степень супрессии активации клеток крови выше, чем с веществами, полученными в виде аналогичных химических соединений,
- они не обладают токсическим действием на печень и другие органы, как другие лекарственные средства, так как они полностью растительного происхождения,
- они представляют собой продукт растительного происхождения, который можно использовать вместо лечения стволовыми клетками, которое используется для супрессии иммунной системы при трансплантации тканей и органов,
- поскольку они не содержат примесей растительного, животного или химического происхождения, то побочные эффекты за счет указанных примесей не возникают,
- применение этих экзосом заменяет использование таких элементов, как алюминий, который, как известно, токсичен для организма в случае избыточного применения.
Ссылки
1. Ludwig A. K. and B. Giebel (2012). «Exosomes: small vesicles participating in intercellular communication», Int. J. Biochem. Cell Biol., 44(1): 11-15.
2. Iraci N., T. Leonardi F. Gessler, B. Vega and S. Pluchino (2016). «Focus on Extracellular Vesicles: Physiological Role and Signalling Properties of Extracellular Membrane Vesicles», Int. J. Mol. Sci., 17(2): 171.
3. Stegmayr B. and G. Ronquist (1982). «Promotive effect on human sperm progressive motility by prostasomes», Urol. Res., 10(5): 253-257.
4. Gupta A, Punatar S, Mathew L, Kannan S, Khattry N. Cyclosporine Plus Methotrexate or Cyclosporine Plus Mycophenolate Mofetil as Graft Versus Host Disease Prophylaxis in Acute Leukemia Transplant: Comparison of Toxicity, Engraftment Kinetics and Transplant Outcome. Indian Journal of Hematology & Blood Transfusion. 2016;32(3):248-256. doi:10.1007/s12288-015-0577-3.
| название | год | авторы | номер документа |
|---|---|---|---|
| ЭКЗОСОМА, ВЫДЕЛЕННАЯ ИЗ СЕПТАЛЬНОГО ХРЯЩА, ИСПОЛЬЗОВАННАЯ ДЛЯ ПОЛУЧЕНИЯ ХРЯЩЕВОЙ ТКАНИ | 2019 |
|
RU2833888C2 |
| Способ прогнозирования неблагоприятного течения хронического посттравматического увеита после однократного проникающего хирургического вмешательства на глазном яблоке | 2020 |
|
RU2733745C1 |
| СПОСОБ ПОЛУЧЕНИЯ НЕДИФФЕРЕНЦИРОВАННОЙ КЛЕТКИ | 1996 |
|
RU2177996C2 |
| Способ диагностики аллергической бронхиальной астмы | 2021 |
|
RU2780687C1 |
| СПОСОБ ИЗМЕРЕНИЯ МИТОХОНДРИАЛЬНОЙ АКТИВНОСТИ ЛИМФОЦИТОВ | 2005 |
|
RU2302635C1 |
| СПОСОБ И КОМПОЗИЦИИ ДЛЯ КЛЕТОЧНОЙ ИММУНОТЕРАПИИ | 2012 |
|
RU2688185C2 |
| СПОСОБ ПОЛУЧЕНИЯ НЕДИФФЕРЕНЦИРОВАННОЙ КЛЕТКИ | 1996 |
|
RU2215539C2 |
| ПРИМЕНЕНИЕ LACTOBACILLUS ДЛЯ ЛЕЧЕНИЯ ВИРУСНЫХ ИНФЕКЦИЙ | 2006 |
|
RU2440123C2 |
| Способ ранней диагностики ревматоидного артрита | 2019 |
|
RU2735738C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ В-КЛЕТОЧНОЙ НЕХОДЖКИНСКОЙ ЛИМФОМЫ | 2023 |
|
RU2831405C1 |
Изобретение относится к области применению экзосом, полученных из растений, для стимуляции, супрессии и модуляции иммунной системы, причем растение представляет собой ревень, сельдерей, гранат, лук-порей или хрен. Вышеописанное изобретение позволяет применять экзосомы растений, выделенных из лизатов растений, в качестве стимуляторов, супрессоров и модуляторов иммунной системы. 6 з.п. ф-лы, 36 ил., 1 табл.
1. Применение экзосом, полученных из растений, для стимуляции, супрессии и модуляции иммунной системы, причем растение представляет собой ревень, сельдерей, гранат, лук-порей или хрен.
2. Применение по п.1 в котором экзосомы получены по меньшей мере из одной части растения, выбранной из группы, состоящей из цельного растения, плода, листа, семени, корня или дифференцированных тканей, таких как среда для культивирования тканей растения, стволовые клетки, отходные вещества, скорлупа или флоэма.
3. Применение по п.1, в котором экзосомы выделяют способом выделения, выбранным из группы, состоящей из выделения с помощью двухфазной жидкой системы, градиентного центрифугирования, ультрафильтрации, хроматографических методов, выделения на основе полимера и выделения с помощью микрогранул.
4. Применение по п.1, где экзосомы, полученные из растений, вводят перорально, интраназально, внутривенно, внутримышечно, внутрикожно, местно, внутрибрюшинно и инъекцией для введения эффективной дозы экзосом выбранных растений пациенту для лечения опосредованных иммунной системой заболеваний.
5. Применение по п.1, в котором экзосомы используют для переноса иммуномодулирующих лекарственных средств.
6. Применение по п.1, в котором экзосомы используют в качестве адъювантов при вакцинации.
7. Применение по п.1, в котором экзосомы используют в качестве пищевой добавки с целью модуляции иммунной системы.
| WO 2018107061 A1, 14.06.2018 | |||
| MINGZHEN ZHANG et al/ Plant derived edible nanoparticles as a new therapeutic approach against diseases, Tissue Barriers, e1134415 DOI: 10.1080/21688370.2015.1134415 p.3 | |||
| JU S., MU J., DOKLAND T | |||
| et al | |||
| Grape exosome-like nanoparticles induce intestinal stem cells and protect mice from DSS-induced colitis // Mol |
Авторы
Даты
2023-10-31—Публикация
2019-09-03—Подача