ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится к области традиционной китайской медицины и, в частности, к композиции традиционной китайской медицины, способу ее приготовления и применению композиции традиционной китайской медицины при приготовлении лекарственного средства для предотвращения или лечения повышенного уровня липидов в крови, повышенного уровня триглицеридов, повышенного уровня холестерина, гиперлипидемии и атеросклероза.
УРОВЕНЬ ТЕХНИКИ
Липиды крови - это общий термин для различных липидных веществ в крови, наиболее важными из которых являются холестерин и триглицериды (также называемые нейтральным жиром). Другие важные липиды включают в себя липопротеины, которые включают липопротеины низкой плотности и липопротеины высокой плотности. Среднее содержание холестерина в крови у здоровых людей составляет 2,8–5,17 ммоль/л, и среднее содержание триглицеридов в крови - 0,56–1,7 ммоль/л. Либо повышенный уровень холестерина, либо повышенный уровень триглицеридов, либо сочетание этих двух патологических состояний можно назвать гиперлипидемией.
В «Отчете о хронических заболеваниях и питании жителей Китая», опубликованном Национальной комиссией здравоохранения и планирования семьи в начале 2015 г., указано, что заболеваемость дислипидемии в 2012 г. составляла 40,40% среди взрослых китайцев, что значительно больше по сравнению с 2002 г., когда заболеваемость гиперхолестеринемии составляла 4,9%, а заболеваемость гипертриглицеридемии - 13,1%. Эти данные указывают на широко распространенное состояние дислипидемии у жителей, что представляет собой серьезную проблему для предотвращения и лечения дислипидемии в Китае.
Атеросклероз (АС) является ведущей причиной ишемической болезни сердца, ишемического инсульта и заболеваний периферических сосудов. Гиперлипидемия является патологической основой атеросклероза и характеризуется накоплением липидов и сложных углеводов, кровоизлиянием, тромбозом и последующей гиперплазией фиброзной ткани и известковыми отложениями, начиная с внутренней оболочки артерий, и постепенным распадом и кальцинозом в средней оболочке пораженных артерий, что в конечном итоге приводит к утолщению и отвердению артериальной стенки и сужению просвета кровеносных сосудов. Такие патологические изменения часто затрагивают крупные и средние мышечные артерии, и как только изменения прогрессируют настолько, что закупоривают просвет артерий, кровоснабжаемые такими артериями ткани или органы подвергаются ишемии или некрозу. Липиды, аккумулирующиеся на внутренней оболочке артерий, имеют желтый цвет и атероматозный вид, поэтому их накопление называют атеросклерозом.
Атеросклеротическое сердечно-сосудистое заболевание известно как «основной убийца» в развитых странах, и заболеваемость им быстро растет в развивающихся странах. Атеросклероз является причиной большинства смертей от инфаркта миокарда и инсульта. Ожидается, что к 2035 году более 130 миллионов взрослых (45,1%) в США будут страдать от определенных сердечно-сосудистых заболеваний, при этом общие финансовые затраты составят до 1,1 триллиона долларов. Заболеваемость и смертность от сердечно-сосудистых заболеваний в Китае еще находятся на стадии возрастания. В Китае сердечно-сосудистые заболевания поражают около 290 млн человек и занимают первое место по смертности, составляя более 30% смертей от болезней. Конечно, гиперлипидемия не обязательно означает сердечно-сосудистое заболевание, но активное лечение гиперлипидемии является одной из важных мер для предотвращения сердечно-сосудистых заболеваний.
Правильная диета и надлежащие физические упражнения являются эффективными и необходимыми мерами для контроля и предотвращения повышения уровня липидов в крови и, таким образом, снижения вреда атеросклеротических сердечно-сосудистых заболеваний. Однако, когда диета и физические упражнения неэффективны, неизбежным выбором становится фармакотерапия.
В настоящее время в клинической практике применяют различные химические гиполипидемические агенты, которые в основном включают в себя статины и фибраты. Хотя конкретные механизмы действия этих препаратов различны, в основном они работают, непосредственно воздействуя на синтетические и метаболические пути жиров. Из-за высокой частоты рецидивов повышения уровня липидов в крови после прекращения лечения синтетические химические гиполипидемические агенты требуют длительного применения, что приводит к потере экономических ресурсов и значительно увеличивает вероятность проявления токсичности и неблагоприятных эффектов. Например, длительное применение часто связано с неблагоприятными эффектами различной степени тяжести, включая мышечные боли, нарушение функций печени и почек и т.п. Кроме того, применение химических гиполипидемических агентов не может принципиально предотвращать и контролировать развитие и прогрессирование роста сосудистых бляшек.
Гиполипидемические агенты на основе натуральных препаратов традиционной китайской медицины включают Dantian Jiangzhi Wan (Hongxing, Гуандун), Zhibituo (DIAO, Ченду), Xuezhikang (Weixin, Пекин) и т.п. Как видно из инструкций к этим препаратам, они имеют определенные неблагоприятные эффекты в той или иной степени. Например, неблагоприятные эффекты Xuezhikang включают желудочно-кишечный дискомфорт, такой как боль в животе, вздутие живота, изжога и т.п., а иногда могут включать обратимое повышение уровней сывороточной аминотрансферазы и креатинфосфокиназы. Кроме того, эти препараты обычно рекомендуются в литературе для комбинированного применения с химическими гиполипидемическими агентами или для применения у пожилых людей и т.д.
Поэтому по-прежнему существует острая клиническая потребность в препаратах традиционной китайской медицины для эффективного предотвращения и лечения повышенного уровня липидов в крови, повышенного уровня триглицеридов, повышенного уровня холестерина и гиперлипидемии. Между тем в настоящее время не существует методов предотвращения и контроля сосудистых бляшек и лечения атеросклероза на основе препаратов традиционной китайской медицины. Поэтому на них существует большой социальный и рыночный спрос.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение направлено на создание композиции традиционной китайской медицины, способа ее приготовления и применения для получения лекарственного средства для предотвращения или лечения повышенного уровня липидов в крови, повышенного уровня триглицеридов, повышенного уровня холестерина, гиперлипидемии, атеросклероза и т.п. Исследования на моделях животных и клинические исследования показали, что композиция традиционной китайской медицины, описанная в данном документе, оказывает превосходные эффекты снижения уровня липидов в крови, снижения уровня холестерина и, в частности, снижения уровня триглицеридов в крови. Между тем исследования на моделях животных моделях и клинические исследования также показали, что композиция традиционной китайской медицины, описанная в данном документе, обладает хорошими эффектами замедления образования атеросклеротических бляшек и их удаления.
Автор настоящего изобретения предложил способ лечения после длительного изучения теории традиционной китайской медицины и основываясь на клинической практике, что значительно отличается от теорий современной медицины относительно предотвращения и лечения повышенного уровня липидов в крови, повышенного уровня триглицеридов, повышенного уровня холестерина, гиперлипидемии и атеросклероза. Считается, что основную причину гиперлипидемии и последующего атеросклероза можно обобщить, используя логику и язык традиционной китайской медицины следующим образом: задержка флегмы-жидкости в крови. Это похоже на понятие повышенной вязкости в контексте современной медицины. Повышенная вязкость является не только причиной гиперлипидемии и атеросклероза, но и нарушением, проявляющимся задержкой флегмы-жидкости в крови. Поскольку задержка флегмы-жидкости в крови в традиционной китайской медицине относится к понятию повышенной вязкости в современной медицине, считается, что виды модулирующей терапии являются основным и эффективным средством предотвращения и лечения гиперлипидемии и атеросклероза.
«Задержка флегмы-жидкости» определяется как влага, выходящая из меридианов в Классике внутренней медицины Желтого императора (The Yellow Emperor's Classic of Internal Medicine), т.е. жидкость организма в циркуляторном метаболизме. Более густые жидкости организма называются флегмой, а более разжиженные - жидкостью, которые в совокупности называются задержкой флегмы-жидкости. «Задержка флегмы-жидкости» в традиционной китайской медицине в основном относится к густой или разжиженной жидкости в пищеварительном тракте, легких и дыхательных путях, которая трудно метаболизируется и может непрерывно образовываться в пищеварительном тракте или дыхательных путях, даже если выводится из организма. Такие густые жидкости могут также перетекать из пищеварительного тракта и дыхательных путей и оставаться под кожей, в мышцах, в соединениях костей и даже во внутренних органах и головном мозге, приводя к различным образованиям, кистам и полипам. Даже опухоли считаются связанными с задержкой флегмы-жидкости в организме. Традиционная китайская медицина считает, что многие болезни связаны с такими густыми жидкостями, которые с трудом выводятся из организма или метаболизируются. Однако традиционная китайская медицина не обсуждает, что задержка флегмы-жидкости в крови вызывает ее повышенную вязкость.
В современной медицине понятие «повышенная вязкость» включает в себя десятки биохимических показателей. Например, оно может включать в себя некоторые показатели гиперлипидемии (общий холестерин сыворотки, холестерин низкой плотности, холестерин высокой плотности, транслипопротеины, триглицериды), некоторые показатели гипергликемии (глюкоза натощак, гликированный гемоглобин, инсулин натощак, С-пептид, гликированный белок сыворотки, фруктозамин), показатели тромбоцитов (количество тромбоцитов, адгезия тромбоцитов, оседание тромбоцитов и др.), некоторые показатели эритроцитов (количество эритроцитов, оседание эритроцитов, адгезия эритроцитов, гематокрит, деформируемость эритроцитов, размер эритроцитов), показатели повышенной вязкости (кажущаяся вязкость, относительная вязкость, приведенная вязкость, удельная вязкость и др.) и некоторые другие соответствующие показатели (фибриноген, иммуноглобулин и др.). Эти показатели имеют относительно сходное влияние на повышенную вязкость, но все же не все. Повышенная вязкость может иметь различные проявления. Современная медицина еще не определила подходящую и общепризнанную патогенетическую причину, а методы лечения повышенной вязкости по-прежнему являются терапией, ориентированной на показатель, например пероральные препараты для лечения гиперлипидемии и гипергликемии. Однако, поскольку проблема повышенной вязкости не решается фундаментально, гиполипидемический и гипогликемический эффекты являются короткими по продолжительности и не излечимыми, что требует длительного введения препаратов.
Задержка флегмы-жидкости в крови вызывает ее повышенную вязкость, что значительно повышает риск гиперлипидемии и гипергликемии, в дальнейшем вызывает атеросклероз, блокирует кровеносные сосуды, а затем вызывает заболевания сердца, головного мозга и почек. Основываясь на этой теории, в медицинской клинической практике авторы разработали композицию традиционной китайской медицины для эффективного и длительного снижения уровня липидов в крови, в частности снижения уровня триглицеридов, а также для эффективного предотвращения и лечения гиперлипидемии и атеросклероза.
В настоящем изобретении предлагается композиция традиционной китайской медицины, содержащая следующее сырье в весовых частях: 10–35 частей корня володушки, 5–25 частей незрелых плодов апельсина, 3–20 частей корня ревеня, 3–20 частей корня шлемника байкальского, 3–20 частей корня пиона белого, 3–15 частей сушеного имбиря, 5–20 частей пиявки, 3–20 частей корня солодки, 3–20 частей кодонопсиса, 3–20 частей корневища атрактилодеса большеголового и 3–25 частей клубня пинеллии.
Предпочтительно, композиция для традиционной китайской медицины содержит следующее сырье в весовых частях: 20–30 частей корня володушки, 10–20 частей незрелых плодов апельсина, 5–15 частей корня ревеня, 5–10 частей корня шлемника байкальского, 5–15 частей корня пиона белого, 5–10 частей сушеного имбиря, 7–15 частей пиявки, 5–15 частей корня солодки, 5–15 частей кодонопсиса, 5–15 частей корневища атрактилодеса большеголового и 10–20 частей клубня пинеллии.
Более предпочтительно, композиция традиционной китайской медицины, описанная в данном документе, дополнительно содержит следующее сырье в весовых частях: 3–45 частей, предпочтительно 10–35 частей, раковины устрицы. Более предпочтительно, исходя из этого, композиция традиционной китайской медицины, описанная в данном документе, дополнительно содержит следующее сырье в весовых частях: 3–15 частей, предпочтительно 5–12 частей, красного ферментированного риса.
Предпочтительно описанную в данном документе композицию традиционной китайской медицины готовят из сырья в весовых частях.
Более предпочтительно композицию традиционной китайской медицины, описанную в данном документе, готовят из следующего сырья в весовых частях: 25 частей корня володушки, 15 частей незрелых плодов апельсина, 10 частей корня ревеня, 6 частей корня шлемника байкальского, 10 частей корня пиона белого, 6 частей сушеного имбиря, 10 частей пиявки, 10 частей корня солодки, 10 частей кодонопсиса, 10 частей корневища атрактилодеса большеголового и 15 частей клубня пинеллии.
Более предпочтительно композицию традиционной китайской медицины, описанную в данном документе, готовят из следующего сырья в весовых частях: 25 частей корня володушки, 15 частей незрелых плодов апельсина, 10 частей корня ревеня, 6 частей корня шлемника байкальского, 10 частей корня пиона белого, 6 частей сушеного имбиря, 10 частей пиявки, 10 частей корня солодки, 10 частей кодонопсиса, 10 частей корневища атрактилодеса большеголового, 15 частей клубня пинеллии и 30 частей раковины устрицы.
Более предпочтительно композицию традиционной китайской медицины, описанную в данном документе, готовят из следующего сырья в весовых частях: 25 частей корня володушки, 15 частей незрелых плодов апельсина, 10 частей корня ревеня, 6 частей корня шлемника байкальского, 10 частей корня пиона белого, 6 частей сушеного имбиря, 10 частей пиявки, 10 частей корня солодки, 10 частей кодонопсиса, 10 частей корневища атрактилодеса большеголового, 15 частей клубня пинеллии, 30 частей раковины устрицы и 10 частей красного ферментированного риса.
В описанной выше композиции часть представляет собой весовую часть, а вес рассчитан на сырое лекарственное средство. В процессе изготовления навески могут пропорционально увеличивать или уменьшать. Например, при крупномасштабном изготовлении вес может быть выражен в килограммах или тоннах, может быть увеличен или уменьшен, но соотношение навесок лекарственного сырья между компонентами остается неизменным.
Введение родственного сырья по настоящему изобретению осуществляется следующим образом.
Корень володушки представляет собой высушенный корень Bupleurum Chinense DC. или Bupleurum scorzonerifolium Willd. Он гармонизирует внешний и внутренний аспекты, успокаивает печень и повышает ян.
Незрелый апельсин (или незрелый горький апельсин, незрелый сладкий апельсин, fructus aurantii immaturus) представляет собой высушенный молодой плод Citrus aurantium L. и его культурных разновидностей или Citrus × sinensis (сем. Rutaceae). Он оказывает влияние на устранение застоя флегмы и облегчение ощущения сдавления в груди и животе.
Корень ревеня представляет собой высушенные корень и корневище Rheum palmatum L., Rheum tanguticum Maxim. ex Balf. или Rheum officinale Baill. (сем. Polygonaceae). Он обладает эффектами уменьшения жара, расслабления кишечника, снижения температуры крови, противодействия токсичности, устранения стаза крови и стимуляции менструации.
Корень шлемника байкальского представляет собой высушенный корень Scutellaria baicalensis Georgi (сем. Labiatae). Он обладает эффектами купирования синдрома «влажности-тепла», снижения жара, противодействия токсинам, остановки кровотечения и предотвращения аборта.
Корень белого пиона представляет собой высушенный корень Paeonia lactiflora Pall. (сем. Ranunculaceae). Он успокаивает печень, снимает боль, питает кровь и регулирует менструацию, останавливает чрезмерное потоотделение и т.д.
Сушеный имбирь представляет собой сушеное корневище Zingiber officinale (Willd.) Rosc. (сем. Zingiberaceae). Имбирь собирают зимой, удаляя мочковатые корни и грязь, и сушат на солнце или при низкой температуре. Кусочки, нарезанные перед сушкой, называются «сушеными кусочками имбиря». Имбирь согревает тело изнутри, рассеивает холод, способствует восстановлению после коллапса, устраняет избыток влаги, растворяет флегму и т.д.
Пиявка представляет собой высушенный организм Whitmania pigra Whitman, Hirudo mipponica Whitman или Whitmania acranulata Whitman (сем. Hirudinidae). Пиявок отлавливают летом и осенью, умерщвляют кипятком и сушат на солнце или при низкой температуре. Они обладают эффектами разжижения крови, устраняют явления стаза крови и стимулируют менструацию.
Корень солодки представляет собой высушенные корень и корневище Glycyrrhiza uralensis Fisch. (травянистый многолетник из сем. Leguminosae). Он применяется для усиления функции селезенки, пополнения ци, удаления жара, противодействия токсичности, удаления флегмы и облегчения кашля, купирования спазматических болей и регуляции действия лекарственных средств в желудочно-кишечном тракте.
Кодонопсис представляет собой высушенный корень Codonopsis pilosula (Franch.) Nannf., Codonopsis pilosula Nannf. var. modesta (Nannf.) L.T. Shen или Codonopsis tangshen Oliv. (сем. Campanulaceae). Он обладает эффектом тонизирования ци и активизации функции селезенки и легких.
Корневище атрактилодеса большеголового представляет собой высушенное корневище Atractylodes macrocephala Koidz. (сем. Compositae). Оно обладает эффектами усиления функции селезенки, восполнения ци, устранения избытка влаги за счет диуреза и прекращении чрезмерного потоотделения.
Клубень пинеллии представляет собой высушенный клубень Pinellia ternata (Thunb.) Breit. (сем. Araceae). Он обладает эффектами купирования избытка влаги путем растворения флегмы, направления ци вниз для облегчения тошноты и рвоты, и устранения сдавления в груди и эпигастральной области.
Раковина устрицы представляет собой раковину Ostrea gigas Thunberg, Ostrea talienwhanensis Crosse или Ostrea rivularis Gould (сем. Osteridae). Она оказывает успокоительное действие, питает инь и подавляет избыток ян, смягчает твердые массы и устраняет узелки.
Красный ферментированный рис получают с помощью мицелия Monascus purpureus Went. (сем. Aspergillaceae), паразитирующего на зернах японского риса. Он оказывает укрепляющее действие на функцию селезенки, способствует пищеварению, активизирует кровообращение и устраняет стаз крови.
Рецепт по настоящему изобретению разработан путем объединения опыта клинической практики на основе полного исследования, описанного в «Трактате о болезнях, вызываемых холодом» (Treatise on Cold Damage Diseases), и соответствующих лекарственных веществ. В рецепте по настоящему изобретению корень володушки применяют в качестве основного лекарственного средства, и корень володушки очищает ци печени, так что функция печени может быть восстановлена до нормального уровня, что является ключом к метаболизму жира. Корень володушки также является очень хорошим лекарственным средством для иммунитета, уменьшения воспаления, снижения температуры и охлаждения. Он может регулировать иммунный механизм всего организма, играть ключевую роль в восстановлении некоторых ключевых гормонов для повторного разложения и балансировки липидов крови, а также оказывает хорошее влияние на функциональное восстановление тироксина. Корень ревеня является лекарственным средством, которое играет ключевую роль в очистке желудочно-кишечного тракта и устранении воспалений и вредной флоры в желудочно-кишечном тракте. Незрелый апельсиновый плод также является содействующим лекарственным средством, которое можно применять с корнем володушки для достижения надлежащей работы верхней и нижней части внутренних органов, а также с корнем ревеня для улучшения функций желудочно-кишечного тракта и устранения воспаления и вредной флоры в кишечном тракте. Корень шлемника байкальского также является содействующим лекарственным средством, которое применяют для уменьшения секреции желудочной кислоты и уменьшения уровня гастрина, а также для устранения воспаления в желудке и вредной флоры в кишечном тракте. Корень солодки, кодонопсис, корень пиона белого, корневище атрактилодеса большеголового и клубень пинеллии являются вспомогательными лекарственными средствами, которые применяют для выведения избыточной слизи в кишечнике и желудке, уменьшения поступления в кровь вязких веществ и снижения вязкости крови. Сушеный имбирь вместо имбиря применяют в рецептуре для уменьшения желудочно-кишечной реакции на ревень, так что рецептура подходит для среднесрочного и долгосрочного приема, и соблюдаются требования периода приема при лечении гиперлипидемии и артериальных бляшек. Пиявка, содержащаяся в рецептуре, применяется для активизации крови, устранения стаза, удаления накопления и вязкости различных тромбоцитов и эритроцитов в кровеносных сосудах, что способствует устранению бляшек в кровеносных сосудах. К рецептуре можно добавлять раковину устрицы, которая применяется для переваривания накопившихся и недостаточно переваренных веществ в кишечнике и желудке человека. В то же время раковина устрицы может способствовать успокоению переутомленной печени и лучшему перевариванию печеночного жира. К рецептуре можно добавлять красный ферментированной рис, который применяется для усиления эффекта расщепления холестерина, но он не является ключевым компонентом.
Активный ингредиент композиции традиционной китайской медицины, описанной в данном документе, может быть получен экстракцией или другими способами, известными в данной области техники. Активный ингредиент можно получать путем раздельной экстракции природного сырья составного лекарственного средства или путем совместной экстракции природного сырья составного лекарственного средства.
Предпочтительно его получают способом водной экстракции. Более предпочтительно, способ приготовления композиции традиционной китайской медицины, описанной в данном документе, включает: взвешивание сырья, добавление воды в количестве, в 4–12 раз превышающем количество сырья, и отваривание при 75–95 °C в течение 30–120 мин для получения первого отвара; добавление воды в количестве, в 3–10 раз превышающем количество сырья, и отваривание при температуре 75–95 °С в течение 30–120 мин с получением второго отвара; и объединение этих двух отваров, фильтрование и объединение фильтратов. Более предпочтительно, способ приготовления композиции традиционной китайской медицины, описанной в данном документе, включает: взвешивание сырья, добавление воды в количестве, в 8 раз превышающем количество сырья, и отваривание при 80 °C в течение 60 мин для получения первого отвара; добавление воды в количестве, в 6 раз превышающем количество сырья, и отваривание при температуре 80 °С в течение 60 мин с получением второго отвара; и объединение этих двух отваров, фильтрование и объединение фильтратов. Полученный экстракт может быть дополнительно сконцентрирован в виде мазевого экстракта, который может быть сухим мазевым экстрактом или жидким мазевым экстрактом. Предпочтительно его концентрируют при пониженном давлении (-0,05 МПа, 60 °С) до относительной плотности 1,05–1,15 (60 °С).
Описанная в данном документе композиция традиционной китайской медицины может быть приготовлена в виде препаратов путем добавления фармацевтически приемлемых носителей в соответствии с требованиями. Весовой процент экстрагированного или обработанного активного ингредиента композиции традиционной китайской медицины, описанной в данном документе, в препарате составляет 0,1–99,9%, а остальное составляет фармацевтически приемлемые носители.
Композиция традиционной китайской медицины, описанная в данном документе, может представлять собой любые фармацевтически приемлемые лекарственные формы, включая: отвар, таблетку, таблетку с сахарным покрытием, таблетку с пленочным покрытием, таблетку с кишечнорастворимым покрытием, капсулу, твердую капсулу, мягкую капсулу, жидкость для перорального применения, пастилку, гранулу, электуарий, пилюлю, мелкий порошок, мазь, пеллеты, суспензию, порошок, раствор, инъекцию, суппозиторий, мазь, пластырь, крем, спрей, капли и повязку. Предпочтительно композиция находится в лекарственной форме для перорального применения и еще более предпочтительно в форме отвара, капсулы, таблетки, пероральной жидкости, гранулы, пилюли, мелкого порошка, пеллет, мази и т.п. Наиболее предпочтительно композиция находится в форме отвара, гранул, капсул и таблеток.
Настоящее изобретение дополнительно относится к применению композиции традиционной китайской медицины для приготовления лекарственного средства для предотвращения или лечения повышенного уровня липидов в крови.
Настоящее изобретение дополнительно относится к применению композиции традиционной китайской медицины для приготовления лекарственного средства для предотвращения или лечения повышенного уровня триглицеридов.
Настоящее изобретение дополнительно относится к применению композиции традиционной китайской медицины для приготовления лекарственного средства для предотвращения или лечения повышенного уровня холестерина.
Настоящее изобретение дополнительно относится к применению композиции традиционной китайской медицины для приготовления лекарственного средства для предотвращения или лечения гиперлипидемии.
Настоящее изобретение дополнительно относится к применению композиции традиционной китайской медицины для приготовления лекарственного средства для предотвращения или контроля сосудистых бляшек.
Настоящее изобретение дополнительно относится к применению композиции традиционной китайской медицины для приготовления лекарственного средства для предотвращения или лечения атеросклероза.
Настоящее изобретение дополнительно относится к применению композиции традиционной китайской медицины для приготовления лекарственного средства для предотвращения или лечения хронических заболеваний обмена веществ.
Настоящее изобретение дополнительно относится к способу предотвращения или лечения повышенного уровня липидов в крови, включающему: введение нуждающемуся в этом человеку профилактически или терапевтически эффективного количества композиции традиционной китайской медицины, описанной в данном документе, как указано выше.
Настоящее изобретение дополнительно относится к способу предотвращения или лечения повышенного уровня триглицеридов, включающему: введение нуждающемуся в этом человеку профилактически или терапевтически эффективного количества композиции традиционной китайской медицины, описанной в данном документе, как указано выше.
Настоящее изобретение дополнительно относится к способу предотвращения или лечения повышенного уровня холестерина, включающему: введение нуждающемуся в этом человеку профилактически или терапевтически эффективного количества композиции традиционной китайской медицины, описанной в данном документе, как указано выше.
Настоящее изобретение дополнительно относится к способу предотвращения или лечения гиперлипидемии, включающему: введение нуждающемуся в этом человеку профилактически или терапевтически эффективного количества композиции традиционной китайской медицины, описанной в данном документе, как указано выше.
Настоящее изобретение дополнительно относится к способу предотвращения или контроля сосудистых бляшек, включающему: введение нуждающемуся в этом человеку профилактически или терапевтически эффективного количества композиции традиционной китайской медицины, описанной в данном документе, как указано выше.
Настоящее изобретение дополнительно относится к способу предотвращения или лечения атеросклероза, включающему: введение нуждающемуся в этом человеку профилактически или терапевтически эффективного количества композиции традиционной китайской медицины, описанной в данном документе, как указано выше.
Настоящее изобретение дополнительно относится к способу предотвращения или лечения хронических заболеваний обмена веществ, включающему: введение нуждающемуся в этом человеку профилактически или терапевтически эффективного количества композиции традиционной китайской медицины, описанной в данном документе, как указано выше.
Композицию традиционной китайской медицины, описанную в данном документе, можно вводить от одного до трех раз в сутки, и когда она приготовлена в виде стандартной дозы, каждый раз вводят 1–10 стандартных доз. После отваривания композиции традиционной китайской медицины, описанной в данном документе, в воде, отвар может быть сконцентрирован и высушен для приготовления порошка для получения сухого мазевого экстракта. Соответствующее количество вспомогательных веществ добавляли для приготовления гранулированного состава (каждая доза содержит 1250 мг порошка для получения сухого мазевого экстракта, что эквивалентно 20 г сырья). Гранулированный состав можно принимать от одного до трех раз в сутки по 1–2 дозы каждый раз. В альтернативном варианте, порошок для получения сухого мазевого экстракта также можно помещать в капсулы или готовить в форме таблеток (каждая доза содержит 312,5 мг порошка для получения сухого мазевого экстракта, что эквивалентно 5 г сырья). Капсулы или таблетки можно принимать от одного до трех раз в сутки по 2–8 капсул или таблеток каждый раз. Конкретное применение и доза могут быть скорректированы в соответствии с конкретным состоянием пациента.
Рецептура препарата традиционной китайской медицины по настоящему изобретению представляет собой инновационную конструкцию, основанную на теории и практике «задержки флегмы-жидкости в крови» и «Трактате о болезнях, вызываемых холодом». Изобретатель настоящего изобретения дополнительно оптимизировал соотношение компонентов на основе полного исследования и рассмотрения свойств и эффективности компонентов в данной рецептуре. В частности, рецептура по настоящему изобретению творчески содержит сушеный имбирь и пиявку в пропорциях, оптимизированных для клинической практики. Описанная в данном документе композиция традиционной китайской медицины оказывает очень значительное влияние на повышенную вязкость и оптимизирует общую вязкость крови двумя путями. Первый путь заключается в уменьшении вязкого вещества - задержки флегмы-жидкости в кишечнике и желудке и уменьшении причины повышенной вязкости за счет улучшения пищеварения в кишечнике и желудке, а также выделения. Второй путь заключается в непосредственном метаболизме органических компонентов повышенной вязкости, включая липиды крови, путем стимуляции метаболизма. Композиция традиционной китайской медицины, описанная в данном документе, также может снижать степень агрегации, степень оседания и степень разрезания эритроцитов, а также снижать степень агрегации, степень оседания и степень разрезания тромбоцитов. Клинические исследования продемонстрировали, что рецептура препарата традиционной китайской медицины по настоящему изобретению обладает превосходной эффективностью в снижении уровня липидов в крови, снижении уровня холестерина и, в частности, снижении уровня триглицеридов в крови, с уровнем ответа более 90%. Препарат оказывает значительное влияние на сильное повышение уровня триглицеридов в крови (триглицериды >5,6 ммоль/л), которое может быть снижено на 90% и более за короткое время (14 дней, один курс лечения). Рецептура препарата традиционной китайской медицины по настоящему изобретению обладает превосходной эффективностью, что также было подтверждено исследованиями на моделях животных, проведенными сторонними учреждениями. Кроме того, исследования продемонстрировали, что описанная в данном документе композиция традиционной китайской медицины также обладает хорошей эффективностью в отношении специфического замедления образования атеросклеротических бляшек и их удаления.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
Варианты осуществления настоящего изобретения подробно описаны ниже со ссылкой на прилагаемые графические материалы.
ФИГ. 1: сравнение полноразмерной аорты, окрашенной Oil Red O, у мышей ApoE-/- в группе отрицательного контроля по сравнению с группой контроля моделирования наличия атеросклеротических бляшек. A: репрезентативная картина окрашивания Oil Red O в группе отрицательного контроля; B: репрезентативная картина окрашивания Oil Red O в группе контроля моделирования после моделирования патологии.
ФИГ. 2: сравнение действия композиции традиционной китайской медицины, описанной в данном документе, на образование атеросклеротических бляшек у мышей ApoE-/- (полноразмерная аорта, окрашенная Oil Red O). A: репрезентативная картина окрашивания Oil Red O в группе отрицательного контроля; B: репрезентативная картина окрашивания Oil Red O в группе контроля моделирования; C: репрезентативная картина окрашивания Oil Red O в группе, получавшей композицию традиционной китайской медицины по 833 мг/кг; D: репрезентативная картина окрашивания Oil Red O в группе, получавшей композицию традиционной китайской медицины по 1677 мг/кг.
ФИГ. 3: сравнение действия композиции традиционной китайской медицины, описанной в данном документе, на образование атеросклеротических бляшек у мышей ApoE-/- (срез дуги аорты, окрашенный HE) в группе отрицательного контроля, группе контроля моделирования, группе положительного контроля, группе, получавшей композицию традиционной китайской медицины по 833 мг/кг, и группе, получавшей композицию традиционной китайской медицины по 1677 мг/кг.
ФИГ. 4: сравнение действия композиции традиционной китайской медицины, описанной в данном документе, на образование атеросклеротических бляшек у мышей ApoE-/- (срез дуги аорты, окрашенный Sirius) в группе отрицательного контроля, группе контроля моделирования, группе положительного контроля, группе, получавшей композицию традиционной китайской медицины по 833 мг/кг, и группе, получавшей композицию традиционной китайской медицины по 1677 мг/кг.
ФИГ. 5: сравнение действия композиции традиционной китайской медицины, описанной в данном документе, на образование атеросклеротических бляшек у мышей ApoE-/- (срез сонной артерии, окрашенный Oil Red O) в группе отрицательного контроля, группе контроля моделирования, группе положительного контроля, группе, получавшей композицию традиционной китайской медицины по 833 мг/кг, и группе, получавшей композицию традиционной китайской медицины по 1677 мг/кг.
ФИГ. 6: результат лечения описанной в данном документе композицией традиционной китайской медицины у 14 пациентов с повышенным уровнем общего холестерина и повышенным уровнем триглицеридов. А: анализ общего холестерина до и после лечения; B: анализ триглицеридов до и после лечения.
ФИГ. 7: результат лечения описанной в данном документе композицией традиционной китайской медицины у 11 пациентов с гиперхолестеринемией и анализ общего холестерина до и после лечения.
ФИГ. 8: результат лечения описанной в данном документе композицией традиционной китайской медицины у 88 пациентов с гипертриглицеридемией и анализ триглицеридов до и после лечения.
ПОДРОБНОЕ ОПИСАНИЕ
Настоящее изобретение будет далее подробно описано ниже со ссылкой на конкретные варианты осуществления, и примеры даны только для иллюстрации настоящего изобретения, но не для ограничения его объема.
Все методы испытаний в следующих примерах являются обычными методами, если не указано иное; все сырье, реагенты, вещества и т. п., используемые в следующих примерах, являются коммерчески доступными продуктами, если не указано иное.
В описании настоящей заявки, если не указано иное, количество растворителя в процессе приготовления каждого исследуемого лекарственного средства кратно объему в расчете на массу лекарственных веществ.
Пример 1. Приготовление композиции традиционной китайской медицины, описанной в данном документе
Пример 1-1:
Взвешивали следующее сырье: 25 г корня володушки, 15 г незрелых плодов апельсина, 10 г корня ревеня, 6 г корня шлемника байкальского, 10 г корня пиона белого, 6 г сушеного имбиря, 10 г пиявки, 10 г корня солодки, 10 г кодонопсиса, 10 г корневища атрактилодеса большеголового, 15 г клубня пинеллии и 30 г раковины устрицы. Сырье дважды отваривали для экстракции в закрытом контейнере. В первый раз добавляли воду в количестве, в 8 раз превышающем количество сырья, и смесь отваривали при 80 °C в течение 60 мин с получением отвара. Затем во второй раз добавляли воду в количестве, в 6 раз превышающем исходное сырье, и смесь отваривали при 80 °С в течение 60 мин с получением второго отвара. Два отвара объединяли и фильтровали, а фильтраты объединяли. Фильтрат концентрировали при пониженном давлении (-0,05 МПа, 60 °С) до относительной плотности 1,05–1,15 (60 °С) и лиофилизировали при пониженном давлении с получением порошка А для сухого мазевого экстракта с выходом 25% относительно сырья.
К полученному порошку А для сухого мазевого экстракта добавляли β-циклодекстрин в соотношении 4:1 для получения гранул порошка А для сухого мазевого экстракта. Гранулы сушили, охлаждали и упаковывали в виде гранулированного состава (каждый пакетик содержал 1250 мг порошка для получения сухого мазевого экстракта традиционной китайской медицины, что эквивалентно 20 г сырья).
Пример 1-2:
Взвешивали следующее сырье: 25 г корня володушки, 15 г незрелых плодов апельсина, 10 г корня ревеня, 6 г корня шлемника байкальского, 10 г корня пиона белого, 6 г сушеного имбиря, 10 г пиявки, 10 г корня солодки, 10 г кодонопсиса, 10 г корневища атрактилодеса крупноголового и 15 г клубня пинеллии. Сырье дважды отваривали для экстракции в закрытом контейнере. В первый раз добавляли воду в количестве, в 8 раз превышающем количество сырья, и смесь отваривали при 80 °C в течение 60 мин с получением отвара. Затем во второй раз добавляли воду в количестве, в 6 раз превышающем исходное сырье, и смесь отваривали при 80 °С в течение 60 мин с получением второго отвара. Два отвара объединяли и фильтровали, а фильтраты объединяли. Фильтрат концентрировали при пониженном давлении (-0,05 МПа, 60 °С) до относительной плотности 1,05–1,15 (60 °С) и лиофилизировали при пониженном давлении с получением порошка B для сухого мазевого экстракта с выходом 25% относительно сырья.
К полученному порошку В для сухого мазевого экстракта добавляли β-циклодекстрин в соотношении 4:1 для получения гранул порошка В для сухого мазевого экстракта. Гранулы сушили, охлаждали и упаковывали в виде гранулированного состава (каждый пакетик содержал 1250 мг порошка для получения сухого мазевого экстракта традиционной китайской медицины, что эквивалентно 20 г сырья).
Пример 1-3:
Взвешивали следующее сырье: 25 г корня володушки, 15 г незрелых плодов апельсина, 10 г корня ревеня, 6 г корня шлемника байкальского, 10 г корня пиона белого, 6 г сушеного имбиря, 10 г пиявки, 10 г корня солодки, 10 г кодонопсиса, 10 г корневища атрактилодеса большеголового, 15 г клубня пинеллии, 10 г красного ферментированного риса и 30 г раковины устрицы. Сырье дважды отваривали для экстракции в закрытом контейнере. В первый раз добавляли воду в количестве, в 8 раз превышающем количество сырья, и смесь отваривали при 80 °C в течение 60 мин с получением отвара. Затем во второй раз добавляли воду в количестве, в 6 раз превышающем исходное сырье, и смесь отваривали при 80 °С в течение 60 мин с получением второго отвара. Два отвара объединяли и фильтровали, а фильтраты объединяли. Фильтрат концентрировали при пониженном давлении (-0,05 МПа, 60 °С) до относительной плотности 1,05–1,15 (60 °С) и лиофилизировали при пониженном давлении с получением порошка С для сухого мазевого экстракта с выходом 25% относительно сырья.
К полученному порошку С для сухого мазевого экстракта добавляли β-циклодекстрин в соотношении 4:1 для получения гранул порошка С для сухого мазевого экстракта. Гранулы сушили, охлаждали и упаковывали в виде гранулированного состава (каждый пакетик содержал 1250 мг порошка для получения сухого мазевого экстракта традиционной китайской медицины, что эквивалентно 20 г сырья).
Пример 2. Исследование действия композиции традиционной китайской медицины, описанной в данном документе, на крысиной модели с гибридной гиперлипидемией
2.1 Цели: исследовать действие композиции традиционной китайской медицины, описанной в данном документе, на крысиной модели с гибридной гиперлипемией.
2.2 Исследуемое соединение: порошок А для сухого мазевого экстракта, полученный в примере 1-1. Внешний вид: коричневый порошок; условия хранения: 2–8 °С, в сухом месте.
2.3 Эталонное соединение: аторвастатин кальция в таблетках (Lipitor). Внешний вид: белые овальные таблетки, покрытые пленочной оболочкой; доза: 10 мг/таблетку; упаковка: алюминий/алюминиевая контурно-ячейковая упаковка; производитель: Pfizer Inc.; условия хранения: герметичная упаковка.
2.4 Носитель, эмульгатор и другие среды:
2.4.1 Карбоксиметилцеллюлоза натрия
Условия хранения: комнатная температура;
Способ приготовления 0,5% раствора карбоксиметилцеллюлозы натрия: 5,0 г КМЦ-Na точно взвешивали и медленно добавляли в химический стакан, содержащий около 800 мл очищенной воды, и смесь перемешивали магнитной мешалкой при комнатной температуре до тех пор, пока КМЦ-Na не растворилась. Раствор оставляли на ночь при температуре 2–8 °С и разбавляли до 1000 мл. Полученный раствор тщательно перемешивали и хранили при температуре 2–8 °C для последующего применения.
2.4.2 Название: очищенная вода
Производитель: Лаборатория сравнительной медицины, Медицинский центр лабораторных животных провинции Гуандун.
2.5 Основные приборы и реактивы
Электронные аналитические весы BS-3000A, чувствительность: 0,1 г, Shanghai Yousheng Weighing Apparatus Co., Ltd.;
электронные аналитические весы BS224S, чувствительность: 0,1 мг, Sartorius Scientific Instruments (Пекин) Co., Ltd.;
настольная высокоскоростная центрифуга 5418, EPPENDORF, Германия;
автоматический биохимический анализатор 7020, Hitachi High-tech Corporation;
Изофлуран: партия № 217171101, срок годности: 1 ноября 2020 г., Shenzhen RWD Life Science Co., Ltd.;
Уретан: партия № 20160920, срок годности: 20 сентября 2021 г., Sinopharm Chemical Reagent Co., Ltd.;
Хлорид натрия для инъекций: партия № H18052802-2, Guangdong Kelun Pharmaceutical Co., Ltd.;
20% раствор уретана для анестезии: 20,0 г уретана добавляли к 100 мл инъекционного раствора хлорида натрия, смесь тщательно перемешивали и стерилизовали через фильтрующую мембрану с порами 0,2 мкм;
Набор для определения TC (общий холестерин): партии № 20180722 и 20190222, срок годности: 10 января 2020 г. и 20 августа 2020 г., Shanghai Kehua Bio-Engineering Co., Ltd.;
Набор для определения TG (триглицериды): партии № 20180822 и 20190222, срок годности: 23 февраля 2020 г. и 25 августа 2020 г., Shanghai Kehua Bio-Engineering Co., Ltd.;
Набор для определения HDL-C (холестерин липопротеинов высокой плотности): партия № 20181012, срок годности: 11 октября 2019 г., Shanghai Kehua Bio-Engineering Co., Ltd.;
Набор для определения LDL-C (холестерин липопротеинов низкой плотности): партия № 20190212, срок годности: 26 февраля 2020 г., Shanghai Kehua Bio-Engineering Co., Ltd.
2.6 Экспериментальная система
Виды: крыса SD; статус: статус SPF; самцы 190,2–223,9 г;
Источник и сертификаты: приобретены в Медицинском центре лабораторных животных провинции Гуандун, Лицензия на производство животных № SCXK (Гуандун) 2018-0002, Сертификат животных № 44007200066274;
Идентификация: животных пронумеровали насыщенной пикриновой кислотой путем окрашивания шерсти, и шерсть на разных участках поверхности тела животного была окрашена красящими пятнами для обозначения разных номеров. Животных идентифицировали по окрашиванию кожи и этикеткам на клетках.
Благополучие животных: тесты и процедуры, связанные с экспериментом на животных, проводимым в это исследование, отвечали соответствующим законам и правилам использования и обращения с экспериментальными животными, а также соответствующим правилам институционального этического комитета в области исследования на животных, для обеспечения благополучия экспериментальных животных.
Эвтаназия: исключенных животных после моделирования умерщвляли ингаляцией углекислого газа. После исследования животных анестезировали внутрибрюшинным введением 20% раствора уретана из расчета 6 мл/кг массы тела, а затем умерщвляли путем обескровливания. Перед захоронением трупы временно хранили в морозильной камере.
Карантин: приобретенных крыс помещали в карантин на 3 дня и наблюдали 1 раз в день, при этом не было обнаружено ни одного нездорового животного.
Содержание и обращение: животных содержали в помещении для животных статуса SPF Медицинского центра лабораторных животных провинции Гуандун. Лицензия на использование лабораторных животных № SYXK (Гуандун) 2018-0002; Сертификат эксперимента на животных № 00219646. Условия содержания животных: групповое содержание, 5 особей/клетку; температура и влажность: 20–26 °C, 40–70%; цикл свет/темнота: 12 ч/12 ч; состояние жилого помещения всегда поддерживалось стабильным для обеспечения достоверности результатов эксперимента. В ходе эксперимента животных кормили соответствующими гранулированными кормами в соответствии с требованиями эксперимента и обеспечивали свободный доступ к пище и воде.
2.7 Дозы и разделение на группы
Дозы: в предварительном испытании 4 крысам SD внутрижелудочно вводили исследуемое соединение в дозах 2000 мг/кг массы тела и 5000 мг/кг массы тела. Ни одно животное не умерло в течение 72 часов. Доза исследуемого соединения для взрослого человека составляет 5 г/сутки. В расчете на 60 кг массы тела взрослого человека в качестве исследуемых доз применяли 5-кратную и 10-кратную рекомендуемую дозу для человека, и исследуемые дозы составляли 417 мг/кг массы тела и 833 мг/кг массы тела соответственно. Клиническая доза эталонного препарата, аторвастатина кальция в таблетках, составляла 10 мг/сутки. Из расчета на 60 кг массы тела взрослого человека. В качестве исследуемой дозы эталонного препарата применяли 20-кратную рекомендуемую дозу для организма человека, т. е. исследуемая доза эталонного препарата, аторвастатина кальция в таблетках, составляла 3,3 мг/кг массы тела.
Разделение на группы: после карантина животных рандомизировали в группу отрицательного контроля из 10 животных, а остальных животных - в группы моделирования. После того как группам моделирования давали моделирующий корм в течение 2 недель, животных анестезировали ингаляцией изофлурана без голодания. Кровь отбирали из орбитального венозного синуса и центрифугировали при 3000 об/мин в течение 10 мин для отделения сыворотки. Определяли уровни общего холестерина (TC), триглицеридов (TG), холестерина липопротеинов низкой плотности (LDL-C) и холестерина липопротеинов высокой плотности (HDL-C). Исключали животных с более низким уровнем TG. Отбирали 40 животных и рандомизировали в группу контроля моделирования, группу положительного контроля и группы, получавшие исследуемое соединение по 417 мг/кг и 833 мг/кг, в соответствии с уровнями TG, по 10 животных в каждую.
(мг/кг массы тела)
10 мл/кг массы тела
10 мл/кг массы тела
10 мл/кг массы тела
10 мл/кг массы тела
10 мл/кг массы тела
2.8 Методология
2.8.1 Моделирующий корм с высоким содержанием жиров и холестерина: поддерживающий корм, содержащий 20,0% сахарозы, 5% сала, 1,0% холестерина, 0,1% холата натрия, соответствующие количества казеина, бикарбоната кальция, известковой крошки и т. п. Помимо сырого жира, в моделирующем корме все параметры содержание влаги, сырого протеина, сырого жира, сырой клетчатки, сырой золы, кальция, фосфора и соотношение «кальций:фосфор» соответствовали национальному стандарту для поддерживающего корма. Корм был предоставлен Медицинским центром лабораторных животных провинции Гуандун.
2.8.2 Приготовление раствора исследуемого соединения: необходимое количество исследуемого соединения добавляли в мерную колбу, растирали и растворяли в небольшом количестве очищенной воды. Смесь доводили до заданного объема очищенной водой и перемешивали до полного растворения до получения концентрации 166,7 мг/мл. Раствор последовательно разбавляли до концентраций 83,3 мг/мл и 41,7 мг/мл.
2.8.3 Приготовление раствора эталонного препарата: 1 таблетку аторвастатина кальция (доза: 10 мг/таблетку) добавляли в мерную колбу, растирали и растворяли в 0,5% растворе КМЦ-Na. Смесь доводили до 60 мл с помощью 0,5% раствора КМЦ-Na, получая концентрацию около 0,33 мг/мл. С целью тщательного перемешивания, раствор перед применением встряхивали.
2.8.4 Моделирование: группа отрицательного контроля получала поддерживающий корм, а остальные группы получали моделирующий корм до конца исследования. За исключением группы отрицательного контроля, другие группы получали западный корм с высоким содержанием жира с 30 по 36 день в течение периода лечения.
2.8.5 Введение: после завершения моделирования группе положительного контроля и группам, получавшим исследуемое соединение по 417 мг/кг и 833 мг/кг, с исследуемыми образцами внутрижелудочно вводили соответствующую дозу лечебной жидкости по 10 мл/кг массы тела ежедневно, а группе отрицательного контроля и группе контроля моделирования вводили очищенную воду в том же объеме в течение 67–68 дней (первым 5 животным в каждой группе вводили в течение 67 дней, а последним 5 животным в каждой группе вводили в течение 68 дней).
2.8.6 Измерения
2.8.6.1 Общее состояние: за клиническим состоянием животных наблюдали один раз в день до конца исследования.
2.8.6.2 Масса тела: массу тела животных измеряли один раз в начале и в конце исследования и один раз в неделю в ходе исследования.
2.8.6.3 Липиды крови: через 2, 4, 7 и 9 недель лечения (день 14, день 28, день 52 и день 65) животных анестезировали ингаляцией изофлюрана без голодания. Кровь отбирали из орбитального венозного синуса и центрифугировали при 3000 об/мин в течение 10 мин для отделения сыворотки. Определяли уровни TC, TG, LDL-C и HDL-C.
2.8.6.4 Первые 5 животных в каждой группе голодали в течение ночи на день 66, а последние 5 животных - на день 67. Животных лечили, взвешивали и на следующий день анестезировали внутрибрюшинным введением 20% раствора уретана из расчета 6 мл/кг массы тела. Кровь собирали из брюшной аорты, сыворотку отделяли и криоконсервировали. Животных умерщвляли путем обескровливания. Взвешивали яички и околопочечную жировую ткань. Часть печени фиксировали в нейтральном формальдегиде, остальную часть печени криоконсервировали в жидком азоте.
2.9 Статистика: данные представлены (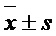
2.10 Результаты
2.10.1 Общее наблюдение: во время исследования у животных не наблюдалось никаких аномальных реакций в форме тела, шерсти, коже, фекалиях, напряжении мышц, походке, настроении, дыхании и т. п.
2.10.2 Масса тела (см. таблицу 2): во время исследования не было статистически значимой разницы (P > 0,05) в массе тела животных в каждой группе.
2.10.3 Липиды крови (см. таблицы 3–7)
2.10.3.1 Липиды крови на исходном уровне после моделирования (см. таблицу 3): по сравнению с группой отрицательного контроля увеличение значений TC, TG и LDL-C в сыворотке в группе контроля моделирования на исходном уровне после моделирования было статистически значимым (P <0,05 или 0,01); по сравнению с группой контроля моделирования четыре измерения липидов крови в каждой группе на исходном уровне после моделирования не были статистически значимыми (P > 0,05).
2.10.3.2 Липиды крови на неделе 2 лечения (см. таблицу 4): по сравнению с группой отрицательного контроля увеличение значений TC, TG и LDL-C в сыворотке в группе контроля моделирования на неделе 2 лечения было статистически значимым (P <0,05 или 0,01); по сравнению с группой контроля моделирования снижение значений TC, TG, HDL-C и LDL-C в сыворотке в группе положительного контроля на неделе 2 лечения не было статистически значимыми (P > 0,05); по сравнению с группой контроля моделирования измерения в сыворотке в группах, получавших исследуемое соединение по 417 мг/кг и 833 мг/кг, на неделе 2 лечения не были статистически значимыми (P > 0,05). По сравнению с группой контроля моделирования среднее значение TG было снижено с 3,22 ммоль/л в группе контроля моделирования до 2,89 ммоль/л в группе, получавшей исследуемое соединение по 417 мг/кг, и до 2,51 ммоль/л в группе, получавшей исследуемое соединение по 833 мг/кг, но это снижение не было статистически значимым (значение Р было между 0,05 и 0,1).
2.10.3.3 Липиды крови на неделе 4 лечения (см. таблицу 5): по сравнению с группой отрицательного контроля увеличение значений TC, TG и LDL-C в сыворотке в группе контроля моделирования на неделе 4 лечения было статистически значимым (P <0,05 или 0,01); по сравнению с группой контроля моделирования снижение значений TC и LDL-C в сыворотке в группе положительного контроля на неделе 4 лечения было близким к статистически значимому (P = 0,10 для ТС и P = 0,05 для LDL-C); по сравнению с группой контроля моделирования снижение значений TG и LDL-C в группе, получавшей исследуемое соединение по 833 мг/кг, на неделе 4 лечения было статистически значимым (P <0,05). В группе, получавшей исследуемое соединение по 417 мг/кг, значения TG и LDL-C продемонстрировали тенденцию к снижению на неделе 4 лечения, что не было статистически значимым (P > 0,05). Уровень TG снизился с 3,03 ммоль/л в группе контроля моделирования до 2,32 ммоль/л (P = 0,05). В то же время исследуемое соединение также продемонстрировало тенденцию к снижению уровня ТС. Уровень ТС снизился с 3,44 ммоль/л в группе контроля моделирования до 2,72 ммоль/л (группа, получавшая исследуемое соединение по 417 мг/кг, P = 0,08) и 2,75 ммоль/л (группа, получавшая исследуемое соединение по 833 мг/кг, P = 0,09).
2.10.3.4 Липиды крови на неделе 7 лечения (см. таблицу 6): по сравнению с группой отрицательного контроля, увеличение значений TC и LDL-C в сыворотке в группе контроля моделирования на неделе 7 лечения было статистически значимым (P < 0,01), а значение TG имело тенденцию к увеличению, которая не была статистически значимой (P > 0,05); значение TC в сыворотке в группе положительного контроля на неделе 7 лечения составило 3,03 ммоль/л, и по сравнению с группой контроля моделирования (3,55 ммоль/л) снижение не было статистически значимым (P = 0,10); по сравнению с группой контроля моделирования снижение уровня TG в сыворотке в группах, получавших исследуемое соединение по 417 мг/кг и 833 мг/кг, на неделе 7 лечения имело статистически значимые или почти значимые статистические различия (значения P для групп, получавших исследуемое соединение по 417 мг/кг и 833 мг/кг, составляли P = 0,05 и P = 0,04 соответственно). Кроме того, не было статистически значимой разницы (P < 0,05) в снижении уровня LDL-C в группе, получавшей исследуемое соединение по 833 мг/кг.
2.10.3.5 Липиды крови на неделе 9 лечения (см. таблицу 7): по сравнению с группой отрицательного контроля увеличение значений TC, TG и LDL-C в сыворотке в группе контроля моделирования на неделе 9 лечения было статистически значимым (P < 0,01); по сравнению с группой контроля моделирования снижение значений TC, TG и LDL-C в сыворотке в группе положительного контроля на неделе 9 лечения не было статистически значимым (P > 0,05); по сравнению с группой контроля моделирования, четыре измерения уровня липидов в сыворотке в группе, получавшей исследуемое соединение по 417 мг/кг, на неделе 9 лечения не были статистически значимыми (P > 0,05). Однако снижение TC, TG и LDL-C в группе, получавшей исследуемое соединение по 833 мг/кг, было статистически значимым (P < 0,05) на неделе 9 лечения.
2.10.4 Масса и коэффициент орган/ткань (см. таблицу 8): по сравнению с группой отрицательного контроля увеличение массы и коэффициента для печени у крыс в группе контроля моделирования было статистически значимым (P < 0,01); по сравнению с группой контроля моделирования масса и коэффициент для печени в группе положительного контроля не имели статистически значимой разницы (P < 0,05 или 0,01); по сравнению с группой контроля моделирования, массы и коэффициенты органов/тканей в группах, получавших исследуемое соединение по 417 мг/кг и 833 мг/кг, не имели статистически значимой разницы (P > 0,05). Органы сохраняли.
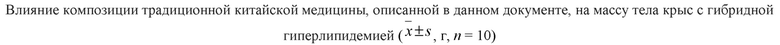
Примечание: статистический анализ основан на повторных измерениях.
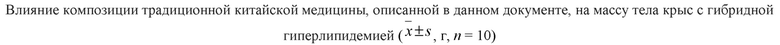
Примечание: статистический анализ основан на повторных измерениях.

Примечание: сравнение между группами, Т-критерий независимой выборки; «▲» указывает на P < 0,05, «▲▲» указывает на P < 0,01, «#» указывает на P от 0,05 до 0,10.

Примечание: сравнение между группами, Т-критерий независимой выборки; «▲» указывает на P < 0,05, «▲▲» указывает на P < 0,01, «#» указывает на P от 0,05 до 0,10.

Примечание: сравнение между группами, Т-критерий независимой выборки; «▲» указывает на P < 0,05, «▲▲» указывает на P < 0,01, «#» указывает на P от 0,05 до 0,10.

Примечание: сравнение между группами, Т-критерий независимой выборки; «▲» указывает на P < 0,05, «▲▲» указывает на P < 0,01, «#» указывает на P от 0,05 до 0,10.

Примечание: сравнение между группами, Т-критерий независимой выборки; «▲» указывает на P < 0,05, «▲▲» указывает на P < 0,01.

Масса тела (г)
Масса (г)
Коэффициент
Примечание: сравнение между группами, Т-критерий независимой выборки; «▲» указывает на P < 0,05, «▲▲» указывает на P < 0,01.
2.11 Резюме:
1) Не было статистически значимой разницы (P > 0,05) в массе тела животных в каждой группе.
2) По сравнению с группой отрицательного контроля, значения TC, TG и LDL-C в сыворотке в группе контроля моделирования на исходном уровне, после моделирования и на неделях 2, 4 и 9 лечения были повышены (P < 0,05 или 0,01). Была создана модель гибридной гиперлипемии у крыс.
3) По сравнению с группой контроля моделирования в каждый момент времени группа положительного контроля демонстрировала определенные эффекты в отношении снижения уровня общего холестерина в сыворотке крови у крыс, которые, однако, не были значимыми, что указывает на то, что эталонный препарат аторвастатин не оказывает значимого влияния на снижение уровня липидов крови в крысиной модели с гибридной гиперлипидемией и не является идеальным терапевтическим средством.
4) Композиция традиционной китайской медицины, описанная в данном документе, начала демонстрировать эффект снижения уровня TG на неделе 2 лечения, особенно в группе, получавшей 833 мг/кг, и эффекты снижения уровней TG на неделях 4, 7 и 9 лечения было статистически значимым (Р < 0,05). Между тем, группа, получавшая 833 мг/кг, также продемонстрировала предварительный эффект снижения уровня ТС, и, в частности, на неделе 9 лечения снижение уровня ТС было статистически значимым (P < 0,05). Эффект снижения уровня TG в группе, получавшей 417 мг/кг, на неделе 4, 7 и 9 лечения был критическим моментом для статистической разницы в статистических тестах (значение Р между 0,05 и 0,10).
5) По сравнению с группой отрицательного контроля, масса и коэффициент для печени в группе контроля моделирования были увеличены (P < 0,01); по сравнению с группой контроля моделирования масса и коэффициент орган/ткань в группах, получавших исследуемое соединение, статистически значимо не изменялись (P > 0,05). Органы были сохранены для дальнейшей доставки спонсору.
6) Вывод: в экспериментальных условиях исследования на животных продемонстрировали, что описанная в данном документе композиция традиционной китайской медицины оказывает статистически значимые влияния на снижение уровня липидов в крови и снижение уровня холестерина и, в частности, оказывает статистически значимое влияние на снижение уровня триглицеридов в крови. Между тем влияние на снижение липидов крови имеет определенную зависимость от дозы.
Пример 3. Изучение влияния композиции традиционной китайской медицины, описанной в данном документе, на образование атеросклеротических бляшек у мышей ApoE-/-
3.1 Цели: исследовать влияние композиции традиционной китайской медицины, описанной в данном документе, на образование атеросклеротических бляшек в модели атеросклеротических бляшек у мышей ApoE-/-.
3.2 Исследуемое соединение: порошок А для сухого мазевого экстракта, полученный в примере 1-1. Внешний вид: коричневый порошок; условия хранения: 2–8 °С, в сухом месте.
3.3 Эталонной препарат: розувастатин кальция в таблетках (Крестор); внешний вид: розовая таблетка, покрытая пленочной оболочкой; доза/чистота: 10 мг/таблетку; упаковка: алюминиево-пластиковая контурно-ячейковая упаковка; производитель: AstraZeneca Pharmaceuticals (Китай) Co., Ltd.; условия хранения: герметично и в сухом месте.
3.4 Носитель, эмульгатор и другие среды:
3.4.1 Карбоксиметилцеллюлоза натрия
Условия хранения: комнатная температура;
Способ приготовления 0,5% раствора карбоксиметилцеллюлозы натрия: 5,0 г КМЦ-Na точно взвешивали и медленно добавляли в химический стакан, содержащий около 800 мл очищенной воды, и смесь перемешивали магнитной мешалкой при комнатной температуре до тех пор, пока КМЦ-Na не растворилась. Раствор оставляли на ночь при температуре 2–8 °С и разбавляли до 1000 мл. Полученный раствор тщательно перемешивали и хранили при температуре 2–8 °C для последующего применения.
3.4.2 Название: очищенная вода
Производитель: Лаборатория сравнительной медицины, Медицинский центр лабораторных животных провинции Гуандун.
3.5 Основные приборы и реактивы
Электронные аналитические весы BS-3000A, чувствительность: 0,1 г, Shanghai Yousheng Weighing Apparatus Co., Ltd.;
электронные аналитические весы BS224S, чувствительность: 0,1 мг, Sartorius Scientific Instruments (Пекин) Co., Ltd.;
настольная высокоскоростная центрифуга 5418, EPPENDORF, Германия;
автоматический биохимический анализатор 7020, Hitachi High-tech Corporation;
Изофлуран: партия № 217171101, срок годности: 1 ноября 2020 г., Shenzhen RWD Life Science Co., Ltd.;
Уретан: партия № 20160920, срок годности: 20 сентября 2021 г., Sinopharm Chemical Reagent Co., Ltd.;
Хлорид натрия для инъекций: партия № H18052802-2, Guangdong Kelun Pharmaceutical Co., Ltd.;
20% раствор уретана для анестезии: 20,0 г уретана добавляли к 100 мл инъекционного раствора хлорида натрия, смесь тщательно перемешивали и стерилизовали через фильтрующую мембрану с порами 0,2 мкм;
Наборы TC, TG, HDL-C, LDL-C: Shanghai Kehua Bio-Engineering Co., Ltd.;
Сыворотка для контроля качества: Randox Laboratories Limited
3.6 Экспериментальная система
Виды и статус: статус SPF, мышь ApoE-/-; 6 мышей ApoE, самки, в возрасте 28–35 дней; 48 мышей ApoE, половина самцов и половина самок, в возрасте 49–56 дней.
Идентификация: мышей идентифицировали по ушным биркам. Перед перфорацией ухо животного и перфорационное устройство дезинфицировали. Затем животному перфорировали ухо и прикрепляли ушную бирку с номером животного.
Благополучие животных: тесты и процедуры, связанные с экспериментом на животных, проводимым в это исследование, отвечали соответствующим законам и правилам использования и обращения с экспериментальными животными, а также соответствующим правилам институционального этического комитета в области исследования на животных, для обеспечения благополучия экспериментальных животных.
Эвтаназия: после окончания исследования животных анестезировали ингаляцией изофлурана. Из глазного яблока отбирали кровь, мышей умерщвляли путем смещением шейных позвонков и забирали образцы. Перед захоронением трупы временно хранили в морозильной камере.
Карантин: приобретенных мыши помещали в карантин на 7 дней. В течение этого периода животных исследовали один раз в день. Если обнаруживались нездоровые животные, их немедленно удаляли, и добавляли здоровых.
Содержание и обращение: животных содержали в помещении для животных статуса SPF Медицинского центра лабораторных животных провинции Гуандун. Лицензия на использование лабораторных животных № SYXK (Гуандун) 2018-0002. Условия содержания животных: 1 особь/клетку; температура и влажность: 20–26 °C, 40–70%; цикл свет/темнота: 12 ч/12 ч; состояние жилого помещения всегда поддерживалось стабильным для обеспечения достоверности результатов эксперимента. В ходе исследования животных кормили соответствующим гранулированным кормом в соответствии с экспериментальными требованиями, и корма были предоставлены Медицинским центром лабораторных животных провинции Гуандун. Животным предоставляли свободный доступ к пище и воде.
3.7 Дозы и разделение на группы
Дозы: в предварительном испытании 4 крысам SD (половина самок, половина самцов) внутрижелудочно вводили исследуемое соединение в дозах 2000 мг/кг массы тела и 5000 мг/кг массы тела. Ни одно животное не погибло в течение 72 ч. Согласно информации, предоставленной спонсором, доза исследуемого соединения для взрослого человека составляет 5 г/сутки. В расчете на 60 кг массы тела взрослого человека в качестве исследуемых доз применяли 10-кратную и 20-кратную рекомендуемую дозы для человека, и эти дозы составляли 833 мг/кг массы тела и 1667 мг/кг массы тела для групп, получавших исследуемые соединения 1 и 2, соответственно. Максимальная клиническая суточная доза эталонного препарата розувастатина кальция в таблетках составляет 20 мг. Из расчета на 60 кг массы тела взрослого человека. В качестве исследуемой дозы эталонного препарата применяли 20-кратную рекомендуемую дозу для организма человека, то есть исследуемая доза эталонного препарата, розувастатина кальция в таблетках, составляла 6,6 мг/кг массы тела.
Разделение на группы: после карантина мышей содержали в течение 1 неделю обычным способом. При первом разделении на группы (период моделирования), 6 мышей ApoE-/- были рандомизированы в группу отрицательного контроля и получали поддерживающий корм. Остальные 48 мышей ApoE-/- были рандомизированы в группы моделирования и получали корм с высоким 21% содержанием жира в течение 1 месяца. Кровь отбирали для определения четырех показателей липидов крови. При втором разделении группы (период лечения) мышей ApoE-/- рандомизировали в группу контроля моделирования, группу положительного контроля, группу, получавшую исследуемое соединение по 833 мг/кг, группу, получавшую исследуемое соединение по 1667 мг/кг, в соответствии с уровнями ТС, по 12 мышей в каждую группу, половина самцов и половина самок.
(мг/кг массы тела)
3.8 Методология
3.8.1 Моделирующий корм с высоким содержанием жиров и холестерина: поддерживающий корм, содержащий 20,0% сахарозы, 5% сала, 1,0% холестерина, 0,1% холата натрия, соответствующие количества казеина, бикарбоната кальция, известковой крошки и т. п. Помимо сырого жира, в моделирующем корме все параметры содержание влаги, сырого протеина, сырого жира, сырой клетчатки, сырой золы, кальция, фосфора и соотношение «кальций:фосфор» соответствовали национальному стандарту для поддерживающего корма. Корм был предоставлен Медицинским центром лабораторных животных провинции Гуандун.
3.8.2 Приготовление раствора исследуемого соединения: необходимое количество исследуемого соединения измельчали и растворяли в небольшом количестве очищенной воды. Смесь переносили в мерную колбу, доводили до заданного объема очищенной водой и перемешивали до полного растворения с получением раствора для группы 2, получавшей исследуемое соединение по 83,35 мг/мл. Раствор разбавляли в 2 раза до около 41,65 мг/мл для группы 1, получавшей исследуемое соединение.
3.8.3 Приготовление раствора эталонного препарата: 1 таблетку розувастатина кальция (доза: 10 мг/таблетка) растирали и растворяли в 0,5% растворе КМЦ-Na. Смесь переносили в мерную колбу и доводили до 30 мл 0,5% раствором КМЦ-Na, получая концентрацию около 0,33 мг/мл. С целью тщательного перемешивания, раствор перед применением встряхивали.
3.8.4 Моделирование: группа отрицательного контроля получала поддерживающий корм, а остальные группы получали корм с высоким 21% содержанием жира до конца исследования.
3.8.5 Введение: мышам в группе положительного контроля, группе, получавшей исследуемое соединение по 833 мг/кг, и группе, получавшей исследуемое соединение по 1667 мг/кг, ежедневно вводили внутрижелудочно соответствующий раствор лекарственного средства в дозе 20 мл/кг массы тела, а мышам в группе отрицательного контроля и группе контроля моделирования вводили очищенную воду в том же объеме 1 раз в день в течение 60 дней.
3.8.6 Измерения:
1) Общее состояние: общее клиническое состояние мышей наблюдали и регистрировали 1 раз в день.
2) Масса тела: массу тела измеряли один раз в начале и в конце исследования и один раз в неделю в ходе исследования. Рассчитывали прирост массы тела на День 30 лечения (День 29 лечения - День 1 лечения) и День 60 лечения (День 60 лечения - День 1 лечения).
3) Уровни TC, TG, LDL-C и HDL-C: после окончания периода моделирования животных подвергали анестезии ингаляцией изофлюрана без голодания. Кровь отбирали из орбитального венозного сплетения и центрифугировали при 3000 об/мин при низкой температуре в течение 10 мин. Сыворотку разделяли для определения общего холестерина TC, триглицеридов TG, уровней липопротеинов высокой плотности HDL-C и липопротеинов низкой плотности LDL-C, а оставшиеся образцы сыворотки хранили в морозильной камере при температуре -80 °C.
4) Масса органов: измеряли массу печени, левой почки, околопочечного жира слева, правой почки и околопочечного жира справа, и рассчитывали коэффициент органа по следующей формуле. Печень и правую почку взвешивали и хранили при -80°С.
5) Патологистологическое исследование: после окончания исследования мышей фиксировали в положении лежа на спине, грудные полости мышей быстро вскрывали, перфузировали физиологическим раствором по всему телу из левого желудочка, а затем перфузировали 4% параформальдегидом для фиксации. Всю артерию от сердца до нижней ветви подвздошной артерии удаляли, консервировали в 4% фиксирующем растворе параформальдегида, обрабатывали и окрашивали Oil Red O. Дугу аорты вместе с сердцем и общей сонной артерией (справа) быстро выделяли и фиксировали 4% параформальдегидом. Общую сонную артерию окрашивали Oil Red O, а дугу аорты окрашивали HE и Sirius.
3.9 Статистика: данные представлены (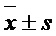
3.10 Результаты
3.10.1 Общее клиническое наблюдение: во время исследования животное №2 в группе отрицательного контроля погибло на день 30 лечения. Анатомическое исследование продемонстрировало увеличенную левую почку, причем верхняя половина левой почки была молочно-белой, а нижняя половина темно-красной. В левой почке при продольном рассечении обнаруживали большую полость, содержащую молочную жидкость и прозрачную жидкость. Правая почка была сморщена и атрофирована, с обнаруженными агрегированными тромбами. В мочевом пузыре определялась молочно-белая жироподобная жидкость, которая скапливалась на выходе из мочевого пузыря, составляя около половины внутрипросветного объема мочевого пузыря. Видимых аномалий в макроанатомической структуре остальных органов брюшной полости не наблюдалось, видимых аномалий в макроанатомической структуре грудной полости не наблюдалось и бляшек в грудной аорте не наблюдалось. Обсуждение: накопление холестерина in vivo и гиперлипидемия являются нормальными проявлениями у мышей с нокаутом ApoE, и предполагается, что причина смерти мышей выходила из индивидуальных различий, нарушения жирового обмена и избыточного накопление холестерина. Никаких аномалий в форме тела, шерсти, коже, фекалиях, напряжении мышц, походке, настроении, дыхании и т. п. у животных не наблюдалось.
3.10.2 Данные в период моделирования
3.10.2.1 Масса тела в период моделирования (таблица 10): статистической разницы (p > 0,05) в массе тела животных в каждой группе в период моделирования не было.
3.10.2.2 Измерения липидов крови в период моделирования (таблица 11): по сравнению с группой отрицательного контроля (♂), уровни TC, TG, HDL-C и LDL-C в сыворотке в группе моделирования (♂) повысились (p < 0,01), и уровень ТС в сыворотке в группе моделирования (♂) повысился (p < 0,05).
3.10.3 Данные в период лечения
3.10.3.1 Масса тела в период лечения (таблица 12): статистической разницы (p > 0,05) в массе тела животных между группами в период лечения не было; по сравнению с группой отрицательного контроля (♂) прирост массы тела в группе контроля моделирования (♂) увеличился на день 30 и день 60 лечения (p < 0,05); по сравнению с группой контроля моделирования (♂) прирост массы тела в группе положительного контроля (♂), группе, получавшей исследуемое соединение по 833 мг/кг (♂), и группе, получавшей исследуемое соединение по 1667 мг/кг (♂), уменьшился на день 30 и день 60 лечения (p < 0,05).
3.10.3.2 Масса и коэффициенты для органов на день 60 лечения (таблицы 13 и 14): по сравнению с группой отрицательного контроля (♂) массы и коэффициенты для печени и околопочечного жира слева в группе контроля моделирования (♂) увеличились (p < 0,05 или 0,01), коэффициенты для левой почки и правой почки снизились (p < 0,05 или 0,01), и массы левой почки и правой почки и коэффициент для левой почки в группе контроля моделирования (♀) уменьшились (p < 0,05 или 0,01); по сравнению с группой контроля моделирования (♂) масса левой почки в группе положительного контроля (♂) и группе, получавшей исследуемое соединение по 833 мг/кг (♂), уменьшилась (p < 0,05); по сравнению с группой контроля моделирования (♀) масса правой почки в группе, получавшей исследуемое соединение по 833 мг/кг (♀), уменьшилась (p < 0,05).
3.10.4 Результаты патогистологического исследования: окрашивание аорты Oil Red O по всей длине показало, что вещества, похожие на красные бляшки, были обнаружены в бифуркационной части аорты мышей ApoE-/-, которым давали корм с высоким содержанием жира, и количество атеросклеротических бляшек в группе моделирования было значительно увеличено по сравнению с таковым в группе отрицательного контроля (ФИГ. 1). Между тем, по сравнению с группой контроля моделирования окрашивание аорты Oil Red O при применении исследуемого соединения в группах, получавших его по 833 мг/кг и 1677 мг/кг, показало, что образование атеросклеротических бляшек явно уменьшилось после 60 дней лечения (ФИГ. 2). Окрашенные красителем HE срезы дуги аорты продемонстрировали, что определенные гистологические изменения наблюдались в группе контроля моделирования по сравнению с группой отрицательного контроля и проявлялись в основном накоплением пенистых клеток под внутренней оболочкой в дуге аорты и образованием бляшек на внутренней оболочке (ФИГ. 3). Группа положительного контроля не продемонстрировала значительной разницы по сравнению с группой контроля моделирования. Однако в группах, получавшей исследуемое соединение по 833 мг/кг и 1667 мг/кг, наблюдалась только агрегация пенистых клеток под внутренней оболочкой в дуге аорты, и бляшки на внутренней оболочке не образовывались (ФИГ. 3). Срезы дуги аорты, окрашенные красителем Sirius, продемонстрировали, что в группе контроля моделирования наблюдалась значительная гиперплазия коллагеновых волокон в части бляшки во внутренней оболочке и адвентициальной оболочке по сравнению с группой отрицательного контроля. В группах исследуемых соединений, особенно в группе, получавшей по 1667 мг/кг, была обнаружена только более легкая гиперплазия коллагеновых волокон в адвентициальной оболочке, а во внутренней оболочке не наблюдалось гиперплазии коллагеновых волокон (ФИГ. 4). Как продемонстрировано на ФИГ. 5, окрашивание сонных артерий Oil Red O показало, что внутри просвета образовались красные липидные капли, и группы, получавшие исследуемое соединение по 833 мг/кг и 1667 мг/кг, значительно превосходили группу контроля моделирования и группу, получавшую лечение статинами. В группе, получавшей исследуемое соединение по 1667 мг/кг, в просвете сонных артерий наблюдалось лишь незначительное количество красных липидных капель (ФИГ. 5).
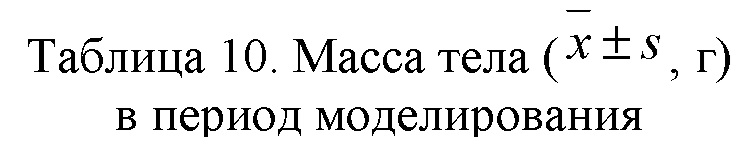

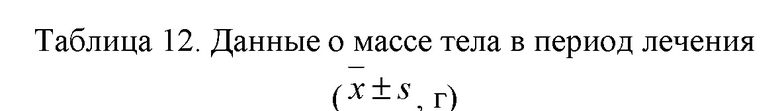
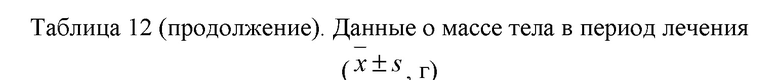
Примечание: по сравнению с группой отрицательного контроля (♂) # указывает на p < 0,05; по сравнению с группой контроля моделирования (♂) ■ указывает на p < 0,05.
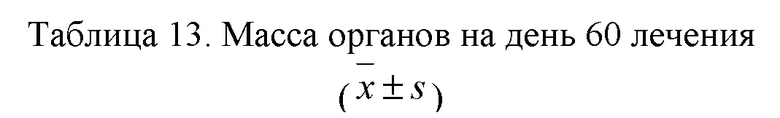
Примечание: по сравнению с группой отрицательного контроля (♂) # указывает на p < 0,05, ## указывает на p < 0,01; по сравнению с группой контроля моделирования (♂) ■ указывает на p < 0,05; по сравнению с группой контроля моделирования (♀) * указывает на p < 0,05.
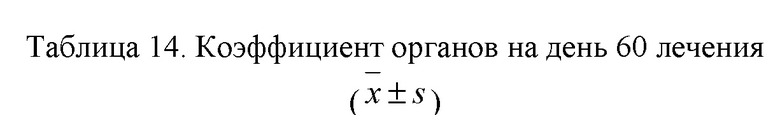
Примечание: по сравнению с группой отрицательного контроля (♂) # указывает на p < 0,05, ## указывает на p < 0,01; по сравнению с группой контроля моделирования (♂) ■ указывает на p < 0,05; по сравнению с группой контроля моделирования (♀) * указывает на p < 0,05.
3.11 Резюме
Композиция традиционной китайской медицины, описанная в данном документе, оказывает значительное влияние на снижение образования атеросклеротических бляшек и снижение прибавки массы у модельных животных.
Пример 4. Клинические исследования лечения гиперлипидемии
Субъекты были из клиники традиционной китайской медицины Zhejiang Huzhou Ruibo (№ 322, улица Мейчжоу, город Хучжоу, провинция Чжецзян) и клиники Beijing Tongyitang Clinic (1-й этаж, корпус 4, Парк биологических наук Zhongguancun, район Чанпин, Пекин).
Были собраны данные о лечении из двух клиник, как описано выше, с применением порошка A, B или C для сухого мазевого экстракта по настоящему изобретению у этих субъектов, при этом у 14 субъектов был повышен уровень общего холестерина (> 6,2 ммоль/л) и триглицеридов (> 1,7 ммоль/л), у 11 субъектов был повышен уровень общего холестерина и у 88 субъектов был повышен уровень триглицеридов (таблица 15).
Пациенты получали от одного до трех 14-дневных курсов лечения. Пациентам вводили препарат два раза в день, каждый раз 1 или 2 пакета гранулированного состава в зависимости от тяжести заболевания, каждый пакет гранулированного состава содержал 1250 мг порошка A, B или C для сухого мазевого экстракта.
Со снижением уровня общего холестерина или триглицеридов на 10% в качестве критерия эффективности, у 14 пациентов с повышенным уровнем общего холестерина и триглицеридов почти у 79% пациентов было эффективное снижение общего холестерина, у 93% пациентов было эффективное снижение уровня триглицеридов, и у 10 пациентов наблюдались эффективные снижения обоих показателей (таблица 15 и ФИГ. 6).
Композиция традиционной китайской медицины, описанная в данном документе, имеет эффективную скорость снижения повышенного уровня общего холестерина, составляющую 45% (показано в таблице 15 и на ФИГ. 7) и эффективную скорость снижения гипертриглицеридемии, близкую к 90% (показано в таблице 15 и на ФИГ. 8). Композиция традиционной китайской медицины, описанная в данном документе, обладает превосходной эффективностью у пациентов с тяжелой гиперлипидемией, особенно у субъектов с высоким уровнем триглицеридов в крови (триглицериды > 5,6 ммоль/л).
(количество)
Примечание: сравнение между группами, Т-критерий независимой выборки; «▲» указывает на P < 0,05, «▲▲» указывает на P < 0,01.
Пример 5. Типовые случаи лечения гиперлипидемии
Пример 5-1:
Шао (Shao), пациент мужского пола, посетил врача в клинике традиционной китайской медицины Zhejiang Huzhou Ruibo (№ 322, улица Мейчжоу, город Хучжоу, провинция Чжецзян) в 2016 году. Диагностическое обследование продемонстрировало, что кровь была молочно-белой, триглицериды крови - 33,4 ммоль/л, и общий холестерин крови - 6,71 ммоль/л. Гранулированный состав вводили два раза в день по 2 пакета каждый раз, каждый пакет содержал 1250 мг порошка А для сухого мазевого экстракта. После одного курса лечения (14 дней) триглицериды снизились до 0,62 ммоль/л, а общий холестерин - до 4,41 ммоль/л, оба показателя вернулись к нормальным уровням.
Пример 5-2:
Чень (Chen), пациентка женского пола, посетила врача в клинике традиционной китайской медицины Zhejiang Huzhou Ruibo (№ 322, улица Мейчжоу, город Хучжоу, провинция Чжецзян) в 2016 году. Чень на момент посещения длительное время принимала статины, снижающие уровень липидов, и диагностическое обследование продемонстрировало, что уровень триглицеридов в крови составлял 8,31 ммоль/л, а общего холестерина - 6,59 ммоль/л, что было выше нормальных значений. В частности, уровень триглицеридов в крови был намного выше нормального уровня. Гранулированный состав вводили два раза в день по 2 пакета каждый раз, каждый пакет содержал 1250 мг порошка А для сухого мазевого экстракта. После одного курса лечения (14 дней) триглицериды снизились до 1,01 ммоль/л, а общий холестерин - до 4,77 ммоль/л, оба показателя вернулись к нормальным уровням.
Пример 5-3:
Хуанг (Huang), пациент мужского пола, посетил врача в клинике традиционной китайской медицины Zhejiang Huzhou Ruibo (№ 322, улица Мейчжоу, город Хучжоу, провинция Чжецзян) в 2017 году. Когда Дай (Dai) посетил врача, диагностическое обследование продемонстрировало, что уровень триглицеридов в крови составляет 8,05 ммоль/л, а общего холестерина - 5,51 ммоль/л, оба показателя были выше нормальных значений. Особенно был повышен уровень триглицеридов. Гранулированный состав вводили два раза в день по 1 пакету каждый раз, каждый пакет содержал 1250 мг порошка B для сухого мазевого экстракта. После двух курсов лечения уровень триглицеридов снизился до 1,45 ммоль/л и вернулся к нормальному уровню.
Пример 5-4:
Юй (Yu), пациент мужского пола, посетил врача в клинике традиционной китайской медицины Zhejiang Huzhou Ruibo (№ 322, улица Мейчжоу, город Хучжоу, провинция Чжецзян) в 2018 году. Когда Чень посетил врача, диагностическое обследование продемонстрировало, что уровень триглицеридов в крови составляет 7,13 ммоль/л, а общего холестерина - 4,51 ммоль/л, что свидетельствует о гипертриглицеридемии. Гранулированный состав вводили два раза в день по 1 пакету каждый раз, каждый пакет содержал 1250 мг порошка B для сухого мазевого экстракта. После двух курсов лечения уровень триглицеридов снизился до 1,75 ммоль/л и вернулся к нормальному уровню. Уровень общего холестерина не изменился.
Пример 5-5:
Шен (Shen), пациент мужского пола, посетил врача в клинике традиционной китайской медицины Zhejiang Huzhou Ruibo (№ 322, улица Мейчжоу, город Хучжоу, провинция Чжецзян) в 2017 году. Когда Сюй (Xu) посетил врача, диагностическое обследование продемонстрировало, что уровень триглицеридов в крови составляет 0,95 ммоль/л, а общего холестерина - 7,22 ммоль/л, что свидетельствует о гиперхолестеринемии. Гранулированный состав вводили два раза в день по 1 пакету каждый раз, каждый пакет содержал 1250 мг порошка C для сухого мазевого экстракта. После трех курсов лечения уровень общего холестерина снизился до 4,91 ммоль/л и вернулся к нормальному уровню. Уровень триглицеридов не претерпел существенных изменений.
Пример 6. Типовые случаи лечения атеросклероза
Пример 6-1:
Ян (Yang), пациент мужского пола, посетил врача в клинике Beijing Tongyitang (1-й этаж, корпус 4, Парк биологических наук Zhongguancun, район Чанпин, Пекин) в 2019 году. При посещении диагностическое обследование продемонстрировало, что атеросклеротические бляшки образовались в общей сонной артерии и правой подключичной артерии с обеих сторон и в правой общей сонной артерии образовались множественные бляшки, самая крупная из которых имела длину 16,5 мм и толщину 3,9 мм; при этом в правой подключичной артерии образовались артериосклеротические бляшки. В левой общей сонной артерии образовалось множество бляшек максимальной длиной 3,5 мм и толщиной 1,6 мм; диаметр правой позвоночной артерии составлял 2,8 мм, средняя скорость кровотока составляла 0,21 м/с, и объем кровотока составлял 77 мл/мин.
Гранулированный состав вводили два раза в день по 2 пакета каждый раз, каждый пакет содержал 1250 мг порошка А для сухого мазевого экстракта. После восьми курсов лечения и четырех месяцев лечения склеротические бляшки в правой общей сонной артерии уменьшились в размерах и исчезли, самая большая из них имела длину 10,0 мм и толщину 1,8 мм. Исчезли атеросклеротические бляшки в верхнем отделе правой подключичной артерии, увеличился диаметр позвоночной артерии (3,2 мм), значительно улучшились скорость кровотока (0,21 м/с) и объем кровотока (до 135 мл/мин после лечения по поводу нарушенного объема кровотока).
Пример 6-2:
Ван (Wang), пациент мужского пола, 40 лет, посетил врача в клинике Beijing Tongyitang (1-й этаж, корпус 4, Парк биологических наук Zhongguancun, район Чанпин, Пекин) в 2018 году. При посещении врача диагностическое обследование продемонстрировало, что в общей сонной артерии с обеих сторон образовались артериосклеротические бляшки размером около 1,6 мм.
Гранулированный состав вводили два раза в день по 2 пакета каждый раз, каждый пакет содержал 1250 мг порошка А для сухого мазевого экстракта. После шести курсов лечения (3 месяца лечения) явных бляшек в левой и правой общих сонных артериях не образовалось, а исходные склеротические бляшки исчезли.
| название | год | авторы | номер документа |
|---|---|---|---|
| Химическое соединение тетразамещенный гликолевой кислотой пайсатаннол (E)-2,2'-((4-(3,5-бис(карбоксилатометокси) стирил)-1,2-фенилен)бис(окси)) диацетат, фармацевтическая композиция и её применение для лечения системных воспалительных заболеваний и состояний, в том числе острого респираторного дистресс-синдрома | 2023 |
|
RU2826492C1 |
| КОМПОЗИЦИЯ НА ОСНОВЕ ЛЕКАРСТВЕННЫХ МАТЕРИАЛОВ ТРАДИЦИОННОЙ КИТАЙСКОЙ МЕДИЦИНЫ ДЛЯ ЛЕЧЕНИЯ МЕТАБОЛИЧЕСКОГО СИНДРОМА, СПОСОБ ЕЕ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ, И ФАРМАЦЕВТИЧЕСКИЙ ПРЕПАРАТ НА ЕЕ ОСНОВЕ И ЕГО ПРИМЕНЕНИЕ | 2019 |
|
RU2780451C1 |
| Средство, обладающее противоопухолевым действием, для лечения онкологических заболеваний | 2018 |
|
RU2761429C2 |
| ЛЕКАРСТВЕННОЕ СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ГИПЕРКЕРАТОЗОВ, ВРОСШЕГО НОГТЯ, А ТАКЖЕ ДЛЯ ГИГИЕНИЧЕСКОЙ ОБРАБОТКИ НОГТЕЙ, ДЕФОРМИРОВАННЫХ В РЕЗУЛЬТАТЕ ТРАВМЫ И/ИЛИ ВОЗРАСТНЫХ ИЗМЕНЕНИЙ | 2005 |
|
RU2292879C2 |
| N-АЦИЛЬНЫЕ ПРОИЗВОДНЫЕ АМИНОКИСЛОТ, ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕВЫЕ СОЛИ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И ПРИМЕНЕНИЕ В КАЧЕСТВЕ ГИПОЛИПИДЕМИЧЕСКИХ СРЕДСТВ | 2005 |
|
RU2335495C2 |
| ГИПОЛИПИДЕМИЧЕСКОЕ ФИТОСРЕДСТВО | 2013 |
|
RU2553309C2 |
| ПУТИ ПРИМЕНЕНИЯ ТРИАЦЕТИЛ-3-ГИДРОКСИФЕНИЛАДЕНОЗИНА В ЛЕЧЕНИИ ВОСПАЛИТЕЛЬНЫХ ПРОЦЕССОВ В СОСУДАХ ИЛИ УЛУЧШЕНИИ ФУНКЦИЙ ЭНДОТЕЛИЯ СОСУДОВ | 2017 |
|
RU2783498C2 |
| Биологически активная добавка к пище и способ ее получения | 2023 |
|
RU2825783C1 |
| СПОСОБ МОДЕЛИРОВАНИЯ ИММУНОЗАВИСИМОГО НЕВЫНАШИВАНИЯ АЛЛОГЕННОЙ БЕРЕМЕННОСТИ У ЛАБОРАТОРНЫХ МЫШЕЙ | 2012 |
|
RU2511107C1 |
| 2-ЭТИЛ-6-МЕТИЛ-3-ГИДРОКСИПИРИДИНИЙГИДРОКСИБУТАНДИОАТ, ОБЛАДАЮЩИЙ ПРОТИВОИШЕМИЧЕСКОЙ, ЦЕРЕБРОПРОТЕКТОРНОЙ, НЕЙРОТРОПНОЙ И ЛИПИДРЕГУЛИРУЕМОЙ АКТИВНОСТЯМИ, ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ И ЛЕКАРСТВЕННОЕ СРЕДСТВО | 2008 |
|
RU2377237C1 |
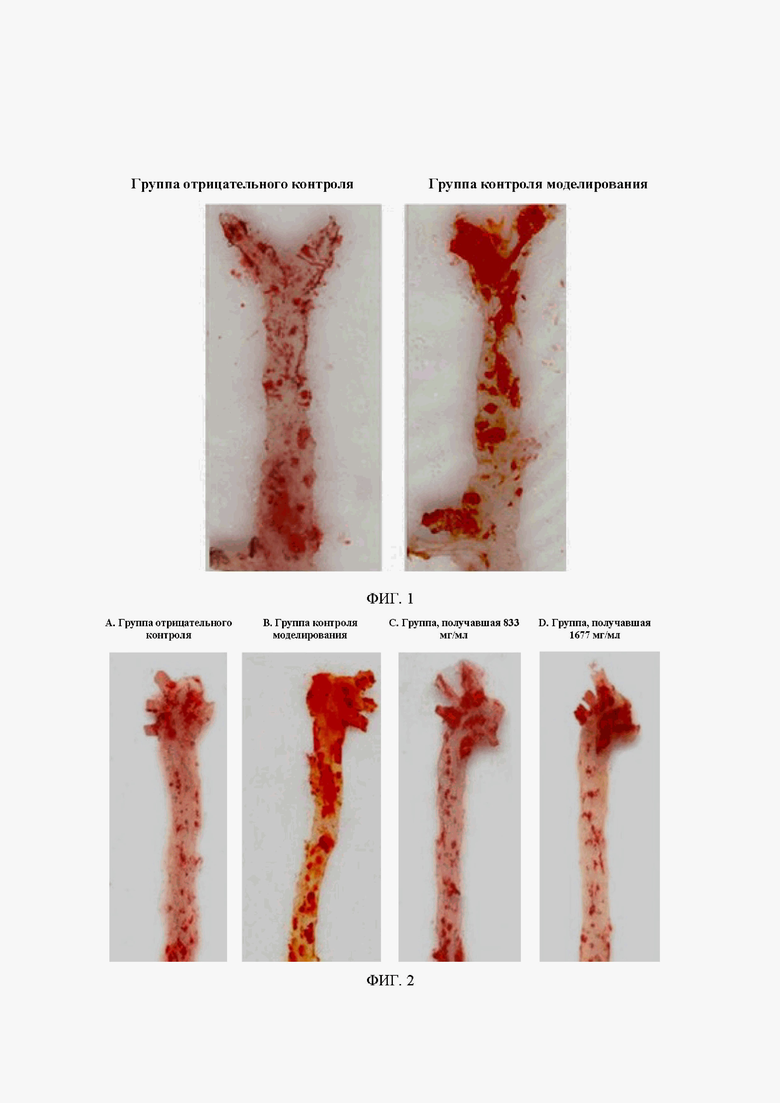
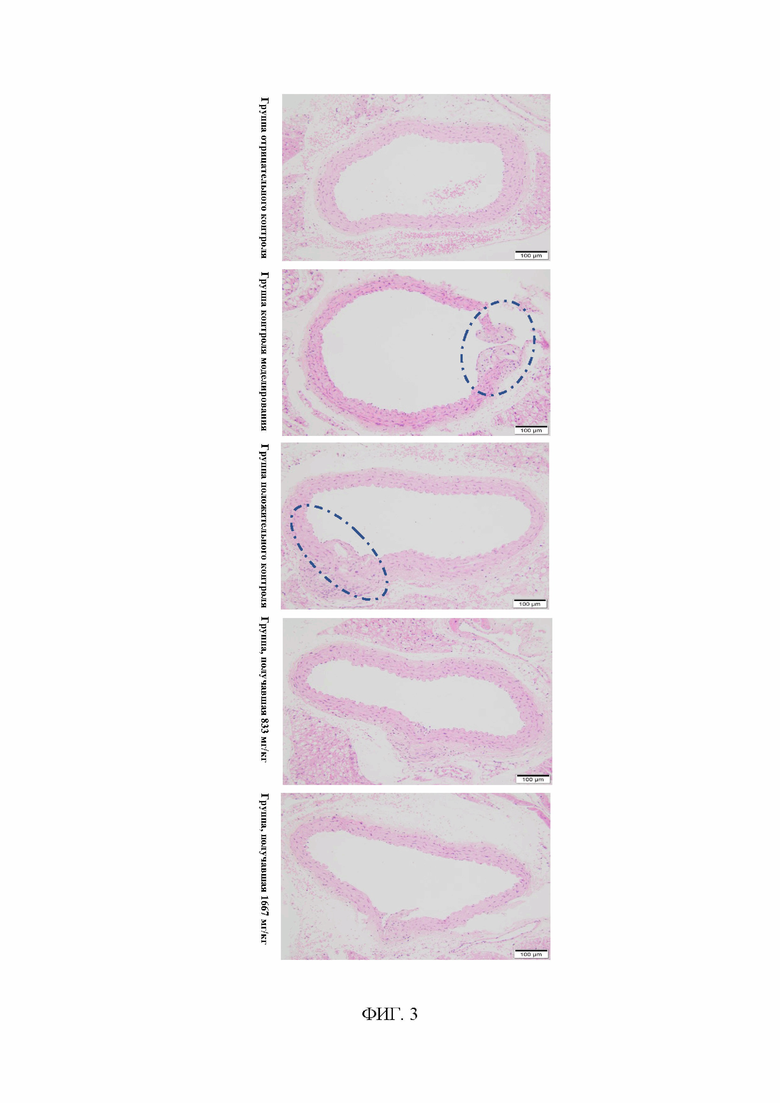
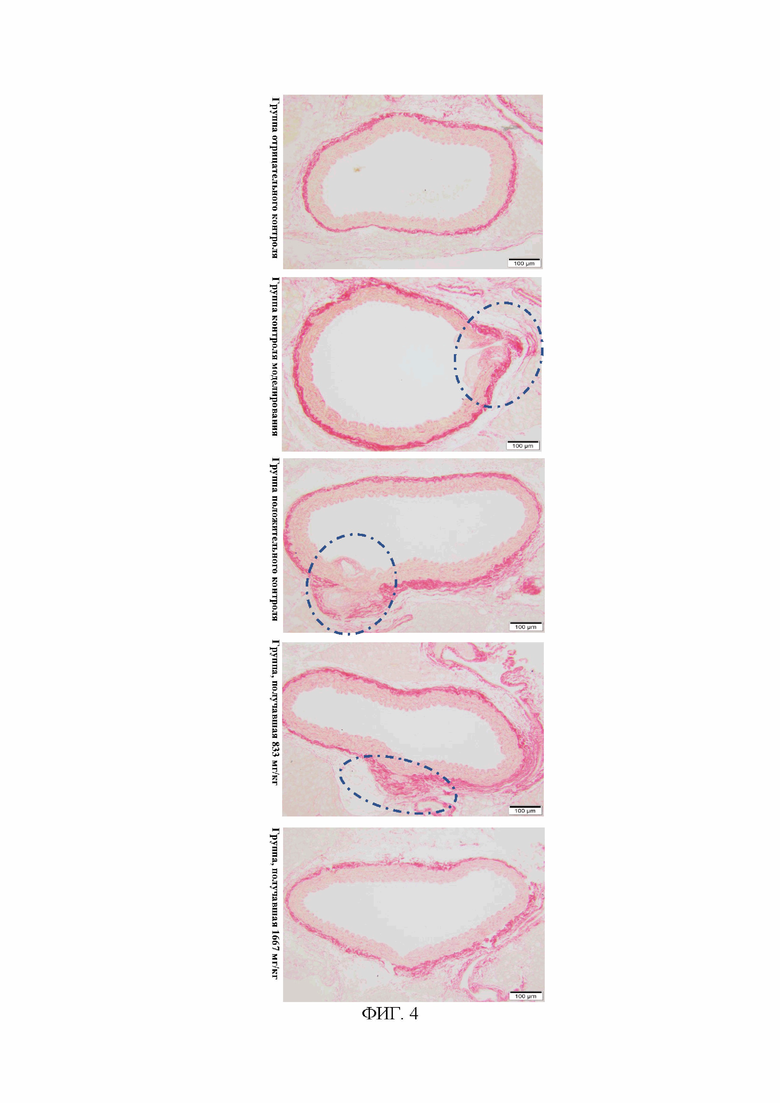
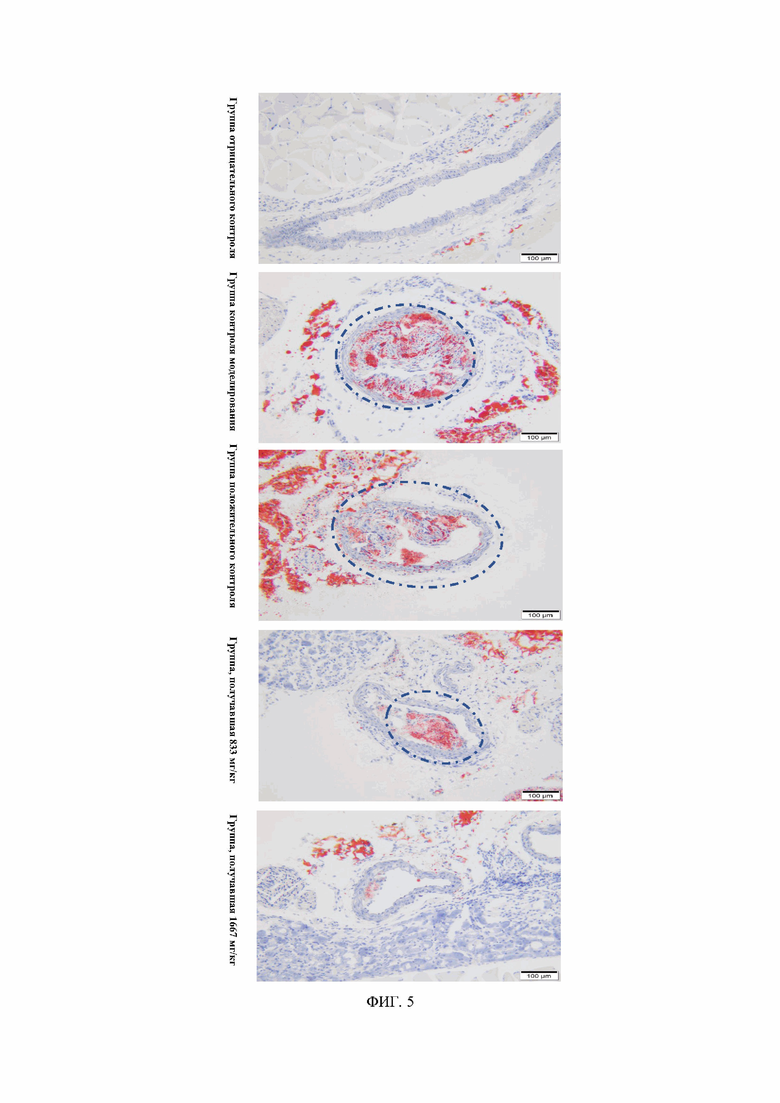
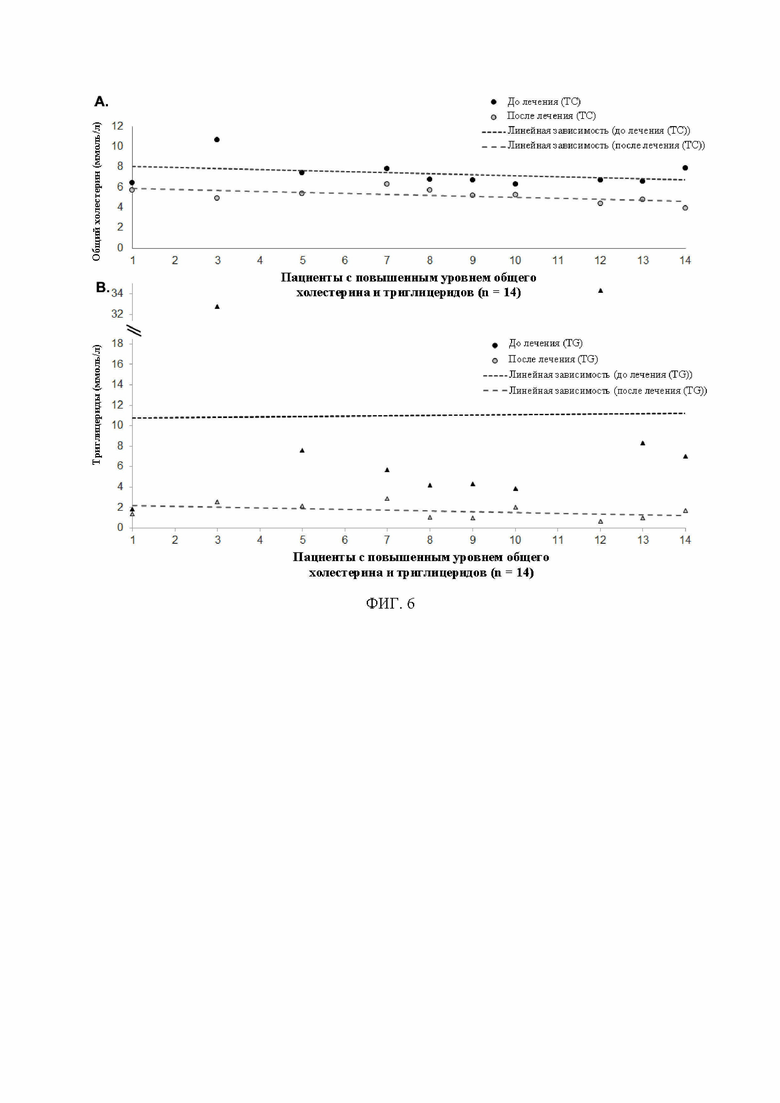
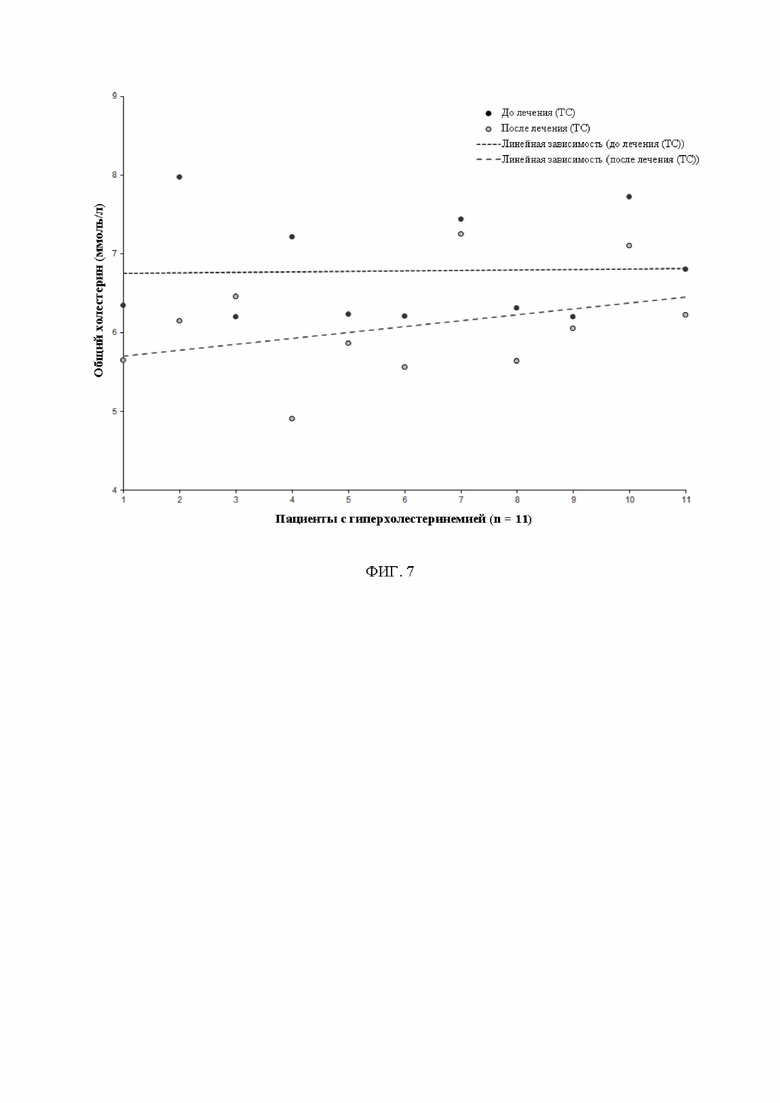

Группа изобретений относится к фармацевтике, а именно к композициям традиционной китайской медицины для профилактики или лечения повышенного уровня липидов в крови, повышенного уровня триглицеридов, повышенного уровня холестерина, гиперлипидемии и атеросклероза. Композиция традиционной китайской медицины для профилактики или лечения повышенного уровня липидов в крови, повышенного уровня триглицеридов, повышенного уровня холестерина, гиперлипидемии и атеросклероза, при этом композицию традиционной китайской медицины готовят из следующих исходных материалов, в весовых частях: 20-30 частей корня володушки, 10-20 частей незрелых плодов апельсина, 5-15 частей корня ревеня, 5-10 частей корня шлемника байкальского, 5-15 частей корня пиона белого, 5-10 частей сушеного корневища имбиря, 7-15 частей пиявки, 5-15 частей корня солодки, 5-15 частей высушенного корня кодонопсиса, 5-15 частей корневища атрактилодеса крупноголового и 10-20 частей клубня пинеллии. Композиция традиционной китайской медицины для профилактики или лечения повышенного уровня липидов в крови, повышенного уровня триглицеридов, повышенного уровня холестерина, гиперлипидемии и атеросклероза, где композиция традиционной китайской медицины приготовлена из следующих исходных материалов в весовых частях: 20-30 частей корня володуши, 10-20 частей незрелых плодов апельсина, 5-15 частей корня ревеня, 5-10 частей корня шлемника байкальского, 5-15 частей корня белого пиона, 5-10 частей сушеного корневища имбиря, 7-15 частей пиявки, 5-15 частей корня солодки, 5-15 частей высушенного корня кодонопсиса, 5-15 частей корневища атрактилодеса крупноголового, 10-20 частей клубня пинеллии и 10-35 частей раковины устрицы. Композиция традиционной китайской медицины для предотвращения или лечения повышенного уровня липидов в крови, повышенного уровня триглицеридов, повышенного уровня холестерина, гиперлипидемии и атеросклероза, где композиция традиционной китайской медицины готовится из следующих исходных материалов в весовых частях: 20-30 частей корня володуши, 10-20 частей незрелых плодов апельсина, 5-15 частей корня ревеня, 5-10 частей корня шлемника байкальского, 5-15 частей корня белого пиона, 5-10 частей сушеного корневища имбиря, 7-15 частей пиявки, 5-15 частей корня солодки, 5-15 частей высушенного корня кодонопсиса, 5-15 частей корневища атрактилодеса крупноголового, 10-20 частей клубня пинеллии, 10-35 частей раковины устрицы и 5-12 частей красного ферментированного риса. Вышеописанные композиции эффективны для профилактики или лечения повышенного уровня липидов в крови, повышенного уровня триглицеридов, повышенного уровня холестерина, гиперлипидемии и атеросклероза. 3 н. и 5 з.п. ф-лы, 8 ил., 15 табл., 6 пр.
1. Композиция традиционной китайской медицины для профилактики или лечения повышенного уровня липидов в крови, повышенного уровня триглицеридов, повышенного уровня холестерина, гиперлипидемии и атеросклероза, при этом композицию традиционной китайской медицины готовят из следующих исходных материалов в весовых частях: 20-30 частей корня володушки, 10-20 частей незрелых плодов апельсина, 5-15 частей корня ревеня, 5-10 частей корня шлемника байкальского, 5-15 частей корня пиона белого, 5-10 частей сушеного корневища имбиря, 7-15 частей пиявки, 5-15 частей корня солодки, 5-15 частей высушенного корня кодонопсиса, 5-15 частей корневища атрактилодеса крупноголового и 10-20 частей клубня пинеллии.
2. Композиция традиционной китайской медицины по п. 1, причем указанную композицию традиционной китайской медицины готовят из следующего сырья в весовых частях: 25 частей корня володушки, 15 частей незрелых плодов апельсина, 10 частей корня ревеня, 6 частей корня шлемника байкальского, 10 частей корня пиона белого, 6 частей сушеного корневища имбиря, 10 частей пиявки, 10 частей корня солодки, 10 частей высушенного корня кодонопсиса, 10 частей корневища атрактилодеса крупноголового и 15 частей клубня пинеллии.
3. Композиция традиционной китайской медицины для профилактики или лечения повышенного уровня липидов в крови, повышенного уровня триглицеридов, повышенного уровня холестерина, гиперлипидемии и атеросклероза, где композиция традиционной китайской медицины приготовлена из следующих исходных материалов в весовых частях: 20-30 частей корня володуши, 10-20 частей незрелых плодов апельсина, 5-15 частей корня ревеня, 5-10 частей корня шлемника байкальского, 5-15 частей корня белого пиона, 5-10 частей сушеного корневища имбиря, 7-15 частей пиявки, 5-15 частей корня солодки, 5-15 частей высушенного корня кодонопсиса, 5-15 частей корневища атрактилодеса крупноголового, 10-20 частей клубня пинеллии и 10-35 частей раковины устрицы.
4. Композиция традиционной китайской медицины по п. 3, причем указанную композицию традиционной китайской медицины готовят из следующего сырья в весовых частях: 25 частей корня володушки, 15 частей незрелых плодов апельсина, 10 частей корня ревеня, 6 частей корня шлемника байкальского, 10 частей корня пиона белого, 6 частей сушеного корневища имбиря, 10 частей пиявки, 10 частей корня солодки, 10 частей высушенного корня кодонопсиса, 10 частей корневища атрактилодеса крупноголового, 15 частей клубня пинеллии и 30 частей раковины устрицы.
5. Композиция традиционной китайской медицины для предотвращения или лечения повышенного уровня липидов в крови, повышенного уровня триглицеридов, повышенного уровня холестерина, гиперлипидемии и атеросклероза, где композиция традиционной китайской медицины готовится из следующих исходных материалов в весовых частях: 20-30 частей корня володуши, 10-20 частей незрелых плодов апельсина, 5-15 частей корня ревеня, 5-10 частей корня шлемника байкальского, 5-15 частей корня белого пиона, 5-10 частей сушеного корневища имбиря, 7-15 частей пиявки, 5-15 частей корня солодки, 5-15 частей высушенного корня кодонопсиса, 5-15 частей корневища атрактилодеса крупноголового, 10-20 частей клубня пинеллии, 10-35 частей раковины устрицы и 5-12 частей красного ферментированного риса.
6. Композиция традиционной китайской медицины по п. 5, причем указанную композицию традиционной китайской медицины готовят из следующего сырья в весовых частях: 25 частей корня володушки, 15 частей незрелых плодов апельсина, 10 частей корня ревеня, 6 частей корня шлемника байкальского, 10 частей корня пиона белого, 6 частей сушеного корневища имбиря, 10 частей пиявки, 10 частей корня солодки, 10 частей сушенного корня кодонопсиса, 10 частей корневища атрактилодеса крупноголового, 15 частей клубня пинеллии, 30 частей раковины устрицы и 10 частей красного ферментированного риса.
7. Композиция традиционной китайской медицины по любому из пп. 1-6, причем указанная композиция традиционной китайской медицины представляет собой состав для перорального применения.
8. Композиция традиционной китайской медицины по п. 7, причем указанная композиция традиционной китайской медицины представляет собой отвар, гранулу, таблетку или капсулу.
| CN 106922892 A, 07.07.2017 | |||
| ЛЕКАРСТВЕННЫЙ ПРЕПАРАТ ДЛЯ ЛЕЧЕНИЯ ДИАБЕТА И СПОСОБ ЕГО ИЗГОТОВЛЕНИЯ | 2008 |
|
RU2485968C2 |
| CN 10642113 A, 15.03.2017 | |||
| CN 107789479 A, 13.03.2018 | |||
| CN 108671111 A, 19.10.2018. | |||
Авторы
Даты
2023-11-02—Публикация
2021-01-20—Подача