Настоящее изобретение относится к области здравоохранения. Более конкретно, изобретение относится к применению холиновой соли янтарной кислоты в производстве инъекционного лекарственного средства для лечения инфаркта мозга у человека.
Инфарктом мозга (инфарктом головного мозга) называют фокальный ишемический некроз вещества мозга. Инфаркт мозга вызывает неврологический дефицит, являющийся преобладающей причиной инвалидизации населения (3,2 на 1000 человек), причем 31% пациентов перенесших инфаркт мозга нуждаются в посторонней помощи для ухода за собой, 20% не могут самостоятельно ходить и только лишь 8% могут вернуться к прежней работе. Медико-демографические показатели Российской Федерации в 2012 году` 2013: Стат. справочник/Минздрав России. - М., 2013. - 180 c.
Нормальный средний мозговой кровоток у взрослых людей составляет около 50 мл/100г/мин. Lassen NA. J Cereb Blood Flow Metab. 1985 Sep;5(3):347-9. Церебральной ишемией называют любое снижение мозгового кровотока ниже этой нормы, причем последствия зависят от степени снижения. Снижение кровотока в два раза от нормального уровня ведет к нарушениям метаболизма, а именно обратимому снижению синтеза белка и экспрессии генов в ткани мозга. Снижение кровотока в три раза от нормы до уровня 16-18 мл/100 г/мин вежет к потере электрической функции нейронов. Инфаркт мозга возникает при падении кровотока в пять раз до порогового уровня 10-12 мл/100 г/мин и связан с острым нарушением ионного гемостаза клеток мозга и общего коллапса потенциала клеточных мембран. Markus HS. Cerebral perfusion and stroke. J Neurol Neurosurg Psychiatry. 2004 Mar;75(3):353-61. Таким образом, церебральная ишемия не всегда и необязательно ведет к инфаркту мозга, а инфаркт мозга возникает только при падении мозгового кровотока ниже порогового значения, составляющего одну пятую от нормы.
Инфаркт мозга как заболевание указан в классе I63 Международной классификации болезней 10-й персмотр (МКБ-10). Клинические руководства выделяют следующие временные периоды после инфаркта мозга: острейший период - первые 3 сут; острый период - до 28 сут; ранний восстановительный период - до 6 мес.; поздний восстановительный период - до 2 лет; период остаточных явлений - после 2 лет, причем медикаментозная терапия инфаркта мозга в эти периоды отличается по целям и выбору лекарственного средства. Неврология: национальное руководство. Под ред. Е. И. Гусева, А. Н. Коновалова, В. И. Скворцовой. 2-е изд., перераб. и доп. М.: ГЭОТАР-Медиа 2018; 1: 880.
Медикаментозная терапия инфаркта мозга в острый период направлена на поддержание основных жизненно-важных функций организма (базисная терапия) и включает в себя обеспечение адекватного дыхания, поддержание кровообращения, контроль и коррекцию водно-электролитных нарушений, уменьшение отека мозга, профилактику и лечение пневмонии, а также, тромболитическую терапию.
Медикаментозная терапия клинического синдрома, вызванного инфарктом мозга, в восстановительный период отличается от терапии острого периода и направлена на стабилизацию и постепенный регресс неврологической симптоматики. Согласно действующим клиническим рекомендациям, коммерчески доступная медикаментозная терапия, направленная на улучшение восстановления неврологических функций в восстановительный период после инфаркта мозга в настоящее время не является абсолютно обоснованной с позиций доказательной медицины (с уровнем убедительности рекомендаций А и уровнем достоверности доказательств - 1), и в настоящее время не существует "золотого стандарта" такой терапии. Таким образом, существует потребность в новых и эффективных средствах лечения инфаркта мозга, особенно в восстановительном периоде, для снижения неврологического дефицита, снижения общей инвалидизации, повышения активности повседневной жизнедеятельности и снижения зависимости больного от помощи других лиц.
Холиновая соль янтарной кислоты (2:1), известная также как дихолинсукцинат, бис[(2-гидрокси)-N,N,N-триметилэтанаминий] янтарнокислый и бис[(N-2-гидроксиэтил)-N,N,N-триметиламиний] янтарнокислый, представляет собой соль холина и янтарной кислоты с широким спектром фармакологической активности, выявленной в исследованиях на животных. Storozheva ZI et al., BMC Pharmacol. 2008, 8:1. Pomytkin IA, Semenova NA. Dokl Biochem Biophys. 2005, 403:289-92. Pomytkin IA et al. Izv Akad Nauk Ser Biol. 2007:183-7.
Патент RU2281765 раскрывает cпособ лечения церебральной ишемии на ее модели (как указано в формуле изобретения) у млекопитающего путем инъекционного введения эффективных количеств янтарнокислого бис[(2-гидроксиэтил)-N,N,N-триметиламиния], где указанная модель была вызвана хронической перевязкой двух сонных артерий у крыс. Эта модель известна как модель хронической церебральной гипоперфузии с уровнем снижения церебрального кровотока в два раза от нормы из-за хорошо развитого виллизиевого круга у крыс и ведущая к нейропатологическим изменениям, релевантным наблюдаемым при нейродегенеративных заболеваниях типа сосудистой деменции и болезни Альцгеймера, но не приводящая к инфаркту мозга. Farkas E et al. Brain Res Rev. 2007 Apr;54(1):162-80. Таким образом, лечение инфаркта мозга янтарнокислым бис[(2-гидроксиэтил)-N,N,N-триметиламинием] неизвестно из RU2281765.
Практика показывает, что в настоящее время нет экспериментальных животных моделей инфаркта мозга (биомоделей), релевантных инфаркту мозга у человека и эффективность средства-кандидата для лечения инфаркта мозга у человека не может быть предсказана по результатам исследований на животных. Так, несмотря на наличие более 1000 успешных доклинических исследований средств-кандидатов на биомоделях инфаркта мозга, только два кандидата (<0,2% от общего числа) показали эффективность в клинических испытаниях на людях. O'Collins VE et al. Ann Neurol. 2006 Mar;59(3):467-77. Lourbopoulos A et al. Front Neurosci. 2021 May 14;15:652403. Таким образом, эффективность новых лекарственных средств лечения инфаркта мозга у человека может быть выявлена только в рандомизированных клинических испытаниях.
С позиций доказательной медицины, эффективность медикаментозной терапии инфаркта мозга оценивают с использованием шкалы оценки неврологического дефицита Национального института здравоохранения (NIHSS), шкалы Бартела для оценки активности повседневной жизнедеятельности и независимости в повседневной жизни, и шкалы Рэнкина для оценки общей инвалидизации и примерной степени зависимости больного от помощи других лиц. Клинические рекомендации - 2021-2022-2023 (01.09.2021) - Утверждены Минздравом РФ.
Авторы изобретения обнаружили, что холиновая соль янтарной кислоты (2:1) эффективна в лечении инфаркта мозга у человека при инъекционном введении.
Настоящее изобретение относится к применению соединения формулы (I):
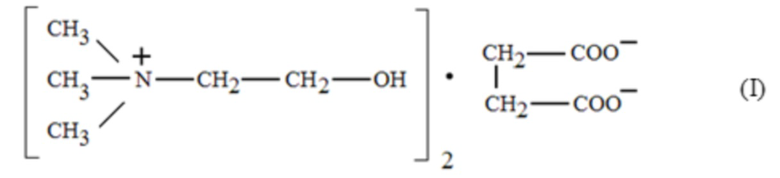
в производстве инъекционного лекарственного средства для лечения инфаркта мозга у человека.
Техническим результатом настоящего изобретения является статистически значимое клиническое улучшение у пациентов, перенесших инфаркт мозга и получавших инъекционное лекарственное средство, произведенное с применением соединения (I) по сравнению с пациентами, получавшими плацебо, в рандомизированных клинических испытаниях.
Термин «клиническое улучшение» означает улучшение, выявленное по результатам рандомизированных двойных слепых, плацебо-контролируемых клинических испытаний.
Предпочтительно, клиническое улучшение включает снижение неврологического дефицита по шкале NIHSS, повышение активности повседневной жизнедеятельности и независимости в повседневной жизни по шкале Бартела, снижение общей инвалидизации и примерной степени зависимости больного от помощи других лиц по шкале Рэнкина, и/или по шкале общего клинического впечатления.
Получение соединения формулы (I) описано в патенте RU2228174.
Термин «лекарственное средство» используется в настоящем изобретении в значении, установленном Федеральным законом от 12.04.2010 N 61-ФЗ (ред. от 28.11.2018) "Об обращении лекарственных средств", статья 4.
Термин «производство» лекарственного средства означает производство лекарственного средства в значении, установленном Федеральным законом от 12.04.2010 N 61-ФЗ (ред. от 28.11.2018) "Об обращении лекарственных средств", статья 4, а именно как деятельность по производству лекарственных средств организациями-производителями лекарственных средств на одной стадии, нескольких или всех стадиях технологического процесса, а также по хранению и реализации произведенных лекарственных средств.
Термин «инъекционное лекарственное средство» означает лекарственное средство произведенное в форме, подходящей для инъекционного введения и обеспечивающей достижение необходимого лечебного эффекта.
Термин «инъекционное введение» означает внутримышечное, внутривенное и/или подкожное введение.
Предпочтительно, лекарственное средство настоящего изобретения производится в виде водного раствора с содержанием соединения (I) от 1,0 до 20,0 мас.%, более предпочтительно от 5,0 до 10,0 мас. %, в ампулированной форме.
Предпочтительно, лекарственное средство настоящего изобретения вводится путем внутримышечной инъекции.
Лекарственное средство настоящего изобретения может быть произведено с использованием методов и фармацевтических процедур, хорошо известных из уровня техники и описанных, например, в Фармацевтическом научном справочнике Ремингтона. Remington's Pharmaceutical Sciences, seventeenth edition, ed. Alfonso R. Gennaro, Mack Publishing Company, Easton, Pa., Eighteenth edition, 1990.
Лекарственное средство настоящего изобретения может содержать вспомогательные вещества.
Термин «вспомогательное вещество» относится к веществам неорганического или органического происхождения, используемым в процессе производства, изготовления лекарственных препаратов для придания им необходимых физико-химических свойств. Неисключительными примерами таких веществ являются растворители, консерванты, антиоксиданты, поверхностно-активные вещества (ПАВ), и регуляторы рН среды.
Примерами приемлемых регуляторов рН среды являются буферные растворы янтарной кислоты, натрия фосфата одно- и двузамещенного, натрия цитрата, натрия гидроксида, натрия гидрокарбоната, натрия тетрабората, которые могут обеспечить поддержание рН раствора соединения формулы (I) в интервале от 5,0 до 8,0.
Термин «инфаркт мозга» означает фокальный ишемический некроз вещества головного мозга. Предпочтительно, инфаркт мозга выявляется с использованием методов магнитно-резонансной томографии (МРТ) и/или компьютерной томографии (КТ).
Лекарственное средство настоящего изобретения может быть использовано для лечения инфаркта мозга в разных временных периодах после инфаркта, в том числе в острейшем, остром периоде, а также в восстановительном периоде, согласно классификации руководства Неврология: национальное руководство. Под ред. Е. И. Гусева, А. Н. Коновалова, В. И. Скворцовой. 2-е изд., перераб. и доп. М.: ГЭОТАР-Медиа 2018; 1: 880.
Предпочтительно, лекарственное средство настоящего изобретения может быть использовано для лечения инфаркта мозга в восстановительном периоде.
Следующие примеры демонстрируют изобретение. Примеры имеют иллюстративное значение и не предназначены для ограничения объема изобретения.
Пример 1
Пример иллюстрирует применение соединения настоящего изобретения в производстве инъекционного лекарственного средства для лечения инфаркта мозга у человека.
Таблица 1 показывает состав лекарственного средства в виде раствора для инъекционного введения, произведенного с применением соединения настоящего изобретения.
При производстве лекарственного средства ингредиенты смешивают в пропорциях, указанных в Таблице 1, полученный раствор подвергают стерильной фильтрации, разливают в ампулы с номинальным объемом 2 мл, и ампулы запаивают в токе азота. Лекарственное средство вводят инъекционно пациенту с инфарктом мозга, три раза в день, в течение 14 дней.
Пример 2
Пример иллюстрирует эффективность соединения настоящего изобретения в снижении неврологического дефицита у больных, перенесших инфаркт мозга.
Эффективность соединения настоящего изобретения в составе инъекционного лекарственного средства из примера 1 была изучена в многоцентровом рандомизированном двойном слепом, плацебо-контролируемом исследовании у пациентов с инфарктом мозга, подтвержденным компьютерной и/или магнитно-резонансной томографией. В исследовании участвовало 160 пациентов с давностью инфаркта мозга не менее 3 недель и не более 2 месяцев от момента появления неврологической симптоматики. Пациенты были рандомизированы в две группы и получали: в первой группе внутримышечно инъекционное лекарственное средство (Препарат) из примера 1 по 200 мг 3 раза в день в течение 14 дней (n=80); во второй группе внутримышечно плацебо (Плацебо), отличающееся от инъекционного лекарственного средства из примера 1 только отсутствием действующего вещества, 3 раза в день в течение 14 дней (n=80).
Для оценки влияния лечения на неврологический дефицит у пациентов с инфарктом мозга, использовали шкалу Национального института здравоохранения (NIHSS), где оценка дефицита проводили по одиннадцати показателям, включая: уровень сознания, движение глазных яблок, поле зрения, парез лицевой мускулатуры, движение верхних конечностей, движение нижних конечностей, атаксия конечностей, чувствительность, речь, дизартрия, и угнетение восприятия (невнимание). Отсутствие неврологического дефицита соответствует 0 баллов, а 42 балла соответствует максимальному количеству баллов при самом тяжелом неврологическом дефиците.
Оценку неврологического дефицита у пациентов проводили до начала терапии (Д0), в конце двухнедельного периода терапии (Д14) и в конце двухнедельного периода наблюдений после прекращения терапии (Д30). Результаты представлены в Таблице 2 как среднее количество баллов по шкале NIHSS ± стандартное отклонение. Изменение неврологического статуса в группах в процессе исследования рассчитывали в баллах по уравнению: Δ = среднее баллов NIHSS (Д14 или Д30) - среднее баллов NIHSS (Д0).
***Достоверное отличие от Плацебо (p <0,001).
Двусторонний дисперсионный анализ ANOVA с повторными измерениями выявил статистически значимое различие между группами как по фактору времени (p <0,0001; F = 99,5), так и по фактору применяемой терапии (р = 0,004; F = 5,58). Таблица 2 показывает статистически значимое снижение индекса неврологического дефицита в группе пациентов, применявших Препарат, по сравнению с группой пациентов, применявших Плацебо, к моменту окончания терапии (Д14, p = 0,0005) и через две недели после окончания терапии (Д30, p = 0,0007). Таким образом, инъекционное лекарственное средство, произведенное с применением соединения (I) настоящего изобретения, обеспечивает статистически значимое клиническое улучшение у пациентов, перенесших инфаркт мозга, по шкале неврологического дефицита NIHSS.
Пример 3
Пример иллюстрирует эффективность соединения настоящего изобретения в снижении инвалидизации и степени зависимости от помощи других лиц у больных с инфарктом мозга.
Для оценки влияния лечения на общую инвалидизацию и примерную степень зависимости больного от помощи других лиц использовали шкалу Рэнкина, где 0 баллов соответствует отсутствию у пациента ограничений жизнедеятельности, в том числе незначительных; 1 балл соответствует отсутствию у пациента существенных нарушений, несмотря на наличие некоторых симптомов, причем пациент может выполнять все свои обычные действия и обязанности; 2 балла соответствуют легкой степени инвалидности, причем пациент не способен выполнять прежние действия, но может справляться с повседневными обязанностями без посторонней помощи; 3 балла соответствуют умеренной степени инвалидности, причем пациент нуждается в некоторой посторонней помощи, но может самостоятельно передвигаться; 4 балла соответствуют выраженной степени инвалидности, причем пациент не способен ходить и обслуживать себя без посторонней помощи; 5 баллов соответствуют тяжелой степени инвалидности, причем пациент прикован к постели и требует постоянный уход.
Оценку проводили у пациентов из примера 2 до начала терапии (Д0), в конце двухнедельного периода терапии (Д14) и в конце двухнедельного периода наблюдений после прекращения терапии (Д30). Результаты представлены в Таблице 3 как среднее количество баллов по шкале Рэнкина ± стандартное отклонение. Изменение индекса Рэнкина в группах в процессе исследования рассчитывали в баллах по уравнению: Δ = среднее баллов Рэнкина (Д14 или Д30) - среднее баллов Рэнкина (Д0).
**Достоверное отличие от Плацебо (p <0,01). ***Достоверное отличие от Плацебо (p <0,001).
Двусторонний дисперсионный анализ ANOVA с повторными измерениями выявил статистически значимое различие между группами как по фактору времени (p <0,0001; F = 58,04), так и по фактору применяемой терапии (р = 0,037; F = 3,36). Таблица 3 показывает статистически значимое снижение индекса Рэнкина в группе пациентов, применявших Препарат, по сравнению с группой пациентов, применявших Плацебо, к моменту окончания терапии (Д14, p = 0,0003) и через две недели после окончания терапии (Д30, p = 0,0029). Таким образом, инъекционное лекарственное средство произведенное с применением соединения (I) настоящего изобретения обеспечивает статистически значимое клиническое улучшение у пациентов, перенесших инфаркт мозга, по шкале Рэнкина.
Пример 4
Пример иллюстрирует эффективность соединения настоящего изобретения в повышении активности повседневной жизнедеятельности у больных с инфарктом мозга.
Для оценки влияния лечения на активность повседневной жизнедеятельности и независимость в повседневной жизни использовали индекс Бартела, где 0-20 баллов соответствует полной зависимости, 25-60 баллов - выраженной зависимости, 65-90 баллов - умеренной зависимости, 95 баллов - легкой зависимости и 100 баллов - полной независимости (не нуждается в помощи).
Оценку проводили у пациентов из примера 2 до начала терапии (Д0), в конце двухнедельного периода терапии (Д14) и в конце двухнедельного периода наблюдений после прекращения терапии (Д30). Результаты представлены в Таблице 4 как среднее количество баллов по шкале Бартела ± стандартное отклонение. Изменение индекса Бартела в группах в процессе исследования рассчитывали в баллах по уравнению: Δ = среднее баллов Бартела (Д14 или Д30) - среднее баллов Бартела (Д0).
*Достоверное отличие от Плацебо (p <0,05).
Двусторонний дисперсионный анализ ANOVA с повторными измерениями выявил статистически значимое различие между группами по фактору времени (p <0,0001; F = 27,33). Таблица 4 показывает статистически значимое повышение индекса Бартела в группе пациентов, применявших Препарат, по сравнению с группой пациентов, применявших Плацебо к моменту окончания исследования (Д30, p = 0,039). Таким образом, инъекционное лекарственное средство произведенное с применением соединения (I) настоящего изобретения обеспечивает статистически значимое клиническое улучшение у пациентов, перенесших инфаркт мозга, по шкале Бартела.
Пример 5
Пример иллюстрирует влияние соединения настоящего изобретения на тяжесть когнитивного расстройства у больных с инфарктом мозга.
Для оценки влияния лечения на тяжесть когнитивного расстройства использовали Монреальскую шкалу оценки когнитивных функций (MoCA), включая внимание и концентрацию, управляющие функции, память, язык, зрительно-конструктивные навыки, абстрактное мышление, счет и ориентацию. Отсутствие когнитивных нарушений соответствует оценке ≥26 баллов, о наличии когнитивных нарушений свидетельствует оценка <26 баллов.
Оценку проводили у пациентов из примера 2 до начала терапии (Д0), в конце двухнедельного периода терапии (Д14) и в конце двухнедельного периода наблюдений после прекращения терапии (Д30). Результаты представлены в Таблице 5 как среднее количество баллов по шкале MoCA ± стандартное отклонение. Изменение индекса MoCA в группах в процессе исследования рассчитывали в баллах по уравнению: Δ = среднее баллов MoCA (Д14 или Д30) - среднее баллов MoCA (Д0).
Двусторонний дисперсионный анализ ANOVA с повторными измерениями выявил статистически значимое различие между группами по фактору времени (p <0,0001; F = 210,52), но не по фактору применяемой терапии (р = 0,974; F = 0,03). Таблица 5 показывает успешное восстановление когнитивной функции как в группе пациентов, применявших Препарат, так и в группе пациентов, применявших Плацебо, но без статистически значимого различия между группами.
Пример 6
Пример иллюстрирует эффективность соединения настоящего изобретения в общем клиническом улучшении у больных с инфарктом мозга.
Для оценки влияния лечения на общее клиническое улучшение до и после начала приема лекарств использовали шкалу общего клинического впечатления, включающей следующие оценки: выраженное улучшение/ умеренное улучшение/ легкое улучшение/ нет изменений/ легкое ухудшение/ умеренное ухудшение/ выраженное ухудшение по визитам и терапевтическим группам.
Оценку проводили у пациентов из примера 2. Точный критерий Фишера выявил статистически значимое улучшение общего клинического впечатления в группе пациентов, применявших Препарат, по сравнению с группой пациентов, применявших Плацебо как моменту окончания терапии (Д14; p <0,001) и через две недели после окончания терапии (Д30; p = 0,009).
Таким образом, инъекционное лекарственное средство произведенное с применением соединения (I) настоящего изобретения обеспечивает статистически значимое клиническое улучшение у пациентов, перенесших инфаркт мозга, по шкале общего клинического впечатления.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПРОГНОЗИРОВАНИЯ ТЕЧЕНИЯ ОСТРОГО ПЕРИОДА ИШЕМИЧЕСКОГО ИНСУЛЬТА В ПЕРВЫЕ 24 ЧАСА ПРИ ПРОВЕДЕНИИ ТРОМБОЛИТИЧЕСКОЙ ТЕРАПИИ | 2015 |
|
RU2573801C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ВОССТАНОВЛЕНИЯ ДВИГАТЕЛЬНОЙ ФУНКЦИИ У БОЛЬНЫХ В ОСТРОМ ПЕРИОДЕ ИШЕМИЧЕСКОГО ИНСУЛЬТА В БАССЕЙНЕ АРТЕРИЙ КАРОТИДНОЙ СИСТЕМЫ | 2012 |
|
RU2508048C1 |
| Способ проведения тромболитической терапии при инсульте | 2023 |
|
RU2820542C1 |
| Способ мониторинга пациентов с острыми нарушениями мозгового кровообращения | 2023 |
|
RU2820541C1 |
| Способ прогноза неблагоприятного исхода у пациентов с ишемическим инсультом | 2021 |
|
RU2769488C1 |
| СПОСОБ ЛЕЧЕНИЯ ИШЕМИЧЕСКОГО ИНСУЛЬТА | 2018 |
|
RU2670203C1 |
| Способ оценки реабилитационного потенциала пациента, перенесшего ишемический инсульт | 2021 |
|
RU2777805C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМБИНАЦИЯ, ВКЛЮЧАЮЩАЯ ЭПИДЕРМАЛЬНЫЙ ФАКТОР РОСТА И ПЕПТИД GHRP6 В КАЧЕСТВЕ СТИМУЛЯТОРА СЕКРЕЦИИ, ДЛЯ ВОССТАНОВЛЕНИЯ ПОСЛЕ ПОВРЕЖДЕНИЯ ГОЛОВНОГО МОЗГА | 2019 |
|
RU2776812C1 |
| Способ комплексного лечения больных с ишемическим инсультом в остром периоде и на этапе ранней реабилитации с использованием инфракрасного терагерцевого излучения | 2018 |
|
RU2706382C1 |
| Способ улучшения раннего функционального неврологического восстановления у больных с ишемическим инсультом и нарушением дыхания во сне | 2017 |
|
RU2645410C1 |
Изобретение относится к области медицины и фармацевтики, а именно, к применению соединения формулы (I) в производстве инъекционного лекарственного средства для лечения инфаркта мозга у человека. Использование изобретения позволяет эффективно лечить инфаркт мозга у человека. 5 табл., 6 пр.
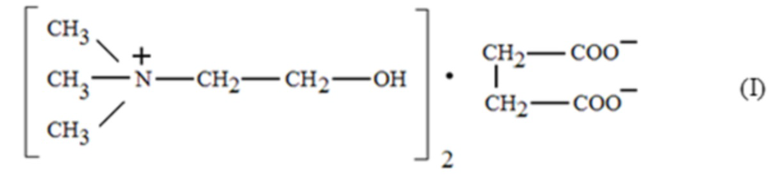
Применение соединения формулы (I):
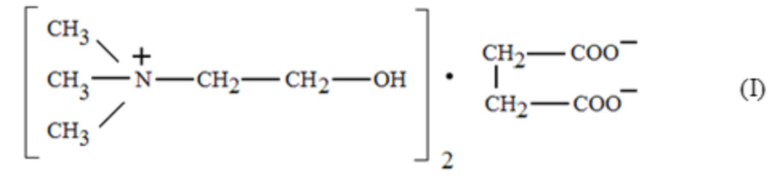
в производстве инъекционного лекарственного средства для лечения инфаркта мозга у человека.
| Приспособление для держания электролампы в полости рта для врачебных целей | 1928 |
|
SU10890A1 |
| ЛЕКАРСТВЕННЫЕ СРЕДСТВА ДЛЯ ЛЕЧЕНИЯ ИШЕМИЧЕСКИХ ЗАБОЛЕВАНИЙ | 2001 |
|
RU2311921C2 |
| ПРОИЗВОДНЫЕ БЕНЗАМИДИНА | 2000 |
|
RU2222529C2 |
| WO 2017046304 A1, 23.03.2017 | |||
| WO 2015149707 A1, 08.10.2015. | |||
Авторы
Даты
2023-11-08—Публикация
2023-04-25—Подача