Область техники
Настоящее изобретение относится к области органической химии, а именно к способу получения новых тиопроизводных пирролидин-2,5-дионов с фрагментом хиназолина общей формулы (I), которые представляют интерес как вещества с потенциальной биологической активностью, в частности, проявляющих противовирусную ингибирующую активность в отношении главной протеазы Mpro бета-коронавируса SARS-CoV-2.
Уровень техники
Пандемия, известная как COVID-19, была вызвана severe acute respiratory syndrome coronavirus 2 (SARS-CoV-2). Связанные с ней последствия, являются угрозой для общественного здравоохранения и экономики практически всех стран мира.
Высоко патогенный SARS-CoV-2 принадлежит к роду бета-коронавирусов семейства Coronaviridae, наряду с SARS-CoV и Middle East respiratory syndrome coronavirus (MERS-CoV) [T. Pillaiyar, L. L. Wendt, M. Manickam, M. Easwaran The recent outbreaks of human coronaviruses: A medicinal chemistry perspective. Med Res Rev. 2021. V.41. P. 72-135]. Именно эти вирусы, в отличие от других бета-коронавирусов (HCoV-ОС43, HCoVHKU1), являются причиной наиболее тяжелых инфекций человека.
Биомишенями при создании лекарственных средств для подавления патогенного действия SARS-CoV-2 могут являться его структурные белки, в частности, спайковый (S) гликопротеин, мембранный (М) белок, малый оболочечный (Е) белок, нуклеокапсидный (N) белок.
Еще большее внимание уделяется поиску ингибиторов жизненного цикла вируса, действующих на неструктурные белковые ферменты (non-structural proteins, nsps) [Anas Shamsi, Taj Mohammad, Saleha Anwar, Samreen Amani, Mohd Shahnawaz Khan, Fohad Mabood Husain, Md. Tabish Rehman, Asimul Islama, Md Imtaiyaz Hassan. Potential drug targets of SARS-CoV-2: From genomics to therapeutics. Internat. J. Biol. Macromolecules. 2020. V. 177. P. 1-9].
Одной из биомишеней этого класса является РНК зависимая полимераза РНК (RNA-dependent RNA polymerase (RdRp) [С.Gil, Т. Ginex, I. Maestro, V. Nozal, L. Barrado-Gil, M. 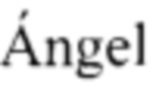 Cuesta-Geijo, J. Urquiza, D. Ramirez, C. Alonso, N. E. Campillo, A. Martinez. COVID-19: Drug Targets and Potential Treatments J. Med. Chem. 2020, 63, P. 12359-12386; T. Pillaiyar, L. L. Wendt, M. Manickam, M. Easwaran The recent outbreaks of human coronaviruses: A medicinal chemistry perspective. Med Res Rev. 2021. V.41. P. 72-135].
Cuesta-Geijo, J. Urquiza, D. Ramirez, C. Alonso, N. E. Campillo, A. Martinez. COVID-19: Drug Targets and Potential Treatments J. Med. Chem. 2020, 63, P. 12359-12386; T. Pillaiyar, L. L. Wendt, M. Manickam, M. Easwaran The recent outbreaks of human coronaviruses: A medicinal chemistry perspective. Med Res Rev. 2021. V.41. P. 72-135].
К другим важным биомишеням относятся, в частности, главная протеаза (main protease) Mpro (или 3CLpro) и papaine-like протеаза (PLpro) [Sk. Abdul Amin, Suvankar Banerjee, Kalyan Ghosh, Shovanlal Gayen, Tarun Jha. Protease targeted COVID-19 drug discovery and its challenges: Insight into viral main protease (Mpro) and papain-like protease (PLpro) inhibitors. Bioorg. Med. Chem. 2021. V. 29. 115860; Vijay Kumar Bhardwaj, Rahul Singh, Pralay Das, Rituraj Purohit. Evaluation of acridinedione analogs as potential SARS-CoV-2 main protease inhibitors and their comparison with repurposed anti-viral drugs. Computers in Biology and Medicine. 2021. V. 128. 104117; Sheng Guo, Hang Xie, Yu Lei, Bin Liu, Li Zhang, Yechun Xu, Zhili Zuo. Discovery of novel inhibitors against main protease (Mpro) of SARS-CoV-2 via virtual screening and biochemical evaluation Bioorg. Chem. 2021. V. 110. 104767; Sk. Amin, S. Banerjee, S. Gayen, T. Jha. Protease targeted COVID-19 drug discovery: What we have learned from the past SARS-CoV inhibitors? Eur. Jour.Med. Chem. 2021. V. 215. 113294; Ashish M. Kanhed, Dushyant V. Patel, Divya M. Teli, Nirav R. Patel, Mahesh T. Chhabria, Mange Ram Yadav. Identification of potential Mpro inhibitors for the treatment of COVID-19 by using systematic virtual screening approach. Mol. Div. 2021. V. 25. P. 383-401; H. M. Mengist, T. Dilnessa, T. Jin. Structural Basis of Potential Inhibitors Targeting SARS-CoV-2 Main Protease. Front. Chem. 2021. V. 9. 622898. Riddhidev Banerjee, Lalith Perera, L.M. Viranga Tillekeratne. Potential SARS-CoV-2 main protease inhibitors. Drug Discovery Today. 2021. V. 26., P. 804-816].
Наибольший интерес представляет главная протеаза (main protease) Mpro, выполняющая одну из ключевых функций в процессе репликации и транскрипции РНК SARS-CoV-2. Помимо своей функциональной необходимости в вирусной транскрипции и репликации, Mpro не имеет гомологии к любой протеазе человека, и, следовательно, может рассматриваться как безопасная терапевтическая мишень [Zhang, L., Lin, D., Sun, X., Curth, U., Drosten, С, Sauerhering, L., Becker, S., Rox, K., Hilgenfeld, R. Crystal structure of SARS-CoV-2 main protease provides a basis for design of improved a-ketoamide inhibitors. Science (New York, N.Y.). 2020. V. 368 (6489). P. 409-412].
К рекомендованным для лечения COVID-19 известным лекарственных средств, механизм действия которых связывают с подавлением репликации вируса в результате ингибирования главной протеазы (main protease) Mpro, относят эбселен (ebselen), обычно применяемый для лечения сердечно-сосудистых, воспалительных заболеваний, инсультов [Н. Siesa, M. J. Parnham. Potential therapeutic use of ebselen for COVID-19 and other respiratory viral infections. Free Radical Biol. Medicine. 2020. V. 156. P. 107-112; H. M. Mengist, D. Mekonnen, A. Mohammed, R. Shi, T. Jin Potency, Safety, and Pharmacokinetic Profiles of Potential Inhibitors Targeting SARS-CoV-2 Main Protease. Front. Pharmacol. 2021. V. 11. 630500; C. Ma, Y. Hu, J. A. Townsend, P. I. Lagarias, M. T. Marty, A. Kolocouris, J. Wang. Ebselen, Disulfiram, Carmofur, PX-12, Tideglusib, and Shikonin Are Nonspecific Promiscuous SARS-CoV-2 Main Protease Inhibitors. ACS Pharmacol. Transl. Sci. 2020. V. 3. P. 1265-1277; Jin, Z., Du, X., Xu, Y., Deng, Y., Liu, M., Zhao, Y., Zhang, В., Li, X., Zhang, L., Peng, C, Duan, Y., Yu, J., Wang, L., Yang, K., Liu, F., Jiang, R., Yang, X., You, Т., Liu, X., Yang, X., Bai, F., Liu, PL, Liu, X., Guddat, L. W., Xu, W., Xiao, G., Qin, C, Shi, Z., Jiang, H., Rao, Z., Yang, H. Structure of M(pro) from SARS-CoV-2 and discovery of its inhibitors. Nature. 2020. V. 582. P. 289-293], средство для лечения алкоголизма дисульфирам (disulfiram) [N. Fillmore, S. Bell, C. Shen, V. Nguyen, J. La, M. Dubreuil, J. Strymish, M. Brophy, G. Mehta, H. Wu, J. Lieberman, N., C. Sander. Disulfiram associated with lower risk of Covid-19: a retrospective cohort study. MedRxiv preprint. Doi: https://doi.org/10.1101/2021.03.10.21253331; K. Steuten, H. Kim, J. C. Widen, В. M. Babin, O. Onguka, S. Lovell, O. Bolgi, B. Cerikan, C. J. Neufeldt, M.Cortese, R. K. Muir, J. M. Bennett, R. Geiss-Friedlander, C. Peters, R. Bartenschlager, M. Bogyo. Challenges for Targeting SARS-CoV-2 Proteases as a Therapeutic Strategy for COVID-19. ACS Infectious Diseases. 2021, Article ASAP; S. Guo, H. Xie, Y. Lei, B. Liu, L. Zhang, Y. Xu, Z. Zuo. Discovery of novel inhibitors against main protease (Mpro) of SARS-CoV-2 via virtual screening and biochemical evaluation. Bioorganic Chemistry. 2021. V. 110, 104767; N. Lobo-Galo, M. 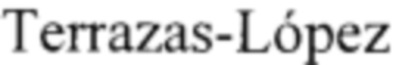 , A.
, A. 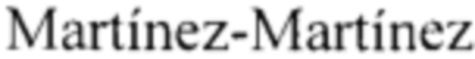 ,
, 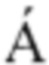 . Gabriel Diaz-Sanchez (2020): FDA-approved thiol-reacting drugs that potentially bind into the SARS-CoV-2 main protease, essential for viral replication, Journal of Biomolecular Structure and Dynamics, DOI: 10.1080/07391102.2020.1764393].
. Gabriel Diaz-Sanchez (2020): FDA-approved thiol-reacting drugs that potentially bind into the SARS-CoV-2 main protease, essential for viral replication, Journal of Biomolecular Structure and Dynamics, DOI: 10.1080/07391102.2020.1764393].
Недостатком вышеперечисленных препаратов является, например, противопоказания к применению при гиперчувствительности, печеночной и почечной недостаточности, необходимость их использования в достаточно высоких дозах, что также может вызывать нежелательные реакции у пациентов [Yoshimura, A., Kimura, M., Nakayama, H., Matsui, Т., Okudaira, F., Akazawa, S., Ohkawara, M., Cho, Т., Kono, Y., Hashimoto, K., Kumagai, M., Sahashi, Y., Roh, S., Higuchi, S. (2014). Efficacy of disulfiram for the treatment of alcohol dependence assessed with a multicenter randomized controlled trial. Alcoholism, Clinical and Experimental Research, 2014. V.38 (2). P. 572-578], а также невысокая эффективность (концентрация полумаксимального ингибирования Mpro IC50 для дисульфирама 6,10-9,35 μM эбселена 0,67-1,39 μM [С. Ma, Y. Hu, J. A. Townsend, Р. I. Lagarias, M. Т. Marty, A. Kolocouris, J. Wang. Ebselen, Disulfiram, Carmofur, PX-12, Tideglusib, and Shikonin Are Nonspecific Promiscuous SARS-CoV-2 Main Protease Inliibitors. ACS Pharmacol. Transl. Sci. 2020. V. 3. P. 1265-1277].
К настоящему времени отсутствуют целевые терапевтические препараты, которые одобрены для лечения COVID-19, а также не всегда эффективными являются варианты лечения COVID-19.
Заявляемое изобретение основано на использовании соединений класса тиопроизводных пирролидин-2,5-дионов с фрагментом хиназолина, как ингибиторов главной протеазы (main protease) Mpro бета-коронавируса SARs-CoV-2, и которые могут быть рекомендованы для применения в терапии COVID-19.
Известные из уровня техники способы получения тиопроизводных пирролидин-2,5-дионов (сукцинимидов) основаны, как правило, на реакциях нуклеофильного присоединения реагентов, содержащих тиольные (меркапто) группы к циклическим N-замещенным имидам малеиновой кислоты (малеимидам). Процессы проводят в присутствии неорганических (например, NaOH) или органических оснований (например, триэтиламин, пиридин) в различных растворителях. [Ki Duk Park, Rihe Liu, Harold Kohn. Useful Tools for Biomolecule Isolation, Detection, and Identification: Acylhydrazone-Based Cleavable Linkers. Chemistry & Biology. 2009. V. 16. P. 763-772; M. Jegelka, B. Plietker. α-Sulfonyl Succinimides: Versatile Sulfinate Donors in Fe-Catalyzed, Salt-Free, Neutral Allylic Substitution. Chem. Eur. J. 2011, V. 17. P. 10417-10430; S. Yamamoto, H. Tochigi, S. Yamazaki, S. Nakahama, K. Yamaguchi. Synthesis of Amphiphilic Diblock Copolymer Using Heterobifunctional Linkers, Connected by a Photodegradable N-(2-Nitrobenzyl)imide Structure and Available for Two Different Click Chemistries. Bull. Chem. Soc. Japan. 2016. V. 89. P. 481-489; D. Matsuoka, H. Watanabe, Y. Shimizu, H. Kimura, Y. Yagi, R. Kawai, M. Ono, H. Saji. Structure-activity relationships of succinimidyl-Cys-C(O)-Glu derivatives with different near-infrared fluorophores as optical imaging probes for prostate-specific membrane antigen. Bioorg. Med. Chem. 2018, V. 26. P. 2291-2301].
Однако круг меркаптопроизводных, применяемых для этой цели, ограничен карбо-и структурно простыми гетероциклическими соединениями, например, тиофенолами [Mustafa, A.; Askar, W.; Khattab, S.; Mohmad, S.; Sayed, D. On the reactivity of the unsaturated system in N-arylmaleimides. J. Org. Chem. 1960. V. 26, P. 787-789; Pastor, D. S.; Hessel, Т. E.; Odorisio, A. P.; Spivack, D. J. 3-(4-Hydroxyphenylthio)pyrroidine-2,5-diones. J. Heterocycl. Chem. 1985. V. 22. P. 1195-1197], меркаптопиридинами [M. Jegelka, В. Plietker. α-Sulfonyl Succinimides: Versatile Sulfinate Donors in Fe-Catalyzed, Salt-Free, Neutral Allylic Substitution. Chem. Eur. J. 2011, V. 17. P. 10417-10430], меркаптопиримидинами [V. Kumar, R. Mitra, S. Bhattarai, V. A. Nair. Reaction on water: a greener approach for the thia Michael addition on N-aryl maleimides. Synth. Comm. 2011. V. 41. P. 392-404]. При этом выходы целевых продуктов составляют 48-88%, а для их выделения из реакционной массы используются достаточно трудоемкие хроматографические методы.
До настоящего времени неизвестны примеры применения в реакциях с малеимидами меркаптопроизводных, в которых тиольная группа связана с конденсированной гетероциклической системой, в частности, хиназолина.
Для получения соединений формулы I наиболее предпочтительным является выбор алифатических спиртов в качестве растворителей для исключения гетерогенного характера реакции и триэтиламина, как наиболее эффективного основного катализатора.
Технической проблемой, решаемой заявляемым изобретением, является поиск соединений для лечения заболеваний, вызванных бета-коронавирусом, включая SARS-CoV-2, характеризующихся высокой эффективностью связывания с мишенью (главной протеазой Mpro), и, соответственно, подавлением репликации коронавируса.
Раскрытие изобретения
Техническим результатом заявляемого изобретения является получение тиопроизводных пирролидин-2,5-дионов с фрагментом хиназолина с выходами, не ниже, чем для известных методов (до 88%) при достаточно простой процедуре их выделения из реакционной массы посредством простого фильтрования без применения более трудоемких хроматографических методов.
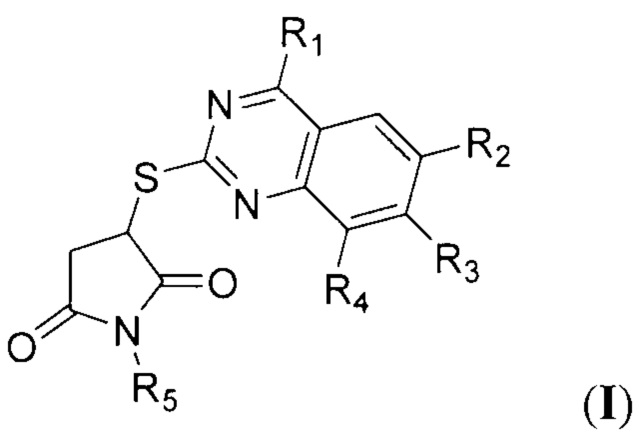
Технический результат достигается способом получения тиопроизводных пирролидин-2,5-дионов с фрагментом хиназолина общей формулы I:
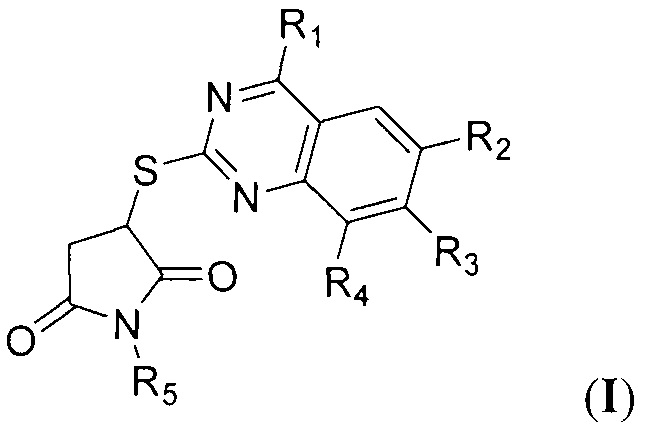
где R1 - метил или арил без заместителей или замещенный по положениям 2, 3, 4, 5, 6;
R2, R3, R4 представляют собой заместитель, выбранный из водорода, алкила С1-С2, алкоксила С1-С2, хлора или фтора;
R5 является бензилом, фенетилом, нафтилом или фенилом, необязательно замещенным один, два или три раза алкилом, галогеном, метокси-, этокси-, ацилокси-, этоксикарбонильной группой, циклоалкилом С3-С6
заключающимся во взаимодействии замещенных 2-меркаптохиназолинов с N-арилмалеимидами в среде метанола в присутствии триэтиламина. Для этого к раствору соответствующего 2-меркаптохиназолина в метаноле сначала прибавляют 1-3 капли триэтиламина, затем прибавляют небольшими порциями N-арилмалеимида, полученную реакционную смесь перемешивают в течение 1-1,5 ч, кипятят 3-4 ч, охлаждают, осадок отфильтровывают и перекристаллизовывают из метанола. При этом используют от 0.01 до 0.011 моль N-арилмалеимида, а для приготовления раствора 2-меркаптохиназолина используют 0.01 моль соответствующего 2-меркаптохиназолина и 20 мл абсолютного метанола.
Осуществление изобретения
Ниже приведены определения терминов, которые используются в описании настоящего изобретения.
«Лекарственное средство (препарат)» - вещество (или смесь веществ в виде фармацевтической композиции), в виде таблеток капсул инъекций, мазей и др. готовых форм предназначенное для восстановления, исправления или изменения физиологических функций у человека и животных, а также для лечения и профилактики болезней, диагностики, анестезии, контрацепции, косметологии и прочего.
«Фармацевтическая композиция» обозначает композицию, включающую в себя соединение формулы 1 и, по крайней мере, один из компонентов, выбранных из группы, состоящей из фармацевтически приемлемых и фармакологически совместимых наполнителей, растворителей, разбавителей, носителей, вспомогательных средств, средств доставки, консерванты, стабилизаторы, наполнители, измельчители, увлажнители, эмульгаторы, суспендирующие агенты, загустители, подсластители, отдушки, ароматизаторы. Пролонгированное действие композиции может быть обеспечено с помощью агентов, замедляющих абсорбцию активного начала, например, моностеарат алюминия и желатин. Примерами подходящих носителей, растворителей, разбавителей и средств доставки являются вода, этанол, полиспирты, а также их смеси, растительные масла (такие, как оливковое масло) и инъекционные органические сложные эфиры (такие, как этилолеат). Примерами наполнителей являются лактоза, молочный сахар, цитрат натрия, карбонат кальция, фосфат кальция и им подобные. Примерами измельчителей и распределяющих средств являются крахмал, алгиновая кислота и ее соли, силикаты. Примерами лубрикантов являются стеарат магния, лаурилсульфат натрия, тальк, а также полиэтиленгликоль с высоким молекулярным весом. Фармацевтическая композиция для перорального, сублингвального, внутримышечного, внутривенного, подкожного, одного или в комбинации с другим активным началом, может быть введена животным и людям в стандартной форме введения, в виде смеси с традиционными фармацевтическими носителями. Пригодные стандартные формы введения включают пероральные формы, такие как таблетки, желатиновые капсулы, пилюли, порошки, гранулы, пероральные растворы или суспензии, сублингвальные и трансбуккальные формы введения, аэрозоли, имплантаты, местные, трансдермальные, подкожные, внутримышечные, внутривенные, интраназальные формы введения.
Термин «терапевтически эффективное количество» означает количество действующего вещества, которое (1) лечит или предупреждает конкретное заболевание, состояние или расстройство, (2) ослабляет, улучшает или устраняет один или более симптомов конкретного заболевания, состояния или расстройства, или (3) предупреждает или задерживает наступление одного или более симптомов конкретного заболевания, состояния или расстройства, изложенного в данном описании. Термин «терапевтически эффективное количество» означает такое количество соединения формулы (I), которое достаточно для того, чтобы обеспечить желаемый терапевтический эффект. При этом суточная доза у взрослых обычно составляет 1~500 мг, предпочтительно - 10~300 мг. Поэтому во время приготовления из фармацевтической композиции лекарственного средства по настоящему изобретению в виде единиц дозировки необходимо учитывать вышеназванную эффективную дозировку, при этом каждая единичная дозировка препарата должна содержать 10~500 мг средства общей формулы I предпочтительно - 50~300 мг. В предпочтительном варианте, терапевтически эффективное количество составляет от 0,01 до 1 мг/кг веса тела субъекта. В соответствии с указаниями врача или фармацевта данные препараты могут приниматься несколько раз в течение определенных промежутков времени (предпочтительно - от одного до шести раз). При этом, дозировка средства, содержащего соединения общей формулы (I), у пациентов может корректироваться в зависимости от терапевтической эффективности и биодоступности активного ингредиента в организме, скорости их обмена и выведения из организма, а также в зависимости от возраста, пола и стадии заболевания пациента.
Лекарственные средства могут вводиться перорально или парентерально (например, внутривенно, подкожно, внутрибрюшинно или местно).
IC50 - концентрация полумаксимального ингибирования белка-мишени в экспериментах с флюорогенным субстратом в тестовой системе белок-субстрат-ингибитор.
Биологическая активность соединения формулы (I), заключающаяся в ингибировании главной протеазы Mpro бета-коронавируса, была предварительно выявлена при помощи метода молекулярного моделирования. На основании докинга были выявлены тиопроизводные пирролидин-2,5-дионов с фрагментом хиназолина с лучшими параметрами, которые в последующем нашли экспериментальные подтверждения их ингибирующей активности. Молекулярный докинг был реализован с использованием разработанной в МГУ им. М.В. Ломоносова программы SOL [Романов А.Н., Кондакова О.А., Григорьев Ф.В., Сулимов А.В., Лущекина С.В., Мартынов Я.Б., Сулимов В.Б. Компьютерная разработка лекарств: программа докинга SOL // Вычислительные методы и программирование, 2008, Т. 9, №2, С. 64-84; Sulimov V.B., Ilin I.S., Kutov D.C., Sulimov A.V. Development of docking programs for Lomonosov supercomputer, Journal of the Turkish Chemical Society Section A: Chemistry, 2020, V. 7, №1, p. 259-276], определяющей энергию связывания белок-лиганд, и получившей международное признание среди аналогичных программных продуктов [Alexey V. Sulimov, Danil С. Kutov, Igor V. Oferkin, Ekaterina V. Katkova, and Vladimir B. Sulimov, Application of the Docking Program SOL for CSAR Benchmark // J. Chem. Inf. Model. 2013. 53, 1946-1956]. Выявленная группа соединений затем была дополнительно проверена с помощью квантово-химического полуэмпирического метода РМ7 [Sulimov A.V., Kutov D.C., Taschilova A.S., Ilin I.S., Stolpovskaya N.V., Shikhaliev Kh S., Sulimov V.B., In search of non-covalent inhibitors of SARS-CoV-2 main protease: Computer aided drug design using docking and quantum chemistry, Supercomputing Frontiers and Innovations, 2020, V. 7, №3, p. 41-56] с континуальной моделью растворителя: дополнительная локальная оптимизация из найденного при докинге положения лиганда в белке и вычисление энтальпии связывания белок-лиганд. Для эксперимента были отобраны соединения, молекулы которых по данной мишени имели достаточно отрицательный скор докинга и достаточно отрицательную энтальпию связывания белок-лиганд. Именно среди этих соединений, отобранных на основании их высокой энергии связывания с главной протеазой коронавируса SARS-CoV-2, были обнаружены соединения, эффективно ингибирующих этот фермент.
Далее представлено более подробное описание примеров осуществления данного изобретения с достижением заявленного результата. Приведенные ниже примеры иллюстрируют, но не ограничивают данное изобретение.
Все используемые реагенты являются коммерчески доступными, контроль за ходом реакции осуществляли при помощи тонкослойной хроматографии (ТСХ), и время реакции указано только для иллюстрации; структуру и чистоту всех выделенных соединений подтверждали, по меньшей мере, одним из следующих методов: ТСХ (пластины для ТСХ с предварительно нанесенным силикагелем 60 F254 Merck), масс-спектрометрия или ядерный магнитный резонанс (ЯМР). Выход продукта приведен только для иллюстрации. Масс-спектры высокого разрешения были зарегистрированы на приборе Bruker micrOTOF II методом электрораспылительной ионизации (ESI) [1]. Измерения выполнены на положительных (напряжение на капилляре - 4500 V) или отрицательных (напряжение на капилляре 3200 V) ионах. Диапазон сканирования масс - m/z 50-3000 Д, калибровка - внешняя или внутренняя (Electrospray Calibrant Solution, Fluka). Использовался шприцевой ввод вещества для растворов в ацетонитриле, метаноле или воде, скорость потока - 3 мкл/мин. Газ-распылитель - азот (4 л/мин), температура интерфейса - 180°С. Спектры ЯМР регистрировали на приборах Bruker Advance-400 (рабочая частота 400.1 и 100.6 МГц для 1H и 13С, соответственно) и Agilent 400-MR (рабочая частота 400.0 и 100.6 МГц для 1H и 13С, соответственно), используя дейтерированный хлороформ (99,8% D) диметилсульфоксид (99,8% D) в качестве растворителя и тетраметилсилан (TMS) в качестве внутреннего стандарта. Шкала химических сдвигов приведена в миллионных долях (м.д.).
Температуры плавления определены на аппарате Stuart SMP30.
Все процедуры, если не оговорено отдельно проводили при комнатной температуре или температуре окружающей среды, т.е. в диапазоне 20-25°С.
Высушивание продуктов до постоянного веса проводили при температуре 35-45°С при атмосферном давлении или с использованием вакуум-сушильного шкафа при остаточном давлении 0,35±0,005 кг/см2 (35±5 кПа).
Для промывания осадков/фильтрата использовали дистиллированную воду, если не оговорено особо.
Схема синтеза соединений I, способы их получения, а также спектральные данные, физико-химические характеристики представлены в примерах ниже.
Целевые тиопроизводные пирролидин-2,5-дионов с фрагментом хиназолина I получают в результате взаимодействия замещенных различным образом 2-меркаптохиназолинов с N-арилмалеимидами в метаноле в присутствии триэтиламина в качестве основания (схема 1).
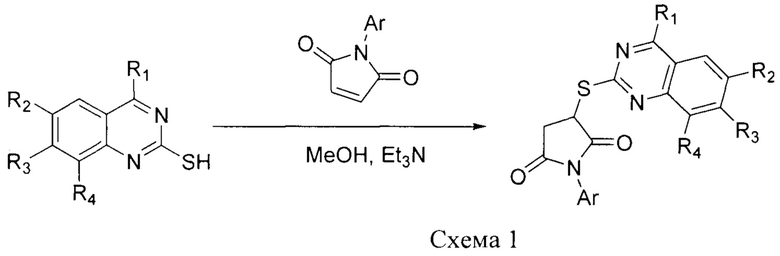
Исходные 2-меркапто-4-метилхиназолины были получены по известной методике из соответствующих 2,2,4-триметил-1,2-дидрохинолинов и роданида калия в присутствии соляной кислоты [A. Brack.  4-Mefhylen-chinazolone-(2). Justus Liebigs Annalen der Chemie. 1969, V. 730, P. 166-171].
4-Mefhylen-chinazolone-(2). Justus Liebigs Annalen der Chemie. 1969, V. 730, P. 166-171].
Исходные 2-меркапто-4-фенилхиназолины были получены по методике, аналогичной ранее описанной, из соответствующих 2-аминобензофенонов и роданида калия в уксусной кислоте [Y. Tamura, Т. Kawasaki, M. Tanio, Y. Kita. A new convenient synthesis of 2-thioxo-1,2-dihydroquinazolines. Synthesis. 1979. P. 120-121].
Для получения целевых тиопроизводных пирролидин-2,5-дионов с фрагментом хиназолина I при комнатной температуре к раствору 0.01 моль соответствующего 2-меркаптохиназолина в 20 мл абсолютного метанола прибавляют 1-3 капли триэтиламина, затем прибавляют небольшими порциями N-арилмалеимида, взятого в количестве от 0.01 до 0.011 моль. Реакционную смесь перемешивают при той же температуре в течение 1-1,5 ч, кипятят 3-4 ч, охлаждают, осадок отфильтровывают и перекристаллизовывают из метанола.
ПРИМЕР 1
Синтез 3-((6-хлор-4-фенилхиназолин-2-ил)тио)-1-(4-феноксифенил)пирролидин-2,5-диона (Ia).
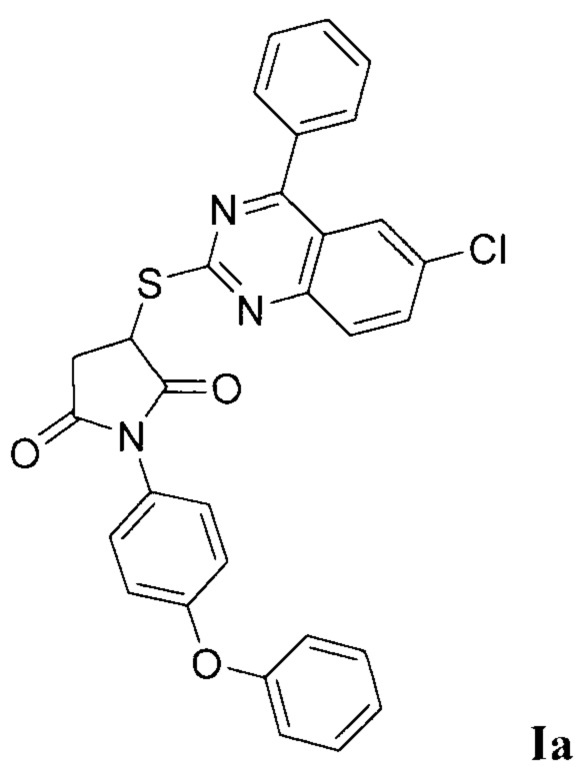
При 20°С к раствору 0,01 моль 2-меркапто-4-фенил-6-хлорхиназолина в 20 мл абсолютного метанола прибавляли каплю триэтиламина, затем прибавляли небольшими порциями 0,01 моль N-(4-феноксифенил)малеимида. Реакционную смесь перемешивали при этой же температуре в течение 1 ч, кипятили 3 ч, охлаждали, осадок отфильтровывали и перекристаллизовывали из метанола. Выход 82%. Белый кристаллический порошок, температура плавления 195°С; ЯМР 1H, δ (м.д.): 3.26 - 3.30 (м, 1H, СН2-СН), 3.43 - 3.49 (м, 1H, СН2-СН), 4.78 - 4.82 (м, 1H, СН2-СН), 6.95 - 8.05 (м, 17Н, Наром); HPLC-HRMS (ESI) вычислено для C30H20ClN3O3S+Н+, 538.0988; найдено, 538.0995.
ПРИМЕР 2
Синтез 3-((6-хлор-4-фенилхиназолин-2-ил)тио)-1-(4-этоксифенил)пирролидин-2,5-диона (Ib).
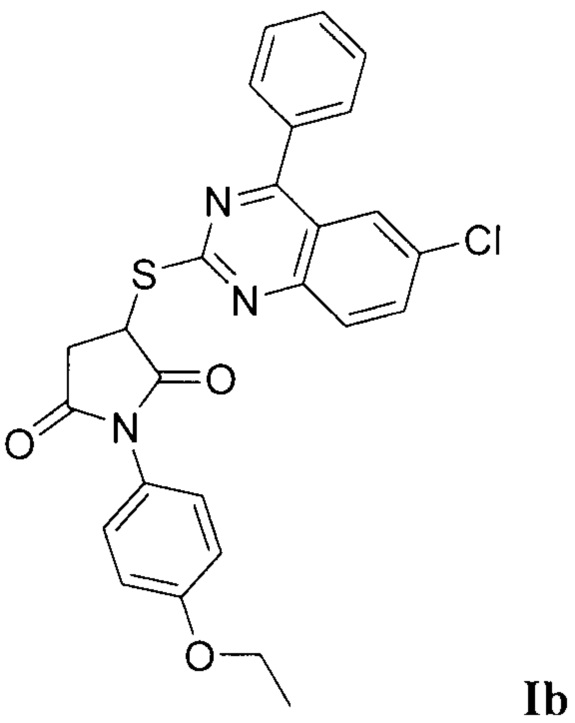
Синтез проводили аналогично примеру 1, при этом в качестве исходных реагентов использовали 2-меркапто-4-фенил-6-хлорхиназолин и N-(4-этоксифенил)малеимид. Выход 79%. Белый кристаллический порошок, температура плавления 183°С; ЯМР 1H, δ (м.д.): 1,11 (т, 3Н, J=8.0 Гц, СН3), 3.24 - 3.28 (м, 1H, СН2-СН), 3.45 - 3.51 (м, 1H, СН2-СН), 4.01 (к, 2Н, J=8.0 Гц, СН3СН2), 4.80 - 4.84 (м, 1H, СН2-СН), 6.88 - 8.00 (м, 12Н, Наром); HPLC-HRMS (ESI) вычислено для C26H20ClN3O3S+H+, 490.0988; найдено, 490.0994.
ПРИМЕР 3
Синтез 3-((6-хлор-4-фенилхиназолин-2-ил)тио)-1-(нафталин-1-ил)пирролидин-2,5-диона (Ic).
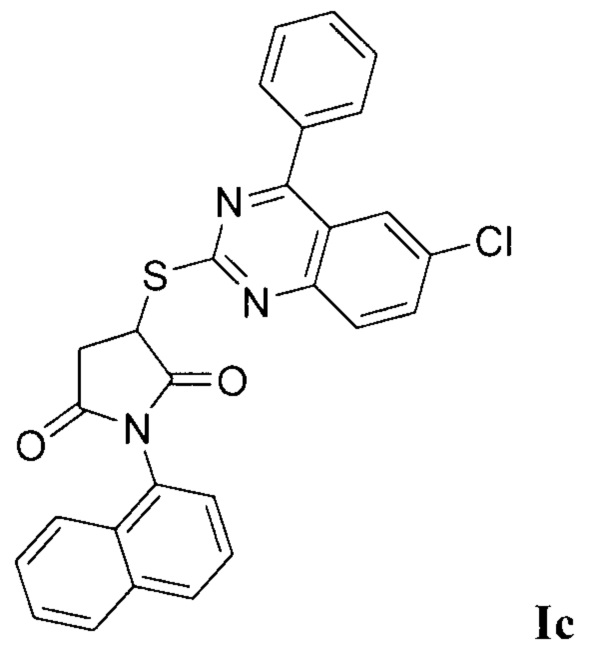
Синтез проводили аналогично примеру 1, при этом в качестве исходных реагентов использовали 2-меркапто-4-фенил-6-хлорхиназолин и N-(нафталин-1-ил)малеимид. Выход 79%. Белый кристаллический порошок, температура плавления 199°С; ЯМР 1H, δ (м.д.): 3.22 - 3.28 (м, 1H, СН2-СН), 3.44 - 3.50 (м, 1H, СН2-СН), 4.81 - 4.83 (м, 1Н, СН2-СН), 6.91 - 7.98 (м, 15Н, Наром); HPLC-HRMS (ESI) вычислено для C28H18ClN3O2S+H+, 496.0882; найдено, 496.0887.
ПРИМЕР 4
Синтез 3-((6-хлор-4-фенилхиназолин-2-ил)тио)-1-(4-фторфенил)пирролидин-2,5-диона (Id).
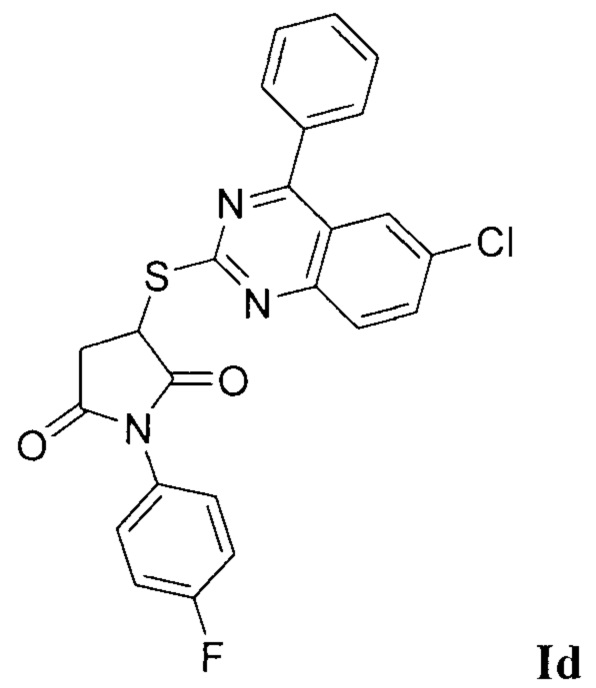
Синтез проводили аналогично примеру 1, при этом в качестве исходных реагентов использовали 2-меркапто-4-фенил-6-хлорхиназолин и N-(4-фторфенил)малеимид. Выход 79%. Белый кристаллический порошок, температура плавления 186°С; ЯМР 1H, δ (м.д.): 3.23 - 3.29 (м, 1Н, СН2-СН), 3.44 - 3.49 (м, 1H, СН2-СН), 4.80 - 4.82 (м, 1Н, СН2-СН), 6.95 - 7.91 (м, 12Н, Наром); HPLC-HRMS (ESI) вычислено для C24H15ClFN3O2S+H+, 464.0631; найдено, 464.0638.
ПРИМЕР 5
Синтез 3-((4,7-диметилхиназолин-2-ил)тио)-1-(4-метоксифенил)пирролидин-2,5-диона (Ie).
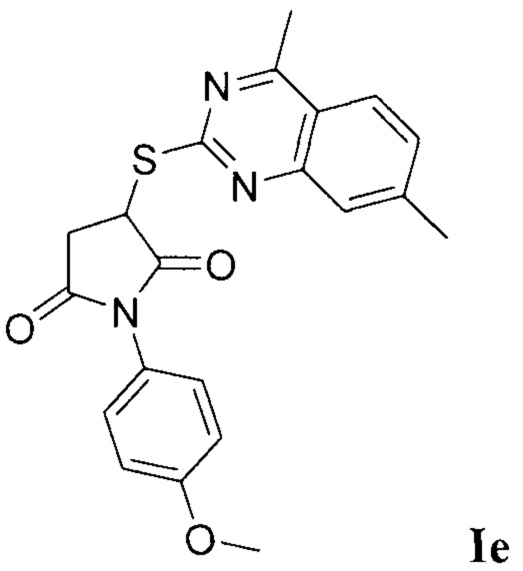
Синтез проводили аналогично примеру 1, при этом в качестве исходных реагентов использовали 2-меркапто-4,7-диметилхиназолин и N-(4-метоксифенил)малеимид. Выход 75%. Белый кристаллический порошок, температура плавления 198°С; ЯМР 1H, δ (м.д.): 2.37, 2.39 (оба с, 3Н, 6,7-Ме2), 2,80 (3Н, с, 4-Ме), 3.21 - 3.27 (м, 1Н, СН2-СН), 3.45 - 3.49 (м, 1Н, СН2-СН), 3.95 (3Н, с, МеО), 4.80 - 4.83 (м, 1H, СН2-СН), 7.01 - 7.44 (м, 7Н, Наром); HPLC-HRMS (ESI) вычислено для C21H19N3O3S+H+, 394.1221; найдено, 394.1222.
ПРИМЕР 6
Синтез 3-((4-метил-6-метоксихиназолин-2-ил)тио)-1-(3,4-диметилфенил)пирролидин-2,5-диона (If).
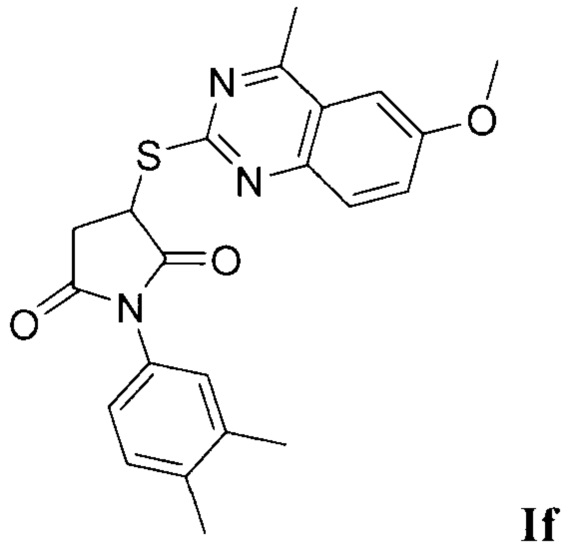
Синтез проводили аналогично примеру 1, при этом в качестве исходных реагентов использовали 2-меркапто-4-метил-6-метоксихиназолин и N-(3,4-диметилфенил)малеимид. Выход 88%. Белый кристаллический порошок, температура плавления 202°С; ЯМР 1H, δ (м.д.): 2.35, 2.42 (оба с, 3Н, 3,4-Ме2С6Н3), 2,81 (3Н, с, 4-Ме), 3.22 - 3.28 (м, 1Н, СН2-СН), 3.43 - 3.49 (м, 1Н, СН2-СН), 3.89 (3Н, с, МеО), 4.81 - 4.83 (м, 1Н, СН2-СН), 7.08 - 7.48 (м, 6Н, Наром); HPLC-HRMS (ESI) вычислено для C22H21N3O3S+H+, 410.1534; найдено, 410.1541.
ПРИМЕР 7
Синтез 3-((4-фенил-6-хлорхиназолин-2-ил)тио)-1-(4-этилфенил)пирролидин-2,5-диона (Ig).
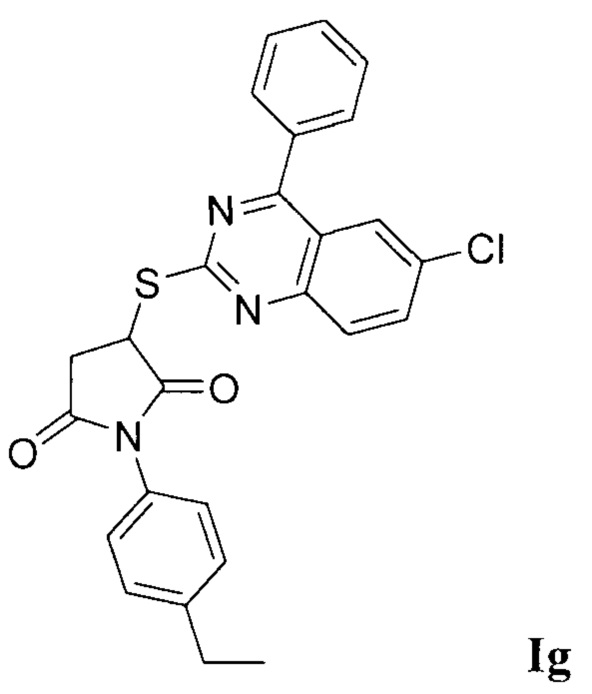
Синтез проводили аналогично примеру 1, при этом в качестве исходных реагентов использовали 2-меркапто-4-фенил-6-хлорхиназолин и N-(4-этилфенил)малеимид. Выход 81%. Белый кристаллический порошок, температура плавления 173°С; ЯМР 1H, δ (м.д.): 1,23 (т, 3Н, J=7.9 Гц, Me), 2.38 (к, 2Н, J=7.9 Гц, СН2Ме), 3.21 - 3.25 (м, 1Н, СН2-СН), 3.43 - 3.50 (м, 1Н, СН2-СН), 4.81 - 4.83 (м, 1Н, СН2-СН), 7.06 - 7.85 (м, 12Н, Наром); HPLC-HRMS (ESI) вычислено для C26H20ClN3O2S+H+, 474.1039; найдено, 474.1046.
ПРИМЕР 8
Синтез 3-((4,7-диметилхиназолин-2-ил)тио)-1-(4-метил-3-хлорфенил)пирролидин-2,5-диона (Ih).
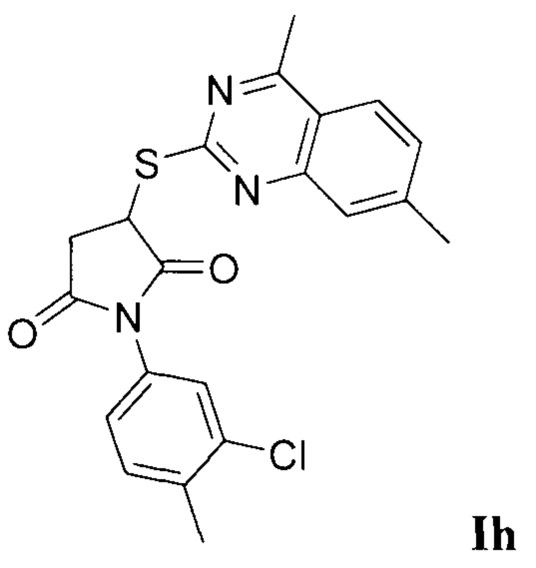
Синтез проводили аналогично примеру 1, при этом в качестве исходных реагентов использовали 2-меркапто-4,7-диметил-6-хиназолин и N-(4-метил-3-хлорфенил)малеимид. Выход 81%. Белый кристаллический порошок, температура плавления 173°С; ЯМР 1H, δ (м.д.): 2.36, 2.38 (оба с, 3Н, 6,7-Ме2), 2,41 (3Н, с, 4-Ме-3-ClC6H4), 2,81 (3Н, с, 4-Ме), 3.22 - 3.26 (м, 1H, СН2-СН), 3.44-3.49 (м, 1Н, СН2-СН), 4.81 - 4.83 (м, 1H, СН2-СН), 7.11 - 7.52 (м, 6Н, Наром); HPLC-HRMS (ESI) вычислено для C21H18ClN3O2S+H+, 412.0882; найдено, 412.0890.
Также были синтезированы соединения и с другими вариантами радикалов, приведенных в общей формуле I, которые продемонстрировали схожую активность в ингибировании главной протеазы MPR0 бета-коронавирусов, включая SARS-Cov-2.
ПРИМЕР 9
Исследование ингибирующей активности синтезированных веществ в отношении главной протеазы Mpro коронавируса SARS-CoV-2
Последовательность кодирующую главную протеазу SARS-CoV-2 (Mpro or 3CL) изолята Wuhan-Hu-1 (GenBank:MN908947), синтезировали на заказ (ООО ДНК-синтез, Россия). Перед заказом проводили оптимизацию кодонного состава последовательности с помощью инструмента GeneOptimizer для оптимального синтеза протеазы в клетках Е. coli. Чтобы избежать аккумуляцию целевого белка в виде плохо растворимых телец включения и обеспечить транспорт Mpro в периплазматическое пространство было проведено клонирование генов GST (глутатион-S-трансфераза) и Mpro в единой рамки считывания для получения слитого белка GST-Mpro. Для этого были рассчитаны олигонуклеотидные праймеры GST-F 5'-aaaaaacatatgtcccctatactaggttatt-3' и GST3CL-R 5'-aaaaaaggatccttttggaggatggtcgccac-3' (умножение копий GST в ПЦР) и 3CLGST-F 5'-aaaaaaggatccacctcagctgttttgcagagcggttttcgtaaaatggcat-3' и 3CL-R 5'-aaaaaagcggccgcttaaccgctaccaccgctctgaaaggtaacaccgctacactg-3' (умножение копий 3CL в ПЦР). Для обеспечения получения активной формы протеазы в последовательности фланкирующие Mpro были заложены гомологичные сайты протеолиза SAVLQSGFR на N-конце и TFQSG на С-конце, которые впоследствии помогают вырезать Mpro из синтезированного слитого белка. После умножения количества копий молекул ДНК два ПЦР продукта были одновременно перенесены в составе вектора рЕТ21. Полученной плазмидой pET21-GST-3CL трансформировали клетки Е. coli BL21(DE3). Индивидуальные колонии Е. coli, содержащие рекомбинантные плазмиды, культивировали в течение ночи на орбитальном шейкере («Biosan», Латвия) в среде LB («AppliChem», США), содержащей 100 мкг/мл ампициллина (для селекции клеток, которые получили плазмиду), при 37°С и 180 об./мин. После культивации раствор с трансформированными бактериями в соотношении 1/100 переносили в колбу Эрленмейера, содержащую среду LB, и растили до поглощения 0,8 (при λ=600 нм). Добавляли индуктор изопропил-β-D-1-тиогалактопиранозид (ИПТГ) («Anatrace Products», США) до конечной концентрации 1 мМ для запуска синтеза белка. Культуру дополнительно культивировали на шейкере в течение 5 ч при 37°С и 180 об./мин. Биомассу осаждали центрифугированием («Beckman Coulter», США) в течении 20 мин при 5000 g и 4°С.Полученный осадок растворяли в буфере: 12 мМ Tris; 120 мМ NaCl; 0,1 мМ EDTA; 1 мМ DTT. Клетки разрушали с использованием ультразвукового гомогенизатора Soniprep 150 Plus («MSE», КНР). Очистку проводили последовательной хроматографией с промежуточным диализом в 20 мМ Трис-HCl, рН 7,6 на колонках с катионообменными сорбентами (SP-сефароза и Nuvia HR-S), уравновешенными 20 мМ Трис-HCl, рН 7,6. Целевую фракцию элюировали в линейном градиенте концентрации NaCl от 0 до 1 M в 20 мМ Трис-HCl, рН 7,6 и анализировали при помощи электрофореза в денатурирующих условиях в 15% ПААГ. Конечный препарат диализовали против 20 мМ Трис-HCl, рН 7,6 и подвергали стерилизующей фильтрации через фильтры с размером пор 0,22 мкМ.
Анализ ингибиторов проводили с использованием синтетического флуоресцентно меченого пептидного субстрата, включающего сайт протеолиза основной протеазы коронавируса состава Dabcyl-VNSTLQSGLRK(FAM)MA (чистота более 95%, СРС Scientific Inc, Китай). Интенсивность флуоресценции контролировали с помощью прибора CLARIOstar Plus (BMG Labtech, ФРГ), используя длины волн - 495 и - 520 нм для возбуждения и излучения соответственно. При взаимодействии фермента с пептидным субстратом происходит расщепление сайта протеолиза основной протеазы коронавируса, что приводит к увеличению интенсивности флуоресценции из-за физического удаления флуорофора от тушителя. При добавлении в реакционную смесь тестируемых соединений наблюдается снижения уровня свечения. Реакционные смеси готовили в 384 луночном планшете, после чего инкубировали при комнатной температуре в течение 5 мин. Все измерения проводили при 25°С. Реакционные смеси содержали 5 мкл Трис-HCl буфера (рН 8,0; 50 мМ Трис; 50 мМ NaCl), 2 мкл субстрата (С=33 мкг/мл) и ингибитор различной концентрации (0,000058594-0,03 мг/мл). Реакцию запускали добавлением 3 мкл Mpro (С=0,025 мг/мл). За величину IC50 принимают такую концентрацию тестируемого вещества, которая снижает уровень флуоресценции на 50% от максимального, наблюдаемого без добавления ингибитора. В качестве стандартных, (реперных) соединений были использованы два известных лекарственных соединения дисульфирам и эбселен.
В таблице 1 приведены результаты определения активности синтезированных соединений как ингибиторов главной протеазы коронавируса SARS-CoV-2
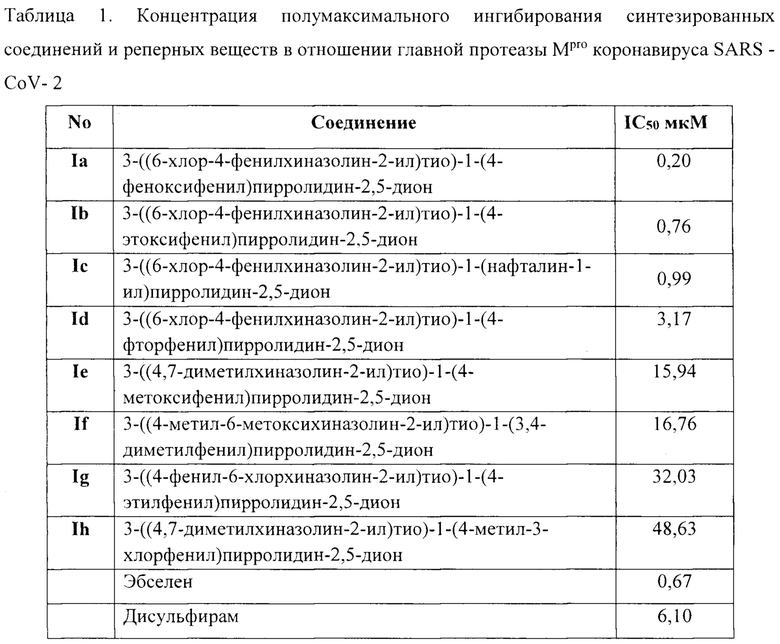
Данные, приведенные в таблице 1, показывают, что, в целом, большинство исследованных (6-хлор-4-фенилхиназолин-2-ил)тиопроизводных пирролидин-2,5-дионов по ингибирующей активности в отношении главной протеазы Mpro коронавируса SARS-CoV-2 превосходят или сравнимы с известными лекарственными препаратами эбселеном и дисульфирамом. Все указанные соединения общей формулы I сохраняют стабильность в течение длительного времени (1 года) на воздухе при комнатной температуре. Анализ стабильности осуществляли на основе данных хроматографических и спектральных методов анализа.
ПРИМЕР 10
Для получения лекарственного средства в форме таблеток смешивают 1600 мг крахмала, 1600 мг измельченной лактозы, 400 мг талька и 1000 мг соединения Id, спрессовывают в брусок. Полученный брусок измельчают в гранулы и просеивают через сита, собирая гранулы размером 14-16 меш. Полученные гранулы таблетируют в подходящую форму таблетки весом 560 мг.
ПРИМЕР 11
Для получения лекарственного средства в форме капсул тщательно смешивают соединение Id с порошком лактозы в соотношении 2:1. Полученную порошкообразную смесь упаковывают по 250 мг в желатиновые капсулы подходящего размера.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРИМЕНЕНИЕ КИСЛОРОДСОДЕРЖАЩЕГО ПРОИЗВОДНОГО 6-ГАЛОГЕНХИНОЛИНА ДЛЯ ИНГИБИРОВАНИЯ РЕПЛИКАЦИИ БЕТА-КОРОНАВИРУСОВ, ВКЛЮЧАЯ SARS-COV-2, И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2021 |
|
RU2780245C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ВКЛЮЧАЮЩАЯ ПРОИЗВОДНОЕ 1,3,5-ТРИАЗИН-2,4-ДИАМИНА, ДЛЯ ИНГИБИРОВАНИЯ РЕПЛИКАЦИИ БЕТА-КОРОНАВИРУСОВ, ВКЛЮЧАЯ SARS-COV-2, И СПОСОБ ЕЕ ПРИМЕНЕНИЯ | 2021 |
|
RU2827891C1 |
| ПРИМЕНЕНИЕ ПРОИЗВОДНОГО 1,3,5-ТРИАЗИН-2,4-ДИАМИНА ДЛЯ ИНГИБИРОВАНИЯ РЕПЛИКАЦИИ БЕТА-КОРОНАВИРУСОВ, ВКЛЮЧАЯ SARS-COV-2 | 2021 |
|
RU2780249C1 |
| СПОСОБ ПОЛУЧЕНИЯ КИСЛОРОДСОДЕРЖАЩЕГО ПРОИЗВОДНОГО 6-ГАЛОГЕНХИНОЛИНА ДЛЯ ИНГИБИРОВАНИЯ РЕПЛИКАЦИИ БЕТА-КОРОНАВИРУСОВ, ВКЛЮЧАЯ SARS-COV-2 | 2021 |
|
RU2827892C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ВКЛЮЧАЮЩАЯ КИСЛОРОДСОДЕРЖАЩЕЕ ПРОИЗВОДНОЕ 6-ГАЛОГЕНХИНОЛИНА, ДЛЯ ИНГИБИРОВАНИЯ РЕПЛИКАЦИИ БЕТА-КОРОНАВИРУСОВ, ВКЛЮЧАЯ SARS-COV-2, И СПОСОБ ЕЕ ПРИМЕНЕНИЯ | 2021 |
|
RU2827893C1 |
| ПРИМЕНЕНИЕ ТРИЦИКЛИЧЕСКОГО СЕРУСОДЕРЖАЩЕГО ПРОИЗВОДНОГО 1,2-ДИГИДРОХИНОЛИНА ДЛЯ ИНГИБИРОВАНИЯ РЕПЛИКАЦИИ БЕТА-КОРОНАВИРУСОВ, ВКЛЮЧАЯ SARS-CoV-2 | 2021 |
|
RU2780247C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ВКЛЮЧАЮЩАЯ ТРИЦИКЛИЧЕСКОЕ СЕРУСОДЕРЖАЩЕЕ ПРОИЗВОДНОЕ 1,2-ДИГИДРОХИНОЛИНА ДЛЯ ИНГИБИРОВАНИЯ РЕПЛИКАЦИИ БЕТА-КОРОНАВИРУСОВ, ВКЛЮЧАЯ SARS-COV-2, И СПОСОБ ЕЕ ПРИМЕНЕНИЯ | 2021 |
|
RU2814434C1 |
| СПОСОБ ПОЛУЧЕНИЯ ТРИЦИКЛИЧЕСКОГО СЕРУСОДЕРЖАЩЕГО ПРОИЗВОДНОГО 1,2-ДИГИДРОХИНОЛИНА ДЛЯ ИНГИБИРОВАНИЯ РЕПЛИКАЦИИ БЕТА-КОРОНАВИРУСОВ, ВКЛЮЧАЯ SARS-COV-2 | 2021 |
|
RU2819783C1 |
| Средство для ингибирования штаммов вируса SARS-CoV-2 на основе (+)-усниновой кислоты | 2023 |
|
RU2832905C1 |
| ЛИПОСОМАЛЬНАЯ КОМПОЗИЦИЯ 5-ХЛОРПИРИДИН-3-ИЛ-1Н-ИНДОЛ-4-КАРБОКСИЛАТА КАК ПОТЕНЦИАЛЬНОЕ СРЕДСТВО ЭКСТРЕННОЙ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ КОРОНАВИРУСНЫХ ИНФЕКЦИЙ | 2023 |
|
RU2810261C1 |
Изобретение относится к области органической химии, а именно к способу получения тиопроизводных пирролидин-2,5-дионов с фрагментом хиназолина общей формулы (I), проявляющих противовирусную ингибирующую активность в отношении главной протеазы Мрrо бета-коронавируса SARS-CoV-2. В общей формуле I R1 - фенил; R2, R3, R4 представляют собой заместитель, выбранный из водорода, алкила С1-С2, алкоксила С1-С2, хлора; R5 является нафтилом или фенилом, необязательно замещенным один или два раза С1-С2 алкилом, галогеном, метокси-, этокси-. Способ заключается в том, что к раствору, содержащему 0.01 моль соответствующего 2-меркаптохиназолина и 20 мл абсолютного метанола, сначала прибавляют 1-3 капли триэтиламина, затем прибавляют небольшими порциями от 0.01 до 0.011 моль N-арилмалеимида, полученную реакционную смесь перемешивают в течение 1 ч, кипятят 3-4 ч, охлаждают, осадок отфильтровывают и перекристаллизовывают из метанола. Изобретение позволяет получать тиопроизводные пирролидин-2,5-дионов с фрагментом хиназолина с высокими выходами (до 88%) при простой процедуре их выделения из реакционной массы посредством простого фильтрования без применения более трудоемких хроматографических методов. 1 табл., 11 пр.
Способ получения тиопроизводных пирролидин-2,5-дионов с фрагментом хиназолина общей формулы I:
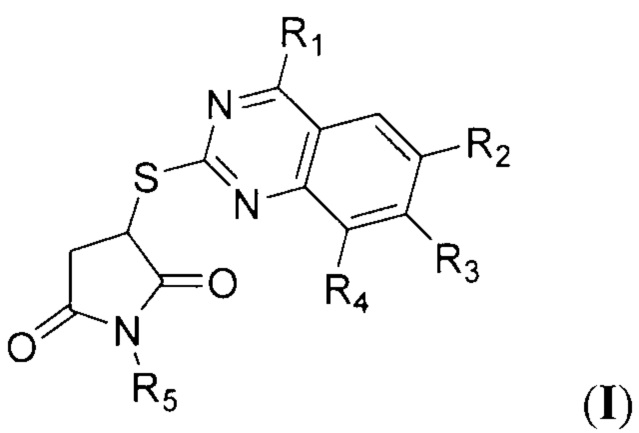
где R1 - фенил; R2, R3, R4 представляют собой заместитель, выбранный из водорода, алкила С1-С2, алкоксила С1-С2, хлора; R5 является нафтилом или фенилом, необязательно замещенным один или два раза С1-С2 алкилом, галогеном, метокси-, этокси-,
характеризующийся тем, что к раствору, содержащему 0.01 моль соответствующего 2-меркаптохиназолина и 20 мл абсолютного метанола, сначала прибавляют 1-3 капли триэтиламина, затем прибавляют небольшими порциями от 0.01 до 0.011 моль N-арилмалеимида, полученную реакционную смесь перемешивают в течение 1 ч, кипятят 3-4 ч, охлаждают, осадок отфильтровывают и перекристаллизовывают из метанола.
| KH | |||
| S | |||
| SHIKHALIEV et al | |||
| Приспособление для точного наложения листов бумаги при снятии оттисков | 1922 |
|
SU6A1 |
| Russian Journal Of General Chemistry, 2004, Vol | |||
| Приспособление в центрифугах для регулирования количества жидкости или газа, оставляемых в обрабатываемом в формах материале, в особенности при пробеливании рафинада | 0 |
|
SU74A1 |
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
| SHARMA, ANUJ et al | |||
| Thia-Michael addition: An emerging strategy in organic synthesis | |||
| Asian Journal of Organic Chemistry, 2018, vol | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| KUMAR, VARUN | |||
Авторы
Даты
2023-11-09—Публикация
2021-04-30—Подача