Ссылка на родственные заявки
[0001] Согласно настоящей заявке испрашивается приоритет по заявке с серийным номером 62/689419, поданной 25 июня 2018 года, раскрытие которой включено в данный документ посредством ссылки.
Предшествующий уровень техники настоящего изобретения
[0002] В данном документе раскрыт способ применения одной суспензии как для идентификации микроорганизмов в биологическом образце (например, крови), так и для определения их чувствительности к противомикробным средствам.
[0003] В рамках установившейся практики в медицинской диагностике биологические образцы, такие как кровь, забирают у пациентов и анализируют. В зависимости от показаний образцы можно анализировать для определения того, присутствуют ли микроорганизмы в образце, например, с помощью посева крови (как например, с помощью серий ВАСТЕС™ FX и ВАСТЕС™ 9000 от Becton, Dickinson and Company) или с помощью посева штрихом на агаровую плашку (вручную или с помощью автоматического инструмента, такого как Innova™ или Inoqula, которые реализует Becton, Dickinson and Company). Если определено присутствие микроорганизмов, существует как медицинская, так и экономическая обоснованность и для идентификации конкретного присутствующего микроорганизма, и для определения устойчивости/чувствительности микроорганизма к антибиотикам с целью облегчения лечения.
[0004] Многие виды микроорганизмов (которые также будут называться в данном документе микробами), в особенности, бактерии и одноклеточные грибки, можно идентифицировать с помощью масс-спектрометрических («масс-спектр.») способов, таких как матрично-активированная лазерная десорбция/ионизация («MALDI»). В процессе MALDI небольшие количества микробов из колонии, культивируемой обычным образом в питательной среде, переносят на подложку планшета для масс-спектрометрического анализа образца, известного как планшет для MALDI, а затем сразу подвергают масс-спектрометрическому анализу, обычно, с помощью время-пролетного (TOF) MALDI. Масс-спектрометрический анализ показывает разные белки при условии, что они присутствуют в микробах в достаточной концентрации. Идентификационную информацию для микроба затем определяют на основании профиля белков у микроба посредством компьютерного поиска в спектральных библиотеках, содержащих тысячи эталонных спектров. Если в библиотеке для точного определения вида оцениваемого микроба отсутствует эталонный масс-спектр, компьютерный поиск в библиотеке с менее строгими требованиями к поиску может обеспечивать по меньшей мере некоторые данные о порядке, семействе или роде микробов, поскольку родственные микробы часто содержат ряд идентичных типов белков. Способ MALDI описан более подробно в публикации международной заявки WO-2009/065580 A1 за авторством Ulrich Weller, озаглавленной «Идентификация патогенов в биологических жидкостях», содержание которой включено в данный документ во всей своей полноте. Для идентификации можно применять разнообразные масс-спектрометрические инструменты.
[0005] Желательным является анализ эффективности противомикробного средства в подавлении роста микробных изолятов из клинических образцов. Такой анализ известен как исследование чувствительности к противомикробным средствам («AST»). Методика AST из уровня техники представляет собой методику разведения, которая включает воздействие на бактерии снижающимися концентрациями противомикробных средств в жидкой среде с серийным двукратным разведением. Самую низкую концентрацию противомикробного средства, при которой отсутствует видимый рост бактерий, определяют как минимальную ингибирующую концентрацию («MIC»). MIC представляет собой стандартную меру чувствительности к противомикробным средствам. В уровне техники известны инструменты для AST, такие как система BD Phoenix™, реализуемая Becton, Dickinson and Company, которая осуществляет и идентификацию, и AST.
[0006] Аппарат, который известен в уровне техники и может готовить образцы для таких процессов AST, представляет собой BD Phoenix™ АР, доступный от Becton, Dickinson and Company. Рабочий процесс, как правило, включает в себя приготовление инокулята, как например, посредством мечения соответствующей пробирки, выбора микробных колоний и получения концентрированной суспензии в пробирках с бульоном для ID и помещения пробирок в один или несколько штативов, удерживающих пробирки с бульоном для AST. Рабочий процесс затем включает осуществление автоматизированной нефелометрии для доведения пробирки для ID до 0,5 или 0,25 единицы МакФарланда («McF»), добавление индикатора для AST в бульон для AST, перенос части образца в бульон для AST и смешивание обеих пробирок. Рабочий процесс затем включает удаление медицинским работником обработанных пробирок для ID и AST и помещение их на инокуляционную станцию, имеющую панели для ID/AST, такие как панели Phoenix, и инокуляцию образцов в панелях. См. также публикацию заявки на патент США №2008/0072664 А1, содержание которой включено в данный документ во всей своей полноте.
[0007] Панели затем поддерживаются в системе для ID/AST (например, в инструменте Phoenix), имеющем контролируемую среду (например, контролируемую температуру, влажность, количество освещения и т.д.), в течение предварительно определенного периода времени с целью стимуляции микробного роста в присутствии противомикробного средства. Система, как правило, обладает способностью к анализу для того, чтобы измерять микробный рост в одной или нескольких микролунках без нарушения поддержания контролируемой среды. Система также может обладать способностью к выдаче результатов анализа на дополнительные устройства для дальнейшей обработки. Такая система может обладать способностью как к ID, так и к AST или способностью только к ID или только к AST. Более того, даже система для ID/AST может работать только для результатов ID или только для результатов AST. Панели см., например, в патентах США №№5922593, 6096272, 6372485, 7115384 и 6849422, содержание которых включено в данный документ посредством ссылки в своей полноте.
[0008] Различные лабораторные аппараты могут иметь сообщение с системой управления данными, такими как BD Epicenter™, для того, чтобы обеспечить единое место для отслеживания лабораторным работником состояния и результатов от различных лабораторных аппаратов. Своевременное отслеживание, анализ и обмен микробиологическими данными может оказывать непосредственное воздействие на уход за пациентом. Тем не менее, получение, организация и обмен информацией от различных лабораторных аппаратов являются трудоемкими. Современные информационные системы могут делать сложными даже стандартную идентификацию и исследование AST. Микробиологам, работникам, ответственным за санитарно-эпидемиологическое состояние, врачам и фармацевтам необходим немедленный доступ к сосредоточенной информации о пациенте для быстрой идентификации и реакции на возникающие явления устойчивости или HAI (внутрибольничные инфекции).
[0009] Способы и аппарат, в котором общую суспензию образца получают как для MALDI, так и для AST, описаны в патенте США №9180448, опубликованном 10 ноября 2015 года, по заявке, поданной 6 июля 2011 года и озаглавленной «Способ и аппарат для идентификации бактерий», который выдан Becton, Dickinson and Company. Другие системы, которые получают образец и образуют суспензию из образца как для MALDI, так и для AST, описаны в патенте США №9556495, опубликованном 31 января 2017 года, по заявке на патент США с серийным номером 14/388430, поданной 2 апреля 2013 года, права по которому переуступлены BD Kiestra B.V., и который озаглавлен «Автоматизированный отбор микроорганизмов и идентификация с применением MALDI». Еще одна система описана в заявке на патент США US2016/034554, которая была подана 27 мая 2016 года и права по которой переуступлены BD Kiestra B.V. Все из публикаций патента №9180448, патента №9556495 и патентной заявки US 2016/034554 включены посредством ссылки.
Краткое раскрытие настоящего изобретения
[0010] В соответствии с одним вариантом осуществления настоящее изобретение, описанное в данном документе, относится к автоматизированному способу, в котором общую суспензию образца используют в качестве источника образца как для системы, которая идентифицирует микроорганизмы, присутствие которых определено в образце, так и для системы, которая исследует микроорганизмы в отношении их устойчивости/чувствительности к противомикробным средствам. Система имеет первую станцию, которая готовит общую суспензию как для масс-спектрометрического процесса (например, MALDI) для идентификации микроорганизма, так и для исследования чувствительности к противомикробным средствам (AST).
[0011] В соответствии со способом образец инокулируют в разбавитель. В соответствии с одним вариантом осуществления образец собирают с плашки с культурой. Сбор образца с плашки с культурой является известным специалистам в данной области техники и не описывается подробно в данном документе. Сбор образца с плашки с культурой и внесение образца в разбавитель описаны в международной заявке WO/2016/034554.
[0012] Забранный образец вносят в разбавитель для образца. Такие разбавители являются хорошо известными и не описываются подробно в данном документе. Такие разбавители описаны в международной заявке WO/2016/034554.
[0013] Затем измеряют мутность образца. Нефелометр применяют для получения измеренных значений мутности. Измерение мутности с применением нефелометра описано в международной заявке WO/2016/034554. Если измеренная мутность находится в пределах предварительно определенного диапазона, то первую аликвоту суспензии применяют для MALDI, а вторую аликвоту суспензии доставляют в пробирку с бульоном для исследования чувствительности к антибиотикам (AST). Объем суспензии, применяемый для AST, рассчитывают на основании мутности суспензии, поскольку для AST требуется, чтобы определенное количество КОЕ (колониеобразующих единиц) образца было доставлено в пробирку с бульоном для AST, объем рассчитывают, исходя из мутности суспензии и целевого количества инокулированного образца. Предварительно определенный диапазон мутности является необходимым вследствие ограничений, накладываемых автоматическим пипетирующим аппаратом. Бульон, применяемый в качестве питательной среды или среды культивирования для обеспечения возможности роста микроорганизмов при AST, является хорошо известным специалисту в данной области техники и не описывается подробно в данном документе. При AST отсутствие микробного роста указывает на то, что исследуемый микроорганизм является чувствительным к антибиотику, доставляемому в комбинации с суспензией образца. Бульон для AST также называется в данном документе средой культивирования.
[0014] Количество суспензии, которое применяют для инокуляции планшетов для идентификации (например, планшетов для MALDI) или пробирок с бульоном для исследования чувствительности к антибиотикам (AST), основывается на количестве образца, содержащемся на единицу объема суспензии. После образования суспензии, если концентрация образца в суспензии (т.е. мутность образца) является слишком высокой, то объем суспензии, требующийся для инокуляции этого количества образца на планшет для MALDI или в пробирки с бульоном для AST, может быть достаточно небольшим. Небольшие объемы сложно точно дозировать пипеткой. Напротив, больший объем очень «разбавленной» суспензии требуется для инокуляции планшета для MALDI или пробирки с бульоном целевым количеством образца. Тем не менее, объем, который может быть перенесен с применением общепринятых устройств для пипетирования, ограничен.
[0015] Следовательно, если количество образца, доставляемого в суспензию, является таким, что концентрация образца в суспензии (которую измеряют на основании мутности суспензии) является более высокой, чем предварительно определенный диапазон (например, от приблизительно 0,2 единицы МакФарланда до приблизительно 2 единиц МакФарланда), то суспензию подвергают протоколу разведения для снижения мутности таким образом, чтобы мутность суспензии находилась в пределах предварительно определенного диапазона. Если количество образца, доставляемого в суспензию, является таким, что мутность суспензии находится ниже предварительно определенного диапазона, то суспензию подвергают протоколу концентрирования. В соответствии с одним вариантом осуществления протокол концентрирования предусматривает получение дополнительного образца для повышения концентрации образца в суспензии. Тем не менее, если дополнительный образец не доступен, то протокол концентрирования предусматривает слив суспензии.
[0016] Приготовление суспензии и инокуляция планшета для MALDI такой приготовленной суспензией описаны в международной заявке WO/2016/034554, которая включена в данный документ посредством ссылки. Процесс MALDI происходит на второй станции, a AST происходит на третьей станции.
[0017] После того как аликвота суспензиии была удалена для MALDI, система определяет, сколько суспензии следует применять для инокуляции панели для AST. Величину объема суспензии определяют на основании общего количества образца, которое согласно предварительно определенным требованиям нужно ввести в пробирку с бульоном для AST. Исходя из известной мутности суспензии и целевого количества образца для инокуляции панели, система рассчитывает объем суспензии, требующийся для инокуляции пробирки с бульоном для AST. Система затем получает определенный объем суспензии и инокулирует панель этим объемом. Система и способ в данном документе не требуют, чтобы мутность суспензии доводили до стандартизированного значения в единицах МакФарланда для AST после того, как аликвоту образца для MALDI удалили из пробирки с суспензией, что делает способ и систему более эффективными и менее насыщенными оборудованием, чем системы и способы, которые требуют стандартизации мутности суспензии до целевого значения в единицах МакФарланда перед инокуляцией пробирки с бульоном для AST с применением суспензии.
[0018] Система имеет пользовательский интерфейс и программное обеспечение, в котором образцы отслеживаются таким образом, что результаты исследования с второй и третьей станций связаны с образцом и пациентом, от которого был получен образец. Система также включает в себя станцию для определения того, присутствуют ли микроорганизмы в образце, и только те образцы, в которых определено присутствие образцов, подвергают дальнейшей обработке и исследованию.
Краткое описание чертежей
[0019] На фиг. 1 представлена блок-схема, которая описывает способ применения суспензии, который не требует стандартизации мутности перед инокуляцией пробирки с бульоном для AST.
[0020] На фиг. 2 представлена блок-схема, которая описывает способ применения суспензии, который не требует стандартизации мутности перед инокуляцией пробирки с бульоном для AST, а обеспечивает протокол разведения для приготовления суспензии образца, когда исходная суспензия является слишком концентрированной.
[0021] На фиг. 3 представлена блок-схема, которая описывает способ применения суспензии, который не требует стандартизации мутности перед инокуляцией пробирки с бульоном для AST, а обеспечивает протокол разведения для приготовления суспензии образца в соответствии с другим вариантом осуществления настоящего изобретения, который разделен на фиг. 3А и фиг. 3В. На фиг. 3А проиллюстрирована первая часть способа, и на фиг. 3В описана вторая часть способа.
[0022] На фиг. 4 проиллюстрирована концентрация Е. coli в пробирке с бульоном для AST в сравнении с окончательной мутностью суспензии при применении способа, проиллюстрированного на фиг. 2.
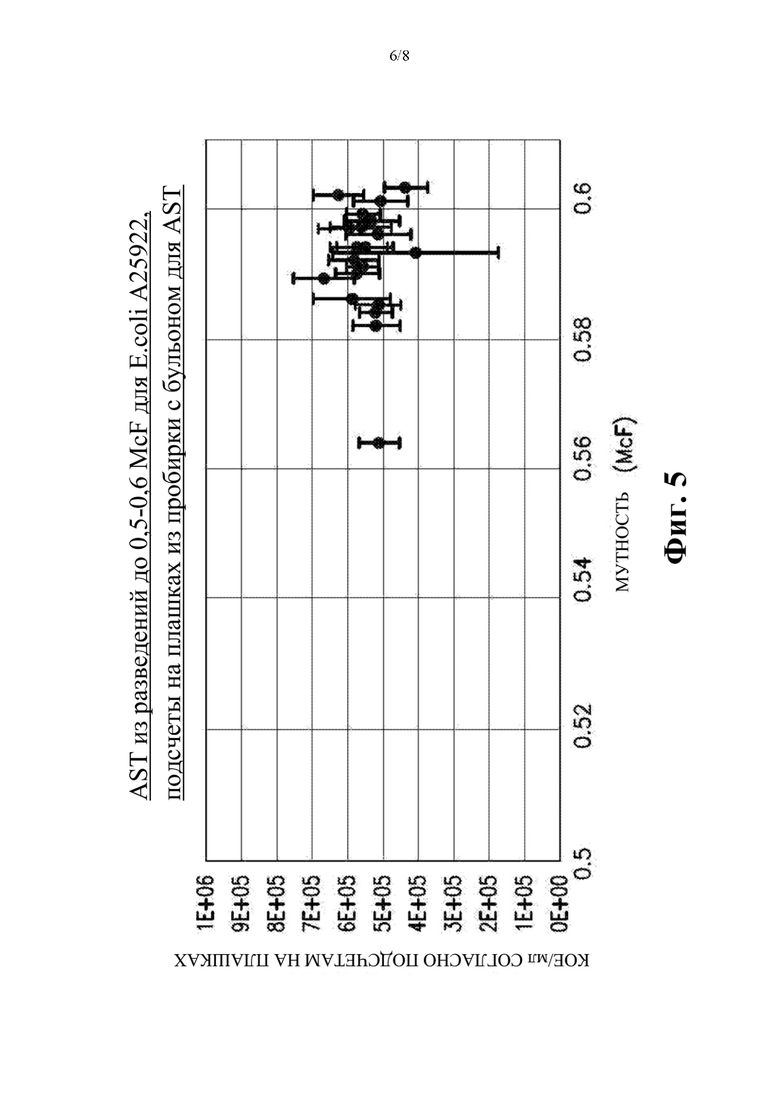
[0023] На фиг. 5 проиллюстрирована концентрация Е. coli в пробирке с бульоном для AST в сравнении с окончательной мутностью суспензии при применении способа, проиллюстрированного на фиг.2, для суспензии, образованной с применением только одного измерения мутности.
[0024] На фиг. 6 представлено краткое изложение результатов AST с применением суспензии, приготовленной с помощью способов с фиг. 4 и 5.
[0025] На фиг. 7 представлена схема системы.
Подробное раскрытие настоящего изобретения
[0026] Раскрытие в данном документе относится к аппарату для подготовки образца (далее в данном документе устройство пробоподготовки или станция пробоподготовки) в виде «Phoenix АР» или системе для AST в виде BD Phoenix™, или относится к системе управления данными с пользовательским интерфейсом в виде системы «BD EpiCenter», или относится к аппарату для анализа посева крови в виде «BD ВАСТЕС™», или относится к масс-спектрометрической системе в виде MALDI, но следует понимать, что значение этих терминов не ограничивается аппаратами, имеющими эти торговые названия, но могут включать аппарат, имеющий, по существу, аналогичные функциональные возможности. Аппарат, имеющий, по существу, аналогичные функциональные возможности, может включать системы для посева крови ВасТ/Alert (bioMerieux) и VersaTREK (Trek) и системы для ID/AST Vitek (bioMerieux) и MicroScan (Siemens Healthcare).
[0027] В соответствии с одним вариантом осуществления система, описанная в данном документе, объединяет возможности идентификации микробов у инструмента для MALDI с возможностями AST и обработки данных при лабораторном анализе или с системой обработки, такой как системы Phoenix, Phoenix АР, ВАСТЕС или EpiCenter.
[0028] В соответствии с другим вариантом осуществления Phoenix АР модифицируют для приготовления не только инокулята для AST на панелях Phoenix, но также для приготовления этого же образца для планшета для MALDI. Этот признак обеспечивает преимущество автоматизации положительной идентификации для образца, приготовленного на планшете для MALDI, гарантируя, что изолят, наносимый на планшет для MALDI, происходит из того же самого образца, который применяют для исследования чувствительности к противомикробным средствам.
[0029] Система для MALDI, устройство пробоподготовки, система для AST и/или инструменты для посева крови имеют сообщение с системой управления данными, такой как система EpiCenter. EpiCenter обеспечивает доступ к данным в реальном масштабе времени и аналитический инструментарий для улучшения ухода за пациентом. EpiCenter способна своевременно отслеживать, анализировать и обмениваться микробиологическими данными, тем самым напрямую контролируя, отслеживая и улучшая уход за пациентом. Phoenix выдает результат AST, и инструмент для MALDI выдает результат идентификации. EpiCenter объединяет результаты и применяет экспертные правила, выдавая окончательные результаты ID/AST для образца. Примером такой системы, которая применяет экспертные правила, является BDXpert™.
[0030] На фиг. 7 представлена блок-схема системы 100, которая выявляет и анализирует микробные образцы в соответствии с вариантом осуществления настоящего изобретения. Различные компоненты системы 100 включают станцию 102 пробоподготовки (такую как Phoenix АР), масс-спектрометрический инструмент 104 (такой как MALDI-TOF), систему 106 для AST (такую как Phoenix), систему 108 для посева крови (такую как инструмент ВАСТЕС), приготовленную среду 110 для посева (например, приготовленную вручную или приготовленную системой, такой как Innova), систему 112 управления данными (такую как EpiCenter) и информационную систему 116 лаборатории («LIS»), которая получает данные от системы 112 управления данными через канал 114 ID/AST и которая обеспечивает информацией о пациенте систему 112 управления данными через канал 118 РТ Info.
[0031] В системе 100 систему пробоподготовки обеспечивают бактериями, например, собранными с подготовленной плашки или взятыми из флакона для посева крови. В соответствии с одним вариантом осуществления кюветы инокулируют бактериальным образцом с избытком. Кюветы преимущественно применяют в качестве источника образца как для ID, так и для AST. Это гарантирует, что исследованию ID и AST подвергают не только образец от одного и того же пациента, но также один и тот же изолят.
[0032] Станция 102 пробоподготовки готовит образец как для ID, так и для AST, в то время как система 106 для AST выдает результат AST, а масс-спектрометрический инструмент 104 выдает результат ID. Система 112 обработки данных хранит результат ID и результат AST, необязательно, применяя экспертные правила для получения окончательных объединенных результатов ID/AST для образца, а также взаимодействует с системой LIS.
[0033] Что касается фиг. 1, процесс начинается со стадии 150 сбора образца (как правило, с плашки с культурой или из пробирки с культурой) и стадии 155 доставки этого образца в суспензию. Мутность суспензии измеряют на стадии 160 и мутность затем оценивают для определения того, находится ли измеренная мутность в пределах предварительно определенного диапазона на стадии 165. Предварительно определенный диапазон является необходимым, поскольку объем образца, который применяют для инокуляции планшета для MALDI или пробирок с бульоном, ограничен объемом, который можно переносить с помощью автоматического пипетирующего устройства точно и в рамках ограничений пипетирующего устройства по объему. В связи с этим современные пипетирующие устройства выполнены с возможностью переноса объема суспензии, не большего чем от приблизительно 10 мл (т.е. 1000 мкл) до приблизительно 12 мл (т.е. 1200 мкл).
[0034] Если суспензия имеет мутность в пределах целевого диапазона, то, исходя из показаний мутности, требующийся объем суспензии, необходимый для инокуляции пробирки с бульоном необходимым количеством образца, рассчитывают на стадии 170. Пипетирующее устройство применяют для отсасывания рассчитанного объема суспензии из суспензии на стадии 175. Если суспензия является слишком разбавленной, объем, требующийся для доставки целевого количества образца с целью инокуляции планшета для MALDI или пробирок с бульоном, будет слишком большим для размещения в пипетирующем устройстве (по меньшей мере за один перенос). Если суспензия является слишком концентрированной, то только малый объем суспензии требуется для инокуляции планшета для MALDI или пробирки с бульоном. Отсасыванием и дозированием малых объемов сложно точно управлять, что делает сложной доставку точного количества образца для инокуляции планшета для MALDI или пробирки с бульоном. Согласно способу, проиллюстрированному на фиг. 1, в соответствии с одним вариантом осуществления предварительно определенная мутность находится в диапазоне от приблизительно 0,2 единицы МакФарланда до приблизительно 2 единиц МакФарланда. Если суспензия находится за пределами этого диапазона, корректирующий протокол выполняют на стадии 180. Если суспензия является слишком концентрированной, суспензию подвергают протоколу 185 разведения, который будет снижать концентрацию в целевом диапазоне. Протокол 185 разведения преимущественно является предметом проектного решения и, как правило, заключается в удалении некоторого объема суспензии и замены его разбавителем. Удаляемый объем суспензии выбирают на основании измерения мутности. Если протокол 185 разведения является успешным, то на стадии 190 суспензию применяют для инокуляции пробирок с бульоном для AST с применением объема суспензии, рассчитанного на стадии 170. Один иллюстративный пример протокол разведения описан ниже в данном документе. Если протокол разведения не является успешным, образец сливают на стадии 191.
[0035] Если на стадии 180 определено, что суспензия является слишком разбавленной, суспензию подвергают протоколу концентрирования на стадии 195 для повышения концентрации образца в суспензии. Такие протоколы концентрирования требуют добавления образца в суспензию. Протокол 195 концентрирования преимущественно является предметом проектного решения и, как правило, заключается в добавлении некоторого количества дополнительного образца к разбавителю. Количество дополнительного образца, доставляемое в суспензию, сложно точно контролировать, поэтому протокол концентрирования может требовать дополнительных измерений мутности для определения мутности суспензии по завершению протокола концентрирования. Если протокол является успешным на стадии 190, то суспензию применяют для инокуляции пробирки с бульоном, рассчитывая объем суспензии, требующийся для инокуляции целевого количества образца в пробирку с бульоном на стадии 170, и объем суспензии отсасывают для инокуляции целевого планшета на стадии 175. Если протокол концентрирования не является успешным, то образец сливают на стадии 191.
[0036] Один пример протокола разведения описан ниже в данном документе. Предполагается, что как протокол разведения, так и протокол концентрирования требуют дополнительного измерения мутности после концентрирования или разведения суспензии.
[0037] Количество суспензии, которое применяют для инокуляции планшетов для идентификации (например, планшетов для MALDI) или пробирок с бульоном для исследования чувствительности к антибиотикам (AST), основывается на количестве образца, содержащемся на единицу объема суспензии. После образования суспензии, если концентрация образца в суспензии (т.е. мутность образца) является слишком высокой (например, приблизительно 2 единицы МакФарланда или выше), то объем суспензии, требующийся для инокуляции этого количества образца на планшет для MALDI или в пробирки с бульоном для AST, может быть достаточно небольшим. Небольшие объемы сложно точно дозировать пипеткой.
[0038] Следовательно, если количество образца, доставляемого в суспензию, является таким, что концентрация образца в суспензии (которую измеряют на основании мутности суспензии) является более высокой, чем верхнее пороговое значение (например, выше 2 единиц МакФарланда) в предварительно определенном диапазоне, то суспензию подвергают протоколу разведения для снижения мутности таким образом, чтобы мутность суспензии находилась в пределах предварительно определенного диапазона. Если количество образца, доставляемого в суспензию, является таким, что мутность суспензии находится ниже нижнего порогового значения (например, ниже приблизительно 0,2 единицы МакФарланда) в предварительно определенном диапазоне, то дополнительный образец получают для повышения концентрации образца в суспензии (если не доступен дополнительный образец, то суспензию исключают).
[0039] В одном примере измеренная мутность приготовленной суспензии находится в диапазоне приблизительно 3 единиц МакФарланда. В этом примере предварительно определенный диапазон мутности составляет от приблизительно 0,2 единицы МакФарланда до приблизительно 2 единиц МакФарланда. Исходя из этого измерения мутности, система определяет, что эту суспензию нужно подвергнуть протоколу разведения.
[0040] Предварительно определенный диапазон мутности преимущественно является предметом проектного решения. Факторы, которые определяют широкий диапазон, включают в себя: i) точность аппарата, применяемого для измерения мутности (например, нефелометра); ii) окно считывания нефелометра и iii) точность и емкость пипетирующего устройства. В соответствии со способом образуют суспензию с предельно высоким значением в единицах МакФарланда, а затем разводят для снижения мутности до значения, которое будет доставлять целевое количество образца для исследования ID или AST.
[0041] В еще одном примере образец получают и инокулируют в разбавитель суспензии. Измеряют мутность суспензии. Определяют, находится ли измеренная мутность в пределах предварительно определенного диапазона (например, от приблизительно 0,2 единицы МакФарланда до приблизительно 2 единиц МакФарланда). Исходя из количества образца, требующегося для инокуляции, получают объем суспензии, который будет содержать целевое количество образца, на планшет для MALDI или в пробирку с бульоном для AST. В соответствии с одним вариантом осуществления суспензию готовят посредством сбора количества колонии с чашки для культивирования и доставки собранного образца в суспензию.
[0042] В еще одном примере образец получают и инокулируют в разбавитель суспензии. Определяют, находится ли измеренная мутность ниже предварительно определенного диапазона (т.е. ниже приблизительно 0,2 единицы МакФарланда). В этом примере дополнительный образец получают и инокулируют в суспензию для повышения мутности образца. Повторно измеряют мутность суспензии. Если мутность находится в пределах предварительно определенного диапазона, определенный объем суспензии получают для доставки целевого количества образца на планшет для MALDI или в пробирку с бульоном для AST. Если скорректированная мутность является слишком высокой, то протокол разведения применяют для разведения суспензии. Если скорректированная мутность остается слишком высокой, процесс повторяют (если остается дополнительный образец, который нужно получить). Если дополнительный образец отсутствует, то суспензию не применяют и исключают из автоматизированного процесса. Если предпринимаемые повторные попытки получения суспензии с мутностью в пределах предварительно определенного диапазона являются безуспешными, то суспензию исключают из автоматизированного процесса.
[0043] Объем разбавителя суспензии преимущественно является предметом проектного решения. Объем суспензии не может быть слишком низким, поскольку он будет приводить к тому, что мутность суспензии будет намного выше, чем целевой диапазон мутности, что требует нескольких стадий разведения для получения суспензии с целевой мутностью. Объем суспензии не может быть слишком высоким, или мутность инокулируемых суспензий будет слишком низкой, что требует нескольких стадий для получения концентрации суспензии в пределах целевого диапазона мутности.
[0044] В соответствии с одним вариантом осуществления объем разбавителя суспензии, в который образец первоначально инокулируют, составляет от приблизительно 200 мкл до приблизительно 400 мкл. В качестве альтернативы, диапазон объема разбавителя суспензии составляет от приблизительно 250 мкл до приблизительно 350 мкл. В одном примере объем разбавителя суспензии, в который инокулируют образец, составляет приблизительно 300 мкл.
[0045] Примеры рабочих процессов с конкретными протоколами концентрирования/разведения проиллюстрированы на фиг. 2 и 3. Обычно образец получают на стадии 200. На 210, если определено, что образец представляет собой слизеподобный образец, то образец смешивают с разбавителем на стадии 220, и его мутность (в единицах МакФарланда) измеряют на 270.
[0046] Если образец не представляет собой слизеподобный образец, то мутность образца определяют перед разведением на стадии 230. На стадии 240, если исходное значение в единицах МакФарланда у суспензии для обычного образца является большим чем 2 единицы МакФарланда, или если исходное значение в единицах МакФарланда у суспензии для образца, предположительно содержащего стрептококк, является большим чем приблизительно 1 единица МакФарланда, суспензия отправляется на стадию 250, где деионизированную воду добавляют к суспензии и суспензию перемешивают.Если исходное значение в единицах МакФарланда для обычного образца является меньшим или равным приблизительно 2 (или для образца, предположительно содержащего стрептококк, если исходное значение в единицах МакФарланда является меньшим или равным 1), образец является готовым к смешиванию и образец отправляется на стадию 220.
[0047] На стадии 250 в автоматизированной системе с роботизированным пипетирующим устройством роботизированное пипетирующее устройство собирает в наконечник пипетки 1000 мкл и дозирует 950 мкл деионизированной воды в кювету, содержащую суспензию. Если образец предположительно содержит стрептококк, то роботизированное пипетирующее устройство собирает в наконечник пипетки 1000 мкл и дозирует 495 мкл деионизированной воды в кювету, содержащую суспензию. При ручной процедуре получают 1000 мкл в наконечник пипетки и количество деионизированной воды, описанной выше, дозируют в суспензию.
[0048] На стадии 220 получают аликвоту суспензии объемом 1000 мкл и применяют ее для перемешивая образца серией приблизительно из пяти (5) всасываний и выталкиваний приблизительно 250 мкл суспензии. Наконечник пипетки затем сбрасывают.
[0049] На стадии 260 деионизированную воду, которую не дозировали в суспензию на стадии 250, дозируют в отходы. Также, если объем разведенного образца превышает верхний предел объема, избыточный объем суспензии удаляют.
[0050] На стадии 270 мутность разведенной суспензии измеряют с применением нефелометра. Измерение мутности и устройства, применяемые для измерения мутности, являются хорошо известными специалистам в данной области техники и не описываются подробно в данном документе. Способы и аппарат для измерения мутности описаны в международной заявке WO 2016/034554. В протоколах на фиг. 2 и 3 любая стадия, которая вызывает изменение концентрации образца в суспензии, требует нового измерения мутности, поскольку значение мутности образца определяет, куда суспензия отправится в рабочем процессе, проиллюстрированном на фиг.2 и 3.
[0051] На стадии 280 оценивают измеренную мутность образца. Если значение в единицах МакФарланда у суспензии в кювете является меньшим чем 0,2, то суспензию нельзя применять для инокуляции пробирок с бульоном для AST. Система будет связывать образец с флагом ошибки, чтобы гарантировать, что суспензию не применят для инокулирования пробирок с бульоном для AST. Систему обновляют этой информацией и суспензию исключают.Если значение в единицах МакФарланда для суспензии является большим чем 0,2, то суспензию потенциально можно применять для инокуляции пробирок с бульоном для AST.
[0052] На стадии 290, если значение в единицах МакФарланда для суспензии является большим или равным 0,2, но меньшим или равным 2 (если образец предположительно содержит стрептококк, то диапазон является большим или равным 0,2, но меньшим или равным 1), то способ переходит к стадии 295, где рассчитывают инокулируемый объем суспензии, который будет доставлять целевое количество образца в пробирки с бульоном для AST.
[0053] Объем рассчитывают для обычных бульонов для AST с применением следующего соотношения:
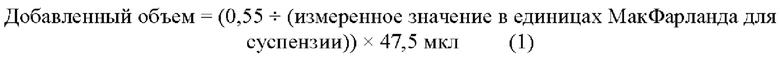
Например, если измеренная мутность для суспензии составляет 2,3, то объем суспензии, применяемый для инокуляции пробирки с бульоном для AST, составляет (0,55÷2,3)×47,5 мкл = 11,36 мкл. Если образец представляет собой образец стрептококка для AST, то бульон инокулируют объемом в соответствии со следующим соотношением:

[0054] Если значение в единицах МакФарланда является большим чем 2 (1, если суспензия предположительно содержит стрептококк), то на стадии 296 определяют число раз, которое образец был разведен. Если число разведений составляет менее трех, суспензию возвращают на стадию 250 для дальнейшего разведения и перемешивания (и уменьшения объема суспензии, если оно требуется для дополнительного разведения). Если число разведений составляет три (3), то выдается сообщение об ошибке, что образец превысил максимальное допустимое число стадий разведения.
[0055] На фиг. 3 описан процесс, при котором суспензию применяют для инокуляции пробирки с бульоном без стандартизации мутности суспензии. Процесс начинается с приготовленной суспензией, из которой было удалено небольшое количество и которую применяют для инокуляции планшета для MALDI. Что касается фиг. 3А, эту суспензию получают на стадии 300. На стадии 310 объем суспензии определяют после нанесения пятен для MALDI. Фактический объем определяют в соответствии со следующим соотношением:

В вышеуказанном уравнении Vs представляет собой объем суспензии, Vspot представляет собой объем суспензии на пятно, наносимое на планшет для MALDI. Например, кювета, содержащая суспензию, из которой был удален достаточный объем для одного пятна и 4 слоев на целевом планшете, будет иметь объем 330 мкл - ((1×4)×3 мкл)-(4×3)-(10×3)=276 мкл фактического объема суспензии в кювете. Это предполагает, что суспензия имеет время нахождения на платформе, составляющее три часа. На стадии 320 образец оценивают для определения того, является ли он слизеподобный образцом или нет. Если образец является слизеподобный, то образец направляется на стадию 370, где образец разводят, суспензию перемешивают и измеряют ее мутность. Если образец не является слизеподобный, образец направляется на стадию 330. Определение исходной мутности суспензии применяют для начала обработки первоначально концентрированной суспензии таким образом, чтобы суспензию можно было применять для инокуляции пробирки с бульоном для AST.
[0056] На стадии 340, если исходная мутность суспензии является большей или равной предварительно определенному пороговому значению (например, 0,75 единицы МакФарланда), то деионизированную воду добавляют в суспензию и суспензию перемешивают на стадии 350. Если исходная мутность суспензии является меньшей, чем предварительно определенное пороговое значение (например, 0,75 единицы МакФарланда), то способ переходит на стадию 370 в случае такой суспензии. Как упомянуто в других местах в данном документе, пороговые значения мутности и объема, изложенные в описаниях фиг. 2 и 3, представлены в качестве примера, а не ограничения.
[0057] На стадии 350 получают наконечник пипетки (1000 мкл) и он дозирует объем деионизированной воды в целевую кювету. Это может быть выполнено вручную или с применением роботизированного пипетирующего устройства, смонтированного на опорной раме. Объем деионизированной воды, который дозируют, рассчитывают согласно следующей формуле:

В соответствии с уравнением 4, соотношение фактического значения в единицах МакФарланда и порогового значения в единицах МакФарланда применяют для определения объема добавляемой деионизированной воды. Если фактическое значение в единицах МакФарланда ниже верхнего порогового значения, в суспензию не добавляют деионизированную воду. При применении вышеизложенного примера, в котором исходное значение в единицах МакФарланда составляет 1,4, объем деионизированной воды составляет ((1,4÷0,75)×276 мкл)-276 мкл = 239 мкл. На стадии 360, если рассчитанный объем меньше максимального объема (например, 950 мкл для наконечника пипетки на 1000 мкл), то рассчитанный объем деионизированной воды добавляют к образцу (что указано как «применять определенный объем» на фиг.3А). Если количество деионизированной воды, которую нужно добавить, превышает 950 мкл, то добавляют только максимальный объем 950 мкл (что указано как «установить максимальный объем» на фиг. 3А).
[0058] На стадии 370 наконечник пипетки (1000 мкл) применяют для перемешивания образца серией приблизительно из пяти (5) всасываний и выталкиваний приблизительно 250 мкл суспензии. После пятого цикла наконечник пипетки затем сбрасывают.
[0059] На стадии 380 определяют, нужно ли добавлять в суспензию дополнительный объем (т.е. деионизированную воду). Если требуется дополнительный объем, суспензия направляется на стадию 390, где в суспензию добавляют дополнительный разбавитель (деионизированную воду). Если добавленный объем приводит к превышениям ограничений по объему суспензии, то суспензию удаляют для снижения объема суспензии таким образом, чтобы объем приблизительно соответствовал верхней границе объема или был ниже нее. Если дополнительный разбавитель не требуется, способ переходит на стадию 400 (фиг. 3В), где нефелометр применяют для измерения мутности суспензии. Последующую обработку суспензии определяют на основании измеренной мутности (в соответствии с этим вариантом осуществления измеренная мутность измеряется в единицах МакФарланда).
[0060] В частности, если значение в единицах МакФарланда составляет менее 0,2, суспензию нельзя применять и в результате выводится сообщение об ошибке. См. стадию 410 на фиг. 3В. Если значение в единицах МакФарланда является большим или равным 0,2, то на стадии 420, если значение в единицах МакФарланда составляет от 0,2 до 0,3 (то есть значение 0,25 единицы МакФарланда +/- 20 процентов), суспензию применяют в качестве источника образца для панели для AST.
[0061] Если значение в единицах МакФарланда является большим чем 0,3, то на стадии 430 определяют, находится ли значение в единицах МакФарланда в диапазоне от 0,5 до 0,6 (то есть значение 0,55 единицы МакФарланда +/- 10 процентов). Такие суспензии определяют как подходящие для применения в качестве источника образца для инокуляции бульона для применения в панели для AST. Если мутность суспензии находится вне диапазона от 0,5 до 0,6 единицы МакФарланда на стадии 430, то образец направляется на стадию 440, где число предшествующих разведений суспензии определяет дальнейшую обработку суспензии. Если суспензию разводили 5 раз, то выдается сообщение об ошибке для этой суспензии, и ее не применяют в качестве источника образца для инокуляции бульона для AST.
[0062] Если суспензию разводили менее пяти раз, то на стадии 450 суспензия возвращается на стадию 360 для дальнейшего разведения на стадии 370. В случае тех суспензий, которые были определены как имеющие значения в единицах МакФарланда в предварительно определенном диапазоне, что делает такие суспензии подходящими для применения в качестве источника образца для инокуляции бульона для AST, суспензии разводят без дополнительных измерений мутности согласно следующей схеме, представленной в таблице 1.

[0063] Для получения суспензии с целевым объемом для значения в единицах МакФарланда из образцов, имеющих мутность в диапазонах, описанных выше в таблице 1, образец разводят в соответствии со следующим соотношением:

Например, при применении объема кюветы на стадии 350, если исходное измеренное значение в единицах МакФарланда у суспензии составляет 1, то добавленный объем равен ((1÷0,75)×276)-276, что составляет 92 мкл разбавителя (например, деионизированной воды), которую нужно добавить к суспензии для получения на выходе суспензии с целевым значением в единицах МакФарланда, составляющим 0,75. Тем не менее, если величина объема, который нужно добавить, превышает 950 мкл, к образцу добавляют только 950 мкл.
[0064] На стадии 370 после определения добавленного объема, определенный объем разбавителя (например, деионизированной воды) добавляют к образцу. Наконечник пипетки на 1000 мкл получают для этой цели (в автоматизированной рабочей среде роботизированное пипетирующее устройство принимает наконечник пипетки и пипетирующее устройство затем переносится посредством опорной рамы в положение пипетирующего устройства над суспензией). Наконечник пипетки применяют для перемешивания суспензии посредством всасывания объема суспензии, а затем выталкивания объема суспензии из наконечника пипетки. Последние пятьдесят (например, 50 мкл) дозируют через наконечник пипетки над суспензией, чтобы гарантировать, что наконечник пипетки является полностью пустым.
[0065] Если целевое значение в единицах МакФарланда составляет 0,55 или 0,25, и после разведения общий объем суспензии в кювете является большим чем 1500 мкл, то объем удаляют из суспензии так, чтобы суспензия не превышала максимальный объем. Применительно к стадии 390 избыточный объем удаляют в соответствии со следующей формулой:

[0066] Тем не менее, если число разведений превышает 5, то образец подвергали разведению слишком часто и его нельзя применять для последующего автоматизированного AST. В таких случаях результатом будет сообщение об ошибке. Если число предыдущих разведений является меньшим чем, то суспензия возвращается на стадию 360 для разведения, как описано выше.
[0067] Представленный выше способ, в котором объем инокулята для AST рассчитывали в соответствии вышеуказанными способами (вместо коррекции значения в единицах МакФарланда у концентрированной суспензии, образованной для MALDI, и инокуляции панелей для AST предварительно определенным объемом, исходя из требований к мутности (например, в единицах МакФарланда))), оценивали для определения его эффективности для инокуляции бульона для AST. Для этого определения штамм QC Е. coli, ВАСТЕС А25922, применяли для исследования воспроизводимости расчета объема инокулята, необходимого для достижения приемлемой концентрации организма в пробирке с бульоном для AST. Предварительно определенный диапазон концентраций составляет от 2×105 до 8×105 КОЕ/мл в случае Е. coli (ВАСТЕС А25922). ВАСТЕС А25922 также применяли для сравнения способа, описанного в данном документе (в котором суспензию оценивают и объем суспензии определяют, исходя из мутности суспензии), с процессом, в котором концентрированную суспензию готовят для MALDI, которую затем разводят до целевой мутности (например, либо 0,5-0,6 единицы МакФарланда, либо 0,2-0,3 единицы МакФарланда), и соответствующий объем этой суспензии применяют для инокуляции пробирки с бульоном для AST. Двадцать (20) образцов исследовали с применением обоих способов (в сумме 40 образцов), и подсчеты на плашках применяли для измерения концентрации бактерий в пробирке с бульоном для AST. Результаты AST от обработанных панелей для AST также анализировали.
[0068] Как показано на фиг. 6, все 40 образцов давали в результате концентрации бульона для AST в пределах от 2×105 до 8×105 КОЕ/мл для ряда начальных значений в единицах МакФарланда. Все из минимальных ингибирующих концентраций точно совпадали для всех 40 образцов. Таким образом, сделали вывод, что процесс разведения концентрированной суспензии, а затем определения объема суспензии, требующегося для доставки целевого количества образца в бульон для AST, является воспроизводимым и осуществляется аналогично процессу разведения до стандартизированного значения мутности (единиц МакФарланда) для этого штамма QC.
[0069] Что касается фиг. 4, проиллюстрирована концентрация Е. coli в пробирке с бульоном для AST в сравнении с окончательной мутностью суспензии, применяемой для инокуляции пробирки с бульоном для AST при применении прямого AST. «Усы» на графике представляют собой стандартное отклонение для 9 подсчетов на плашках, полученных для каждого образца. Верхней и нижней пунктирными линиями указаны границы приемлемого диапазона концентраций, от 2×105 до 8×105 КОЕ/мл, а пунктирная линия посередине представляет собой середину диапазона (5×105 КОЕ/мл).
[0070] Что касается фиг.5, концентрация Е. coli в пробирке с бульоном для AST в сравнении с окончательной мутностью суспензии, применяемой для инокуляции пробирки с бульоном для AST при применении схемы разведения для разведения суспензии до целевого значения в единицах МакФарланда (0,5-0,6 единицы МакФарланда). «Усы» на графике представляют собой стандартное отклонение для 9 подсчетов на плашках, полученных для каждого образца. Верхней и нижней пунктирными линиями указаны границы приемлемого диапазона концентраций, от 2×105 до 8×105 КОЕ/мл, а пунктирная линия посередине представляет собой середину диапазона (5×105 КОЕ/мл).
[0071] Что касается фиг. 6, минимальная ингибирующая концентрация (MIC) для каждого антибиотика была одинаковой независимо от того, корректировали ли мутность суспензии, чтобы она находилась в рамках целевой мутности, или корректировали объем инокулята для инокуляции целевого количества образца в бульон для AST.
[0072] Несмотря на то что настоящее изобретение в данном документе было описано со ссылкой на конкретные варианты осуществления, следует понимать, что эти варианты осуществления являются только иллюстрирующими принципы и применения настоящего изобретения. Таким образом, следует понимать, что многочисленные модификации могут быть выполнены в иллюстративных вариантах осуществления, и что другие схемы могут быть разработаны без отступления от идеи и объема настоящего изобретения, которые определяются пунктами приложенной формулы изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| АВТОМАТИЗИРОВАННЫЙ СПОСОБ И СИСТЕМА ДЛЯ ПОЛУЧЕНИЯ И ПРИГОТОВЛЕНИЯ ОБРАЗЦА МИКРООРГАНИЗМА КАК ДЛЯ ИДЕНТИФИКАЦИИ, ТАК И ДЛЯ ТЕСТОВ НА ЧУВСТВИТЕЛЬНОСТЬ К АНТИБИОТИКАМ | 2016 |
|
RU2718086C2 |
| УСТРОЙСТВО И КЮВЕТЫ ДЛЯ ОПТИЧЕСКОГО КОНТРОЛЯ НЕБОЛЬШИХ ОБЪЕМОВ ЖИДКОГО ОБРАЗЦА | 2015 |
|
RU2657020C1 |
| Способ измерения подавления бактерий антибактериальными средствами, устройство для подсчета бактерий и способ подсчета | 2020 |
|
RU2792041C1 |
| ПРЕЦИЗИОННЫЙ СПОСОБ СРАВНИТЕЛЬНОЙ ЭКСПРЕСС-ОЦЕНКИ ЭФФЕКТИВНОСТИ АНТИМИКРОБНЫХ ВЕЩЕСТВ В ОТНОШЕНИИ УСЛОВНО ПАТОГЕННОГО ВИДА Pseudomonas aeruginosa | 2021 |
|
RU2760788C1 |
| Способ определения показателя антибиотикорезистентности бактерий рода Desulfovibrio spp. | 2023 |
|
RU2821994C1 |
| АНТИБАКТЕРИАЛЬНАЯ КОМПОЗИЦИЯ НА ОСНОВЕ ЭНДОЛИЗИНОВ И ЛЕКАРСТВЕННЫЕ СРЕДСТВА В ФОРМЕ ГЕЛЯ ИЛИ СПРЕЯ С ЕЕ ИСПОЛЬЗОВАНИЕМ | 2021 |
|
RU2790481C1 |
| НОВЫЙ СПОСОБ ОТДЕЛЕНИЯ И ОПРЕДЕЛЕНИЯ ВИРУСНОЙ НАГРУЗКИ В ОБРАЗЦЕ ПАНКРЕАТИНА | 2008 |
|
RU2491341C2 |
| СПОСОБ ВЫДЕЛЕНИЯ И ОПРЕДЕЛЕНИЯ ВИРУСНОЙ НАГРУЗКИ В ОБРАЗЦЕ ПАНКРЕАТИНА | 2007 |
|
RU2466187C2 |
| КОМБИНАЦИЯ, ВКЛЮЧАЮЩАЯ ФУЛЬВОВУЮ КИСЛОТУ И АНТИБИОТИКИ | 2009 |
|
RU2505295C2 |
| СПОСОБ ПОЛУЧЕНИЯ ИНОКУЛЮМА С ЕДИНИЧНЫМ КОЛИЧЕСТВОМ МИКРООРГАНИЗМОВ | 2024 |
|
RU2830890C1 |







Изобретение относится к биотехнологии. Предложен способ приготовления суспензии биологического образца для идентификации микроорганизмов и определения их чувствительности к противомикробным средствам, предусматривающий приготовление суспензии образца в контейнере посредством объединения биологического образца, который предположительно содержит один или несколько микроорганизмов, с разбавителем образца; измерение мутности приготовленной суспензии образца; определение того, находится ли измеренная мутность в пределах предварительно определенного диапазона от 0,2 единиц МакФарланда до 2 единиц МакФарланда; расчет объема приготовленной суспензии, требующегося для инокуляции предварительно определенного объема среды культивирования, исходя из соотношения предварительно определенной целевой мутности для суспензии для инокуляции среды культивирования и измеренной мутности, умноженного на фактический объем приготовленной суспензии образца, требующийся для доставки предварительно определенного количества биологического образца в среду культивирования; и нанесение рассчитанного объема суспензии образца на среду культивирования. Изобретение обеспечивает расширение арсенала автоматизированных способов приготовления суспензии образца как для системы, которая идентифицирует микроорганизмы, так и для системы, которая исследует микроорганизмы в отношении их устойчивости/чувствительности к противомикробным средствам. 11 з.п. ф-лы, 8 ил., 1 табл.
1. Способ приготовления суспензии биологического образца для обеспечения целевого количества образца для идентификации микроорганизмов и определения их чувствительности к противомикробным средствам, предусматривающий:
приготовление суспензии образца в контейнере для суспензии образца посредством объединения биологического образца, который предположительно содержит один или несколько микроорганизмов, с разбавителем образца;
измерение мутности приготовленной суспензии образца;
определение того, находится ли измеренная мутность в пределах предварительно определенного диапазона от 0,2 единиц МакФарланда до 2 единиц МакФарланда;
расчет объема приготовленной суспензии, требующегося для инокуляции предварительно определенного объема среды культивирования, исходя из соотношения предварительно определенной целевой мутности для суспензии для инокуляции среды культивирования и измеренной мутности, умноженного на фактический объем приготовленной суспензии образца, требующийся для доставки предварительно определенного количества биологического образца в среду культивирования; и
нанесение рассчитанного объема суспензии образца на среду культивирования.
2. Способ по п. 1, дополнительно предусматривающий:
если измеренная мутность приготовленной суспензии образца ниже предварительно определенного диапазона, выполнение протокола концентрирования для повышения мутности приготовленной суспензии образца и повторное измерение мутности приготовленной суспензии образца; и
если измеренная мутность выше предварительно определенного диапазона, выполнение протокола разведения для снижения мутности приготовленной суспензии образца и повторное измерение мутности приготовленной суспензии образца.
3. Способ по п. 2, причем протокол концентрирования предусматривает добавление дополнительного образца в приготовленную суспензию образца перед повторным измерением мутности приготовленной суспензии образца.
4. Способ по п. 2, причем протокол разведения предусматривает добавление дополнительного разбавителя в приготовленную суспензию образца перед повторным измерением мутности приготовленной суспензии образца.
5. Способ по п. 3, причем протокол концентрирования дополнительно предусматривает:
определение того, превышает ли приготовленная суспензия образца предварительно определенные требования к объему; и
удаление избыточного объема из контейнера для приготовленной суспензии образца с обеспечением приготовленной суспензии образца в пределах предварительно определенных требований к объему перед добавлением дополнительного образца к приготовленной суспензии образца.
6. Способ по п. 4, причем протокол разведения дополнительно предусматривает:
определение того, превышает ли приготовленная суспензия образца предварительно определенные требования к объему; и
удаление избыточного объема из контейнера для приготовленной суспензии образца с обеспечением приготовленной суспензии образца в пределах предварительно определенных требований к объему перед добавлением дополнительного разбавителя к приготовленной суспензии образца.
7. Способ по п. 5, причем, если повторно измеренная мутность находится в пределах предварительно определенного диапазона значений мутности, выполняют расчет объема приготовленной суспензии образца, требующегося для инокуляции среды культивирования, исходя из соотношения предварительно определенной целевой мутности для суспензии образца для инокуляции среды культивирования и повторно измеренной мутности умноженного на объем приготовленной суспензии образца, требующийся для доставки предварительно определенного количества биологического образца в среду культивирования с применением приготовленной суспензии образца, имеющей предварительно определенную целевую мутность; и
нанесение рассчитанного объема приготовленной суспензии образца на среду культивирования.
8. Способ по п. 6, причем, если повторно измеренная мутность находится в пределах предварительно определенного диапазона значений мутности, выполняют расчет объема приготовленной суспензии образца, требующегося для инокуляции среды культивирования, исходя из соотношения предварительно определенной целевой мутности для суспензии образца для инокуляции среды культивирования и повторно измеренной мутности, умноженного на объем приготовленной суспензии образца с предварительно определенной целевой мутностью, требующегося для доставки предварительно определенного количества биологического образца в среду культивирования; и
нанесение рассчитанного объема приготовленной суспензии образца на среду культивирования.
9. Способ по п. 5, причем, если повторно измеренная мутность не находится в пределах предварительно определенного диапазона значений мутности, выполняют повторение протокола концентрирования.
10. Способ по п. 6, причем, если повторно измеренная мутность не находится в пределах предварительно определенного диапазона значений мутности, выполняют повторение протокола разведения.
11. Способ по п. 9, дополнительно предусматривающий слив приготовленной суспензии образца, если протокол концентрирования был повторен предварительно определенное число раз.
12. Способ по п. 10, дополнительно предусматривающий слив приготовленной суспензии образца, если протокол разведения был повторен предварительно определенное число раз.
| Токарный резец | 1924 |
|
SU2016A1 |
| Токарный резец | 1924 |
|
SU2016A1 |
| АВТОМАТИЗИРОВАННЫЙ ОТБОР МИКРООРГАНИЗМОВ И ИХ ИДЕНТИФИКАЦИЯ С ПОМОЩЬЮ МАЛДИ | 2013 |
|
RU2639777C9 |
Авторы
Даты
2023-11-09—Публикация
2019-06-24—Подача