Уровень техники
Варианты осуществления настоящего изобретения относятся к способу инактивации вируса в оде непрерывного получения биологических продуктов, в частности, терапевтических продуктов на основе антител.
Регулирующие органы требуют от производителей продемонстрировать, что их процессы производства способны уничтожать инфекционные вирусы путем удаления и/или инактивации вирусных загрязнителей, которые могут присутствовать в их биотерапевтических продуктах. Инактивация эндогенных или экзогенных вирусов в оболочке с помощью обработки низким рН обычно применяется в производственных процессах, поскольку она является простой, недорогостоящей и надежной. Инактивация вирусов при низком рН обычно проводится на объединенном элюате, собранном из колонки для аффинного захвата белка, а условие низкого рН достигается титрованием слабой кислоты к объединенному элюату. Однако не все антитела очень стабильны в условиях низкого рН и могут образовывать агрегаты, поэтому обработку следует проводить в более высоком диапазоне рН. В результате вирусная инактивация становится менее надежной, и требуется более длительное время обработки для достижения такого же логарифмического снижения вирусной инфекционности.
Помимо инактивации вирусов при низком рН, в качестве стадий удаления вирусов при производстве антител обычно используются аффинная колоночная хроматография, анионообменная хроматография и вирусная фильтрация. Было показано, что как анионообменная хроматография, так и вирусная фильтрация очень эффективны при удалении вирусов как в оболочке, так и без нее. Однако, в отличие от анионообменной хроматографии и вирусной фильтрации, эффективность сродства к белку А при удалении вирусов очень ограничена. Таким образом, желательно исключить аффинную хроматографию для белка А как подтвержденную стадию очистки от вирусов и заменить ее более простой и надежной стадией инактивации вируса.
Детергенты ранее использовались для инактивации вирусов в процессе производства биологических средств. Добавление детергентов к осветленному супернатанту клеточной культуры часто используется для инактивации вирусов в оболочке, в то время как антитела лабильны к обработке низким рН, хотя традиционно используются растворитель или детергент. Было показано, что Triton Х-100 очень эффективен и надежен для инактивации вирусов в оболочке. Также использовались общие условия для инактивации вирусов в оболочке с помощью Triton Х-100. Однако октлифенол, продукт разложения Triton х-100, является эндокринным разрушителем, который может нанести вред людям, рыбам и другим организмам, тем самым оказывая неблагоприятное воздействие на окружающую среду. Более того, установленные пределы для сброса октилфенола составляют от 0,01 до 0,1 частей на миллиард (ppb), которые для производителей биологических средств является очень дорогостоящим удалять из сточных вод биотехнологических процессов.
В биофармацевтической промышленности растет интерес к переходу от периодического режима к непрерывному режиму производства, чтобы удовлетворить будущие потребности биофармацевтической промышленности. Производственный процесс считается полностью непрерывным, если он состоит из интегрированных (физически связанных) непрерывных узлов с нулевым или минимальным промежуточным объемом. В настоящее время почти все узлы стандартного производства моноклональных антител находятся в режиме готовности к непрерывной обработке, за исключением стадии инактивации вируса при низком рН, которая в настоящее время выполняется в периодическом процессе. Как правило, объединенный элюат стадии захвата колонкой для аффинной хроматографии с белком А доводят до желаемого значения рН путем титрования слабой кислоты в объединенный элюат белка А и выдерживают в сосуде или мешке в течение требуемого времени инактивации 60-120 минут. Хотя эффективная инактивация вируса при низком рН≥5,0 log уменьшения ретровируса может быть достигнута в условиях рН≤3,6, при комнатной температуре и в течение времени инкубации ≥30 минут (ASTM, 2012), не все моноклональные антитела очень стабильны при этом условии низкого рН и будут образовывать агрегаты. Следовательно, обработки с целью вирусной инактивации необходимо проводить при более высоком рН (например, от 3,7 до 3,9). Как правило, чем выше рН и чем более длительное время инактивации требуется, тем выше потери продукта из-за агрегации антител, что представляет собой проблему при адаптации к непрерывному процессу. Следовательно, задача состоит в том, чтобы преобразовать инактивацию вирусов при низком рН в периодическом режиме в непрерывный процесс, обеспечивая при этом, чтобы время инактивации вирусов в проточном режиме контролировалось так же точно, как и в периодическом режиме.
Чтобы обеспечить типичное время пребывания (1-2 часа) для инактивации вирусов при низком рН и проточных элюатов, необходима длинная и узкая труба для разработки узла для непрерывной инактивации вирусов при низком рН. Однако такой узел создаст высокое противодавление и широкое распределение времени пребывания, что приведет к более длительному времени пребывания молекул антител вблизи стенок трубы. Это может вызвать резкое уменьшение количества мономеров в пользу образования агрегатов антител из-за бесконечно долгого времени пребывания для обработки низким рН. В настоящее время для решения этих проблем был предложен «катушечный инвертор потока» (CFI), состоящий из спиральных модулей и 90-градусных изгибов с узким распределением времени пребывания. Необходима более точная система обработки с узким распределением времени пребывания для операции непрерывной инактивации вирусов. Эти и другие проблемы решены вариантами осуществления настоящего изобретения.
Сущность изобретения
Варианты осуществления включают способы, используемые для инактивации вируса при непрерывном производстве биологических средств. Способы включают отделение элюата с биологическим средством и активным вирусом с использованием колонки, воздействие на элюат с активным вирусом ортогональной обработкой низким рН и неионным детергентом одновременно с инактивацией вируса, где время для инактивации вируса элюата сокращено по сравнению с временем обработки элюата с использованием низкого рН или неионного детергента по отдельности, и биологическое средством сохраняется.
Краткое описание чертежей
Квалифицированному специалисту понятно, что чертежи, описанные ниже, предназначены только для целей иллюстрации. Чертежи никоим образом не предназначены для ограничения объема настоящего изобретения или формулы изобретения.
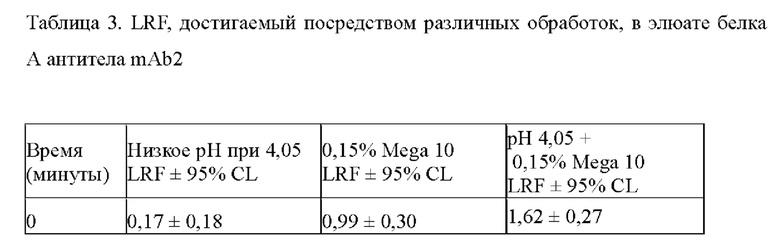
На Фиг. 1 показана кинетика инактивации X-MuLV при различных концентрациях Mega-10 при 16°С в (А) образце элюата белка А антитела mAb1 при рН 7,01 и (В) образце элюата белка А антитела mАb2 при рН 7,01. X-MuLV добавляли в нейтрализованный элюат белка А антитела, содержащий различные концентрации Mega-10. После тщательного перемешивания смесь инкубировали на водяной бане, установленной на 16°С, и в указанное время отбирали аликвоту образца для оценки кинетики инактивации вируса с помощью анализа TCID50.
Фиг. 2 показывает синергетические эффекты двойной обработки низким рН и Mega-10 на снижение инфекционности X-MuLV после инкубации при 16°С в образце элюата белка А антитела mAb1. Линия в 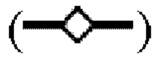 показывает кинетику инактивации X-MuLV и Log 10 фактор снижения (LRF), достигаемые в течение 30 минут инкубации с 0,10% Mega-10; линия
показывает кинетику инактивации X-MuLV и Log 10 фактор снижения (LRF), достигаемые в течение 30 минут инкубации с 0,10% Mega-10; линия 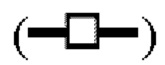 показывает кинетику инактивации X-MuLV и LRF, достигаемые в ходе 30 минут инкубации в образце элюата белка А антитела mAb1 при рН 3,91; линия в
показывает кинетику инактивации X-MuLV и LRF, достигаемые в ходе 30 минут инкубации в образце элюата белка А антитела mAb1 при рН 3,91; линия в 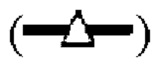 показывает кинетику инактивации X-MuLV и LRF, достигаемые в ходе 30 минут инкубации в образце элюата белка А антитела mAb1 при рН 3,91 и в присутствии 0,1% Mega-10.
показывает кинетику инактивации X-MuLV и LRF, достигаемые в ходе 30 минут инкубации в образце элюата белка А антитела mAb1 при рН 3,91 и в присутствии 0,1% Mega-10.
Фиг.3 показывает синергетические эффекты двойной обработки низким рН и Mega-10 на снижение инфекционности X-MuLV после инкубации при 16°С в образце элюата белка А антитела mАb2. Линия в 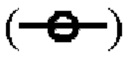 показывает кинетику инактивации X-MuLV и LRF, достигаемые в ходе 30 минут инкубации с 0,15% Mega-10; линия в
показывает кинетику инактивации X-MuLV и LRF, достигаемые в ходе 30 минут инкубации с 0,15% Mega-10; линия в 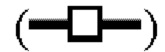 показывает кинетику инактивации X-MuLV и LRF, достигаемые в ходе 30 минут инкубации в образце элюата белка А антитела mAb2 при рН 4,05; линия в
показывает кинетику инактивации X-MuLV и LRF, достигаемые в ходе 30 минут инкубации в образце элюата белка А антитела mAb2 при рН 4,05; линия в  показывает кинетику инактивации X-MuLV и LRF, достигаемые в ходе 30 минут инкубации в образце элюата белка А антитела mAb2 при рН 4,05 и в присутствии 0,15% Mega-10.
показывает кинетику инактивации X-MuLV и LRF, достигаемые в ходе 30 минут инкубации в образце элюата белка А антитела mAb2 при рН 4,05 и в присутствии 0,15% Mega-10.
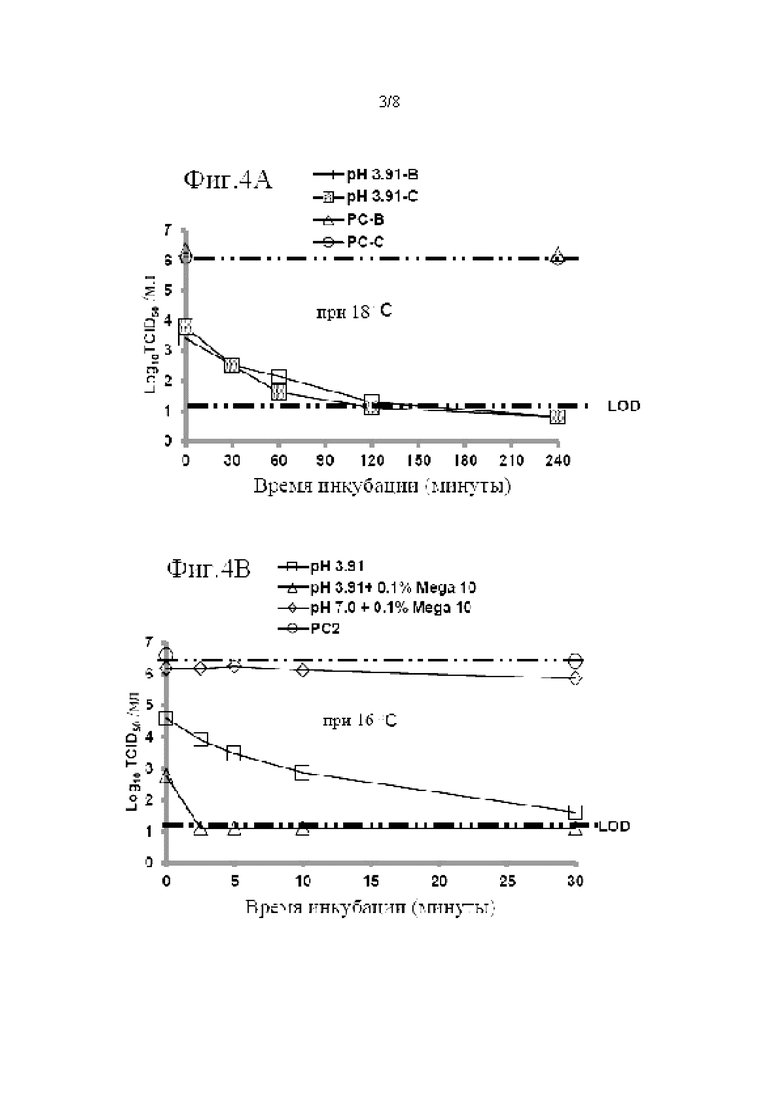
Фиг. 4 показывает синергетические эффекты двойной обработки низким рН и Mega-10 на сокращение времени, необходимого для инактивации X-MuLV ниже уровня предела обнаружения в образце элюата белка А антитела mAb1. (А) Кинетика инактивации X-MuLV посредством обработки низким рН и оставшаяся вирусная инфекционность в течение 240 минут инкубации в образце элюата белка А антитела mAb1 при 18°С и рН 3,91, линия в 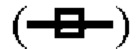 и
и 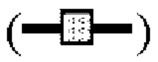 означает двойное проведение экспериментов. (В) Кинетика инактивации X-MuLV путем двойной обработки и оставшаяся вирусная инфекционность в течение 30 минут инкубации в образце элюата белка А антитела mAbl при 16°С и рН 3,91, линия в
означает двойное проведение экспериментов. (В) Кинетика инактивации X-MuLV путем двойной обработки и оставшаяся вирусная инфекционность в течение 30 минут инкубации в образце элюата белка А антитела mAbl при 16°С и рН 3,91, линия в 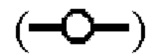 показывает стабильность и титры положительного контроля, линия в
показывает стабильность и титры положительного контроля, линия в 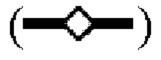 показывает кинетику инактивации X-MuLV и оставшуюся вирусную инфекционность в течение 30 минут инкубации с 0,1% Mega-10; линия в
показывает кинетику инактивации X-MuLV и оставшуюся вирусную инфекционность в течение 30 минут инкубации с 0,1% Mega-10; линия в 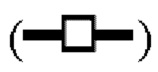 показывает кинетику инактивации X-MuLV и оставшуюся вирусную инфекционность в течение 30 минут инкубации в образце элюата белка А антитела mAb1 при рН 3,91; линия в
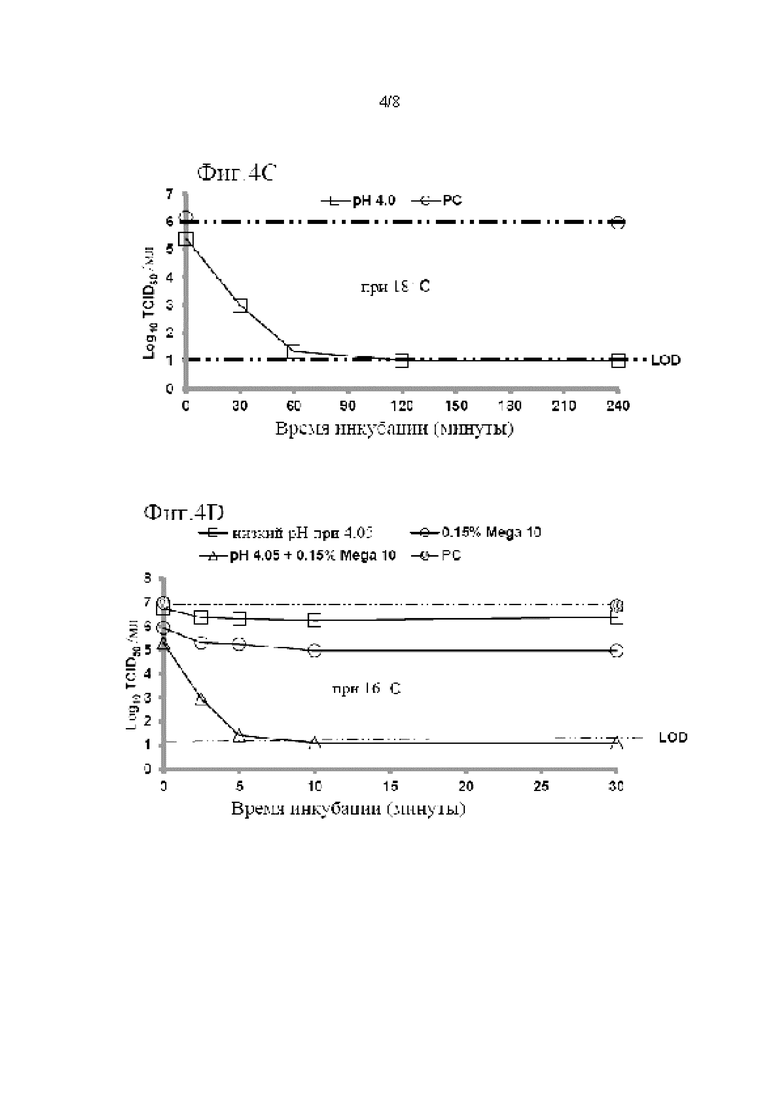
показывает кинетику инактивации X-MuLV и оставшуюся вирусную инфекционность в течение 30 минут инкубации в образце элюата белка А антитела mAb1 при рН 3,91; линия в 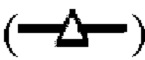 показывает кинетику инактивации X-MuLV и оставшуюся вирусную инфекционность в течение 30 минут инкубации в образце элюата белка А антитела mAb1 при рН 3,91 и в присутствии 0,1% Mega-10. (С) Кинетика инактивации X-MuLV посредством обработки низким рН и оставшаяся вирусная инфекционность в течение 240 минут инкубации в образце элюата белка А антитела mAb2 при 18°С и рН 4,0. (D) Кинетика инактивации X-MuLV путем двойной обработки и оставшаяся вирусная инфекционность в течение 30 минут инкубации в образце элюата белка А антитела mAb2 при 16°С и рН 4,05, линия в
показывает кинетику инактивации X-MuLV и оставшуюся вирусную инфекционность в течение 30 минут инкубации в образце элюата белка А антитела mAb1 при рН 3,91 и в присутствии 0,1% Mega-10. (С) Кинетика инактивации X-MuLV посредством обработки низким рН и оставшаяся вирусная инфекционность в течение 240 минут инкубации в образце элюата белка А антитела mAb2 при 18°С и рН 4,0. (D) Кинетика инактивации X-MuLV путем двойной обработки и оставшаяся вирусная инфекционность в течение 30 минут инкубации в образце элюата белка А антитела mAb2 при 16°С и рН 4,05, линия в 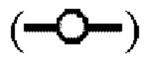 показывает стабильность и титры положительного контроля, линия в
показывает стабильность и титры положительного контроля, линия в  показывает кинетику инактивации X-MuLV и оставшуюся вирусную инфекционность в течение 30 минут инкубации с 0,15% Mega-10; линия в
показывает кинетику инактивации X-MuLV и оставшуюся вирусную инфекционность в течение 30 минут инкубации с 0,15% Mega-10; линия в 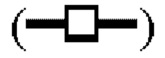 показывает кинетику инактивации X-MuLV и оставшуюся вирусную инфекционность в течение 30 минут инкубации в образце элюата белка А антитела mAb2 при рН 4,05; линия в
показывает кинетику инактивации X-MuLV и оставшуюся вирусную инфекционность в течение 30 минут инкубации в образце элюата белка А антитела mAb2 при рН 4,05; линия в  показывает кинетику инактивации X-MuLV и оставшуюся вирусную инфекционность в течение 30 минут инкубации в образце элюата белка А антитела mAb2 при рН 4,05 и в присутствии 0,15% Mega-10.
показывает кинетику инактивации X-MuLV и оставшуюся вирусную инфекционность в течение 30 минут инкубации в образце элюата белка А антитела mAb2 при рН 4,05 и в присутствии 0,15% Mega-10.
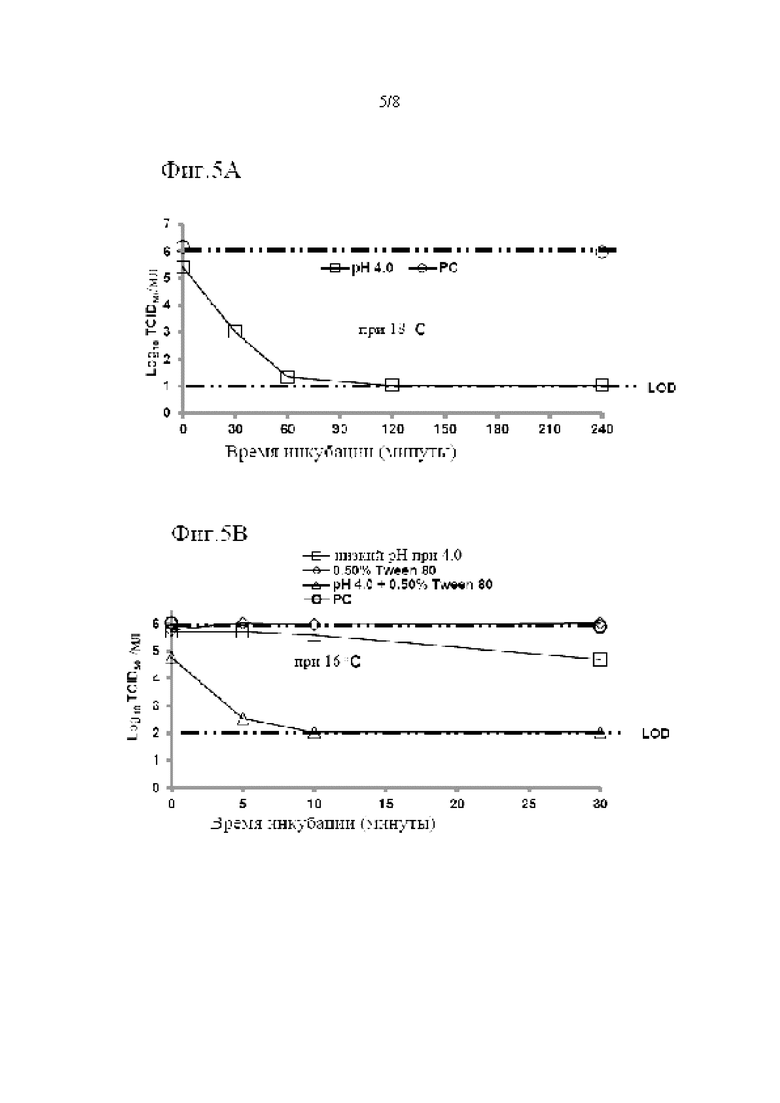
Фиг. 5 показывает синергетические эффекты двойной обработки низким рН и Tween 80 на сокращение времени, необходимого для инактивации X-MuLV ниже уровня предела обнаружения в образце элюата белка А антитела mAb2. (А) Кинетика инактивации X-MuLV посредством обработки низким рН и оставшаяся вирусная инфекционность в течение 240 минут инкубации в образце элюата белка А антитела mAb2 при 18°С и рН 4,0. (В) Кинетика инактивации X-MuLV путем двойной обработки и оставшаяся вирусная инфекционность в течение 30 минут инкубации в образце элюата белка А антитела mAb2 при 16°С и рН 4,0, линия в 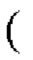
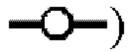 показывает стабильность и титры положительного контроля, линия в
показывает стабильность и титры положительного контроля, линия в  показывает кинетику инактивации X-MuLV и оставшуюся вирусную инфекционность в течение 30 минут инкубации с 0,5% Tween 80; линия в
показывает кинетику инактивации X-MuLV и оставшуюся вирусную инфекционность в течение 30 минут инкубации с 0,5% Tween 80; линия в 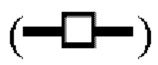 показывает кинетику инактивации X-MuLV и оставшуюся вирусную инфекционность в течение 30 минут инкубации в образце элюата белка А антитела mAb2 при рН 4,0; линия в
показывает кинетику инактивации X-MuLV и оставшуюся вирусную инфекционность в течение 30 минут инкубации в образце элюата белка А антитела mAb2 при рН 4,0; линия в 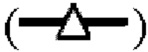 показывает кинетику инактивации X-MuLV и оставшуюся вирусную инфекционность в течение 30 минут инкубации в образце элюата белка А антитела mAb2 при рН 4,0 и в присутствии 0,5% Tween 80.
показывает кинетику инактивации X-MuLV и оставшуюся вирусную инфекционность в течение 30 минут инкубации в образце элюата белка А антитела mAb2 при рН 4,0 и в присутствии 0,5% Tween 80.
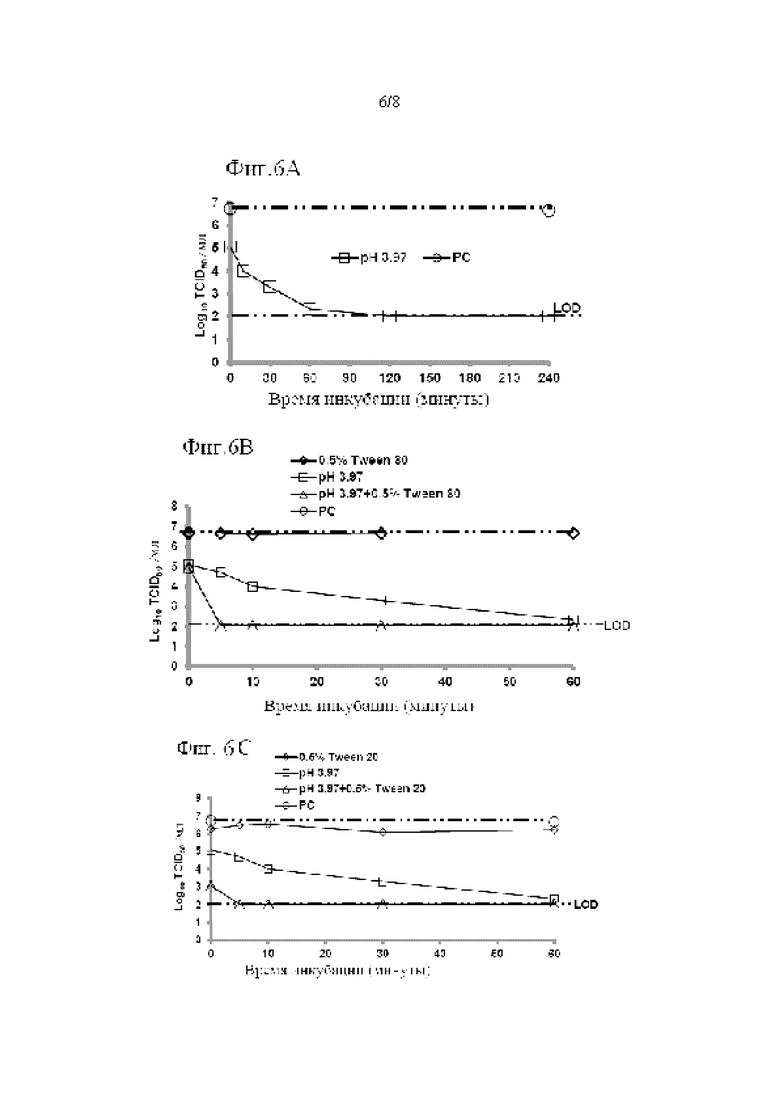
Фиг. 6 показывает синергетические эффекты двойной обработки низким рН и Tween 80 или Tween 20 на сокращение времени, необходимого для инактивации X-MuLV ниже уровня предела обнаружения в образце элюата белка А антитела mAb3. (А) Кинетика инактивации X-MuLV посредством обработки низким рН и оставшаяся вирусная инфекционность в течение 240 минут инкубации в образце элюата белка А антитела mAb3 при 16 С и рН 3,97. (В) Кинетика инактивации Х-MuLV путем двойной обработки низким рН и Tween 80 и оставшаяся вирусная инфекционность в течение 60 минут инкубации в образце элюата белка А антитела mAb3 при 16°С и рН 3,97, линия в 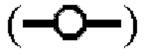 показывает стабильность и титры положительного контроля, линия в
показывает стабильность и титры положительного контроля, линия в  показывает кинетику инактивации X-MuLV и оставшуюся вирусную инфекционность в течение 60 минут инкубации с 0,5% Tween 80; линия в
показывает кинетику инактивации X-MuLV и оставшуюся вирусную инфекционность в течение 60 минут инкубации с 0,5% Tween 80; линия в 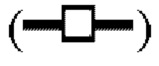 показывает кинетику инактивации X-MuLV и оставшуюся вирусную инфекционность в течение 60 минут инкубации в образце элюата белка А антитела mAb3 при рН 3,97; линия в (
показывает кинетику инактивации X-MuLV и оставшуюся вирусную инфекционность в течение 60 минут инкубации в образце элюата белка А антитела mAb3 при рН 3,97; линия в ( показывает кинетику инактивации X-MuLV и оставшуюся вирусную инфекционность в течение 60 минут инкубации в образце элюата белка А антитела mAb3 при рН 3,97 и в присутствии 0,5% Tween 80. (С) Кинетика инактивации X-MuLV путем двойной обработки низким рН и 0,5% Tween 20 и оставшаяся вирусная инфекционность в течение 60 минут инкубации в образце элюата белка А антитела mAb3 при 16°С и рН 3,97, линия в
показывает кинетику инактивации X-MuLV и оставшуюся вирусную инфекционность в течение 60 минут инкубации в образце элюата белка А антитела mAb3 при рН 3,97 и в присутствии 0,5% Tween 80. (С) Кинетика инактивации X-MuLV путем двойной обработки низким рН и 0,5% Tween 20 и оставшаяся вирусная инфекционность в течение 60 минут инкубации в образце элюата белка А антитела mAb3 при 16°С и рН 3,97, линия в 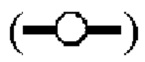 показывает стабильность и титры положительного контроля, линия в
показывает стабильность и титры положительного контроля, линия в 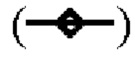 показывает кинетику инактивации X-MuLV и оставшуюся вирусную инфекционность в течение 60 минут инкубации с 0,5% Tween 20; линия в
показывает кинетику инактивации X-MuLV и оставшуюся вирусную инфекционность в течение 60 минут инкубации с 0,5% Tween 20; линия в 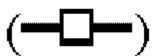 показывает кинетику инактивации X-MuLV и оставшуюся вирусную инфекционность в течение 60 минут инкубации в образце элюата белка А антитела mAb3 при рН 3,97; линия в
показывает кинетику инактивации X-MuLV и оставшуюся вирусную инфекционность в течение 60 минут инкубации в образце элюата белка А антитела mAb3 при рН 3,97; линия в  показывает кинетику инактивации X-MuLV и оставшуюся вирусную инфекционность в течение 60 минут инкубации в образце элюата белка А антитела mAb3 при рН 3,97 и в присутствии 0,5% Tween 20.
показывает кинетику инактивации X-MuLV и оставшуюся вирусную инфекционность в течение 60 минут инкубации в образце элюата белка А антитела mAb3 при рН 3,97 и в присутствии 0,5% Tween 20.
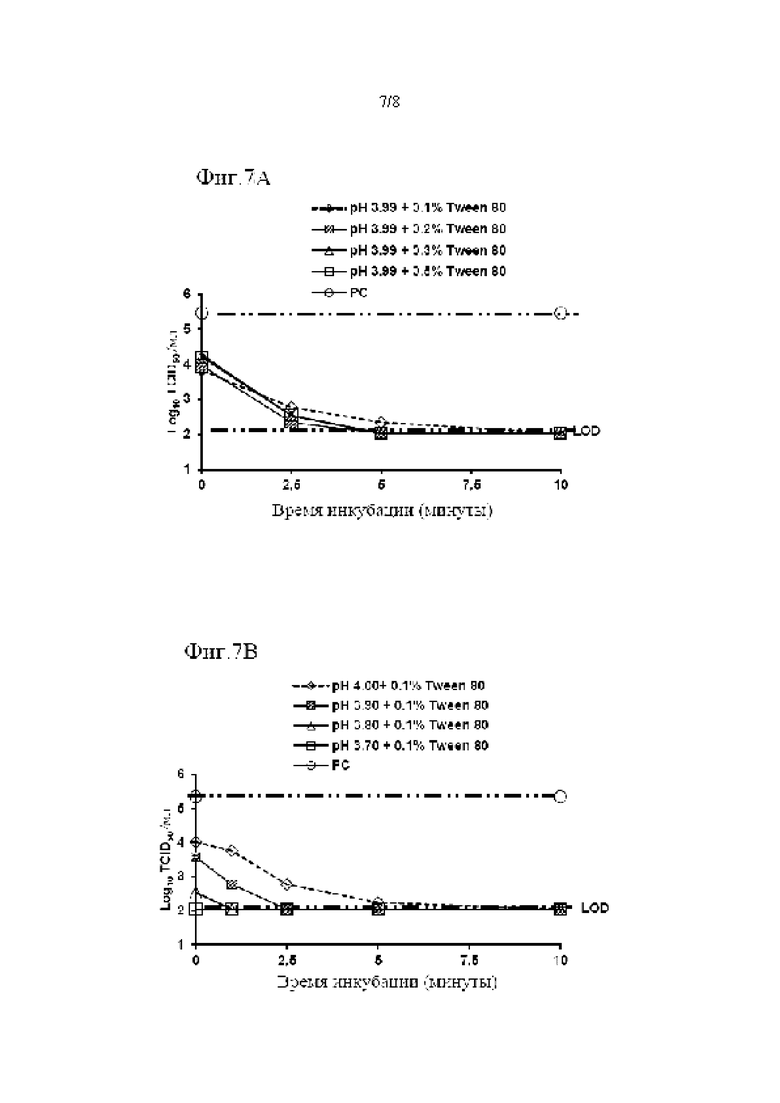
Фиг. 7 показывает эффекты различной концентрации Tween 80 и различных значений рН на двойную обработку для снижения времени, необходимого для инактивации X-MuLV ниже уровня предела обнаружения в образце элюата белка А антитела mAb3. (А) Кинетика инактивации X-MuLV с 0,1%, 0,2%, 0,3% и 0,5% Tween 80 в образце элюата белка А антитела mAb3 при 16°С и рН 3,99. Линия в 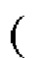
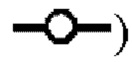 показывает стабильность и титры положительного контроля; линия в
показывает стабильность и титры положительного контроля; линия в 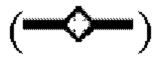 показывает кинетику инактивации X-MuLV в течение 10 минут инкубации в образце элюата белка А антитела mAb3 при рН 3,99, содержащем 0,1% Tween 80; линия в
показывает кинетику инактивации X-MuLV в течение 10 минут инкубации в образце элюата белка А антитела mAb3 при рН 3,99, содержащем 0,1% Tween 80; линия в 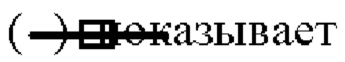 кинетику инактивации X-MuLV в течение 10 минут инкубации в образце элюата белка А антитела mAb3 при рН 3,99, содержащем 0,2% Tween 80; линия в
кинетику инактивации X-MuLV в течение 10 минут инкубации в образце элюата белка А антитела mAb3 при рН 3,99, содержащем 0,2% Tween 80; линия в  показывает кинетику инактивации X-MuLV в течение 10 минут инкубации в образце элюата белка А антитела mAb3 при рН 3,99, содержащем 0,3% Tween 80; линия в
показывает кинетику инактивации X-MuLV в течение 10 минут инкубации в образце элюата белка А антитела mAb3 при рН 3,99, содержащем 0,3% Tween 80; линия в 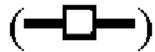 показывает кинетику инактивации X-MuLV в течение 10 минут инкубации в образце элюата белка А антитела mAb3 при рН 3,99, содержащем 0,5% Tween 80. (В) Кинетика инактивации X-MuLV с 0,1% Tween 80 в образце элюата белка А антитела mAb3 при 16°С и при рН 4,00, 3,90, 3,80 и 3,70. Линия в
показывает кинетику инактивации X-MuLV в течение 10 минут инкубации в образце элюата белка А антитела mAb3 при рН 3,99, содержащем 0,5% Tween 80. (В) Кинетика инактивации X-MuLV с 0,1% Tween 80 в образце элюата белка А антитела mAb3 при 16°С и при рН 4,00, 3,90, 3,80 и 3,70. Линия в 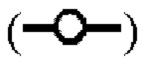 показывает стабильность и титры положительного контроля; линия в
показывает стабильность и титры положительного контроля; линия в  показывает кинетику инактивации X-MuLV в течение 10 минут инкубации в образце элюата белка А антитела mAb3 при рН 4,00, содержащем 0,1% Tween 80; линия в
показывает кинетику инактивации X-MuLV в течение 10 минут инкубации в образце элюата белка А антитела mAb3 при рН 4,00, содержащем 0,1% Tween 80; линия в 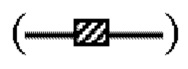 показывает кинетику инактивации X-MuLV в течение 10 минут инкубации в образце элюата белка А антитела mAb3 при рН 3,90, содержащем 0,1% Tween 80; линия в
показывает кинетику инактивации X-MuLV в течение 10 минут инкубации в образце элюата белка А антитела mAb3 при рН 3,90, содержащем 0,1% Tween 80; линия в 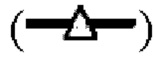 показывает кинетику инактивации X-MuLV в течение 10 минут инкубации в образце элюата белка А антитела mAb3 при рН 3,80, содержащем 0,1% Tween 80; линия в
показывает кинетику инактивации X-MuLV в течение 10 минут инкубации в образце элюата белка А антитела mAb3 при рН 3,80, содержащем 0,1% Tween 80; линия в  показывает кинетику инактивации X-MuLV в течение 10 минут инкубации в образце элюата белка А антитела mAb3 при рН 3,70, содержащем 0,1% Tween 80.
показывает кинетику инактивации X-MuLV в течение 10 минут инкубации в образце элюата белка А антитела mAb3 при рН 3,70, содержащем 0,1% Tween 80.
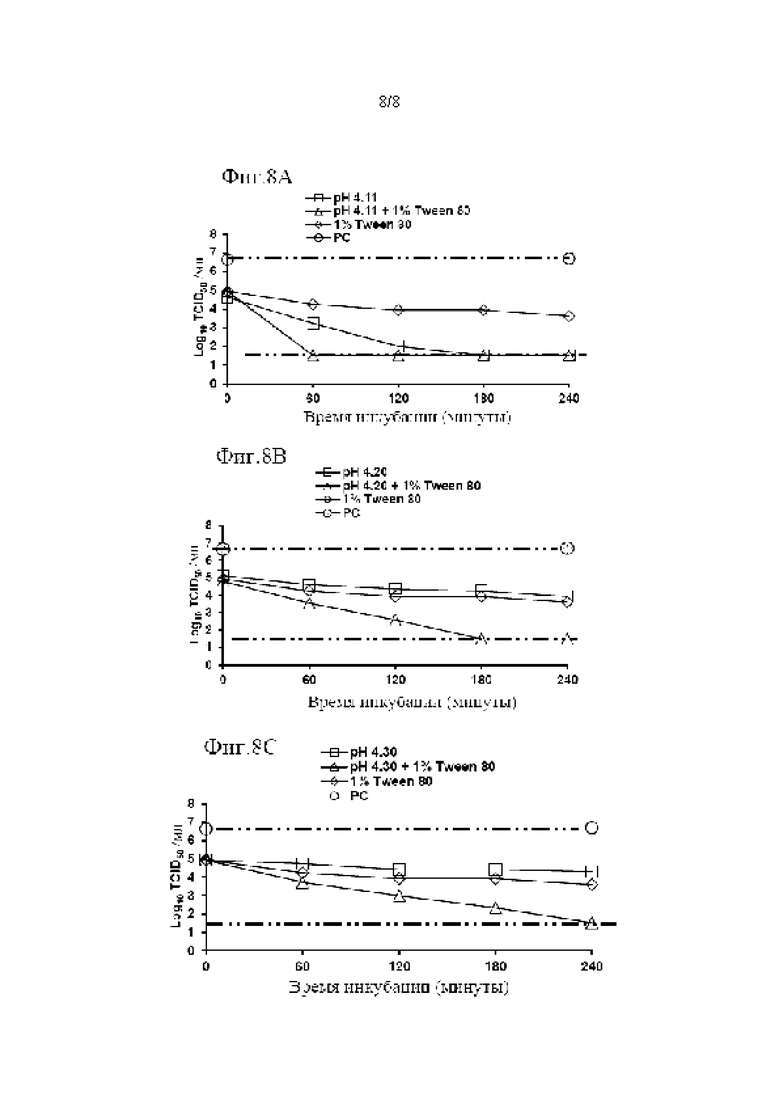
Фиг. 8 показывает, что одновременная обработка низким рН и детергентом может снижать время, необходимое для полной инактивации X-MuLV низким рН, даже при значении рН вплоть до 4,30. (А) Кинетика инактивации X-MuLV с 1% Tween 80 в образце элюата белка А антитела mAb4 при 18°С и рН 4,11. Линия в 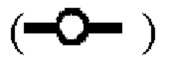 показывает стабильность и титры положительного контроля; линия в
показывает стабильность и титры положительного контроля; линия в 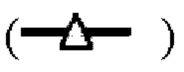 показывает кинетику инактивации X-MuLV в образце элюата белка А антитела mAb4 при рН 4,11, содержащем 1% Tween 80; линия в
показывает кинетику инактивации X-MuLV в образце элюата белка А антитела mAb4 при рН 4,11, содержащем 1% Tween 80; линия в 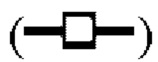 показывает кинетику инактивации X-MuLV в образце элюата белка А антитела mAb4 при рН 4,11; линия в
показывает кинетику инактивации X-MuLV в образце элюата белка А антитела mAb4 при рН 4,11; линия в  показывает кинетику инактивации X-MuLV в образце элюата белка А антитела mAb4 при рН 7,0, содержащем 1% Tween 80; (В) Кинетика инактивации X-MuLV с 1% Tween 80 в образце элюата белка А антитела mAb4 при 18°С и рН 4,20. Линия в
показывает кинетику инактивации X-MuLV в образце элюата белка А антитела mAb4 при рН 7,0, содержащем 1% Tween 80; (В) Кинетика инактивации X-MuLV с 1% Tween 80 в образце элюата белка А антитела mAb4 при 18°С и рН 4,20. Линия в 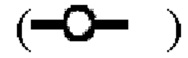 показывает стабильность и титры положительного контроля; линия в
показывает стабильность и титры положительного контроля; линия в 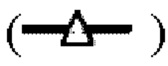 показывает кинетику инактивации X-MuLV в образце элюата белка А антитела mAb4 при рН 4,20, содержащем 1% Tween 80; линия в
показывает кинетику инактивации X-MuLV в образце элюата белка А антитела mAb4 при рН 4,20, содержащем 1% Tween 80; линия в 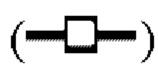 показывает кинетику инактивации X-MuLV в образце элюата белка А антитела mAb4 при рН 4,20; линия в
показывает кинетику инактивации X-MuLV в образце элюата белка А антитела mAb4 при рН 4,20; линия в  показывает кинетику инактивации X-MuLV в образце элюата белка А антитела mAb4 при рН 7,0, содержащем 1% Tween 80; (С) Кинетика инактивации X-MuLV с 1% Tween 80 в образце элюата белка А антитела mAb4 при 18°С и рН 4,30. Линия в
показывает кинетику инактивации X-MuLV в образце элюата белка А антитела mAb4 при рН 7,0, содержащем 1% Tween 80; (С) Кинетика инактивации X-MuLV с 1% Tween 80 в образце элюата белка А антитела mAb4 при 18°С и рН 4,30. Линия в 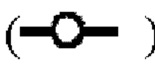 показывает стабильность и титры положительного контроля; линия в
показывает стабильность и титры положительного контроля; линия в 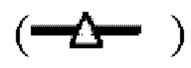 показывает кинетику инактивации X-MuLV в образце элюата белка А антитела mAb4 при рН 4,30, содержащем 1% Tween 80; линия в
показывает кинетику инактивации X-MuLV в образце элюата белка А антитела mAb4 при рН 4,30, содержащем 1% Tween 80; линия в 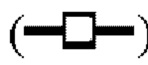 показывает кинетику инактивации X-MuLV в образце элюата белка А антитела mAb4 при рН 4,30; линия в
показывает кинетику инактивации X-MuLV в образце элюата белка А антитела mAb4 при рН 4,30; линия в 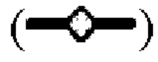 показывает кинетику инактивации X-MuLV в образце элюата белка А антитела mAb4 при рН 7,0, содержащем 1% Tween 80.
показывает кинетику инактивации X-MuLV в образце элюата белка А антитела mAb4 при рН 7,0, содержащем 1% Tween 80.
Подробное описание
Настоящее изобретение относится к способам и композициям, которые относятся к инактивации вируса.
Определения
В целях интерпретации настоящего описания будут применяться следующие определения. В случае, если любое из приведенных ниже определений вступает в противоречие с использованием этого термина в любом другом документе, включая любой документ, включенный в настоящий документ посредством ссылки, определение, изложенное ниже, всегда будет интерпретироваться в контексте настоящего изобретения и связанных с ним пунктов формулы изобретения, если явно не подразумевается противоположное значение (например, в документе, где термин первоначально использовался).
При необходимости термины, используемые в единственном числе, также включают множественное число и наоборот. Использование формы единственного числа в настоящем документе означает «один или более», если не указано иное, или если использование «одного или более» явно неуместно. Использование «или» означает «и/или», если не указано иное. Использование «содержат», «содержит», «содержащий», «включают», «включает» и «включающий» является взаимозаменяемым и не является ограничивающим. Термины «такие как», «например» и «в качестве примера» также не предназначены для ограничения. Например, термин «включая» означает «включая, но без ограничения».
Как применяется в настоящем документе, термин "около" относится к +/- 10% от единичного приведенного значения.
Как применяется в настоящем документе, термин «по существу» относится к качественному условию проявления полной или приблизительной степени характеристики или свойства, представляющего интерес. Специалисту в биологической области техники понятно, что биологические и химические явления редко, если вообще когда-либо достигают или избегают абсолютного результата из-за множества переменных, которые влияют на испытания, производство и хранение биологических и химических композиций и материалов, а также из-за ошибки, присущей инструментам и оборудованию, используемым при испытаниях, производстве и хранении биологических и химических композиций и материалов. Поэтому термин «по существу» используется в настоящем документе для обозначения потенциального недостатка полноты, присущей многим биологическим и химическим явлениям.
В контексте настоящего изобретения термин «ортогональный» относится к отдельным идентифицируемым стадиям или способам, которые используют отдельный механизм для удаления/инактивации вирусов. Что касается разработки способа, это обычно означает, что в процедурах многоступенчатой очистки должны использоваться механизмы разделения, которые отличаются друг от друга; каждая стадия представляет ось в пространстве прямоугольных координат. Двухстадийный способ с использованием анионообменной хроматографии и хроматографии гидрофобного взаимодействия (HIC) следует понимать как ортогональный.
С 1980-х годов детергенты использовались в качестве основного инструмента для инактивации вирусов в объединенной крови, собранной у доноров крови. Этот процесс важен для безопасности пациентов, получающих кровь, плазму или компоненты, полученные из крови/плазмы, такие как фактор VIII, полученный из плазмы (pdFVIII). Кроме того, это средство очистки повышает безопасность персонала, непосредственно участвующего в обработке крови в клинических лабораториях или на объектах производства биологических продуктов, получаемых из плазмы (PDBP). Совсем недавно эта практика стала неотъемлемой частью процесса производства биофармацевтических лекарственных средств для биологических терапевтических средств или вакцин, содержащих материалы животного происхождения. Материалы животного происхождения (то есть кровь, плазма, ткани и белки, продуцируемые в клетках млекопитающих) могут нести эндогенные вирусы или могут легко загрязняться занесенными вирусами. Таким образом, процесс производства лекарственного средства включает ряд мер эффективной инактивации вируса (т.е. растворитель-детергент, низкое значение рН и тепловые обработки) и методик удаления (т.е. фильтрации вируса), чтобы гарантировать пациентам свободные от вируса биотерапевтические продукты. Эти процессы жизненно важны для безопасности терапевтических или вакцинных продуктов биологического происхождения. Новые способы повышения эффективности, надежности и, что самое главное, общей безопасности этих продуктов крайне необходимы.
Типы детергентов
Детергенты представляют собой амфифильные молекулы, которые состоят из гидрофильной (полярной) головной группы и гидрофобной (неполярной) хвостовой группы. Эта универсальная структура позволяет детергентам взаимодействовать с другими молекулами, особенно с белками или оболочечными вирусами в водном растворе. В фундаментальной науке и прикладных технологиях детергенты могут использоваться в качестве солюбилизирующего агента или в качестве стабилизирующего агента для предотвращения агрегации биологической молекулы или для солюбилизации мембранных белков из клеточных культур или тканевых суспензий. При использовании для солюбилизации белков следующие свойства делают некоторые детергенты более желательными, чем другие: 1) Детергенты, в которых отсутствуют заряды (неионные детергенты), помогают сохранить структуру и активность представляющего интерес белка, 2) детергенты с низкой критической концентрацией мицеллообразования (CMC) позволяют легко удалять детергент с помощью диализа, 3) детергенты, которые являются прозрачными и, следовательно, не влияют на показания поглощения белка, и 4) детергенты, которые являются весьма чистыми, уменьшая изменчивость от эксперимента к эксперименту. Аналогичным образом, большинство из этих свойств применимы при выборе кандидатов детергента для инактивации вируса, поскольку необходимо не разрушать белковое лекарственное средство, определять концентрацию белка без вмешательства детергента и обеспечивать высокую чистоту детергента, чтобы инактивация вируса происходила последовательно.
В общем, инактивация оболочечного вируса зависит от амфифильной структуры и критической концентрации мицеллообразования (CMC) конкретного детергента. CMC относится к концентрации, при которой детергентные мономеры агрегируют с образованием мицеллярных структур. В водных растворах, когда все больше детергентных мономеров вступают в контакт, гидрофильные головки могут примыкать, чтобы защитить гидрофобные хвосты от водного раствора, в конечном счете, превращаясь в структуры мицелл. CMC, вероятно, связана с концентрацией, при которой инактивация вируса будет происходить для данного детергента при определенных условиях. Теоретический механизм инактивации вируса заключается в том, что мономеры внедряются в вирусную оболочку при концентрации ниже CMC детергента, что может быть вредным для вируса. Как только концентрация достигает или превышает CMC, эти детергентные мономеры, присутствующие в мембране, образуют мицеллы, которые могут нарушить целостность или полностью разрушить вирусную оболочку. Без вирусной оболочки вирус не способен связываться со своим рецептором на плазматической мембране клеток-хозяев и облегчать его репликацию и распространение. Детергенты представляют собой амфифильные молекулы, которые состоят из гидрофильной (полярной) головной группы и гидрофобной (неполярной) хвостовой группы. Эта универсальная структура позволяет детергентам взаимодействовать с другими молекулами, особенно с белками или оболочечными вирусами в водном растворе. В фундаментальной науке и прикладных технологиях детергенты могут использоваться в качестве солюбилизирующего агента или в качестве стабилизирующего агента для предотвращения агрегации биологической молекулы или для солюбилизации мембранных белков из клеточных культур или тканевых суспензий. При использовании для солюбилизации белков следующие свойства делают некоторые детергенты более желательными, чем другие: 1) Детергенты, в которых отсутствуют заряды (неионные детергенты), помогают сохранить структуру и активность представляющего интерес белка, 2) детергенты с низкой критической концентрацией мицеллообразования (CMC) позволяют легко удалять детергент с помощью диализа, 3) детергенты, которые являются прозрачными и, следовательно, не влияют на показания поглощения белка, и 4) детергенты, которые являются весьма чистыми, уменьшая изменчивость от эксперимента к эксперименту. Аналогичным образом, большинство из этих свойств применимы при выборе кандидатов детергента для инактивации вируса, поскольку необходимо не разрушать белковое лекарственное средство, определять концентрацию белка без вмешательства детергента и обеспечивать высокую чистоту детергента, чтобы инактивация вируса происходила последовательно.
В общем, инактивация оболочечного вируса зависит от амфифильной структуры и критической концентрации мицеллообразования (CMC) конкретного детергента. CMC относится к концентрации, при которой детергентные мономеры агрегируют с образованием мицеллярных структур. В водных растворах, когда все больше детергентных мономеров вступают в контакт, гидрофильные головки могут примыкать, чтобы защитить гидрофобные хвосты от водного раствора, в конечном счете, превращаясь в структуры мицелл. CMC, вероятно, связана с концентрацией, при которой инактивация вируса будет происходить для данного детергента при определенных условиях. Теоретический механизм инактивации вируса заключается в том, что мономеры внедряются в вирусную оболочку при концентрации ниже CMC детергента, что может быть вредным для вируса. Как только концентрация достигает или превышает CMC, эти детергентные мономеры, присутствующие в мембране, образуют мицеллы, которые могут нарушить целостность или полностью разрушить вирусную оболочку. Без вирусной оболочки вирус не способен связываться со своим рецептором на плазматической мембране клеток-хозяев и облегчать его репликацию и распространение.
До сих пор промышленность, производящая биотерапевтические средства, использовала несколько детергентов для инактивации вирусов в оболочке. Один из популярных неионных детергентов Triton Х-100 эффективен при инактивации вирусов в оболочке без нарушения белкового лекарственного средства. После использования Triton Х-100 в процессах производства биофармацевтических средств он удаляется на установки обработки сточных вод или высвобождается непосредственно в водную среду (Madsen et al., 1996, JAOCS, 73: 929-933). К сожалению, побочный продукт Triton Х-100 содержит октилфенол, который признан токсичным химическим веществом для окружающей среды рядом стран. Многие биофармацевтические отрасли были направлены на поиск экологически безопасных детергентов, эффективность которых сопоставима с Triton Х-100. Например, некоторые компании рассматривали лаурилдиметиламин N-оксид (LDAO) и алкилглюкозиды, соответственно (Conley et al., 2014, Патент США №WO2014025771А2; Conley et al., 2016, Biotechnol. Bioeng., Epub ahead of print; Fisher et al., 2016, патент США №20160333046A1). Хотя этим компаниям удалось выделить новые детергенты разных классов, варианты осуществления настоящего изобретения определяют совершенно новый и высокоэффективный класс неионных детергентов для инактивации вирусов в оболочке.
Детергенты на основе сахара обладают превосходными физическими свойствами, являются весьма биоразлагаемыми и не токсичны, что способствует их профилю безопасности, особенно для водной среды (Bogdan, 2007, Stalmans et al., 1993). Таким образом, раскрытые варианты осуществления направлены на использование детергентов на основе сахара, N-метилглюкамиды, в качестве нового способа инактивации вирусов при производстве биологически активных лекарственных средств. N-метилглюкамиды являются неионными детергентами, которые состоят из высокогидрофильного глюкозного фрагмента и гидрофобной цепи жирной кислоты, связанных амидной связью. Эти детергенты являются экологически безопасными, так как они, как известно, являются весьма биоразлагаемыми с примерно 95-ным индексом возобновляемого углерода и считаются нетоксичными, особенно для водных организмов (Stalmans et al., 1993, SOFW, 119: 794-808).
Mega-10 представляет собой неионный детергент на основе сахара, который состоит из высокогидрофильного фрагмента глюкозы и цепи гидрофобной жирной кислоты, связанных амидной связью, что делает его высоко биоразлагаемым с индексом возобновляемого углерода около 95% и без токсичности для водной среды (Burczyk, В., Wilk, К.A., Sokolowski, A., and Syper, L., 2001) (Foley, P., Pour, A.K., Beach, E.S., and Zimmerman, J.B., 2012). Кроме того, впервые было обнаружено, что двойная обработка низким рН в присутствии детергента, такого как Mega-10 или Tween 80 или Tween 20, может иметь синергетический эффект в отношении снижения вирусной инфекционности и времени, необходимого для эффективной инактивации ретровирусов. Эти двойные механизмы инактивации вируса могут иметь потенциальную полезу при вирусной инактивации моноклональных антител, получаемых путем непрерывной обработки.
Вирусы, бели и детергенты
Модельным вирусом в оболочке, используемым для оценки инактивации вируса, был ксенотропный вирус лейкемии мышей (X-MuLV), который был приобретен у BioReliance (Rockvile, MD). X-MuLV был выбран в качестве специфического модельного вируса для исследований инактивации низким рН и детергентом, поскольку он подобен эндогенным ретровирусоподобным частицам (ERLP), обычно обнаруживаемые при производстве культур млекопитающих.
Модельные белки, образец mAb1 (IgG1), образец mAb2 (IgG1) и образец mAb3 (IgG2) собирали в виде пулов элюата колонки для аффинной хроматографии с белком А после осветления соответствующей клеточной культуры. Значения изоэлектрической точки (pI) этих mAb составляли 8,9, 7,1 и 7,7 соответственно.
N-Метилглюкамид (Мега-10), Tween 20 и Tween 80 были приобретены у Sigma-Aldrich (Сент-Луис, Миссури). 5% сток-раствор Mega-10 (мас./об.) получали путем растворения 0,5 грамм порошка Mega-10 в 10 мл воды Milli-Q. Сток-раствор детергента Tween 20 или Tween 80 получали с использованием воды Milli-Q при концентрации 5% (мае./об.).
Эксперименты по инактивации вируса
Инактивация вируса детергентами
Значение рН различных элюатов белка А доводили до 7,0 с помощью 1 М Трис-буфера. Затем элюат с установленным значением рН фильтровали через фильтр 0,22 мкм. К отфильтрованным нейтрализованным элюатам белка А добавляли различные объемы 5% сток-раствора Mega-10, Tween 20 или Tween 80. Эти операции проводили для получения элюатов белка А, содержащих различные концентрации каждого детергента. Затем X-MuLV добавляли при соотношении 1:20 к нейтрализованному элюату белка А, содержащему различные концентрации каждого детергента, который был предварительно инкубирован на водяной бане при 16°С перед добавлением вируса. После тщательного перемешивания аликвоту образца немедленно удаляли и гасили разбавителем (среда Мак-Коя, содержащая 3 мкг/мл полибрена) при соотношении 1:12 для Mega-10 или 1: 100 для Tween 20 и Tween 80, чтобы остановить инактивацию, и образец обозначали как эталон нулевого времени. Оставшийся элюат с добавками возвращали на водяную баню, и образцы собирали в указанное время для оценки кинетики инактивации вируса.
Инактивация вируса низким рН
Значение рН элюатов белка А антитела mAb1, mAb2 и mAb3 доводили до 3,91, 4,05 или 3,97 с помощью 1М уксусной кислоты. Затем элюат с установленным значением рН фильтровали через фильтр 0,22 мкм. Отфильтрованные элюаты белка А предварительно инкубировали на водяной бане при 16°С перед добавлением X-MuLV при соотношении 1:20. После тщательного перемешивания аликвоту образца немедленно удаляли и нейтрализовали 1 М Трис-буфером для гашения инактивации, и его обозначали как эталон нулевого времени. Оставшиеся элюаты с добавками возвращали в водяную баню, и образцы собирали в указанное время для оценки кинетики инактивации вируса.
Двойная инактивация вируса низким рН и детергентом
Значение рН элюатов белка А антитела mAb1, mAb2 и mAb3 доводили до 3,91, 4,05 или 3,97 с помощью 1М уксусной кислоты. Затем элюат с установленным значением рН фильтровали через фильтр 0,22 мкм. Различные объемы 5% сток-раствора детергента затем добавляли в отфильтрованные элюаты белка А. Элюаты белка А с низким рН, содержащие Mega-10, Tween 80 или Tween 20, предварительно инкубировали на водяной бане при 16°С перед добавлением X-MuLV при соотношении 1:20. После тщательного перемешивания аликвоту образца немедленно удаляли и нейтрализовали 1 М Трис-буфером, чтобы остановить инактивацию вируса низким рН, затем немедленно гасили разбавителем при соотношении 1:12 для Mega-10 или 1: 100 для Tween 20 и Tween 80, чтобы остановить инактивацию вируса детергентом. Собранный образец был обозначен как эталон нулевого времени. Оставшийся элюат с добавками возвращали на водяную баню, и образцы собирали в указанное время для оценки кинетики инактивации вируса.
Анализ инфекционности X-MuLV на основе клеток
Оставшуюся инфекционность X-MuLV в образцах после инактивационной обработки определяли с помощью анализа TCID50, который представляет собой анализ разведения конечной точки для количественного определения количества вируса, необходимого для получения цитопатического эффекта в 50% клетках инокулированной тканевой культуры. Титры вирусов оценивали с использованием метода Спирмана-Кербера и выражали как ТСID50/мл с рассчитанным 95% доверительным интервалом (CI). Вкратце, достаточное количество 96-луночных планшетов с клетками PG-4 (кошачьи S+L-, ATCC#CRL-2032) готовили за день до начала экспериментов по инактивации вирусов и инкубировали в течение ночи в инкубаторе с СО2 и увлажнением при 37°С. Набор из десяти 3,2-кратных разведений разведенного положительного контроля (1:100) и образцы инактивированного вируса получали в узле разбавления. Каждый набор из 11 серийных разведений образцов соответственно засеивали в лунки (100 мкл на лунку) первых 11 колонок 96-луночного планшета, который был предварительно засеян клетками PG-4. 12-ую колонку в том же планшете была засеивали соответствующим разбавителем, чтобы она служила в качестве невирусного отрицательного контроля. Положительный контроль получали путем добавления X-MuLV в отфильтрованный нейтрализованный элюат белка А при соотношении 1:20. Затем инокулированные планшеты инкубировали в инкубаторе с СO2 и увлажнением при 37°С в течение приблизительно 2 часов. В конце инкубации в каждую лунку планшетов добавляли 100 мкл среды для 2Х анализа (92% среды Мак-Коя 5А, 4% FBS, 2% пенициллина/стрептомицина, 2% L-глутамина). Затем планшеты возвращали в тот же инкубатор и продолжали инкубацию в течение 6 дней. Каждую лунку планшетов оценивали под микроскопом на наличие цитопатического эффекта (СРЕ), и результаты записывали в таблице оценок. Затем титры вирусов оценивали с использованием метода Спирмана-Кербера и представляли как ТСID50/мл с рассчитанным 95% доверительным интервалом (CI).
Надежность инактивации X-MuLV с помощью Mega-10 в элюатах белка А антитела mAb
Для оценки надежности инактивации X-MuLV с помощью Mega-10 в элюатах белка А антитела mAb1, X-MuLV добавляли при соотношении 1:20 в нейтрализованный элюат белка А антитела mAb1, содержащий 0,1%, 0,2% и 0,3% Mega-10. После тщательного перемешивания аликвоту образца удаляли в момент времени 0, 2,5, 5, 10 и 30 минутах после инкубации при 16°С. Остающийся титр вируса в собранных образцах определяли с помощью анализа TCID50. Результаты анализа TCID50 показали, что Mega-10 при концентрации 0,2% и 0,3% быстро инактивировал X-MuLV до уровня ниже предела обнаружения после обработки в течение 2,5 минут (Фиг. 1А) и обеспечивал значения LRF≥5,58±0,19 и ≥5,58±0,19. соответственно (таблица 1А).
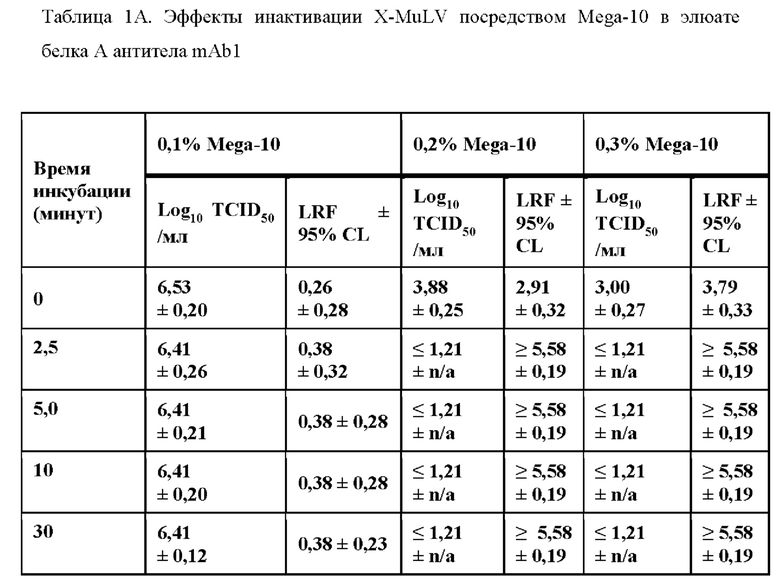
Эффективность детергента Mega-10 по инактивации вирусов также оценивали на элюатах белка А второго продукта mAb, образце mAb2. Аналогичные эффекты инактивации вируса наблюдались, когда X-MuLV инкубировали с нейтрализованным элюатом белка А антитела mAb2, содержащим 0,1%, 0,15%, 0,2% и 0,3% Mega-10 (Фиг. 1 В). Было показано, что Mega-10 при концентрации 0,3% быстро инактивирует X-MuLV до уровня ниже предела обнаружения после обработки в течение 2,5 минут и обеспечивает значения LRF≥5,81±0,18 (таблица 1В). Значительная инактивация вируса также была достигнута с помощью 0,2% Mega-10 после 2,5 минут обработки с LRF 5,31±0,75 (таблица 1В).
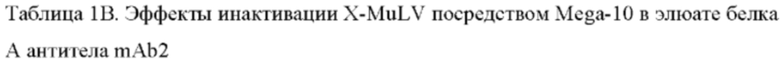
Синергетические эффекты двойной обработки низким рН и Mega-10 на снижение инфекционности X-MuLV
Механизм, используемый детергентами для инактивации вирусов в оболочке, относят к взаимодействию детергента с липидной мембраной вируса в оболочке. Взаимодействие разрушает мембраны и вызывает распад вирусных капсидных белков, что, в свою очередь, предотвращает связывание вируса в оболочке с клетками, что приводит к потере инфекционности вируса (Pamphilon, 2000) (Kempf, С., Stucki, М., and Boschetti, N., 2007). С другой стороны, полагают, что инактивация вируса, опосредованная низким рН, действует через другой механизм. Среда с низким рН вызывает изменения морфологии вируса, приводящие к агрегации вирусных частиц, которая рассматривается как механизм инактивации вирусов низким рН (Gaudin, Y., Ruigrok, R., Knossow, M., and Flamand, A., 1993).
Поскольку механизмы, лежащие в основе инактивации вирусов в оболочке детергентом и низким рН, сильно различаются, было бы нелогично или неочевидно комбинировать эти способы обработки вместе.
Инактивацию X-MuLV проводили в условиях, которые были неоптимальными как для опосредованной низким рН, так и для опосредованной детергентом инактивации вируса. Неожиданным образом синергетический эффект на снижение инфекционности X-MuLV наблюдался, когда X-MuLV инкубировали с образцом элюата белка А антитела mAb1, содержащим 0,1% Mega-10, при рН 3,91 (Фиг. 2 в таблице 2). После инкубации в течение 2,5 минут образцы 0,1% Mega-10 не показали эффекта на инактивацию X-MuLV и вызвали LRF 0,33±0,29. Обработка только рН 3,91 сама по себе вызывала умеренное снижение вирусной инфекционности с LRF 2,60±0,33 после того же времени инкубации. Неожиданным образом двойная обработка 0,1% Mega-10 и рН 3,91 эффективно инактивировала X-MuLV до уровня ниже предела обнаружения и приводила к LRF≥5,40±0,21 после того же времени инкубации. Подобные эффекты также наблюдались, когда инактивацию X-MuLV проводили в образце элюата белка А антитела mAb2, содержащем 0,15% Mega-10, при рН 4,05 (Фиг. 3 и Таблица 3).
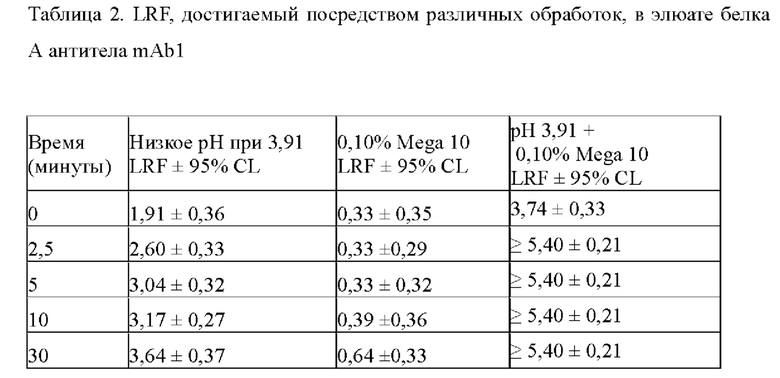
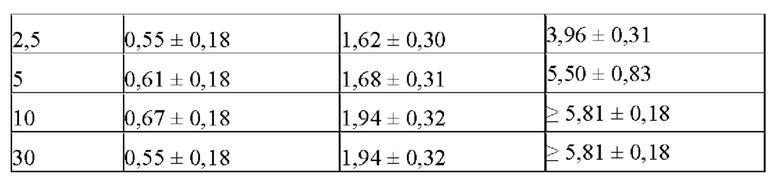
После 5 минут инкубации только 0,15% Mega-10 привел к LRF только 1,68±0,31, а обработка только рН 4,05 привела к LRF 0,61±0,18. Однако двойная обработка 0,15% Mega-10 и рН 4,05 привела к LRF 5,50±0,83, что было намного больше, чем сумма их индивидуальных эффектов. Следовательно, можно предположить, что обработка элюата белка А низким рН в присутствии детергента оказывает синергетический эффект на снижение инфекционности вируса в оболочке из-за двойных ортогональных механизмов инактивации вируса.
Синергетические эффекты двойной обработки низким рН и детергентом на сокращение времени, необходимого для инактивации X-MuLV о уровня ниже предела обнаружения
В дополнение к синергетическим эффектам двойной обработки низким рН и Mega-10 на уменьшение инфекционности X-MuLV, также наблюдали синергетические эффекты одновременной обработки низким рН и Mega-10 на сокращение продолжительности времени, необходимого для инактивации X-MuLV до уровня ниже предела обнаружения или полностью неактивного X-MuLV. Как показано на Фиг. 4А, требовалось 240 минут для инактивации X-MuLV до уровня ниже предела обнаружения, когда образец элюата белка А антитела mAb1 инкубировали при рН 3,91 и 18°С (FIG. 4А). Неожиданным образом, потребовалось только 2,5 минуты для инактивации X-MuLV до уровня ниже предела обнаружения после инкубации того же элюата белка А при рН 3,91 в присутствии еще 0,1% Mega-10 при температуре 16 С (FIG. 4В). Подобным образом, двойная обработка X-MuLV в образце другого mAb, элюат белка А антитела mAb2, содержащий 0,15% Mega-10 при рН 4,05 и температуре 16 С, также была способна снижать время, необходимое для инактивации X-MuLV до уровня ниже предела обнаружения, от 120 минут инкубации при более низком рН (рН 4,0) и более высокой температуре (18°С) (Фиг. 4С) до только 10 минут (Фиг. 4D).
Также было исследовано ограничены ли синергетические эффекты двойной обработки на инактивацию вируса только детергентом Mega-10. Эксперименты проводили для инактивации X-MuLV при низком рН в присутствии других неионных детергентов, таких как Tween 80 или Tween 20. Двойная обработка X-MuLV в элюатах белка А антитела mAb2, содержащих 0,5% Tween 80, при рН 4,05 и температуре 16 С, также была способна снижать время, необходимое для инактивации X-MuLV до уровня ниже предела обнаружения, от 120 минут инкубации при рН 4,0 и более высокой температуре (18°С) (Фиг. 5А) до 10 минут (FIG. 5 В). Подобные синергетические эффекты также наблюдались при проведении двойной инактивации вируса в элюате белка А другого подтипа антитела mAb3 (IgG2), содержащем 0,5% Tween 80 (Фиг. 6 В) или 0,5%Tween 20 (Фиг. 6С) при рН 3,97. В любом случае время инкубации, необходимое для инактивации X-MuLV до уровня ниже предела обнаружения, было сокращено от 120 минут посредством обработки только низким рН (фиг. 6А) до 5 минут (Фиг. 6В и 6С).
Также продемонстрировали, что добавления минимальной концентрации 0,2% Tween 80 к элюату белка А при рН 3,99 является достаточным для сокращения необходимого времени инактивации о 120 до 5 минут, и дальнейшего сокращения времени не наблюдалось, пока концентрация Tween 80 не была увеличена до 0,3% или 0,5% (Фиг. 7А). С другой стороны, время, необходимое для инактивации X-MuLV, было сокращено от 10 минут до 2,5 минут, 1 минуты, а затем 0 минут, соответственно, когда значение рН элюата белка А антитела mAb3, содержащего 0,1% Tween 80, снижалось от 4,0 до 3,9, 3,8, а затем 3,7 (Фиг. 7 В). Таким образом, время, необходимое для инактивации X-MuLV путем одновременной двойной обработки, уменьшается по мере увеличения концентрации детергента и уменьшения значения рН элюата белка А. Кроме того, минимальная эффективная концентрация Tween 80, необходимая для двойной обработки, зависит от рН, более низкая минимальная эффективная концентрация необходима для более низкого значения рН.
Также продемонстрировали, что одновременная обработка низким рН и детергентом может сократить время, необходимое для полной инактивации X-MuLV с помощью низкого рН, даже при значении рН, равном 4,30. Элюат белка А антитела mAb4 при рН 4,11, 4,20 или 4,30, содержащий 1% Tween 80, был способен полностью инактивировать X-MuLV, соответственно, через 1, 3 или 4 часа обработки, что позволяет проводить стадию инактивации вируса низким рН при производстве антител без какой-либо корректировки рН для значения рН элюата белка А ниже 4,30 с 1% Tween 80 или вплоть до рН 4,50 с Tween 20 или Triton Х-100. В настоящее время инактивацию вирусов низким рН проводят при рН от 3,70 до 3,90 путем регулирования значения рН элюата белка А, обычно до значения рН от 4,10 до 4,50. Таким образом, проведение инактивации вирусов низким рН без корректировки рН элюата белка А может сделать процесс очистки антител более быстрым и более эффективным (Фиг. 8).
Как уже отмечено, варианты осуществления настоящего изобретения демонстрируют, что экологически безопасный детергент, Mega-10, может эффективно инактивировать модельный вирус в оболочке, X-MuLV, при низкой концентрации в нейтрализованном элюате белка А моноклональных антител. Таким образом, инактивация вируса детергентом для вирусов в оболочке с помощью Mega-10 может быть включена в процесс производства моноклональных антител в качестве надежной стадии инактивации вируса после инактивации вируса низким рН. Для достижения LRF≥4,0 инактивации ретровирусов на осветленном, бесклеточном промежуточном соединении mAb или слитого белка Fc и IgG при рН 6,0-8,0, необходимы концентрация Triton X-100≥0,5% и время выдержки ≥60 минут при температуре 15-25°С, но с Mega-10 LRF>5,81 инактивации вируса в нейтрализованном элюате белка А (рН 7,0) моноклональных антител может быть достигнут при концентрация 0,2% после выдержки 30 минут при 16°С. Следовательно, Mega-10 может быть жизнеспособной альтернативой для Triton Х-100 для использования в качестве детергента для инактивации вирусов при производстве моноклональных антител, поскольку Mega-10 более эффективен, чем Triton Х-100 при инактивации ретровирусов, и обладает высокой биоразлагаемостью и не токсичен для водной среды.
Также впервые наблюдали, что одновременная двойная обработка низким рН и детергентом, таким как Mega-10, или Tween 80, или Tween 20, может иметь синергетический эффект в отношении снижения вирусной инфекционности и времени, необходимого для эффективной инактивации ретровирусов. Например, обработка X-MuLV в течение 2,5 минут с 0,1% Mega-10, присутствующем в нейтрализованном элюате белка А образца, или с рН 3,91 элюата белка А, приводила к LRF 0,33±0,29 и 2,50±0,33, соответственно. Двойная обработка X-MuLV с 0,1% Mega-10 в присутствии элюата белка А с рН 3,91 (одновременная обработка низким рН и детергентом) в течение 2,5 минут эффективно инактивировала X-MuLV до уровня ниже предела обнаружения и приводила к LRF≥5,40±0,21. Подобные эффекты также наблюдали, когда инактивацию X-MuLV проводили в образце элюата белка А при рН 4,05, содержащем 0,15% Mega-10. В то время как 5-ти минутная обработка X-MuLV с 0,15% Mega-10, присутствующим в нейтрализованном элюате белка А, или с рН 4,05 элюата белка А, приводила к LRF 1,68±0,31 и 0,61±0,18, соответственно. Двойная обработка X-MuLV с 0,15% Mega-10 в присутствии элюата белка А с рН 4,05 (одновременная обработка низким рН и детергентом) приводила к LRF 5,50±0,83, что было намного больше, чем сумма их индивидуальных эффектов. Наблюдаемый синергетический эффект двойной обработки Mega-10 и низким рН объясняется различными механизмами, используемыми при обработке детергентом или низким рН для инактивации вирусов в оболочке. Кроме того, одновременная двойная обработка детергентом и низким рН оказывает синергетический эффект не только на снижение вирусной инфекционности, но также оказывает синергетический эффект на сокращение времени, необходимого для инактивации вирусов в оболочке. Наблюдали, что двойная обработка элюатом белка А с низким рН в присутствии детергента, такого как Mega-10 или Tween-80 или Tween 20, может сократить время, необходимое для инактивации X-MuLV до уровня ниже предела обнаружения, от 1-2 часов, необходимое при обработке только низким рН, до 2,5-10 минут при двойной обработке. Синергетические эффекты одновременной обработки низким рН и детергентом на сокращение времени, необходимого для достижения LRF≥5,0 при обработке низким рН, от≥120 минут при рН≥3,90 при 16°С до менее 10 минут, будут иметь потенциал применения для инактивации ретровирусов в оде производства моноклональных антител посредством непрерывной обработки.
Благодаря ее низкой стоимости, меньшим капиталовложениям, большей гибкости, большему контролю процесса, простоте масштабирования и лучшему качеству продукции непрерывная обработка стала более распространенной среди биофармацевтических компаний. Биофармацевтическая промышленность проявляет растущий интерес к переходу от работы в периодическом режиме к непрерывному производству, чтобы удовлетворить будущие потребности биофармацевтической промышленности. Рынок биофармацевтических средств, особенно биотерапевтических продуктов на основе антител, резко изменился за последнее десятилетие, поскольку скоро истекает срок действия патентов на более чем 20 биопрепаратов-блокбастеров первого поколения. Следовательно, существует потребность в рентабельных производственных процессах, которые могут гибко переключать производство для различных биотерапевтических продуктов, стабильных или нестабильных, в разных объемах. Производственный процесс считается полностью непрерывным, если он состоит из интегрированных (физически связанных) непрерывных узлов с нулевым или минимальным промежуточным объемом. В настоящее время почти все узлы стандартного производства моноклональных антител находятся в режиме готовности к непрерывной обработке, за исключением стадии инактивации вируса при низком рН, которая в настоящее время выполняется в периодическом процессе. Как правило, объединенный элюат стадии захвата колонкой для аффинной хроматографии с белком А доводят до желаемого значения рН и выдерживают в сосуде или мешке в течение требуемого времени инактивации 60-120 минут, в зависимости от параметров процесса. Как правило, чем выше рН, тем более длительное время инактивации требуется и будут более высокие потери продукта из-за агрегации антител. Это представляет собой проблему при адаптации к непрерывному процессу. Важной концепцией при преобразовании существующей в настоящее время инактивации вирусов низким рН в периодическом процессе в непрерывный процесс является обеспечение того, чтобы время инактивации вирусов в проточном режиме было таким же точным и контролируемым, как и в периодическом режиме. Чтобы обеспечить типичное время пребывания (1-2 часа) для инактивации вируса при низком рН и скорости потока элюатов белка А непрерывной хроматографии (50-300 л/ч), а также большое число объединенных элюатов, необходима очень длинная и узкая труба для разработки узла для непрерывной инактивации вирусов при низком рН. Однако необходимо отметить, что такой узел создаст высокое противодавление и широкое распределение времени пребывания, вызывая существенное снижение мономеров с образованием агрегатов. В настоящее время для решения этих проблем был предложен «катушечный инвертор потока» (CFI), состоящий из спиральных модулей и 90-градусных изгибов с узким распределением времени пребывания (Klutz, S., Lobedann, М., Bramsiepe, С., and Schembecker, G., 2016), и он в настоящее время находится на стадии проверки данной концепции.
Варианты осуществления настоящего изобретения направлены на решение технических проблем, связанных с преобразованием инактивации вирусов низким рН из существующего в настоящее время периодического процесса в непрерывный процесс путем замены существующих способов обработки одновременной двойной обработкой низким рН и детергентом для сокращения времени, необходимого для инактивации вирусов. Варианты осуществления настоящего изобретения и открытия явно и неожиданно демонстрируют, что двойная обработка элюатом белка А с низким рН с добавлением низкой концентрации детергента, такого как Mega-10 или Tween-80 или Tween 20, может сократить время, необходимое для инактивации ретровируса, от 60-120 минут при обработке низким рН, до 2,5-10 минут. Таким образом, включение одновременной двойной обработки низким рН и детергентом в непрерывный процесс производства моноклональных антител может резко сократить время, необходимое для инактивации вируса низким рН, тем самым устраняя необходимость в длинной узкой трубке или CFI для обеспечения продолжительного времени, необходимого для инактивации вируса низким рН. Это может обеспечить улучшенные производственные результаты и выход антител, которые лабильны в условиях более низких значений рН и длительного времени выдержки. Кроме того, включение одновременной двойной обработки низким рН и детергентом в непрерывный процесс будет рентабельным и поможет устранить необходимость в разработке и использовании дорогостоящей модели CFI в уменьшенном масштабе.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБЫ ИНАКТИВАЦИИ ВИРУСОВ С ПРИМЕНЕНИЕМ N-МЕТИЛГЛЮКАМИДА И ЕГО ПРОИЗВОДНЫХ | 2018 |
|
RU2783667C2 |
| СТАБИЛИЗИРОВАННЫЕ СОДЕРЖАЩИЕ АНТИТЕЛА ЖИДКИЕ КОМПОЗИЦИИ | 2011 |
|
RU2653447C2 |
| СПОСОБ ОЧИСТКИ АНТИТЕЛ С НИЗКОЙ ИЗОЭЛЕКТРИЧЕСКОЙ ТОЧКОЙ | 2014 |
|
RU2714967C2 |
| АНТИТЕЛА ПРОТИВ BTN3A И ИХ ПРИМЕНЕНИЕ ПРИ ЛЕЧЕНИИ РАКА ИЛИ ИНФЕКЦИОННЫХ ЗАБОЛЕВАНИЙ | 2019 |
|
RU2800726C2 |
| СПОСОБ ИНКУБАЦИИ ЖИДКОСТЕЙ И ВИРУСНОЙ ИНАКТИВАЦИИ | 2018 |
|
RU2779191C2 |
| ВАЛИДАЦИЯ ОЧИЩЕНИЯ ВИРУСА В НЕПРЕРЫВНОМ РЕЖИМЕ | 2017 |
|
RU2755634C2 |
| СПОСОБ РЕПЛИКАЦИИ ВИРУСА ГРИППА В КУЛЬТУРЕ | 2007 |
|
RU2491339C2 |
| СУБЪЕДИНИЧНЫЙ ВАКЦИННЫЙ ПРЕПАРАТ РЕСПИРАТОРНО-СИНЦИТИАЛЬНОГО ВИРУСА | 1997 |
|
RU2243234C2 |
| СПОСОБ ПОЛУЧЕНИЯ ИММУНОГЛОБУЛИНОВ ДЛЯ ВНУТРИВЕННОГО ВВЕДЕНИЯ И ДРУГИЕ ИММУНОГЛОБУЛИНОВЫЕ ПРОДУКТЫ | 1999 |
|
RU2197500C2 |
| ИНАКТИВАЦИЯ ВИРУСОВ С ПРИМЕНЕНИЕМ КАПРИЛАТА | 2013 |
|
RU2633059C2 |
Изобретение относится к способам для инактивации вирусов. Способ инактивации вируса для применения в непрерывном процессе получения биологического средства включает: отделение элюата с биологическим средством и активным вирусом с использованием колонки и воздействие на указанный элюат с указанным активным вирусом ортогональной обработкой низким pH от 3,0 до 4,0 и неионным детергентом Mega-10 одновременно с инактивацией указанного вируса. Mega-10 представляет собой N-метилглюкамид. Время для инактивации вируса элюата сокращено по сравнению с временем обработки элюата с использованием низкого pH или неионного детергента Mega-10 по отдельности. Вирус содержит вирусы в оболочке из семейства, выбранного из группы, состоящей из Retroviridae, Flaviridae, Togaviridae, Coronaviridae, Filoviridae, Rhabdoviridae, Bunyaviridae, Orthomyxoviridae, Paramyxoviridea, Arenaviridae, Hepadnaviridae, Herpesviridae, Baculoviridae и Poxviridae. Концентрация неионного детергента Mega-10 находится в интервале 0,05-1% (мас./об.). Биологическое средство сохраняется в каждом случае обработки. Способ ускоряет инактивацию вируса до 3-4 мин и подходит для непрерывного процесса. 12 з.п. ф-лы, 18 ил., 3 табл.
1. Способ инактивации вируса для применения в непрерывном процессе получения биологического средства, включающий:
(a) отделение элюата с биологическим средством и активным вирусом с использованием колонки;
(b) воздействие на указанный элюат с указанным активным вирусом ортогональной обработкой низким рН, где значение рН составляет от 3,0 до 4,0,
и неионным детергентом Mega-10, где Mega-10 представляет собой N-метилглюкамид,
одновременно с инактивацией указанного вируса;
где время для инактивации вируса элюата сокращено по сравнению с временем обработки элюата с использованием низкого рН или неионного детергента Mega-10 по отдельности, биологическое средство сохраняется, вирус содержит вирусы в оболочке из семейства, выбранного из группы, состоящей из Retroviridae, Flaviridae, Togaviridae, Coronaviridae, Filoviridae, Rhabdoviridae, Bunyaviridae, Orthomyxoviridae, Paramyxoviridea, Arenaviridae, Hepadnaviridae, Herpesviridae, Baculoviridae и Poxviridae, и
концентрация неионного детергента Mega-10 находится в интервале 0,05-1% (мас./об.).
2. Способ инактивации вируса по п. 1, где колонка содержит колонку для аффинной хроматографии.
3. Способ инактивации вируса по п. 2, где колонка для аффинной хроматографии содержит колонку с белком А.
4. Способ инактивации вируса по п. 1, где биологическое средство содержит белок.
5. Способ инактивации вируса по п. 1, где биологическое средство содержит антитело.
6. Способ инактивации вируса по п. 1, где биологическое средство содержит фрагмент антитела.
7. Способ инактивации вируса по п. 1, где элюат содержит от 1 до 100 мг/мл (мас./об.) биологического средства.
8. Способ инактивации вируса по п. 1, где время инактивации вируса сокращено от 60-120 минут до 3-4 минут.
9. Способ инактивации вируса по п. 1, где ретровирус содержит X-MuLV.
10. Способ инактивации вируса по п. 1, где Herpesviridae содержит вирус свиного герпеса (PRV).
11. Способ инактивации вируса по п. 1, где способ инактивации вируса протекает в диапазоне температур 2-30°С.
12. Способ инактивации вируса по п. 1, где элюат дополнительно содержит детергент Tween 80, Tween 20 или Triton Х-100.
13. Способ инактивации вируса по п. 12, где значение рН элюата составляет 4,5.
| WO 2012014183 A1, 02.02.2012 | |||
| Устройство для оценки амплитуды узкополосного случайного процесса | 1983 |
|
SU1161958A1 |
| WO 1994013329 A1, 23.06.1994 | |||
| СПОСОБ ПОЛУЧЕНИЯ ВИРУСНОГО АНТИГЕНА И ВАКЦИН | 2012 |
|
RU2565827C2 |
| WO 2015158776 A1, 22.10.2015 | |||
| WO 2016207328 A1, 29.12.2016. | |||
Авторы
Даты
2023-11-10—Публикация
2019-11-14—Подача