Область, к которой относится изобретение
Настоящее изобретение относится к способу очистки иммуноглобулинов, то есть иммуноглобулина G (IgG), из сырой плазмы или из белковой фракции сырой плазмы. Изобретение также относится к иммуноглобулиновому продукту и к использованию такого иммуноглобулинового продукта для медицинских целей.
Предпосылки к созданию изобретения
Нормальный иммуноглобулин человека (НИЧ) для использования при предупреждении и лечении ряда инфекционных заболеваний был введен в практику в конце сороковых годов 20 столетия. Оказалось, что НИЧ, приготовленный методом фракционирования с использованием охлажденного этанола по Кону и Онкли (Conn E. , et al. , (1946), J.Am.Chem.Soc., 68, 459-475), (Oncley et al., (1949), J. Am. Chem.Soc., 11, 541-550) и затем также в модификации, которую осуществили Кистлер и Нитшманн (Kistler P. and Nitschmann H.S., (1952), Vox Sang, 7, 414-424), был как эффективным, так и безопасным в отношении передачи вирусной инфекции при введении подкожно или внутримышечно.
Врожденная или приобретенная полная или частичная недостаточность иммуноглобулина (первичные и вторичные синдромы иммунологической недостаточности, соответственно) проявляется через частые обычные и серьезные инфекции, особенно бактериальной природы. Предохранение от таких инфекций раньше достигалось повторными внутримышечными и подкожными инъекциями больших количеств НИЧ до нескольких раз в неделю как пожизненное лечение, что является очень болезненным, когда лекарство вводится внутримышечно.
Поэтому в начале шестидесятых годов было предпринято введение НИЧ внутривенным путем. Испытания показали, что примерно у 5% здоровых добровольцев и примерно у 95% больных с недостатком иммуноглобулина развились непосредственные побочные эффекты, варьирующиеся от одышки до циркуляторной недостаточности и имеющие такую серьезную природу, что введение НИЧ должно было быть прекращено.
Причиной побочных вышеупомянутых эффектов оказались агрегаты иммуноглобулинов, которые среди прочих эффектов сильно активировали систему комплемента. Это особенно было видно у больных с недостатком иммуноглобулинов. Особо тяжелые побочные эффекты анафилактической природы можно было наблюдать у больных, у которых вырабатывались антитела к IgA. Следовательно, были разработаны методы, позволяющие избежать образования агрегатов и/или удалить эти агрегаты в процессе получения, и около двадцати лет назад было испытано и найдено подходящим первое поколение иммуноглобулина для внутривенного введения (ИГВВ).
Первоначальной задачей ИГВВ являлось облегчение состояния инфекционных больных с врожденной или приобретенной полной или частичной недостаточностью иммуноглобулинов и ликвидация дискомфорта, связанного с введением НИЧ. Другое достоинство ИГВВ заключается в том, что в течение короткого периода времени могут быть введены большие дозы иммуноглобулина и тем самым возможно очень быстро получить достаточно высокую концентрацию в крови. Особенно важно быстро достичь высоких концентраций в местах заражений при лечении серьезных бактериальных инфекций.
Недавно было доказано, что ИГВВ, кроме того, эффективен и при других тяжелых заболеваниях, лечение которых трудно провести другим путем, например, кровотечениях, вызванных исчезновением в крови тромбоцитов по иммунологической причине, идиопатической тромбоцитопенической пурпуры (ITP), при некоторых редких заболеваниях, как, например, синдром Кавасаки и ряд аутоиммунных заболеваний, как, например, полирадикулоневрит (синдром Гийена-Варре). В отношении других заболеваний, лечение которых затруднено до сих пор, в настоящее время с применением ИГВВ проходят клинические испытания. Механизм действия в случаях этих заболеваний был прояснен лишь частично. Предполагают, что эффект связан с так называемыми иммуномодулирующими свойствами IgG, например, блокада рецепторов Feγ на фагоцитарных клетках, повышенный метаболизм IgG, понижающая регуляция продукции цитокинов, и с вмешательством в предполагаемую сеть идиотипов/антиидиотипов, особенно связанными с нейтрализацией аутоиммунной реактивности.
Первое поколение ИГВВ было получено при расщеплении пепсином исходного материала (фракция II по Кону), целью расщепления было удаление агрегатов иммуноглобулина. Способ не включал никаких стадий колоночной хроматографии. Продукт должен был быть подвергнут сублимационной сушке для того, чтобы оставаться стабильным какой-то разумный период времени, и его растворяли непосредственно перед использованием.
Исходным материалом для ИГВВ служил НИЧ, который оказался безопасным в отношении передачи вирусов, когда его использовали для внутримышечной инъекции. Поэтому считали, что ИГВВ является таким же безопасным. После нескольких лет клинического применения было, однако, неожиданно обнаружено, что продукты ИГВВ от некоторых производителей вызывали перенос вирусной инфекции гепатита С.
Исследования по выяснению судьбы вирусов при продуцировании НИЧ показали, что перемещение вируса в процессе фракционирования от плазмы к НИЧ ограничено. По-видимому, безопасность НИЧ для внутримышечного использования связана с тем фактом, что он содержит защитные иммуноглобулины. В комбинации с умеренным инъецируемым объемом и с внутримышечным путем введения эти защитные иммуноглобулины могут нейтрализовать и переводить обычные вирусы в плазме в неинфекционные. Вирусные инфекции могут обнаруживаться, как было продемонстрировано в начале девяностых годов, преимущественно тогда, когда внутривенно вводятся большие дозы иммуноглобулина. Поэтому было установлено, что способы получения должны включать одну или несколько явно выраженных стадий инактивации и/или удаления вируса.
Второе поколение ИГВВ, основанное на нерасщепленных и немодифицированных молекулах иммуноглобулина с низкой антикомплементарной активностью и более высокой стабильностью, было представлено в середине восьмидесятых годов, но также в виде лиофильно высушенного продукта. Этот ИГВВ очищали с помощью нескольких стадий хроматографии. Продукты такого типа в настоящее время преобладают на рынке ИГВВ. Первое и второе поколения ИГВВ существуют, таким образом, в виде лиофильно высушенных порошков, которые растворяют непосредственно перед использованием.
Растворение высушенных при лиофилизации ИГВВ происходит медленно (до 30 минут для одной ампулы). Для одного больного часто следует растворить несколько порций. Так как для потребителей имеет большое преимущество наличие ИГВВ в виде раствора, готового для применения, на рынок были представлены жидкие продукты. Более важно то, что еще существует необходимость улучшения способа производства с целью получения высокоочищенного, стабильного и полностью нативного препарата ИГВВ с высокой клинической эффективностью и с меньшим уровнем побочных реакций от препарата. Таким образом, требуется дальнейшее развитие и совершенствование способа очистки IgG из сырой плазмы или белковой фракции плазмы для безопасного в отношении вирусной активности жидкого продукта ИГВВ. Наконец, способ должен быть так спроектирован, чтобы его можно было применить для крупномасштабного производства.
Способ очистки, описанный в настоящей заявке, приводит к жидкому иммуноглобулиновому продукту для внутривенного введения, который может быть охарактеризован как высокоочищенный, полностью нативный, биологически активный, дважды инактивированный в отношении вируса и стабильный ИГВВ нового поколения, который не содержит какого-либо детергента, полиэтиленгликоля (ПЭГ) или альбумина в качестве стабилизатора.
Краткое описание изобретения
Настоящее изобретение относится к усовершенствованной методике очистки и к улучшенному жидкому иммуноглобулиновому продукту, который, кроме того, может быть введен внутривенно.
Иммуноглобулиновый продукт, полученный по способу настоящего изобретения, мог бы быть назван ИГВВ третьего поколения. Способ характеризуется следующими условиями фракционирования: избегают расщепления пепсином, агрегаты и частицы удаляют осаждением (стадия способа, признанная выполнять функцию стадии удаления вируса), дальнейшая очистка достигается с помощью методов ионообменной хроматографии на колонках, обработка растворителем/детергентом (Р/Д) вводится как инактивирующая вирус стадия и препарат как лекарственное средство готовится в виде жидкого продукта.
Благодаря улучшенной чистоте иммуноглобулинового продукта, получаемого способом по изобретению, по сравнению с продуктами, полученными ранее описанными способами, добавление стабилизаторов, таких как неионогенный детергент, ПЭГ или альбумин, не является необходимым, для того, чтобы избежать агрегации IgG при хранении ИГВВ в виде жидкого продукта. Продукт, получаемый способом по изобретению, имеет более высокое качество, чем полученные ранее другим способом продукты, и обеспечивает улучшенные клинические эффекты, а нежелательные побочные эффекты фактически отсутствуют.
Подробное описание изобретения
Настоящее изобретение относится к способу очистки иммуноглобулинов, то есть IgG, из сырой плазмы или из содержащей иммуноглобулин белковой фракции плазмы, где способ включает стадии:
(a) получения водной суспензии, содержащей иммуноглобулин белковой фракции сырой плазмы;
(b) добавления водорастворимого, неденатурирующего в значительной степени белок осадителя к упомянутой суспензии со стадии (а) в количестве, достаточном, чтобы вызвать осаждение большей части белков без иммуноглобулина G, агрегированных иммуноглобулинов и частиц, включая потенциально инфекционные частицы, как, например, вирусные частицы, не вызывая существенного осаждения мономерного иммуноглобулина G, образуя таким образом смесь твердого осадка и надосадочной жидкости;
(с) выделения осветленной, содержащей иммуноглобулин G надосадочной жидкости из смеси со стадии (b);
(d) нанесения осветленной, содержащей иммуноглобулин G надосадочной жидкости со стадии (с) на анионообменную смолу и затем на катионообменную смолу;
(е) вымывания белковых загрязняющих примесей и осадителя белка с катионообменной смолы буфером, имеющим рН и ионную силу, достаточные для удаления загрязняющих примесей со смолы, не вызывая существенного элюирования иммуноглобулина G;
(f) элюирования иммуноглобулина G с катионообменной смолы фактически неденатурирующим буфером со значением рН и ионной силой, достаточными для того, чтобы вызвать эффективное элюирование иммуноглобулина G, получая при этом содержащий иммуноглобулин G элюат;
(g) осуществления диафильтрации/ультрафильтрации содержащего иммуноглобулин G элюата со стадии (f) для концентрирования и/или диализа элюата и, не обязательно, добавления стабилизирующего средства;
(h) добавления вирулицидного количества инактивирующего вирус средства к содержащей иммуноглобулин G, подвергнутой диафильтрации/ультрафильтрации и, не обязательно, стабилизированной фракции со стадии (g), приводящего, по существу, к безопасному в отношении вирусной активности раствору, содержащему иммуноглобулин G;
(i) нанесения содержащего иммуноглобулин G раствора со стадии (h) на анионообменную смолу и затем на катионообменную смолу;
(j) промывания катионообменной смолы со стадии (i) буфером с рН и ионной силой, достаточными для вымывания со смолы белковых загрязняющих примесей и инактивирующего вирус средства, не вызывая существенного элюирования иммуноглобулина G;
(k) элюирования иммуноглобулина G с катионообменной смолы со стадии (j) с помощью в основном неденатурирующего буфера с рН и ионной силой, достаточными, чтобы вызвать эффективное элюирование иммуноглобулина G, получая при этом содержащий иммуноглобулин G элюат, и
(l) обработки содержащего иммуноглобулин G элюата со стадии (k) путем диафильтрации/ультрафильтрации для понижения ионной силы и концентрирования раствора иммуноглобулина G и регулирования осмоляльности путем добавления сахарида.
Исходным материалом для настоящего способа очистки может служить сырая плазма, но преимущественно это содержащая иммуноглобулин белковая фракция сырой плазмы. Исходным материалом для очистки этим способом может быть нормальная человеческая плазма или плазма может быть от доноров с высокими титрами специфических антител, например, гипериммунная плазма. В настоящем описании термин "содержащая иммуноглобулин фракция плазмы" должна охватить все возможные исходные материалы для данного способа, например, плазму, освобожденную от выпавшего при замораживании осадка, или плазму, освобожденную от выпавшего при замораживании осадка, из которой были удалены различные плазменные белки, как, например, фактор IX и антитромбин, различные фракции по Кону и фракции, полученные по методикам осаждения с помощью ПЭГ (Polson et al., (1964), Biochem. Biophys. Acta, 82, 463-475; Polson and Ruiz-Bravo, (1972) Vox Sang, 23, 107-118) или сульфата аммония. В предпочтительном варианте осуществления изобретения белковой фракцией плазмы является фракция II и III по Кону, но также могут быть использованы фракция II по Кону или фракции I, II и III по Кону. Различные фракции по Кону предпочтительно готовят из плазмы стандартным способом фракционирования по Кону, в основном, в модификации Кистлера-Нитшманна. В дополнение к иммуноглобулинам фракции по Кону содержат, например, фибриноген, α-глобулины и β-глобулины, включая различные липопротеины, которые предпочтительно должны быть удалены во время последующего процесса очистки. Ускоритель фильтрации может присутствовать или нет в зависимости от способа выделения, применяемого для получения фракций по Кону (то есть центрифугирования или фильтрации).
Первая стадия способа согласно изобретению включает получение водной суспензии, содержащей иммуноглобулин белковой фракции плазмы, где концентрация IgG в суспензии настолько высока, чтобы во время последующей стадии осаждения большая часть не содержащих IgG белков, особенно с более высокой молекулярной массой, агрегированные иммуноглобулины и другие агрегированные белки, а также потенциально инфекционные частицы осаждались без существенного осаждения мономерного IgG. Это обычно достигается, если концентрация IgG в забуференной и профильтрованной суспензии составляет, как минимум, примерно 4 г/л до прибавления осадителя. Следует принять во внимание, что влияние на осаждение концентрации белка, а также рН и температуры суспензии зависит от выбранного осадителя.
Предпочтительно, чтобы белковая фракция плазмы подвергалась суспендированию в воде и/или буфере при в значительной степени неденатурирующих температуре и рН. Термин "в значительной степени неденатурирующих" подразумевает, что условие, к которому относится термин, не вызывает значительной необратимой потери функциональной активности молекул IgG, например, потери активности связывания антигенов и/или потери биологической Fc-функции (см. пример 2).
Полезно, когда белковую фракцию плазмы суспендируют в воде, подкисленной, как минимум, одной неденатурирующей буферной системой, в 6-9-кратном объеме, предпочтительно в 7-8-кратном, по отношению к объему белковой фракции плазмы. Для обеспечения максимальной растворимости иммуноглобулина и обеспечения оптимального эффекта последующей стадии осаждения с помощью ПЭГ рН содержащей иммуноглобулин суспензии предпочтительно устанавливают ниже 6, например, в диапазоне от 4,0 до 6,0, предпочтительно 5,1-5,7, наиболее предпочтительно около 5,4. Может быть использован любой подходящий кислотный буфер, но буферная система предпочтительно содержит, как минимум, один из следующих буферов и кислот: фосфат натрия, ацетат натрия, уксусная кислота, соляная кислота. Специалисты в данной области поймут, что могут быть использованы многочисленные другие буферы.
Суспензия иммуноглобулина предпочтительно находится при низкой температуре, среди прочего еще и для того, чтобы предотвратить существенную денатурацию белка и минимизировать активность протеаз. Суспензия иммуноглобулина и вода, а также добавленная буферная система имеют предпочтительно одинаковую температуру в диапазоне 0-12oС, предпочтительно 0-8oС, наиболее предпочтительно 1-4oС.
Суспензия осажденной этанолом пасты содержит относительно большие количества агрегированного белкового материала. При необходимости содержащая иммуноглобулин суспензия фильтруется для удаления, например, больших агрегатов, ускорителя фильтрации, если он присутствует, и остаточной нерастворенной пасты. Фильтрацию предпочтительно проводят с помощью объемных фильтров, например, С150 AF, AF 2000 или AF 1000 (Schenk), 30LA (Cuno) или подобных фильтров. Удаление агрегатов, ускорителя фильтрации, если он присутствует, и остаточного нерастворенного белкового материала может быть также выполнено центрифугированием.
Как минимум, один водорастворимый осадитель, в значительной степени неденатурирующий белок, добавляется к содержащей иммуноглобулин профильтрованной суспензии в количестве, достаточном для того, чтобы вызвать осаждение большой части высокомолекулярных белков, липопротеинов, агрегированных белков, в том числе агрегированных иммуноглобулинов. Другой материал в виде частиц, например, потенциально инфекционные частицы, например, вирусные частицы, также осаждается, не вызывая значительного осаждения мономерного IgG. Термин "инфекционные частицы" в настоящем контексте включает, например, вирусные частицы (как, например, вирусы гепатита, ВИЧ1 и ВИЧ2) и бактерии.
В области очистки белка хорошо известны в значительной степени неденатурирующие водорастворимые осадители белка. Такие осадители используются для фракционирования белков, приводящего к частичной очистке белков из суспензий. Подходящие осадители белков для использования в способе по настоящему изобретению включают ПЭГ с различными молекулярными массами, каприловую кислоту и сульфат аммония. Специалисты в данной области поймут, что в качестве альтернативных средств для осаждения могут быть использованы некоторые другие неденатурирующие водорастворимые осадители. Термин "добавление осадителя белка" и варианты этого термина подразумевает добавление одного или нескольких типов средств для осаждения белка.
Предпочтительным осадителем является органическое средство в виде ПЭГ, в частности, ПЭГ с молекулярной массой в диапазоне 3000-8000 Да, как, например, ПЭГ 3350, ПЭГ 4000, ПЭГ 5000 и особенно ПЭГ 6000 (числа в этих конкретных соединениях ПЭГ представляют их среднюю молекулярную массу). Преимущество использования ПЭГ в качестве осадителя состоит в том, что ПЭГ является неионогенным и обладает стабилизирующими белок свойствами, т.е. ПЭГ в низкой концентрации хорошо известен как стабилизатор продуктов ИГВВ. Стадия осаждения также выполняет функцию стадии удаления вирусов. ПЭГ концентрирует и осаждает вирусы, независимо от их вида, размера и их поверхностной оболочки.
Определенное количество осадителя белка добавляется к профильтрованной суспензии для осаждения большей части белков с высокой молекулярной массой и агрегированных белков и частиц без существенного осаждения мономерного IgG, при этом образуется прозрачный раствор надосадочной жидкости. Осадитель белка может быть добавлен в виде твердого порошка или концентрированного раствора.
Для ПЭГ как осадителя применяется общее правило, заключающееся в том, что чем выше молекулярная масса соединения, тем ниже требуется концентрация ПЭГ, чтобы вызвать осаждение белка. Когда используется ПЭГ 3350, ПЭГ 4000 или предпочтительно ПЭГ 6000, полезно, чтобы концентрация осадителя в фильтруемой суспензии была в диапазоне 3-15% по массе, как, например, 4-10% (например, около 5, 6, 7, 8, 9, 10%), где наиболее предпочтительна 6%. На стадии осаждения процесс осаждения проводят, по меньшей мере, до достижения равновесия между твердой и жидкой фазой, например, обычно не менее двух часов, как, например, примерно от 2 до 12 часов, предпочтительно около 4 часов. В течение всего осаждения суспензию предпочтительно сохраняют при низкой температуре (например, ниже, чем примерно 12oС, как, например, ниже, чем примерно 10oС, предпочтительно при температуре между 2 и 8oС). Наиболее подходящая температура зависит от особенностей осадителя белка.
После окончания осаждения белка осветленная надосадочная жидкость, содержащая IgG почти исключительно в виде мономера, выделяется из смеси твердого осадка и надосадочной жидкости, образующейся в результате осаждения. Выделение может быть осуществлено с помощью обычных методик отделения жидкости от твердой фазы, как, например, центрифугирование и/или фильтрация. Предпочтительно используют проточную центрифугу (например, фирмы Westfalia) с 1000-5000 г.
При необходимости выделенная осветленная надосадочная жидкость, содержащая IgG, фильтруется через объемный фильтр для удаления более крупных частиц и агрегатов. При необходимости осуществляется стерильная фильтрация с использованием обычного стерилизационного фильтра (как, например, фильтр 0,22 мкм от фирмы Millipore или Sartorius), при которой удаляются, например, бактерии из раствора.
Осветленная и, при необходимости, профильтрованная надосадочная жидкость, содержащая IgG, подвергается, по меньшей мере, одной операции обработки, например, в два этапа, но при необходимости и нескольким этапам анионообменной и катионообменной хроматографии для удаления значительной доли оставшихся загрязняющих примесей, не содержащих IgG, например IgA, альбумина, а также агрегатов. В предпочтительном варианте осуществления изобретения осветленная и, при необходимости, профильтрованная надосадочная жидкость, содержащая IgG, наносится на анионообменную смолу и затем на катионообменную смолу, которой заполнены две колонки соответствующих размеров.
При проведении операций ионообменной хроматографии для очистки IgG предпочтительно, чтобы условия, например, рН и ионная сила, были выбраны так, что основная часть загрязняющих примесей (например, белки, не относящиеся к IgG, как, например, IgA, трансферрин, альбумин и агрегаты) в нанесенном растворе связывается с анионообменной смолой, так чтобы, в основном, IgG не адсорбировался на анионообменной смоле. Что касается последующей катионообменной хроматографии, предпочтительно выбранные условия приводят к связыванию, в основном, всех молекул IgG, присутствующих в растворе, нанесенном на катионообменную смолу. Белковые загрязняющие примеси, не адсорбированные на анионообменной смоле, и средство для осаждения удаляются при последующем промывании катионообменной смолы.
В предпочтительном варианте осуществления данного способа анионообменная смола и катионообменная смола соединены последовательно. В данном контексте "соединены последовательно" при использовании в связи с ионообменными смолами означает, что белки, проходящие через анионообменную смолу, непосредственно загружаются на катионообменную смолу без изменения буфера или других условий.
Несколько причин объясняют полезность того, что анионообменная и катионообменная хроматография проводятся в одну стадию с использованием двух последовательно соединенных хроматографических колонок вместо двух независимых хроматографических стадий, например, с различными буферными композициями. Использование двух последовательно соединенных хроматографических колонок делает операцию более практичной, например, нет необходимости в промежуточном этапе сбора содержащих IgG фракций между двумя ионообменными хроматографическими методами, возможно, в регулировании рН и ионной силы. В дополнение к этому, поток буфера поступает в обе колонки в одно и то же время и две колонки уравновешиваются одним и тем же буфером. Однако предполагается, что также возможно осуществлять хроматографическую стадию в две ступени, то есть анионообменная смола и катионообменная смола не соединяются последовательно. Проведение хроматографии в две ступени было бы, однако, как указывалось выше, более трудоемким по сравнению с вариантом, когда ионообменные смолы соединены последовательно.
В настоящее время предполагается, что высокая степень чистоты, высокое содержание мономеров и димеров IgG и низкое содержание IgA в продуктах ИГВВ данного изобретения отчасти имеют место благодаря использованию двух последовательно соединенных хроматографических колонок.
Как известно специалисту, ионообменники могут основываться на различных материалах в отношении матрицы, а также присоединенных заряженных групп. Например, могут быть использованы следующие матрицы, в которых указанные материалы могут быть в большей или меньшей степени соединены поперечными связями: на основе агарозы (как, например, сефароза CL-6B®, сефароза Fast Flow® и сефароза High Performance®), на основе целлюлозы (как, например, ДЭAЭ-сефацел®), на основе декстрана (как, например, сефадекс®), на основе двуокиси кремния и на основе синтетических полимеров. Для анионообменной смолы заряженными группами, ковалентно присоединенными к матрице, могут быть, например, диэтиламиноэтил (ДЭАЭ), четвертичный аминоэтил (ЧАЭ) и/или четвертичный аммоний (ЧА). Для катионообменной смолы заряженными группами, которые ковалентно связаны с матрицей, могут быть, например, карбоксиметил (КМ), сульфопропил (СП) и/или метилсульфонат (МС). В предпочтительном варианте осуществления настоящего способа используемой анионообменной смолой является ДЭАЭ-сефароза Fast Flow®, но могут применяться и другие анионообменники. Предпочтительной катионообменной смолой является КМ-сефароза Fast Flow®, но могут применяться и другие катионообменники.
Подходящий объем используемой смолы при наполнении колонки для ионообменной хроматографии отражает размеры колонны, то есть диаметр колонны и высоту заполнения смолой, и варьируется в зависимости, например, от количества IgG в наносимом растворе и связывающей способности используемой смолы.
Перед проведением ионообменной хроматографии ионообменную смолу предпочтительно уравновешивают буфером, который позволяет смоле связать ее противоионы. Предпочтительно анионообменные и катионообменные смолы уравновешивают тем же самым буфером и это облегчает процесс, поскольку нужно готовить и использовать только один буфер.
Если, например, выбранной анионообменной смолой является ДЭАЭ-сефароза FF® и катионообменной смолой является КМ-сефароза FF® и колонки соединены последовательно, тогда выгодно, чтобы обе колонки уравновешивались неденатурирующим кислотным буфером, имеющим примерно такие же рН и ионную силу, как наносимый на колонку раствор IgG. Любой из различных буферов пригоден для уравновешивания ионообменных колонок, например, ацетат натрия, фосфат натрия, трис(гидроксиметил)аминометан. Специалист в данной области знает, что могут быть использованы многочисленные другие буферы для уравновешивания, пока рН и электропроводность примерно такие же, как у наносимого раствора IgG. Предпочтительным буфером для уравновешивания анионообменной колонки и катионообменной колонки, соединенных последовательно, является буферный раствор с ацетатом натрия, имеющий концентрацию ацетата натрия в диапазоне 5-25 мМ, например, в диапазоне 10-20 мМ, предпочтительно 15 мМ. Предпочтительно, чтобы рН буфера с ацетатом натрия, используемого для уравновешивания, находился в диапазоне 5,0-6,0, например, в диапазоне 5,4-5,9, предпочтительно около 5,7. Электропроводность находится в диапазоне 1,0-1,4 мСм/см, предпочтительно около 1,2 мСм/см. Подходящие ацетатные буферы могут быть получены из тригидрата ацетата натрия и ледяной уксусной кислоты.
Перед загрузкой осветленной и при необходимости профильтрованной, содержащей IgG надосадочной жидкости в ионообменные колонки концентрацию буфера и рН упомянутой надосадочной жидкости предпочтительно доводят, если необходимо, до значений, по существу, эквивалентных концентрации и рН применяемого уравновешивающего буфера.
После загрузки содержащей IgG надосадочной жидкости в последовательно соединенные колонки, их предпочтительно промывают (первоначальная промывка) буфером для промывки в объеме, равном объему колонны, чтобы обеспечить количественный перенос содержащего IgG раствора из анионообменной колонки в катионообменную колонку. Затем анионообменную и катионообменную колонки разъединяют и катионообменную колонку предпочтительно промывают для удаления белковых загрязняющих примесей со смолы буфером, имеющим рН и ионную силу, достаточные для элюирования, в основном, всех из загрязняющих примесей с катионообменной смолы, не вызывая существенного элюирования IgG.
Первоначальную промывку полезно проводить, используя уравновешивающий буфер, хотя даже другие буферы с такими же концентрацией и значением рН могут быть использованы для промывки. Предпочтительно, чтобы для вымывания загрязняющих примесей с катионообменной смолы использовался ацетатный буфер. Значение рН буфера может быть от 5,0 до 6,0, например, в диапазоне 5,2-5,8, например, около 5,4.
Элюирование IgG с катионообменной смолы предпочтительно осуществляют в значительной степени не денатурирующим буфером с рН и ионной силой, достаточными для эффективного элюирования IgG, получая таким образом содержащий IgG элюат. В этом контексте эффективное элюирование подразумевает, что, как минимум, 75%, например, как минимум, 80%, например, по меньшей мере, 85%, белков, включая IgG, нанесенных на анионообменную и катионообменную смолы последовательно, элюируются с катионообменной смолы. Элюирование полезно проводить в виде операции элюирования с градиентом. В способе по настоящему изобретению предпочтительным используемым буфером является ацетат натрия с рН в диапазоне 5,0-6,0, как, например, 5,2-5,8, предпочтительно около 5,4, и концентрацией в диапазоне 5-40 мМ, как, например, в диапазоне 10-25 мМ, предпочтительно около 15 мМ.
Предпочтительно, чтобы концентрация соли в буфере для элюирования была достаточна велика, чтобы вытеснить IgG со смолы. Однако не исключается и то, что увеличение рН и более низкая концентрация соли могут использоваться при элюировании IgG со смолы. В предпочтительном варианте осуществления настоящего способа элюирование проводят как непрерывное элюирование с градиентом по соли при концентрации хлористого натрия в диапазоне 50-500 мМ, предпочтительно при концентрации хлористого натрия примерно от 125 до 350 мМ.
Элюция также может быть проведена в виде стадии градиентной элюции. Подразумевается, что элюция могла бы быть также проведена в виде элюции при постоянной концентрации соли, когда буфер для элюирования, используемый в катионообменной колонке, характеризуется только одной концентрацией соли в отличие от градиентной элюции. Если проводят элюирование при постоянной концентрации соли, концентрация соли может с успехом быть в интервале примерно от 350 до примерно 500 мМ хлористого натрия. Преимущество градиентного элюирования по сравнению с элюированием при постоянной концентрации соли состоит в том, что элюирование более эффективно с градиентом по соли, но другое преимущество заключается в том, что элюат имеет более низкую ионную силу, что полезно, поскольку высокая ионная сила является опасной для устойчивости IgG. Буфер для элюирования может, кроме того, включать стабилизирующее белок средство, такое, как указанное ниже. Могут быть использованы различные другие подходящие буферные системы для элюирования IgG, что понятно специалистам в этой области.
Предпочтительно, что, как минимум, одно стабилизирующее белок средство добавляется к фракции с IgG сразу после или во время элюирования. Стабилизирующие белок средства известны специалистам в данной области и включают, к примеру, различные спирты, получаемые восстановлением сахара, и сахариды (например, сорбит, манноза, глюкоза, трегалоза, мальтоза), белки (например, альбумин), аминокислоты (например, лизин, глицин) и органические средства (например, ПЭГ). Полезно, когда выбранный промежуточный стабилизатор может быть таким, который может быть удален из содержащего IgG раствора на последующих стадиях.
Подходящая концентрация стабилизирующего белок средства в содержащем IgG растворе зависит от конкретного примененного средства. В одном предпочтительном варианте осуществления изобретения стабилизирующим средством является сорбит, предпочтительно в конечной концентрации в диапазоне от 2 до 15% (м/о) сорбита, например, примерно 2,5%.
После элюирования с катионообменной колонки элюат предпочтительно обессоливают (то есть подвергают диализу) и преимущественно концентрируют. Замена буфера и концентрирование IgG могут быть осуществлены при объединенном процессе диафильтрации/ультрафильтрации. Термин "диафильтрация/ультрафильтрация" означает, что диализ и концентрирование путем диафильтрации и ультрафильтрации соответственно проводятся в одну стадию. Не исключается, чтобы диафильтрация и ультрафильтрация проводились в две различные стадии. Однако для предотвращения ненужной потери продукта в настоящее время предпочитают проводить диализ и концентрирование методами диафильтрации и ультрафильтрации в одну стадию.
Мембраны, применяемые для диафильтрации/ультрафильтрации, преимущественно имеют номинальный массовый порог в диапазоне 10000-100000 Да. Предпочтительным типом мембран для настоящего способа является полисульфоновая мембрана с номинальным массовым порогом 30000 Да, полученная от фирмы Millipore. Могут применяться и другие мембраны для ультрафильтрации из сравнимого материала и сравнимой пористости.
Степень концентрирования может значительно варьироваться. Раствор концентрируют от примерно 10 г/л IgG до примерно 100 г/л, предпочтительно до примерно 50 г/л. После концентрирования концентрат IgG преимущественно подвергается диализу против буфера с низкой ионной силой. Помимо удаления ионов солей на этой стадии также удаляются из раствора загрязняющие примеси с низкой молекулярной массой и предоставляются возможности для обмена буфера для следующей стадии очистки. Предпочтительным буфером для диафильтрации является 15 мМ ацетат натрия, рН 5,4, содержащий 2,5% (м/о) сорбита. Обмен буфера продолжается до тех пор, пока электропроводность подвергаемого ультрафильтрации раствора уменьшается до величины, меньшей, чем примерно 1,5 мСм/см, предпочтительно, менее чем примерно 1,3 мСм/см. При диафильтрации/ультрафильтрации рН предпочтительно поддерживают в диапазоне 4,0-6,0, предпочтительно 5,1-5,7, наиболее предпочтительно около 5,4.
После диафильтрации/ультрафильтрации концентрация стабилизирующего белок средства преимущественно доводится в растворе, если необходимо, до конечной оптимальной концентрации, характерной для конкретного примененного средства, стабилизирующего белок. Если применяется сорбит, концентрация сорбита предпочтительно доводится до примерно 10% по массе.
Предпочтительно, чтобы стабилизированный раствор фильтровали через фильтр с диаметром пор в диапазоне 0,2-1,0 мкм, предпочтительно около 0,45 мкм, для удаления агрегатов перед следующей стадией. На этой стадии содержащий IgG раствор является прозрачным раствором соответствующего объема с высокой стабильностью, что является комплексным результатом высокой чистоты, низкой ионной силы, кислотного рН, относительно высокой концентрации IgG и добавления стабилизатора.
В способ получения продукта ИГВВ в настоящее время включаются, как минимум, две определенные и обоснованные стадии удаления и инактивации вируса, предпочтительно это стадии осаждения с помощью ПЭГ в качестве общей стадии удаления вируса и обработки растворителем/детергентом в качестве стадии инактивации вируса в отношении вирусов с липидной оболочкой. Помимо строгих требований к безопасности исходного материала в отношении вирусной активности, согласно международным нормам, и хорошо известной способности уменьшения титра вирусов в процессе многостадийной очистки, включение двух независимых, уменьшающих титр вирусов стадий, активных как против вирусов с оболочкой, так и безоболочечных вирусов, обеспечивает в значительной степени безопасность лекарственного средства по настоящему изобретению в отношении вирусной активности.
Инфекционные вирусы с липидной оболочкой, которые могут еще присутствовать в растворе, содержащем IgG, предпочтительно инактивируются на этой стадии способа при добавлении вирулицидного количества инактивирующего вирус средства к содержащему IgG раствору. "Вирулицидное количество" инактивирующего вирус средства означает количество, приводящее к раствору, в котором вирусные частицы оказываются в значительной степени неинфицирующими и который, таким образом, является "безопасным в отношении вирусной активности раствором, содержащим IgG", как определяется в данной области. Такое "вирулицидное количество" будет зависеть от примененного инактивирующего средства, а также от условий, таких, как время инкубирования, рН, температура, содержание липидов и концентрация белка.
Термин "инактивирующее вирус средство" предполагает обозначение такого средства или метода, которые могут быть применены для инактивации вирусов с липидной оболочкой, а также вирусов без липидной оболочки. Термин "инактивирующее вирус средство" следует понимать как включающее и комбинацию таких средств и/или методов, всякий раз, когда это подходит, и только один вид такого средства или метода.
Предпочтительными инактивирующими вирус средствами являются детергенты и/или растворители, наиболее предпочтительно - смеси детергент-растворитель. Следует понимать, что инактивирующее вирус средство при необходимости является смесью одного или нескольких детергентов с одним или несколькими растворителями. Обработка растворителем/детергентом (Р/Д) является широко применяемой стадией для инактивации вирусов с липидной оболочкой (например, ВИЧ1 и ВИЧ2, вируса гепатита типа С и не А-В-С, Т-лимфотропного вируса человека (HTLV 1 и 2), семейства герпес вирусов, включая цитомегаловирус (CMV) и вирус Эпштейна Барра) в продуктах крови. Большое разнообразие детергентов и растворителей может быть использовано для инактивации вирусов. Детергент может быть выбран из группы, состоящей из неионогенных и ионогенных детергентов, и выбирается так, чтобы быть в значительной степени не денатурирующим. Предпочтительно используется неионогенный детергент, так как он облегчает последующее удаление детергента из препарата IgG на последующей стадии. Подходящие детергенты описываются, например, Shanbrom et al. в патенте США 4314997 и патенте США 4315919. Предпочтительными детергентами являются продающиеся под торговыми марками Тритон Х-100 и Твин 80. Предпочтительными растворителями для использования в инактивирующих вирус средствах являются ди- или триалкилфосфаты, как описывают, например, Neurath и Horowitz в патенте США 4764369. Предпочтительным растворителем является три(н-бутил)фосфат (ТНБФ). Особо предпочтительным инактивирующим вирус средством в практике настоящего изобретения является смесь ТНБФ и твина 80, но, альтернативно, могут применяться другие комбинации. Предпочтительная смесь добавляется в таком объеме, что концентрация ТНБФ в содержащем IgG растворе находится в диапазоне от 0,2 до 0,6% по массе, предпочтительно концентрация составляет около 0,3% по массе. Концентрация твина 80 в содержащем IgG растворе лежит в диапазоне 0,8-1,5% по массе, предпочтительно концентрация составляет примерно 1% по массе.
Стадия инактивации вируса проводится в условиях, инактивирующих вирусы с оболочкой, что приводит к содержащему IgG раствору, в значительной степени безопасному в отношении вирусной активности. В общем, такие условия подразумевают температуру 4-30oС, как например, 19-28oС, 23-27oС, предпочтительно около 25oС, и время инкубирования, которое было определено как эффективное подтверждающими исследованиями. Обычно достаточно времени инкубирования 1-24 часа, предпочтительно 4-12 часов, например, около 6 часов, для обеспечения достаточной инактивации вируса. Однако подходящие условия (температура и время инкубирования) зависят от примененного инактивирующего вирус средства, рН и концентрации белка, и содержания липидов в растворе.
Предполагается, что другие методы для удаления или инактивации вируса также могут быть применены для получения безопасного в отношении вирусной активности продукта, как, например, прибавление метиленового синего с последующей инактивацией ультрафиолетовым излучением или нанофильтрацией.
После обработки растворителем/детергентом раствор преимущественно разбавляется буфером. При необходимости в значительной степени безопасный в отношении вирусной активности раствор, содержащий IgG, фильтруется, предпочтительно через объемный фильтр, как описано выше для ранней стадии настоящего способа, и/или через стерильный фильтр.
После инактивации вируса и, предпочтительно, фильтрации проводят ионообменную хроматографию для удаления инактивирующего вирус средства и белковых загрязняющих примесей. Эту стадию предпочтительно проводят, как уже описывалось для предыдущей стадии ионообменной хроматографии в данном способе, за исключением того, что объем анионообменной смолы составляет примерно половину объема катионообменной смолы и что промывка перед элюированием IgG более экстенсивная, используя буфер в объеме, как минимум, равном шести объемам колонки. Кроме этого, в предпочтительном варианте осуществления изобретения уравновешивающим буфером является ацетат натрия с концентрацией в диапазоне примерно 5-25 мМ, предпочтительно 15 мМ, и рН примерно в интервале 5,0-5,8, предпочтительно 5,4. Как указывалось ранее, содержание ацетата натрия и рН содержащего IgG раствора предпочтительно доводятся до таких же концентраций и рН, как в буфере для уравновешивания. Дополнительно в предпочтительном варианте осуществления изобретения стабилизирующее белок средство, предпочтительно мальтоза, добавляется к полученному элюату до конечной концентрации в диапазоне 1-5%, предпочтительно около 2,5% по массе.
Предпочтительный способ удаления инактивирующего вирус средства осуществляется с помощью ионообменной хроматографии. Однако другие способы, как, например, экстракция маслом и альтернативные хроматографические методы, рассматриваются как пригодные. Подходящий метод зависит от применяемого инактивирующего вирус средства. Удаление растворителя/детергента может быть достигнуто путем связывания IgG со смолой и затем тщательного вымывания инактивирующего средства буфером. Используемым методом является катионообменная хроматография. В предпочтительном варианте осуществления настоящего изобретения проводят также анионообменную хроматографию в дополнение к катионообменной хроматографии для улучшения качества и общей чистоты конечного продукта по настоящему способу.
После стадии ионообменной хроматографии содержащий IgG элюат предпочтительно подвергают диализу и концентрируют; таким образом содержание оставшихся меньших белковых компонентов также эффективно понижается. Преимущественно это может быть осуществлено путем диафильтрации/ультрафильтрации, как описано ранее. Применяемым для диафильтрации буфером является ацетат натрия, предпочтительно в концентрации от примерно 4 до 10 мМ, предпочтительно 7,5 мМ, и с рН в диапазоне от примерно 4,0 до 6,0, предпочтительно около 5,1-5,7, например, 5,4. Альтернативно, для диафильтрации могут быть использованы другие буферы, как, например, фосфат натрия или кислоты. Диафильтрация продолжается до электропроводности, менее или равной 1 мСм/см. При необходимости содержащий IgG раствор далее фильтруется в стерильных условиях.
Если желательно, очищенный, содержащий IgG раствор, который в основном свободен от инактивирующего вирус средства, подвергается дальнейшим обработкам с целью сделать его пригодным для приготовления готовой лекарственной формы в виде жидкого продукта для использования, например, внутривенно, подкожно или внутримышечно.
С практической точки зрения предпочтительно, чтобы содержание жидкой лекарственной формы иммуноглобулинового продукта было одинаковым и для хранения, и для использования. Конечная концентрация IgG в продукте предпочтительно находится в диапазоне 0,25-20% по массе (соответствует 2,5-200 г IgG/л), как, например, примерно 1-20% по массе, то есть около 2-10%, 12, 14, 16, 18.
Известно, что высокая концентрация белка приводит к более высокой стабильности IgG. С другой стороны, высокая концентрация IgG означает, что максимальная скорость инфузии при введении IgG больному внутривенно должна быть достаточно низкой, чтобы избежать проблем с внутривенным вливанием из-за высокого осмотического давления продукта. Рекомендуемая сейчас Европейской Фармакопеей (Ph.Eur.) концентрация для внутривенного введения составляет 5% (м/о). С другой стороны, достаточно концентрированный продукт (например, 10% или выше) имеет преимущества для внутримышечных или подкожных инъекций.
Хотя этому не отдается предпочтение, очевидно, что продукты, получаемые на различных стадиях способа по изобретению, могут быть также использованы, как, например, лиофильно высушенные продукты вместо жидких лекарственных форм, хотя это менее удобно по сравнению с использованием иммуноглобулиновых продуктов в виде непосредственных жидких лекарственных форм. Последний вариант осуществления изобретения будет более подробно описан далее.
Жидкие иммуноглобулиновые продукты наиболее стабильны при ионной силе значительно более низкой, чем ионная сила плазмы, то есть электропроводность является предпочтительно меньше, чем 1,0 мСм/см, предпочтительно около 0,8 мСм/см.
Значение рН влияет на стабильность IgG и на скорость вливания. Жидкие иммуноглобулиновые продукты более устойчивы в кислых условиях, то есть ниже изоэлектрической точки IgG, рН 6,4-8,5. Чем ближе значение рН к физиологическому значению рН (7,1-7,3), тем более высокая скорость вливания может быть применена. Как следствие требуемой стабильности, рН иммуноглобулинового продукта по изобретению предпочтительно будет лежать в диапазоне 5,1-5,7, как, например, между 5,2 и 5,6, например, около 5,4.
Кроме того, иммуноглобулиновый продукт может включать стабилизирующие белок средства, как описано ранее. В дополнение к спиртам, полученным восстановлением сахара, и сахаридам (как, например, сорбит, манноза, глюкоза, трегалоза, мальтоза) могут быть использованы также в качестве стабилизаторов белки (как, например, альбумин), аминокислоты (как, например, лизин, глицин) и органические соединения (как, например, ПЭГ и твин 80). Подходящая концентрация стабилизирующего средства в содержащем IgG растворе зависит от конкретного примененного средства, как ранее описано.
Очищенный раствор IgG соответственно регулируется, если необходимо, для получения стабильного и изотонического раствора. Термин "изотонический раствор" предназначается для определения того, что раствор имеет такое же осмотическое давление, как в плазме. Как указано выше, ионная сила в иммуноглобулиновом продукте по изобретению в жидкой лекарственной форме заметно ниже, чем в плазме. По этой причине предпочтительно, чтобы использовались моно- и дисахариды для повышения осмоляльности раствора, поскольку это не влияет на ионную силу. В предпочтительном варианте осуществления настоящего изобретения прибавляют мальтозу в концентрации, обеспечивающей изотоничность раствора, и в то же время мальтоза действует как стабилизирующее иммуноглобулин средство. Это предпочтительно осуществляют путем прибавления мальтозы до конечной концентрации в диапазоне от примерно 5% до 15% (м/о), предпочтительно 10% (м/о); другие сахариды, как, например, манноза и глюкоза, могут быть использованы альтернативно.
Предпочтительные конечные условия для иммуноглобулинового продукта представляют компромисс между стабильностью и физиологически приемлемыми условиями в отношении, например, рН, ионной силы и тоничности. Кроме того, иммуноглобулиновый продукт должен удовлетворять требованиям тестов контроля качества, как установлено в Monograph 918, Ph.Eur., 1997.
Главными преимуществами продукта, получаемого способом по изобретению, являются те, что когда его получают в виде жидкого препарата, продукт является сочетанием жидкого, готового к использованию продукта, который в то же время очень устойчив, имеет высокую чистоту, имеет в значительной мере нормальное распределение подклассов IgG и имеет чрезвычайно низкое содержание IgA, а также низкое содержание IgM, и продукта, поддерживающего активность антител и биологическую активность, демонстрируемую Fc-функцией.
Более того, он не содержит по существу агрегатов иммуноглобулинов и/или других белков плазмы, измеренных в виде полимеров, больших, чем димеры, и обладает низкой антикомплементарной активностью, и он имеет очень высокое содержание мономеров и димеров IgG. Мономерный IgG составляет, как минимум, 90%, что считается идеальным. Благодаря высокой стабильности возможно избежать прибавления других стабилизаторов, как, например, альбумин, глицин, детергент или ПЭГ. Наконец, продукт безопасен в отношении вирусной активности, так как способ включает хорошо определенные и подтвержденные стадии ослабления вируса, нацеленные на удаление и/или инактивацию как вирусов с липидной оболочкой, так и вирусов с нелипидной оболочкой.
С целью подтверждения того, что стадия получения обладает свойствами стадии уменьшения титра вируса, является предоставление доказательства, что способ получения будет способствовать эффективному инактивированию/удалению вирусов, которые либо, как известно, загрязняют исходные материалы, либо имеют возможность сделать это. Исследования для подтверждения включают преднамеренное прибавление вируса до стадий получения, чтобы подтвердить и измерить степень его удаления/инактивации после стадии или стадий получения. Гуанозин-5'-монофосфата (GMP) предотвращает преднамеренное введение любого вируса в оборудование для получения. Поэтому подтверждающие исследования следовало бы проводить в отдельной лаборатории, оборудованной для работ по вирусологии, на уменьшенной в масштабе модели производственной стадии и проводить силами персонала, компетентного в вирусологии, вместе с работающими на производстве инженерами. Количество вируса, добавляемого к исходному материалу для стадии получения, которая требует подтверждения, должно быть максимально возможно высоким, чтобы определить возможность адекватного инактивирования/удаления вирусов на стадии получения. Однако вирусы для введения должны быть добавлены так, чтобы состав материала для получения значительно не изменялся. Предпочтительно объем вирусов для введения равен или меньше 10%.
Количественные анализы в отношении инфекционности должны быть проведены в соответствии с принципами GLP и могут включать образование бляшек, детектирование других цитопатических эффектов, как, например, образование синцития или очагов, титрование до конечной точки (например, анализы TCID50), детектирование синтеза вирусного антигена или другие методы. Метод должен иметь адекватную чувствительность и воспроизводимость и должен быть осуществлен с достаточными повторами и контролем, чтобы обеспечить адекватную статистическую точность результатов.
Как правило, на стадии получения проводится заражение дозой 6 log вируса и, если обнаруживается снижение на уровне в 4 logs или более, то это указывает на чистый эффект для конкретного анализируемого вируса, подвергающегося исследованию. Подобным же образом, снижение на уровне в 4,5 logs, 5 logs или даже 5,5 logs указывает на чистый эффект в случае анализа конкретного вируса, подвергающегося исследованию, и стадия может быть классифицирована как стадия, подтверждающая снижение титра вируса.
Подтверждающие исследования с вирусами должны быть проведены с вирусами, наиболее близкими тем, которые могут загрязнять продукт, и, во-вторых представлять как можно более широкий диапазон физико-химических свойств для оценки способности удалять вирусы системой в целом.
Подтверждающие исследования с вирусами должны проводиться в соответствии с Запиской СРМР к Guidance on Virus Validation Studies: The Design, Contribution and Interpretation of Studies Validating the Inactivation and Removal of Viruses (CPMP/BWP/268/95) и Запиской к Guidance on Plasma Derived Medicinal Products (CPMP/BWP/269/95).
Подтверждающие исследования настоящего способа представлены в примере 5.
Продукт по изобретению имеет чистоту более 95%, предпочтительно более 98%. Высокая степень чистоты объясняется, среди прочего, тем фактом, что продукт по изобретению получают с помощью, как минимум, одной, предпочтительно двух, и, необязательно, последовательно объединенных стадий анионо-катионообменной хроматографии. В этом контексте следует отметить, что несмотря на большое число примененных в способе стадий, можно получить высокий выход в производственном масштабе, как минимум, 3,5 г белка IgG на кг свежезамороженной плазмы.
Сравнительные исследования, которые были проведены (пример 2), показали, что иммуноглобулиновый продукт, полученный способом по изобретению, имеет идеальные функциональные свойства, как, например, очень высокая активность связывания антигенов и высокая Fc-функция. Предпочтительное в настоящее время лекарственное средство, полученное авторами изобретения, представляет 5% по массе раствор иммуноглобулина. Проведенные тесты на стабильность показали устойчивость при хранении при 4oС более чем один год, то есть в иммуноглобулиновом продукте не образуются агрегаты, нет фрагментации иммуноглобулинов G, не наблюдается потеря желаемой биологической активности или повышение нежелаемой активности, например, антикомплементарной активности или прекалликреиновой активности, при измерениях in vitro.
На основании данного изобретения возможно получить продукт IgG с чистотой более 95%, как, например, по меньшей мере, 96% или, как минимум, 97%, например, как минимум, 98%, предпочтительно, как минимум, 99%, более предпочтительно, как минимум, 99,5%. Продукт IgG должен содержать менее 6 мг IgA/л, как, например, менее 4 мг IgA/л, предпочтительно менее 3 мг IgA/л, более предпочтительно менее 2 мг IgA/л.
Следует подчеркнуть, что другие продукты содержат стабилизаторы в виде детергента, ПЭГ или альбумина. В предпочтительном варианте осуществления изобретения продукт по настоящему изобретению не содержит какого-либо из упомянутых стабилизаторов, вместо этого был выбран хорошо переносимый сахарид.
Продукт по настоящему изобретению имеет в качестве одной из характеристик очень низкое содержание полимеров и агрегатов. В предпочтительном варианте осуществления изобретения продукт по настоящему изобретению содержит менее 1,5% полимеров и агрегатов, как, например, менее 1%, например, менее 0,5%, или менее 0,25% полимеров и агрегатов. Содержание мономеров и димеров IgG составляет, как минимум, 95%, например, не менее 96% или не менее 97%, например, как минимум, 98%, предпочтительно, как минимум, 98,5% или 99%. Содержание мономерного IgG составляет в продукте, как минимум, 90%.
Испытания показали клинический эффект продукта по настоящему изобретению, сравнимый с эффектом зарегистрированных продуктов ИГВВ. Продукт хорошо переносился больными, и время оборота иммуноглобулинов при кровообращении было определено как четыре недели. В представленных исследованиях был показан убедительный иммуномодулирующий эффект ИГВВ, SSI (данные представлены в примере 3).
Показаниями для ИГВВ являются первичная гипо/агаммаглобулинемия, включая обычное изменчивое иммунодефицитное состояние, синдром Wiskott-Aldrich и серьезные комбинированные иммунодефицитные состояния (SCID), вторичная гипо/агаммаглобулинемия у больных с хроническим лимфатическим лейкозом (CLL) и множественная миелома, СПИД и бактериальные инфекции у детей, острая и хроническая идиопатическая тромбоцитопеническая пурпура (ITP), аллогенная трансплантация костного мозга (ВМТ), болезнь Кавасаки и синдром Гийена-Барре.
Неврология: хроническая воспалительная демиелинизирующая полиневропатия (CIDP), многоочаговая двигательная невропатия, рассеянный склероз, тяжелая миастения, синдром Итона-Ламберта, ретробульбарный неврит, эпилепсия.
Гинекология: привычный аборт, первичный антифосфолипидный синдром.
Ревматология: ревматоидный артрит, системная красная волчанка, системная склеродермия, васкулит, гранулематоз Вегенера, синдром Шегрена, юношеский ревматоидный артрит.
Гематология: аутоиммунная нейтропения, аутоиммунная гемолитическая анемия, нейтропения.
Желудочно-кишечные заболевания: болезнь Крона, язвенный колит, брюшной полости заболевания.
Другие: астма, синдром септического шока, синдром хронической усталости, псориаз, синдром токсического шока, диабет, синусит, расширенная кардиомиопатия, эндокардит, атеросклероз, СПИД и бактериальные инфекции у взрослых.
Кроме указанных показаний для лечения с помощью продуктов ИГВВ, некоторые серьезные аутоиммунные заболевания, которые обычно связаны с кортикостероидной и иммуносупрессивной терапией, рассматриваются как состояния, представляющие цель состояния для лечения продуктом по настоящему изобретению. Среди них несколько неврологических заболеваний, как, например, полирадикулоневрит и некоторые иммуноопосредствованные периферические полиневропатии, а также некоторые хронические воспалительные ревматические и сосудистые состояния, как, например, системный васкулит, охватывающий мелкие сосуды, полимиозит, и другие.
Другой способ действия продукта по изобретению может выражаться в ликвидации инфекционных антигенов при хронических инфекциях и в повышении метаболизма IgG.
Изобретение далее иллюстрируется следующими примерами, которые не рассматриваются как лимитирующие.
Примеры
Пример 1
Технологические стадии при очистке иммуноглобулина (за исключением стадии 5, все стадии проводятся при температуре 5±3oС).
Стадия 1: Получение фракций II+III по Кону в виде пасты:
Паста фракций II+III по Кону готовится из человеческой плазмы стандартным методом фракционирования по Кону (Cohn E., et al., (1946) J.Am.Chem.Soc., 459-475), в основном, в модификации Кистлера-Нитшманна (Kistler P. and Nitschmann H.S., (1952), Vox Sang, 7, 414-424). Осаждение этанолом инициируется после удаления выпавшего при низкой температуре осадка и, если желательно, после адсорбции некоторых белков плазмы (как, например, фактор IX и антитромбин) на, например, ионообменной смоле и/или матрице из гепарин-сефарозы®.
Конкретные условия (рН, концентрация этанола, температура, концентрация белка) для получения фракций II-III в виде пасты показаны на фигуре на стр. 266 в кн. Harns JR (ред.), Blood Separation and Plasma Fractionation, Wiley-Liss, New York, 1991. Пасту выделяют на фильтр-прессе, добавляя ускоритель фильтрации до фильтрации.
Стадия 2: Экстракция иммуноглобулинов из пасты фракций II+III по Кону:
Из 140 кг пасты фракций II+III, включая 30 кг ускорителя фильтрации (фирма Schenk, Германия) (соответствующего начальному объему плазмы около 1150 кг), проводят экстракцию, добавляя сначала 525 кг 2,33 мМ буфера фосфат натрия/ацетат, рН 4,0, при медленном перемешивании примерно 1,5 часа, сопровождаемую 2 последовательными добавлениями 350 кг воды для инъекций при перемешивании в течение примерно 1,5 часов после каждой порции. В конце добавляют около 280 кг 21,5 мМ фосфата натрия/ацетата, рН 7,0, доводя при этом рН суспензии до 5,4.
Суспензию фильтруют через объемный фильтр (C-150AF, Schenk, Германия). Фильтрат содержит, среди других белков, иммуноглобулины.
Стадия 3: Осаждение белковых агрегатов и удаление вируса с помощью ПЭГ 6000:
ПЭГ 6000 (фирмы Merck, Германия) прибавляют к фильтрату со стадии 2 до конечной концентрации в 6% по массе. После осаждения в течение 4 часов суспензию с ПЭГ центрифугируют до прозрачности в проточной центрифуге (фирма Westfalia ВКА28, Германия) и фильтруют через объемный фильтр (50 LA и 90LA, фирма Cuno, Франция), и затем фильтруют в стерильных условиях через фильтр 0,22 мкм (Durapore, Millipore, США). К отфильтрованной надосадочной жидкости с ПЭГ добавляется буфер так, чтобы 1 часть 0,45 М натрийацетатного буфера, рН 5,7, добавлялась к 29 частям надосадочной жидкости до достижения рН 5,7.
Стадия 4: Очистка с помощью последовательной анионообменной и катионообменной хроматографии (I):
Две хроматографические колонки заполняются 56 л ДЭАЭ-сефарозы FF® (фирма Pharmacia Biotech, Швеция) и 56 л КМ-сефарозы FF® (Pharmacia Biotech, Швеция), соответственно. Колонки соединяются последовательно, так что поток жидкости сначала проходит через смолу ДЭАЭ-сефароза, а затем через смолу КМ-сефароза. Смолы в колонках уравновешиваются 15 мМ натрийацетатным буфером, рН 5,7. Затем раствор со стадии 3 наносится на две колонки, соединенные последовательно.
Во время ионообменной хроматографии большинство загрязняющих белков в наносимых растворах связывается с ДЭАЭ-сефарозной смолой. В то же время IgG проходит, не связываясь с ДЭАЭ-сефарозной смолой, IgG соединяется с КМ-сефарозной смолой, когда раствор продвигается через колонку. После нанесения раствора и промывания буфером для уравновешивания в объеме, равном одному объему колонки, колонку с ДЭАЭ-сефарозой отсоединяют от колонки с КМ-сефарозой. Затем колонку с КМ-сефарозой промывают 15 мМ натрийацетатным буфером, рН 5,4, объемом, равным трем объемам колонки, затем IgG элюируют с градиентом NaCl от 125 до 350 мМ NaCl, 15 мМ ацетатом натрия, рН 5,4. Элюированную фракцию с IgG собирают в сорбите до конечной концентрации 2,5% по массе.
Стадия 5: Обработка растворителем/детергентом (Р/Д) фракции с IgG:
Элюированную фракцию с IgG концентрируют и обессоливают с помощью ультрафильтрации/диафильтрации до концентрации примерно 50 г IgG/л. Используемой мембраной является полисульфоновая мембрана с номинальным порогом массы 30 кДа (фирма Millipore). Диафильтрацию проводят против буфера, содержащего 15 мМ ацетата натрия, рН 5,4 и 2,5% по массе сорбита, и продолжают до тех пор, пока электропроводность становится меньше 1,4 мСм/см. Содержание IgG в растворе определяется спектрофотометрически путем измерения при 280 нм (A280). Концентрация сорбита доводится до 10% по массе и раствор фильтруется через фильтр 0,45 мкм (фирма Pall Corporation, Великобритания). Затем добавляют твин 80 и ТНБФ до конечной концентрации в 1% и 0,3% по массе, соответственно, для дальнейшей Р/Д-обработки. Р/Д-обработка продолжается, как минимум, 6 часов при 25oС.
Стадия 6: Удаление Р/Д с помощью ионообменной хроматографии (II):
Две последовательно соединенные колонки, заполненные 28 л ДЭАЭ-сефарозы FF и 56 л КМ-сефарозы FF, соответственно, уравновешивают 15 мМ ацетатом натрия, рН 5,4. Обработанную растворителем/детергентом (Р/Д) фракцию с IgG со стадии 5 разбавляют 5 частями 15 мМ ацетатного буфера, рН 5,4, фильтруют через объемный фильтр (Cuno 90 LA) и затем фильтруют в стерильных условиях (Sartobran, Sartorius), и наносят на две последовательно соединенные колонки. Ионообменную хроматографию и последующее элюирование IgG с колонки с КМ-сефарозой проводят, в основном, как описано на стадии 4, за исключением того, что колонка с КМ-сефарозой интенсивно промывается буфером в объеме, равном 6 объемам колонки, для удаления веществ после Р/Д-обработки. Элюированную фракцию с IgG собирают в мальтозе (фирма Merck, Германия) до конечной концентрации в 2,5% по массе.
Стадия 7: Окончательное концентрирование и приготовление лекарственной формы иммуноглобулина для внутривенного применения:
Элюированную фракцию с IgG после стадии 6 подвергают ультрафильтрации и обессоливанию путем диафильтрации против 7,5 мМ ацетата натрия, содержащего 2,5% мальтозы по массе, рН 5,4, до конечной электропроводности менее чем 1 мСм/см. Используемой мембраной является полисульфоновая мембрана с номинальным массовым порогом в 100 кДа, позволяющая удалять белки с меньшей молекулярной массой. Конечная концентрация IgG доводится до 50 г/л, а мальтоза доводится до конечной концентрации в 10% (м/о). Конечный препарат с установленной концентрацией мальтозы фильтруется через стерильный фильтр (Sartopure GF 2, Sartorius) и разливается в асептических условиях.
Пример 2
Результаты аналитического изучения продукта, полученного описываемым способом, по сравнению с другими продуктами ИГВВ (см. табл.1).
Чистота (белковый состав)
В соответствии с требованиями фармакопеи чистота препарата ИГВВ составляет, как минимум, 95% IgG, что соответствует присутствию не более 5% белков, не относящихся к IgG. Чистота имеет очень важное значение по ряду причин. С рациональной точки зрения, должен присутствовать только белок, исполняющий желательную функцию, и другие загрязняющие белки могут быть потенциально вредными, например, вызывать нежелательные побочные эффекты и/или влиять на стабильность продукта.
Чистота может быть, например, проанализирована с помощью электрофоретической методики, как подробно описано в Ph. Eur., 1997, стр.964-965, где белки отделяются в целлюлозно-ацетатном геле. Для практических целей, однако, применяется агарозный гель. После электрофореза гель фиксируют, сушат и окрашивают. Белковые полосы регистрируют при сканировании. Из табл.1 следует, что продукт по изобретению в действительности чистый (99,8%).
Альбумин
Содержание альбумина анализировали с помощью перекрестного иммуноэлектрофореза, по существу, как описано С.В. Laurell (Anal. Biochem. (1965), 10, 358-361). Анализировали 5 мкл продукта при помощи антител против человеческого альбумина (DAKO A/S, Дания, No. A0001 (1/100)). Благодаря высокой чистоте, альбумин не определялся в анализируемом продукте по изобретению.
Содержание мономеров и димеров IgG
Содержание мономеров и димеров IgG может быть проанализировано с помощью гель-проникающей хроматографии и определено на хроматограмме путем интегрирования площадей пика мономера и димера, см. Ph.Eur. Результаты различных анализов приведены в табл.1, из которой видно, что сумма площадей мономер + димер составляет 99,3% от общей площади хроматограммы (из которой мономерный IgG составляет 92%) продукта по изобретению.
Содержание полимеров и агрегатов
Известно, что присутствие полимеров и агрегатов является причиной серьезных побочных эффектов, часто симптомов, подобных симптомам эпидемического гриппа. Благодаря очень высокой степени чистоты, достигнутой при довольно простом способе получения, иммуноглобулиновый продукт, получаемый способом по изобретению, в значительной степени свободен от полимеров и агрегатов.
Полимеры могут быть проанализированы с помощью гель-проникающей хроматографии, и любые пики белков с временем удерживания короче, чем время удерживания для димерного IgG, считаются пиками от полимеров, как описано в Ph. Eur.
Согласно Ph. Eur. и другим руководствам, содержание белковых агрегатов должно предпочтительно быть менее 3%. Продукт по данному способу содержит неизмеряемые агрегаты, и, таким образом, считается, что он содержит менее 0,1% полимеров и агрегатов.
Антикомплементарная активность (АКА) и активность прекалликреинового активатора (ПКА)
АКА и ПКА измеряют, как описано в Ph. Eur.
АКА предпочтительно должна быть насколько возможно низкой. Согласно Ph. Eur. расход комплемента должен быть менее или равен 50%. Расход комплемента измеренного образца продукта по изобретению около 30%, то есть сравним с таковым других анализируемых продуктов. Следует заметить, что присутствие альбумина имеет тенденцию сдерживать расход комплемента (наблюдение заявителя).
ПКА, если наблюдается в значительной мере, характерна для гипотензивного побочного эффекта продукта. Поэтому ПКА предпочтительно должна быть насколько возможно низкой в иммуноглобулиновом продукте. Согласно Ph.Eur., она должна быть <35 МЕд/мл при измерении, как указано в Ph. Eur. ПКА продукта по изобретению, а также других проанализированных продуктов меньше, чем уровень количественной оценки метода, то есть ниже 8,5 МЕд/мл.
Гемагглютинин
Содержащая IgG фракция иммуноглобулинов плазмы включает гемагглютинины, которые являются антителами против антигенов крови типа А и В. Присутствие таких антител может вызвать нежелательные побочные эффекты вследствие возможной гемолитической реакции, если реципиент является носителем крови типов А и/или В.
Согласно требованиям фармакопеи содержание гемагглютининов должно быть ниже, чем вызывающее агглютинацию А/В эритроцитов при разведении иммуноглобулинового продукта 1: 64. Все проанализированные продукты удовлетворяют этому требованию.
Fc-функция
Сохраняемая активность связывания антигена необходима для биологических функций ИГВВ. Это также верно для иммуномодулирующей активности. С другой стороны, сохраненная Fc-функция необходима для воздействия ИГВВ на различные фагоцитарные клетки и активации системы комплемента. Fс-функция может быть продемонстрирована при использовании различных методик, но принятая методология, описанная в Ph.Eur., измеряет активирующий комплемент потенциал антител в препарате против антигена краснухи. Активность сравнивается с активностью для биологического эталонного препарата (BRP, Ph. Eur.) иммуноглобулинов, принятой за 100%. Продукт соответствует тесту, если относительная активность более 60% от эталонного препарата. Оказывается, что Fc-функция продукта по изобретению очень хорошо сохраняется, в особенности, по сравнению с другим анализируемым жидким продуктом, наиболее вероятно благодаря мягкому способу очистки.
Распределение подклассов
Распределение подклассов IgG измеряется с помощью стандартного метода иммунодиффузии Манчини, в основном, как описано A.Ingild (Scand.J.Immunol., (1983), 17, 41). Концентрации определяют при использовании эталона сыворотки Всемирной организации здравоохранения (ВОЗ) (67/97). Требуется, чтобы распределение подклассов было бы в пределах нормальной человеческой плазмы со средними концентрациями в диапазоне 3,7-10,2 г IgGl/л сыворотки, 1,1-5,9 г IgG2/л сыворотки, 0,15-1,3 г IgG3/л сыворотки и 0,06-1,9 г IgG4/л сыворотки (R. Djurup et al. , Scand.J.Clin.Lab.Invest. 48, 77-83). Таким, образом, распределение подклассов всех продуктов приемлемо.
Содержание IgA
Известно, что присутствие IgA потенциально вызывает сенсибилизацию реципиентов с дефицитом IgA. Если больной с дефицитом IgA получает содержащий IgA иммуноглобулиновый препарат, IgA может рассматриваться как чужеродный антиген и результатом может быть индукция антител против IgA у реципиента. В следующий раз при инфузии больному, содержащему IgA препарат, может быть спровоцирована анафилактическая реакция. Поэтому необходимо, чтобы иммуноглобулиновый препарат содержал насколько возможно мало IgA. IgA в продукте ИГВВ может регулироваться с применением метода иммуноферментного твердофазного анализа (ELISA), например, когда используют поликлональный анти-IgA для захвата IgA и используют меченый анти-IgA для определения связанного IgA. Стандарты получают путем разведения эталона для калибровки ( Х908, DAKO A/S, Дания) с заявленным содержанием IgA.
Продукт, полученный способом, описанным в примере 1, содержит менее 2 мг IgA/л, что является значительно более низким содержанием IgA, чем содержание в другом анализируемом жидком продукте. Сходство физико-химических свойств IgG и IgA создает трудности для разделения этих иммуноглобулинов в процессе очистки. Однако две стадии анионо/катионообменной хроматографии в данном способе понижают содержание IgA до очень низкого уровня.
Содержание IgM
IgM при получении иммуноглобулинов может контролироваться с применением метода ELISA, например, когда используется поликлональный анти-IgM для захватывания IgM и меченый анти-IgM используется для детектирования. Стандарты получают разведениями эталона для калибровки ( Х908, DAKO A/S, Дания) с заявленным содержанием IgM. Из таблицы следует, что содержание IgM в продукте по изобретению является очень низким и заметно ниже, чем содержание в другом жидком продукте.
Твин 80, ТНБФ и ПЭГ
Твин 80, ТНБФ и ПЭГ измеряются с помощью стандартных методик. В целом, содержание этих добавок должно быть насколько возможно низким.
рН анализируемых жидких продуктов является кислым, рН 5,6-5,7, в то время как анализируемые лиофилизованные продукты являются нейтральными после растворения с рН 6,7.
Общая концентрация белка
В соответствии с Ph.Eur. концентрация белка должна быть, как минимум, 50 г/л ± 10%; все продукты удовлетворяют требованию. Концентрация белка измеряется методом Кьельдаля.
Мальтозные и глюкозные стабилизаторы
Сахариды являются обычно используемыми стабилизаторами иммуноглобулиновых продуктов, они обладают хорошими стабилизирующими свойствами и быстро выделяются. Содержание мальтозы, сахарозы и глюкозы определяется с применением коммерческого набора (фирмы Boehringer Mannheim, Германия) с мальтозой в качестве эталона.
Оказывается, что два лиофилизованных продукта, стабилизированных альбумином и альбумином, а также ПЭГ, соответственно, также содержат сахаридный стабилизатор в концентрации от 15 мг/мл до 20 мг/мл. Продукт по изобретению и другой жидкий продукт стабилизируются почти одинаково, то есть с помощью примерно 9%, 88 мг/мл и 92 мг/мл мальтозы. Рассматривая содержание полимеров и агрегатов в качестве параметра стабильности, продукт по изобретению имеет более высокую стабильность, чем другой анализируемый жидкий продукт, хотя технологии приготовления из них лекарственных средств очень похожи.
Пример 3
Результаты клинических испытаний
Клинические испытания продукта по настоящему изобретению также указанного как ИГВВ, SSI, проводят в соответствии с нормами ICH и СРМР/388/95.
Изучены фармакокинетика, эффект и безопасность. Клинические исследования до настоящего времени включали четыре группы больных: больные с первичным синдромом иммунологической недостаточности (15 больных), с вторичным синдромом иммунологической недостаточности (6 больных), с тромбоцитопенической пурпурой неясного происхождения (15 больных) и больные с хронической воспалительной демиелинизирующей полиневропатией (5 больных).
Больных с первичным синдромом иммунологической недостаточности или вторичным синдромом иммунологической недостаточности обрабатывали 0,2-0,4 г/кг с интервалами в 2-5 недель. Больных с тромбоцитопенической пурпурой неясного происхождения обрабатывали 400 мг/кг в день в течение пяти дней или 1000 мг/кг в день в течение двух дней.
В качестве мер безопасности у всех больных определяли трансаминазы сыворотки, креатинин сыворотки и вирусные маркеры. У пяти больных с тромбоцитопенической пурпурой неясного происхождения следили за вирусом, маркерами безопасности почек и печени в течение вплоть до 24 недель в общей сложности.
Фармакокинетика
T1/2 измеряли до 30,5 дней (среднее значение). Это находится в соответствии с результатами для других лекарственных средств ИГВВ.
Эффект
Для больных с первичным и вторичным синдромами иммунологической недостаточности дни, потерянные из-за болезни, госпитализации, дни лечения антибиотиками, дни с температурой и число пневмоний регистрировались ретроспективно за период в 6 месяцев, в который больных лечили другими зарегистрированными лекарственными средствами ИГВВ. В последующие 6 месяцев, во время которых больных лечили иммуноглобулином SSI, жидким, регистрировались те же самые параметры.
Выводом является то, что иммуноглобулин SSI, жидкий, так же эффективен, как другие композиции ИГВВ для профилактики/предотвращения инфекций у больных с первичным и вторичным синдромами иммунологической недостаточности.
У 80% больных с тромбоцитопенической пурпурой неясного происхождения число тромбоцитов повышалось от <30•109/л до лечения иммуноглобулином SSI, жидким до ≥50•109/л после лечения. Увеличение подсчитанных тромбоцитов и продолжительность ремиссии у отдельного больного были на таком же уровне, как после введения такой же дозы других лекарственных средств ИГВВ, в случаях, когда сравнение было возможно. Один больной, получавший ИГВВ в первый раз, был невосприимчив к исследуемому лекарству. Такая реакция на ИГВВ не является редкой и, таким образом, неудивительна. Частные вопросы повышения тромбоцитов и продолжительности подъема находятся в процессе разработки.
Можно заключить, что иммуноглобулин SSI, жидкий, так же эффективен, как другие лекарственные средства ИГВВ при лечении низкого уровня тромбоцитов у больных с хронической тромбогенной пурпурой неясного происхождения.
По данным клиницистов и у больных, страдающих хронической воспалительной демиелинизирующей полиневропатией, ИГВВ, SSI показал эффективность, идентичную эффективности ИГВВ, введенного до испытания. ИГВВ, SSI переносился больными так же хорошо, как переносились больными и другие продукты ИГВВ.
Безопасность
Кроме одного серьезного побочного явления, спленэктомии, оцененной исследователем, как не имеющей отношения к испытываемому препарату, были зарегистрированы только незначительные побочные явления. Этими побочными эффектами были, главным образом, головная боль, повышение температуры и рвота. Насколько известно, не было сообщений об аномальных, опасных для жизни симптомах при введении ИГВВ, SSI. Не было зарегистрировано никаких вирусных сероконверсий. Не было никаких сообщений о поражениях почек или печени или случаях анафилактического шока.
Клинические исследования показывают, что иммуноглобулин SSI, жидкий, хорошо переносится. Частота побочных эффектов, степень и виды не отклоняются от случаев с другими лекарственными средствами ИГВВ.
Пример 4
Результаты изучения стабильности жидкого ИГВВ
Для того чтобы проанализировать, является ли жидкий продукт ИГВВ стабильным во времени, было проведено исследование в реальном времени в реальных условиях. В общей сложности 4 последовательные партии (250 мл каждого образца) продукта ИГВВ были вовлечены в исследование и хранились при температуре 2-8oС в течение, как минимум, 12 месяцев. Образцы от четырех партий анализировались в время ноль, после 6 месяцев хранения и 12 месяцев хранения. Результаты исследования представлены ниже как средние значения от четырех партий (см. табл. 2).
Все указанные выше испытания проводились в соответствии с Ph.Eur, и как описано в примере 2.
Наблюдение, что содержание мономеров и димеров постоянно в течение периода в 12 месяцев, указывает, что в образце не образуются полимеры. Известно, что присутствие иммуноглобулиновых полимеров, среди прочего, является причиной серьезных побочных эффектов, часто симптомов, напоминающих грипп. Вследствие очень высокой стабильности иммуноглобулинового продукта, получаемого способом по изобретению, продукт в высокой степени свободен от полимеров и агрегатов, даже после длительного периода хранения.
Не наблюдается никакого повышения АКА во времени, хотя партии, проявляющие довольно высокую АКА, преднамеренно были включены в это изучение стабильности. Если бы наблюдалось увеличение АКА, то это могло указывать, что агрегаты образовывались во время хранения. Таким образом, постоянная АКА на протяжении времени указывает, что агрегаты не образуются.
Далее результаты показывают, что во время хранения продукта не развивается активность прекалликреинового активатора, так как активность ПКА не возрастает. Следует отметить, однако, что измеренные значения ниже уровня низшей количественной оценки.
Измерение Fc-функции указывает, что присутствие интактного функционального IgG поддерживается при хранении. Таким образом, никакие протеазы не присутствуют в образцах, так как они разлагали бы белки и тем самым понижали Fc-функцию. Денатурация молекул IgG также не происходит, так как это понижало бы активность связывания антигена.
Как известно специалисту в данной области, могут быть различия в стабильности различных подклассов IgG. Как можно видеть из представленных результатов, все подклассы сохраняются при хранении, что указывает на стабильность продукта. Это, кроме того, подтверждается полученным результатом, что белковый состав IgG в образцах с примерно одинаковой общей концентрацией белка остается почти неизменным в течение времени, указывая на то, что разложения IgG в целом нет, то есть продукт по настоящему изобретению стабилен и может храниться не менее 12 месяцев при 2-8oС без значительных изменений характеристик, и при этом демонстрируется эффективность и безопасность.
Пример 5
Подтвержденные стадии уменьшения титра вируса в представленном способе получения ИГВВ
Удаление вируса с помощью стадии распределения
Осаждение вируса, присутствующего в растворе иммуноглобулина, с помощью полиэтиленгликоля.
Подтверждающие исследования с вирусами были проведены при использовании двух малых безоболочечных вирусов, и были получены следующие уменьшения уровня вирусов:
удаление 6,3 log10 вируса гепатита A (HAV);
удаление 1,2 log10 вируса полиомиелита.
Подтверждающие исследования с вирусами были проведены с использованием двух вирусов с оболочкой, и были получены следующие уменьшения уровня вирусов:
удаление 7,6 log10 вируса иммунодефицита человека (ВИЧ);
удаление 7,5 log10 BVDV.
Инактивация вирусов с помощью стадии обработки растворителем/детергентом
Обработка раствора иммуноглобулина 1% твина 80+0,3% ТНБФ, при 25oС в течение ≥ 6 часов.
Подтверждающие исследования с вирусами были проведены с использованием четырех вирусов с оболочкой, и были получены следующие уменьшения уровня вирусов:
инактивация 7,4 log10 ВИЧ;
инактивация 5,3 log10 вируса Синдбис;
инактивация 4,1 log10 BVDV;
инактивация 5,1 log10 PRV.
Всего было проведено 8 подтверждающих исследований на двух различных стадиях способа по настоящему изобретению. Стадия осаждения с помощью ПЭГ была подтверждена как стадия удаления вируса при использовании четырех различных вирусов, двух малых безоболочечных вирусов, вируса гепатита А (HAV) и вируса полиомиелита, и двух вирусов с оболочкой, ВИЧ и BVDV в качестве модели вируса гепатита С. Эти исследования показали, что все четыре вируса были эффективно удалены при осаждении с помощью ПЭГ. Поэтому стадия осаждения с применением ПЭГ подтверждена как эффективная стадия удаления вируса. Стадия обработки растворителем/детергентом была подтверждена с использованием четырех различных вирусов с оболочкой. Из данных, подтверждающих исследования ясно, что стадия обработки растворителем/детергентом эффективно инактивировала все четыре вируса. Поэтому стадия Р/Д-обработки подтверждается в качестве стадии эффективной инактивации вируса. Было подтверждено, что каждая из двух стадий уменьшения титра вирусов в способе получения ИГВВ, как осаждение с помощью ПЭГ, так и инактивация путем Р/Д-обработки, эффективна для удаления и инактивирования четырех различных вирусов. Совокупные факторы уменьшения титра ВИЧ и BVDV в способе составляют 15 и 11,6, соответственно. Благодаря этому, продукт по настоящему способу может рассматриваться как вирус-безопасный.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ РАСТВОРА ГАММА-ГЛОБУЛИНА, ПРЕДНАЗНАЧЕННОГО ДЛЯ ВНУТРИВЕННОГО ВВЕДЕНИЯ, И ПРОДУКТ, ПОЛУЧАЕМЫЙ ЭТИМ СПОСОБОМ | 1998 |
|
RU2198668C2 |
| Способ получения иммуноглобулинов | 2016 |
|
RU2708394C2 |
| ОЧИСТКА И ПРИМЕНЕНИЕ ФАКТОРА, СПОСОБСТВУЮЩЕГО ЗАЖИВЛЕНИЮ РАН | 2007 |
|
RU2520817C2 |
| ПРЕПАРАТ ИММУНОГЛОБУЛИНА IgG И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2005 |
|
RU2337109C2 |
| ПОЛУЧЕНИЕ ИММУНОГЛОБУЛИНОВ С ПОНИЖЕННЫМ СОДЕРЖАНИЕМ ТРОМБОГЕННЫХ АГЕНТОВ И ИММУНОГЛОБУЛИНОВАЯ КОМПОЗИЦИЯ | 2012 |
|
RU2627162C2 |
| УЛУЧШЕНИЕ АФФИННОЙ ХРОМАТОГРАФИИ ИММУНОГЛОБУЛИНОВ ПУТЕМ ПРИМЕНЕНИЯ ФЛОКУЛЯЦИИ ДО ЗАХВАТА | 2020 |
|
RU2794431C1 |
| СПОСОБ ОЧИСТКИ ИММУНОГЛОБУЛИНА (ВАРИАНТЫ) | 2007 |
|
RU2332247C1 |
| Способ получения гомологического иммуноглобулина против COVID-19 | 2022 |
|
RU2792819C1 |
| СПОСОБ ОЧИСТКИ РАСТВОРА АЛЬФА-1-АНТИТРИПСИНА | 2004 |
|
RU2370500C2 |
| СПОСОБ ПОЛУЧЕНИЯ КОМПОЗИЦИИ ИММУНОГЛОБУЛИНОВ | 2011 |
|
RU2612899C2 |
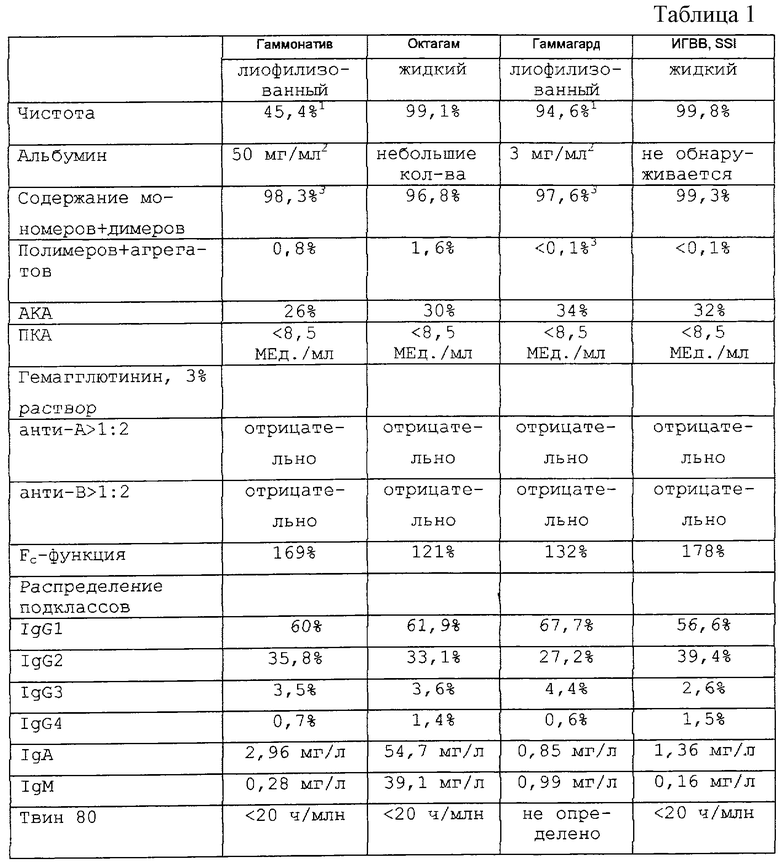
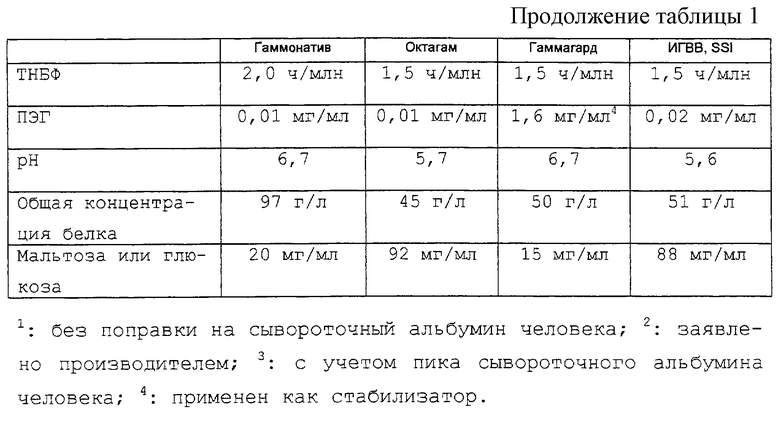
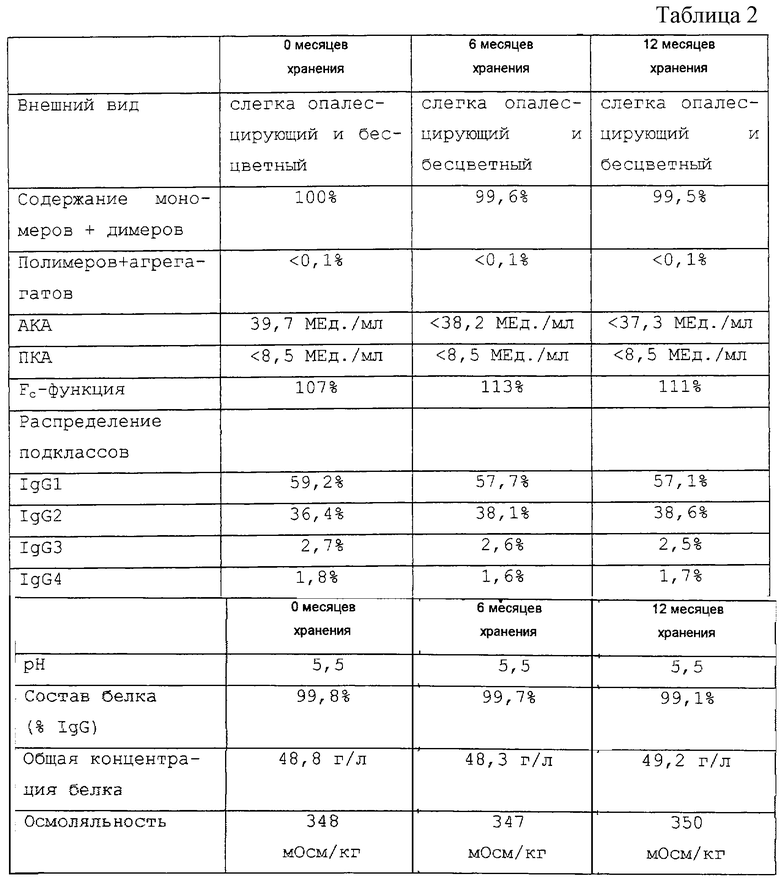
Изобретение относится к способу очистки иммуноглобулина G из содержащей иммуноглобулин белковой фракции сырой плазмы. Указанный способ включает ряд стадий, из которых анионообменная хроматография и катионообменная хроматография предпочтительно соединены последовательно. Предпочтительно в способе очистки используется ацетатный буфер с рН примерно 5,0-6,0 и с молярностью примерно 5-25 мМ. Изобретение далее включает высокоочищенный нативный иммуноглобулиновый продукт, получаемый указанным способом. Изобретение также относится к иммуноглобулиновому продукту, который имеет чистоту более 98%, содержание мономеров и димеров IgG более 98,5%, содержание IgA менее 4 мг IgA/л и содержит менее 0,5% полимеров и агрегатов. Указанный продукт не включает детергент, ПЭГ или альбумин в качестве стабилизатора. Продукт стабилен, безопасен в отношении вирусной активности, является жидким и пригоден для непосредственного внутривенного введения. 4 с. и 21 з.п. ф-лы, 2 табл.
9. Способ по любому из предшествующих пунктов, где катионообменная смола на стадии (d) и/или стадии (i) содержит карбоксиметильные группы, являясь предпочтительно такой смолой, как КМ-сефароза FF®.
10. Способ по любому из предшествующих пунктов, где буфером, используемым везде на стадиях от (b) до (l), является ацетатный буфер, как, например, ацетатный буфер с рН 5,0-6,0 и имеющий молярность 5-25 мМ.
Приоритет по пунктам:
09.06.1998 - по пп. 1-14;
28.09.1998 - по пп. 15-25.
| Пюпитр для работы на пишущих машинах | 1922 |
|
SU86A1 |
| МОНОКЛОНАЛЬНЫЙ ИММУНОГЛОБУЛИН ЧЕЛОВЕКА КЛАССА IGGI ПРОТИВ АНТИГЕНА D СИСТЕМЫ РЕЗУС | 1995 |
|
RU2094462C1 |
| US 4606825 A, 19.08.1986 | |||
| JP 3271234 A2, 03.12.1991. | |||
Авторы
Даты
2003-01-27—Публикация
1999-06-09—Подача