ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение в целом относится к обработке органов ex vivo и, в частности, к таким обработкам органов ex vivo, которые способны ингибировать или предотвращать тромбовоспаление и гипотонию, вызванную реперфузией органов.
УРОВЕНЬ ТЕХНИКИ
Ишемически-реперфузионное (И/Р) повреждение (ИРП) является основным фактором, вносящим вклад в патологию некоторых состояний, включая трансплантацию, тромботические расстройства, сепсис и сердечно-легочное шунтирование, все из которых вызывают тромбовоспаление.
На сегодняшний день трансплантация почки является наиболее эффективным лечением для пациентов с терминальной стадией почечной недостаточности. Несмотря на впечатляющее улучшение результатов лечения по сравнению с внедрением в 1960 г, по-прежнему возникает утрата трансплантата у 25 % пациентов через 5 лет и почти у 50 % - через 10 лет. Основной мишенью для улучшения результатов трансплантации почки является ИРП, поскольку ИРП вызывает острую почечную недостаточность, отсроченную функцию трансплантата и недостаточность отдаленных органов. Иммуносупрессия не влияет в значительной степени на гуморальную врожденную иммунную систему и, следовательно, не уменьшает ИРП. В области трансплантации также есть сложность, связанная с нехваткой органов. Одним вариантом для увеличения донорского пула является более частое использование органов пограничной пригодности, таких как органы из доноров, скончавшихся после смерти сердца. Тем не менее, данные органы также тяжело поражены ИРП.
Во время ишемии метаболизм переключается в анаэробное состояние, которое, в конечном счете, приводит к воспалительному состоянию, которое запускается повышенной и пониженной регуляцией множества генов, включая ядерный фактор энхансер легких цепей каппа активированных B-клеток (NF-κB), и посредством него цитокинов, хемокинов и тканевого фактора (TF), но также генов, которые защищают от ишемии, таких как гемоксигеназа 1 (HO-1), индуцируемые гипоксией факторы (HIF) 1 и 2 и нитротирозин. При условиях с нормальным содержанием кислорода поверхность эндотелиальных клеток покрыта отрицательно заряженной “волосатой” сетью, называемой гликокаликсом (GCX), которая содержит сложную сеть протеогликанов, гликозаминогликанов и гликопротеинов, которая содержит противовоспалительные и антикоагулянтные белки, чтобы гарантировать микрососудистый гомеостаз и предотвратить тромбовоспаление. Более того, толстый GCX защищает поверхность клетки и молекулы адгезии, такие как молекула межклеточной адгезии 1 (ICAM-1), молекула адгезии сосудистого эндотелия 1 (VCAM-1) и E-селектин, тем самым предотвращая привлечение лейкоцитов и тромбоцитов к поверхности эндотелия. GCX очень чувствителен к окислительному стрессу и вызванному ишемией структурному повреждению, что часто приводит к быстрой утрате покрытия GCX. Это вызывается экспрессией гепариназы и металлопротеиназы в выстилке эндотелиальных клеток, что приводит к расщеплению и разрушению GCX, который защищает эндотелиальные клетки от атаки врожденной иммунной системы. GCX содержит множество факторов роста, таких как фактор роста гепатоцитов (HGF) и фактор роста эндотелия сосудов (VEGF), которые при этом высвобождаются во время распада GCX. Это также будет приводить к тому, что регуляторы систем комплемента, свертывания и контактов будут высвобождаться с поверхности клетки. Такие регуляторы представляют собой, например, антитромбин (AT), белок C, ингибитор пути тканевого фактора (TFPI), C4b-связывающий белок (C4BP), фактор H и C1-ингибитор (C1-INH), в результате чего поверхность эндотелиальных клеток будет не защищена от атак системами комплемента, свертывания и контактов. Наконец, если ишемия затягивается, запасы аденозинтрифосфата (АТФ) исчерпываются, приводя к апоптозу и некрозу.
Реперфузия ишемического органа вызывает процесс восстановления, но изначально он запускает губительное повреждение органа вследствие патологических изменений, уже вызванных ишемией. Быстрая оксигенация создает повреждения, включая образование активных форм кислорода (АФК), и незащищенная поверхность эндотелия запускает разрушительную активацию систем комплемента и контактов. При трансплантации экспрессированный коллектин-11/12 (CL-11/12) в трансплантате почки распознает ишемические клетки и способствует активации комплемента посредством лектинового пути (LP). Также другие распознающие молекулы, такие как связывающий маннозу лектин (MBL) и фиколин-2, пути LP были связаны с активацией комплемента. Доказательством активации комплемента служит депонирование C4d на эндотелиальных клетках в сочетании с депонированием мембраноатакующего комплекса (MAC) в околососудистой паренхиме, свидетельствующее о повреждении клеток в данных областях. Запущенное повышенной экспрессией TF и активацией системы контактов, депонирование фибрина показывает, что задействована система свертывания. В комбинации с активацией комплемента, повышенной экспрессией и воздействием фактора фон Виллебранда (vWF) с последующим связыванием и активацией тромбоцитов и полиморфоядерных нейтрофилов (ПМН) с поверхностью эндотелия вызывается тромбовоспаление. Большая часть этого тромбовоспаления запускается продуцированными локально факторами комплемента, что было явно продемонстрировано в модели трансплантации почки у мышей, в которой нокаут C3 защищал трансплантированный орган от отторжения.
Реперфузия трансплантированного органа также связана с гемодинамической нестабильностью после реперфузии. Данный феномен, который ранее был описан как постреперфузионный синдром (ПРС), впервые был описан у реципиентов трансплантата печени, которые испытывали сильную гемодинамическую нестабильность после реперфузии трансплантата печени. Тем не менее, данный феномен также наблюдали у реципиентов трансплантата почки и поджелудочной железы, которые часто страдают от моментальной гемодинамической нестабильности после реперфузии. В результате, быстрое снижение системного артериального давления приводит к нарушению перфузии трансплантата и продлению тепловой ишемии трансплантата. Данные пациенты могут страдать от отсроченной функции трансплантата, повышенного риска отторжения и преждевременной утраты трансплантата.
Амфифильный полимер полиэтиленгликоль-фосфолипид (конъюгированный с ПЭГ-фосфолипид, или просто ПЭГ-фосфолипид) спонтанно внедряется в липидный бислой мембраны клеток посредством гидрофобных взаимодействий [1, 2]. Более того, создание ПЭГ-фосфолипидом искусственного слоя на поверхности клетки может ослабить мгновенную опосредованную кровью воспалительную реакцию (IBMIR) и продлить как выживаемость, так и функцию островков после инфузии в воротную вену у мышей с диабетом [3, 6].
Ранее было показано, что ПЭГ-фосфолипид, конъюгированный с регуляторами врожденного иммунитета, такими как апираза и фактор H, защищает клетки и поверхности материала от атаки врожденной иммунной системой in vitro [4, 5].
Тем не менее, существует потребность в улучшениях применительно к трансплантации органов.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Главной целью является создание улучшений применительно к трансплантации органов.
Данная и другие цели удовлетворяются вариантами реализации, описанными в данной заявке.
Настоящее изобретение определяется независимыми пунктами формулы изобретения. Дополнительные варианты реализации настоящего изобретения определяются зависимыми пунктами формулы изобретения.
Способ лечения ex vivo органа или части органа включает инфузию ex vivo раствора, содержащего молекулы ПЭГ-фосфолипида, в сосудистую систему органа или части органа. Указанный способ также включает инкубацию ex vivo раствора, содержащего молекулы ПЭГ-фосфолипида, в сосудистой системе, чтобы обеспечить покрытие по меньшей мере части эндотелиальной выстилки сосудистой системы молекулами ПЭГ-фосфолипида, при этом выдерживая орган или часть органа погруженными в раствор для консервации органов, содержащий молекулы ПЭГ-фосфолипида.
В соответствии с настоящим изобретением также предложен ПЭГ-фосфолипид для применения для ингибирования или предотвращения гипотонии, связанной с реперфузией, развившейся после реперфузии трансплантата органа в субъекте-реципиенте.
В трансплантате органа ex vivo, обработанном молекулами ПЭГ-фосфолипида, наблюдали значительно меньшее тромбовоспаление по сравнению с необработанными контрольными трансплантатами органов, судя по уровням в плазме маркеров свертывания, таких как TAT, и маркеров комплемента, таких как C3a и sC5b-9. Также экспрессия цитокинов, в частности, IL-6 и IL-1β, значительно подавлялась в обработанных ПЭГ-фосфолипидом трансплантатах органов. Функционирование органа улучшалось в обработанных ПЭГ-фосфолипидом трансплантатах органов. В обработанных ПЭГ-фосфолипидом трансплантатах органов также выявили сниженное депонирование маркеров комплемента, таких как C3b и MAC, и экспрессию C5aR. Весьма неожиданно, но значимо с медицинской точки зрения, влияние обработки ex vivo трансплантата органа молекулами ПЭГ-фосфолипида было таким, что такая обработка ПЭГ-фосфолипидом была способна снизить губительное падение артериального давления у реципиента, которое часто связано с реперфузией трансплантата органа. Более того, после 4 суток обработка ПЭГ-фосфолипидом была способна снизить повышение количества зависимых от T-клеток цитокинов IL-4 и IL-12, которые связаны с активацией приобретенного иммунного ответа.
КРАТКОЕ ОПИСАНИЕ ФИГУР
Варианты реализации вместе с дополнительными их объектами и преимуществами, лучше всего будут понятны при обращении к следующему описанию вместе с сопроводительными фигурами, на которых:
На фиг. 1 схематически показан механизм гидрофобного взаимодействия молекулы ПЭГ-липида с липидными бислоями мембран клеток.
На фиг. 2A - 2C проиллюстрировано влияние различных функциональных групп ПЭГ-фосфолипида на свертывание крови (фиг. 2A) и комплемент (фиг. 2B и 2C), когда покрытые мезенхимальные стволовые клетки (МСК) анализировали в модели петли Чендлера in vitro по сравнению с контролем (непокрытыми клетками).
На фиг. 3 показана концентрация жидкой фазы в течение 60 мин во время перфузии 25 мл 2 мг/мл FITC-ПЭГ-фосфолипида. Кругами обозначено без подсоединенной почки и квадратами обозначено с подсоединенной почкой. Рассчитанное поглощение ПЭГ-фосфолипида составляло 76 %.
На фиг. 4A - 4F проиллюстрированы биоптаты, извлеченные из контрольных и обработанных почек в момент времени 5 мин (фиг. 4A: контроль, фиг. 4B: обработанный), 60 мин (фиг. 4C: контроль, фиг. 4D: обработанный) и 360 мин (фиг. 4E: контроль, фиг. 4F: обработанный) после реперфузии. Почки подвергали перфузии раствором биотин-ПЭГ-фосфолипид и подтверждение покрытия эндотелия почки ПЭГ-фосфолипидом осуществляли путем контрастного окрашивания стрептавидином-488. Срезы анализировали с помощью конфокальной микроскопии.
На фиг. 5A - 5E проиллюстрирована активация комплемента в модели кратковременной аллогенной трансплантации почки свиньи. Депонирование фиг. 5A C3a, фиг. 5B sC5b-9, фиг. 5C C4d, фиг. 5D C3b и фиг. 5E MAC из плазмы в биоптатах из почки. Квадраты и столбики со стрелками обозначают обработанные ПЭГ-фосфолипидом почки и круги и столбики без стрелок обозначают необработанный контроль. * p<0,05; ** p<0,01; *** p<0,001; **** p<0,0001.
На фиг. 6A - 6D проиллюстрирована активация свертывания в модели кратковременной аллогенной трансплантации почки. Фиг. 6A TAT, фиг. 6B TF, фиг. 6C FXII/AT и фиг. 6D FXII/C1INH в плазме. Квадраты обозначают обработанные ПЭГ-фосфолипидом почки и круги обозначают необработанный контроль. * p<0,05; ** p<0,01; *** p<0,001.
На фиг. 7A - 7C проиллюстрирована концентрация провоспалительных цитокинов в модели кратковременной аллогенной трансплантации почки. Фиг. 7A IL-1β, фиг. 7B IL-6 и фиг. 7C TNF в плазме. Квадраты обозначают обработанные ПЭГ-фосфолипидом почки и круги обозначают необработанный контроль. * p<0,05; ** p<0,01.
На фиг. 8A - 8C проиллюстрирована активация комплемента и свертывания в модели долговременной аллогенной трансплантации почки. Фиг. 8A C3a, фиг. 8B sC5b-9 и фиг. 8C TAT в плазме. Квадраты обозначают обработанные ПЭГ-фосфолипидом почки и круги обозначают необработанный контроль. * p<0,05; ** p<0,01.
На фиг. 9A - 9L проиллюстрирована концентрация цитокинов/хемокинов в модели долговременной аллогенной трансплантации почки. Фиг. 9A INFγ, фиг. 9B IL-1β, фиг. 9C IL-1α, фиг. 9D IL-1R, фиг. 9E IL-2, фиг. 9F IL-4, фиг. 9G IL-6, фиг. 9H, IL-10, фиг. 9I IL-8, фиг. 9J IL-12, фиг. 9K IL-18 и фиг. 9L TNF в плазме. Квадраты обозначают обработанные ПЭГ-фосфолипидом почки и круги обозначают необработанный контроль.
На фиг. 10A и 10B проиллюстрирована функциональная оценка обработанной ПЭГ-фосфолипидом почки в модели кратковременной (фиг. 10A) и долговременной (фиг. 10B) аллогенной трансплантации почки. На фиг. 10A оценивали диурез и на фиг. 10B измеряли уровни креатинина. Квадраты обозначают обработанные ПЭГ-фосфолипидом почки и круги обозначают необработанный контроль. * p<0,05.
На фиг. 11 показана функциональная оценка в отношении компенсаторного повышения частоты пульса сразу после реперфузии у свиней, которым трансплантировали обработанные ПЭГ-фосфолипидом почки, по сравнению с животными, которым трансплантировали контрольные почки, в моделях долговременной аллогенной трансплантации почки. * p<0,05.
На фиг. 12 показано макроскопическое патоморфологическое исследование почек свиньи после (1) сбора, (2) статической гипотермической перфузии и (3) перфузии ПЭГ-фосфолипидом.
На фиг. 13 показано сохранение молекул ПЭГ-фосфолипида с различными длинами субъединицы ПЭГ (1 кДа - круги, 5 кДа - квадраты и 40 кДа - треугольники) при использовании клеток CCRF-CEM.
На фиг. 14 показан синтез [68Ga]NO2A-пропилазида.
На фиг. 15 показан синтез 68Ga-NO2A-ПЭГ-липида.
На фиг. 16A и 16B проиллюстрированы значения TAT и значения креатинина в плазме после инкубации почек свиньи в течение 24 часов в дополненном ПЭГ-фосфолипидом растворе HTK (обработанные) или только в растворе HTK (контроль) при 4°C.
На фиг. 17A - 17D проиллюстрирована активация комплемента и свертывания и уровни креатинина в модели долговременной аллогенной трансплантации почки: TAT (фиг. 17A), C3a (фиг. 17B), sC5b-9 (фиг. 17C) и креатинин (фиг. 17D) в плазме. Линии с квадратами обозначают обработанные ПЭГ-фосфолипидом почки и линии с кругами обозначают необработанный контроль. * p<0,05.
На фиг. 18A - 18G проиллюстрирована концентрация цитокинов/хемокинов в модели долговременной аллогенной трансплантации почки: IL-1β (фиг. 18A), IL-2 (фиг. 18B), IL-4 (фиг. 18C), IL-6 (фиг. 18D), IL-8 (фиг. 18E), IL-10 (фиг. 18F) и TNF (фиг. 18G) в плазме. Квадраты обозначают обработанные ПЭГ-фосфолипидом почки и круги обозначают необработанный контроль. * p<0,05.
На фиг. 19 показано поглощение 5 кДа ПЭГ-липида и 40 кДа ПЭГ-липида после инфузии молекул ПЭГ-липида в почки из четырех различных свиней, причем одну почку использовали для 5 кДа ПЭГ-липида, а другую - для 40 кДа ПЭГ-липида. Почки подвергали перфузии раствором FITC-ПЭГ-фосфолипид и визуализировали подтверждение покрытия эндотелия и паренхимы почки ПЭГ-фосфолипидом. Срезы анализировали с помощью конфокальной микроскопии.
На фиг. 20 показана возможность смешивать молекулы ПЭГ-липид с тремя широко применяемыми жидкостями для перфузии (HTK, IGL-1 и UW). Не наблюдали преципитацию в любой из данных смесей при концентрации ПЭГ-липида 2 мг/мл.
ПОДРОБНОЕ ОПИСАНИЕ изобретения
В настоящем изобретении в целом предложена обработка органов ex vivo и, в частности, такая обработка органов ex vivo, которая способна лечить, ингибировать или предотвращать тромбовоспаление, которое предшествует активации адаптивной иммунной системы и гипотонии, вызванной реперфузией органов.
Способ ex vivo согласно настоящему изобретению приводит к существенным улучшениям в трансплантации органов и обработке органов, обеспечивая защитное экранирование или покрытие эндотелиальной выстилки или эндотелия сосудистой системы и паренхимы таких органов или частей таких органов. Данное защитное покрытие формирует эффективную защиту от тромбовоспаления и вредного воздействия ишемически-реперфузионного (И/Р) повреждения (ИРП).
Гликокаликс необходим для обеспечения микрососудистого гемостаза и предотвращения тромбовоспаления. Этот гликокаликс, тем не менее, очень чувствителен к окислительному стрессу и вызванному ишемией повреждению. Следовательно, защитное покрытие гликокаликсом быстро утрачивается во время ишемии, которая возникает в связи со сбором органов и консервацией органов in vitro. После того, как трансплантат органа был трансплантирован и подвергнут реперфузии, запускается процесс восстановления, который начинает губительное повреждение трансплантата органа вследствие отсутствия или повреждения гликокаликса. Следовательно, активируется система комплемента и контактов. Тромбоциты поглощаются и лейкоциты становятся активированными и инфильтрируют трансплантат органа. Вследствие активации данных систем продуцируются цитокины, в конечном счете приводящие к гибели клеток и утрате трансплантата или отсроченной функции трансплантата. Такое губительное повреждение трансплантата органа представляет собой тромбовоспаление, которое, главным образом, запускается гуморальной врожденной иммунной системой, которая преимущественно состоит из каскадных систем крови, т.е., системы комплемента, контакта/свертывания крови и фибринoлитической системы. Активация данных систем впоследствии вызывает активацию эндотелиальных клеток, лейкоцитов и тромбоцитов, в конечном итоге приводящую к тромботическим и воспалительным реакциям.
Как показано в данной заявке, путем обработки ex vivo органа или части органа молекулами полиэтиленгликоля-фосфолипида (ПЭГ-фосфолипида), орган или часть органа можно защитить от тромбовоспаления. Следовательно, молекулы ПЭГ-фосфоpлипида способны связываться с мембранами клеток эндотелиальной выстилки сосудистой системы органа или части органа и посредством этого компенсировать утрату гликокаликса. Следовательно, молекулы ПЭГ-фосфолипида образуют защитное покрытие эндотелия, которое ингибирует или по меньшей мере значительно уменьшает вредное воздействие тромбовоспаления, включая более низкие уровни свертывания крови и активации комплемента, подавление экспрессии цитокинов и общее улучшение функции трансплантата.
В частности, обработка ex vivo органа молекулами ПЭГ-фосфолипида приводила к значительному снижению количества цитокинов, например, специфических для T-клеток цитокинов, включая интерлейкин 4 (IL-4) и IL-12. В необработанных контрольных органах наблюдался высокий уровень таких цитокинов в течение нескольких дней после трансплантации, который оказывал отрицательное влияние на продолжение иммунизации и будущее подавление иммунитета. Следовательно, покрытие эндотелия молекулами ПЭГ-фосфолипида ингибирует вызванные цитокинами эффекты и повреждения органа или части органа после трансплантации, а также улучшает результат подавления иммунитета после трансплантации.
Другим весьма неожиданным эффектом, достигнутым путем обработки ex vivo органов или частей органов молекулами ПЭГ-фосфолипида, было лечение, ингибирование или предотвращение гемодинамической нестабильности с повышенной частотой пульса и гипотонией, связанной с реперфузией, развившейся после реперфузии трансплантата органа. Такая гипотония, связанная с трансплантацией, может привести к плохой перфузии, органной недостаточности и даже привести к смерти пациента. Гипотония вызывается, когда трансплантат органа соединяют с сосудистой системой пациента и тем самым подвергают реперфузии. Лечение такой гипотонии на сегодняшний день является важной задачей при трансплантации органов, поскольку если гипотония не может быть вылечена, то существует значительный риск смерти пациента во время трансплантации. Тем не менее, путем обработки ex vivo трансплантата органа перед трансплантацией молекулами ПЭГ-фосфолипида гипотонию можно предотвратить или по меньшей мере значительно ингибировать или уменьшить. Следовательно, риск вызванных гипотонией повреждений, связанных с трансплантацией органов, снижается при применении молекул ПЭГ-фосфолипида согласно настоящему изобретению. Молекулы ПЭГ-фосфолипида согласно настоящему изобретению, следовательно, пригодны для лечения, предотвращения и/или ингибирования постреперфузионного синдрома (ПРС).
В конкретном аспекте настоящего изобретения, следовательно, предложен способ обработки ex vivo органа или части органа. Указанный способ включает инфузию ex vivo раствора, содержащего молекулы ПЭГ-фосфолипида, в сосудистую систему, и необязательно в паренхиму, органа или части органа. Указанный способ также включает инкубацию ex vivo раствора, содержащего молекулу ПЭГ-фосфолипида, в сосудистой системе, и необязательно в паренхиме, чтобы обеспечить покрытие по меньшей мере части эндотелиальной выстилки сосудистой системы, и предпочтительно паренхимы, молекулами ПЭГ-фосфолипида, при этом выдерживая орган или часть органа погруженными в раствор для консервации органов, содержащий молекулы ПЭГ-фосфолипида.
Таким образом, способ ex vivo включает введение молекул ПЭГ-фосфолипида в сосудистую систему органа или части органа и обеспечение возможности молекулам ПЭГ-фосфолипида там взаимодействовать и связываться с мембранами клеток эндотелия и паренхимы. На фиг. 1 схематически показан данный принцип с молекулами ПЭГ-фосфолипида, гидрофобно взаимодействующими с мембраной липидного бислоя эндотелия, чтобы тем самым заякорить или прикрепить молекулы ПЭГ-фосфолипида к клеточной мембране через фосфолипидную группу.
Взаимодействие между молекулами ПЭГ-фосфолипида и липидным бислоем мембраны эндотелия и необязательно паренхимы, такой как паренхима почки в случае почки, происходит ex vivo в то время как орган или часть органа погружена или залита раствором для консервации органов, содержащим молекулы ПЭГ-фосфолипида. Экспериментальные данные, представленные в данной заявке, свидетельствуют о том, что выдерживание органа погруженным в раствор для консервации органов, содержащий молекулы ПЭГ-фосфолипида, приводит к значительно меньшей активации системы каскада и экспрессии цитокинов по сравнению с выдерживанием органа или части органа погруженным только в раствор для консервации органов, в котором отсутствуют молекулы ПЭГ-фосфолипида, даже если сосудистая система, и необязательно паренхима, органа или части органа покрыта молекулами ПЭГ-фосфолипида.
Следовательно, для того чтобы добиться эффективной обработки ex vivo органов или частей органов, сосудистую систему, и необязательно паренхиму, органа или части органа нужно привести в контакт с молекулами ПЭГ-фосфолипида и орган или часть органа нужно погрузить в раствор для консервации органов, содержащий молекулы ПЭГ-фосфолипида. Антитромбовоспалительный эффект такой обработки ex vivo значительно улучшен по сравнению с инфузией ex vivo только раствора, содержащего молекулы ПЭГ-фосфолипида, в сосудистую систему, и необязательно в паренхиму, органа или части органа. В действительности, антитромбовоспалительные эффекты обработки ex vivo согласно настоящему изобретению уже были вызваны во время периода холодовой ишемии, когда орган или часть органа держали погруженной в раствор для консервации органов, содержащий молекулы ПЭГ-фосфолипида, т.е., еще до реперфузии органа или части органа.
В конкретном варианте реализации сначала осуществляют инфузию ex vivo в орган или часть органа раствора, содержащего молекулы ПЭГ-фосфолипида, в сосудистую систему, и необязательно в паренхиму, органа или части органа. Такая инфузия ex vivo предпочтительно происходит как можно раньше после эксплантации и удаления органа или части органа из организма донора. Подвергнутый перфузии орган или часть органа затем погружают в раствор для консервации органов, содержащий ПЭГ-фосфолипид, и выдерживают в нем, предпочтительно при пониженной температуре, такой как приблизительно 4°C, что обсуждается далее в данной заявке.
В другом конкретном варианте реализации орган или часть органа сначала погружают в раствор для консервации органов, содержащий молекулы ПЭГ-фосфолипида, а затем раствор, содержащий молекулы ПЭГ-фосфолипида, вводят путем инфузии ex vivo в сосудистую систему, и необязательно в паренхиму, органа или части органа. Такую инфузию ex vivo можно осуществить при выдерживании органа или части органа погруженными в раствор для консервации органов, содержащий молекулы ПЭГ-фосфолипида. В качестве альтернативы, орган или часть органа временно удаляют из раствора для консервации органов для осуществления инфузии ex vivo, а затем помещают обратно в раствор для консервации органов, содержащий молекулы ПЭГ-фосфолипида.
В одном варианте реализации указанный способ также включает инфузию ex vivo раствора для консервации органов в сосудистую систему, чтобы вымыть несвязавшиеся молекулы ПЭГ-фосфолипида из сосудистой системы. Следовательно, несвязавшиеся молекулы ПЭГ-фосфолипида предпочтительно вымывают на одном или множестве, т.е., на по меньшей мере двух, этапах промывки, применяя раствор для консервации органов.
Такой раствор для консервации органов также можно применять для промывки сосудистой системы органа или части органа перед инфузией раствора, содержащего молекулы ПЭГ-фосфолипида, на одном или множестве этапах промывки. В таком варианте реализации указанный способ также включает инфузию ex vivo раствора для консервации органов в сосудистую систему перед инфузией ex vivo раствора, содержащего молекулы ПЭГ-фосфолипида, в сосудистую систему. Предварительная инфузия раствора для консервации органов перед добавлением молекул ПЭГ-фосфолипида промоет сосудистую систему органа или части органа, чтобы тем самым облегчить эффективное покрытие эндотелия молекулами ПЭГ-фосфолипида.
В одном варианте реализации инфузия ex vivo раствора, содержащего молекулы ПЭГ-фосфолипида, включает установку ex vivo зажима на одну из артерии и вены сосудистой системы. В данный вариант реализации также входит инфузия ex vivo раствора, содержащего молекулы ПЭГ-фосфолипида, в другую из артерии и вены и установка зажима ex vivo на другую из артерии и вены.
Следовательно, в одном варианте реализации на вену (или артерию) сосудистой системы органа или части органа сначала устанавливают зажим, чтобы предотвратить вытекание раствора, который нужно добавить, из сосудистой системы. Раствор с молекулами ПЭГ-фосфолипида добавляют в артерию (или вену) сосудистой системы и на данную артерию (или вену) затем устанавливают зажим, чтобы предотвратить вытекание раствора, который нужно добавить, из сосудистой системы. Следовательно, входящие и выходящие кровеносные сосуды сосудистой системы органа или части органа закрывают путем установки зажима, чтобы тем самым сохранить раствор, содержащий молекулы ПЭГ-фосфолипида, внутри сосудистой системы и посредством этого обеспечить связь молекул ПЭГ-фосфолипида с эндотелием сосудистой системы.
В другом варианте реализации раствор с молекулами ПЭГ-фосфолипида вводят путем инфузии в артерию (или вену) сосудистой системы органа или части органа до тех пор, пока указанный раствор не появится в вене (или артерии) органа или части органа. Это подтверждает, что раствор с молекулами ПЭГ-фосфолипида заполнил сосудистую систему. В этот момент на артерию и вену устанавливают зажим.
Раствор, содержащий молекулы ПЭГ-фосфолипида, можно добавить либо через вену, либо через артерию. В конкретном варианте реализации раствор вводят путем инфузии в артерию. В таком конкретном варианте реализации затем предпочтительно осуществляют необязательную исходную установку зажима на вену сосудистой системы.
Варианты реализации с установкой зажима, описанные выше, в частности, пригодны, когда раствор, который вводят путем инфузии ex vivo в сосудистую систему, отличен от раствора для консервации органов, в который погружен орган или часть органа, и/или молекулы ПЭГ-фосфолипида, содержащиеся в растворе, отличны от молекул ПЭГ-фосфолипида, содержащихся в растворе для консервации органов. В других случаях не требуется установка зажима, поскольку затем будут вводить путем инфузии ex vivo тот же содержащий ПЭГ-фосфолипид раствор для консервации органов, что и раствор, в который погружен орган или часть органа.
Раствор, содержащий молекулы ПЭГ-фосфолипида, предпочтительно инкубируют ex vivo в сосудистой системе в течение периода времени от 10 минут до 48 часов, чтобы обеспечить гидрофобное взаимодействие молекул ПЭГ-фосфолипида с мембранами клеток эндотелия и, тем самым, покрыть по меньшей мере часть сосудистой системы органа или части органа. Инкубацию ex vivo предпочтительно осуществляют в течение от 20 минут до 36 часов и более предпочтительно от 30 минут до 24 часов, например, от 30 минут до 12 часов, до 8 часов, до 4 часов или до 1 часа.
Количество раствора, содержащего молекулы ПЭГ-фосфолипида, которое вводят путем инфузии в сосудистую систему, зависит от типа органа и размера органа (взрослого/ребенка). Как правило, объем раствора должен быть достаточным, чтобы заполнить сосудистую систему органа. В большинстве практических применений в сосудистую систему вводят путем инфузии ex vivo от 5 мл до 250 мл раствора, содержащего молекулы ПЭГ-фосфолипида. В предпочтительном варианте реализации от 5 мл до 100 мл и предпочтительно от 5 мл до 50 мл раствора, содержащего молекулы ПЭГ-фосфолипида, вводят путем инфузии ex vivo в сосудистую систему.
В одном варианте реализации раствор содержит от 0,25 мг/мл до 25 мг/мл молекул ПЭГ-фосфолипида. В предпочтительном варианте реализации раствор содержит от 0,25 мг/мл до 10 мг/мл, предпочтительно от 0,25 мг/мл до 5 мг/мл, например, 2 мг/мл молекул ПЭГ-фосфолипида.
Описанные выше концентрации молекул ПЭГ-фосфолипида также можно использовать для раствора для консервации органов, содержащего молекулы ПЭГ-фосфолипида.
Согласно настоящему изобретению, раствор, содержащий молекулы ПЭГ-фосфолипида, инкубируют ex vivo в сосудистой системе, при этом выдерживая орган или часть органа погруженными или залитыми раствором для консервации органов, содержащим молекулы ПЭГ-фосфолипида. Кроме того, орган или часть органа предпочтительно также держат при температуре выше 0°C, но ниже 8°C, предпочтительно выше 0°C, но равной или ниже 6°C, и более предпочтительно выше 0°C, но равной или ниже 4°C.
В данном варианте реализации орган или часть органа погружают в раствор для консервации органов, содержащий молекулы ПЭГ-фосфолипида, во время инкубации, когда молекулам ПЭГ-фосфолипида позволяют взаимодействовать и связываться с мембранами клеток эндотелия в сосудистой системе. Орган или часть органа предпочтительно также держат в холоде, т.е., при температуре, близкой, но выше 0°C.
Согласно настоящему изобретению, орган или часть органа держат погруженными в раствор для консервации органов, содержащий молекулы ПЭГ-фосфолипида.
Было показано, что теоретическая идеальная температура для консервации органов составляет 4°C - 8°C. Тогда как более высокие температуры приводят к гипоксическому повреждению органа вследствие не достаточно эффективного снижения метаболизма, более низкие температуры, чем 4°C, повышают риск холодового повреждения с денатурацией белка.
На сегодняшний день в золотом стандарте консервации донорских органов при трансплантации органов в клинике применяется три пластиковых пакета и холодильная камера. Первый пластиковый пакет содержит сам орган, погруженный в раствор для консервации органов. Данный первый пластиковый пакет помещают во второй пластиковый пакет, заполненный солевым раствором, а затем данные два пластиковых пакета помещают в третий пластиковый пакет, заполненный солевым раствором, который затем помещают в холодильную камеру. Доступны и могут применяться более совершенные устройства для консервации органов для хранения органов в среде с контролируемой температурой, такие как системы для транспортировки Sherpa Pak™ от Paragonix Technologies, Inc., Waves от Waters Medical Systems, системы для транспортировки LifePort от Organ Recovery Systems, и т.д.
Раствор, содержащий молекулы ПЭГ-фосфолипида, может представлять собой солевой раствор, водный буферный раствор или раствор для консервации органов.
Типичные, но неограничивающие примеры водных буферных растворов, которые можно применять, включают фосфатно-солевой буферный раствор (ФБР) и цитратный раствор.
Раствор для консервации органов, который можно применять для инфузии молекул ПЭГ-фосфолипида и/или промывки сосудистой системы органа или части органа до или после инфузии ex vivo молекул ПЭГ-фосфолипида и/или в который орган или часть органа можно погрузить, можно выбрать из известных растворов для консервации органов. Типичные, но неограничивающие примеры таких растворов для консервации органов включают раствор гистидин-триптофан-кетоглутарат (HTK), цитратный раствор, раствор университета Висконсина (UW), раствор Коллинза, раствор Цельсиор, раствор университета Киото и раствор института Джордж-Лопез-1 (IGL-1).
Экспериментальные данные, представленные в данной заявке, показали, что молекулы ПЭГ-фосфолипида легко поддаются смешиванию с растворами для консервации органов без какой-либо преципитации (фиг. 20).
В одном варианте реализации молекулы ПЭГ-фосфолипида представляют собой нефункционализированные молекулы ПЭГ-фосфолипида, состоящие из ПЭГ-фосфолипидов. Следовательно, в данном варианте реализации молекулы ПЭГ-фосфолипида не содержат никаких функциональных групп. Это соответствует наличию R, соответствующего CH2 или H на фиг. 1.
В другом варианте реализации молекулы ПЭГ-фосфолипида представляют собой функционализованные молекулы ПЭГ-фосфолипида, содержащие соответствующую функционализированную молекулу, присоединенную к ПЭГ молекул ПЭГ-фосфолипида.
В дополнительном варианте реализации раствор содержит смесь нефункционализированных молекул ПЭГ-фосфолипида, состоящих из ПЭГ-фосфолипидов, и функционализированных молекул ПЭГ-фосфолипида, содержащих соответствующую функционализированную молекулу, присоединенную к ПЭГ молекул ПЭГ-фосфолипида.
В конкретных вариантах реализации, включающих только функционализованные молекулы ПЭГ-фосфолипида или смесь функционализированных и нефункционализированных молекул ПЭГ-фосфолипида, функционализированную молекулу предпочтительно выбирают из группы, состоящей из ингибитора комплемента, ингибитора свертывания крови, ингибитора тромбоцитов, молекулы, способной связывать ингибитор комплемента, молекулы, способной связывать ингибитор свертывания крови, молекулы, способной связывать ингибитор тромбоцитов, и их смеси.
Типичные, но неограничивающие примеры ингибиторов комплемента включают Фактор H; C4b-связывающий белок (C4BP); от 4 до 6 N-концевых коротких консенсусных повторов (SCR) рецептора комплемента 1 (CR1), также известного как рецептор C3b/C4b или кластер дифференцировки 35 (CD35); регуляторный белок комплемента CD46 (CD46), также известный как мембранный кофакторный белок (MCP); и ускоряющий распад комплемента фактор (DAF), также известный как CD55.
Типичный, но неограничивающий пример ингибиторов свертывания крови включает гепарин.
Типичный, но неограничивающий пример ингибитора тромбоцитов представляет собой расщепляющий аденозиндифосфат (АДФ) фермент, такой как апираза и эктонуклеозидтрифосфатдифосфогидролаза-1 (НТФДаза 1), также известная как CD39.
Типичные, но неограничивающие примеры молекулы, способной связывать ингибитор комплемента, представляют собой связывающий Фактор H пептид, такой как 5C6, описанный в [4]; и связывающий C4BP пептид, такой как происходящий из белка M Streptococcus пептид M2-N, M4-N или M22-N, описанный в [5]
Типичный, но неограничивающий пример молекулы, способной связывать ингибитор свертывания крови, представляет собой связывающий гепарин пептид, такой как описанный в [7].
Следовательно, в одном варианте реализации функционализированная молекула выбрана из группы, состоящей из связывающего гепарин пептида, от 4 до 6 N-концевых SCR CR1, CD46, DAF, связывающей Фактор H молекулы, расщепляющего АДФ фермента и их смеси.
В конкретном варианте реализации функционализированная молекула выбрана из группы, состоящей из пептида 5C6, апиразы, CD39, C4B и их смеси.
В одном варианте реализации молекулы ПЭГ-фосфолипида имеют формулу (I) или формулу (II):
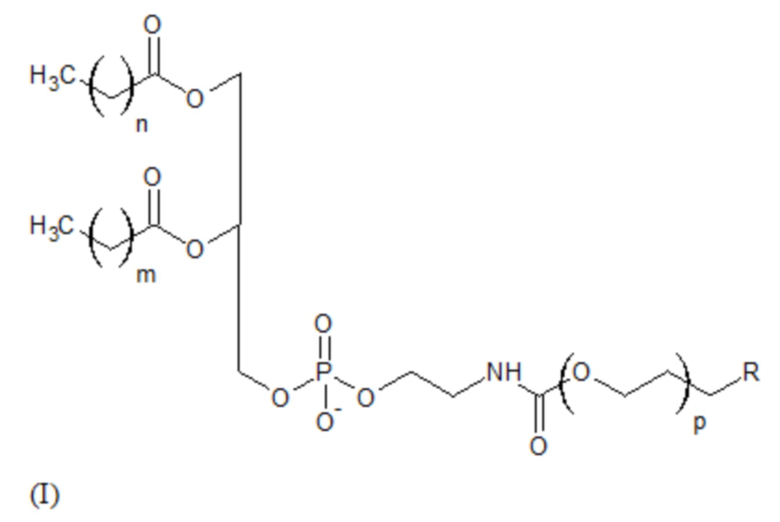
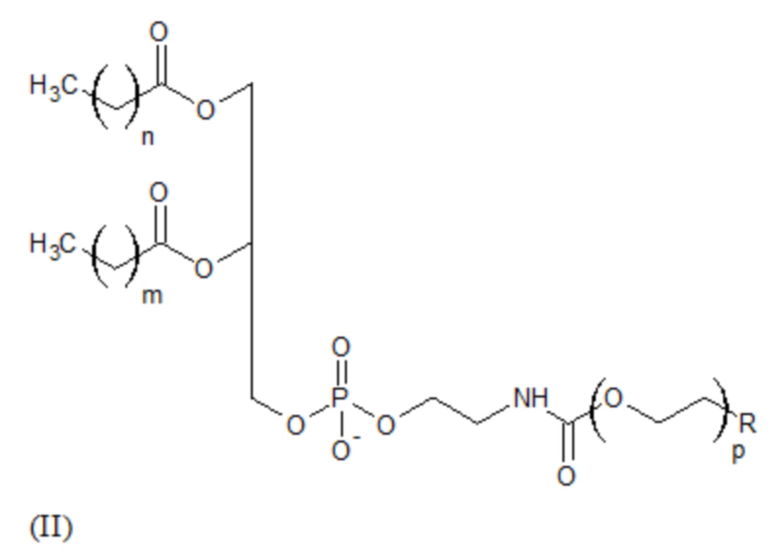
В одном варианте реализации n, m представляют собой целые числа, независимо выбранные в диапазоне от 10 до 16. Параметры n, m предпочтительно независимо представляют собой 10, 12, 14 или 16, и более предпочтительно n = m = 14.
В одном варианте реализации p выбирают таким образом, что цепь ПЭГ имеет среднюю молекулярную массу, выбранную в диапазоне от 1 000 Да до 40 000 Да. Параметр p предпочтительно выбирают таким образом, что цепь ПЭГ имеет среднюю молекулярную массу от 3 000 до 10 000 Да и более предпочтительно 5 000 Да.
Средняя молекулярная масса, согласно определению в данной заявке, указывает на то, что отдельные молекулы ПЭГ-фосфолипида могут иметь молекулярную массу, отличную от данной средней молекулярной массы, но что средняя молекулярная масса представляет собой среднее значение молекулярных масс молекул ПЭГ-фосфолипида. Это дополнительно подразумевает, что будет естественное распределение молекулярных масс около данной средней молекулярной массы у образца ПЭГ-фосфолипида.
Концевая группа R представляет собой, в конкретном варианте реализации, H, CH2, NH2, малеимидную группу, биотиновую группу, стрептавидиновую группу, авидиновую группу или функционализированную молекулу. В случае функционализированной молекулы, ее предпочтительно выбирают из группы, состоящей из ингибитора комплемента, ингибитора свертывания крови, ингибитора тромбоцитов, молекулы, способной связывать ингибитор комплемента, молекулы, способной связывать ингибитор свертывания крови, молекулы, способной связывать ингибитор тромбоцитов, и их смеси.
Цепи жирных кислот молекулы ПЭГ-фосфолипида могут быть насыщенными. По меньшей мере одна или обе цепи жирных кислот, в качестве альтернативы, могут быть ненасыщенными, т.е., содержать по меньшей мере одну группу -CH=CH-, по меньшей мере одну группу -C≡C- или их комбинацию. Каждая цепь жирной кислоты может быть прямой или разветвленной.
Молекулы ПЭГ-фосфолипида, которые вводят ex vivo путем инфузии в сосудистую систему, и необязательно паренхиму, органа или части органа, могут быть того же типа, что и молекулы ПЭГ-фосфолипида, содержащиеся в растворе для консервации органов, погруженными в который держат орган или часть органа. В другом варианте реализации можно применять различные типы молекул ПЭГ-фосфолипида в растворе, который вводят ex vivo путем инфузии в сосудистую систему, и необязательно в паренхиму, органа или части органа, по сравнению с раствором для консервации органов, погруженными в который держат орган или часть органа. Например, размер цепи ПЭГ может быть различным у молекул ПЭГ-фосфолипида, причем размер цепи ПЭГ молекул ПЭГ-фосфолипида выбирают таким образом, чтобы он достиг целевого размера для сосудистой системы, и необязательно паренхимы, органа или части органа. На фиг. 19 показано, что размер цепи ПЭГ ограничивает части сосудистой системы и паренхимы, которых могут достигнуть молекулы ПЭГ-фосфолипида. В частности, молекулы ПЭГ-фосфолипида размером 5 кДа могут достигнуть более обширных частей сосудистой системы и паренхимы по сравнению с более крупными молекулами ПЭГ-фосфолипида размером 40 кДа.
Следовательно, в конкретном варианте реализации молекулы ПЭГ-фосфолипида, содержащиеся в растворе, который вводят путем инфузии ex vivo в сосудистую систему, и необязательно паренхиму, органа или части органа, могут иметь отличный средний размер цепи ПЭГ по сравнению молекулами ПЭГ-фосфолипида, содержащимися в растворе для консервации органов, в который погружен орган или часть органа.
В качестве альтернативы или дополнения, молекулы ПЭГ-фосфолипида в растворе для инфузии ex vivo и молекулы ПЭГ-фосфолипида в растворе для консервации органов могут содержать различные функциональные группы, т.е., концевые группы R в формуле (I) и (II).
Способ ex vivo согласно настоящему изобретению можно применять по отношению к любому органу, или части органа, содержащему сосудистую систему, и который можно применять в качестве трансплантируемого органа, т.е., трансплантировать реципиенту. Типичные, но неограничивающие примеры таких органов включают почку, печень, поджелудочную железу, сердце, легкое, матку, мочевой пузырь, тимус и кишечник.
В конкретном варианте реализации орган представляет собой почку. В данном конкретном варианте реализации инкубация ex vivo раствора, содержащего молекулы ПЭГ-фосфолипида, в сосудистой системе позволяет покрытие не только эндотелия почки сосудистой системы почки, но и предпочтительно также канальцев паренхимы почки молекулами ПЭГ-фосфолипида. Таким образом, экспериментальные данные представленные в данной заявке, показывают, что молекулы ПЭГ-фосфолипида равномерно распределялись в околоканальцевых сосудах, клубочках и канальцах почки при инъекции ex vivo раствора, содержащего молекулы ПЭГ-фосфолипида, через остаток аорты.
Экспериментальные данные, представленные в данной заявке, показали, что у обработанных ПЭГ-фосфолипидом трансплантатов органов было значительно меньше тромбовоспаления по сравнению с необработанными контрольными трансплантатами органов, судя по уровням в плазме маркеров свертывания, таких как TAT, и маркеров комплемента, таких как C3a и sC5b-9. Также экспрессия цитокинов, в частности, IL-6 и IL-1β, значительно подавлялась в обработанных ПЭГ-фосфолипидом трансплантатах органов. Функционирование органа улучшалось в обработанных ПЭГ-фосфолипидом трансплантатах органов. В обработанных ПЭГ-фосфолипидом трансплантатах органов также выявили сниженное депонирование маркеров комплемента, таких как C3b и мембраноатакующие комплексы, и экспрессию C5aR.
Таким образом, покрытие ex vivo трансплантатов органов молекулами ПЭГ-фосфолипида защищает от вызванного И/Р тромбовоспаления, что свидетельствует о том, что оно эффективно против повреждения И/Р при трансплантации в клинике.
В дополнительном аспекте настоящего изобретения предложен ПЭГ-фосфолипид для применения для лечения, ингибирования или предотвращения гипотонии, связанной с реперфузией, развившейся после реперфузии трансплантата органа.
В еще одном аспекте настоящего изобретения предложен ПЭГ-фосфолипид для применения для лечения, ингибирования или предотвращения ПРС.
Осложнением во время и незамедлительно, обычно до 24 часов, после трансплантации органов является значительное падение артериального давления после реперфузии трансплантата органа в реципиенте. Такое гемодинамическое изменение у реципиента может в тяжелых случаях приводить к ишемии в органах реципиента и в пересаженном трансплантате, вызывающей повреждение любого из данных органов и даже гибель пациента, если лечение не успешно.
Наблюдаемая защита ПЭГ-фосфолипидом от сосудистой нестабильности может быть следствием ингибирования системы контакта/калликреина. Неожиданно обнаружили, что система контакта/калликреина активировалась после реперфузии. Система контакта/калликреина генерировала брадикинин - высоковазоактивный пептид, который вызывает вазодилатацию и повышенную проницаемость, приводящую к гипотонии, которая вызывает компенсаторную тахикардию. При оперативном вмешательстве снижение артериального давления лечат фармацевтическими веществами и жидкостями, тем не менее, может возникнуть опасная для жизни ситуация. Таким образом, способность предотвращать гипотонию имеет огромное клиническое значение.
Таким образом, предотвращение, лечение или по меньшей мере уменьшение такой гипотонии и падения артериального давления, связанного с реперфузией трансплантата органа, является существенным улучшением при трансплантации органов. Экспериментальные данные, представленные в данной заявке, показали, что обработка ex vivo трансплантата органа перед трансплантацией раствором, содержащим молекулы ПЭГ-фосфолипида, защищала реципиента от такой гипотонии или падения артериального давления, когда трансплантат органа подвергали реперфузии.
В одном варианте реализации ПЭГ-фосфолипид находится в форме раствора, содержащего молекулы ПЭГ-фосфолипида, и предназначен для инфузии ex vivo в сосудистую систему трансплантата органа, чтобы обеспечить покрытие эндотелиальной выстилки сосудистой системы и паренхимы молекулами ПЭГ-фосфолипида.
В сходном аспекте настоящего изобретения предложено применение ПЭГ-фосфолипида для производства лекарственного средства для лечения, ингибирования или предотвращения гипотонии, связанной с реперфузией, развившейся после реперфузии трансплантата органа. В аспекте также предложен способ лечения, ингибирования или предотвращения гипотонии, связанной с реперфузией, развившейся после реперфузии трансплантата органа. Данный способ включает ранее описанные этапы способа - инфузию ex vivo раствора, содержащего молекулы ПЭГ-фосфолипида, в сосудистую систему трансплантата органа и инкубацию ex vivo раствора, содержащего молекулы ПЭГ-фосфолипида, в сосудистой системе, чтобы обеспечить покрытие по меньшей мере части эндотелиальной выстилки сосудистой системы молекулами ПЭГ-фосфолипида, необязательно, но предпочтительно, при этом выдерживая трансплантат органа погруженным в раствор для консервации органов, содержащий молекулы ПЭГ-фосфолипида.
экспериментЫ
ЭКСПЕРИМЕНТ 1
МАТЕРИАЛЫ, МЕТОДЫ И ЭКСПЕРИМЕНТЫ НА ЖИВОТНЫХ
Синтез производных ПЭГ-фосфолипида
a. FITC-ПЭГ-фосфолипид
Синтез ПЭГ-фосфолипидов осуществляли с помощью способов, описанных ранее [1]. Вкратце, 1,2-дипальмитоил-sn-глицеро-3-фосфатидилэтаноламин (NOF Corporation, Токио, Япония, DPPE, 21 мг) растворяли в 3 мл дихлорметана (Sigma-Aldrich Chemical Co. (Сент-Луис, Миссури, США)). α-N-гидроксисукцинимидил-ω-трет-бутоксикарбонилполиэтиленгликоль (NHS-ПЭГ-Boc, Mw: 5000, от NOF, 185 мг) и триэтиламин (3 мкл, Nacalai Tesque (Киото, Япония)) добавляли в реакционный раствор, а затем перемешивали в течение 4 суток при комнатной температуре (КТ ~20°C). Группа NHS NHS-ПЭГ-Boc легко реагировала с аминогруппой фосфолипидов. Защитную группу Boc аминогруппы снимали путем добавления 2 мл 99 % трифторуксусной кислоты (Wako Pure Chemical (Осака, Япония)) и дополнительной инкубации при 4°C в течение 30 мин. Неочищенный продукт очищали путем переосаждения в диэтиловом эфире (Nacalai Tesque). После экстрагирования хлороформом (Nacalai Tesque) и выпаривания ПЭГ-фосфолипиды получали в виде белого твердого вещества. Выход составлял 85 %. Для флуоресцентного мечения флуоресцеинизотиоцианатом (FITC) (Dojindo Laboratories (Kumamoto, Япония)) ПЭГ-фосфолипидам (200 мг) позволяли прореагировать с FITC (31 мг) в ацетоне в течение 12 ч. FITC-ПЭГ-фосфолипид очищали с помощью гель-проникающей хроматографии (Sephadex G-25, GE Healthcare (Бакингемшир, Великобритания)).
Синтез FITC-ПЭГ-фосфолипида (40 кДа) осуществляли в соответствии с описанным далее способом. α-N-гидроксисукцинимидил-ω-малеимидилполиэтиленгликоль (NHS-ПЭГ(40к)-Mal, Mw: 40000) и DPPE (9,6 мг) растворяли в 3 мл дихлорметана и добавляли в реакционный раствор триэтиламин (3 мкл, Nacalai Tesque), а затем перемешивали в течение 4 суток при комнатной температуре (КТ, ~20°C). Неочищенный продукт очищали путем переосаждения в диэтиловом эфире. После экстрагирования хлороформом и выпаривания получали Mal-ПЭГ-фосфолипиды (40 кДа) в виде белого твердого вещества. Выход составлял 80 %. Для флуоресцентного мечения флуоресцеинизотиоцианатом (FITC) Mal-ПЭГ-фосфолипиды (40 кДа) (1200 мг) растворяли в ДМСО (Nacalai Tesque, 20 мл), а затем добавляли FITC-глицин-цистеин (FITC-GC, BEX Co., Ltd., Токио, Япония, 12 мг) и инкубировали в течение 24 ч при 37°C. Неочищенный продукт очищали путем переосаждения в диэтиловом эфире. После экстрагирования хлороформом и выпаривания получали FITC-ПЭГ-фосфолипиды (40 кДа) в виде желтого твердого вещества.
b. Биотин-ПЭГ-фосфолипид
Биотин-ПЭГ-фосфолипид синтезировали путем объединения полиэтиленгликоля- эфира (N-гидроксисукцинимид-5-пентаноата)-2-(биотиниламино)этана (биотин-ПЭГ-NHS, Mw: 5000 от NOF, 180 мг) и 1,2-дипальмитоил-sn-глицеро-3-фосфатидилэтаноламина (DPPE) (20 мг) с триэтиламином (50 мкл) и дихлорметаном (4 мл) и перемешивания в течение 48 ч при КТ. Преципитация диэтиловым эфиром позволила получить биотин-ПЭГ-фосфолипид в виде белого порошка (165 мг; выход 80 %). Биотин-ПЭГ-фосфолипид применяли для визуализации без дополнительной очистки.
c. ПЭГ-фосфолипид
ПЭГ-фосфолипид синтезировали путем объединения α-сукцинимидилоксисукцинил-ω-метоксиполиоксиэтилена (MeO-ПЭГ-NHS, Mw: 5000 от NOF, 171 мг) и DPPE (22 мг) с триэтиламином (25 мкл) и дихлорметаном (5 мл) и перемешивания в течение 72 ч при КТ. Преципитация диэтиловым эфиром позволила получить ПЭГ-фосфолипид в виде белого порошка (160 мг; выход 80 %). ПЭГ-фосфолипид применяли для обработки почки без дополнительной очистки.
Функциональная оценка различных типов ПЭГ-фосфолипидов
Для того чтобы оценить, оказывала ли функциональная группа какое-либо влияние на защитные свойства, проводили серию экспериментов на первичных мезенхимальных стволовых клетках человека (hMSC). hMSC покрывали ПЭГ-фосфолипидом, FITC-ПЭГ-фосфолипидом и биотин-ПЭГ-фосфолипидом. После модификации поверхности анализировали жизнеспособность покрытых клеток с помощью анализа с аламаровым синим (Life technologies, Стокгольм; Швеция), в соответствии с инструкциями производителя. Вкратце, покрытые клетки культивировали в культуральной среде МСК в 96-луночном микропланшете для культивирования клеток. После 6 часов культивирования добавляли 10 мкл реагента аламарового синего в 100 мкл культуральной среды, а затем инкубировали 4 часа при 37°C. Затем измеряли флуоресцентное излучение на 580 - 610 нм.
Для того чтобы определить гемосовместимость hMSC, МСК с модифицированной поверхностью приводили в контакт с цельной кровью в модели петли, описанной ранее [7]. Вкратце, цельную кровь брали у здоровых добровольцев в покрытые гепарином пробирки (Corline AB, Уппсала; Швеция). Использовали гепаринизированные трубки периферического внутривенного катетера (30 см). Каждую трубку заполняли 3 мл крови, в которую добавляли 10000 МСК/мл. Трубки вращали при скорости 30 об/мин при 37°C в течение 60 мин. После инкубации 1,2 мл крови собирали в пробирки емкостью 2 мл (Eppendorf, Германия), содержащие ЭДТА в конечной концентрации 10 мМ. Затем кровь центрифугировали при 4200×g в течение 15 мин при 4°C с получением плазмы. Плазму разделяли на аликвоты и хранили при -80°C до проведения дальнейшего анализа.
Сохранение ПЭГ-фосфолипида с различной длиной субъединицы ПЭГ
Клетки (CCRF-CEM, суспензионная линия клеток; n=3) инкубировали с FITC-ПЭГ-фосфолипидом (2 мг/мл в ФБР) в течение 30 мин при КТ, а затем промывали культуральной средой. В данном случае использовали FITC-ПЭГ-фосфолипиды с различной молекулярной массой цепи ПЭГ - 1 кДа, 5 кДа и 40 кДа. Обработанные клетки культивировали в культуральной среде при 37°C и собирали для анализа методом проточной цитометрии через 0, 1, 3, 6, 24 и 48 ч.
Модель аллогенной трансплантации на свиньях
Свинью выбирали в качестве модели на большом животном по причине ее анатомии и физиологии, которые очень похожи на таковые у людей. В частности, структура и функция почки очень сходны с таковыми у указанного органа примата. Во всех исследованиях на свиньях использовали обычные породы с высоким стандартом здоровья. В долговременных экспериментах по выживаемости животным позволяли акклиматизироваться в течение двухнедельного периода и выполнить программу по подготовке и социализации. Клинические исследования, включая ультразвук мочевыводящих путей, гематологию и клиническую патологию, проводили часто, и типирование SLA для выявления несовпадения доноров и реципиентов осуществляли перед трансплантацией. Свиньи-реципиенты быстро восстанавливались после хирургического вмешательства, но их не лечили иммуносупрессивными лекарственными средствами. Введение таких лекарственных средств нарушает иммунный ответ и было исключено из экспериментов. Свиней, следовательно, подвергали эвтаназии через 96 ч, чтобы избежать острого отторжения трансплантата. Проводили полную некропсию после умерщвления. Все исследования были одобрены этическим комитетом по экспериментам над животными, Уппсала, Швеция.
A. Кратковременная модель (перфузия почки ПЭГ-фосфолипидом отдельно в течение 40 мин)
Ишемически-реперфузионное повреждение (И/Р-повреждение) вносит основной вклад в патологию некоторых состояний, включая трансплантацию, тромботические нарушения, сепсис и сердечно-легочное шунтирование. В настоящем эксперименте исследовали, защищает ли покрытие ex vivo поверхностей ишемических клеток трансплантатов почки свиньи ПЭГ-фосфолипидом от И/Р повреждения в модели аллогенной трансплантации почки единым блоком.
Животные. Исследование проводили в экспериментальной лаборатории Hedenstierna, Больница университета Уппсала, Швеция. В исследование включили шесть свиней-доноров и шесть свиней-реципиентов обоих полов. Масса тела и возраст свиней варьировались в диапазоне 30 - 35 кг и 10 - 12 недель, соответственно. Использовали процедуры невыживания и животных умерщвляли по окончании периода наблюдения после трансплантации, составляющего 8 часов.
Анестезия. По прибытии в лабораторию для седации проводили внутримышечную инъекцию 2,2 мг/кг ксилазина (Rompun; Bayer, Леверкузен, Германия) в комбинации с золазепамом 6 мг/кг (Zoletil; Virbac, Карро, Франция). Затем животных фиксировали в положении лежа на животе. Периферические внутривенные катетеры вводили в обе ушные вены, чтобы индуцировать и поддерживать анестезию, и для введения жидкостей. Делали эпитрахеальный небольшой разрез для обнажения трахеи и транстрахеального интубирования для искусственной вентиляции легких с помощью механического аппарата ИВЛ Servo-I, MAQUET, Medical Systems, США. Животным проводили ИВЛ с 30% кислорода в воздухе с достижением 5,0 - 5,5 кПа CO2. Целью было среднее артериальное давление (САД) > 60 мм рт.ст., чтобы гарантировать достаточную перфузию органа.
Модель трансплантации. Мы разработали модель трансплантации для свиней, позволяющую двойное извлечение единым блоком и имплантацию обеих почек из животного-донора животному-реципиенту. Благодаря изолированной инкубации ex vivo с ПЭГ-фосфолипидом лишь одной произвольно выбранной почки из комплекта единого блока, данная методика позволила нам котрансплантировать обработанный орган с идеально совместимой контрольной тканью в одну свинью-реципиента, что не только уменьшило количество экспериментальных животных, но также минимизировало экспериментальные искажающие переменные.
Ствол супра- и инфраренальной аорты, а также нижнюю полую вену мобилизовали, так что создавался комплект единого блока, состоящий из двух почек, мочеточников и всей сосудистой сети почки. Комплект единого блока незамедлительно удаляли и промывали холодным раствором HTK (Custodiol;  Chemie GmbH, Германия). После этого комплект единого блока хранили на холоде в растворе HTK при 4°C в течение 24 часов.
Chemie GmbH, Германия). После этого комплект единого блока хранили на холоде в растворе HTK при 4°C в течение 24 часов.
После хранения одну почку из каждого комплекта единого блока произвольно выбирали для инкубации с ПЭГ-фосфолипидом. На вену и артерию контралатеральной почки (контроль), а также на вену выбранной почки устанавливали зажим. Всего 10 - 15 мл раствора ПЭГ-фосфолипида при концентрации 2 мг/мл медленно вводили путем инфузии в выбранную почку. На артерию обработанной почки затем устанавливали зажим и комплект единого блока хранили на холоде в течение дополнительных 40 мин при 4°C в HTK. После инкубации и перед имплантацией лишний ПЭГ-фосфолипид вымывали из обработанной почки с помощью HTK, не удаляя зажимы с контроля.
С свиньями-реципиентами обращались и анестизировали их, как описано ранее. Комплект единого блока помещали горизонтально внутрь брюшины. Дистальный конец полой вены и аорты трансплантата соединяли терминолатеральным анастомозом с полой веной и аортой реципиента, соответственно. После снятия зажима обработанную и контрольную почку последовательно подвергали реперфузии с отсроченным снятием зажима с контрольной почки с интервалом в несколько секунд, за которые вымывали элюат из обработанной почки. Это делали, чтобы предотвратить контаминирование контрольной почки оставшимся раствором ПЭГ-фосфолипида внутри кондуита аорты. Оба трансплантированных мочеточника катетеризировали отдельно для документирования количества выделяемой мочи.
B. Долговременная модель (перфузия почки ПЭГ-фосфолипидом отдельно в течение 40 мин)
Животные. На основании результатов типирования SLA выбирали кроссбредных свиней доноров (n=12) и реципиентов (n=21) для несовместимой трансплантации. Животных поселяли в отдельные загоны размером 3 м2 в пределах видимости и слышимости друг друга. Солому и древесные опилки использовали в качестве подстилки. Использовали 14:10 ч цикл света/темноты (свет включали в 06:00 ч) и в каждом загоне была инфракрасная лампа (24 ч). Температура составляла 16 - 18°C. Животным давали коммерчески доступный корм заключительного периода откорма без стимуляторов роста (SOLO 330,  Швеция) дважды в день, количество зависело от массы тела и соответствовало диете для выращивания свиней Шведского университета сельскохозяйственных наук. Воду давали без ограничения. Донорных свиней обезболивали комбинацией медетомидина (Домитор® вет, 1 мг/мл; Orion Pharma Animal Health, Соллентуна, Швеция) в дозе 0,1 мг/кг массы тела, буторфанола (Бутомидор вет, 10 мг/мл; Salfarm Scandinavia, Хельсингборг, Швеция) в дозе 0,2 мг/кг массы тела и кетамина (Кетаминол® вет, 100 мг/мл; Intervet International BV, Боксмеер, Нидерланды) в дозе 5 мг/кг массы тела внутримышечно (в/м) и почки исследовали с помощью ультразвука (Logiq e R6, GE Healthcare, Уоууотоса, США), используя линейные (10 МГц) и криволинейные (4 МГц) зонды, чтобы исключить свиней с кистами в почках. Оценивали длину, эхогенность и кортико-медуллярную дифференциацию, брюшную область около почки оценивали для выявления признаков пиелэктазии и цветовой доплер использовали для оценки присутствия кровотока в почках. Во время двухнедельного периода акклиматизации за свиньями ухаживали ежедневно и позволяли привыкнуть к различным обследованиям, чтобы проводить их без фиксации после трансплантации.
Швеция) дважды в день, количество зависело от массы тела и соответствовало диете для выращивания свиней Шведского университета сельскохозяйственных наук. Воду давали без ограничения. Донорных свиней обезболивали комбинацией медетомидина (Домитор® вет, 1 мг/мл; Orion Pharma Animal Health, Соллентуна, Швеция) в дозе 0,1 мг/кг массы тела, буторфанола (Бутомидор вет, 10 мг/мл; Salfarm Scandinavia, Хельсингборг, Швеция) в дозе 0,2 мг/кг массы тела и кетамина (Кетаминол® вет, 100 мг/мл; Intervet International BV, Боксмеер, Нидерланды) в дозе 5 мг/кг массы тела внутримышечно (в/м) и почки исследовали с помощью ультразвука (Logiq e R6, GE Healthcare, Уоууотоса, США), используя линейные (10 МГц) и криволинейные (4 МГц) зонды, чтобы исключить свиней с кистами в почках. Оценивали длину, эхогенность и кортико-медуллярную дифференциацию, брюшную область около почки оценивали для выявления признаков пиелэктазии и цветовой доплер использовали для оценки присутствия кровотока в почках. Во время двухнедельного периода акклиматизации за свиньями ухаживали ежедневно и позволяли привыкнуть к различным обследованиям, чтобы проводить их без фиксации после трансплантации.
Модель трансплантации. Анестезию вызывали комбинацией медетомидина (Домитор® вет, 1 мг/мл; Orion Pharma Animal Health, Соллентуна, Швеция) в дозе 0,05 мг/кг массы тела и тилетамина и золазепама (Золетил®, 50 мг + 50 мг/мл; Virbac, Reading, Карро, Франция) в дозе 5 мг/кг массы тела в/м. Бупренорфин (Ветергестик (Vetergesic)® вет, 0,3 мг/мл; Orion Pharma Animal Health, Соллентуна, Швеция) в дозе 0,01 мг/кг массы тела внутримышечно и эпидуральный морфин (Morfin Epidural Meda, 2 мг/мл; Meda, Сольна, Швеция) в дозе 0,1 мг/кг давали перед операцией для дополнительного обезболивания. Прокаин-бензилпенициллин (Пеновет® вет, 300 мг/мл; Boehringer Ingelheim Vetmedica, Ингельхайм-ам-Райн, Германия) давали перед операцией в дозе 20 мг/кг массы тела в/м. После индукции анестезии вставляли венозные катетеры для длительного применения (Careflow™, 3Fr, 200 мм, BD, Франклин Лейкс, Нью-Джерси, США) в ушную вену (vena auricularis) по методике Сельдингера. После операции данные катетеры облегчали взятие крови без стресса. Катетеры промывали раз в день гепаринизированным солевым раствором 100 МЕ/мл (Гепарин LEO, 5000 МЕ/мл; Leo Pharma, Баллеруп, Дания). Анестезию поддерживали с помощью изофлурана (IsoFlo® вет; Orion Pharma Animal Health, Соллентуна, Швеция), испаренного в кислороде. Свиньи непрерывно получали терапию жидкостями с кристаллоидами (ацетат Рингера; Fresenius-Kabi, Бад-Хомбург, Германия). Коллоиды (Гелофузин® 40 мг/мл; Braun, Мельзунген, Германия) и добутамин (Dobutamin Carino, 250 мг/мл; Carinopharm, Эльце, Германия) давали при необходимости для поддержания артериального давления в пределах эталонных значений. Во время анестезии отслеживали дыхательные и сердечно-сосудистые параметры.
Процедура донорства. В первой серии экспериментов (3 + 3 донора и 6 + 5 реципиентов) извлекали обе почки, сходным образом обрабатывали перфузией HTK (n=11), хранили на льду в течение ночи, а затем одну из почек произвольно обрабатывали ПЭГ-фосфолипидом 60 мин перед имплантацией, тогда как другую почку оставляли необработанной. Альтернативное применение ПЭГ-фосфолипида осуществляли с другими десятью почками (5 доноров и 10 реципиентов), которые обрабатывали либо перфузией HTK, содержащей ПЭГ-фосфолипид, либо обычным раствором для перфузии HTK. После процедуры свиней-доноров подвергали эвтаназии путем в/в инъекции пентобарбитала натрия (Allfatal vet, 100 мг/мл; Omnidea AB, Стокгольм, Швеция) под общей анестезией.
Операция трансплантации. Свиньям-реципиентам проводили аллогенную трансплантацию одной почки. Все процедуры проводили внутрибрюшинно через 15 - 20 см срединный разрез, и подвздошные сосуды в правой подвздошной впадине идентифицировали и аккуратно мобилизовали. Дистальный фрагмент полой вены, а также подвздошную артерию (от ее выхода из аорты) мобилизовали, лигируя окружающую лимфоидную ткань. После этого трансплантат почки помещали в правую подвздошную впадину рядом с подвздошными сосудами. Вену и артерию почки обрезали и впоследствии соединяли анастомозом терминолатеральным способом с правой подвздошной артерией и дистальной полой веной реципиента с помощью непрерывного шва с использованием полипропиленовой нити 7/0 (PROLENE®, Ethicon, США). Мочеточники имплантировали путем внепузырной уретероцистонеостомии в верхушку мочевого пузыря с помощью полидиоксаноновой нити 6-0 (PDS®, Ethicon, США). После этого проводили билатеральную нефрэктомию собственных почек. Срединный разрез зашивали с помощью непрерывного фасциального шва с использованием полиглактиновой нити 2/0 (Викрил® Ethicon, США) и кожных скобок. Средняя продолжительность хирургического вмешательства составляла 3 ч (2,5 - 5,5 ч).
К окончанию хирургического вмешательства введение изофлурана прекращали, фракцию вдыхаемого кислорода повышали (FiO2 1,0) и свиней снимали с механического аппарата ИВЛ, и самостоятельное дыхание восстанавливалось. Свиней помещали в клетку интенсивной терапии, где персонал мог легко непрерывно следить за их состоянием. Свиньям давали дополнительный кислород и контролировали частоту пульса, частоту дыхательных движений, насыщение кислородом и температуру тела до того, как свиньи пришли в сознание. В течение первых суток свиней кормили вручную фруктами и помогали пить воду при необходимости. Им также помогали стоять и ходить и несколько раз делали массаж средней ягодичной мышцы, двуглавой мышцы бедра и большой ягодичной мышцы. Для послеоперационного обезболивания вводили в/в бупренорфин в течение двух суток.
Умерщвление и некропсия. Реципиентов подвергали эвтаназии с помощью передозировки пентобарбиталом натрия (Allfatal vet, 100 мг/мл; Omnidea AB, Стокгольм, Швеция) через 96 ч. Биоптаты почки для гистологического исследования собирали незамедлительно после смерти и проводили патологоанатомическое исследование всех свиней на Кафедре медико-биологических наук и ветеринарного здравоохранения, в Отделении патологии, SLU.
Предварительная обработка раствором HTK. В другой серии экспериментов четырем свиньям трансплантировали обработанные ПЭГ-фосфолипидом почки и пяти свиньям - контрольные почки. В данной серии экспериментов после извлечения почки подвергали перфузии с помощью раствора HTK (Кустодиол;  Chemie GmbH, Германия) с 2 мг/мл ПЭГ-фосфолипида (обработанные почки) или без ПЭГ-фосфолипида (контрольные почки). Почки также хранили погруженными в раствор HTK с 2 мг/мл ПЭГ-фосфолипида (обработанные почки) или в раствор HTK без добавления ПЭГ-фосфолипида (контрольные почки) при 4°C в течение 24 часов.
Chemie GmbH, Германия) с 2 мг/мл ПЭГ-фосфолипида (обработанные почки) или без ПЭГ-фосфолипида (контрольные почки). Почки также хранили погруженными в раствор HTK с 2 мг/мл ПЭГ-фосфолипида (обработанные почки) или в раствор HTK без добавления ПЭГ-фосфолипида (контрольные почки) при 4°C в течение 24 часов.
C. Долговременная модель для оценки отделения ПЭГ-фосфолипида от эндотелия почки.
Почки извлекали из свиней-доноров и трансплантировали свиньям-реципиентам после двух недель акклиматизации и подготовки, описанной выше. Почки обрабатывали, применяя ту же процедуру, что и для трансплантатов, в которые вводили ПЭГ-фосфолипид за 60 мин до имплантации. Для измерения отделения от эндотелия ПЭГ-фосфолипид флуоресцентно метили. Использовали те же анестезирующее средство и хирургический протокол, но собственные почки оставили у реципиентов (n = 4). Свиней подвергали эвтаназии через 12, 24, 48 и 72 часа, соответственно. Всем свиньям проводили некропсию и собирали биоптаты для гистолгического анализа и отслеживания флуоресценции.
Взятие проб крови
В кратковременной модели образцы крови получали из вен левого и правого трансплантата почки через 5, 15, 30, 60, 120, 240 и 360 минут после начала реперфузии. В долговременной модели кровь получали через 1, 24, 48, 72 и 96 часов. Образцы брали в пробирки с ЭДТА Vacutainer (Becton Dickinson AB, Швеция) и незамедлительно центрифугировали при КТ в течение 15 минут. Собранную плазму хранили при -80°C для дальнейшего анализа.
ИФА TAT, C3a и sC5b-9
TAT, C3a и sC5b-9 в плазме измеряли с помощью сэндвич ИФА, как описано ранее [7]. Вкратце, для оценки TAT образцы плазмы разбавляли 1/100 в нормальной плазме с цитратом-фосфатом-декстрозой (CPD). Моноклональное антитело против тромбина человека применяли для захвата и конъюгированное с HRP антитело против антитромбина человека (AT) применяли для детектирования (Enzyme Research Laboratories, Саут-Бенд, Индиана, США). Стандарт получали путем разбавления объединенной сыворотки человека в нормальной плазме CPD. Значения выражали в единицах мкг/л. Для оценки C3a плазму разбавляли 1/1000 в рабочем буфере (ФБР, содержащем 0,05% твин 20, 10 мг/мл БСА и 10 мМ ЭДТА). МАТ против C3a человека 4SD17.1 применяли для захвата C3a и биотинилированное поликлональное антитело кролика против C3a, а затем конъюгированный с HRP стрептавидин - для детектирования C3a в плазме. Активированная зимозаном сыворотка, откалиброванная по очищенному C3a, служила в качестве стандарта. Значения выражали в единицах нг/мл. Для sC5b-9 плазму разбавляли 1/50 в рабочем буфере (как описано выше). sC5b-9 захватывали МАТ против C5b-9 человека (a9e) и детектировали с помощью поликлонального антитела кролика против C5 человека (Dako) и конъюгированного с HRP IgG против кролика (Dako). Активированную зимозаном сыворотку, содержащую 6x104 у.е./мл, использовали в качестве стандарта. Значения выражали в единицах у.е./мл.
Гистологический анализ
Биоптаты ткани почки брали из контрольной и обработанной биотином-ПЭГ-фосфолипидом почки через 5, 60 и 360 минут после реперфузии. Для обнаружения ПЭГ-фосфолипида биоптаты незамедлительно замораживали в жидком азоте и хранили при -80°C до проведения дальнейшего анализа. Замороженные срезы почки (толщиной 4 мкм), обработанной биотином-ПЭГ-фосфолипидом, инкубировали в Alexa488-стрептавидине (GE Healthcare, 1:500) при КТ в течение 10 мин. Срезы анализировали с помощью лазерной сканирующей конфокальной микроскопии (LSM510, META, Carl Zeiss, Германия). Оценивали как биотин-ПЭГ-фосфолипид, так и FITC-ПЭГ-фосфолипид (5 кДа, 40 кДа).
Образцы ткани также фиксировали в 4% растворе параформальдегида в течение ночи и хранили в 70% этаноле до заключения в парафин. Парафиновые срезы (толщиной 5 мкм) депарафинизировали ксилолом и регидратировали в этаноле. Вызванное нагреванием извлечение антигена осуществляли путем двукратного кипячения срезов в натрий-цитратном буфере. Блокировали сывороткой козы перед инкубацией с первичным антителом. Полученные срезы окрашивали гематоксилином и эозином (окрашивание HE) и антителами к маркерам комплемента, такими как C5aR (Acris Antibodies, Херфорд, Германия), C3b (Bioss Antibodies, Уоберн, Массачусетс, США), C4d (Abcam, Кембридж, Великобритания) и C5b-9 (MAC; Abcam). В качестве контрольного эксперимента использовали IgG кролика (Dako, Glostrup, Дания) и IgG мыши (Abcam). Детектирование первичного антитела осуществляли с помощью системы детектирования Dako real щелочная фосфатаза/красный (Dako), а затем контрастного окрашивания гематоксилином. Стекла визуализировали, применяя микроскоп Zeiss Axio Imager A1. Объектив представлял собой 10X объектив и оцениваемые области были площадью 800000 мкм2. Проводили количественный анализ квадратных областей для определения интенсивности и площади иммунореактивных областей, применяя программное обеспечение Axio Visio (изд. 4.8) (Zeiss, Йена, Германия). Результаты представлены в виде считанной средней денситометрической суммы. Гистологический анализ проводил патолог с соблюдением двойной анонимности образцов для детектирования расширения канальцев и некроза, повреждения клубочков и вакуолизации.
Статистический анализ
Результаты представлены в виде средних значений ± стандартная ошибка среднего значения. Построение графика данных и статистический анализ проводили, применяя программное обеспечение Prism, версия 6, для Macintosh (Graphpad, Сан-Диего, Калифорния, США). Различия между средними значениями для двух групп оценивали статистически, применяя парный критерий Уилкоксона, тогда как статистическую значимость между более чем двумя группами анализировали с помощью двухфакторного дисперсионного анализа повторных измерений, а затем апостериорной оценки Бонферрони. Сравнение между группами считают значимыми, когда p < 0,05, тогда как значения выше считают незначимыми (н/з).
Результаты
Сравнение функциональных свойств различных препаратов ПЭГ-фосфолипида
hMSC обрабатывали различными типами препаратов ПЭГ-фосфолипида. Жизнеспособность hMSC не изменялась после модификации поверхности ПЭГ-фосфолипидами отдельно (97,3%), FITC-мечеными ПЭГ-фосфолипидами (98,3%), а также меченными биотином ПЭГ-фосфолипидами (97%), указывая на то, что ПЭГ-фосфолипиды не влияют на жизнеспособность.
Сохранение ПЭГ-фосфолипида с различными длинами субъединицы ПЭГ исследовали, используя суспензионные клетки CCRF-CEM. Клетки покрывали ПЭГ-фосфолипидом с субъединицами ПЭГ 1 кДа, 5 кДа и 40 кДа, конъюгированными с FITC. Клетки инкубировали при 37°C и связывание отслеживали с помощью проточной цитометрии. Показали, что связывание всех препаратов утрачивалось на 90% через 24 часа, но препарат 5 кДа сохранялся наиболее долгое время (фиг. 13).
Уровни TAT значительно снижались, когда покрытые ПЭГ-фосфолипидом клетки приводили в контакт с цельной кровью, по сравнению с непокрытыми клетками. Такое снижение образования TAT было сходным для клеток, покрытых либо ПЭГ-фосфолипидом отдельно (61,5 ± 2,9 по сравнению с 110 ± 7,6), либо меченым FITC ПЭГ-фосфолипидом (60,1 ± 2,7), либо меченым биотином ПЭГ-фосфолипидом (61,4 ± 5,1), по сравнению с контролями без покрытия ПЭГ-фосфолипидом (110 ± 7,6) (фиг. 2A).
Сходную тенденцию наблюдали для маркеров активации комплемента, когда покрытые и непокрытые клетки приводили в контакт с цельной кровью. Через 60 мин после контакта с кровью уровни в плазме C3a и sC5b-9 значительно снижались, если клетки были покрыты ПЭГ-фосфолипидом (50,8 ± 3,2, 37,7 ± 1,5), меченым FITC ПЭГ-фосфолипидом (51,3 ± 3,8, 35,0 ± 2,1) и меченым биотином ПЭГ-фосфолипидом (49,8 ± 4,1, 38,3 ± 2,0) по сравнению с непокрытыми клетками (104 ± 7,7, 104 ± 6,2) (фиг. 2A и 2B).
Распределение меченого FITC фосфолипида в почках свиньи, обработанных ПЭГ-фосфолипидами
Аллогенные почки трансплантировали единым блоком реципиентам (n = 6), как описано в материалах и методах. Распределение ПЭГ-фосфолипида в ткани почки после реперфузии в реципиенте анализировали в биоптатах, взятых через 5, 60 и 360 мин. На фиг. 4 показано, что флуоресценция перед реперфузией от меченого FITC ПЭГ-фосфолипида равномерно распределялась в околоканальцевых сосудах, клубочках и канальцах всей почки, отражая, что ткань почки равномерно модифицировали ПЭГ-фосфолипидом путем инъекции раствора ПЭГ-фосфолипида через остаток аорты. В отличие от этого, не наблюдали флуоресценции в тканях контрольных почек, что свидетельствовало о том, что нет значительного перетекания между тестируемой и контрольной почками.
Когда сравнивали ткани почки через 5, 60 и 360 мин, флуоресценция, в частности, в клубочках, но также в околоканальцевых сосудах и канальцах, в обработанных меченым FITC ПЭГ-фосфолипидом тканях почки постепенно уменьшалась со временем, что свидетельствовало о том, что ПЭГ-фосфолипид отделялся от клеток, хотя все еще оставалось некоторое количество ПЭГ-фосфолипида, связанного с канальцами, через 360 мин.
В долговременном исследовании для оценки отделения (C. Долговременная модель для оценки отделения ПЭГ-фосфолипида от эндотелия почки) была видна только незначительная флуоресценция через 24 ч, и через 48 ч не наблюдалась флуоресценция, что показывает, что весь ПЭГ-фосфолипид отделился. Ex vivo меченый FITC ПЭГ-фосфолипид также присоединялся к эндотелию сосудов сердца.
A. Кратковременная модель аллогенной трансплантации
Иммуногистохимический анализ трансплантированных почек
Трансплантированные почки анализировали с помощью иммуногистохимии на наличие утечки альбумина, депонирования комплемента и экспрессию рецептора (C3a, sC5b-9, C4d, C3b; фиг. 5A - 5D). Гистологическая оценка выявила более низкие уровни депонирования маркеров активации комплемента, таких как C3b/iC3b и C5b-9, и экспрессии рецептора комплемента C5aR в обработанных ПЭГ-фосфолипидом трансплантатах почки по сравнению с контрольными почками. Наблюдалось значимое снижение депонирования C3b/iC3b через 5 мин в обработанной ПЭГ-фосфолипидом почке после перфузии. Для альбумина или маркеров окислительного стресса HO-1, iNOS и нитротирозина наблюдали тенденцию (н/з), что данные маркеры были ниже в обработанных ПЭГ-фосфолипидом почках по сравнению с контрольными почками. Таким образом, результаты гистологического ранжирования подтверждают, что обработка поверхности трансплантата почки ПЭГ-фосфолипидом защищает от активации комплемента, и что наблюдается тенденция к подавлению окислительного стресса.
Активация свертывания крови и комплемента
Для того чтобы оценить влияние обработки ПЭГ-фосфолипидом на врожденную иммунную систему сосудов после реперфузии почек в модели кратковременный аллогенной трансплантации единым блоком свиньям, анализировали маркеры активации свертывания крови (TAT, фиг. 6A) и активации комплемента (C3a, sC5b-9, фиг. 5A и 5B) в крови. Уровни TAT были ниже в крови реципиентов с обработанными ПЭГ-фосфолипидом почками по сравнению с контрольными реципиентами. Наблюдали значимое снижение уровней TAT в обработанных ПЭГ-фосфолипидом почках по сравнению с непокрытыми контролями через 5 мин (46,1 ± 5,2 по сравнению с 73 ± 12,3, p: 0,01), 15 мин (48 ± 8,4 по сравнению с 73 ± 9, p: 0,02), 30 мин (41 ± 9,1 по сравнению с 57 ± 4,9, н/з), 60 мин (32 ± 4,8 по сравнению с 58 ± 3,7, p: 0,02), и 120 мин (28,6 ± 5,1 по сравнению с 53 ± 4, p: 0,02), но не через 240 мин (32 ± 4 по сравнению с 49 ± 6,1, н/з) и 360 мин (29 ± 9 по сравнению с 41 ± 14, н/з) после реперфузии. Данные результаты свидетельствовали о том, что активация свертывания крови значительно подавлялась с помощью модификации поверхности после трансплантации почки.
Сходные результаты наблюдали для маркеров комплемента (C3a и sC5b-9). Наблюдалось значимое снижение уровней C3a в крови реципиентов, которым трансплантировали обработанные ПЭГ-фосфолипидом почки, по сравнению с контрольными реципиентами через 5 мин (40 ± 2,8 по сравнению с 63,6 ± 5,4, p: 0,03), 15 мин (39 ± 4 по сравнению с 61 ± 7,2, p: 0,04), 60 мин (41 ± 5,2 по сравнению с 68 ± 5,1, p: 0,01), 120 мин (44 ± 6,1 по сравнению с 67 ± 3,1, p: 0,03), 240 мин (45 ± 12 по сравнению с 93 ± 3, p<0,0001) и 360 мин (45 ± 12 по сравнению с 80 ± 16, p<0,001), но не через 30 мин (39 ± 5,8 по сравнению с 54 ± 5,9, н/з) после реперфузии. Кроме того, также наблюдали значимое снижение уровня sC5b-9 по сравнению с контрольными реципиентами. Образование sC5b-9 в образцах из обработанных почек снижалось во все моменты времени, за исключением момента через 5 мин, по сравнению с контролями. Уровни sC5b-9 в плазме через 5 мин после реперфузии обработанных и контрольных почек составляли (16 ± 6 по сравнению с 31 ± 5, p: 0,2), через 15 мин (15 ± 3 по сравнению с 45 ± 11, p: 0,01), через 30 мин (16 ± 4 по сравнению с 45 ± 3, p: 0,01), через 60 мин (25 ± 7 по сравнению с 54 ± 4, p: 0,01), через 120 мин (36 ± 12 по сравнению с 64 ± 9, p: 0,01), через 240 мин (45 ± 11 по сравнению с 75 ± 11, p: 0,01) и через 360 мин (44 ± 14 по сравнению с 79 ± 11, p=0,008). Таким образом, данные результаты показали, что активация комплемента значительно подавлялась при покрытии эндотелия ПЭГ-фосфолипидом.
Функция почек
Функцию почек анализировали путем оценки диуреза после трансплантации почки с обработкой и без обработки ПЭГ-фосфолипидом (фиг. 10A). Наблюдалось значимое повышение общего количества выработанной мочи у реципиентов с обработанными ПЭГ-фосфолипидом почками по сравнению с контрольными реципиентами через 360 мин после реперфузии (48,3 ± 22,2 мл по сравнению с 33,5 ± 18,2 мл, p<0,05). Тем не менее, не наблюдали значимых различий между группами в отношении времени диуреза или уровней креатинина в сыворотке, поскольку почки реципиентов не удаляли.
B. Модель долговременной аллогенной трансплантации
Активация свертывания крови и комплемента
Для того чтобы оценить влияние обработки ПЭГ-фосфолипидом на врожденную иммунную систему после реперфузии почек в модели долговременной аллогенной трансплантации на свиньях, анализировали маркеры активации комплемента (C3a, sC5b-9, фиг. 8A и 8B) и активации свертывания (TAT, фиг. 8C) в крови. Уровни TAT были ниже в крови реципиентов с обработанными ПЭГ-фосфолипидом почками по сравнению с контрольными реципиентами. Значимое снижение уровней TAT в обработанных ПЭГ-фосфолипидом почках по сравнению с непокрытыми контролями наблюдали через 24 часа (372 ± 123 по сравнению с 137 ± 21, p<0,05), 48 часов (365 ± 82 по сравнению с 152 ± 17, p<0,05), 72 часа (467 ± 96 по сравнению с 135 ± 18, p<0,001) и 96 часов (428,6 ± 111 по сравнению с 168 ± 23, p<0,01), но не через 1 час (378 ± 82 по сравнению с 176 ± 24, н/з) после реперфузии. Данные результаты свидетельствовали о том, что активация свертывания крови значительно подавлялась с помощью модификации поверхности после трансплантации почки.
Сходные результаты наблюдали для маркеров комплемента (C3a и sC5b-9). Наблюдалось значимое снижение уровней C3a в крови реципиентов, которым трансплантировали обработанные ПЭГ-фосфолипидом почки, по сравнению с контрольными реципиентами через 48 часов (119 ± 40 по сравнению с 67 ± 9, p<0,001), 72 часа (95 ± 13 по сравнению с 63 ± 10, p<0,01), но не через 1 час (68 ± 11 по сравнению с 54 ± 4, н/з), 24 часа мин (128 ± 54 по сравнению с 63 ± 18, н/з) или 96 часов (103 ± 21 по сравнению с 74 ± 8, н/з) после реперфузии. Кроме того, также наблюдали значимое снижение уровня sC5b-9 по сравнению с контрольными реципиентами. Образование sC5b-9 в образцах из обработанных почек снижалось во все моменты времени, кроме момента через 5 мин, по сравнению с контролями. Уровни sC5b-9 в плазме через 5 мин после реперфузии обработанных и контрольных почек составляли через 24 часа мин (73 ± 29 по сравнению с 33 ± 16, p<0,05), 48 час (94 ± 33 по сравнению с 33 ± 11, p<0,001), 72 часа (126 ± 46 по сравнению с 41 ± 18, p<0,0001) и 96 (108 ± 23 по сравнению с 51 ± 11, p<0,01), но не через 1 час (63 ± 11 по сравнению с 33 ± 16, н/з). Таким образом, данные результаты показали, что активация комплемента значительно подавлялась при покрытии эндотелия ПЭГ-фосфолипидом.
Провоспалительные цитокины
Оценивали концентрацию цитокинов/хемокинов при долговременной аллогенной трансплантации почки. Применяя мультиплексный анализ оценивали концентрацию в плазме INFγ, IL-1β, IL-2, IL-1α, IL-1R, IL-4, IL-6, IL-10, IL-18, IL-8, IL-12 и TNF, см. фиг. 9A - 9L. Уровни IL-1β, IL-1R, IL-4, IL-6, IL-12, IL-18 и TNF значительно снижались у животных, которым трансплантировали обработанные ПЭГ-липидом почки, через 4 суток.
Функция почек
Все животные хорошо восстанавливались после трансплантации и начинали есть в течение 24 ч. Продукцию мочи подтверждали с помощью ультразвукового исследования и мочу обнаруживали в мочевом пузыре в течение 72 ч у всех свиней. Функцию почек анализировали путем оценки уровней креатина после трансплантации почки с обработкой и без обработки ПЭГ-фосфолипидом (фиг. 10B). Наблюдали значительно более низкий уровень у реципиентов с обработанными ПЭГ-фосфолипидом почками по сравнению с контрольными реципиентами за весь четырехсуточный период.
Некропсия
Не наблюдали признаков заболеваний, за исключением изменений, связанных с трансплантацией почек. Патологоанатомическое исследование проводили в Отделе патологии, SLU, Уппсала.
Постперфузионный синдром
В наших исследованиях долговременной выживаемости на свиньях показали, что у животных, которым трансплантировали обработанные ПЭГ-фосфолипидом почки, наблюдали минимальные изменения или не наблюдали изменений частоты пульса и артериального давления после реперфузии. Таким образом, продукт ПЭГ-фосфолипид также предотвращал активацию системы контакта и, в конечном счете, ПРС, см. фиг. 11.
Предварительная обработка раствором HTK
На фиг. 16A и 16B показаны результаты оценки инкубации почек свиней в течение 24 часов в дополненном ПЭГ-фосфолипидом растворе HTK при 4°C. Значения TAT представлены на фиг. 16A и значения креатинина в плазме представлены на фиг. 16B. Наблюдали значительные улучшения при выдерживании почек свиньи в растворе HTK, дополненном ПЭГ-фосфолипидом, по сравнению с контролем только с раствором HTK и без обработки ПЭГ-фосфолипидом. Низких уровней креатинина в плазме, наблюдаемых в обработанных почках свиньи, добивались даже без какой-либо дополнительной иммуносуппрессии.
Хранение органа
Когда ПЭГ-липид растворяли в жидкости для перфузии в комбинации с длительным хранением трансплантата при +4°C, наблюдали значительно меньшую активацию системы каскада (фиг. 17A - 17D) и уровни экспрессии цитокинов (фиг. 18A - 18G) в обработанных ПЭГ-липидом почках после реперфузии.
Гистологический анализ FITC-ПЭГ-фосфолипида
На фиг. 19 показаны изображения конфокальной микроскопии биоптатов из почек, обработанных FITC-ПЭГ-фосфолипидом (5 кДа) и FITC-ПЭГ-фосфолипидом (40 кДа), вместе с контролем. На данных изображениях, таким образом, показано поглощение 5 кДа ПЭГ-липида и 40 кДа ПЭГ-липида после инфузии ex vivo ПЭГ-липидов в почки из четырех различных свиней, где одну почку использовали для 5 кДа ПЭГ-липида, а другую для 40 кДа ПЭГ-липида. На фиг. 19 показано, что 5 кДа ПЭГ-липид более эффективно проникал в паренхиму почки по сравнению с 40 кДа ПЭГ-липидом. Соответственно, 40 кДа молекулы ПЭГ-липида менее эффективно фильтровались через клубочки нефронов, чем 5 кДа молекулы ПЭГ-липида.
Обсуждение
При множестве заболеваний и патологических состояний ишемия вызывает патологические изменения. В основном, четыре типа механизмов вызывают ишемию в ткани, а именно: тромбоз, трансплантация, установка зажима на артерию, ведущую к органу, и сепсис. ИРП является неизбежным событием при трансплантации органов, но оно также возникает при широком диапазоне других клинически значимых состояний, таких как смерть головного мозга, сепсис, операция на сердце, а также после реперфузии ишемической области при угрожающем инфаркте миокарда или инсульте. В данном эксперименте мы продемонстрировали, что покрытие эндотелиальной выстилки и системы канальцев конструкцией ПЭГ-фосфолипида перед трансплантацией в модели как кратковременной, так и долговременной аллогенной трансплантации свиньям, функционально заменяет GXC и сильно ослабляет первичный ответ И/Р на повреждение in vivo.
Трансплантируемая почка подвергается ишемическому повреждению на различных стадиях, начиная с периода времени в доноре до фактического события трансплантации. Поскольку трупные доноры служат основными источниками донорских органов, гемодинамическая нестабильность кровотока в трупных донорах является одной из главных причин ишемии. Теплая ишемия возникает во время сбора органа из трупных доноров и холодное ишемическое повреждение происходит в процессе консервации органов при более низкой температуре. Реперфузия органа у реципиента завершает И/Р повреждение.
Для того чтобы преодолеть данные проблемы, мы предложили новый способ местной защиты от атаки врожденной иммунной системы при трансплантации почки. Эндотелий почки и канальцы покрывали ПЭГ-фосфолипидами посредством гидрофобных взаимодействий с липидным бислоем мембраны клетки, тем самым заменяя слой GXC. Цепи ПЭГ инертны и обладают высокой биосовместимостью. Следовательно, ПЭГ-фосфолипид отдельно защищает от И/Р повреждения путем защиты мембран эндотелиальных клеток и клеток канальцев и препятствования достижению их белками и активированию последних на поверхностях эндотелиальных клеток почки.
Для обработанных ПЭГ-фосфолипидом почек у реципиентов выявили меньшую активацию иммунной системы, что отражали аттенуированные уровни в плазме TAT, FXIIa, TF, C3a и sC5b-9 и депонирование C3b на поверхности эндотелия трансплантатов почек. Это показало, что цепи ПЭГ, торчащие из липидного бислоя мембраны, могут ингибировать активацию комплемента и защищать мембраны клеток от депонирования компонентов комплемента после реперфузии свежей кровью реципиентов. Это также приводило к подавлению активации свертывания. Активация комплемента и свертывания является отличительным признаком И/Р, и пониженные уровни маркеров комплемента подтверждают концепцию защитного действия от И/Р повреждения, приводящего к отторжению.
В кратковременном исследовании за трансплантатом наблюдали в течение до 6 часов для оценки функции почек и местной гемосовместимости. Когда суспензию ПЭГ-фосфолипида вводили путем инъекции через общий фрагмент аорты для двух трансплантатов почки, ткань всей тестируемой почки равномерно покрывалась ПЭГ-фосфолипидом, включая клубочки (фиг. 4B, 4D, 4F). Макроскопическое патоморфологическое исследование трансплантатов почки не изменялось, свидетельствуя о том, что обработка трансплантата почки ПЭГ-фосфолипидом не оказывает нежелательного влияния на жизнеспособность клеток. Также, когда сравнивали суммарное выделение мочи между контрольной почкой и обработанной ПЭГ-фосфолипидом почкой, наблюдали существенные улучшения диуреза в исследуемой почке. Данные результаты свидетельствуют не только о том, что эндотелий почки был защищен от атаки врожденной иммунной системой, но также что функция почек была хорошо сохранена, несмотря на то, что клубочки были покрыты ПЭГ-фосфолипидом. Учитывая установленную связь между морфологическими изменениями после ишемического повреждения и функцией почек как инструмент, чтобы отличить жизнеспособные и нежизнеспособные почки ex-vivo, наше исследование с кратковременным наблюдением продемонстрировало эффективность покрытия ПЭГ-фосфолипидом для ослабления атаки И/Р без каких-либо нежелательных явлений на функцию почек.
Эффект ПЭГ-фосфолипида ограничен поверхностью клетки, поскольку связывание опосредовано гидрофобным взаимодействием. По результатам отслеживания флуоресценции ПЭГ-фосфолипида, связавшегося в почках, как в кратковременной, так и в долговременной модели, показали, что наблюдалось снижение интенсивности в течение периода наблюдения, свидетельствующее о том, что ПЭГ-фосфолипид отсоединялся от эндотелия. Похоже, флуоресценция мигрировала из клубочков в систему канальцев, в конечном итоге достигая основания клеток канальцев через 6 часов после трансплантации. Флуоресценция была обнаружена в моче в течение периода наблюдения, что подтверждает, что молекулы ПЭГ-фосфолипида метаболизировались почкой. В долговременном исследовании значительную флуоресценцию детектировали до 12 - 24 часов после реперфузии, и она полностью исчезала через 48 часов. Возможно, что первоначально присутствует перенасыщение ПЭГ-фосфолипидом, который легко вымывают, и что фактическая защита эндотелиальных клеток осуществляется молекулами, дающими только слабую флуоресценцию. Это подкрепляется относительно низкой флуоресценцией ПЭГ-фосфолипида в кратковременном исследовании через 6 часов после трансплантации в комбинации с защитным действием от атаки врожденной иммунной системой, о чем свидетельствуют значительные различия в уровнях TAT, C3a и sC5b-9 в крови и в депонировании C3b в трансплантатах почки. Это также поддерживалось тем, что эффективность сохранялась в долговременном исследовании до 72 часов, несмотря на то, что наблюдали более низкую плотность ПЭГ-фосфолипида, встроенного в поверхность эндотелия. Следовательно, долговременная стабильность ПЭГ-фосфолипидов достаточна.
Данное кратковременное исследование подтверждает концепцию эффективности покрытия только ПЭГ-фосфолипидом для ослабления событий И/Р повреждения путем непосредственного подавления тромбовоспаления. ПЭГ-фосфолипид был разработан, чтобы действовать как связь и спейсер для регуляторов врожденного иммунитета, связанных с клетками. Функционализованные молекулы ПЭГ-фосфолипида очень эффективно аттенуируют различные типы врожденных иммунных и тромботических реакций, таких как активация комплемента, активация системы контакта и активация тромбоцитов. Например, пептид с аффинностью к Фактору H ингибирует активацию комплемента, и апираза способна уменьшать тромботические реакции, связанные с активацией тромбоцитов. Вместе данные два регулятора могут полностью ингибировать тромбовоспаление, запускаемое в ксеногенной системе, когда эндотелиальный клетки аорты свиньи приводят в контакт с кровью человека в системе in vitro цельной крови. При рассмотрении эффекта погружения от ПЭГ-фосфолипида отдельно, добавление регуляторов в ПЭГ-фосфолипид дополнительно улучшает конструкцию в отношении ингибирования И/Р повреждения в аллогенных трансплантатах почки.
Активация системы контакта, которая является частью врожденного иммунитета, может вызывать серьезные осложнения во время операции, такие как сердечно-сосудистые нарушения и гемодинамическая нестабильность после реперфузии. Данный феномен, который ранее был описан как постреперфузионный синдром (ПРС), сначала наблюдали у реципиентов трансплантата печени, которые испытывали тяжелую гемодинамическую нестабильность после реперфузии трансплантата печени. Тем не менее, данный феномен также наблюдали у реципиентов трансплантата почки и поджелудочной железы, которые часто страдают от мгновенной гемодинамической нестабильности после реперфузии. Во время ПРС активируются белок плазмы фактор XII, пре-калликреин и высокомолекулярный кининоген, приводя к активации каскада свертывания крови и продукции брадикинина, который представляет собой очень эффективное сосудорасширяющее средство, вызывающее гемодинамическую нестабильность. Следовательно, быстрое снижение системного артериального давления приводит к нарушению перфузии трансплантата и продлению теплой ишемии трансплантата. Данные пациенты могут страдать от отсроченной функции трансплантата, повышенного риска отторжения и преждевременной утраты трансплантата. У здоровых индивидов повышенная частота пульса может частично компенсировать падение артериального давления.
В наших долговременных исследованиях выживаемости свиней было показано, что у животных, которым трансплантировали обработанные ПЭГ-фосфолипидом почки, были минимальные изменения или не было изменений в частоте пульса и артериальном давлении после реперфузии. Таким образом, продукт ПЭГ-фосфолипид также предотвращал активацию системы контакта и, в конечном счете, ПРС.
Отличие между различными длительными экспериментами состояло в том, что трансплантат в более ранних экспериментах хранили в холодильной камере при +4°C в течение 24 ч без погружения в жидкость для перфузии и что ПЭГ-фосфолипид вводили путем перфузии в сосудистую систему за 40 мин до трансплантации почки. В более поздних экспериментах трансплантат подвергали перфузии ПЭГ-фосфолипидом незамедлительно после сбора и после этого погружали в ПЭГ-фосфолипид, растворенный в жидкости для перфузии, на 24 ч при +4°C до момента трансплантации и реперфузии. Уже в первом исследовании наблюдали значительно меньшую активацию системы каскада (фиг. 8A - 8C) и экспрессию цитокинов (фиг. 9A - 9L) у животных с обработкой ПЭГ-фосфолипидом. Тем не менее, во втором исследовании активация системы каскада (фиг. 17A - 17D) и экспрессия цитокинов (фиг. 18A - 18G) были гораздо ниже по сравнению с первым исследованием и, кроме того, обработка ПЭГ-фосфолипидом приводила к значительному уменьшению активации системы каскада (фиг. 17A - 17D) и экспрессии цитокинов (фиг. 18A - 18G). Следовательно, в настоящем эксперименте явно продемонстрировали, что комбинация жидкости для перфузии и ПЭГ-фосфолипида представляла собой лучшую комбинацию. В данном эксперименте также показали, что экспрессия цитокинов была явно ниже непосредственно после реперфузии обработанных ПЭГ-фосфолипидом трансплантатов (фиг. 18A - 18G), указывая на то, что противовоспалительный эффект вызывался уже во время периода холодовой ишемии перед реперфузией, возможно благодаря ингибиторному действию на CL-11 во время ишемии, как упоминали выше.
ЭКСПЕРИМЕНТ 2
Целью эксперимента была оценка безопасности ПЭГ, конъюгированного с фосфолипидом (1,2-дипальмитоил-sn-глицерин-3-фосфатидилэтаноламин, DPPE), на крысах. Разовую дозу соединения вводили внутривенно, а затем следовал период восстановления в течение 14 суток. В условиях клиники 2 г соединения ПЭГ (MW: 5,0 кДа)/фосфолипид будут разбавлять в 1000 мл раствора для перфузии, который обычно вводят в трансплантаты органов ex vivo перед имплантацией реципиенту. Крысам в группе низкой дозы давали такую же концентрацию, и крысам в группе высокой дозы давали в 10 раз большую концентрацию, соответственно.
Дизайн исследования
Тридцать крыс Sprague Dawley обоих полов приобретали в Charles River и перевозили в Уппсалу. Эксперимент продолжался всего четыре недели, начиная с периода акклиматизации в течение двух недель, после которого животным вводили путем инъекции в произвольном порядке либо NaCl, либо низкую дозу, либо высокую дозу ПЭГ-фосфолипида (день 1). Инъекции вводили в боковую хвостовую вену. Крыс затем неоднократно осматривали в их клетках в течение 6 часов, используя для наблюдения тест Ирвина, который включает расширенное клиническое исследование неврологических и двигательных функций для выявления признаков острой токсичности. Лечение было заслеплено от наблюдающего персонала. Клинические исследования пять дней в неделю затем продолжали в течение двух недель. По окончании исследования кровь собирали путем пункции сердца под терминальной анестезией. После умерщвления всех животных незамедлительно подвергали некропсии (день 15).
Группа 1: 10 контрольных животных (5 самок, 5 самцов) получили NaCl, 1 мл
Группа 2: 10 крыс (5 самок, 5 самцов) получили 2 мг/мл ПЭГ-фосфолипида, 1 мл
Группа 3: 10 крыс (5 самок, 5 самцов) получили 20 мг/мл ПЭГ-фосфолипида, 1 мл
Клинические наблюдения
На всем протяжении исследования всех животных осматривали и проводили манипуляции 5 дней в неделю. Их вынимали из клетки и помещали на кусок синтетического флиса по одной или по двое за раз. Три раза в неделю всех крыс выпускали на большую игровую площадку, по 5 крыс за раз, чтобы они лазали, купались и исследовали. Использовали положительное подкрепление в виде кукурузных хлопьев сразу после проведения манипуляций. Им проводили полный клинический осмотр по прибытии в виварий и перед инъекцией вещества. Сразу после инъекции крыс осматривали для выявления признаков токсичности в течение шести часов с определенными интервалами. После этого их регулярно осматривал квалифицированный ветеринар. Не наблюдали клинических признаков заболевания или токсичности ни у одного животного во время акклиматизации и экспериментального периода.
Масса тела
Массы тела всех животных регистрировали перед внутривенной инъекцией и после нее дважды в неделю на всем оставшемся протяжении исследования. Набор массы тела животными был сходной величины во всех трех группах.
Офтальмологический осмотр
Всем животным проводили офтальмологический осмотр с биомикроскопией (KOWA-SL17) и офтальмоскопией (Heine Omega 500) за одну неделю до и через одну неделю после введения путем инъекции ПЭГ-фосфолипида. Крысы получали глазные капли Мидриацил® (тропикамид), 0,5%, 5 мг/мл перед осмотром. Их удерживали путем аккуратной фиксации вручную на всем протяжении процедуры.
Не наблюдали признаков токсичности на офтальмологическом осмотре. Перед введением вещества у одной самки крысы наблюдали непрозрачность роговицы правого глаза и у двух самок крыс наблюдали ядерную непрозрачность хрусталика: у одной в обоих глазах и у другой - только в правом глазу. Не наблюдали офтальмологических изменений после введения вещества, за исключением легкого раздражения эпителия у одной из самок. У двух самцов крыс перед инъекцией вещества наблюдали дегенерацию роговицы: у одной билатеральную, а у другой - только правой роговицы. У одного самца наблюдали ядерные дефекты хрусталика, а у другого - катаракту. Интравитреальное кровоизлияние в левом глазу можно было наблюдать у одного самца крысы. После введения вещества не наблюдали изменений у самцов крыс, и кровоизлияние рассосалось.
Клиническая патология
По окончании исследования кровь брали из всех животных путем пункции сердца, один мл крови разделяли по пробиркам с ЭДТА и Li-гепарином. После центрифугирования при 3000 об/мин в течение 10 мин собирали плазму и хранили при -20°C до анализа клинической биохимии. Кровь с ЭДТА незамедлительно анализировали на гематологию с помощью медицинского устройства Advia 2120 Siemens, а плазму - с помощью Architect c4000, Abbott Laboratories, согласно руководству для пользователя и стандартным операционным процедурам, в отделе клинической патологии, SLU, Уппсала. Данные анализы утверждены для грызунов. Проводили следующие гематологические исследования: кровь (B)-тромбоциты (B-TPK), B-эритроциты (B-EPK), B-гемоглобин (B-Hb), B-средний объем эритроцитов (B-MCV), B-средняя концентрация гемоглобина в эритроцитах (B-MCHC), эритроциты-ретикулоциты, ширина распределения эритроцитов по объему (RDW), среднее содержание гемоглобина в эритроците (MCH), средний объем тромбоцитов (MPV), эритроциты-морфология, B-лейкоциты (B-LPK), B-нейтрофилы, B-эозинофилы, B-базофилы, B-лимфоциты, B-моноциты, - и в качестве клинической биохимии проводили следующие измерения: натрий, калий, глюкоза, общий холестерин, мочевина, креатинин, общий белок и альбумин, аланинаминотрансфераза (АЛТ), аспартатаминотрансфераза (АСТ) и желчные кислоты. Когда возможно, проводили следующие анализы мочи: pH, белок, глюкоза и кровь.
Результаты всех анализов крови и плазмы находились в рамках нормальной области значений для крыс Sprague Dawley в возрасте 8 - 16 недель. В пяти образцах мочи была обнаружена кровь.
Патология
Всех животных подвергали эвтаназии в рамках запланированной некропсии в день 15 путем обескровливания под анестезией изофлураном и кислородом. Массы тела регистрировали после умерщвления и проводили макропатологию. Не было обнаружено макроскопических отклонений от нормы ни у одного из животных.
Выводы
Клинические исследования, включая офтальмологические исследования, не выявили каких-либо признаков токсичности ни в одной из групп животных с низкой дозой, высокой дозой и контрольной группе. Все гематологические и биохимические анализы находились в рамках нормальной области значений и не были обнаружены макроскопические отклонения от нормы при некропсии ни у одного из животных. Можно заключить, что внутривенное введение ПЭГ-фосфолипида хорошо переносится крысами при концентрации до 20 мг/мл.
ЭКСПЕРИМЕНТ 3
Галлий-68 (68Ga) представляет собой излучатель позитронов со временем полужизни 68 мин, который широко применяют в качестве диагностического радионуклида в позитрон-эмиссионной томографии (ПЭТ)/компьютерной томографии (КТ). Радиоактивно меченую молекулу ПЭГ-фосфолипида 68Ga-NO2A-ПЭГ-фосфолипид получали путем двухэтапного синтеза.
Получение буферов и исходных растворов.
Соляная кислота (HCl) 0,1 М для элюирования 68Ga. Концентрированную HCl (9,00 мл, d=1,17 г×мл-1, 11,23 М, 32-35% Ultrapure NORMATOM для анализа металлических микроэлементов) добавляли в воду (1000 мл, Thermo Fisher, Ultra Trace Analytical Grade) и смешивали и хранили при 4°C в темноте непосредственно во флаконе с водой. Аликвоту держали при КТ в пластиковом флаконе (Nalgene, полиэтилен высокой плотности с низким содержанием металлов в смоле, Thermo Fischer) перед элюированием из генератора.
Вода без металлов. Получали деионизированную воду в стеклянном флаконе из очистителя воды (MillieQ). Аликвоту переносили в пластиковый контейнер и хранили над Chelex-100, чтобы удалить ионы металлов.
NO2A-азид, 1,0 М раствор в ДМСО и воде. 1,4,7-триазациклононан-1,4-бис(уксусная кислота)-7-(3-азидопропилацетамид)тригидрохлорид (NO2A-азид, Macrocyclics, молекулярная масса по формуле соединения 494,8 г/моль) (1,0 мг, 2,0 мкмоль) добавляли в пробирку Eppendorf (2 мл). Твердое вещество сначала растворяли в диметилсульфоксиде (ДМСО, 50 мкл) и очень медленно разбавляли по каплям водой без металлов (1950 мкл) до получения гомогенного 1,0 М раствора.
Ацетат натрия, 1,0 M, буфер pH 3,5. Воду без металлов использовали на всех этапах получения буфера. Ацетат натрия (8,203 г, 0,100 моль, 99,995% исходя из массы металлов, TraceSELECT) растворяли в воде (100 мл) в пластиковой бутыли (Nalgene, HDPE, низкое содержание металлов в смоле) и pH подводили до 4,5, 4,0 или 3,5 путем добавления концентрированной уксусной кислоты (≥99%, TraceSELECT для анализа на микроэлементы), используя пластиковую пипетку. Конечный объем составлял более 100 мл из-за добавления соли и кислоты, следовательно, молярность конечного раствора составляла менее 1,0 М. Последовательно отбирали аликвоты буфера приблизительно по 5 мл и измеряли pH с помощью откалиброванного pH-метра (Mettler Toledo). Аликвоты отбрасывали после измерения pH, чтобы избежать какого-либо контаминирования металлами от pH-зонда. Конечный буфер хранили над Chelex 100 и фильтровали через 0,5 мкм шприцевой фильтр перед дальнейшим использованием.
Гидроксид натрия, 1,0 М раствор. Раствор гидроксида натрия (100 мкл, 10 М, биологической чистоты выше стандартной, Sigma Aldrich) разбавляли водой без металлов (900 мкл) в пробирке Eppendorf.
Элюирование из генератора 68Ga
68Ga элюировали из генератора 68Ga/68Ge (генератор 50 мКи, Обнинск, Россия) с 0,1 М HCl (5,0 мл, прибл. 0,8 мл/мин), применяя пластиковый шприц емкостью 10 мл и моторизованный шприцевой инфузионный насос (Univentor 864, Мальта). Полученный в результате этого раствор фракционировали в пробирках Eppendorf с получением малого объема и высокой концентрации радиоактивности.
Фракция 1: время 0 - 45 с, 600 мкл, 0 МБк - отбрасывали
Фракция 2: время 45 - 1 мин, 15 с, 400 мкл, 212 МБк - сохраняли для мечения
Фракция 3: время 1 мин, 15 с - 6 мин, 15 с, 4000 мкл, 281 МБк - отбрасывали
Способ ВЭЖХ
Система ВЭЖХ LaPrep Sigma (Hitachi), оборудованная ручным инжектором (Rehodyne 7225i, размер петли 20 мкл), УФ-детектором (4D LWL, Knauer) с внешней аналитической УФ-проточной кюветой (2 мкл), соединенной оптическими кабелями, и детектором радиоактивности (Flow Count, Bioscan), оборудованным модулем расширенного диапазона FC 6106 (Eckert и Ziegler) и луночным детектором PMT/NaI FC-3300 (Eckert и Ziegler), который был присоединен последовательно после УФ-детектора. Петля из нержавеющей стали была предпочтительна над пластиковой петлей внутри радиодетектора вследствие склонности к прилипанию анализируемых радиоактивных материалов. Устройство ВЭЖХ контролировалось программным обеспечением, в качестве которого использовали OpenLAB (Agilent), и результаты анализировали, применяя то же программное обеспечение.
Ионизационная камера (VDC 202, Veenstra Istruments, используемый фактор калибровки для 68Ga составлял 751).
Способ A: обращенно-фазовый, колонка C18 YMC-Pack ODS-AL, AL12S05-1046WT, AL-301, (YMC Europe GmbH) 100×4,6 мм (внутр. диаметр), 5 мкм, 120A. Растворитель A: вода и 0,1 % ТФУ, растворитель B: ацетонитрил и 0,1% ТФУ. Градиент растворителя 5 - 70 % B в течение 5 мин, затем 70% B в течение 3 мин. Скорость потока 1,0 мл∙мин-1.
Способ B: Эксклюзионная хроматография, колонка: Superdex™ Peptide 10/300 GL, GE Healthcare. Изократический элюент 30% B. Скорость потока 0,80 мл∙мин-1.
Синтез [68Ga]NO2A-азида
Гидроксид натрия 1,0 М (40 мкл, 40 мкмоль) и буфер ацетат натрия 0,10 М (25 мкл, pH 3,5) смешивали в пробирке Eppendorf (2 мл) и добавляли к 68Ga (179 МБк) в 0,1 М HCl (400 мкл). После этого добавляли раствор NO2A-азида (10 мкл, 1,0 М в смеси ДМСО/чистая вода (1/39) в объемном отношении) (общий объем реакции 250 мкл) и пробирку встряхивали на вортексе, центрифугировали и нагревали до 80°C в нагревательном устройстве в течение 15 мин с получением меченого 68Ga NO2A-азида, см. фиг. 14 Неочищенную реакционную смесь анализировали, используя способ A радио-ВЭЖХ, длина волны λ = 215 нм, tR: нет сигнала (УФ), 3,7 мин (радио), и применяли для последующих реакций без дополнительной очистки. Радио-ВЭЖХ, способ B, использовали для получения непрореагировавшего эталона 1 для клик-реакции, tR: нет сигнала (УФ), tR: 25,7 мин (радио).
Синтез дибензоциклооктина (ДБЦО)-ПЭГ-липида
Mal-ПЭГ-липид (20 мг) приводили в реакцию с цистеином (2 мг) в ФБР (1 мл) в течение 1 ч при КТ и очищали с помощью центрифужной колонки (Protein Desalting Spin Column, Thermo Fisher Scientific) с получением Cys-ПЭГ-липида после лиофилизации. Затем Cys-ПЭГ-липид (10 мг в ФБР) приводили в реакцию с ДБЦО-C6-NHS эфиром (6 мг, Click Chemistry Tools LLC) в ДМСО (1 мл) в течение 1 ч при КТ. После добавления 10 мл чистой воды преципитат удаляли путем фильтрации (размер пор: 0,2 мкм, Millex®-GV, Merck Millipore Ltd.), с последующей сушкой под вакуумом с получением ДБЦО-ПЭГ-липида (5 мг). Эффективность мечения ДБЦО составляла 80 %, что рассчитывали по поглощению УФ ДБЦО.
Синтез 68Ga-NO2A-ПЭГ-липида
ДБЦО-ПЭГ-липид (2,0 мг, 333 нмоль липида, 75% функционализации ДБЦО, 250 нмоль ДБЦО) и ФБР (50 мкл) добавляли в пробирку Eppendorf (2 мл). Центрифугу использовали для осаждения всего материала на дно пробирки. Затем добавляли 450 мкл из полученного ранее раствора [68Ga]NO2A-азид (116 МБк, 9,0 нмоль). Конечное отношение ДБЦО/азида в реакционной смеси составляло 1/28 в молярном отношении. Реакционную смесь оставляли при КТ в течение 10 мин, а затем нагревали до 60°C в нагревательном устройстве в течение 10 мин.
450 мкл реакционной смеси переносили в колонку NAP-5 (колонка с сефадексом ® G-25, степени чистоты для работы с ДНК, заранее уравновешенная 5 мл ФБР, порог 5 кДа, GE Healthcare), которую элюировали ФБР фракциями по 200 мкл. Желательный продукт 68Ga-NO2A-ПЭГ-липид, см. фиг. 15, элюировали фракциями 2 - 4 (35,0 МБк, радиохимический выход с поправкой на распад 32% в клик-реакции на основании добавленного количества [68Ga]NO2A-азида, радиохимический выход без поправки на распад 7% на основании общего количества элюированного 68Ga) и анализировали на радио-ВЭЖХ, оборудованном колонкой для эксклюзионной хроматографии (Superdex™ Peptide, 10/300 GL, GE), длина волны λ=254 нм, tR: 21,5 мин, радиохимическая чистота >92%. Основной примесью был непрореагировавший [68Ga]NO2A-азид (5%), tR: 25,7 мин.
ЭКСПЕРИМЕНТ 4
Исследования с помощью ПЭТ/магнитно-резонансной томографии (МРТ) проводили на основании результатов исследований in vitro, чтобы отследить распределение конструкции ПЭГ-фосфолипида в почках свиньи и оценить количество ПЭГ-фосфолипида, которое распределилось в почках.
68Ga-NO2A-ПЭГ-липид (в ФБР) смешивали с немеченым MeO-ПЭГ-липидом (в растворе HTK) непосредственно перед применением (68Ga-NO2A-ПЭГ-липид/MeO-ПЭГ-липид = 1/4 в молярном отношении, [ПЭГ-липид] = 2,0 мг/мл).
Кровь вымывали из почки свиньи с помощью холодного ФБР, а затем почку промывали раствором HTK при 4°C и помещали в пластиковый пакет, заполненный раствором HTK, на ночь. Раствор 68Ga-NO2A-ПЭГ-липида (2 мг/мл, в HTK, 20 мл, по меньшей мере 10 МБк) аккуратно вводили путем инъекции в артерию почки свиньи с помощью шприца и инкубировали в течение 30 мин на льду. После промывки почки холодным раствором HTK (50 мл), обработанную почку помещали на платформу устройства ПЭТ/МРТ (nanoScan®, Mediso Medical Imaging Systems, Будапешт, Венгрия). Платформа была предназначенная для большой крысы от сканера ПЭТ/3T МРТ для доклинических исследований небольшого животного. Использовали поисковое сканирование МРТ (GRE Multi-FOV) для установки положения ложа для сканирования целой почки на ПЭТ. Статическое исследование ПЭТ, множество сканирований ложа, проводили в течение 40 минут. Измерения МРТ проводили при 3 T, используя катушку приемопередатчика для исследования всего тела почки свиньи. Последовательность градиентного эха (GRE MultiFOV) получали со следующими параметрами: количество возбуждений (NEX): 2; время повторения (TR): 396 мс; эхо-время (TE): 4,15 мс; переворот: 45; срезы: 180; толщина среза: 1 мм; поле зрения (FOV): 64×64 мм2; пространственное разрешение: 0,5×0,5 мм2; время захвата: 14 мин. Данные ПЭТ в режиме списка реконструировали, применяя алгоритм Tera tomo 3D (4 итерации, размер воксела: 0,40 мм, матрица: 212×212×582).
Изображения ПЭТ и МРТ анализировали, применяя PMOD (версии 3.510; PMOD Technologies Ltd.). Интересующие объемы очерчивали вручную на наложенных изображениях ПЭТ-МРТ, чтобы они содержали целую почку и область вокруг мозгового вещества. Распределение изотопного маркера в остальной части почки оценивали путем вычитания из значения для целой почки значения для области вокруг мозгового вещества.
Поглощение каждой тканью выражали в МБк, распад корректировали на время введения. Количество введенной радиоактивности и элюаты из вены со всех этапов промывки измеряли на дозкалибраторе (VDC-405, Veenstra Instrumenten, Нидерланды) и распад корректировали на время введения. Все измерения проводили при КТ. После первого измерения с помощью ПЭТ/МРТ и гамма-счетчика почку снова промывали холодным раствором HTK (50 мл), а затем почку помещали на платформу устройства ПЭТ/МРТ для второго измерения.
Результаты
Почку свиньи обрабатывали 68Ga-NO2A-ПЭГ-липидом таким же способом, как при трансплантации почки свиньям-реципиентам, а затем проводили визуализацию ПЭТ/МРТ. После обработки почки 68Ga-NO2A-ПЭГ-липидом путем инъекции и вымывания через артерию проводили визуализацию, чтобы оценить распределение 68Ga-NO2A-ПЭГ-липида. Сигнал 68Ga-NO2A-ПЭГ-липида был распределен по всей почке, и также более высокий сигнал был, в частности, обнаружен в области мозгового вещества (81 %) по сравнению с областью коркового вещества (19 %). Когда ту же почку визуализировали повторно через 90 мин после дополнительной промывки раствором HTK, результат визуализации был почти таким же. Сигнал 68Ga-NO2A-ПЭГ-липида был все еще распределен по всей почке, и более высокий сигнал был обнаружен в области мозгового вещества (93 %) по сравнению с областью коркового вещества (7 %). Данные результаты показали, что все ткани и сосуды в почке были покрыты 68Ga-NO2A-ПЭГ-липидом благодаря инъекции, и ткани и сосуды в области мозгового вещества были хорошо модифицированы 68Ga-NO2A-ПЭГ-липидом.
Варианты реализации, описанные выше, следует понимать как несколько иллюстрирующих примеров настоящего изобретения. Специалистам в данной области техники очевидно, что можно осуществить различные модификации, комбинации и изменения в вариантах реализации, не отклоняясь от объема настоящего изобретения. В частности, различные части решений в различных вариантах реализации можно комбинировать в других конфигурациях, когда это технически возможно. Объем настоящего изобретения, тем не менее, определяется прилагаемой формулой изобретения.
ссылочные материалы
[1] Miura et al., Encapsulation of islets with ultra-thin polyion complex membrane through poly(ethylene glycol)-phospholipids anchored to cell membrane. Biomaterials, 2006, 27:5828-5835.
[2] Teramura et al., Behavior of Synthetic Polymers Immobilized on Cell Membrane. Biomaterials, 2008, 29:1345-1355.
[3] Teramura and Iwata, Improvement of graft survival by surface modification with poly(ethylene glycol)-lipid and urokinase in intraportal islet transplantation. Transplantation. 2011, 91(3):271-278.
[4] Nilsson et al., Autoregulation of thromboinflammation on biomaterial surfaces by a multicomponent therapeutic coating. Biomaterials. 2013, 34(4):985-994.
[5] Engberg et al., Inhibition of complement activation on a model biomaterial surface by streptococcal M protein-derived peptides. Biomaterials. 2009, 30(13):2653-2659.
[6] Teramura and Iwata, Surface Modification of Islets With PEG-Lipid for Improvement of Graft Survival in Intraportal Transplantation. Transplantation. 2009, 88(5):624-630.
[7] Asif et al., Heparinization of cell surfaces with short peptide-conjugated PEG-lipid regulates thromobinflammation in transplantation of human MSCs and hepatocytes. Acta Biomateriala. 2016, 35:194-205.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ ПРОЛОНГИРОВАНИЯ ВЫЖИВАЕМОСТИ ПОСЛЕ ОРТОПИЧЕСКОЙ И ГЕТЕРОТОПИЧЕСКОЙ ТРАНСПЛАНТАЦИИ КСЕНОГЕННОГО СЕРДЦА, ПОЧКИ, ЛЕГКОГО ИЛИ ПЕЧЕНИ | 2019 |
|
RU2795429C2 |
| РАСТВОР ДЛЯ КОНСЕРВАЦИИ ОРГАНОВ | 2024 |
|
RU2840731C1 |
| СПОСОБЫ РЕЦЕЛЛЮЛЯРИЗАЦИИ ТКАНИ ИЛИ ОРГАНА ДЛЯ УЛУЧШЕНИЯ ПРИЖИВЛЕНИЯ ТРАНСПЛАНТАТА | 2011 |
|
RU2611361C2 |
| УЛУЧШЕНИЕ ОРГАНОВ ДЛЯ ТРАНСПЛАНТАЦИИ | 2014 |
|
RU2665364C2 |
| Способ профилактики криза отторжения почечного аллотрансплантата | 1990 |
|
SU1827253A1 |
| Способ гипотермической оксигенированной двойной машинной перфузии трансплантата печени от посмертного донора | 2023 |
|
RU2830104C1 |
| СПОСОБ ПРОФИЛАКТИКИ РЕПЕРФУЗИОННЫХ ПОВРЕЖДЕНИЙ ДОНОРСКИХ ОРГАНОВ | 2011 |
|
RU2487704C2 |
| УЛУЧШЕНИЕ ОРГАНОВ ДЛЯ ТРАНСПЛАНТАЦИИ | 2014 |
|
RU2778304C2 |
| ПРИМЕНЕНИЕ ОКИСИ УГЛЕРОДА ДЛЯ УЛУЧШЕНИЯ РЕЗУЛЬТАТА ТКАНЕВОЙ И ОРГАННОЙ ТРАНСПЛАНТАЦИИ И ПОДАВЛЕНИЯ АПОПТОЗА | 2002 |
|
RU2376997C2 |
| Способ профилактики отторжения трансплантата трупной почки | 2018 |
|
RU2688172C1 |
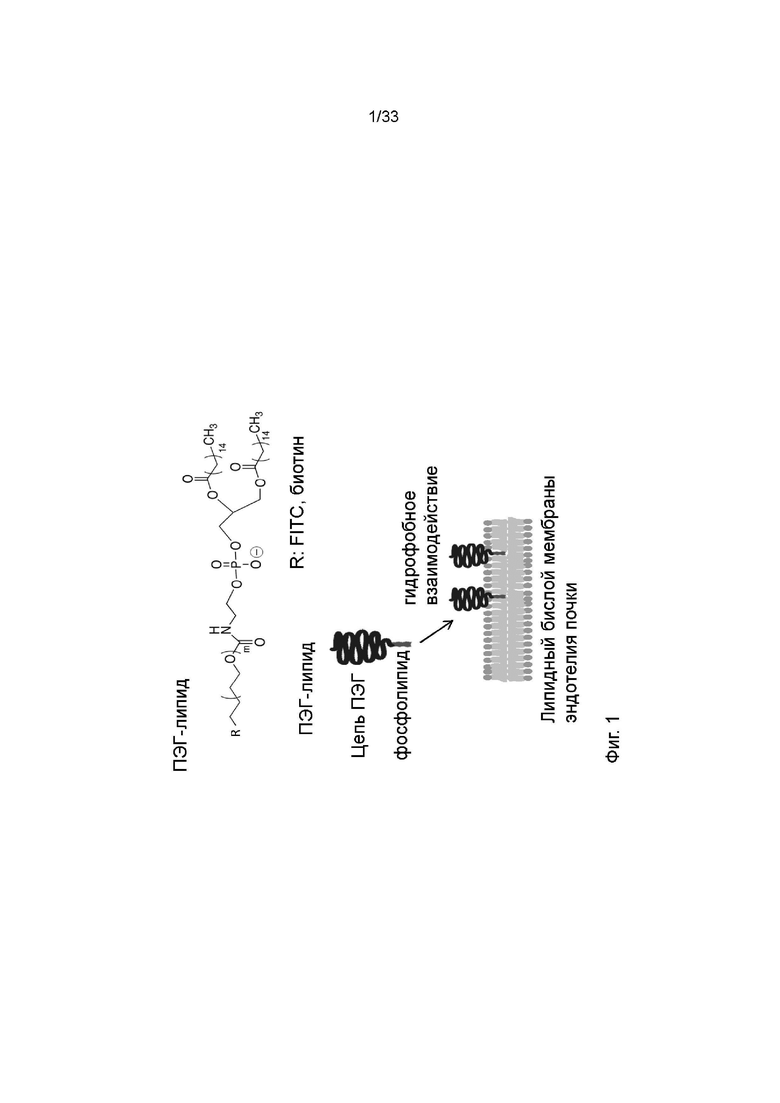
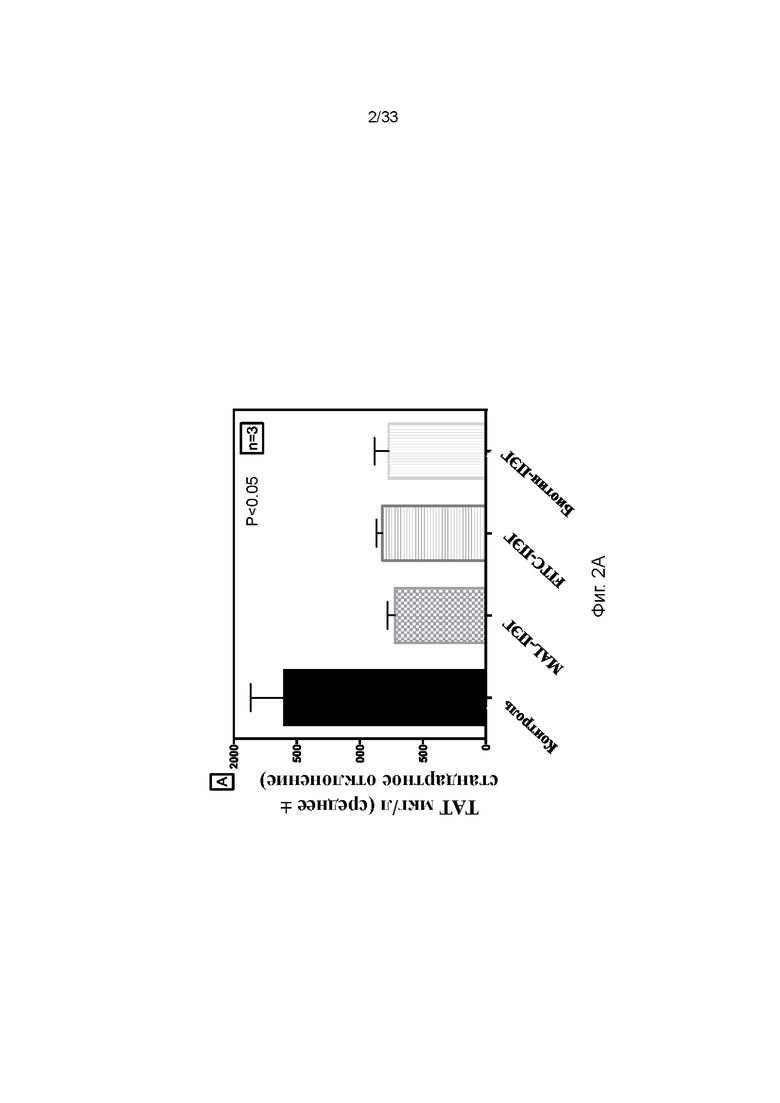
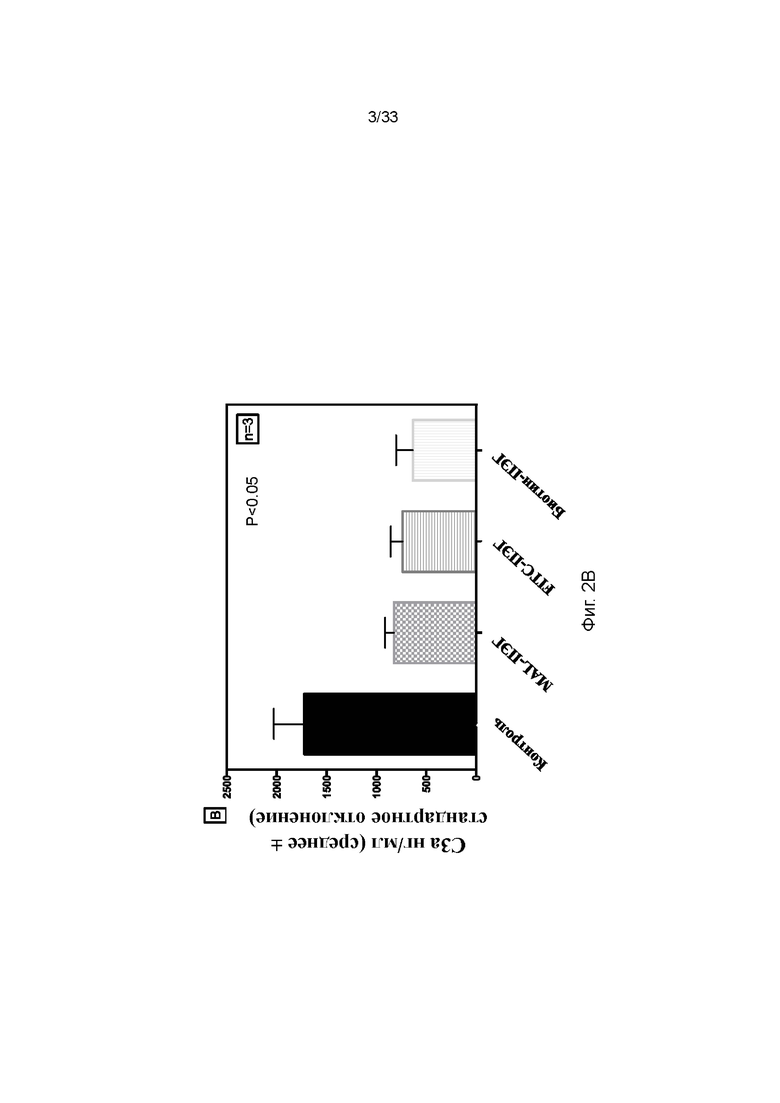
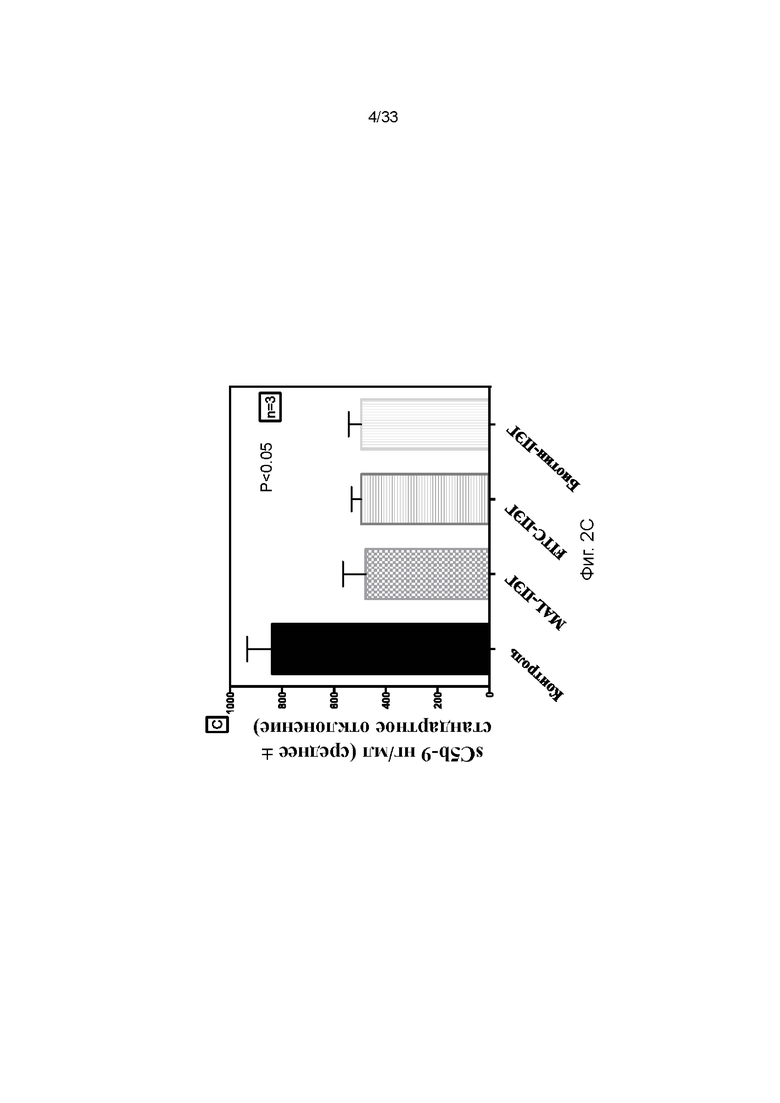
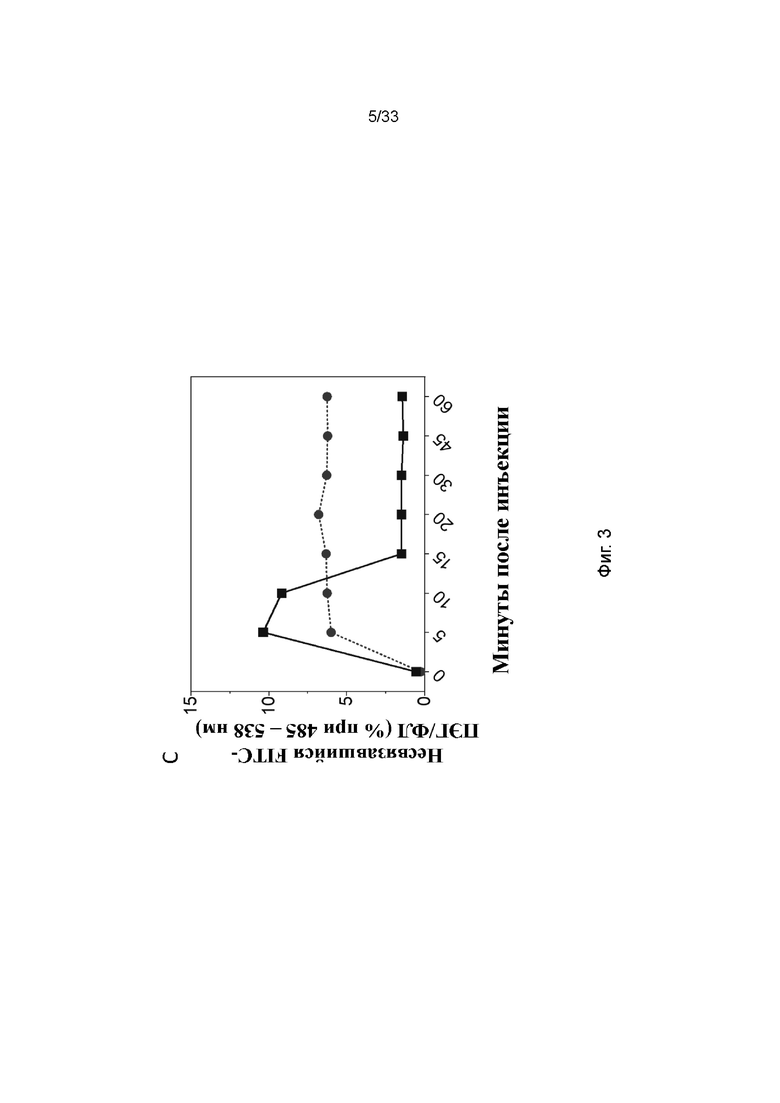
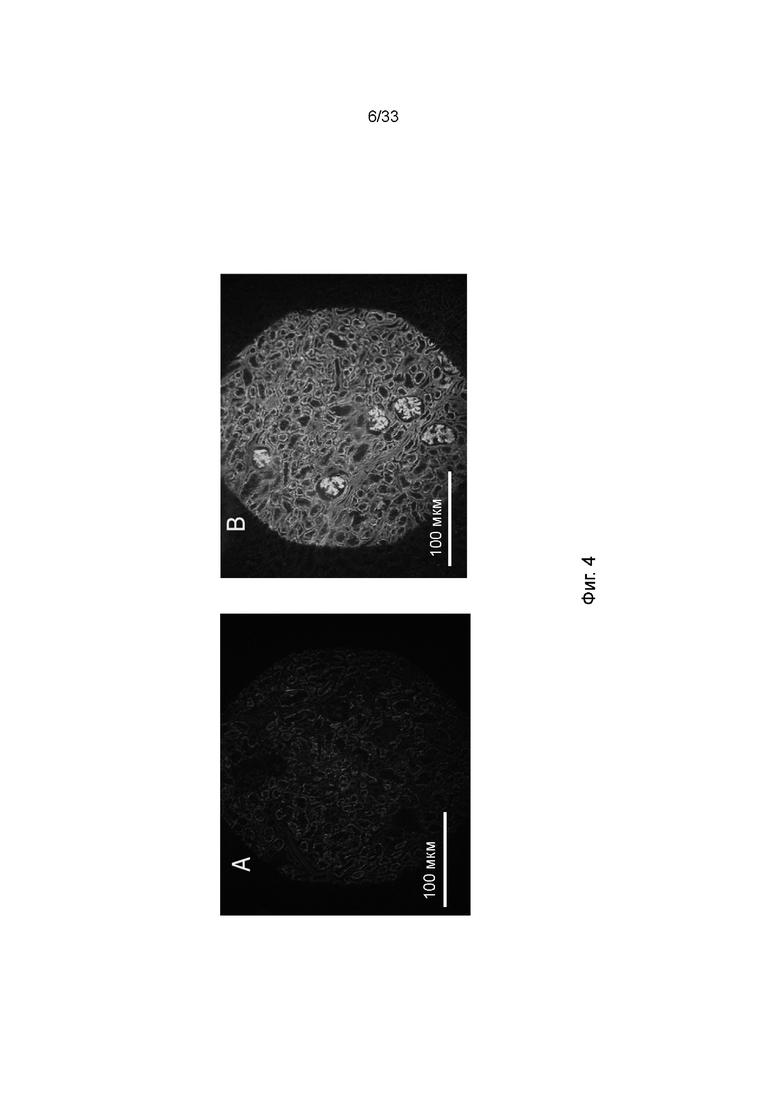
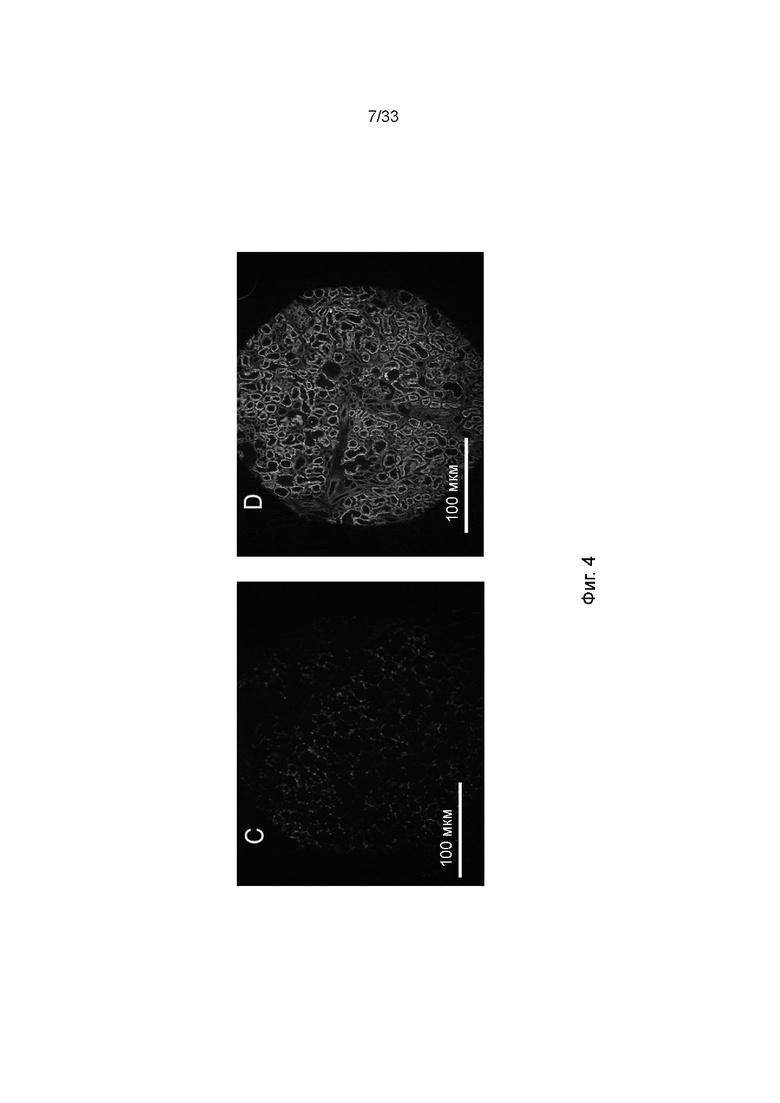
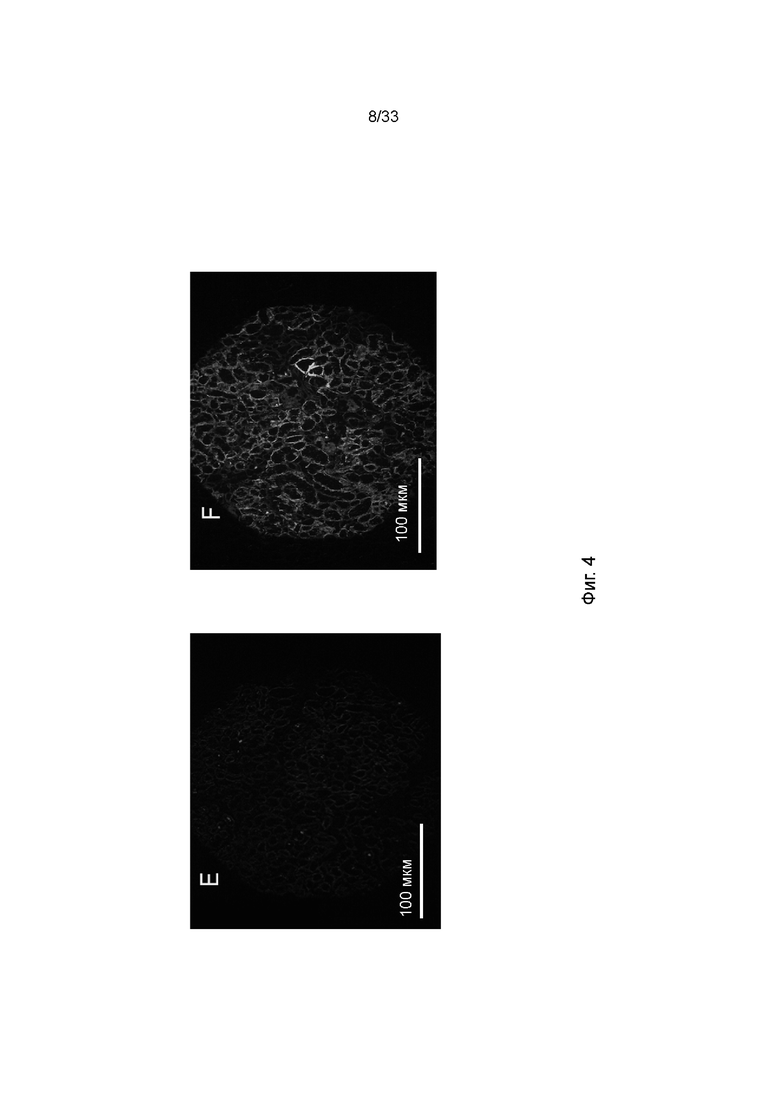
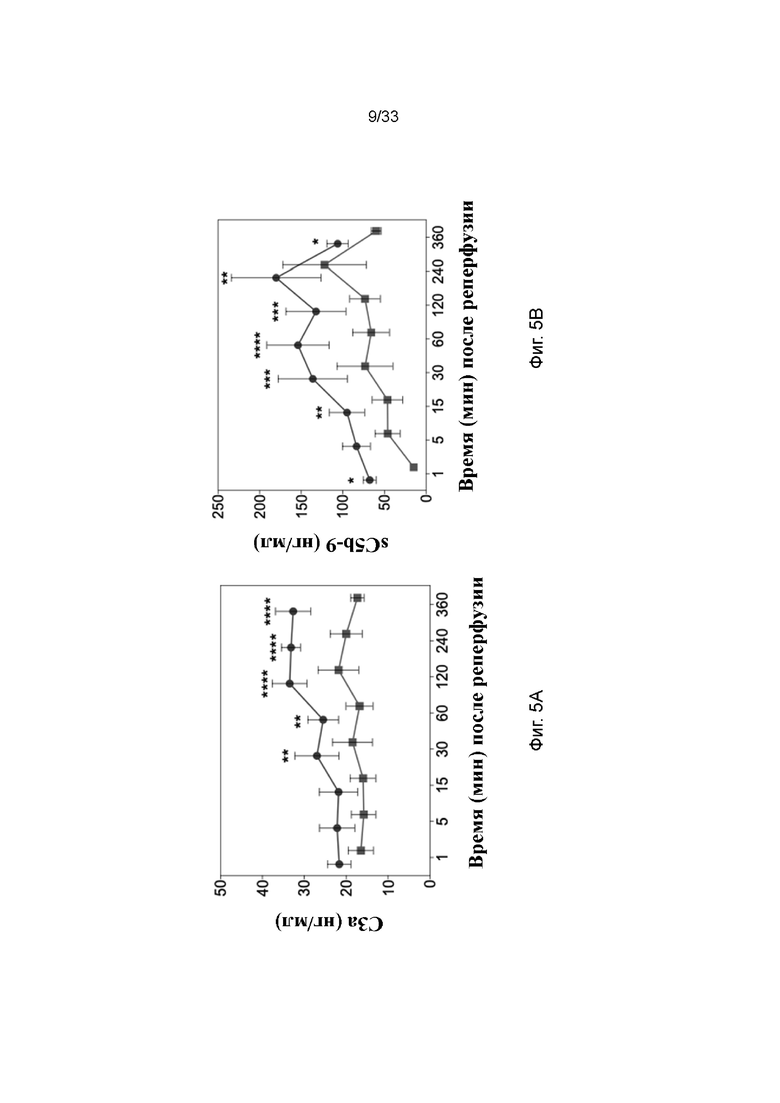
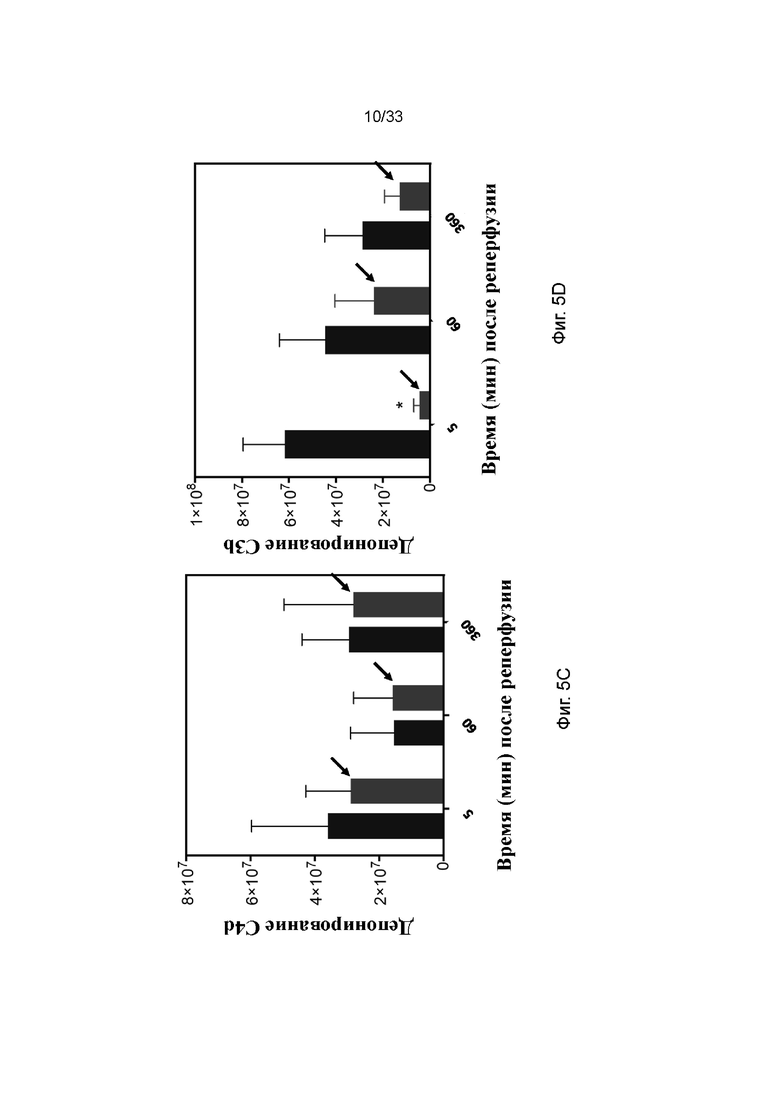
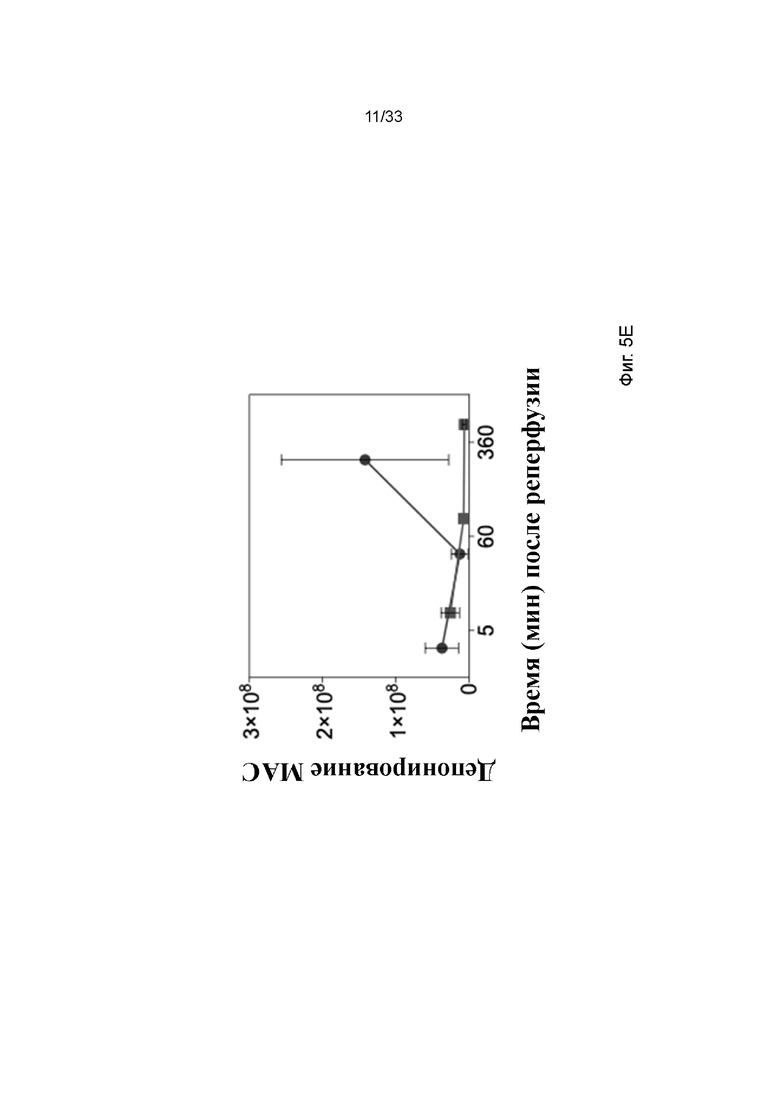
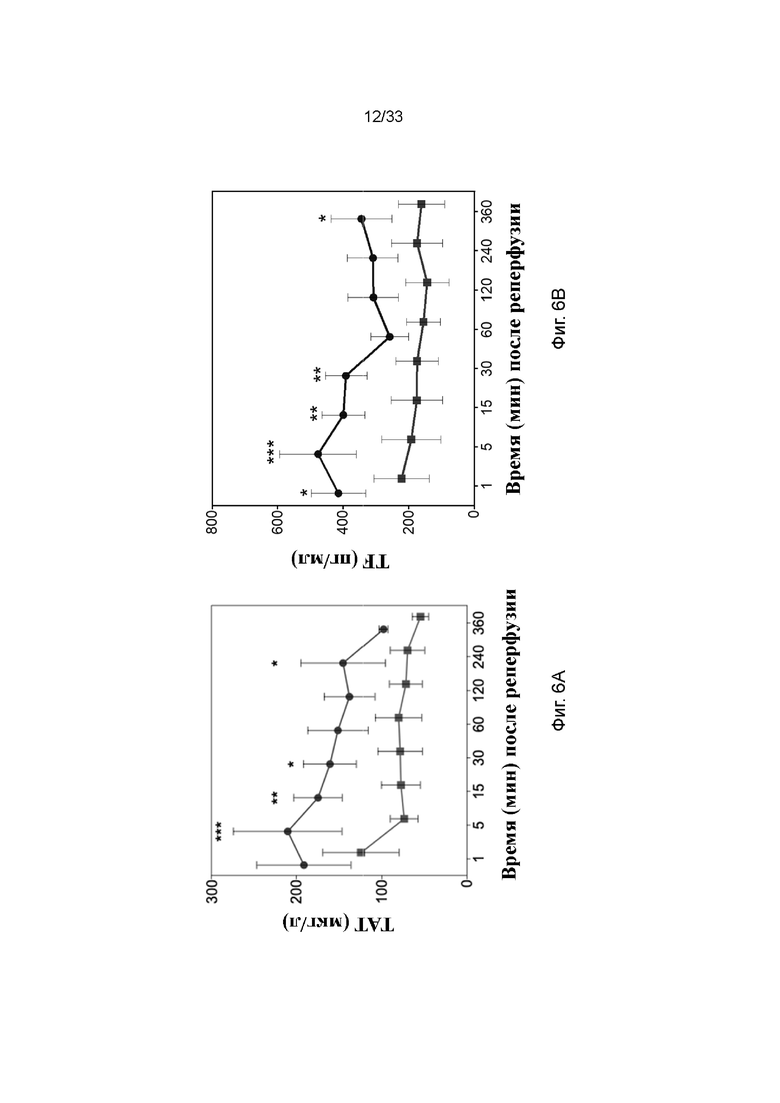
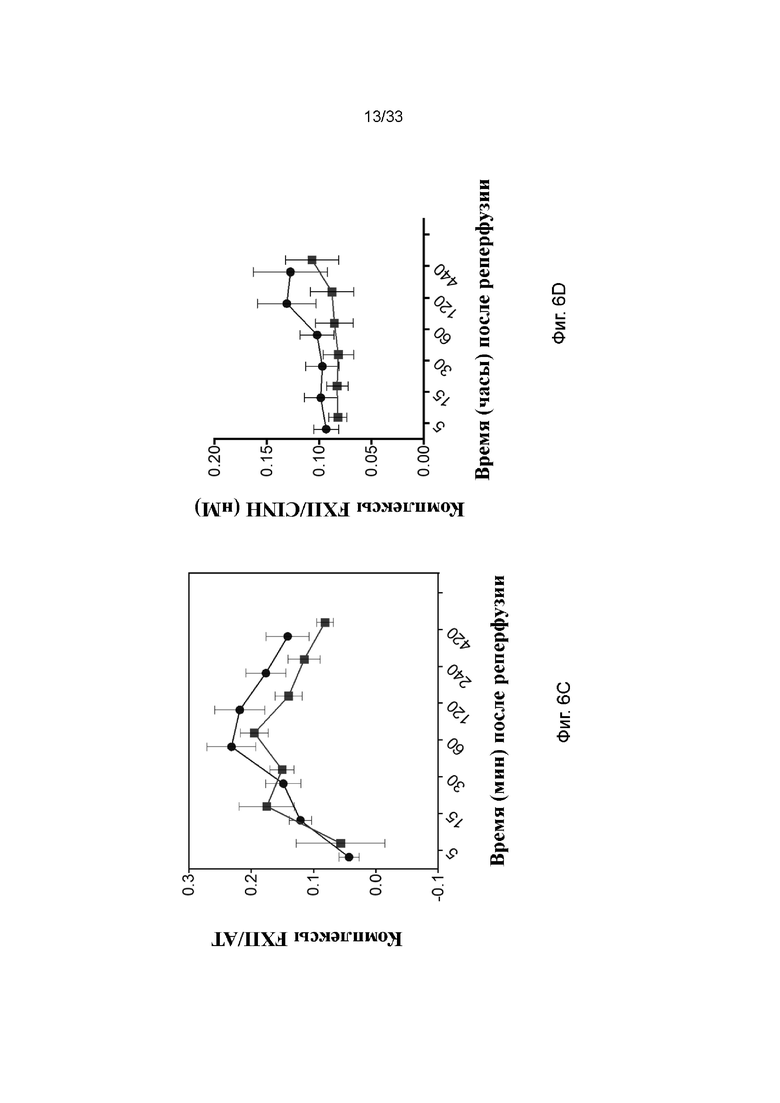
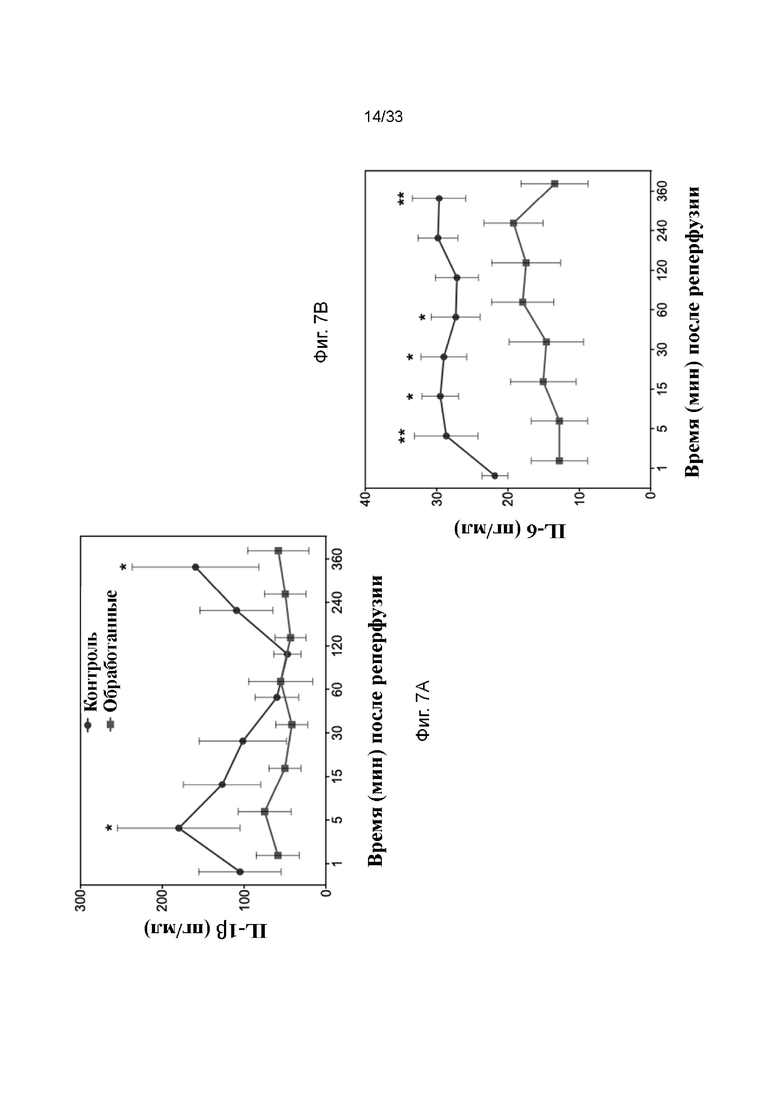
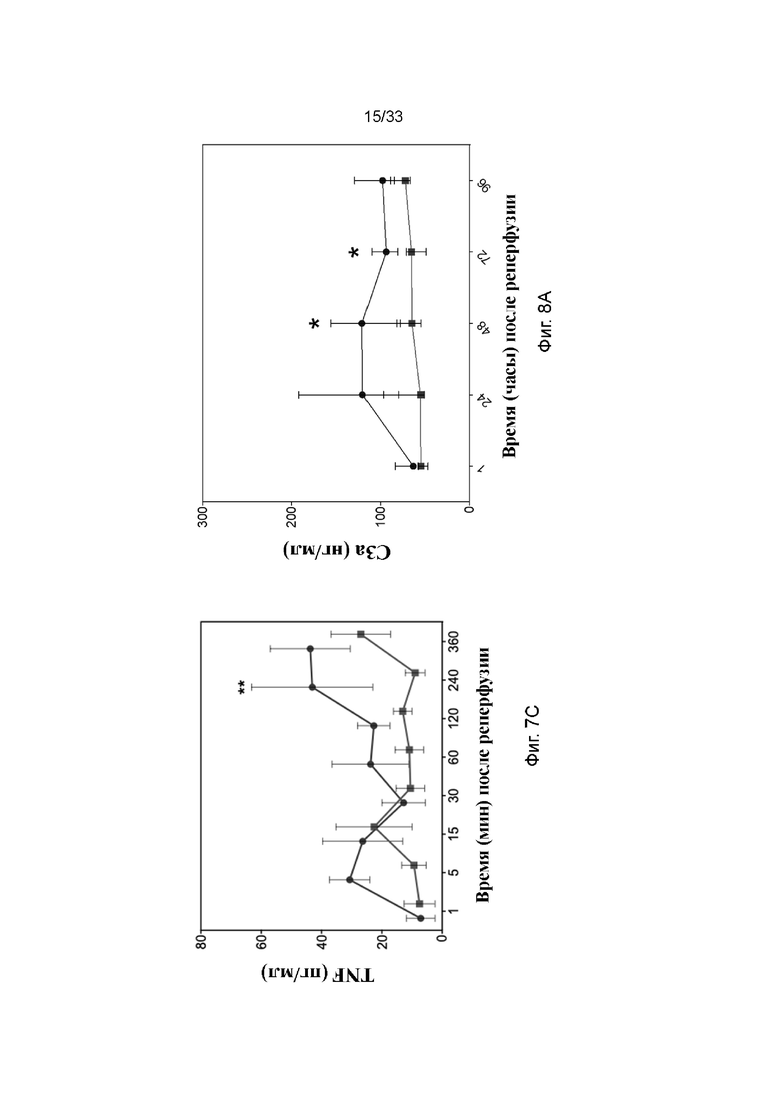
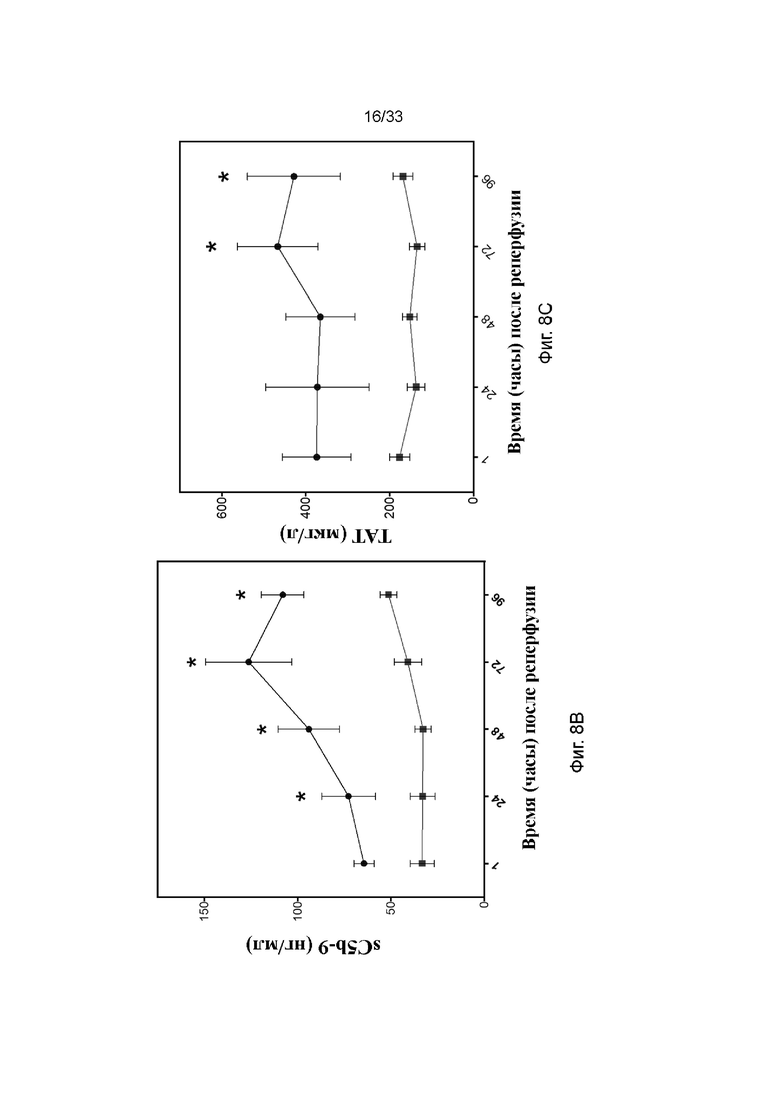
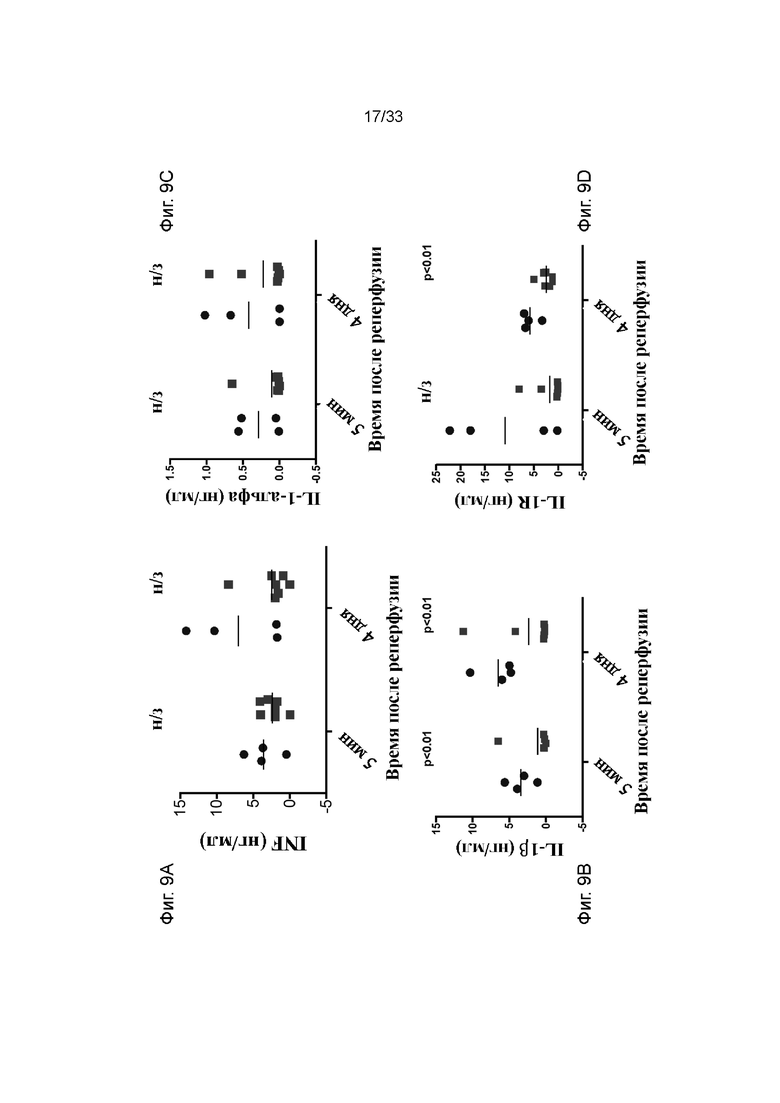
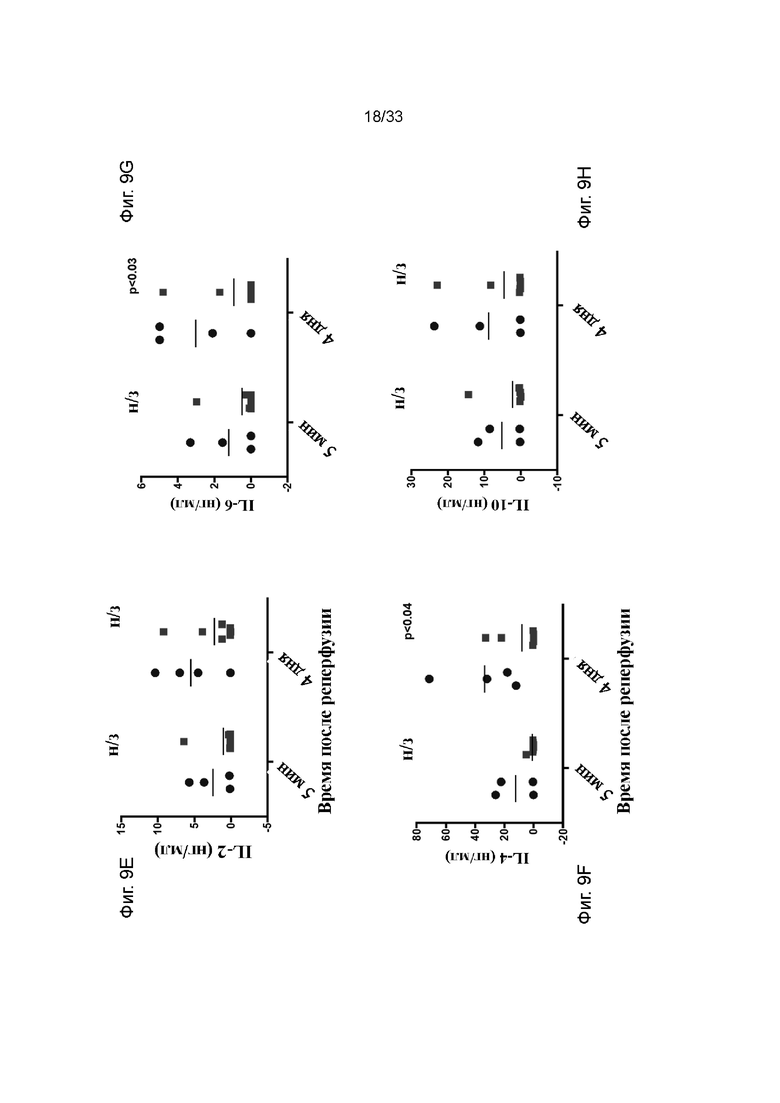
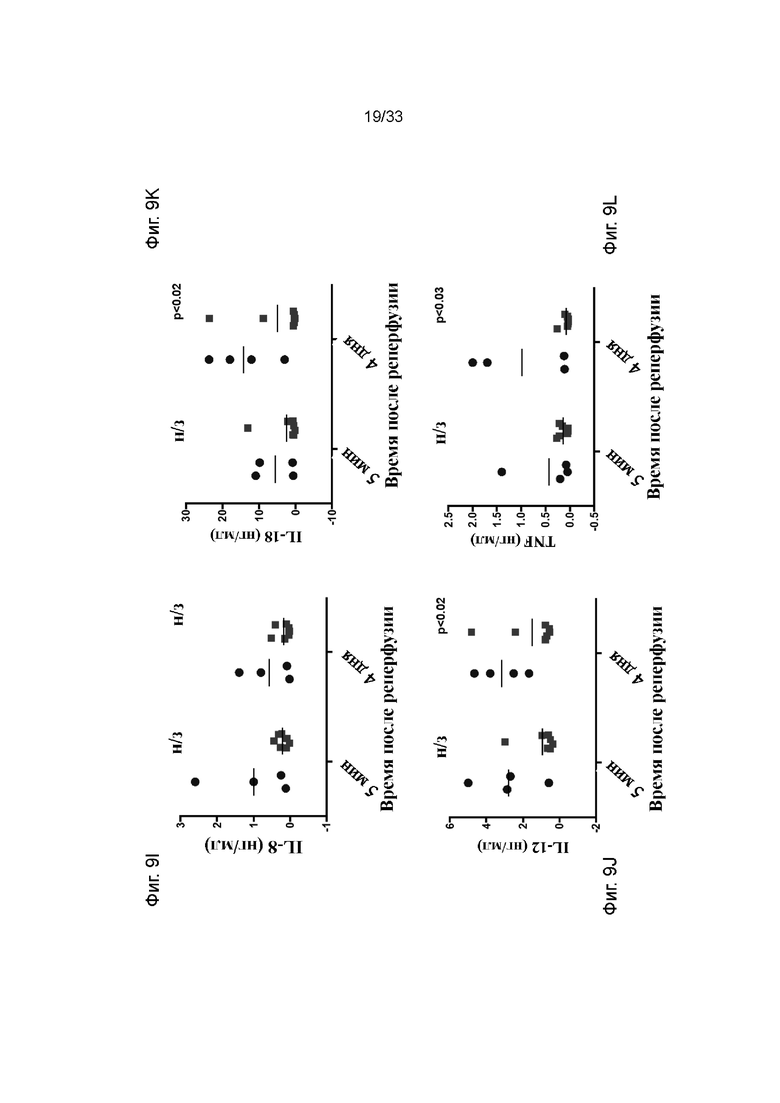
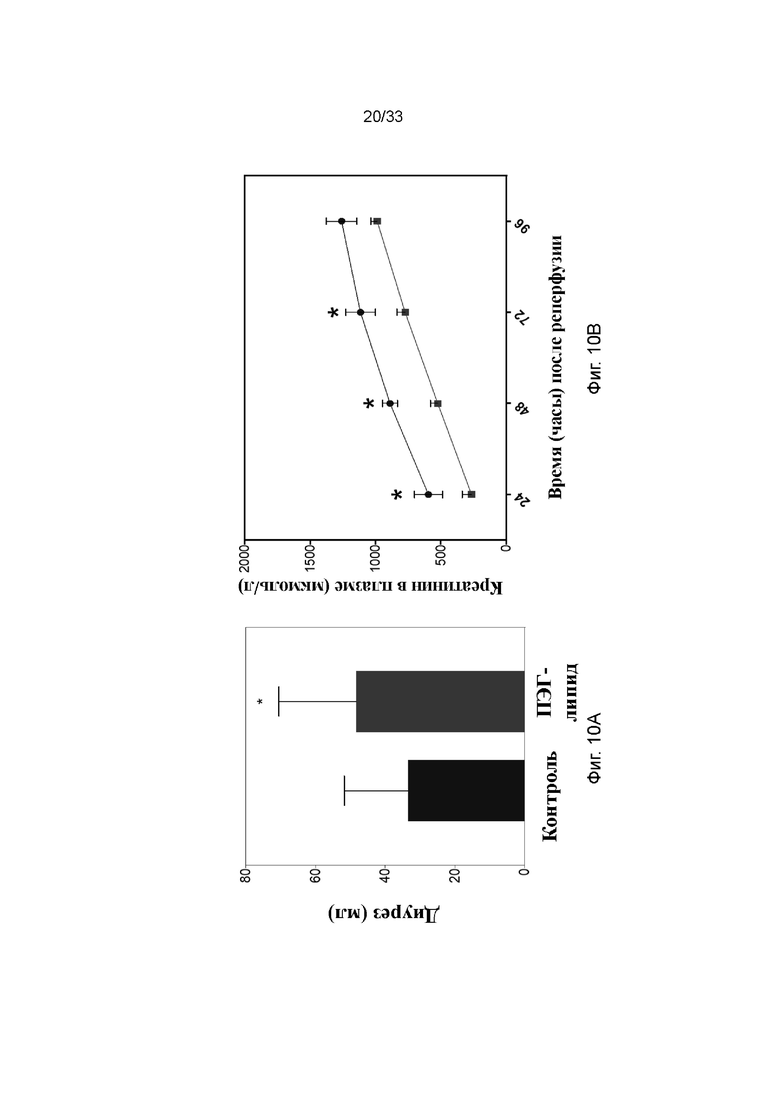
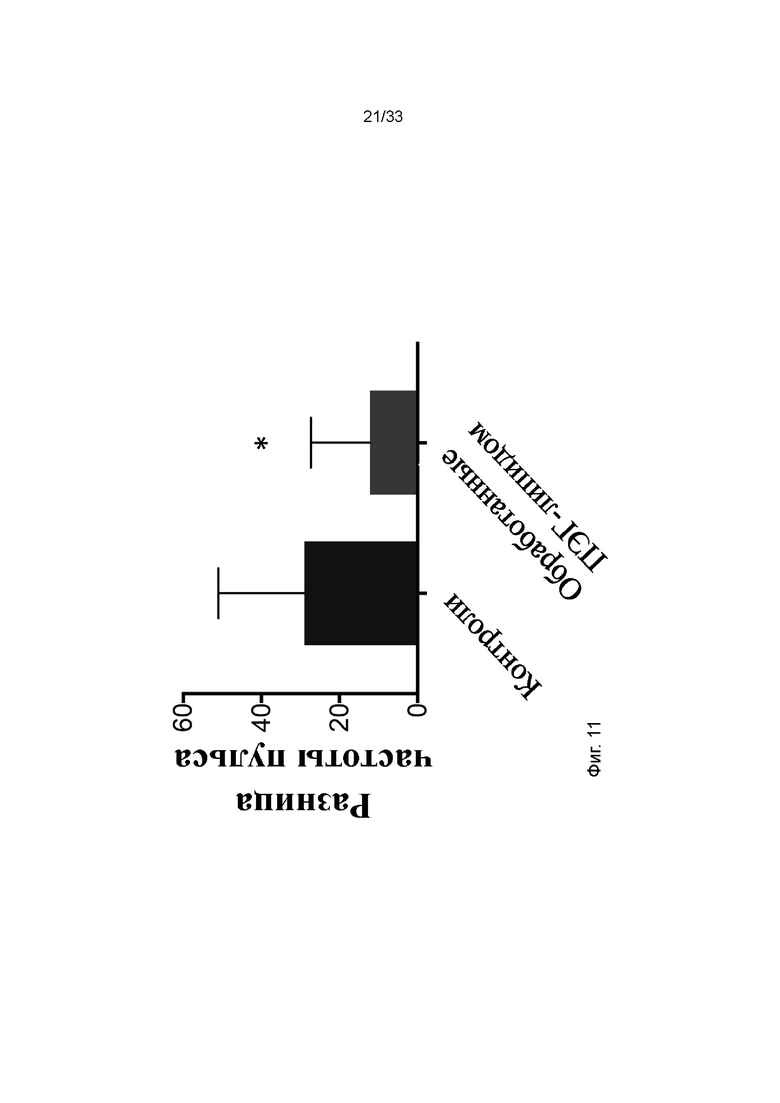
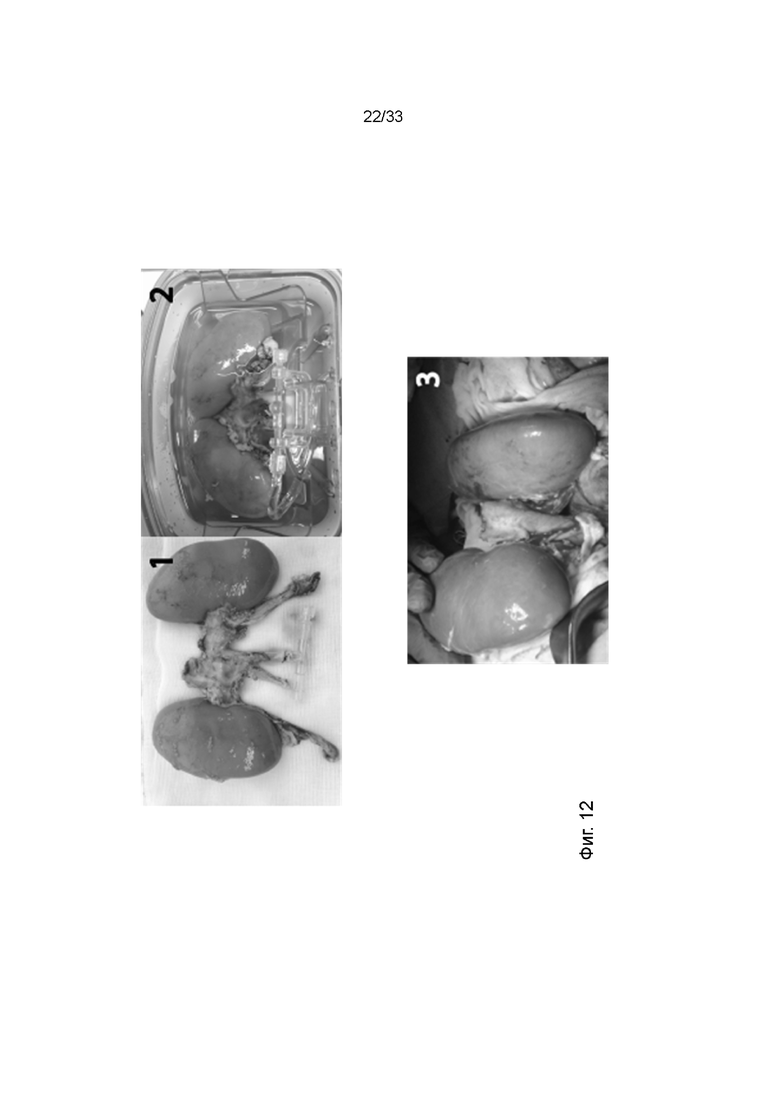
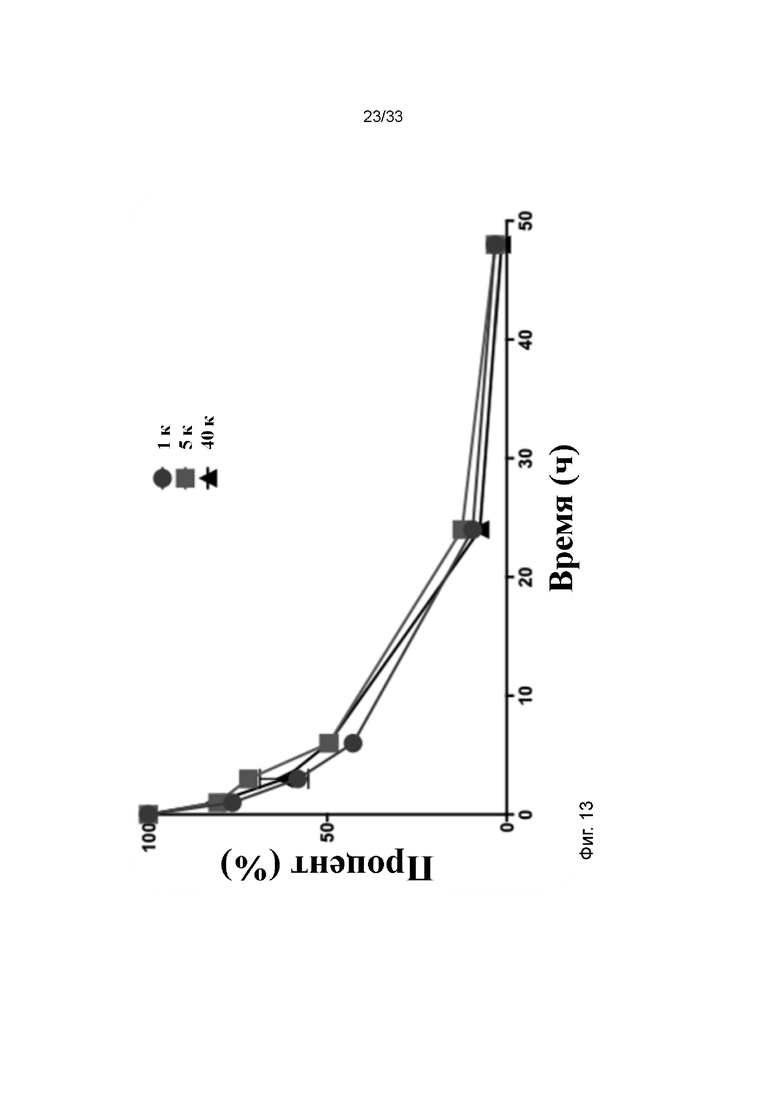
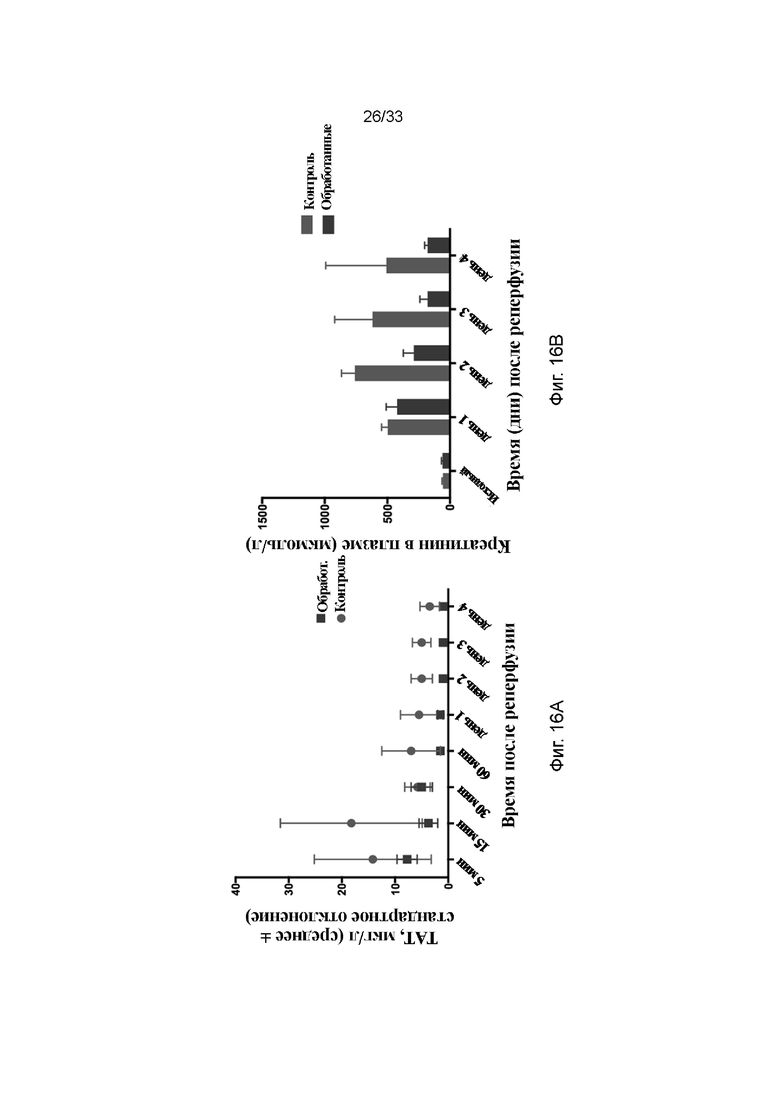
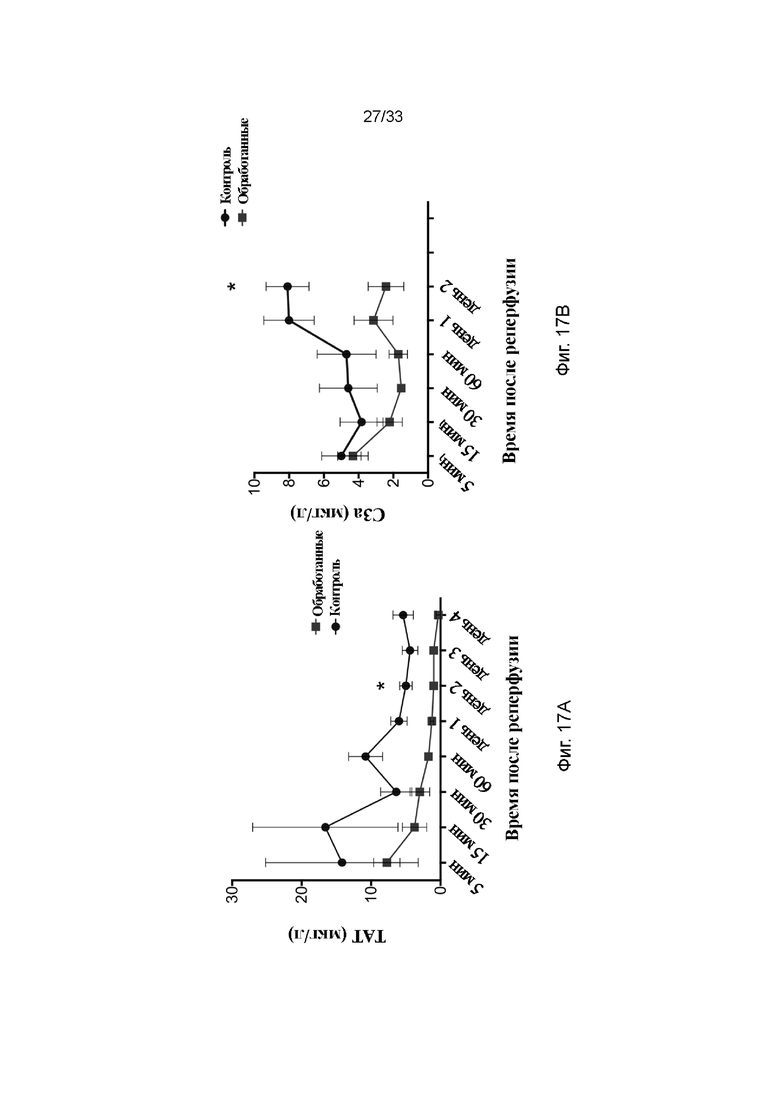
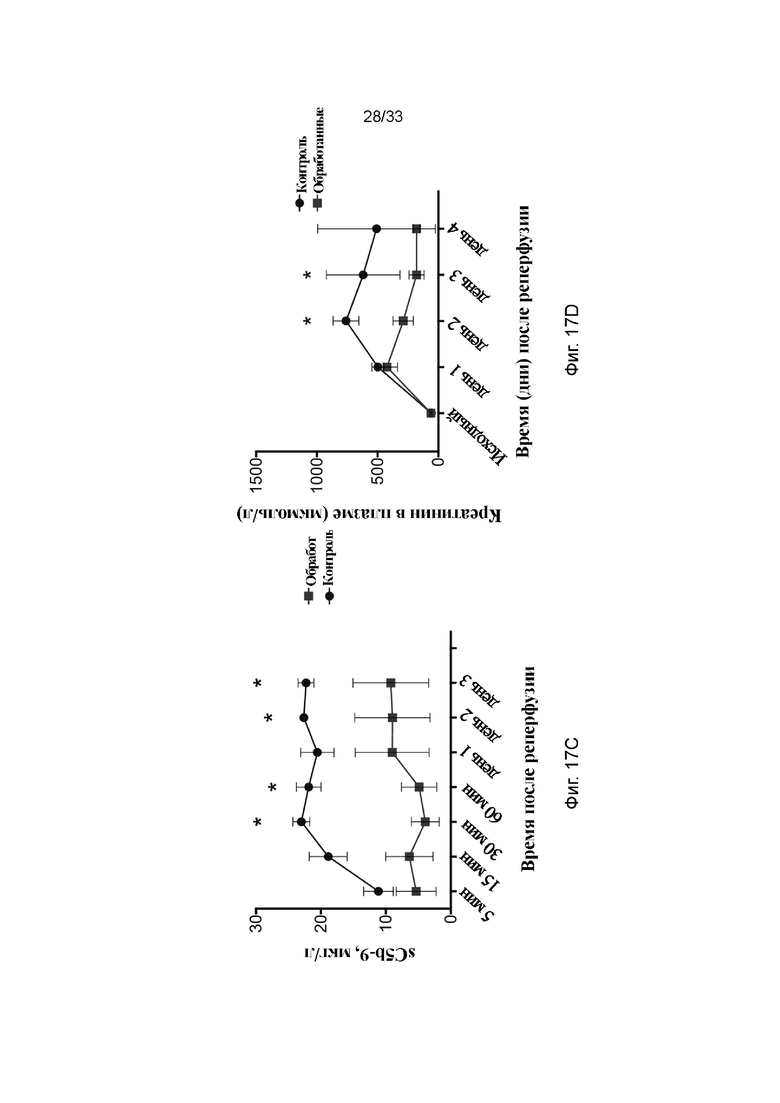
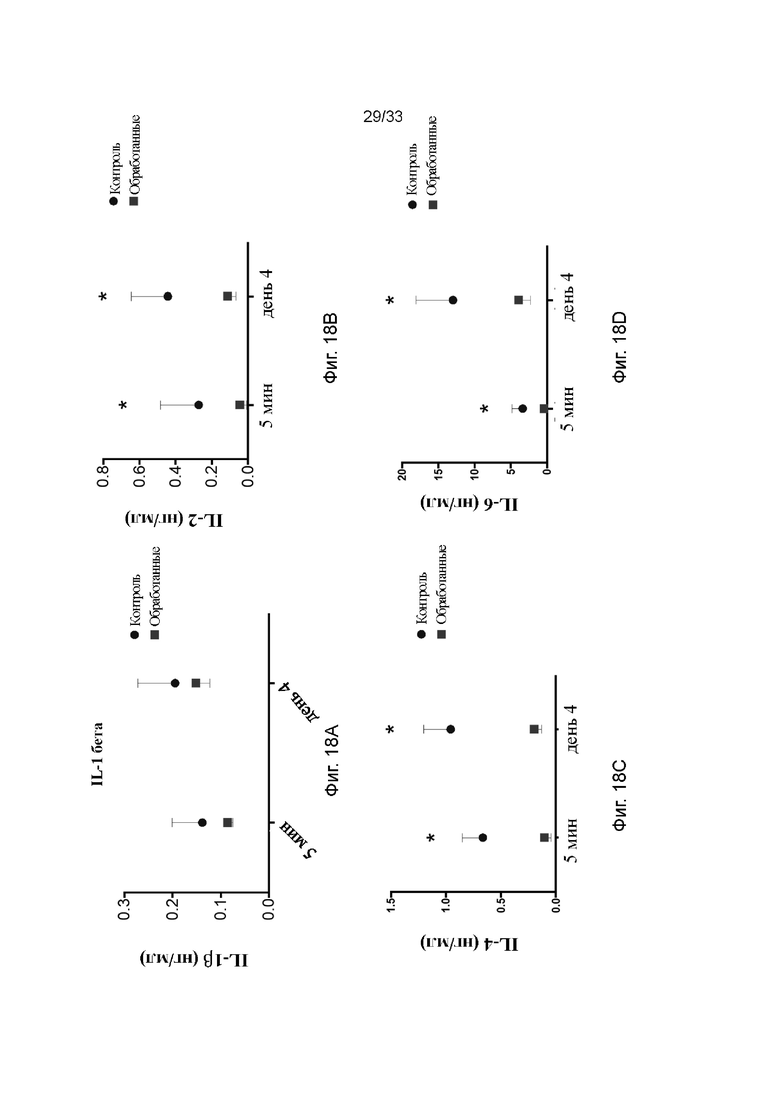
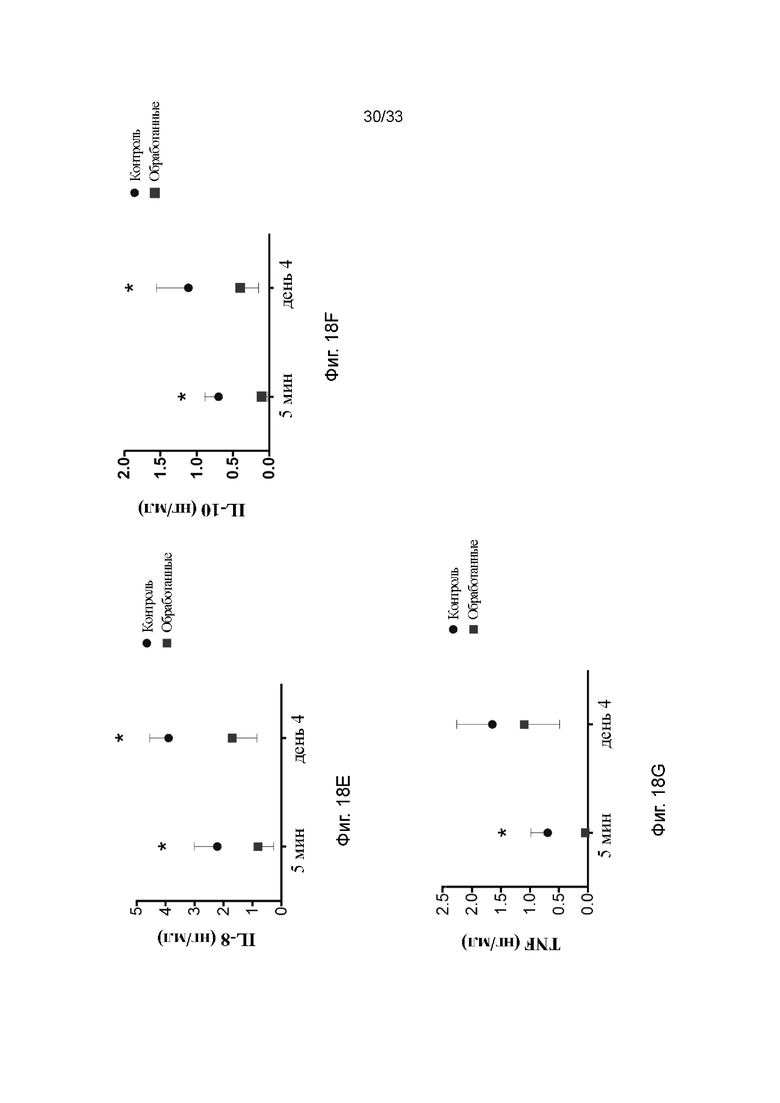
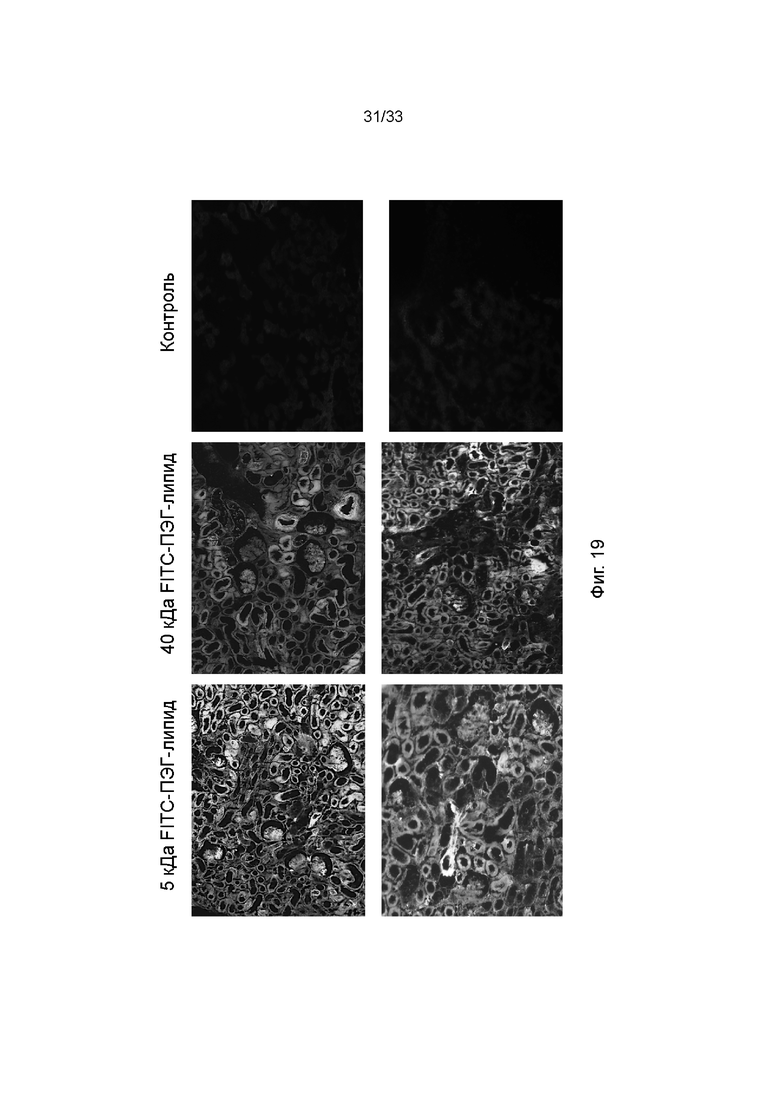
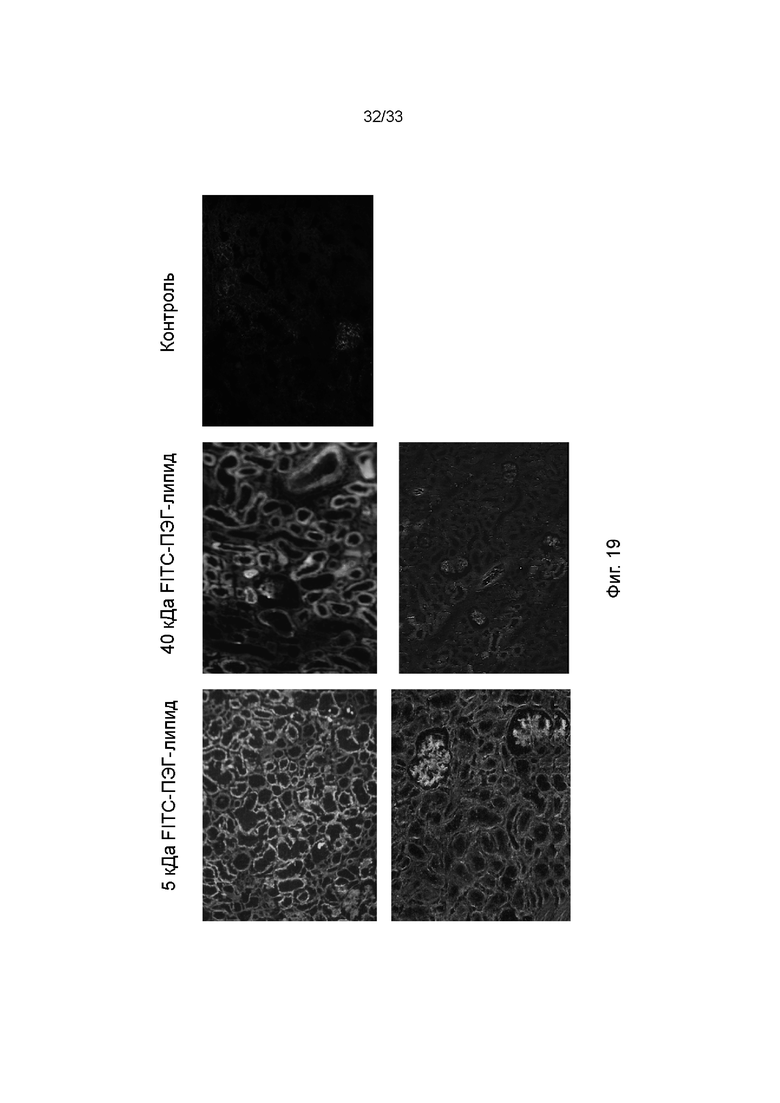

Изобретение относится к области биотехнологии. Описан способ ex vivo обеспечения покрытия по меньшей мере части эндотелиальной выстилки сосудистой системы органа или части органа. Способ включает стадии инфузии ex vivo раствора, содержащего молекулы ПЭГ-фосфолипида, в сосудистую систему органа или части органа; и инкубации ex vivo раствора, содержащего молекулы ПЭГ-фосфолипида, в сосудистой системе. Способ позволяет формировать защиту от тромбовоспаления, вызванного перфузией органа или части органа. 14 з.п. ф-лы, 58 ил., 4 пр.
1. Способ ex vivo обеспечения покрытия по меньшей мере части эндотелиальной выстилки сосудистой системы органа или части органа, причем указанный способ включает:
инфузию ex vivo раствора, содержащего молекулы полиэтиленгликоль-фосфолипида (ПЭГ-фосфолипида), в указанную сосудистую систему органа или части органа; и
инкубацию ex vivo раствора, содержащего молекулы ПЭГ-фосфолипида, в сосудистой системе для обеспечения покрытия по меньшей мере части эндотелиальной выстилки сосудистой системы молекулами ПЭГ-фосфолипида, при этом выдерживая орган или часть органа погруженными в раствор для консервации органов, содержащий молекулы ПЭГ-фосфолипида, причем указанное покрытие формирует защиту от тромбовоспаления, вызванного перфузией указанного органа или части органа.
2. Способ по п. 1, дополнительно включающий:
инфузию ex vivo раствора для консервации органов в сосудистую систему для вымывания несвязавшихся молекул ПЭГ-фосфолипида из сосудистой системы.
3. Способ по п. 1 или 2, дополнительно включающий:
инфузию ex vivo раствора для консервации органов в сосудистую систему перед инфузией ex vivo раствора, содержащего молекулы ПЭГ-фосфолипида, в сосудистую систему.
4. Способ по любому из пп. 1-3, отличающийся тем, что инфузия ex vivo раствора включает:
установку ex vivo зажима на один сосуд, выбранный из артерии и вены сосудистой системы;
инфузию ex vivo раствора, содержащего молекулы ПЭГ-фосфолипида, в другой сосуд, выбранный из артерии и вены; и
установку ex vivo зажима на другой сосуд, выбранный из артерии и вены.
5. Способ по любому из пп. 1-4, отличающийся тем, что инфузия ex vivo раствора включает инфузию ex vivo раствора, содержащего от 0,25 мг/мл до 25 мг/мл, предпочтительно от 0,25 мг/мл до 10 мг/мл и более предпочтительно от 0,25 мг/мл до 5 мг/мл, например 2 мг/мл, молекул ПЭГ-фосфолипида, в сосудистую систему.
6. Способ по любому из пп. 1-5, отличающийся тем, что инфузия ex vivo раствора включает инфузию ex vivo от 5 мл до 250 мл, предпочтительно от 5 мл до 100 мл и более предпочтительно от 5 мл до 50 мл раствора, содержащего молекулы ПЭГ-фосфолипида, в сосудистую систему.
7. Способ по любому из пп. 1-6, отличающийся тем, что инкубация ex vivo включает инкубацию ex vivo раствора, содержащего молекулы ПЭГ-фосфолипида, в сосудистой системе, при выдерживании органа или части органа погруженными в раствор для консервации органов, содержащий молекулы ПЭГ-фосфолипида и при температуре выше 0°C, но ниже 8°C, предпочтительно выше 0°C, но ниже 6°C, и более предпочтительно выше 0°C, но равной или ниже 4°C.
8. Способ по любому из пп. 1-7, отличающийся тем, что раствор для консервации органов выбран из группы, состоящей из раствора гистидин-триптофан-кетоглутарата (HTK), цитратного раствора, раствора университета Висконсина (UW), раствора Коллинза, раствора Цельсиор, раствора университета Киото и раствора института Джордж-Лопез-1 (IGL-1).
9. Способ по любому из пп. 1-8, отличающийся тем, что инкубация ex vivo включает инкубацию ex vivo раствора, содержащего молекулы ПЭГ-фосфолипида, в сосудистой системе в течение периода времени от 10 минут до 48 часов, предпочтительно от 20 минут до 36 часов и более предпочтительно от 30 минут до 24 часов.
10. Способ по любому из пп. 1-9, отличающийся тем, что
молекулы ПЭГ-фосфолипида выбраны из группы, состоящей из нефункционализированных молекул ПЭГ-фосфолипида, состоящих из ПЭГ-фосфолипидов, функционализированных молекул ПЭГ-фосфолипида, содержащих соответствующую функционализированную молекулу, присоединенную к ПЭГ молекул ПЭГ-фосфолипида, и их смеси; и
указанная функционализированная молекула выбрана из группы, состоящей из ингибитора комплемента, ингибитора свертывания крови, ингибитора тромбоцитов, молекулы, способной связывать ингибитор комплемента, молекулы, способной связывать ингибитор свертывания крови, молекулы, способной связывать ингибитор тромбоцитов, и их смеси.
11. Способ по любому из пп. 1-10, отличающийся тем, что молекулы ПЭГ-фосфолипида имеют формулу (I) или формулу (II):
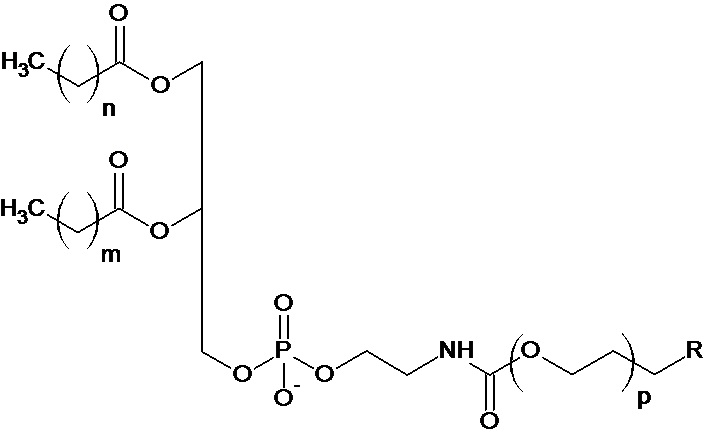 ,
,
(I)
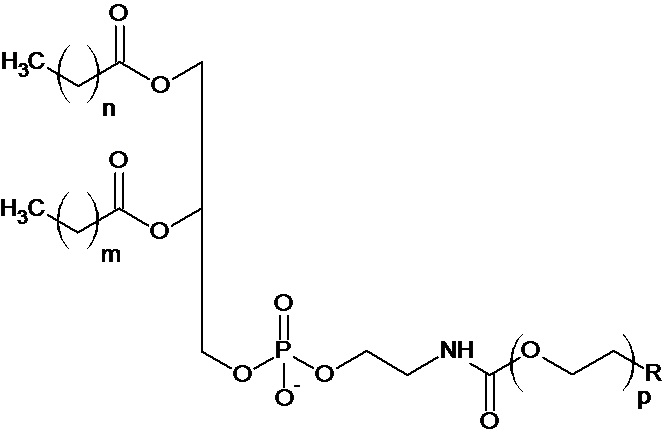 ,
,
(II)
где
n, m представляют собой целые числа, независимо выбранные в диапазоне от 10 до 16, предпочтительно n, m независимо представляют собой 10, 12, 14 или 16 и более предпочтительно n=m=14;
p выбран таким образом, что цепь ПЭГ имеет среднюю молекулярную массу, выбранную в диапазоне от 1000 Да до 40000 Да, предпочтительно от 3000 до 10000 Да и более предпочтительно 5000 Да; и
R представляет собой H, CH3, NH2, малеимидную группу, биотиновую группу, стрептавидиновую группу, авидиновую группу или функционализированную молекулу, выбранную из группы, состоящей из ингибитора комплемента, ингибитора свертывания крови, ингибитора тромбоцитов, молекулы, способной связывать ингибитор комплемента, молекулы, способной связывать ингибитор свертывания крови, молекулы, способной связывать ингибитор тромбоцитов, и их смеси.
12. Способ по п. 10 или 11, отличающийся тем, что функционализированная молекула выбрана из группы, состоящей из связывающего гепарин пептида, от 4 до 6 N-концевых коротких консенсусных повторов (SCR) рецептора комплемента 1 (CR1), регуляторного белка комплемента CD46 (CD46), ускоряющего распад комплемента фактора (DAF), связывающей Фактор H молекулы, разрушающего аденозиндифосфат (АДФ) фермента и их смеси, предпочтительно выбрана из группы, состоящей из пептида 5C6, апиразы, кластера дифференцировки 39 (CD39), C4b-связывающего белка (C4BP) и их смеси.
13. Способ по любому из пп. 1-12, отличающийся тем, что орган выбран из группы, состоящей из почки, печени, поджелудочной железы, сердца, легкого, матки, мочевого пузыря, тимуса и кишечника.
14. Способ по п. 13, отличающийся тем, что
орган представляет собой почку; и
инкубация ex vivo включает инкубацию ex vivo раствора, содержащего молекулы ПЭГ-фосфолипида, в сосудистой системе для обеспечения покрытия эндотелия сосудистой системы почки и покрытия канальцев паренхимы почки молекулами ПЭГ-фосфолипида при выдерживании почки погруженной в раствор для консервации органов, содержащий молекулы ПЭГ-фосфолипида.
15. Способ по п. 1, отличающийся тем, что молекулы ПЭГ-фосфолипида могут быть получены путем объединения α-сукцинимидилоксисукцинил-ω-метоксиполиоксиэтилена, имеющего среднюю молекулярную массу 5000 Да и 1,2-дипальмитоил-sn-глицеро-3-фосфатидилэтаноламина с триэтиламином и дихлорметаном и перемешивания в течение 72 ч при комнатной температуре с поcледующим осаждением диэтиловым эфиром.
| WO 2017019214 A1, 02.02.2017 | |||
| WO 2016159773 A1, 06.10.2016 | |||
| Хугаева О | |||
| В | |||
| и др | |||
| Химико-фармацевтические исследования липосомальной формы митоксантрона //Российский биотерапевтический журнал, 2012, 11(4), с | |||
| Механический грохот | 1922 |
|
SU41A1 |
| Asif S | |||
| et al | |||
| Heparinization of cell surfaces with short peptide-conjugated PEG-lipid regulates thromboinflammation in | |||
Авторы
Даты
2023-11-22—Публикация
2019-11-29—Подача