Лиофилизирование, хранение и транспортирование лиофилизированных продуктов давно используют в пищевой [1] и фармацевтической [2] промышленности.
Однако в медицинской промышленности, в особенности для крови и ее компонентов, преобладает традиционный подход к замораживанию, хранению и транспортированию замороженной крови и гемокомпонентов. Кровь хранят обычно при отрицательной температуре - 20 0С для сохранения белков и лабильных факторов. Это ограничение требует организации и сопровождения холодовой цепи доставки, наличия холодильного и размораживающего оборудования, помещений и больших затрат. Такие требования не всегда выполнимы в отдаленных районах с отсутствующей инфраструктурой, при поступлении большого количества пострадавших с массивной кровопотерей в результате травм и ранений в условиях ЧС, когда необходимо неотложное переливание гемокомпонентов. Пациенты не всегда и вовремя могут получить трансфузиологическую помощь. Лиофилизирование гемокомпонентов, в первую очередь плазмы, могло бы решить значительную часть этой проблемы. Сухая плазма имеет небольшую массу, длительный срок хранения при плюсовой температуре 5 - 25 0/С, не требует замораживания и размораживания. Её можно легко и быстро восстановить в полевых условиях, когда необходимо экстренное реагирование на кровопотерю.
Широкое распространение удобного способа преобразования гемокомпонентов в сухую форму путем лиофилизации сдерживается тем, что имеются технологические и экономические ограничения из-за сложившегося уровня техники.
В большинстве случаев лиофилизацию плазмы проводят в открытом виде в стеклянных флаконах вместимостью 400 - 500 мл, используя стационарные и дорогостоящие лиофилизаторы с асептическими функциями и автоматическими линиями укупорки флаконов после лиофилизации. Стеклянные флаконы [3, 4] являются аналогом заявленного многофункционального контейнера. Не удобны, громоздки, имеют небольшую площадь лиофилизации, сложны в логистике и могут разбиться.
Аналогами заявленного устройства также являются полимерные контейнеры, широко используемые для гемокомпонентов, выполненные из ПВХ материалов [5, 6]. Этот материал допускает замораживание, но не обладает высокой воздухопроницаемостью. Лиофилизация гемокомпонентов в таких контейнерах продолжается несколько недель и экономически не оправдана.
Аналогом также является одноразовый полимерный контейнер для лиофилизации GORE LYOGUARD [7] производства фирмы GORE (Германия). Контейнер выполнен в виде закрытого жесткого лотка для гемокомпонента, имеющего воздухопроницаемую мембрану, через которую удаляются водяные пары при лиофилизации замороженного гемокомпонента. Контейнер позволяет проводить лиофилизацию в простых лиофилизаторах, не имеющих асептических функций. Но заполнять контейнер гемокомпонентом и регидратировать лиофилизат в нем с сохранением стерильности возможно только в чистых помещениях и ламинарных шкафах с асептическими функциями. Кроме того, такой контейнер из-за жесткой и громоздкой конструкции неудобно транспортировать и компактно хранить.
Наиболее близким аналогом является «Система для лиофилизации, хранения и использования биоматериала» [8]. Устройство представляет собой бинарную закрытую систему, состоящую из двух сопряженных контейнеров, один из которых - традиционный контейнер из ПВХ для гемокомпонентов, другой - имеет воздухопроницаемую мембрану. Контейнеры изолированы друг от друга швом. Гемокомпонент вводят в контейнер с мембраной, проводят лиофилизацию, раскрывают шов, пересыпают лиофилизат в ПВХ контейнер, который запаивают. Контейнер с мембраной отделяют и утилизируют. Такое устройство неудобно в использовании: занимает удвоенную площадь в лиофилизаторе, требует проведения множества ручных манипуляций, запаивающего термооборудования, утилизации отходов. Обезвоженный гемокомпонент во время продолжительных ручных манипуляций с системой вновь увлажняется воздухом из окружающей среды, проникающим через мембрану. Ухудшается качество лиофилизата, который становится непригодным к длительному хранению.
Преимуществом лиофилизации, хранения и транспортировки лиофилизированных гемокомпонентов для медицинского применения можно воспользоваться, преодолев недостатки аналогов, если решить поставленную ниже задачу.
Задачей изобретения является создание закрытого контейнера и способа обезвоживания, содержащегося в нем гемокомпонента, которые без использования «чистых помещений» и асептических условий позволяют в одном закрытом контейнере стерильно лиофилизировать и длительно хранить лиофилизат гемокомпонента.
Технический результат состоит в снижении риска микробной контаминации лиофилизата гемокомпонента и сохранении качества, восстановленного гемокомпонента.
Дополнительный технический результат обусловлен компактностью и малым весом лиофилизированного в контейнере гемокомпонента, хранением и простой логистикой без необходимости замораживания гемокомпонента.
Поставленная задача решена, и технический результат согласно изобретению, достигнут благодаря тому, что предложен гибкий контейнер для лиофилизации. Контейнер содержит газопроницаемую и непроницаемую для микробных контаминантов плоскую переднюю мембранную поверхность; газо-, водонепроницаемую плоскую заднюю мембранную поверхность; по меньшей мере одну трубку, сообщающуюся с внутренней полостью контейнера, и присоединительные элементы.
Технический результат достигается также благодаря тому, что предложен способ использования гибкого контейнера. Способ включает: соединение контейнера с гемокомпонентом с гибким контейнером; перевод в него гемокомпонента, размещение и замораживание гибкого контейнера на лотке; сублимацию свободной воды из замороженного гемокомпонента в вакууме, десорбцию связанной воды путем нагревания; извлечение контейнера из лиофилизатора и герметизацию его воздухопроницаемой мембраны; отбор порции лиофилизата для анализа; складывание контейнера, помещение его в непроницаемый для воздуха и влаги полимерный пакет, вакуумирование и запаивание пакета.
Предпочтительные и конкретизирующие признаки изобретения указаны в зависимых пунктах формулы изобретения. В частности, дополнительно технический результат достигнут за счет того, что передняя поверхность контейнера выполнена из пористой гидрофобной одно- или двухслойной гибкой мембраны, имеющей поверхностную пористость в диапазоне 20-80%, водоупорность не менее 150 см, средний размер пор в диапазоне 0,1-0,45 мкм, преимущественно 0,2 мкм и толщину от 100 до 300 мкм, преимущественно 150 ± 50 мкм.
Кроме того, материал мембраны выбран из группы пористых полимеров: политетрафторэтилен, полиэтилентерефталат, линейный полиэтилен низкой плотности, дополнительно нанесен на упрочняющую его подложку из нетканного пористого полиамида или полипропилена и обеспечивает герметичность контейнера в диапазоне температур от -196 до +100 0С, преимущественно от -85 до +70 0С.
Целесообразно заднюю поверхность контейнера выполнить из газо-, водонепроницаемой прозрачной мембраны, толщиной от 100 до 300 мкм, преимущественно 150 ± 50 мкм, причем материал мембраны выбрать из группы композитных полимеров: полиамид/полиэтилен, полипропилен/полиэтилен, этиленвинилацетат/полиэтилен, а сторону мембраны из полиэтилена обратить внутрь контейнера. Мембраны должны быть гемосовместимыми, гибкими, допускать складывание контейнера в два и более раз с сохранением герметичности при складывании и распрямлении контейнера.
Полезно, чтобы контейнер имел форму прямоугольника, длина которого находится в пределах от 20 до 50 см, преимущественно 30 см ± 10%; ширина - в пределах от 14 до 25 см, преимущественно 20 см ± 10%, передняя и задняя поверхности контейнера герметично соединены по периметру прямоугольника от двух до пяти термосформированными швами, отстоящими друг от друга на расстоянии 1-2 мм, при общей ширине шва от 4 до 12 мм. Причем вместимость контейнера должна находиться в диапазоне от 50 до 1000 мл, преимущественно от 300 до 600 мл, при этом толщина заполненного жидкостью контейнера находится в пределах от 3 до 20 мм, преимущественно от 5 до 8 мм.
Удобно, чтобы в шве или вне шва была выполнена прорезь для подвески контейнера. В шов герметично встроена закрытая с одного конца технологическая трубка с внутренним/внешним диаметром 3,0/4,1 мм ± 10 %. Причем длина отрезка технологической трубки от разветвителя до полимерной иглы - не менее 30 см. Технологическая трубка снабжена зажимом-защелкой и соединена с разветвителем, с которым соединены два штуцера с внутренней перфорируемой мембраной, закрытых отделяемым защитным элементом, и технологическая трубка, оканчивающаяся полимерной иглой с колпачком.
Возможен вариант исполнения, когда указанные два или более штуцеров непосредственно встроены в шов контейнера.
С целью предотвращения снижения качества лиофилизируемого гемокомпонента, предложено ввести в контейнер лиопротектор, выбираемый из группы: глутамин, глицин, сахароза, хепес и дополнительно - криопротектор в случае лиофилизации клеточного гемокомпонента, выбираемый из группы: глицерол, диметилсульфоксид, декстран, полиэтиленгликоль в концентрациях, сохраняющих биологические свойства восстановленного после лиофилизации гемокомпонента.
Кроме того, дополнительно технический результат достигнут за счет того, что сублимацию проводят при отрицательной температуре ниже точки эвтектики гемокомпонента, который замораживают в морозильной камере со скоростью 1-3 0/мин до температуры не менее -40 0С, выдерживают в течении 4 - 24 часов, преимущественно 12 часов, перемещают в лиофилизатор, сублимацию ведут при температуре от -20 до -40 0С и вакуумметрическом давлении в диапазоне 40 - 100 мТорр в течение 24 - 48 часов, после чего проводят десорбцию не менее 72 часов, постепенно повышая температуру до 37 0С.
С целью предотвращения увлажнения лиофилизата герметизируют воздухопроницаемую мембрану контейнера за время не более 30 сек после его извлечения из лиофилизатора, герметизируя всю поверхность мембраны предварительно подготовленным воздухо-, влагонепроницаемым пленочным материалом с клеящейся поверхностью.
Для придания конечному продукту компактности контейнер с загерметизированной мембраной перед помещением в вакуумируемый полимерный пакет предварительно складывают пополам. Этот пакет для надежности транспортирования может быть помещен во второй пакет. Пакет вакуумируют и запаивают.
Стерильность при соединении контейнеров обеспечивают путем термосваривания технологических трубок или в отсутствии термосваривающего оборудования перфорируют полимерной иглой мембрану штуцера контейнера с гемокомпонентом, обеспечивая тем самым стерильное соединение.
Для проведения анализа качества лиофилизата порцию его порошка отсыпают в технологическую трубку путем встряхивания перевернутого контейнера; стерильно запаивают с двух сторон отрезок трубки длиной не менее 20 см, отсоединяют трубку, высыпают, регидратируют лиофилизат и определяют параметры его качества. В 20 см трубки содержится примерно 0,5 г порошка лиофилизата, количество которого достаточно для проведения анализов.
С целью равномерной теплопередачи, предложено разместить на лотках лиофилизатора контейнеры с лиофилизируемым гемокомпонентом вплотную друг к другу, без промежутков, полностью покрыть ими всю поверхность лотков. Лотки необходимо расположить строго горизонтально и использовать лотки с шероховатостью поверхности не более 0,1 мм и неплоскостностью не более 0,5 мм/м. Лотки помещают на полках лиофилизатора, которые установлены на расстоянии не менее 40 мм друг от друга по высоте.
Для формирования передней поверхности контейнера выбрана пористая, гидрофобная мембрана, т.к. такая мембрана пропускает воздух и не смачивается жидкостью, блокирующей поры. Двухслойная мембрана повышает прочность контейнера. Толщина мембраны в пределах 100 - 300 мкм, поверхностная пористость 20 - 80% и средний размер пор, находящийся в диапазоне 0,1 - 0,45 мкм, создают незначительное препятствие оттоку паров воды при сублимации и практически не удлиняют время сублимации. Рекомендованный для мембраны средний размер пор 0,2 мкм также используют в биотехнологии для холодной стерилизации жидкостей. Доказано, что бактериальные контаминанты не могут проникнуть через поры такого размера. Выбор водоупорности не менее 150 см водяного столба обусловлен тем, что контейнер подвешивают на штативе для трансфузии. Капли жидкости не должны просачиваться через мембрану контейнера, подвешенного на штативе, под воздействием давления гидростатического столба высотой 150 см.
Выбор материала мембраны из группы пористых полимеров: политетрафторэтилен, полиэтилентерафталат, линейный полиэтилен низкой плотности, и дополнительное армирование их подложкой из нетканного пористого полиамида или полипропилена обусловлен тем, что эти материалы обладают высокой гидрофобностью и прочностью, сохраняющейся в диапазоне температур -100/+100 0С. Материал композитных мембран, выбранный из группы: полиамид/полиэтилен, полипропилен/полиэтилен, этиленвинилацетат/полиэтилен, имеет небольшую толщину 100 - 300 мкм, не пропускает воздух и жидкость, обладает гибкостью и прозрачностью. Эти свойства позволяют визуально и тактильно приближенно определять качество лиофилизата до завершения процесса лиофилизации. Складывать контейнер в несколько раз для уменьшения его габаритов при хранении и транспортировании. Сторона композитной мембраны, выполненная из полиэтилена, обращена внутрь контейнера в силу того, что этот материал обладает высокой гемосовместимостью и инертностью.
Вместимость контейнера от 50 до 1000 мл выбрана для возможности размещения в контейнере вместимостью 1000 мл максимальной разрешенной дозы однократной донации, например, аферезной плазмы: 900 мл ± 10%, Контейнер вместимостью 50 мл удобен для лиофилизирования плазмы новорожденных или малолетних детей. В случае необходимости лиофилизирования одной, кратной 300 мл, или двух стандартных донорских доз плазмы, предпочтительно использовать контейнер вместимостью от 300 до 600 мл.
Прямоугольная форма контейнеров позволяет максимально плотно укладывать их на лотки лиофилизатора без промежутков и потери площади лотков, что обеспечивает равномерное нагревание контейнеров при сублимации и десорбции. Длина 20 - 50 см и ширина 14 - 25 см при вместимости контейнера 50 - 1000 мл задают оптимальную толщину замороженного в контейнере гемокомпонента 5 - 8 мм для быстрой и качественной лиофилизации без карамелизации и ухудшения структуры лиофилизата гемокомпонента.
Необходимое количество термошвов, герметизирующих контейнер по периметру его прямоугольной формы, их размеры и структура определены из прочностных экспериментов при приложении усилия 20 Н и внутреннего давления 40 кПа. Прорезь в шве или в уширении контейнера необходима для подвески контейнера на штативе.
Наличие у контейнера присоединительных элементов, выполненных в виде штуцеров с перфорируемой мембраной, зажима-защелки, полимерной иглы и технологической трубки позволяет стерильно вводить в контейнер гемокомпонент для лиофилизации. Присоединять контейнеры с регидратирующим лиофилизат раствором и трансфузионную систему, предназначенную для вливания восстановленного гемокомпонента.
Для быстрого и равномерного отвода тепла при замораживании и подвода тепла при сублимации гемокомпонента, находящегося в контейнерах, расположенных на лотках, необходимо, чтобы контейнеры максимально плотно прилегали к лоткам, а лотки - к полкам лиофилизатора. В связи с этим установлены экспериментально проверенные требования к качеству лотков: шероховатость поверхности - не более 0,1 мм, неплоскостность - не более 0,5 мм/м. Расстояние между лотками по высоте не менее 40 мм задано тем, что во время сублимации образуются пары воды, которые куполообразно приподнимают мембрану контейнера, и для беспрепятственного отвода паров она не должна соприкасаться с расположенной над ней полкой.
Множество биопродуктов, включая гемокомпоненты, может быть лиофилизировано, сохранено и транспортировано с применением предложенного гибкого контейнера и способа его использования, раскрытых в настоящей заявке. Наибольший интерес представляют такие биопродукты, как кровь и компоненты крови человека и животных, прежде всего плазма крови - часто применяемый в клинической практике гемокомпонент. Предпочтительные признаки изобретения описаны в зависимых пунктах формулы изобретения. Они также раскрыты в приведенном ниже конкретном, но не ограничивающим объем формулы изобретения примере выполнения контейнера для лиофилизации плазмы крови и способа его использования со ссылками на прилагаемые рисунки.
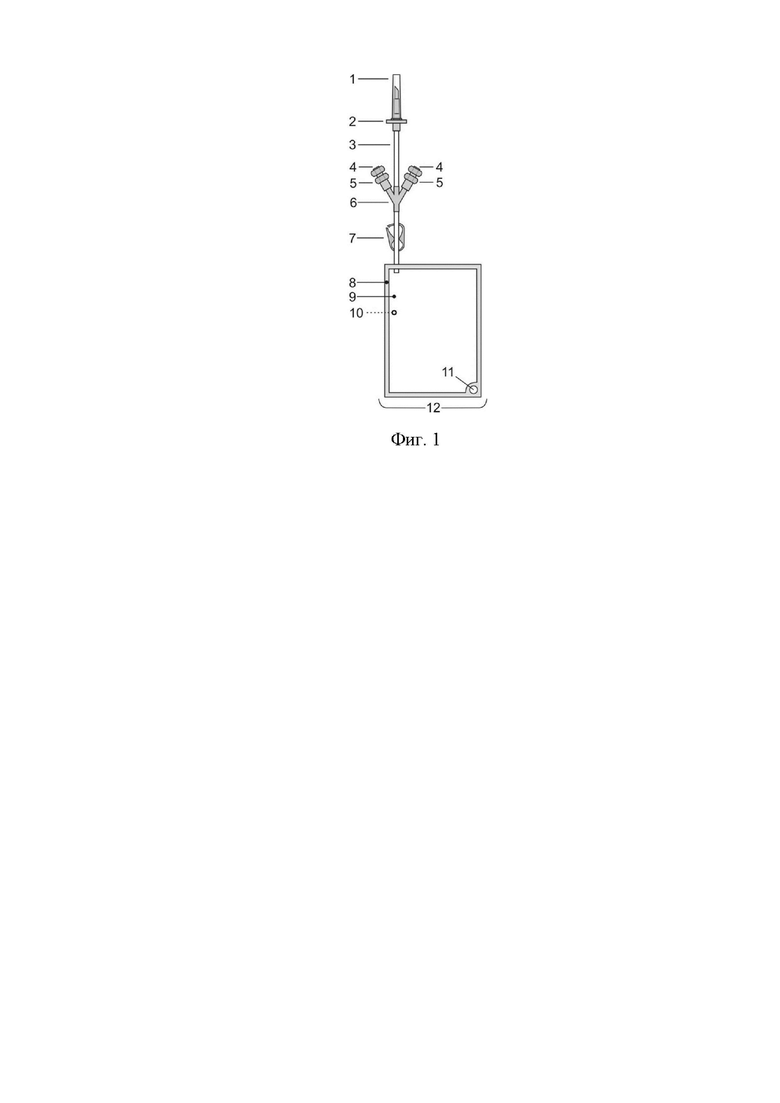
Фиг. 1. Контейнер для лиофилизации.
1. Съемный защитный колпачок полимерной иглы, 2. Полимерная игла, 3. Технологическая трубка с внутренним/внешним диаметром 3,0/4,1 мм ± 10%, длиной 30 см. 4. Защитный отделяемый элемент штуцера (2 шт.). 5. Штуцер с перфорируемой мембраной (2 шт.). 6. Разветвитель (четверник). 7. Зажим-защелка, 8. Термошов контейнера, 9. Передняя поверхность контейнера, выполненная из гидрофобной воздухопроницаемой и непроницаемой для бактериальных контаминантов гибкой мембраны, 10. Задняя поверхность контейнера, выполненная из прозрачной воздухо- и влагонепроницаемой гибкой мембраны (показано пунктирной линией). 11. Прорезь в шве в виде ушка для подвески контейнера.12. Контейнер.
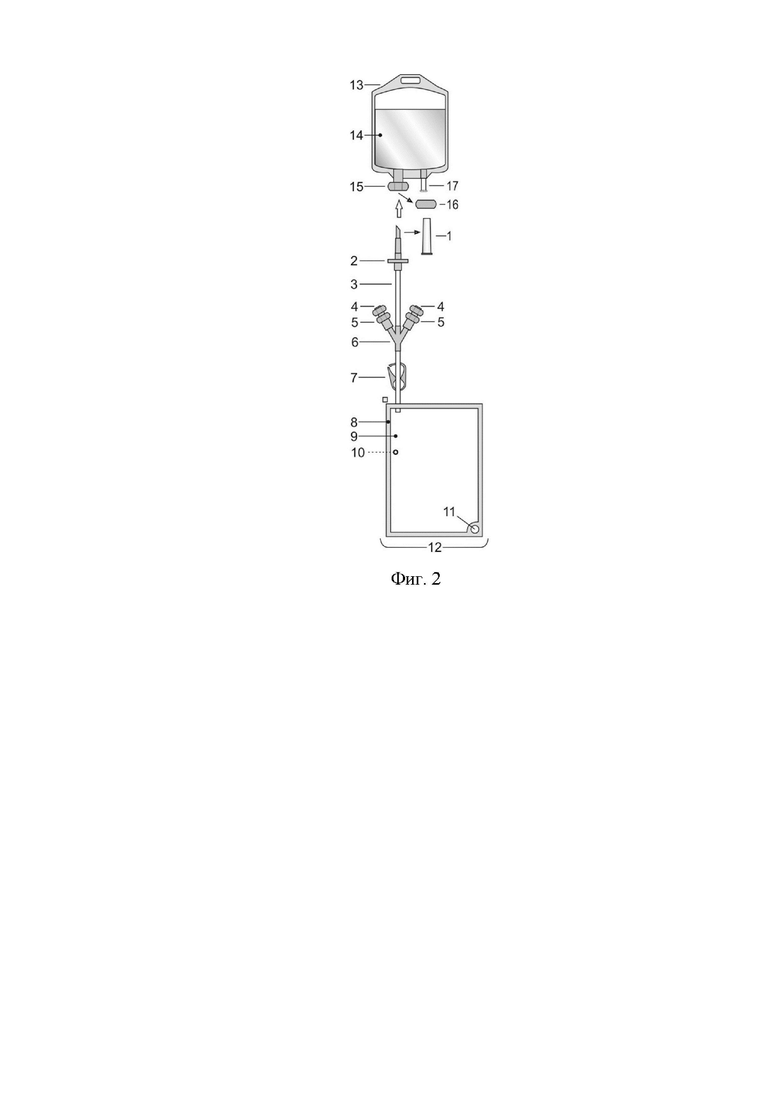
Фиг. 2. Присоединение контейнера с гемокомпонентом к контейнеру для лиофилизации.
Наименования элементов 1 - 12 приведены в описании фиг. 1; 13. Контейнер для гемокомпонента. 14. Гемокомпонент. 15. Штуцер контейнера для гемокомпонента. 16. Защитный элемент штуцера контейнера для гемокомпонента. 17. Технологическая трубка контейнера для гемокомпонента. Колпачок 1 снят, защитный элемент 16 отделен. Полимерная игла 2 введена в штуцер 15 контейнера для гемокомпонента 13
Фиг. 3. Переливание гемокомпонента в контейнер для лиофилизации.
18. Место запаивания (пунктирная линия) трубки и отсоединения контейнеров по завершении переливания гемокомпонента. 19. Гемокомпонент, перелитый в контейнер 12. Пустой контейнер 13 с введенной полимерной иглой 2, отделенный для утилизации.
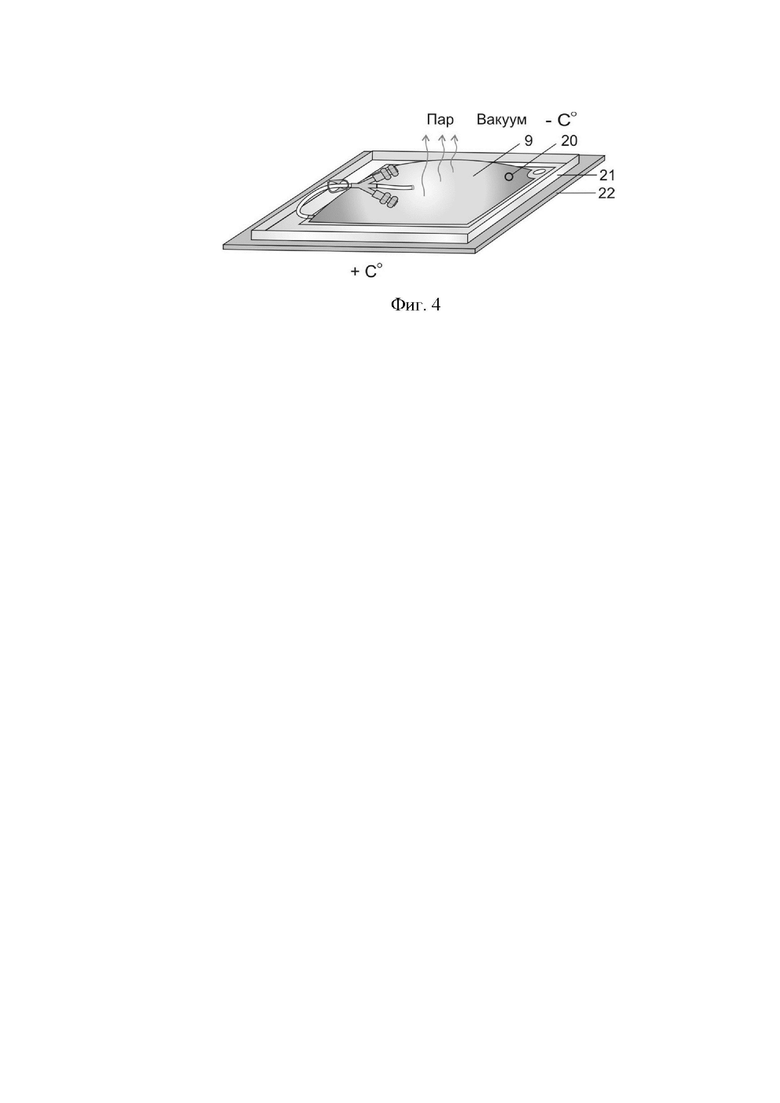
Фиг. 4. Лиофилизация гемокомпонента в контейнере. Контейнер расположен на лотке, воздухопроницаемой мембранной вверх. Лоток помещен на полку лиофилизатора.
9. Передняя воздухопроницаемая мембранная поверхность контейнера. 20. Замороженный гемокомпонент. 21. Лоток для размещения контейнеров. 22. Полка лиофилизатора.
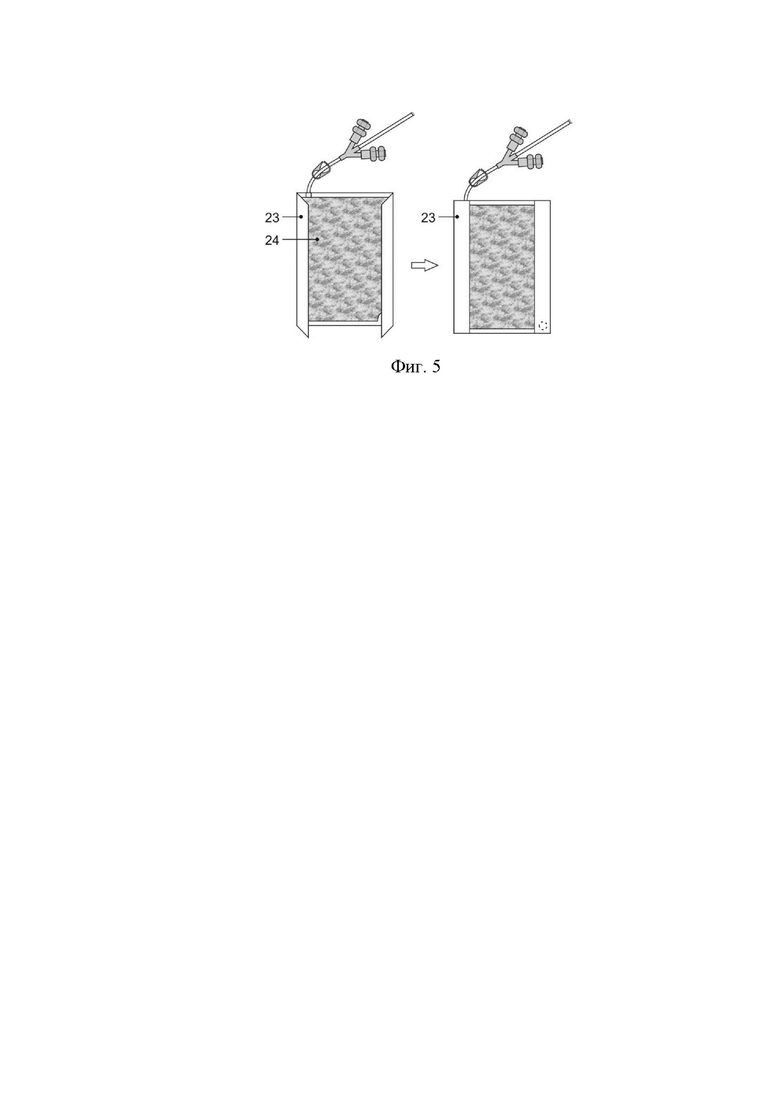
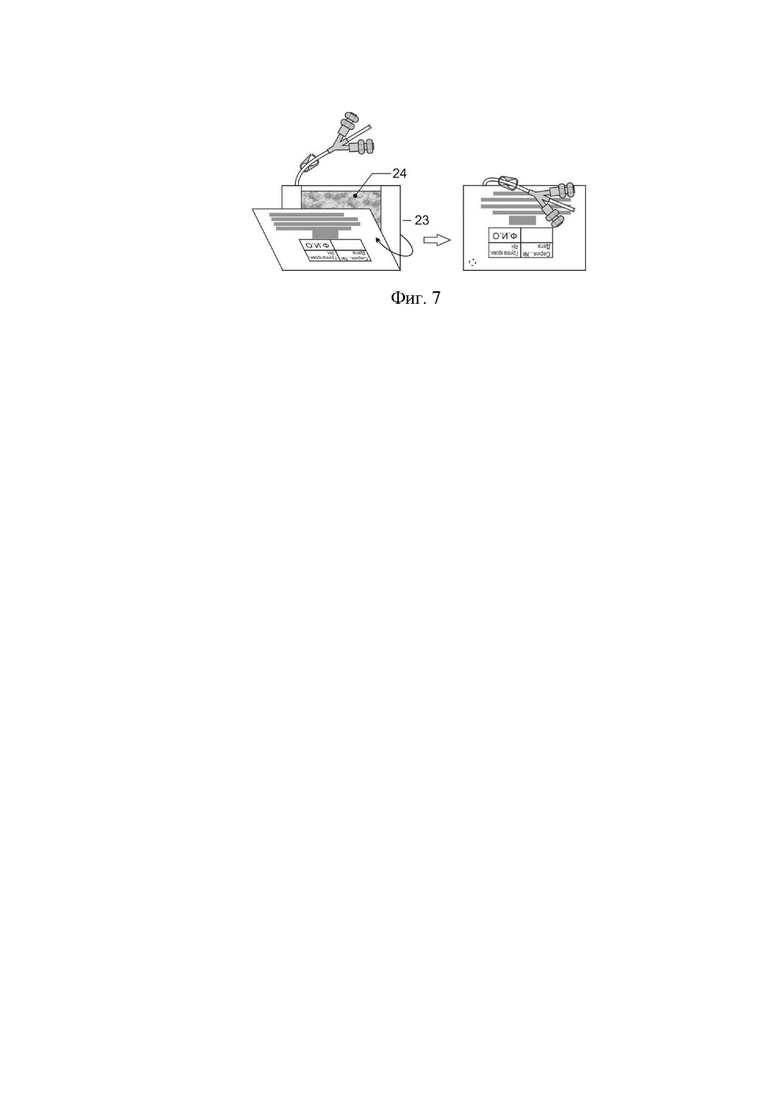
Фиг. 5. Герметизация воздухопроницаемой мембраны контейнера. Полимерная пленка с этикеткой и штрих - кодом наклеивается на мембрану и подворачивается с двух сторон. Пленка предотвращает проникновение воздуха и влаги в контейнер.
23. Полимерная воздухо-, влагонепроницаемая пленка с клеящейся поверхностью. 24. Лиофилизат гемокомпонента.
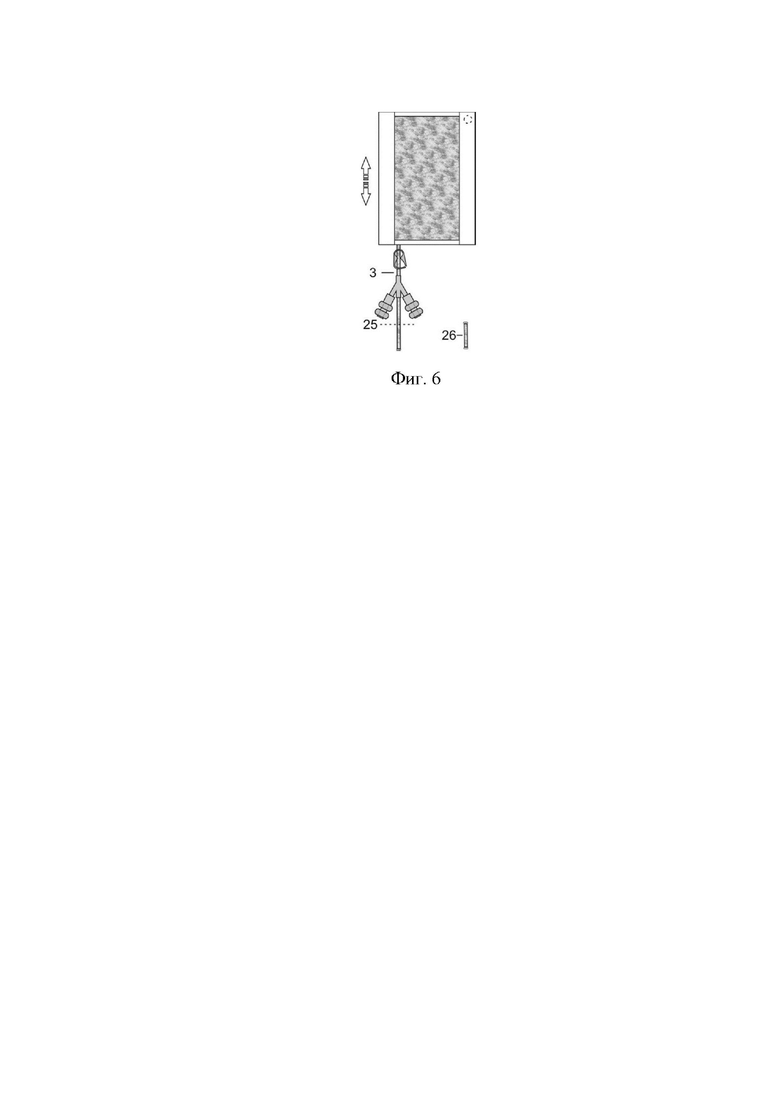
Фиг. 6. Отбор пробы лиофилизата гемокомпонента. Контейнер 12 переворачивают и периодически встряхивают, порошок лиофилизата засыпается в трубку.
3. Трубка; 25. Место запаивания (пунктирная линия) и отделения трубки; 26. Отрезок трубки с порошком лиофилизата для анализа, запаянный с двух сторон.
Фиг. 7. Складывание пополам контейнера с лиофилизатом прозрачной стороной внутрь.
23. Полимерная пленка; 24. Лиофилизат гемокомпонента;
Фиг. 8. Упаковывание сложенного контейнера с лиофилизатом в полимерный пакет.
27. Полимерный пакет для хранения и транспортировки контейнера с лиофилизатом; 28. Термоиндикатор, наклеенный на пакет 27; 29. Транспортный пакет 27 с вложенным контейнером с лиофилизатом.
Фиг.9. Вакуумирование и герметизация воздухо-, влагонепроницаемого пакета для хранения и транспортирования.
29. Вставка в вакууматор, вакуумирование, заваривание полимерного пакета; 30. Извлечение вакуумированного и заваренного пакета; 31. Вакууматор с функцией заваривания полимерных пакетов.
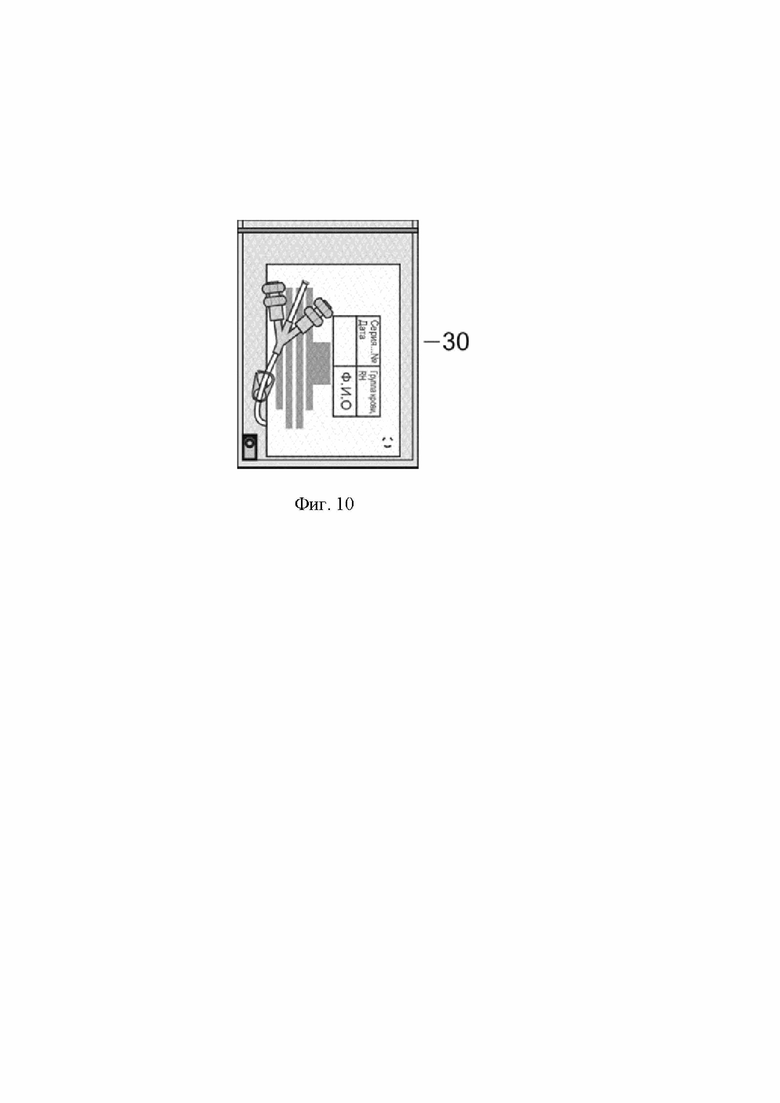
Фиг. 10. Контейнер 30 с лиофилизатом гемокомпонента, этикеткой, маркировкой, штрих - кодом и термоиндикатором в вакуумированном и герметизированном воздухо-, влагонепроницаемом полимерном пакете для хранения и транспортирования.
Фиг. 11. Последовательность этапов способа использования контейнера для лиофилизации.
В настоящем описании и формуле изобретения термины «контейнер» и «контейнер для лиофилизации» взаимозаменяемые. Также взаимозаменяемы термины «лиофилизация», «сублимация», «возгонка».
Параметры изготовленных в соответствии с предложенным техническим решением контейнеров для лиофилизации и способа их использования, а также показатели качества лиофилизатов гемокомпонента приведены ниже на примере лиофилизации плазмы доноров в лиофилизаторе «Лиомед» с использованием предложенного способа.
Изготовили 15 прямоугольных контейнеров для лиофилизации плазмы вместимостью 400 мл, размером 25 × 30 см, площадью поверхности 600 см2 и общей шириной герметизирующего шва 10 мм. Шов выполнили из 3-х одинаковых параллельных швов и расстояний между ними - 2 мм. В 7 контейнеров поместили навеску лиопротектора хепес. Для изготовления верхней поверхности контейнеров использовали воздухопроницаемую и непроницаемую для бактериальных контаминантов мембрану. Материал мембраны - пористый линейный полиэтилен низкой плотности толщиной 150 мкм с поверхностной пористостью 40%, средним размером пор 0,2 мкм. Водоупорность мембраны - 150 см. Водонепроницаемую нижнюю поверхность контейнера выполнили из композитного пленочного непористого прозрачного полимерного материала той же толщины. Контейнеры проверили на герметичность с приложением внутреннего давления 40 кПа и на водоупорность под воздействием гидростатического столба высотой 150 см.
В каждый контейнер стерильно перевели стандартную дозу аферезной плазмы доноров 300 мл ± 10% из контейнера для сбора плазмы аппарата для плазмафереза «Haemonetics PCS-2». Трубки контейнеров соединили с использованием аппарата для стерильного спаивания трубок TSCD, после перевода плазмы в контейнер трубку запаяли ТВЧ-устройством «Гекон-С» и удалили пустой контейнер. Высота заполненного контейнера не превысила 7 мм. По 3-и контейнера с плазмой разместили на каждом из 5-и лотков площадью 0,19 м2, установленных в лиофилизатор «Лиомед».
Лотки с плазмой со скоростью замораживания 1 - 3 0/мин заморозили в низкотемпературном холодильнике «Haier» до температуры -40 0/С, выдержали 12 часов и переместили на полки лиофилизатора «Лиомед». Лиофилизацию свободной воды плазмы вели при температуре от -20 до -40 0С и вакуумметрическом давлении в диапазоне 40 - 100 мТорр в течение 24 - 48 часов, после чего проводили десорбцию связанной воды не менее 72 часов, постепенно повышая температуру до 37 0С. По завершении лиофилизации извлекли лотки, загерметизировали клеящейся полимерной пленкой воздухопроницаемые мембраны контейнеров и отобрали пробы лиофилизата плазмы, как показано на фиг. 5 и 6. В отрезке запаянной трубки 20 см содержалось 0,5 г лиофилизата, который регидратировали 3 мл стерильной инъекционной воды.
Провели оценку качества и стерильности полученного продукта на соответствие требованиям ПП РФ от 22.06.2019 г. № 797, п. 27 «Лиофилизированная плазма» (качество продукта), и соответствие ГОСТу Р ИСО 11737-2-2011 (стерильность), ГОСТу Р ИСО 13408-3-2011 (лиофилизация).
Качество лиофилизированной и восстановленной плазмы в названном постановлении (п. 27) определено следующими параметрами: содержание общего белка – не менее 50 г/л, концентрация фактора VIII – не менее 0,5 МЕ/мл, остаточная влажность – не более 2%, стерильно, регидратация лиофилизата 250 мл воды для инъекций.
Содержание общего белка в пробах определяли биуретовым методом, концентрацию фактора VIII одностадийным клоттинговым методом, остаточную влажность лиофилизата - методом Фишера.
Показатели качества (средние значения): остаточная влажность лиофилизата плазмы - 1,8%, содержание общего белка - 55 г/л, концентрация фактора VIII - 0,6 МЕ/мл. Дисперсия ± 10 %. Те же параметры в присутствии лиопротектора хепес были на 12 - 18 % лучше.
Представленные экспериментальные данные свидетельствуют о том, что значения параметров качества плазмы соответствовали выше названному нормативному документу. Тесты на стерильность всех 15 доз регидратированного лиофилизата плазмы, проведенные в соответствии с требованиями ГОСТов ИСО 11737-2-2011 и 13408-03-2011, не выявили сверхнормативной бактериальной контаминации и нарушение стерильности плазмы, что подтверждает достижение заявленного технического результата.
Тесты на стерильность продемонстрировали, что описанные технологические операции предложенного способа, реализуемого с использованием контейнера, могут быть проведены в обычных условиях, не требующих обеспечения стерильности окружающей среды. То есть без использования сложной и дорогостоящей техники, такой как ламинарные шкафы, стерильные лиофилизаторы, чистые производственные помещения.
Полученные преимущества обусловлены тем, что все технологические операции с гемокомпонентом проводят в едином закрытом стерильном контейнере, который не разгерметизируют ни на одном из технологических этапов. Этим достигается снижение риска бактериальной контаминации как лиофизируемого гемокомпонента, так и оператора, проводящего лиофилизацию. Изделия с такими свойствами востребованы не только для лиофилизации крови и ее компонентов, но и при производстве вакцин, сывороток, антибиотиков, для длительного хранения бактерий, вирусов, сухих препаратов из костей и тканей, используемых в хирургии.
Таким образом, предложенный контейнер для лиофилизации и способ его использования позволяют вне асептических условий стерильно лиофилизировать гемокомпонент, отбирать пробы лиофилизата на анализы, компактно хранить, легко транспортировать, сохраняя качество и стерильность лиофилизата на уровне, который соответствует нормативным требованиям.
| название | год | авторы | номер документа |
|---|---|---|---|
| Комплекс мобильный для стерильной лиофилизации гемокомпонентов | 2024 |
|
RU2840198C1 |
| Контейнер для лиофилизации и переливания гемокомпонентов | 2020 |
|
RU2740839C1 |
| Контейнер для высушивания гемокомпонентов | 2024 |
|
RU2826756C1 |
| Комплект с лиофилизатом и способ его использования | 2023 |
|
RU2811648C1 |
| КОНТЕЙНЕР ДЛЯ ЛИОФИЛИЗАЦИИ КРОВИ, ЕЕ КОМПОНЕНТОВ И БИОЛОГИЧЕСКОГО МАТЕРИАЛА | 2022 |
|
RU2794106C1 |
| Способ изготовления гемоконтейнера для лиофилизирования, хранения и регидратирования гемокомпонента | 2024 |
|
RU2822960C1 |
| Сдвоенный контейнер для гемокомпонентов и способ его применения | 2020 |
|
RU2743609C1 |
| Способ подготовки гемокомпонента к хранению и регидратации | 2024 |
|
RU2836796C1 |
| Система для лиофилизации, хранения и использования биологического материала | 2020 |
|
RU2749633C1 |
| УСОВЕРШЕНСТВОВАННЫЕ ЛИОФИЛИЗИРОВАННЫЕ И ФОСФАМИДНЫЕ КОМПОЗИЦИИ | 1992 |
|
RU2106138C1 |




Изобретение относится к медицинской технике, используемой в трансфузиологии. Гибкий контейнер выполнен из двух пленочных мембран, одна из которых гидрофобная газопроницаемая, но непроницаемая для микробных контаминантов и гемокомпонентов. Вторая прозрачная мембрана – газо-, водонепроницаемая. Контейнер содержит присоединительные элементы и позволяет вне асептических условий подготавливать к лиофилизации и лиофилизировать гемокомпоненты. Способ обеспечивает проведение лиофилизации, герметизацию газопроницаемой мембраны после лиофилизации, стерильный пробоотбор и хранение в сложенном виде компактного и маловесного контейнера с лиофилизатом в вакуумированном влагозащитном и газонепроницаемом пакете. Технический результат состоит в сохранении качества и снижении риска микробной контаминации восстановленного из лиофилизата гемокомпонента, в частности плазмы крови. 2 н. и 25 з.п. ф-лы, 11 ил.
1. Контейнер для лиофилизации, содержащий газопроницаемую и непроницаемую для микробных контаминантов плоскую переднюю мембранную поверхность; по меньшей мере одну трубку, сообщающуюся с внутренней полостью контейнера, и присоединительные элементы, отличающийся тем, что выполнен гибким с возможностью складываться и имеет воздухо- и водонепроницаемую плоскую заднюю мембранную поверхность, при этом передняя и задняя мембранные поверхности контейнера герметично соединены друг с другом термосформированными швами, а присоединительные элементы включают штуцеры с перфорируемой мембраной.
2. Контейнер по п. 1, отличающийся тем, что передняя поверхность выполнена из пористой гидрофобной одно- или двухслойной гибкой мембраны.
3. Контейнер по п. 2, отличающийся тем, что мембрана имеет поверхностную пористость в диапазоне 20-80% и водоупорность не менее 150 см.
4. Контейнер по п. 2, отличающийся тем, что мембрана имеет средний размер пор в диапазоне 0,1-0,45 мкм, преимущественно 0,2 мкм.
5. Контейнер по п. 2, отличающийся тем, что мембрана имеет толщину от 100 до 300 мкм, преимущественно 150 ± 50 мкм.
6. Контейнер по п. 2, отличающийся тем, что материал мембраны выбран из группы пористых полимеров, включающей политетрафторэтилен, полиэтилентерефталат и линейный полиэтилен низкой плотности.
7. Контейнер по п. 6, отличающийся тем, что материал мембраны дополнительно нанесен на упрочняющую его подложку из нетканого пористого полиамида или полипропилена.
8. Контейнер по п. 1, отличающийся тем, что мембраны выполнены из материала, обеспечивающего герметичность контейнера в диапазоне температур от -100 до +100°С, преимущественно от -85 до +70°С.
9. Контейнер по п. 1, отличающийся тем, что его задняя поверхность выполнена из воздухо-, водонепроницаемой прозрачной мембраны толщиной от 100 до 300 мкм, преимущественно 150 ± 50 мкм.
10. Контейнер по п. 9, отличающийся тем, что материал мембраны выбран из группы композитных полимеров, включающей: полиамид/полиэтилен, полипропилен/полиэтилен, этиленвинилацетат/полиэтилен, причем сторона мембраны из полиэтилена обращена внутрь контейнера.
11. Контейнер по п. 1, отличающийся тем, что имеет форму прямоугольника, длина которого находится в пределах от 20 до 50 см, преимущественно 30 см ± 10%; ширина - в пределах от 14 до 25 см, преимущественно 20 см ± 10%.
12. Контейнер по п. 11, отличающийся тем, что передняя и задняя поверхности контейнера герметично соединены по периметру прямоугольника от двух до пяти термосформированными швами, отстоящими друг от друга на расстоянии 1-2 мм, при общей ширине шва от 4 до 12 мм.
13. Контейнер по п. 11, отличающийся тем, что имеет вместимость от 50 до 1000 мл, преимущественно от 300 до 600 мл, причем толщина заполненного жидкостью контейнера находится в пределах от 3 до 20 мм, преимущественно от 5 до 8 мм.
14. Контейнер по п. 1, отличающийся тем, что выполнен складывающимся по меньшей мере в 2 раза с сохранением герметичности при складывании и распрямлении контейнера.
15. Контейнер по п. 12, отличающийся тем, что имеет прорезь для подвески контейнера, выполненную в шве или вне шва.
16. Контейнер по п. 12, отличающийся тем, что в шов герметично встроены закрытая с одного конца технологическая трубка с внутренним/внешним диаметром 3,0/4,1 мм ± 10 % и по меньшей мере два присоединительных элемента, выполненных в виде штуцеров с внутренней перфорируемой мембраной, закрытых отделяемым защитным элементом.
17. Контейнер по п. 16, отличающийся тем, что технологическая трубка снабжена зажимом-защелкой и соединена с разветвителем, с которым соединены два штуцера с внутренней перфорируемой мембраной, закрытых отделяемым защитным элементом, и технологическая трубка, оканчивающаяся полимерной иглой с колпачком.
18. Контейнер по п. 17, отличающийся тем, что длина отрезка технологической трубки от разветвителя до полимерной иглы не менее 30 см.
19. Контейнер по п. 1, отличающийся тем, что содержит лиопротектор, выбираемый из группы, содержащей: глутамин, глицин, сахарозу и хепес, и дополнительно - криопротектор в случае лиофилизации клеток крови, выбираемый из группы, содержащей: глицерол, диметилсульфоксид, декстран и полиэтиленгликоль в концентрациях, сохраняющих биологические свойства восстановленных после лиофилизации гемокомпонентов.
20. Способ использования контейнера для лиофилизации по п.1, включающий: соединение контейнера, содержащего гемокомпонент, с контейнером для лиофилизации по п.1, перевод в него гемокомпонента, размещение и замораживание контейнера по п.1 на лотке, сублимацию свободной воды из замороженного гемокомпонента в вакууме, десорбцию связанной воды нагреванием; извлечение контейнера по п.1 из лиофилизатора и герметизацию его газопроницаемой мембраны; отбор порции лиофилизата для анализа; складывание контейнера по п.1, помещение его в непроницаемый для воздуха и влаги полимерный пакет, вакуумирование и запаивание пакета.
21. Способ по п. 20, отличающийся тем, что сублимацию проводят при отрицательной температуре ниже точки эвтектики гемокомпонента.
22. Способ по п. 20, отличающийся тем, что герметизацию воздухопроницаемой мембраны контейнера осуществляют за время не более 30 сек после его извлечения из лиофилизатора, герметизируют всю поверхность мембраны предварительно подготовленным воздухо- и влагонепроницаемым пленочным материалом с клеящейся поверхностью.
23. Способ по п. 22, отличающийся тем, что контейнер с загерметизированной мембраной перед помещением в вакуумируемый полимерный пакет предварительно складывают пополам.
24. Способ по п. 20, отличающийся тем, что соединение контейнеров проводят путем термосваривания технологических трубок или перфорируют полимерной иглой мембрану штуцера контейнера с гемокомпонентом.
25. Способ по п. 20, отличающийся тем, что порцию порошка лиофилизата для анализа отсыпают в технологическую трубку путем встряхивания перевернутого контейнера, стерильно запаивают с двух сторон отрезок трубки длиной не менее 20 см, отсоединяют трубку, высыпают лиофилизат, регидратируют его и определяют параметры качества.
26. Способ по п. 20, отличающийся тем, что контейнеры с гемокомпонентом вплотную друг к другу и без промежутков размещают на лотках, полностью покрывая всю поверхность лотков, лотки в горизонтальном положении замораживают в морозильной камере со скоростью 1-3 °/мин до температуры не менее -40°С, выдерживают в течение 4-24 часов, преимущественно 12 часов, перемещают в лиофилизатор, сублимацию проводят при температуре от -20 до -40°С и вакуумметрическом давлении в диапазоне 40-100 мТорр в течение 24-48 часов, после чего проводят десорбцию не менее 72 часов, постепенно повышая температуру до 37°С.
27. Способ по п. 26, отличающийся тем, что используют лотки с шероховатостью поверхности не более 0,1 мм и неплоскостностью не более 0,5 мм/м, размещенные в лиофилизаторе на расстоянии не менее 40 мм друг от друга по высоте.
| US 20200288703 A1, 17.09.2020 | |||
| US 20100049156 A1, 25.02.2010 | |||
| Система для лиофилизации, хранения и использования биологического материала | 2020 |
|
RU2749633C1 |
| КОНТЕЙНЕР ДЛЯ ЗАМОРАЖИВАНИЯ И ХРАНЕНИЯ БИОПРОДУКТОВ | 2007 |
|
RU2381783C2 |
| КОНТЕЙНЕР ДЛЯ КРОВИ И/ИЛИ КОМПОНЕНТОВ КРОВИ | 2005 |
|
RU2300365C2 |
| Контейнер для лиофилизации и переливания гемокомпонентов | 2020 |
|
RU2740839C1 |
| КОНТЕЙНЕР ДЛЯ ЛИОФИЛИЗАЦИИ КРОВИ, ЕЕ КОМПОНЕНТОВ И БИОЛОГИЧЕСКОГО МАТЕРИАЛА | 2022 |
|
RU2794106C1 |
Авторы
Даты
2023-11-28—Публикация
2023-05-16—Подача