Комплекс мобильный для лиофилизации гемокомпонентов относится к медицинской технике. Комплекс может быть использован для получения стерильных лиофилизатов, в частности плазмы, в отсутствии асептических производственных условий.
Лиофилизацию – высушивание в замороженном состоянии гемокомпонентов под вакуумом с сохранением основных биологических параметров, используют давно. В 1939 г. в СССР в Ленинградском институте переливания крови была создана первая в мире установка для лиофилизации плазмы («Сухая плазма крови и ее применение с лечебной целью», А.Н. Филатов и др. Л. Медицина, 1964, 144 с.). В настоящее время лиофилизацию широко применяют в фармакологическом производстве («Промышленная технология лекарств» Чуешов В.И. и др., в 2-х т. Том 1. - X.: МТК – Книга, 2002, 560 с.). Установки для стерильной лиофилизации биомедицинских продуктов – это сложные и громоздкие стационарные устройства с большой массой, высоким энергопотреблением, требующие для работы асептических условий окружающей среды. Установки снабжаются автоматическими линиями погрузки и выгрузки контейнеров, как правило стеклянных, и гидравлическими механизмами их укупорки в вакууме. По завершении лиофилизации, не извлекая контейнеры с сухим лиофилизатом, их герметизируют внутри установки для сохранения стерильности, т.к. во время лиофилизации контейнеры открыты для выхода паров воды.
Небольшие Центра крови, Станции заготовки и переливания крови, отделения переливания крови в клиниках часто не имеют «чистых» производственных помещений, оснащенных ламинарными микробиологическими боксами для стерильной лиофилизации. В силу этого имеется потребность в простых мобильных лиофилизаторах для стерильной лиофилизации гемокомпонентов в не стерильных лабораторных или производственных условиях.
Известен аналог - вакуумная сублимационная установка для сушки биологических материалов (RU 2119622), имеющая две герметичные камеры, три вакуумных насоса, соединенных трубопроводами, которая не отличается простотой, стационарна и не может быть использована в мобильном исполнении. Известна группа аналогов - передвижных сублимационных машин Lio-8, Lio -25, HFD-1, VLP, LZY-0,5. Группа аналогов не обладает функциями стерильной лиофилизации. Наиболее близким аналогом является установка лиофильной сушки Scientz 10YG Top press. Установка обладает небольшим весом, габаритами, возможностью автономного перемещения по помещению. Имеет функцию стерильной лиофилизации биопродуктов в стеклянных пробирках, колбах и небольших флаконах, но не может быть использована для лиофилизации больших донорских объемов плазмы, содержащихся в полимерных контейнерах.
Задачей изобретения является создание простого мобильного комплекса, конструктивно не обладающего функцией стерильной лиофилизации, но, который совместно с закрытыми мембранными контейнерами, например, по RU 2808342, содержащими гемокомпоненты, обеспечивает стерильную лиофилизацию гемокомпонентов в отсутствии асептических условий на месте применения. При этом регидратированный лиофилизат сохраняет значения параметров качества, которые удовлетворяют нормативным требованиям.
Технический результат состоит в получении стерильного лиофилизата гемокомпонента с регламентированными параметрами качества на производстве, не располагающим асептическими условиями для лиофилизации гемокомпонентов.
Дополнительный технический результат состоит в упрощении конструкции, уменьшении массогабаритных характеристик, энергопотребления и в приобретении комплексом функции мобильности.
Поставленная задача решена, и технический результат, согласно изобретению, достигнут благодаря тому, что предложен мобильный комплекс для стерильной лиофилизации гемокомпонентов. В корпусе комплекса расположена лиофильная камера, содержащая систему теплоотвода, теплоподвода, вакуумирования, конденсации паров, удаления неконденсированных паров, управления и индикации параметров, стеллаж с полками. На полках размещены противни, на которых расположены емкости для лиофилизации гемокомпонентов. При этом корпус выполнен с колесами для транспортировки и выдвигающимися опорами для стационарной установки. Лиофильная камера выполнена цилиндрической, имеет внутренний объем по меньшей мере 0,1 м3 и снабжена герметично закрывающей её дверцей из прозрачного материала с низкой теплопроводностью, съемным теплоизолирующим элементом и штурвальным замком. Емкости для лиофилизируемого гемокомпонента выполнены в виде закрытых уплощенных контейнеров из полимерных гидрофобных мембран, имеющих возможность пропускать пары воды и исключать пропускание жидкости и контаминантов.
Предпочтительные и конкретизирующие признаки изобретения указаны в зависимых пунктах формулы изобретения. В частности, технический результат получают также за счет того, что стеллаж имеет по меньшей мере пять полок, противни выполнены из нержавеющей стали и плотно прилегают к полкам. Противни имеют размер 330 х 520 мм, разделены перегородками на три секции для размещения на них без пустых промежутков контейнеров. Контейнеры имеют размер 170 х 300 мм и содержат гемокомпонент объемом 300 мл +/- 10%.
Для удобства, повышения качества и производительности лиофилизации предпочтительно, чтобы противни имели толщину не более 1,2 мм, с четырех сторон были ограничены бортами высотой не более 20 мм. Имели неплоскостность не более 0,5 мм/м, шероховатость Ra - не более 0,4 мкм, угол отклонения от горизонтали – не более 2°, расстояние между противнями – не менее 45 мм, а неравномерность нагрева и охлаждения по поверхности противней и между противнями не превышала 2°С.
Также для достижения оптимальных условий лиофилизации гемокомпонентов, энергоэффективности и мобильности комплекса целесообразно, чтобы системы теплоотвода и теплоподвода обеспечивали устойчивое охлаждение и нагревание полок с противнями до температуры -45°С и + 60°С соответственно. Производительность по льду была не менее 10 кг, а система вакуумирования создавала в лиофильной камере вакуум на уровне до 60 Па при установленной мощности не более 2 кВт, массе комплекса не более 100 кг, габаритах не более 80 × 80 × 95 см и питании от однофазной сети переменного тока 220 В/50 Гц.
Практично, чтобы контейнеры были выполнены из полимерных мембран толщиной не более 100 мкм. Имели, по меньшей мере, два штуцера с внутренними перфорируемыми мембранами, закрытыми отделяемыми защитными элементами. Причем штуцеры удобно установить на трубках с зажимами, сообщающимися через разветвитель с внутренней полостью контейнера.
Наличие у мобильного комплекса систем: теплоотвода, теплоподвода, вакуумирования, конденсации паров, удаления неконденсированных паров, управления и индикации параметров, стеллажа с полками, на которых установлены противни с расположенными на них закрытыми контейнерами из полимерных плоских мембран с лиофилизируемым гемокомпонентом, необходимо и достаточно для осуществления лиофилизации. Процесс лиофилизации проводят путем вымораживания свободной и связанной воды из замороженного гемокомпонента через мембраны в вакууме. Вначале при отводе тепла при отрицательной температуре ниже точки эвтектики гемокомпонента. После чего, подводят тепло к подогреваемому лиофилизируемому гемокомпоненту для досушивания. Управление, слежение за ходом лиофилизации и визуализацию параметров процесса осуществляют с помощью контроллера и тактильного дисплея. Мембраны создают барьер, непреодолимый для проникновения контаминирующих микроорганизмов из окружающей среды в гемокомпонент, но не препятствуют обезвоживанию замороженного гемокомпонента. Четыре колеса, расположенные по углам корпуса, позволяют одному оператору перемещать мобильный комплекс по производственному цеху. Выдвигающиеся опоры приподнимают и неподвижно фиксируют мобильный комплекс в рабочем положении.
Объем 0,1 м3 и пространственная форма лиофильной камеры в виде цилиндра оптимальны для размещения в ограниченном объеме лиофильной камеры 5 полок общей площадью около 0,85 м2. На полках размещают 15 ед. закрытых уплощенных мембранных контейнеров размером 170 х 300 мм, в совокупности содержащих 4,5 - 5,0 л гемокомпонента. При этом в максимальной степени используют пространство цилиндрической лиофильной камеры с коэффициентом плотности упаковки контейнеров - 8,5 м2/м3. Экономится электроэнергия, которая преимущественно используется на нагревание, охлаждение и вакуумирование, что позволяет быстро удалять влагу из 4,5 - 5,0 л замороженного гемокомпонента за 4 – 5 суток с производительностью около 40 мл/час. Найденные соотношения объема лиофильной камеры, минимального удаления друг от друга противней, расположенных на полках стеллажа, площади закрытых мембранных контейнеров и объема их заполнения стандартной донорской дозой гемокомпонента 300 мл +/- 10% задают высоту заполненного мембранного контейнера в 5 – 7 мм и минимизируют продолжительность лиофилизации. Такая высота заполненного гемокомпонентом контейнера позволяет быстро, гомогенно и качественно высушить гемокомпонент без образования участков карамелизации и остаточных островков замороженного и влажного материала по завершении лиофилизации. Если такие дефекты образовались, то их невозможно устранить за счет повышения производительности и/или длительности лиофилизации.
Качество лиофилизата гемокомпонента существенным образом зависит от того, насколько плотно и равномерно прилегают мембранные поверхности контейнеров к плоскостям противней. Гибкие, гладкие и плоские мембраны контейнеров обеспечивают максимально плотное и равномерное прилегание. Качество лиофилизата также зависит от неплоскостности противней, отклонения их от горизонтального уровня расположения, задающего одинаковый уровень жидкости в разных частях контейнера, и от гладкости изготовления поверхности. С учетом этих ограничений оптимальным образом экспериментально подобраны конфигурация и параметры противней из полированной нержавеющей стали, толщиной не более 1,2 мм, которые с четырех сторон ограничены бортами высотой не более 20 мм. Такая толщина металла и высота бортов практически не препятствует теплопередаче и одновременно сохраняет форму противней без изгибов при их помещении и извлечении из лиофилизатора, когда на противнях расположены контейнеры с лиофилизируемым гемокомпонентом. Противни имеют неплоскостность не более 0,5 мм/м, шероховатость Ra - не более 0,4 мкм, угол отклонения от горизонтали – не более 2°, расстояние между противнями – не менее 45 мм. Неравномерность нагрева и охлаждения по поверхности противней и между противнями не превышает 2°С. Расстояние в 45 мм по вертикали между противнями выбрано из-за того, что при меньшем расстоянии купол мембраны контейнера, образующийся под воздействием давления выходящих водяных паров, соприкасается снизу с расположенным над ним полкой, уменьшает площадь испарения и удлиняет процесс лиофилизации. Неравномерность нагрева более 2 0С по поверхности полок и между полками значимо ухудшает однородность и качества порошка высушиваемого материала.
Энергопотребление (2 кВт) и массогабаритные характеристики (100 кг, 80 × 80 × 95 см) мобильного комплекса минимизированы для достижения компактности, мобильности, маловесности и возможности работы от широко распространенной на производстве обычной однофазной электрической сети переменного тока 220В/50Гц при сохранении высокой производительности процесса лиофилизации и получении качественного лиофилизата гемокомпонента. Минимизированы также теплопотери, которые в наибольшей степени происходят через дверцу лиофильной камеры, за счет использования материала дверцы с низкой теплопроводностью, достаточной толщины дверцы, дополнительного съемного теплоизолирующего элемента, устанавливаемого между дверцей и стеллажом. Штурвальный замок, обеспечивает надежное и герметичное примыкание дверцы к эластичному торцу лиофильной камеры. Благодаря перечисленным конструктивным элементам достигается устойчивая низкая отрицательная -45°С температура замораживания лиофилизата и достаточно высокая положительная температура +60°С при досушивании лиофилизата без потери его качества. Возможность намораживания за один раз 10 кг льда на внутренней цилиндрической поверхности лиофильной камеры обеспечивает повышенную надежность высушивания гемокомпонента, т.к. емкость лиофильной камеры по льду двукратно превышает максимальный жидкий объем лиофилизируемого гемокомпонента. Лед образуется из водяных паров, испаряющихся из гемокомпонента и его лиофилизата. Одновременно в лиофильной камере устойчиво удерживается вакуум на уровне 60 Па. При этом укупоривать внутри лиофилизатора емкости с лиофилизатом по завершении лиофилизации не нужно, т.к. весь процесс лиофилизации происходит в закрытых мембранных контейнерах. Такими преимуществами не обладают стационарные лиофилизаторы. Задействовать свои асептические функции они могут, только работая совместно с автоматизированными линиями загрузки, выгрузки, охлаждения, нагревания, вакуумирования и, главное, наличия внутри них гидравлических механизмов стерильного укупоривания, как правило, стеклянных емкостей с лиофилизатом, которые открыты во время лиофилизации для выхода паров воды. Кроме того, необходимы механизмы, которые после укупоривания, обвальцовывают горловины емкостей, как правило, алюминиевыми колпачками. В противном случае емкости после лиофилизации остаются доступными для проникновения микроорганизмов. Перечисленное энергоемкое оборудование, обязательное в обычных лиофилизаторах, препятствует мобильности и требует наличия выделенной 3-х фазной линии электропитания 380В/50Гц повышенной мощности, которая не всегда имеется на небольших производствах.
Прямоугольная форма закрытых мембранных контейнеров позволяет без свободных промежутков полностью покрыть всю поверхность противней, что обеспечивает равномерный и интенсивный теплообмен с охлаждаемыми и подогреваемыми полками стеллажа для однородного высушивания гемокомпонента во всех частях контейнера. Толщина мембран контейнера 100 мкм практически не препятствует теплообмену и одновременно сохраняет прочность и герметичность контейнера. Присоединительные элементы контейнера, установленные с помощью разветвителя на трубках с зажимами, необходимы для присоединения и перевода в него гемокомпонента из контейнера его содержащего, пробоотбора по завершении лиофилизации, регидратации лиофилизата и присоединения трансфузионной системы для переливания гемокомпонента, восстановленного из сухой формы.
Предпочтительные и конкретизирующие признаки мобильного комплекса указаны в зависимых пунктах формулы изобретения. Они подробно описаны в представленном ниже примере, который не ограничивает объем формулы изобретения. В примере приведены экспериментальные данные, подтверждающие достижение технического результата. Пример также описывает изготовление и работу комплекса со ссылками на рисунки, представленные на фиг. 1 и 2.
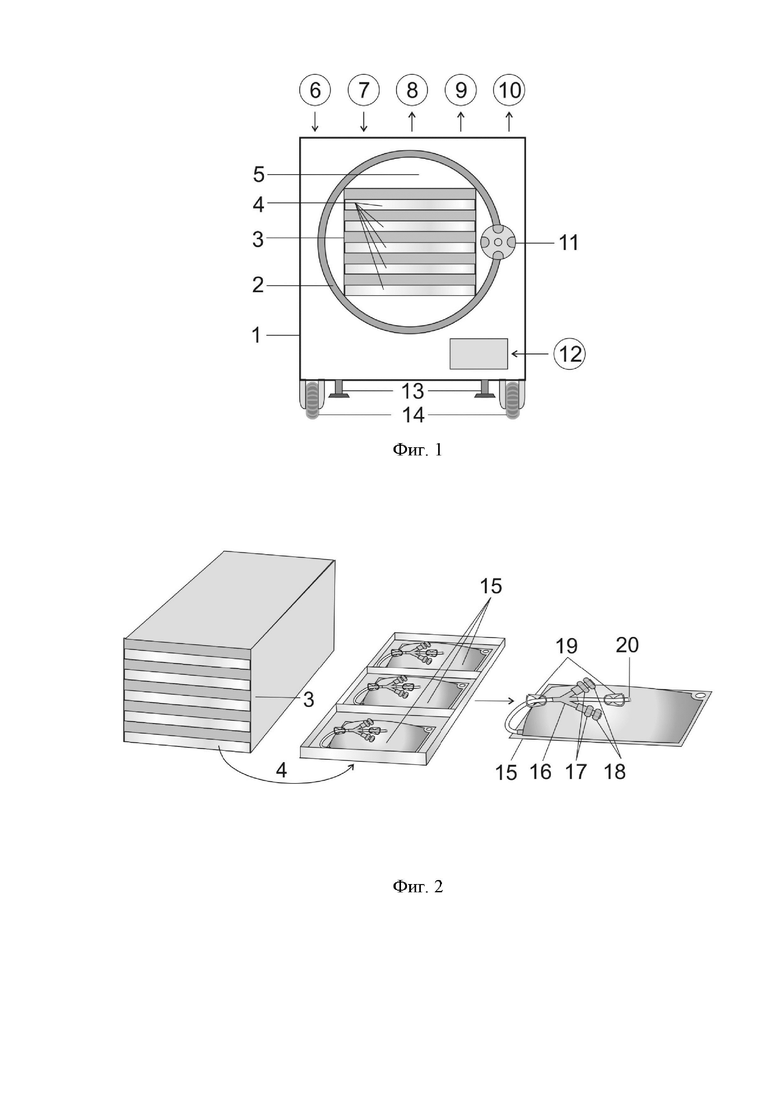
Фиг. 1. Блок-схема комплекса мобильного для стерильной лиофилизации гемокомпонентов. Вид спереди. Съемный теплоизолирующий элемент не показан.
Цифрами 6 – 10, 12 в кругах условно обозначены функциональные системы, входящие с состав комплекса и обеспечивающие его работу.
1. Корпус комплекса; 2. Камера лиофильная; 3. Стеллаж с полками и противнями; 4. Противни; 5. Дверца прозрачная; 6. Система теплоподвода; 7. Система конденсации паров; 8. Система вакуумирования; 9. Система удаление неконденсированных паров; 10. Система теплоотвода; 11. Замок штурвальный; 12. Система управления и индикации параметров с тактильным дисплеем; 13. Колеса транспортные; 14. Опоры выдвижные.
Фиг. 2. Стеллаж с полками и противнями трехсекционными, извлеченный из лиофильной камеры. На противнях размещены закрытые мембранные контейнеры с гемокомпонентами.
3. Стеллаж с полками и противнями; 4. Противни трехсекционные; 15. Закрытые мембранные контейнеры с гемокомпонентом; 16. Разветвитель; 17. Штуцеры с внутренними перфорируемыми мембранами; 18. Отделяемые защитные элементы штуцеров; 19. Зажимы; 20. Трубка.
Коммутационные элементы 17 и трубка 29 предназначены для стерильного присоединения к мембранному контейнеру 15 контейнеров с плазмой, растворителем и трансфузионной системы для переливания, восстановленного лиофилизата плазмы реципиенту.
Изготовили комплекс мобильный для лиофилизации плазмы, содержащий камеру лиофильную 2 с конструктивными элементами 1 – 5, 11, 13, 14 в сборе и с обеспечивающими её работу системами 6 – 10, 12 с параметрами, указанными в зависимых пунктах 2 – 4 формулы настоящего изобретения. Комплекс не обладал асептическими функциями. Изготовили также 15 закрытых мембранных контейнеров для лиофилизации плазмы, способ изготовления которых, конструкция и параметры соответствовали указанным в патенте на изобретение RU 2740839. Комплекс мобильный и закрытые мембранные контейнеры использовали для экспериментальной проверки совместной работы по достижению заявленного технического результата в обычных, не асептических производственных условиях, без использования «чистых» помещений и ламинарного асептического оборудования.
В каждый из 15 закрытых мембранных контейнеров 15 стерильно перевели стандартную дозу аферезной плазмы доноров 300 мл ± 10% из ПВХ полимерных контейнеров, полученной на аппарате «Haemonetics PCS-2». Трубки коммутационные 20 закрытых мембранных контейнеров 15 стерильно соединили с технологическими трубками ПВХ полимерных контейнеров, содержащих аферезную плазму. Для соединения трубок использовали аппарат TSCD -П стерильного спаивания трубок. После перевода плазмы в закрытые мембранные контейнеры 15 трубки 20 запаяли ТВЧ-аппаратом «Гекон-С» и отделили вместе с пустыми ПВХ контейнерами из-под донорской плазмы, которые утилизировали. Мембранные закрытые контейнеры 15, заполненные плазмой, подлежащей лиофилизации, разместили на противнях 4 по три на каждом. Путем быстрого замораживания и выдерживания в течение не менее 12 часов при низкой отрицательной температуре предварительно провели криостабилизацию плазмы в закрытых мембранных контейнерах 15, расположенных на противнях 4. После чего замороженную плазму лиофилизировали в мембранных контейнерах в мобильном комплексе (фиг. 1) способом, раскрытом в патенте на изобретение RU 2808342. Из каждого закрытого мембранного контейнера 15 отобрали пробы лиофилизата. После регидратации лиофилизата плазмы водой для инъекций, в каждой пробе определили значения следующих параметров качества восстановленной плазмы: содержание общего белка, концентрацию фактора VIII, остаточную влажность и стерильность.
Содержание общего белка в пробах определяли биуретовым методом, концентрацию фактора VIII одностадийным клоттинговым методом с использованием реагентов фирмы «Ренам», остаточную влажность лиофилизата - методом Фишера. Вычислили средние значения и дисперсию.
Средние значения показателей качества (n - 15): содержание общего белка - 57 г/л, концентрация фактора VIII - 0,65 МЕ/мл, остаточная влажность лиофилизата плазмы - 1,6%, Дисперсия показателей ± 12 %. Таким образом, значения показателей качества соответствовали нормативным требованиям п. 27 «Лиофилизированная плазма» ПП РФ от 22.06.2019 г. № 797.
Анализ стерильности лиофилизата плазмы в каждом закрытом мембранном контейнере провели согласно нормативному документу ОФС.1.2.4.0003.15, п.2.1, утвержденного Приказом МЗ России от 31.10.2018 № 749. Использовали метод мембранной фильтрации в асептических условиях в ламинарном микробиологическом боксе «Ламинар-С». Исследовали 30 проб, отобранных для анализа. По две из каждого закрытого мембранного контейнера. Каждую пробу с лиофилизатом плазмы 1 г, предварительно регидратированную 10 мл стерильной водой для инъекций, фильтровали через стерильные дисковые фильтры фирмы Миллипор диаметром 13 мм с порами 0,45 мкм. После фильтрации фильтры перенесли в тиогликолевую среду и инкубировали в термостате при температуре 32,5 +/- 2,5°С в течение 14 суток. По истечении указанного контрольного времени рост микроорганизмов во всех пробах не обнаружен, что свидетельствовало о стерильности лиофилизатов плазмы во всех 15 закрытых мембранных контейнерах.
Таким образом, достигнут заявленный технический результат, что подтверждают положительные тесты на стерильность и анализы параметров качества восстановленной из лиофилизата плазмы. Тесты продемонстрировали, что может быть получен стерильный лиофилизат, удовлетворяющий нормативным требованиям, предъявляемым к параметрам качества восстановленной из лиофилизата плазмы, при обычных, не асептических, условиях внешней среды с использованием простого мобильного лиофилизационного комплекса, если лиофилизацию гемокомпонентов проводить в закрытых мембранных контейнерах. При этом комплекс мобильный для стерильной лиофилизации гемокомпонентов не обладал асептическими функциями и был использован на обычном производстве, также не имеющим асептических функций. То есть поставленная задача решена без наличия сложной и дорогостоящей техники, такой как ламинарные микробиологические боксы, лиофилизаторы со стерильными функциями, «чистые» производственные помещения, которые необходимы для стерильной работы и получения стерильного лиофилизата, если не использовать предложенное техническое решение.
Предложенное техническое решение может быть распространено на лиофилизацию биомедицинских продуктов, выбираемых из группы: кровь и её компоненты, включая суспензии клеток крови, криопреципитат, супернатантную и иммунную плазму, плазму, обогащенную тромбоцитами, или с лизированными тромбоцитами; белковые растворы и белковые композиции, препараты фактора УШ и других лабильных факторов крови, иммунноглобулины, бактериальные и вирусные суспензии и фармацевтические композиции.
Изобретение относится к медицинской технике. Комплекс мобильный для стерильной лиофилизации гемокомпонентов включает корпус и установленную в нем лиофильную камеру, содержащую систему теплоотвода, теплоподвода, вакуумирования, конденсации паров, удаления неконденсированных паров, управления и индикации параметров, стеллаж с полками и размещенными на них противнями и емкости для лиофилизируемого гемокомпонента, размещенные на противнях. Корпус выполнен с колесами для транспортировки и выдвигающимися опорами для стационарной установки. Лиофильная камера выполнена цилиндрической, имеет внутренний объем по меньшей мере 0,1 м3 и снабжена герметично закрывающей ее дверцей из прозрачного материала с низкой теплопроводностью, съемным теплоизолирующим элементом и штурвальным замком. Емкости для лиофилизируемого гемокомпонента выполнены в виде закрытых уплощенных контейнеров из полимерных гидрофобных мембран, имеющих возможность пропускать водяные пары и исключать пропускание жидкости и контаминантов. Изобретение обеспечивает получение стерильного лиофилизата гемокомпонента на производстве, не располагающего асептическими условиями. 3 з.п. ф-лы, 2 ил.
1. Комплекс мобильный для стерильной лиофилизации гемокомпонентов, включающий корпус и установленную в нем лиофильную камеру, содержащую систему теплоотвода, теплоподвода, вакуумирования, конденсации паров, удаления неконденсированных паров, управления и индикации параметров, стеллаж с полками и размещенными на них противнями и емкости для лиофилизируемого гемокомпонента, размещенные на противнях, при этом корпус выполнен с колесами для транспортировки и выдвигающимися опорами для стационарной установки, лиофильная камера выполнена цилиндрической, имеет внутренний объем по меньшей мере 0,1 м3 и снабжена герметично закрывающей ее дверцей из прозрачного материала с низкой теплопроводностью, съемным теплоизолирующим элементом и штурвальным замком, а емкости для лиофилизируемого гемокомпонента выполнены в виде закрытых уплощенных контейнеров из полимерных гидрофобных мембран, имеющих возможность пропускать водяные пары и исключать пропускание жидкости и контаминантов.
2. Комплекс по п. 1, отличающийся тем, что стеллаж имеет по меньшей мере пять полок, противни выполнены из нержавеющей стали и плотно прилегают к полкам, противни имеют размер 330 × 520 мм, разделены перегородками на три секции для размещения на них без пустых промежутков контейнеров, контейнеры имеют размер 170 × 300 мм и содержат гемокомпонент объемом 300 мл +/- 10%.
3. Комплекс по п. 1, отличающийся тем, что противни имеют толщину 1,2 мм, с четырех сторон ограничены бортами высотой не более 20 мм, имеют неплоскостность не более 0,5 мм/м, шероховатость Ra - не более 0,4 мкм, угол отклонения от горизонтали - не более 2°, при этом расстояние между противнями составляет не менее 45 мм.
4. Комплекс по п. 1, отличающийся тем, что контейнеры выполнены из мембран толщиной не более 100 мкм и имеют по меньшей мере два штуцера с внутренними перфорируемыми мембранами, закрытыми отделяемыми защитными элементами, установленные на трубках с зажимами, сообщающимися через разветвитель с внутренней полостью контейнеров.
| ВАКУУМНАЯ СУБЛИМАЦИОННАЯ УСТАНОВКА ДЛЯ СУШКИ БИОЛОГИЧЕСКИХ МАТЕРИАЛОВ | 1996 |
|
RU2119622C1 |
| Контейнер для лиофилизации и способ его использования | 2023 |
|
RU2808342C1 |
| Контейнер для лиофилизации и переливания гемокомпонентов | 2020 |
|
RU2740839C1 |
| Способ ротационной гамма-терапии | 1954 |
|
SU105570A1 |
| US 20060051731 A1, 09.03.2006 | |||
| CN 106461327 A, 22.02.2017 | |||
| ПИРИМИДИН-ЗАМЕЩЕННЫЕ ПУРИНОВЫЕ СОЕДИНЕНИЯ В КАЧЕСТВЕ ИНГИБИТОРОВ КИНАЗЫ (ИЛИ КИНАЗ) | 2009 |
|
RU2506264C2 |
Авторы
Даты
2025-05-19—Публикация
2024-07-09—Подача