Изобретение относится к медицинской технике, используемой в трансфузиологии, и предназначено для высушивания замороженных гемокомпонентов в вакууме (лиофилизирования).
Лиофилизированные гемокомпоненты обладают рядом преимуществ по сравнению со свежезамороженными: малый вес, небольшой объем, хранятся при положительной температуре, легко регидратируются и практически на отличаются по биомедицинским показателям качества. Могут быть быстро доставлены, восстановлены и немедленно перелиты реципиенту. Не требуют низкотемпературной доставки, холодильного и размораживающего оборудования на месте применения.
Эти преимущества сухих биопродуктов давно используют в пищевой («Промышленная технология лекарств» Чуешов В.И. и др., в 2-х т. Том 1. - X.: МТК - Книга. Издательство НФAУ, 2002, 560 с.) и фармацевтической промышленности («Теоретические и практические основы лиофилизации лекарственных препаратов: монография». Алексеев К.В. и др. Издательство ООО «Типография «Миттель пресс», 2019, 219 с.). Однако в медицинской промышленности до сих пор сухие гемокомпоненты производят ограничено, несмотря на то что разработка технологии высушивания плазмы была начата еще в СССР. Первая установка для высушивания плазмы создана в 1939 г. в Ленинградском институте переливания крови, а в 1959 сотрудники института А.Н. Филатов и Л.Г. Богомолова были отмечены Сталинской премией за методы лиофилизированной сушки плазмы в стеклянных сосудах. В настоящее время в медицинской промышленности по-прежнему преобладает традиционный подход, когда замороженные гемокомпоненты в асептических условиях высушивают в вакууме в открытых стеклянных флаконах: тяжелых, громоздких и хрупких. Стеклянные флаконы, описанные в патентах на изобретение RU 2126242 C1, RU 2481825 C2, являются аналогом заявленного мембранного контейнера.
ПВХ-полимерные контейнера для гемокомпонентов, раскрытые в патентах на изобретение RU 2127578 C1, RU 137197 U1, удобные при заготовке гемокомпонентов, также являются аналогами, т.к. имеют некоторые функции, совпадающие с заявленным мембранным контейнером. В них замораживают и размораживают гемокомпоненты. Можно получить и сухие гемокомпоненты, но процесс высушивания в таких контейнерах длится больше месяца из-за незначительной воздухопроницаемости ПВХ-материала, что не рентабельно при массовом производстве.
Наиболее близким аналогом является полимерный контейнер лоткового типа для лиофилизации биомедицинских продуктов, в т. ч. гемокомпонентов, GORE LYOGUARD производства фирмы GORE (Германия) (https://www.gore.com/system/files/2020-04/GORE_LYOGUARD_Trays%20Datasheet%20EN_APR20_e_0.pdf), который не является закрытой системой. Верхняя поверхность контейнера представляет собой воздухопроницаемую мембрану, а нижняя - жесткий лоток из полимерного материала, который удерживает жидкость и не смачивает мембрану, герметизирующую лоток по его периметру. Мембрана пропускает водяные пары при высушивании гемокомпонентов и не пропускает контаминанты. Контейнер можно использовать в сушильных машинах, не имеющих асептических функций, для решения исследовательских задач. Промышленной применимостью контейнер не обладает. Заполнять контейнер гемокомпонентом и восстанавливать его из сухой формы с сохранением стерильности можно только в чистых помещениях, локальных стерильных зонах или ламинарных шкафах с асептическими функциями. Кроме того, такой контейнер из-за жесткой и громоздкой конструкции неудобно транспортировать, компактно хранить. Невозможно стерильно регидратировать сухой гемокомпонент в контейнере и перелить из него реципиенту восстановленный гемокомпонент на месте возникновения потребности, например, для компенсации массивной кровопотери. Причина этого - отсутствие присоединительных элементов для сопряжения с контейнерами с гемокомпонентом, с регидратирующим раствором и с трансфузионной системой.
Задачей изобретения является создание компактного, закрытого контейнера, полностью выполненного из мембран, в котором высушивают гемокомпоненты, хранят, восстанавливают и из контейнера переливают реципиенту.
Технический результат состоит в сохранении качества восстановленного в контейнере сухого гемокомпонента.
Дополнительный технический результат состоит в повышении производительности высушивания гемокомпонента в контейнере; легкости, компактности и простоте транспортирования сухого гемокомпонента в контейнере.
Поставленная задача решена, и технический результат согласно изобретению, достигнут благодаря тому, что предложен контейнер для высушивания гемокомпонентов прямоугольной уплощенной формы, выполненный из полимерных мембран, соединенных по периметру швом, содержащим присоединительные элементы. По меньшей мере два присоединительных элемента - штуцеры контейнера, соединены с разветвителем, установленным на гибкой трубке с зажимом, один конец которой запаян, а другой - открытый конец трубки, сообщается с внутренней полостью контейнера. Трубка герметично проникает сквозь шов, причем все элементы, установленные на трубке, размещаются в границах поверхности контейнера при её изгибах без кольцевого скручивания. Противоположный шов содержит отверстие. Вместимость и минимальная допустимая площадь поверхности контейнера таковы, что высота высушиваемого объема гемокомпонента в контейнере не превышает 10 мм.
Конкретизирующие и предпочтительные признаки указаны в зависимых пунктах формулы изобретения.
В частности, штуцеры контейнера симметрично расположены относительно трубки под углом не более 45° к ней и содержат внутреннюю перфорируемую мембрану, закрытую отделяемым защитным элементом. Полимерные гидрофобные мембраны контейнера газопроницаемые и непроницаемые для жидкости и контаминантов, причем, по меньшей мере, одна из полимерных мембран выполнена из прозрачного полимерного материала.
Кроме того, открытый конец трубки проникает во внутреннюю полость контейнера на глубину не больше диаметра трубки, а выход трубки из шва смещен к его периферии, причем трубка выходит из шва, наклоненной к нему под острым углом.
Полезно, чтобы контейнер имел отверстие, через которое свободно проходит стержень подвески контейнеров на трансфузионной стойке, и отверстие было смещено на периферию шва в направлении, противоположном направлению смещения трубки.
Целесообразно чтобы зажим, через который проходит трубка, был выполнен в виде управляемого одной рукой зажима-защелки.
Удобно, чтобы контейнер имел на боковых швах прямую и обратную шкалу объема заполнения гемокомпонентом.
Выбор для конструирования контейнера прямоугольной уплощенной формы без выступающих из шва штуцеров, перенос их на разветвитель гибкой трубки, обусловлен необходимостью достижения максимально плотной укладки контейнеров, покрывающих без промежутков всю площадь плоского противня сушильной машины. Через противень осуществляется охлаждение и подвод тепла к гемокомпоненту в контейнере. Гибкую трубку минимальной длины, выходящую под острым углом к шву, и ее элементы легко разместить без кольцевого скручивания трубки на мембранной поверхности контейнеров, что позволяет достичь максимально плотной укладки контейнеров. Такая укладка обеспечивает равномерную теплопередачу для быстрого и качественного высушивания гемокомпонентов во всех частях контейнера без образования неоднородностей, ухудшающих качество сухого гемокомпонента.
Для изготовления контейнера выбраны газопроницаемые гидрофобные мембраны повышенной пористости с размером пор не более 0,2 мкм, т.к. такие мембраны сохраняют стерильность и обеспечивают быстрый отвод водяных паров из контейнера при высушивании замороженных гемокомпонентов в вакууме. Прозрачность одной из мембран позволяет визуально оценивать качество сухого порошка гемокомпонента, образовывающегося в процессе высушивания, и при необходимости вовремя корректировать параметры высушивания.
Два штуцера с установленной внутри перфорируемой мембраной, закрытой отделяемым защитным элементом для сохранения стерильности мембраны, и симметрично установленных на разветвителе под углом не более 45°, минимально необходимы для полноценного функционирования контейнера. В процессе работы с контейнером один из штуцеров после удаления отделяемого защитного элемента используют для присоединения полимерной иглы контейнера с раствором, восстанавливающим гемокомпонент после его высушивания и длительного хранения в контейнере. Иглой перфорируют внутреннюю мембрану штуцера, после чего переливают регидратирующий раствор в контейнер с лиофилизатом гемокомпонента. Другой штуцер после удаления отделяемого защитного элемента используют для присоединения полимерной иглы трансфузионной системы, с помощью которой переливают восстановленный гемокомпонент реципиенту. В процессе переливания восстановленного гемокомпонента полимерные иглы находятся в штуцерах и не могут быть извлечены из-за нарушения стерильности. Необходимо наблюдать в капельнице трансфузионной системы темп образования капель регидратированного гемокомпонента при трансфузии реципиенту. В случае необходимости регулируют роликовым зажимом трансфузионной системы темп образования капель. При расположении штуцеров с введенными полимерными иглами под углами больше 45° капли не визуализируются, т.к. стекают по боковой поверхности капельницы.
Отверстие в шве, расположенное в углу контейнера и диаметрально противоположное выходу трубки из шва контейнера, а также заглубление трубки в полость контейнера на величину ее диаметра позволяют полностью опорожнить контейнер от жидкости при его подвеске на трансфузионной стойке
Зажим защелку легко перемещать по трубке, устанавливать в удобном месте и открывать/закрывать одной рукой.
Прямая шкала на шве позволяет определить объем заполнения контейнера гемокомпонентом, который учитывают при настройке программы сушильной машины. Обратная шкала необходима для контроля объема, восстановленного гемокомпонента, переливаемого реципиенту.
Критерий высоты уровня гемокомпонента в контейнере – 10 мм задает соотношение вместимости и площади поверхности контейнера, необходимого для заданного объема гемокомпонента, подлежащего качественному высушиванию. Если превысить этот порог, то структура сухого порошка гемокомпонента становится неоднородной, имеются вкрапления из невысушенных замороженных и карамелизированных островков, остаточная влажность превышает допустимый уровень, который не удается корректировать за счет продолжительности высушивания.
Гемокомпоненты, такие как: эритроцитная взвесь, эритроцитная масса, криопреципитат, супернатантная плазма и, наиболее часто используемая в клинической практике, аферезная плазма или плазма из цельной крови, могут быть высушены в предложенном контейнере. В нем же сухие гемокомпоненты можно длительно хранить при положительной температуре, восстановить и перелить из контейнера восстановленный гемокомпонент реципиенту.
Предложенный контейнер для высушивания гемокомпонентов совместим с любым стационарным и мобильным оборудованием для высушивания замороженных биопродуктов в вакууме. Например, сушильные машины «Лиомед», ТГ-50, Virtis и другие, Используя предложенный контейнер, можно высушивать биопродукты, сохраняя стерильность, без обеспечения асептических условий, т.к. контейнер для высушивания гемокомпонентов представляет собой закрытую систему. Гемосовместимые мембраны, из которых изготовлен контейнер, удерживают жидкость, пропускают водяные пары, но создают непроницаемый барьер для бактерий и других контаминантов, сохраняя тем самым стерильность биопродуктов при высушивании в контейнере.
Предпочтительные признаки изобретения описаны в зависимых пунктах формулы изобретения. Они также раскрыты в приведенном ниже конкретном, но не ограничивающим объем формулы изобретения примере выполнения контейнера для высушивания гемокомпонентов с поясняющими ссылками на технический рисунок (фиг.)
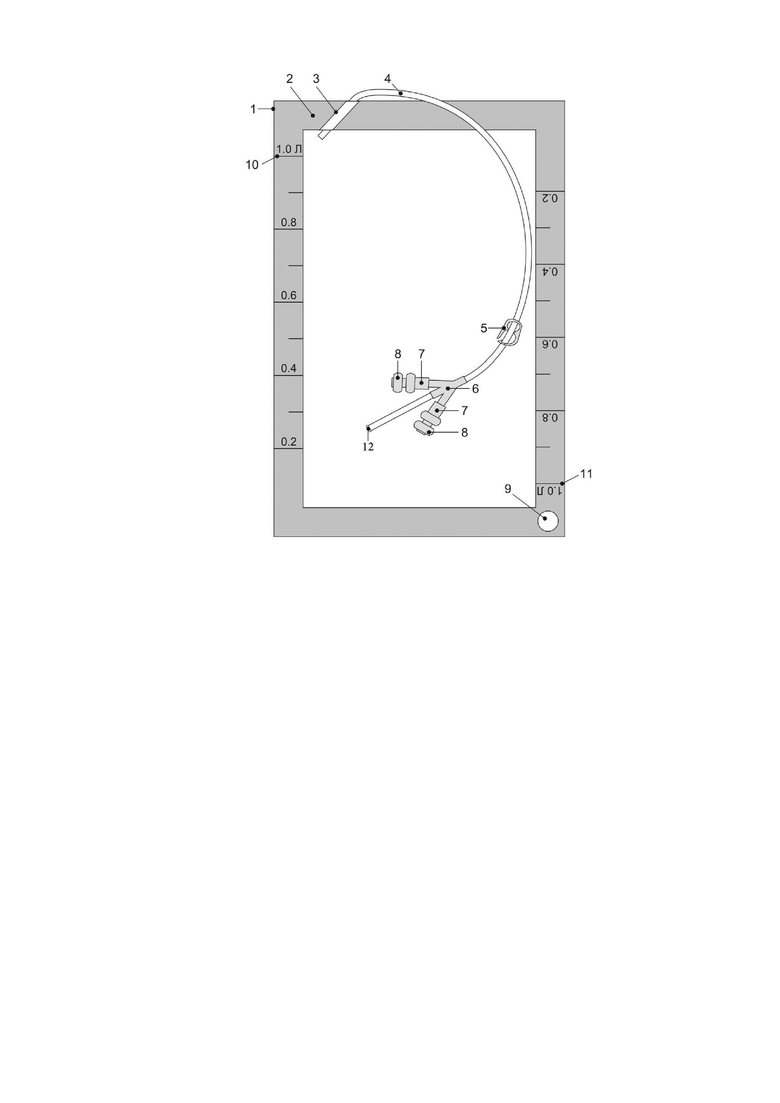
Фиг. Контейнер для высушивания гемокомпонентов.
1 - контейнер, 2 - шов, скрепляющий мембранные поверхности контейнера, 3 - герметичный угловой выход трубки из шва контейнера, 4 - гибкая трубка, 5 - зажим-защелка, 6 - разветвитель на один вход и три выхода, 7 - штуцеры с внутренней перфорируемой мембраной, 8 - отделяемый защитный элемент штуцеров, сохраняющий стерильность мембраны. 9 - отверстие для подвести контейнера на трансфузионной стойке, 10 - прямая шкала объема заполнения контейнера гемокомпонентом, нанесенная на левый боковой шов, 11 - обратная шкала объема заполнения контейнера гемокомпонентом, нанесенная на правый боковой шов, 12 - запаянный конец трубки.
Контейнер для высушивания гемокомпонентов используют следующим образом. Трубку 4 между запаянным концом 12 и разветвителем 6 стерильно спаивают с технологической трубкой контейнера с гемокомпонентом. Переводят гемокомпонент в контейнер. Запаивают трубку и отделяют пустой контейнер из-под гемокомпонента. По шкале 10 определяют объем перелитого в контейнер гемокомпонента, который необходимо знать для настройки программы высушивания. Контейнеры для высушивания гемокомпонентов плотно укладывают без промежутков на противнях. Противни помещают на полки оборудования для высушивания замороженных биопродуктов при отрицательной температуре в вакууме с последующим досушиванием при положительной температуре. Высушивание проводят по заданной программе, настраиваемой под объем и вид гемокомпонента, по завершении которой извлекают контейнеры с высушенным гемокомпонентом и передают на хранение.
В случае необходимости к контейнеру с сухим гемокомпонентом, используя один из штуцеров 7, отделив защитный элемент 8, присоединяют контейнер с водой для инъекций или с 0,9% раствором натрия хлорида, один из которых самотеком переводят в контейнер с сухим гемокомпонентом при помешивании. Проделав аналогичные манипуляции с другим штуцером, присоединяют к нему трансфузионную систему, подвешивают контейнер на штативе, используя отверстие 9, и переливают восстановленный гемокомпонент реципиенту.
Параметры изготовленных в соответствии с предложенным техническим решением контейнеров для высушивания гемокомпонентов и показатели качества, высушенного в них и восстановленного из сухой формы гемокомпонента - плазмы, приведены ниже на примере высушивания аферезной плазмы 8 доноров в сушильной машинеТГ-50.
Изготовили 8 уплощенных прямоугольных контейнеров для высушивания плазмы размером 20 × 30 см из гидрофобных мембран, одна из которых прозрачна. Контейнер не содержал в шве штуцеры. Штуцеры были установлены на разветвителе гибкой трубки длиной 15 см, выходящей из внутренней полости контейнера под углом 30° к линии шва и запаянной с одного конца. В каждый контейнер перевели одну единицу аферезной донорской плазмы, равную 300 мл +/- 15 мл, путем стерильного спаивания трубки контейнера для высушивания плазмы и трубки контейнера, содержащего аферезную донорскую плазму. Трубку запаяли и отделили вместе с пустым контейнером. Использовали аппарат для стерильного спаивания трубок TSCD и аппарат для запаивания трубок Гекон-С. Высота контейнера с 300 мл плазмы не превысила 5 мм, что соответствовало приведенному в формуле изобретения ограничению в 10 мм для эффективного и качественного высушиваемого тонкого слоя плазмы.
Всю площадь противней сушильной машины ТГ-50 покрыли без промежутков контейнерами с плазмой, уложенных попарно. Промежутки отсутствовали, т. к. в шве не было штуцеров, препятствующих плотной укладке. Изогнув трубку, разместили все установленные на ней элементы на мембранной поверхности каждого контейнера. Элементы точечно контактировали с пропускающей водяные пары поверхностью мембраны и не препятствовали испарению. Ни один из элементов не вышел за контур контейнера и не мешал плотной укладке контейнеров на противнях. Противни поместили на охлаждаемые и подогреваемые полки сушильной машины; настроили программу для высушивания плазмы общим объемом 2400 мл.
Высушили плазму. В силу того, что контейнеры не имели штуцеров, выступающих как у стандартных контейнеров из шва на 4 см и плотной укладки контейнеров на противне - на 20% увеличилась полезная площадь и равномерность теплопередачи подогреваемых полок. Как было экспериментально определено, на 8 % сократилось время сублимации свободной воды плазмы. Последнее свидетельствовало о достижении дополнительного технического результата – повышении производительности высушивания гемокомпонента в контейнере.
Перелили в контейнер 250 мл воды для инъекций при помешивании. Восстановили в течение 2 – 3 минут до полного растворения содержащийся в контейнере сухой порошок плазмы весом 25 г, полученный из 300 мл нативной плазмы,
Определили параметры качества восстановленной плазмы, проверив на соответствие требованиям ПП РФ от 22.06.2019 г. № 797, прилож. 1, п. 27 «Лиофилизированная плазма» (качество продукта) и на соответствие ОФС.1.2.4.0003.15 (стерильность). Содержание общего белка в пробах определили биуретовым методом, концентрацию фактора VIII - одностадийным клоттинговым методом, остаточную влажность сухой плазмы - методом Фишера.
Средние (n - 8) значения параметров качества восстановленной плазмы были равны: 59,0 г/л - содержание общего белка в плазме, 0,65 МЕ/мл - концентрация фактора VIII, остаточная влажность сухой плазмы не превысила 1,7%. Отклонение от средних значений параметров - не более ± 15 %. Стерильность, определенная методом, изложенным в ОФС.1.2.4.0003.15, - стерильно. Средние значения параметров плазмы до высушивания: общий белок - 65 г/л, фактор VIII - 0,8 МЕ/мл. Кроме того, дополнительно определили не нормируемые значения показателей качества плазмы: АЧТВ - 30 с, фибриноген 4,8 г/л, осмолярность - 300 мОсмоль/л., которые также не превысили границы нормы.
Таким образом, параметры качества восстановленной в контейнере плазмы удовлетворяли нормативным требованиям п. 27, прилож. 1, ПП РФ от 22.06.2019 г. № 797, что свидетельствовало о достижении заявленного технического результата: сохранении качества, восстановленного в контейнере сухого гемокомпонента, а именно плазмы.
| название | год | авторы | номер документа |
|---|---|---|---|
| Контейнер для лиофилизации и способ его использования | 2023 |
|
RU2808342C1 |
| Комплекс мобильный для стерильной лиофилизации гемокомпонентов | 2024 |
|
RU2840198C1 |
| Комплект с лиофилизатом и способ его использования | 2023 |
|
RU2811648C1 |
| Контейнер для лиофилизации и переливания гемокомпонентов | 2020 |
|
RU2740839C1 |
| Сдвоенный контейнер для гемокомпонентов и способ его применения | 2020 |
|
RU2743609C1 |
| КОНТЕЙНЕР ДЛЯ ЛИОФИЛИЗАЦИИ КРОВИ, ЕЕ КОМПОНЕНТОВ И БИОЛОГИЧЕСКОГО МАТЕРИАЛА | 2022 |
|
RU2794106C1 |
| Способ изготовления гемоконтейнера для лиофилизирования, хранения и регидратирования гемокомпонента | 2024 |
|
RU2822960C1 |
| Устройство для глицеролизации эритроцитов и способ его применения | 2024 |
|
RU2832288C1 |
| Способ подготовки гемокомпонента к хранению и регидратации | 2024 |
|
RU2836796C1 |
| Устройство для ручного отмывания эритроцитов и способ его применения | 2024 |
|
RU2831894C1 |
Изобретение относится к медицинской технике, используемой в трансфузиологии. Представлен контейнер для высушивания гемокомпонентов прямоугольной уплощенной формы, выполненный из соединенных по периметру швами полимерных гидрофобных мембран повышенной пористости с размером пор не более 0,2 мкм. Контейнер содержит герметично пронизывающую шов гибкую трубку с размещенными на ней и не выходящими за периметр контейнера при ее изгибах без скручивания зажимом и разветвителем с симметрично установленными на нем относительно участка трубки с запаянным концом под углом не более 45° как минимум двумя штуцерами. Противоположный открытый конец гибкой трубки герметично пронизывает извне во внутреннюю полость указанный шов, в противоположном шве выполнено отверстие для подвешивания контейнера на трансфузионной стойке, а вместимость и минимальная допустимая площадь поверхности таковы, что высота высушиваемого объема гемокомпонента во внутренней полости не превышает 10 мм. Достигается сохранение качества восстановленного в контейнере сухого гемокомпонента. 9 з.п. ф-лы, 1 ил.
1. Контейнер для высушивания гемокомпонентов прямоугольной уплощенной формы, выполненный из соединенных по периметру швами полимерных гидрофобных мембран повышенной пористости с размером пор не более 0,2 мкм, содержащий герметично пронизывающую шов гибкую трубку с размещенными на ней и не выходящими за периметр контейнера при ее изгибах без скручивания зажимом и разветвителем с симметрично установленными на нем относительно участка трубки с запаянным концом под углом не более 45° как минимум двумя штуцерами, противоположный открытый конец гибкой трубки герметично пронизывает извне во внутреннюю полость указанный шов, в противоположном шве выполнено отверстие для подвешивания контейнера на трансфузионной стойке, а вместимость и минимальная допустимая площадь поверхности таковы, что высота высушиваемого объема гемокомпонента во внутренней полости не превышает 10 мм.
2. Контейнер по п. 1, отличающийся тем, что штуцеры снабжены внутренней перфорируемой мембраной, закрытой отделяемым защитным элементом.
3. Контейнер по п. 1, отличающийся тем, что полимерные гидрофобные мембраны контейнера выполнены газопроницаемыми и непроницаемыми для жидкости и контаминантов.
4. Контейнер по п. 3, отличающийся тем, что по меньшей мере одна из полимерных мембран прозрачна.
5. Контейнер по п. 1, отличающийся тем, что зажим выполнен в виде управляемого одной рукой зажима-защелки, через который проходит трубка.
6. Контейнер по п. 1, отличающийся тем, что открытый конец трубки пронизывает шов во внутреннюю полость контейнера на глубину не больше диаметра трубки.
7. Контейнер по п. 1, отличающийся тем, что выход трубки из шва смещен к периферии, причем трубка выходит из шва наклоненной к нему под острым углом.
8. Контейнер по п. 1, отличающийся тем, что отверстие смещено на периферию шва в направлении, противоположном направлению смещения трубки.
9. Контейнер по п. 8, отличающийся тем, что через отверстие свободно проходит стержень подвески контейнеров на трансфузионной стойке.
10. Контейнер по п. 1, отличающийся тем, что на его боковые швы нанесена прямая и обратная шкала объема заполнения гемокомпонентом.
| КОНТЕЙНЕР ДЛЯ ЛИОФИЛИЗАЦИИ КРОВИ, ЕЕ КОМПОНЕНТОВ И БИОЛОГИЧЕСКОГО МАТЕРИАЛА | 2022 |
|
RU2794106C1 |
| Y-ОБРАЗНЫЙ СОЕДИНИТЕЛЬ ДЛЯ СИСТЕМЫ ДЛЯ ОБРАБОТКИ КРОВИ И ОДНОРАЗОВЫЙ НАБОР, СОДЕРЖАЩИЙ ЕГО | 2017 |
|
RU2742015C2 |
| СМЕСИТЕЛЬНОЕ УСТРОЙСТВО ДЛЯ ПРИГОТОВЛЕНИЯ ГОТОВЫХ К УПОТРЕБЛЕНИЮ МЕДИЦИНСКИХ ПРОМЫВОЧНЫХ РАСТВОРОВ, ПРЕЖДЕ ВСЕГО КОНЦЕНТРАТОВ ДЛЯ ГЕМОДИАЛИЗА | 2013 |
|
RU2537583C2 |
| КОНТЕЙНЕР ДЛЯ ВЫДАЧИ ПЕНЫ | 2011 |
|
RU2577491C2 |
| US 8961489 B2, 24.02.2015 | |||
| DE 19507580 A1, 31.08.1995 | |||
| Устройство для закрепления лыж на раме мотоциклов и велосипедов взамен переднего колеса | 1924 |
|
SU2015A1 |
Авторы
Даты
2024-09-16—Публикация
2024-04-01—Подача