Предшествующий уровень техники
Болезнь Альцгеймера (БА) является одной из самых распространенных форм деменции, от которой, по разным оценкам, страдают более 4,5 млн. человек. В последнее время был достигнут существенный прогресс в понимании патогенеза заболевания, однако, несмотря на это, БА остается пятой по значимости причиной смертности населения старше 60 лет. [Serrano-Pozo A, Growdon JH. Is Alzheimer's Disease Risk Modifiable? J Alzheimers Dis. 2019;67(3):795-819. doi:10.3233/JAD181028]. В настоящий момент лечение БА подразумевает применение симптоматических средств, например, ингибиторов ацетилхолинэстеразы. [Briggs R, Kennelly SP, O'Neill D. Drug treatments in Alzheimer's disease. Clin Med (Lond). 2016;16(3):247-253. doi:10.7861/clinmedicine.16-3-247]. Стоит отметить, что разработки новых терапевтических агентов для лечения данного заболевания ведутся постоянно. Одной из потенциально эффективных стратегий лечения БА может являться целенаправленное воздействие на митохондриальную функцию. [Macdonald R, Barnes K, Hastings C, Mortiboys H. Mitochondrial abnormalities in Parkinson's disease and Alzheimer's disease: can mitochondria be targeted therapeutically? Biochem Soc Trans. 2018 Aug 20;46(4):891-909. doi: 10.1042/BST20170501. Epub 2018 Jul 19. PMID: 30026371.] Митохондриальную дисфункцию определяют как одно из ранних неблагоприятных событий патогенеза БА, ассоциированного с энергодефицитом и повышением интенсивности нейронального апоптоза. Вместе с тем восстановить активность митохондрий в мозговой ткани можно за счет воздействия на ряд регуляторных систем, к которым относится анион-зависимый митохондриальный канал 1 типа VDAC1. [Shoshan-Barmatz V, Nahon-Crystal E, Shteinfer-Kuzmine A, Gupta R. VDAC1, mitochondrial dysfunction, and Alzheimer's disease. Pharmacol Res. 2018 May;131:87-101. doi: 10.1016/j.phrs.2018.03.010. Epub 2018 Mar 15. PMID: 29551631.].
Техническим результатом разработки является применение 4-гидрокси-3,5-ди-третбутил коричной кислоты в качестве церебропротекторного средства, которое оказывает цереброзащитное действие за счет регуляции функции каналов VDAC1.
Пример 1. Оценка влияния применение 4-гидрокси-3,5-ди-третбутил коричной кислоты на изменение функции VDAC1 у животных с экспериментальной БА.
БА моделировали у крыс самцов линии Wistar (масса тела 240-260 грамм) путем внутригиппокампальной инъекции фрагмента β-амилоида (Aβ) 1-42 в количестве 2 мкл и конечной концентрации 1 ммоль. Aβ1-42 был получен от Sigma-Aldrich. Перед инъекцией фрагмент Aβ1-42 растворяли в охлажденном фосфатно-солевом буфере (pH =7,4) при непрерывном перемешивании в течение 36 ч до образования фибриллярных агрегатов. Затем крыс анестезировали хлоралгидратом (внутрибрюшинно, 350 мг/кг), скальпировали теменную область и вводили Aβ1-42 с помощью микро-дозатора объемом 5 мл, снабженного иглой G30. Инъекция была выполнена в СА1 часть гиппокампа (передне-задняя = -3,8 мм, медиально-латеральная = 2,0 мм, дорсально-вентральная = 2,6 мм от брегмы, как определено Paxinos G., 1984). Игла оставалась в месте инъекции в течение 5 минут, после чего иглу извлекали, а хирургическую рану зашивали и обрабатывали 10%-ным раствором повидон-йода. Крыс оставляли под согревающей лампой до пробуждения. 4-гидрокси-3,5-ди-третбутил коричную кислоту (ATACL) вводили в дозе 100 мг/кг [D. Pozdnyakov, A. Voronkov. Correction of Mitochondrial Dysfunction by 4-Hydroxy-3,5-Ditretbutyl Cinnamic Acid in Experimental Alzheimer's Disease Induced by Aβ Injection in Rats. Pharmaceutical Sciences. - 2021. - Vol. 27. - No 3. - P. 313-325. - DOI 10.34172/PS.2020.92.], перорально на протяжение 60 дней с момента воспроизведения БА. Группа крыс негативного контроля (НК) терапии не получала. В группе ложнооперированных животных (ЛО) выполнялись все последовательные операции за исключением введения фрагмента Aβ1-42. Количество животных в группе равнялось 10 особям. По истечение 60 дней у животных осуществляли забор гиппокампа с выделением митохондриальной фракции для чего гиппокамп гомогенизировали в среде, состоящей из 1 ммоль ЭДТА + 215 ммоль маннита + 75 ммоль сахарозы + 0,1% раствор БСА+ 20 ммоль HEPES, с рН 7,2. Для выделения митохондрий полученный гомогенат центрифугировали при 1100g в течение 2-х минут. Полученный супернатант в количестве 700 мкл переносили в пробирки Эппендорфа и смешивали с 75 мкл 10% перколла и центрифугировали при 18000g в течение 10 минут. Осадок ресуспендировали в 1 мл изолирующей среды и центрифугировали в течение 5 минут при 10 000g. Все процедуры проводились при температуре 4°C. [Connolly NMC, Theurey P, Adam-Vizi V.Guidelines on experimental methods to assess mitochondrial dysfunction in cellular models of neurodegenerative diseases. Cell Death Differ. 2018;25(3):542-572. DOI:10.1038/s41418-017-0020-4]. В полученной митохондриальной фракции оценивали изменение концентрации VDAC1 методом твердофазного иммуноферментного анализа. Статистический анализ полученных данных проводился с использованием программного пакета STATISTICA 6.0. Результаты были выражались в виде M ± SEM (среднее значение ± стандартная ошибка среднего значения). Сравнение средних проводилось методом ANOVA с post-hoc тестом Ньюмена-Кейлса в случае данных, подчиняющихся закону нормального распределения, и тестом Краскелла-Уоллиса, при распределении данных отличном от нормального. Нормальность распределения проверялась с помощью теста Шапиро-Уилка. Различия между исследуемыми группами считались статистически значимыми при р <0,05.
В ходе исследования было установлено, что в митохондриальной фракции гиппокампа у крыс НК группы содержание VDAC1 (табл.1) было выше аналогичного у ЛО животных в 2,8 раза (р <0,05). На фоне введения соединения ATACL концентрация VDAC1 относительно НК группы животных уменьшилась на 29,1% (р <0,05).
Пример 2. Оценка влияния применение 4-гидрокси-3,5-ди-третбутил коричной кислоты на изменение жизнеспособности клеток гиппокампа у животных с экспериментальной БА.
БА у животных моделировали согласно процедуре аналогичной описанной в примере 1. 4-гидрокси-3,5-ди-третбутил коричную кислоту (ATACL) вводили в дозе 100 мг/кг [D. Pozdnyakov, A. Voronkov. Correction of Mitochondrial Dysfunction by 4-Hydroxy-3,5-Ditretbutyl Cinnamic Acid in Experimental Alzheimer's Disease Induced by Aβ Injection in Rats. Pharmaceutical Sciences. - 2021. - Vol. 27. - No 3. - P. 313-325. - DOI 10.34172/PS.2020.92.], перорально на протяжение 60 дней с момента воспроизведения БА. Группа крыс негативного контроля (НК) терапии не получала. В группе ложнооперированных животных (ЛО) выполнялись все последовательные операции за исключением введения фрагмента Aβ1-42. Количество животных в группе равнялось 10 особям. По истечение 60 дней у животных осуществляли забор гиппокампа, который гомогенизировали в охлажденном фосфатно-солевом буфере (рН=7,4). Полученный гомогенат центрифугировали при 10000g 10 минут. В полученном супернатанте методом твердофазного иммуноферментного анализа оценивали изменение концентрации апоптоз-индуцирующего фактора. Также жизнеспособность клеток оценивали по изменению активности цитратсинтазы. Активность цитратсинтазы оценивали в соответствии с методом, предложенным Shepherd & Garland, который основан на спектрофотометрическом определении окрашенных продуктов распада 5,5'-ди-тиобис- (2-нитробензойной кислоты) в присутствии ацетил-КоА и оксалоацетата. Реакционная смесь содержала: 5,5'-ди-тиобис- (2-нитробензойная кислота) 100 мм; буфер Трис-HCl с рН 7,8; ацетил СоА 100 ммоль; 0,1% Тритон-Х 100 мкл и 4 мкл исследуемого супернатанта. Реакцию начинали с добавления 100 мкл оксалоацетата. Изменение поглощения регистрировали при длине волны 412 нм в течение 3 минут при комнатной температуре. Активность цитратсинтазы выражали в Ед/мг белка. Концентрацию белка оценивали по методу Брэдфорда. [Shepherd D, Garland PB. The kinetic properties of citrate synthase from rat liver mitochondria.The Bioch. J. 1969; 114(3):597.]. Статистическая обработка результатов эксперимента выполнялась аналогично примеру 1.
При проведении данного исследования было установлено, что у НК группы животных по отношению к ЛО крысам отмечено повышение концентрации апоптоз-индуцирующего фактора в 4,3 раза (р <0,05) при снижении активности цитратсинтазы на 42,1%(р <0,05). Применение соединения ATACL способствовало увеличению активности цитратсинтазы в сравнении с НК группой животных на 36,0% (р <0,05). Также у крыс, получавших соединение ATACL, содержание апоптоз-индуцирующего фактора в супернатанте гиппокампа было на 43,5% (р <0,05) ниже аналогичного у НК группы животных (табл.1).
Примечание: ЛО - ложнооперированные животные, НК - негативный контроль, ATACL - группа животных, получавших соединение ATACL; АИФ - апоптоз-индуцирующий фактор, # - статистически значимо относительно ЛО животных; * - статистически значимо относительно НК группы крыс.
| название | год | авторы | номер документа |
|---|---|---|---|
| Таргетная неинвазивная трансплантация в мозг функционально активных митохондрий для лечения нейродегенеративных заболеваний | 2019 |
|
RU2744453C2 |
| ЦЕРЕБРОПРОТЕКТОР МЕТАБОЛИЧЕСКОГО ДЕЙСТВИЯ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2020 |
|
RU2761549C1 |
| 4-(3-((2-Адамантил)амино)-3-оксопроп-1-ен-1-ил)-N-гидроксибензамид - новое средство для лечения болезни Альцгеймера | 2022 |
|
RU2783995C1 |
| ТЕРАПЕВТИЧЕСКИЕ КОМПОЗИЦИИ (II) | 1999 |
|
RU2242227C2 |
| Способ лечения болезни Альцгеймера, прогрессирующего рассеянного склероза, тяжелого инсульта, последствий черепно-мозговой и родовой травмы мозга, паркинсонизма и других нейродегенеративных заболеваний | 2019 |
|
RU2737995C1 |
| МЕТИЛТИОНИНИЙ, ПРЕДНАЗНАЧЕННЫЙ ДЛЯ ЛЕЧЕНИЯ СИНАПТОПАТИЙ | 2020 |
|
RU2835868C2 |
| Применение производного бензопирана для лечения деменций альцгеймеровского типа, связанных с нарушением кальциевой регуляции | 2023 |
|
RU2804398C1 |
| КОМПОЗИЦИЯ ДЛЯ ПОВЫШЕНИЯ ЭКСПРЕССИИ PGC-1α | 2017 |
|
RU2814560C2 |
| ТЕРАПЕВТИЧЕСКИЕ ВЗАИМОДЕЙСТВИЯ ЛЕЙКОМЕТИЛТИОНИНИЯ | 2020 |
|
RU2834773C2 |
| Способ предотвращения развития инфаркта миокарда мышей с меланомой, развившейся на фоне хронической нейрогенной боли | 2022 |
|
RU2786322C1 |
Изобретение относится к медицине, а именно к применению 4-гидрокси-3,5-ди-третбутил коричной кислоты (формулы I) в дозе 100 мг/кг перорально при болезни Альцгеймера в качестве церебропротекторного средства, регулирующего функцию каналов VDAC1. Изобретение обеспечивает эффективное лечение болезни Альцгеймера путем применения 4-гидрокси-3,5-ди-третбутил коричной кислоты в качестве церебропротекторного средства, регулирующего функцию каналов VDAC1. 1 табл., 2 пр.
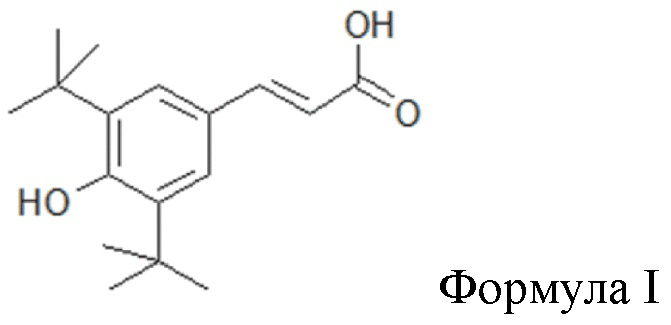
Применение 4-гидрокси-3,5-ди-третбутил коричной кислоты (формулы I)

в дозе 100 мг/кг перорально при болезни Альцгеймера в качестве церебропротекторного средства, регулирующего функцию каналов VDAC1.
| US 10508091 B2, 17.12.2019 | |||
| US 20210330744 A1, 28.10.2021 | |||
| WO 2021001380 A1, 07.01.2021 | |||
| WO 2006108666 A1, 19.10.2006 | |||
| Д.И | |||
| Поздняков, Д.С | |||
| Золотых, М.В | |||
| Ларский "Влияние производного коричной кислоты на изменение активности комплексов митохондриальной дыхательной цепи в условиях экспериментальной ишемии головного мозга", Вопросы биологической, |
Авторы
Даты
2023-12-26—Публикация
2022-04-08—Подача